BAHAN DAN METODE
Waktu dan Tempat
Penelitian ini dilaksanakan pada bulan Juni 2006 sampai Juli 2007 di Laboratorium Pengolahan Pangan Departemen Ilmu dan Teknologi Pangan, serta laboratorium SEAFAST Center Institut Pertanian Bogor.
Bahan dan Alat
Bahan yang digunakan adalah cabe rawit merah, bawang merah, bawang daun, kemangi, jagung, kelapa parut, ikan cakalang kering, MSG, garam, Natrium bisulfit, aguadest, larutan garam jenuh NaOH, MgCl2, KI, KCl, BaCl2, K2SO4, KNO3, K2CO3, NaCl, HCl, H2SO4, H3BO3, HCl, Na2SO4, NaOH, BaCl2, batu didih, heksan, asam tartarat, phenolptalin 1%, alkohol 95%, PCA, PDA, vaselin, aluminium foil, silika gel, polipropilen (PP), polietilen densitas tinggi (HDPE).
Alat yang digunakan adalah timbangan analitik, oven, desikator, freeze
drying, pisau, baskom, talenan, sealer, blender, cawan aluminium, cawan porselin,
labu kjedhal, tabung reaksi, erlenmeyer, kertas saring, saringan, soxhlet, tanur, cawan petri, pipet, lampu bunsen dan gelas piala.
Metode Penelitian
Penelitian ini dilakukan dalam 3 tahap yaitu penelitian tahap pertama, tahap kedua dan tahap ketiga.
Penelitian Tahap Pertama
pembuatan bawang merah bubuk, pengeringan daun bawang dan daun kemangi, pengeringan ikan cakalang serta pembuatan kelapa parut kering. Tahapan pembuatannya adalah sebagai berikut:
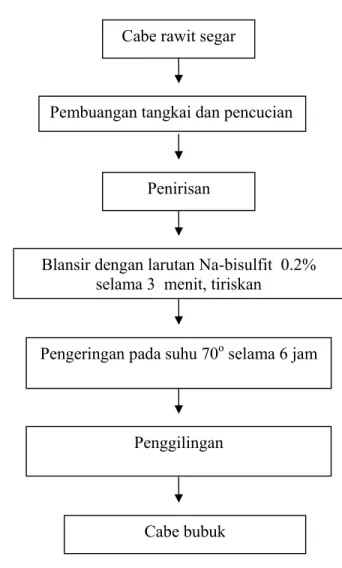
Proses pembuatan cabe rawit bubuk
a. Pembuangan tangkai cabe dan bagian yang rusak atau busuk, kemudian dicuci sampai bersih dan ditiriskan.
b. Pemanasan (blansir) cabe dalam larutan Natrium bisulfit 0.2% yang mendidih selama 3 menit, kemudian dimasukkan kedalam air dingin (25-30oC) dan tiriskan.
c. Pengeringan dengan menggunakan oven pada suhu 70o selama 6 jam. Tanda cabe telah benar-benar kering yaitu hancur bila cabe diremas.
d. Penggilingan cabe kering dengan menggunakan blender
Tahapan proses pembuatan cabe rawit bubuk disajikan pada Gambar 3 (Hambali et al. 2002).
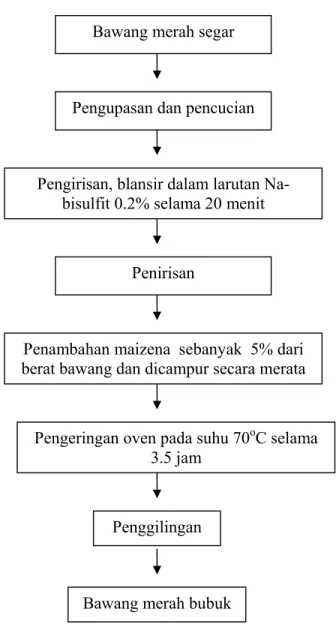
Proses pembuatan bawang merah bubuk
a. Pengupasan bawang merah yang akan digunakan kemudian dicuci sampai bersih dan ditimbang
b. Pengirisan bawang merah kemudian diblansir dalam larutan Na-bisulfit 0.2% selama 20 menit dan ditiriskan.
c. Panambahan bahan pengisi yaitu maizena sebanyak 5% dari berat bawang dan kemudian dicampur sampai merata dengan irisan bawang merah yang telah ditiriskan.
d. Pengeringan dengan menggunakan oven pada suhu 70o selama 3.5 jam. e. Penggilingan bawang merah yang sudah dikeringkan dan diayak untuk
Gambar 3 Diagram pembuatan cabe rawit bubuk.
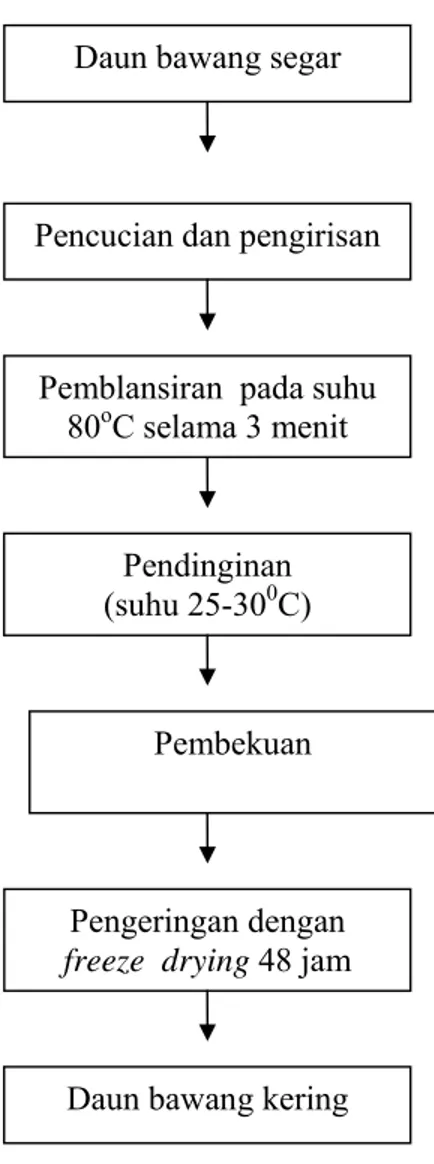
Proses pembuatan daun bawang kering
a. Daun bawang dicuci kemudian diiris-iris sesuai dengan ukuran yang diinginkan.
b. Pemblansiran daun bawang ke dalam air panas (80oC) selama 3 menit. Irisan daun bawang diangkat dengan saringan kemudian dimasukkan kedalam air dingin (25-30oC).
c. Dimasukkan kedalam plastik kemudian disimpan dalam freezer sampai daun bawang menjadi beku.
Cabe rawit segar
Pembuangan tangkai dan pencucian
Penirisan
Blansir dengan larutan Na-bisulfit 0.2% selama 3 menit, tiriskan
Pengeringan pada suhu 70o selama 6 jam
Penggilingan
d. Pengeringan dengan freeze drying selama 48 jam.
Tahapan proses pembuatan daun bawang kering disajikan pada Gambar 5.
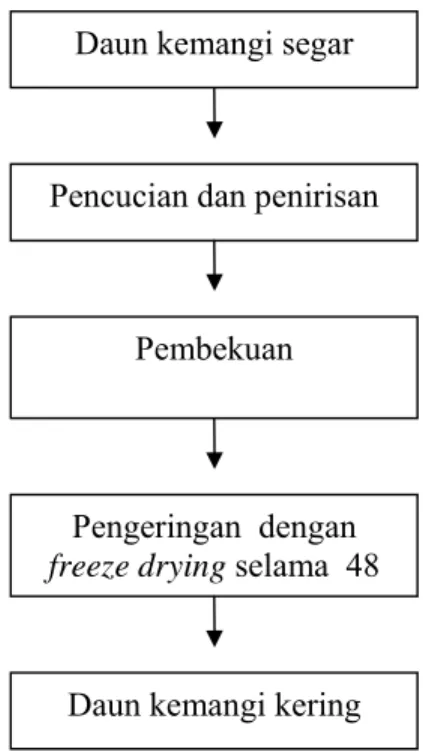
Proses pembuatan daun kemangi kering (Sopian et al 2005)
a. Daun kemangi dicuci dan ditiriskan.
b. Dimasukkan ke dalam plastik kemudian disimpan dalam freezer sampai daun kemangi menjadi beku
c. Pengeringan dengan freeze drying selama 48 jam
Tahapan proses pembuatan daun kemangi kering disajikan pada Gambar 6 (Sopian et al 2005).
Gambar 4 Diagram pembuatan bawang merah bubuk. Bawang merah segar
Penirisan
Pengupasan dan pencucian
Pengirisan, blansir dalam larutan Na-bisulfit 0.2% selama 20 menit
Pengeringan oven pada suhu 70oC selama 3.5 jam
Penggilingan
Bawang merah bubuk
Penambahan maizena sebanyak 5% dari berat bawang dan dicampur secara merata
Gambar 5 Diagram pembuatan daun bawang kering. Daun bawang segar
Pencucian dan pengirisan
Pemblansiran pada suhu 80oC selama 3 menit
Pendinginan (suhu 25-300C)
Pengeringan dengan
freeze drying 48 jam
Daun bawang kering Pembekuan
Gambar 6 Diagram pembuatan daun kemangi kering.
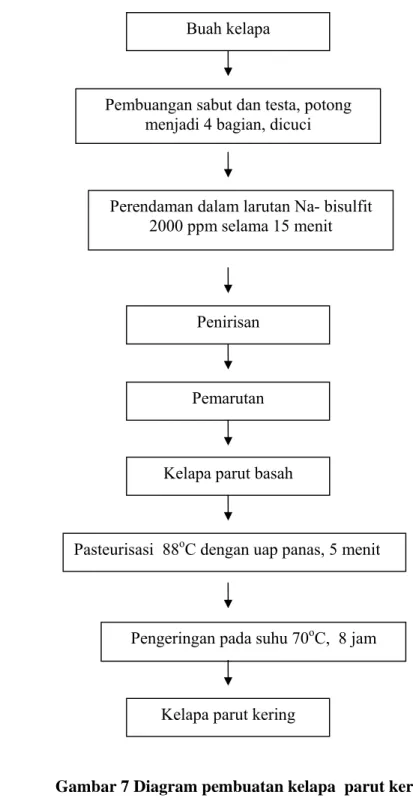
Proses pembuatan kelapa parut kering
a. Buah kelapa dikupas dan dibuang testanya sehingga diperoleh daging kelapa yang putih.
b. Daging kelapa kemudian dipotong menjadi empat bagian, setelah itu dicuci dengan aguades.
c. Setelah itu dilakukan perendaman dalam larutan Na-bisulfit 2000 ppm, selama 15 menit dan ditiriskan selama 10 menit.
d. Dilakukan pemarutan sehingga diperoleh kelapa parut basah
e. Pasteurisasi dengan menggunakan uap panas pada suhu 88oC selama 5 menit.
f. Kelapa parut basah disusun dalam loyang aluminium dengan tebaran setebal 1 cm dan dikeringkan dalam oven dengan suhu 70oC selama 8 jam.
Tahapan proses pembuatan kelapa parut kering disajikan pada Gambar 7. Daun kemangi segar
Pencucian dan penirisan
Pembekuan
Pengeringan dengan
freeze drying selama 48
Gambar 7 Diagram pembuatan kelapa parut kering. Buah kelapa
Pembuangan sabut dan testa, potong menjadi 4 bagian, dicuci
Penirisan
Pemarutan
Kelapa parut basah
Perendaman dalam larutan Na- bisulfit 2000 ppm selama 15 menit
Pengeringan pada suhu 70oC, 8 jam
Kelapa parut kering
Formulasi Bumbu
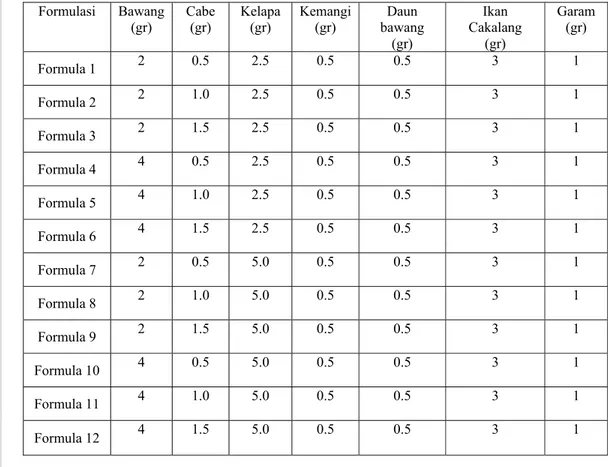
Formulasi bumbu dilakukan untuk mengetahui komposisi bumbu yang paling disukai berdasarkan uji organoleptik. Bumbu yang digunakan terdiri dari bawang merah bubuk, cabe rawit bubuk, kalapa parut kering, daun bawang kering, daun kemangi kering, ikan cakalang kering, MSG dan garam.
Formulasi bumbu yang dilakukan untuk setiap 100 gram bumbu adalah disajikan pada Tabel 4.
Tabel 4. Formulasi bumbu instan binthe biluhuta / 100 gr bumbu Formulasi Bawang
(gr) Cabe (gr) Kelapa (gr) Kemangi (gr) bawang Daun (gr) Ikan Cakalang (gr) Garam (gr) Formula 1 2 0.5 2.5 0.5 0.5 3 1 Formula 2 2 1.0 2.5 0.5 0.5 3 1 Formula 3 2 1.5 2.5 0.5 0.5 3 1 Formula 4 4 0.5 2.5 0.5 0.5 3 1 Formula 5 4 1.0 2.5 0.5 0.5 3 1 Formula 6 4 1.5 2.5 0.5 0.5 3 1 Formula 7 2 0.5 5.0 0.5 0.5 3 1 Formula 8 2 1.0 5.0 0.5 0.5 3 1 Formula 9 2 1.5 5.0 0.5 0.5 3 1 Formula 10 4 0.5 5.0 0.5 0.5 3 1 Formula 11 4 1.0 5.0 0.5 0.5 3 1 Formula 12 4 1.5 5.0 0.5 0.5 3 1
Pada formulasi bumbu ini: garam, MSG, ikan cakalang kering, bawang goreng, kemangi dan daun bawang kering diberikan dalam jumlah yang sama untuk semua perlakuan. Ikan cakalang yang digunakan adalah ikan cakalang yang diasap selama 10 jam, kemudian dikeringkan dengan menggunakan oven selama 4 jam. Setelah itu dihaluskan dengan menggunakan blender. Dari 12 formulasi
organoleptik. Analisis yang dilakukan adalah analisis kadar air, kadar abu, kadar protein, kadar lemak, kadar karbohidrat, kadar lemak bebas, total mikroba dan uji organoleptik.
Penelitian Tahap Kedua
Setelah diperoleh formula bumbu instan binthe biluhuta yang paling disukai
berdasarkan uji organoleptik maka penelitian dilanjutkan ke tahap kedua. Penelitian tahap kedua dilakukan dengan tujuan menghasilkan kurva Isotermis Sorpsi Air (ISA) yang akan digunakan untuk analisa pendugaan umur simpan bumbu instan binthe biluhuta.
Penentuan Kurva Sorpsi Isotermis
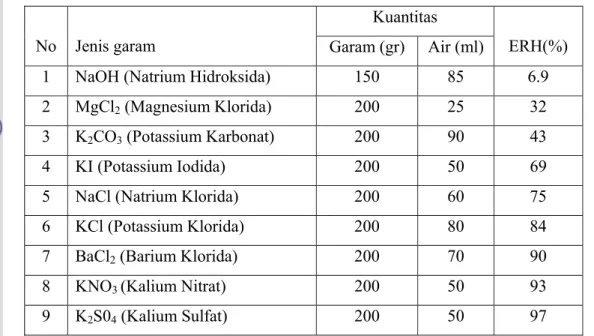
Dalam preparasi larutan garam jenuh digunakan 9 jenis garam. Garam yang telah ditimbang dengan berat tertentu dimasukkan ke dalam desikator kemudian ditambahkan sejumlah air dan diaduk Jenis garam yang digunakan untuk preparasi larutan garam dapat dilihat pada Tabel 5. Setelah diaduk, desikator kemudian ditutup dan dibiarkan selama 24 jam pada kondisi 30oC (Spiess dan Wolf 1987).
Kemudian sebanyak lima gram bumbu ditempatkan dalam cawan porselin kering yang telah diketahui beratnya. Cawan yang berisi sampel tersebut lalu diletakkan dalam desikator yang berisi larutan garam jenuh, kemudian disimpan dalam inkubator dengan suhu 30oC.
Sampel dalam cawan kemudian ditimbang bobotnya secara periodik sampai diperoleh bobot yang konstan yang berarti kadar air kesetimbangan tercapai. Menurut Lang dan Steinberg (1980), berat yang konstan lalu diukur kadar airnya dengan menggunakan metode oven (AOAC 1995) dan dinyatakan
Tabel 5 Jenis dan jumlah garam serta jumlah yang digunakan untuk menentukan nilai aw
Kuantitas
No Jenis garam Garam (gr) Air (ml) ERH(%) 1 NaOH (Natrium Hidroksida) 150 85 6.9 2 MgCl2 (Magnesium Klorida) 200 25 32 3 K2CO3 (Potassium Karbonat) 200 90 43 4 KI (Potassium Iodida) 200 50 69 5 NaCl (Natrium Klorida) 200 60 75 6 KCl (Potassium Klorida) 200 80 84 7 BaCl2 (Barium Klorida) 200 70 90 8 KNO3 (Kalium Nitrat) 200 50 93 9 K2S04 (Kalium Sulfat) 200 50 97
Pengamatan meliputi pengukuran kadar air (AOAC 1995) dan kadar air kritis yang ditandai dengan adanya perubahan pada bumbu.
Penentuan air terikat primer, sekunder dan tersier
Setelah diperoleh kadar air kesetimbangan untuk setiap aw maka dapat ditentukan air terikat primer, sekunder dan tersier.
Air terikat primer ditentukan dengan menggunakan model matematika isotermis sorpsi air BET, yang penerapannya hanya berlaku pada aw 0.05-0.60. Persamaannya adalah aw CMm C CMm M a a w w 1 ( 1) ) 1 ( − + = −
dimana: M adalah kadar air basis kering (%), Mm adalah kadar air monolayer (%), aw adalah aktivitas air, C adalah tetapan energi adsorpsi, yaitu dengan cara membuat kurva regresi antara kadar air kesetimbangan dengan aw. Kisaran aw yang digunakan adalah 0.07-0.43. Dari kurva regresi tersebut dihasilkan persamaan Y = a + bx. Dari persamaan tersebut nilai a disubstitusi menjadi 1/MPC dan nilai b menjadi (C-1)/MpC sehingga diperoleh nilai Mm sebagai air terikat
Air terikat sekunder ditentukan dengan menggunakan model persamaan logaritma. Persamaannya adalah log (1 - aw) = bM + a
dimana: M adalah kadar air (gr air/gr bahan kering) pada aktivitas air aw. Cara mencari air terikat sekunder adalah dengan cara membuat kurva regresi antara log (1-aw) dengan kadar air kesetimbangan. Persamaan regresi pertama diambil dari 4 data yaitu pada aw 0.32 hingga 0.75 sehingga diperoleh persamaan (misalnya Y1). Persamaan regresi kedua diambil dari 4 data juga yaitu dari aw 0.75 hingga 0.93 sehingga diperoleh persamaan (misalnya Y2). Pada kurva plot logaritma dihasilkan garis patah yang terdiri dari dua garis lurus dimana garis lurus pertama mewakili air terikat sekunder dan garis lurus kedua mewakili air terikat tersier. Dengan menggunakan kedua persamaan tersebut, maka diperoleh titik potong keduanya yang menunjukkan batas air terikat sekunder.
Penentuan air terikat tersier dilakukan melalui 3 pendekatan yaitu pendekatan model polinomial ordo 2, pendekatan ekstrapolasi dan pendekatan kuadratik. Perhitungan air terikat tersier model ordo 2 dilakukan dengan cara membuat kurva polinomial ordo 2 antara kadar air kesetimbangan dengan aw dimana aw yang adalah 0.84 sampai 0.93 sehingga diperoleh persamaan Y=ax2 + bx + c dimana Y adalah kadar air (% bk) dan x adalah aw, sehingga pada saat RH = 100% atau aw = 1 diperoleh air terikat tersier. Penentuan air terikat tersier dengan pendekatan ekstrapolasi dilakukan dengan menarik garis kurva ISA sampai aw = 1 sehingga diperoleh nilai kadar air keseimbangan yang juga menunjukkan besarnya fraksi air terikat tersier.
Penentuan Model Sorpsi Isotermis (Spiess dan Wolf 1987)
Persamaan yang dipilih adalah persamaan yang dapat diaplikasikan pada bahan pangan yang mempunyai parameter kurang atau sama dengan tiga serta dapat digunakan pada jangkauan kelembaban relatif yang lebar (0-95%), sehingga dapat mewakili ketiga daerah pada kurva sorpsi isotermis. Persamaan tersebut
Guna memudahkan perhitungan maka model-model persamaan matematis yang digunakan dimodifikasi bentuknya dari persamaan non linier menjadi persamaan linier.
Uji Ketepatan Model (Isse et al. 1983)
Untuk menguji ketepatan suatu persamaan sorpsi isotermis digunakan Mean Relative Determination (MRD)
MRD =
∑
= − n i Mi Mpi Mi n 1 100dimana Mi adalah kadar air percobaan, Mpi adalah kadar air hasil perhitungan, n adalah jumlah data.
Jika nilai MRD<5 maka model sorpsi isotermis itu dapat menggambarkan
keadaan yang sebenarnya atau sangat tepat, jika 5<MRD<10 maka model tersebut agak tepat, dan jika MRD>10 maka model tersebut tidak tepat untuk menggambarkan keadaan yang sebenarnya.
Umur Simpan
Pendugaan umur simpan berdasarkan kurva sorpsi isotermis menggunakan rumus yang dikembangkan oleh Labuza (1982) yaitu:
ts = ⎟ ⎠ ⎞ ⎜ ⎝ ⎛ ⎟⎟ ⎠ ⎞ ⎜⎜ ⎝ ⎛ ⎟ ⎠ ⎞ ⎜ ⎝ ⎛ − − b P W A x k M M M M Ln o s c e i e dimana :
ts = umur simpan produk (hari) Me = kadar air kesetimbangan (%bk) Mi = kadar air awal (% bk)
Po = tekanan uap air jenuh pada ruang penyimpanan (mm Hg) k/x = permeabilitas kemasan (gr H2O/ m2. hari.mmHg)
A = luas kemasan (m2)
b = kemiringan kurva sorpsi isotermis (gr H2O/ gr bk)
Kemasan yang digunakan adalah HDPE (polietelen densitas tinggi), PP (polipropilen) dan Alufo. Nilai k/x (permeabilitas kemasan) diambil dari data sekunder dimana permeabilitas kemasan HDPE, PP dan Alufo berturut-turut adalah 0.12, 0.10 gr/m2.mmHg.hari (Eskin dan Robinson 2001) dan 0.02 gr/ m2.mmHg.hari (Histifarina 2002).
Penelitian Tahap Ketiga
Penelitian tahap ketiga adalah uji penyimpanan. Formulasi bumbu yang paling disukai berdasarkan uji organoleptik dikemas dengan menggunakan kemasan polipropilen (PP), aluminium foil dan polietilen densitas tinggi (HDPE). Dalam penelitian ini, bumbu dikemas dalam keadaan vakum dan tidak vakum kemudian disimpan pada RH 97% dan suhu ruang. Setiap dua minggu dilakukan uji hedonik terhadap sampel. Analisis yang dilakukan adalah kadar air, kadar asam lemak bebas, total mikroba dan total kapang -khamir.
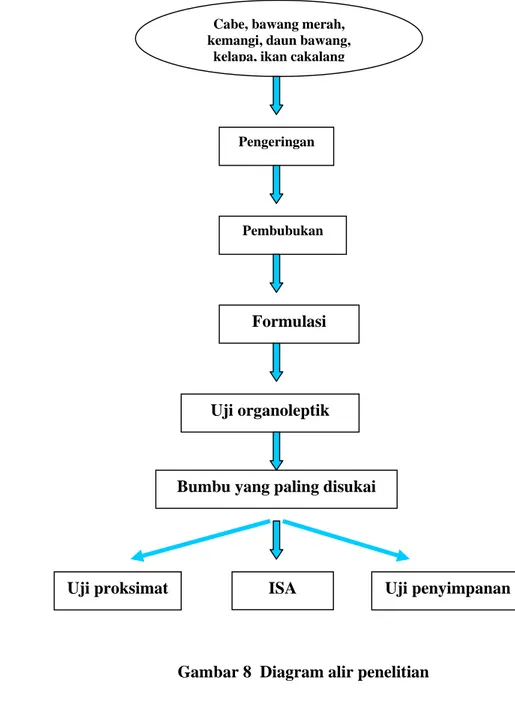
Gambar 8 Diagram alir penelitian
Pengeringan Cabe, bawang merah, kemangi, daun bawang,
kelapa, ikan cakalang
Pembubukan
Formulasi
Uji organoleptik
Bumbu yang paling disukai
Rancangan Percobaan
Rancangan percobaan yang digunakan dalam penelitian tahap ketiga ini adalah Rancangan Acak Lengkap Faktorial dengan 3 kali ulangan, terdiri dari 2 faktor yaitu:
• Jenis bahan kemasan terdiri dari 3 taraf yaitu polietilen densitas tinggi (A1) polipropilen (A2) dan aluminium foil (A3).
• Cara pengemasan terdiri dari 2 taraf yaitu tidak vakum (B1)dan vakum (B2)
sehingga terdapat 6 kombinasi perlakuan dan 18 unit percobaan.
Apabila perlakuan berpengaruh nyata pada taraf 5% maka akan dilanjutkan dengan uji jarak berganda Duncan untuk mengetahui apakah ada perbedaan nyata antar perlakuan. Analisis dilakukan dengan menggunakan software SAS v 9.1.
Model Statistik yang digunakan menurut Mattjik dan Made (2002) adalah sebagai berikut:
Yijk = µ + αi + βj + (αβ)ij + εijk
Dimana:
Yijk = variabel yang diukur µ = rata-rata umum
αi = pengaruh aditif dari taraf jenis kemasan ke-i
βj = pegaruh aditif dari taraf cara pengemasan ke-j (αβ)ij = pengaruh interaksi faktor α dan β
Metode Pengamatan
Kadar Air Metode Oven (AOAC 1995)
Cawan aluminium dikeringkan dalam oven selama 15 menit dan didinginkan dalam desikator selama 10 menit, kemudian ditimbang. Sebanyak empat sampai lima gram contoh dimasukkan kedalam cawan dan dikeringkan dalam oven dengan suhu 105oC selama 6 jam atau hingga sampai berat sampel dan cawan konstan. Setelah itu cawan dikeluarkan dan didinginkan dalam desikator selama 15 menit dan kemudian ditimbang. Pengeringan dilakukan kembali sampai berat konstan. Persentase kadar air dihitung dengan rumus sebagai berikut: Kadar air (%bb ) = a b a− x 100% Kadar air (%bk ) = b b a− x 100% Keterangan
a = berat sampel awal (g) b = berat sampel kering (g)
Kadar Abu (AOAC 1995)
Cawan pengabuan disiapkan, kemudian dikeringkan dalam oven selama 15 menit, didinginkan dalam desikator dan ditimbang. Sampel ditimbang sebanyak 3 gram dimasukkan kedalam cawan porselin, kemudian dibakar dalam ruang asam sampai tidak berasap lagi. Hasil pembakaran kemudian dimasukkan kedalam tanur pengabuan. Proses pengabuan dilakukan sampai didapat abu berwarna abu-abu atau memiliki berat yang tetap.
Proses pengabuan dilakukan dalam dua tahap yaitu tahap pertama pada suhu 400oC dan pada tahap kedua pada suhu 550oC. Sampel kering beserta cawan didinginkan dalam desikator dan ditimbang. Persentase kadar abu (%) dapat dihitung dengan rumus :
Kadar abu (%)= ) ( ker ) ( g ing sampel berat g abu berat x 100%
Kadar Protein Metode Mikro Kjeldahl (AOAC 1995)
Sampel yang akan diukur ditimbang sebanyak 2 gr dan dimasukkan kedalam labu kjeldahl 30 ml. Kemudian kedalam labu kjeldahl ditambahkan 1.9 ± 0.1 gr K2SO4, 40 ± 10mg HgO serta 3.8 ± 0.1 ml H2SO4 pekat dan batu didih. Kemudian sampel didihkan selama1-1.5 jam sampai cairan menjadi jernih. Setelah di didihkan tabung berisi sampel didinginkan dengan air dingin. Selanjutnya isi labu dipindahkan beserta air bekas pembilasnya ke dalam alat destilasi dan ditambahkan 8-10 ml larutan NaOH-Na2S2O3.
Labu erlenmeyer 125 ml yang diisi dengan 5 ml H3BO3 dan ditambahkan 4 tetes indikator (campuran 2 bagian metil merah dan 0.2 % dalam alkohol) kemudian diletakkan dibawah kondensor (ujung kondensor harus terendam dalam larutan H3BO3). Destilasi dilakukan sampai diperoleh destilat ± 15 ml dalam erlenmeyer. Destilat dalam erlenmeyer tersebut kemudian dititrasi dengan larutan HCl 0.02 N hingga terjadi perubahan warna hijau menjadi biru. Dilakukan perhitungan jumlah Nitrogen setelah sebelumnya didapat jumlah volume (ml) blanko. Jumlah N (%)= ing sampel mg x HCl N x blanko HCl ml sampel HCl ml ker 007 . 14 ) ( − x 100
Kadar protein (%) = jumlah N (%) x faktor koversi (6.25)
Kadar Lemak Metode Soxhlet (AOAC 1995)
Labu lemak dikeringkan dalam oven, kemudian didinginkan dalam desikator dan ditimbang beratnya. Sebanyak 5 gr sampel ditimbang dalam bentuk
Kemudian dilakukan refluks selama 5 jam sampai pelarut heksan turun kembali menjadi bening.
Pelarut yang tersisa dalam labu lemak destilasi dan kemudian labu dipanaskan dalam oven pada suhu 105oC. Setelah dikeringkan sampai berat tetap dan didinginkan dalam desikator, kemudian labu beserta lemak didalamnya ditimbang dan dilakukan perhitungan kadar lemak:
Kadar lemak (%) = (g) ker berat (g) lemak berat ing sampel x 100%
Kadar Karbohidrat by difference
Pengukuran kadar karbohidrat dilakukan dengan cara by difference yaitu
dihitung dengan menggunakan rumus:
Kadar Karbohidrat = 100% - % (air + abu + protein + lemak)
Asam Lemak Bebas (FFA) (AOAC, 1991)
Ditimbang sekitar 2 gram sampel, kemudian dimasukkan ke dalam sebuah erlenmeyer dan ditambahkan 50 ml alkohol 95%. Panaskan selama 10 menit, tetesi dengan phenolptalin 1%. Titrasi dengan NaOH 0.1N sampai warna merah muda. Kadar asam lemak bebas (FFA) dapat dihitung dengan rumus
Kadar asam lemak bebas (FFA) =
) (g bahan berat lemak asam BM x NaOH N x NaOH ml
Total Mikroba (Fardiaz 1989)
Sebanyak 1 gr bumbu dimasukkan ke dalam tabung pengencer yang berisi 9 ml larutan pengencer steril (tabung 1). Pengenceran 10-1 diperoleh dari campuran itu. Campuran dikocok kemudian kedalam tabung reaksi yang berisi 9 ml larutan
pengenceran 10-2. Dengan cara yang sama diperoleh pengenceran 10-3 dan seterusnya.
Pada tiap-tiap pengenceran yang dikehendaki, dilakukan pemupukan sebanyak 1 ml ke dalam cawan petri steril dan kemudian ditambahkan media PCA (Plate Count Agar) yang telah didinginkan pada suhu 45-50oC (dilakukan duplo).
Cawan kemudian digoyang-goyang untuk meratakan sel-sel mikroba dan setelah agar memadat cawan diinkubasikan pada suhu ruang dengan posisi terbalik selama 24-48 jam. Pengamatan terhadap total mikroba dilakukan setelah inkubasi, dan dihitung jumlah koloni yang tumbuh yang dinyatakan sebagai total mikroba.
Total Kapang-Khamir (Fardiaz, 1987)
Pengujian kapang-Kamir dilakukan menggunakan metode tuang pada media Potato Dextrosa Agar di tambah asam tartarat 10%, 16 ml/1L media (APDA). Sejumlah 1 gram contoh dilarutkan dalam 9 ml larutan pengencer (garam fisiologis) sehingga didapatkan pengenceran 10-1. Dari larutan contoh tersebut dipipet sebanyak 1 ml dan dimasukkan kedalam tabung pengencer 9 ml untuk memperoleh pengenceran 10-2. Begitu seterusnya sampai pada tingkat pengenceran yang diinginkan. Selanjutnya dari masing-masing tabung pengencer dipipet 1 ml contoh dan dituangkan dalam cawan petri yang telah steril. Kemudian ke dalam cawan dituangkan 15 ml media APDA hingga merata. Cawan kemudian digoyang-goyang untuk meratakan sel-sel total kapang-kamir. Setelah media membeku, cawan disimpan pada inkubator selama 48 jam pada suhu 37oC (dilakukan duplo).
Uji Organoleptik, (Soekarto 1990)
Uji organoleptik yang dilakukan adalah uji hedonik. Uji hedonik dilakukan untuk melihat tingkat kesukaan terhadap aroma dan rasa dengan
Bahan disajikan kepada panelis secara acak dengan kode tertentu. Pemberian skor untuk uji organoleptik rasa dengan skala hedonik adalah sebagai berikut: sangat suka (5), suka (4), biasa (3), kurang suka (2) dan tidak suka (1).