EFEK HEPATOPROTEKTIF EKSTRAK ETANOL 30% DAUN JARONG (Stachytarpheta indica (L.) Vahl.) TERHADAP KADAR ALANIN AMINOTRANSFERASE DAN ASPARTAT AMINOTRANSFERASE
PADA TIKUS JANTAN GALUR WISTAR TERINDUKSI KARBON TETRAKLORIDA
Skripsi
Diajukan untuk Memenuhi Salah Satu Syarat
Memperoleh Gelar Sarjana Farmasi (S.Farm.)
Program Studi Farmasi
Oleh :
Etheldreda Everest Norutama
NIM : 128114018
FAKULTAS FARMASI
UNIVERSITAS SANATA DHARMA YOGYAKARTA
i
EFEK HEPATOPROTEKTIF EKSTRAK ETANOL 30% DAUN JARONG (Stachytarpheta indica (L.) Vahl.) TERHADAP KADAR ALANIN AMINOTRANSFERASE DAN ASPARTAT AMINOTRANSFERASE PADA
TIKUS JANTAN GALUR WISTAR TERINDUKSI KARBON TETRAKLORIDA
Skripsi
Diajukan untuk Memenuhi Salah Satu Syarat
Memperoleh Gelar Sarjana Farmasi (S.Farm.) Program Studi Farmasi
Oleh :
Etheldreda Everest Norutama
NIM : 128114018
FAKULTAS FARMASI
UNIVERSITAS SANATA DHARMA YOGYAKARTA
iv
HALAMAN PERSEMBAHAN
All things are possible in God
“Sesungguhnya Aku berkata kepadamu, apa saja yang telah kamu lakukan kepada seseorang yang terkecil dari saudara-saudara-Ku ini, kamu telah melakukannya kepada-Ku”
Matius 25:40
Do it, like tomorrow NEVER come -EEN
Kupersembahkan karya kecil ini untuk...
Tuhan Yesus Kristus yang selalu melindungi dan
memberiku kekuatan,
Bunda Maria yang selalu meneguhkanku
Ayah Ibuku tercinta,adikku Boy dan Denok yang selalu
mendoakan, mendukung dan menyemangatiku
Sahabat-sahabatku tersayang, terutama:
One
Faith Travellers,
Konco Tipis, MDR,ATRD, AKJ,
DP, JEP, DL, SSR, LDSP
Panitia INSADHA 2013 dan 2014
Komunitas Paingan
DIKTI untuk beasiswa PPA
Rekan-rekan asisten dosen dan partner kepanitiaan
Staff Humas Universitas Sanata Dharma
Almamaterku tercinta
vii PRAKATA
Puji syukur penulis panjatkan kepada Tuhan Yang Maha Esa atas segala
perlindungan dan berkat yang telah diberikan sehingga skripsi berjudul “Efek Hepatoprotektif Ekstrak Etanol 30% Daun Jarong (Stachytarpheta indica (L.)
Vahl.) Terhadap Kadar Alanin Aminotransferase dan Aspartat Aminotransferase
pada Tikus Jantan Galur Wistar Terinduksi Karbon Tetraklorida” dapat dikerjakan dengan baik dan lancar.
Penulis menyadari bahwa penulisan skripsi ini tidak terlepas dari campur
tangan berbagai pihak. Kesempatan ini penulis pergunakan untuk mengungkapkan
rasa terima kasih kepada :
1. Ibu Aris Widayati, M.Si., Ph.D., Apt. dan ibu Dra. Sri Hartati Yuliani, Apt.
selaku Dekan dan Ketua Program Studi Farmasi Universitas Sanata Dharma.
2. Bapak Prof. Dr. C.J. Soegihardjo, Apt. selaku Dosen Pembimbing Utama dan
Ibudrh. Sitarina Widyarini, MP., Ph.D. selaku Dosen Pembimbing
Pendamping yang telah membimbing, memotivasi, dan memberikan saran
selama penyusunan skripsi.
3. Ibu Phebe Hendra, M.Si., Ph.D, Apt., dan Ibu Dr. Yustina Sri Hartini, M.Si,
Apt. selaku Dosen Penguji atas bantuan dan saran kepada penulis demi
kemajuan skripsi.
4. Ibu Agustina Setiawati, M.Sc., Apt., selaku Kepala Penanggungjawab
Laboratorium Fakultas Farmasi yang telah memberikan ijin dalam
viii
5. Bapak Yohanes Dwiatmaka, M.Si. yang telah memberikan bantuan dalam
determinasi tanaman Stachytarpheta indica (L,) Vahl..
6. Pak Kayat, Pak Heru, Pak Parjiman, Pak Parlan, Pak Wagiran, dan Pak Bimo
selaku laboran laboratorium Fakultas Farmasi yang telah membantu penulis
dalam proses pelaksanaan penelitian di laboratorium.
7. Keluargaku tercinta ayah, ibu, Denok, Boy, keluarga besarku yang selalu
memberi motivasi, perhatian dan doa demi kelancaran studi dan penyusunan
naskah skripsi.
8. Dedy Lucky, Sylvan, Abidin dan Waluvi, untuk bantuannya dalam penulisan
skripsi ini.
9. Teman-teman seperjuangan Berto, Jojo, dan Anna atas segala kerjasama,
bantuan dan semangat dalam penyusunan skripsi ini dari awal hingga akhir.
10. Laurentius Derry Satria Putra, Konco Tipis, One Faith Travellers, Laurens,
Ardhi, Inge, Rosi, Agnes, Budi, Judith untuk semangat dan motivasi yang
diberikan.
11. Teman-teman FSM-A 2012, FST-A 2012 dan seluruh angkatan 2012
12. Semua pihak yang tidak dapat penulis sebutkan satu per satu sehingga penulis
dapat menyelesaikan tugas akhir ini dengan baik.
Penulis menyadari bahwa skripsi ini masih memiliki banyak kekurangan
sehingga penulis berharap kritik dan saran dari semua pihak. Akhir kata, penulis
berharap semoga tugas akhir ini dapat bermanfaat bagi semua pihak terutama di
bidang ilmu Farmasi.
ix DAFTAR ISI
Halaman
HALAMAN JUDUL ... i
HALAMAN PERSETUJUAN PEMBIMBING ... ii
HALAMAN PENGESAHAN ... iii
HALAMAN PERSEMBAHAN ... iv
PERNYATAAN KEASLIAN KARYA ... v
LEMBAR PERNYATAAN PERSETUJUAN PUBLIKASI KARYA . ... vi
PRAKATA ... vii
DAFTAR ISI ... ix
DAFTAR TABEL ... xiv
DAFTAR GAMBAR ... xvi
DAFTAR LAMPIRAN ...xviii
INTISARI ... xx ABSTRACT ... xxi BAB I PENGANTAR ... 1 A. Latar Belakang ... 1 1. Perumusan masalah ... 5 2. Keaslian penelitian ... 5 3. Manfaat penelitian ... 6 B. Tujuan Penelitian ... 7 1. Tujuan umum ... 7
x
2. Tujuan khusus ... 7
BAB II PENELAAHAN PUSTAKA ... 8
A. Jarong (Stachytarpheta indica (L.) Vahl.) ... 8
B. Anatomi dan Fisiologi Hati ... 11
1. Anatomi hati ... 11
2. Anatomi hati tikus ... 13
3. Fisiologi hati ... 15
C. Kerusakan Hati ... 15
1. Perlemakan hati (steatosis) ... 16
2. Nekrosis hati ... 16
3. Kolestasis ... 17
4. Sirosis ... 17
D. Alanin Aminotransferasi (ALT) dan Aspartat Aminotransferase (AST) 17 E. Hepatotoksin ... 18
F. Karbon Tetraklorida ... 19
1. Perusakan hati oleh karbon tetraklorida ... 20
2. Rute pemejanan karbon tetraklorida ... 20
G. Maserasi ... 21
H. Metode Pengujian ... 22
I. Landasan Teori ... 23
J. Hipotesis ... 24
BAB III METODE PENELITIAN ... 25
xi
B. Variabel dan Definisi Operasional ... 25
1. Variabel utama ... 25 2. Variabel pengacau ... 25 3. Definisi operasional... 26 C. Bahan Penelitian ... 27 1. Bahan utama ... 27 2. Bahan kimia ... 28 D. Alat Penelitian ... 29
E. Tata Cara Penelitian ... 30
1. Determinasi tanaman jarong (Stachytarpheta indica (L.) Vahl) ... 30
2. Pengumpulan bahan uji ... 30
3. Pembuatan serbuk ... 31
4. Penetapan kadar air serbuk daun Stachytarpheta indica (L.) Vahl. .. 31
5. Uji tabung kandungan polifenol ... 32
6. Pembuatan ekstrak kental daun Stachytarpheta indica (L.) Vahl ... 32
7. Pembuatan CMC Na 1% ... 33
8. Penetapan dosis ekstrak etanol 30% daun Stachytarpheta indica (L.) Vahl ... 33
9. Pembuatan larutan karbon tetraklorida konsentrasi 50% ... 33
10.Uji pendahuluan ... 34
a. Penetapan dosis hepatotoksin ... 34
b. Penetapan waktu pencuplikan darah ... 34
xii
12.Pembuatan serum ... 35
13.Pengukuran kadar ALT-AST ... 36
F. Tata Cara Analisis Hasil... 37
BAB IV HASIL DAN PEMBAHASAN... 39
A. Penyiapan Bahan ... 39
1. Hasil determinasi tanaman ... 39
2. Pembuatan serbuk daun jarong (Stachytarpheta indica (L.) Vahl.) . 40 3. Penetapan kadar air serbuk daun jarong (Stachytarpheta indica (L.) Vahl.) ... 41
4. Hasil uji tabung kandungan polifenol ... 41
B. Pembuatan Ekstrak Etanol 30% daun jarong (Stachytarpheta indica (L.) Vahl.)... 43
C. Penentuan waktu pencuplikan darah ... 44
D. Hasil Uji Efek Hepatoprotektif Ekstrak Etanol 30% Daun Jarong (Stachytarpheta indica (L.) Vahl.) pada Tikus Terinduksi Karbon Tetraklorida ... 48
1. Kontrol negatif olive oil 2 mL/kgBB ... 52
2. Kontrol hepatotoksin 2 mL/kgBB ... 56
3. Kontrol perlakuan ekstrak etanol 30% daun jarong 400 mg/kgBB . 57 4. Kelompok praperlakuan ekstrak etanol 30% daun Stachytarpheta indica (L.) Vahl. pada tikus jantan galur Wistar terinduksi karbon tetraklorida ... 58
xiii
BAB V KESIMPULAN DAN SARAN ... 67
A. Kesimpulan ... 67
B. Saran ... 67
DAFTAR PUSTAKA ... 69
LAMPIRAN ... 75
xiv
DAFTAR TABEL
Halaman
Tabel I. Komposisi dan konsentrasi dari reagen ALT ... 29
Tabel II. Komposisi dan konsentrasi dari reagen AST ... 29
Tabel III. Purata kadar ALT tikus setelah induksi karbon tetraklorida dengan
dosis 2 mL/kgBB saat pencuplikan darah pada jam ke 0, 24, dan 48 45
Tabel IV. Hasil Paired-Samples T Test kadar ALT tikus setelah induksi karbon
tetraklorida dengan dosis 2 mL/kgBB saat pencuplikan darah pada
jam ke-0, 24, dan 48 ... 46
Tabel V. Purata kadar AST tikus setelah induksi karbon tetraklorida dengan
dosis 2 mL/kgBB saat pencuplikan darah pada jam ke 0, 24, dan 48 46
Tabel VI. Hasil Paired-Samples T Test kadar AST tikus setelah induksi karbon
tetraklorida dengan dosis 2 mL/kgBB saat pencuplikan darah pada
jam ke-0, 24, dan 48 ... 48
Tabel VII. Purata ± SE kadar ALT dan AST tikus jantan galur Wistar pada
kelompok perlakuan ... 49
Tabel VIII. Hasil uji post hoc Tukey kadar ALT praperlakuan ekstrak etanol 30%
S. indica pada tikus terinduksi karbon tetraklorida dosis 2 mL/kgBB
xv
Tabel IX. Hasil uji post hoc Games Howell kadar AST praperlakuan ekstrak
etanol 30% S. indica pada tikus terinduksi karbon tetraklorida dosis 2
mL/kgBB ... 52
Tabel X. Purata kadar ALT dan AST tikus setelah pemberian olive oil 2
mL/kgBB pada jam ke-0 dan 24 ... 53
Tabel XI. Hasil Paired-Samples T Test kadar ALT tikus setelah pemberian olive
oil 2 mL/kgBB pada jam ke-0 dan 24 ... 54
Tabel XII. Hasil Paired-Samples T Test kadar AST tikus setelah pemberian olive
xvi
DAFTAR GAMBAR
Halaman
Gambar 1. Tanaman jarong (Stachytarpheta indica (L.) Vahl. ... 8
Gambar 2. Hati dalam sistem pencernaan... ... 11
Gambar 3. Struktur dasar lobulus hati ... 12
Gambar 4. Gambar anatomi hati tikus Wistar ... 13
Gambar 5. Representasi skematik saluran pembuluh darah vena pada hati tikus Wistar ... 14
Gambar 6. Biotransformasi karbon tetraklorida ... 19
Gambar 7. Hasil uji polifenol serbuk daun jarong dalam aquadest ... 42
Gambar 8. Hasil uji polifenol serbuk daun jarong dalam etanol 30% ... 42
Gambar 9. Ekstrak etanol 30% daun S. indica cair ... 43
Gambar 10. Ekstrak etanol 30% daun S. indica kental ... 44
Gambar 11. Diagram batang purata kadar ALT pada selang waktu 0, 24, dan 48 jam setelah pemberian karbon tetraklorida dosis 2 mL/kgBB ... 45
Gambar 12. Diagram batang purata kadar AST pada selang waktu 0, 24, dan 48 jam setelah pemberian karbon tetraklorida dosis 2 mL/kgBB ... 47
Gambar 13. Diagram batang purata kadar ALT tikus jantan galur Wistar pada kelompok perlakuan ... 50
Gambar 14. Diagram batang purata kadar AST tikus jantan galur Wistar pada kelompok perlakuan ... 50
xvii
Gambar 15. Diagram batang purata kadar ALT tikus jantan galur Wistar
setelah pemberian olive oil 2 mL/kgBB pada jam ke-0 dan 24 54
Gambar 16. Diagram batang purata kadar AST tikus jantan galur Wistar
xviii
DAFTAR LAMPIRAN
Halaman
Lampiran 1. Hasil determinasi Jarong (Stachytarpheta indica (L.) Vahl.) ... 76
Lampiran 2. Surat pengesahan determinasi Stachytarpheta indica (L.)
Vahl. ... 79
Lampiran 3. Surat pengesahan Medical and Health Research Ethics
Committee (MHREC)... 80
Lampiran 4. Surat keterangan penggunaan program IBM SPSS Statistics 22
Lisensi UGM ... 81 Lampiran 5. Analisis statistik kadar ALT dan AST pada penetapan waktu
pencuplikan darah ... 82 Lampiran 6. Analisis statistik kadar ALT dan AST pada kelompok kontrol olive
oil 2 mL/kgBB ... 84 Lampiran 7. Analisis statistik kadar ALT pada perlakuan ekstrak etanol 30%
daun jarong (Stachytarpheta indica (L.) Vahl.) setelah induksi karbon tetraklorida 2 mL/kgBB ... 85 Lampiran 8. Analisis statistik kadar AST pada perlakuan ekstrak etanol 30%
daun jarong (Stachytarpheta indica (L.) Vahl.) setelah induksi karbon tetraklorida 2 mL/kgBB ... 92 Lampiran 9. Penetapan kadar air serbuk daun Stachytarpheta indica (L.)
Vahl. ... 98
Lampiran 10. Perhitungan dalam pembuatan ekstrak kental
daunStachytarpheta indica (L.) Vahl. ... 99
xix
Lampiran 12. Perhitungan efek hepatoprotektif AST. ... 101
Lampiran 13. Perhitungan konversi dosis ekstrak etanol 30% daun
xx INTISARI
Penelitian ini bertujuan untuk mengetahui efek hepatoprotektif ekstrak etanol 30% daun jarong (Stachytarpheta indica (L.) Vahl.) terhadap kadar ALT dan AST pada tikus jantan galur Wistar yang terinduksi karbon tetraklorida (CCl4), dosis efektif, dan kekerabatan dosis dengan efek hepatoprotektif yang
dihasilkan.
Jenis penelitian adalah eksperimental murni dengan rancangan acak lengkap pola searah. Digunakan30 tikus jantan berumur 2-3 bulan dengan berat badan ± 160-250 gram, dibagi acak dalam 6 kelompok. Kelompok I diberi olive oil dosis 2 mL/kgBB secara intraperitonial, diambil darah pada jam ke-24. Kelompok II diberi larutan CCl4 dalam minyak zaitun (1:1) dosis 2
mL/kgBBsecara intraperitonial, diambil darah pada jam ke-24. Kelompok III diberi ekstrak etanol 30% daun S. indicadosis 400 mg/kgB secara peroral, diambil darah pada jam keenam. Kelompok IV, V, dan VI diberi ekstrak etanol 30% daun
S. indica dengan dosis 100, 200, dan 400 mg/kgBBsecara peroralenam jam sebelum pemberian CCl4secara intraperitonial.Pengambilan darah pada sinus
orbitalis mata untuk penetapan kadar ALT dan AST dilakukan pada jam ke-24 setelah pemberian CCl4. Data kadar ALT dan AST dianalisis menggunakan one wayANOVA, taraf kepercayaan 95% dan dilanjutkan post hoc Tukey atau Games Howell.
Hasil menunjukkan bahwa ekstrak etanol 30% daun S. indica memiliki efek hepatoprotektif, karena dosis 200 dan 400 mg/kgBB menurunkan kadar ALT-AST. Persen efek hepatoprotektif ALT dari dosis terendah ke tertinggi sebesar 75,31% dan 97,38% dan persen hepatoprotektif AST sebesar 83,77% dan 96,17%. Dosis efektif adalah dosis 400 mg/kgBB serta terdapat kekerabatan antara dosis dan efek hepatoprotektif yang dihasilkan.
Kata kunci : efek hepatoprotektif, Stachytarpheta indica (L.) Vahl.,ekstrak etanol 30%, ALT, AST
xxi ABSTRACT
The aim of study research were to prove the hepatoprotective effect of 30% ethanol extract of jarong leaves (Stachytarpheta indica Vahl.) to ALT and AST concentration, found the effective dose, and the correlationbetween the increase dose of S. indica 30% ethanol extract and ALT-AST concentration in male Wistar rats induced carbon tetrachloride (CCl4).
The research was purely experimental research with randomized complete direct sampling design. This research used30 male, aged 2-3 months and 160-250 grams weight and divided randomized into six groups. Group I was given olive oil at a dose of 2 mL/kgBW intraperitonially. Group II was given CCl4
dissolved in olive oil (1:1) at a dose of 2 mL/kgBW intraperitonially. Blood were taken at 24th hour for group I and II. Group III was given 30% ethanol extract S. indicaat dose 400 mg/kgBWorally for six hours. Group IV; V; and VI were given 30% ethanol extract S. indica with doses level 100; 200; and 400 mg/kgBWorally six hours before CCl4administration imtraperitonially. Blood samples from all
group were taken through the eyes orbital sinus for measuring the ALT and AST serum concentration at 24th hour after administration of CCl4. The data were
analyzed by one way ANOVA with 95% significancy level and continued with Tukey orGames Howellpost hoc.
The results showed that 200 and 400 mg/kgBW doses of30% ethanol extract of S. indicaleaves had a hepatoprotective effect by lowering ALT and AST concentration. Hepatoprotective percents for ALTof 200 and 400 mg/kgBW dose were 75,31%and 97,38% and for AST were 83,77% dan 96,17%. The effective dose of 30% ethanol extract of S. Indica leaves was 400 mg/kgBW and there was a correlation between the increase dose of S. indica 30% ethanol extract and ALT-AST concentration reduction.
Keywords : hepatoprotective effect, Stachytarpheta indica Vahl., 30% ethanol extract, ALT, AST
1
BAB I PENGANTAR A. Latar Belakang
Hati merupakan organ yang terbesar dan terkompleks dalam tubuh
manusia, organ ini memiliki tugas utama sebagai organ metabolisme (Wibowo
dan Paryana, 2005). Hati mempunyai peranan besar bagi tubuh. Hati memiliki
lebih dari 500 fungsi antara lain menampung darah, membersihkan darah untuk
melawan infeksi, sebagai tempat empedu diproduksi dan disekresikan, membantu
menjaga keseimbangan glukosa darah (metabolisme karbohidrat), membantu
metabolisme lemak, protein, vitamin dan mineral, mempertahankan suhu tubuh,
serta menetralisir zat-zat beracun dalam tubuh (detoksifikasi) (Wijayakusuma,
2008).
Salah satu bentuk kerusakan hati yang sering dijumpai adalah
perlemakan hati (steatosis). Pada perlemakan hati terjadi penumpukan trigliserida
dalam bentuk droplet di dalam sitoplasma sel hepatosit (Schattner and Knobler,
2008). Berdasarkan etiologinya, perlemakan hati dibedakan menjadi dua, yaitu
perlemakan hati diperantai alkohol dan perlemakan hati yang tidak diperantai
alkohol. Penyakit perlemakan hati yang tidak diperantai alkohol disebut
nonalcoholic fatty liver disease (NAFLD). Penyakit NAFLD menjadi penyakit
hati yang paling umum di beberapa negara. Di Indonesia sendiri, pravelensi
NAFDL diperkirakan sekitar 30% berdasarkan studi lingkungan urban (Sumantri,
Indonesia kaya akan keanekaragaman hayati yang dapat berpotensi
sebagai obat. Penggunaan tumbuhan sebagai obat sudah tidak asing lagi di
kalangan masyarakat. Tumbuhan yang dapat digunakan untuk mengatasi penyakit
hati salah satunya adalah jarong (Stachytarpheta indica (L.) Vahl.).
Wijayakusuma, Kusuma, dan Dalimartha (1994) menyebutkan dalam
penelitiannya bahwa agar peranan tumbuhan, khususnya tumbuhan yang
berkhasiat obat dapat terus ditingkatkan dan dipertanggungjawabkan secara
medis, maka perlu digali lebih mendalam melalui penelitian dan pengujian.
Menurut Joshi, Sutar, Karigar, Patil, Gopalakrishna, dan Sureban (2010),
ekstrak etanol daun Stachytarpheta indica (L.) Vahl. mengandung karbohidrat,
glikosida dan flavonoid. Pada penelitian tersebut juga dijelaskan bahwa ekstrak
etanol Stachytarpheta indica (L.) Vahl. yang dibuat dengan metode sokletasi
memiliki efek hepatoprotektif yang ditunjukkan dengan penurunan nilai SGPT
(ALT), SGOT (AST), SALP dan serum bilirubin pada tikus yang telah diinduksi
karbon tetraklorida (CCl4), dengan demikian pengukuran kadar enzim ALT dan
AST dapat dilakukan untuk mengetahui kerusakan hati akibat CCl4.
Salah satu senyawa kimia yang terkandung pada tanaman Stachytarpheta
indica (L.) Vahl. adalah flavonoid. Sahoo, Dash and Bhatnagar (2014)
melaporkan bahwa kandungan flavonoid pada herba Stachytarpheta indica Vahl.
menimbulkan efek antioksidan. Tanaman Stachytarpheta indica (L.) Vahl. juga
diteliti dengan membuat ekstrak etanol 96% dari bagian daun oleh Joshi et al.
(2010) dan herba (whole plant) oleh Gayatri, Ramesh, Sumalatha, Venkateswarao,
herba Stachytarpheta indica (L.) Vahl. dapat memberi efek hepatoprotektif karena
senyawa flavonoid yang terkandung di dalamnya. Menurut Dalimartha (2000)
rebusan tanaman jarong (Stachytarpheta indica (L.) Vahl.) dapat digunakan
sebagai obat tradisional Indonesia untuk mengatasi penyakit hati.
Flavonoid merupakan salah satu komponen dari tanaman yang dapat
memberikan perlindungan terhadap hati (Gayatri et al., 2011). Flavonoid dapat
mudah tersari oleh pelarut yang memiliki sifat kepolaran yang sama, yaitu etanol
(Joshi et al., 2010). Oleh karena itu dalam penelitian ini digunakan etanol sebagai
komponen pelarut dalam pembuatan ekstrak daun jarong (Stachytarpheta indica
(L.) Vahl.).
Sahoo et al. (2014) meneliti tentang skrining fitokimia dan bioevaluasi
tanaman Stachytarpheta indica (L.) Vahl. Hasil penelitian tersebut menunjukkan
bahwa ekstrak daun tanaman Stachytarpheta indica (L.) Vahl. memiliki aktivitas
antioksidan yang lebih besar jika dibandingkan dengan ekstrak dari bagian batang
tanaman tersebut, ditinjau dari uji kuantitatif penangkapan radikal. Berdasarkan
pertimbangan dari hasil penelitian Sahoo et al. (2014) tersebut, bagian tanaman
yang digunakan dalam penelitian ini adalah bagian daun.
Metode ekstraksi yang digunakan dalam penelitian ini adalah maserasi.
Dua penelitian terdahulu yang meneliti efek hepatoprotektif tanaman
Stachytarpheta indica (L.) Vahl., yakni bagian daun oleh Joshi et al. (2010) dan
herba (whole plant) oleh Gayatri et al. (2011) menggunakan metode sokletasi.
Maserasi memiliki beberapa keunggulan, di antaranya tidak sulit dalam proses
sederhana. Maserasi juga lebih bagus bagi senyawa yang tidak tahan panas jika
dibandingkan dengan metode sokletasi, karena maserasi tidak melibatkan panas
dalam proses ekstraksinya (Masroh, 2010).
Penelitian ini menggunakan karbon tetraklorida sebagai hepatotoksin.
Karbon tetraklorida ( ) dapat menimbulkan kerusakan sel hati berupa
perlemakan hati (steatosis). Senyawa dimetabolisme oleh mikrosomal hati
sitokrom P450 2E1 (CYP2EI) dan kemudian membentuk radikal bebas berupa
triklorometil ( ) (Jeon, Hwang, Park, Jung, Shin, dan Choi, 2003). Ketika
bereaksi dengan oksigen (gas O2) maka akan membentuk radikal
triklorometilperoksi yang lebih reaktif. Radikal dan triklorometilperoksi
akan merusak membran lipid endoplasma yang diawali dengan peroksidasi lipid.
Peningkatan radikal bebas akan berpengaruh pada berbagai perubahan
patologis hati (Cemek, Aymelek, Buyukokuroglu, Karaca, Buyukben, dan Yilmas,
2010).
Pada penelitian ini, pemberian ekstrak dilakukan sebagai praperlakuan.
Ekstrak diberikan dalam jangka waktu enam jam dengan mengacu pada model
penelitian yang dilakukan oleh Eviani (2015) mengenai “Efek Hepatoprotektif
Jangka Pendek Sediaan Dekokta Kulit Persea Americana Mill. terhadap Aktivitas
ALT-AST pada Tikus Terinduksi Karbon Tetraklorida”.
Berdasarkan pemaparan diatas, perlu dilakukan penelitian mengenai efek
hepatoprotektif ekstrak etanol 30% daun jarong (Stachytarpheta indica (L.) Vahl.)
terhadap kadar AST-ALT pada tikus jantan galur Wistar terinduksi karbon
sifat polar (Joshi et al., 2010). Penelitian ini merupakan penelitian payung (dalam
tim) yang meneliti efek hepatoprotektif ekstrak daun Stachytarpheta indica (L.)
Vahl dengan berbagai konsentrasi etanol sebagai pelarut, sehingga dalam
penelitian ini pelarut yang digunakan adalah etanol 30%.
1. Perumusan masalah
a. Apakah ekstrak etanol 30% daun jarong (Stachytarpheta indica (L.) Vahl.) dosis 100, 200, dan 400 mg/kgBB mempunyai efek hepatoprotektif dengan
menurunkan kadar AST-ALT pada tikus jantan galur Wistar terinduksi karbon
tetraklorida?
b. Berapakah dosis efektif ekstrak etanol 30% daun jarong (Stachytarpheta indica (L.) Vahl.) pada tikus jantan galur Wistar terinduksi karbon tetraklorida?
c. Adakah kekerabatan antara dosis pemberian ekstrak etanol 30% daun
Stachytarpheta indica (L.) Vahl. dengan penurunan kadar ALT-AST pada tikus
jantan galur Wistar terinduksi karbon tetraklorida?
2. Keaslian penelitian
Penelitian menggunakan tanaman Stachytarpheta indica Vahl. pernah
dilakukan oleh :
a. Sahoo et al. (2014) melaporkan mengenai efek antioksidan dari
ekstrak metanol Stacytarpheta indica Vahl. dengan menggunakan metode DPPH.
b. Joshi et al. (2010) melakukan penelitian tentang skrining ekstrak
etanol daun Stachytarpheta indica (L.) Vahl. Menggunakan metode ekstraksi
sokletasi dengan beberapa pelarut berdasarkan peningkatan polaritas. Penelitian
dilaporkan memiliki efek hepatoprotektif. Uji efek hepatoprotektif ini dilakukan
dengan menggunakan kontrol positif liv 52 (obat herbal yang diperoleh dari The
Himalaya Drug Company), dengan hepatotoksin karbon tetraklorida, dengan
jangka waktu penelitian 10 hari.
c. Gayatri et al. (2011) melakukan penelitian tentang efek
hepatoprotektif ekstrak etanol herba (whole plant) Stachytarpheta indica (L.)
Vahl. pada tikus jantan galur Wistar. Metode ekstraksi yang digunakan adalah
dengan metode soklet. Pelarut ekstrak yang digunakan adalah etanol 96%. Uji
kadar hepatoprotektif dilakukan dalam jangka waktu 7 hari dengan model
hepatotoksin karbon tetraklorida.
Berdasarkan jurnal penelitian diatas maka penelitian efek hepatoprotektif
dari ekstrak etanol 30% daun Stachytarpheta indica (L.) Vahl. pada tikus jantan
galur Wistar terinduksi karbon tetraklorida dengan metode ekstraksi maserasi
belum pernah dilakukan.
3. Manfaat penelitian
a. Manfaat teoretis
Hasil penelitian ini diharapkan mampu memberikan informasi terkait
ilmu pengetahuan khususnya bidang kefarmasian mengenai pengaruh pemberian
ekstrak etanol 30% daun jarong (Stachytarpheta indica (L.) Vahl.) sebagai
b. Manfaat praktis
Hasil penelitian ini diharapkan mampu memberikan informasi terkait
dosis efektif pemberian ekstrak etanol 30% daun jarong (Stachytarpheta indica
(L.) Vahl.) bagi masyarakat.
B. Tujuan Penelitian 1. Tujuan umum
Mengetahui efek hepatoprotektif pemberian ekstrak etanol 30% daun
jarong (Stachytarpheta indica (L.) Vahl.) terhadap kadar ALT dan AST pada
tikus jantan galur Wistar yang terinduksi karbon tetraklorida.
2. Tujuan khusus
a. Mengetahui efek hepatoprotektif ekstrak etanol 30% daun jarong
(Stachytarpheta indica (L.) Vahl.) dengan menurunkan kadar ALT-AST pada
tikus jantan galur Wistar terinduksi karbon tetraklorida.
b. Mengetahui dosis efektif ekstrak etanol 30% daun jarong (Stachytarpheta
indica (L.) Vahl.) pada tikus jantan galur Wistar terinduksi karbon tetraklorida.
c. Mengetahui ada tidaknya kekerabatan antara dosis pemberian ekstrak
etanol 30% daun Stachytarpheta indica (L.) Vahl. dengan penurunan kadar
8
BAB II
PENELAAHAN PUSTAKA
A. Jarong (Stachytarpheta indica (L.) Vahl.)
Gambar 1. Tanaman Jarong (Stachytarpheta indica (L.) Vahl.) (Chichester, 2015)
Jarong (Gambar 1.) merupakan tumbuhan liar yang berbunga sepanjang
tahun, dapat diperbanyak dengan biji, dan dapat tumbuh di tempat-tempat teduh
dengan ketinggian 1300 meter di atas permukaan laut (Maradjo, 1985). Tumbuhan
jarong berasal dari benua Amerika yang beriklim panas dan dapat ditemukan di
Indo-Cina, Semenanjung Malaka, dan Indonesia (Dharma, 1996).
Tumbuhan ini secara tradisional dapat mengurangi gejala penyakit
kencing nanah, berak darah, amandel (Soedibyo, 1998). Jarong juga dapat
mengurangi gejala rematik, serta hepatitis A (Dalimartha, 2001).
1. Taksonomi
Kingdom : Plantae
Super Divisi : Spermatophyta
Divisi : Magnoliophyta
Kelas : Magnoliopsida
Sub Kelas : Asteridae
Ordo : Lamiales
Famili : Verbenaceae
Genus : Stachytarpheta
Spesies : Stachytarpheta indica Vahl.
Sinonim nama ilmiah
Spesies : Stachytarpheta indica (L.) Vahl.
(Bilgrami dan Dogra, 1990).
2. Nama daerah
Jarong memiliki nama yang berbeda untuk beberapa daerah di Indonesia.
Beberapa diantaranya yaitu Remek getih, Ngadi rengga (Jawa), Jarongan, Jarong
lelaki (Jakarta), Jarong lelaki, Pecut kuda (Sunda), Rum jarum, Roem jharum
(Madura), Selasih hutan (Sumatera) (Dharma, 1996; Soedibyo, 1998).
3. Nama asing
Jarong memiliki beberapa sebutan di negara-negara berbeda. Jarong
disebut Gajihan (Malaysia), Ratstail (Filipina), Yu long bian (China) (Plantamor,
2012).
4. Morfologi
Stachytarpheta indica Vahl. adalah rumput-rumputan yang tegak, tinggi
bertangkai sangat panjang, berbentuk elips memanjang atau bulat telur, dengan
kaki yang menyempit demi sedikit, di atas bagian kaki yang bertepi rata berigigi
beringgit, berambut jarang atau tidak yang ukurannya 4-9 cm dan 2,5-5 cm. Bulir
bertangka pendek, panjang 15-30 cm. Daun pelindung menempel kuat pada
kelopak, bertepi lebar serupa selaput. Kelopak bergigi empat, panjang 0,5 cm.
Tabung dasar bunga berbentuk bantal. Buah berbentuk garis baji, panjang 0,5 cm,
pecah dalam 2 kendaga. Stachytarpheta indica Vahl. terutama hidup di daerah
dengan musim kemarau yang tegas, di tempat yang cerah atau sedikit, 1-1,250 m
(Van Steenis, 1992).
5. Kandungan kimia dan kegunaan
Joshi et al. (2010) dalam penelitiannya menyebutkan bahwa ekstrak
etanol daun Stachytarpheta indica (L.) Vahl. mengandung karbohidrat, glikosida
dan flavonoid. Penelitian yang dilakukan oleh Joshi et al. (2010) dan Gayatri et al.
(2011) menunjukkan bahwa kandungan flavonoid pada daun dan herba jarong
dapat berperan sebagai hepatoprotektor. Sahoo et al. (2014) melaporkan bahwa
kandungan flavonoid pada ekstrak metanol Stacytarpheta indica Vahl. dapat
berperan sebagai antioksidan.
Senyawa antioksidan dapat mempengaruhi ikatan kovalen antara radikal
bebas reaktif dengan molekul seluler (asam nukleat, protein, lemak). Senyawa
antioksidan akan mengurangi dampak yang ditimbulkan radikal tersebut, seperti
gangguan metabolisme lipid dan gangguan sintesis lipoprotein yang
memungkinkan terjadinya penumpukan lemak di hati (Prochazkova, Bousova, dan
B. Anatomi dan Fisiologi Hati
Hati atau hepar merupakan organ sentral dalam proses metabolisme di
dalam tubuh (Sacher and McPherson, 2004). Struktur anatomi dan fisiologi dari
hati yaitu:
1. Anatomi hati
Hati merupakan kelenjar paling besar yang ada dalam tubuh manusia.
Berat hati manusia mencapai 1500 g atau 1,5 kg. Bagian superior dari hati
berbentuk cembung dan terletak pada bagian bawah kubah kanan diafragma.
Bagian inferior dari hepar berbentuk cekung dang di bagian bawahnya terletak
ginjal kanan, gaster, pankreas, dan usus (Baradero, Dayrit, dan Siswandi, 2008).
Letak hati dalam sistem pencernaan manusia dapat dilihat pada gambar 2.
Gambar 2. Hati dalam sistem pencernaan (Baradero dkk., 2008)
Hati berwarna merah cokelat dan bertekstur lunak. Hati berbentuk baji
dengan dasar pada sisi kanan dan apeks pada sisi kiri. Hati dibagi menjadi dua
lobus yakni lobus kiri dan kanan (Hadi, 2002). Lobus kanan terdiri dari bagian
medial dan lateral. Lobus kanan dan lobus kiri dipisahkan di antero-superior oleh
ligamentum falsiformis dari hati melintasi diafragma sampai ke dinding abdomen
anterior.
Hepar memiliki empat saluran, yaitu arteri hepatica, vena porta
hepatica, vena hepatica, dan kanal empedu. Setiap lobus pada hati terbagi
menjadi struktur-struktur yang disebut dengan lobulus. Lobulus hati ditunjukkan
pada gambar 3. Lobulus ini terdiri dari lempeng-lempeng sel hati yang berbentuk
kubus dan tersusun mengelilingi vena sentralis. Hepatosit pada lobulus hati
membentuk piringan tidak merata yang tersusun seperti jari-jari roda, ruang di
antara hepatosit terdapat kapiler yang menjulur ke vena sentral yang disebut
sinusoid. Sinusoid merupakan cabang vena porta dan arteri hepatica dan dibatasi
oleh sel Kupffer. Fungsi sel Kupffer adalah sebagai sistem monosit makrofag
(untuk menelan bakteri dan benda-benda asing dalam darah) sehingga hati
merupakan salah satu organ yang sangat penting untuk pertahanan terhadap
bakteri ataupun agen toksik (Baradero dkk., 2008).
2. Anatomi hati tikus
Perbandingan antara struktur fundamental hati manusia dengan hati tikus
sangat diperlukan, karena umumnya penelitian-penelitian menggunakan hasil
pada tikus untuk direpresentasikan sebagai hasil pada manusia. Hati tikus
memiliki empat lobus (kiri, tengah, kanan, dan kaudatus). Struktur anatomi hati
tikus, yang diambil dari hasil pembedahan tikus Wistar ditunjukkan pada gambar
4.
Gambar 4. Gambar anatomi hati tikus Wistar (Lorente, Rodriguez, Duran, Duran, Alonso, dan Arias, 1995)
Gambar di atas menunjukkan anatomi fungsional hati tikus Wistar. Hati
tikus Wistar terbagi menjadi empat lobulus, yakni right, left, median (central),
dan caudate. Pedikulus porta berada pada anterior hingga terhubung dengan
pembuluh darah vena. Zona caudate (CL), right lateral (RLL), central (C), dan
left (L) dari right middle (RML), left middle (LML), dan left lateral (LLL)
dihubungkan dengan pedikulus yang berhubungan langsung dengan pembuluh
darah vena pertama. Hanya bagian caudate process (CP) dan right (R) dari RML
yang dihungkan oleh pedikulus vena kedua. Dalam hubungan dengan pembuluh
vena, alur aliran yang berasal dari CP, CL, RLL, RML, dan LLL dengan
pedikulus vena pertama. Hanya LML yang bekerja dengan pedikulus yang
Lobus kiri dan tengah membentuk sebuah lobus tunggal yang memiliki
notch dalam yang menjadi tempat penempelan ligamen bulat. Lobus kanan dibagi
menjadi dua sub-lobus dan lobus kaudatus dibagi menjadi bagian paracaval dan
lobus Spiegel, yang dibagi kembali menjadi dua sub-lobus. Lobus kiri, kanan,
dan kaudatus memiliki satu cabang vena porta primer, dimana lobus tengah
memiliki dua cabang porta. Lobus dan sub-lobus kiri maupun kanan
masing-masing memiliki pembuluh darah vena hepatika, dimana tiga vena hepatika besar
ditemukan pada lobus tengah (Kogure, Ishizaki, Nemoto, Kuwano, Makuuchi,
1999).
Berdasarkan pola percabangan dari vena porta dan vena hepatika, lobus
tengah tikus memiliki komponen hepatik kiri dan kanan serta sebuah celah dari
porta utama. Struktur fundamental hati tikus dan manusia disimpulkan mirip.
Representasi skematik saluran pemburuh darah pada tikus Wistar ditunjukkan
pada gambar 5.
Gambar 5. Gambar representasi skematik saluran pembuluh darah vena pada hati tikus Wistar (Lorente et al., 1995)
Keterangan gambar:
H-IVC: intrahepatic inferior vena cava, ICL: inferior caudate lobe, SCL:
superior caudate lobe, LLL: left lateral lobe, RML: right middle lobe, SRLL:
3. Fisiologi hati
Hati menjalankan fungsi yang sangat vital bagi tubuh manusia. Fungsi
hati yaitu mensekresi empedu, metabolisme karbohidrat, protein, lemak, dan
bilirubin; detoksifikasi zat-zat endogen dan eksogen serta sebagai tempat
penyimpanan vitamin dan mineral (Baradero dkk., 2008).
Di dalam hati, terdapat enzim superoksida dismutase (SOD) dan enzim
katalase (CAT). Enzim SOD merupakan enzim yang sangat sensitif bila terjadi
kerusakan hepatoseluler dan berperan sebagai enzim antioksidan alami bagi
tubuh. Enzim SOD mengikat anion superoksida untuk kemudian membentuk
hidrogen peroksida yang berfungsi untuk mengurangi efek toksis yang
ditimbulkan oleh radikal bebas. Enzim CAT memiliki fungsi yang sama dengan
SOD sebagai enzim antioksidan alami bagi tubuh, namun CAT lebih luas tersebar
di semua jaringan hewan dimana kadar tertinggi ditemukan dalam sel darah merah
dan hati. Penurunan kadar SOD dan CAT menandakan adanya kerusakan pada sel
hati (Palanivel, 2008).
Selain SOD dan CAT, hati memiliki perlindungan non enzimatik seperti
glutathione (GSH). Glutation berfungsi untuk melindungi hati dari radikal bebas
seperti hidrogen peroksida, radikal superoksida, dan memelihara membran tiol
protein. Menurunnya kadar GSH pada tikus disebabkan adanya peroksidasi lipid
akibat paparan radikal bebas (Palanivel, 2008).
C. Kerusakan Hati
Kerusakan hati dapat disebabkan oleh berbagai macam substansi kimia
sel-sel hati. Hati memiliki kapasitas cadangan sehingga manifestasi klinis dari
kerusakan hati pada manusia baru akan muncul ketika telah terjadi kerusakan hati
mencapai 80%-90% (Crawford and Liu, 2010). Tidak terdapat patokan pasti
hingga pada persen kerusakan berapakah manifestasi klinis kerusakan hati tikus
akan muncul, tetapi dari penelitian Sasminto (2013) setelah peningkatan SGOT
sebanyak 20 kali lipat, tikus akan mengalami kematian karena telah terjadi
kerusakan fungsi hati.
Hati dapat mengalami berbagai kerusakan. Kerusakan-kerusakan yang
dapat terjadi pada hati, yaitu:
1. Perlemakan hati (Steatosis)
Akumulasi lemak dalam hati atau dikenal sebagai steatosis merupakan
tanda umum toksisitas hati dan dapat diakibatkan oleh zat kimia toksik. Salah satu
senyawa yang dapat mengakibatkan steatosis adalah karbon tetraklorida (CCl4).
Karbon tetraklorida dapat menyebabkan perlemakan hati melalui penghambatan
sintesis satuan protein dari lipoprotein dan penekanan konjugasi trigliserid dengan
lipoprotein (Hodgson, 2010).
2. Nekrosis hati
Nekrosis hati merupakan kematian dari hepatosit yang termasuk dalam
kerusakan akut. Nekrosis hati terjadi akibat paparan sejumlah zat kimia.
Kerusakan hati jenis ini ditandai dengan edema sitoplasma, dilatasi retikulum
3. Kolestasis
Kolestasis merupakan penekanan atau penghentian aliran empedu yang
disebabkan oleh faktor dalam atau luar dari hepar (Hodgson, 2010). Zat-zat yang
dapat menyebabkan kolestasis contohnya adalah steroid anabolik dan kontrasepsi
seperti klorpromazin dan eritromisin laktobionat (Lu, 1995).
4. Sirosis
Sirosis merupakan hepatotoksisitas yang ditandai dengan adanya kolagen
di seluruh bagian hati yang menimbulkan terbentuknya jaringan parut. Hal ini
terjadi karena adanya paparan senyawa kimia secara kronis yang mengakibatkan
akumulasi yang menghambat aliran darah, metabolisme hepar, dan detoksifikasi
(Hodgson, 2010). Pada kasus sirosis, terjadi kematian sejumlah besar hepatosit
yang mengakibatkan hati tidak mampu untuk mengganti hepatosit yang mati.
Jika diurutkan dari beratnya kerusakan hati, kerusakan yang tergolong
ringan adalah steatosis, diikuti nekrosis, dan yang terberat adalah sirosis.
Kolestasis sendiri merupakan gangguan yang jarang ditemui.
D. Alanin Aminotransferase (ALT) dan Aspartat Aminotransferase (AST)
Enzim ALT dan AST sering digunakan dalam uji fungsi hati. Enzim
ALT dan AST mencerminkan keutuhan atau integritas sel-sel hati. Keberadaan
kedua enzim hati tersebut dapat mencerminkan kerusakan sel-sel hati. Makin
tinggi peningkatan kadar ALT dan AST, semakin tinggi tingkat kerusakan sel-sel
hati (Suhardjo dan Cahyono, 2009).
Konsentrasi ALT terbesar terdapat pada hati yang merupakan petunjuk
oksidatif akibat karbon tetraklorida,enzim AST tidak hanya dilepaskan oleh hati.
AST juga dilepaskan dalam jumlah besar ke dalam darah oleh organ-organ lain
seperti jantung, otot rangka, ginjal, otak, paru, dan pankreas (Pratt and Kaplan,
2000). AST lebih sering dijadikan sebagai data pendukung karena tidak spesifik
untuk menandakan terjadinya kerusakan hati (Shivaraj, 2009).
Hastuti (2008) menyebutkan bahwa rentang nilai normal ALT tikus
berada pada kisaran 29,8-77,0 U/L. Terdapat beberapa pendapat mengenai nilai
AST tikus dalam keadaan normal, seperti pada penelitian hepatoprotektor yang
dilakukan Balrianan (2015) dan Eviani (2014). Balrianan (2015) memperoleh
hasil rata-rata AST pada tikus normal sebesar 111,2 ± 11,1 U/L, sedangkan Eviani
(2014) memperoleh hasil rata-rata AST sebesar 127,8 ± 7,3 U/L pada kelompok
kontrol olive oil yang tidak menimbulkan efek hepatoprotektif maupun
hepatokuratif sehingga dapat dianggap sebagai kadar AST normal tikus.
E. Hepatotoksin
Hepatotoksin diklasifikasikan menjadi dua, yaitu :
1. Hepatotoksin intrinsik (Hepatotoksin dapat diramalkan)
Senyawa yang mempunyai efek hepatotoksik hampir pada seluruh
populasi yang terpejankan senyawa tersebut. Senyawa ini bergantung pada dosis
pemberian. Contohnya : karbon tetraklorida, parasetamol, dan alkohol (Friedman
and Keeffe, 2012).
2. Hepatotoksin idiosinkratik (Hepatotoksin tidak dapat diramalkan)
Senyawa yang mempunyai efek hepatotoksik pada sebagian kecil
pemberian. Contohnya : fenitoin, sulfonamida, valproat, dan isoniazid (Friedman
and Keeffe, 2012).
F. Karbon tetraklorida
Rumus molekul untuk karbon tetraklorida yaitu yang berbetuk tidak
berwarna, berbau khas, dan tidak dapat menyala. Berat molekul 153, kelarutan
dalam air 0,08% pada suhu 20 ºC; dapat larut dalam alkohol, benzena, kloroform,
eter, karbon disulfida, petroleum eter, naftalena, aseton, fixed dan volatile oils
(SiKer Nas, 2010).
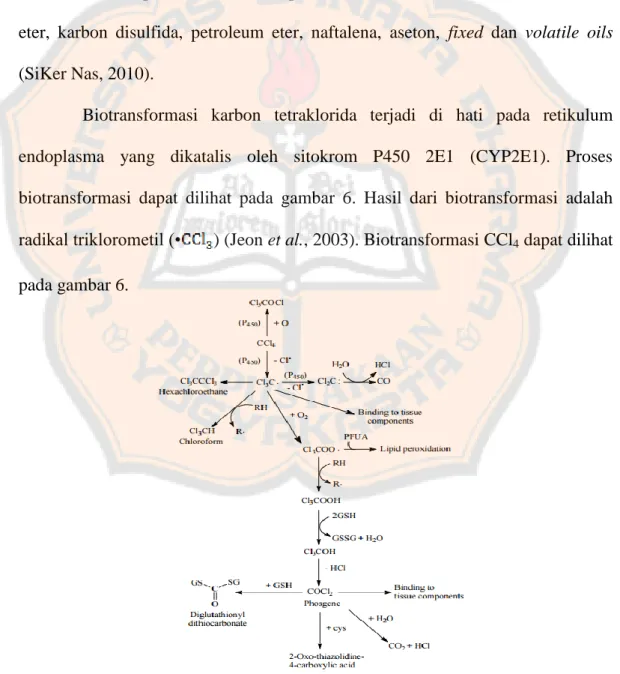
Biotransformasi karbon tetraklorida terjadi di hati pada retikulum
endoplasma yang dikatalis oleh sitokrom P450 2E1 (CYP2E1). Proses
biotransformasi dapat dilihat pada gambar 6. Hasil dari biotransformasi adalah
radikal triklorometil (• ) (Jeon et al., 2003). Biotransformasi CCl4 dapat dilihat
pada gambar 6.
Gambar 6. Biotransformasi karbon tetraklorida (McGregor and Lang, 1999)
1. Perusakan hati oleh karbon tetraklorida
Radikal bebas trikolorometil dapat berikatan dengan komponen sel hati
yang berefek pada penghambatan sekresi lipoprotein. Radikal bebas yang
berinteraksi dengan lipid akan menyebabkan proses oksidasi lemak tak jenuh atau
disebut peroksidasi lipid yang dapat mengganggu fungsi sel dan integritas
membran serta kematian sel (Bateman, Jefferson, Thomas, Thompson, dan Vale,
2014). Peroksidasi lipid ini menyebabkan menumpuk lemak di hati (steatosis)
(Manahan, 2002).
Kerusakan hati oleh karbon tetraklorida dapat dilihat dengan adanya
kenaikan kadar serum ALT dan AST (Ganong and McPhee, 2011). Pada saat
steatosis, dalam tubuh manusia terjadi peningkatan kadar serum ALT sebesar 3x
normal dan kadar serum AST sebesar 4x normal (Zimmerman, 1999). Adewole,
Salako, Doherty, and Naicker (2007) mengemukakan bahwa radikal bebas dari
CCl4 dapat menyebabkan terjadinya stres oksidatif pada berbagai jaringan seperti
hati, ginjal, jantung, otak, dan darah sehingga kadar AST juga dapat meningkat.
2. Rute pemejanan karbon tetraklorida
Administrasi obat terbagi menjadi dua jenis, yakni intravaskular (i.v.)
dan ekstravaskular (e.v.). Rute pemberian yang tergolong i.v. akan
memungkinkan obat yang masuk untuk langsung memasuki pembuluh darah
(sirkulasi sistemik) sedangkan obat yang termasuk e.v. tidak melalui pembuluh
darah (Gupta, 2007).
Beberapa rute pemberian obat yang tergolong e.v. adalah rute pemberian
2007). Obat yang dipejankan dengan rute i.p. pasti akan mengalami first pass
metabolism, tidak seperti rute i.m. atau s.c. yang terdapat pada golongan yang
sama (Hau and Schapiro, 2002). Karbon tetraklorida pada penelitian ini
dipejankan secara i.p. Hal ini memungkinkan hepatotoksin ini untuk mengalami
metabolisme oleh sitokrom P450 yang terdapat pada sel hepatosit hati menjadi
radikal toksik sehingga dapat menginduksi kerusakan hati berupa steatosis.
G. Maserasi
Ekstraksi adalah suatu metode penyarian senyawa dalam suatu bahan,
dalam hal ini simplisia. Dalam proses ekstraksi, terjadi difusi pelarut ke dalam sel
dari bahan yang digunakan. Pelarut yang masuk ke dalam sel akan melarutkan
senyawa bila kelarutan senyawa yang diekstrak sama dengan pelarut.
Kesetimbangan dapat terjadi antara zat terlarut dan pelarut dari proses tersebut.
Salah satu metode ekstraksi adalah maserasi (Bombardelli, 1991).
Maserasi merupakan metode ekstraksi sederhana dengan merendam
simplisia yang berasal dari tanaman dalam pelarut yang sesuai, ditempatkan
dalam wadah tertutup pada suhu kamar. Maserasi memiliki keunggulan
dibandingkan dengan sokletasi, yakni lebih bagus bagi senyawa yang tidak tahan
suhu tinggi, karena maserasi dalam prosesnya tidak melibatkan panas layaknya
sokletasi (Sarker, Latif, dan Grey, 2006). Kecuali dinyatakan lain, seluruh
simplisia harus dihaluskan menjadi serbuk terlebih dahulu (DepKes RI, 1989).
Maserasi dapat menggunakan shaker 120 rpm selama 24 jam untuk
mempercepat proses ekstraksi (Masroh, 2010). Ekstraksi berhenti ketika terjadi
Maserasi menggunakan etanol 70% P jika tidak dinyatakan lain (Badan
POM RI, 2009). Pelarut lain yang dapat digunakan sebagai pelarut dalam maseasi
adalah etanol 30%. Ekstrak etanol 30% dapat menyari senyawa fenolik pada daun
tumbuhan Cymbopogon citratus (Hasim, Falah, Ayunda, dan Faridah, 2015).
Menurut Javaplant (2000) etanol 30% digunakan oleh perusahan pada pilot scale
untuk ekstraksi bahan alam, dimana salah satu pengujian pada proses ini yaitu
pengujian terhadap konsentrasi ekstrak tertentu untuk mengetahui efek
farmakologis yang dihasilkan.
Semua hasil maserasi yang disebut maserat diuapkan untuk mendapatkan
ekstrak kental (Badan POM RI, 2009). Ekstrak adalah sediaan kering, kental, atau
cair yang dibuat dengan menyari simplisia nabati atau hewani menurut cara yang
cocok, di luar pengaruh cahaya matahari langsung (KemenKes RI, 2013).
H. Metode Pengujian
Studi tentang efek toksik pada hati dapat dilakukan dengan beberapa
cara, antara lain tes enzim serum dan analisis histologi kelainan hati yang dapat
dipaparkan sebagai berikut:
1. Tes enzim serum
Pengukuran dilakukan untuk mendeteksi terjadinya ketoksikan pada hati.
Enzim-enzim transaminase adalah contoh enzim yang dapat mengalami
perubahan ketika terjadi kerusakan hepatoseluler. Penentuan kadar ALT dan AST
adalah pengujian yang umum dilakukan untuk mendeteksi kerusakan yang terjadi
pada hati. Peningkatan enzim dapat mencapai beberapa kali lipat dari nilai normal
2. Analisis histologis kelainan hati
Deskripsi histologis mengenai kerusakan pada hati juga sangat penting
dalam analisis potensi hepatotoksik zat kimia terhadap kerusakan yang terjadi.
Pengamatan mikroskopik dengan bantuan cahaya dapat dilakukan untuk
mendeteksi histologis kerusakan hati (Plaa dan Charbonneau, 2001).
I. Landasan Teori
Organ hati merupakan organ sekaligus kelenjar terbesar didalam tubuh.
Organ ini memproduksi empedu dan juga mengeluarkan hasil produksi dari
makanan yang sudah dicerna (Wibowo dan Paryana, 2005).
Beberapa kerusakan hati akibat efek toksik yaitu steatosis, nekrosis,
kolestasis, dan sirosis (Lu, 1995). Hepatotoksin merupakan senyawa yang
mempunyai efek hepatotoksik, dibedakan menjadi dua yaitu hepatotoksin
instrinsik dan indiosinkratik (Friedman and Keeffe, 2012).
Salah satu yang senyawa yang menyebabkan toksik pada hati adalah
karbon tetraklorida atau CCl4 (SiKer Nas, 2010). Biotransformasi karbon
tetraklorida terjadi di hati pada retikulum endoplasma yang dikatalis oleh
sitokrom P450 2E1 (CYP2E1). Hasil dari biotransformasi diperoleh radikal
triklorometil (• ) (Jeon et al., 2003). Radikal bebas trikolorometil dapat berikatan dengan komponen sel hati yang berefek pada penghambatan sekresi
lipoprotein. Hal ini menyebabkan menumpuknya lemak di hati (steatosis)
(Manahan, 2002). Radikal bebas yang berinteraksi dengan lipid akan
menyebabkan peroksidasi lipid yang dapat mengganggu fungsi sel dan integritas
tetraklorida dapat dilihat dengan adanya kenaikan kadar ALT dan AST. Pada saat
steatosis terjadi peningkatan kadar ALT sebesar 3x normal dan kadar AST sebesar
4x normal (Zimmerman, 1999). Konsentrasi enzim ALT terbesar terdapat pada
hati, merupakan petunjuk spesifik kerusakan hati dibandingkan AST yang
terdapat pada hampir semua jaringan (Zimmerman, 1999).
Indonesia kaya akan berbagai sumber daya, antara lain kaya akan
tumbuhan yang dapat digunakan untuk mengobati penyakit. Salah satu tumbuhan
tersebut adalah jarong (Stachytarpheta indica (L.) Vahl.).
Maserasi merupakan metode ekstraksi sederhana dengan cara merendam
simplisia yang berasal dari tanaman dalam pelarut yang sesuai. Metode ini bagus
bagi senyawa yang tidak tahan suhu tinggi (Sarker et al., 2006).
Salah satu senyawa yang berperan sebagai hepatoprotektor adalah
senyawa flavonoid. Penelitian yang dilakukan oleh Joshi et al. (2010) dan Gayatri
et al. (2011) menunjukkan bahwa kandungan flavonoid pada ekstrak etanol 96%
daun jarong (Stachytarpheta indica (L.) Vahl.) dapat berperan sebagai
hepatoprotektor. Berdasarkan pemaparan di atas, diperlukan penelitian untuk
mengetahui efek hepatoprotektif ekstrak etanol 30% daun Stachytarpheta indica
(L.) Vahl. untuk melindungi hati dari steatosis pada tikus akibat pemejanan CCl4.
J. Hipotesis
Ekstrak etanol 30% daun jarong (Stachytarpheta indica (L.) Vahl.)
memiliki efek hepatoprotektif dengan menurunkan kadar ALT-AST pada tikus
25
BAB III
METODE PENELITIAN
A. Jenis dan Rancangan Penelitian
Penelitian mengenai efek hepatoprotektif ekstrak etanol 30% daun jarong
(Stachytarpheta indica (L.) Vahl.) terhadap kadar ALT-AST pada tikus jantan
galur Wistar terinduksi karbon tetraklorida merupakan jenis penelitian
eksperimental murni dengan rancangan acak lengkap pola searah.
B. Variabel dan Definisi Operasional
1. Variabel utama
a. Variabel bebas. Variabel bebas penelitian ini adalah variasi dosis dalam
pemberian ekstrak etanol 30% daun jarong (Stachytarpheta indica (L.) Vahl.).
b. Variabel tergantung. Variabel tergantung penelitian ini adalah nilai kadar
ALT dan AST tikus jantan galur Wistar yang terinduksi karbon tetraklorida
setelah pemberian ekstrak etanol 30% daun jarong (Stachytarpheta indica (L.)
Vahl.).
2. Variabel pengacau
a. Variabel pengacau terkendali. Variabel pengacau terkendali dalam
penelitian ini adalah kondisi hewan uji, yaitu tikus jantan galur Wistar yang
berumur 2-3 bulan dengan berat badan 160-250 gram, cara pemberian ekstrak
secara per oral, cara pemejanan senyawa, frekuensi waktu pemberian ekstrak, dan
b. Variabel pengacau tak terkendali. Variabel pengacau tak terkendali pada
penelitian ini adalah kondisi patologis dari tikus jantan galur Wistar.
3. Definisi operasional
a. Daun Stachytarpheta indica (L.) Vahl.
Daun yang diambil dari tanaman Stachytarpheta indica (L.) Vahl. adalah
daun yang berwarna hijau, segar, dan tidak rusak. Daun diambil ketika tanaman
sudah berbunga (Purwantisari, 2014).
b. Ekstrak etanol 30% daun Stachytarpheta indica
Ekstrak etanol 30% daun Stachytarpheta indica (L.) Vahl.adalah ekstrak
kental yang didapatkan dengan cara merendam (memaserasi) simplisia kering
daun jarong dalam etanol dengan konsentrasi 30%. Ekstrak kemudian dipekatkan
dengan menggunakan vacuum rotary evaporator dan diuapkan dengan waterbath
hingga bobot tetap.
c. Efek hepatoprotektif
Efek hepatoprotektif merupakan kemampuan ekstrak etanol 30% daun
Stachytarpheta indica (L.) Vahl. dengan dosis tertentu yang melindungi hati
dengan cara menurunkan kadar ALT-AST pada tikus jantan galur Wistar
terinduksi karbon tetraklorida. Efek hepatoprotektif dinyatakan dalam persen efek
hepatoprotektif.
d. Waktu pengukuran efek hepatoprotektif
Didefinisikan sebagai pengukuran yang dilakukan 24 jam sejak
pemejanan karbon tetraklorida, dimana waktu 24 jam adalah waktu di mana
pemejanan karbon tetrakloria telah dilakukan pemberian ekstrak etanol
Stachytarpheta indica (L.) Vahl.kepada hewan uji.
e. Dosis efektif
Didefinisikan sebagai sejumlah miligram per kilogram berat badan
(mg/kgBB) ekstrak etanol 30% daun Stachytarpheta indica (L.) Vahl. yang
memiliki % hepatoprotektif paling mendekati 100% proteksi hati.
f. Kontrol ekstrak
Kontrol ekstrak adalah pemberian ekstrak etanol 30% daun
Stachytarpheta indica (L.) Vahl. dosis 400 mg/kgBB kepada hewan uji untuk
kemudian enam jam setelah pemberian, dilakukan pengambilan darah dan
pengukuran kadar ALT dan AST. Kontrol ekstrak ini diberikan tanpa induksi
karbon tetraklorida.
g. ALT-AST
Alanin aminotransferase (ALT) dan Aspartat aminotransferase (AST)
adalah enzim yang ditemukan di dalam serum. Peningkatan kadar kedua enzim ini
dapat mengindikasikan adanya kerusakan pada hati.
C. Bahan Penelitian
1. Bahan utama
a. Hewan uji
Hewan uji yang digunakan dalam penelitian ini adalah tikus jantan galur
Wistar yang berusia 2-3 bulan dengan berat badan 160-250 g yang diperoleh dari
b. Bahan uji
Bahan uji yang digunakan yaitu serbuk daun Stachytarpheta indica (L.)
Vahl. yang diperoleh dari kebun obat Fakultas Farmasi Universitas Sanata
Dharma.
2. Bahan kimia
a. Pelarut ekstrak
Pelarut ekstrak yang digunakan adalah etanol 30% yang terbuat dari
campuran etanol 96% dan aquadest. Etanol 96% diperoleh dari Toko Progo
Mulyo, Yogyakarta dan aquadest diperoleh dari Laboratorium Kultur Jaringan
Fakultas Farmasi Universitas Sanata Dharma.
b. Hepatotoksin
Karbon tetraklorida yang digunakan dalam penelitian ini adalah karbon
tetraklorida Merck®. Karbon Tetraklorida yang diperoleh dari Laboratorium
Kimia Analisis Fakultas Farmasi Universitas Sanata Dharma Yogyakarta.
c. Kontrol negatif
Olive oil yang digunakan sebagai kontrol adalah olive oil Cesar® dari PT
Prambanan Kencana.
d. Pelarut ekstrak ketika digunakan
Pelarut ekstrak yang digunakan adalah CMC Na yang diperoleh dari CV
General Labora, Yogyakarta.
e. Reagen ALT
Reagen ALT yang digunakan adalah reagen ALT DiaSys. Adapun
Tabel I. Tabel komposisi dan konsentrasi reagen ALT
Komposisi pH Konsentrasi
R1: TRIS 7,15 140 mmol/L
L-Alanine 700 mmol/L
LDH (Lactate dehydrogenase) ≥2300 U/L
R2: 2-Oxoglutarate 85 mmol/L NADH 1 mmol/L Pyridoxal-5 phospate FS: God’s buffer Pyridoxal-5-phospate 9,6 100 mmol/L 13 mmol/L f. Reagen AST
Reagen AST yang digunakan adalah reagen AST DiaSys. Komposisi
dan konsentrasi dari reagen AST adalah sebagai berikut:
Tabel II. Tabel komposisi dan konsentrasi reagen AST
Komposisi pH Konsentrasi
R1:TRIS 7,65 110 mmol/L
L-Aspartate 320 mmol/L
MDH (Malate dehydrogenase) ≥800 U/L
LDH (Lactate dehydrogenase) ≥1200 U/L
R2: 2-Oxyglutarate 65 mmol/L NADH 1 mmol/L Pyridoxal-5 phospate FS: God’s buffer Pyridoxal-5-phospate 9,6 100 mmol/L 13 mmol/L D. Alat Penelitian
1. Alat pembuatan serbuk daun Stachytarpheta indica (L.) Vahl.
Alat yang digunakan antara lain oven, mesin penyerbuk, dan ayakan.
2. Alat ekstraksi daun Stachytarpheta indica (L.) Vahl.
Alat-alat yang digunakan antara lain beaker glass, erlenmeyer, gelas
ukur, labu ukur, cawan porselen, pipet tetes, batang pengaduk, shaker, dan
3. Alat uji penetapan kadar air
Alat-alat yang digunakan antara lain moisture balance dan sendok.
4. Alat pengujian hepatoprotektif
Alat-alat yang dibutuhkan adalah gelas Beaker, gelas ukur, tabung reaksi,
labu ukur, pipet tetes, batang pengaduk (Pyrex Iwaki Glass®), timbangan analitik
(Mettler Toledo®), vortex (Genie Wilten®), spuit injeksi per oral untuk tikus, spuit
injeksi intraperitonial, pipa kapiler, micropipet, tabung Eppendorf, sentrifuge,
microvitalab 200 Merck®, blue tip, dan yellow tip.
E. Tata Cara Penelitian
1. Determinasi tanaman jarong (Stachytarpheta indica (L.) Vahl.)
Daun tanaman jarong diperoleh dari kebun obat kampus III Universitas
Sanata Dharma, Paingan, Maguwoharjo. Tanaman jarong dideterminasi dengan
mencocokkan morfologi tanaman jarong dengan buku acuan (Van Steenis, 1992).
Determinasi dilakukan dilakukan di Laboratorium Farmakognosi Fitokimia,
Fakultas Farmasi Universitas Sanata Dharma oleh Bapak Yohanes Dwiatmaka.
2. Pengumpulan bahan uji
Bahan uji yang dipilih adalah daun dari tanaman jarong yang hijau, segar,
tidak didapati penyakit, dan tidak rusak. Daun diambil dari Kebun Obat Fakultas
Farmasi Universitas Sanata Dharma pada bulan Juli dan Agustus 2015.
3. Pembuatan serbuk
Pembuatan serbuk daun jarong (Stachytarpheta indica (L.) Vahl.) diawali
dengan kaidah pembuatan simplisia. Sortasi dilakukan untuk memastikan bahwa
daun yang digunakan adalah daun yang hijau dan tidak berlubang. Pencucian
dilakukan supaya daun yang diperoleh bebas dari kotoran yang dapat berupa debu
ataupun bagian tanaman yang lain. Selanjutnya daun dikeringkan, pengeringan
dilakukan dengan penutupan kain hitam agar tidak langsung terkena sinar
matahari. Pengeringan dilakukan hingga daun tidak lagi basah, kemudian
dipindahkan ke dalam oven bersuhu 40oC. Penetapan suhu berdasarkan pada
aturan Depkes RI (1985) di mana disebutkan bahwa pengeringan simplisia
dilakukan pada suhu antara 30o-90oC.
Setelah daun benar-benar kering (ditunjukkan dengan daun dapat hancur
dengan diremas), daun diserbukkan menggunakan penyerbuk dan disaring
menggunakan pengayak dengan nomor mesh 40. Hal ini sesuai dengan aturan
yang ditetapkan oleh BPOM RI.
4. Penetapan kadar air serbuk daun Stachytarpheta indica (L.) Vahl.
Serbuk daun Stachytarpheta indica (L.) Vahl. dimasukkan ke dalam alat
moisture balance sebanyak 5 gram, lalu diratakan. Bobot serbuk tersebut
ditetapkan sebagai bobot sebelum pemanasan, setelah itu dipanaskan pada suhu
105oC selama 15 menit. Serbuk yang telah dipanaskan ditimbang kembali lalu
dihitung sebagai bobot setelah pemanasan. Kadar air serbuk menurut BPOM RI
5. Uji tabung kandungan polifenol
Serbuk yang telah diuji kadar airnya, digunakan untuk uji sederhana
kandungan polifenol. Uji dilakukan dengan menambahkan 10 mL aquadest pada
sebuah tabung berisi 2 g serbuk dan 10 mL etanol 30% pada tabung lain berisi 2 g
serbuk. Keduanya didihkan di atas tangas air, selanjutnya dilakukan penyaringan.
Setelah dingin, filtrat diteteskan FeCl3 sebanyak 3 tetes, terbentuknya warna
hijau-biru menunjukkan hasil positif adanya polifenol (Wulandari dan Hartini,
2015).
6. Pembuatan ekstrak kental daun Stachytarpheta indica (L.) Vahl.
Pembuatan ekstrak etanol 30% dilakukan dengan metode penyarian
maserasi. Proses maserasi dilakukan dengan memasukkan 30 g serbuk simplisia
ke dalam labu erlenmeyer, yang kemudian direndam dengan pelarut 300 mL
(Hasim dkk., 2015) selama 24 jam dengan bantuan shaker (Masroh, 2010).
Setelah itu dilakukan remaserasi. Remaserasi dilakukan dengan penambahan
pelarut ke dalam ampas dari proses maserasi yang dilakukan sebelumnya, dengan
jumlah pelarut dan waktu ekstraksi yang sama seperti maserasi pertama.
Filtrat hasil dari maserasi dan remaserasi kemudian dicampurkan. Hasil
yang diperoleh berupa ekstrak cair yang kemudian dipekatkan dengan vacuum
rotary evaporator selanjutnya diuapkan kembali dalam cawan porselen di atas
waterbath dengan suhu 80oC sehingga didapatkan ekstrak kental dengan bobot
tetap.
Menurut KemenKes RI (2013), ekstrak kental diperoleh ketika tercapai
analitik berturut-turut tidak melebihi 0,5 mg. Ekstrak ditimbang bobotnya setiap
satu jam. Rendemen ekstrak dihitung dengan rumus:
7. Pembuatan CMC Na 1%
Pembuatan CMC Na 1% dilakukan dengan penimbangan sebanyak satu
gram CMC Na, kemudian dilarutkan dengan 40 mL aquadest lalu didiamkan
selama 24 jam hingga CMC Na mengembang. Setelah CMC Na mengembang,
aquadest ditambahkan hingga 100 mL.
8. Penetapan dosis ekstrak etanol daun Stachytarpheta indica (L.) Vahl.
Penentuan dosis ekstrak etanol 30% mengacu pada penelitian yang
dilakukan oleh Joshi et al. (2010) yang menyebutkan bahwa dosis efektif ekstrak
etanol daun jarong adalah 200 mg/kgBB. Dosis ini dijadikan sebagai dosis tengah.
Penelitian ini menggunakan tiga peringkat dosis dengan faktor kelipatan 2
sehingga dosis rendah sebesar 100 mg/kgBB, dosis tengah sebesar 200 mg/kgBB,
dan dosis tinggi 400 mg/kgBB.
9. Pembuatan larutan karbon tetraklorida konsentrasi 50%
Berdasarkan penelitian Jakanat dan Al-Merie (2002), larutan karbon
tetraklorida dibuat dengan konsentrasi 50% dengan perbandingan volume karbon
tetraklorida dan pelarut yakni 1:1. Larutan karbon tetraklorida dibuat dengan
melarutkan cairan karbon tetraklorida (p.a) ke dalam minyak zaitun dengan
10. Uji pendahuluan
a. Penetapan dosis hepatotoksin
Penetapan dosis hepatotoksin dilakukan melalui studi literatur dari
penelitian yang dilakukan oleh Al-Olayan, el-Khadagry, Aref, Othman, Kassab
dan Monem (2014) yang menyebutkan bahwa dosis hepatotoksin karbon
tetraklorida yang digunakan untuk menginduksi kerusakan hati tikus jantan galur
Wistar adalah 2 mL/kgBB dimana volume CCl4 sama dengan volume minyak
zaitun (1:1) yang menjadi pelarutnya. Dosis karbon tetraklorida 2 mL/kgBB yang
digunakan dalam penelitian dapat menginduksi hepatotoksik pada tikus jantan
sebagai subjek penelitian tersebut tanpa menyebabkan kematian (Janakat dan
Al-Merie, 2002).
b. Penetapan waktu pencuplikan darah
Waktu pencuplikan darah diperoleh dengan cara melakukan orientasi
dengan pengukuran pada tiga titik waktu, yakni pada waktu ke-0 (sebelum
pemejanan larutan karbon tetraklorida) serta jam ke-24 dan 48 setelah pemejanan.
Langkah selanjutnya adalah pengukuran peningkatan kadar AST-ALT. Penelitian
terdapat sebelumnya yang dilakukan oleh Janakat dan Al-Merie (2002) telah
menunjukkan bahwa terdapat peningkatan aktifitas ALT pada tikus yang
terinduksi karbon tetraklorida yang dilarutkan dalam olive oil dengan
perbandingan (1:1), yakni dengan dosis 2 mL/kgBB. Peningkatan kadar maksimal
terjadi pada jam ke-24 setelah pemberian karbon tetraklorida secara injeksi dan
kemudian berangsur menurun pada jam ke-48 dan terjadi perbaikan sel hati