BAB 2
TINJAUAN PUSTAKA
2.1. Pestisida
Pestisida adalah substansi (zat kimia) yang digunakan untuk membunuh atau mengendalikan berbagai hama. Berdasarkan asal katanya pestisida berasal dari bahasa Inggris yaitu pest berarti hama dan cida berarti pembunuh (Djojosumarto, 2008). Asosiasi Kimia Nasional Amerika Serikat menyatakan, bahwa yang juga termasuk pengertian pestisida ialah agensia yang dipergunakan untuk keperluan-keperluan khusus seperti zat pengatur tumbuh, zat penggugur daun, zat pengering (desiccant) dan zat-zat lainnya yang sejenis seperti feromon, zat kimia pemandul, zat anti feedant, atraktan, repelen, sinergis (Oka dan Ida Nyoman, 1993).
2.1.1 Klasifikasi Pestisida
Klasifikasi pestisida dapat dibagi dua yaitu berdasarkan golongan hama yang dibunuh dan berdasarkan efek yang ditimbulkannya pada hama sasaran sebagai berikut,
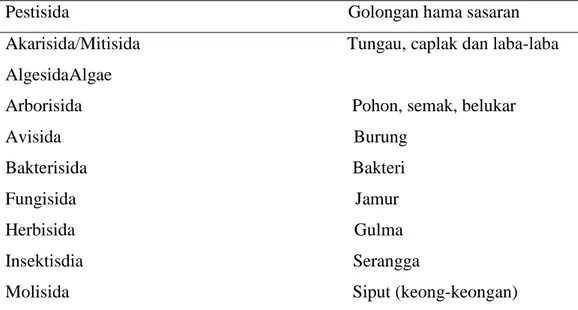
Tabel 2.1 Berdasarkan golongan hama sasaran yang dibunuh
Pestisida Golongan hama sasaran Akarisida/Mitisida Tungau, caplak dan laba-laba AlgesidaAlgae
Arborisida Pohon, semak, belukar Avisida Burung
Bakterisida Bakteri Fungisida Jamur Herbisida Gulma Insektisdia Serangga
Tabel 2.2 Berdasarkan efek pestisida terhadap hama
Pestisida Pengaruhnya
Anti-makan (anti-feedant) Menghalangi makan, hama tetap tinggal pada tanaman, hama klaparan dan
akhirnya mati mengurangi transpirasi. Anti-transpiran Mengurangi transpirasi.
Atrakta Menarik hama kepada lokasi yang memperoleh perlakuan (atraktan seks). Zat kimia pemandul Merusak reproduksi hama.
Penggugur daun (defoliant) Menghilangkan pertumbuhan bagian
tanaman yang tidak dikehendaki, tanpa membunuh tanaman seketika.
Zat pengering (desiccant) Mengeringkan daun, batang dan serangga Feromon Melepaskan atau menghalangi perilaku tertentu dari serangga
Zat pengatur tumbuh Menghentikan, mempercepat atau merubah proses pertumbuhan tanaman Repelen Mengusir hama dari objek sasaran Sinergis Meningkatkan efektifitas dari agensia yang aktif
Sumber: Oka dan Ida Nyoman, 1993.
2.1.2 Jenis-jenis Pestisida
Insektisida dapat diklasifikasikan ke dalam dua kelompok besar yaitu (1) berdasarkan susunan kimia, dan (2) berdasarkan cara kerjanya.
1. Kelompok yang berdasarkan susunan kimia dibagi lagi menjadi kelompok inorganik dan kelompok organik. Kelompok organik ini dibagi lagi ke dalam kelompok organik sintetik dan kelompok organik alamiah.
Kelompok inorganik berasal dari unsur-unsur alamiah dan tidak mengandung karbon. Misalnya arsenikum, merkurium, dan talium, boron, tembaga, sulfur, semuanya persisten yang daya racunnya bersifat akumulatif.
Kelompok organik sintetik terdiri atas unsur karbon, hidrogen, dan satu atau beberapa unsur seperti klorin, oksigen, belerang, fosfor, dan nitrogen.Kelompok ini merupakan hasil sintesa manusia. Kelompok organik sintetik ini dapat diklasifikasikan lagi berdasarkan unsur utama yang dikandungnya yaitu senyawa-senyawa sebagai berikut :
a. Organofosfor (malation, monokrotofos, parathion, fosfamidon, bromofos, diazinon, dimetoat, diklorofos, fenitrotion, fention, dan lain-lain.) Bekerja sebagai insektisida kontal atau sistemik. Kebanyakan diantaranya memiliki aktivitas residu dalam waktu pendek, karena itu perlu diaplikasikan berulang-ulang
b. Metal karbamat yang mengandung fenol seperti BPMC, karbaril, MIPC, metiokarb, propoksur. Metil karbamat yang mengandung senyawa-senyawa hidrosiklik seperti karbofuran, dimetilon.
c. Organoklorin seperti DDT, aldrin, dieldrin, heptaklor, toksafin, pentaklorofenol. Senyawa ini adalah sintetik kebanyakan sebagai racun kontak dan racun perut. Kebanyakan memiliki aktifitas residu yang panjang. Ada kecenderungan menumpuk di dalam rantai makanan yang menimbulkan kematian pada ikan dan kehidupan lainnya. Oleh karena itu penggunaannya sangat dibatasi.
d. Piretroid sintetik yaitu senyawa-senyawa yang struktur kimianya seperti piretrin yang berasal dari tumbuhan. Piretroid ini menunjukkan efikasi yang lebih tinggi terhadap serangga dan pada umumnya toksisitasnya terhadap mamalia lebih rendah dibandingkan dengan insektisida lainnya. Namun kebanyakan diantaranya sangat toksik tehadap ikan, tawon madu dan serangga berguna lainnya. Bekerjanya terutama secara kontak dan tidak sistematik.
e. Fumigan diantaranya metal bromide, etilen bromide, karbon disulfide, fosfin, dan naftalin dipergunakan untuk mengendalikan serangga hama gudang, hama rumah dan tikus.Daya racunnya berbeda-beda satu sama lain, tetapi semuanya sangat mudah diabsorpsi oleh paru-paru.
2. Kelompok insektisida berdasarkan cara kerjanya ialah bagaimana efeknya dan bagaimana cara masuknya ke dalam tubuh hama. Setelah insektisida masuk kedalam tubuh serangga, maka akan mempengaruhi proses hidup hama tersebut.
Efek-efek yang terlihat adalah mati, sakit, perubahan perilaku, pertumbuhan, metabolisme, atau kapasitas reproduksinya. Misalnya :
a. Racun-racun perut masuk kedalam perut serangga hama melalui mulut, diabsorpsi ke dalam tubuh melalui saluran pencernaan
b. Racun kontak pada umumnya masuk kedalam tubuh hama melalui kontak tubuh serangga dengan permukaan daun yang mengandung racun tersebut. Racun-racun ini merusak sistem saraf dan pernapasan hama.
c. Fumigan, mudah sekali menguap dan masuk kedalam tubuh serangga hama dalam bentuk gas melalui sistem pernapasan.
d. Racun sistemik diaplikasikan pada daun, batang, buah-buahan atau akar diabsorpsi oleh tanaman. Didalam tubuh tanaman racun tersebut bergerak melalui sitem vascular menuju bagian-bagian yang tidak terkena perlakuan racun itu. Selama hama memakan racun itu juga akan ikut termakan. Racun sistemik itu juga dipergunakan untuk mengendalikan hama-hama ternak.
e. Racun penyebab mati lemas (suffocation) adalah racun yang menyumbat saluran pernapasan, biasanya senyawa yang mengandung minyak. Karena tidak dapat bernafas maka hama tersebut mati (Oka dan Ida Nyoman, 1993).
2.2. Tanaman Sirih Hutan (Piper aduncum L)
Berdasarkan taksonomi tanaman, Klasifikasi daun sesirihanhasil identifikasi tumbuhan dilaboratorium Herbarium Medanense (MEDA) Universitas Sumatera Utara adalah sebagai berikut : Kerajaan : Plantae Divisi : Spermatophyta Kelas : Dicotyledonae Bangsa : Piperales Familia : Piperaceae Genus : Piper
Gambar 2.1 Foto Tanaman sirih hutan (Piper aduncum L)
Nama daerah : Below-below (Karo), Sirih Hutan, Sesirihan, Kiseriuheun (Sunda). Habitat tanaman ini di areal perkebunan, hutan alami, berkayu, ujung runcing, pangkal membulat, tepi rata pada setiap buku, tangkai berbulu halus, silindris 5-10 mm, panjang daun 10-14 cm, lebar 5-6 cm, pertulangan menjari, hijau muda. Bunga majemuk, bentuk buli, berkelamin satu atau dua, daun pelindung bertangkai 0,5-1,25 mm, melengkung, tangkai benang sari pendek, kepala sari kecil, bakal buah duduk, kepala putik dua sampai tiga, pendek, putih, putih kekuningan. Buah buni, bertangkai pendek, panjang bulir 12-14 cm, masih muda kuning kehijauan, setelah tua hijau. Biji kecil dan berwarna coklat. Akar tunggang, putih kecoklatan.
2.3. Minyak Atsiri
Minyak atsiri adalah salah satu kandungan tanaman yang sering disebut minyak terbang, dinamakan demikian karena minyak tersebut mudah menguap. Selain itu, minyak atsiri juga disebut essential oil (dari kata essence) karena minyak tersebut memberikan bau pada tanaman (Koensoemardiyah, 2010). Minyak atsiri bukan merupakan senyawa tunggal, tetapi tersusun dari berbagai komponen kimia, seperti senyawa – senyawa monoterpen (Gunawan, 1991).
Minyak atsiri dibagi 2 kelompok, yaitu:
1. Minyak atsiri yang dengan mudah dapat dipisahkan menjadi komponen-komponen atau penyusun murninya, komponen-komponen ini dapat menjadi bahan dasar untuk diproses menjadi produk - produk lain. Contohnya: minyak sereh, minyak terpentin.
2. Minyak atsiri yang sukar dipisahkan menjadi komponen murni. Contohnya minyak nilam, minyak kenanga.
Minyak atsiri dari tanaman menghasilkan aroma yang berbeda, bahkan 1 jenis tumbuhaan yang sama bila ditanam ditempat yang berlainan mampu menghasilkan aroma yang berbeda, iklim, keberadaan tanah, dan sinar matahari. Cara pengolahan tidak hanya mempengharui rendeman minyak atsiri tetapi berpengaruh pula pada aromanya (Harris, 1987).
2.3.1. Komponen Kimia Minyak Atsiri
Pada umumnya perbedaan komposisi minyak atsiri disebabkan perbedaan jenis tanaman penghasil, kondisi iklim, tanah tempat tumbuh, umur panenan, metode ekstraksi yang digunakan dan cara penyimpanan minyak.
Minyak atsiri biasanya terdiri dari berbagai campuran persenyawaan kimia yang terbentuk dari unsur Karbon (C), Hidrogen (H), dan Oksigen (O). Pada umumnya komponen kimia minyak atsiri dibagi menjadi dua golongan, yaitu:
1. Golongan hidrokarbon yang terdiri dari persenyawaan Terpen
Persenyawaan yang termasuk golongan ini terbentuk dari unsur Karbon (C), dan Hidrogen (H). Jenis Hidrokarbon yang terdapat dalam minyak atsiri sebagian besar terdiri dari monoterpen (2 unit isopren), dan politerpen.
2. Golongan hidrokarbon teroksigenasi
Komponen kimia dari golongan ini terbentuk dari unsur Karbon (C), Hidrogen (H), dan Oksigen (O). Persenyawaan yang termasuk dari golongan ini adalah persenyawaan alkohol, aldehid, ester, fenol. Ikatan karbon yang terdapat dalam molekulnya dapat terdiri dari ikatan tunggal, dan ikatan rangkap dua dan ikatan rangkap tiga. Terpen mengandung ikatan tunggal dan ikatan rangkap dua. Senyawa terpen memiliki aroma kurang wangi, sukar larut dalam alkohol encer dan jika disimpan dalam waktu lama akan terbentuk resin. Golongan hidrokarbon teroksigenasi merupakan senyawa yang penting dalam minyak atsiri karena umumnya aroma yang lebih wangi. Fraksi terpen perlu dipisahkan untuk tujuan tertentu, misalnya untuk pembuatan parfum, sehingga didapatkan minyak atsiri yang bebas terpen (Ketaren, 1985).Pada minyak atsiri yang bagian utamanya terpenoid, biasanya terpenoid itu terdapat pada fraksi minyak atsiri yang tersuling uap. Zat inilah penyebab wangi, harum atau bau yang khas pada banyak tumbuhan (Harborne, 1987).
2.3.2. Biosintesa pembentukan Minyak Atsiri
Berdasarkan proses biosintesisnya atau pembentukan komponen minyak atsiri di dalam tumbuhan, minyak atsiri dapat dibedakan menjadi dua golongan. Golongan pertama adalah turunan terpen yang terbentuk dari asam asetat melalui jalur biosintesis asam mevalonat. Golongan kedua adalah senyawa aromatik yang terbentuk dari biosintesis asam sikimat melalui jalur fenil propanoid (Agusta, 2000).
Mekanisme dari tahap tahap reaksi biosintesis terpenoid yaitu asam asetat yang telah diaktifkan oleh koenzim A melalui kondensasi jenis Claisen menghasilkan asam asetoasetat. Senyawa yang dihasilkan ini dengan koenzim a melakukan kondensasi sejenis aldol menghasilkan rantai karbon bercabang sebagaimana ditemukan pada asam mevalonat. Reaksi-reaksi berikutnya ialah fosforilasi, eliminasi asam fosfat dan dekarboksilasi menghasilkan IPP (Isopentenil Pirofosfat) oleh enzim isomerase, IPP sebagi unit isopren aktif bergabung secara kepala ke ekor dengan DMAPP dan penggabungan ini merupakan langkah pertama dari polimerasi isopren untuk menghasilkan terpenoid. Penggabungan ini terjadi karena serangan elektron dari ikatan rangkap IPP terhadap atom karbon dari DMAPP yang kekurangan elektron diikuti oleh penyingkiran ion Pirofosfat. Serangan ini menghasilkan geranil pirofosfat (GPP) yakni senyawa antara bagi semua senyawa monoterpen. Penggabungan selanjutnya antara satu unit IPP dan GPP, dengan mekanisme yang sama seperti anatara IPP dan DMAPP menghasilkan Farnesil Pirofosfat (FPP) yang merupakan senyawa antara bagi semua senyawa seskuiterpen.
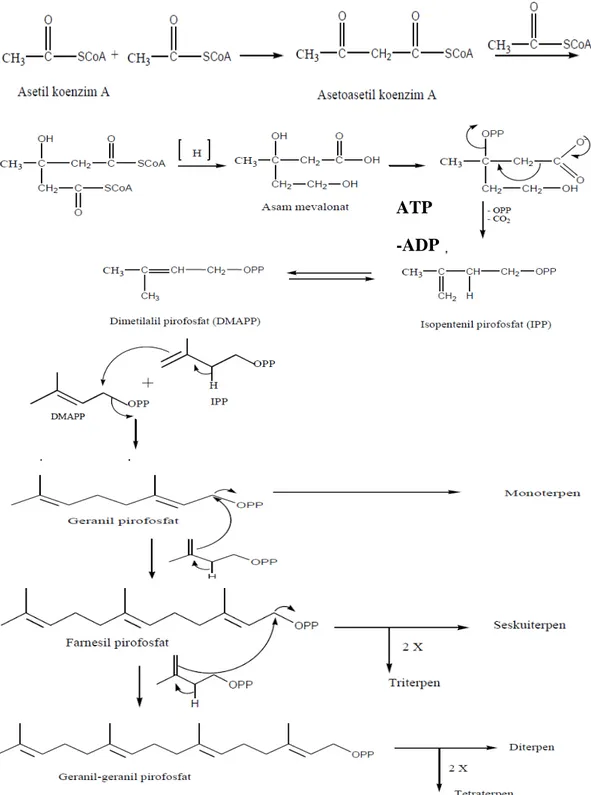
Senyawa-senyawa diterpen diturunkan dari geranil-geranil pirofosfat (GGPP) yang berasal dari kondensasi antara satu unit IPP dan FPP dengan mekanisme yang sama. Sintesa terpenoid sangat sederhana sifatnya. Ditinjau dari segi teori reaksi organik sintesa ini hanya menggunakan beberapa jenis reaksi dasar. Reaksi-reaksi selanjutnya dari senyawa antara GPP, FPP, GGPP untuk menghasilkan senyawa-senyawa terpenoid satu persatu hanya melibatkan beberapa jenis reaksi sekunder. Reaksi-reaksi sekunder ini lazimnya adalah hidrolisa, siklisasi, oksidasi, reduksi, dan reaksi-reaksi spontan yang dapat berlangsung dengan mudah dalam suasana netral dan pada suhu kamar, seperti isomerasi, dehidrasi, dekarboksilasi, dan sebagainya. Berikut ini adalah gambar biosintesa terpenoid sapat dilihat pada gambar dibawah ini
Gambar 2.2 Biosintesa Terpenoid (Achmad, 1985).
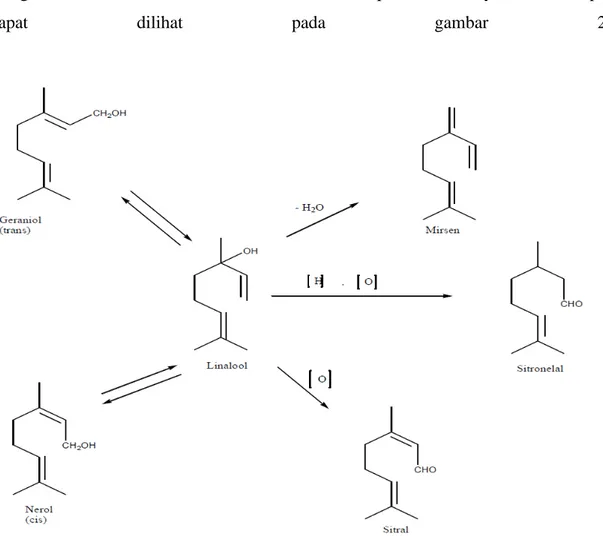
Untuk menjelaskan dapat diambil beberapa contoh monoterpen. Dari segi biogenetik, perubahan geraniol, nerol dan linalool dari yang satu menjadi yang lain berlangsung sebagai akibat reaksi isomerisasi. Ketiga alkohol ini, yang berasal dari hidrolisa geranil pirofosfat (GPP) dapat menjalani reaksi-reaksi sekunder berikut, misalnya dehidrasi menghasilkan mirsena, oksidasi menjadi sitral dan oksidasi reduksi
ATP -ADP
menghasilkan sitronelal. Berikut ini adalah contoh perubahan senyawa monoterpen, dapat dilihat pada gambar 2.3
Gambar 2.3 Perubahan Senyawa Monoterpen (Achmad, 1985)
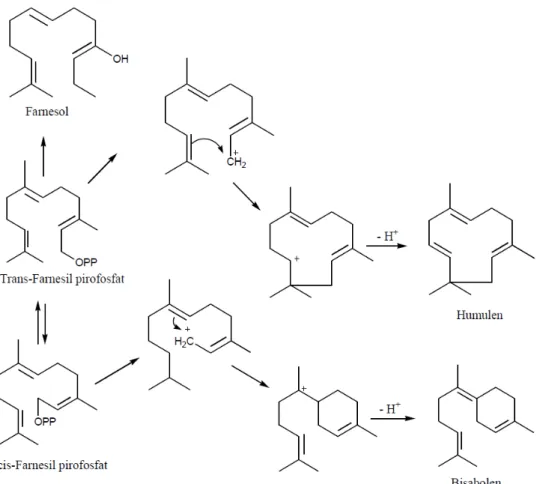
Senyawa- senyawa seskuiterpen diturunkan dari cis-farnesil pirofosfat dan trans- farnesil pirofosfat melalui reaksi siklisasi dan reaksi sekunder lainnya. Kedua isomer farnesil pirofosfat ini dihasilkan in vivo melalui mekanisme yang sama seperti isomerisasi antara geraniol dan nerol. Perubahan farnesil pirofosfat menjadi seskuiterpen terlihat pada gambar 2.4
Gambar 2.4. Reaksi Biogenetik Beberapa Seskuiterpena (Achmad, 1985)
2.3.3. Sumber Minyak Atsiri
Minyak atsiri merupakan salah satu akhir proses metabolisme sekunder dalam tanaman tumbuhan. Tumbuhan penghasil minyak atsiri antara lain termasuk family Pinaceae, Labiatae, Compositae, Lauraceae, Myrtaceae, Rutaceae, Piperaceae, Zingiberaceae, Umbelliferae, dan Gramineae. Minyak atsiri terdapat pada setiap bagian tumbuhan yaitu di daun, bunga, batang, kulit, akar, dan rimpang (Ketaren, 1985).
2.4. Isolasi Minyak Atsiri Dengan Destilasi
Dalam tanaman minyak atsiri, biasanya proses difusi berlangsung sangat lambat, maka untuk mempercepat proses difusi sebelum melakukan penyulingan terlebih dahulu bahan tanaman harus diperkecil dengan cara dipotong - potong atau digerus. Peristiwa terpenting yang terjadi dalam proses penyulingan dengan metode hidrodestilasi ini adalah terjadinya difusi minyak atsiri dan air panas melalui membran bahan yang disuling, terjadinya hidrolisa terhadap beberapa komponen minyak atsiri dan terjadinya dekomposisi yang disebabkan oleh panas (Guenther, 1987). Penyulingan suatu campuran yang berwujud cairan yang tidak saling bercampur, hingga membentuk dua fase atau dua lapisan. Keadaan ini terjadi pada pemisahaan minyak atsiri dengan uap air. Penyulingan dengan uap air sering disebut steam destilasi. Pengertian umum ini memberikan gambaran bahwa penyulingan dapat dilakukan dengan cara mendidihkan bahan tanaman atau minyak atsiri dengan air (Sastrohamidjojo, 2004).
Beberapa jenis tanaman sumber minyak atsiri perlu dirajang terlebih dahulu sebelum disuling. Hal ini untuk memudahkan proses penguapan minyak yang terdapat didalamnya karena perajangan ini menyebabkan kelenjar minyak dapat selebar mungkin (Lutony, 1994).
Dalam industri minyak atsiri dikenal 3 macam metode penyulingan, yaitu: 1. Penyulingan air (Hidrodestilasi)
Pada metode ini bahan yang akan disuling berhubungan langsung dengan air mendidih. Bahan yang akan disuling kemungkinan mengapung diatas air atau terendam seluruhnya (Sastrohamidjojo, 2004).
2. Penyulingan uap (Steam destilasi)
Penyulingan uap disebut juga penyulingan tak langsung. Didalam proses penyulingan dengan uap ini, uap dialirkan melalui pipa uap berlingkar yang berpori dan berada dibawah bahan tanaman yang akan disuling. Kemudian uap akan bergerak menuju ke bagian atas melalui bahan yang disimpan di atas saringan (Lutony, 1994).
3. Penyulingan dengan air dan uap (Water and Steam distillation)
Bahan tanaman yang akan diproses secara penyulingan uap dan air ditempatkan dalam suatu tempat yang bagian bawah dan tengah berlobang-lobang yang ditopang diatas dasar alat penyulingan. Ciri khas model ini yaitu uap selalu
dalam keadaan basah, jenuh, dan tidak terlalu panas. Bahan tanaman yang akan disuling hanya berhubungan dengan uap dan tidak dengan air panas (Lutony, 1994).
2.5. Analisis Komponen Kimia Minyak Atsiri dengan GC-MS
Minyak atsiri yang memiliki komponen tunggal dengan porsi yang sangat besar, kebanyakan mengandung campuran senyawa dengan berbagai tipe. Karena itu analisis dan karakterisasi komponen minyak atsiri merupakan masalah yang cukup rumit, ditambah dengan sifatnya yang mudah menguap pada suhu kamar. Jadi, untuk menganalisa minyak atsiri perlu diseleksi metode yang akan diterapkan. Sejak ditemukan kromatografi gas (GC), kendala dalam analisis komponen minyak atsiri ini mulai dapat diatasi. Pada penggunaan GC efek penguapan dapat dihindari bahkan dihilangkan sama sekali. Perkembangan teknologi instrumentasi yang sangat pesat akhirnya dapat menghasilkan suatu alat yang merupakan gabungan dua sistem dengan prinsip dasar yang berbeda satu sama lain tetapi dapat saling menguntungkan atau saling melengkapi, yaitu gabungan antara kromatografi gas dan spektrometri massa (GC-MS). Kromatografi gas berfungsi sebagai alat pemisah berbagai komponen campuran dalam sampel, sedangkan spektrometrimassa berfungsi untuk mendeteksi masing-masing molekul komponen yang telah dipisahkan pada sistem kromatografi gas (Agusta, 2000).
2.5.1. Analisis Kromatograf Gas
Kromatografi gas digunakan untuk memisahkan komponen campuran kimia dalam suatu bahan berdasarkan perbedaan polaritas campuran. Fase gerak akan membawa campuran sampel menuju kolom. Campuran dalam fase gerak akan berinteraksi dengan kecepatan yang berbeda dimana interaksi komponen dengan fase diam dengan waktu yang paling akhir (Eaton, 1989). Pemisahan tercapai dengan partisi sampel antara fase gas bergerak dan fase diam berupa cairan dengan titik didih tinggi (tidak mudah menguap) yang terikat pada zat padat penunjangnya (Khopkar, 2003).
Gambar 2.5. Skema alat Kromatografi Gas
2.5.1.1. Gas Pembawa
Pemilihan gas pembawa sampai taraf tertentu bergantung pada detektor yang dipakai: hantar hambang, ionisasi nyala, tangkap elektron, atau khas terhadap unsur. Nitrogen, Helium, Argon, Hidrogen, dan Karbon dioksida adalah gas yang paling sering dipakai sebagai gas pembawa karena mereka tidak reaktif serta dapat dibeli dalam keadaan murni dan kering dalam kemasan tangki bervolume besar dan bertekanan tinggi. Hal yang menentukan ialah bahwa kita harus memakai gas paling murni (Gritter, 1991). 2.5.1.2. Sistem Injeksi
Lubang injeksi didesain untuk memasukkan sampel secara cepat dan efesien. Pada dasarnya, ada 4 jenis injektor pada kromatografi gas, yaitu :
1. Injeksi langsung (direct injection), yang mana sampel yang diinjeksikan akan diuapkan dalam injektor yang panas dan 100% masuk menuju kolom.
2. Injeksi terpecah (split injection), yang mana sampel yang diinjeksikan diuapkan dalam injektor yang panas dan selanjutnya dilakukan pemecahan.
3. Injeksi tanpa pemecahan (splitness injection), yang mana hampir semua sampel diuapkan dalam injektor yang panas dan dibawa ke dalam kolom karena katup pemecah ditutup.
4. Injeksi langsung ke kolom (on coloum injection), yang mana ujung semprit dimasukkan langsung ke dalam kolom. Teknik injeksi langsung ke dalam kolom
digunakan untuk senyawa-senyawa yang mudah menguap, karena kalau penyuntikkannya melalui lubang suntik, dikwatirkan akan terjadi peruraian senyawa tersebut karena suhu yang tinggi (Rohman, 2009).
2.5.1.3. Kolom
Kolom merupakan tempat terjadinya proses pemisahaan karena didalamnya terdapat fase diam. Oleh karena itu, kolom merupakan komponen sentral pada kromatografi gas (Rohman, 2009).
2.5.1.4. Fase Diam
Fase diam dibedakan berdasarkan kepolarannya, yaitu nonpolar, semi polar dan polar. Berdasarkan minyak atsiri yang nonpolar sampai sedikit polar, maka untuk keperluan analisis sebaiknya digunakan kolom fase diam yang bersifat nonpolar (Agusta, 2000).
2.5.1.5. Suhu
Suhu merupakan salah satu faktor utama yang menentukan hasil analisis Kromatografi Gas dan Spektrometri Massa. Umumnya yang sangat menentukan adalah pengaturan suhu injektor dan kolom (Agusta, 2000).
2.5.1.6. Detektor
Detektor pada kromatografi gas adalah suatu sensor elektronik yang berfungsi mengubah sinyal gas pembawa komponen-komponen di dalamnya menjadi sinyal elektronik. Sinyal elektronik detektor akan sangat berguna untuk analisis kualitatif maupun kuantitatif terhadap komponen-komponen yang terpisah di antara fase diam dan fase gerak (Rohman, 2009).
2.5.2. Analisis Spektroskopi Massa
Spektrometer massa adalah suatu alat berfungsi untuk mendeteksi masing-masing molekul komponen yang telah dipisahkan pada sistem kromatografi gas yang terdiri dari sistem analisis dan sistem ionisasi dan sistem molekul. Prinsip spektrometri massa (MS) ialah senyawa organik (sampel) ditembak dengan berkas elektron dan menghasilkan ion bermuatan positif yang mempunyai energi yang tinggi karena
lepasnya elektron dari molekul yang dapat pecah menjadi ion positif yang lebih kecil (ion fragmen). Spektrum massa merupakan grafik antara limpahan relatif lawan perbandingan massa/muatan (m/z). Terpisah fragmen ion positif didasarkan pada massanya. Kejadian tersederhana adalah tercampaknya satu elektron dari molekul dalam fasa gas oleh sebuah elektron dalam berkas elektron dan membentuk suatu kation radikal (M•+ )
M • + e → M•+ + 2e
Satu proses yang disebabkan oleh tabrakan elektron pada kamar pengion spektrometer massa adalah ionisasi dari molekul yang berupa uap dengan kehilangan satu elektron dan terbentuk ion molekul bermuatan positif, karena molekul senyawa organik mempunyai elektron berjumlah genap maka proses pelepasan satu elektron menghasilkan ion radikal yang mengandung satu elektron tidak berpasangan.
M M•+
Proses lain molekul yang berupa uap tersebut menangkap sebuah elektron membentuk ion radikal bermuatan negatif dengan kemudian terjadi jauh lebih kecil (10-2) dari pada ion radikal bermuatan positif (Sudjadi, 1983)
Gambar 2.6 Skema alat Spektroskopi Massa
Pada sistem GC-MS ini, yang berfungsi sebagai detektor adalah spektrometer massa itu sendiri yang terdiri dari sistem analisis dan sistem ionisasi, dimana Electron Impact ionization (EI) adalah metode ionisasi yang umum digunakan (Agusta, 2000).
Spektrometer massa pada umumnya digunakan untuk : 1. Menentukan massa suatu molekul
2. Menentukan rumus molekul dengan menggunakan spektrum massa beresolusi tinggi (High Resolution Mass Spectra)
2.6. Ekstraksi
Ekstraksi merupakan salah satu cara pemisahan yang paling banyak digunakan untuk menarik atau memisahkan komponen bioaktif dari suatu bahan baku. Ekstraksi dapat diartikan sebagai suatu proses penarikan komponen yang diinginkan dari suatu bahan dengan menggunakan pelarut yang dipilih sehingga komponen yang diinginkan dapat larut (Ansel, 1989). Menurut Winarno et al 1973, ekstraksi adalah suatu cara untuk memisahkan campuran dari beberapa zat menjadi komponen-komponen yang terpisah. Proses ekstraksi bertujuan untuk mendapatkan bagia-bagian tertentu dari suatu bahan yang mengandung bahan aktif.
Selama proses ekstraksi terdapat gaya yang bekerja akibat adanya perbedaan konsentrasi antara larutan di dalam sel dengan cairan ekstraksi di luar sel. Bahan pelarut yang mengalir ke dalam ruang sel akan menyebabkan protoplasma membengkak dan bahan yang terkandung di dalam sel akan terlarut sesuai dengan kelarutannya (Voight, 1994).
Menurut Ansel (1989) dan Winarno et al (1973), ekstraksi dapat dilakukan dengan dua cara yaitu :
1. Aqueus phase yaitu dilakukan dengan menggunakan air
2. Organic phase dilakukan dengan menggunakan pelarut organik
Berdasarkan prinsipnya, proses ekstraksi dapat berlangsung bila terdapat kesamaan dalam sifa kepolaran antara senyawa yang diekstraksi dengan senyawa pelarut. Suatu zat memiliki kemampuan terlarut yang berbeda dalam pelarut yang berbeda. Hal ini menunjukkan adanya interaksi antara zat terlarut dengan pelarut. Senyawa polar akan larut dalam pelarut polar, begitu juga sebaliknya. Sifat penting yang harus diperhatikan dalam pemilihan pelarut adalah kepolaran senyawa yang dilihat dari gugus polarnya (seperti gugus OH, COOH dan sebagainya). Hal ini yang perlu diperhatikan dalam pemilihan pelarut adalah selektivitas, kemampuan untuk mengekstrak, toksisitas, kemudahan untuk diuapkan, dan harga ( Harbone, 1987).
Metode ekstraksi dengan menggunakan pelarut dapat dilakukan dengan beberapa cara yaitu :
A. Cara Dingin 1. Maserasi
Maserasi berasal dari kata “macerace” yang artinya melunakkan. Maserat adalah hasil penarikan simplisia dengan cara meserasi, sedangkan maserasi adalah cara penarikan simplisia dengan merendam simplisia tersebut dalam cairan dengan beberapa kali pengocokan atau pengadukan pada temperature kamar, sedangkan remaserasi merupakan pengulangan penbambahan pelarut setelah dilakukan penyaringan maserat pertama, dan seterusnya (Depkes, 2000). Keuntungan dari metode maserasi adalah prosedur dan peralatannya sederhana, sedangkan kerugiannya adalah pelarut yang digunakan lebih banyak (Agoes, 2007).
2. Perkolasi
Perkolasi adalah proses penyarian simplisia dengan pelarut yang selalu baru sampai terjadi penyarian sempurna yang umumnya dilakukan pada temperatur kamar. Proses perkolasi terdiri dari tahap pelembaman bahan, tahap perendaman antara, tahap perkolasi sebenarnya (penetasan/penampungan ekstrak) terus-menerus sampai diperoleh perkolat yang jumlahnya 1-5 kali bahan (Harbone, 1987).
B. Cara Panas 1. Sokletasi
Sokletasi adalah ekstrak continue menggunakan alat soklet, dimana pelarut akan terdestilasi dari labu menuju pendinginan, kemudian jatuh membasahi dan merendam sampel yang mengisi bagian tengah alat soklet, setelah pelarut mencapai tinggi tertentu maka akan turun ke labu destilasi, demikian berulang-ulang (Depkes, 2000).
2. Refluks
Refluks adalah ekstraksi dengan pelarut pada temperatur titik didihnya selama waktu tertentu dan pelarut akan terdestilasi menuju pendingin dan akan kembali kelabu (Depkes, 2000).
3. Infudasi
Infudasi adalah ekstraksi dengan pelarut air pada temperature penangas air (bejana infus tercelup dalam penangas air mendidih, temperature terukur 96-980C) selama waktu tertentu 15-20 menit (Depkes, 2000).
4. Dekoktasi
Dekoktasi adalah infus pada waktu yang lebih lama (30 menit) dan temperatur sampai titik didih air (Depkes , 2000).
2.7. Lalat Buah (Bactrocela Carambolae)
Bactrocera carambolae merupakan spesies lalat buah yang paling melimpah. Lalat buah ini selalu ada dan melimpah karena keberadaan tanaman inangnya. Selain menyerang jambu biji, lalat buah ini menyerang berbagai macam buah-buahan antara lain belimbing, kluwih, cabai, nangka, jambu bol, tomat, mangga, papaya (Siwi et al. 2006). Klasifikasi dari lalat buah (Bactrocela carambolae)
Kingdom : Animalia Phylum : Arthropoda Kelas : Insecta Ordo : Diptera Famili : Tephritidae Genus : Batrocera
Spesies : Batrocera carambolae
Gambar 2.6 Foto lalat buah Gambar 2.7 Foto Daur Hidup Lalat Buah 2.7.1. Morfologi Lalat Buah
Lalat buah yang dewasa ukurannya sedang, warnanya kuning, sayapnya datar. Pada tepi ujung sayap ada bercak-bercak cokelat kekuningan. Pada abdomennya ada pita-pita hitam. Dengan ovipositorinya, lalat ini menusuk kulit buah (Pracaya, 1991).
2.7.2. Daur Hidup Lalat Buah
Dengan ovipositorinya, lalat ini menusuk kulit buah. Telurnya diletakkan di bawah kulit buah. Jumlah telurnya kurang lebih 100-120 butir. Pada temperatur 25-350C dalam waktu lebih kurang 2-3 hari telur menetas, belatungnya makan selama lebih kurang satu minggu kemudian keluar dari buah. Belatung yang telah dewasa
mempunyai kebiasaan melenting dan bias melompat sampai jarak ± 30 cm. Belatung masuk kedalam tanah sedalam ± 1-5 cm lalu membuat puparium. Setelah menjadi pupa ± 10 hari menjadi lalat. Setelah berumur ± 5-7 hari lalat betina mulai bertelur. Daur hidup dari telur sampai dewasa 23 sampai 34 hari, tergantung pada keadaan udara. Satu tahun kira-kira ada 8 sampai 10 generasi (Pracaya, 1991).