KESESUAIAN PERHITUNGAN NILAI RATA-RATA ERITROSIT FLOW CYTOMETER DENGAN GAMBARAN POPULASI ERITROSIT PADA
PEMERIKSAAN SEDIAAN APUS DARAH TEPI
Vivin Maria, 2006, Pembimbing I : Penny Setyawati M, dr., Sp.PK., M.Kes. Pembimbing II : Lisawati Sadeli, dr.
Nilai rata-rata eritrosit adalah parameter hematologi yang dipakai untuk menentukan ukuran dan kandungan hemoglobin eritrosit. Nilai rata-rata eritrosit terdiri dari Volume Eritrosit Rata-rata (VER), Konsentrasi Hemoglobin Rata-rata (KHR) dan Konsentrasi Hemoglobin Eritrosit Rata-rata (KHER). Seiring penggunaan cell counter atau alat penghitung sel otomatik yang luas, nilai rata eritrosit secara rutin dianalisis pada setiap sampel yang diperiksa. Nilai rata-rata eritrosit umum digunakan sebagai sarana diagnosis dan klasifikasi anemia. Pemeriksaan Sediaan Apus Darah Tepi (SADT) adalah pemeriksaan hematologi yang penting untuk evaluasi penyakit hematologi termasuk anemia. Tujuan penelitian ini adalah membandingkan hasil perhitungan nilai rata-rata eritrosit metode flow cytometri dengan gambaran populasi eritrosit pada SADT.
Penelitian ini merupakan uji diagnostik. Subjek penelitian ini adalah 100 pasien Rumah Sakit Immanuel Bandung yang diperiksa darahnya menggunakan alat penghitung sel otomatik dengan metode flow cytometri dan dibuat SADT. Bahan pemeriksaan adalah darah vena pasien Rumah Sakit Immanuel Bandung yang telah dicampur antikoagulan EDTA dan diperiksa menggunakan flow
cytometer.
Hasil penelitian ini secara statistik tidak ada perbedaan bermakna antara nilai rata-rata eritrosit dengan gambaran morfologi eritrosit pada SADT, dengan nilai p=0,143 (p<0,05) untuk ukuran eritrosit dan p=0,059 (p<0,05) untuk kromasi eritrosit. Secara klinis terdapat perbedaan bermakna antara nilai rata-rata eritrosit dengan morfologi eritrosit pada SADT, ditemukan 16% perbedaan pada ukuran eritrosit dan 25% perbedaan pada kromasi eritrosit.
Kesimpulan: penghitungan nilai rata-rata eritrosit flow cytometer tidak sepenuhnya sesuai dengan gambaran populasi eritrosit pada SADT.
Significancy of Red Blood Cell Indices with the Morphology of Red Blood Cells Population in Blood Smear
Vivin Maria, 2006, Tutor I : Penny Setyawati M, dr., Sp.PK., M.Kes. Tutor II : Lisawati Sadeli, dr.
The red blood cell indices are used to define the size and hemoglobin content of the red blood cells. They consist of the Mean Corpuscular Volume (MCV), Mean Corpuscular Hemoglobin (MCH) and Mean Corpuscular Hemoglobin Concentration (MCHC). With the widespread use of automated cell counters that routinely determine the red blood cell indices on each blood sample tested, the red blood cells indices are commonly used as an aid in diagnosing and differentiating anemias. A blood smear is an important part of the evaluation of hematologic diseases, includes anemia. The aim of this study is to know the significancy correlation between red blood cell indices and red blood cells population in blood smear.
This is a diagnostic test study. The blood sample of a hundred patients were analyzed by automated cell counter with flow cytometer and made the blood smear with Romanowsky staining. The sample was blood from Immanuel Hospital Bandung patients that have been added with EDTA anticoagulant. The red blood cell indices was compared with the population of red blood cells in the blood smear.
The result of this study: statistically there was no difference between red cell indices with red blood cell morphology in blood smear with p-value 0,143 (p<0,05) for red cell’s size and 0,059(p<0,05) for red cell chromation. Clinically there were differences between red cell indices with red blood cell morphology in blood smear, 16% in sizes and 25% in red cell chromation.
The conclusion of this study : the red blood cells indices that been examined with flow cytometer was not absolutely significant with the morphology of red blood cells population in blood smear.
Halaman
LEMBAR PERSETUJUAN ... ii
SURAT PERNYATAAN ... iii
ABSTRAK... iv
ABSTRACT... v
KATA PENGANTAR... vi
DAFTAR ISI ... viii
DAFTAR TABEL ... xi
DAFTAR GAMBAR... xii
DAFTAR LAMPIRAN ... xiii
BAB I PENDAHULUAN 1.1Latar Belakang... 1
1.2Identifikasi Masalah ... 3
1.3Maksud dan Tujuan Penelitian ... 3
1.3.1 Maksud ... 3
1.3.2 Tujuan... 4
1.4Manfaat Penelitian ... 4
1.5Kerangka Pemikiran... 4
1.6Metode Penelitian ... 5
1.7Lokasi dan Waktu ... 5
1.7.1 Lokasi ... 5
1.7.2 Waktu ... 5
BAB II TINJAUAN PUSTAKA 2.1 Eritrosit... 6
2.1.1 Morfologi Eritrosit ... 6
2.1.2 Eritropoesis ... 6
2.2.2 Etiologi Anemia ... 9
2.2.3 Klasifikasi Anemia ... 9
2.2.3.1 Anemia Hipokromik Mikrositik ... 10
2.2.3.2 Anemia Makrositik ... 11
2.2.3.3 Anemia Normositik... 13
2.2.4 Diagnosis Anemia ... 14
2.3 Pemeriksaan Hematologi Rutin ... 15
2.3.1 Hemoglobin... 15
2.3.2 Hematokrit ... 15
2.3.3 Hitung Jumlah Eritrosit, Leukosit, Trombosit ... 16
2.3.4 Mean Corpuscular Volume (MCV)... 17
2.3.5 Mean Corpuscular Hemoglobin (MCH) ... 17
2.3.6 Mean Corpuscular Hemoglobin Concentration (MCHC)... 18
2.4 Pemeriksaan Sediaan Apus Darah Tepi (SADT)... 19
2.4.1 Tujuan Pembuatan SADT... 19
2.4.2 Teknik Pembuatan SADT... 19
2.4.3 Pewarnaan SADT ... 21
2.4.4 Nilai Rujukan Normal ... 21
2.5 Flow Cytometri ... 23
2.5.1 Sejarah Perkembangan Flow Cytometer... 23
2.5.2 Prinsip Kerja Flow Cytometer ... 24
2.5.2.1 Prinsip Impedansi Listrik (electrical impedance) ... 24
2.5.2.1 Prinsip Pendar Cahaya (light scattering) ... 25
2.5.3 Sysmex XS – 1000i/ XS – 800i ... 26
2.5.3.1 Prinsip Kerja Sysmex XS – 1000i / XS – 800i... 26
2.5.3.2 Spesifikasi Sysmex XS – 1000i / XS – 800i ... 29
3.2 Batasan Operasional... 31
3.3 Ukuran Sampel ... 32
3.4 Cara Pengumpulan Subjek Penelitian ... 33
3.5 Baku Emas... 33
3.6 Alur Penelitian ... 34
3.7 Bahan Pemeriksaan, Reagen dan Alat-Alat ... 34
3.7.1 Pemeriksaan Flow Cytometer ... 35
3.7.2 Pembuatan SADT ... 35
3.8 Prosedur Penggunaan Flow Cytometer (Sysmex XS)... 36
3.9 Prosedur Pembuatan SADT dengan Pewarnaan Giemsa ... 38
3.9.1 Prosedur Pembuatan SADT ... 38
3.9.2 Pewarnaan Giemsa ... 40
3.10 Hipotesis ... 40
3.11 Analisis Data... 41
3.12 Lokasi dan Waktu Penelitian ... 41
3.12.1 Lokasi Penelitian ... 41
3.12.2 Waktu Penelitian ... 42
BAB IV HASIL DAN PEMBAHASAN 4.1 Hasil Penelitian ... 43
4.2 Pembahasan ... 46
BAB V KESIMPULAN DAN SARAN 5.1 Kesimpulan... 48
5.2 Saran... 48
DAFTAR PUSTAKA... 49
LAMPIRAN ... 53
Halaman
Tabel 2.1 Tabel Spesifikasi Sysmex XS – 1000i ... 29
Tabel 2.2 Tabel Spesifikasi Sysmex XS – 800i ... 30
Tabel 4.1 Deskripsi Hasil Pengukuran Variabel Penelitian ... 43
Tabel 4.2 Tabulasi Silang Hasil Pemeriksaan Ukuran Eritrosit Berdasarkan
Flow Cytometer dan Gambaran SADT... 44
Tabel 4.3.Tabulasi Silang Hasil Pemeriksaan Berdasarkan Flow Cytometer dan
Halaman
Gambar 2.1 Eritrosit Matur ... 6
Gambar 2.2 Kurva Afinitas Hb terhadap O2... 8
Gambar 2.3 Gambaran SADT pada Anemia Defisiensi Fe ... 11
Gambar 2.4 Gambaran SADT pada Anemia Megaloblastik... 13
Gambar 2.5 Gambaran SADT Normokromik Normositik... 14
Gambar 2.6 Teknik Pembuatan SADT ... 20
Gambar 2.7 SADT yang Baik (good) & yang Buruk (bad) ... 21
Gambar 2.8 Gambaran SADT Eritrosit Matur ... 22
Gambar 2.9 Prinsip Impedansi Listrik ... 25
Gambar 2.10 Prinsip Pendar Cahaya ... 26
Gambar 2.11 Hydro Dinamic Focusing... 27
Halaman
Lampiran 1 Hasil Penelitian Perbandingan Ukuran Eritrosit... 53
Lampiran 2 Hasil Penelitian Perbandingan Kromasi Eritrosit ... 56
Lampiran 3 Tabel Hasil Tabulasi Silang Dua Jenis Pemeriksaan... 59
Lampiran 4 Tabel 3 x 3 untuk Nilai Proporsi... 61
Lampiran 5 Tabel Tabulasi Silang Proporsi Hasil Pemeriksaan Ukuran Eritrosit Berdasarkan Flow Cytometer dan Gambaran SADT... 63
Lampiran 6 Perhitungan nilai θ1, θ2 Hasil Pemeriksaan Ukuran Eritrosit Berdasarkan Flow Cytometer dan Gambaran SADT... 64
Lampiran 7 Perhitungan Koefisien Kesesuaian Hasil Pemeriksaan Ukuran Eritrosit Berdasarkan Flow Cytometer dan Gambaran SADT ... 65
Lampiran 8 Perhitungan Standar Error Hasil Pemeriksaan Ukuran Eritrosit Berdasarkan Flow Cytometer dan Gambaran SADT... 66
Lampiran 9 Perhitungan Nilai Z Hasil Pemeriksaan Ukuran Eritrosit Berdasarkan Flow Cytometer dan Gambaran SADT... 67
Lampiran 10 Tabel Interpretasi Hasil Perhitungan Koefisien Kappa... 68
Lampiran 11 Tabel Tabulasi Silang Proporsi Hasil Pemeriksaan Kromasi Eritrosit Berdasarkan Flow Cytometer dan Gambaran SADT ... 69
Lampiran 12 Perhitungan nilai θ1, θ2, Hasil Pemeriksaan Kromasi Eritrosit Berdasarkan Flow Cytometer dan Gambaran SADT... 70
Lampiran 13 Perhitungan Koefisien Kesesuaian Hasil Pemeriksaan Kromasi Eritrosit Berdasarkan Flow Cytometer dan Gambaran SADT ... 71
Lampiran 14 Perhitungan Standar Error Hasil Pemeriksaan Kromasi Eritrosit Berdasarkan Flow Cytometer dan Gambaran SADT... 72
Lampiran 15 Perhitungan Nilai Z Hasil Pemeriksaan Kromasi Eritrosit Berdasarkan Flow Cytometer dan Gambaran SADT... 73
Lampiran 1
Hasil Penelitian Perbandingan Ukuran Eritrosit Hasil Perhitungan Flow Cytometer dan
Gambaran SADT
Nama RBC HGB HCT MCV MCH MCHC interpretasi SADT 1 4.99 14.6 43.4
87 29.3 33.6 normositik normositik 2 4.36 12.3 37.7 86.5 28.2 32.6 normositik normositik 3 5.13 14.7 43.7 85.2 28.7 33.6 normositik normositik 4 4.83 12.8 40.1
83 26.5 31.9 normositik normositik 5 4.95 14.1 42.4 85.7 28.5 33.3 normositik normositik 6 5.37 15.9 47.2 87.9 29.6 33.7 normositik normositik 7 5.28 6.5 20.4 89.5 28.5 31.9 normositik normositik 8 3.99 12.6 39.4 98.7 31.6 32.0 normositik normositik 9 4.69 13.6 41.4 88.3 29.0 32.9 normositik normositik 10 4.94 13.2 37.7 76.3 26.7 35.0 mikrositik normositik 11 5.21 13.7 41.2 79.1 26.3 33.3 mikrositik normositik 12 5.32 14.2 44.9 84.4 26.7 31.6 normositik normositik 13 4.86 15.0 42.4 87.2 30.9 35.4 normositik normositik 14 3.82 11.5 34.2 89.5 30.1 33.6 normositik normositik 15 4.74 8.9 28.1 59.3 18.8 31.7 mikrositik normositik 16 5.18 15.4 45.7 88.2 29.7 33.7 normositik normositik 17 5.19 16.1 46.9 90.4 31.0 34.3 normositik normositik 18 3.99 12.2 35.6 89.2 30.6 34.3 normositik normositik 19 3.06 9.3 26.1 85.3 30.4 35.6 normositik normositik 20 5.38 12.9 38.3 71.2 24.0 33.7 mikrositik normositik 21 3.91 10.9 33.3 85.2 27.9 32.7 normositik normositik 22 3.67 11.6 32.3
88 31.6 35.9 normositik normositik 23 4.23 12.4 37.1 87.7 29.3 33.4 normositik normositik 24 4.14 12.5 37.4 90.3 30.2 33.4 normositik normositik 25 4.55 12.8 36.5 80.2 28.1 35.1 normositik normositik 26 4.71 12.3 36.8 78.1 26.1 33.4 mikrositik normositik 27 4.79 12.8 37.5 78.3 26.7 34.1 mikrositik normositik 28 4.73 12.1 36.8 77.8 25.6 32.9 mikrositik normositik 29 4.66 13.2 37.8 81.1 28.3 34.9 normositik normositik 30 5.31 15.9 45.4 85.5 29.9 35.0 normositik normositik 31 3.93 11.8 35.2 89.6 30.0 33.5 normositik normositik 32 6.34 13.3 41.3 65.1 21.0 32.2 mikrositik mikrositik 33 3.22 10.8 32.3 100.3 33.5 33.4 makrositik normositik 34 4.85 13.2 40.8 84.1 27.2 32.4 normositik normositik 35 4.43 13.3 38.6 87.1 30.0 34.5 normositik mikrositik 36 2.88 8.1 24.0 83.3 28.1 33.8 normositik normositik 37 4.24 12.9 38.1 89.9 30.4 33.9 normositik normositik 38 3.21 12.4 37.4
113 37.5 33.2 makrositik makrositik 39 5.10 13.4 39.7 77.8 26.3 33.8 mikrositik normositik 40 4.37 12.8 38.8 88.8 29.3 33.0 normositik normositik 41 3.96 11.4 32.9 83.1 28.8 34.7 normositik normositik 42 4.92 14.0 41.3 83.9 28.5 33.9 normositik normositik 43 4.22 12.2 38.0
90 28.9
44 4.01 11.4 36.7
92 28.5 31.2 normositik normositik 45 4.70 12.3 39.7
84 26.2 31.1 normositik normositik 46 4.37 11.0 35.6
81 25.2 31.0 normositik normositik 47 5.24 12.9 41.8
80 24.6 30.8 normositik normositik 48 4.93 12.7 41.7
85 25.8 30.5 normositik mikrositik 49 4.66 13.1 41.6
89 28.1 31.5 normositik normositik 50 5.64 15.9 51.0
90 28.2 31.2 normositik normositik 51 4.55 11.6 36.0
79 24.2 30.6 mikrositik normositik 52 4.05 12.1 38.4
95 29.9 31.5 normositik normositik 53 4.52 12.0 39.1
86 26.6 30.8 normositik normositik 54 3.80 11.6 37.2
98 30.5 31.2 normositik normositik 55 5.18 13.3 42.2
81 25.7 31.5 normositik normositik 56 4.51 12.9 41.3
92 28.6 31.2 normositik normositik 57 4.58 13.1 42.5
93 28.5 30.8 normositik normositik 58 4.00 11.0 35.1
88 27.5 31.4 normositik normositik 59 4.81 14.4 39.7 82.5 29.9 36.3 normositik normositik 60 5.44 14.2 43.2 79.4 26.1 32.9 mikrositik normositik 61 4.21 11.8 34.8 82.7 28.0 33.9 normositik mikrositik 62 5.03 14.5 43.0 85.5 28.8 33.7 normositik normositik 63 4.74 13.7 43.5
92 28.9 31.5 normositik normositik 64 2.98 8.3 26.6
89 27.7 31.1 normositik normositik 65 4.62 14.5 43.2 93.5 31.4 33.6 normositik normositik 66 4.52 14.0 40.2 88.9 31.0 34.8 normositik normositik 67 2.41 7.1 22.9
95 29.5 31.0 normositik mikrositik 68 5.34 14.1 46.0
86 26.5 30.7 normositik normositik 69 5.12 13.8 44.6
87 26.9 30.9 normositik normositik 70 5.07 13.1 43.1
85 6.03 18.2 54.5 90.4 30.2 33.4 normositik normositik 86 4.72 13.5 43.0
91 28.5 31.3 normositik normositik 87 3.98 12.3 38.7
97 31.0 31.9 normositik normositik 88 4.68 13.8 42.4
90 29.4 32.5 normositik normositik 89 4.63 12.9 40.3
87 27.8 32.0 normositik normositik 90 4.77 12.6 39.5
83 26.5 32.0 normositik normositik 91 3.89 11.5 36.5
94 29.6 31.6 normositik normositik 92 5.18 14.2 44.8
87 27.4 31.7 normositik normositik 93 1.98 7.4 22.3
113 37.3 33.2 makrositik makrositik 94 5.26 14.1 44.6
Lampiran 2
Hasil Penelitian Perbandingan Kromasi Eritrosit Hasil Perhitungan Flow Cytometer dan
Gambaran SADT
Nama RBC HGB HCT MCV MCH MCHC interpretasi SADT 1 4.99 14.6 43.4
87 29.3 33.6 normokromik normokromik 2 4.36 12.3 37.7 86.5 28.2 32.6 normokromik normokromik 3 5.13 14.7 43.7 85.2 28.7 33.6 normokromik normokromik 4 4.83 12.8 40.1
83 26.5 31.9 normokromik hipokromik 5 4.95 14.1 42.4 85.7 28.5 33.3 normokromik normokromik 6 5.37 15.9 47.2 87.9 29.6 33.7 normokromik normokromik 7 5.28 6.5 20.4 89.5 28.5 31.9 normokromik hipokromik 8 3.99 12.6 39.4 98.7 31.6 32.0 normokromik normokromik 9 4.69 13.6 41.4 88.3 29.0 32.9 normokromik normokromik 10 4.94 13.2 37.7 76.3 26.7 35.0 normokromik normokromik 11 5.21 13.7 41.2 79.1 26.3 33.3 normokromik normokromik 12 5.32 14.2 44.9 84.4 26.7 31.6 normokromik normokromik 13 4.86 15.0 42.4 87.2 30.9 35.4 normokromik normokromik 14 3.82 11.5 34.2 89.5 30.1 33.6 normokromik hipokromik 15 4.74 8.9 28.1 59.3 18.8 31.7 normokromik hipokromik 16 5.18 15.4 45.7 88.2 29.7 33.7 normokromik normokromik 17 5.19 16.1 46.9 90.4 31.0 34.3 normokromik normokromik 18 3.99 12.2 35.6 89.2 30.6 34.3 normokromik normokromik 19 3.06 9.3 26.1 85.3 30.4 35.6 normokromik normokromik 20 5.38 12.9 38.3 71.2 24.0 33.7 normokromik normokromik 21 3.91 10.9 33.3 85.2 27.9 32.7 normokromik normokromik 22 3.67 11.6 32.3
88 31.6 35.9 normokromik normokromik 23 4.23 12.4 37.1 87.7 29.3 33.4 normokromik normokromik 24 4.14 12.5 37.4 90.3 30.2 33.4 normokromik normokromik 25 4.55 12.8 36.5 80.2 28.1 35.1 normokromik normokromik 26 4.71 12.3 36.8 78.1 26.1 33.4 normokromik normokromik 27 4.79 12.8 37.5 78.3 26.7 34.1 normokromik normokromik 28 4.73 12.1 36.8 77.8 25.6 32.9 normokromik normokromik 29 4.66 13.2 37.8 81.1 28.3 34.9 normokromik normokromik 30 5.31 15.9 45.4 85.5 29.9 35.0 normokromik normokromik 31 3.93 11.8 35.2 89.6 30.0 33.5 normokromik normokromik 32 6.34 13.3 41.3 65.1 21.0 32.2 normokromik hipokromik 33 3.22 10.8 32.3 100.3 33.5 33.4 normokromik normokromik 34 4.85 13.2 40.8 84.1 27.2 32.4 normokromik normokromik 35 4.43 13.3 38.6 87.1 30.0 34.5 normokromik hipokromik 36 2.88 8.1 24.0 83.3 28.1 33.8 normokromik hipokromik 37 4.24 12.9 38.1 89.9 30.4 33.9 normokromik normokromik 38 3.21 12.4 37.4
113 37.5 33.2 normokromik normokromik 39 5.10 13.4 39.7 77.8 26.3 33.8 normokromik normokromik 40 4.37 12.8 38.8 88.8 29.3 33.0 normokromik normokromik 41 3.96 11.4 32.9 83.1 28.8 34.7 normokromik normokromik 42 4.92 14.0 41.3 83.9 28.5 33.9 normokromik normokromik 43 4.22 12.2 38.0
44 4.01 11.4 36.7
92 28.5 31.2 normokromik normokromik 45 4.70 12.3 39.7
84 26.2 31.1 normokromik normokromik 46 4.37 11.0 35.6
81 25.2 31.0 normokromik normokromik 47 5.24 12.9 41.8
80 24.6 30.8 hipokromik normokromik 48 4.93 12.7 41.7
85 25.8 30.5 hipokromik hipokromik 49 4.66 13.1 41.6
89 28.1 31.5 normokromik normokromik 50 5.64 15.9 51.0
90 28.2 31.2 normokromik normokromik 51 4.55 11.6 36.0
79 24.2 30.6 hipokromik normokromik 52 4.05 12.1 38.4
95 29.9 31.5 normokromik normokromik 53 4.52 12.0 39.1
86 26.6 30.8 hipokromik normokromik 54 3.80 11.6 37.2
98 30.5 31.2 normokromik normokromik 55 5.18 13.3 42.2
81 25.7 31.5 normokromik normokromik 56 4.51 12.9 41.3
92 28.6 31.2 normokromik normokromik 57 4.58 13.1 42.5
93 28.5 30.8 hipokromik normokromik 58 4.00 11.0 35.1
88 27.5 31.4 normokromik normokromik 59 4.81 14.4 39.7 82.5 29.9 36.3 hiperkromik normokromik 60 5.44 14.2 43.2 79.4 26.1 32.9 normokromik normokromik 61 4.21 11.8 34.8 82.7 28.0 33.9 normokromik normokromik 62 5.03 14.5 43.0 85.5 28.8 33.7 normokromik normokromik 63 4.74 13.7 43.5
92 28.9 31.5 normokromik normokromik 64 2.98 8.3 26.6
89 27.7 31.1 normokromik hipokromik 65 4.62 14.5 43.2 93.5 31.4 33.6 normokromik normokromik 66 4.52 14.0 40.2 88.9 31.0 34.8 normokromik normokromik 67 2.41 7.1 22.9
95 29.5 31.0 normokromik hipokromik 68 5.34 14.1 46.0
86 26.5 30.7 hipokromik hipokromik 69 5.12 13.8 44.6
87 26.9 30.9 hipokromik normokromik 70 5.07 13.1 43.1
85 6.03 18.2 54.5 90.4 30.2 33.4 normokromik normokromik 86 4.72 13.5 43.0
91 28.5 31.3 normokromik normokromik 87 3.98 12.3 38.7
97 31.0 31.9 normokromik normokromik 88 4.68 13.8 42.4
90 29.4 32.5 normokromik normokromik 89 4.63 12.9 40.3
87 27.8 32.0 normokromik normokromik 90 4.77 12.6 39.5
83 26.5 32.0 normokromik normokromik 91 3.89 11.5 36.5
94 29.6 31.6 normokromik hipokromik 92 5.18 14.2 44.8
87 27.4 31.7 normokromik normokromik 93 1.98 7.4 22.3
113 37.3 33.2 normokromik normokromik 94 5.26 14.1 44.6
Lampiran 3
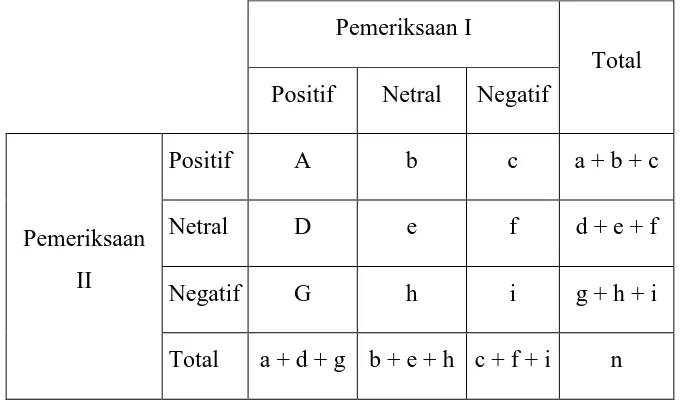
Tabel 1 Tabel Hasil Tabulasi Silang Dua Jenis Pemeriksaan
Pemeriksaan I
Positif
Netral
Negatif
Total
Positif
A
b
c
a + b + c
Netral
D
e
f
d + e + f
Negatif
G
h
i
g + h + i
Pemeriksaan
II
Total
a + d + g b + e + h c + f + i
n
Dengan :
a
:
jumlah subjek yang diidentifikasi positif oleh
pemeriksaan i dan juga diidentifikasi positif oleh
pemeriksaan ii
b
:
jumlah subjek yang diidentifikasi netral oleh
pemeriksaan i tetapi diidentifikasi positif oleh
pemeriksaan ii
c
jumlah subjek yang diidentifikasi negatif oleh
pemeriksaan i tetapi diidentifikasi positif oleh
pemeriksaan ii
d
:
jumlah subjek yang diidentifikasi positif oleh
pemeriksaan i tetapi diidentifikasi netral oleh
pemeriksaan ii
e
:
jumlah subjek yang diidentifikasi netral oleh
pemeriksaan i dan juga diidentifikasi netral oleh
f
:
jumlah subjek yang diidentifikasi negatif oleh
pemeriksaan i tetapi diidentifikasi netral oleh
pemeriksaan ii
g
:
jumlah subjek yang diidentifikasi positif oleh
pemeriksaan i tetapi diidentifikasi negatif oleh
pemeriksaan ii
h
:
jumlah subjek yang diidentifikasi netral oleh
pemeriksaan i tetapi diidentifikasi negatif oleh
pemeriksaan ii
i
:
jumlah subjek yang diidentifikasi negatif oleh
pemeriksaan i dan juga diidentifikasi negatif oleh
pemeriksaan ii
a + d + g
:
jumlah subjek yang diidentifikasi positif oleh
pemeriksaan i
b + e + h
:
jumlah subjek yang diidentifikasi netral oleh
pemeriksaan i
c + f + i
:
jumlah subjek yang diidentifikasi negatifoleh
pemeriksaan i
a + b + c
:
jumlah subjek yang diidentifikasi positif oleh
pemeriksaan ii
d + e + f
:
jumlah subjek yang diidentifikasi netral oleh
pemeriksaan ii
g + h + i
:
jumlah subjek yang diidentifikasi positif oleh
pemeriksaan ii
Lampiran 4
Tabel 2 Tabel 3 x 3 untuk Nilai Proporsi
Pemeriksaan I
Positif
Netral
Negatif
Total
Positif
P
11P
12P
13P
1oNetral
P21
P22
P23
P2o
Negatif
P31
P32
P33
P3o
Pemeriksaan II
Total
Po1
Po2
Po3
Poo
Dengan :
n a P11 =
: proporsi subjek yang diidentifikasi positif oleh
pemeriksaan i dan juga diidentifikasi positif oleh
pemeriksaan ii
n b P12 =
: proporsi subjek yang diidentifikasi netral oleh
pemeriksaan i tetapi diidentifikasi positif oleh
pemeriksaan ii
n c
P11 = : proporsi subjek yang diidentifikasi negatif oleh pemeriksaan i tetapi diidentifikasi positif oleh
pemeriksaan ii
n d
P21 = : proporsi subjek yang diidentifikasi positif oleh pemeriksaan i tetapi diidentifikasi netral oleh
pemeriksaan ii
n e
P22 = : proporsi subjek yang diidentifikasi netral oleh pemeriksaan i dan juga diidentifikasi netral oleh
n d
P23 = : proporsi subjek yang diidentifikasi negatif oleh pemeriksaan i tetapi diidentifikasi netral oleh
pemeriksaan ii
n g
P31 = : proporsi subjek yang diidentifikasi positif oleh pemeriksaan i tetapi diidentifikasi negatif oleh
pemeriksaan ii
n h
P32 = : proporsi subjek yang diidentifikasi netral oleh pemeriksaan i tetapi diidentifikasi negatif oleh
pemeriksaan ii
n i P31 =
: proporsi subjek yang diidentifikasi negatif oleh
pemeriksaan i dan juga diidentifikasi negatif oleh
pemeriksaan ii n g d a Po1 + +
= : proporsi subjek yang diidentifikasi positif oleh pemeriksaan i n h e b Po2 + +
= : proporsi subjek yang diidentifikasi netral oleh pemeriksaan i n i f c
Po3 = + + : proporsi subjek yang diidentifikasi negatifoleh pemeriksaan i n c b a
P1o = + + : proporsi subjek yang diidentifikasi positif oleh pemeriksaan ii n f e d
P2o = + + : proporsi subjek yang diidentifikasi netral oleh pemeriksaan ii n i h g
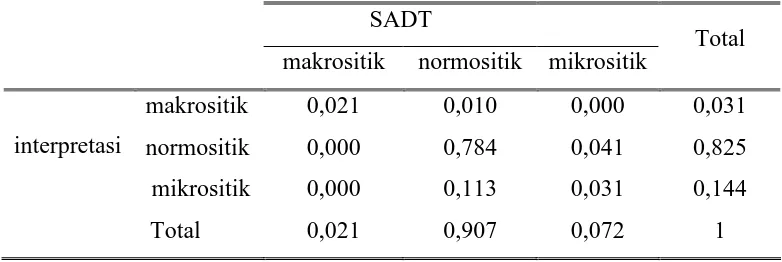
Lampiran 5
Tabel Tabulasi Silang Proporsi Hasil Pemeriksaan Ukuran Eritrosit Berdasarkan
Flow
Cytometer
dan Gambaran SADTSADT
makrositik normositik mikrositik
Total
makrositik 0,021 0,010 0,000 0,031
normositik 0,000 0,784 0,041 0,825 interpretasi
mikrositik 0,000 0,113 0,031 0,144
Lampiran 6
Perhitungan nilai
θ
1,θ
2 Hasil Pemeriksaan Ukuran Eritrosit BerdasarkanFlow Cytometer
dan Gambaran SADT33 22 11 ii
1
P
P
P
P
θ
=
∑
=
+
+
= 0,021 + 0,784 + 0,031 = 0,863
o3 3o o2 2o o1 1o oi i0
2
P
P
P
P
P
P
P
P
θ
=
∑
=
+
+
= (0,031 x 0,021) + (0,825 x 0,907) + (0,144 x 0,072)
= 0,00065 + 0,748275 + 0,020368
Lampiran 7
Perhitungan Koefisien Kesesuaian Hasil Pemeriksaan Ukuran Eritrosit Berdasarkan
Flow Cytometer
dan Gambaran SADT2 2 1
θ
1
θ
θ
κ
ˆ
−
−
=
=
0,759293
1
0,759293
0,863
−
−
Lampiran 8
Perhitungan Standar Error Hasil Pemeriksaan Ukuran Eritrosit Berdasarkan
Flow
Cytometer
dan Gambaran SADT(
i0 oi)
1o o1(
1o o1)
2o o2(
2o o2)
3o o3(
3o o3)
oi
i0P P P P P P P P P P P P P P P
P + = + + + + +
∑
= (0,031 x 0,021)(0,031+0,021)+(0,825 x 0,907)(0,825+0,907) +
(0,144 x 0,072) (0,144+0,072)
= 1,29829
( )
(
)
2(
)
Lampiran 9
Perhitungan Nilai Z Hasil Pemeriksaan Ukuran Eritrosit Berdasarkan
Flow Cytometer
dan Gambaran SADT
( )
0,081716186 0,431κ
ˆSe
κ
ˆLampiran 10
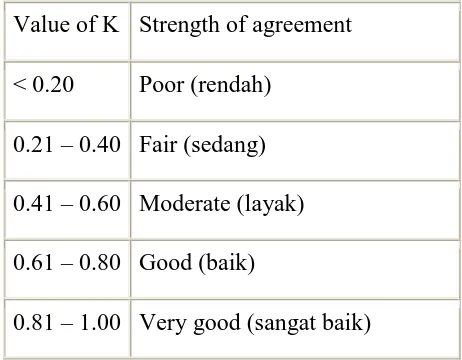
Tabel Interpretasi Hasil Perhitungan Koefisien Kappa (Landis, Koch, 1977)
Value of K Strength of agreement
< 0.20 Poor (rendah)
0.21 – 0.40 Fair (sedang)
0.41 – 0.60 Moderate (layak)
0.61 – 0.80 Good (baik)
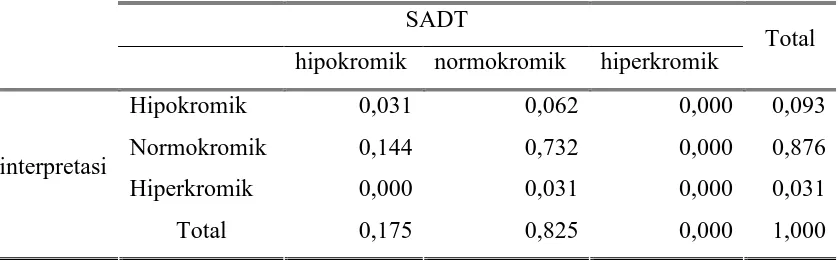
Lampiran 11
Tabel Tabulasi Silang Proporsi Hasil Pemeriksaan Kromasi Eritrosit Berdasarkan
Flow
Cytometer
dan Gambaran SADTSADT
hipokromik normokromik hiperkromik
Total
Hipokromik 0,031 0,062 0,000 0,093
Normokromik 0,144 0,732 0,000 0,876
Hiperkromik 0,000 0,031 0,000 0,031 interpretasi
Lampiran 12
Perhitungan nilai
θ
1,θ
2, Hasil Pemeriksaan Kromasi Eritrosit BerdasarkanFlow
Cytometer
dan Gambaran SADT33 22 11 ii
1
P
P
P
P
θ
=
∑
=
+
+
= 0,031 + 0,732 + 0,000 = 0,763
o3 3o o2 2o o1 1o oi i0
2
P
P
P
P
P
P
P
P
θ
=
∑
=
+
+
= (0,093 x 0,175) + (0,876 x 0,825) + (0,031 x 0,175)
= 0,016275 + 0,72270 + 0,005425
Lampiran 13
Perhitungan Koefisien Kesesuaian Hasil Pemeriksaan Kromasi Eritrosit Berdasarkan
Flow Cytometer
dan Gambaran SADT2 2 1
θ
1
θ
θ
κ
ˆ
−
−
=
=
0,74440
1
0,74440
0,763
−
−
Lampiran 14
Perhitungan Standar Error Hasil Pemeriksaan Kromasi Eritrosit Berdasarkan
Flow
Cytometer
dan Gambaran SADT(
i0 oi)
1o o1(
1o o1)
2o o2(
2o o2)
3o o3(
3o o3)
oi
i0
P
P
P
P
P
P
P
P
P
P
P
P
P
P
P
P
+
=
+
+
+
+
+
∑
=(0,093 x 0,175) (0,093 + 0,175) + (0,876 x 0,825)(0,876+ 0,825) +
(0,031 x 0,175) (0,031 + 0,175)
= 1,23479
( )
(
)
2(
)
2 oi i0 oi i0 2 2 2 1 P P P P
κ
ˆ Seθ
θ
θ
−
+
−
+
=
∑
n
( )
(
)
7932 , 24 06374136 , 0 0,0,74440 1 97 1,23479 0,74440 0,74440κ
ˆ Se 2 2=
−
−
+
Lampiran 15
Perhitungan Nilai Z Hasil Pemeriksaan Kromasi Eritrosit Berdasarkan
Flow Cytometer
dan Gambaran SADT
( )
0,05070425 072 0,κ
ˆSe
κ
ˆLampiran 16
FORMULIR PERNYATAAN PERSETUJUAN KLINIK
(INFORMED CONSENT)
FAKULTAS KEDOKTERAN UNIVERSITAS KRISTEN MARANATHA
SURAT PERNYATAAN PERSETUJUAN KLINIK
Yang bertanda tangan di bawah ini :
Nama : ... Status : ... Usia : ... Alamat : ... Pekerjaan : ... No. KTP/identitas lain : ... No. Urut : ...
Setelah mendapat penjelasan selengkapnya dan menyadari maksud, tujuan dan manfaat penelitian tersebut di bawah ini yang berjudul:
KESESUAIAN PERHITUNGAN NILAI RATA-RATA ERITROSIT FLOW
CYTOMETRI DENGAN GAMBARAN POPULASI ERITROSIT PADA
PEMERIKSAAN SEDIAAN APUS DARAH TEPI
Maka saya/keluarga saya bersedia berperan serta dalam penelitian tersebut di atas sebagai subyek penelitian dan bersedia dilakukan pemeriksaan nilai rata-rata eritrosit dengan flow cytometri dan pemeriksaan sediaan apus darah tepi.
Demikian surat pernyataan ini saya buat dengan penuh kesadaran, penuh tanggung jawab tanpa paksaan pihak manapun.
Bandung, ...2006
Peneliti
(Vivin Maria)
Yang Membuat Pernyataan,
1.1 Latar Belakang
Sel darah merah atau eritrosit merupakan sel yang paling sederhana yang ada
di dalam tubuh. Eritrosit tidak memiliki nukleus dan merupakan sel terbanyak
dalam darah. Eritrosit mengandung hemoglobin, yaitu protein yang mengandung
besi, berperan dalam transpor oksigen dan karbondioksida di dalam tubuh. Oleh
karena itu eritrosit sangat diperlukan dalam proses oksigenasi organ tubuh.
Dengan mengetahui keadaan eritrosit, secara tidak langsung dapat diketahui juga
keadaan organ tubuh seseorang (Brown, 1993; Hoffbrand, Petit; 1996; Gaspard,
1998; Uthman, 2000; Perkins, 2003).
Beberapa pemeriksaan yang dapat menggambarkan parameter penting dari
fungsi dan struktur eritrosit di dalam tubuh antara lain hitung eritrosit, hemoglobin
dan hematokrit. Hitung eritrosit atau red blood cell count (RBC) adalah
menghitung jumlah total eritrosit dalam darah. Nilai rujukan normal eritrosit
adalah 4-5 juta/mm3. Hemoglobin (Hb) adalah protein dalam eritrosit yang
bertugas mengangkut oksigen. Hematokrit (Ht) adalah jumlah eritrosit dalam 100
ml darah (Perkins, 2003). Ketiga parameter di atas biasa digunakan untuk
menegakkan adanya anemia (Glader, 2003).
Anemia secara fungsional didefinisikan sebagai penurunan massa eritrosit
dengan akibat oksigenasi jaringan tidak dapat terpenuhi (Evatt et al, 1992;
Gaspard, 1998; Glader, 2003; Perkins, 2003; Syafrizal Syafei, 2004). Secara
praktis ada 3 parameter untuk menegakkan adanya anemia yaitu: kadar
hemoglobin, hematokrit dan jumlah eritrosit. Dari perhitungan ketiga parameter
tersebut dapat diperoleh nilai rata-rata eritrosit. Nilai rata-rata eritrosit terdiri dari
Mean Corpuscular Volume (MCV), Mean Corpuscular Hemoglobin (MCH) dan Mean Corpuscular Hemoglobin Concentration (MCHC) (Evatt et al, 1992; Desai,
Isa-Pratt, 2000; Davey & Elghetany, 2001; Glader, 2003; Perkins, 2003;
Pemeriksaan laboratorium merupakan pemeriksaan penunjang yang
diperlukan oleh dokter untuk membantu menegakkan diagnosis. Salah satu
pemeriksaan laboratorium yang sering dilakukan adalah pemeriksaan darah.
Darah mempunyai peran penting dalam tubuh manusia. Hasil pemeriksaan darah
secara tidak langsung dapat memantau keadaan dalam tubuh. Pemeriksaan darah
atau pemeriksaan hematologi secara umum dapat dibedakan menjadi dua yaitu
pemeriksaan hematologi rutin dan hematologi lengkap (Brown,1993).
Pemeriksaan hematologi rutin terdiri dari hemoglobin, hematokrit, hitung
jumlah eritrosit, hitung jumlah leukosit, hitung jenis leukosit, hitung jumlah
trombosit dan nilai-nilai rata-rata eritrosit. Pemeriksaan hematologi lengkap
(complete blood count) terdiri dari pemeriksaan darah rutin ditambah pemeriksaan
morfologi sel (ukuran, kandungan hemoglobin, anisositosis, poikilositosis,
polikromasi). Pemeriksaan hematologi lengkap penting untuk mengetahui
morfologi dan fungsi dari berbagai sel yang ada di dalam darah, contohnya sel
darah putih yang berperan dalam imunitas tubuh dan sel darah merah yang
berperan dalam oksigenasi tubuh (Brown, 1993, Perkins 2003;
Adamson, Longo, 2005).
Seiring dengan kemajuan teknologi, alat-alat yang dipakai dalam pemeriksaan
hematologi juga semakin berkembang. Para peneliti mengembangkan alat untuk
menganalisa populasi sel darah secara otomatik. Alat ini dapat digunakan untuk
pemeriksaan hitung eritrosit, hitung leukosit, Hb, Ht, platelet dan nilai-nilai
rata-rata eritrosit. Metode yang banyak dipakai pada alat-alat untuk pemeriksaan
hematologi adalah metode flow cytometri (Kearns & LaMonica, 2001;
Koeswardani dkk., 2001).
Pemeriksaan hematologi dengan metode flow cytometri sekarang sudah
popular dilakukan. Metode flow cytometri memiliki prosedur yang relatif mudah
dan hasilnya dapat diperoleh dalam waktu yang singkat. Namun, menurut Perkins
metode ini mempunyai tingkat false positive yang cukup tinggi, yaitu 10-25%.
Pemeriksaan hematologi lain yang cukup sering dilakukan adalah pembuatan
Sediaan Apus Darah Tepi (SADT). SADT atau blood smear adalah salah satu
lainnya. Pada SADT dapat diketahui morfologi sel-sel darah yaitu ukuran, bentuk,
kesan jumlah, apakah ada sel-sel muda dan sebagainya. SADT dapat digunakan
sebagai kontrol terhadap pemeriksaan hematologi lain seperti nilai rata-rata
eritrosit, Hb, dan lain-lain (Kearns & LaMonica, 2001; Wyrick-Glatzel, Hughes,
2001).
Hasil pemeriksaan nilai rata-rata eritrosit dengan flow cytometer apakah sama
atau tidak dengan gambaran populasi eritrosit pada SADT belum diketahui
dengan pasti. Maka dengan penelitian ini penulis ingin mengetahui sejauh mana
kesesuaian hasil pemeriksaan nilai rata-rata eritrosit dengan flow cytometer
dengan gambaran populasi eritrosit pada SADT. Berbagai jenis anemia juga dapat
diketahui lebih pasti melalui kedua pemeriksaan tersebut.
1.2 Identifikasi Masalah
• Apakah hasil pemeriksaan nilai rata-rata eritrosit dengan flow cytometer sesuai dengan gambaran populasi eritrosit pada SADT?
1.3 Maksud dan Tujuan Penelitian
1.3.1 Maksud Penelitian
Penelitian ini bermaksud ingin mengetahui apakah nilai rata-rata eritrosit hasil
pengukuran flow cytometer sesuai dengan gambaran populasi eritrosit pada
SADT.
1.3.2 Tujuan Penelitian
Penelitian ini bertujuan membandingkan hasil pemeriksaan flow cytometer
dengan gambaran eritrosit pada SADT, yang pada akhirnya dapat diketahui
apakah pemeriksaan nilai rata-rata eritrosit dengan flow cytometer dan gambaran
1.4 Manfaat Penelitian
Penulisan karya tulis ini diharapkan dapan memberikan informasi tentang
apakah ada kesesuaian antara hasil perhitungan nilai rata-rata eritrosit
menggunakan flow cytometer dengan gambaran populasi eritrosit yang sebenarnya
pada SADT. Hal ini dapat membantu para klinisi untuk menegakkan diagnosis
anemia.
1.5 Kerangka Pemikiran
Nilai rata-rata eritrosit merupakan parameter penting untuk diagnosis anemia.
Nilai rata-rata eritrosit terdiri dari MCV, MCH dan MCHC. Perhitungan nilai
rata-rata eritrosit diperoleh melalui perhitungan matematik dari
parameter-parameter seperti Hb, Ht dan jumlah eritrosit. Gambaran populasi eritrosit yang
diperoleh melalui perhitungan tersebut berupa angka yang mengidentifikasi
ukuran, kromasi dan kelainan bentuk eritrosit serta jenis anemia. Gambaran
populasi eritrosit secara nyata juga dapat dilihat melalui pembuatan sediaan apus
darah tepi (SADT). Melalui gambaran SADT dapat dilihat secara langsung
keadaan populasi eritrosit (bentuk, kromasi, adanya sel-sel muda, dan lain-lain).
Gambaran populasi eritrosit yang diperoleh melalui perhitungan matematis
apakah sesuai dengan gambaran populasi eritrosit pada SADT belum diketahui
dengan pasti. Peneliti ingin membandingkan hasil perhitungan MCV, MCH dan
MCHC dengan gambaran populasi eritrosit pada SADT.
1.6 Metodologi
Bentuk penelitian ini adalah uji diagnostik dengan membandingkan nilai
rata-rata eritrosit hasil pemeriksaan flow cytometer dengan morfologi eritrosit pada
1.7 Lokasi dan Waktu
• Lokasi : Laboratorium Diagnostik Rumah Sakit Imanuel Bandung;
Laboratorium Patologi Klinik Fakultas Kedokteran Universitas Kristen
Maranatha
5.1 Kesimpulan
Nilai rata-rata eritrosit hasil perhitungan flow cytometer tidak sepenuhnya
sesuai dengan gambaran populasi eritrosit pada sediaan apus darah tepi.
5.2 Saran
Untuk mengetahui populasi eritrosit yang sebenarnya sebagai pemeriksaan
penunjang diagnosis anemia sebaiknya dilakukan pemeriksaan morfologi eritrosit
pada SADT karena gambaran eritrosit berdasarkan nilai rata-rata eritrosit tidak
Adamson J W, Longo L D. 2005. Anemia and Polycythemia. In L D Kasper, S A Fauci, L D Longo et al. Editors: Harrison’s Principle of Internal Medicine. Volume I. 16th ed. USA: McGraw-Hill. p.329-336
Andrews C N. 2003. Iron Deficiency and Related Disorder. In P J Greer, J Foerster, N J Lukens et al. Editors: Wintrobe’s Clinical Hematology. Volume 1A. 11th ed. Philadelphia: Lippincott Williams & Wilkins. p.980-1004
Ann Bell. 2001. Morphology of Human Blood & Marrow Cells: Hematopoeisis. In M D Harmening. Editor: Clinical Hematology and Fundamentals of
Hemostasis. 4th ed. Philadelphia: F A Davis Company.
Anonim.2007. Gambaran SADT Eritrosit Matur.www.Bloodine.com. January 3rd, 2007
Babior B M. 1995. The Megaloblastic Anemias. In E Beutler, M A Lichtman, B S Coller, T J Kipps. Editors: Williams Hematology. 5th ed. USA: McGraw-Hill, Inc.
Bain JB. 2005. Diagnosis From The Blood Smear. New England Journal of
Medicine, 353 (5) : 498-507
Baughan A S J, Hughes A S B, Patterson G K, Stirling L. 1985. Anemia. In:
Manual of Hematology. Edinburgh London Melbourne New York: Churchill
Livingston. p3-24
_______.1985. Blood Film Abnormalities. In: Manual of Hematology. Edinburgh London Melbourne New York: Churchill Livingston. p243-7
Brown B A. 1993. Routine Hematology Procedures. In Hematology: Principles
and Procedures. 6th ed. USA: Lea & Febiger. P.83-126
Bull B S, Gorius J B. 1995. Morphology of The Erythron. In E Beutler, M A Lichtman, B S Coller, T J Kipps. Editors: Williams Hematology, 5th ed. USA: McGraw-Hill, Inc.
Burns C. 2004. Peripheral Blood Smear. In B S Mckenzie. Editor: Clinical
Cohen, J. 1960. A coefficient of agreement for nominal scales. Educational and
Psychological Measurement 20, 37-46
Craig E F. 2004. Flow Cytometri. In B S Mckenzie. Editor: Clinical Laboratory
Hematology. USA: Pearson Education Inc.
Department of Pathology University of Virginia Health System. 2006. Red Blood
Cells Basic. http://www.med-ed.virginia.edu/ courses/ path/ innes/ nh/
normbasics2.cfm, January 3rd, 2007
Desai S P, Isa-Pratt S. 2000. Clinician’s Guide to Laboratory Medicine. Hudson, Ohio: Lexi-Comp, Inc.
Elghetany M T, Davey F R. 2001. Erythrocytic Disorders. In J B Henry. Editor:
Clinical Diagnosis and Management by Laboratory Methods. 20th ed. Philadephia: W B Saunders Company.
Evatt L B, Gibbs N W, Lewis S M, McArthur R J. 1992. Fundamental Diagnostic
Hematology Anemia. 2nd ed. Atlanta, Georgia: U. S Department of Health and Human Services ; Geneva: World Health Organization.
Fairbanks V F, Beutler E. 1995. Iron deficiency. In E Beutler, M A Lichtman, B S Coller, T J Kipps. Editors: Williams Hematology. 5th ed. USA: McGraw-Hill, Inc.
Gandour M D. 2001. Applications of Flow Cytometry to Hematology and Hemostasis. In M D Harmening. Editor: Clinical Hematology and
Fundamentals of Hemostasis. 4th ed. Philadelphia: F A Davis Company. Gaspard K J. 1998. The Red Blood Cell and Alternations in Oxygen Transport. In
C M Porth. Editor: Pathophysiology Concept of Altered Health States. 5th ed. Philadelphia: Lippincott-Raven Publishers.
Glader B. 2003. Anemia: General Consideration. In P J Greer, J Foerster, N J Lukens, M G Rodgers, F Paraskevas, B Glader. Editors: Wintrobe’s Clinical
Hematology. Volume 1A. 11th ed. Philadelphia: Lippincott Williams & Wilkins. P.947-975
Guyton & Hall. 1997. Sel-sel darah, Imunitas dan Pembekuan Darah. Dalam Buku
_______. 1997. Pernapasan. Dalam Buku Ajar Fisiologi Kedokteran. Edisi 9. Jakarta: EGC.
Hillman R S, Ault K A. 1995. Hematology in Clinical Practice: A Guide to
Diagnosis and Management. 1st ed. USA: McGraw-Hill Company. Hoffbrand A V, Petit J E. 1996. Haematologi. cetakan ke-6. Jakarta: EGC.
Hubbard J. 2004. The Erythrocyte. In S B McKenzie. Editor: Clinical Laboratory
Hematology. 1st ed. New Jersey: Pearson Education, Inc.
Idaningroem Sjahid. 2002. Kelainan Morfologi Sel-sel Darah. Dalam Kursus
Penyegar Pemeriksaan Morfologi Sediaan Hapus Darah Tepi dan Sumsum Tulang. Indonesia.
Kearns H E, LaMonica A L. 2001. Principles of Automated Differential Analysis. In M D Harmening. Editor: Clinical Hematology and Fundamentals of
Hemostasis. 4th ed. Philadelphia: F A Davis Company. P. 594-603
Koeswardani R, Boentoro, Budiman. 2001. Flow Cytometri dan Aplikasi Alat
Hitung Sel Darah Otomatik Technicon H-1 dan H3. Malang: Laboratorium
Patologi Klinik FK Unibraw RSUD Dr. Syaiful Anwar.
http://www.tempo.co.id/medika/arsip/082001/hor-1.htm, January 3rd, 2007
Landis, J.R. and Koch, G.G. 1977. The measurement of observer agreement for categorical data. Biometrics 33, 159-74.
Lee G R, Herbert V. 1999. Nutritional Factors in The Production and Function of Erythrocytes. In G R Lee, J Foerster, J Lukens, F Paraskevas, J P Greer, G M Rodgers. Editors: Wintrobe’s Clinical Hematology. 10th ed. Maryland: Lippincott Williams & Wilkins.
Northington W. 2000. Anemia: Diagnosis and Classification. USA: Murray State
University.http://campus.murraystate.edu/ academic/ faculty/ wade.
northington/ anemia.htm, January 3rd, 2007
Rachmawati A M, Mansyur Arief, Hardjoeno. 2003. Pemeriksaan Anemia. Dalam H Hardjoeno. Editor: Interpretasi Hasil Pemeriksaan Laboratorium
Diagnostik. Cetakan ke-3. Makassar: Lembaga Penerbitan Universitas
Hassanudin (Lephas).
RADIL University of Missouri. 2007. RADIL Standard Operating Procedure for Making Blood Smear. http://www.radil.missouri.edu/ info/ teaching/ MakingBloodSmear. asp. January 3rd, 2007
Simmer M. 2003. Flow Cytometry : A Technology to Count and Sort Cells. The Science Creative Qurterly. http://www.scq.ubc.ca/?p=277. January 3rd, 2007
Sudigdo Sastroasmoro, Sofyan Ismael. 1995. Dasar-dasar Metodologi Penelitian Klinis. Jakarta: Binarupa Aksara.
Sysmex Corporation. 2006. http://www.sysmex.co.jp/sysmex/history/img/xs-1000i.jpg. January 3rd, 2007
Sysmex Corporation. 2006. Instruction for use Sysmex XS – 1000i / XS – 800i. Japan: Sysmex Corporation.
Tagliasacchi D, Carboni G. 1997. Blood Cells., http://www.funsci.com/ fun3_en/ blood/ blood.htm#3, January 3rd, 2007
Uthman O E. 2000. Understanding Anemia. USA: University Press of Mississipi. http://web2.airmail.net/ uthman/ anemia/ anemia.html, January 3rd, 2007
Wallach J B. 2000. Interpretation of Diagnostic Pemeriksaants. 7th ed. Brooklyn, New York: A Wolter Kluwer Company.
WHO. 2001. The clinical use of blood in medicine, obstetrics, paediatrics,
surgery & anaesthesia, trauma & burns. WHO blood transfusion safety.
Geneva.