Do you still remember the
Periodic Table Song for the
Penggolongan Manusia dalam Al Qur’an
Surat Al Fatihah ayat 6-7:
“Tunjukilah kami jalan yang lurus(6), (yaitu) jalan orang-orang yang telah Engkau anugerahkan
nikmat kepada mereka; bukan (jalan) mereka yang dimurkai dan (bukan pula) jalan mereka yang
sesat(7)”
Surat Al Waqi’ah ayat 7-9:
Tujuan Pembelajaran
Menjelaskan dasar pengelompokan
unsur-unsur dalam sistem periodik.
Menentukan elektron valensi dan kulit
valensi
Menentukan periode dan golongan
unsur-unsur dalam tabel periodik.
Mengklasifikasikan unsur ke dalam logam,
non logam, dan metalloid dilihat dari
You’ll Need to ….
Remember about the electron
configuration
Remember about “elektron valensi”
and “kulit valensi”
Remember about the rule:
Evolusi Sistem Periodik
Unsur
Pada awal perkembangan ilmu kimia,
saintis mengelompokkan unsur
berdasarkan massa atomnya karena ide tentang proton, elektron dan neutron
Drobereiner triads
Pada 1892 Dobreiner
mengelompokkan unsur-unsur ke
dalam beberapa kelompok. Setiap kelompok terdiri dari 3 unsur yang disebut Triads
Newland’s law of octaves
Pada 1865 beliau
menemukan apabila unsur-unsur disusun berdsarkn kenaikan massa atomny
maka akan ada 7 kelompok unsur yang masing-masing berisi 8 unsur dengan sifat fisika dan kimia yang sama
Mendeleev’s periodic table
Beliau menemukan jika atom-atom disusun berdasarkan
kenaikan massa atomnya maka dapat diamati kesamaan sifat kimia pada interval tertentu Mendeleev juga menyisakan
beberapa ruang kosong karena beranggapan bahwa ada unsur yang belum ditemukan
Moseley’s Periodic Table
Moseley
melakukan
percobaan untuk meneliti spektrum sinar X dan
hubungannya dengan jumlah muatan listrik
Seaborg’s
(nomor atom 94-102) yang
kemudian
diletakkan pada baris baru Sistem Periodik Unsur
Bagaimana hubungan
antara konfigurasi
Konfigurasi Elektron dan Letak Unsur
11
Na: 1s
2
2s
2
2p
6
3s
1
11
Na: [Ne]
3
s
1
Kulit Valensi
Kulit Valensi: Menunjukkan periode
Elektron Valensi: Menunjukkan
Golongan
Apa fungsi sub kulit s, p, d dan f
dalam menentukan letak
unsur?????
Unsur-unsur pada golongan utama
memiliki konfigurasi elektron dengan
sub kulit terakhirnya s dan/atau p
Unsur-unsur pada golongan transisi
memiliki konfigurasi elektron dengan
sub kulit terakhirnya d
KUIS
1.Tentukanlah letak unsur berikut ini dalam sistem periodik unsur:
2.Tentukan pasangan unsur-unsur yang ada dalam satu golongan
1.Apa perbedaan unsur logam dan non
logam yang Ananda ketahui????
2.Bila dilihat dari letak unsur dalam SPU,
golongan berapakah yang termasuk unsur logam, non logam dan
metaloid?????
3.Apa saja ciri-ciri fisik unsur logam dan
non logam?
Jari-Jari Atom
Bagaimana kecenderungan besarnya
jari-jari atom unsur dalam satu golongan?
Bagaimana kecenderungan besarnya
jari-jari atom unsur dalam satu periode?
Bagaimana hubungan antara jari-jari
atom dengan konfigurasi elektron?
Bagaimana pengaruh jumlah proton di
Energi Ionisasi
Bagaimana hubungan antara
konfigurasi elektron dengan energi ionisasi pertama suatu atom?
Jelaskan mengapa energi ionisasi
unsur golongan VA lebih tinggi dibandingkan golongan VI A?
Bagaimana cara menentukan
golongan suatu unsur berdasarkan energi ionisasi pertama, kedua,
Afinitas Elektron
Jelaskan perbedaan antara afinitas
elektron dan energi ionisasi?
Bagaimana kecederungan afinitas
elektron unsur dalam satu periode?
Bagaimana kecederungan afinitas
elektron unsur dalam satu golongan?
Apa pengaruh besarnya afinitas
elektron dan energi ionisasi
Keelektronegatifan
Apa yang dimaksud dengan
keelektronegatifan?
Bagaimana kecenderungan
keelektronegatifan unsur dalam satu golongan?
Bagaimana kecenderungan
keelektronegatifan unsur dalam satu periode?
Bagaimana hubungan antara
Sifat-sifat Unsur Logam:
Dapat menghantarkan listrik dengan
baik (konduktor)
Warna mengkilap
Tekstur keras dan ulet (Kecuali Hg)
Memiliki titik didih dan titik leleh yang
tinggi
Sifat-sifat Unsur Non Logam:
Tidak menghantarkan arus listrik (non
konduktor)
Titik didih dan titik lelehnya rendah
Dapat berwujud padat, cair dan gas
pada suhu kamar
Unsur Metaloid:
Unsur non logam yang mempnyai sifat
sifat kelogaman secara terbatas
Prediksikan sifat-sifat
unsur metaloid!
Latihan Soal
1. Diketahui konfigurasi elektron dari beberapa atom sebagai berikut:
a)[Ar] 4s2 3d2 b)[He] 2s2 2p3 c) [Kr] 5s2 4d10
Latihan Soal
2. Tuliskanlah konfigurasi unsur-unsur
berikut ini lalu tentukan letaknya pada sistem periodik unsur dan nama
unsurnya:
13
A
28
B
KUIS 2
Tuliskanlah konfigurasi unsur-unsur berikut ini lalu tentukan letaknya
pada sistem periodik unsur
KUIS 3
Tuliskanlah konfigurasi elektron
unsur-unsur berikut, tentukan letaknya dalam SPU, lalu urutkanlah unsur-unsur dari
Kuis 4
Tuliskanlah konfigurasi elektron
unsur-unsur berikut, tentukan letaknya dalam SPU, lalu urutkanlah unsur-unsur
berdasarkan:
Kenaikan jari-jari atom
Kenaikan energi ionisasi
3
Li
7
N
5
B
Keyword:
Atomic radius is the distance between the
nucleus and the valence electron
Jari-jari atom adalah jarak antara inti atom
dengan elektron terluar
TREND of ATOMIC RADII
Picture quoted from:
Can You explain why is that
happen?
TREND of ATOMIC RADII
• For elements along a period, from left to right
the atomic radii are getting smaller because the number of protons in nucleus is increase. Means that the attraction force from the
nucleus to the outer electron become
stronger and makes the atomic radii smaller.
• For elements within a group, from top to
ENERGI IONISASI
Keyword:
• Ionization energy is the minimum energy required to remove the highest energy electron from an isolated gaseous atom or ion in its ground state.
• Energi ionisasi adalah jumlah energi minimum yang
Trend of 1
stIonization Energy
(
IE
1)
Graph quoted from:
Trend of 1
stIonization Energy
(
IE
1)
ratomic increase
ratomic decrease
Can You explain why is that
happen?
TREND OF 1st IONIZATION ENERGY (IE1)
• For elements within a group, from top to bottom the IE1
values are getting smaller because atomic radius increase, the attraction force from nucleus to the outer electrons
getting weaker. The outer electron is easy to be removed and the energy required to remove the outer electron is smaller.
• For elements in a period, from left to right the IE1 values are
vary. From Li to Be the IE1 values increase but decrease in B.
And then from B to N IE1 values increase but decrease in O.
The increasing trend happen because the number of protons in nucleus larger, the attraction force from nucleus to outer electron stronger and the electron need a great energy to be able to removed. The anomaly for B and O are due to the
Why is the difference in the value of
IE
1of H and
Li so great?
H atom only has 1 proton and 1 electron without neutron. the electron in H atom occupy the shell that very close with the nucleus and there is no
repulsion with other electron. Therefore the attraction force between proton and electron are so strong and the energy needed to remove the electron is great.
H atom
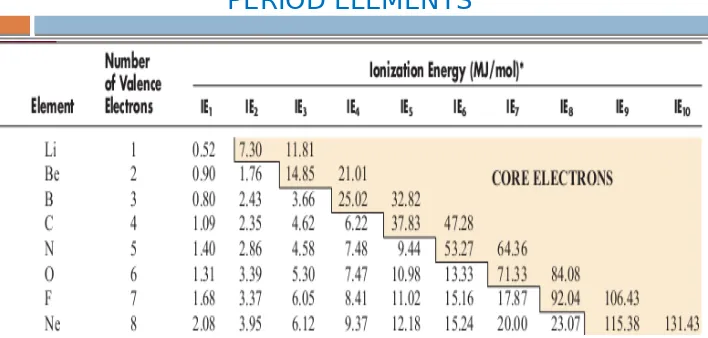
SUCCESSIVE IONIZATION ENERGY FOR 2nd
PERIOD ELEMENTS
Trend of Successive
IE
IE
1
< IE
2<
IE
3< … because in the atom that
already
released an electron the value of
Z
efremains the same but the number of
electrons affected by it is decreases, and
makes the electron attracted strongly to the
ion.
If the outer electrons are all removed, the
AFINITAS ELEKTRON
F(g) + e F-(g) EA1 = -328 kJ/mol
Key Word:
Electron Affinity is the energy change for the process of adding an electron to an isolated gaseous atom or ion
Tanda negatif menunjukkan bahwa reaksi
(sistem) melepaskan energi ke lingkungan
Tanda positif menunjukkan bahwa reaksi
Trend of Elements’ 1
stElectron
ELEKTRONEGATIVITAS
Electronegativity is the relative ability of
an atom to attract toward itself the electrons in chemical bond.
Elektronegativitas adalah kemampuan
Robert
Milikan
He proposed the value of electronegativity based on ionization energy and electron affinity of an
atom
He won the Noble prize twice, in 1954 for Chemistry and in 1962 for peace. He found the elements’ electronegativity
value by considering the bond dissociation energy.
KUIS 3
Tuliskanlah konfigurasi elektron
unsur-unsur berikut, tentukan letaknya dalam SPU, lalu urutkanlah unsur-unsur dari
yang memiliki:
Jari-jari terbesar hingga terkecil
Energi Ionisasi terbesar hingga terkecil
Keelektronegatifan terbesar hingga terkecil
Trend of Elements’ Electronegativity
Picture quoted from:
Kuis
1. Tuliskanah konfigurasi elektron
kemudian urutkanlah unsur berikut ini berdasarkan kenaikan
keelektronegatifannya!
9
F,
11Na,
20Ca,
15P,
6C dan
8
O
2. Tuliskanlah ion-ion yang dapat dibentuk