BAKTERI KITINOLITIK YANG DIISOLASI DARI TAMBAK UDANG
LAMONGAN JAWA TIMUR
CHITINOLYTIC BACTERIA ISOLATED FROM SHRIMP PONDS
LAMONGAN EAST JAVA
Nuniek Herdyastuti
Jurusan Kimia FMIPA Universitas Negeri Surabaya Jl. Ketintang Surabaya (60231), Telp. 031-8298761
Email :nuniekherdyastuti@gmail.com
Abstrak.Eksplorasi kitinolitik dari tambak udang bertujuan untuk mencari keragaman bakteri penghasil kitinase dengan aktivitas yang tinggi dari lingkunga perairan. Aktivitas kitinase ditentukan dengan metode Monreal-Reese berdasarkan pelepasan N-Asetil glukosamin. Diperoleh isolat LA-21 adalah bakteri gram positif berbentuk batang dengan karakteristik koloni berwarna putih, bentuk bulat, elevasi cembung, margin bergerigi (serrate) dan diameter koloni 1-2 mm. Hasil uji 16S-rRNA menunjukkan bahwa isolat LA-21 mempunyai hubungan kekerabatan 97 % terhadap Bacillus sp AHBR 2.
Kata kunci: Aktivitaskitinase, bakteri kitinolitik, tambak udang
Abstract. Chitinolytic exploration of shrimp ponds aimed to diversity of bacteria producing chitinase with high activity of aquatic environments. Chitinase activity was determined by a Monreal-Reese method based on the release N-Acetyl glucosamine. Isolates LA-21 was a gram positive with characteristic rod- shapes, white coloni, rounded shape, serrated margine, convex elevation and diameter coloni 1-2 mm. Test result 16S-rRNA indicate that the isolates-LA-21 97% gene similarity to Bacillus sp AHBR 2
Key words : Chitinase activity, chitinolytic bacteria, shrimp ponds
PENDAHULUAN
Kitinase (EC 3.2.11.14) adalah enzim yang mempunyai kemampuan untuk menghidrolisis senyawa kitin membentuk oligosakarida dan monomernya. Kitinase dapat ditemukan dari berbagai macam organisma seperti virus, bakteri, jamur, serangga, tumbuhan tingkat tinggi dan hewan yang mempunyai peranan penting dalam metabolismenya [1]. Bakteri kitinolitik merupakan penghasil enzim kitinase dapat diperoleh dari berbagai sumber rti lingkungan
perairan seperti laut, danau, tambak, limbah udang dan sebagainya [2,3,4
Eksplorasi habitat telah banyak dilakukan untuk mencari biodiversitas bakteri kitinolitik dengan tujuan mendapatkan keragaman bakteri yang mampu menghasilkan aktivitas kitinase terbaik. Salah satu tempat yang berpotensi menghasilkan bakteri kitinolitik yaitu tambak udang.Beberapa wilayah di Jawa Timur seperti Lamongan Tuban, Situbondo dan Sidoarjo berada di daerah pesisir pantai sehingga sebagian besar mata pencaharian penduduk
adalah sebagai petani tambak. Penelitian ini bertujuan untuk mengetahui keanekaragaman bakteri kitinolitik yang berasal dari lingkungan tambak udang khusunya di daerah Lamongan Jawa Timur.
Udang mempunyai kandungan kitin yang cukup tinggi. Focher menyatakan bahwa, kulit udang mengandung protein (25 – 40 %), kalsium karbonat (45 – 50 %), dan kitin (15 – 20 %), tetapi besarnya kandungan komponen tersebut tergantung pada jenis udangnya. Kitin merupakan bentuk linier polisakarida yang dibentuk dari ikatan -1,4 residu N-asetil-glukosamin [5]. Dengan demikian kitin secara kimiawi adalah suatu polimer golongan polisakarida yang tersusun atas 2-asetamido-2-deoksi-D-glukosa membentuk ikatan -1,4. Ikatan pada molekul tersebut membentuk fibra yang linier. Rantainya dapat membentuk kristal karena adanya ikatan hidrogen intramolekul dan membentuk mikrofibril yang panjang menghasilkan struktur yang rigid dan stabil [6]. Kitin terutama dalam bentuk koloidal kitin banyak digunakan sebagai sumber karbon dan induser untuk memproduksi enzim kitinase dari berbagai strain [7].
BAHAN DAN METODE Alat
Beberapa alat yang digunakan antara lain : peralatan gelas yang umum digunakan, pH meter, Spektrofotometer UV-Vis (Shimadzu, 1800), sentrifuse dingin (5810 R), PCR ABI
Prism 9700, perangkat Applied Biosystems 3730XL Genetic Analyzer
Bahan
Bahan-bahan yang di butuhkan adalah kitin, HCl (37%), aquades, yeast extract (Difco), NaCl, tripton (Difco), Bacto agar (Difco), KH2PO4, Na-K- tartrat tetrahidrat, asam 3,5- dinitrosalisilat (SIGMA), N-asetil glukosamin (SIGMA). universal primer 5’- GGTTACTTGTTACGACTT-3’ (Uni B1) dan 5’-AGAGTTTGATCTGGCTCAG-3’ (Bact F1) , dNTP, Taq DNA polymerase, Etidium Bromida, Red Safe flourecent kit, loading buffer, agarose.
Prosedur Penelitian Seleksi bakteri kitinolitik
Bakteri dari diisolasi dari tambak udang dengan cara menumbuhkan pada media minimal yang mengandung koloidal kitin, dengan komposisi : 0,4 % koloidal kitin ; 0,7 % K2HPO4 ;, 0,3 % KH2PO4 ; 0,5 % MgSO4.5H2O ; 0,01 % FeSO4.7H2O ; 0,001 % MnCl2 dan 0,5 % pepton. Campuran diinkubasi pada suhu ruang selama 45 jam dengan pengocokan kecepatan 150 rpm. Supernatan yang diperoleh selanjutnya ditentukan aktivitas kitinasenya.
Persiapan Koloidal kitin
Kitin dibuat bentuk koloid dengan menggunakan cara menurut Hsu and Lockwood [8]. Sebanyak 40 g kitin dilarutkan dalam 400 mL HCl pekat, diaduk dengan pengaduk magnet selama 30 – 50 menit. Larutan kitin kemudian
diendapkan sebagai suspensi koloid dengan menambahkan 2 liter air dingin (suhu 5 – 10 C) secara pelan-pelan. Suspensi ditampung dengan cara menyaring menggunakan kertas saring, dan residu yang diperoleh dicuci dengan aquades 5 liter. Pencucian diulang sedikitnya 3 kali atau sampai pH sekitar 3,5. Pada proses ini kira-kira akan diperoleh 85 % kitin.
Penentuan aktivitas enzim kitinase
Aktivitas enzim ditentukan berdasarkan jumlah gula reduksi yang dilepaskan dan diukur secara kolorimetri dengan menggunakan metode yang dijelaskan oleh Monreal dan Reese [9]. Sebanyak 2 mL larutan kitin 1,25 % (b/v) dilarutkan dalam 200 mM buffer kalium fosfat diaduk dengan pengaduk magnet dan ditambahkan 0,5 mL larutan enzim. Inkubasi selama 2 jam pada suhu kamar. Setelah 2 jam tempatkan tabung ke dalam air mendidih selama 5 menit dan didinginkan pada suhu kamar. Suspensi disentrifugasi selama 10 menit pada kecepatan 4000 rpm. Sebanyak 1 mL supernatan pada tabung sampel ditambahkan 2 mL air deionisasi dan 1,5 mL reagen pewarna yang mengandung 5,3 M larutan Natrium kalium tartrat dan Asam 3,5 Dinitrosalisilat 96 mM. Campuran dipanaskan dalam air mendidih selama 5 menit setelah dingin diukur serapannya dengan spektrofotometer UV-Vis pada panjang gelombang 540 nm. Sebagai standar digunakan N-asetil glukosamin.
Penentuan gen 16S-rRNA
Penentuan dilakukan berdasarkan tahapan : isolasi DNA, amplifikasi dengan gen 16S-rRNA dengan kondisi reaksi PCR : siklus sebanyak 30 siklus, denaturasi : 95 ºC selama 1 menit; annealing : 55 ºC selama 1 menit ; dan elongasi: 72 ºC selama 1 menit. Hasil PCR yang telah dimurnikan dilakukan sequencing dengan kondisi dengan kondisi initial denaturation 96 ºC selama 1 menit, dengan siklus 25 kali terdiri dari 96 ºC selama 10 detik, 50 ºC selama 5 detik dan 60 ºC selama 4 menit.
HASIL DAN PEMBAHASAN
Isolasi bakteri kitinolitik dari Tambak udang Kitin koloidal adalah kitin yang dilarutkan dalam asam klorida pekat seperti yang telah dijelaskan oleh Hsu dan Lockwood (1975) sebagai media selektif untuk mendapatkan bakteri kitinolitik. Enzim kitinase ekstraseluler dari Bacillus sp WY22 menunjukkan spesifitas substrat paling tinggi dengan menggunakan kitin koloidal bila dibandingkan menggunakan substrat swollen kitin, glikol kitin atau serbuk kitin [10]. Beberapa penelitian yang memanfaatkan kitin koloidal untuk mendapatkan bakteri kitinolitik seperti Enterobacter sp NRG4, Aeromonas sp, Aeromonas schubertii, Bacillus laterosporous MML2270 [11, 12, 13, 14].
Hasil eksplorasi bakteri kitinolitik dari tambak udang di Lamongan, telah diperoleh 54 isolat (LA 1 – LA54). Berdasarkan hasil uji aktivitas pada ekstrak kasar menunjukkan bahwa
37 dari 54 isolat mempunyai aktivitas kitinase seperti pada Gambar 1 [15]. Hasil analisis kuantitatif bakteri kitinolitik berdasarkan uji aktivitas pada ekstrak kasar memberikan hasil yang cukup tinggi. Nilai aktivitas tersebut cukup tinggi bila dibandingkan dengan isolat kitinolitik yang diperoleh dari tambak udang Tuban [16], Stenotrophomonas sp. B2-4 yang diisolasi dari 17] and Enterobacter sp. G-1 yang diisolasi dari kota Matsue, Jepang [18].
Gambar 1. Hasil uji aktivitas ekstrak kasar isolat dari Lamongan
Penentuan spesies Isolat LA-21
Berdasarkan hasil uji fisiologi dan morfologi isolat LA-21 merupakan bakteri gram positif berbentuk batang (Gambar 2) dengan karakteristik koloni berwarna putih, bentuk bulat, elevasi cembung, margin bergerigi (serrate) dan diameter koloni 1-2 mm. Uji morfologi (Tabel 1) menduga bahwa isolat LA-21 merupakan Bacillus cereus dengan percent probability 63.60%.
Gambar 2. Pewarnaan Gram isolat LA-21 dengan perbesaran 100 kali
Tabel 1. Hasil uji Fisiologi isolat LA-21 No Jenis uji Biokimia Hasil 1. 2. 3. 4. 5. Oksidase Motilitas Nitrat Lisin Ornitin + + + - + 6. H2S - 7. Glukosa - 8. Xilosa + 9. ONPG - 10. Indol - 11. 12. 13. 14. 15. 16. 17. 18. 19. 20. 21. 22. 23. 24. 25. 26. 27. 28. 29. Urease VP Sitrat TDA Gelatin Malonat Inositol Sorbitol Ramnosa Sukrosa Laktosa Arabinosa Adonitol Rafinosa Salisin Arginin Amilolitik Proteolitik Lipolitik - - - - + - - - - - - + - - - - + + +
Gambar 3. Penentuan urutan DNA hasil amplifikasi isolat LA-21
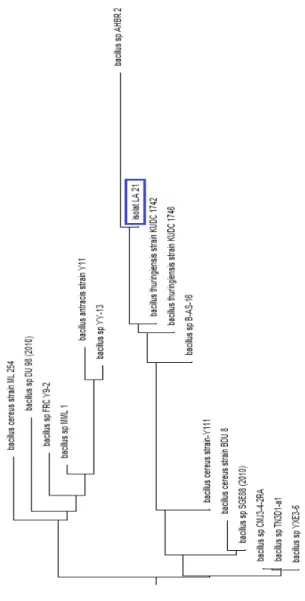
Penentuan spesies secara genetik, telah diperoleh hasil amplifikasi isolat LA-21 dengan ukuran DNA 1500 bp. DNA isolat-LA21 yang telah ditentukan urutannya (Gambar 3) di BLAST melalui situs www.ncbi.nlm.nih.gov untuk mendapatkan sequence alignment. Berdasarkan Sequence alignment menunjukkan bahwa isolat LA-21 mempunyai hubungan kekerabatan yang lebih dekat dengan Bacillus sp AHBR 2 sebesar 97 % seperti tampak pada phylogenetic tree seperti tampak pada Gambar 4 [19]
Gambar 4. Phylogenetic Tree yang menunjukkan kekerabatan isolat LA-21
Bakteri kitinolitik dari kelompok Bacillus tersebut sudah banyak dihasilkan oleh peneliti yang lain, seperti yang telah dilakukan oleh Penelitian lain tentang bakteri kitinolitik diperoleh beberapa bakteri yang tergolong dalam Bacillus, Bacillus sp maupun Bacillus licheniformis [20,21,22,
23]. Penghasil kitinolitik jenis yang lain juga telah ditentukan seperti Pseudomonas sp TKU008 diperoleh dari tanah di Taiwan [24] Pseudomonas sp TNH54 dari tanah sawah [25].
KESIMPULAN
Berdasarkan hasil penelitian dapat disimpulkan bahwa :
1. Bakteri kitinolitik LA-21 yang diisolasi dari tambak udang Lamongan mempunyai aktivitas kitinase yang cukup tinggi yaitu 0,731 U/mL
2. Isolat LA-21 merupakan bakteri gram positif berbentuk batang dan berdasarkan hasil analisis 16s-rRNA tergolong sebagai kelompok Bacillus sp
UCAPAN TERIMA KASIH
Ucapan terimakasih disampaikan kepada kelompok penelitian Kitinase khususnya kepada Fauziah dan Rio Widodo yang telah menyelesaikan penelitian ini.
DAFTAR PUSTAKA
1. Kuddus, S.M., Ahmad, R.I.Z., 2013. “Isolation of novel chitinolytic bacteria and production optimization of extracellular chitinase”, Journal of Genetic Engineering and Biotechnology., 11 : 39-46
2. Donderski W, Brzezinska MS., 2003. “The Utilization of N-Aceyloglu-cosamine and Chitin as Sources of Carbon and Nitrogen by Plantonic and Benthic Bacteria in Lake Jeziorak”. Polish Journal of Enviromental Studies., 12 : 685-692.
3. Chang SC, Wang JT, Vandamme P, Hwang
JH, Chang PS, Chen WM., 2004.
“Chitinimonas taiwanensis gen. nov., sp. nov., a Novel Chitinolytic Bacterium Isolated from a Freshwater Pond for Shrimp Culture” System Appl. Microbiol., 27 : 43–49
4. Moon S.J, Young ML, Yong LC, Cherol HK,Young CL., 2005. “Overexpression and characterization of a novel chitinase gene from marine bacterium Pseudomonas sp BK-1”, Ind. J. Biochem. Biophy.,42 : 339-344 5. Nathalie,C., Fleury, A., Fukamiza,T., and
Ryszard,B., 2006, ‘Two-exo- -D-glukosaminidase from Actinomycetes define anew subfamily 2 of glikoside hydrolases”, Biochem.Journal , 394 : 675-686.
6. Gooday, G.W., 1990, “Physiology of Microbial Degradation of Chitin and Chitosan”, Biodegradation, 1 : 177-190 7. Mejia-Saulés,J.E.,Waliszewski, K.N.,Garcia,
M.A., and Cruz-Camarillo, R., 2006 “The use crude shrimp shell powder for chitinase production by Serratia marcescens”. Food Techn.Biotechnology, 44(1) : 95-100
8. Hsu S.C., and Lockwood J.L., 1975, Powdered Chitin Agar As a Selective
Medium for Enumeration of
Actinomycetes in Water and Soil, Appl.
Microbiol., 29, 3, 422-426.
9. Monreal J. and Reese, E.T., 1969, The Chitinase of Serratia marcescens, Canadian Journal of Microbiology, 15 : 689-696. 10. Woo C.D and Park H.D., 2003, An
Extrasellular Bacillus sp Chitinase for the production of chitotriose as a major chitinolytic product, Biotechnol. Letters, 25 : 409-412.
11. Dahiya N., Tewari, and Hoondai, 2005, Chitinase from Enterobacter sp. NRG4 : Its Purification, Characterization and Reaction Pattern, Electronic J. Biotechnol., 8, 2. 12. Guo, S.H., Chen J.K. and Lee,W.C.,
2004, Purification and Characterization of Extracellular Chitinase From Aeromonas schubertii, Enzyme and Microbial Technology, 35 : 550-556
13. Huang C.J., and Chen C.Y., 2004, “Gene Cloning and Biochemical Characterization of Chitinase CH from Bacillus cereus 28-9”, Annals. Microbiol., 54 (3) : 289-297
14. Shanmugaiah V., Mathivanan N., Balasubramanian N., and Manoharan P.T., 2008, “Optimization of cultural conditions for production of chitinase by Bacillus laterosporous MML2270 isolated from rice rhizosphere soil”, Afric. J. Biotechnol., 7, 15, 2562-2568
15. Fauziah dan Herdyastuti, N. 2013. “Uji Aktivitas Bakteri Kitinolitik dari Tambak Udang Di Lamongan dan Sidoarjo”. UNESA Journal of Chemistry. 2(1) : 36-39
16. Prabowo,Y.Y., dan Herdyastuti, N., 2014, “Aktivitas bakteri kitinolitik yang diisolasi dari tambak udang di Tuban”, UNESA Journal of Chemistry. 3(3) :
17. Soeka, YS, and Sulistiani. 2011. “Seleksi, Karakterisasi, dan Identifikasi Bakteri Penghasil Kitinase yang Diisolasi dari Gunung Bromo Jawa Timur”. Jurnal
Natur Indonesia. 13(2). 155-161
18. Mahata, M., Dharma A., Ryanto, I, and Rizal Y. 2008. Characterization of Extracellular Chitinase from Bacterial Isolate 99 and Enterobacter sp. G-1 from Matsue City, Japan. Microbiology Indonesia. Vol. 2, No. 1. 34-38
19. Widodo, R., dan Herdyastuti, N., 2013, “Penentuan gen penyandi 16S-rRNA bakteri kitinolitik dari tambak udang Lamongan”, UNESA Journal of Chemistry. 3(3) :
20. Anuradha, V. dan Revathi, K. 2013. “Purification and characterization of chitinase fromtwo Bacillus spisolated from crustacean shells”. Journal of Microbiology and Biotechnology Research. 3 (3):160-167.
21. Haliza, Winda dan Suhartono, Maggy Thenawidjaya. 2004. “Karakteristik Kitinase Dari Mikrobia”. Buletin Teknologi Pascananen Pertanian Vol 8 (1).
22. Suryanto, D., Munir, E., and Yurnaliza. 2005. Eksplorasi Bakteri Kitinolitik: Keragaman Gen Kitinase pada Berbagai
Jenis Bakteri dan Pemanfaatannya. Medan: Universitas Sumatera Utara. 23. Anindyaputri, Amaryllis. dkk. 2010.
“Chitinolytic Bacteria Isolated from Chili Rhizosphere: Chitinase Characterization and Its Application as Biocontrol for Whitefly (Bemisia tabaciGenn.)”. American Journal of Agricultural and Biological Sciences. 5 (4): 430-435.
24. Wang S.L., Bo-Shyun L., Liang T.W., Wang C.L., Pei-Chen W., and Je-Ruei L., 2010, “Purification and Characterization of Chitinase from a New Species Strain Pseudomonas sp. TKU008”, J. Microbiol. Biotechnol., 20, (6) : 1001–1005
25.Herdyastuti,N., Cahyaningrum S.E.,
Raharjo T.J., Mudasir, Matsjeh,S., 2012, “Potential antifungal of Chitinolytic Bacteria Pseudomonas sp TNH54 from
Mud Field”, Research Journal of
Pharmaceutical, Biological and
Chemical Sciences, Vol.3 Issue