BAB IV
HASIL DAN PEMBAHASAN
4.1 Hasil Preparasi Kulit Batang Pisang Kepok
Preparasi kulit batang pisang diawali dengan mencucinya menggunakan air
hingga bersih dan dijemur di bawah sinar matahari hingga kering. Proses
pengeringan ini membutuhkan waktu yang cukup lama karena kulit batang pisang
memiliki kandungan air yang cukup tinggi sehingga sukar kering. Setelah kulit
batang pisang kering, kulit batang pisang dipotong-potong dengan ukuran sekitar
1-2 cm bertujuan untuk memperbesar luas permukaan sehingga mempercepat
reaksi dalam pembuatan pulp.
4.2 Hasil Pembuatan Pulp dari Kulit Batang Pisang
Langkah awal pembuatan pulp dari kulit batang pisang yaitu dengan
menimbang kulit batang pisang yang telah kering sebanyak 20 gram lalu
direndam dengan larutan Ca(OH)2 2,5% sebanyak 200 mL selama 7 hari. Tujuan
proses perendaman ini adalah untuk mereaktifkan serat, mengembangkan serat
agar menjadi lebih lunak sehingga mempermudah pembuatan pulp dan
menurunkan derajat polimerisasi. Setelah proses perendaman selesai, kulit batang
pisang tersebut dicuci dengan akuades sampai bebas basa yang dapat diuji
menggunakan kertas lakmus merah dimana warna dari kertas lakmus merah
tersebut tidak berubah. Selanjutnya batang pisang dimasukkan ke dalam labu alas
bulat yang telah diisi dengan 150 mL larutan NaOH 17,5% lalu campuran tersebut
menghilangkan lignin dan hemiselulosa yang terdapat dalam kulit batang pisang.
Lepasnya lignin dan hemiselulosa ditandai dengan berubahnya warna campuran
kulit batang pisang dengan NaOH yang semula berwarna coklat menjadi hitam.
Setelah proses refluks selesai, campuran tersebut didinginkan lalu dicuci kembali
dengan akuades hingga bebas basa yang dapat diuji menggunakan kertas lakmus.
Kulit batang pisang yang bebas basa lalu dikeringkan dalam oven pada suhu 600C
hingga kering selama semalam. Pada penelitian ini diperoleh pulp sebesar
80,75 gram dengan rendemen 22,43%. Rendemen yang didapat sangat kecil hal
ini dikarenakan banyaknya kandungan lignin dan hemiselulosa pada kulit batang
pisang yang hilang selama proses refluks. Hasil refluks batang pisang ditunjukkan
pada Gambar 4.1
Gambar 4.1 Hasil refluks batang pisang
4.3 Pemutihan (Bleaching) Pulp dari Kulit Batang Pisang
Proses bleaching pulp ini diawali dengan menimbang sebanyak 10 gram
pulp kering dari kulit batang pisang lalu ditambahkan 88 mL akuades dalam gelas
beker yang telah dipanaskan pada suhu 60ºC, kemudian campuran tersebut diaduk
hingga bertekstur seperti bubur. Kemudian bubur didinginkan lalu ditambahkan
dengan 100 mL NaOCl 5% dan didiamkan selama 30 menit sambil terus diaduk.
proses refluks. Pada penelitian ini proses bleaching pulp menggunakan NaOCl
yang berperan sebagai bleaching agent yang bersifat oksidator kuat. Penggunaan
NaOCl di sini merupakan teknologi bleaching dengan konsep ECF (Elementally
Chlorin Free) dimana unsur klorida masih boleh digunakan tetapi tidak dalam
bentuk Cl2 yang sangat berbahaya bagi lingkungan tapi dalam bentuk senyawa
lain yang lebih aman terhadap lingkungan misalnya NaOCl. NaOCl bereaksi
dengan lignin melalui reaksi adisi dan subtitusi. Waktu perendaman dengan
NaOCl harus diperhatikan karena jika waktu perendaman terlalu lama maka
selulosa terdegradasi bersama lignin, sehingga dalam penelitian ini dipakai waktu
30 menit (Suryani, 2011). Untuk menghilangkan sisa-sisa NaOCl, pulp dibilas
dengan akuades hingga bebas basa.
Untuk menyempurnakan proses degradasi lignin, maka pulp direndam
kembali dengan NaOH 2% dan dibiarkan selama 30 menit. Pemilihan konsentrasi
dan waktu perendaman dengan NaOH juga menjadi pertimbangan. Apabila
konsentrasi NaOH yang dipakai terlalu besar maka selulosa dapat terdegradasi,
begitu juga waktu perendaman yang tidak boleh terlalu lama. Kemudian pulp
dicuci dengan akuades hingga bebas basa yang diuji dengan menggunakan kertas
lakmus merah. Selanjutnya pulp dikeringkan diudara terbuka selama semalam.
Proses beaching ditandai dengan berubahnya tekstur selulosa menjadi lebih halus
seperti kapas dan perubahan warna dari yang semula coklat menjadi putih. Massa
pulp yang diperoleh setelah proses bleaching sebesar 29,35 gram dengan
cukup banyak. Perbedaan antara pulp batang pisang sebelum dan sesudah
diputihkan ditunjukkan pada Gambar 4.2
Gambar 4.2 Perbedaan pulp sebelum (kanan) dan sesudah (kiri) diputihkan
4.4 Sintesis Selulosa Diasetat dari Kulit Batang Pisang
Proses sintesis selulosa diasetat meliputi 3 tahap yaitu tahap
penggembungan, tahap asetilasi dan tahap hidrolisis. Tahap penggembungan
dimulai dari pulp kulit batang pisang yang telah diputihkan sebanyak 10 gram
ditambahkan asam asetat glasial 24 mL, dan diaduk menggunakan shaker pada
suhu 40ºC dalam waktu 1 jam. Asam asetat glasial di sini berperan sebagai
sweeling agent. Sweeling agent bertujuan untuk menggembungkan serat-serat
selulosa dan mereaktifkan selulosa agar dapat bereaksi dengan anhidrida asetat.
Setelah itu ditambahkan lagi campuran 60 mL asam asetat glasial dan 0,5 mL
H2SO4, kemudian diaduk lagi dengan shaker selama 45 menit pada suhu 400C
(Suryani, 2011). H2SO4 berperan sebagai katalis agar proses asetilasi berjalan
dengan cepat. Tahap asetilasi dimulai dari campuran yang didinginkan lalu
ditambahkan anhidrida asetat sebanyak 27 mL yang telah didinginkan pada suhu
180C dan diaduk selama 3 jam pada temperatur 400C. Anhidrida asetat berperan
sebagai sumber gugus asetil. Reaksi asetilasi berlangsung secara eksoterm
larutan dalam es balok. Pada tahap ini terjadi reaksi subtitusi antara gugus asetil
dari anhidrida asetat dengan gugus -OH pada selulosa, yang mengakibatkan
selulosa memiliki 3 gugus asetil disebut selulosa triasetat yang berbentuk larutan
coklat tua yang sangat kental. Tahap selanjutnya yaitu hidrolisis, dimana
ditambahkan asam asetat glasial 67% sebanyak 30 mL dilakukan tetes demi tetes
selama 3 jam pada temperatur 40ºC. Asam asetat glasial 67% berperan dalam
menghidrolisis gugus asetil pada selulosa triasetat sehingga menjadi selulosa
diasetat. Waktu hidrolisis pada penelitian ini yaitu 15 jam (Sofiana, 2011). Waktu
hidrolisis di sini harus diperhatikan, apabila terlalu lama maka berat molekul dari
selulosa diasetat yang dihasilkan sangat rendah. Setelah proses hidrolisis selesai,
larutan diendapkan dengan menambahkan akuades tetes demi tetes dan diaduk
hingga diperoleh endapan berbentuk serbuk berwarna putih. Endapan yang
terbentuk disaring dan dicuci dengan akuades sampai bebas dari asam, kemudian
dikeringkan pada oven dengan suhu 60-70ºC hingga kering. Endapan yang telah
kering kemudian dihaluskan dengan mortar hingga halus dan siap diuji
kelarutannya dalam aseton. Pada penelitian ini diperoleh massa selulosa diasetat
hasil sintesis sebesar 32,16 gram dengan rendemen 109,57%. Selulosa diasetat
hasil sintesis ditunjukkan pada Gambar 4.3
4.5 Hasil Karakterisasi Selulosa Diasetat
Karakterisasi selulosa diasetat meliputi 3 cara yaitu uji kelarutan dalam
aseton, penentuan berat molekul rata-rata dengan menggunakan viskometer
Ostwald dan analisis gugus fungsi menggunakan FT-IR.
4.5.1 Hasil uji kelarutan selulosa diasetat
Karakterisasi awal selulosa diasetat adalah uji kelarutan. Uji kelarutan
selulosa diasetat menggunakan aseton. Selulosa tidak larut dalam aseton
sedangkan selulosa diasetat larut dalam aseton karena struktur selulosa diasetat
yang amorf sehingga mudah larut dibandingkan struktur selulosa yang kristalin
sukar larut.
4.5.2 Hasil penentuan berat molekul rata-rata selulosa diasetat
Penentuan berat molekul rata-rata yang digunakan pada penelitian ini
adalah metode viskometri. Metode pengukuran ini merupakan metode yang paling
sederhana. Pengukuran dapat dilakukan dengan berbagai variasi konsentrasi
selulosa diasetat yang dibandingkan dengan pelarutnya yaitu aseton.
Setelah diperoleh data-data mengenai waktu alir berbagai variasi larutan
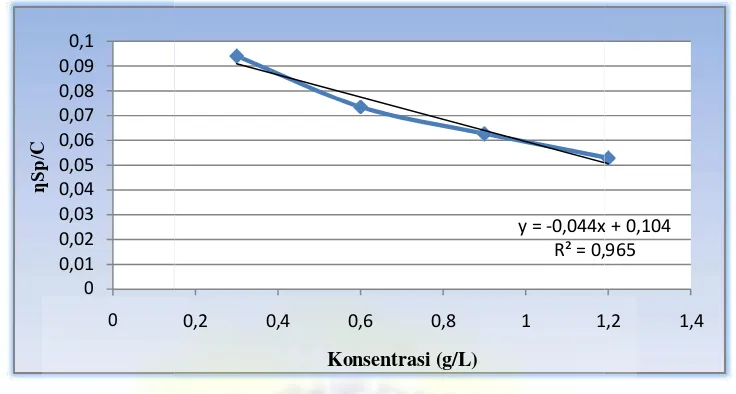
seperti pada Lampiran 3, kemudian dibuat grafik antara viskositas reduksi (ŋsp/C)
sebagai sumbu y dan konsentrasi larutan (C) sebagai sumbu x seperti yang
0,1
Gambar 4.4 Grafik penentuan berat molekul (Mv) selulosa diasetat
Grafik linier yang diperoleh memiliki persamaan regresi sebesar
y = -0.044x + 0.104. Dari nilai intersep tersebut dapat digunakan untuk
menghitung berat molekul rata-rata selulosa diasetat dengan menggunakan
persamaan Mark Houwink-Sakurada dengan nilai konstanta viskometri (K) dan
nilai a masing-masing yaitu 0,000133 L/g dan 0,616. Pada penelitian ini diperoleh
berat molekul rata-rata selulosa diasetat sebesar 49.742,03 g/mol sedangkan berat
molekul rata-rata selulosa diasetat standar sebesar 50.364,67 g/mol (Suryani,
2011)
ƞS
p/
4.5.3 Hasil FT-IR selulosa dan selulosa diasetat
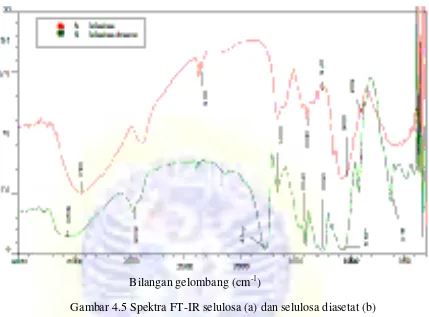
Spektra FT-IR selulosa dan selulosa diasetat ditunjukkan pada Gambar 4.5
unit glukopiranosida dan bilangan gelombang 894,97 cm-1 khas untuk piranosa.
Semua spektra tersebut menunjukkan gambaran gugus fungsi yang terdapat pada
molekul selulosa.
Spektra FT-IR selulosa diasetat menunjukkan bahwa puncak serapan unit
glukopiranosa pada bilangan gelombang 1049,28 cm-1 tetap muncul, begitu pula
dengan puncak serapan -OH yang muncul pada bilangan gelombang Bilangan gelombang (cm-1)
Gambar 4.5 Spektra FT-IR selulosa (a) dan selulosa diasetat (b)
Spektra FT-IR selulosa menunjukkan bahwa muncul puncak serapan pada
bilangan gelombang 3448,72 cm-1 yang menunjukkan adanya gugus fungsi -OH,
bilangan gelombang 1257,59 cm-1 menunjukkan adanya serapan ikatan C-O-C
3502,72 cm-1. Akan tetapi, puncak serapan gugus fungsi -OH pada spektrum
selulosa diasetat mempunyai intensitas yang lebih rendah dibandingkaan dengan
selulosa. Pada spektrum selulosa diasetat juga muncul serapan baru yaitu pada
bilangan gelombang 1751,36 cm-1 yang merupakan pita serapan gugus karbonil
ester. Terbentuk ester ini didukung dengan munculnya pita serapan pada daerah
bilangan gelombang 1234,44 cm-1 yang merupakan pita serapan yang khas C-O
ester dari asetat. Dengan adanya spektra baru ini, menunjukkan bahwa selulosa
telah terasetilasi menjadi selulosa diasetat.
4.6 Hasil Preparasi Serbuk Cangkang Rajungan
Preparasi serbuk cangkang rajungan diawali dengan mencuci cangkang
rajungan dengan air sampai bersih dari kotoran yang menempel lalu dimasak
dalam air mendidih selama 15 menit. Kemudian cangkang rajungan dikeringkan
di bawah sinar matahari. Pengeringan ini bertujuan agar cangkang rajungan lebih
mudah diblender. Setelah benar-benar kering, cangkang rajungan tersebut dipecah
menjadi bagian yang lebih kecil lalu dihaluskan dengan blender hingga halus
kemudian diayak dengan menggunakan saringan Mesh ukuran 50 µ m. Tujuan dari
memblender di sini adalah untuk meningkatkan luas permukaan sehingga dapat
mempermudah proses transformasi kitin ke kitosan. Pada penelitian ini diperoleh
serbuk cangkang rajungan berwarna coklat.
4.7 Hasil Proses Transformasi Kitin ke Kitosan dari Cangkang Rajungan
Proses transformasi kitin menjadi kitosan melalui beberapa tahap yaitu
deproteinasi, demineralisasi, depigmentasi dan deasetilasi. Tahap awal merupakan
cangkang rajungan dimasukkan ke dalam gelas beker dan ditambahkan larutan
NaOH 3,5% dengan perbandingan antara serbuk cangkang rajungan dengan
larutan NaOH 1:10 (w/v). Larutan NaOH yang digunakan pada tahap ini
berkonsentrasi rendah karena jika digunakan NaOH berkonsentrasi tinggi maka
cangkang rajungan akan mengalami deasetilasi. Proses ini dilakukan pada
temperatur 65oC dengan pengadukan selama + 2 jam (Ernasuryaningtyas, 2011).
Kemudian serbuk ini disaring lalu dicuci menggunakan akuades hingga pH air
cucian mencapai netral yang diuji dengan menggunakan kertas lakmus merah.
Setelah itu serbuk cangkang rajungan dikeringkan dalam oven pada suhu 65oC
sampai kering, dalam proses ini didapatkan crude kitin. Crude kitin yang
diperoleh pada penelitian kali ini sebesar 613 gram dari berat awal serbuk
cangkang rajungan sebesar 684 gram. Dapat dilihat bahwa terjadi pengurangan
massa sebesar 10,38% yang menandakan terjadinya pelepasan protein dari
cangkang rajungan atau yang disebut deproteinasi.
Tahap selanjutnya yaitu demineralisasi yaitu pemisahan mineral dari
cangkang rajungan. Crude kitin hasil deproteinasi dimasukkan ke dalam gelas
beaker lalu ditambahkan larutan HCl 2N dengan perbandingan antara kitin kasar
dan larutan HCl 1:15 (w/v). Reaksi yang terjadi adalah sebagai berikut:
CaCO3 (s) + 2HCl (aq) CaCl2 (aq) + H2O (l) + CO2 (g)
Ca3(PO4)2(s) + 4HCl(aq) 2CaCl2(aq) + Ca(H2PO4)2(l)
Penambahan larutan HCl 2N dilakukan tetes demi tetes secara hati-hati
dikarenakan adanya gelembung-gelembung gas CO2 apabila crude kitin ditetesi
basa sehingga bereaksi aktif dengan asam. Kemudian dilakukan pengadukan pada
suhu kamar selama 30 menit. Kemudian kitin kasar disaring dan ditiriskan. Kitin
kasar dicuci dengan akuades hingga pH air cucian mencapai netral yang diuji
dengan menggunakan kertas lakmus biru dan dikeringkan dalam oven pada suhu
80oC sampai kering sehingga diperoleh kitin (No et al, 2000). Kitin yang
diperoleh pada penelitian ini sebesar 91,8 gram dari 613 gram crude kitin. Dari
data tersebut dapat terlihat bahwa kandungan mineral dalam cangkang rajungan
sangat banyak sehingga terjadi penurunan massa yang sangat signifikan sebesar
85,1%.
Pada tahap depigmentasi yaitu tahap penghilangan warna, kitin hasil dari
proses demineralisasi lalu dihilangkan pigmennya dengan menggunakan aseton
dan diaduk terus selama 2 jam. Hasil perendaman dibilas dengan akuades hingga
netral lalu dikeringkan dalam oven pada suhu 1100C sampai kering. Tahap akhir
yaitu deasetilasi di mana terjadi transformasi gugus asetamida pada kitin menjadi
gugus amina pada kitosan melalui reaksi hidrolisis. Kitin hasil depigmentasi
dimasukkan ke dalam gelas beaker kemudian ditambahkan larutan NaOH 50%
dengan perbandingan antara kitin dan larutan NaOH 1:10 (w/v) (Kolodziesjska,
2000). Penggunaan NaOH dengan konsentrasi tinggi pada tahap ini dikarenakan
gugus asetil yang sulit lepas. Campuran tersebut direbus selama 2 jam pada 950C,
lalu disaring dan ditiriskan. Campuran dicuci dengan akuades hingga pH
mencapai netral yang diuji dengan menggunakan kertas lakmus merah dan
dikeringkan dalam oven pada suhu 65oC sampai kering hingga diperoleh kitosan.
(a)
kitin setelah proses depigmentasi sehingga terjadi pengurangan massa sebesar
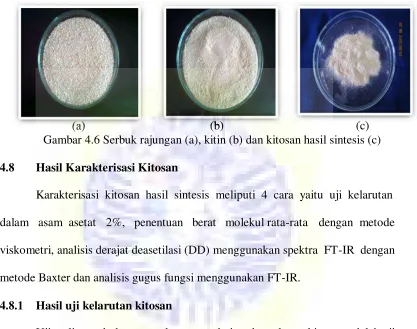
22,69%. Serbuk rajungan, kitin dan kitosan hasil sintesis ditunjukkan pada
Gambar 4.6
(b) (c)
Gambar 4.6 Serbuk rajungan (a), kitin (b) dan kitosan hasil sintesis (c)
4.8 Hasil Karakterisasi Kitosan
Karakterisasi kitosan hasil sintesis meliputi 4 cara yaitu uji kelarutan
dalam asam asetat 2%, penentuan berat molekul rata-rata dengan metode
viskometri, analisis derajat deasetilasi (DD) menggunakan spektra FT-IR dengan
metode Baxter dan analisis gugus fungsi menggunakan FT-IR.
4.8.1 Hasil uji kelarutan kitosan
Uji paling sederhana untuk mengetahui terbentuknya kitosan adalah uji
kelarutan. Uji kelarutan kitosan menggunakan asam asetat 2%. Kitosan larut
sempurna dalam asam asetat 2% sedangkan kitin tidak larut (Khor, 2001). Hal ini
disebabkan oleh pembentukan ikatan hidrogen antara N dari gugus amina pada
kitosan dengan H+ dari asam asetat.
4.8.2 Hasil uji penentuan berat molekul rata-rata kitosan
Penentuan berat molekul rata-rata kitosan dengan menentukan waktu alir
pada Lampiran 4, kemudian dibuat grafik antara viskositas reduksi (ŋsp/C)
Gambar 4.8 Grafik penentuan berat molekul (Mv) kitosan
Grafik linier yang diperoleh memiliki persamaan regresi sebesar
y = 392,3x + 8,183. Dari nilai intersep tersebut dapat digunakan untuk
menghitung berat molekul rata-rata kitosan dengan menggunakan persamaan
Mark Houwink-Sakurada dengan nilai k dan a masing-masing sebesar 1,4x10-4
dan 0,83. Pada penelitian ini diperoleh berat molekul rata-rata kitosan sebesar
553.495,22 Dalton. Nilai tersebut memenuhi rentang dari berat molekul rata-rata
kitosan komersil yaitu 100 kDa – 1200 kDa (Kim et al., 2004).
ƞsp
4.8.3 Hasil FT-IR kitin dan kitosan
Spektra FT-IR kitin dan kitosan ditunjukkan pada Gambar 4.8 dan 4.9
Berdasarkan Gambar 4.8 terlihat bahwa pada spektra FT-IR kitin muncul
puncak-puncak serapan pada bilangan gelombang 3448,72 cm-1 yang
menunjukkan vibrasi ulur –OH. Munculnya serapan pada bilangan gelombang
2931,80 cm-1 dan 2885,51 cm-1 yang masing-masing merupakan vibrasi ulur
simetri CH3 dan vibrasi ulur C-H, menunjukkan keberadaan gugus asetil
(Yanming et al., 2001). Serapan pada bilangan gelombang 1627,92 cm-1
menunjukkan pita amida I (ulur C=O) juga menandakan keberadaan gugus asetil.
Bilangan gelombang 1550,77 cm-1 merupakan serapan dari amida II (tekuk –NH)
dan 1381,03 cm-1 menunjukkan serapan amida III (ulur C-N) juga merupakan
bukti keberadaan gugus asetil.
Berdasarkan Gambar 4.9 pada spektra FT-IR kitosan, muncul puncak
serapan pada bilangan gelombang 3448,72 cm-1 (Velde dan Kiekens, 2004).
Melebarnya puncak serapan pada bilangan gelombang 3448,72 cm-1 menunjukkan
telah terjadinya proses deasetilasi. Puncak serapan pada bilangan gelombang
2924,09 cm-1 mempunyai intensitas lebih lemah daripada 2931,80 cm-1 pada
spektra FT-IR kitin, hal ini menunjukkan telah hilangnya sebagian gugus asetil
akibat proses deasetilasi dengan basa kuat konsentrasi tinggi. Adanya serapan
pada bilangan gelombang 1658,78 cm-1 yang merupakan serapan amina primer
ditandai dengan munculnya 2 puncak bersebelahan.
4.8.4 Hasil perhitungan derajat deasetilasi
Perhitungan derajat deasetilasi pada kitin dan kitosan dilakukan
menggunakan hasil analisa FT-IR dengan software DDK Project metode Baxter.
masing sebesar 43,54% dan 84,43%. Suatu molekul dikatakan kitin bila
mempunyai derajat deasetilasi (DD) kurang dari 70% dan dikatakan kitosan bila
derajat deasetilasi (DD) lebih dari 70% (Kim et al.,2001).
4.9 Hasil Pembuatan Membran Fotokatalitik Komposit Kitosan-Selulosa Diasetat-TiO2
Pembuatan membran komposit diawali dengan melarutkan selulosa
diasetat dengan variasi konsentrasi 2%, 4%, 6%, 8% dan 10% dalam aseton dan
masing-masing ditambahkan kitosan dengan konsentrasi 3% dalam asam asetat
2%. Kemudian campuran dituangkan ke dalam labu erlenmeyer bertutup lalu
ditambahkan formamida 8% (v/v) dan diaduk dengan magnetic stirer sampai
larutan homogen. Formamida berfungsi sebagai zat aditif. Larutan dope
didiamkan 1 malam untuk menghilangkan gelembung udara agar tidak terbentuk
pin hole pada saat dicetak. Larutan yang telah bebas dari gelembung udara dibuat
membran dengan metode inversi fasa.
Metode inversi fasa ini berdasarkan pada prinsip termodinamika, di mana
larutan dicetak dengan kondisi awal yang stabil, kemudian larutan ini mengalami
ketidakstabilan pada proses demixing (perubahan fasa). Langkah awal metode
inversi fasa ialah dengan menuangkan larutan dope sebanyak 5 mL di atas cawan
petri seperti ditunjukkan pada Gambar 4.4. Tujuan pencetakan membran pada
cawan petri untuk mempercepat dan mempermudah pengelupasan membran yang
akan dicetak, karena permukaan cawan petri lebih halus dibandingkan dengan plat
kaca. Kemudian untuk membentuk dan meratakan permukaan membran, cawan
yang telah dicetak kemudian dikeringkan dalam oven dengan suhu penguapan
800C untuk menghilangkan pelarut-pelarut yang terdapat di dalam campuran
membran.
Gambar 4.10 Larutan dope membran dalam cawan petri
Setelah membran kering, cawan petri dituangi dengan NaOH 4% sebagai
koagulan untuk membantu melepaskan membran dari cawan petri. Membran yang
diperoleh lalu dicuci dengan air mengalir untuk menghilangkan sisa-sisa pelarut.
Kemudian membran ditempatkan pada plastik mika dan dikeringkan di udara
terbuka. Hal ini bertujuan untuk meminimalisir mengerutnya membran setelah
kering. Membran yang telah kering lalu diuji sifat mekaniknnya dengan alat
autograph untuk mengetahui membran yang mempunyai komposisi selulosa
diasetat yang optimum. Setelah diperoleh komposisi selulosa diasetat yang
optimum, mengulangi prosedur diatas dengan menambahkan suspensi TiO2 dalam
metanol dengan variasi konsentrasi 0,1%, 0,15%, 0,2%, 0,25%, dan 0,3% ke
dalam larutan dope membran. Kemudian dilakukan uji mekanik dan kinerja
membran untuk mengetahui membran yang optimum dalam mengolah limbah zat
warna tekstil congo red. Membran komposit kitosan-selulosa diasetat-TiO2 hasil
Gambar 4.11 Membran kitosan-selulosa diasetat-TiO2
4.10 Hasil Karakterisasi Membran Kitosan dengan Variasi Konsentrasi Selulosa Diasetat
Karakterisasi terhadap membran kitosan dengan variasi konsentrasi
selulosa diasetat meliputi uji tarik menggunakan alat autograph untuk mengetahui
nilai stress agar diperoleh membran yang memiliki sifat mekanik kuat.
4.10.1 Hasil uji sifat mekanik membran kitosan dengan variasi konsentrasi selulosa diasetat
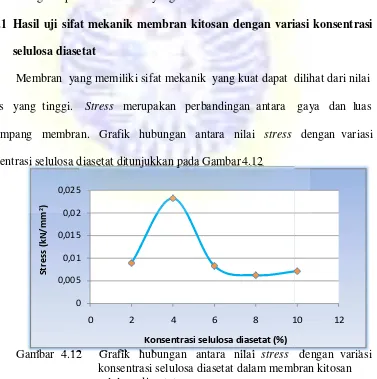
Membran yang memiliki sifat mekanik yang kuat dapat dilihat dari nilai
stress yang tinggi. Stress merupakan perbandingan antara gaya dan luas
penampang membran. Grafik hubungan antara nilai stress dengan variasi
konsentrasi selulosa diasetat ditunjukkan pada Gambar 4.12
Berdasarkan Gambar 4.12, membran kitosan yang memiliki nilai stress
tertinggi yaitu membran dengan konsentrasi selulosa diasetat 4%. Pada umumnya,
semakin banyak komposisi selulosa diasetat maka kekuatan mekaniknya rendah
karena selulosa diasetat berperan untuk memperbesar pori sehingga kekuatan dari
membran tersebut semakin menurun yang disebabkan oleh kurang rapatnya
strukur membran.
4.11 Hasil Karakterisasi Membran Kitosan-Selulosa Diasetat dengan Variasi Konsentrasi TiO2
Karakterisasi membran dilakukan untuk memperoleh membran yang
terbaik. Karakterisasi membran kitosan-selulosa diasetat-TiO2 meliputi uji
ketebalan dengan mikrometer sekrup, uji kekuatan mekanik membran, uji kinerja
membran berupa fluks dan rejeksi serta uji SEM untuk mengetahui morfologi
membran kitosan-selulosa diasetat-TiO2 dan FT-IR untuk mengetahui gugus-
gugus fungsi membran komposit yang optimum.
4.11.1 Hasil uji ketebalan membran kitosan-selulosa diasetat dengan variasi konsentrasi TiO2
Pengukuran ketebalan membran adalah indikator keseragaman dan
kontrol kualitas membran. Membran diukur dari sisi kanan, kiri, tengah, atas dan
bawah. Tebal membran diukur sebanyak 2 kali, menggunakan mikrometer sekrup
kemudian dihitung ketebalan rata-ratanya. Pengukuran ketebalan membran
dilakukan menggunakan mikrometer sekrup. Pada penelitian ini diperoleh
0,012
Gambar 4.13 Grafik hubungan antara ketebalan rata-rata membran dengan variasi konsentrasi TiO2 dalam membran
diasetat- TiO2
kitosan-selulosa
Ketebalan yang dihasilkan sama rata yaitu 0,01 mm. Membran yang baik
adalah membran yang tipis tapi kuat. Ketebalan membran akan berpengaruh pada
sifat permeabilitas karena semakin tebal membran, maka jarak yang akan
ditempuh umpan akan semakin panjang sehingga laju alir fluida umpan akan
semakin lama dan berpotensi memperbesar terjadinya fouling karena penumpukan
material umpan di atas permukaan membran (Baker, 2004).
4.11.2 Hasil uji sifat mekanik membran kitosan-selulosa diasetat dengan variasi konsentrasi TiO2
Karakterisasi sifat mekanik perlu dilakukan untuk mengetahui kekuatan
membran terhadap gaya. Uji sifat mekanik menggunakan alat autograph meliputi
nilai stress, strain, modulus young (Stevens, 2001). Stress adalah perbandingan
gaya dengan luas penampang membran. Grafik hubungan antara nilai stress
dengan variasi komposisi TiO2 dapat dilihat pada Gambar 4.14
0,025
Gambar 4.14 Grafik hubungan antara nilai stress konsentrasi TiO2 dalam membran
diasetat-TiO2
dengan variasi kitosan-selulosa
Berdasarkan data-data yang ditunjukkan pada Gambar 4.14, membran
yang memiliki sifat mekanik tertinggi adalah membran kitosan-selulosa diasetat
dengan konsentrasi TiO2 0,3% yang dapat dilihat dari nilai stress yang tinggi.
Dari data tersebut juga diperoleh bahwa semakin banyak komposisi TiO2 maka
semakin tinggi nilai stress. Hal ini disebabkan oleh struktur membran yang
semakin rapat sehingga kekuatan membran meningkat dan gaya yang diberikan
pada membran juga semakin besar.
Strain adalah perbandingan antara perubahan panjang membran setelah
diberi gaya dengan panjang mula-mula. Nilai strain membran menunjukkan
elastisitas membran. Grafik hubungan antara nilai strain dengan variasi komposisi
TiO2 ditunjukkan pada Gambar 4.15
0,2
Gambar 4.15 Grafik hubungan antara nilai strain konsentrasi TiO2 dalam membran
diasetat-TiO2
dengan variasi kitosan-selulosa
Berdasarkan Gambar 4.15, membran yang memiliki nilai strain tertinggi
yaitu membran kitosan-selulosa diasetat dengan konsentrasi TiO2 0,1%. Semakin
banyak komposisi TiO2, nilai strain juga semakin rendah. Hal ini disebabkan
karena dengan bertambahnya komposisi TiO2 akan menyebabkan struktur
membran semakin rapat sehingga elastisitasnya berkurang. Membran yang baik
adalah membran yang memiliki elastisitas rendah, karena apabila elastisitas suatu
membran besar maka dapat mengakibatkan pembesaran pada pori sehingga
selektifitas membran semakin kecil (Baker, 2004).
Modulus young adalah perbandingan nilai stress dan strain. Pada membran
kitosan-selulosa diasetat-TiO2, hubungan nilai modulus young
komposisi TiO2 dapat ditunjukkan pada Gambar 4.16
dengan variasi
S
tr
ai
0,45
Gambar 4.16 Grafik hubungan antara nilai modulus young dengan variasi konsentrasi TiO2 dalam membran
diasetat-TiO2
kitosan-selulosa
Berdasarkan Gambar 4.16, membran yang memiliki nilai modulus young
tertinggi yaitu membran kitosan-selulosa diasetat dengan konsentrasi TiO2 0,3%.
Nilai modulus young mengalami peningkatan sebanding dengan tingginya
konsentrasi TiO2. Semakin besar komposisi TiO2 maka nilai modulus young
semakin besar. Nilai
juga meningkat.
modulus young yang tinggi dipengaruhi nilai stress yang
4.11.3 Hasil uji kinerja membran kitosan-selulosa diasetat dengan variasi konsentrasi TiO2
Kinerja suatu membran sangat ditentukan oleh parameter utama berupa
nilai fluks dan rejeksi. Nilai fluks dan rejeksi membran ditentukan dengan
menggunakan alat sel filtrasi dead end dan spektrofotometer UV-Vis. Hubungan
antara fluks dengan variasi komposisi TiO2 ditunjukkan pada Gambar 4.17
1200
Gambar 4.17 Grafik hubungan antara nilai fluks dengan variasi konsentrasi TiO2 dalam membran kitosan-selulosa diasetat- TiO2
Berdasarkan Gambar 4.17, nilai fluks dipengaruhi oleh komposisi TiO2
dalam membran. Membran dengan komposisi TiO2 0,1%, 0,15% dan 0,2%
mengalami kenaikan fluks karena semakin besar konsentrasi TiO2 yang aktif
dalam membran maka semakin besar pula kemampuan TiO2 dalam mendegradasi
congo red menjadi struktur yang lebih kecil sehingga laju aliran umpan semakin
besar. Namun ketika konsentrasi TiO2 0,25% dan 0,3% nilai fluks mengalami
penurunan. Hal ini dikarenakan adanya proses filtrasi oleh membran. Proses
filtrasi ini menyebabkan membran menjadi berwarna merah dan terjadi
penumpukan solut pada pori-pori membran (fouling) sehingga menyebabkan
penyempitan yang menghalangi laju umpan (Baker, 2004).
Parameter kinerja membran yang kedua adalah rejeksi. Hubungan antara
rejeksi dengan variasi komposisi TiO2 ditunjukkan pada Gambar 4.18
100
Gambar 4.18 Grafik hubungan antara nilai rejeksi konsentrasi TiO2 dalam membran
diasetat- TiO2
dengan variasi kitosan-selulosa
Berdasarkan Gambar 4.18, membran yang memiliki nilai rejeksi tertinggi
yaitu dengan konsentrasi TiO2 0,3%. Nilai rejeksi meningkat sebanding dengan
meningkatnya konsentrasi TiO2. Semakin tinggi konsentrasi TiO2 maka semakin
rapat ukuran dan distribusi pori yang dihasilkan oleh membran sehingga
kemampuan membran dalam menahan umpan semakin besar.
Membran optimum adalah membran yang memiliki sifat mekanik yang
kuat ditandai dengan nilai stress yang tinggi, kinerja yang baik dilihat dari nilai
rejeksi tinggi dan fluks yang cukup tinggi pula. Berdasarkan penelitian yang telah
dilakukan, maka membran optimum adalah membran dengan komposisi kitosan
3%, selulosa diasetat 4% dan TiO2 0,3% dimana nilai stress yang diperoleh
sebesar 0,02250 kN/mm2, fluks 1061,54 L/m2 hari dan rejeksi 99,60%.
4.11.4 Hasil penentuan morfologi membran kitosan-selulosa diasetat-TiO2
Uji SEM bertujuan untuk mengetahui morfologi membran, distribusi dan
ukuran pori membran pada permukaan dan penampang melintang membran. Uji
ini dilakukan pada membran fotokatalitik dengan kondisi optimum yaitu dengan
konsnetrasi kitosan 3%, selulosa diasetat 4% dan TiO2 0,3%. Hasil penentuan
morfologi membran
Gambar 4.19
komposit kitosan-selulosa diasetat-TiO2 ditunjukkan pada
Gambar 4.19 Hasil SEM permukaan membran kitosan-selulosa diasetat-TiO2
Gambar 4.19 merupakan hasil SEM permukaan membran yang bertujuan
untuk mengetahui distribusi dan ukuran pori membran. Dari
diketahui bahwa membran ini memiliki pori dan persebaran
gambar tersebut
porinya cukup
merata. Pada gambar tersebut terlihat butiran-butiran putih TiO2 yang tidak larut
sempurna pada pembuatan larutan dope membran, hal ini dikarenakan TiO2 yang
4.11.5 Hasil analisis FT-IR membran kitosan-selulosa diasetat-TiO2
Spektra FT-IR membran kitosan-selulosa diasetat-TiO2 ditunjukkan pada
Gambar 4.20
Gambar 4.20 Spektra FTIR membran kitosan-selulosa diasetat (a) dan membran kitosan-selulosa diasetat-TiO2 (b)
Berdasarkan Gambar 4.20 dapat dilihat bahwa tidak terdapat banyak
perbedaan pita serapan yang muncul pada membran kitosan-selulosa diasetat dan
membran kitosan-selulosa diasetat-TiO2 terbukti masih terlihat pita serapan C-O
ester pada bilangan gelombang 1265,30 cm-1 ciri khas dari selulosa diasetat dan
pita serapan –NH pada bilangan gelombang 1635,64 cm-1 ciri khas dari kitosan.
Pada spektra FT-IR membran kitosan-selulosa diasetat-TiO2 tidak terlihat pita
serapan pada bilangan gelombang 509 cm-1 yang menunjukkan ikatan Ti-O pada
TiO2. Munculnya pita serapan pada spektra FT-IR membran kitosan-selulosa
ikatan kimia antara TiO2 dengan kitosan pada membran fotokatalitik ini yang
ditandai dengan perubahan gugus fungsi.
4.12 Hasil Penentuan Panjang Gelombang Maksimum Congo Red
Penentuan panjang gelombang maksimum dilakukan dengan mengukur
absorbansi dari larutan standar congo red 100 ppm menggunakan
spektrofotometer UV-Vis. Pada penelitian ini diperoleh panjang gelombang
maksimum dari larutan congo red sebesar 496 nm. Hasil penentuan panjang
geombang maksimum dari larutan congo red ditunjukkan pada Gambar 4.21
Gambar 4.21 Grafik panjang gelombang maksimum dari congo red
4.13 Hasil Pembuatan Kurva Standar Larutan Congo Red
Larutan standar congo red dengan konsentrasi 1, 20, 40, 60, 80, dan
100 ppm diukur absorbansinya dengan spektrofotometer UV-Vis pada panjang
gelombang maksimum 496 nm. Kemudian dibuat grafik linier dengan konsentrasi
sebagai sumbu x dan absorbansi sebagai sumbu y. Persamaan regresi yang
diperoleh sebesar y = 0,025x + 0,019. Kurva standar larutan congo red
TiO2 0,1%
TiO2 0,15%
TiO2 0,2%
TiO2 0,25%
TiO2 0,3%
Gambar 4.23 Grafik hubungan antara waktu penyinaran dengan absorbansi congo red
Berdasarkan grafik di atas dapat diketahui bahwa waktu optimum dalam
3
Gambar 4.22 Kurva standar larutan congo red
4.14 Hasil Pengaruh Variasi Waktu Kontak antara Membran Fotokatalitik dengan Lampu UV terhadap Konsentrasi Congo Red yang Tersisa
Menentukan waktu optimasi TiO2 dalam mendegradasi congo red
dilakukan dalam reaktor fotokatalitik dengan cara membran dari berbagai variasi
konsentrasi TiO2 dikontakkan dengan larutan congo red. Kemudian diukur
absorbansinya setiap variasi waktu yang telah ditentukan. Hubungan antara
waktuc penyinaran dengan absorbansi congo red ditunjukkan pada Gambar 4.23
absorbansi congo red yang paling signifikan. Semakin lama waktu penyinaran
maka absorbansi dari larutan congo red semakin menurun. Menurunnya
absorbansi menandakan konsentrasi congo red sisa juga menurun. Hal ini
disebabkan oleh semakin lamanya waktu kontak antara TiO2 dalam membran
dengan sinar UV dalam reaktor sehingga kemampuan TiO2 semakin aktif dalam
mendegradasi congo red.
4.15 Hasil Aplikasi Membran Kitosan-Selulosa Diasetat-TiO2 untuk Pengolahan Limbah Zat Warna Tekstil Congo Red
Aplikasi membran kitosan-selulosa diasetat-TiO2 untuk pengolahan limbah
zat warna tekstil congo red ditentukan dari nilai fluks dan rejeksi. Limbah tekstil
congo red yang digunakan berwarna biru hal ini dikarenakan kondisi larutan
limbah tekstil bersuasana asam. Perlakuan awal adalah menyaring limbah tekstil
dengan kertas saring What mann ukuran 42. Kemudian mengukur absorbansinya
dengan spektrofotometer UV-Vis, namun karena konsentrasinya terlalu pekat
sehingga dilakukan pengenceran 100 kali, diperoleh absorbansi sebesar 1,094
dengan konsentrasi sebesar 4300 ppm. Selanjutnya, limbah tekstil dikontakkan
dengan membran dalam reaktor fotokatalitik selama 3 jam lalu diukur
absorbansinya, sehingga didapat absorbansi sebesar 0,528 dengan konsentrasi
sebesar 2036 ppm maka diperoleh % degradasi sebesar 52,65%. Kemudian
dilanjutkan dengan proses dead end yang menghasilkan nilai fluks dan % rejeksi
masing-masing sebesar 715,529 L/m2.hari dan 92,19 %. Nilai rejeksi dan fluks
yang dihasilkan dari pengolahan limbah zat warna tekstil congo red lebih rendah
100 ppm dengan fluks 1061,540 L/m2 hari dan rejeksi 99,60%. Hal ini disebabkan
oleh terlalu banyaknya komponen yang terkandung dalam limbah tekstil tersebut
sehingga dapat mengganggu kinerja dari membran yang seharusnya spesifik
terhadap zat tertentu. Proses pengolahan limbah tekstil congo red terjadi karena
kemampuan membran dalam memfiltrasi limbah zat warna tekstil dan adanya
atom Ti pada TiO2 yang berikatan dengan atom N pada kitosan membentuk
senyawa kompleks yang mampu mendegradasi zat warna dengan pembentukan
radikal hidroksil yang merupakan oksidator kuat (Lodha et al., 2008). Mekanisme
pembentukan radikal hidroksil oleh senyawa kompleks [Ti-N kitosan] sebagai
berikut:
[Ti-N kitosan] n+1 hv [Ti-N kitosan] (n+1)
+
Perbandingan nilai fluks dan rejeksi sampel congo red murni dan limbah tekstil
ditunjukkan seperti Gambar 4.24 dan 4.25
(a (b (c
Hasil pengolahan sampel congo red murni ditunjukkan pada Gambar 4.26
Gambar 4.26 Congo red awal (a), Congo red setelah didegradasi dalam reaktor fotokatalitik (b), dan Congo red setelah difiltrasi dengan membran kitosan-selulosa diasetat-TiO2 (c)
Hasil pengolahan sampel limbah tekstil congo red ditunjukkan pada Gambar 4.27
Gambar 4.27 Limbah tekstil congo red awal (a), limbah tekstil congo red setelah didegradasi dalam reaktor fotokatalitik (b), dan limbah tekstil congo red setelah difiltrasi dengan membran kitosan-selulosa diasetat-TiO2 (c)