BAB III
METODE PENELITIAN
3.1 Lokasi Penelitian
Lokasi penelitian dilaksanakan di Laboratorium Penelitian Terpadu Fakultas Farmasi Universitas Sumatera Utara, Medan-Sumatera Utara dengan sampel yang diperoleh dari air limbah sintetik, larutan ion NO3 dan NO2 disediakan dengan melarutkan jumlah garam NaNO3 dan NaNO2 masing-masing ±100 mg pada air suling dengan volume 75-100 mL.
3.2 Waktu Penelitian
Waktu penelitian dilakukan selama 2 bulan, yaitu mulai bulan Desember - Januari 2016 yang dilanjutkan dengan pengolahan dan penyusunan data serta penyusunan laporan.
3.3 Jenis Penelitian
Penelitian ini termasuk dalam jenis penelitian yang bersifat eksperimental yang dilaksanakan dalam skala laboratorium dengan metode penelitian secara kuantitatif.
3.4 Variabel Penelitian
Variabel penelitian yang digunakan dalam penelitian ini meliputi : 1. Variabel bebas (independent variable) meliputi :
Pengolahan limbah cair untuk proses pertukaran ion dengan variasi dosis resin anion: 0,2; 0,4; 0,6; 0,8; 1,0 dan 1,2 gram dan variasi waktu kontak 10, 20, 40, 80, 160 dan 320 menit
2. Variabel Terikat (dependent variable) meliputi :
Kandungan nitrat dan nitrit yang berasal dari limbah cair sintetik. 3.5 Kerangka Penelitian
Adapun kerangka penelitian untuk tugas akhir ini dapat dilihat dalam bentuk diagram alir penelitian pada Gambar 3.1.
III-2
Gambar 3.1 Diagram Alir PenelitianPerancangan Kolom Reaktor Batch
Pengolahan dan Analisa Data serta Pembahasan
Kesimpulan dan Saran
Selesai Perumusan Masalah
Penentuan Metode Penelitian
Pengujian Perbandingan Resin Anion yaitu
unmodified resin dan
modified resin Data Primer
Studi
Pembuatan Sampel Air Limbah
Metode Impregnasi
Pengujian SEM
Pengujian EDS
Perlakuan Variasi Dosis Resin
Perlakuan Variasi Waktu Kontak
Pengujian Sampel Efluen (Nitrat dan Nitrit)
Mulai
Proses Penelitian
Desain Peralatan 1. Persiapan alat dan bahan 2. Desain dimensi reaktor
Pengumpulan Alat dan Bahan
III-3
3.6 Pengumpulan DataData yang dikumpulkan meliputi : a. Data Primer
Data primer merupakan data yang diperoleh dari hasil analisa penelitian di laboratorium ataupun penelitian di lapangan secara langsung mulai dari pengujian awal sampai pengujian akhir
b. Data Sekunder
Data sekunder merupakan data yang diperoleh dari studi literatur pustaka.
3.7 Alat dan Bahan 3.7.1 Alat 1. Labu erlenmeyer 1000 ml 2. Stirrer elektromagnetik 3. pH meter 4. Jerigen 5 L 5. Corong 6. Oven
7. Neraca analitik digital 8. Seperangkat alat gelas 9. Desikator
10. Scanning electron microscope
11. Energy dispersion spectrometry
12. Spektrofotometer UV-Vis
3.7.2 Bahan
1. Resin anion Purolite A400 sebanyak ± 1 kg.
2. Tembaga-modifikasi resin anion Purolite A400 sebanyak ± 1 kg. 3. Air limbah sintetik dari larutan garam NaNO3 dan NaNO2. 4. Akuades
5. Larutan CuCl2.2H2O 6. Larutan NaOH
7. Bahan kimia yang digunakan untuk pengujian parameter nitrat dan nitrit diperoleh di laboratorium.
III-4
3.8 Langkah Penelitian3.8.1 Tahap Persiapan
Tahapan awal persiapan dari penelitian ini adalah pembuatan sampel dari air limbah sintetik dengan larutan garam NaNO3 dan NaNO2 untuk menghasilkan ion NO3 dan NO2. Untuk pengujian awal, pengambilan sampel air limbah yang telah dilakukan dimasukkan kedalam jerigen melalui corong. Berikutnya jerigen diisi penuh dan dibawa untuk dilakukan penelitian.
3.8.2 Reaktor Penelitian
Desain Reaktor
Dalam penelitian ini akan digunakan reaktor yang terdiri dari sebagai berikut : Reaktor Batch
Sebagai tempat penampungan limbah yang masuk (influent) kedalam labu erlenmeyer (Gambar 3.2) untuk mengetahui variabel kinetika adsorpsi dan isotherm kesetimbangan.
Gambar 3.2. Reaktor batch
3.8.3 Proses Penelitian
1.Tahap Persiapan dan Pemeriksaan
Tahapan pengoperasian alat dimulai dengan pemeriksaan bahwa semua rangkaian reaktor telah tersusun dengan baik dan benar sebelum memulai proses pengolahan.
2. Impregnasi Resin Purolite A400 - Cu
Air limbah sintetik yang telah diambil dimasukkan kedalam jerigen sebanyak ±10 L untuk dilakukan tahapan 1 metode impregnasi, resin Purolite A400 dimodifikasi dengan tembaga (Purolite-Cu) dengan 10 g resin Purolite dimasukkan kedalam 1 L larutan CuCl2.2H2O (Yang
III-5
dkk., 2015) selama 1 jam dan diaduk dengan kecepatan 120 rpm (Kalaruban dkk, 2015 dalam Sengupta dan Pandit, 2011). Penambahan larutan 1 M NaOH untuk meningkatkan nilai pH menjadi 8,0 dan didiamkan selama 3 jam. Kecepatan pengadukan dikurangi hingga 30 rpm dan suspensi didiamkan selama 24 jam. Kemudian resin disaring dan dicuci dengan air deionisasi, lalu dikeringkan dengan oven pada suhu 45°C selama 24 jam (Kalaruban dkk., 2015).Analisa Purolite kering dan Purolite-Cu menggunakan suatu alat yaitu scanning electron microscope (SEM) yang bertujuan untuk mengetahui struktur morfologi dari perbandingan resin tersebut dan energy dispersion spectrometry (EDS) yang berfungsi dalam menentukan komposisi suatu unsur dari perbandingan resin yang digunakan (Kalaruban dkk., 2015; Sowmya dan Meenakshi, 2013).
3. Proses Reaktor Batch
Setelah diperoleh resin Purolite-Cu kering berikutnya air limbah dilakukan dengan reaktor
batch, perlakuan percobaan ada 2, antara lain : a. Kinetika adsorpsi
10 g resin dimasukkan kedalam labu erlenmeyer yang berisi 100 mL air limbah yang mengandung nitrat (50 mg N/L) tersebut (konsentrasi awal nitrat diuji terlebih dahulu), suspensi yang telah terbentuk diaduk dengan stirrer elektromagnetik pada kecepatan 120 rpm selama 5 jam pada suhu ruangan (24 ± 1 °C).
Sampel diambil pada interval waktu yang berbeda (10, 20, 40, 80, 160 dan 320 menit) dengan volume sampel efluen 30-50 ml. Dan konsentrasi nitrat akhir dilakukan pengujian dengan metode spektrofotometer UV-Vis dan menghitung jumlah adsorpsi nitrat pada waktu t. Begitu juga untuk pengujian nitrit berikutnya dengan konsentrasi 20 mg N/L.
b. Isotherm adsorpsi kesetimbangan
100 mL air limbah yang mengandung nitrat (konsentrasi awal nitrat diuji terlebih dahulu, 50 mg N/L) pada labu erlenmeyer, kemudian ditambahkan beberapa dosis adsorben dengan interval dosis yang berbeda (0,2; 0,4; 0,6; 0,8; 1,0 dan 1,2 gram) pada suhu ruangan (24 ± 1°C). Suspensi yang telah terbentuk diaduk dengan stirrer elektromagnetik pada kecepatan 120 rpm selama 24 jam untuk mencapai kesetimbangan adsorpsi dan volume sampel efluen yang akan dilakukan pengujian 30-50 ml. Konsentrasi nitrat akhir dilakukan pengujian dengan metode spektrofotometer UV-Vis dan dihitung jumlah adsorpsi nitrat pada pada saat kesetimbangan qe. Begitu juga untuk pengujian nitrit berikutnya dengan konsentrasi 20 mg N/L.
III-6
3.8.4 Pengujian SampelDalam penelitian ini prinsip pengukuran Nitrat dan Nitrit mengacu pada metode Spektrofotometer UV-Vis DR5000.
3.8.5 Analisa Data
Data hasil percobaan akan disajikan dalam bentuk tabel dan grafik dengan pemodelan persamaan pada reaktor batch yang digunakan yaitu persamaan Orde Semu Pertama, persamaan Orde Semu Kedua dan Model Difusi Permukaan Homogen (untuk kinetika adsorpsi), persamaan Langmuir dan persamaan Freundlich (untuk isotherm adsorpsi kesetimbangan).
Data yang diperoleh akan menunjukkan nilai yang paling optimal tentang perubahan konsentrasi nitrat dan nitrit. Untuk mengetahui efisiensi penurunan kadar Nitrat dan Nitrit pada sampel air limbah, maka dalam penelitian ini dapat dihitung efisiensinya dengan membandingkan influen dan efluen yang dinyatakan dalam persen (%) seperti rumus berikut :
Perhitungan efisiensi :
%
100
x
C1
C
-C
E
1 2 (3.1) dimana : E = EfisiensiC1 = Konsentrasi Nitrat atau Nitrit sebelum treatment
BAB IV
HASIL DAN PEMBAHASAN
4.1. Hasil Scanning electron microscope (SEM), Energy Dispersion Spectrometry (EDS) Permukaan Resin Purolite A400 & Purolite A400-Cu
Identifikasi keberadaan Cu2+ pada resin Purolite A 400 dapat dilihat dari morfologi permukaan Purolite A400-Cu yang diperoleh dengan uji Scanning electron microscope (SEM) ditunjukkan pada Gambar 4.1, dapat dilihat bahwa terdapat perubahan permukaan resin. Pada Gambar 4.1 (a) dan Gambar 4.2 (a), morfologi permukaan resin Purolite A400 murni menunjukkan struktur permukaan resin yang halus. Sedangkan hasil foto SEM pada Gambar 4.1 (b) resin Purolite A400 yang diimpregnasi dengan logam Cu terlihat partikel-partikel yang melekat pada permukaan resin dan Gambar 4.2 (b) menunjukkan permukaan resin yang kasar, ini dapat diartikan sebagai adanya Cu yang telah berikatan pada permukaan adsorben. Sedangkan untuk hasil analisa EDS yang ditunjukkan pada gambar 4.3, diperoleh perbedaan kandungan unsur Cu, yaitu pada resin Purolite A400 yang telah diimpregnasi sebesar 24,20%, hal ini semakin membuktikan bahwa ion Cu2+ telah berikatan pada permukaan resin. Penambahan logam dapat meningkatkan area permukaan dan volume pori adsorben yang juga meningkatkan kapasitas adsorpsi adorbat (Loganathan.2013). Komponen Klorida (Cl) juga meningkat setelah proses impregnasi dari 7,77% menjadi 9,67%, hal ini membuat resin semakin baik karena komponen Cl merupakan anion pertukaran ion utama (Purolite., 2017). Dari Gambar 4.3 (b) dibawah diperoleh kandungan unsur Cu pada Purolite A 400 yang telah dimpregnasi Cu2+, membuktikan bahwa ion Cu2+ telah berikatan dengan resin Purolite A 400.
(a) (b) Gambar 4.1. Uji SEM pembesaran 100 µm pada (a)Purolite A400 (b)Purolite A400-Cu
IV - 2
(a) (b)
Gambar 4.2. Uji SEM pemebesaran 5.000 µm pada (c) Purolite A400 (d) Purolite A400-Cu
(a)
(b)
IV - 3 4.2 Pengaruh Waktu Kontak Terhadap Adsorpsi Ion Nitrat Dan Nitrit
Waktu kontak merupakan salah satu parameter yang penting pada proses adsorpsi karena berkaitan dengan laju reaksi yang dinyatakan sebagai perubahan konsentrasi terhadap waktu. Penentuan waktu kontak digunakan untuk mendapat waktu pengadukan optimum selama proses batch sehingga diketahui batas maksimal adsorpsi terhadap adsorbat. Pada penelitian ini, variasi waktu kontak yang dilakukan menunjukkan waktu yang dibutuhkan sehingga kesetimbangan adsorpsi tercapai dan mengetahui maksimal resin Purolite A 400 dan Purolite A 400 – Cu dalam menyerap ion nitrat dan nitrit. Variasi waktu kontak yang dilakukan antara adsorben dan adsorbat pada variasi 10, 20, 40, 80, 160, dan 320 menit.
4.2.1 Pengaruh Waktu Kontak Terhadap Adsorpsi Ion Nitrat
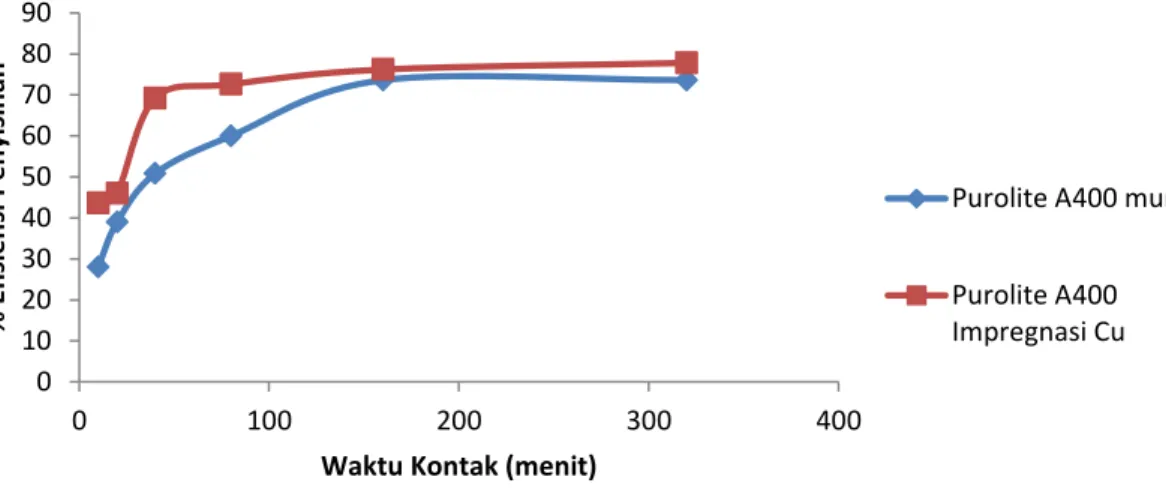
Pada uji adsorpsi nitrat dengan konsentrasi awal nitrat 50 mg/l, hasil pengaruh waktu terhadap adsorpsi nitrat pada resin Purolite A 400 murni dan Purolite A400 impregnasi Cu dapat dilihat pada gambar 4.4. Adsorpsi nitrat dengan menggunakan resin murni, pada 10 menit pertama diperoleh efisiensi penyisihan adsorpsi sebesar 28%, kapasitas adsorpsi 1,4 mg/g, dan pada menit ke-20 efisiensi meningkat secara signifikan (efisiensi penyisihan 39%, kapasitas adsorpsi 1,95 mg/g) dan terus mengalami kenaikan mencapai menit ke 160 dengan efisiensi penyisihan 76,2 %, kapasitas adsorpsi 3,81mg/g. Namun setelah menit ke-160 menuju menit ke-360, efisiensi penyisihan nitrat tidak mengalami perubahan sama sekali.
Berbeda dengan resin Purolite A400 murni, Purolite A400 impregnasi Cu tidak mengalami perubahan yang terlalu signifikan pada menit ke-10 hingga menit ke-20, yaitu dengan efisiensi penyisihan dari 43,6%, kapasitas adsorpsi 2,18 mg/g menjadi efisiensi penyisihan 46%, kapasitas adsorpsi 2,3 mg/g. Namun, seiring dengan pertambahan waktu kontak pada menit ke-40 hingga menit ke-80 terjadi peningkatan efisiensi adsorpsi (69,2% dan 72,6%) dan kapasitas adsorpsi (3,46 mg/g dan 3,63 mg/g). Setelah menit ke-80 perubahan kenaikan efisiensi penyisihan tidak terlalu signifikan, hanya mencapai 76,2 % dengan kapasitas adsorpsi 3,81 mg/g pada menit ke 160 dan 77,8% dengan kapasitas adsorpsi 3,89 mg/g pada menit ke-360 menit.
Hasil analisa diatas, didapatkan bahwa semakin meningkatnya waktu kontak antara adsorben resin dengan ion nitrat, maka efisiensi penyisihan ion nitrat dan kapasitas adsorpsi semakin besar. Peningkatan kapasitas adsorpsi ini terjadi karena jumlah sisi aktif (Said, A., et al. 2014) yang tersedia pada permukaan adsorben masih banyak yang belum terisi atau kondisinya belum jenuh (Ravancic, M., et al. 2015), sehingga memudahkan interaksi antara ion nitrat dengan permukaan adsorban. Semakin lama waktu interaksi adsorben dengan adsorbat memungkinkan terjadinya banyaknya tumbukan yang terjadi (Said, H et all. 2014), maka semakin banyak adsorbat yang teradsorpsi (Muna., 2011). Peneliti Mahmoud El Quardi, et all (2015) menyatakan proses adsorpsi terjadi dalam dua fase
IV - 4 yaitu fase cepat yang terjadi pada saat adsorpsi permulaan dan fase kedua perlahan adsorpsi ion nitrat melambat seiring dengan pertambahan waktu hingga mencapai kesetimbangan. Didapatkan bahwa waktu kontak optimal pada resin Purolite A400 murni adalah pada menit ke-160 dan menit ke-80 pada resin Purolite impregnasi Cu. Pada waktu tersebut adsorben dianggap telah mengalami kesetimbangan, karena tidak ada perubahan yang signifikan terhadap efisiensi penyisihan dan kapasitas adsorpsi setelah waktu optimal. Ini terjadi karena, dengan bertambahnya waktu kontak yang lebih lama, maka sisi aktif pada adsorben hampir terisi penuh atau sudah terisi penuh (Hidayati, dkk. 2013).
Gambar 4.4 Pengaruh Waktu Kontak Terhadap Efisiensi Adsorpsi Ion Nitrat dengan Konsentrasi Awal 50 mg/l
Pada Gambar 4.4 juga menunjukkan perbandingan efisiensi adsorpsi antara kedua adsorben, didapatkan bahwa efisiensi penyisihan dan kapasitas adsorpsi ion nitrat pada resin Purolite A400 impregnasi Cu lebih besar dari resin Purolite A400 murni, hal ini membuktikan bahwa dengan adanya impregnasi, efisiensi penyisihan nitrat lebih besar. Kapasitas adsorpsi dapat meningkat dengan impregnasi logam karena adanya peningkatan pertukaran ion positif pada permukaan adsorben, kenaikan muatan positif ini akan meningkatan adsorpsi muatan ion negatif seperti nitrat dengan daya tarik elektrostatik (Kalaruban, M., et al. 2016).
4.2.2 Pengaruh Waktu Kontak Terhadap Adsorpsi Ion Nitrit
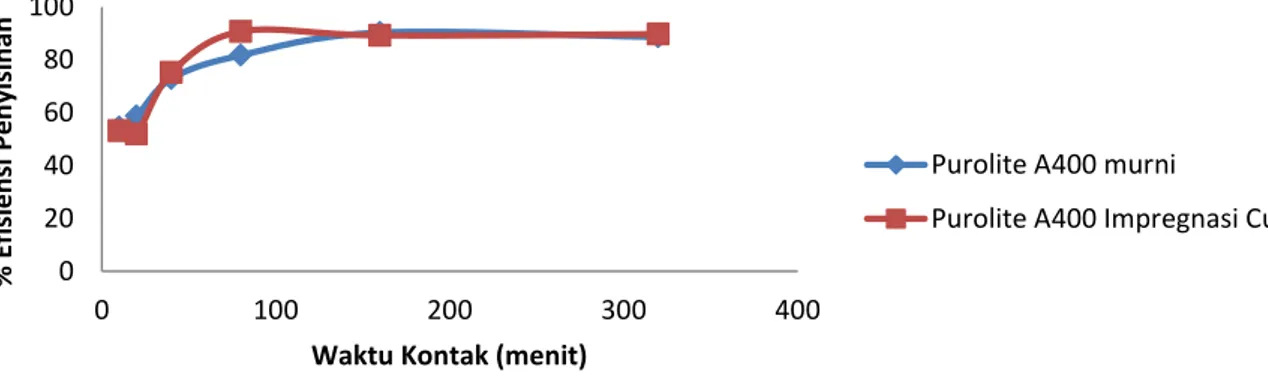
Hasil pengaruh waktu kontak terhadap adsorpsi nitrit dengan konsentrasi awal 10 mg/l dapat dilihat pada Gambar 4.5. Berdasarkan gambar tersebut resin Purolite A400 murni, pada 10 menit pertama uji diperoleh efisiensi adsorpsi ion nitrit sebesar 54,5% dan kapasitas adsorpsi 0,545 mg/g kemudian pada menit ke-20 mengalami kenaikan efisiensi adsorpsi hingga 58,75%, 05875 mg/g untuk kapasitas adsorpsi, begitu juga pada menit ke-40 hingga menit ke-160, yang mencapai efisiensi penyisihan 90,25% dan kapasitas adsorpsi 0,9025. Namun selanjutnya, setelah menit 160 yaitu pada menit ke-320 mengalami penurunan efisiensi penyisihan dan kapasitas adsorpsi menjadi 88,55% dan 1,145 mg/g. 0 10 20 30 40 50 60 70 80 90 0 100 200 300 400 % E fi si e n si Pen yi si h an
Waktu Kontak (menit)
Purolite A400 murni
Purolite A400 Impregnasi Cu
IV - 5 Begitu juga dengan adsorpsi nitrit pada resin purolite A400 impregnasi Cu, didapatkan pada menit ke-10 efisiensi penyisihan 51,95% dan kapasitas adsorpsi 0,5195 mg/g, pada menit ke-20 53,15% dan 0,5315 mg/g, dan terus mengalami kenaikan hingga menit ke-80 dengan efisiensi penyisihan 90,65 dan kapasitas adsorpsi 0,9065 mg/g. Namun, pada menit ke 160 mengalami penurunan efisiensi penyisihan dan kapasitas adsorpsi menjadi 89,15% dan 0,8915 mg/g, kemudian mengalami kenaikan lagi, namun kenaikan kecil mencapai 89,65% dan 0,8965 mg/g.
Hasil analisa diatas, bahwa pada resin Purolite A400 murni didapatkan waktu optimal untuk proses adsorpsi yaitu pada menit ke-160 dan pada resin Purolite A400 impregnasi Cu menit ke-80 karena setelah waktu optimal tersebut, kedua adsorben mengalami penurunan efisiensi adsorpsi dan kapasitas adsorpsi, maka diasumsikan telah mencapai kesetimbangan.
Penurunan persen efisiensi adsorpsi nitrit ini menunjukkan bahwa resin telah mengalami desorpsi (Irmanto 2009), hal ini terjadi karena pori-pori pada adsorben telah jenuh atau telah tertutup oleh adsorbat (Amin, dkk. 2016) dan ketidakmampuan molekul-molekul adsorbat berikatan dengan sisi aktif adsorben (Anjani, dkk., 2014) sehingga adsorben tidak mampu lagi menyerap adsorbat. Dan jika pengadukan diperpanjang, maka adsorben yang telah menyerap ion nitrit akan melepas kembali dalam larutan dimana adsorben memiliki daya serap maksimum dalam menyerap ion nitrit.
Analisa diatas juga menunjukkan bahwa kedua adsorben yaitu resin Purolite A400 murni dan resin Purolite A400 impregnasi Cu, memiliki perbandingan waktu kontak optimum sangat besar yaitu 80 menit untuk resin yang telah diimpregnasi dan 160 menit utuk resin murni. Resin yang telah diimpregnasi lebih cepat mengalami kesetimbangan. Namun jika ditinjau dari efisiensi penyisihan dan kapasitas adsorpsi, hanya memiliki sedikit perbedaan, hal ini karena adanya penyisipan logam Cu pada permukaan resin. Purolite A400 impregnasi Cu memiliki efisiensi penyisihan lebih besar 0,40% dalam penyisihan nitrit, namun resin murni juga telah cukup bagus dalam penyisihan. Hal ini disebabkan karena ion nitrit yang bersifat tidak stabil, artinya nitrit sangat mudah teroksidasi menjadi nitrat.
Gambar 4.5 Pengaruh Waktu Kontak Terhadap Efisiensi Adsorpsi Ion Nitrit dengan Konsentrasi Awal 10 mg/l 0 20 40 60 80 100 0 100 200 300 400 % E fi si e n si Pen yi si h an
Waktu Kontak (menit)
Purolite A400 murni Purolite A400 Impregnasi Cu
IV - 6 4.3 Pengaruh Dosis Resin Terhadap Adsorpsi Ion Nitrat Dan Nitrit
Variasi dosis adsorben resin yang ditambahkan pada larutan nitrat maupun nirit menghasilkan efisiensi adsorpsi ion nitrat dan nitrit yang berbeda-beda sesuai dengan kapasitas adsorpsi dari adsorben yang digunakan. Penentuan dosis optimum adsorben penting untuk diuji, hal ini bertujuan untuk memperoleh jumlah optimum resin Purolite A400 impregnasi Cu untuk adsorpsi ion nitrat dan nitrit, yang dilakukan pada variasi 0,1; 0,2; 0,4; 0,6; 0,8; 1,0 dan 1,2 gram, dengan waktu kontak yang setimbang (perlakuan sebelumnya) dalam 100 ml larutan nitrat (konsentrasi 50 mg/l) dan nitrit (konsentrasi 10 mg/l).
4.3.1 Pengaruh Dosis Resin Terhadap Adsorpsi Ion Nitrat
Pengaruh dosis adsorben resin Purolite A400 murni dan resin purolite A400 impregnasi Cu, dilakukan pada variasi 0,1 sampai 1,2 gram dengan waktu kontak masing-masing 160 menit dan 80 menit. Dari hasil pengujian yang terdapat pada Gambar 4.6, resin Purolite A400 murni dengan dosis resin 0,2 gram didapatkan efisiensi penyisihannya nitrat sebesar 15%, pada dosis resin 0,4 gram menjadi 30%, selanjutnya dosis resin 0,6 gram didapatkan efisiensi penyisihan 46%, pada dosis resin 0,8 menjadi 57%, selanjutnya dosis resin 1 mencapai 74%, dan pada dosis resin 1,2 menjadi 75,2 %. Rentang antara dosis adsorben 0,2 gram hingga dosis resin 1,0 gram terdapat perubahan efisiensi penyisihan yang signifikan, sedangkan pada dosis resin 1,0 gram hingga 1,2 gram, kenaikan efisiensi penyisihan tidak terlalu signifikan. Maka diperoleh dosis resin 1,0 gram merupakan dosis resin optimal untuk resin murni.
Pada resin Purolite A400 impregnasi Cu, pada dosis resin 0,2 efisiensi penyisihan nitrat adalah 39%, dosis resin 0,4 gram sebesar 51,6%, dosis resin 0,6 gram sebesar 65,6%, dosis resin 0,8 gram sebesar 69,6%, selanjutnya dosis resin 1,0 gram sebesar 77,6 dan dosis resin 1,2 gram menjadi 78%. Sama halnya dengan resin Purolite murni, terdapat peningkatan yang signifikan antara rentang dosis resin 0,2 gram hingga 1,0 gram dan kemudian menurun pada dosis resin 1,2 gram, sehingga dosis resin 1,0 gram menjadi dosis resin optimal pada proses adsorpsi.
Peningkatan efisiensi adsorpsi terjadi karena semakin besar dosis adsorben, maka semakin banyak luas permukaan adsorben yang tersedia (Teka, T., 2014; Dehghani, M, et all., 2015; Ertugay, N and Malkoc, E., 2014) yang membuka situs adsorpsi yang lebih aktif untuk mengikat ion nitrat (Azouaou., 2013). Peningkatan efisiensi penyisihan oleh meningkatnya dosis adsorben disebabkan oleh pembentukan kompleks antara adsorben dan adsorbat telah optimum (Dehghani, M, et all., 2015). Gambar 4.6. juga menunjukkan pada dosis adsorben yang sama yaitu 1 gram, resin Purolite A400-Cu mempunyai efisiensi penyisihan adsorpsi nitrat lebih besar, ini disebabkan oleh semakin luas daya adsorpsi permukaan adsorben yang telah diimpregnasi karena adanya penambahan ion positif Cu yang mampu menarik ion nitrat.
IV - 7 Gambar 4.6 Pengaruh Dosis Adsorben Terhadap Efisiensi Adsorpsi Ion Nitrat dengan Konsentrasi
Awal 50 mg/l
4.3.2 Pengaruh Dosis Resin Terhadap Adsorpsi Ion Nitrit
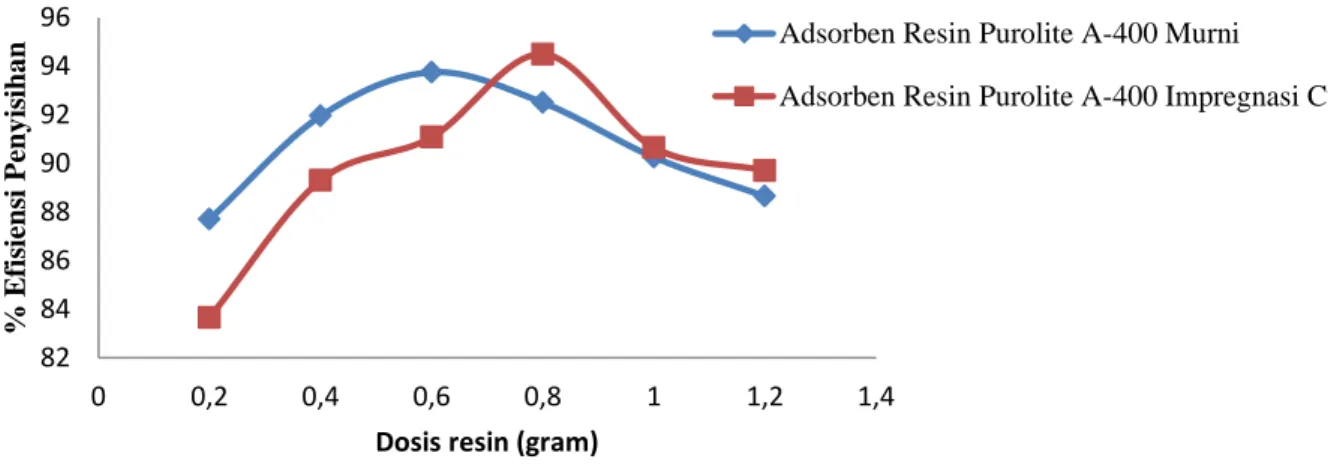
Pengaruh dosis resin kedua adsorben tersebut, dilakukan pada variasi 0,1 gram sampai dengan 1,2 gram, pada waktu kontak masing-masing 160 menit dan 80 menit. Dari Gambar 4.7, resin Purolite A 400 murni, didapatkan hasil pada dosis resin 0,2 gram hingga dosis resin 0,6 gram mengalami kenaikan efisiensi adsorpsi nitrit dengan efisiensi adsorpsi masing-masing dari 87,7% menjadi 91,95% hingga 93,75%, namun dosis resin setelahnya yaitu 0,8 gram hingga 1,2 gram mengalami penurunan efisiensi adsorpsi nitrit dari 92,5% menjadi 88,65 dan menurun kembali hingga 88,65%. Sehingga, untuk dosis adsorben optimal pada resin Purolite A400 murni yaitu pada dosis adsorben 0,6 gram dengan kapasitas adsorpsi 1,15625 mg/g.
Hal yang sama juga terjadi pada adsorben resin Purolite A400 impregnasi Cu, pada dosis resin 0,2 gram hingga 0,8 gram mengalami kenaikan efisiensi adsorpsi dari 83,655% hingga 94,495% . Hal ini menunjukkan, bahwa pada dosis adsorben resin tertinggi, maka permukaan adsorben dan volume pori yang tersedia lebih banyak atau besar untuk adsorpsi (Ertugay, et all., 2014; Nassar., 2012). Pada waktu yang sama, dengan pertambahan adsorben pada dosis resin 1 gram hingga 1,2 gram mengalami penurunan efsiensi adsorpsi menjadi 90,65% hingga 89,71% dengan kapasitas adsorpsi nitrit masing-masing dari 0,9065 mg/g menurun menjadi 0,7475 mg/g. Penurunan densitas adsorpsi dan jumlah massa yang teradsorpsi per unit disebabkan oleh adanya pemisahan efek fluks (gradien konsentrasi) antara adsorben dengan meningkatnya konsentrasi adsorben yang menyebabkan penurunan dalam jumlah adsorpsi nitrit ke satuan bobot biomassa (Ertugay, et all., 2014). Pada gambar 4.7 menunjukkan bahwa adsorben resin Purolite A400 impregnasi Cu memiliki efisiensi penyisihan yang lebih baik dari resin Purolite A400 murni, dengan dosis adsorben optimal pada dosis adsorben 0,8 gram dengan efisiensi penyisihan mencapai 94,495% dan kapasitas adsorpsi 1,1811 mg/g. Hasil analisa diatas, didapatkan bahwa resin Purolite A400 impregnasi Cu memiliki persen efisiensi penyisihan nitrit lebih besar.
0 20 40 60 80 100 0 0,5 1 1,5 % E fi si e n si Pen yi si h an
Dosis adsorben (gram)
Adsorben Resin Purolite A-400 Murni
Adsorben Resin Purolite A-400 Impregnasi Cu
IV - 8 Pada umumnya dengan penambahan dosis adsorben maka jumlah situs aktif adsorpsi akan meningkat. Akan tetapi, ketika penambahan adsorben terus dilakukan di atas jumlah optimal, situs yang aktif dapat menutup situs yang aktif satu sama lain (Tesyafe, et all., 2014), memungkinkan terjadinya tumpang tindih situs adsorpsi karena kepadatan adsorben yang berlebihan (Tumin, N., et al. 2008). Sehingga konsentrasi ion yang telah terikat pada permukaan adsorben akan terdesorpsi kembali ke larutan (Irawan, dkk)
Gambar 4.7 Pengaruh Dosis Adsorben Terhadap Efisiensi Penyisihan Ion Nitrit dengan Konsentrasi Awal 10 mg/l
4.4 Kinetika Adsorpsi
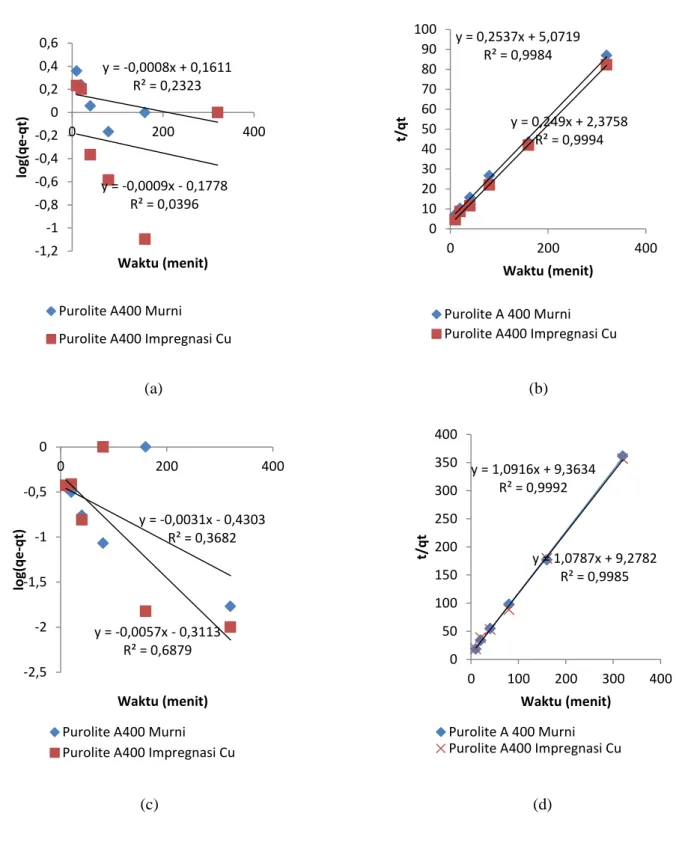
Model kinetika pseudo orde pertama dan pseudo orde kedua digunakan untuk menyesuaikan hubungan data kinetik ion exchange (Bulgarui, et al. 2010). Penentuan model kinetika adsorpsi dalam model pseudo orde pertama (pers 2.6) dan pseudo orde kedua (pers 2.7). Dari persamaan 2.6, diplot kurva t vs log (qe-qt) yang disajikan pada Gambar 4.8 (a) & (c), sedangkan persamaan 2.7 diplot kurva t vs
dengan slope
dan intersep yang disajikan pada Gambar 4.8 (b) & (d).
82 84 86 88 90 92 94 96 0 0,2 0,4 0,6 0,8 1 1,2 1,4 % E fis iens i P eny is iha n
Dosis resin (gram)
Adsorben Resin Purolite A-400 Murni
IV - 9
(a) (b)
(c) (d)
Gambar 4.8 Grafik linear Kinetika Adsorpsi Nitrat (a)Pseudo orde Pertama (b)Pseudo orde kedua Grafik linear Kinetika Adsorpsi Nitrit (c)Pseudo orde Pertama (d)Pseudo orde kedua
y = -0,0008x + 0,1611 R² = 0,2323 y = -0,0009x - 0,1778 R² = 0,0396 -1,2 -1 -0,8 -0,6 -0,4 -0,2 0 0,2 0,4 0,6 0 200 400 lo g(q e -q t) Waktu (menit)
Purolite A400 Murni Purolite A400 Impregnasi Cu
y = 0,2537x + 5,0719 R² = 0,9984 y = 0,249x + 2,3758 R² = 0,9994 0 10 20 30 40 50 60 70 80 90 100 0 200 400 t/ q t Waktu (menit) Purolite A 400 Murni Purolite A400 Impregnasi Cu
y = -0,0031x - 0,4303 R² = 0,3682 y = -0,0057x - 0,3113 R² = 0,6879 -2,5 -2 -1,5 -1 -0,5 0 0 200 400 lo g(q e -q t) Waktu (menit)
Purolite A400 Murni Purolite A400 Impregnasi Cu
y = 1,0916x + 9,3634 R² = 0,9992 y = 1,0787x + 9,2782 R² = 0,9985 0 50 100 150 200 250 300 350 400 0 100 200 300 400 t/ q t Waktu (menit) Purolite A 400 Murni Purolite A400 Impregnasi Cu
IV - 10 Dari Gambar 4.8 didapatkan persamaan dan nilai koefisien korelasi masing-masing model kinetika yang disajikan pada Tabel 4.1.
Tabel 4.1 Persamaan dan Nilai Koefisien Korelasi Kinetika
Adsorben
Model Kinetika
Pseudo orde Pertama Pseudo Orde Kedua
Persamaan R2 Persamaan R2 Adsorpsi Nitrat Purolite A400 Murni y = -0,0008x + 0,1611 0,2323 y = 0,2537x + 5,0719 0,9984 Purolite A400 impregnasi Cu y = -0,0009x – 0,1778 0,0396 y = 0,249x + 2,3758 0,9994 Adsorpsi Nitrit Purolite A400 Murni y = -0,0031x - 0,4303 0,3682 y = 1,0916x + 9,3634 0,9992 Purolite A400 impregnasi Cu y = -0,0057x - 0,3113 0,6879 y = 1,0787x + 9,2782 0,9985
Pada Gambar 4.8 (a) dan Tabel 4.1 resin Purolite A400 murni dengan plot garis lurus dari log (qe-qt) terhadap waktu (t) diperoleh persamaan y = 0,0018x + 0,371, sehingga diperoleh nilai qe atau kapasitas serapan maksimum untuk pseudo orde pertama adalah 2,35 mg/g. Laju adsorpsi untuk pseudo orde pertama (k1) adalah 0,0041 min-1. Dan nilai koefisien korelasi (R2) sebesar 0,2323. Untuk kinetika adsorpsi pseudo orde kedua pada resin Purolite A400 murni ditentukan dengan menggunakan persamaan 2.7. Dari gambar 4.8 (b), dimana plot t/qt terhadap waktu (t) memberikan persamaan linear y= 0,2537x + 5,0719 min-1. Nilai koefisien korelasi (R2) sebesar 0,9984. Untuk lebih jelas, parameter model kinetika adsorpsi nitrat dan nitrit dapat dilihat pada Tabel 4.2.
Berdasarkan analisis data model kinetika adsorpsi pada Tabel 4.2, dapat diketahui bahwa adsorpsi ion nitrat dan nitrit dengan menggunakan resin Purolite A400 murni dan resin Purolite A400 impregnasi Cu cocok menggunakan model pseudo orde kedua. Hal ini ditunjukkan dengan nilai koefisien korelasi yang mendekati angka satu. Ini juga didukung pada model kinetika pseudo orde pertama tidak sepenuhnya valid untuk sistem adsorpsi karena koefisien korelasi yang relatif rendah (Rouabeh and Amrani., 2012) hingga jumlah adsorpsi mencapai nilai minus. Pemilihan model pseudo orde kedua menunjukkan bahwa diasumsikan interaksi pada proses adsorpsi yang terjadi merupakan reaksi secara kimia (Bulgariu, et al. 2010) antara permukaan adsorben dengan adsorbat (Nassar. 2012).
IV - 11 Tabel 4.2Parameter Model Kinetik Adsorpsi Nitrat-Nitrit
Adsorben Model Jumlah adsorpsi/qe (mg/g) Konstanta laju kesetimbangan adsorpsi
pada orde pertama/K1
(1/min)
Konstanta laju kesetimbangan adsorpsi pada orde
kedua/K2 (1/min) Resin Purolite A400 Murni NITRAT Pseudo orde pertama 1,45 0,001824 - Pseudo orde kedua 3,9416 - 0,0126 Resin Purolite A400 Impregnasi Cu Pseudo orde pertama -1,5059 0,207 - Pseudo orde kedua 4,016 - 0,026 Resin Purolite A400 Murni NITRIT Pseudo orde pertama -2,6933 0,007 - Pseudo orde kedua 0,916 - 0,127 Resin Purolite A400 Impregnasi Cu Pseudo orde pertama -2,047 0,1312 - Pseudo orde kedua 0,927 - 0,125
Nilai k menunjukkan cepat lambatnya proses adsorpsi, semakin besar nilai k, maka semakin cepat pula proses adsorpsi berlangsung (Riyanti. 2016). Berdasarkan model kinetika pseudo orde kedua pada Tabel 4.2, didapatkan bahwa nilai konstanta laju adsorpsi nitrat pada resin Purolite A400 murni yaitu sebesar 0,0126 1/min, sedangkan pada resin Purolite A400 impregnasi Cu yaitu 0,026 1/min. Harga konstanta laju adsorpsi nitrat untuk resin Purolite A400 impregnasi meningkat dari pada konstanta resin Purolite A400 murni. Peningkatan terjadi 2 kali lipat daripada harga konstanta resin murni, hal ini disebabkan oleh karena resin yang diimpregnasi telah disisipkan oleh ion positif dari Cu pada permukaan adsorben, sehingga kecepatan laju adsorpsi nitrat semakin besar. Hal ini diungkapkan oleh Loganathan, et al (2013), dengan adanya impregnasi logam atau oksida logam pada permukaan, terkhusus logam berat, umumnya dapat meningkatkan adsorpsi pada adsorben secara elktrostatis yaitu terjadinya pertukaran ion positif logam dengan ion negatif pada permukaan adsorben. Berbeda halnya pada konstanta laju adsorpsi nitrit resin purolite A400 murni dan resin Purolite A400 impregnasi Cu, diperoleh harga konstanta laju adsorpsi nitrit masing-masing 0,127 1/min dan 0,125 1/min. Hal ini menunjukkan bahwa laju adsorpsi nitrit antara resin Purolite A400 murni dan Purolite A400 impregnasi Cu hampir sama.
IV - 12 4.5 Isoterm Adsorpsi
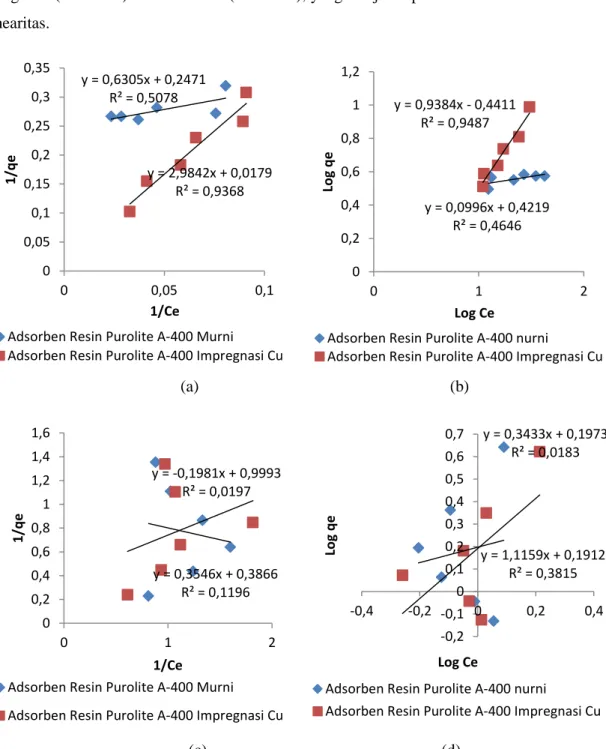
Isoterm adsorpsi merupakan indikasi distribusi antara larutan dengan adsorben pada kesetimbangan proses adsorpsi, yang ditunjukkan dengan hubungan antara dosis adsorben/resin per gram. Penentuan jenis pemodelan adsorpsi sangat penting yaitu untuk mengetahui karateristik sistem adsorpsi antara larutan dengan permukaan adsorben (Quard, et al.2015). Untuk isoterm adsorpsi digunakan pemodelan Langmuir (Pers 2.13) dan Freudlich (Pers 2.15), yang disajikan pada Gambar 4.9 dalam bentuk grafik linearitas.
(a) (b)
(c) (d) Gambar 4.9 Grafik linear Isoterm Adsorpsi Nitrat (a)Langmuir (b)Freundlich
Grafik linear Isoterm Adsorpsi Nitrit (c)Langmuir (d)Freundlich
y = 0,6305x + 0,2471 R² = 0,5078 y = 2,9842x + 0,0179 R² = 0,9368 0 0,05 0,1 0,15 0,2 0,25 0,3 0,35 0 0,05 0,1 1/q e 1/Ce
Adsorben Resin Purolite A-400 Murni Adsorben Resin Purolite A-400 Impregnasi Cu
y = 0,0996x + 0,4219 R² = 0,4646 y = 0,9384x - 0,4411 R² = 0,9487 0 0,2 0,4 0,6 0,8 1 1,2 0 1 2 Log q e Log Ce
Adsorben Resin Purolite A-400 nurni
Adsorben Resin Purolite A-400 Impregnasi Cu
y = -0,1981x + 0,9993 R² = 0,0197 y = 0,3546x + 0,3866 R² = 0,1196 0 0,2 0,4 0,6 0,8 1 1,2 1,4 1,6 0 1 2 1/q e 1/Ce
Adsorben Resin Purolite A-400 Murni Adsorben Resin Purolite A-400 Impregnasi Cu
y = 0,3433x + 0,1973 R² = 0,0183 y = 1,1159x + 0,1912 R² = 0,3815 -0,2 -0,1 0 0,1 0,2 0,3 0,4 0,5 0,6 0,7 -0,4 -0,2 0 0,2 0,4 Log q e Log Ce
Adsorben Resin Purolite A-400 nurni
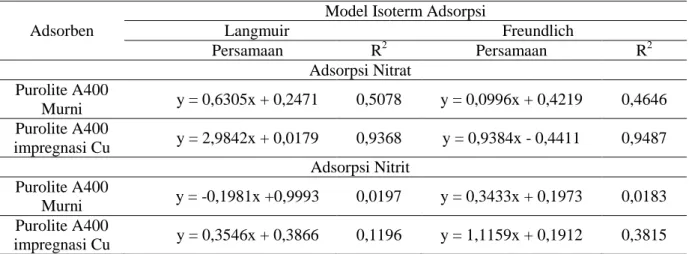
IV - 13 Dari Gambar 4.9 didapatkan persamaan dan nilai koefisien korelasi masing-masing model isoterm adsorpsi yang disajikan pada Tabel 4.3.
Tabel 4.3 Persamaan dan Nilai Koefisien Korelasi Pemodelan Isoterm Adsorpsi
Adsorben
Model Isoterm Adsorpsi
Langmuir Freundlich Persamaan R2 Persamaan R2 Adsorpsi Nitrat Purolite A400 Murni y = 0,6305x + 0,2471 0,5078 y = 0,0996x + 0,4219 0,4646 Purolite A400 impregnasi Cu y = 2,9842x + 0,0179 0,9368 y = 0,9384x - 0,4411 0,9487 Adsorpsi Nitrit Purolite A400 Murni y = -0,1981x +0,9993 0,0197 y = 0,3433x + 0,1973 0,0183 Purolite A400 impregnasi Cu y = 0,3546x + 0,3866 0,1196 y = 1,1159x + 0,1912 0,3815 Pada gambar 4.9 (a) dan Tabel 4.3 dengan adsorben resin Purolite A400 murni yang mengadsorpsi ion nitrat disajikan kurva pola isoterm adsorpsi Langmuir dengan persamaan garis lurus y = 0,6305x + 0,2471 yang memiliki gradien 1/qmaks KL = 0,6305 dan garis ini memotong sumbu 1/qe = 0,247 dengan menghasilkan nilai regresi (R2) sebesar 0,5078. Kapasitas adsorpsi maksimum diperoleh sebesar (qmaks) = 4,046 mg/g dan konstanta kesetimbangan (KL) sebesar 0,392/mg.
Gambar 4.9 (b) dengan adsorben resin Purolite A400 murni yang mengadsorpsi ion nitrat disajikan kurva pola isoterm adsorpsi Freundlich dengan persamaan garis lurus y = 0,996x + 0,4219 yang memiliki gradien 1/n = 0,996 dan memotong sumbu log qe pada 0,4219, sehingga diperoleh nilai kapasitas adsorpsi maksimum yang diperoleh dengan model isoterm Freundlich (kf) adalah 2,6418 dengan nilai R2 = 0,4646. Nilai intensitas adsorpsi menggunakan model isoterm Freundlich (n) diperoleh sebesar 10,0. Untuk lebih jelas, parameter model isoterm adsorpsi nitrat dan nitrit dapat dilihat pada Tabel 4.4.
Model isoterm Langmuir merupakan adsorpsi terbatas pada beberapa lapisan molekul atau monolayer pada permukaan adsorben yang diasumsikan bahwa proses adsorpsi terjadi secara kimia. Pola isoterm adsorpsi Langmuir menunjukkan bahwa afinitas yang relatif tinggi antara zat terlarut ion nitrat dan nitrit dengan adsorben pada tahap awal, selanjutnya semakin menurun secara perlahan pada tahap selanjutnya (Simpen, dkk. 2012). Nilai parameter adsorpsi nitrat dan nitrit dengan menggunakan pemodelan isoterm Langmuir dapat dilihat pada tabel 4.4.
IV - 14 Tabel 4.4 Parameter Isoterm Adsorpsi Nitrat & Nitrit
Model Parameter Nitrat Nitrit
Purolite A400 Purolite A400-Cu Purolite A400 Purolite A400-Cu Model Isoterm Langmuir
Adsorpsi maks (mgN/g) 4,046 55,86 1,0070 2,5866
Konstanta afinitas Langmuir
(l/mg) 0,392 0,0059 0,8288 1,0902
RL Dimensi kuantitas
adsorpsi 0,0485 0,772 0,10766 0,0840
Model Isoterm Freundlich
Intensitas adsorpsi (mgN/g) 10,0 1,065 2,9129 0,8961 Konstanta freundlich (l/mg) 2,6418 2,76 0,7048 0,7185
Dari Tabel 4.4 diperoleh bahwa kapasitas maksimum tertinggi untuk adsorpsi nitrat yaitu terjadi pada adsorben resin Purolite A400 impregnasi Cu dengan nilai masing-masing 55,86 mg/g dan 1,032 mg/g. Kapasitas maksimum jauh lebih tinggi pada resin yang telah diimpregnasi Cu, hal ini disebabkan karena dengan adanya logam Cu yang telah disisipkan pada permukaan adsorben sehingga memunculkan situs-situs aktif baru yang semula tersembunyi dan terjadi lipatan-lipatan baru pada permukaan adsorben resin Purolite A 400 impregnasi Cu, yang mempengaruhi nilai luas permukaan spesifik adsorben (Simpen, dkk. 2012) yaitu menjadi lebih besar. Begitu juga dengan adsorpsi nitrit, pada resin Purolite A 400 murni nilai kapasitas maksimum sebesar 0,993 mg/g, sedangkan pada resin Purolite A400 impregnasi Cu mempunyai nilai kapasitas maksimum adsorpsi yaitu 2,5866 mg/g. Kenaikan nilai kapasitas maksimum adsorpsi mencapai 2,5 kali dari adsorben resin murni. Ciri penting dari isoterm Langmuir yaitu RL (dimensi kuantitas adsorpsi) dengan rumus:
RL = 1/(1+KL Co)
Nilai RL yaitu antara 0 dan 1 merupakan indikasi adsorpsi baik (favourable). Jika nilai RL =0 merupakan indikasi adsorpsi irreveribel, RL = 1 adalah linear dan RL > 1 adalah adsorpsi unfavorable (Igwe. 2007).
Dapat dilihat pada Tabel 4.4 nilai RL untuk adsorpsi nitrat pada adsorben resin purolite A400 murni dan resin Purolite A400 impregnasi Cu masing-masing adalah 0,0485 dan 0,772, dengan konsentrasi mula-mula 50 mg/l. Maka, proses adsorpsi adalah baik (favorable). Begitu juga untuk adsorpsi ion nitrit dapat dilihat pada tabel 4.4 nilai RL adalah baik (favorable). Untuk adsorpsi nitrit, nilai RL
IV - 15 0,10766 untuk adsorben resin Purolite A400 murni dan 0,0840 untuk resin Purolite A400 impregnasi Cu, maka proses adsorpsi nitrit tergolong baik (favorable).
Isoterm adsorpsi Freundlich digunakan untuk menjelaskan karakteristik adsorpsi permukaan adsorben hetererogen (Dada, et al. 2012). Nilai parameter adsorpsi nitrat dan nitrit menggunakan pemodelan isoterm Freundlich dapat dilihat pada Tabel 4.4. Nilai konstanta kf merupakan indikator perkiraan kapasitas adsorpsi, kemudian 1/n adalah fungsi dari kekuatan adsorpsi dalam proses adsorpsi (Dada et al. 2012). Nilai Kf dan n dihitung dari intersep dan slope pada masing-masing plot (Igwe et al. 2007) Gambar 4.9 (b) untuk adsorpsi nitrat dan (d) adsorpsi nitrit. Namun, nilai parameter karekteristik Kf dan n pada sistem adsorben-adsorbat, yang ditentukan oleh data yang cocok sedangkan nilai regresi linear umumnya digunakan sebagai parameter untuk menentukan model kinetika dan isoterm (Dada et al. 2012). Nilai kf dan 1/n juga dapat menentukan perbandingan kemampuan mengadsorpsi ion nitrat maupun ion nitrit (Kusuma, dkk., 2014). Jika nilai n berkisar antara 1-10, ini merupakan indikasi proses adsorsi yang baik (favorable). Pada Tabel 4.4 untuk adsorpsi nitrat nilai n= 10,0 untuk adsorben resin Purolite A400 murni dan n= 1,065 untuk resin Purolite A400 impregnasi Cu, maka proses adsorpsi baik (favorable).
Sama halnya dengan dengan nilai n untuk adsorpsi nitrit pada adsorben resin A400 dengan nilai n= 2,9129, namun berbanding terbalik dengan nilai n pada adsorben Purolite A400 impregnassi Cu yang mempunyai nilai n=0,8961, ini menunjukkan proses adsorpsi nitrit yaitu unfavourable.
Untuk mengetahui kekuatan interaksi antara adsorben dan adsorbat dapat dilihat dari nilai 1/n, semakin kecil nilai 1/n maka semakin kuat interaksi antara adsorben dengan adsorbat (Situmorang, dkk. 2016). Untuk adsorpsi nitrat, resin Purolite A400 murni dan resin Purolite A400 impregnasi memiliki nilai 1/n masing-masing sebesar 0,0996 dan 0,9384, sedangkan untuk adsorpsi nitrit nilai 1/n masing-masing yaitu 0,3433 dan 1,1159. Nilai 1/n ini menunjukkan bahwa kekuatan interaksi (ikatan) yang terjadi antara ion nitrat dan ion nitrit dengan permukaan resin Purolite A400 murni lebih lemah dibandingkan dengan interaksi (ikatan) yang terjadi antara ion nitrat dan nitrit pada permukaan resin Purolite A400 impregnasi Cu. Kekuatan interaksi (ikatan) antara adsorben dengan adsorbat dapat diperhitungkan dalam proses recorvery, dimana kekuatan interaksi lemah menyebabkan adsorben dapat direcorvery lebih mudah (Kusuma, dkk., 2014).
Begitu juga untuk nilai Kf, semakin besar nilai Kf maka semakin besar intensitas adsorpsi (Igwe et al. 2007). Dari tabel 4.4, untuk adsorpsi nitrat nilai kf pada adsorben resin Purolite A400 impregnasi Cu (Kf = 2,76) lebih besar dari pada resin murni (Kf = 2,6418), hal ini menunjukkan bahwa kapasitas adsorpsi pada resin Purolite A400 impregnasi Cu lebih bagus. Pada adsorpsi nitrit terdapat nilai kontanta, Kf yang hampir sama, hal ini menunjukkan bahwa intensitas adsorpsi antara resin Purolite A400 murni dan resin Purolite A400 impregnasi Cu adalah sama.
IV - 16 Dari Gambar 4.9 dan Tabel 4.3, dapat ditentukan pola adsorpsi ion nitrat maupun nitrit oleh adsorben resin Purolite A400 murni dan Purolite A400 impregnasi Cu dengan membandingkan nilai koefisien regresi linear (R2) dari kurva isoterm adsorpsi. Untuk adsorpsi nitrat, nilai R2 resin Purolite A400 impregnasi Cu adalah 0,9368 untuk isoterm adsorpsi langmuir dan 0,9487 untuk isoterm adsorpsi freundlich. Ini menunjukkan bahwa proses adsorpsi yang terjadi cenderung mengikuti pola isoterm adsorpsi Freundlich.
Akan tetapi, karena nilai regresi linear (R2) dari persamaan isoterm adsorpsi cukup tinggi dan hampir sama, maka penentuan kapasitas adsorpsi resin Purolite A400 impregnasi Cu digunakan dengan persamaan isoterm adsorpsi Langmuir dan persaman adsorpsi Freundlich.
Demikian juga untuk adsorpsi nitrit dengan menggunakan adsorben resin Purolite A400 murni yang memiliki nilai R2 yang hampir sama yaitu 0,0197 untuk isoterm adsorpsi Langmuir dan 0,0183 untuk isoterm adsorpsi Freundlich. Hal ini menunjukkan untuk penentuan kapasitas adsorpsi digunakan persaman isoterm adsorpsi Langmuir dan Freudlich. Namun untuk adsorpsi nitrit dengan menggunakan resin Purolite A400 impregnasi Cu, didapatkan nilai R2 untuk isoterm adsorpsi Langmuir dan Freundlich masing-masing yaitu 0,1196 dan 0,3815. Hal ini menunjukkan bahwa proses adsorpsi yang terjadi cenderung mengikuti pola isoterm adsorpsi Freundlich. Isoterm Freundlich mengasumsikan bahwa isoterm adsorpsi ini menandakan adanya ikatan fisik pada adsorben (Sawyer et al. 2003). Adsorpsi fisika terjadi karena adanya gaya tarik-menarik intramolekul antara molekul padatan dengan solut yang teradsorpsi lebih besar daripada gaya tarik-menarik sesama solut itu sendiri dalam larutan, sehingga solut terkonsentrasi pada permukaan padatan (Irmanto., 2009).
BAB V
KESIMPULAN DAN SARAN
5.1. KesimpulanKesimpulan yang dapat diambil dari penelitian yang telah dilakukan adalah :
1. Pada hasil SEM dan EDS resin Purolite A 400 yang telah diimpregnasi memiliki permukaan yang lebih kasar sebagai bukti bahwa logam Cu2+ telah berikatan di permukaan resin, yang diharapkan akan meningkatkan efisiensi penyisihan ion nitrat dan nitrit.
2. Efisiensi Penyisihan nitrat dan nitrit pada waktu kontak optimum dengan menggunakan resin Purolite A 400 murni sebesar 75,2% ; 92,5% sedangkan dengan menggunakan Purolite A400 impregnasi Cu mencapai 78% ; 94,495%. Maka, ini membuktikan bahwa efisiensi adsorpsi nitrat dan nitrit lebih tinggi menggunakan resin Purolite A400 impregnasi Cu.
3. Waktu kontak optimal untuk adsorpsi nitrat dengan menggunakan Resin Purolite A400 impregnasi Cu adalah 80 menit dengan dosis resin 1,0 gram. Pada nitrit yaitu pada waktu 80 menit dengan dosis resin 0,8 gram.
4. Model kinetika yang terpilih untuk Purolite A 400 impregnasi Cu adalah model pseudo orde kedua dengan nilai R2 0,9994 untuk nitrat dan 0,9985 untuk nitrit.
5. Pemodelan isoterm adsorpsi yang mewakili adsorpsi nitrat menggunakan Purolite A 400 impregnasi Cu adalah Langmuir dan Freundlich sedangkan untuk adsorpsi nitrit yaitu isoterm Freundlich.
5.2. Saran
Saran yang dapat diberikan untuk penelitian selanjutnya adalah :
1. Proses impregnasi resin sebaiknya menggunakan bukan logam berat sehingga lebih ramah lingkungan.
2. Proses adsorpsi dengan parameter waktu kontak dan dosis resin sebaiknya dilakukan dengan suhu yang berbeda sehingga diketahui keoptimalan dari proses adsorpsi terhadap suhu.
3. Perlu dilakukan penerapan metode adsorpsi aplikasi langsung pada limbah pertanian, industri dan sampel limbah lainnya.