i
TUGAS AKHIR
Untuk memenuhi sebagian persyaratan mencapai derajat sarjana S-1
Program Studi Teknik Mesin Jurusan Teknik Mesin
Diajukan oleh :
GREGORIUS IBNU PAMUNGKAS NIM: 045214031
FAKULTAS SAINS DAN TEKNOLOGI
UNIVERSITAS SANATA DHARMA
YOGYAKARTA
ii
THE CORROTION OF 304 STAINLESS STEEL FOR HNO3 CHEMERY
WITH pH 0,2 AND pH 0,5
FINAL PROJECT
Presented as Partial Fulfillment of the Requirements To Obtain then Sarjana Teknik Degree
in Mechanical Engineering
By :
Gregorius Ibnu Pamungkas Student Number : 045214031
MECHANICAL ENGINEERING STUDY PROGRAM MECHANICAL ENGINEERING DEPARTMENT
SCIENCE AND TECHNOLOGY FACULTY SANATA DHARMA UNIVERSITY
v
yang pernah diajukan untuk memperoleh gelar kesarjanaan di suatu Perguruan Tinggi, dan sepanjang pengetahuan saya juga tidak terdapat karya atau pendapat yang pernah ditulis atau diterbitkan oleh orang lain, kecuali yang secara tertulis diacu dalam naskah ini dan disebutkan dalam daftar pustaka.
Yogyakarta, 14 Mei 2009
vi
LEMBAR PERNYATAAN PERSETUJUAN PUBLIKASI KARYA ILMIAH UNTUK KEPENTINGAN AKADEMIS
Yang bertanda tangan di bawah ini, saya mahasiswa Universitas Sanata Dharma:
Nama : Gregorius Ibnu Pamungkas
Nomor Mahasiswa : 045214031
Demi pengembangan ilmu pengetahuan, saya memberikan kapada Perpustakaan Universitas Sanata Dharma Karya ilmiah saya yang berjudul :
“ KOROSI STAINLESS STEEL 304 PADA LARUTAN HNO3 DENGAN
pH 0,2 DAN pH 0,5 ”
Beserta perangkat yang diperlukan (bila ada). Dengan demikian saya memberikan kepada Perpustakaan Universitas Sanata Dharma hak untuk menyimpan, mengalihkan, dalam bentuk media lain, mengelolanya dalam bentuk pangkalan data, mendistribusikan secara terbatas, dan mempublikasikannya di internet atau media lain untuk kepentingan akademis tanpa perlu meminta ijin dari saya maupun memberikan royalti kepada saya selama tetap mencantumkan nama saya sebagai penulis.
Demikian pernyataan ini saya buat dengan sebenarnya.
Dibuat di Yogyakarta Pada tanggal : 14 Mei 2009 Yang menyatakan
vii
sehingga penulis dapat menyelesaikan Tugas Akhir ini.
Tugas Akhir ini merupakan salah satu syarat untuk mencapai derajat Sarjana S-1 pada Program Studi Teknik Mesin, Fakultas Sains dan Teknologi, Universitas Sanata Dharma. Isi Tugas Akhir ini adalah mengenai korosi stainless steel 304 pada larutan HNO3 dengan pH 0,2 dan pH 0,5.
Dalam kesempatan ini penulis menyadari bahwa dalam proses belajar di Program Studi Teknik Mesin, sejak awal studi sampai berakhirnya studi melibatkan banyak hal. Atas segala saran, bimbingan, dukungan dan bantuan, pada kesempatan ini penulis mengucapkan terima kasih kepada :
1. Dr. Ir. Paulus Wiryono Priyotamtama, S.J., Rektor Universitas Sanata Dharma.
2. Yosef Agung Cahyanta, S.T., M.T., Dekan Fakultas Sains dan Teknologi.
3. Budi Sugiharto, S.T., M.T., Ketua Program Studi Teknik Mesin Fakultas Sains dan Teknologi Universitas Sanata Dharma Yogyakarta. 4. Budi Setyahandana, S.T., M.T., Dosen Pembimbing Tugas Akhir. 5. Ir. FX. Agus Unggul Santosa, Dosen Pembimbing Akademik.
viii
7. Teman – teman yang telah membantu dalam menyelesaikan skripsi ini, yang tidak bisa saya sebutkan satu persatu.
8. Br. Sunari. SJ, yang telah membantu dengan doa, memberikan dukungan dan harapan secara moril dan materiil.
9. Bapak alm dan Ibu saya, serta semua kakak-kakak saya yang selalu memberikan doa dan dukungan secara moril dan materiil pula sehingga skripsi ini bisa saya selesaikan dengan baik.
Penulis menyadari bahwa penulisan Tugas Akhir ini masih jauh dari sempurna. Meskipun demikian penulis berharap bahwa penulisan Tugas Akhir ini dapat memberikan kontribusi dalam pengembangan ilmu khususnya mengenai perancangan turbin aliran silang. Atas kritik dan saran yang bersifat membangun guna sempurnanya karya tulis ini penulis mengucapkan terima kasih.
Yogyakarta, 14 Mei 2009
ix
bahan yang digunakan adalah baja tahan karat (Stainless Steel) 304, dengan komposisi : Cr = 18,358 %, Ni = 8,408 %, C = 0,047 %, Fe = 70,47 %.
Stainless Steel 304 direndam larutan HNO3 pada pH 0,5 dengan suhu 700C selama 6jam, lalu suhu diturunkan menjadi 290C selama 18 jam. Hal ini dilakukan secara periodik selama 12 minggu. Pada tiap minggu dilakukan pengamatan terhadap berat benda uji dengan cara ditimbang. Penelitian yang sama juga dilakukan pada Stainless Steel 304 dengan larutan HNO3 yang memiliki pH 0,2.
x
DAFTAR ISI
Halaman
HALAMAN JUDUL... i
HALAMAN PERSETUJUAN PEMBIMBING ... iii
HALAMAN PENGESAHAN... iv
HALAMAN PERNYATAAN ... v
HALAMAN PERSETUJUAN PUBLIKASI ... vi
KATA PENGANTAR... vii
B. Jenis-jenis Korosi Pada Stainless Steel ... 9
B.1. Uniform Corrosion... ... 10
B.2. Pitting Corrosion... ... 10
B.3. Crevice Corrosion... 13
B.4. Stress Corrosion Cracking... 14
xi
xii
B. Larutan HNO3 pH 0,2 ... ... 41
C. Larutan HNO3 pH 0,2 dan 0,5 ... 42
D. Grafik Laju Korosi/Tahun SS 304 Pada Larutan HNO3 pH 0,2 dan pH 0,5 ... ... 43
BAB V KESIMPULAN DAN SARAN ... 44
5.1. Kesimpulan ... 44
5.2. Saran ... 44
1 1.1 Latar Belakang Masalah
Baja Tahan Karat (Stainless Steel) sangat cocok untuk pembuatan tabung-tabung reaksi untuk reaksi-reaksi nuklir. Contoh penggunaan Stainless Steel 304 adalah tabung Reaktor SAMOP (Sub Critical Assembly for Mo99 Prad Action). Pemanfaatan teknologi nuklir memiliki banyak keunggulan oleh adanya sifat radiasi yang mudah dideteksi sampai kadar yang sangat rendah, berdaya tembus besar dan dapat dikendalikan baik arah, luas berkas maupun energi partikelnya. Hampir semua peralatan dan mesin-mesin industri serta komponennya dirancang sedemikian rupa sehingga dapat diketahui kekuatan maksimum dan umur pemakaiannya. Hal ini membutuhkan waktu penelitian dan juga ketelitian yang tinggi. Pada kenyataanya larutan yang digunakan pada reaktor nuklir tersebut menggunakan uranium nitrat, namun karena kesulitan dalam mencari larutan tersebut maka penelitian yang penulis lakukan menggunakan asam nitrat yang banyak ditemukan di pasaran.
2
1.2 Tujuan Penelitian
Tujuan penelitian ini adalah untuk mengetahui laju korosi Stainless Steel 304 yang telah mengalami pengelasan dan yang tidak mengalami pengelasan dalam lingkungan HNO3 dengan pH 0,2 dan juga pada pH 0,5
1.3 Batasan Masalah
Judul dari Tugas Akhir yang penulis susun ini sebenarnya bisa mencakup permasalahan yang luas. Maka agar pembahasannya tidak terlalu banyak dan lebih terarah, maka penulis memberikan batasan permasalahan sebagai berikut:
1. Bahan yang digunakan dalam penelitian adalah Stainless Steel tipe 304 yang telah mengalami pengelasan.
2. Proses pembuatan larutan HNO3 dengan pH 0,2 dan pH 0,5 dengan kondisi awal HNO3 65 %.
3. Benda kerja yang akan diteliti dimasukkan ke dalam tabung kimia berisi larutan HNO3 dengan pH 0,2 dan juga pH 0,5.
1.4 Sistematika Penulisan
Penulisan Tugas Akhir ini akan dibagi dalam beberapa bagian, yaitu :
1. Bab I membahas mengenai latar belakang penelitian, batasan masalah, tujuan penelitian, dan sistematika penulisan.
paduan pada Stainless Steel, korosi pada logam, dan pengelasan berperisai tungsten (TIG).
3. Bab III membahas mengenai metode penelitian yang berisi skema penelitian, bahan yang digunakan, alat-alat yang digunakan.
4. Bab IV membahas mengenai hasil penelitian dan pembahasan yang berisi data dan perhitungan laju korosi benda uji.
4
BAB II
TINJAUAN PUSTAKA
2.1. Klasifikasi Stainless Steel
Dengan pesatnya perkembangan teknologi, manfaat nuklir yang dahulunya dipakai sebagai senjata perang maka sekarang nuklir banyak dimanfaatkan untuk mencukupi kebutuhan manusia. Pemanfaatan teknologi nuklir memiliki banyak keunggulan oleh adanya sifat radiasi yang mudah dideteksi sampai kadar yang sangat rendah, berdaya tembus besar dan dapat dikendalikan baik arah, luas berkas maupun energi partikelnya.
Baja Tahan Karat (Stainless Steel) sangat cocok untuk pembuatan tabung-tabung reaksi untuk reaksi-reaksi nuklir. Contoh penggunaan Stainless Steel adalah tabung Reaktor SAMOP (Sub Critical Assembly for Mo99 Prad Action).
2.2. Baja Tahan Karat ( Stainless Steel )
(Copper), Ti (Titanium) yang berfungsi untuk meningkatkan ketahanan terhadap temperatur serta korosi.
Golongan utama baja tahan karat (Stainless Steel) adalah Austenit, Ferrit, Martensit, Duplex.
a. Austenit Stainless Steel
Komposisi Autenit Stainless Steel antara 18% Cr dan 8% Ni atau biasa disebut sebagai baja tahan karat delapan belas delapan. Baja tahan karat Austenit ketahanan karatnya lebih baik, mampu bentuk dan mampu las. Jenis ini sering digunakan pada berbagai industri kimia, untuk bahan konstruksi, perabot dapur, turbin, mesin jet, mobil, komponen berputar, bangunan kapal, reactor atom, dan sebagainya.
b. Ferritic Stainless Steel
Kadar chrom sekitar 16% sampai 18% dan kadar Nickel sekitar 2 %. Ketahanan korosi kurang begitu baik dan relatif sulit untuk difabrikasi atau dimachining. Sifat yang menguntungkan dari baja tahan karat ferit adalah tanpa kandungan Ni sulit untuk terjadi retakan korosi tegangan.
c. Martensit Stainless Steel
6
penemperan dapat diperoleh sifat-sifat mekanik yang baik. Baja tahan karat jenis ini digunakan untuk alat potong dan perkakas. d. Duplex Stainless Steel
Baja tahan karat jenis duplex mempunyai fasa ganda yaitu fasa austenit dan ferit. Umumnya mempunyai komposisi 12 % Cr + 5 % Ni + 1,5 % Mo + 0,03 % C. Memiliki sifat kombinasi antara sifat austenite dan ferit yang saling menutupi. Sebagai contoh, tegangan mulur yang rendah dari sifat austenit diperbaiki dengan adanya sifat ferit. Dan keuletan rendah dari sifat ferit diperbaiki oleh sifat austenit. Ketahanan korosi pada umumnya melebihi baja 18-8, terutama baja yang mempunyai kadar Cr tinggi dan mengandung Mo sangat baik dalam ketahanan korosi lubangnya sehingga baja ini dapat dipakai untuk penukar panas yang menggunakan air laut.
2.3 Pengaruh Unsur Paduan Pada Stainless Steel
Dalam aplikasi, Stainless Steel selain dibutuhkan sebagai logam yang tahan terhadap korosi juga dibutuhkan sifat tambahan guna meningkatkan sifat mekaniknya.
1. Kromium (Cr) berguna untuk membentuk lapisan pasif untuk melindungi dari korosi.
2. Nikel (Ni) sebagai penstabil austenit, meningkatkan sifat mekanik, maningkatkan ketahanan korosi pada lingkungan asam mineral. 3. Mangan (Mn) membantu fungsi Ni.
4. Molybdenum (Mo) sebagai penstabil lapisan pasif dalam lingkungan yang mengandung banyak ion klorida (Cl - ), seperti lingkungan air laut (NaCl).
5. Karbon (C) meningkatkan kemampuan dikeraskan (hardenability) dari material Stainless Steel.
6. Nitrogen (N) membentuk duplex stainlees steel dengan meningkatkan terbentuknya austenit, meningkatkan sifat mekanik Stainless Steel.
2.4 Korosi Pada Logam A. Korosi Secara Umum
8
maupun air. Material lain yang memiliki sifat sejenis antara lain Titanium (Ti) dan juga Aluminium (Al).
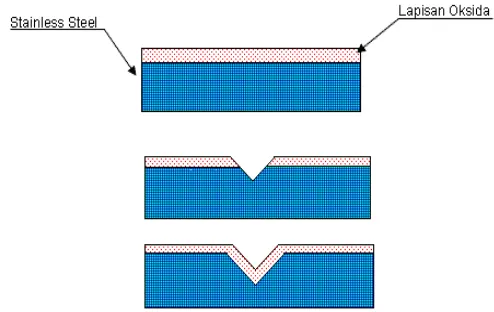
Secara umum protective layer terbentuk dari reaksi kromium + oksigen secara spontan membentuk krom-oksida. Jika lapisan oksida S tergores/terkelupas, maka protective layer akan segera terbentuk secara spontan, tentunya jika kondisi lingkungan cukup mengandung oksigen (Gambar 2.3). Walaupun demikian kondisi lingkungan tetap menjadi penyebab kerusakan protective layer tersebut. Pada keadaan dimana protective layer tidak dapat lagi terbentuk, maka korosi akan terjadi. Banyak media yang dapat menjadi penyebab korosi, seperti halnya udara, cairan/ larutan yang bersifat asam/basa, gas-gas proses (misalnya gas asap hasil buangan ruang bakar atau reaksi kimia lainnya), logam yang berlainan jenis dan saling berhubungan dan sebagainya.
B. Jenis-Jenis Korosi Pada Stainless Steel
Meskipun alasan utama penggunaan stainless steel adalah ketahanan korosinya, tetapi pemilihan stainless steel yang tepat harus disesuaikan dengan aplikasi yang tepat pula. Pada umumnya, korosi menyebabkan beberapa masalah seperti :
1. Terbentuknya lubang-lubang kecil/halus pada tangki dan pipa-pipa sehingga menyebabkan kebocoran cairan ataupun gas.
2. Menurunnya kekuatan material disebabkan penyusutan atau pengurangan ketebalan atau volume material sehingga 'strength' juga menurun, akibatnya dapat terjadi retak, bengkok, patah dan sebagainya.
3. Penampilan permukaan material menjadi tidak menarik disebabkan kerak karat ataupun lubang-lubang
4. Terbentuknya karat-karat yang mungkin mengkontaminasi zat atau material lainnya, hal ini sangat dihindari khususnya pada proses produksi makanan.
Secara umum korosi pada stainless steel dapat dikategorikan sbb. : 1. Uniform Corrosion
2. Pitting Corrosion 3. Crevice Corrosion
10
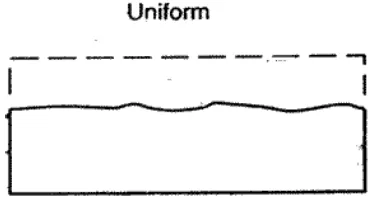
B.1 Uniform Corrosion
Uniform corrosion terjadi disebabkan rusaknya sebagian atau seluruh protective layer pada SS sehingga SS secara merata akan berkurang/aus terlihat pada gambar 2.4. Korosi ini terjadi umumnya disebabkan oleh cairan atau larutan asam kuat maupun alkali panas. Asam hidroklorit dan asam hidrofluor adalah lingkungan yang perlu dihindari SS apalagi dikombinasikan dengan temperatur serta konsentrasi yang cukup tinggi.
Gambar 2.4 Korosi uniform yang menyebabkan berkurangnya dimensi permukaan benda secara merata.
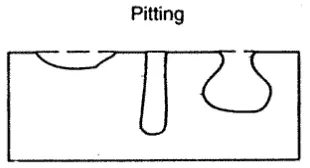
B.2 Pitting Corrosion
protective layer pada permukaan SS terutama permukaan yang cacat. Timbulnya cacat ini dapat disebabkan oleh kotoran sulfida, retak-retak kecil akibat penggerindaan, pengelasan, penumpukan kerak, penumpukan larutan padat. Proses kimia yang terjadi saat pitting korosi ini dapat dilihat dalam gambar 2.6. Umumnya SS berkadar Krom (Cr), Molybdenum (Mo) dan Nitrogen (N) yang tinggi cenderung lebih tahan terhadap pitting corrosion. Pada industri petrokimia korosi ini sangat berbahaya karena menyerang permukaan dan penampakan visualnya sangat kecil, sehingga sulit untuk diatasi dan dicegah terutama pada pipa-pipa bertekanan tinggi.
Ketahanan material terhadap pitting korosi jenis ini di formulasikan sbb :
PREN = %Cr + (3,3 x %Mo) + (16 x %N)
12
6B. SS 304 memiliki komposisi (dalam %): < 0,015 C, 18.5 Cr, 12 Ni sedangkan untuk SS 316L memiliki komposisi : < 0,030 C, 17.5 Cr, 13,5 Ni, 2,6 Mo. SS super-austenitik UR 6B memiliki komposisi : < 0,020 C, 20 Cr, 25 Ni, 4,3 Mo, dan 0,13 N. Dengan komposisi yang berbeda maka nilai PREN untuk masing-masing SS adalah: 304 = 18, 316L = 26, dan UR B6 = 37. Dengan demikian UR B6 memiliki ketahanan akan pitting korosi paling kuat sedangkan 304 memiliki ketahanan pitting korosi yang terlemah.
Gambar 2.5 IIustrasi pitting corrosion pada material SS.
Gambar 2.6 Skema proses kimia yang terjadi saat pitting corrosion menyerang dan terus
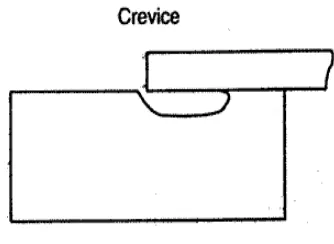
B.3 Crevice Corrosion
Korosi jenis ini sering terjadi di daerah yang kondisi oksidasi terhadap krom (Cr) SS sangat rendah bahkan tidak ada sama sekali (miskin oksigen). Sering pula terjadi akibat desain konstruksi peralatan yang tidak memungkinkan terjadinya oksidasi tersebut misal celah antara gasket/packing, celah yang terbentuk akibat pengelasan yang tidak sempurna, sudut-sudut yang sempit, celah/sudut antara 2 atau lebih lapisan metal, celah antara mur/baut dsb. Peristiwa korosi ini terjadi di daerah yang sangat sempit (celah, sudut, takik dsb) seperti disajikan pada gambar 2.7. Crevice Corrosion dapat dipandang sebagai pitting corrosion yang lebih berat/hebat dan terjadi pada temperatur di bawah temperatur moderat yang biasa menyebabkan pitting corrosion. Cara untuk menghindari masalah ini, salah satunya dengan membuat desain peralatan lebih 'terbuka' walaupun kenyataannya sangat sulit untuk semua aplikasi.
14
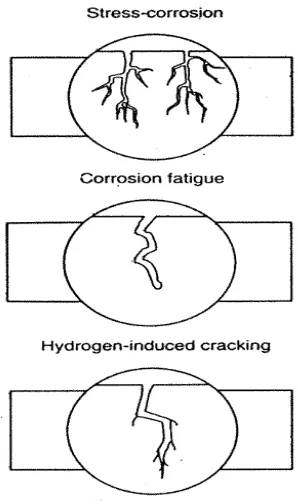
B.4 Stress Corrosion Cracking
permesinan, sehingga dapat mengurangi tegangan pada permukaan logam.
Gambar 2.8 Ilustrasi stress-cracking-corrosion akibat adanya tegangan sisa dan lingkungan korosif.
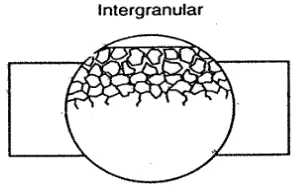
B.5 Intergranular Corrosion
16
menghilangkan/mengurangi sifat perlindungan kromium pada daerah tengah butir. Sehingga daerah ini akan dengan mudah terserang oleh korosi (Gambar 2.9). Umumnya SS dengan kadar karbon kurang dari 2 % relative tahan terhadap korosi ini. Ketidaksempurnaan mikrostruktur ini diperbaiki dengan menambahkan unsur yang memiliki daya tarik terhadap karbon lebih besar untuk membentuk karbida, seperti Titanium (misal pada SS 321) dan Niobium (misal pada SS 347). Cara lain adalah dengan menggunakan SS berkadar karbon rendah yang ditandai indeks 'L' -low carbon steel- (misal 316L atau 304L). SS dengan kadar karbon tinggi akan tahan terhadap korosi jenis ini asalkan digunakan pada temperatur tinggi pula (misal 304H, 316H, 321H, 347H).
Gambar 2.9 Ilustrasi korosi pada butir akibat terjadinya sensitasi krom (Cr).
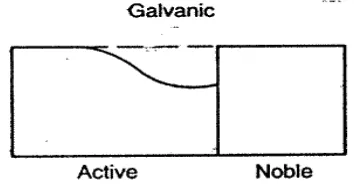
B.6 Galvanic Corrosion
dengan bodi tangki, hasil welding dengan benda kerja) dan atau terendam dalam larutan elektrolit, sehingga dissimilar material tersebut menjadi semacam sambungan listrik. Mekanisme ini disebakan satu material berfungsi sebagai anoda dan yang lainnya sebagai katoda sehingga terbentuk jembatan elektrokimia tersaji pada gambar 2.10. Dengan terjadinya hubungan elektrik tersebut maka logam yang bersifat anoda akan lebih mudah terkorosi. Urutan tersebut ditunjukkan pada seri elektrokimia logam berikut :
Logam deret sebelah kiri cenderung menjadi anoda (mudah berkarat) sementara logam sebelah kanan cenderung menjadi katoda. Galvanic corrosion ini tergantung pada :
1. Perbedaan ke-mulia-an dissimilar material
2. Rasio luas permukaan dissimilar material, dan konduktifitas
Gambar 2.10 Ilustrasi terjadinya korosi antara dua logam yang berbeda jenis keaktifannya (logam A dan B).
2.5 Pengelasan Berperisai Tungsen (TIG)
18
dalam suatu atmosfer argon murni, dengan atau tanpa tambahan kecil gas-gas berfaedah lain. Perisai gas-gas mencegah kontaminasi logam las oleh udara. Permukaan paduan alumunium ditutupi oleh lapisan oksida tahan api bertitik lebur tinggi yang harus dihilangkan sebelum suatu las yang memuaskan dapat dibuat. Suatu kawat pengisi dapat juga ditambahkan pada tepi depan genangan cairan untuk membentuk las. Ini merupakan salah satu sifat busur api arus bolak-balik sehingga menghilangkan oksida yang kuat selama proses pengelasan.
Proses pengelasan TIG dipakai bila diperlukan las yang rapi, berkualitas tinggi, dan ekonomis untuk ketebalan sampai 6 mm. Untuk ketebalan yang lebih dari 6 mm, biasanya digunakan pengelasan MIG, atau proses pengelasan busur api logam lainnya. Lubang-lubang akar, di dalam sambungan pipa dengan atau tanpa sisipan yang mampu lebur dimasuki dengan menggunakan pengelasan TIG karena penetrasi dapat dikontrol untuk memberikan suatu akhir siraman yang halus.
19 3.1 Bagan Alir penelitian
Bagan alir penelitian ditunjukkan di dalam gambar 3.1 :
Gambar 3.1 Diagram alir penelitian
Benda Uji (Stainless Steel 304),benda uji 1 mengalami pengelasan, benda uji 2,3,4,5 tidak mengalami pengelasan. Larutan HNO3 65 %
pH 0,2 dan 0,5 Pencelupan Benda Uji 1,2,3 ke dalam
Larutan HNO3 pH 0,2 dan benda 4,5
kedalam larutan HNO3 pH 0,5.
Direndam pada suhu 700C selama 6 jam, diturunkan sampai pada suhu 290C direndam selama 18 jam. Dilakukan
20
3.2 Bahan dan Peralatan A. Bahan
A.1 Spesimen / benda uji
Bahan yang digunakan sebagai spesimen adalah baja tahan karat 304, dengan komposisi : Cr = 18,358 %, Ni = 8,408 %, C = 0,047 %, Fe = 70,47 %
Gambar 3.2 Baja tahan karat 304 yang dilas
A.2 Larutan HNO3 65 %.
Gambar 3.3 Larutan HNO3 65 %.
B. Peralatan
Peralatan yang digunakan dalam penelitian ini adalah :
B.1 Tabung Reaksi, digunakan untuk merendam benda uji.
Gambar 3.4 Tabung reaksi
22
Gambar 3.5 pH meter digital
B.3 Timbangan Elektrik Digital, milik Laboratorium Analisis dan Instrumen, Jurusan Farmasi Universitas Sanata Dharma, Yogyakarta, dengan ketelitian sampai .
1000 1
gram
B.4 Water Bath digunakan untuk memanaskan larutan supaya dicapai suhu 700C, dan Thermometer untuk mengukur suhu larutan
Gambar 3.7 Water bath
3.3 Proses Pembuatan Larutan HNO3 pH 0,2 dan 0,5 Dan Proses
Perendaman
Proses pembuatan larutan HNO3 pH 0,2 dan 0,5 dari larutan HNO3 65 % dilakukan pencampuran dengan aquades.
Langkah-langkah dalam proses tersebut :
1. Peralatan dan bahan yang disiapkan : • Tabung reaksi
• Larutan HNO3 65 % • Pipet
24
2. Dalam keadaan normal kadar 1 N HNO3 = 63 gr/ltr HNO3 murni. Maka untuk memperoleh larutan HNO3 dengan pH 0,2 dari larutan HNO3 65 %, dengan berat jenis 1,39.
Dari hasil pengitungan diatas maka untuk mendapatkan larutan HNO3 dengan pH 0,2 maka diambil 34,23 ml/ltr.
Untuk memperoleh larutan HNO3 dengan pH 0,5 dari larutan HNO3 65 %, dengan berat jenis 1,39.
pH 0,5 = 10−0,5N
Dari hasil penghitungan diatas maka untuk memperoleh larutan HNO3 dengan pH 0,5 maka diambil 22,05 ml/ltr.
3. Spesimen dimasukkan ke dalam masing-masing tabung reaksi yang telah berisi Larutan HNO3 pH 0,2 dan 0,5.
4. Tabung reaksi dimasukkan ke dalam water bath sampai mencapai suhu 700 C. Untuk suhu 290 C tabung dimasukkan pada water bath yang tidak dipanaskan sehingga air pada water bath pada suhu kamar.
5. Proses pencelupan dilakukan pada suhu larutan dalam tabung 700 C selama 6 jam dan juga pada suhu 290C selama 18 jam. Hal ini untuk mendekatkan pada penggunaan secara nyata di dalam prakteknya.
6. Dalam waktu 1 minggu spesimen diambil, dikeringkan dan ditimbang. Setelah itu spesimen dicelup ke dalam larutan yang sama dengan volume sama yaitu 1 liter. Karena adanya penguapan maka setiap hari perlu ditambahkan larutan untuk menjaga pH dan kejenuhannya.
3.4 Analisis Hasil Penelitian
26
26
BAB IV
HASIL DAN PEMBAHASAN
4.1 Hasil penelitian pada Larutan HNO3 dengan pH 0,5
A. Stainless Steel Yang Mengalami Pengelasan TIG (Benda Uji I) Benda uji I adalah Stainless Steel 304 yang telah mengalami
pengelasan, direndam pada larutan HNO3 dengan pH 0,5.
Gambar benda uji I :
Gambar 4.3 Benda uji I
Data Spesimen (benda uji I)
1. Tebal benda uji = 2,75 mm
2. Tebal benda uji dengan las = 3,4 mm
3. Berat mula-mula = 18,238 gram
4. Panjang benda uji = 30 mm
5. Lebar benda uji = 26,5 mm
Data perubahan berat Stainless Steel 304 yang telah mengalami
28
Dalam persoalan ini digunakan ∆y dengan satuan gram dan waktu dihitung dalam satuan minggu. Hal ini dikarenakan untuk mempermudah pengamatan. Dalam penelitian ini benda uji
dicelupkan kedalam larutan HNO3 pH 0,5 dengan suhu 700C selama
6 jam dilanjutkan pada suhu 290C selama 18 jam setiap harinya. Hal
ini untuk mendekatkan pada keadaan sebenarnya.
Gambar 4.4 Keterangan luas benda uji
Luas spesimen = luas I + luas II + luas III
Luas I = 30 mm x 26,5 mm
= 795 mm2
Luas II = 30 mm x 26,5 mm
= 795 mm2
Luas III = (2p + 2l) x tebal
= 310,75 mm2
Luas spesimen = (795 mm2 + 795 mm2 + 310,75 mm2)
= 1900,75 mm2 = 0,190075 dm2
Luas I = Luas II
Dari data diperoleh laju korosi :
Laju korosi pada minggu I :
Berat mula-mula = 18,238 gram
Berat pada minggu I = 18,237 gram
Waktu = 168 jam
Maka diperoleh,
∆x = Berat mula-mula – Berat pada minggu I
= 18,238 gram – 18,237 gram = 0,001 gram
Laju korosi minggu II =
2
Data laju korosi SS 304 yang telah mengalami pengelasan yang
direndam dalam larutan HNO3 dengan pH0,5 :
Tabel 4.2 Laju korosi SS 304 setelah mengalami pengelasan dalam larutan HNO3 dengan pH0,5
30
B. Benda Uji II
Benda uji II merupakan pelat stainless steel yang tanpa
mengalami pengelasan.
Gambar 4.5 Benda uji II
Data Spesimen II :
1. Tebal benda uji = 2,75 mm
2. Berat mula-mula = 17,992 gram
3. Panjang benda uji = 54,5 mm
4. Lebar benda uji = 16,3 mm
Luas spesimen = luas I +luas II + luas III
Luas I = 54,5 mm x 16,3 mm
= 888,35 mm2
Luas II = 54,5 mm x 16,3 mm
= 888,35 mm2
Luas III = (2p + 2l) x tebal
= 389,4 mm2
Luas spesimen = (888,35 mm2 + 888,35 mm2 + 389,4 mm2)
Tabel 4.3 Data perubahan berat benda uji II pada larutan HNO3 dengan pH 0,5
Dari data diperoleh maka laju korosi :
Laju korosi minggu II =
2
Tabel 4.4 Laju korosi benda uji II pada larutan HNO3 dengan pH 0,5
32
C. Benda Uji III
Benda uji III merupakan pelat stainless steel tanpa mengalami
pengelasan. Benda uji III ini, sebelumnya telah mengalami
perendaman dalam larutan H2SO4 dengan pH 0,5 selama 13 minggu.
Kemudian dilanjutkan lagi dengan pencelupan ini.
Gambar 4.8 Benda uji III
Data Spesimen III
1. Tebal benda uji = 2,75 mm
2. Berat mula-mula = 13,845 gram
3. Panjang benda uji = 41 mm
4. Lebar benda uji = 16,45 mm
Luas spesimen = luas I +luas II + luas III
Luas I = 41 mm x 16,45 mm
= 674,45 mm2
Luas II = 41 mm x 16,45 mm
Luas III = (2p + 2l) x tebal
= 315,975 mm2
Luas spesimen = (674,45 mm2 + 674,45 mm2 + 315,975 mm2)
= 1664,875 mm2 = 0,1664875 dm2
Tabel 4.5 Data perubahan berat benda uji III pada larutan HNO3 dengan pH 0,5
No Minggu ke- Berat benda uji
Dari data diperoleh maka laju korosi :
Laju korosi minggu II =
34
Tabel 4.6 Laju korosi benda uji III pada larutan HNO3 dengan pH 0,5
No minggu
4.2 Hasil penelitian pada Larutan HNO3 dengan pH 0,2
A. Benda Uji IV
Benda uji IV merupakan pelat stainless steel yang tidak
mengalami pengelasan, dan sudah pernah mengalami perendaman
dalam larutan H2SO4. .
Data Percobaan Laju Korosi Stainless Steel 304 tanpa
mengalami pengelasan pada Larutan HNO3 pH 0,2.
Gambar benda uji IV :
Data Spesimen IV :
1. Tebal benda uji = 2,75 mm
2. Berat mula-mula = 19,428 gram
3. Panjang benda uji = 54,25 mm
Tabel 4.7 Data perubahan berat benda uji IV pada larutan HNO3 dengan pH 0,2
36
Tabel 4.8 Laju korosi benda uji IV pada larutan HNO3 dengan pH 0,2
No minggu
Benda uji IV merupakan pelat stainless steel yang tidak
mengalami pengelasan, dan sudah pernah mengalami perendaman
dalam larutan H2SO4.
Data Percobaan Laju Korosi Stainless Steel 304 tanpa
mengalami pengelasan pada Larutan HNO3 pH 0,2.
Gambar benda uji V :
Data Spesimen V :
1. Tebal benda uji = 2,75 mm
2. Berat mula-mula = 14,403 gram
3. Panjang benda uji = 41,3 mm
4. Lebar benda uji = 15 mm
Tabel 4.9 Data perubahan berat benda uji V pada larutan HNO3 dengan pH 0,2
38
Benda uji yang telah mengalami pengelasan maupun yang tidak
mengalami pengelasan dapat terkorosi, ini dapat diketahui karena adanya
pengurangan berat dari benda uji setelah mengalami perendaman dalam
larutan HNO3 pH 0,5 dan juga pada pH 0,2. Korosi yang terjadi secara
merata pada seluruh permukaan dikarenakan adanya kerusakan lapisan
uji yang mengalami pengelasan dengan benda uji yang tidak mengalami
pengelasan tidak ada perbedaan laju korosi yang signifikan, ini
dikarenakan hasil dari pengelasan yang cukup baik. Pada saat terjadi
pengurangan berat benda uji maka benda uji mengalami korosi karena ada
sebagian dari lapisan protective layer yang rusak. Pada saat benda uji
kembali tidak mengalami pengurangan berat atau beratnya stabil, maka
benda uji tidak mengalami korosi. Kemungkinan lapisan protective layer
yang telah rusak kembali terbentuk setelah terjadi reaksi oksidasi antara
Cr yang ada pada Stainless Steel dengan oksigen yang ada di lingkungan
bebas pada saat dilakukan penjemuran dengan sinar matahari sebelum
dilakukan pengukuran berat pada setiap satu minggu sekali. Dari
penampilan visual benda uji tidak ada perubahan warna dari sebelum
40
4.4. Grafik Laju Korosi
A. Larutan HNO3 pPH 0,5
Grafik 4.3 Grafik laju korosi stainless steel 304 dalam larutan HNO3 dengan pH 0,2
B. LarutanHNO3 pH 0,2
C. LarutanHNO3 pH 0,2 dan pH 0,5
Grafik 4.4 Grafik laju korosi stainless steel 304 pada larutan HNO3 dengan pH 0,2 dan pH 0,5
Dari data benda uji secara keseluruhan yang telah mengalami
perendaman selama 12 minggu pada larutan HNO3 dengan pH 0,2
dan pH 0,5 maka dapat diperoleh data sebagai berikut:
Benda uji I direndam dalam larutan HNO3 dengan pH 05
Berat awal : 18,238 gram
Berat akhir : 18,233 gram
Penurunan berat : 0,005 gram
Laju korosi/tahun =
190075 ,
0 12 52 005 ,
42
Tabel 4.11 Laju korosi benda uji pada larutan HNO3 dengan pH 0,2 selama 12 minggu
Benda
D. Grafik Laju korosi/Tahun SS 304 pada Larutan HNO3
pH 0,5 dan pH 0,2
44 5.1. Kesimpulan
Dari hasil penelitian, maka dapat diambil kesimpulan sebagai berikut :
1. Dari hasil penelitian selama 12 minggu maka dapat diambil kesimpulan, antara benda uji yang telah mengalami pengelasan dengan benda uji yang tidak mengalami pengelasan tidak ada perbedaan yang signifikan laju korosinya. Semuanya sama-sama mengalami korosi baik yang mengalami pengelasan maupun yang tidak mengalami pengelasan. Korosi yang terjadi merata pada seluruh permukaan benda uji karena rusaknya sebagian dari lapisan protective layer. Laju korosi rata-rata tertinggi terjadi pada pH 0,2 diprediksikan sebesar 0,139 gram/dm2/tahun , sedangkan untuk laju korosi rata-rata tertinggi yang terjadi pada pH 0,5 diprediksikan sebesar 0,113 gram/dm2/tahun.
5.2 Saran
1. Gunakanlah alat penimbang berat benda uji yang akurat dan jangan ganti-ganti timbangan.
DAFTAR PUSTAKA
Surdia, T., Saito, S.,1985, Pengetahuan Bahan Teknik, Pradnya Paramita, Jakarta.
Korosi, www.tasteel/main.php, diakses 05 April 2008
Kenyon, W, Diterjemahkan Dines Ginting, 1985, Dasar-dasar Pengelasan, Erlangga, Jakarta.
Chamberlain, J. & Trethewey, KR. Korosi Untuk Mahasiswa Dan Rekayasawan, Gramedia Pustaka Utama, Jakarta.
TIG Welding Proces, www.alu-info.dk/Html/alulib/modul/A00537.htm, diakses 23 juni 2008