B A B I I
TINJAUAN P U S T A K A _ :i r-. ., ^ 2.1. Tinjauan Umum Calkon
Senyawa calkon merupakan l,3-difenil-2-propen-l-on. Kedua cincin aromatis pada senyawa tersebut dihubungkan oleh 3 atom karbon yang merupakan sistem karbonil a, p t£ik jenuh (Patil dkk, 2009) seperti yang digambarkan di bawah ini.
O
Gambar 1. Rumus umum senyawa calkon (l,3-difenil-2-propen-l-on) (Sumber: Patil dkk, 2009)
Senyawa calkon mengandung gugus etilen keto (-CO-CH=CH-) yang reaktif. Adanya gugus tersebut menyebabkan molekul calkon mempunyai berbagai macam aktivitas biologi (Jayapal dan Sreedhar, 2010).
Senyawa calkon terdapat pada berbagai jenis tumbuhan di alam yang berperan sebagai senyawa perkursor untuk biosintesis flavonoid dan isoflavonoid (Patil dkk, 2009). Senyawa calkon juga berguna dalam sintesis berbagai macam senyawa heterosiklik seperti isoksazol, quinolinon, thiadiazin, benzofuranon, benzodiazepin dan lain sebagainya (Jayapal dkk, 2010).
Calkon biasanya disintesis melalui kondesasi Claisen-Schmidt dari suatu aldehid dan keton aromatik menggunakan katalis basa atau asam yang diikuti oleh reaksi dehidrasi (Patil dkk, 2009). Namun, dengan semakin berkembangnya teknik sintesis pada saat ini, metode sintesis calkon menjadi semakin beragam. Selain menggunakan katalis asam dan basa, juga dapat digunakan K2C03 anhidrat sebagai katalis dan sintesis dilakukan tanpa menggunakan pelarut dengan iradiasi microwave (Jayapal dan Sreedhar, 2010).
Dewasa ini, pemanfaatan senyawa calkon yang telah ditemukan baik melalui sintesis maupun isolasi telah banyak diaplikasikan di bidang farmasi, seperti sebagai zat sitotoksik dikarenakan beberapa calkon memiliki aktivitas sitotoksik, antivirus, anestesi, antimikroba, antitumor, antiulser, antijamur, antikanker, dan lain sebagainya (Jayapal dkk, 2010). Selain itu, calkon juga dapat digunakan sebagai antioksidan, anti-inflamasi, antihepatotoksik, antimalaria, dan beberapa calkon lainnya digunakan sebagai inhibitor tirosin dan juga dilaporkan memiliki aktivitas
hypoglycemic {Patil d]ik, 2009).
-2.2. Reaksi Kondensasi Aldol
Reaksi kondensasi adalah reaksi penggabungan dari dua atau lebih molekul yang sama atau berlainan dengan atau tanpa hilangnya suatu molekul kecil seperti air (Riawan, 1990). Sedangkan kondensasi aldol merupakan suatu reaksi organik yang dalam hal ini ion enolat bereaksi dengan senyawa karbonil membentuk P-hidroksi aldehida atau [3-hidroksi keton yang diikuti dengan dehidrasi membentuk enon terkonjugasi. Tahap pertama dari reaksi ini adalah reaksi aldol dan tahap kedua yaitu reaksi eliminasi, hilangnya molekul kecil seperti air (dehidrasi) yang diikuti dengan dekarboksilasi ketika gugus karbonil aktif ditambahkan (Fessenden dan Fessenden, 1994). Dalam kondensasi aldol, suatu ikatan karbon-karbon baru terbentuk antara atom karbon a dari satu senyawa karbonil dan atom karbon karbonil yang lainnya. Karena keasaman atom hidrogen a dari senyawa karbonil memungkinkan senyawa karbonil tersebut untuk bereaksi dengan yang lainnya sehingga menghasilkan suatu produk gabungan keduanya yaitu suatu aldehida dan suatu alkohol (Quellette, 1994). Reaksi kondensasi hampir mirip dengan reaksi polimerisasi. Perbedaanya, pada reaksi kondensasi, penggabungan hanya melibatkan dua atau tiga molekul yang berkondensasi, sedangkan pada polimerisasi dapat sampai ratusan atau bahkan jutaan molekul (Fessenden dan Fessenden, 1994). •>
Kata "aldol" diturunkan dari aldehida dan alkohol yang merupakan produk dari aldehida P-hidroksi bila direaksikan dengan alkil keton atau alkil aldehida (Hart, 1991). Dalam kondisi sedikit asam atau basa, keton
yang mempunyai minimal satu atom hidrogen a akan kehilangan proton yang kemudian akan menyerang aldehid dan membentuk produk aldol. Reaksi ini lebih spesifik dikenal sebagai reaksi kondensasi Claisen-Schmidt. 2.2.1. Reaksi kondensasi aldoi dengan katalis basa .
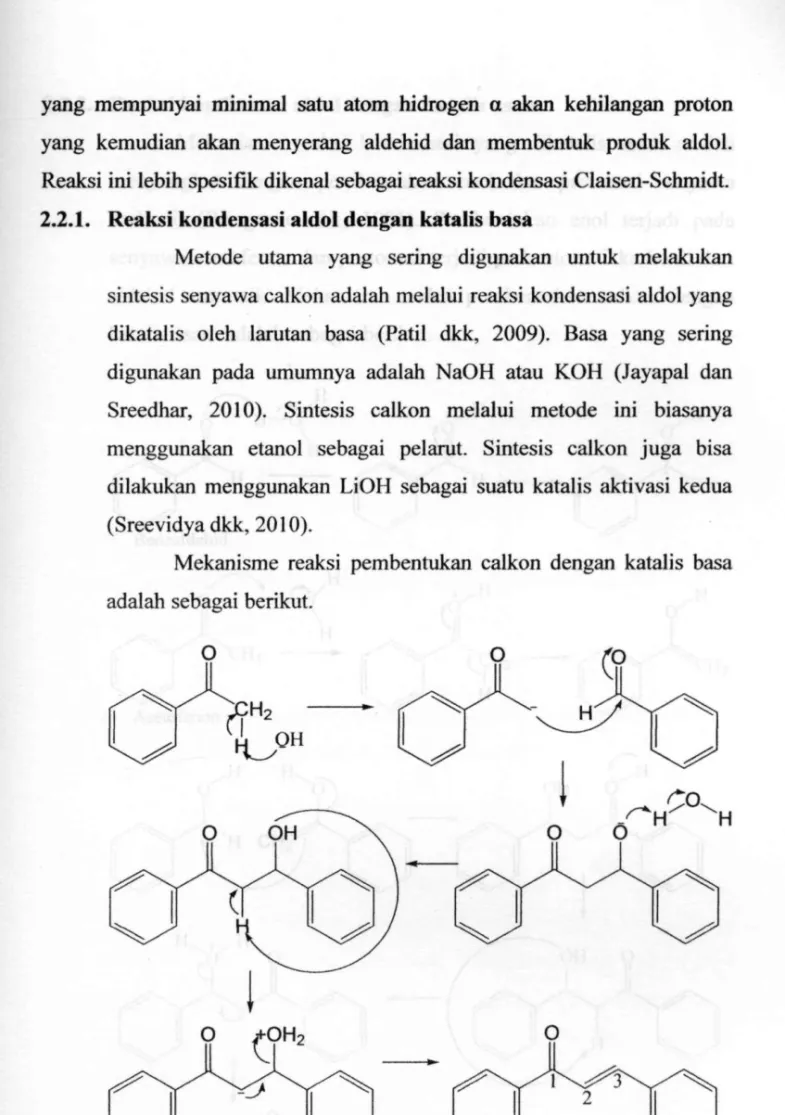
Metode utama yang sering digunakan untuk melakukan sintesis senyawa calkon adalah melalui reaksi kondensasi aldol yang dikatalis oleh larutan basa (Patil dkk, 2009). Basa yang sering digunakan pada umumnya adalah NaOH atau KOH (Jayapal dan Sreedhar, 2010). Sintesis calkon melalui metode ini biasanya menggunakan etanol sebagai pelarut. Sintesis calkon juga bisa dilakukan menggunakan LiOH sebagai suatu katalis aktivasi kedua (Sreevidya dkk, 2010).
Mekanisme reaksi pembentukan calkon dengan katalis basa
adalah sebagai berikut. ' '
2.2.2. Reaksi kondensasi aldol dengan katalis asam
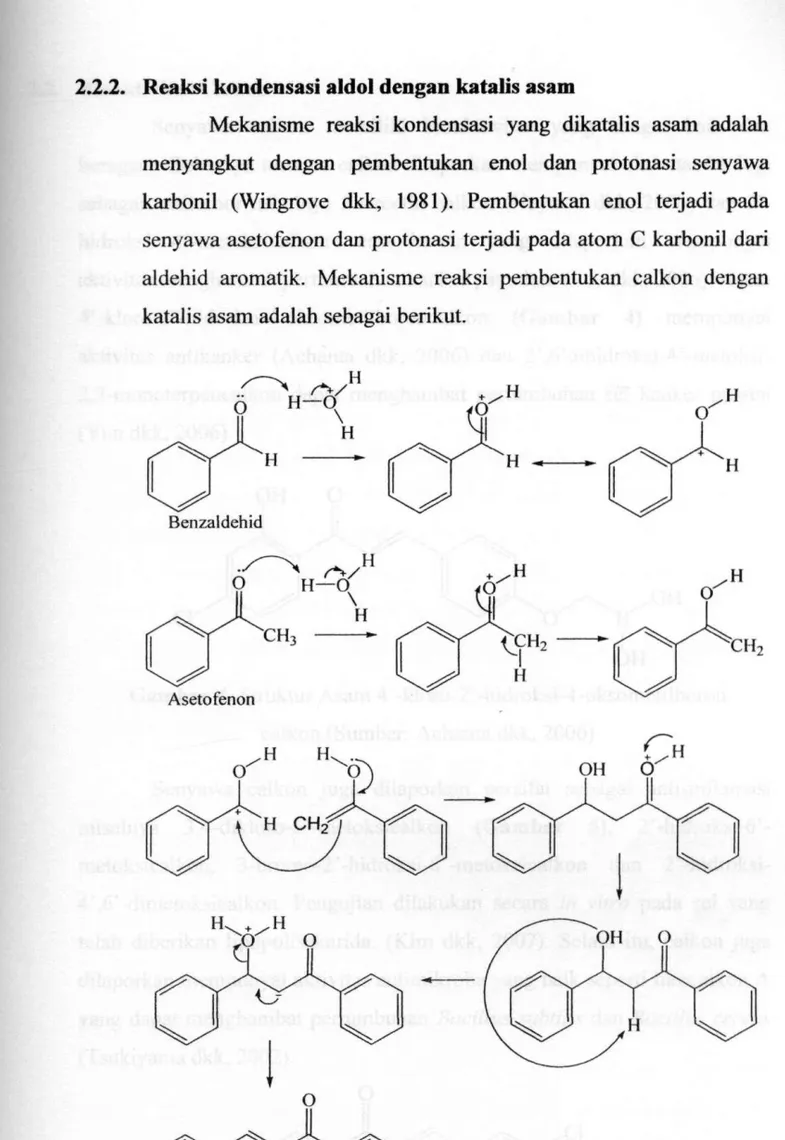
Mekanisme reaksi kondensasi yang dikatalis asam adalah menyangkut dengan pembentukan enol dan protonasi senyawa karbonil (Wingrove dkk, 1981). Pembentukan enol terjadi pada senyawa asetofenon dan protonasi terjadi pada atom C karbonil dari aldehid aromatik. Mekanisme reaksi pembentukan calkon dengan katalis asam adalah sebagai berikut. • ; r ,-r
Calkon
Gambar 3. Meknisme reaksi pembentukan senyawa calkon menggunakan katalis asam (Sumber: Patil dkk, 2009)
2.3. Bioaktivitas Calkon
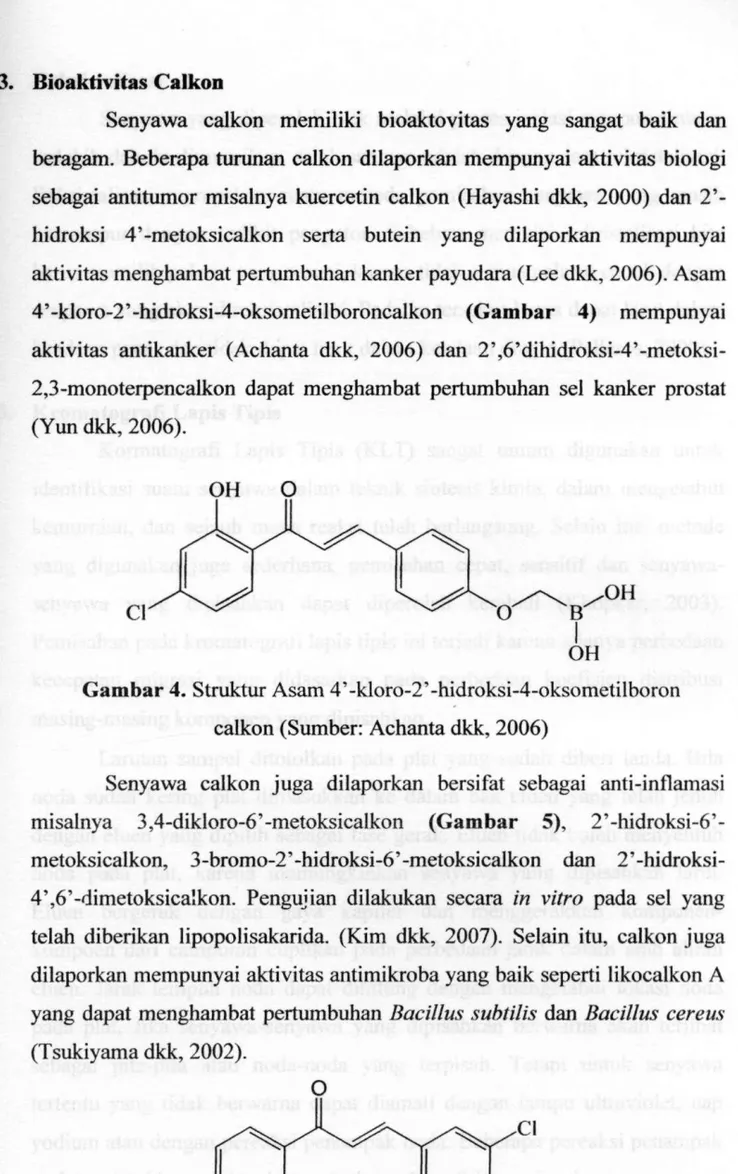
Senyawa calkon memiliki bioaktovitas yang sangat baik dan beragam. Beberapa turunan calkon dilaporkan mempimyai aktivitas biologi sebagai antitumor misalnya kuercetin calkon (Hayashi dkk, 2000) dan 2'-hidroksi 4'-metoksicalkon serta butein yang dilaporkan mempunyai aktivitas menghambat pertumbuhan kanker payudara (Lee dkk, 2006). Asam 4'-kloro-2'-hidroksi-4-oksometilboroncalkon (Gambar 4) mempunyai aktivitas antikanker (Achanta dkk, 2006) dan 2',6'dihidroksi-4'-metoksi-2,3-monoterpencalkon dapat menghambat pertumbuhan sel kanker prostat (Yun dkk, 2006).
.li'
Gambar 4. Struktur Asam 4'-kloro-2'-hidroksi-4-oksometilboron calkon (Sumber: Achanta dkk, 2006)
Senyawa calkon juga dilaporkan bersifat sebagai anti-inflamasi misalnya 3,4-dikloro-6'-metoksicalkon (Gambar 5), 6'-metoksicalkon, 3-bromo-6'-metoksicalkon dan 2'-hidroksi-4',6'-dimetoksicaIkon. Pengujian dilakukan secara in vitro pada sel yang telah diberikan lipopolisakarida. (Kim dkk, 2007). Selain itu, calkon juga dilaporkan mempunyai aktivitas antimikroba yang baik seperti likocalkon A yang dapat menghambat pertumbuhan Bacillus subtilis dan Bacillus cereus (Tsukiyama dkk, 2002).
O
Gambar 5. Struktur 3,4-dikloro-6'-metoksicalkon (Sumber: Kim dkk, 2007)
2.4. Rekristalisasi
Senyawa yang diperoleh baik melalui proses isolasi maupun sintesis terlebih dahulu dimumikan, salah satunya adalah dengan cara rekristalisasi. Rekristalisasi merupakan suatu metode pemisahan senyawa yang masih bercampur dengan sedikit pengotor. Sebelum memulai rekristalisasi kita harus memilih pelarut yang sesuai, karena tidak semua pelarut cocok dengan senyawa yang akan direkristalisasi. Padatan tersebut harus dapat larut dalam keadaan panas dan tidak dapat larut dalam keadaan dingin (Palleros, 2000).
2.5. Kromatografi Lapis Tipis
Kormatografi Lapis Tipis (KLT) sangat umum digunakan untuk identifikasi suatu senyawa dalam teknik sintesis kimia, dalam mengetahui kemumian, dan sejauh mana reaksi telah berlangsung. Selain itu metode yang digunakan juga sederhana, pemisahan cepat, sensitif dan senyawa-senyawa yang dipisahkan dapat diperoleh kembali (Khopkar, 2003). Pemisahan pada kromatografi lapis tipis ini terjadi karena adanya perbedaan kecepatan migrasi yang didasarkan pada perbedaan koefisien distribusi masing-masing komponen yang dipisahkan.
Larutan sampel ditotolkan pada plat yang sudah diberi tanda. Bila noda sudah kering plat dimasukkan ke dalam bak eluen yang telah jenuh dengan eluen yang dipilih sebagai fase gerak. Eluen tidak boleh menyentuh noda pada plat, karena memungkinkan senyawa yang dipisahkan larut. Eluen bergerak dengan gaya kapiler dan menggerakkan komponen-kompoen dari campuran cuplikan pada perbedaan jarak dalam arah aliran eluen. Jarak tempuh noda dapat dihitung dengan mengetahui lokasi noda pada plat. Jika senyawa-senyawa yang dipisahkan berwama akan terlihat sebagai pita-pita atau noda-noda yang terpisah. Tetapi untuk senyawa tertentu yang tidak berwama dapat diamati dengan lampu ultraviolet, uap yodium atau dengan pereaksi penampak noda. Beberapa pereaksi penam.pak noda yang biasa digunakan misalnya Carr-Price yaitu larutan antimon klorida 20% dalam kloroform, pereaksi serium sulfat dan pereaksi Liebermann-Burchard (Harbone, 1987).
Noda yang telah didapat ditandai dengan menggunakan pensil. Hal tersebut dilakukan untuk mencari harga Rf. Harga R f dapat diperoleh dengan cara membandingkan jarak antara noda dengan eluen. Harga R f berkisar antara nol sampai satu. . . . .
Rf = Jarak yang ditempuh sampel dari garis awal (cm) i u Jarak yang ditempuh eluen dari garis awal (cm)
2.6. Penentuan Titik Leleh
Titik leleh merupakan temperatur keadaan suatu kristal mulai meleleh sampai meleleh seluruhnya. Pemeriksaan titik leleh suatu senyawa yang tidak dikenal dapat dilakukan dengan menggunakan alat yang sederhana, misalnya Ordinary, Thiele, dan Fisher-Jones. Pengamatan titik leleh dilakukan secermat mungkin, terutama bila telah mendekati titik lelehnya. Jadi titik leleh sebenamya merupakan harga antara yang dimaksud tidak boleh lebih dari 2°C (Seager dan Slabaugh, 1980). Penentuan titik leleh diperlukan untuk penentuan kemumian dan identifikasi senyawa tak dikenal
2.7. Metode Karakterisasi
Dalam penentuan karakterisasi suatu senyawa kimia ada beberapa metode yang digunakan. Secara umum metode yang biasa digunakan adalah teknik spektroskopi. Diantaranya adalah spektroskopi ultraviolet (UV), inframerah (IR), spektroskopi massa (MS) dan resonansi magnetik inti
(Nuclear Magnetic Resonance, NMR). Semua metode ini menghasilkan data
spektroskopi yang dapat digunakan untuk mengidentifikasi senyawa-senyawa bahan alam dan senyawa-senyawa-senyawa-senyawa kimia yang belum diketahui. 2.7.1. Spektroskopi ultraviolet
Spektroskopi ultraviolet digunakan untuk mengidentifikasi ikatan rangkap terkonjugasi dalam suatu molekul kimia. Spektmm ultraviolet dari suatu senyawa organik berhubungan dengan transisi elektron dari satu tingkat energi ke tingkat energi yang lebih tinggi. Transisi ini pada umunmya terjadi antara orbital ikatan atau orbital bonding yang tidak berisi (Sudjadi, 1983).
2.7.2. Spektroskopi inframerah
Spektroskopi inframerah digunakan untuk menentukan gugus fiingsi dalam suatu senyawa berdasarkan energi vibrasi dari suatu
molekul. Adanya vibrasi molekul dapat memberikan sifat-sifat yang 7, khas dari suatu senyawa dalam spektrum inframerah yang
dihasilkan. Pancaran inframerah pada umumnya mengacu pada bagian spektrum elektromagnetik yang terletak diantara daerah tampak dan daerah gelombang mikro. Penggunaan spektrum inframerah dalam kimia organik menggunakan daerah yang berkisar pada bilangan gelombang 666-4000 cm"' (Silverstain dkk, 1986). 2.7.3. Spektroskopi NMR
Spektroskopi NMR (Nuclear Magnetic Resonance) atau Resonansi Magnetik Jnti (RMI) digunakan untuk mengidentifikasi lingkungan proton dan untuk mengidentifikasi jumlah atom karbon pada suatu senyawa. Metode spektroskopi ini didasarkan pada pengukuran absorbs! radiasi elektromagnetik oleh partikel yang sedang berputar. (Fessenden dan Fessenden, 1994).
Antibakteri ::.;;:!.;••>, Senyawa antibakteri merupakan senyawa yang dapat menghambat
dan mengurangi pertumbuhan bakteri yang bersifat patogen maupun yang non-patogen. Senyawa-senyawa kimia yang dapat menghambat pertumbuhan bakteri terdiri dari garam logam-logam, senyawa fenol, formaldehid, alkohol, yodium, senyawa klor, deterjen, sulfonamida dan antibiotik (Tortora, 2001). Suatu zat kimia yang hanya dapat menghambat pertumbuhan bakteri disebut bakteriostatik. Sedangkan zat kimia yang dapat
mematikan bakteri disebut bakterisida (Dwidjoseputro, 1994). . Bakteri merupakan suatu mikroorganisme hidup bersel satu (uni
seluler) yang sangat penting dan beraneka ragam yang dapat berhubungan dengan makanan bahkan dengan manusia. Ada bakteri yang dapat mengakibatkan pembusukan yang tidak diinginkan pada makanan dan
menimbulkan penyakit dan ada pula bakteri yang menguntungkan diantaranya dapat melangsungkan fermentasi (Buckle dkk, 1985).
Staphylococcus aureus, Escherichia coli, dan Bacillus subtilis
merupakan contoh bakteri patogen yang dapat menyebabkan penyakit bagi manusia. Setiap jaringan atau alat tubuh dapat diinfeksi oleh bakteri S.
aureus dan menyebabkan timbulnya penyakit dengan tanda-tanda khas,
yaitu peradangan dan pembentukan abses. S. aureus dapat menyebabkan pneumonia, meningitis, endokarditis, dan infeksi kulit (Jawetz dkk, 2001).
E. coli banyak ditemukan di dalam usus besar manusia sebagai
flora normal, tetapi bila kesehatan menurun, bakteri ini dapat bersifat patogen terutama akibat toksin yang dihasilkan. E. coli umumnya tidak menyebabkan penyakit bila masih berada dalam usus, tetapi dapat menyebabkan penyakit pada saluran kencing, paru, saluran empedu, dan saluran otak. E. coli dapat menyebabkan penyakit seperti diare, infeksi saluran kemih, pneumonia, meningitis pada bayi yang baru lahir dan infeksi luka.
B. subtilis merupakan bakteri Gram positif, bersifat aerob dan
berbentuk basil panjang yang disebut streptobasil. B. subtilis banyak ditemukan dalam tanah, air dan berbagai jenis makanan (Hans dan Schmidt,
1994). Bakteri ini dikenal sebagai penyebab keasaman dari makanan kaleng karena fermentasi gula yang dikandung pada makanan tersebut (Buckle dkk,
1985).
Penyakit-penyakit yang ditimbulkan oleh bakteri di atas dapat diatasi dengan penggunaan antibiotik. Antibakteri ataupun antibiotik dapat menghambat ataupun membunuh bakteri dengan cara menyerang situs tertentu yang ada pada bakteri. Secara umum, kemungkinan situs serangan suatu zat antibakteri dapat diduga dengan meninjau struktur serta komposisi sel bakteri. Kerusakan pada salah satu situs dapat mengawali terjadinya perubahan-perubahan yang menuju kepada matinya sel tersebut. Mekanisme kerja antibakteri menurut Pelczar dan Chan (1988) adalah sebagai berikut.
1. Kerusakan pada dinding sel 2. perubahan permeabilitas sel
3. Perubahan molekul protein dan asam nukleat 4. Penghambatan kerj a enzim
5. Penghambatan sintesis asam nukleat dan protein
2.9. Calkon sebagai Antibakteri
Penggunaan antibiotik yang terus menerus menyebabkan berkembangnya resistensi mikroorganisme terutama bakteri terhadap antibiotik. Untuk mengatasi permasalahan tersebut, seiain harus memikirkan cara mencegah resistensi bakteri terhadap antibiotik, juga perlu dilakukan penelitian untuk penemuan antibiotik-antibiotik baru dikarenakan tidak semua resistensi bakteri terhadap antibiotik dapat dicegah.
Calkon merupakan salah satu senyawa kimia yang sangat berpotensi sebagai antibakteri ataupun antibiotik altematif seperti likocalkon A yang dapat menghambat pertumbuhan Bacillus subtilis dan Bacillus cereus (Tsukiyama dkk, 2002). Selain itu, calkon juga mempakan senyawa intermediet untuk sintesis senyawa flavanoid lain seperti flavanon, flavon, flavanol dan lain sebagainya yang juga dikenal mempunyai bioaktivitas sebagai antibakteri dan antijamur (Vender dkk, 1993).
Senyawa calkon mengandung gugus etilen keto (-CO-CH=CH-) yang reaktif (Jayapal dan Sreedhar, 2010). Struktur keton a, p tak jenuh pada senyawa calkon tersebut diketahui bertanggung jawab terhadap sifat antimikroba senyawa calkon (Lahtchev dkk, 2008). Sifat antimikroba calkon juga tergantung pada substituen yang terikat pada kedua cincin aromatik
calkon, seperti gugus CI, Br, OH dan lain sebagainya. Jika pada cincin aromatik mempunyai gugus elektronegatif seperti Br, CI dan OH, aktivitas antimikrobanya sebanding dengan kloramfenikol (Prasad dkk, 2006).