perpustakaan.uns.ac.id digilib.uns.ac.id
commit to user
KAJIAN SINTESIS DAN KARAKTERISASI
Mg-Al HYDROTALCITE
PENGHILANGAN ION KALSIUM
Ditulis dan diajukan untu
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN
i
KAJIAN SINTESIS DAN KARAKTERISASI
HYDROTALCITE-LIKE DARI BRINE WATER
PENGHILANGAN ION KALSIUM
Disusun oleh: DWI WAHYUNI
M0307010
SKRIPSI
Ditulis dan diajukan untuk memenuhi sebagian persyaratan mendapatkan gelar Sarjana Sains
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN UNIVERSITAS SEBELAS MARET
SURAKARTA Juli, 2012
KAJIAN SINTESIS DAN KARAKTERISASI
BRINE WATER TANPA
k memenuhi sebagian persyaratan
perpustakaan.uns.ac.id digilib.uns.ac.id
commit to user
Jurusan Kimia Fakultas Matematika dan Ilmu Pengetahuan Alam Universitas Maret Surakarta Telah Mengesahkan Skripsi Mahasiswa:
Dwi Wahyuni M0307010, dengan judul ”
Hydrotalcite-Like Dari
Pembimbing
Dr. Eddy Heraldy, M.Si NIP. 19640305 200003 1002
Dipertahankan di depan TIM Penguji Skripsi pada:
Hari Tanggal
Anggota TIM Penguji :
1. Dr. Fitria Rahmawati, M. Si NIP. 19751010 200003 2001 2. Edi Pramono, M. Si NIP. 19830918 200812 1003 Fakultas Matem HALAMAN PENGESAHAN
Jurusan Kimia Fakultas Matematika dan Ilmu Pengetahuan Alam Universitas Maret Surakarta Telah Mengesahkan Skripsi Mahasiswa:
hyuni M0307010, dengan judul ” Kajian Sintesis Dan Karakterisasi Dari Brine Water Tanpa Penghilangan Ion Kalsium
Skripsi ini dibimbing oleh :
Pembimbing I
Dr. Eddy Heraldy, M.Si. NIP. 19640305 200003 1002
Pembimbing II
I.F. Nurcahyo, M. Si. NIP. 19780617 200501 1001
Dipertahankan di depan TIM Penguji Skripsi pada:
: Kamis : 26 Juli 2012 : Dr. Fitria Rahmawati, M. Si 1... 19751010 200003 2001 amono, M. Si 2... 19830918 200812 1003 Disahkan Oleh: Jurusan Kimia
Fakultas Matematika dan Ilmu Pengetahuan Alam Universitas Sebelas Maret Surakarta
Ketua Jurusan Kimia
Dr. Eddy Heraldy, M.Si. NIP. 19640305 200003 1002
Jurusan Kimia Fakultas Matematika dan Ilmu Pengetahuan Alam Universitas Sebelas
Kajian Sintesis Dan Karakterisasi Mg-Al Tanpa Penghilangan Ion Kalsium”
Pembimbing II
F. Nurcahyo, M. Si. NIP. 19780617 200501 1001
Dipertahankan di depan TIM Penguji Skripsi pada:
1...
perpustakaan.uns.ac.id digilib.uns.ac.id
commit to user PERNYATAAN
Dengan ini saya menyatakan bahwa skripsi saya yang berjudul ”KAJIAN SINTESIS DAN KARAKTERISASI Mg-Al HYDROTALCITE-LIKE DARI BRINE WATER
TANPA PENGHILANGAN ION KALSIUM ” adalah benar-benar hasil penelitian sendiri dan tidak terdapat karya yang pernah diajukan untuk memperoleh gelar kesarjanaan di suatu perguruan tinggi, dan sepanjang pengetahuan saya juga tidak terdapat kerja atau pendapat yang pernah ditulis atau diterbitkan oleh orang lain, kecuali yang secara tertulis diacu dalam naskah ini dan disebutkan dalam daftar pustaka.
Surakarta, Juli 2012
perpustakaan.uns.ac.id digilib.uns.ac.id
commit to user
KAJIAN SINTESIS DAN KARAKTERISASI Mg-Al HYDROTALCITE-LIKE
DARI BRINE WATER TANPA PENGHILANGAN ION KALSIUM
DWI WAHYUNI
Jurusan Kimia. Fakultas Matematia dan Ilmu Pengetahuan Alam. Universitas Sebelas Maret
ABSTRAK
Telah dilakukan sintesis dan karakterisasi Mg-Al hydrotalcite-like dari brine water tanpa penghilangan ion kalsium. Penelitian bertujuan untuk memanfaatkan limbah desalinasi (brine water) sebagai bahan dasar sintesis Mg-Al hydrotalcite-like
tanpa penghilangan ion kalsium dengan metode kopresipitasi pada perbandingan rasio molar Mg/Al (2:1), suhu 65oC, pH 10 selama satu jam reaksi. Hasil sintesis diidentifikasi menggunakan X-Ray Diffractometer (XRD), Fourier Transform Infrared Spectrosphotomete (FTIR), X-Ray Fluorescence (XRF), Surface Area Analyzer (SAA), Thermo Gravimetric/Differential Thermal Analyzer (TG/DTA). Hasil karakterisasi sampel dari analisis kualitatif XRD menunjukkan bahwa terdapat anion penyeimbang muatan CO32- pada Mg-Al hydrotalcite-like. Hasil karakterisasi FTIR menunjukkan adanya uluran O-H pada bilangan gelombang 3466,08 cm-1. 1629,85 cm-1 merupakan tekukan O-H, 1361,74 cm-1 merupakan uluran simetris CO32-, 449,41cm-1 dan 536,21 cm-1 uluran Mg-O dan Al-O serta 713,66 cm-1 merupakan uluran Ca-O. Adanya ikatan Mg-O, Al-O, Ca-O serta gugus hidroksil dan karbonat mengidentifikasikan senyawa yang disintesis merupakan hydrotalcite like. Analisis XRF menunjukkan adanya kandungan Al, Mg serta Ca di dalam
hydrotalcite-like serta terjadi proses dehidrogenasi dan dekarboksilasi pada analisis TG/DTA. Luas permukaan dan jari-jari pori Mg-Al hydrotalcite-like adalah 154,898 m2/g dan 44,8632 Å. Penambahan zat aktif KF dapat menurunkan luas permukaan dan jari-jari pori Mg-Al hydrotalcite-like tetapi juga mampu meningkatkan kristalinitas hydrotalcite.
Kata kunci: Sintesis, karakterisasi, brine water, ion kalsium, Mg-Al hydrotalcite like, Kalium Fluorida.
perpustakaan.uns.ac.id digilib.uns.ac.id
commit to user
THE STUDY OF SYNTHESIS AND CHARACTERIZATION OF Mg-Al HYDROTALCITE LIKE FROM BRINE WATER WITHOUT CALCIUM ION
ELIMINATION DWI WAHYUNI
Department of Chemistry. Mathematic and Natural Science Faculty. Sebelas Maret Univercity
ABSTRACT
The synthesis and characterization of Mg-Al hydrotalcite-like from brine water without calcium ion elimination have been carried out. The aim of the research is to use brine water as raw material for the synthesis Mg-Al hydrotalcite-like without the removal of calcium ion. The synthesis method is co-precipitation at molar ratio of Mg to Al is 2:1 at 65 oC, pH of reaction is 10 and the reaction time is 1 hour. The prepared materials were identified by X-Ray Diffractometer (XRD), Fourier Transform Infrared Spectrophotometer (FTIR), X-Ray Fluorescence (XRF), Surface Area Analyzer (SAA) and Thermo Gravimetric/Differential Thermal Analyzer (TG/DTA). The XRD pattern shows the present of CO32- anion in Mg-Al hydrotalcite-like. The result of FTIR characterization shows the presence of –OH streching at wavenumber 3466.08 cm-1, 1629.85 cm-1 the presence of –OH bending, 1361.74 cm-1 the presence of CO32- symmetric streching, 449.1 cm-1 and 536.21 cm-1 are Mg-O streching and Al-O. And 713.66 cm-1 is the Ca-O streching. The presence of Mg-O bonds, Al-O bonds, hydroxyl and carbonate groups which is characterized as O-H bending indicates that the prepared material is Mg-Al hydrotalcite-like. The XRF analysis show a contents of Al, Mg and Ca in hydrotalcite-like and process dehydrogenation and decarboxylation in the analys of TG/DTA. The surface area and the pore radius of Mg-Al hydrotalcite-like 154.898 m2/g and 44.8632 Å. The addition of the active substance KF can reduce the surface area and pore radius of Mg-Al hydrotalcite-like and also improve the hydrotalcite cristallinity.
Keywords: Synthesis, Characterization, Brine Water, Calcium Ion, Mg-Al Hydrotalcite-Like, Photasium Fluoride
perpustakaan.uns.ac.id digilib.uns.ac.id
commit to user
MOTTO
“...
Dan barang siapa yang taat kepada Allah SWT,
dan Rosul-NYA dan takut kepada Allah SWT dan
bertaqwa kepada-NYA, maka mereka adalah
orang-orang yang mendapat kemenangan...”
(QS An-Nur : 52)
“...
“...
“...
“...Kesempurnaan hanya milik ALLAH SWT,
Kesempurnaan hanya milik ALLAH SWT,
Kesempurnaan hanya milik ALLAH SWT,
Kesempurnaan hanya milik ALLAH SWT,
tapi berusahalah menjadi sempurna
tapi berusahalah menjadi sempurna
tapi berusahalah menjadi sempurna
tapi berusahalah menjadi sempurna agar
agar
agar
agar
mereka
mereka
mereka
mereka (keluarga) bangga
(keluarga) bangga
(keluarga) bangga
(keluarga) bangga karena
karena
karena telah
karena
telah
telah
telah
memilikimu
memilikimu
memilikimu
memilikimu...”
...”
...”
...”
“...
jangan kau jadikan semua
cobaan-Nya sebagai penghalang
tapi jadikan itu sebagai kekuatan
untuk menjadikanmu sebagai sang
perpustakaan.uns.ac.id digilib.uns.ac.id
commit to user PERSEMBAHAN
Karya ini saya persembahkan untuk kalian
,
☺
Orangtuaku tersayang “
Orangtuaku tersayang “
Orangtuaku tersayang “
Orangtuaku tersayang “Bapak &
Bapak &
Bapak & Ibu
Bapak &
Ibu
Ibu””””
Ibu
☺
maaf kalau tidak bisa menyelesaikan ini semua tepat
waktu.Terimakasih atas semua bimbingan, cinta, kasih
sayang dan doa yang tak henti-hentinya selama ini.
☺
Saudaraku
Saudaraku
Saudaraku
Saudaraku tercinta “
tercinta “
tercinta “Astuti
tercinta “
Astuti &
Astuti
Astuti
&
&
& Bekti
Bekti
Bekti
Bekti””””
☺
yang selalu memberikan dukungan untukku.
☺
Sahabat
Sahabat
Sahabat
Sahabat----sahabatku
sahabatku
sahabatku
sahabatku ““““Melina, Pipit, Furi,
Melina, Pipit, Furi,
Melina, Pipit, Furi,
Melina, Pipit, Furi,
Husna, Nila, Siwi, Irma
Husna, Nila, Siwi, Irma
Husna, Nila, Siwi, Irma
Husna, Nila, Siwi, Irma””””
☺
yang telah setia memberikan semangat dan motivasi serta
kebersamaanya.
perpustakaan.uns.ac.id digilib.uns.ac.id
commit to user KATA PENGANTAR
Puji Syukur kehadirat Tuhan Yang Maha Esa yang telah melimpahkan rahmat, karunia, dan ijin-Nya sehingga penulis dapat menyelesaikan penulisan skripsi ini untuk memenuhi sebagian persyaratan guna mencapai gelar Sarjana Sains dari Jurusan Kimia Fakultas Matematika dan Ilmu Pengetahuan Alam, Universitas Sebelas Maret.
Skripsi ini tidak akan selesai tanpa adanya bantuan dari banyak pihak, karena itu dengan kerendahan hati penulis menyampaikan terimakasih kepada :
1. Prof. Ir. Ari Handono Ramelan., M.Sc., Ph.D., selaku dekan Fakultas Matematika dan Ilmu Pengetahuan Alam Universitas Sebelas Maret Surakarta.
2. Dr. Eddy Heraldy., M.Si., selaku ketua jurusan FMIPA UNS dan sebagai pembimbing I.
3. I. F. Nurcahyo, M.Si., selaku pembimbing II. 4. Drs. Pranoto, M.Si., selaku pembimbing Akademik. 5. Bapak Ibu dosen dan seluruh staf jurusan Kimia.
6. Kedua orang tua serta seluruh keluarga atas doa, dukungan dan motivasi yang diberikan untuk segera menyelesaikan karya ini.
7. Teman-teman seperjuangan tyas, eka, tyo, fajar, jati, muri dan devi, warga dewi sumbi (mel, dini, trias, arti, dito), mas dedi, om lala serta teman-teman kimia ’07 atas semangat dan dukungannya.
8. Semua pihak yang tidak mungkin disebutkan satu per satu, terimakasih atas semua dukungannya selama ini.
Penulis menyadari bahwa skripsi ini masih jauh dari sempurna. Oleh karena itu, penulis mengharapkan kritik dan saran yang membangun dari semua pihak dalam menyempurnakan skripsi ini. Penulis berharap, semoga karya kecil ini dapat memberikan manfaat bagi ilmu pengetahuan dan pembaca.
Surakarta, Juli 2012
perpustakaan.uns.ac.id digilib.uns.ac.id
commit to user DAFTAR ISI
HALAMAN JUDUL ... i
HALAMAN PENGESAHAN ... ii
HALAMAN PERNYATAAN... ... iii
HALAMAN ABSTRAK... ... iv
HALAMAN ABSTRACT ... . v
HALAMAN MOTTO ... vi
HALAMAN PERSEMBAHAN ... vii
KATA PENGANTAR ... viii
DAFTAR ISI ... ix
DAFTAR TABEL ... xi
DAFTAR GAMBAR ... xii
DAFTAR LAMPIRAN ... xiii
BAB I. PENDAHULUAN ... 1
A. Latar Belakang Masalah ... 1
B. Perumusan Masalah ... 3 1. Identifikasi Masalah ... 3 2. Batasan Masalah ... 4 3. Rumusan Masalah ... 5 C. Tujuan Penelitian ... 5 D. Manfaat Penelitian ... 5
BAB II. LANDASAN TEORI ... 7
A. Tinjauan Pustaka ... 7
1. Komposisi Dan Pengolahan Air Laut... ... 7
2. Hydrotalcite ... 8
3. Kalium Fluorida... ... 12
4. Karakterisasi hydrotalcite-like... . 13
B. Kerangka Pemikiran ... 21
C. Hipotesis ... 22
perpustakaan.uns.ac.id digilib.uns.ac.id
commit to user
A. Metode Penelitian ... 23
B. Tempat dan Waktu Penelitian ... 23
C. Alat dan Bahan ... 23
D. Prosedur Penelitian ... 24
1. Sintesis dan Karakterisasi Mg-Al hydrotalcite-like ... 24
2. Preparasi KF/Mg-Al hydrotalcite-like dan Karakterisasi ... 24
E. Teknik Pengumpulan Data ... ... 24
F. Teknik Analisis Data... ... 25
BAB IV. HASIL PENELITIAN DAN PEMBAHASAN ... 27
A. Sintesis dan Karakterisasi Mg-Al hydrotalcite-like dari Brine Water ... ... 27
B. Efek ion kalsium pada karakteristik Mg-Al hydrotalcite-like ... 32
C. Sintesis dan Karakterisasi Mg-Al hydrotalcite-like ... ... 35
BAB V. KESIMPULAN DAN SARAN ... 40
A. Kesimpulan ... 40
B. Saran ... 41
DAFTAR PUSTAKA ... 42
perpustakaan.uns.ac.id digilib.uns.ac.id
commit to user DAFTAR TABEL
Tabel 1. Tabel 1. Komposisi kimia air laut dan brine water
(Heraldy et al., 2010)... 7
Tabel 2. Gugus-gugus fungsi Mg/Al hydrotalcite-like ... ... 14
Tabel 3. Komponen penyusun hydrotalcite-like (Wegrzyn et al., 2010)... 19
Tabel 4. XRF komposisi sampel hydrotalcite (Carja et al., 2002)... 19
Tabel 5. Harga d tiga puncak tertinggi senyawa hasil sintesis... ... 30
Tabel 6. Tabulasi gugus fungsi hydrotalcite-like... ... 31
Tabel 7. Komposisi Mg-Al hydrotalcite-like dengan XRF... ... 33
Tabel 8. Data analisis termal TG/DTA... ... 34
Tabel 9. Tabulasi intensitas d003, d006dan d009.... ... 35
Tabel 10. Hasil analisis luas muka spesifik, volume pori total dan rerata jejari pori sampel Mg-Al hydrotalcite-likea... .... 36
Tabel 11. Karakteristik sifat fisik hasil sintesis... ... 37
Tabel 12. Tabulasi intensitas d003, d006dan d009... ... 37
Tabel 13. Hasil analisis luas muka spesifik, volume pori total dan rerata jejari pori sampel KF/Mg-Al hydrotalcite-likea... .... 39
perpustakaan.uns.ac.id digilib.uns.ac.id
commit to user DAFTAR GAMBAR
Gambar 1. Struktur lapisan LDH (Raki et al. 2004) ... 10
Gambar 2. Struktur lapisan hydrotalcite ... 10
Gambar 3. Spektra FTIR dari LDH dengan perbedaan rasio molar. A spektra OH, B spectra serapan H2O, C spektra serapan -CO32- dan D spektra serapan [Metal]-OH stretching. (Kang et al.,2005). ... ... 15
Gambar 4. Spektra FTIR Ca-Al LDH Raki and Beaudoin (2008). ... 15
Gambar 5. Difraktogram XRD LDH dengan perbedaan rasio mol (a) Mg/Al=2 (b) Mg/Al=2.5(c) Mg/Al=3 (Kang et al. 2005)... ... 16
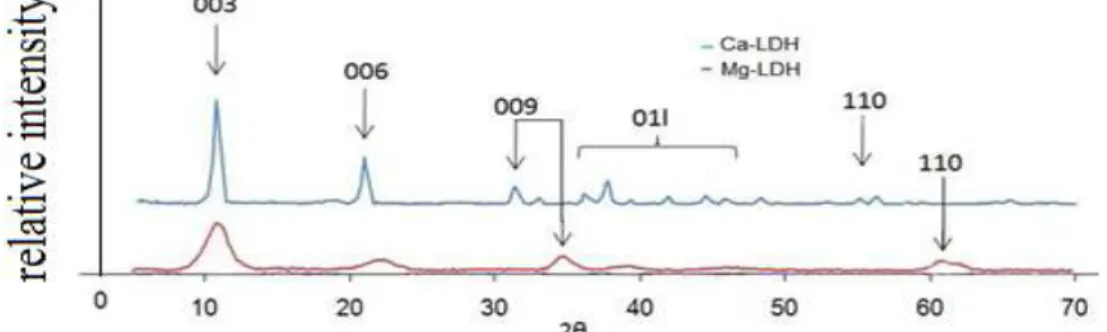
Gambar 6. Difraktogram Ca-LDH dan Mg-LDH (Fayyazbakhsh et al. 2012)... ... 16
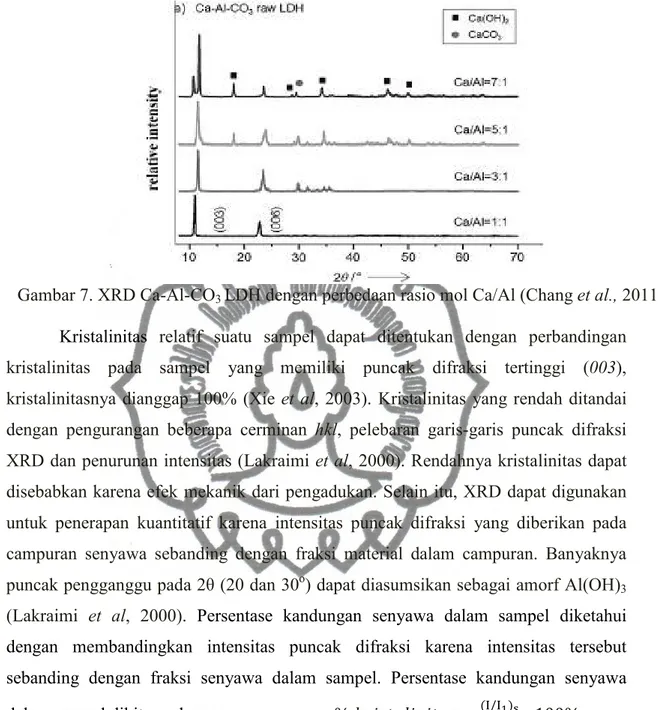
Gambar 7. XRD Ca-Al-CO3 LDH dengan perbedaan rasio mol Ca/Al (Chang et al., 2011)... .... 20
Gambar 8. TG/DTA Mg/Al hydrotalcite dengan rasio mol Mg/Al (2,0) dengan variasi suhu pemanasan selama 11 jam. (A) 70 oC (B) 110 oC dan (C) 140 oC... .. 22
Gambar 9. TG/DTA Ca/Al LDH (Raki et al., 2004)... . 20
Gambar 10. TG/DTA KF/Mg(Al)O-dy (Xu et al., 2011)... ... 20
Gambar 11. Difraktogram XRD ... ... 28
Gambar 12. Difraktogram XRD Mg-Al hydrotalcite... ... 29
Gambar 13. Spektra FTIR (a) Mg-Al hydrotalcite-likea (b) Mg-Al hydrotalcite-like (Setyowati, 2011)... ... 32
Gambar 14. Difraktogram XRD KF/ Mg-Al hydrotalcite-likea ... ... 35
Gambar 15. Difraktogram XRD KF/ Mg-Al hydrotalcite-likea... ... 37
Gambar 16. Spektra FTIR (A) KF/Mg-Al hydrotalcitea (B) KF/Mg-Al hydrotalcite-like (Setyowati, 2011)... .. 38
perpustakaan.uns.ac.id digilib.uns.ac.id
commit to user DAFTAR LAMPIRAN
Lampiran 1. Perhitungan Sintesis Mg/Al Hydrotalcite-Like ... 46 Lampiran 2. Desain Penelitian ... 48 Lampiran 3. Skema Sintesis Mg/Al Hydrotalcite-Like... ... 49 Lampiran 4. Data X-Ray Diffraction (XRD) Mg-Al Hydrotalcite
Tanpa Penghilangan Ion Kalsium ... 50 Lampiran 5. Data X-Ray Diffraction (XRD) KF/Mg-Al Hydrotalcite ... 51 Lampiran 6. Data JCPDS Mg/Al Hydrotalcite ... 52 Lampiran 7. Perbanbingan Harga d Sampel Mg-Al Hydrotalcite-Like
Dengan Data JCPDS Mg-Al Hydrotalcite-Like Dan
Perhitungan Persentase Relatif... 53 Lampiran 8. Perbanbingan Harga d Sampel Mg-Al Hydrotalcite-Like
Dengan Data JCPDS Mg-Al Hydrotalcite-Like Dan
Perhitungan Persentase Relatif... 55 Lampiran 9. Spektra FTIR... ... 57 Lampiran 10. Kurva Luas Area Mg-Al Hydrotalcite Dengan Metode BET .... 60 Lampiran 11. Kurva Luas Area Mg-Al Hydrotalcite Dengan Metode BJH.. ... 60 Lampiran 12. Kurva Luas Area KF/Mg-Al Hydrotalcite Dengan
Metode BET... ... 62 Lampiran 13. Kurva Luas Area KF/Mg-Al Hydrotalcite Dengan
Metode BJH... ... 63 Lampiran 14. Kurva TG/DTA... ... 64 Lampiran 15. Data XRF.. ... 65
perpustakaan.uns.ac.id digilib.uns.ac.id
commit to user 1
BAB I PENDAHULUAN
A.Latar Belakang Masalah
Indonesia dikenal sebagai negara maritim karena sebagian besar wilayahnya merupakan perairan teritorial dengan luas 3,2 juta km2 sehingga memiliki banyak potensi yang dapat dimanfaatkan untuk kehidupan manusia baik dalam bidang transportasi, ekonomi, sosial budaya maupun bidang pendidikan. Pemanfaatan air laut dalam bidang ekonomi dapat berupa pemanfaatan hasil laut untuk kehidupan manusia serta pemanfaatan dalam bidang industri seperti Pembangkit Listrik Tenaga Uap (PLTU) yang memanfaatkan air laut sebagai sumber alami yang akan dijadikan sebagai air bersih untuk proses produksi steam (uap). Untuk keperluan tersebut, PLTU menyediakan unit proses desalinasi air laut. Namun, dalam proses desalinasi hanya 40% air laut dapat diubah menjadi air bersih, sementara sisanya sebanyak 60% yang disebut dengan brine water dikembalikan lagi ke laut sebagai limbah (Heraldy, 2012). Adapun komposisi kimia brine water yang dikembalikan ke laut hampir sama dengan komposisi air laut yaitu mengandung ion Cl-, Na+, SO42-, Mg2+, Ca2+, dan K+ (Anderson, 2003). Salah satu logam alkali tanah yang terkandung dalam brine water
yang memiliki potensi tinggi untuk dimanfaatkan sebagai komponen penyusun
hydrotalcite-like adalah ion magnesium.
Hydrotalcite merupakan salah satu mineral anionik yang menarik dan prospektif karena dapat disintesis dengan mudah serta dapat digunakan dalam berbagai aplikasi seperti sebagai eksipien farmasi, adsorben, katalis atau precursor
katalis (Tong et al., 2003; Heraldy, 2011). Hydrotalcite dalam bentuk naturalnya adalah suatu hidroksikarbonat dari magnesium dan aluminium dengan rumusan [Mg6Al2(OH)16]2+CO32-.4H2O. Semua kelompok senyawa yang hampir sama dengan
hydrotalcite baik yang natural maupun sintetis disebut hydrotalcite-like. Hydrotalcite
atau hydrotalcite–like termasuk jenis lempung anionik yang dikenal pula sebagai
layered double hydroxides, dengan rumus umum : [M2+1-xM3+x(OH)2]x+[An-x/n].mH2O
di mana M2+ = kation divalen ( Mg, Cu, Ni, Co, Zn, Fe, Mn, Cd, Ca) ; dan M3+= kation trivalen (Al, Ga, Co, Fe, Mn, Cr,V, Ti, In). Sementara An- merupakan anion
perpustakaan.uns.ac.id digilib.uns.ac.id
commit to user
2
yang mengisi interlayer (OH−, Cl−, NO3−, CO32−, SO42−) akibat adanya muatan positif pada permukaan hydrotalcite. Muatan positif pada permukaan ini ditimbulkan oleh adanya substitusi anion divalen oleh anion trivalen (Hickey et al., 2000).
Kameda et al. (2000; 2002) telah mensintesis Mg-Al hydrotalcite dari air laut tiruan serta Heraldy (2011) dan Setyowati (2011) telah mensintesis Mg-Al
hydrotalcite-like dari bahan dasar brine water dengan cara menghilangkan keberadaan ion kalsium karena beranggapan adanya ion kalsium dalam air laut tiruan maupun brine water dianggap merupakan pengotor yang mampu menghambat terbentuknya kristal hydrotalcite. Disisi lain Gao et al. (2010) telah melakukan sintesis hydrotalcite dengan mengkombinasikan tiga senyawa murni sebagai komponen penyusun hydrotalcite yaitu dengan mengkombinasikan senyawa Ca(NO3)2.4H2O, Mg(NO3)2.6H2O, dan Al(NO3)3.9H2O menjadi Ca-Mg-Al/hydrotalcite.
Dalam penelitiannya selain membuat Ca-Mg-Al/hydrotalcite, Gao juga membuat senyawa Mg-Al/hydrotalcite dan Ca-Al/hydrotalcite. Setelah itu, untuk pembuatan katalis, Gao et al. (2010) menambahkan senyawa Kalium Fluorida (KF) ke dalam hydrotalcite yang dihasilkan. Dari hasil karakterisasi katalis tersebut, menunjukkan bahwa terjadi peningkatan kristalinitas dan hasil uji katalis. Pada uji katalis, KF/Ca-Mg-Al hydrotalcite memiliki hasil konversi biodiesel yang lebih banyak bila dibandingkan dengan konvesri biodiesel menggunakan katalis KF/Mg-Al
hydrotalcite maupun KF/Ca-Al hydrotalcite. Hasil konversi biodiesel yang diperoleh adalah mendekati 100 %. Hal tersebut dikarena KF/Ca-Mg-Al hydrotalcite memiliki situs aktif yang dimiliki oleh KF/Mg-Al hydrotalcite dan KF/Ca-Al hydroatlcite. Situs aktif tersebut antara lain KMgF3, KCaF3, CaAlF5 dan KCaCO3F.
Berdasarkan penelitian Gao et al. (2010) yang telah mensintesis KF/Ca-Mg-Al hydrotalcite dengan bahan dasar senyawa murni tersebut, serta belum ada penelitian tentang sintesis hydrotalcite-like dari brine water tanpa penghilangan ion Ca2+, maka diperlukan kajian lanjut sintesis hydrotalcite-like dari brine water dengan cara tetap mempertahankan kandungan ion kalsium dalam brine water serta penambahan zat aktif KF. Dilakukannya penambahan KF ke dalam Mg-Al
hydrotalcite-like dalam penelitian ini, dimaksudkan untuk mengetahui kemungkinan perubahan karakteristik dari KF/hydrotalcite-like. Kajian awal yang akan dilakukan
perpustakaan.uns.ac.id digilib.uns.ac.id
commit to user
3
difokuskan pada karakter fisik hydrotalcite-like dan KF/hydrotalcite-like. Dengan demikian akan dapat dilihat sifat kristalinitas, luas permukaan, jari-jari pori serta analisis termal antara hydrotalcite-like serta KF/hydrotalcite-like yang disintesis dari
brine water tanpa penghilangan ion Ca2+.
B.Perumusan Masalah 1. Identifikasi Masalah
Salah satu logam alkali tanah yang terkandung dalam brine water yang memiliki potensi tinggi sebagai komponen penyusun hydrotalcite-like adalah ion magnesium. Pada umumnya Mg-Al/hydrotalcite tersusun atas kation divalent (Mg2+) dan trivalent (Al3+) dengan interlayer CO32-. Ion kalsium merupakan ion dominan yang memiliki pengaruh besar sebagai untuk menghambat terbentuknya kristal Mg/Al
hydrotalcite sehingga dalam sintesis Mg/Al hydrotalcite perlu dilakukan proses pengendapan ion Ca2+ dalam brine water tiruan (Kameda et al., 2000). Oleh karena itu, sifat kimia Ca2+ dan Mg2+ hampir sama diduga memberikan pengaruh yang hampir sama pula terhadap proses terbentuknya kristal hydrotalcite-like. Sehingga agar diperoleh fasa Mg/Al hydrotalcite yang optimum diperlukan penghilangan ion Ca2+. Namun, preparasi larutan awal untuk penghilangan ion Ca2+ memerlukan waktu yang relatif lama sehingga langkah tersebut dirasa kurang efisien. Disisi lain, Gao et al. (2010) telah mengkombinasikan tiga senyawa murni untuk mensintesis Ca-Mg-Al
hydrotalcite. Berdasarkan penelitian Gao et al. (2010) tersebut, dapat dikatakan bahwa kalsium juga berpotensi dalam penyusunan fase hydrotalcite sehingga ion kalsium yang terkandung di dalam brine water dan juga dikenal sebagai pengotor dapat digunakan sebagai bahan dasar pembuatan fase hydrotalcite-like.
Upaya peningkatkan kristalinitas dan aktifitas katalis suatu hydrotalcite dapat dilakukan dengan penambahan zat aktif seperti kalium fluorida (KF) (Setyowati, 2011). Peningkatan rasio KF akan memperbesar kristalinitas dan aktifitas katalis. Akan tetapi ketika rasio KF mencapai ambang batas distribusi monolayer maka kristalinitas akan menurun seiring dengan kenaikan rasio KF sebab ketika rasio KF lebih besar dari ambang batas maka akan menutupi sisi aktif yang mengakibatkan menurunnya kristalinitas. Selain itu penambahan KF akan merusak struktur
perpustakaan.uns.ac.id digilib.uns.ac.id
commit to user
4
Berdasarkan penelitian sebelumnya (Gao et al., 2010) kondisi optimum dicapai dengan perbandingan berat KF/berat Mg-Al hydrotalcite-like adalah 100 %.
2. Batasan Masalah
Berdasarkan identifikasi masalah tersebut, maka dibuat batasan masalah sebagai berikut:
a. Sintesis Mg-Al hydrotalcite-like dilakukan dengan tanpa penghilangan kandungan ion Ca2+ yang terdapat dalam brine water.
b. Untuk meningkatkan kristalinitas hydrotalcite-like dilakukan penambahan zat aktif KF ke dalam hydrotalcite-like dengan rasio berat KF/berat hydrotalcite-like adalah 100% (1:1).
3. Rumusan Masalah
Berdasarkan identifikasi masalah dan batasan masalah di atas, maka dibuat rumusan masalah sebagai berikut:
a. Apakah senyawa Mg-Al hydrotalcite-like dari brine water dapat disintesis tanpa penghilangan ion Ca2+ yang terkandung di dalam brine water ?
b. Bagaimanakah karakteristik kristalinitas, luas permukaan dan jari-jari pori KF/Mg-Al hydrotalcite-like hasil sintesis?
C.Tujuan Penelitian Tujuan dari penelitian ini adalah sebagai berikut:
1. Membuat senyawa Mg-Al hydrotalcite-like dari bahan dasar brine water dengan tanpa penghilangan ion Ca2+ yang terkandung di dalam brine water.
2. Mengetahui karakteristik kristalinitas, luas permukaan, dan jari-jari pori KF/Mg-Al hydrotalcite-like hasil sintesis.
D.Manfaat Penelitian Manfaat penelitian ini adalah sebagai berikut:
1. Memberi informasi tentang alternatif pemanfaatan brine water sebagai bahan dasar sintesis Mg-Al hydrotalcite-like tanpa penghilangan ion kalsium yang terkandung di dalamnya.
2. Memberi informasi tentang karakteristik kristalinitas, luas permukaan, jari-jari pori dan analisis termal KF/ Mg-Al hydrotalcite-like hasil sintesis dari brine water
perpustakaan.uns.ac.id digilib.uns.ac.id commit to user 6 BAB II LANDASAN TEORI A.Tinjauan Pustaka
1. Komposisi Dan Pengolahan Air Laut
a. Komposisi Kimia Air Laut
Pada dasarnya komposisi air laut disetiap wilayah didunia adalah hampir selalu konstan. Dalam 1000 gram air laut, terkandung 965 gram (96,5 %) air yang merupakan komponen terbesar penyusun air laut dan 35 gram (3,5 %) merupakan komponen garam-garam yang terlarut (salinitas). Terdapat garam-garaman utama yang berpengaruh terhadap salinitas air laut yaitu klorida (55 %), natrium (31 %), sulfat (8 %), magnesium (4 %), kalsium (1 %) dan sisanya terdiri dari bikarbonat, bromide, asam borak, stronsium dan florida (Anderson, 2003).
Berikut merupakan perbandingan komposisi kimia antara air laut dengan
brine water yang tercantum pada Tabel 1 di bawah ini :
Tabel 1. Komposisi kimia air laut dan brine water (Heraldy et al., 2011)
Ion Komposisi Kimia (mg L
-1
)
Air Laut Brine Water
Kalium (K+) 396 661 Natrium (Na+) 16.200 27.054 Kalsium (Ca2+) 1.205 2.012 Magnesium (Mg2+) 5.395 9.010 Klorida (Cl-) 31.800 53.106 Sulfat (SO42-) 2.600 4.342
b. Proses Pengolahan Air Laut (Desalinasi)
Proses desalinasi air laut adalah proses pemisahan yang digunakan untuk mengurangi kandungan garam terlarut dari air laut hingga level tertentu sehingga dapat digunakan sebagai air. Proses desalinasi melibatkan tiga aliran cairan, yaitu umpan berupa air garam misalnya air laut, produk bersalinitas rendah, dan konsentrat bersalinitas tinggi. Produk proses desalinasi umumnya merupakan air dengan kandungan garam terlarut kurang dari 500gram/L, yang digunakan untuk keperluan domestik, industri, dan pertanian. Hasil sampingan dari proses desalinasi adalah
brine. Brine adalah larutan garam berkonsentrasi tinggi (lebih dari 35000 mg/L garam terlarut).
perpustakaan.uns.ac.id digilib.uns.ac.id
commit to user
7
Distilasi adalah metode desalinasi yang paling lama dan paling umum digunakan yang merupakan metode pemisahan dengan cara memanaskan air laut untuk menghasilkan uap air, yang selanjutnya dikondensasi untuk menghasilkan air bersih. Umumnya proses distilasi menggunakan prinsip mengurangi tekanan uap dari air agar pendidihan dapat terjadi pada suhu yang lebih rendah, tanpa menggunakan panas tambahan. Metode lain desalinasi adalah dengan menggunakan membran. Terdapat dua tipe membran yang dapat digunakan untuk proses desalinasi, yaitu
reverse osmosis (RO) dan electrodialysis (ED). Pada proses desalinasi menggunakan membran RO, air pada larutan garam dipisahkan dari garam terlarutnya dengan mengalirkannya melalui membran water-permeabel. Permeate dapat mengalir melalui membran akibat adanya perbedaan tekanan yang diciptakan antara umpan bertekanan dan produk, yang memiliki tekanan dekat dengan tekanan atmosfer. Sisa umpan selanjutnya akan terus mengalir melalui sisi reaktor bertekanan sebagai brine. Proses ini tidak melalui tahap pemanasan ataupun perubahan fasa. Kebutuhan energi utama adalah untuk memberi tekanan pada air umpan. Desalinasi air payau membutuhkan tekanan operasi berkisar antara 250 hingga 400 psi, sedangkan desalinasi air laut memiliki kisaran tekanan operasi antara 800 hingga 1000 psi. Sistem RO terdiri dari 4 proses utama, yaitu (1) pretreatment, (2) pressurization, (3) membrane separation, (4) post teatment stabilization. Bila unit desalinasi menggunakan Reverse Osmose
(RO) membrane, hanya 40% air laut dapat diubah menjadi air bersih, sementara sisanya sebanyak 60% yang disebut brine water dikembalikan lagi ke laut sebagai limbah. Padahal, brine water tersebut mengandung logam alkali dan alkali tanah dalam konsentrasi yang tinggi (Heraldy, 2012).
2. Hydrotalcite
a. Struktur hydrotalcite
Hydrotalcite merupakan salah satu jenis material anorganik yang memiliki portensi dalam berbagai aplikasi industri. Hydrotalcite termasuk kedalam jenis lempung anionik yang dikenal pula sebagai layered double hydroxides (LDH) yang terdiri dari lapisan bermuatan positif dengan anion penyeimbang dan molekul air pada daerah interlayernya (Rajamanthi et al., 2001) yang memiliki struktur mirip dengan brucite Mg(OH)2. Senyawa tersebut terdiri atas lapisan berbentuk heksagonal dengan sisi oktahedral yang 100 % diisi oleh kation magnesium untuk setiap lapis
perpustakaan.uns.ac.id digilib.uns.ac.id
commit to user
8
hidroksida. Lapisan struktur dibentuk dari perulangan unit OH-Mg-OH-OH-Mg-OH-OH-Mg-OH dengan interaksi OH-OH merupakan interaksi Van der Waals. Jika kation dengan muatan tinggi tetapi memiliki ukuran jari-jari yang kecil mengganti kation Mg2+ maka lapisan mirip brucite tersebut akan memiliki muatan positif. Kelebihan muatan ini diseimbangkan dengan penenpatan anion pada lapisan yang tidak diisi oleh atom logam bersama dengan air. Pada senyawa hydrotalcite di alam, untuk setiap satu set yang terdiri dari delapan kation Mg2+, dua diantaranya digantikan oleh kation Al3+. Penggantian ini menyebabkan kelebihan muatan positif pada lapisan hidroksida logam. Daerah antarlapisan hidroksida logam yang satu dengan yang lain akan dipisahkan oleh suatu interlayer yang merupakan gabungan antara anion dengan empat molekul H2O yang terikat lemah pada sisi muatan positif yang berlebih (Arrhenius, 2003).
Hydrotalcite terdiri dari tumpukan lapisan-lapisan hidroksida dari magnesium dan aluminium yang bermuatan positif sehingga membutuhkan anion di antara lapisan tersebut (anion interlayer) untuk menyeimbangkan muatannya (Orthman et al, 2000). Kelompok senyawa yang hampir sama dengan hydrotalcite baik yang natural maupun sintesis disebut sebagai hydrotalcite-like. Pada umumnya
hydrotalcite-like tersusun atas kation logam divalent (M2+), kation logam trivalent
(M3+), dan anion penyeimbang (An-) yang memiliki rumus umum sebagai berikut: [M2+1-xM3+x(OH)2]x+[An-x/n].mH2O
Di mana M2+ dapat berupa kation logam divalen (bervalensi dua), seperti Mg2+, Fe2+, Ni2+, Cu2+, Co2+, Mn2+, Zn2+ atau Cd2+ sedangkan M3+ adalah kation logam trivalen (bervalensi tiga), seperti Al3+, Cr3+, Ga3+, atau Fe3+ dan anion penyeimbang An-dapat berupa CO32-, SO42-, Cl-, NO3-. Sedangkan x sebagai molar rasio yang berkisar antara 0,10 ≤ ≤ 0,33, m sebagai jumlah molekul air pada
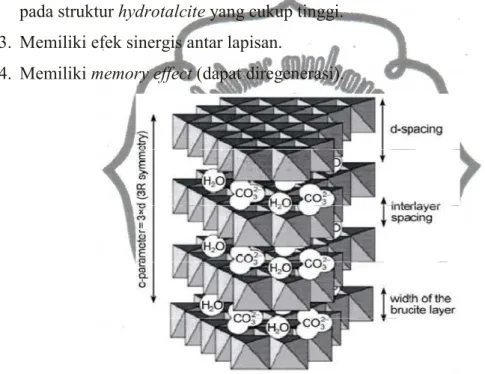
interlayernya. Kestabilan LDH atau hydrotalcite-like dipengaruhi oleh besar kecilnya ukuran jari-jari kation penyusunnya sehingga struktur LDH menjadi tidak stabil apabila jari jari kation M2+ < 0,06 nm. Struktur LDH ditunjukkan oleh Gambar 1. Menurut Cavani et al. (1991) salah satu syarat dari sintesis hydrotalcite adalah ukuran jari-jari kation logam yang digunakan tidak jauh berbeda dari kation logam Mg2+. Struktur hydrotalcite ditunjukkan pada Gambar 2.
perpustakaan.uns.ac.id digilib.uns.ac.id
commit to user
9
Senyawa hydrotalcite telah banyak dikembangkan karena memiliki potensi yang baik sebagai adsorben (Wright, 2002), penukar ion (Miyata, 1983) dan sebagai katalis (Kishore and Kannan, 2002; 2004). Wright (2002) menyebutkan bahwa
hydrotalcite memiliki sejumlah sifat yang membuatnya berpotensi seperti tersebut di atas, diantaranya adalah:
1. Luas permukaan yang cukup besar (100-300 m2/gram).
2. Padatan pendukung yang dapat disisipi oleh logam katalis dengan dispersi logam pada struktur hydrotalcite yang cukup tinggi.
3. Memiliki efek sinergis antar lapisan.
4. Memiliki memory effect (dapat diregenerasi).
Gambar 1 . Struktur lapisan LDH (Raki et al., 2004)
Gambar 2. Struktur Lapisan Hydrotalcite
b. Sintesis Hydrotalcite
Senyawa hydrotalcite merupakan mineral yang menarik karena dapat disintesis dengan mudah serta menghasilkan material berguna dalam berbagai aplikasi (Tong et al., 2003). Oleh karena itu, beberapa peneliti telah membuat dan
perpustakaan.uns.ac.id digilib.uns.ac.id
commit to user
10
mengembangkan senyawa hydrotalcite like berbahan dasar magnesium dengan berbagai kondisi sintesis baik dari senyawa murni maupun bahan alam yaitu:
1. Sintesis Hydrotalcite Menggunakan Bahan Senyawa Murni
Gao et al. (2010) telah melakukan sintesis hydrotalcite menggunakan bahan dasar senyawa murni berupa campuran senyawa Ca(NO3)2.4H2O, Mg(NO3)2.6H2O, dan Al(NO3)3.9H2O menjadi Ca-Mg-Al hydrotalcite dengan kondisi sintesis pada pH 10 selama 1 jam pada suhu reaksi 65 °C. Sementara itu, Ahmad (2011) juga membuat Mg/Al hydrotalcite-like dari bahan senyawa murni yaitu dari campuran magnesium klorida dan aluminium klorida ditambahkan larutan natrium karbonat dan disintesis pada pH 10 temperatur 70 °C selama 1 jam. Heraldy et. al. (2006) juga mensintesis Mg/Al hydrotalcite-like dengan nisbah mol Mg/Al 2,0 ; 2,5 dan 3,0 dari campuran magnesium klorida dan aluminium klorida melalui metode kopresipitasi secara langsung.
2. Sintesis Hydrotalcite Menggunakan Bahan Dari Alam
Kameda dan kelompok penelitiannya yang telah membuat hydrotalcite-like
dari magnesium yang berasal dari air laut tiruan (artificial seawater) yang mengandung natrium klorida (NaCl), natrium sulfat (Na2SO4), magnesium klorida (MgCl2) dan kalsium klorida (CaCl2). Sintesis ini diawali dengan membuat larutan awal (starting solution) dari air laut tiruan dengan cara menghilangkan ion kalsium terlebih dahulu. Oleh Kameda et. al. (2000), penghilangan ion kalsium dilakukan dengan menggunakan larutan campuran antara NaHCO3 0,2 M dan Na2CO3 0,1 M dengan pengadukan selama satu jam pada suhu 95 °C. Setelah itu, filtrat yang diperoleh ditambahkan sumber aluminium (AlCl3) dengan nisbah mol awal Mg/Al bervariasi dari 2 sampai 3,7. Proses berikutnya adalah penambahan Na2CO3 1,0 M hingga diperoleh pH 10 dan kemudian larutan ini diaduk dan dipanaskan selama 1 jam pada suhu 60 °C.
Dari bahan alam seperti bittern, Oza dan sesama peneliti dalam kelompoknya telah membuat Mg/Al hydrotalcite-like dengan cara mengencerkan bittern terlebih dahulu, lalu diproses sedemikian rupa sampai diperoleh ion magnesium dengan konsentrasi antara 0,53–0,90 molar. Kemudian sintesis dilakukan dalam kondisi reaksi pada perbandingan mol antara ion aluminium dengan mol total ion magnesium
perpustakaan.uns.ac.id digilib.uns.ac.id
commit to user
11
dan aluminium 0,28 - 0,33; pH antara 8,5 - 10,5 dan temperatur antara 60 – 70 °C (Oza et. al., 2006).
Heraldy (2011) telah memanfaatkan ion magnesium yang terdapat dalam
brine water sebagai bahan dasar pembuatan hydrotalcite-like dengan penambahan AlCl3.6H2O pada rasio mol Mg/Al 2,0 yang kemudian disintesis dengan metode kopresipitasi pada pH 10,5 selama 1 jam dengan suhu reaksi 70 °C.
3. Kalium Fluorida(KF)
Kalium Fluorida merupakan golongan logam alkali tanah yang tersusun atas logam alkali dan halida. Kalium merupakan golongan IA yang bersifat sangat reaktif, karena memiliki elektropositif yang tinggi dan merupakan senyawa ionik yang stabil bila membentuk KF bila berikatan dengan F golongan VII A yang bersifat elektronegatif sehingga disebut sebagai logam alkali halida. Sifat fisik dari kalium fluorida berupa serbuk putih dan sangat higroskopis. Selain itu juga bersifat korosif.
Dalam penelitian Gao et al.(2008 dan 2010) KF dikombinasikan dengan Mg-Al hydrotalcite-like dan Ca-Mg-Al hydrotalcite-like yang digunakan untuk katalis transesterifikasi biodiesel dari minyak sawit dengan methanol. Penambahan KF dipercaya mampu meningkatkan aktivitas dari gugus aktif penyusun hydrotalcite-like, kristalinitas serta efek sinergis sehingga diperoleh konversi metil ester yang tinggi. Semakin banyak konsentrasi KF yang dicampur maka kemampuan meningkatkan aktifitas gugus aktif juga semakin besar. Akan tetapi apabila penambahan berlebih maka akan menyebabkan penurunan aktifitas gugus aktifnya. Teng et al.(2009) menggunakan KF/Al2O3 untuk katalis transesterifikasi minyak kedelai menjadi biodiesel. Xu et al. (2011) telah melakukan penambahan KF kedalam katalis heterogen Mg-Al HTlc, MO, dan M2+(M3+)O dalam sintesis biodiesel. Dalam penelitiannya penambahan KF untuk meningkatkan aktivitas katalis tidak tergantung pada jenis campuran oksida ataupun oksida tunggal yang digunakan. Selain itu luas permukaan katalis juga tidak berpengaruh langsung terhadap peningkatan kemampuan aktivitas katalis. Hal tersebut terlihat pada hasil konversi biodiesel pada penelitiannya dimana luas permukaan katalis antara 190 m2/g dan 8 m2/g memiliki perbedaan hasil konversi yang <10 %. Sehingga meningkatnya aktivitas katalis dengan penambahan KF dapat terjadi karena sebagian besar situs aktif telah berada dipermukaan yaitu KF, KOH, KMxFy, dan situs aktif pada komponen itu sendiri
perpustakaan.uns.ac.id digilib.uns.ac.id
commit to user
12
sehingga mengakibatkan luas permukaan maupun pori-pori dari komponen tersebut menjadi berkurang.
4. KarakterisasiHydrotalcite-Like
a. Atomic Absorption Spectroscopy (AAS)
Atomic Absorption Spectroscopy (AAS) merupakan salah satu instrument
yang digunakan untuk analisis konsentrasi unsur-unsur logam dan semi logam dalam jumlah renik (trace) dengan hasil analisa berupa kadar total unsur logam atau semi logam yang terkandung dalam sampel. Untuk mengetahui kandungan Mg2+ dan Ca2+ dalam sampel brine water yang akan digunakan, sebelum eksperimen sampel brine water dianalisis terlebih dahulu dengan metode Spektrofotometer Serapan Atom (SSA). Dengan diketahuinya konsentrasi Mg2+ dalam brine water, maka dapat dihitung jumlah Al3+ yang harus ditambahkan sesuai dengan rasio mol Mg/Al yang dibutuhkan. Atomic Absorption Spectroscopy (AAS) merupakan salah satu instrument
yang digunakan untuk analisis konsentrasi unsur-unsur logam dan semi logam dalam jumlah renik (trace) dengan hasil analisa berupa kadar total unsur logam atau semi logam yang terkandung dalam sampel. Hal ini didasarkan pada kemampuan adsorpsi logam pada keadaan dasar terhadap sinar pada panjang gelombang spesifik. Sehingga, konsentrasi logam pada larutan brine water dapat dianalisis menggunakan AAS. Sehingga, dapat digunakan dalam penentuan rasio mol ion divalen dan ion
divalent pada penyusun Layered Double Hydroxides (LDH).
Roto et al. (2009) menyebutkan bahwa konsentrasi Fe2+ pada filtrat Zn-Al-Fe(CN)6 ditentukan menggunakan AAS sehingga diketahui kapasitas anion pengganti. Larutan standar Fe2+ menggunakan 0,0189 g K4[Fe(CN)6] dilarutkan pada 100 mL air yang telah dideionisasi hingga diperoleh 25 mg/L Fe2+ yang kemudian digunakan sebagai larutan standar pada 1000 mg/L Fe(II)NO3. Disisi lain, Padmasri
et al.(2002) dalam penelitiannya mengungkapkan bahwa rasio komposisi Mg–Al
hydrotalcite yang dikalsinasi dapat tentukan menggunakan AAS. Dalam penelitiannya, perbandingan antara M2+: M3+ dalam hydrotalcite adalah 1,98. Selain itu, Thevenot et al. (1989) mengungkapkan bahwa dalam analisis kimia suatu A1, Zn, dan Na yang terkandung didalam sampel A1-rich Zn-A1hydrotalcite-like
perpustakaan.uns.ac.id digilib.uns.ac.id
commit to user
13
b. Fourier Transform Infrared Spectroscopy (FTIR)
Fourier Transform Infra Red (FTIR) digunakan untuk penentuan struktur senyawa organik biasanya antara 650-4.000 cm-1. Daerah di bawah frekuensi 650 cm -1
dinamakan infra merah jauh dan daerah di atas frekuensi 4.000 cm-1 dinamakan infra merah dekat. Jika suatu molekul menyerap sinar infra merah, maka di dalam molekul itu terjadi perubahan energi vibrasi dan perubahan tingkat energi rotasi. Syarat molekul dapat menyerap energi sinar infra merah adalah momen dwikutub harus tergetar (sebab dari vibrasi molekul) berinteraksi dengan vektor listrik tergetar dari berkas infra merah menyebabkan perubahan netto momen dwikutub dari gerakan vibrasi dan atau gerakan rotasi.
Johnson and Glasser (2003) telah melaporkan adanya puncak-puncak yang khas dari vibrasi gugus-gugus fungsi pada senyawa hydrotalcite. Puncak pada bilangan gelombang 3400 cm-1 menunjukkan vibrasi ulur -OH, 1400 cm-1 menunjukkan vibrasi ulur asimetris -CO3, 800 cm-1 menunjukkan deformasi luar bidang -CO3, sementara pada bilangan gelombang 600-400 cm-1 menunjukkan vibrasi ulur M-Al-O dan vibrasi ulur serta tekuk dari M-O dengan M adalah logam.
Hydrotalcite-like memiliki gugus fungsi penyusun yang khas pada bilangan gelombang tertentu seperti pada Tabel 2.
Tabel 2. Gugus-gugus fungsi Mg/Al hydrotalcite-like
Gugus Fungsi Bilangan Gelombang (cm-1)
Uluran OH dan M-O 3400-3500a,b
Tekukan OH 1650d
Uluran simetris O=C-O 1385a,c Uluran asimetris O=C-O 1500,5c
Tekukan O=C-O 650a
Uluran Mg-O dan Al-O 400-600a (2 puncak)
Uluran Ca-O 700e
Sumber aKannan (1995) dalam Johnson and Glasser (2003), bBhaumik, et al. (2004),
c
Di Cosimo, etal. (1998), dYang etal. (2007), eGupta et al. (2008)
Spektra IR pada senyawa LDH (Kang et al.,2005), dengan perbedaan rasio
molar antara Mg dan Al ditunjukkan pada Gambar 3. Plank et al. (2006) menyatakan
bahwa pada daerah bilangan 3600 cm-1 merupakan daerah serapan –OH dari lapisan
anorganik dan lapisan air. Untuk Ca-Al-NO3-LDH pada daerah serapan 1385cm-1
M-perpustakaan.uns.ac.id digilib.uns.ac.id
commit to user
14
O dan M-OH (M=Ca, Al) dalam struktur LDH berada pada daerah serapan 421, 530, dan 790 cm-1. Raki and J. J. Beaudoin (2008) dalam penelitiannya Controlled Release of Chemical Admixtures in Cement-Based Materials mengkombinasikan kalsium dan alumunium sebagai komponen penyusun hydrotalcite-like yang ditunjukkan dalam spektra FTIR pada Gambar 4.
Gambar 3. Spektra FTIR dari LDH dengan perbedaan rasio molar (A) spektra OH, (B) spektra serapan H2O (C) spektra serapan -CO32- dan (D) spektra serapan [Metal]-OH
stretching.(Kang et al.,2005).
Gambar 4. Spektra FTIR Ca-Al LDH Raki and Beaudoin (2008).
c. X-Ray Diffraction (XRD)
Analisis terhadap padatan hasil sintesis dapat ditentukan dengan menggunakan X-Ray Diffractometer (XRD). XRD digunakan untuk memperoleh informasi tentang struktur, komposisi dan tingkat kristalinitas dari suatu material. Analisis secara kualitatif bertujuan untuk mengidentifikasi senyawa utama dalam sampel yaitu dengan membandingkan harga d ( ) sampel yang diperoleh dengan harga d ( ) dari senyawa yang sudah diketahui. Referensi harga d ( ) dari senyawa
perpustakaan.uns.ac.id digilib.uns.ac.id
commit to user
15
yang sudah diketahui tersebut berasal dari data Joint Committee on Powder Diffraction Standars (JCPDS).
Kang et al.,2005 telah melakukan penelitian tentang Layered Double Hydroxide and its Anion Exchange Capacity dengan perbedaan rasio mol Mg/Al diketahui dengan semakin kecilnya molar rasio Mg/Al maka puncak d003 yang
dihasilkan memiliki intensitas yang semakin tinggi seperti pada Gambar 5.
Gambar 5. Difraktogram XRD LDH dengan perbedaan rasio mol (a) Mg/Al=2 (b) Mg/Al=2.5 (c) Mg/Al=3 (Kang et al. 2005)
Fayyazbakhsh et al. (2012) menyebutkan bahwa Ca-LDH memiliki kristalinitas yang lebih bagus dan ukuran partikel yang lebih besar serta parameter lapisan yang lebih tinggi bila dibandingkan dengan Mg-LDH. Perbedaan tersebut dapat dilihat pada Gambar 6. Sementara itu, Chang et al. (2011) menyebutkan bahwa Ca-Al CO3 LDH denagn rasio mol Ca/Al (1:1 dan 3:1) memiliki karakteristik fase
hydrotalcite-like dengan karakteristik puncak difraksi pada 2θ 11o dan 23o yang merupakan bidang dasar d003 dan d006. Puncak tersebut mengindikasikan bahwa
kristal yang terbentuk dengan struktur rombohedral. Difraktogram dapat dilihat pada Gambar 7.
perpustakaan.uns.ac.id digilib.uns.ac.id
commit to user
16
Gambar 7. XRD Ca-Al-CO3 LDH dengan perbedaan rasio mol Ca/Al (Chang et al., 2011)
Kristalinitas relatif suatu sampel dapat ditentukan dengan perbandingan kristalinitas pada sampel yang memiliki puncak difraksi tertinggi (003), kristalinitasnya dianggap 100% (Xie et al, 2003). Kristalinitas yang rendah ditandai dengan pengurangan beberapa cerminan hkl, pelebaran garis-garis puncak difraksi XRD dan penurunan intensitas (Lakraimi et al, 2000). Rendahnya kristalinitas dapat disebabkan karena efek mekanik dari pengadukan. Selain itu, XRD dapat digunakan untuk penerapan kuantitatif karena intensitas puncak difraksi yang diberikan pada campuran senyawa sebanding dengan fraksi material dalam campuran. Banyaknya puncak pengganggu pada 2θ (20 dan 30o) dapat diasumsikan sebagai amorf Al(OH)3 (Lakraimi et al, 2000). Persentase kandungan senyawa dalam sampel diketahui dengan membandingkan intensitas puncak difraksi karena intensitas tersebut sebanding dengan fraksi senyawa dalam sampel. Persentase kandungan senyawa dalam sampel dihitung dengan rumus: % = (/)
(/) 100%
Dengan (I/I1)s : jumlah intensitas relatif puncak senyawa dalam sampel dan (I/I1)t : jumlah intensitas relatif total sampel (Willard et al., 1988).
d. X-Ray Fluorescence (XRF)
X-Ray Flourescene (XRF) merupakan metode analisis kuantitatif
non-destruktif yang menganalisis kandungan logam dalam suatu batuan, sedimen, mineral dengan tingkat keakurasian yang tinggi dan presisi yang baik. Adapun analisa yang dapat dilakukan dengan XRF adalah analisa minyak dan bahan bakar, plastik, karet
perpustakaan.uns.ac.id digilib.uns.ac.id
commit to user
17
dan tekstil, produk farmasi, bahan makanan, kosmetik, pupuk, mineral, keramik, dan sebagainya.
Sebagai salah satu contoh analisis komponen penyusun hydrotalcite-like
dalam sampel random dengan anion penyeimbang nitrat/karbonat menggunakan XRF. Adapun komponen penyusun pada penelitian “ The influence of mixed anionic composition of Mg–Al hydrotalcites on the termal decomposition mechanism based on in situ study” dapat dilihat pada Tabel 3.
Tabel 3. Komponen penyusun hydrotalcite-like (Wegrzyn et al., 2010)
Sampel Formula Mg/Al molar ratio
AN93 N88 AN54
Mg0,697Al0,303(OH)2(NO3)0,280(CO3)0,011.0,520 H2O Mg0,657Al0,343(OH)2(NO3)0,302(CO3)0,028.0,889 H2O Mg0,6831Al0,317(OH)2(NO3)0,132(CO3)0,092.0,439 H2O
2,30 1,92 2,16
Selain itu, Carja et al.(2002) dalam penelitian penggantian Co dan Fe
hydrotalcite dengan magnesium sebagai prekursor katalis pada sintesis metilamina tersaji pada Tabel 4.
Tabel 4. XRF komposisi sampel hydrotalcite (Carja et al., 2002) Sampel Mg:Me:Al (from XRF) MgAlLDH CuLDH FeLDH 2,96:0,1 1,87:1,13:1 1,9:1,1:1
e. Specific Surface Area And Porosity dengan SAA
Surface Area Analyzer (SAA) merupakan salah satu instrument yang digunakan untuk menentukan luas permukaan suatu pertikel dan penentuan distribusi ukuran pori partikel. Luas permukaan dapat diukur dengan beberapa metode,
diantaranya metode Brunauer-Emmet-Teller (BET) dan Metilen Biru. Pada teknik
Metilen biru adsorpsi membentuk lapisan monolayer dan merupakan chemisorption.
Adapun dalam teknik BET, adsorpsi terjadi secara fisika dan lapisan multilayer dapat
terbentuk. Metode BET ini biasa digunakan untuk menentukan luas permukaan. Luas permukaan spesifik dari adsorben berongga tergantung pada ukuran partikel penyusunnya. Adsorben mungkin memiliki porositas yang berbeda dalam ukuran maupun bentuknya.
Fetter et al (2000) menyebutkan bahwa surface area dari hydrotalcite dengan
perpustakaan.uns.ac.id digilib.uns.ac.id
commit to user
18
surface area nitrated hydrotalcites dengan rasio mol Al/(Mg+Al) = 0.249 berkisar antara 5 sampai 15 m2/g. Sharma et al. (2007) menyebutkan bahwa peningkatan luas area hydrotalcite berbanding lurus dengan peningkatan mol Mg/Al dari 2,0 sampai 3,5 pada suhu 70oC selama 11 jam dalam keadaan termal dengan luas area dari 62 menjadi 73 m2/g. Wegrzyn et al (2010), menyatakan bahwa luas area hydrotalcite
dengan rasio mol Mg/Al (2,3) adalah 200 m2/g. Sedangkan Chang et al. (2011) menyebutkan bahwa peningkatan luas permukaan Ca/Al LDH sebanding dengan semakin bertambahnya rasio mol Ca/Al. Terlihat pada hasil penelitiannya Ca/Al LDH yang telah dikalsinasi pada suhu 600 oC dengan rasio mol Ca/Al (1:1 dan 3:1) menggunakan metode BET memiliki luas permukaan sebesar 5,15 dan 9,14 m2/g. f. Thermogravimetric/Differential Termal Analysis (TG/DTA)
Analisis termal didefinisikan sebagai pengukuran sifat fisika dan kimia dari material sebagai fungsi suhu. Tipe analisis termal ini meliputi entalpi, kapasitas panas, massa dan koefisien ekspansi termal. Thermogravimetry Termal Analysis
(TGA) merupakan metode analisa penentuan perubahan berat suatu bahan dengan perubahan suhu saat pemanasan maupun pendinginan dengan kecepatan tertentu.
Differential Termal Analysis (DTA) mengukur perbedaan suhu (T) antara sampel dan materi pembanding inert sebagai fungsi suhu, apabila suhu keduanya dinaikkan dengan kecepatan yang sama dan konstan. Perubahan keadaan sistem karena naiknya suhu ini merupakan konsekuensi dari proses yang terjadi pada sampel yaitu eksoterm dan endoterm, yang kemudian ditampilkan dalam bentuk termogram differential.
Lakraimi et al. (2000) dalam penelitiannya melaporkan adanya puncak-puncak endoterm dari kurva DTA yang menunjukkan hilangnya molekul H2O. Puncak pada 85 oC dan 40 oC menunjukkan hilangnya molekul air yang teradsorp dan molekul air pada interlayer. Pada 200 oC terjadi dehidroksilasi senyawa serupa
brucite, hilangnya CO2 dari anion interlayer CO3. Xie et al. (2003) melaporkan bahwa kurva endotermik 116 oC menunjukkan hilangnya air pada daerah interlayer
dan kurva endotermik pada 238 oC menunjukkan hilangnya gugus OH. Zulaikha (2005) melaporkan bahwa puncak melebar pada suhu 92,56 oC dan 136,94 oC diasumsikan sebagai pelepasan air pada daerah interlayer serta pada suhu 176,74 oC dan 228,86 oC mengindikasikan adanya pelepasan air dari lapisan serupa brucite
perpustakaan.uns.ac.id digilib.uns.ac.id
commit to user
19
interlayer air pada suhu 70-190 °C, sedangkan antara 190-280 °C suhu, OH -berikatan dengan Al3+ yang mulai lepas pada suhu 190 °C dan terlepas seluruhnya pada suhu 280 °C, suhu antara 280 - 405 °C, OH- berikatan dengan Mg2+ yang mulai lepas pada suhu 280 °C dan terlepas seluruhnya pada suhu 405 °C, degradasi dari struktur layered double hydroxide juga diamati pada daerah yang sama dan pada suhu 405 - 508 °C, CO32- mulai lepas dan terlepas seluruhnya pada suhu 508 °C. Pada suhu ini material menjadi suatu campuran larutan padatan oksida amorf metastabil. Salah satu contoh bentuk termogram TG/DTA Mg-Al hydrotalcite dan Ca-Al LDH seperti ditunjukkan oleh Gambar 8 dan Gambar 9.
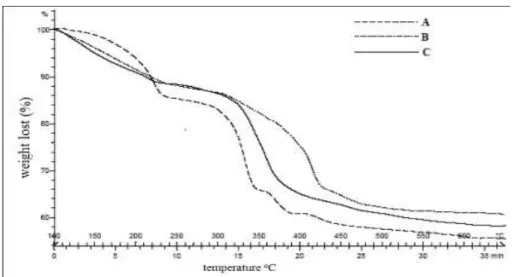
Pada Gambar 8 terlihat bahwa tiga tahapan pengutangan massa terjadi pada analisis termal suhu 70 oC. Terjadi pengurangan massa sebesar 15 % pada kisaran suhu 220 oC yang mengindikasikan terjadinya pelepasan molekul H2O dari pori-pori
hydrotalcite. Dengan pengurangan massa yang kedua sebesar 38 % pada rentang suhu 330-380 oC yang mengindikasikan terjadinya proses pelepasan gugus OH- dari
interlayer hydrotalcite yang berikatan dengan Mg2+ [Mg-(OH)-Mg] dan [Al-(OH)-Mg. Tahap pengurangan massa yang ketiga terjadi dekarbonasi ion CO32- pada
interlayer dengan rentang suhu 400-500 oC sebesar 44 %. Setelah terjadi pelepasan ion CO32- dari interlayer maka material menjadi bersifat amorf metastabil padatan logam oksida. Sedangkan pengurangan massa terjadi pada perlakuan termal suhu 110 dan 140 oC terjadi dua tahapan.
Gambar 8. TGA Mg/Al hydrotalcite dengan rasio mol Mg/Al (2,0),variasi suhu pemanasan selama 11 jam (A) 70 °C (B) 110 °C dan (C) 140 °C
perpustakaan.uns.ac.id digilib.uns.ac.id
commit to user
20
Gambar 9. TG/DTA Ca/Al LDH (Raki et al., 2004)
Pada Gambar 10. menunjukkan bahwa KF/Mg(Al)O-dy mengalami pengurangan massa ketika dilakukan pemanasan hingga suhu 1000 °C. Pada suhu 211 °
C merupakan pengurangan massa air dan terjadi dehidroksilasi sehingga kehilangan CO2 (Xu et al., 2011).
Gambar 10. TG/DTA KF/Mg(Al)O-dy (Xu et al., 2011)
B.Kerangka Pemikiran
Hydrotalcite dapat disintesis apabila terdapat ion divalent dan ion trivalent
dalam suatu camputan larutan. Brine water mengandung ion magnesium dalam konsentrasi tinggi sehingga mengindikasikan dapat digunakan sebagai bahan dasar pembuatan hydrotalcite-like dengan penambahan aluminium hidroksida sebagai komponen penyusun hydrotalcite-like dan natrium karbonat sebagai ion penyeimbang
perpustakaan.uns.ac.id digilib.uns.ac.id
commit to user
21
pada interlayernya melalui metode kopresipitasi,yaitu suatu metode sintesis yang sering digunakan karena merupakan metode termudah dan dapat dilakukan pencegahan kontaminasi dari karbondioksida pada daerah antar lapisnya pada sintesis yang dilakukan. Selain itu keberadaan CO32- dapat mempercepat proses pembentukan kristal hydrotalcite dan dapat langsung terikat kuat dengan lapisan antar lapisnya. Beberapa peneliti terdahulu menyatakan bahwa kalsium pada umumnya merupakan pengotor dalam pembentukan Mg-Al hydrotalcite-like. Namun belakangan ini, beberapa peneliti telah memanfaatkan kalsium sebagai komponen penyusun
hydrotalcite-like karena termasuk kation divalen, memiliki aktivitas yang tinggi dan memiliki jari-jari ion yang besar.
Pada dasarnya setiap senyawa padat memiliki karakteristik yang berbeda-beda sehingga dari karakteristik atau sifat khusus tersebut dapat diketahui termasuk golongan apa senyawa yang dihasilkan. Sebagai contoh, senyawa Mg/Al
hydrotalcite-like yang dianalisis menggunakan XRD diketahui 3 puncak khusus yaitu
d003, d006 dan d009. Dari tiga puncak tersebut, dapat pula digunakan untuk penentuan
kristalinitas Mg/Al hydrotalcite dengan adanya puncak d110 sebagai identifikasi lapisan interlayer. Kristalinitas dipengaruhi oleh beberapa faktor seperti banyak sedikitnya pengotor yang ikut mengendap. Dalam pembentukan Mg/Al hydrotalcite,
beberapa peneliti terdahulu menyebutkan bahwa kalsium merupakan pengotor sehingga kemungkinan kristalinitas Mg/Al hydrotalcite-like yang terbentuk rendah apabila terdapat ion kalsium di dalamnya. Hal ini dikarenakan adanya interaksi yang tidak maksimal antara magnesium dengan ion karbonat yang dikarenakan adanya ion kalsium yang memiliki sifat kimia yang relatif sama dengan magnesium sehingga probabilitas untuk mengendap adalah sama.
Penambahan suatu zat aktif KF ke dalam hydrotalcite-like dapat meningkatkan kristalinitas hydrotalcite-like serta mampu meningkatkan aktivitas
hydrotalcite-like sebagai suatu katalis. Hal tersebut dikarenakan adanya interaksi antara senyawa penyusun hydrotalcite dengan KF yang bersifat sangat reaktif. Selain itu, KF juga mampu menurunkan ukuran jari-jai pori sehingga menurunkan luas pernukaan hydrotalcite-like (Bernhardt et al., 2010).
perpustakaan.uns.ac.id digilib.uns.ac.id
commit to user
22
C.Hipotesis
1. Hydrotalcite-like dapat disintesis dari brine water dengan tanpa penghilangan ion Ca2+ yang terkandung di dalam brine water.
2. Penambahan zat aktif KF kedalam Mg/Al hydrotalcite-like dapat meningkatkan kristalinitas, luas permukaan dan jari-jari pori Mg-Al hydrotalcite-like.
perpustakaan.uns.ac.id digilib.uns.ac.id commit to user 23 BAB III METODOLOGI PENELITIAN A.Metode Penelitian
Penelitian ini dilakukan dengan metode eksperimental laboratorium. Penelitian yang dilakukan meliputi dua tahap yaitu tahap sintesis Mg/Al hydrotalcite-like yang dilakukan menggunakan metode kopresipitasi dari bahan dasar brine water dengan tanpa penghilangan ion Ca2+ dan sintesis KF/Mg-Al hydrotalcite-like yang kemudian dikarakterisasi menggunakan XRD, FTIR, TG/DTA, SAA, XRF.
B.Tempat dan Waktu Penelitian
Penelitian dilaksanakan di Laboratorium Pusat Kimia FMIPA UNS, Laboratorium Dasar Kimia FMIPA UNS, Laboratorium Kimia Analitik FMIPA UGM pada bulan April 2011 sampai Desember 2011.
C.Alat dan Bahan 1. Alat-alat
Alat yang digunakan dalam penelitian ini adalah sebagai berikut: a. Peralatan gelas dan alat-alat penunjang laboratorium
b. Atomic Absorption Spectroscopy (AAS) Shimadzu AA 630-12 c. X-ray Diffraction (XRD) Bruker D8 Advance
d. Fourier Transform Infra Red (FTIR) Shimadzu IRPrestige-21 e. Surface Area Analysis (SAA) Quantachrome Nova Win 1200
f. Thermogravimetric/Differential Thermal Analysis (TG/DTA) Linseis STA PT-1600
g. X-ray Flourescene (XRF) Bruker S2 Ranger 2. Bahan-bahan
Bahan yang digunakan dalam penelitian ini adalah sebagai berikut: a. Brine water ( sampel dari PLTU Tanjung Jati B, Jepara )
b. Aluminium Hydroxcide ( AlCl3.6H2O) p.a (Merck) c. Kalium Fluorida(KF) p.a (Merck)
perpustakaan.uns.ac.id digilib.uns.ac.id
commit to user
24
e. pH indikator f. Na2CO3 p.a (Merck)
g. Akuades (Laboratorium Dasar Kimia FMIPA UNS)
D.Prosedur Penelitian
1. Sintesis dan Karakterisasi Mg-Al hydrotalcite-like
Material yang digunakan adalah brine water yang berasal dari PLTU Tanjung Jati B, Jepara. Sintesis hydrotalcite-like dilakukan dengan menggunakan metode kopresipitasi. Sejumlah AlCl3.6H2O ditambahkan ke dalam larutan brine water dengan perbandingan mol awal antara magnesium yang terkandung di dalam brine water, aluminium, (2:1). Kemudian ditambahkan larutan Na2CO3 0,1 M kedalam 1550 mL larutan brine water hingga pH campuran 10 lalu direfluks pada suhu 65 oC selama satu jam.
Endapan yang diperoleh dicuci dengan akuades sampai bebas ion Cl-. Keberadaan ion Cl- diketahui dengan menguji filtrat pencucian dengan larutan AgNO3. Filtrat bebas ion Cl- bila saat ditetesi larutan AgNO3 tidak menghasilkan endapan putih. Endapan yang bebas ion Cl- disaring dengan centrifuge,4000 rpm selama 10 menit lalu dioven pada suhu 110 oC selama 24 jam. Padatan putih yang telah kering yang diperoleh merupakan hydrotalcite-like. Padatan hydrotalcite-like dihaluskan dan disaring dengan ayakan 150 mess kemudian dikarakterisasi menggunakan difraksi sinar-X (XRD) dan FT-IR, SAA, XRF, dan TG-DTA.
2. Preparasi KF/hydrotalcite-like dan Karakterisasi
Preparasi katalis dilakukan dengan cara hydrotalcite-like ditambah serbuk KF serat ditetesi akuades hingga menjadi pasta. Pasta hasil pencampuran kemudian dioven pada suhu 65 oC selama 24 jam atau sampai kering kemudian dihaluskan.
Serbuk yang diperoleh kemudian dikarakterisasi menggunakan FT-IR, XRD, SAA, XRF, dan TG/DTA.
E.Teknik Pengumpulan Data
Data kualitatif dan kuantitatif yang diperoleh dari hasil eksperiment hydrotalcite
dianalisa dengan AAS untk mengetahui kandungan Mg2+ dan Ca2+, difraksi sinar-x
(XRD) sehingga dapat diketahui struktur penyusun dan tingkat kristalinitas dari
perpustakaan.uns.ac.id digilib.uns.ac.id
commit to user
25
komposisi penyusun hydrotalcite dengan XRF, pengurangan massa dengan TG/DTA dan identifikasi gugus fungsi penyusun hydrotalcite menggunakan FT-IR.
F. TeknikAnalisis Data
1. Kandungan Mg2+ dan Ca2+ dalam brine water dapat dianalisis dengan AAS yang dapat dikonversi ke dalam satuan mol logam.
2. Data XRD menghasilkan difraktogram 2θ vs intensitas dari masing-masing kristal hydrotalcite-like. Dari 2θ dapat diperoleh besarnya jarak antara kisi kristal (d) sesuai dengan persamaan nλ = 2d sin θ yang kemudian dicocokkan dengan d
pada Joint Committee Powder on Diffraction Standart (JCPDS). Munculnya puncak-puncak dengan hkl dominan hydrotalcite-like (d003, d006, d009) pada difraktogram sampel yang sama dengan JCPDS menunjukkan bahwa sampel yang dianalisis sama dengan senyawa pada standart JCPDS. Dengan (I/I1)s : jumlah intensitas relatif puncak senyawa dalam sampel dan (I/I1)t : jumlah intensitas relatif total sampel (Willard et al., 1988) maka persentase relatif kandungan senyawa/kristalinitas dalam sampel dihitung dengan rumus:
% =
(I/I
1)
s(I/I
1)
t100%
3. Gugus-gugus fungsi yang ada di dalam hydrotalcite-like diketahui dengan membandingkan puncak-puncak spektra FTIR Mg-Al hydrotalcite-like dengan referensi. Berdasarkan strukturnya hydrotalcite-like memiliki gugus fungsi M-O yang terletak pada bilangan gelombang 400 - 600 cm-1, O-C=O dan karbonat pada bilangan gelombang 1385 dan 1500 cm-1 serta O-H pada bilangan gelombang 3400-3500 dan 1650 cm-1 dari lapisan hidroksida maupun interlayer. 4. Analisis termal DTA yang mendeteksi setiap perubahan termal terkait dengan
peristiwa atau reaksi kimia, baik yang berjalan secara eksotermik maupun endotermik. Dengan terjadinya pelepasan H2O dari pori hydrotalcite pada kisaran suhu 220 oC, pelepasan gugus –OH dari interlayer-nya yang berikatan dengan Mg2+[Mg-(OH)-Mg] dan [Al-(OH)-Al] pada suhu 330-380 oC. Terjadi proses dekarbonasi ion karbonat dari interlayer–nya pada suhu 400-500 oC. Sementara itu, TGA mendeteksi setiap perubahan massa yang terjadi pada
perpustakaan.uns.ac.id digilib.uns.ac.id
commit to user
26
cuplikan sebagai akibat dari kenaikan suhu, baik yang diikuti oleh perubahan fase kristal maupun tidak.
5. Data SAA yang diperoleh meliputi surface area, average pore radius dan total pore volume yang kemudian dibandingkan dengan referensi sehingga dapat diketahui perbedaan luas permukaan dan pori-pori hydrotalcite-like sebelum dan sesudah penambahan zat aktif KF.
6. Data XRF yang diperoleh berupa kandungan logam yang terdapat dalam senyawa hydrotalcite dengan bentuk oksidanya yang dinyatakan dalam persen.

![Gambar 3. Spektra FTIR dari LDH dengan perbedaan rasio molar (A) spektra OH, (B) spektra serapan H 2 O (C) spektra serapan -CO 3 2- dan (D) spektra serapan [Metal]-OH](https://thumb-ap.123doks.com/thumbv2/123dok/2291779.2730521/26.892.254.699.315.516/gambar-spektra-perbedaan-spektra-spektra-serapan-spektra-serapan.webp)