PRA RANCANGAN PABRIK PERKLOROETILEN DARI ETILEN DIKLORIDA DAN GAS KLOR
KAPASITAS 99.000 TON/TAHUN
Disusun Oleh:
Desi Ramadani (4518044007)
PROGRAM STUDI TEKNIK KIMIA FAKULTAS TEKNIK UNIVERSITAS BOSOWA
MAKASSAR
2023
KATA PENGANTAR
Puji dan syukur kehadirat Tuhan Yang Maha Esa atas segala rahmat dan karuniaNya sehingga penulis dapat menyelesaikan pra rancangan pabrik ini, tugas ini disusun sebagai salah satu syarat yang harus dipenuhi untuk menyelesaikan program studi S1 pada Program Studi Teknik Kimia Fakultas Teknik Universitas Bosowa Makassar. Pada kesempatan ini penulis mengucapkan terima kasih atas segala bantuan baik berupa bimbingan, dorongan, serta semangat dari banyak pihak. Oleh karena itu penulis ingin mengucapkan terima kasih yang sebesar-besarnya kepada :
1. Bapak Dr. H. Nasrullah, S.T., M.T selaku Dekan Fakultas Teknik Universitas Bosowa Makassar.
2. Bapak Dr. Ir. A. Zulfikar, M.T selaku ketua jurusan Teknik Kimia Universitas Bosowa.
3. Bapak Dr. Ridwan, S.T., M.Si selaku dosen Pembimbing 1 4. Ibu Hermawati, S.Si., M.Eng. selaku dosen Pembimbing 2
5. Bapak M.Tang,S.T.,M.Pkim dan Bapak Al Gazali,ST.,MT selaku dosen Penguji.
6. Dosen jurusan Teknik Kimia Fakultas Teknik Universitas Bosowa
7. Teristimewa, Orangtua tercinta dan keluarga besar, terkhusus Ayahanda terhebat Juhari dan Ibunda tersayang Atika, yang tak pernah lelah memberikan semangat, dukungan serta motivasi untuk menggapai gelar Sarjana. Kerja keras dan doa yang tak henti dipanjatkan agar penulis dimudahkan dalam setiap langkah dalam mengerjakan Prancangan pabrik ini. Semoga Allah SWT membalas ketulusan serta kebaikan hati Bapak dan Ibu.
8. Kakanda dan Ayunda di KBM-FT UNIBOS, HIMATEK-FT UNIBOS, HMI KOMISARIAT TEKNIK, HMI KORKOM UNIBOS, dan teman – teman seperjuangan Argon’18 dan TEKNIK18 yang selalu memberikan semangat.
9. Sahabat seperjuangan, “RM”, Nur Rifkatul Hikmayani, S.T, Nurul Salama, S.T, Sari Andira Tahir, S.T, Evelyn Stacy Pabeo, S.T, Irfan Ramadhan, S.T dan Aryawira Sese Tritama, S.T. Berawal dari PROPERSTIK sampai diujung perjuangan menyandang gelar Sarjana Teknik kalian masih bersama penulis.
Tanpa kalian, Prancangan yang hari ini pembaca lihat tidak akan ada, terima kasih telah membersamai suka dan duka selama menjadi mahasiswa. Kebaikan serta ketulusan hati kalian tidak bisa penulis lontarkan dengan kata-kata, serta terima kasih atas segala rasa dan karsa yang selalu membersamai di setiap proses. Enjoy for the new chapter of the journey, selamat datang di dunia yang sebenarnya, dimanapun kalian nantinya, semoga kalian sukses dan sehat selalu.
Terima kasih, tanpa kalian penulis bukan siapa-siapa.
10. Kakanda Maulana Ishaq, S.T , Kakanda Mursid, dan Ayunda Humahera Yanti, S.T, yang selalu memotivasi, serta membimbing penulis dalam menyelesaikan Prancangan serta revisi-revisi, “Ternyata revisi itu tidak serumit yang ada di pikiran apabila dibarengi dengan healing”.
11. Sahabat saya, Bripda Yusman Nur Adyaksa, S.H , Agustina, S.Pd, Nur Ahmad Saputra, S.E ,Resky Wahyu, S.M ,Ifada kasih, dr.Sitti Zhahirah Khairunnisah, S.Ked, dr.Sri Sulfianti, S.Ked, dr.Andi Fajrul Islam, S.Ked, Ria Risky Aprilia, S.IP, Putri Mangadi, S.Pd, Andi Nursyamsuriani A.Md Kes, Kezia Erary, S.T , Afik Piko, S.H , Dandrea Qustalani, S.T, yang memberikan semangat untuk menggapai gelar Sarjana.
12. Keluarga besar Ayahanda Zainuddin, Ibunda Wahida, adek Cica, adek Aulia, dan adek Upi, yang selalu memberikan penulis semangat dalam mengerjakan Prancangan Pabrik ini.
13. Muh. Zaid Yusuf, yang membersamai penulis dalam berproses, selalu memberikan penulis semangat serta mendoakan penulis untuk segera menyandang gelar Sarjana Teknik.
14. Seluruh pihak yang tidak dapat penulis sebutkan satu persatu dalam membantu
menyelesaikan Prancangan Pabrik ini.
15. Last but not least, I wanna thank me, for believing in me, for doing all these hard work, for having no days off, for never quitting, for always being me a giver and trying give more than I receive, for trying to do more right than wrong, for just being me at all times.
Akhirnya dengan segala keterbatasan yang ada, penulis berharap pra rancangan pabrik ini dapat bermanfaat dan digunakan sebagaimana mestinya.
Makassar, 28 Februari 2023
Penulis
DAFTAR ISI
SAMPUL... i
HALAMAN PERSETUJUAN ... Error! Bookmark not defined. SURAT PERNYATAAN ... iii
KATA PENGANTAR... iv
DAFTAR ISI ... vii
DAFTAR GAMBAR ... ix
DAFTAR TABEL ... x
INTISARI ... xii
BAB 1. PENDAHULUAN ... 1
1.1 Latar Belakang Pendirian Pabrik ... 1
1.2 Penentuan Kapasitas Pabrik ... 2
1.3 Pemilihan Lokasi Pabrik... 4
1.4 Tinjauan Pustaka ... 6
BAB II. URAIAN PROSES ... 18
2.1 Tahap Persiapan Bahan Baku ... 18
2.2 Tahap Reaksi Pembentukan Perkloroetilen ... 19
2.3 Tahap Pemurnian ... 20
2.4 Diagram Alir Kualitatif ... 21
2.5 Diagram Alir Kuantitatif ... 22
BAB III. SPESIFIKASI BAHAN ... 23
3.1 Spesifikasi Bahan Baku ... 23
3.2 Spesifikasi Bahan Bantu ... 24
3.3 Spesifikasi Bahan Produk ... 25
BAB IV. NERACA MASSA ... 27
4.1 Neraca Massa Setiap Alat ... 27
4.2 Neraca Massa Total ... 30
BAB V. Neraca Panas ... 31
BAB VI. SPESIFIKASI ALAT PROSES ... 36
BAB VII. UTILITAS ... 47
7.1 Unit Penyediaan Uap (Steam) ... 47
7.2 Spesifikasi Alat Utilitas ... 48
7.4 Unit penyediaan bahan bakar ... 53
BAB VIII. LAY OUT PABRIK DAN PERALATAN PROSES ... 54
8.1 Tata Letak Pabrik ... 54
8.2 Lokasi Pabrik ... 58
8.3 Tata Letak Peralatan Pabrik ... 63
BAB IX. STRUKTUR ORGANISASI PERUSAHAAN ... 65
9.1 Organisasi Perusahaan ... 65
9.2 Struktur Organisasi ... 66
9.3 TUGAS DAN WEWENANG ... 68
9.4 Pembagian Jam Kerja ... 71
9.5 SISTEM KEPEGAWAIAN DAN SISTEM GAJI ... 74
9.6 Fasilitas Karyawan ... 76
BAB X. ANALISIS EKONOMI ... 77
10.1 Dasar Perhitungan ... 78
10.2 Penaksiran Harga Peralatan ... 78
10.3 Penentuan Investasi Modal Total (TCI) ... 79
10.4 Penentuan Biaya Total Produksi (TPC) ... 83
10.5 General Expense ... 85
10.6 Total Penjualan ... 86
10.7 Perkiraan Laba Usaha ... 86
10.8 Analisa Kelayakan ... 86
BAB XI. KESIMPULAN... 90
BAB XII. DAFTAR PUSTAKA ... 91
DAFTAR GAMBAR
Gambar 1.1 Letak Lokasi Pabrik…... 6
Gambar 1.2 Rumus Molekul Etilen Diklorida ... 7
Gambar 1.3 Rumus Molekul Klorin ... 9
Gambar 1.4 Rumus Molekul Ferriclorida ... 10
Gambar 1.5 Rumus Molekul Perkloroetilen ... 11
Gambar 1.6 Rumus Molekul HCl... 13
Gambar 2.1 Diagram Alir Kualitatif ... 25
Gambar 2.2 Diagram Alir Kuantitatif ... 26
Gambar 8.1 Tata Letak Pabrik ... 65
Gambar 8.2 Peta Lokasi Pabrik ... 67
Gambar 8.3 Tata Letak Peralatan ... 73
Gambar 9.1 Struktur Organisasi Perusahaan… ... 76
DAFTAR TABEL
Tabel 1.2 Perbandingan Jenis-jenis Proses Acetaldehyde ... 16
Tabel 4.1 Neraca Massa Tangki Pencampur (TP)… ... 31
Tabel 4.2 Neraca Massa Mix Point Gas Khlor… ... 32
Tabel 4.3 Neraca Massa Reaktor (R)… ... 32
Tabel 4.4 Neraca Massa Kondensor (CD-01) dan Knock Out Drum (KOD) ... 33
Tabel 4.5 Neraca Massa Absorber (AB)… ... 33
Tabel 4.6 Neraca Massa Distilasi (D) ... 34
Tabel 4.7 Neraca Massa Total ... 35
Tabel 5.1 Neraca Panas Tangki Pencampur (TP)… ... 36
Tabel 5.2 Neraca Panas Vaporizer (VP)… ... 36
Tabel 5.3 Neraca Panas Mix Point Gas Umpan Reaktor (MP-02)…... 37
Tabel 5.4 Neraca Panas Furnace (F)… ... 37
Tabel 5.5 Neraca Panas Reaktor (R)… ... 37
Tabel 5.6 Neraca Panas Cooler (C-01)... 37
Tabel 5.7 Neraca Panas Cooler (C-02)... 37
Tabel 5.8 Neraca Pana Partial Kondensor (CD-01). ... 38
Tabel 5.9 Neraca Panas Knock Out Drum (KOD) ... 38
Tabel 5.10 Neraca Panas Cooler (C-03)... 39
Tabel 5.11 Neraca Panas Absorber (AB) ... 39
Tabel 5.12 Neraca Panas Mix Point Khlor (MP-01). ... 39
Tabel 5.13 Neraca Panas Cooler (C-04)... 40
Tabel 5.14 Neraca Panas Distilasi (D) ... 40
Tabel 5.15 Neraca Panas Cooler (C-05)... 40
Tabel 7.1 Kebutuhan Steam Untuk Pemanas ... 53
Tabel 7.2 Spesifikasi Boiler ... 53
Tabel 7.3 Spesifikasi Pompa Air Sungai ... 54
Tabel 7.4 Spesifikasi Bak Air Penampungan Air Sungai ... 54
Tabel 7.5 Spesifikasi Clarifier… ... 55
Tabel 7.6 Spesifikasi Sand Filter ... 55
Tabel 7.7 Spesifikasi Bak Air Bersih… ... 56
Tabel 7.8 Spesifikasi Deminirilizer Water ... 56
Tabel 7.9 Spesifikasi Bak Air Lunak ... 57
Tabel 7.10 Spesifikasi Tangki Umpan Boiler ... 57
Tabel 7.11 Spesifikasi Bak Air Pendingin. ... 58
Tabel 7.12 Spesifikasi Bak Air Sanitasi ... 58
Tabel 7.13 Spesifikasi Cooling Tower. ... 58
Tabel 7.14 Perhitungan Spesifikasi Alat Pompa Water Treatment... 59
Tabel 7.15 Kebutuhan Tenaga Listrik untuk Unit Proses ... 60
Tabel 7.16 Kebutuhan Tenaga Listrik untuk Unit Utilitas ... 60
Tabel 7.17 Spesifikasi Power Generator. ... 61
Tabel 7.18 Spesifikasi Tangki Bahan Bakar Generator. ... 61
Tabel 9.1 Jadwal Kerja Karyawan Shift ... 82
Tabel 9.2 Perincian Gaji Karyawan… ... 84
INTISARI
Perkloroetilen atau C2Cl4 dibuat dengan mereaksikan etilen diklorida (C2H4Cl2) dengan gas klor (Cl2) dengan menggunakan katalis Ferriclorida dimana kondisi operasi 425°C dan tekanan 1,2 atm. Reaksi tersebut berlangsung didalam reaktor fluidized bed . Reaksinya bersifat eksotermis dan digunakan air sebagai pendingin. Kapasitas produksi pabrik perkloroetilen dirancang 99.000 ton/tahun membutuhkan bahan baku etilen dikhlorida 99% sebesar 7.450,00 ton/tahun dan gas klor sebesar 16.010,99 ton/tahun . Utilitas berupa air 1.176.106,6590 kg/jam, listrik sebesar 643,2790 kwatt. Pabrik ini direncanakan didirikan di Cilegon, Banten di atas tanah seluas 33.600 m2. Bentuk perusahaan adalah Perseroan Terbatas (PT) dengan system garis dan staff yang membutuhkan tenaga kerja sebanyak 124 orang. Pabrik ini beroperasi selama 330 hari efektif setiap tahum dan 24 jam/hari. Berdasarkan perhitungan evaluasi ekonomi untuk pendirian pabrik perkloroetilen dibutuhkan modal sebesar Rp.2.480.119.746.719. Pabrik perkloroetilen ini membutuhkan Fixed Capital Invesment (FCI) Rp.1.855.624.718.925 dan Working Capital (WC) Rp.1.554.858.867.893. Analisis ekonomi pabrik perkloroetilen menunjukan nilai ROI sebelum pajak sebesar 50,93%, dan ROI setelah pajak 33,11%. Nilai POT sebelum pajak 1,64 tahun dan POT setelah pajak 2,32 tahun. BEP sebesar 42,95% kapasitas produksi dan SDP sebesar 29,19% kapasitas produksi. Berdasarkan data analisis ekonomi tersebut, maka pabrik perkloroetilen ini layak untuk dikaji lebih lanjut.
Kata Kunci : Etilen Diklorida, Klor, Etilen Diklorida, Pra rancangan.
BAB 1. PENDAHULUAN
1.1 Latar Belakang Pendirian Pabrik
Perkloroetilen atau yang biasa disebut Tetrakloroetilena merupakan salah satu dari sekian banyak zat kimia yang banyak digunakan sebagai bahan baku industri kimia. Perkloroetilen memiliki rumus molekul yaitu C2Cl4. Penggunaan utama dari produk perkloroetilen ini yaitu sebagai pelarut dalam industri dry cleaning, biasanya perkloroetilen ini digunakan sebagai penggosok logam, industri penghasil cairan pengering untuk tekstil atau industri produsen pelarut untuk sejumlah senyawa organik. Etilen diklorida sedikit larut dalam air tetapi larut dalam pelarut polar seperti ethanol dan benzene.
Penggunaan lain perkloroetilen merupakan intermediet produk yang selanjutnya digunakan untuk memproduksi bahan kimia lainnya, antara lain untuk menghasilkan trikloroetilen acid dan fluorocarbon. Pertimbangan untuk mendirikan sebuah pabrik di dunia industri adalah untuk mendapatkan sebuah keuntungan yang optimal. Berdirinya pabrik ini, diharapkan dapat memanfaatkan sebuah potensi yang ada serta dukungan teknologi perkloroetilen dengan menggunakan bahan baku berupa etilen diklorida (C2H4Cl2) dan klorin (Cl2) yang banyak tersedia di Indonesia. Etilen diklorida atau 1.2 dichloroethane dengan rumus molekul C2H4Cl2 adalah senyawa yang sangat beracun dengan kenampakan berupa cairan seperti minyak tapi tidak berwarna dan mempunyai aroma yang enak. Perkembangan sektor industri di Indonesia, khususnya industri kimia dari tahun ketahun telah mengalami peningkatan baik kualitas maupun kuantitas, sehingga kebutuhan akan bahan baku, bahan pembantu maupun tenaga kerja semakin meningkat
Dilihat dari kebutuhan perkloroetilen pada saat ini yang semakin meningkat dari tahun ke tahun, beriringan dengan industri yang memakai produk perkloroetilen, maka dengan berdirinya pabrik ini diharapkan dapat memberi peluang perkembangan industri kimia lainnya. Oleh karena itu, pabrik perkloroetilen perlu didirikan di Indonesia dengan beberapa pertimbangan-pertimbangan sebagai
berikut :
Dapat menghemat devisa negara, karena sampai saat ini kebutuhan perkloroetilen di Indonesia masih dipenuhi dengan impor. Dengan adanya pabrik perkloroetilen di dalam negeri maka impor perkloroetilen dapat dikurangi dan jika berlebih dapat di ekspor.
Dapat memacu pertumbuhan serta pembangunan pabrik industri yang baru menggunakan bahan dasar perkloroetilen di Indonesia.
Bahan baku yang berupa etilen diklorida yang mudah diperoleh di Indonesia.
Berperan serta dalam menunjang usaha pemerintah dalam hal menciptakan lapangan kerja baru di bidang industri kimia. Produksi dari etilen diklorida dengan reaksi oksiklorinasi :
C2H4Cl2 + 3Cl2 C2Cl4 + 4HCl
Penggunaan etilen sebagai bahan baku yang harganya lebih murah dan mudah didapat. Reaksi terjadi pada temperature tinggi sehingga memiliki reaksi yang cepat dengan konversi sekitar +-90% (Kirk and Othmer,1967).
1.2 Penentuan Kapasitas Pabrik
Kapasitas produksi pabrik perkloroetilen akan ditentukan berdasarkan banyaknya kebutuhan dalam negeri. Berdasarkan data statistik dan Bahan Pusat Statistik dari tahun 2017-2021, dapat dilihat pada table berikut :
Tabel 1.1 Data Impor Perkloroetilen di Indonesia 2017-2021
Tahun Impor (Kg)
2017 59.723.568
2018 56.245.315
2019 60.159.138
2020 72.025.854
2021 63.884.897
Sumber : Badan Pusat Statistik,2022
Berikut grafik data impor di Indonesia tahun 2017-2021
Kapasitas bahan baku pabrik menggunakan metode pertumbuhan rata-rata per tahun, yaitu sebagai berikut:
TAHUN Kebutuhan KENAIKAN (%)
2017 59.723.568 -
2018 56.245.315 -0,06
2019 60.159.138 0,07
2020 72.025.854 0,20
2021 63.884.897 -0,11
n=5 P
I
0,02 0.004778641 Keterangan :
F = P (1 + i)n
F : Perkiraan nilai impor pada tahun 2027 P : Nilai impor tahun 2021
i : kenaikan rata-rata impor setiap tahun dalam % n : jangka waktu pabrik berdiri (2022 – 2027) = 5 tahun Sehingga:
F = P (1 + i)n
= 63.961,25 ton (1 + 0,004778641%)5
= 65504.16948 ton/tahun
Apabila belum ada pabrik di dalam negeri, maka kapasitas produksi dapat diterapkan 1,5 kali dari peluang yang ada :
75.000.000,00 70.000.000,00 65.000.000,00 60.000.000,00 55.000.000,00
y = 2E+06x - 5E+09 R² = 0,4009
50.000.000,00
2016 2017 2018 2019 Tahun
2020 2021 2022
Kebutuhan
Kapasitas produksi = 65504.16948 ton x 1,5
= 98256.25422 ton/tahun
= 99.000 ton/tahun
Sampai saat ini pabrik Perkloroetilen belum ada di Indonesia dan masih mengimpor untuk kebutuhan dalam negeri. Dengan perhitungan pertumbuhan rata-rata diatas dan mempertimbangkan beberapa aspek maka dipilih kapasitas pabrik 99.000 ton/tahun agar dapat mencukupi kebutuhan dalam negeri.
1.3 Pemilihan Lokasi Pabrik
Untuk merancang sebuah pabrik hal yang penting untuk diperhatikan yaitu penentuan lokasi pabrik. Pemilihan lokasi pabrik merupakan salah satu hal yang dapat mempengaruhi keberhasilan, kelangsungan dan perkembangan dari sebuah pabrik. Pendirian pabrik perkloroetilen ini direncanakan di Cilegon, Banten.
Dengan beberapa pertimbangan, sebagai berikut : 1.3.1 Sumber bahan baku
Bahan baku merupakan faktor yang sangat penting dalam penentuan lokasi sebuah pabrik. Perhatian utama yang harus diberikan untuk penyiapan bahan baku adalah kesiapan suplay dari sumber bahan baku secara continue serta peralatan penyimpanan. Dalam hal ini, pabrik perkloroetilen ini akan didirikan di Cilegon, Banten karena dekat dengan sumber bahan baku. Bahan baku etilen diklorida diperoleh dari PT. Sulfindo Adi Usaha, Jawa Barat dan bahan baku klorin diperoleh dari PT. Asahimas, Jawa Barat. Tersedianya bahan baku yang cukup besar diharapkan kebutuhan bahan baku bisa terpenuhi.
1.3.2 Pemasaran
Dipilihnya Cilegon, Banten sebagai lokasi pabrik dengan adanya pertimbangan bahwasanya sebagian besar industri di pulau Jawa terutama di Jakarta dan Jawa Barat yang merupakan sasaran empuk pemasaran produk perkloroetilen sehingga memudahkan dalam pemasaran produk nantinya.
1.3.3 Utilitas
Didaerah Cilegon, Banten terdapat PLTU (Pembangkit Listrik Tenaga Uap)
Sularaya sehingga memudahkan untuk mendapatkan suplay listrik dari PLN.
Fasilitas pendukung berupa air dan bahan bakar tersedia cukup memadai dikarenakan merupakan kawasan industri.
1.3.4 Transportasi
Tersedianya sarana jalan raya memudahkan untuk pendistribusian produk ke konsumen ke berbagai daerah di Pulau Jawa dan sarana pelabuhan untuk pendistribusian diluar Pulau Jawa.
1.3.5 Tenaga Kerja
Pada daerah Banten, khususnya Cilegon merupakan daerah yang kapasitas penduduknya cukup tinggi sehingga kebutuhan tenaga kerja ini dapat mudah dipenuhi.
1.3.6 Letak Pabrik
Tata letak pabrik merupakan pengaturan atau penyusunan peralatan dan fasilitas pabrik lainnya, sedemikian sehingga pabrik bisa berfungsi dengan efektif, efesien, dan aman. Tujuan yang akan dicapai, yaitu :
Memberikan efisien yang tinggi
Memudahkan pemasangan, pemeliharaan, dan perbaikan
Memberikan semangat kerja untuk karyawan
Memberikan jaminan keselamatan kerja
Menekan biaya produksi serendah mungkin dengan hasil semaksimal mungkin.
Untuk memudahkan mendapatkan kondisi seperi ini, maka adapun hal- hal yang perlu di perhatikan, sebagai berikut :
Tata letak alat proses diatur sedemikian rupa sehingga memudahkan penyusunan.
Bahan baku, tenaga kerja, dan transportasi ditangani seefektif dan seefisien mungkin.
Fasilitas untuk karyawan seperti koperasi, kantin, sarana olahraga, poliklinik dan sebagainya diletakan secara strategis dan tidak mengganggu jalannya proses.
Jarak antar unit satu dengan yang lainnya diatur sedemikian rupa sehingga memudahkan aktivitas saat bekerja dilapangan dan
memudahkan proses pengalian, perbaikan, dan tidak mengganggu lalu lintas pekerja.
Pengontrolan terhadap jalannya alat-alat proses dilakukan secara rutin pada ruang control tersendiri.
Persediaan lahan tanah untuk perluasan dan pengembangan pabrik.
Kawasan industri Cilegon, merupakan lokasi yang sangat mendukung untuk pendirian pabrik Perkloroetilen dikarenakan lokasinya sangat strategis. Kawasan industri ini adalah lokasi yang sangat memadai mulai dari sarana dan prasarana dan merupakan bagian dari otonomi daerah yang telah mendapatkan dukungan dari pemerintah dan sudah ada beberapa industri yang beroperasi di kawasan tersebut.
Gambar 1.1 Letak Lokasi Pabrik 1.3.7 Power dan Persediaan Bahan Bakar
Power dari steam sangat dibutuhkan sehingga besarnya sebuah industri, dan bahan bakar umumnya digunakan untuk penyediaan utilitas. Biaya power lokal dapat menolong menentukan di mana power itu harus diangun atau dihasilkan sendiri.
1.4 Tinjauan Pustaka 1.4.1 Bahan Baku
Bahan baku adalah bahan yang harus ada dalam sebuah industri, karena bahan baku akan diolah menjadi suatu pabrik dan produk tersebut akan dijualkembali. Adapun bahan baku yang digunakan dalam pabrik ini adalah :
1. Etilen Diklorida (1,2 – Dikloroetana)
Etilen diklorida atau 1.2 dichloroethane dengan rumus molekul C2H4Cl2
adalah senyawa yang sangat beracun dengan kenampakan berupa cairan seperti minyak tapi tidak berwarna dan mempunyai aroma yang enak. Etilen diklorida sedikit larut dalam air tetapi larut dalam pelarut polar seperti ethanol dan benzene. (Kirk &Othmer, vol 6, 1993).
Etilen diklorida (C2H4Cl2) merupakan salah satu bahan kimia produk industri yang digunakan sebagai bahan baku untuk memproduksi monomer vinil klorida yang merupakan bahan baku utama pembuatan polivinil klorida . Etilen diklorida juga bahan baku etilene diamina, perkloretilen, karbon tetra klor- ida dan trikloroetilen. Etilen diklorida juga digunakan sebagai zat antara (interme-diete) dalam proses pembuatan berbagai zat-zat organik disamping itu juga digunakan sebagai zat pelarut/solven pada industri anti-knocking agent, minyak dan lilin. Serta sebagai bahan baku ethylene diamina, perchlor ethylene, carbon tetra chlorida dan trichloro ethylene.
2. Klorin
Gambar 1.2 Rumus Molekul Etilen Diklorida Sumber: roboguru.ruangguru.com
Klorin adalah bahan kimia yang biasanya digunakan sebagai pembunuh kuman. Zat klorin akan bereaksi dengan airmembentuk asam hipoklorus yang diketahui dapat merusak sel-sel dalamtubuh. Klorin berwujud gas berwarna kuning kehijauan dengan bau cukup menyengat. Penggunaan klorin dalam pangan bukan hal yang asing. Klorin sekarang bukan hanya digunakan untuk bahan pakaian dan kertas saja, tetapi telah digunakan sebagai bahan pemutih atau pengkilat beras, agar beras yang berstandar medium menjadi beras
berkualitas super (Darniadi dalam Wongkar, 2014).
Klor (berasal dari bahasa Yunani Chloros, yang berarti “hijau pucat”), adalah unsur kimia dengan nomor atom 17 dan simbol Cl termasuk dalam golongan halogen. Klorin merupakan unsur kedua dari keluarga halogen, terletak padahalogen VII A periode III. Sifat kimia klorin sangat ditentukan oleh konfigurasi elektron pada kulit terluarnya. Keadaan ini membuatnya tidak stabil dan sangatreaktif. Hal ini disebabkan karena struktuk electron gas mulia. Disamping itu, klorin juga bersifat sebagai oksidator. Seperti halnya oksigen, klorin juga membantu reaksi pembakaran dengan mengahasilkan panas cahaya. Dalam air laut maupaun sungai, klorin akan terhidrolisa membentuk asam hipoklorit (HClO) yang merupakan suatu oksidator. Klorin tidak terbakar di udara, melainkan bereaksi secara kimia.
Klorin ialah unsur yang sangat aktif hampir dengan setiap unsur dapat langsungbersenyawa dan reaksinya besar sekali .
Gas klor yang mudah dikenal karena baunya yang khas itu, bersifat merangsang (iritasi terhadap selaput lendir pada mata/conjunctiva). Selaput lender hidung, selaput lender tenggorok, tali suaradan paru-paru. Menurut World HealthOrganization (WHO) nilai ambang batasresidu klorin dalam air adalah 0,5 ppm (Suryaningrum, dkk, 2007).
1.4.2 Bahan Bantu
Gambar 1.3 Rumus Molekul Klorin Sumber: roboguru.ruangguru.com
Bahan pembantu adalah bahan yang dipakai dalam proses produksi, tetapi tidak dapat diidentifikasikan dengan barang jadi yang dihasilkan. Bahan pembantu yang dipakai pada proses peroduksi adalah asam sulfat yang berperan sebagai katalis.
1. Ferri Chlorida
Besi(III) klorida, atau ferri klorida, adalah suatu senyawa kimia yang merupakan komoditas skala industri, dengan rumus kimia FeCl3. Senyawa ini umum digunakan dalam pengolahan limbah, produksi air minum maupun sebagai katalis,baik di industri maupun di laboratorium. Warna dari kristal besi (III) klorida tergantung pada sudut pandangnya, dari cahaya pantulan ia berwarna hijau tua, tetapi dari cahaya pancaran ia berwarna ungu-merah.
Besi (III) klorida bersifat deliquescent, berbuih di udara lembap, karena munculnya HCl, yang terhidrasi membentuk kabut. Bila dilarutkan dalam air, besi (III) klorida mengalami hidrolisis yang merupakan reaksi eksotermis (menghasilkan panas). Hidrolisis ini menghasilkan larutan yang coklat, asam,dan korosif, yang digunakan sebagai koagulan pada pengolahan limbah dan produksi air minum. Larutan ini juga digunakan sebagai pengetsa untuk logam berbasis-tembaga pada papan sirkuit cetak (PCB). Anhidrat dari besi(III) klorida adalah asam Lewis yang cukup kuat, dan digunakan sebagai katalis dalam sintesis organik.
1.4.3 Produk
Gambar 1.4 Rumus Molekul Ferri Chlorida Sumber: roboguru.ruangguru.com
Pengertian produk secara umum adalah segala sesuatu yang mampu dihasilkan dari proses produksi berupa barang ataupun jasa yang nantinyabisa diperjualbelikan di pasar.
1. Perkloroetilen
Perkloroetilen yang memiliki rumus molekul C2Cl4, berat molekulnya 165,83 sering juga disebut tetrakloroetilen, dalam dunia industri kimia secara luas dikenal dengan nama PER. Perkloroetilen adalah zat yang dalam bentuk
cairan tidak berwarna, baunya seperti eter, tahan terhadap hidrolisis, larut dalam alkohol, eter dan minyak dalan berbagai proporsi, serta tidak larut dalam air. Dihasilkan pertama kali oleh Faraday pada tahun 1821, melalui pembusukan karekan disebabkan adanya pemanasan heksakloroetan. Produksi dasar dari industri asetilen dimulai sejak dasawarsa pertama abad ini. Pada tahun 1950-an, perkloroetilen menjadi dry-cleaning solvent. Pada tahun 1887 Combes membuat perkloroetilen dengan memanaskan chloral dan anhydrous alumunium chloride. Kemudian pada awal tahun 1925 ditemukan kegunaan perkloroetilen sebagai penggosok logam dan cairan pengering untuk tekstil.
Sejak itu perkloroetilen mulai diproduksi secara komersial. Perkloroetilen merupakan salah satu senyawa organik yang sangat luas penggunaannya, antara lain :
- Sebagai bahan penggosok logam (metal degreasing)
- Sebagai cairan pengeringan (dry cleaning liquid) untuk semua jenistekstil, baik alam maupun sintetis
- Sebagai pelarut untuk asam benzoat, asam amoniak, asam cinnamic,asam trikloroasetat, karet, cat, tinta dan sabun
- Sebagai bahan untuk mengekstraksi sulfur dari butiran-butiran oksida yang dipakai dalam purifikasi
Perkloroetilen dapat diproduksi dengan menggunakan bahan baku asetilen, etilen, propilen, diklorid propane, klorid dan HCl, tergantung pada proses yang akan digunakan. Sebagai contoh, proses yang dilakukan oleh Pittsburgh , sebuah pabrik yang berlokasi di Barberton, Ohio, dengan menggunakan bahan baku propane, dan propilen diklorida, sedangkan du poat di New York menggunakan bahan baku asetilen,(Kirk and Othmer, 1967).
Dari beberapa proses maka pada prarancangan pabrik ini akan menggunakan proses dari bahan baku etilen diklorida karena :
- Harga bahan baku lebih murah
- Dalam proses produksinya tidak menggunakan pelarut - Bahan baku dapat terkonversi sampai 90%
- Tekanan prosesnya rendah Reaksi yang terjadi :
C2H4Cl2 + 3Cl2 C2Cl4 + 4HCl
Gambar 1.5 Rumus Molekul Perkloroetilen Sumber: roboguru.ruangguru.com 2. Hidrogen Klorida
Asam klorida adalah larutan akuatik dari gas hidrogen klorida (HCl).
HCl adalah asam kuat, dan merupakan komponen utama dalam asam lambung.Senyawa ini juga digunakan secara luas dalam industri. Asam klorida harus ditangani dengan wewenang keselamatan yang tepat karena merupakan cairan yang sangat korosif. Asam klorida adalah asam anorganik kuat yang digunakan dalam berbagai proses industri seperti pengolahan logam.
Asam klorida dikenal oleh alkemiawan Eropa sebagai roh garam atau acidum salis (asam garam). Kedua nama tersebut masih digunakan terutama dalam bahasa lain: Salzsäure, Belanda: Zoutzuur, Swedia: Saltsyra, dan Polandia: kwas solny. Gas HCl disebut udara asam laut. Nama sebelumnya (pra-sistematis) adalah asam muriatat(bahasa Inggris: muriatic acid) (muriatic berarti "yang berkaitan dengan air garam atau garam", dan dari situ muriat berarti hidroklorida), dan nama ini masih kadang-kadang digunakan. Nama
"asam klorida" diciptakan oleh kimiawan Perancis Joseph Louis Gay- Lussac pada tahun 1814. Asam klorida pernah menjadi zat yang sangat penting dan sering digunakandalam awal sejarahnya. Ia ditemukan oleh alkimiawan Persia Abu Musa Jabir bin Hayyan sekitar tahun 800.
Senyawa ini digunakan sepanjang abad pertengahanoleh alkimiawan dalam pencariannya mencari batu filsuf, dan kemudian digunakan juga oleh ilmuwan Eropa termasuk Glauber, Priestley, and Davy dalam rangka membangun pengetahuan kimia modern.
Sejak Revolusi Industri, senyawa ini menjadi sangat penting dan digunakan untuk berbagai tujuan, meliputi sebagai pereaksi dalam produksi massal senyawa kimia organik seperti vinil klorida untuk plastik PVC dan MDI/TDI ntuk Poliuretana. Kegunaan kecil lainnya meliputi penggunaan dalam pembersih rumah, produksi gelatin, aditif makanan, dan pengolahan kulit. Sekitar 20 juta ton gas HCl diproduksi setiap tahun. pada abad ke-20 proses Leblanc digantikandengan proses Slovay yang tidak menghasilkan asam klorida sebagai produk sampingan.
1.4.4 Pemilihan Proses 1.4.4.1 Dasar Reaksi
Gambar 1.6 Rumus Molekul HCl Sumber: roboguru.ruangguru.com
Reaksi pembentukan perkloroetilen merupakan reaksi klorinasi fase uap menggunakan reaktor fixed bed dengan bantuan katalis. Katalis yang digunakan adalah ferriklorida. Pada proses ini dapat menghasilkan perkloroetilene dengan kemurnian 99 %. Pembuatan perkloroetilen dari etilen diklorida dengan proses klorinasi fase uap berjalan pada suhu 200 – 440 0C dan tekanan 1- 2 atm.
C2H4Cl2 + 3Cl2 C2Cl4 + 4HCl 1.4.4.2 Mekanisme Reaksi
Reaksi yang terjadi antara gas etilen diklorida dan gas chlorine dengan adanya katalisator FeCl3 adalah reaksi ionik dengan mekanisme sebagai berikut :
FeCl + Cl FeCl + Cl-
C2H4Cl2 + Cl- C2Cl4 + H+ H+ + FeCl4-
FeCl3 + HCl
Secara komersial perkloroetilen dapat diproduksi dengan proses sebagai berikut :
1. Proses klorinasi Acetylene
Reaksi yang terjadi selama proses klorinasi asetilen terbagi dalam 4 tahapan reaksi, yaitu :
C2H2 + 2Cl2 C2H2Cl4 ∆H298°K = -379,45 Kkal/Kmol C2H2Cl4 C2HCl3 + HCl ∆H298°K = 50,8 Kkal/Kmol C2HCl3 + Cl2 C2HCl5 ∆H298°K = 132,64 Kkal/Kmol C2HCl5 C2Cl4 + HCl ∆H298°K = 37,83 Kkal/Kmol
Klorin dan asetilen di reaksikan, menghasilkan tetrakloroetana (C2H2Cl3) dialirkan secara countercurrent dengan suspense milk of lime (10%) dalam packed tower yang dipanaskan. HCl diperoleh sebagai produk samping dan trikloroetilen diperoleh sebagai produk utama.
(Austin, 1977).
Trikloroetilen diklorinasi dimenara klorinasi (70-100°C) dengan katalis lewis-acid (0,1 – 1 wt% FeCl3) menghasilkan pentakloroetan.
Perkloroetilen diperoleh dari katalis pemecah panas (170-330°C, karbon aktif). Yield overall (berdasarkan asetilen) 90-94%.
Karena harga bahan baku yang mahal dan melalui 4 tahapan reaksi, menyebabkan lamanya waktu produksi sehingga biaya produksinya besar.
Proses ini sudah lama tidak digunakan lagi.
2. Proses klorinasi etilen diklorida
Pada proses ini, etilen diklorida (C2H4Cl2) dan Klorin (Cl2) cair diuapkan secara terpisah terlebih dahulu, kemudian keduanya dimasukan kedalam reaktor fixed bed multitubular yang berisi katalis feri klorida. Pada proses ini, tinggi suhu mencapai 200-440°C, dengan tekanan 1-2 atm.
Reaksi yang terjadi sebagai berikut :
C2H4Cl2 + 3Cl2 C2Cl4 + 4HCl ∆H298°K=-251,63 Kkal/Kmol
Produk dari hasil reaksi klorinasi dialirkan kedalam absorber untuk penyerapan perkloroetilen dan terpisah dari HCl. Lalu, terpisah pada proses destilasi. Keuntungan proses klorinasi etilen diklorida yaitu pembetukan produk samping sedikit, dioperasikan pada tekanan rendah, bahan bakunya banyak tersedia di Indonesia sehinggan kontinuitas terjaga, dan proses ini merupakan proses yang sekarang banyak digunakan dalam industri untuk memproduksi perkloroetilen.
3. Oksi klorinasi (Oxychlorination)
Etilen diklorida, HCl, dan Oksigen dimasukan kedalam reaktor fluidized bed dengan katalis ferriclorida. Reaksi terjadi pada suhu 370-425°C dan tekanan 7-20 atm. Dari reaktor kemudian dimasukan kedalam separator untuk untu memisahkan fraksi berat dan fraksi ringan. Fraksi ringan keluar dari bagian atas separator dan masuk ke dalam kolom scrubber yang berfungsi yang menetralisir gas-gas yang bersifat asam, terutama HCl yang akan keluar ke udara bebas (Stack Gas).
Pada bagian bawah kolom separator keluar fraksi berat yang kemudian dimasukan kedalam kolom destilasi untuk memurnikan produk. Dibagian atas kolom destilasi akan keluar produk samping trikkloroetilen dan pada bagian bawah kolom destilasi akan keluar produk saping tetrakloroetilen beserta sedikit air (H2O). Reaksi yang terjadi pada proses ini, sebagai berikut :
C2H4Cl2 + Cl2 + O2 C2Cl4 + 2H2O ∆H298°K = -366,03 Kkal/Kmol 4C2H4Cl2 + 2Cl2 + 3O2 4C2HCl3 + 6H2O ∆H298°K = -970,48 Kkal/Kmol Keuntungan pada proses ini yaitu tidak ada produk samping HCl yang dihasilkan. Sedangkan kerugiannya adalah proses dioperasikan pada tekanan tinggi (Kirk Othmer, 1996).
Tabel 1.2. Perbandingan Jenis-Jenis Proses Acetaldehyde
Proses Suhu
(°C)
Tekanan (atm)
Katalis Yield (%) Klorinasi Asetilen 70-110 8-15 Karbon Aktif 90-94 Klorinasi etilen
diklorida 200-440 1 Feriklorida 90-92
Oksiklorinasi 370-425 7-20
Pottasium klorida, tembaga klorida
85-90
Dari beberapa macam proses pembuatan perkloroetilen dipilih jenis pembuatan dengan proses klorinasi etilen diklorida karena pembentukan produk samping sedikit, dioperasikan pada tekanan rendah, bahan bakunya banyak tersedia di Indonesia sehingga kontinuitas terjaga, dan proses ini adalah proses yang sekarang banyak digunakan oleh industri untuk memproduksi perkloroetilen.
1.4.5 Tinjauan Proses Secara Umum
Penemu perkloroetilen yang pertama kali yaitu M. Faraday pada tahun 1821.
Etilen diklorida direaksikan dengan klorin menghasilkan perkloroetilen dan asam klorida menggunakan katalis feri klorida. Reaksinya berupa :
C2H4Cl2 + 3Cl2 C2Cl4 + 4HCl
Konversi etilen diklorida sebesar 95% dan kondisi operasi pada suhu 200-400°C dengan tekanan 1-2 atm.
1.4.6 Tinjauan Kinetika
Pada reaktor terjadi reaksi utama :
C2H4Cl2 + 3Cl2 C2Cl4 + 4HCl
Pengaruh suhu terhadap konstanta kecepatan reaksi dapat ditinjau dari persamaan :
Keterangan :
k = 0,69.104 exp [ - 15000 / RT ] k = konstanta kecepatan reaksi, liter/mol.detik
Dari persamaan diatas, diketahui bahwa dengan semakin tingginya suhu reaksi, harga konstanta k akan semakin besar (kecepatan reaksi bertambah).
1.4.7 Tinjauan Termodinamika Data :
∆G C2H4Cl2 (298°K) = -73,85 kkal/mol
∆G C2Cl4 (298°K) = 22,64 kkal/mol
∆G HCl (298°K) = -95,3 kkal/mol Perubahan energi Gibbs dapat dihitung dengan persamaan :
∆G 298 = - R . T In K Dengan :
∆G 298 = Energi bebas Gibbs standart suatu reaksi pada 298°K (kkal/mol)
R = Konstanta gas (R = 0,0019872 kkal/mol.K) T = Temperatur (°K)
K = Konstanta keseimbangan Reaksi :
C2H4Cl2 + 3Cl2 C2Cl4 + 4HCl
G 298 = G 298 produk - G 298 reaktan
= -385,56 – (-73,85)
= -284,71 kkal/mol
G 298 = - R T ln K
-284,71 kkal/mol = - 0,0019872 kkal/mol.K x 298 oK x ln K -284,71 kkal/mol = - 0,592186 kkal/mol x ln K
K = 6,3004E+208 Dari persamaan :
Keterangan :
ln (K/K1) =-(H298/R)x(1/T-1/T1)
K1 = Konstanta kesetimbangan pada temperature tertentu T1 = Temperatur tertentu (oK)
∆H298 = Panas reaksi pada 298°K Data panas reaksi pada 298oK :
H C
H C2Cl4 (298 K) : -12,13 kkal/mol
H HCl (298 K) : -92,3 kkal/mol
H 298 = H 298 produk - H 298 reaktan
= –381,33 – (-129,7) kkal/mol
= -251,63 kkal/mol
Pada suhu T1 = 200°C = 473°K, besarnya konstanta kesetimbangan diperoleh dari perhitungan sebagai berikut :
ln (K/K1) = - (H 298 / R) x (1/T - 1/T1)
ln (K / K1) = - (-251,63 / 0,0019872 ) x (1/298 – 1/473) ln (K / K1) = 126.625,4026 x 1,2415.10-3
ln (K / K1) = 157,2104 K1 = 3,3399E+140
Setelah dilakukan perhitungan, diperoleh harga K1 = 3,3399E+140, karena harga konstanta kesetimbangan yang cukup besar, maka reaksi ini adalah reaksi irreversible (searah / tidak dapat balik).
BAB II. URAIAN PROSES
Proses pembuatan perkloroetilen yaitu dengan mereaksikan etilen diklorida dan khlor dalam fase gas. Proses yang dilakukan dalam 3 tahapan, yaitu :
1. Tahap persiapan bahan baku
2. Tahap reaksi pembentukan perkloroetilen 3. Tahap pemurnian
2.1 Tahap Persiapan Bahan Baku
Larutan etilen diklorida yang diumpankan pada tangki bahan baku pada kondisi suhu 30°C dan P=1 atm dengan adanya bantuan pompa dialirkan ketangki pencampuran untuk dicampur dengan aliran recycle etilen diklorida yang berasal dari produk atas kolom Distilasi. Campuran larutan etilen diklorida keluar tangki pencampuran pada temperatur 30°C, selanjutnya dengan menggunakan pompa dialirkan ke Vaporizer untuk diuapkan dengan kondisi temperatur 98°C dan tekanan 1 atm. Sementara itu gas klor dari tangki bahan baku gas klor yang disimpan pada kondisi suhu T=30°C dan tekanan P=1,5 atm dialirkan melewati Expander untuk diturunkan tekanannya sampai 1 atm dan dicampur dengan aliran gas klor recycle yang berasal dari produk atas Absorber pada kondisi temperatur 72°C dan tekanan 1 atm. Campuran gas klor pada temperatur 30°C selanjutnya dicampur dengan aliran uap etilen diklorida yang keluar dari Vaporizer. Campuran gas etilen diklorida dan gas klor pada temperatur °C selanjutnya dilewatkan ke furnace untuk dinaikan temperaturnya sampai 425°C sebelum diumpankan masuk kedalam reactor. Proses pembuatan perkloroetilen yang digunakan oleh industri-industri ada (dua) macam proses yang penting, antara lain :
1. Produksi dari asetilen dan trikloroetilen Reaksi :
C2H2 + 2Cl2 C2H2Cl4
C2H2Cl4 C2HCl3 + HCl
C HCl + Cl C HCl
C2HCl5 C2Cl4 + HCl
Dikarenakan panjangnya rangkaian produksi terdiri dari 4 langkah reaksi dan penggunaan asetilen memerlukan biaya yang lebih tinggi, proses ini telah berkurang penggunaannya selama 20 tahun belakangan ini, (Kirk and Othmer, 1967).
2. Produksi dari etilen
Etilen diklorida pada suhu ruangan dan tekanan atmosfer berupa cairan tak berwarna, berbau enak sedikit larut dalam air tetapi larut dalam pelarut organik (alkohol, eter, benzene). Etilen diklorida tidak mudah teroksidasi, tidak korosif terhadap logam , mudah menguap, menstabilkan proses hidrolisa pada kondisi normal, tidak mudah terbakar namun mempercepat pembakaran. Produksi dari etilen diklorida dengan reaksi oksiklorinasi :
C2H4Cl2 + 3Cl2 C2Cl4 + 4HCl
Penggunaan etilen sebagai bahan baku yang harganya lebih murah dan mudah didapat. Reaksi terjadi pada temperature tinggi sehingga memiliki reaksi yang cepat dengan konversi sekitar +-90% (Kirk and Othmer,1967).
2.2 Tahap Reaksi Pembentukan Perkloroetilen
Reaksi yang terjadi antara etilen diklorida dengan klor membentuk perkloroetilen, dijalankan didalam reaktor tipe fluidized bed reaktor pada kondisi operasi temperatur isothermal 425°C dan tekanan 1,2 atm dengan bantuan katalis Silica Alumina. Sebanyak 90% reaktan terkonversi membentuk produk.
Mekanisme reaksi pada reaktor sebagai berikut :
C2H4Cl2(g) + 2Cl2(g) C2Cl4 + 4HCl
Reaksi yang terjadi bersifat eksotermis sehingga dibutuhkan air sebagai pendingin untuk menyerap panas reaksi pembentukan produk. Produk gas keluaran reaktor yang terdiri dari perkloroetilen, hydrogen klorida, etilen diklorida dan klor sisa reaksi, selanjutnya dialirkan menuju Cooler untuk diturunkan temperaturnya sampai 125°C sebelum masuk kedalam Partial Condensor.
2.3 Tahap Pemurnian
Pada Partial Condensor komponen yang terkondensasi hanya komponen perkloroetilen, air, dan etilen diklorida. Sedangkan klor dan hidrogen klorida tetap dalam fase gas keluar Patrial Condensor. Campuran gas-cair keluaran Patrial Condensor selanjutnya dipisahkan pada Knockout Drum.
Produk atas Knockout Drum berupa gas klor dan hidrogen klorida selanjutnya dilewatkan pada Cooler untuk diturunkan temperaturnya sampai 40°C, sebelum diumpankan ke menara penyerap (absorber). Pada kolom absorber, gas hidrogen klorida diabsorbsi dengan menggunakan air untuk dipisahkan dari campuran gas klor sehingga menghasilakn produk samping larutan HCl dengan kemurnian sekitar 21%. Produk larutan HCl keluar Bottom absorber pada temperatur 30°C selanjutnya dialirkan dengan bantuan pompa ke tangki penampung larutan HCl.
Sedangkan produk atas kolom Absorber berupa gas klor sisa reaksi selanjutnya di Recycle dan dicampur dengan aliran gas klor umpan segar yang berasal dari tangki bahan baku gas klor.
Produk liquid knockout drum berupa campuran perkloroetilen, etilen diklorida dan air, selanjutnya dialirkan melewati cooler sebelum diumpankan ke kolom distilasi untuk dimurnikan. Produk atas kolom berupa larutan etilen diklorida dengan konsentrasi 99% pada temperatur 85°C selanjutnya dikembalikan ke tangki pencampuran sebelum diumpankan ke tangki reacktor.
Sedangkan produk bawah kolom berupa larutan perkloroetilen dengan kemurnian 99,3% pada temperatur 125°C dengan bantuan pompa dialirkan melewati cooler untuk diturunkan temperaturnya sampai 30°C sebelum ditampung pada tangki produk perkloroetilen.
F-102 P = 15 atm T=30°C
Q-101 P=1 atm T=98°C
H-101 P=1,2 atm T=125°C
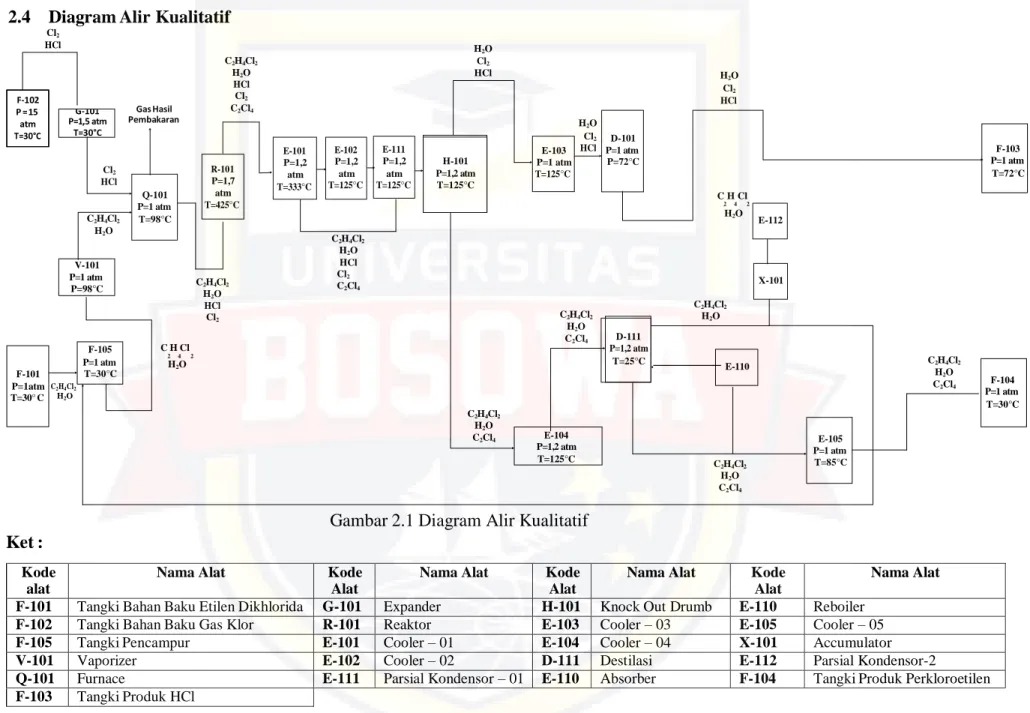
2.4 Diagram Alir Kualitatif
Cl2
HCl
C2H4Cl2
H2O HCl Cl2
H2O Cl2
HCl H2O
Cl2
HCl
C2H4Cl2
H2O Cl2
HCl
C2H4Cl2
H2O
F-105 P=1 atm
T=30°C
Gas Hasil Pembakaran
C H Cl
2 4 2
H2O C2H4Cl2
H2O HCl Cl2
C2Cl4
C2H4Cl2
H2O HCl Cl2
C2Cl4
C2H4Cl2
H2O C2Cl4
H2O Cl2
HCl
C2H4Cl2
H2O C2Cl4
D-101 P=1 atm
P=72°C
C H Cl
2 4 2
H2O
C2H4Cl2
H2O
E-110
C2H4Cl2
H2O C2Cl4
E-112
X-101
C2H4Cl2
H2O C2Cl4
Gambar 2.1 Diagram Alir Kualitatif Ket :
Kode alat
Nama Alat Kode
Alat
Nama Alat Kode Alat
Nama Alat Kode Alat
Nama Alat F-101 Tangki Bahan Baku Etilen Dikhlorida G-101 Expander H-101 Knock Out Drumb E-110 Reboiler
F-102 Tangki Bahan Baku Gas Klor R-101 Reaktor E-103 Cooler – 03 E-105 Cooler – 05 F-105 Tangki Pencampur E-101 Cooler – 01 E-104 Cooler – 04 X-101 Accumulator
V-101 Vaporizer E-102 Cooler – 02 D-111 Destilasi E-112 Parsial Kondensor-2
Q-101 Furnace E-111 Parsial Kondensor – 01 E-110 Absorber F-104 Tangki Produk Perkloroetilen F-103 Tangki Produk HCl
F-103 P=1 atm T=72°C E-102
P=1,2 atm T=125°C E-101
P=1,2 atm T=333°C
E-104 P=1,2 atm T=125°C
E-105 P=1 atm T=85°C
F-104 P=1 atm T=30°C D-111
P=1,2 atm T=25°C V-101
P=1 atm P=98°C
R-101 P=1,7 atm T=425°C
E-103 P=1 atm T=125°C E-111
P=1,2 atm T=125°C G-101
P=1,5 atm T=30°C
F-101 P=1atm T=30° C
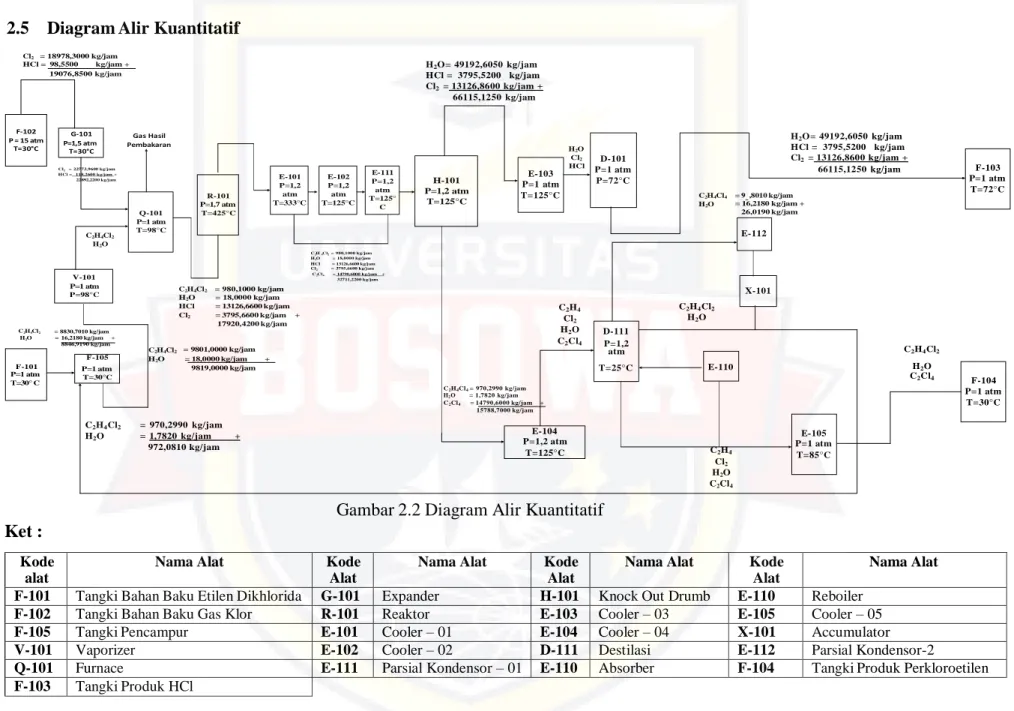
2.5 Diagram Alir Kuantitatif
Cl2 = 18978,3000 kg/jam
HCl = 98,5500 kg/jam + 19076,8500 kg/jam
H2O= 49192,6050 kg/jam HCl = 3795,5200 kg/jam Cl2 = 13126,8600 kg/jam +
66115,1250 kg/jam
F-102 P = 15 atm
T=30°C
G-101 P=1,5 atm
T=30°C
Cl2 = 22773,9600 kg/jam
HCl = 118,2600 kg/jam + 22892,2200 kg/jam
C2H4Cl2 H2O
Gas Hasil Pembakaran
Q-101 P=1 atm T=98°C
R-101 P=1,7 atm T=425°C
E-101 P=1,2 atm T=333°C
E-102 P=1,2 atm T=125°C
E-111 P=1,2 atm T=125°
C
H-101 P=1,2 atm
T=125°C
E-103 P=1 atm T=125°C
H2O Cl2 HCl D-101
P=1 atm P=72°C
C2H4Cl4 H2O
H2O= 49192,6050 kg/jam HCl = 3795,5200 kg/jam Cl2 = 13126,8600 kg/jam +
66115,1250 kg/jam
= 9 ,8010 kg/jam
= 16,2180 kg/jam + 26,0190 kg/jam
E-112
F-103 P=1 atm T=72°C
C2H4Cl2
V-101 P=1 atm P=98°C
= 8830,7010 kg/jam
C2H4Cl2 = 980,1000 kg/jam
H2O = 18,0000 kg/jam HCl = 13126,6600 kg/jam Cl2 = 3795,6600 kg/jam +
17920,4200 kg/jam
C2H 4Cl2 = 980,1000 kg/jam H2O = 18,0000 kg/jam HCl = 13126,6600 kg/jam
Cl2 = 3795,6600 kg/jam
C2Cl4 = 14790,6000 kg/jam +
32711,2200 kg/jam
C2H4
Cl2
H2O D-111
C2H4Cl2
H2O
X-101
H2O = 16,2180 kg/jam + 8846,9190 kg/jam
F-105
C2H4Cl2 = 9801,0000 kg/jam
H2O = 18,0000 kg/jam +
C2Cl4 P=1,2
atm C2H4Cl2
F-101 P=1 atm T=30° C
P=1 atm T=30°C
9819,0000 kg/jam
C2H4Cl4 = 970,2990 kg/jam H2O = 1,7820 kg/jam C2Cl4 = 14790,6000 kg/jam +
15788,7000 kg/jam
T=25°C E-110 H2O
C2Cl4 F-104 P=1 atm T=30°C
Ket :
C2H4Cl2 = 970,2990 kg/jam H2O = 1,7820 kg/jam +
972,0810 kg/jam
E-104 P=1,2 atm
T=125°C
Gambar 2.2 Diagram Alir Kuantitatif
C2H4
Cl2
H2O C2Cl4
E-105 P=1 atm T=85°C
Kode alat
Nama Alat Kode
Alat
Nama Alat Kode Alat
Nama Alat Kode Alat
Nama Alat F-101 Tangki Bahan Baku Etilen Dikhlorida G-101 Expander H-101 Knock Out Drumb E-110 Reboiler
F-102 Tangki Bahan Baku Gas Klor R-101 Reaktor E-103 Cooler – 03 E-105 Cooler – 05 F-105 Tangki Pencampur E-101 Cooler – 01 E-104 Cooler – 04 X-101 Accumulator
V-101 Vaporizer E-102 Cooler – 02 D-111 Destilasi E-112 Parsial Kondensor-2
Q-101 Furnace E-111 Parsial Kondensor – 01 E-110 Absorber F-104 Tangki Produk Perkloroetilen
BAB III. SPESIFIKASI BAHAN
3.1 Spesifikasi Bahan Baku
3.1.1 Etilen Diklorida (PT. Sucofindo Adi Usaha, Jawa Barat) Rumus molekul : C2H4Cl2
Berat molekul : 98,97 g/mol Titik didih : 83,47°C Titik leleh : -96,81°C Titik beku : -35,66°C Kondisi kritis : Tc = 290°C
Pc = 5360 kPa Densitas pada 20°C : 1,253 g/cm3
Bentuk : Cair
Toxicitas : Menyebabkan iritasi terhadap kulit dan mata serta menyebabkan kanker.
Warna : Tak berwarna
Pengotor : TCE 0,07%
Tekanan Uap :
T°C 0 20 30 50 70 80
P kPa 3,33 8,53 13 32 66,65 93,31
Panas pembentukan 25°C : -157,3 kJ/mol Panas spesifik (liquid pada 25°C) : 1,288 kJ/mol Panas penguapan 25°C : 343,7 kJ/mol
Viscositas 25°C : 0,00083
3.1.2 Klorin (PT. Asahimas, Jawa Barat)
Rumus molekul : Cl2
Berat molekul : 70,905 g/mol
Titik didih : -34,05°C
Titik leleh : -101,03°C Kondisi Kritis : Tc = 144°C
Pc =7,71083 kPa Densitas pada 20°C : 0,573 g/cm3
Bentuk : Gas
Toxitas : Menyebabkan iritasi pada kulit dan menyebabkan kanker
Warna : Hijau kekuningan
Entalpi peleburan : 90,33 kJ/kg Entalpi penguapan : 287,1 kJ/kg Densitas kritis : 565 kg/m3 Potensial elektroda standar : 1,359 V
Entalpi peruraian : 239,44 kJ/mol (2,481 eV) Entalpi Hidrasi Cl : 405,7 kJ/mol
3.2 Spesifikasi Bahan Bantu 3.2.1 Ferriclorida
Rumus molekul : FeCl3
Berat molekul : 162,2 g/mol
Titik lebur : 306°C
Titik didih : 315°C
Aroma : Sedikit berbau HCl
Warna : Hijau-hitam oleh pantulan cahaya, ungu-merah oleh transmisi cahaya
Densitas : 2,898 g/cm3
Kelarutan dalam air : 74,4 g/100ml (0°C) Viskositas : 40% larutan 12 cP
3.3 Spesifikasi Bahan Produk 3.3.1 Perkloroetilen
Rumus molekul : C2Cl4
Berat molekul : 165,8 g/mol
Titik didih : 121,2°C
Titik beku : -22,35°C
Kondisi Kritis : Tc = 347,3°C Pc = 9740 kPa Densitas pada 20°C : 1,478 g/cm3
Bentuk : Cair
Toxitas : Jika uap perkloroetilen terhisap melebihi 200 ppm akan
menyebabkan pusing, dan
terganggunya sistem pernapasan.
Konsentrasi diatas 1000 ppm akan menyebabkan kematian
Warna : Tak berwarna
Tekanan Uap :
T°C 0 20 40 60 80 100 120
P kPa 1 2 5 14 30 59 100
Panas pembentukan (liquid) : -51,1 kJ/mol Panas spesifik 20°C : 0,87 kJ/mol.K Panas penguapan 25°C : 34,7 kJ/mol Konduktivitas Panas : 0,13 W/k.m Viscositas 25°C : 0,00086
Mekanisme utama untuk memindahkan perkloroetilen dari udara yaitu dengan mereaksikannya dengan hidroksil radikal.
3.3.2 Hidrogen Klorida
Rumus molekul : HCl
Berat molekul : 36,461 g/mol
Titik didih : -85°C
Titik lebur : -114,4°C
Titik leleh : -62,2°C
Kondisi kritis : Tc = 51,6°C Pc = 8,3 Mpa Densitas kritis : 0,41 g/cm3 Densitas uap (-85°C) : 1,187 g/cm3 Entalpi peleburan : 54 J/g Entalpi penguapan : 0,443 kJ/g
BAB IV. NERACA MASSA
4.1 Neraca Massa Setiap Alat
Kapasitas Produksi : 99.000 ton/tahun
Satuan : kg/jam
Waktu Operasi : 330 hari/tahun Rate Produksi : 12.500 kg/jam
Berdasarkan perhitungan untuk basis 100 kgmol jam umpan C2H4Cl2 masuk reaktor didapat hasil akhir produk C2Cl4 = 14816,619 kg/jam (produk bawah distilasi,(D-111)).
Faktor Pengali : = 𝑅𝑎𝑡𝑒 𝑃𝑟𝑜𝑑𝑢𝑘𝑠𝑖 𝐵𝑒𝑟𝑎𝑡 𝑃𝑟𝑜𝑑𝑢𝑘
12.500 𝑘𝑔⁄𝑗𝑎𝑚
= 14816,619 kg/jam
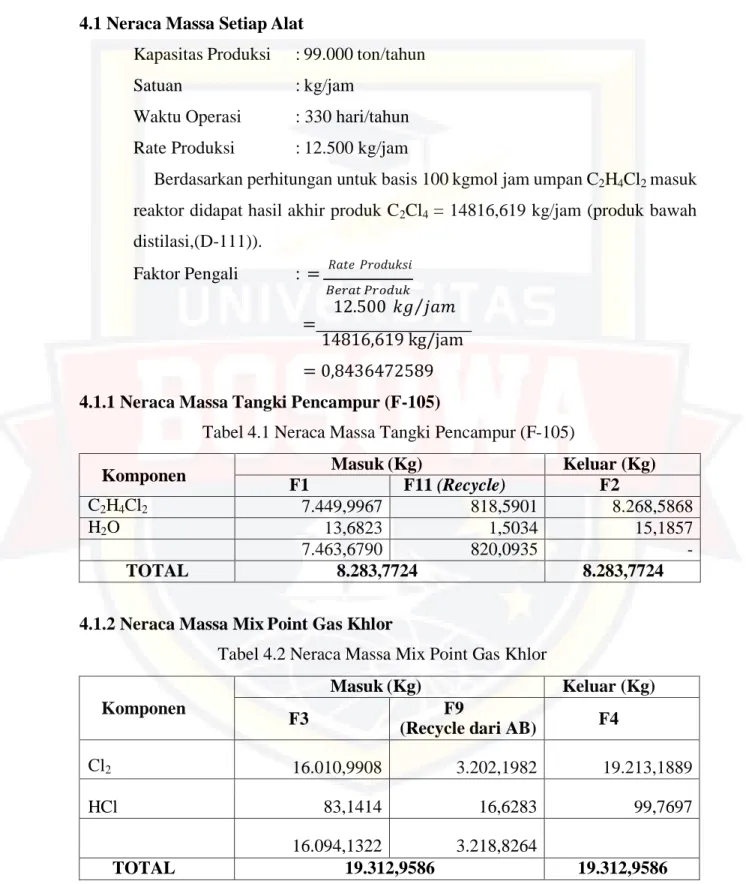
= 0,8436472589 4.1.1 Neraca Massa Tangki Pencampur (F-105)
Tabel 4.1 Neraca Massa Tangki Pencampur (F-105)
Komponen Masuk (Kg) Keluar (Kg)
F1 F11 (Recycle) F2
C2H4Cl2 7.449,9967 818,5901 8.268,5868
H2O 13,6823 1,5034 15,1857
7.463,6790 820,0935 -
TOTAL 8.283,7724 8.283,7724
4.1.2 Neraca Massa Mix Point Gas Khlor
Tabel 4.2 Neraca Massa Mix Point Gas Khlor Komponen
Masuk (Kg) Keluar (Kg)
F3 F9
(Recycle dari AB) F4
Cl2 16.010,9908 3.202,1982 19.213,1889
HCl 83,1414 16,6283 99,7697
16.094,1322 3.218,8264
TOTAL 19.312,9586 19.312,9586
4.1.3 Neraca Massa Reaktor (R-101)
Tabel 4.3 Neraca Massa Reaktor (R-101) Komponen BM
Kg/kgmol
Masuk Keluar
F2 F4 F5
Kgmol Kg/Jam Kgmol Kg
C2H4Cl2 99 8.268,5868 - 10,0394 826,8587
H2O 18 15,1857 - 1,0141 15,1857
HCl 36,5 - 99,7697 364,6986 11.074,4395
Cl2 71 - 19.213,1889 54,2128 3.202,1982
C2Cl4 166 - - 90,3546 12.478,0491
TOTAL 27.596,7311 - 27.596,7311
4.1.4 Neraca Massa Kondensor (E-111) dan Knockout Drum (H-101)
Tabel 4.4 Neraca Massa Kondensor (E-111) dan Knockout Drum (H-101) Komponen
Masuk (Kg) Keluar (Kg)
F5 F6
Gas (top KOD)
F10
Cair(bottom KOD)
C2H4Cl2 826,8587 - 826,8587
H2O 15,1857 - 15,1857
HCl 11.074,4395 11.074,4395 -
Cl2 3.202,1982 3.202,1982 -
C2Cl4 12.478,0491 - 12.478,0491
Total 27.596,7311 14.276,6376 13.320,0935 27.596,7311
4.1.4 Neraca Massa Absorber (D-101)
Tabel 4.5 Neraca Massa Absorber (D-101) Komponen
Masuk (Kg) Keluar (Kg)
F6 F7 F9 F8
Gas Liquid Gas Liquid
H2O - 41.501,2063 - 41.501,2063
HCl 11.074,4395 - 16,6283 11.057,8112
Cl2 3.202,1982 - 3.202,1982 -
TOTAL 14.276,6376 41.501,2063 3.218,8264 52.559,0175
55.777,8440 55.777,8440