BEBERAPA GENOTIPE UBI JALAR
(
Ipomea batatas
(L) Lam)
JANE K J LAISINA
SEKOLAH PASCASARJANA
INSTITUT PERTANIAN BOGOR
PERNYATAAN MENGENAI TESIS DAN
SUMBER INFORMASI
Dengan ini saya menyatakan bahwa tesis Pelestarian Secara In Vitro
Melalui Metode Pertumbuhan Minimal pada Beberapa Genotipe Ubi Jalar
(Ipomea batatas (L) Lam) adalah karya saya dengan arahan dari komisi
pembimbing dan belum diajukan dalam bentuk apapun kepada perguruan tinggi manapun. Sumber informasi yang berasal atau dikutip dari karya yang diterbitkan maupun tidak diterbitkan dari penulis lain telah disebutkan dalam teks dan dicantumkan dalam Daftar Pustaka di bagian akhir tesis ini.
Bogor, Februari 2009.
JANE K J LAISINA. 2009. Slow Growth Method of In Vitro Preservation of Several Sweet Potato Genotipe (Ipomea batatas (L) Lam). Supervised by ASEP SETIAWANandGUSTAAF ADOLF WATTIMENA.
The objectives of this research are (1) to achieve the suitable sweet potato preservation medium (Ipomea batatas (L) Lam) in order to make plant grow slowly and healthy; (2) to achive cheap and accessible medium ; (3) to estimate respons of some genotype in preservation medium through slow growth conservation. Three experiment were done in Molecular Biologi laboratory of PAU IPB. Experiment I and II were arranged in factorial complete random design, while experiment III was arranged in simple complete random design. Experiment I used sweet potato clone 421.34 in order to know the effect of coconut water (0,10,15,20%) and aspirin (0,10,20,30 mg/l) which added with 1 g/l Hyponex (20-20-20) and sucrose 40 g/l. Experiment II used sweet potato Sukuh in order to know the effect of sucrose (40,50,60,70,80 g/l) and agar (7 and 8 g/l) which added with Hyponex 1 g/l. Experiment III used one experiment factor that was sweet potato genotype (Sukuh, 421.34, 343.15, 2040.8). All of these genotype were tested in a conservation media which consist of 15% coconut water + 30 mg/l aspirin + 50 g/l sucrose + 7 g/l agar. Experiment I, II and III were replicated four times. Data were analyzed parametrically and non-parametrycally. The result of these experiment showed the suitable conservation media through slow growth i.e. 1 g/l Hyponex (20-20-20) + 20% coconut water + 20 mg/l aspirin + 60 g/l sucrose + 8 g/l agar. This media composition could produce high green internodes number, high root number and more than two green leaf number. Tested genotype showed different respons to preservation medium, where Sukuh produce the highest leaves number, while 421.34 produce the highest root and internodes number. This experiment also showed that MS media could be replaced by which is cheaper and easier conservation medium.
RINGKASAN
JANE K J LAISINA. 2009. Pelestarian Secara In Vitro Melalui Metode Pertumbuhan Minimal Pada Beberapa Genotipe Ubi Jalar (Ipomea batatas (L) Lam). Dibawah bimbingan ASEP SETIAWAN sebagai ketua dan GUSTAAF ADOLF WATTIMENAsebagai anggota.
Peningkatan produksi ubi jalar salah satunya adalah melalui penggunaan varietas unggul. Strategi pemuliaan untuk membentuk varietas ubi jalar yang unggul langkah awalnya adalah koleksi. Pemuliaan tanaman dapat dilakukan jika tersedia keragaman genotipe untuk berbagai tujuan pemuliaan. Genotipe-genotipe perlu dilestarikan baik secara konvensional maupun secara in vitro. Untuk itu koleksi menjadi sangat penting dalam pembentukan varietas. Koleksi plasma nutfah termasuk pelestarian plasma nutfah. Pelestarian plasma nutfah dapat dilakukan secara in vitro. Pelestarian plasma nutfah in vitro jangka pendek biasa disebut pertumbuhan lambat karena pertumbuhan planlet ditekan untuk sementara. Dalam pelestarian in vitro jangka pendek ini diharapkan tanaman pertumbuhannya lambat namun tidak mati.
Tujuan dari penelitian ini adalah menentukan taraf konsentrasi yang tepat dari komponen-komponen media (sukrosa, air kelapa, aspirin dan agar) yang ditambahkan dengan pupuk daun Hyponex 20-20-20 untuk pertumbuhan minimal, mendapatkan satu susunan komponen media yang tepat, murah dan mudah diperoleh dan mengetahui respon beberapa genotipe terhadap media pelestarian secara pertumbuhan minimal.
Penelitian dilaksanakan di Laboratorium Biologi Molekuler dan Seluler Tanaman, Pusat Antar Universitas (PAU) Bioteknologi, Institut Pertanian Bogor, Bogor. Percobaan yang berurut secara benar adalah percobaan penapisan, percobaan optimasi dan percobaan verifikasi. Namun karena waktu pengamatan yang agak lama maka percobaan optimasi (percobaan I dan II) dan percobaan verifikasi (percobaan III) dilakukan secara simultan. Percobaan I dan II menggunakan rancangan acak lengkap (RAL) pola faktorial dengan tiap percobaan terdiri dari dua faktor, sedangkan percobaan III menggunakan rancangan acak lengkap (RAL) faktor tunggal. Faktor percobaan I terdiri atas perlakuan aspirin dan air kelapa, percobaan II terdiri dari faktor sukrosa dan agar dan percobaan III genotipe Sukuh, 421.34, 2040.8 dan 343.15 diuji pada media pelestarian. Setiap unit percobaan dari ketiga percobaan diulang 4 kali. Respon tanaman yang diamati tiap 2 minggu adalah peubah kuantitatif dan kualitatif. Data hasil pengamatan peubah kuantitatif dianalisis menggunakan analisis sidik ragam dan uji lanjut Duncan pada taraf 5% untuk melihat kombinasi perlakuan yang terbaik bagi pertumbuhan tanaman. Pada peubah kualitatif menggunakan uji Kruskal Wallis.
kelapa 15% dan aspirin 20 mg/l menghasilkan jumlah akar tertinggi. Namun dari hasil uji beda Duncan kombinasi air kelapa 15% dan aspirin 20 mg/l menghasilkan jumlah akar yang berbeda tidak nyata dengan kombinasi air kelapa 20% dan aspirin 20 mg/l, sehingga kombinasi air kelapa 20% dan aspirin 20 mg/l diangap komposisi media yang tepat untuk pelestarian in vitro melalui pertumbuhan lambat. Pengaruh aspirin dalam media pelestarian ini adalah berhubungan dengan senesensdaun dan penghambatan pertumbuhan, dimana terdapat fakta yang membuktikan bahwa SA mengontrol pengaturan senesens
daun, yaitu tingkat endogenus SA dalam daun arabidopsis meningkat dengan meningkatnya senesens. Sitokinin memperlambat proses penghancuran klorofil daun dan memperlambat proses senesens daun. Dengan adanya sitokinin yang terkandung dalam air kelapa, planlet dapat mempertahankan daun. Dari hasil uji kualitatif terdapat perbedaan respon yang ditunjukkan oleh kombinasi air kelapa 20% dan aspirin 20 mg/l yang berantagonis dan memberi respon skor 6 yang berarti kombinasi air kelapa 20% dan aspirin 20 mg/l merupakan kombinasi yang membentuk planlet yang pertumbuhannya lambat tetapi sehat.
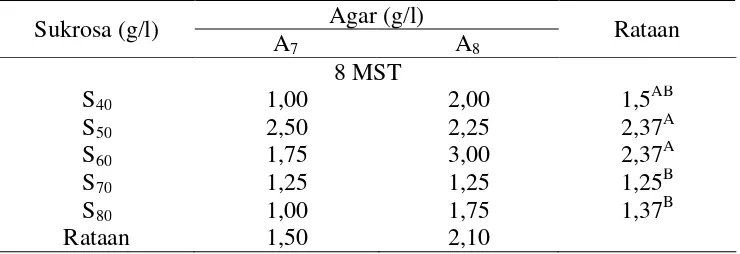
Hasil percobaan II menunjukkan bahwa komponen media yang tepat bagi media pelestarian ialah sukrosa 60 g/l sebagai sumber energi dan agar-agar 8 g/l sebagai bahan pemadat. Media dengan komposisi ini akan menghasilkan jumlah daun yang lebih dari 2 daun hijau, jumlah batang hijau dan akar yang tinggi.
Hasil percobaan III menunjukkan adanya perbedaan respon dari 4 genotipe yang dicobakan pada media pelestarian yang terdiri dari pupuk daun Hyponex (20-20-20) 1 g/l + air kelapa 15% + aspirin 30 mg/l + sukrosa 50 g/l + agar-agar 7 g/l. Genotipe Sukuh memberikan respon berupa jumlah daun tertinggi sedangkan genotipe 421.34 memberikan respon jumlah ruas dan akar tertinggi. Hal ini menyebabkan skor dari respon genotipe Sukuh lebih tinggi dari genotipe 421.34, karena skor berdasarkan daya hidup yaitu jumlah daun dan hijaunya ruas dan akar bukan terhadap jumlah daun, jumlah ruas dan jumlah akar.
Dari hasil percobaan I, II dan III dapat disimpulkan bahwa dengan meningkatkan taraf air kelapa menjadi 20%, sukrosa menjadi 60 g/l dan agar-agar menjadi 8 g/l sedangkan taraf aspirin diturunkan menjadi 20 mg/l, dengan Hyponex (20-20-20) l g/l maka dapat dipastikan genotipe Sukuh, 2040.8 dan 421.34 akan semakin baik responnya.
Hasil penelitian ini juga menunjukkan bahwa komponen media dasar MS dapat digantikan dengan pupuk daun Hyponex 20-20-20, dimana Hyponex 20-20-20 lebih murah 18 kali dari media dasar MS. Komponen media pelestarian dalam penelitian ini seperti Hyponex, air kelapa, aspirin, sukrosa dan agar-agar sangat mudah diperoleh dan mudah dikerjakan.
©Hak Cipta Milik IPB, tahun 2009
Hak Cipta dilindungi Undang-Undang
1. Dilarang mengutip sebagian atau seluruh karya tulis ini tanpa
mencantumkan atau menyebutkan sumbernya.
a. Pengutipan hanya untuk kepentingan pendidikan, penelitian, penulisan karya ilmiah, penyusunan laporan, penulisan kritik, atau tinjauan suatu masalah; dan
b. Pengutipan tersebut tidak merugikan kepentingan yang wajar IPB
2. Dilarang mengumumkan dan memperbanyak sebagian atau seluruh karya
PELESTARIAN SECARA
IN VITRO
MELALUI
METODE PERTUMBUHAN MINIMAL PADA
BEBERAPA GENOTIPE UBI JALAR
(
Ipomea batatas
(L) Lam)
JANE K J LAISINA
Tesis
sebagai salah satu syarat untuk memperoleh gelar Magister Sains pada
Program Studi Agronomi
SEKOLAH PASCASARJANA
INSTITUT PERTANIAN BOGOR
Judul Thesis : Pelestarian secara In Vitro melalui Metode Pertumbuhan Minimal pada Beberapa Genotipe Ubi Jalar (Ipomea batatas(L) Lam)
Nama : Jane K J Laisina
NRP : A151060111
Disetujui
Komisi Pembimbing
Dr. Ir. Asep Setiawan, MS Prof. Dr. Ir. G. A. Wattimena, MSc
Ketua Anggota
Diketahui
Ketua Program Studi Agronomi
Dekan Sekolah Pascasarjana
Dr. Ir. Munif Ghulamahdi, MS Prof. Dr. Ir. Khairil A. Notodipuro, MS
“Tuhan Membuat Segala Sesuatu
Indah Pada Waktunya”
PRAKATA
Puji dan syukur penulis panjatkan kepada Tuhan kita Yesus Kristus atas segala penyertaanNya sehingga karya ilmiah ini berhasil diselesaikan. Tema yang dipilih dalam penelitian yang dilaksanakan sejak bulan Maret 2008 adalah pelestarian in vitro, dengan judul Pelestarian secara In Vitro melalui Metode Pertumbuhan Minimal pada Beberapa Genotipe Ubi Jalar (Ipomea batatas(L) Lam).
Terima kasih penulis ucapakan kepada Bapak Dr. Ir. Asep Setiawan, MS dan Bapak Prof. Dr. Ir. G A Wattimena, MSc selaku pembimbing. Ucapan terima kasih disampaikan juga kepada pimpinan Fakultas Pertanian dan Universitas
Pattimura yang telah memberikan izin untuk melanjutkan studi S2 di IPB dan DIKTI yang telah memberikan beasiswa selama 4 semester, kepala PPSHB IPB
yang telah memberikan ijin penggunaan fasilitas laboratorium, juga kepada Mba Nia, Pak Asep dan Ara dari laboratorium PAU yang telah membantu dalam penelitian, Yayasan Dana Bantuan Maluku (YDBM) dan Pemerintah Daerah Propinsi Maluku yang telah memberikan bantuan dana penelitian.
Terima kasih penulis ucapkan kepada teman-teman Arie, tante Popi, Luki, Rajab dan Wahyu yang membantu dalam pengolahan data dan teman-teman PERMAMA yang membantu dalam doa. Ungkapan terima kasih juga penulis sampaikan kepada suami dan anak-anak yang telah banyak berkorban dan selalu mendukung dalam dalam doa dan juga kepada seluruh keluarga atas dukungan materi, kasih sayang dan doa.
Semoga karya ilmiah ini bermanfaat.
Bogor, Februari 2009
RIWAYAT HIDUP
Penulis dilahirkan di Bogor pada tanggal 1 Juni 1971 dari ayah Ir. Bram Victor Laisina, MS dan ibu Ir. Martha Latuihamallo. Penulis merupakan putri pertama dari dua bersaudara. Pada tahun 2000 penulis menikah dengan Barlev M Kesaulya, SPi dan dikaruniai dua orang putra Ralf Imanuel Kesaulya dan Raul Imanuel Kesaulya.
Tahun 1990 penulis lulus dari SMA Negeri I Ambon dan pada tahun 1993 masuk menjadi mahasiswa Universitas Pattimura pada Fakultas Pertanian Program Studi Agronomi dengan minat Pemuliaan Tanaman. Pada tahun 2002 penulis diterima menjadi dosen pada Fakultas Pertanian Universitas
DAFTAR ISI
Halaman
DAFTAR TABEL ……….. xiv
DAFTAR GAMBAR ……….. xvi
DAFTAR LAMPIRAN ……….. xvii
1. PENDAHULUAN ………. 1
1.1 Latar Belakang ………. 1
1.2 Tujuan ………. 3
1.3 Hipotesis ………. 3
1.4 Manfaat ……… 3
1.5 Ruang Lingkup ……… 4
2. TINJAUAN PUSTAKA ……….. 5
2.1 Kandungan Gizi Umbi dan Genetik Ubi Jalar ……… 5
2.2 Pelestarian Plasma Nutfah SecaraIn Vitro……….. 5
2.3 PelestarianIn VitroUbi Jalar melalui Pertumbuhan Lambat ……….. 7
2.3.1 Pupuk Daun Hyponex 20-20-20 ……… 9
2.3.2 Aspirin ……….. 10
2.3.3 Air Kelapa ………. 11
2.3.4 Sukrosa ……….. 12
2.3.5 Agar-Agar ……….. 14
3. METODOLOGI PENELITIAN ……….. 15
3.1 Tempat dan Waktu Penelitian ……… 15
3.2 Bahan Penelitian ……… 15
3.3 Metode Penelitian ………. 16
3.3.1 Percobaan I ……….. 16
3.3.2 Percobaan II ………. 17
3.3.3 Percobaan III ……… 18
3.4.1 Percobaan I ……….. 19
3.4.2 Percobaan II ………. 20
3.4.3 Percobaan III ……… 21
4. HASIL DAN PEMBAHASAN……… 22
4.1 Percobaan I ……… 22
4.1.1 Kondisi Umum ……… 22
4.1.2 Jumlah Daun ……… 23
4.1.3 Jumlah Akar ………. 27
4.1.4 Jumlah Ruas ………. 29
4.1.5 Uji Kualitatif ……… 31
4.1.6 Pembahasan ……… 34
4.2 Percobaan II ……….. 36
4.2.1 Kondisi Umum ……… 36
4.2.2 Jumlah Daun ……… 37
4.2.3 Jumlah Akar ………. 40
4.2.4 Jumlah Ruas ………. 41
4.2.5 Uji Kualitatif ……… 42
4.2.6 Pembahasan ………. 44
4.3 Percobaan III ……… 45
4.3.1 Kondisi Umum ……… 45
4.3.2 Jumlah Daun ……….. 46
4.3.3 Jumlah Akar ……… 47
4.3.4 Jumlah Ruas ……… 48
4.3.5 Uji Kualitatif ……….. 49
4.3.6 Pembahasan ………. 51
4.4 Pembahasan Umum ……….. 52
5. KESIMPULAN DAN SARAN ………. 58
5.1 Kesimpulan ………. 58
5.2 Saran ……… 58
DAFTAR PUSTAKA ………... 59
DAFTAR TABEL
Halaman
1. Rekapitulasi uji F pengaruh air kelapa dan aspirin terhadap peubah
daun, akar dan ruas selama 2 MST sampai dengan 24 MST ……… 22
2. Pengaruh perlakuan perlakuan air kelapa dan aspirin terhadap jumlah
daun selama 8 MST, 16 MST dan 24 MST ……….. 23 3. Persentase daun gugur untuk air kelapa dan aspirin pada 8 MST, 16 MST
dan 24 MST……… 24
4. Pengaruh perlakuan air kelapa dan aspirin terhadap jumlah akar pada
8 MST, 16 MST dan 24 MST………. 27
5. Pengaruh perlakuan air kelapa dan aspirin terhadap jumlah ruas pada
8 MST, 16 MST dan 24 MST………. 29
6. Pengaruh perlakuan air kelapa dan aspirin terhadap daya hidup pada
8 MST, 16 MST dan 24 MST ……… 32
7. Rekapitulasi uji F pengaruh agar dan sukrosa terhadap peubah daun, akar dan ruas selama 2 MST sampai dengan 24 MST……… 37 8. Pengaruh perlakuan agar dan sukrosa terhadap jumlah daun selama 8 MST,
16 MST dan 24 MST ………. 38
9. Persentase daun gugur untuk perlakuan agar dan sukrosa pada 8 MST,
16 MST dan 24 MST ……….. 39
10. Pengaruh perlakuan agar dan sukrosa terhadap jumlah akar pada 8 MST,
16 MST dan 24 MST ……….. 40
11. Pengaruh perlakuan agar dan sukrosa terhadap jumlah ruas pada 8 MST,
16 MST dan 24 MST ………. 41
12. Pengaruh perlakuan air kelapa dan aspirin terhadap daya hidup pada
8 MST, 16 MST dan 24 MST ……… 42
13. Rekapitulasi uji F pengaruh genotipe pada media pelestarian terhadap
peubah daun, akar dan ruas selama 2 MST sampai dengan 24 MST ……. 46 14. Pengaruh perlakuan genotipe pada media pelestarian terhadap jumlah daun
selama 2 MST sampai dengan 24 MST……….. 47 15. Persentase daun gugur untuk perlakuan genotipe pada media pelestarian
pada 2 MST sampai dengan 24 MST ... 47 16. Pengaruh genotipe pada media pelestarian terhadap jumlah akar pada
17. Pengaruh genotipe pada media pelestarian terhadap jumlah ruas pada
2 MST sampai dengan 24 MST ……….. 49
18. Pengaruh genotipe pada media pelestarian terhadap daya hidup pada
DAFTAR GAMBAR
Halaman 1. Ruang lingkup percobaan ……….. 4 2. Pemanfaatan kulturin vitrodalam koleksi plasma nutfah dan pertukaran
plasma nutfah ………. 7
3. Lintasan biosintesissalicylic acid ………. 11 4. Grafik interaksi air kelapa pada 4 taraf aspirin terhadap jumlah daun
pada 24 MST ………. 26
5. Grafik interaksi aspirin pada 4 taraf air kelapa terhadap jumlah daun
pada 24 MST ………. 26
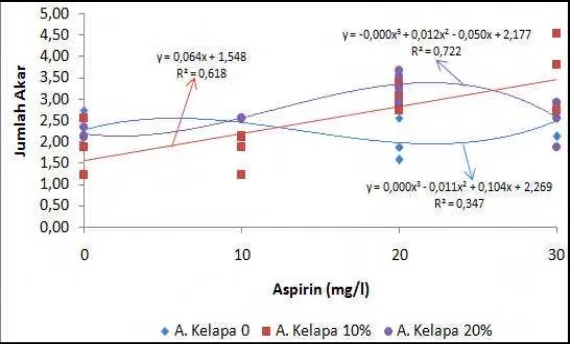
6. Grafik interaksi air kelapa pada 4 taraf aspirin terhadap jumlah akar
pada 24 MST ………. 28
7. Grafik interaksi aspirin pada 4 taraf air kelapa terhadap jumlah akar
pada 24 MST ………. 29
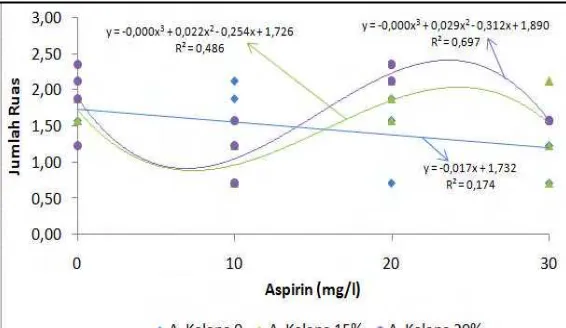
8. Grafik interaksi air kelapa pada 4 taraf aspirin terhadap jumlah ruas
pada 8 MST ………. 31
9. Grafik interaksi aspirin pada 4 taraf air kelapa terhadap jumlah ruas
pada 8 MST ……… 31
10.Planletpada kombinasi perlakuan air kelapa 20% dan aspirin 20 mg/l (K20A20) dan air kelapa 15% dan aspirin 20 mg/l (K15A20) yang berumur
24 minggu ………. 33
11.Planletdengan skor 3, skor 5 dan skor 6 setelah dipindahkan ke media
MS berumur 2 minggu ……….. 33
12.Planlet pada kombinasi perlakuan agar-agr 7 g//l dan sukrosa 60 g/l (A7S60) dan agar-agar 8 g/l dan sukrosa 60 g/l (A8S60) yang berumur
24 minggu ……….. 44
13.Planletdari kombinasi perlakuan agar-agar 7 g/l dan sukrosa 60 g/l (A7S60) dan kombinasi perlakuan agar-agar 8 g/l dan sukrosa 60 g/l
(A8S60) setelah dipindahkan ke media MS berumur 2 minggu ………. 44
14.Planletgenotipe Sukuh, 421.34, dan 2040.8 pada media pelestarian
berumur 24 minggu ……… 50
15.Planlet genotipe Sukuh, 421.34 dan 2040.8 setelah dipindahkan ke
DAFTAR LAMPIRAN
Halaman
1. Produksi ubi jalar menurut propinsi tahun 2003-2007……… 64 2. Jumlah daun gugur, jumlah ruas dan jumlah akar tanaman ubi jalar
pada media perbanyakan MS ……….…. 65 3. Tabel sidik ragam pengaruh air kelapa dan aspirin terhadap pertumbuhan
Daun ……….. 66
4. Tabel sidik ragam pengaruh air kelapa dan aspirin terhadap pertumbuhan
akar ………. 68
5. Tabel sidik ragam pengaruh air kelapa dan aspirin terhadap pertumbuhan
ruas ………. 70
6. Tabel sidik ragam pengaruh agar dan sukrosa terhadap pertumbuhan
daun ……… 72
7. Tabel sidik ragam pengaruh agar dan sukrosa terhadap pertumbuhan
akar ……….…..…. 74
8. Tabel sidik ragam pengaruh agar dan sukrosa terhadap pertumbuhan
ruas ………..………. 76
9. Persentase daun gugur untuk perlakuan air kelapa dan aspirin pada
2 MST sampai dengan 24 MST ………. 78 10. Persentase daun gugur untuk perlakuan agar dan sukrosa pada 2 MST
sampai dengan 24 MST ………. 80
11. Hasil uji beda Duncan dan polinomial orthogonal antara perlakuan air kelapa dan aspirin terhadap jumlah daun pada 2 MST sampai
dengan 24 MST ……….. 81
12. Hasil uji beda Duncan dan polinomial orthogonal antara perlakuan air kelapa dan aspirin terhadap jumlah akar pada 2 MST sampai
dengan 24 MST ……….….……… 84
13. Hasil uji beda Duncan dan polinomial orthogonal antara perlakuan air kelapa dan aspirin terhadap jumlah ruas pada 2 MST sampai
dengan 24 MST ……….………… 87
14. Pengaruh agar dan sukrosa terhadap jumlah daun pada 2 MST sampai
dengan 24 MST ……….. 90
15. Pengaruh agar dan sukrosa terhadap jumlah akar pada 2 MST sampai
dengan 24 MST ……….. 91
16. Pengaruh agar dan sukrosa terhadap jumlah ruas pada 2 MST sampai
17. Uji kualitatif terhadap pengaruh air kelapa dan aspirin dengan
menggunakan metode Kruskal Wallis……… 93 18. Uji kualitatif terhadap pengaruh agar dan sukrosa dengan
1.1 Latar Belakang
Ubi jalar telah banyak dimanfaatkan untuk berbagai keperluan seperti makanan, tujuan industri seperti bahan makanan, non makanan dan makanan ternak. Di Indonesia ubi jalar khususnya di beberapa daerah seperti Papua dan NTT dimanfaatkan sebagai makanan pokok. Ubi jalar juga memiliki kandungan gizi yang cukup baik. Menurut Hartana (2003) ubi jalar merupakan tanaman berenergi tinggi dan penghasil vitamin A dan C.
Perkembangan produksi ubi jalar di Indonesia sampai saat ini belum menggembirakan. Menurut Badan Pusat Statistik dan Direktorat Jenderal
Tanaman Pangan selama periode 2001-2008, produksi ubi jalar di Indonesia mengalami fluktuasi. Dari tahun 2001 sampai tahun 2003 terjadi peningkatan
produksi, kemudian terjadi penurunan produksi dari tahun 2004 sampai tahun 2006 dan selanjutnya terjadi peningkatan produksi pada tahun 2007 sampai tahun 2008 sebesar 1,03% (Lampiran 1). Produksi ubi jalar di Indonesia cenderung tetap karena permintaan untuk konsumsi sebagai makanan menurun tapi permintaan untuk tujuan industri dan makanan ternak meningkat (Jusuf dan Rahayuningsih, 2003).
Menurut data Badan Pusat Statistik perkembangan luas panen ubi jalar fluktuatif dan perkembangan produktivitas ubi jalar selama 30 tahun (1974-2003) meningkat dari 7,5 t/ha menjadi 10,1 t/ha, namun potensi produktivitas ubi jalar dapat mencapai 25-30 t/ha (Hafsah, 2004). Bila dibandingkan dengan negara lain seperti Israel 34,26 t/ha, Jepang 24,73 t/ha dan China 18,52 t/ha maka produktivitas ubi jalar di Indonesia lebih rendah (Nainggolan, 2003).
dilepas sebagai varietas ubi jalar kaya antosianin, yakni klon MSU 01022-12, MSU 03028-10 dan RIS 03063-05 dengan potensi hasil 20-25 ton/ha dan kadar bahan kering lebih dari 30% (Hasyim dan Jusuf, 2007).
Produktivitas ubi jalar di Indonesia yang lebih rendah dari potensi produktivitas ubi jalar, menyebabkan perlu pembentukan varietas unggul yang dapat meningkatkan produksi ubi jalar. Salah satu langkah strategis yang perlu dilakukan untuk mendukung pemuliaan ubi jalar adalah dengan memperkuat aspek pelestarian plasma nutfah. Strategi pemuliaan untuk membentuk varietas ubi jalar yang unggul langkah awalnya adalah koleksi, pelestarian, evaluasi dan penggunaan sumber keragaman. Koleksi plasma nutfah yang beragam merupakan aset utama bagi pemulia. Pemuliaan itu ada jika tersedia keragaman genotipe untuk berbagai tujuan pemuliaan. Sumber-sumber sifat penting seringkali hanya dimiliki oleh kultivar-kultivar lokal yang saat ini terancam punah dengan berkembangnya varietas-varietas ubi jalar unggul. Oleh karena itu upaya pelestarian plasma nutfah ubi jalar yang efisien perlu dikembangkan.
Pelestarian plasma nutfah dapat dilakukan secara konvensional maupun secarain vitro. Pelestarianin vitro merupakan salah satu teknologi alternatif yang dapat digunakan untuk melestarikan plasma nutfah ubi jalar secara lebih efisien mengingat genotipe ubi jalar hanya dapat dilestarikan secara vegetatif. Genotipe-genotipe perlu dilestarikan baik secara konvensional maupun secara
in vitro. Untuk itu koleksi menjadi sangat penting dalam pembentukan varietas.
Pelestarian plasma nutfah termasuk koleksi plasma nutfah. Salah satu topik penting dalam pelestarianin vitroadalah menciptakan metodein vitroyang efektif dan efisien yaitu metode yang dapat menekan pertumbuhan plantlet untuk waktu yang cukup lama dengan biaya relatif murah.
Untuk menekan biaya pelestarian dalam penelitian ini akan diuji pemanfaatan komposisi mediain vitroyang murah. Dari penelitian ini diharapkan menghasilkan metode penyimpanan plasma nutfah ubi jalar melalui pertumbuhan minimal dengan menggunakan media yang murah, mudah didapat dan efektif memperpanjang masa simpan.
1.2 Tujuan Penelitian
Tujuan dari penelitian ini adalah :
1. Menentukan taraf konsentrasi yang tepat dari komponen-komponen media (sukrosa, air kelapa, aspirin dan agar) untuk pertumbuhan minimal.
2. Mendapatkan satu susunan komponen media yang tepat, murah dan mudah diperoleh.
3. Mengetahui respon pertumbuhan lambat beberapa genotipe pada media pelestarian secara pertumbuhan minimal.
1.3 Hipotesis
Hipotesis yang diajukan dalam penelitian ini adalah
1. Terdapat satu konsentrasi tepat dari komponen-komponen media yang dapat membentuk tanaman dengan pertumbuhan minimal.
2. Terdapat respon yang berbeda dari genotipe-genotipe yang diuji pada media pelestarian secarain vitro.
1.4 Manfaat Hasil Penelitian
Hasil penelitian ini berupa satu susunan komponen media pelestarian yang
1.5 Ruang Lingkup Penelitian
Dalam penelitian ini terdapat tiga percobaan, dimana percobaan I dan percobaan II adalah percobaan optimasi dan percobaan III adalah percobaan verifikasi. Ketiga percobaan dilaksanakan bersamaan.
Pengujian Pada Media Kombinasi Air Kelapa (0, 10, 15, 20%) + Aspirin (0, 10, 20, 30 mg/l) + Sukrosa (40 g/l) +
Agar (7 g/l) + Hyponex (1 g/l)
Pengujian Pada Media Kombinasi Sukrosa (40, 50, 60, 70, 80 g/l) + Agar (7, 8 g/l) + Hyponex (1 g/l)
Pengujian 4 Genotipe Pada Media Kombinasi Air Kelapa (15%) + Aspirin (30 mg/l) + Sukrosa (50 g/l) +
Agar (7 g/l) + Hyponex (1 g/l)
PERCOBAAN I PERCOBAAN II PERCOBAAN III
PLANLET GENOTIPE 421.34
PLANLET GENOTIPE SUKUH
PLANLET GENOTIPE SUKUH,
421.34, 2040.8, 343.15
DATA RESPON PLASMA NUTFAH
2. TINJAUAN PUSTAKA
2.1 Kandungan Gizi Umbi dan Genetik Ubi jalar
Umbi merupakan produk utama ubi jalar, dimana peran ubi jalar tidak terbatas untuk bahan pangan tetapi berkembang menjadi produk industri yang memiliki nilai tambah yang tinggi. Sebagai bahan pangan ubi jalar memiliki kandungan karbohidrat yang baik, selain itu karbohidrat yang dikandung ubi jalar masuk dalam klasifikasi Low Glycemix Index (LGI, 54), artinya komoditi ini sangat cocok untuk penderita diabetes (Salma, 2005). Ubi jalar juga sebagai sumber serat pangan yang dapat menyerap kolesterol dan sumber β karoten yang baik untuk kesehatan mata. Menurut Sarwono (2005) kelebihan ubi jalar
berdaging jingga yaitu merupakan sumber vitamin C dan β karoten (pro vitamin A) yang tinggi, sedangkan ubi jalar berdaging putih mengandung
vitamin C danβkaroten sangat rendah.
Ubi jalar (Ipomea batatas (L) Lam) merupakan tanaman polipolid yang mempunyai kromosom 2n = 6X = 90. Menurut Basuki (1986) ubi jalar merupakan amphiploid yang diduga berasal dari kombinasi spesies diploid dengan spesies tetraploid dari genus Ipomea dan kemudian diikuti duplikasi kromosom secara alamiah. Nishiyama (1982) yang meneliti jumlah kromosom dan mengadakan analisis genom Ipomea menentukan satu kelompok yang terdiri dari Ipomea batatas(2n = 6X = 90),Ipomea trifida(2n = 6X = 90),Ipomea littorallis(2n = 4X = 60) dan Ipomea leucantha(2n = 2X = 30), spesies-spesies tersebut nampaknya merupakan seri diploid ke heksaploid. Tetua yang asli adalah I.leucantha dan
I.batatasmerupakan duplikasi secara alami dari I.leucantha(2X) menjadiI.trifida
(6X) dan kemudian membentuk I.batatas(6X) atau dari I.leucantha(2X) dengan
I.littorallis(4X) menjadiI.trifida(6X) dan kemudian menjadiI.batatas(6X).
2.2 Pelestarian Plasma Nutfah secara In Vitro
ubi jalar. Ubi jalar diperbanyak secara vegetatif sehingga pengaturan koleksi plasma nutfah lebih sulit dibandingkan dengan tanaman lain yang diperbanyak dengan biji, untuk itu sebagian besar pemulia melestarikan genotipe ubi jalar secarain vitro(Wattimenaet al, 2003).
Pelestarian plasma nutfah melalui penyimpanan in vitro terbagi atas 1) penyimpanan jangka panjang dimana aktivitas metabolisme dihentikan tetapi sel-sel tidak mati dengan menggunakan nitrogen cair (N2) dalam suhu yang sangat
rendah, teknik ini dikenal dengan istilah kriopreservasi. 2) Penyimpanan jangka pendek yaitu dengan menekan pertumbuhan untuk sementara atau biasa disebut pertumbuhan minimal menggunakan suhu rendah, penambahan zat penghambat, penambahan gula alkohol dan pemiskinan media (Imelda dan Soetisna, 1992). Pertumbuhan minimal lebih disukai pemulia karena mudah, materi mudah tersedia dan genetik plasma nutfah stabil. Kerugian dari teknik pertumbuhan minimal adalah membutuhkan frekuensi subkultur yang lebih sering (Wattimenaet al, 2003).
Menurut Roostika dan Mariska (2003), plasma nutfah yang disimpan dengan kriopreservasi berstatus sebagai base collection (koleksi dasar) dalam bank gen in vitro, sedangkan yang disimpan dengan teknik pertumbuhan minimal berstatus sebagaiactive collection(koleksi aktif) dan koleksi tanaman di lapangan merupakanworking collection(koleksi kerja) (Gambar 1).
Pelestarian plasma nutfah melalui penyimpanan secarain vitromempunyai
Gambar 2. Pemanfaatan kultur in vitro dalam koleksi plasma nutfah dan pertukaran plasma nutfah ( Karta, 1985).
2.3 Pelestarian In Vitro Ubi Jalar melalui Pertumbuhan Minimal
Pelestarian ubi jalar secarain vitro jangka pendek sering dilakukan dengan menekan pertumbuhan atau sering disebut pertumbuhan minimal. Pelestarian melalui pertumbuhan minimal salah satunya dengan menambahkan zat penghambat atau senyawa retardan seperti paclobutrazol, cycocel, ancymidol dan asam absisat (Withers, 1985; Tambunan dan Sunarlim, 2001). Penelitian yang
dilakukan Munantyorini et al (2000), menyatakan bahwa konsentrasi
paclobutrazol yang baik yaitu pada konsentrasi 30 mg/l. Hal in diperkuat oleh
penelitian Tambunan dan Sunarlim (2001) yang menyimpulkan penyimpanan in vitro ubi jalar dengan menggunakan zat penghambat paclobutrazol lebih efisien dan efektif memperpanjang masa penyimpanan daripada menggunakan zat penghambatancymidol, dimana konsentrasipaclobutrazol yang dicobakan terbaik adalah 30 mg/l, sedangkan pada penyimpanan tanaman pule (Rauvolvia serpentina), ancymidol1 mg/l lebih baik dari paclobutrazol(Purnamaningsih dan Lestari,1997; Lestari dan Purnamaningsih, 2005). Pada tanaman obat pulasari
(Alyxia stelata) paclobutrazol 5 mg/I dapat menghambat pertumbuhan sampai
Koleksi lapang
PUSAT PLASMA NUTFAH
Bank genin vitro
Mikropropagasi iro
Koleksi dasar (kriopreservasi) Koleksi aktif
(pertumbuhan minimal)
PERTUKARAN PLASMA NUTFAH
minggu ke 12 (Lestari et a1,1994; Lestari dan Purnamaningsih, 2005),
konsentrasi paclobutrazol 5 mg/l juga dapat menekan pertumbuhan tanaman
obat temu lawak (Curcuma xanthoriza) dalam media pelestarian (Syahid, 2007).
Selain paclobutrazol danancymidol dapat juga digunakan ABA (Asam Absisik)
sebagai penghambat pertumbuhan. Penggunaan ABA dalam media penyimpanan pada tanaman obat sambang colok (Aerva sanguinolenta) diperoleh media yang terbaik adalah MS + ABA I mg/I (Amalia et al, 2004), sedangkan media penyimpanan terbaik untuk tanaman obat daun dewa (Gynura procumbens) adalah media MS ½ + ABA 5 mg/l (Lestari dan Purnamaningsih, 2005).
Penyimpanan dengan menekan pertumbuhan dapat juga dilakukan dengan menggunakan senyawa stabilisator osmotik yaitu untuk meningkatkan osmolaritas media sehingga penyerapan nutrisi ke dalam jaringan menjadi terhambat (Tambunan dan Sunarlim, 2001). Senyawa yang dapat digunakan sebagai stabilisator osmotik antara lainmanitol (Withers, 1985; Tambunan dan Sunarlim,
2001) atau sukrosa (Bessembinder, 1993; Sunarlimet al, 1999). Dalampenelitian Sunarlim (1999), diperoleh beberapa varietas ubi jalar yang cocok disimpan menggunakan media MS + manitol 40 g/l dan juga diperoleh beberapa varietas tidak cocok menggunakan media ini. Untuk tanaman inggu media penyimpanan
menggunakan ABA 4 mg/l dan manitol 500-1500 mg/1 dapat menekan
pertumbuhan tunas sampai dengan. 6 bulan (Bermawie dan Kristina, 2003). Pelestarian ubi jalar selain menggunakan senyawa retardan dan osmotikum, dapat
juga menggunakan senyawa penghambat lain. Dalam penelitian awal oleh Wattimena (2005), penyimpanan ubi jalar melalui pertumbuhan lambat
dicapai melalui kombinasi dari pengaruh air kelapa dan asipirin, dimana air kelapa bersifat sebagai pendorong dari aspirin sebagai penghambat.
Penyimpanan ubi jalar secara in vitro dapat juga melalui pemiskinan media dasar MS. Pemiskinan media dasar MS berarti pengurangan hara dalam media in vitro, hal ini disebabkan media MS, merupakan media yang mengandung hara makro maupun mikro yang dibutuhkan oleh jaringan tanaman. Seperti dalam penyimpanan tanaman obat daun dewa, media ½ MS merupakan media
terbaik untuk penyimpananin vitro(Lestari dan Purnamaningsih, 2005), sedangkan
(Seswita et al, 2003). Namun media MS dapat digantikan oleh pupuk damn
hyponex 20-20-20 yang dapat menghasilkan unsur hara makro dan mikro,
dimana vitamin dalam media MS dapat digantikan oleh vitamin yang berasal dari
air kelapa.
Penggunaan sukrosa dalam penyimpanan in vitro yaitu karena sukrosa
merupakan karbohidrat yang dibutuhkan tanaman sebagai sumber energi, selain
itu sukrosa juga dapat bersifat sebagai stabilisator osmotik media (Winata, 1992).
Penggunaan media dasar lain dalam penyimpanan in vitro ubi jalar dilakukan oleh
Tambunan (2001) dengan menggunakan media dasar KH (Knop dan Heller) +
sukrosa 5 g/l dan 10 g/l + poclobutrazol 30 mg/1 menghasilkan masa
penyimpanan yang lebih panjang dan persentasi hidup yang lebih tinggi.
2.3.1 Pupuk Daun Hyponex (20-20-20)
Pupuk daun Hyponex (20-20-20) berbentuk bubuk dibuat dengan formula
khas sehingga dapat memupuk semua jenis tanaman. Pupuk daun Hyponex
(20-20-20) mengandung 4% nitrogen nitrat, 4% nitrogen ammonium, 12%
nitrogen yang larut dalam air, N 20% P20520%, K2O 20% dilengkapi dengan B,
Ca, Co, Fe, Mg, Mn, Mo, S, dan Zn. Bila dibandingkan dengan media MS,
kandungan nitrogen dalam 1 liter Hyponex (20-20-20) lebih rendah
dari kandungan nitrogen dalam 1 liter MS karena di dalam 1 liter Hyponex
(20-20-20) terdapat 200 mg/l N, sedangkan dalam 1 liter MS terdapat 821,5 mg/l
N (Muawanah, 2005). Dalam penelitian yang dilakukan Nadapdap (2000), media
MS dapat disubsitusi dengan pupuk Hyponex (20-20-20) dengan konsentrasi 1,5
g/l. Pada perbanyakan in vitro kentang, dimana Hyponex (20-20-20) hanya
mensubtitusi unsur hara makro dan mikro, sedangkan vitamin dan zat pengatur
tumbuh disubtitusi oleh air kelapa dengan konsentrasi 30%. Dalam penelitian
Muawanah (2005), Hyponex (20-20-20) 1 g/l dan ekstrak pisang 100 g/l
menghasilkan jumlah daun tertinggi dari tanaman anggrek, sedangkan Hyponex
(20-20-20) 1 g/l dan ekstrak tomat 100 g/l menghasilkan panjang akar dan jumlah
akar tertinggi dari tanaman anggrek. Penggunaan Hyponex (20-20-20) yang
ditambahkan ekstrak kentang pada perkecambahan in vitro biji anggrek Vanda
parishii dan Vanda denisoniana menghasilkan perkecambahan yang tinggi
2.3.2 Aspirin
Saat ini Salicylic Acid (SA) dikenali sebagai hormon tanaman, dalam
tanaman diinduksi oleh hipersensitif (Wattimena, 2005). SA selama ini dikenal
sebagai molekul signal transduksi dalam pertahanan tanaman terhadap penyakit.
Pengaruh SA dalam senesens daun selama ini tidak diketahui, namun menurut
Gan (2004) terdapat fakta yang membuktikan bahwa SA mengontrol pengaturan
senesens daun, yaitu tingkat endogenus SA dalam daun Arabidopsis meningkat
dengan meningkatnyasenesens.
Pada tahun 1898 perusahaan bayer di Jerman membuat senyawa sintetik
pertama yaitu Acetil Salicylic Acid (ASA) dan nama dagangnya adalah aspirin
yang dikenal sebagai sebagai obat sakit kepala. ASA dalam air akan terhidrolisis menjadi salicylic acid (SA). SA berbeda dengan retardan, menurut Wattimena
et al (2003) retardan adalah senyawa yang secara fisiologis memperpendek ruas eksplan dan menaikkan kandungan klorofil, sedangkan SA secara fisiologis memperpanjang durasi inisiasi daun. SA juga dapat memperpanjang katahanan umur bunga potong karena berfungsi sebagai penghambat biosintesis etilen
(Leslie dan Romani, 1988).
Di dalam tanaman tembakau didapati salicylic acid diproduksi dari
lintasan shikimic acid. Lintasan shikimic acid merupakan awal dari beberapa
lintasan senyawa aromatik termasuk senyawa asam amino aromatik esensial. Satu
cabang dari chorismate menghasilkan phenylalanine yang merupakan substrat
untuk enzim phenylalanine ammonia lyase (PAL) merubah menjadi trans
cinnamic acid yang dapat membentuk dua senyawa yang dilibatkan dalam
sintesis SA, kedua senyawa tersebut adalahortho coumeric aciddanbenzoic acid.
Kemudian senyawa benzoic acid dihidroksilasi menjadi SA oleh enzim benzoic
acid 2 hydroxylase (BA2H), dimana enzim ini diinduksi oleh serangan virus. SA
dari senyawaortho coumeric aciddi dalam tanaman tembakau tidak dihidroksilasi
oleh enzim BA2H. Lintasan lain dari chorismate yang dikatalis oleh enzim
sintase isochorismate(ICS) menghasilkanisochorismic acid, selanjutnya senyawa
ini dikatalis oleh enzim isochorismate pyruvate lyase menjadi SA. Di dalam
mikroorganisme lintasan ini menggambarkan sintesis SA, namun studi genetik
dari Arabidopsis menunjukkan lintasan ini juga berfungsi dalam tanaman
IP
L
P
A
L
Gambar 3. Lintasan biosintesissalicylic acid(Delaney, 2004)
2.3.3 Air Kelapa
Selain golongan persenyawaan organik yang konstitusinya jelas,
kadang- kadang dalam media kultur jaringan juga ditambahkan persenyawaan
organik kompleks, salah satunya adalah air kelapa. Air kelapa dalam kultur
jaringan sebagai pemicu pertumbuhan kalus, pertumbuhan suspensi sel dan
morfogenesis (Winata, 1992).
Bahan-bahan yang terkandung dalam air kelapa antara lain asam amino,
asam-asam organik, asam nukleat, purin, gula, gula alkohol, vitamin, zat pengatur
tumbuh (Winata,1992). Komposisi air kelapa merupakan sumber alami darizeatin
(Trigiano dan Gray, 2004). Air kelapa mempunyai aktivitas sitokinin yang tinggi
dengan kehadiran dari zeatin, zeatin glukosida, ribosida dan 1,3 difenil urea
(Wattimena et al, 2003). Sitokinin memperlambat proses penghancuran
butir-butir klorofil pada daun-daun yang terlepas pada tanaman dan
memperlambat proses senesens pada daun, buah dan organ-organ lainnya
Selain itu air kelapa juga mengandung IAA (Mandang, 1993) dimana
pengaruh fisiologis dari auksin antara lain pembesaran sel, mencegah absisi
(pengguguran daun), pertumbuhan akar yaitu mendorong pembesaran sel-sel akar,
dimaan selang konsentrasi yang mendorong pembesaran sel-sel akar adalah sangat
rendah (Wattimena, 1988).
Dalam penelitian Wattimena (1992), air kelapa digunakan untuk
menginduksi umbi kentang secara in vitro dimana air kelapa digunakan sebagai
penghasil sitokinin untuk mensubtitusi sitokinin komersial seperti zeatin, benzyl
adeninedan kinetin. Dalam media in vitro, subtitusi media MS dengan air kelapa
dapat menghemat penggunaan media MS sampai 50% dan menghemat sukrosa
10 g/l, selain itu semakin besar konsentrasi air kelapa pengaruh perubahan pH
media semakin kecil (Mandang, 1993). Hal ini disebabkan oleh kandungan asam
organic yang dijumpai pada air kelapa berfungsi sebagai buffer terhadap
perubahan pH (Wattimena, 1990).
Gula dalam air kelapa merupakan sumber karbohidrat yang meliputi
sukrosa, glukosa, fruktosa dan manitol (George dan Sherington, 1984). Gula
dalam proses respirasi dirombak sehingga menghasilkan suatu ikatan kimia
berenergi tinggi yaitu ATP yang digunakan dalam berbagai proses seperti sintesis,
transport, penyerapan dan lain-lain. Selain itu gula juga berpengaruh terhadap
pertumbuhan kultur melalui pengaruhnya terhadap potensial osmotik media.
Potensial osmotik berpengaruh nyata pada sifat-sifat membran, baik terhadap
pengaturan keseimbangan ion dalam sel juga pada sifat-sifat protein membran
(Mandang, 1993). Gula alkohol yang terkandung dalam air kelapa (inositol) dalam
jumlah 100 mg/l dapat memperbaiki pertumbuhan tanaman in vitro
(Wattimena, 1990). Manitol merupakan senyawa stabilisator osmotik yang dapat
meningkatkan osmolaritas media, sehingga penyerapan nutrisi ke dalam jaringan
terhambat (Tambunan, 2001).
Dalam kultur jaringan air kelapa digunakan dalam media perbanyakan
in vitro, yaitu dengan penambahan air kelapa 10%, IBA 0,5 ppm dan 1,5 ppm
merupakan konsentrasi terbaik untuk percepatan tunas, jumlah tunas dan jumlah
daun tebu (Farid, 2003). Dalam media seleksi aluminium, media induksi kalus
embriogenik yang ditambahkan dengan 150 ml air kelapa, 3% manitol dan Al Cl3
400 M membentuk kalus embrionik dengan presentasi tertinggi (Sutjahjo, 2006).
Dalam media induksi embryogenesis somatic dari eksplan embriozigotik buah
2.3.4 Sukrosa
Di dalam kultur jaringan eksplan atau planlet tidak berfotosintesis
sehingga bahan fotosintesis diberikan berupa sukrosa. Dengan demikian banyak
bahan organik yang perlu ditambahkan ke dalam media untuk mendukung
pertumbuhan yang optimal. Karbohidrat terutama gula merupakan komponen
yang selalu ada dalam media tumbuh, kecuali dalam media untuk tujuan khusus.
Gula merupakan bagian terpenting dari medium. Sebagian besar kultur tanaman
tidak dapat berfotosintesis secara efektif karena ketidakmampuan dalam
pengembangan sel dan jaringan, kekurangan klorofil, pertukaran CO2 yang
terbatas dalam jaringan dan cahaya yang lebih rendah dibandingkan dengan
keadaan optimum (Robert dan Dennis, 2004), sehingga dalam media perlu
ditambahkan gula sebagai penghasil energi. Gula bukan saja sebagai penghasil
energi tetapi juga untuk pembentukan metabolit sekunder yang penting dalam
pertumbuhan dan perkembangan tanaman. Selain itu menurut George and
Sherington (1984) pengaruh nitrat dan ammonium tergantung konsentrasi sukrosa
dan pengaruh pengaruh sitokinin dalam pembelahan sel juga tergantung dari
ketersediaan gula.
Sukrosa merupakan gula yang sering digunakan sebagai penghasil energi
dalam media kultur jaringan. Konsentrasi sukrosa 20-60 g/l (disakarida yang
dibuat dari glukosa dan fruktosa) adalah sebagian besar digunakan sebagai
penghasil energi karena gula ini ditransport dan disintesis secara alami dalam
tanaman (Trigiano dan Gray, 2004). Sukrosa dalam media dihidrolisis menjadi
monosakarida selama masa kultur, hidrolisa terjadi karena aktivitas enzim
invertase yang terdapat dalam dinding sel dan paling efektif pada pH rendah
(Winata, 1992). Sukrosa adalah yang paling baik lalu glukosa, maltosa dan
rafinosa. Fruktosa dan galaktosa kurang efektif, sedangkan laktosa dan manosa
adalah karbohidrat yang paling tidak efektif. Konsentrasi gula tergantung tipe dan
umur eksplan dalam kultur (Trigiano dan Gray, 2004).
Selain sebagai penghasil energi, gula juga berfungsi sebagai penghasil
tekanan osmotik media. Kontribusi nutrisi garam berkisar antara 20-50 % untuk
potensi osmotikum media dan sukrosa memberi kontribusi sisanya. Kontribusi
sukrosa untuk meningkatkan tekanan osmotik yaitu sukrosa dihidrolisis ke dalam
glukosa dan fruktosa selama outoklaf (Trigiano dan Gray, 2004). Menurut George
dan Sherington (1984), sukrosa memberikan pengaruh yang besar terhadap
potensial asmotik media, pada media White 4/5 bagian dari potensial osmotik
disebabkan oleh sukrosa sedangkan media MS hanya 2/5 bagian dari potensial
Dalam penyimpanan in vitro ubi jalar dengan perlakuan retardan, sukrosa
yang ditambahkan sebesar 5 atau 10 g/l (Sunarlim, 2001), sedangkan
penyimpanan ubi jalar dengan perlakuan kombinasi aspirin dan air kelapa,
konsentrasi sukrosa yang digunakan adalah 30 g/l (Wattimena et al, 2003).
Konsentrasi sukrosa 30 g/l juga ditemui pada penyimpanan in vitro panili
(Seswita et al, 2003), penyimpanan in vitro daun dewa (Lestari dan
Purnamaningsih, 2005) dan penyimpananin vitrotemu lawak (Syahid, 2007).
2.3.5 Agar-Agar
Agar-agar adalah pemadat yang paling banyak digunakan. Agar-agar adalah
campuran polisakarida yang diperoleh dari beberapa spesies algae. Dalam analisa
unsur agar-agar mengandung sedikit Ca, Mg, K dan Na. Keuntungan dari
memakai agar-agar adalah agar-agar membeku pada suhu 45οC dan mencair pada
suhu 100οC sehingga dalam kisaran suhu kultur agar-agar dalam keadaan beku
yang stabil, agar tidak dicerna oleh enzim tanaman dan agar-agar tidak bereaksi
dengan persenyawaan-persenyawaan penyusun media (Winata, 1992).
Kekerasan media meningkat secara linier pada pertambahan konsentrasi
agar. Konsentrasi agar-agar yang terlalu tinggi dapat mengurangi difusi
persenyawaan dari dan ke arah eksplan, sehingga pengambilan hara dan zat
tumbuh berkurang sedangkan zat penghambat dari eksplan tetap berkumpul di
sekitar eksplan (Winata, 1992). Kekerasan media tergantung jenis agar-agar dan
menurut keasaman media, pH rendah umumnya digunakan dalam kultur jaringan
tanaman. Pertumbuhan kalus atau organ tanaman pada media agar-agar secara
umun kecepatannya lebih berkurang dibandingkan dengan media cair namun
pertumbuhannya akan diperbaiki jika ditambahkan nutrisi (George and
Sherington, 1984).
Potensial air pada media agar-agar lebih rendah dari media cair, hal ini
diindikasikan dari meningkatnya kandungan prolin eksplan jika konsentrasi
agar-agar ditingkatkan dimana diketahui bahwa kandungan prolin meningkat jika
tanaman dalam keadaan stress air (George and Sherington,1984).
Dalam penyimpanan in vitro konsentrasi agar-agar yang sering digunakan
adalah sebesar 8 g/l, misalnya pada tanaman ubi jalar (Tambunan dan
Sunarlim, 2001), pada tanaman panili (Seswita et al, 2003) dan pada tanaman
3. METODOLOGI PENELITIAN
3.1 Tempat dan Waktu Penelitian
Penelitian dilaksanakan di Laboratorium Biologi Molekuler dan Seluler Tanaman, Pusat Antar Universitas (PAU) Bioteknologi, Institut Pertanian Bogor, Bogor. Penelitian I dan III dilaksanakan awal bulan Maret 2008 sampai akhir bulan Agustus 2008, sedangkan penelitian II dilaksanakan awal bulan April 2008 sampai akhir bulan September 2008.
3.2 Bahan Penelitian
Bahan tanaman yang digunakan adalah ubi jalar yang berasal dari kultur
in vitro koleksi Laboratorium Biologi Molekuler dan Seluler Tanaman PAU.
Bahan tanaman yang ditanam pada media perlakuan adalah planlet yang telah memiliki 1-2 daun dan memiliki akar ataupun tidak memiliki akar. Tanaman
diperbanyak dengan menggunakan media dasar Murashige dan Skoog (media MS), bahan pemadat agar-agar dan gula sukrosa.
Komposisi bahan untuk media perlakuan pada percobaan I adalah kombinasi zat pengatur tumbuh yaitu aspirin dan air kelapa, dan sebagai sumberl unsur hara makro dan mikro digunakan pupuk daun Hyponex (20-20-20) 1 g/l. Pemadat media adalah agar dan sebagai penghasil energi digunakan sukrosa. Pada percobaan I ini hanya digunakan klon 421.34.
Komposisi bahan untuk perlakuan pada percobaan II adalah kombinasi pemadat agar dan penghasil energi sukrosa, ditambahkan Hyponex (20-20-20) 1 g/l. Pada percobaan II hanya digunakan varietas Sukuh.
Komposisi bahan untuk media pelestarian pada percobaan III yaitu Hyponex (20-20-20) + sukrosa + air kelapa + aspirin + agar. Komposisi media tersebut selanjutnya diuji pada 4 genotipe ubi jalar yaitu genotipe Sukuh, 343.15, 421.34 dan 2040.8.
3.3 Metode Penelitian
yang agak lama maka percobaan optimasi (percobaan I dan II) dan percobaan verifikasi (percobaan III) dilakukan secara simultan.
Percobaan I dan II menggunakan rancangan acak lengkap (RAL) pola faktorial dengan tiap percobaan terdiri dari dua perlakuan, sedangkan percobaan III menggunakan rancangan acak lengkap (RAL) faktor tunggal.
Model linier dari rancangan RAL faktorial adalah sebagai berikut :
Yijk= µ +αi+βj+ (αβij) +ijk
Model linier dari rancangan RAL faktor tunggal adalah sebagai berikut :
Yij= µ +αi+ ij
Dimana : Yijk = Nilai pengamatan pada faktor A taraf ke-i, faktor B taraf
ke-j, ulangan ke-k
Yij = Nilai pengamatan faktor A taraf ke-I, ulangan ke-k
αi = Pengaruh faktor A taraf ke-i
βj = Pengaruh faktor B taraf ke-j
αβij =Pengaruh antara faktor A taraf ke-I dan faktor B taraf
ke-j
ijk = Galat percobaan
ij = Galat percobaan
3.3.1 Percobaan I
Pada percobaan I perlakuan terdiri atas dua faktor yaitu aspirin dan air kelapa, dimana konsentrasi aspirin terbagi atas 4 taraf yaitu 0,10,20,30 mg/l dan konsentrasi air kelapa terbagi atas 4 taraf yaitu 0,10,15 dan 20%. Setiap kombinasi perlakuan I diulang 4 kali. Tiap botol merupakan unit percobaan, tiap botol ditanam 1 planlet. Setelah 2 minggu respon tanaman yang diamati adalah peubah kuantitatif dan kualitatif. Peubah kuantitatif yaitu jumlah daun, jumlah ruas dan jumlah tanaman. Peubah kualitatif adalah pengamatan subjektif dalam bentuk sistem skoring.
yang terbaik bagi pertumbuhan tanaman. Pengaruh dari tiap perlakuan diuraikan ke dalam pembandingan polinomial orthogonal untuk percobaan faktorial.
Data pengamatan peubah kualitatif dianalisis menggunakan uji menurut Kruskal Wallis, dengan hipotesis untuk air kelapa dan aspirin sebagai berikut :
H0 :1 =2 =3 =4
H1 :1≠ 2 =3 =4 1 =2≠ 3 =4 1 =2 =3≠ 4
Dimana : H0 = Hipotesis nol
H1 = Hipotesis 1 bandingan dari hipotesis nol
= Median yaitu nilai yang berada ditengah setelah
diurutkan
1,2,3,4 = Perlakuan yang dicobakan.
Dimana skoring adalah : Skor 1 : Tanaman mati
Skor 2 : Tanaman memiliki batang hijau
Skor 3 : Tanaman memiliki batang hijau dan akar hijau Skor 4 : Tanaman memiliki batang hijau dan 1-2 daun hijau
Skor 5 : Tanaman memiliki batang hijau,1-2 daun hijau dan akar hijau Skor 6 : Tanaman memiliki batang hijau, lebih dari 2 daun hijau dan
akar hijau.
3.3.2 Percobaan II
Pada percobaan II perlakuan terdiri dari dua faktor yaitu sukrosa dengan konsentrasi 5 taraf yaitu 40, 50, 60, 70, 80 g/l dan konsentrasi agar terdiri atas 2 taraf yaitu 7 dan 8 g/l. Setiap kombinasi perlakuan dari percobaan II dicoba dengan 4 ulangan. Tiap botol merupakan unit percobaan, tiap botol ditanam
1 planlet. Setelah 2 minggu respon tanaman yang diamati adalah peubah
Data hasil pengamatan peubah kuantitatif dianalisis menggunakan analisis sidik ragam dan uji Duncan pada taraf 5% untuk melihat kombinasi perlakuan yang terbaik bagi pertumbuhan tanaman. Pada peubah kualitatif menggunakan uji Kruskal Wallis, dengan hipotesis untuk perlakuan agar adalah sebagai berikut :
H0 :1 =2
H1 :1≠ 2
Dimana : H0 : Hipotesis nol
H1 : Hipotesis 1 bandingan dari hipotesis nol
: Median yaitu nilai yang berada ditengah setelah
diurutkan
1,2,3,4 : Perlakuan yang dicobakan.
Hipotesis untuk perlakuan sukrosa adalah
H0 :1 =2 =3 =4 =5
H1 :1≠ 2 =3 =4 =5 1 =2≠ 3 =4 =5 1 =2 =3≠ 4 =5 1 =2 =3 =4≠ 5
Dimana : H0 : Hipotesis nol
H1 : Hipotesis 1 bandingan dari hipotesis nol
: Median yaitu nilai yang berada ditengah setelah
diurutkan
1,2,3,4,5 : Perlakuan yang dicobakan.
Dimana skoring sama dengan pada percobaan I.
3.3.3 Percobaan III
perlakuan yang terbaik bagi pertumbuhan tanaman. Pada peubah kualitatif menggunakan uji Kruskal Wallis.
Hipotesis untuk perlakuan genotipe adalah :
H0 :1 =2 =3 =4
H1 :1≠ 2 =3 =4 1 =2≠ 3 =4 1 =2 =3≠ 4
Dimana : H0 = Hipotesis nol
H1 = Hipotesis 1 bandingan dari hipotesis nol
= Median yaitu nilai yang berada ditengah setelah
diurutkan
1,2,3,4 = Perlakuan yang dicobakan.
Dimana skoring sama pada percobaan I dan II.
3.4 Pelaksanaan Percobaan
Pelaksanaan percobaan diawali dengan perbanyakan tanaman, perbanyakan dengan menggunakan media dasar MS, sukrosa 30 g/l dan agar 7 g/l.
Eksplandiambil dari bukuplanletubi jalar.
3.4.1 Percobaan I
Seluruh unit percobaan disimpan dalam ruang kultur dengan penyinaran 24 jam tiap hari dengan suhu antara 21-24 οC salama 24 minggu. Pengamatan dilakukan 2 minggu setelah tanam, dan dilakukan tiap 2 minggu. Peubah yang diamati adalah peubah kuantitatif yaitu jumlah daun hijau dimana pengamatan dilakukan dengan menghitung jumlah daun yang hidup dan telah membuka sempurna. Peubah jumlah ruas hijau dimana pengamatan dilakukan dengan menghitung jumlah ruas diatara dua buku pada setiapplanlet. Peubah jumlah akar dimana pengamatan dilakukan dengan menghitung jumlah akar yang terbentuk langsung dari planlet dan bukan akar cabang. Parameter kualitatif berdasarkan sistem skoring seperti dituliskan pada bagian 3.3.1.
3.4.2 Percobaan II
Kegiatan awal percobaan II adalah pembuatan media yang terdiri dari perlakuan sukrosa dan agar, dimana sukrosa yang dicobakan adalah konsentrasi 40, 50, 60, 70, 80 g/l dan aspirin yang dicobakan 7 g/l dan 8 g/l. Untuk penghasil unsur hara makro dan mikro digunkan pupuk daun Hyponex (20-20-20) sebanyak 1 g/l pada pH 5,7. Seluruh kombinasi perlakuan berjumlah 10 perlakuan yang diulang 4 kali sehingga seluruh unit percobaan berjumlah 40 unit percobaan. Tiap botol dari seluruh perlakuan ditanam dengan planlet dari kulturin vitro sebanyak 1planlet,dimanaplanlettersebut telah memiliki akar ataupun tidak memiliki akar namun memiliki 1-2 daun.
Seluruh unit percobaan disimpan dalam ruang kultur dengan penyinaran
24 jam tiap hari dengan suhu antara 21-24 οC salama 24 minggu. Pengamatan dilakukan 2 minggu setelah tanam, dan dilakukan tiap 2 minggu. Peubah yang diamati adalah peubah kuantitatif yaitu jumlah daun hijau dimana pengamatan dilakukan dengan menghitung jumlah daun yang hidup dan telah membuka sempurna. Peubah jumlah ruas hijau dilakukan dengan menghitung jumlah ruas diatara dua buku pada setiap planlet. Peubah jumlah akar dimana pengamatan dilakukan dengan menghitung jumlah akar yang terbentuk langsung dari planlet
3.4.3 Percobaan III
Kegiatan awal percobaan III adalah pembuatan media pelestarian yang terdiri dari Hyponex (20-20-20) 1 g/l + sukrosa 50 g/l + air kelapa 15% + aspirin 30 mg/l + agar 7 g/l. Media ini dicobakan pada 4 genotipe pada pH 5,7. Seluruh perlakuan berjumlah 4 perlakuan yang diulang 4 kali sehingga seluruh unit percobaan berjumlah 16 unit percobaan. Tiap botol dari seluruh perlakuan ditanam dengan planlet dari kultur in vitro sebanyak 1 planlet, dimana planlet
tersebut telah memiliki akar ataupun tidak memiliki akar namun harus memiliki 1-2 daun.
4. HASIL DAN PEMBAHASAN
4.1 Percobaan I : Pengaruh Taraf Konsentrasi Air Kelapa dan Aspirin terhadap Pertumbuhan Jumlah Daun, Akar dan Ruas Tanaman Ubi Jalar Genotipe 421.34.
4.1.1 Kondisi Umum
Kondisi planlet yang bertahan selama 24 minggu yaitu daun berwarna hijau muda, batang berwarna kuning muda dan planlet terlihat tegar. Kontaminasi terjadi sampai dengan 12 MST. Kontaminasi disebabkan oleh cendawan dapat segera terlihat dari hifa yang terbentuk di permukaan media. Kontaminasi yang disebabkan oleh bakteri awalnya berupa selaput bening yang menempel pada permukaan media dan kemudian berubah menjadi selaput lendir yang berwarna putih kekuningan yang membentuk koloni.
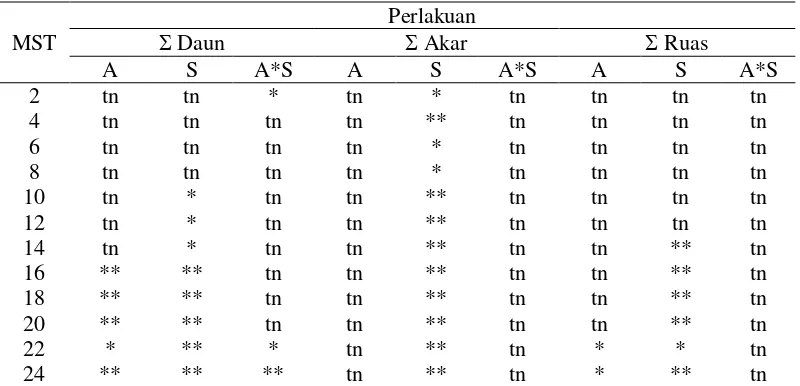
Tabel 1 Rekapitulasi uji F untuk peubah daun, akar dan ruas
MST
Perlakuan
Daun Akar Ruas
K A K*A K A K*A K A K*A
2 tn * tn tn * tn tn tn tn
4 tn ** tn tn ** tn tn tn tn
6 tn ** tn tn ** * ** ** **
8 ** ** ** tn ** ** ** ** **
10 ** ** ** ** ** ** * ** **
12 ** tn ** * ** ** tn ** tn
14 ** ** ** ** ** ** tn ** tn
16 ** ** ** ** ** ** tn ** tn
18 ** ** ** ** ** ** tn ** tn
20 ** ** ** ** ** ** tn ** tn
22 ** ** ** ** ** ** tn ** tn
24 ** * ** ** ** ** tn ** tn
Keterangan : tn = berpengaruh tidak nyata, * = berpengaruh nyata pada taraf 5% dan ** = berpengaruh nyata pada taraf 1%, K = Air Kelapa, A = Aspirin, K*A = Interaksi Antara Air Kelapa dan Aspirin.
akar dimulai dari 2 MST, sedangkan pengaruh aspirin terhadap ruas dimulai 6 MST. Pengaruh interaksi antara air kelapa dan aspirin terhadap pembentukan daun dimulai pada 8 MST, terhadap akar dan ruas dimulai pada 6 MST, namun pengaruh interaksi antara air kelapa dan aspirin terhadap ruas hanya sampai 10 MST (Tabel 1). Hal ini menunjukkan air kelapa hanya berpengaruh terhadap daun dan akar, namun untuk pertambahan ruas tanaman pengaruh air kelapa dihambat oleh pengaruh aspirin.
4.1.2 Jumlah Daun
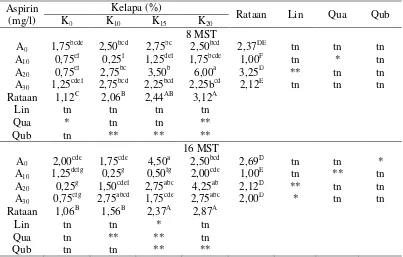
Berdasarkan Tabel 2 terlihat bahwa rata-rata jumlah daun tertinggi dihasilkan oleh kombinasi K20A20pada 8, 16, dan 24 MST, sedangkan rata-rata
jumlah daun terendah diperoleh pada kombinasi K10A10dan K0A20pada 8, 16 dan
24 MST. Hasil uji beda Duncan menunjukkan bahwa perlakuan kombinasi K20A20
berbeda tidak nyata dengan perlakuan kombinasi K15A0 pada 16 dan 24 MST.
Media pelestarian dengan kombinasi perlakuan K20A20 dan K15A0 menghasilkan
jumlah daun yang lebih rendah dibandingkan dengan media kontrol (MS) pada 24 MST (Lampiran 2).
Tabel 2 Pengaruh perlakuan air kelapa dan aspirin terhadap jumlah daun pada 8, 16 dan 24 MST
Aspirin (mg/l)
Kelapa (%)
Lanjutan
Aspirin (mg/l)
Kelapa (%)
Rataan Lin Qua Qub K0 K10 K15 K20
Keterangan : Untuk tabel interaksi : angka yang diikuti oleh huruf yang sama (a-g) pada baris dan kolom yang berbeda tidak berbeda nyata menurut uji Duncan 5%. Untuk rataan pengaruh air kelapa : angka yang diikuti huruf yang sama (A-C) pada kolom yang berbeda dalam satu baris tidak berbeda nyata menurut uji Duncan 5%. Untuk rataan Aspirin : angka yang diikuti huruf yang sama (D-F) pada baris yang berbeda dalam satu kolom tidak berbeda nyata menurut uji Duncan 5%.
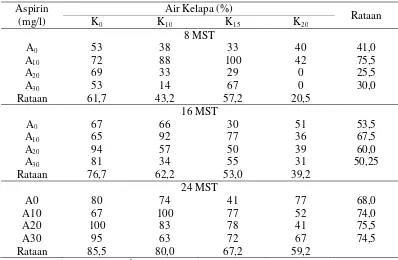
Hasil persentase daun gugur pada media pelestarian yang mengandung Hyponex 20-20-20 menunjukkan daun gugur dimulai pada 4 MST lebih cepat daripada media MS yaitu dimulai pada 8 MST.
Tabel 3 Persentase daun gugur untuk perlakuan air kelapa dan aspirin selama 8, 16 dan 24 MST
Aspirin
Rataan 61,7 43,2 57,2 20,5 16 MST
A0 67 66 30 51 53,5
A10 65 92 77 36 67,5
A20 94 57 50 39 60,0
A30 81 34 55 31 50,25
Rataan 76,7 62,2 53,0 39,2 24 MST
A0 80 74 41 77 68,0
A10 67 100 77 52 74,0
A20 100 83 78 41 75,5
A30 95 63 72 67 74,5
Rataan 85,5 80,0 67,2 59,2
Keterangan : MST = Minggu Setelah Tanam, K = Kelapa, A = Aspirin
mengalami daun gugur 100%, sedangkan perlakuan K15A0dan K20A20mengalami
daun gugur terendah sebesar 41% (Tabel 3). Hal ini menyebabkan pada 24 MST kombinasi perlakuan K0A20dan K10A10tidak memiliki daun, sedangkan perlakuan
K20A20memiliki jumlah daun tertinggi.
Berdasarkan rataan daun gugur dari tiap konsentrasi air kelapa terlihat bahwa semakin meningkat konsentrasi air kelapa pada semua taraf aspirin akan mengurangi jumlah daun gugur, namun pada 8 MST pengaruh air kelapa tersebut belum nampak, pengaruh tersebut baru terlihat pada 12 MST (Lampiran 12). Rataan dari tiap konsentrasi aspirin pada semua taraf air kelapa pada 24 MST memperlihatkan jumlah daun gugur yang semakin meningkat diikuti dengan meningkatnya konsentrasi aspirin sampai konsentrasi 20 mg/l. Pada konsentrasi aspirin 30 mg/l memperlihatkan rataan jumlah daun gugur yang menurun. Pengaruh dari air kelapa menghambat daun gugur terlihat dari rataan daun gugur untuk perlakuan tanpa air kelapa (K0) menghasilkan jumlah daun gugur tertinggi.
Pengaruh yang antagonis dari aspirin yaitu mempercepat daun gugur terlihat dari rataan daun gugur pada perlakuan tanpa aspirin (A0) menghasilkan jumlah daun
gugur terendah pada 24 MST.
Dari hasil uji F (Tabel 3), air kelapa dan aspirin berpengaruh nyata terhadap jumlah daun. Hasil uji Duncan juga menunjukkan kombinasi-kombinasi yang dicobakan memberikan respon yang berbeda-beda, untuk itu dilakukan uji lanjut polinomial orthogonal terhadap perlakuan air kelapa dan aspirin.
Berdasarkan hasil uji polinomial terlihat bentuk dari pengaruh K20dan K15pada 8,
16 dan 24 MST adalah kuadratik dan kubik, dari kedua bentuk ini yang lebih tepat adalah kubik karena nilai R2dari bentuk kubik lebih besar dari bentuk kuadratik. Hasil yang sama juga ditunjukkan pada penelitian awal yang dilakukan Wattimena et al (2003) dimana pengaruh air kelapa 20% pada 8 MST adalah kuadratik. Bentuk kubik dari pengaruh air kelapa dalam penelitian ini disebabkan pengaruh K15 dan K20 pada A10dan A30terjadi penurunan jumlah daun, dan pada
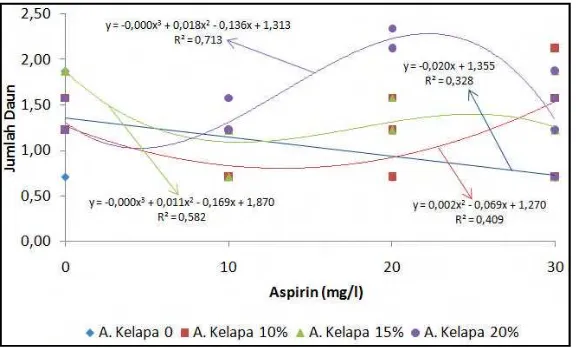
A20 terjadi peningkatan jumlah daun. Grafik interaksi air kelapa dan aspirin
terlihat K20 pada A20 memiliki jumlah daun yang lebih tinggi dibandingkan K15
Gambar 4 Grafik interaksi air kelapa pada 4 taraf aspirin terhadap jumlah daun pada 24 MST.
Bentuk pengaruh dari konsentrasi A20pada keempat taraf air kelapa adalah
linier, berarti semakin tinggi konsentrasi air kelapa yang dikombinasikan dengan konsentrasi A20 maka akan meningkatkan jumlah daun (Gambar 5), hal ini
diperlihatkan oleh kombinasi perlakuan K20A20 yang menghasilkan jumlah daun
tertinggi. Hasil penelitian Wattimena et al (2003) menunjukkan hal yang sama dimana pengaruh aspirin 20 mg/l adalah linier.
Gambar 5 Grafik interaksi aspirin pada 4 taraf air kelapa terhadap jumlah daun pada 24 MST.
4.1.3 Jumlah Akar
yang berbeda tidak nyata dengan K15A20 adalah K10A30 dan K20A20. Rata-rata
jumlah akar terendah pada 8, 16 dan 24 MST terdapat pada media dengan kombinasi perlakuan K10A0 dan menurut uji Duncan perlakuan yang berbeda
tidak nyata dengan perlakuan K10A0 adalah perlakuan K10A10, K0A20 K20A0 dan
K0A0(Tabel 4).
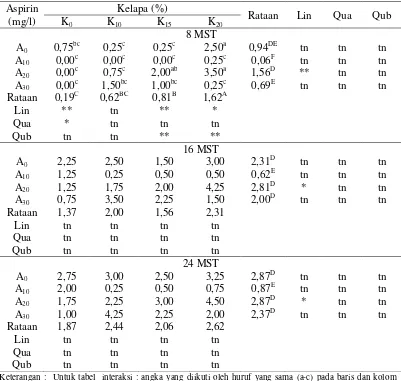
Tabel 4 Pengaruh perlakuan air kelapa dan aspirin terhadap jumlah akar pada 8, 16 dan 24 MST
Aspirin (mg/l)
Kelapa (%)
Rataan Lin Qua Qub K0 K10 K15 K20 Rataan 3,75 3,87 5,00 4,00
Lin tn ** tn tn
Keterangan : Untuk tabel interaksi : angka yang diikuti oleh huruf yang sama (a-f) pada baris dan kolom yang berbeda tidak berbeda nyata menurut uji DMRT 5%. Untuk rataan pengaruh air kelapa : angka yang diikuti huruf yang sama (A-C) pada kolom yang berbeda dalam satu baris tidak berbeda nyata menurut uji DMRT 5%. Untuk rataan Aspirin : angka yang diikuti huruf yang sama (D-F) pada baris yang berbeda dalam satu kolom tidak berbeda nyata menurut uji DMRT 5%.
Berdasarkan uji beda Duncan antar konsentrasi air kelapa, terlihat konsentrasi K15 berbeda nyata dengan konsentrasi air kelapa yang lain dimana
dihasilkan oleh konsentrasi A20 diikuti konsentrasi A30, dimana berdasarkan hasil
uji beda Duncan kedua konsentrasi aspirin tersebut berbeda tidak nyata.
Uji lanjut polinomial orthogonal menunjukkan konsentrasi K15 bentuk
pengaruhnya terhadap jumlah akar adalah tidak nyata, hal ini disebabkan konsentrasi K15pada konsentrasi A10, A20, dan A30berbeda tidak nyata.
Gambar 6 Grafik interaksi air kelapa pada 4 taraf aspirin terhadap jumlah akar pada 24 MST.
Bentuk pengaruh dari konsentrasi A20 pada 8, 16 dan 24 MST adalah
linier, berarti semakin meningkat konsentrasi air kelapa yang dikombinasikan dengan konsentrasi A20 akan meningkatkan jumlah akar sedangkan bentuk
pengaruh dari A30 pada 16 dan 24 MST adalah kuadratik, dimana konsentrasi A30
pada konsentrasi K10 menghasilkan jumlah akar lebih banyak dibandingkan pada
konsentrasi air kelapa yang lain (Gambar 7).
4.1.4 Jumlah Ruas
Berdasarkan pengamatan terhadap peubah jumlah ruas, maka media dengan kombinasi perlakuan K20A20 menghasilkan jumlah ruas tertinggi pada 8,
16 dan 24 MST. Media yang berbeda tidak nyata dengan media dengan kombinasi perlakuan K20A20 adalah media dengan kombinasi perlakuan K20A0, K15A20,
K10A30. Sebaliknya jumlah ruas yang terendah dihasilkan oleh media dengan
kombinasi perlakuan K10A10pada 8, 16 dan 24 MST (Tabel 5).
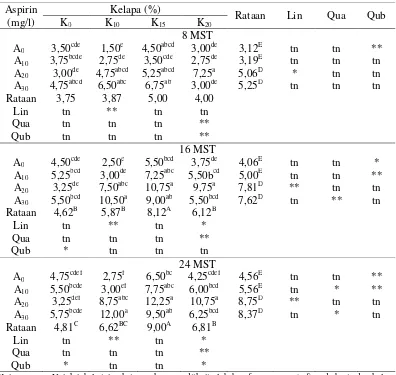
Tabel 5 Pengaruh perlakuan air kelapa dan aspirin terhadap jumlah ruas pada 8, 16 dan 24 MST
Aspirin (mg/l)
Kelapa (%)
Rataan Lin Qua Qub K0 K10 K15 K20 Rataan 1,37 2,00 1,56 2,31
Lin tn tn tn tn Rataan 1,87 2,44 2,06 2,62
Lin tn tn tn tn
Qua tn tn tn tn
Qub tn tn tn tn
Keterangan : Untuk tabel interaksi : angka yang diikuti oleh huruf yang sama (a-c) pada baris dan kolom yang berbeda tidak berbeda nyata menurut uji DMRT 5%. Untuk rataan pengaruh air kelapa : angka yang diikuti huruf yang sama (A-C) pada kolom yang berbeda dalam satu baris tidak berbeda nyata menurut uji DMRT 5%. Untuk rataan Aspirin : angka yang diikuti huruf yang sama (D-F) pada baris yang berbeda dalam kolom yang sama tidak berbeda nyata menurut uji DMRT 5%.
Selanjutnya hasil uji beda Duncan terhadap konsentrasi aspirin menunjukkan konsentrasi A20 menghasilkan jumlah ruas tertinggi, dimana pada 8 MST
konsentrasi A20 berbeda tidak nyata dengan tanpa aspirin, sedangkan pada 16 dan
24 MST konsentrasi A20 berbeda tidak nyata dengan konsentrasi A0 dan
konsentrasi A30.
Berdasarkan hasil uji beda diatas maka konsentrasi air kelapa dan aspirin diuji lanjut dengan uji polinomial orthogonal, namun hanya pada 8 MST karena pada 16 MST dan 24 MST interaksi antara air kelapa dan aspirin terhadap jumlah ruas berbeda tidak nyata. Hasil uji polinomial terhadap air kelapa menunjukkan pengaruh konsentrasi K20 berbentuk kubik, ini berarti konsentrasi K20 bila
dikombinasikan dengan aspirin yang lebih tinggi dari aspirin 20 mg/l (A20) maka
jumlah ruas akan menurun (Gambar 8).
Gambar 8 Grafik interaksi air kelapa pada 4 taraf aspirin terhadap jumlah ruas pada 8 MST.
Sebaliknya konsentrasi aspirin pada 8 MST menunjukkan pengaruh konsentrasi A20 berbentuk linier. Hal ini berarti konsentrasi A20 bila
Gambar 9 Grafik interaksi aspirin pada 4 taraf air kelapa terhadap jumlah ruas pada 8 MST.
4.1.5 Uji Kualitatif
Hasil uji kualitatif berdasarkan metode Kruskal-Walis untuk pengaruh air kelapa dan aspirin (Tabel 6) menunjukkan pengaruh keempat taraf air kelapa terhadap respon tanaman tidak berbeda nyata pada 8 MST, sedangkan pada 16 MST K15memiliki satu median yang berbeda dan pada 24 MST K15 dan K20
memiliki satu median yang berbeda. Hal ini berarti konsentrasi K15 dan K20 pada
keempat taraf aspirin responnya ada yang berbeda. Pada 24 MST untuk konsentrasi K20 dan K20 skor yang dominan adalah skor 5, berarti pada K15 dan
K20 planlet dominan memiliki batang hijau, akar hijau dan memiliki 1-2 daun
hijau.
Pengaruh aspirin pada 8 dan 16 MST hanya konsentrasi A20yang memiliki
satu median yang berbeda, pada 24 MST media dengan konsentrasi K0, K10 dan
K20 memiliki satu median yang berbeda berarti ketiga taraf aspirin pada keempat
taraf air kelapa ada yang berbeda responnya. Kombinasi perlakuan K20A20
Tabel 6 Pengaruh air kelapa dan aspirin terhadap daya hidup pada 8, 16 dan 24 MST
Aspirin (mg/l)
Air Kelapa (%)
p
K0 K10 K15 K20
8 MST
A0 5,0 5,5 5,5 5,5 tn
A10 5,0 3,0 5,0 5,0 tn
A20 5,0 5,5 6,0 6,0 *
A30 5,0 5,5 5,5 5,0 tn
p tn tn tn tn P = **
16 MST
A0 5,5 5,0 6,0 6,0 tn
A10 5,0 3,0 4,0 5,0 tn
A20 3,0 5,0 5,5 6,0 *
A30 5,0 5,5 5,0 5,5 tn
p tn tn * tn P = **
24 MST
A0 5,0 5,0 6,0 5,0 *
A10 5,0 3,0 4,0 5,0 *
A20 3,0 4,0 5,0 6,0 *
A30 3,0 5,0 5,0 5,0 tn
p tn tn * * P = **
Keterangan : Skor 1 (tanaman mati), skor 2 (tanaman memiliki batang yang hijau), skor 3 (tanaman memiliki batang yang hijau dan akar yang hijau), skor 4 (tanaman memiliki batang yang hijau dan 1-2 daun yang hijau), skor 5 (tanaman memiliki batang yang hijau, 1-2 daun yang hijau dan akar yang hijau), skor 6 (tanaman memiliki batang yang hijau, lebih dari 2 daun yang hijau dan akar yang hijau). p = nilai p untuk masing-masing konsentrasi perlakuan; P = nilai P untuk seluruh perlakuan yang dicobakan
Gambar 10 Planletpada kombinasi perlakuan air kelapa 20% dan aspirin 20 mg/l (K20A20) dan kombinasi perlakuan air kelapa 15% dan aspirin 20
mg/l (K15A20) yang berumur 24 minggu.
Gambar 11 Planlet dengan skor 3, skor 5 dan skor 6 setelah dipindahkan ke media MS berumur 2 minggu.
4.1.6 Pembahasan