TINJAUAN PUSTAKA
Tablet Effervescent
Effervescent didefenisikan sebagai bentuk sediaan yang menghasilkan
gelembung gas sebagai hasil reaksi kimia larutan. Gas yang dihasilkan saat
pelarutan Effervescent adalah karbon dioksida sehingga dapat memberikan efek
sparkling (rasa seperti air soda) (Lieberman, et al., 1992).
Tablet Effervescent dibuat dengan cara mengempa formulasi sari buah dan
bahan-bahan aktif berupa sumber asam dan sumber karbonat. Bila tablet
effervescent dimasukkan ke dalam air, akan terjadi reaksi kimia antara sumber
asam dan sumber karbonat tersebut sehingga membentuk garam natrium dari
asam kemudian menghasilkan larutan gas dalam bentuk karbon dioksida (CO2).
Reaksinya berjalan cukup cepat dan biasanya dalam waktu kurang dari satu menit.
Di samping menghasilkan larutan yang jernih, tablet juga memberikan rasa yang
enak karena adanya karbonat yang membantu memperbaiki rasa (Arya, 2004).
Reaksinya adalah sebagai berikut :
H3C6H5O7 + 3 NaHCO3 Na3C6H5O7 + 4 H2O + 3 CO2
Asam sitrat Na-Bikarbonat Na-Sitrat Air Karbon dioksida
H2C4H4O6 + 2 NaHCO3 Na2C4H4O6 + 2 H2O + 2 CO2
Asam Tartarat Na-Bikarbonat Na-Tartarat Air Karbon dioksida
Reaksi di atas tidak dikehendaki terjadi sebelum effervescent dilarutkan,
oleh karena itu kadar air bahan baku dan kelembaban lingkungan perlu
akan berlangsung terus secara cepat karena hasil reaksi adalah air. Kelarutan dari
bahan baku merupakan salah satu hal yang penting dalam pembuatan tablet
effervescent jika kelarutannya kurang baik, maka reaksi tidak akan terjadi dan
tablet tidak larut dengan cepat (Lieberman, et al., 1992).
Secara sederhana proses pembuatan tablet effervescent dibagi menjadi dua
tahap yaitu :
1. Proses pencampuran
Proses pencampuran ini bertujuan untuk mendapatkan massa tablet yang
homogen. Tujuan ini dapat dicapai bila sifat partikel penyusun campuran dan
faktor lainnya yang mempengaruhi proses pencampuran adalah sama. Sifat fisis
dari partikel yang mempengaruhi proses pencampuran adalah ukuran, bentuk,
densitas dan kelembaban partikel, sedangkan faktor lainnya adalah kadar partikel.
Pada proses pencampuran ini bahan-bahan yang dicampurkan meliputi sumber
karbonat, sumber asam, bahan pengikat, bahan pengisi, bahan pelincir, bahan cita
rasa dan bila perlu ditambahkan pewarna (Arya, 2004).
2. Proses pencetakan tablet
Pada prinsipnya, tablet dapat dibuat melalui kempa langsung atau
granulasi, baik granulasi basah atau granulasi kering. Untuk menentukan metoda
pembuatannya apakah dibuat kempa langsung atau granulasi sangat tergantung
pada dosis dan sifat zat aktifnya. Dibandingkan dengan metoda granulasi, metoda
kempa langsung dinilai lebih menguntungkan dalam hal penghematan waktu,
peralatan, ruangan maupun energi yang dibutuhkan. Namun demikian, untuk
metoda kempa langsung ini semua komponen tablet baik zat aktif, bahan pengisi,
Pada proses pengempaan untuk zat aktif dengan dosis kecil hal ini tidak akan
menjadi masalah selama homogenitasnya diperhatikan. Tetapi untuk zat aktif
dengan dosis besar, jika sifat alir dan kompresibilitasnya tidak baik diperlukan
bahan tambahan yang efektif untuk mengatasi sifat alir dan kompresibilitas
(Arya, 2004).
Pada pembuatan tablet effervescent suhu dan RH (relative humidity)
merupakan salah satu faktor yang sangat penting. RH yang rendah dan suhu yang
rendah (cool) sangat penting untuk mencegah proses granulasi dan pembentukan
tablet dari penyerapan uap air, yang menyebabkan ketidakstabilan tablet. Ruangan
ber-RH maksimal 25% dan bersuhu 25oC, merupakan kondisi yang baik untuk proses pembuatan tablet effervescent (Lieberman, et al., 1992).
Asam Organik
Salah satu tujuan utama penambahan asam pada makanan adalah untuk
memberikan rasa asam. Asam juga dapat mengintensifkan penerimaan rasa-rasa
lain. Asam yang banyak digunakan pada bahan makanan adalah asam organik
seperti asam asetat, asam laktat, asam sitrat, asam fumarat, asam malat, asam
suksinat dan asam tartarat (Winarno, 2002).
Asam sitrat merupakan asam yang umum digunakan sebagai asam
makanan dan harganya relatif murah. Asam ini memiliki kelarutan yang tinggi,
mempunyai kekuatan asam yang tinggi dan tersedia dalam bentuk granular,
anhidrous dan bentuk monohidrat. Selain itu, tersedia juga dalam bentuk serbuk.
Asam ini sangat higroskopis, oleh karena itu penanganan dan penyimpanannya
memerlukan perhatian khusus (Lieberman, et al., 1992).
Asam tartarat merupakan asam yang biasa digunakan sebagai sumber
asam effervescent. Asam tartarat kelarutannya lebih baik dan lebih higroskopis
dibandingkan asam sitrat (Lieberman, et al., 1992).
Asam malat merupakan asam yang digunakan dalam sistem effervescent.
Asam ini bersifat higroskopis dan kelarutannya relatif cukup baik. Kekuatan
asamnya lebih kecil dari asam sitrat dan asam tartarat tetapi dapat menghasilkan
reaksi karbonasi ketika direaksikan dengan sumber basa (Lieberman, et al., 1992).
Asam askorbat berwarna putih, membentuk kristal dan sangat larut dalam
air. Vitamin C ditemukan hampir sepenuhnya dalam makanan nabati, yaitu
sayuran dan buah-buahan segar (Winarno, 2002).
Markisa
Markisa yang ada di Indonesia dikenal ada dua jenis, yaitu markisa yang berwarna
ungu (Passiflora edulis SIMS), yang dikenal dengan sebutan buah negeri atau
siuh, dan markisa yang buahnya kuning disebut (Passiflora laurifolia L.), yang
dikenal dengan sebutan buah susu atau konyal. P.edulis (buah negeri) memiliki
rasa yang asam dan cocok ditanam pada dataran tinggi, sedangkan P. laurifolia
(buah konyal) memiliki rasa yang agak manis dan cocok ditanam di dataran
rendah. Meskipun demikian keduanya memiliki bentuk tanaman yang sama dan
mahkota bunganya keduanya berwarna ungu keputih-putihan. Bunganya
berkelamin dua (hermaphrodite) dan memiliki aroma khas harum namun memilki
biji yang banyak. Markisa jenis P.edulis SIMS jarang dikonsumsi dalam bentuk
segar karena rasanya yang asam. Di Indonesia masih terdapat balewa atau markisa
umumnya hanya ditanam di dataran rendah dan buahnya hanya untuk sari buah
segar (Sunarjono, 1997).
Musim buah terjadi pada bulan Desember sampai Februari, sedangkan
pada bulan Juni, Juli dan Agustus hasilnya sangat rendah. Bagian-bagian buah
markisa terdiri dari bagian kulit sebesar 51% dan bagian isi sebesar 49%. Bagian
isi terdiri dari biji sebesar 20,2% dan sari buah sebesar 28,8%. Sari berwarna
kuning kemerah-merahan dan rasanya asam dengan pH 3,0-4,5
(Faatmah, et al., 1985).
Buah famili Passiflora mengandung banyak sari buah dan daging buahnya
selalu dimanfaatkan, namun pada markisa spesies Passiflora quadrangularis
daginga buah yang rasanya khas hanya dimanfaatkan untuk sari buah segar. Akan
tetapi daging buah yang matanglah yang merupakan produk utama. Sari buah
dapat dicampur dengan jeruk manis, papaya dan jambu biji
(Verheij dan Coronel, 1997).
Komposisi Kimia Markisa
Sari markisa adalah cairan yang di ekstrak, diperas atau dikeluarkan dari
bagian buah dengan penekanan atau pengepresan atau dengan cara mekanis lain
dan umumnya digunakan untuk minuman segar. Sari buah markisa kaya dengan
zat nutrisi dan merupakan sumber vitamin C yang baik. Komposisi sari markisa
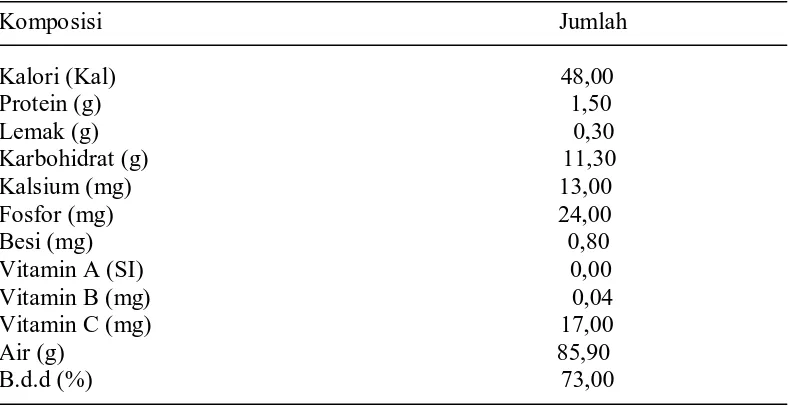
Tabel 1. Komposisi kimia markisa per 100 g bahan
Komposisi Jumlah
Kalori (Kal) 51,00 Protein (g) 0,40 Lemak (g) 0,10 Karbohidrat (g) 13,60 Kapur (mg) 3,60 Fosfor (mg) 12,50 Besi (mg) 0,20 Vitamin A (IU) 717,00 Vitamin B (mg) 0,10 Vitamin C (mg) 30,00 Air (g) 85,60 Abu (g) 0,30
Sumber: Rismunandar, (1986).
Daging buah markisa banyak mengandung sari buah. Karena rasanya yang khas,
daging buah markisa dapat dicampur dengan buah-buahan yang lain. Daging buah
ini dikonsumsi dalam keadaan segar atau diolah menjadi konsentrat sari buah atau
sirup. Daging buah markisa kaya akan gizi dan setiap 100 g berisi 88 g air; 0,9 g
protein; 0,2 g lemak; 10,1 g karbohidrat; 0,9 g abu; 10 mg kalsium; 20 mg fosfor;
0,6 mg besi; 70 SI vitamin A; 2,7 mg niasin dan 20 mg vitamin C, nilai energinya
mencapai 170 kJ/100 g (Verheij dan Coronel, 1997).
Terung Belanda
Terung belanda (Syphomandra betacea) diduga berasal dari pegunungan
Andes wilayah Peru. Kemudian disebarkan ke sebagian besar dataran tinggi tropis
(di tempat tersebut dijadikan tanaman peliharaan kembali) di daerah sub tropis,
dan juga di beberapa daerah yang memiliki iklim sedang. Tanaman ini sangat
cocok tumbuh di daerah Sumatera Utara seperti di daerah Tanah Karo yang telah
Buah terung belanda dimanfaatkan untuk berbagai bahan makanan seperti
konsentrat, sirup dan dodol. Setiap 100 g bagian buah terung belanda yang dapat
dimakan mengandung air 85%; protein 1,5 g; lemak 0,06-1,28 g; karbohidrat 10
g; serat 1,4-4,2 g; abu 0,7 g;vitamin A 150-500 SI dan vitamin C 25 mg. sebagian
vitamin akan hilang dengan perebusan (Verheij dan Coronel, 1997).
Komposisi Kimia Terung Belanda
Komposisi kimia terung belanda secara umum dapat dilihat pada Tabel 2.
Tabel 2. Komposisi kimia terung belanda per 100 g bahan
Komposisi Jumlah
Sumber : Departemen Kesehatan R.I., (1996).
Bahan-bahan Tambahan Gula Sukrosa
Sukrosa adalah polisakarida yang mempunyai peran penting dalam
pengolahan makanan dan banyak terdapat pada tebu, bit, siwalan dan kelapa
kopyor. Sukrosa merupakan gula yang murah dan diproduksi dalam jumlah besar.
Secara komersial gula pasir dibuat melalui proses penyulingan dan kristalisasi
(Almatsier, 2001).
Sukrosa mempunyai sifat yang mudah larut dalam air, berbentuk kristal
dan mempunyai rasa manis sehingga sukrosa yang ditambahkan sebagai pemanis
terutama untuk meningkatkan cita rasa. Di samping itu juga digunakan sebagai
pengawet karena tekanan osmosanya yang tinggi sehingga menyebabkan
terjadinya plasmolisis yang mengakibatkan kematian bagi mikroba
(Buckle, et al., 1987).
Acesulfame
Pemanis baru, yang diizinkan sejak tahun 1988, ialah K-asesulfam.
Pemanis ini adalah garam kalium 6-metil-1,2,3-oksatiozina-4
(3H)-on-2,2-dioksida dan merupakan glikosida fenolik. Senyawa ini berbentuk serbuk kristal
dengan kemanisan sekitar 200 kali kemanisan gula. Daya memaniskannya
bergantung sampai tingkat tertentu, pada keasaman makanan yang ditambahi
senyawa ini. K-asesulfam menurut laporan lebih stabil dari pada pemanis lain.
Pemanis hidrokarbon diperoleh dari glikosida fenolik yang terdapat dalam kulit
jeruk. Senyawa seperti ini dapat diperoleh dari jeruk, anggur atau dari flavanoid
neophesperidin (deMan, 1997).
Aroma
Aroma buah-buahan disebabkan oleh berbagai ester yang bersifat volatil.
Proses timbulnya aroma ini pada bahan yang berbeda tidak sama. Pada
buah-buahan, produksi senyawa aroma ini meningkat ketika mendekati masa
klimakterik (Winarno, 2002).
Aroma buatan sering sekali ditambahkan pada minuman yang tidak
jumlahnya relatif rendah. Apabila perbandingan air yang digunakan sangat besar
dibandingkan bubur buahnya,maka perlu ditambahkan aroma untuk menutupi
kekurangan tersebut (Satuhu, 1994).
Gelatin
Gelatin adalah protein ynag diperoleh dari kolagen tak larut. Meskipun
gelatin dapat dibuat dari bermacam-macam hasil tambahan hewan, kulit
merupakan sumber umum produksi gelatin. Proses perubahan kolagen menjadi
gelatin melibatkan tiga perubahan berikut :
1. Pemutusan sejumlah terbatas ikatan peptida untuk memperpendek rantai
2. Pemutusan atau pengacauan sejumlah ikatan samping antar rantai
3. Perubahan konfigurasi rantai
Perubahan terakhir merupakan satu-satunya perubahan penting untuk perubahan
kolagen menjadi gelatin. Proses pembentuk gel kemungkinan berkaitan erat
dengan adanya gugus guanidin arginin (deMan, 1997).
Gelatin diekstrak dari jaringan tubuh hewan khususnya dari kulit dan
tulang hewani, umumnya dari tulang sapi atau hewan memamah biak lainnya.
Jaringan-jaringan tersebut diletakkan dalam larutan alkali lemah selama seminggu
kemudian dididihkan untuk mendapatkan gelatin. Gelatin merupakan bentuk gel
yang stabil pada suhu panas yang berbentuk padat pada suhu 20oC dan Cair pada
suhu 30oC, oleh karena itu gel-gel gelatin mencair didalam mulut.(Hughes, 1991). Gelatin umum tidak larut dalam air dingin, tetapi larut dalam air pada
suhu diatas 45oC, kecuali bubuk gelatin yang diperoleh dengan spray drying. Gel gelatin melembut pada suhu 25o-28oC yang mana tergantung pada sel padatannya (Tranggono, et al., 1990).
Natrium Bikarbonat (NaHCO3)
NaHCO3 akan menghasilkan gas CO2 yang dibutuhkan dalam proses
karbonasi. Proses yang paling penting dalam pembuatan minuman ini adalah
proses karbonasi karena rasa yang spesifik dan efek yang menyegarkan diberikan
oleh proses karbonasi ini. Karbonasi merupakan pelarutan CO2 di dalam air
dengan kondisi temperatur dan tekanan yang terkontrol. Penyerapan CO2 akan
semakin banyak dengan naiknya tekanan dan turunnya temperatur. Keuntungan
dari menggunakan NaHCO3 adalah relatif tidak mempengaruhi rasa, harganya
relatif murah dan tingkat kemurniannya tinggi (Dania dan Hidayat, 2005).
Natrium bikarbonat merupakan bagian terbesar sumber karbonat dengan
kelarutan yang sangat baik di dalam air, higroskopis serta tersedia secara
komersial mulai dari bentuk bubuk sampai granular (Atwawijaya, 2004).
Reaksi NaHCO3 dalam air (Winarno, 2002) adalah sebagai berikut :
NaHCO3 Na+ + HCO3
-HCO3- + H2O H2CO3 + OH
-HCO3- CO3- + H
ABSTRAK
IMRAN: Pengaruh Jenis Asam Organik dan Perbandingan Sari Markisa dan Terung Belanda terhadap Mutu Tablet Effervescent. Dibimbing oleh ZULKIFLI LUBIS dan HERLA RUSMARILIN.
Penelitian ini dilakukan untuk mengetahui pengaruh jenis asam organik dan perbandingan sari markisa dan terung belanda terhadap mutu tablet effervescent. Penelitian ini menggunakan rancangan acak lengkap dengan dua faktor, yakni jenis asam (A): (asam sitrat, asam malat, asam tartarat dan asam askorbat) dan perbandingan sari markisa dan terung belanda (M): (90:10%, 80:20%, 70:30%, dan 60:40%). Parameter analisa adalah kadar air, kadar vitamin C, total asam, daya larut, pH, dan uji organoleptik (warna, aroma, dan rasa).
Hasil penelitian menunjukkan bahwa jenis asam organik berpengaruh sangat nyata terhadap kadar vitamin C, total asam, daya larut, pH dan uji organoleptik (warna, aroma dan rasa) dan berpengaruh nyata terhadap kadar air. Perbandingan sari markisa dan terung belanda berpengaruh sangat nyata terhadap kadar vitamin C, total asam, pH dan uji organoleptik (warna, aroma dan rasa) tetapi berpengaruh tidak nyata terhadap kadar air dan daya larut. Interaksi jenis asam organik dan perbandingan sari markisa dan terung belanda berpengaruh sangat nyata terhadap kadar vitamin C tetapi berpengaruh tidak nyata terhadap kadar air, total asam, daya larut, pH, dan uji organoleptik (warna, aroma, dan rasa). Asam askorbat dan perbandingan sari markisa dan terung belanda 90:10% menghasilkan tablet effervescent yang terbaik.
Kata kunci : Tablet effervescent, asam organik, sari markisa, sari terung belanda.
ABSTRACT
IMRAN: The Effect of Different Organic Acids and Composition of Marquisa and Tamarillo Juice on the Quality of Effervescent Tablet. Under the supervision of ZULKIFLI LUBIS and HERLA RUSMARILIN.
The research was performed to find the effect of different organic acids and composition of marquisa and tamarillo juice on the quality of effervescent tablet. The research had been performed using factorial completely randomized design with two factors i.e: different organic acids (A): (citric acid, maleic acid, tartaric acid, and ascorbic acid) and composition of marquisa and tamarillo juice (M): (90:10%, 80:20%, 70:30% and 60:40%). Parameters analysed were moisture content, vitamin C content, total acid, solubility, pH and organoleptic values (colour, flavour, and taste).
The result showed that the different organic acid had highly significant effect on vitamin C content, total acid, solubility, pH and organoleptic values (colour, flavour, and taste), and had significant effect on moisture content. The composition of marquisa and tamarillo juice had highly significant effect on vitamin C content, total acid, pH and organoleptic values (colour, flavour, and taste), but had no significant effect on moisture content and solubility. The interaction of the different organic acid and composition of marquisa and tamarillo juice had highly significant effect on vitamin C content, but had no significant effect on moisture content, total acid, solubility, pH and organoleptic values (colour, flavour, and taste). Ascorbic acid and composition of marquisa and tamarillo juice of 90:10% produced the best effervescent tablet.
Latar Belakang
Indonesia merupakan negara agraris yang kaya akan produk hortikultura.
Produk hortikultura terutama buah-buahan menempati posisi yang penting dalam
hal pemenuhan kebutuhan zat gizi bagi manusia, khususnya vitamin A, B dan C,
mineral dan serat kasar. Pada kondisi pasca panen buah-buahan mudah sekali
mengalami kerusakan, hal ini dikarenakan terjadinya perubahan pada buah baik
perubahan fisiologis, kimiawi maupun mikrobiologis bila tidak diikuti dengan
penanganan dan pengawetan yang tepat. Dalam jangka 5-10 hari buah menjadi
tidak segar lagi, yang akhirnya mengakibatkan mutu dari buah-buahan akan turun
drastis.
Karena sifatnya yang mudah rusak maka pengolahan buah-buahan adalah
salah satu alternatif untuk mengantisipasi hasil panen yang berlebihan dan tidak
dapat dipasarkan karena mutunya yang rendah.
Markisa dan terung belanda dapat diperoleh dari pasar lokal di daerah
tropis, hampir sepanjang tahun. Buah markisa dan terung belanda tidak selamanya
habis terjual terutama pada saat musim panen besar. Hal ini akan memberikan
dampak merugikan bagi petani. Untuk itu diperlukan penanganan yang serius
sehingga buah ini dapat digunakan semaksimal mungkin.
Salah satu cara pengawetan buah-buahan tersebut adalah mengolahnya
menjadi minuman berkarbonasi dalam bentuk tablet yaitu effervescent. Minuman
effervescent atau tablet effervescent dapat dibuat dengan cara mengempa
dimasukkan ke dalam air, maka akan terjadi reaksi kimia antara sumber asam dan
sumber karbonat tersebut sehingga menghasilkan gas dalam bentuk karbon
dioksida (CO2). Di samping menghasilkan larutan yang jernih, rasanya juga enak
karena adanya karbonat yang membantu memperbaiki cita rasa. Pada pembuatan
tablet effervescent selain sumber asam dan karbonat, ada faktor lain yang
memiliki pengaruh seperti bahan pengikat, bahan cita rasa dan penambahan
warna.
Penambahan natrium bikarbonat (NaHCO3) dan asam organik sangat
mempengaruhi tablet effervescent yang dihasilkan. Sumber karbonat yang umum
digunakan dalam pembuatan tablet effervescent adalah NaHCO3 yang memiliki
daya larut sangat baik di dalam air. Sedangkan jenis asam organik yang sering
digunakan dalam pembuatan tablet effervescent adalah asam sitrat, asam malat,
asam tartarat dan asam askorbat. Asam sitrat mempunyai kelarutan yang tinggi di
dalam air dan mempunyai pengaruh yang baik terhadap aroma dan rasa.
Penambahan asam juga berperan dalam menurunkan pH. Oleh karena itu
diperlukan konsentrasi NaHCO3 dan konsentrasi asam yang tepat untuk
memperoleh tablet effervescent dengan kelarutan yang baik di dalam air.
Hal inilah yang mendasari penulis untuk melakukan penelitian tentang
“Pengaruh Jenis Asam Organik dan Perbandingan Sari Markisa dan Terung Belanda Terhadap Mutu Tablet Effervescent”
Tujuan Penelitian
Tujuan penelitian ini adalah untuk mengetahui pengaruh jenis asam
organik dan perbandingan sari markisa dan terung belanda terhadap mutu tablet
effervescent.
Kegunaan Penelitian
Penelitian ini berguna untuk mendapatkan data penyusunan skripsi sebagai
salah satu syarat untuk mendapatkan gelar sarjana di Fakultas Pertanian,
Universitas Sumatera Utara, Medan, dan dapat berguna untuk pihak-pihak yang
berkepentingan dalam industri tablet effervescent.
Hipotesis Penelitian
Ada pengaruh jenis asam organik, perbandingan sari markisa dan terung
belanda dan interaksi antara jenis asam organik dan perbandingan sari markisa
TINJAUAN PUSTAKA
Tablet Effervescent
Effervescent didefenisikan sebagai bentuk sediaan yang menghasilkan
gelembung gas sebagai hasil reaksi kimia larutan. Gas yang dihasilkan saat
pelarutan Effervescent adalah karbon dioksida sehingga dapat memberikan efek
sparkling (rasa seperti air soda) (Lieberman, et al., 1992).
Tablet Effervescent dibuat dengan cara mengempa formulasi sari buah dan
bahan-bahan aktif berupa sumber asam dan sumber karbonat. Bila tablet
effervescent dimasukkan ke dalam air, akan terjadi reaksi kimia antara sumber
asam dan sumber karbonat tersebut sehingga membentuk garam natrium dari
asam kemudian menghasilkan larutan gas dalam bentuk karbon dioksida (CO2).
Reaksinya berjalan cukup cepat dan biasanya dalam waktu kurang dari satu menit.
Di samping menghasilkan larutan yang jernih, tablet juga memberikan rasa yang
enak karena adanya karbonat yang membantu memperbaiki rasa (Arya, 2004).
Reaksinya adalah sebagai berikut :
H3C6H5O7 + 3 NaHCO3 Na3C6H5O7 + 4 H2O + 3 CO2
Asam sitrat Na-Bikarbonat Na-Sitrat Air Karbon dioksida
H2C4H4O6 + 2 NaHCO3 Na2C4H4O6 + 2 H2O + 2 CO2
Asam Tartarat Na-Bikarbonat Na-Tartarat Air Karbon dioksida
Reaksi di atas tidak dikehendaki terjadi sebelum effervescent dilarutkan,
oleh karena itu kadar air bahan baku dan kelembaban lingkungan perlu
akan berlangsung terus secara cepat karena hasil reaksi adalah air. Kelarutan dari
bahan baku merupakan salah satu hal yang penting dalam pembuatan tablet
effervescent jika kelarutannya kurang baik, maka reaksi tidak akan terjadi dan
tablet tidak larut dengan cepat (Lieberman, et al., 1992).
Secara sederhana proses pembuatan tablet effervescent dibagi menjadi dua
tahap yaitu :
1. Proses pencampuran
Proses pencampuran ini bertujuan untuk mendapatkan massa tablet yang
homogen. Tujuan ini dapat dicapai bila sifat partikel penyusun campuran dan
faktor lainnya yang mempengaruhi proses pencampuran adalah sama. Sifat fisis
dari partikel yang mempengaruhi proses pencampuran adalah ukuran, bentuk,
densitas dan kelembaban partikel, sedangkan faktor lainnya adalah kadar partikel.
Pada proses pencampuran ini bahan-bahan yang dicampurkan meliputi sumber
karbonat, sumber asam, bahan pengikat, bahan pengisi, bahan pelincir, bahan cita
rasa dan bila perlu ditambahkan pewarna (Arya, 2004).
2. Proses pencetakan tablet
Pada prinsipnya, tablet dapat dibuat melalui kempa langsung atau
granulasi, baik granulasi basah atau granulasi kering. Untuk menentukan metoda
pembuatannya apakah dibuat kempa langsung atau granulasi sangat tergantung
pada dosis dan sifat zat aktifnya. Dibandingkan dengan metoda granulasi, metoda
kempa langsung dinilai lebih menguntungkan dalam hal penghematan waktu,
peralatan, ruangan maupun energi yang dibutuhkan. Namun demikian, untuk
metoda kempa langsung ini semua komponen tablet baik zat aktif, bahan pengisi,
Pada proses pengempaan untuk zat aktif dengan dosis kecil hal ini tidak akan
menjadi masalah selama homogenitasnya diperhatikan. Tetapi untuk zat aktif
dengan dosis besar, jika sifat alir dan kompresibilitasnya tidak baik diperlukan
bahan tambahan yang efektif untuk mengatasi sifat alir dan kompresibilitas
(Arya, 2004).
Pada pembuatan tablet effervescent suhu dan RH (relative humidity)
merupakan salah satu faktor yang sangat penting. RH yang rendah dan suhu yang
rendah (cool) sangat penting untuk mencegah proses granulasi dan pembentukan
tablet dari penyerapan uap air, yang menyebabkan ketidakstabilan tablet. Ruangan
ber-RH maksimal 25% dan bersuhu 25oC, merupakan kondisi yang baik untuk proses pembuatan tablet effervescent (Lieberman, et al., 1992).
Asam Organik
Salah satu tujuan utama penambahan asam pada makanan adalah untuk
memberikan rasa asam. Asam juga dapat mengintensifkan penerimaan rasa-rasa
lain. Asam yang banyak digunakan pada bahan makanan adalah asam organik
seperti asam asetat, asam laktat, asam sitrat, asam fumarat, asam malat, asam
suksinat dan asam tartarat (Winarno, 2002).
Asam sitrat merupakan asam yang umum digunakan sebagai asam
makanan dan harganya relatif murah. Asam ini memiliki kelarutan yang tinggi,
mempunyai kekuatan asam yang tinggi dan tersedia dalam bentuk granular,
anhidrous dan bentuk monohidrat. Selain itu, tersedia juga dalam bentuk serbuk.
Asam ini sangat higroskopis, oleh karena itu penanganan dan penyimpanannya
memerlukan perhatian khusus (Lieberman, et al., 1992).
Asam tartarat merupakan asam yang biasa digunakan sebagai sumber
asam effervescent. Asam tartarat kelarutannya lebih baik dan lebih higroskopis
dibandingkan asam sitrat (Lieberman, et al., 1992).
Asam malat merupakan asam yang digunakan dalam sistem effervescent.
Asam ini bersifat higroskopis dan kelarutannya relatif cukup baik. Kekuatan
asamnya lebih kecil dari asam sitrat dan asam tartarat tetapi dapat menghasilkan
reaksi karbonasi ketika direaksikan dengan sumber basa (Lieberman, et al., 1992).
Asam askorbat berwarna putih, membentuk kristal dan sangat larut dalam
air. Vitamin C ditemukan hampir sepenuhnya dalam makanan nabati, yaitu
sayuran dan buah-buahan segar (Winarno, 2002).
Markisa
Markisa yang ada di Indonesia dikenal ada dua jenis, yaitu markisa yang berwarna
ungu (Passiflora edulis SIMS), yang dikenal dengan sebutan buah negeri atau
siuh, dan markisa yang buahnya kuning disebut (Passiflora laurifolia L.), yang
dikenal dengan sebutan buah susu atau konyal. P.edulis (buah negeri) memiliki
rasa yang asam dan cocok ditanam pada dataran tinggi, sedangkan P. laurifolia
(buah konyal) memiliki rasa yang agak manis dan cocok ditanam di dataran
rendah. Meskipun demikian keduanya memiliki bentuk tanaman yang sama dan
mahkota bunganya keduanya berwarna ungu keputih-putihan. Bunganya
berkelamin dua (hermaphrodite) dan memiliki aroma khas harum namun memilki
biji yang banyak. Markisa jenis P.edulis SIMS jarang dikonsumsi dalam bentuk
segar karena rasanya yang asam. Di Indonesia masih terdapat balewa atau markisa
umumnya hanya ditanam di dataran rendah dan buahnya hanya untuk sari buah
segar (Sunarjono, 1997).
Musim buah terjadi pada bulan Desember sampai Februari, sedangkan
pada bulan Juni, Juli dan Agustus hasilnya sangat rendah. Bagian-bagian buah
markisa terdiri dari bagian kulit sebesar 51% dan bagian isi sebesar 49%. Bagian
isi terdiri dari biji sebesar 20,2% dan sari buah sebesar 28,8%. Sari berwarna
kuning kemerah-merahan dan rasanya asam dengan pH 3,0-4,5
(Faatmah, et al., 1985).
Buah famili Passiflora mengandung banyak sari buah dan daging buahnya
selalu dimanfaatkan, namun pada markisa spesies Passiflora quadrangularis
daginga buah yang rasanya khas hanya dimanfaatkan untuk sari buah segar. Akan
tetapi daging buah yang matanglah yang merupakan produk utama. Sari buah
dapat dicampur dengan jeruk manis, papaya dan jambu biji
(Verheij dan Coronel, 1997).
Komposisi Kimia Markisa
Sari markisa adalah cairan yang di ekstrak, diperas atau dikeluarkan dari
bagian buah dengan penekanan atau pengepresan atau dengan cara mekanis lain
dan umumnya digunakan untuk minuman segar. Sari buah markisa kaya dengan
zat nutrisi dan merupakan sumber vitamin C yang baik. Komposisi sari markisa
Tabel 1. Komposisi kimia markisa per 100 g bahan
Komposisi Jumlah
Kalori (Kal) 51,00 Protein (g) 0,40 Lemak (g) 0,10 Karbohidrat (g) 13,60 Kapur (mg) 3,60 Fosfor (mg) 12,50 Besi (mg) 0,20 Vitamin A (IU) 717,00 Vitamin B (mg) 0,10 Vitamin C (mg) 30,00 Air (g) 85,60 Abu (g) 0,30
Sumber: Rismunandar, (1986).
Daging buah markisa banyak mengandung sari buah. Karena rasanya yang khas,
daging buah markisa dapat dicampur dengan buah-buahan yang lain. Daging buah
ini dikonsumsi dalam keadaan segar atau diolah menjadi konsentrat sari buah atau
sirup. Daging buah markisa kaya akan gizi dan setiap 100 g berisi 88 g air; 0,9 g
protein; 0,2 g lemak; 10,1 g karbohidrat; 0,9 g abu; 10 mg kalsium; 20 mg fosfor;
0,6 mg besi; 70 SI vitamin A; 2,7 mg niasin dan 20 mg vitamin C, nilai energinya
mencapai 170 kJ/100 g (Verheij dan Coronel, 1997).
Terung Belanda
Terung belanda (Syphomandra betacea) diduga berasal dari pegunungan
Andes wilayah Peru. Kemudian disebarkan ke sebagian besar dataran tinggi tropis
(di tempat tersebut dijadikan tanaman peliharaan kembali) di daerah sub tropis,
dan juga di beberapa daerah yang memiliki iklim sedang. Tanaman ini sangat
cocok tumbuh di daerah Sumatera Utara seperti di daerah Tanah Karo yang telah
Buah terung belanda dimanfaatkan untuk berbagai bahan makanan seperti
konsentrat, sirup dan dodol. Setiap 100 g bagian buah terung belanda yang dapat
dimakan mengandung air 85%; protein 1,5 g; lemak 0,06-1,28 g; karbohidrat 10
g; serat 1,4-4,2 g; abu 0,7 g;vitamin A 150-500 SI dan vitamin C 25 mg. sebagian
vitamin akan hilang dengan perebusan (Verheij dan Coronel, 1997).
Komposisi Kimia Terung Belanda
Komposisi kimia terung belanda secara umum dapat dilihat pada Tabel 2.
Tabel 2. Komposisi kimia terung belanda per 100 g bahan
Komposisi Jumlah
Sumber : Departemen Kesehatan R.I., (1996).
Bahan-bahan Tambahan Gula Sukrosa
Sukrosa adalah polisakarida yang mempunyai peran penting dalam
pengolahan makanan dan banyak terdapat pada tebu, bit, siwalan dan kelapa
kopyor. Sukrosa merupakan gula yang murah dan diproduksi dalam jumlah besar.
Secara komersial gula pasir dibuat melalui proses penyulingan dan kristalisasi
(Almatsier, 2001).
Sukrosa mempunyai sifat yang mudah larut dalam air, berbentuk kristal
dan mempunyai rasa manis sehingga sukrosa yang ditambahkan sebagai pemanis
terutama untuk meningkatkan cita rasa. Di samping itu juga digunakan sebagai
pengawet karena tekanan osmosanya yang tinggi sehingga menyebabkan
terjadinya plasmolisis yang mengakibatkan kematian bagi mikroba
(Buckle, et al., 1987).
Acesulfame
Pemanis baru, yang diizinkan sejak tahun 1988, ialah K-asesulfam.
Pemanis ini adalah garam kalium 6-metil-1,2,3-oksatiozina-4
(3H)-on-2,2-dioksida dan merupakan glikosida fenolik. Senyawa ini berbentuk serbuk kristal
dengan kemanisan sekitar 200 kali kemanisan gula. Daya memaniskannya
bergantung sampai tingkat tertentu, pada keasaman makanan yang ditambahi
senyawa ini. K-asesulfam menurut laporan lebih stabil dari pada pemanis lain.
Pemanis hidrokarbon diperoleh dari glikosida fenolik yang terdapat dalam kulit
jeruk. Senyawa seperti ini dapat diperoleh dari jeruk, anggur atau dari flavanoid
neophesperidin (deMan, 1997).
Aroma
Aroma buah-buahan disebabkan oleh berbagai ester yang bersifat volatil.
Proses timbulnya aroma ini pada bahan yang berbeda tidak sama. Pada
buah-buahan, produksi senyawa aroma ini meningkat ketika mendekati masa
klimakterik (Winarno, 2002).
Aroma buatan sering sekali ditambahkan pada minuman yang tidak
jumlahnya relatif rendah. Apabila perbandingan air yang digunakan sangat besar
dibandingkan bubur buahnya,maka perlu ditambahkan aroma untuk menutupi
kekurangan tersebut (Satuhu, 1994).
Gelatin
Gelatin adalah protein ynag diperoleh dari kolagen tak larut. Meskipun
gelatin dapat dibuat dari bermacam-macam hasil tambahan hewan, kulit
merupakan sumber umum produksi gelatin. Proses perubahan kolagen menjadi
gelatin melibatkan tiga perubahan berikut :
1. Pemutusan sejumlah terbatas ikatan peptida untuk memperpendek rantai
2. Pemutusan atau pengacauan sejumlah ikatan samping antar rantai
3. Perubahan konfigurasi rantai
Perubahan terakhir merupakan satu-satunya perubahan penting untuk perubahan
kolagen menjadi gelatin. Proses pembentuk gel kemungkinan berkaitan erat
dengan adanya gugus guanidin arginin (deMan, 1997).
Gelatin diekstrak dari jaringan tubuh hewan khususnya dari kulit dan
tulang hewani, umumnya dari tulang sapi atau hewan memamah biak lainnya.
Jaringan-jaringan tersebut diletakkan dalam larutan alkali lemah selama seminggu
kemudian dididihkan untuk mendapatkan gelatin. Gelatin merupakan bentuk gel
yang stabil pada suhu panas yang berbentuk padat pada suhu 20oC dan Cair pada
suhu 30oC, oleh karena itu gel-gel gelatin mencair didalam mulut.(Hughes, 1991). Gelatin umum tidak larut dalam air dingin, tetapi larut dalam air pada
suhu diatas 45oC, kecuali bubuk gelatin yang diperoleh dengan spray drying. Gel gelatin melembut pada suhu 25o-28oC yang mana tergantung pada sel padatannya (Tranggono, et al., 1990).
Natrium Bikarbonat (NaHCO3)
NaHCO3 akan menghasilkan gas CO2 yang dibutuhkan dalam proses
karbonasi. Proses yang paling penting dalam pembuatan minuman ini adalah
proses karbonasi karena rasa yang spesifik dan efek yang menyegarkan diberikan
oleh proses karbonasi ini. Karbonasi merupakan pelarutan CO2 di dalam air
dengan kondisi temperatur dan tekanan yang terkontrol. Penyerapan CO2 akan
semakin banyak dengan naiknya tekanan dan turunnya temperatur. Keuntungan
dari menggunakan NaHCO3 adalah relatif tidak mempengaruhi rasa, harganya
relatif murah dan tingkat kemurniannya tinggi (Dania dan Hidayat, 2005).
Natrium bikarbonat merupakan bagian terbesar sumber karbonat dengan
kelarutan yang sangat baik di dalam air, higroskopis serta tersedia secara
komersial mulai dari bentuk bubuk sampai granular (Atwawijaya, 2004).
Reaksi NaHCO3 dalam air (Winarno, 2002) adalah sebagai berikut :
NaHCO3 Na+ + HCO3
-HCO3- + H2O H2CO3 + OH
-HCO3- CO3- + H
BAHAN DAN METODE
Waktu dan Tempat Penelitian
Penelitian dilaksanakan pada bulan Juni – Juli 2010 di Laboratorium
Analisa Kimia Bahan Pangan Departemen Teknologi Pertanian Fakultas Pertanian
Universitas Sumatera Utara.
Bahan Penelitian
Bahan yang digunakan dalam penelitian ini adalah markisa dan terung
belanda yang dibeli dari Pasar Sore Padang Bulan, Medan. Bahan tambahan yang
digunakan adalah gula pasir yang diperoleh dari Pasar Sore Padang Bulan,
Medan.
Reagensia
Reagensia yang digunakan dalam penelitian ini adalah Iodin 0,01N, NaOH
0,1N, aquadest, asam sitrat, asam malat, asam tartarat, dan asam askorbat.
Alat Penelitian
Adapun alat yang digunakan dalam penelitian ini adalah timbangan,
erlenmeyer, blender, cawan aluminium, oven, pipet tetes, pH-meter, cawan petri,
Metode Penelitian (Bangun, 1991)
Penelitian ini dilakukan dengan menggunakan rancangan acak lengkap
(RAL), yang terdiri dari dua faktor, yaitu:
faktor I : jenis asam organik (A) yang terdiri dari 4 taraf, yaitu:
A1 = Asam Sitrat
A2 = Asam Malat
A3 = Asam Tartarat
A4 = Asam Askorbat
faktor II : Perbandingan sari markisa dan terung belanda (M) yang terdiri dari 4
taraf, yaitu :
M1 = 90 : 10
M2 = 80 : 20
M3 = 70 : 30
M4 = 60 : 40
Banyaknya kombinasi perlakuan atau Treatment Combination (Tc) adalah
4 x 4 = 16, maka jumlah ulangan (n) minimum adalah sebagai berikut:
Tc (n-1) ≥ 15
16 (n-1) ≥ 15
16 n ≥ 30
n ≥ 1,93...dibulatkan menjadi 2
Model Rancangan (Bangun, 1991)
Penelitian ini dilakukan dengan model rancangan acak lengkap (RAL) dua
faktorial dengan model sebagai berikut:
Ŷijk= µ + αi+ βj+ (αβ)ij+ εijk
dimana:
Ŷijk : Hasil pengamatan dari faktor A pada taraf ke-i dan faktor M pada taraf
ke-j dalam ulangan ke-k
µ : Efek nilai tengah
αi : Efek faktor A pada taraf ke-i
βj : Efek faktor M pada taraf ke-j
(αβ)ij : Efek interaksi faktor A pada taraf ke-i dan faktor M pada taraf ke-j
εijk : Efek galat dari faktor A pada taraf ke-i dan faktor M pada taraf ke-j
dalam ulangan ke-k
Apabila diperoleh hasil yang berbeda nyata dan sangat nyata maka uji
dilanjutkan dengan uji beda rataan, menggunakan uji Least Significant Range
(LSR).
Pelaksanaan Penelitian
Buah markisa dan terung belanda yang segar dipilih yang benar-benar
baik dan dibersihkan terlebih dahulu. Buah markisa dan terung belanda yang telah
dibersihkan kemudian diblansing selama 5 menit, kemudian ditiriskan lalu
dipotong, buah terung belanda yang telah dipotong dicampur dengan air masak
dengan perbandingan (1:1) lalu diambil sarinya dengan blender, sedangkan
disaring untuk mendapatkan sari buah dengan perbandingan sari markisa dan
terung belanda 90 : 10, 80 : 20, 70 : 30 dan 60 : 40 sebanyak 200g.
Campuran sari buah sebanyak 200g ditambahkan aroma markisa sebanyak
3 tetes dimasak sampai volume menjadi 1/3 volume semula lalu pemasakan
dihentikan. Kemudian ditambahkan tepung gula 100g, masing-masing asam sitrat,
malat, tartarat dan askorbat sebanyak 1% sambil terus diaduk sampai terjadi
pengkristalan. Setelah terjadi pengkristalan, dikeringkan dalam oven dengan suhu
60oC. Tepung yang terbentuk, dihaluskan dengan blender. Untuk menyeragamkan
ukuran kehalusannya, tepung tersebut diayak dengan menggunakan ayakan 80
mesh.
Tepung hasil ayakan ditambahkan Natrium bikarbonat (NaHCO3) 3%,
gelatin 3% dan acesulfame 1% lalu dicetak. Tablet effervescent yang dihasilkan
dikemas dengan menggunakan plastik dan ditutup dengan rapat dengan
menggunakan plastic clip sehingga udara tidak dapat masuk.
Pengamatan dan Pengukuran Data
Pengamatan dan pengukuran data dilakukan dengan cara analisis terhadap
parameter sebagai berikut:
1. Kadar air (%)
2. Kadar vitamin C
3. Total asam
4. Daya larut
5. pH
1. Penentuan Kadar Air (Dengan Metode Oven) (AOAC, 1984)
Ditimbang bahan sebanyak 5 gram di dalam aluminium foil yang telah
diketahui berat kosongnya. Kemudian bahan tersebut dikeringkan dalam oven
dengan suhu sekitar 105 oC – 110 oC selama 3 jam, selanjutnya didinginkan di dalam desikator selama 15 menit lalu ditimbang kembali. Setelah itu, bahan
dipanaskan kembali di dalam oven selama 30 menit, kemudian didinginkan
kembali dengan desikator selama 15 menit lalu ditimbang. Perlakuan ini diulangi
sampai diperoleh berat yang konstan.
Kadar air = x100%
awal berat
akhir berat awal
berat −
2. Penentuan Kadar Vitamin C (Ranganna, 1977)
Ditimbang bahan sebanyak 10 gram, dimasukkan ke dalam beaker glass
dan ditambahkan akuades sampai volume 100 ml. Diaduk hingga rata dan disaring
dengan kertas saring. Diambil filtrat sebanyak 10 ml dan dimasukkan ke dalam
erlenmeyer lalu ditambahkan 2-3 tetes larutan pati 1% dan dititrasi dengan Iodium
0,01N. Titrasi dianggap selesai bila telah terbentuk warna biru stabil.
Vitamin C = ml I2 0,01N x 0,88 x fp x 100
Berat Contoh
Fp = faktor pengencer (10) 1 ml I2 0,01N = 0,88 mg vitamin C
3. Penentuan Total Asam (Ranganna, 1977)
Bahan ditimbang sebanyak 10 gram, dimasukkan ke dalam beaker glass
dan ditambahkan akuades sampai volume 100 ml. Diaduk hingga merata dan
disaring dengan kertas saring dan diambil filtratnya sebanyak 10 ml dan
dimasukkan ke dalam erlenmeyer dan ditambahkan phenolptalein 1% 2-3 tetes.
Kemudian dititrasi dengan menggunakan NaOH 0,1N. Titrasi dihentikan setelah
timbul warna merah jambu yang stabil.
Total asam = ml NaOH x N NaOH x BM asam dominan x fp x 100 %
Berat contoh (gr) x 1000 x valensi asam
fp = faktor pengencer
Asam dominan = Asam sitrat (C6H8O7), BM = 192, valensi = 3
4. Penentuan Daya Larut (%) (SNI 06-1451-1989)
Ditimbang bahan sebanyak 2 gr lalu dimasukkan ke dalam labu takar 100
ml, ditambahkan air panas sampai tanda tera. Dikocok selama 1 menit dan
didiamkan selama 30 menit. Setelah itu disaring dengan menggunakan kertas
saring, kemudian diambil 10 ml dan dituang ke dalam cawan porselin yang sudah
ditimbang beratnya. Kemudian dimasukkan ke dalam oven dengan suhu pertama
80oC untuk 1 jam pertama, lalu langsung dinaikkan suhunya menjadi 90oC untuk 1 jam kedua dan dinaikkan lagi menjadi 100oC untuk 1 jam ketiga, kemudian dikeluarkan dari oven dan ditimbang. Sampel tersebut dimasukkan lagi ke dalam
oven selama 30 menit, lalu diangkat dan ditimbang. Perlakuan ini diulangi sampai
Daya larut = 10 ( A – B ) x 100% C
Keterangan : A = Berat akhir
B = Berat cawan porselin C = Berat sampel
5. Penentuan pH
Bahan berupa tablet effervescent dilarutkan dalam air kemudian diukur
pH dengan menggunakan pH-meter.
6. Penentuan Uji Organoleptik Warna, Aroma dan Rasa (numerik)
Uji organoleptik terhadap warna, aroma dan rasa terhadap tablet
effervescent yang dihasilkan dari sari markisa dan terung belanda dilakukan
kepada 10 orang panelis pada hari ke-1 dengan ketentuan uji hedonik sebagai
berikut:
Tabel 3. Skala uji hedonik terhadap warna, aroma dan rasa
Skala hedonik Skala numerik Sangat suka 4
Suka 3 Agak suka 2 Tidak suka 1
HASIL DAN PEMBAHASAN
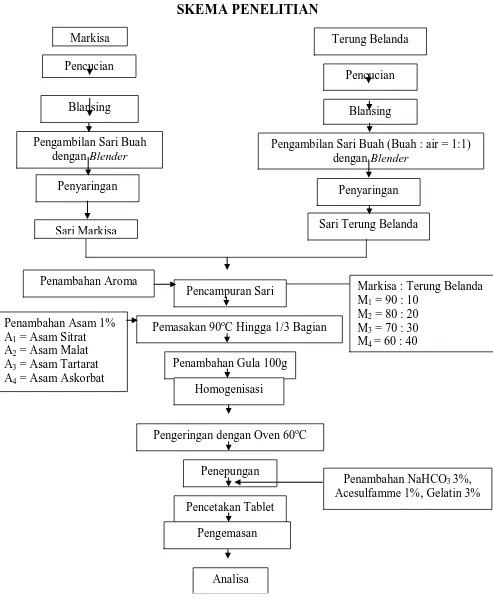
Pengambilan Sari Buah (Buah : air = 1:1) dengan Blender
Penyaringan
Sari Terung Belanda
Pencampuran Sari
Pemasakan 90oC Hingga 1/3 Bagian
Markisa : Terung Belanda
Pengeringan dengan Oven 60oC
Penepungan
Gambar 1. Skema pembuatan tablet effervescent dari sari markisa dan terung belanda Penambahan Aroma
HASIL DAN PEMBAHASAN
Pengaruh Jenis Asam Organik Terhadap Parameter yang Diamati
Secara umum hasil penelitian yang dilakukan menunjukkan bahwa jenis
asam organik memberikan pengaruh terhadap kadar air, kadar vitamin C, total
asam, daya larut, pH dan uji organoleptik (warna, aroma dan rasa) seperti pada
Tabel 4 berikut ini.
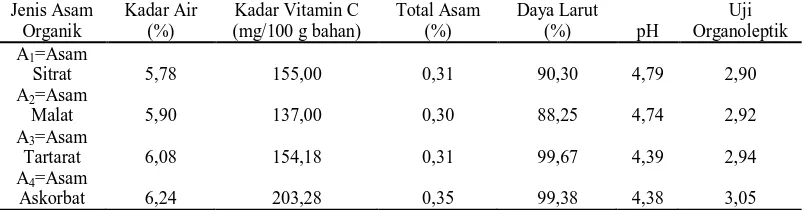
Tabel 4. Pengaruh jenis asam organik terhadap parameter yang diamati
Jenis Asam
Tabel 4 memperlihatkan bahwa jenis asam organik memberikan pengaruh
terhadap parameter yang diamati. Kadar air tertinggi terdapat pada perlakuan A4
(asam askorbat) yaitu sebesar 6,24% dan terendah pada perlakuan A1 (asam sitrat)
yaitu sebesar 5,78%. Kadar vitamin C tertinggi terdapat pada perlakuan A4 (asam
askorbat) yaitu sebesar 203,28 mg/100 g bahan dan terendah pada perlakuan A2
(Asam Malat) yaitu sebesar 137,00 mg/100 g bahan. Total asam tertinggi terdapat
pada perlakuan A4 (asam askorbat) yaitu sebesar 0,35% dan terendah pada
perlakuan A2 (asam malat) yaitu sebesar 0,30%. Daya larut tertinggi terdapat pada
perlakuan A3 (asam tartarat) yaitu sebesar 99,67% dan terendah terdapat pada
perlakuan A2 (asam malat) yaitu sebesar 88,25%. pH tertinggi terdapat pada
perlakuan A4 (asam askorbat) yaitu sebesar 4,38. Uji rganoleptik tertinggi terdapat
pada perlakuan A4 (asam askorbat) yaitu sebesar 3,05 dan terendah terdapat pada
perlakuan A1 (asam sitrat) yaitu sebesar 2,90.
Pengaruh Perbandingan Sari Markisa dan Terung Belanda terhadap Parameter yang Diamati
Secara umum hasil penelitian menunjukkan bahwa perbandingan sari
markisa dan terung belanda memberikan pengaruh terhadap kadar air, kadar
vitamin C, total asam, daya larut, pH, dan uji organoleptik (warna,aroma dan rasa)
seperti pada Tabel 5 berikut ini.
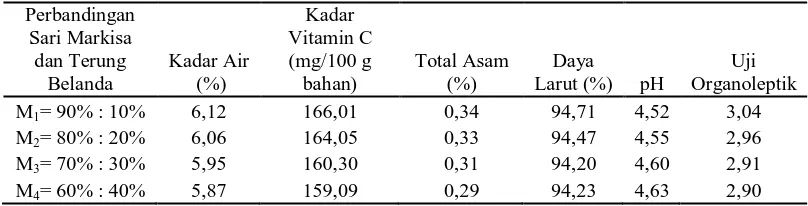
Tabel 5. Pengaruh perbandingan sari markisa dan terung belanda terhadap
Tabel 5 memperlihatkan bahwa perbandingan sari markisa dan dan terung
belanda memberikan pengaruh terhadap parameter yang diamati. Kadar air
tertinggi terdapat pada perlakuan M1 (perbandingan sari markisa dan terung
belanda 90:10%) yaitu sebesar 6,12% dan terendah terdapat pada perlakuan M4
(perbandingan sari markisa dan terung belanda 60:40%) yaitu sebesar 5,87%.
Kadar vitamin C tertinggi terdapat pada perlakuan M1 (perbandingan sari markisa
dan terung belanda 90:10%) yaitu sebesar 166,01 mg/100 g bahan dan terendah
terdapat pada perlakuan M4 (perbandingan sari markisa dan terung belanda
perlakuan M1 (perbandingan sari markisa dan terung belanda 90:10%) yaitu
sebesar 0,34% dan terendah terdapat pada perlakuan M4 (perbandingan sari
markisa dan terung belanda 60:40%) yaitu sebesar 0,29%. Daya larut tertinggi
terdapat pada perlakuan M1 (perbandingan sari markisa dan terung belanda
90:10%) yaitu sebesar 94,71% dan terendah terdapat pada perlakuan M4
(perbandingan sari markisa dan terung belanda 60:40%) yaitu sebesar 94,23%. pH
tertinggi terdapat pada perlakuan M4 (perbandingan sari markisa dan terung
belanda 60:40%) yaitu sebesar 4,63 dan terendah terdapat pada perlakuan M1
(perbandingan sari markisa dan terung belanda 90:10%) yaitu sebesar 4,52. Uji
organoleptik tertinggi terdapat pada perlakuan M1 (perbandingan sari markisa dan
terung belanda 90:10%) yaitu sebesar 3,04 dan terendah terdapat pada perlakuan
M4 (perbandingan sari markisa dan terung belanda 60:40%) yaitu sebesar 2,90.
Kadar Air (%)
Pengaruh Jenis Asam Organik terhadap Kadar Air (%)
Dari daftar analisis sidik ragam (Lampiran 1) diketahui bahwa jenis asam
askorbat memberikan pengaruh yang berbeda nyata (P<0,05) terhadap kadar air
tablet effervescent. Hasil uji LSR pengauh jenis asam organik terhadap kadar air
tablet effervescent dapat dilihat pada Tabel 6 berikit ini.
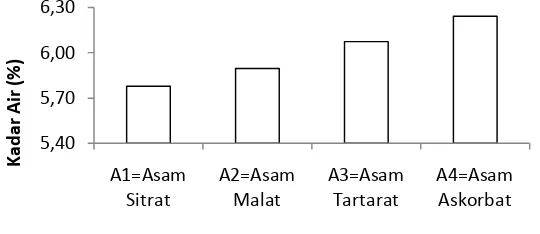
Tabel 6. Uji LSR efek utama pengaruh jenis asam organik terhadap kadar air (%)
Jarak LSR Jenis Asam Organik Rataan Notasi
0,05 0,01 0,05 0,01
- - - A1 = Asam Sitrat 5,78 b A
2 0,32 0,44 A2 = Asam Malat 5,90 b A
3 0,33 0,46 A3 = Asam Tartarat 6,08 ab A
4 0,34 0,47 A4 = Asam Askorbat 6,24 a A Keterangan : Notasi huruf yang berbeda menunjukkan pengaruh yang berbeda nyata pada taraf
5% (huruf kecil) dan berbeda sangat nyata pada taraf 1% (huruf besar)
Dari Tabel 6 dapat diketahui bahwa perlakuan A1 berbeda tidak nyata
dengan A2 dan A3, berbeda nyata dengan A4. Perlakuan A2 berbeda tidak nyata
dengan A3 dan berbeda nyata dengan A4. Perlakuan A3 berbeda tidak nyata
dengan A4. Kadar air tertinggi diperoleh pada perlakuan A4 yaitu sebesar 6,24%
dan terendah pada perlakuan A1 yaitu sebesar 5,78%.
Hubungan antara jenis asam organik terhadap kadar air tablet effervescent
dapat dilihat pada Gambar 2. Gambar 2 menunjukkan bahwa penambahan asam
sitrat menyebabkan kadar air tablet effervescent relatif rendah hal ini karena asam
sitrat dan garam natrium sangat stabil dalam keadaan tanpa air, tetapi dalam
keadaan ada air dan oksigen atau bahan pengoksidasi lainnya maka asam sitrat
menjadi sangat labil (Winarno, 1995). Penambahan asam askorbat menghasilkan
kadar air yang relatif tinggi, karena asam askorbat dapat bersifat antioksidan,
sehingga tablet effervescent lebih stabil.
Gambar 2. Hubungan antara jenis asam organik terhadap kadar air (%)
Pengaruh Perbandingan Sari Markisa dan Terung Belanda terhadap Kadar Air (%)
Dari daftar analisis sidik ragam (Lampiran 1) diketahui bahwa
perbandingan sari markisa dan terung belanda memberikan pengaruh yang
berbeda tidak nyata (P<0,05) terhadap kadar air tablet effervescent yang
dihasilkan, sehingga uji LSR tidak dilanjutkan.
Pengaruh Interaksi antara Jenis Asam Organik dan Perbandingan Sari Markisa dan Terung Belanda terhadap kadar air (%).
Dari daftar analisis sidik ragam (Lampiran 1) dapat dilihat bahwa
interaksi jenis asam organik dan dan perbandingan sari markisa dan terung
belanda memberikan pengaruh berbeda tidak nyata (P<0,05) terhadap kadar air
tablet effervescent yang dihasilkan, sehingga uji LSR tidak dilanjutkan.
Kadar Vitamin C (mg/100 g bahan)
Pengaruh Jenis Asam Organik terhadap Kadar Vitamin C (mg/100 g bahan)
Dari daftar analisis sidik ragam (Lampiran 2) diketahui bahwa jenis asam
organik memberikan pengaruh yang berbeda sangat nyata (P<0,01) terhadap kadar
vitamin C tablet effervescent. Hasil uji LSR pengaruh jenis asam organik terhadap
kadar vitamin C tablet effervescent dapat dilihat pada Tabel 7 berikut ini.
Tabel 7. Uji LSR efek utama pengaruh jenis asam organik terhadap kadar vitamin C (mg/100 g bahan)
Jarak LSR Jenis Asam Organik Rataan Notasi
0,05 0,01 0,05 0,01
- - - A1 = Asam Sitrat 155,00 b B
2 1,57 2,16 A2 = Asam Malat 137,00 c C
3 1,65 2,27 A3 = Asam Tartarat 154,18 b B
4 1,69 2,33 A4 = Asam Askorbat 203,28 a A Keterangan : Notasi huruf yang berbeda menunjukkan pengaruh yang berbeda nyata pada taraf
5% (huruf kecil) dan berbeda sangat nyata pada taraf 1% (huruf besar)
Dari Tabel 7 dapat diketahui bahwa perlakuan A1 berbeda sangat nyata
dengan A2 dan A4, dan berbeda tidak nyata dengan A3. Perlakuan A2 berbeda
sangat nyata dengan A3 dan A4. Perlakuan A3 berbeda sangat nyata dengan A4.
Kadar vitamin C tertinggi diperoleh pada perlakuan A4 yaitu sebesar 203,28
mg/100 g bahan dan terendah pada perlakuan A2 yaitu sebesar 137,00 mg/100 g
bahan.
Hubungan antara jenis asam organik dengan kadar vitamin C tablet
effervescent dapat dilihat pada Gambar 3. Gambar 3 menunjukkan bahwa tablet
effervescent yang menggunakan asam askorbat dan asam sitrat memiliki kadar
vitamin C yang tinggi karena adanya kandungan asam dapat menghambat proses
oksidasi vitamin C dalam bahan. Oksidasi tidak akan terjadi bila vitamin C
dibiarkan dalam keadaan asam (Winarno, 2002).
Gambar 3. Hubungan antara jenis asam organik terhadap kadar vitamin C (mg/100 g bahan)
Pengaruh Perbandingan Sari Markisa dan Terung Belanda terhadap Kadar Vitamin C (mg/100 g bahan)
Dari daftar analisis sidik ragam (Lampiran 2) diketahui bahwa
perbandingan sari markisa dan terung belanda memberikan pengaruh yang
berbeda sangat nyata (P<0,01) terhadap kadar vitamin C tablet effervescent. Hasil
uji LSR pengaruh perbandingan sari markisa dan terung belanda dengan kadar
vitamin C dapat dilihat pada Tabel 8 berikut ini.
Tabel 8. Uji LSR efek utama pengaruh perbandingan sari markisa dan terung belanda terhadap kadar vitamin C (mg/100 g bahan)
Jarak
LSR Perbandingan Sari
Rataan
Notasi
0,05 0,01 Markisa dan Terung
Belanda 0,05 0,01
- - - M1= 90% : 10% 166,01 a A
2 1,57 2,16 M2= 80% : 20% 164,05 b A
3 1,65 2,27 M3= 70% : 30% 160,30 c B
4 1,69 2,33 M4= 60% : 40% 159,09 c B
Keterangan : Notasi huruf yang berbeda menunjukkan pengaruh yang berbeda nyata pada taraf 5% (huruf kecil) dan berbeda sangat nyata pada taraf 1% (huruf besar)
Dari Tabel 8 dapat diketahui bahwa perlakuan M1 berbeda nyata dengan
M2, dan berbeda sangat nyata dengan M3 dan M4. Perlakuan M2 berbeda sangat
nyata dengan M3 dan M4. Perlakuan M3 berbeda tidak nyata dengan M4. Kadar
vitamin C tertinggi diperoleh pada perlakuan M1 yaitu sebesar 166,01 mg/100 g
bahan dan terendah pada perlakuan M4 yaitu sebesar 159,09 mg/100 g bahan.
Hubungan antara perbandingan sari markisa dan terung belanda dengan
kadar vitamin C tablet effervescent dapat dilihat pada Gambar 4. Gambar 4
menunjukkan bahwa semakin rendah perbandingan sari markisa maka kadar
vitamin C tablet effervescent semakin menurun. Markisa merupakan sumber
vitamin C yang tinggi yaitu sebesar 30 mg/100 g bahan (Rismunandar, 1986),
sehingga dengan menurunnya perbandingan sari markisa maka kadar vitamin C
semakin menurun.
Gambar 4. Hubungan antara perbandingan sari markisa dan terung belanda terhadap kadar vitamin C (mg/100 g bahan)
Pengaruh Interaksi Jenis Asam Organik dan Perbandingan Sari Markisa dan Terung Belanda terhadap Kadar Vitamin C (mg/100 g bahan)
Dari daftar analisis sidik ragam (Lampiran 2) dapat dilihat bahwa
interaksi jenis asam organik dan perbandingan sari markisa dan terung belanda
memberikan pengaruh yang berbeda sangat nyata (P<0,01) terhadap kadar vitamin
C tablet effervescent yang dihasilkan dapat dilihat pada Tabel 9 berikut ini.
Dari Tabel 9 di bawah dapat dilihat bahwa kombinasi perlakuan antara
jenis asam organik dan perbandingan sari markisa dan terung belanda
memberikan pengaruh yang berbeda sangat nyata terhadap kadar vitamin C.
Kadar vitamin C tertinggi terdapat pada perlakuan A4M1 yaitu sebesar 210,00
mg/100 g bahan dan terendah pada perlakuan A2M4 yaitu sebesar 133,35 mg/100
g bahan.
Tabel 9. Uji LSR efek utama interaksi jenis asam organik dan perbandingan sari markisa dan terung belanda terhadap kadar vitamin C (mg/100 g bahan)
Jarak LSR Perlakuan Rataan Notasi
Keterangan : Notasi huruf yang berbeda menunjukkan pengaruh yang berbeda nyata pada taraf 5% (huruf kecil) dan berbeda sangat nyata pada taraf 1% (huruf besar)
Hubungan interaksi antara jenis asam organik dan perbandingan sari
markisa dan terung belanda terhadap kadar vitamin C dapat dilihat pada Gambar
5. Gambar 5 menunjukkan bahwa semakin tinggi perbandingan sari markisa dan
dengan penambahan jenis asam seperti asam askorbat maka semakin tinggi kadar
vitamin C tablet effervescent. Hal ini disebabkan karena markisa mengandung
kadar vitamin C yang tinggi dan juga karena adanya kandungan asam yang dapat
menghambat proses oksidasi vitamin C pada sari markisa. Oksidasi tidak akan
terjadi bila vitamin C dibiarkan dalam keadaan asam (Winarno, 2002).
Gambar 5. Hubungan interaksi antara jenis asam organik dan perbandingan sari
markisa dan terung belanda dengan kadar vitamin C (mg/100 g bahan)
Total Asam (%)
Pengaruh Jenis Asam Organik terhadap Total Asam (%)
Dari daftar analisis sidik ragam (Lampiran 3) diketahui bahwa jenis asam
organik memberikan pengaruh yang berbeda sangat nyata (P<0,01) terhadap total
asam tablet effervescent. Hasil uji LSR pengaruh jenis asam organik terhadap
total asam tablet effervescent dapat dilihat pada Tabel 10 berikut ini.
Tabel 10. Uji LSR efek utama pengaruh jenis asam organik terhadap total asam (%) Keterangan : Notasi huruf yang berbeda menunjukkan pengaruh yang berbeda nyata pada taraf
5% (huruf kecil) dan berbeda sangat nyata pada taraf 1% (huruf besar)
Dari Tabel 10 dapat diketahui bahwa perlakuan A1 berbeda sangat nyata
dengan A2 dan A4, dan berbeda tidak nyata dengan A3. Perlakuan A2 berbeda
nyata dengan A3, dan berbeda sangat nyata dengan A4. Perlakuan A3 berbeda
0,00
Perbandingan Sari Markisa dan Terung Belanda (%)
A1=asam sitrat
A2=asam malat
A3=asam tartarat
sangat nyata dengan A4. Total asam tertinggi diperoleh pada perlakuan A4 yaitu
sebesar 0,349% dan terendah pada perlakuan A3 yaitu sebesar 0,308%.
Hubungan antara jenis asam organik terhadap total asam tablet
effervescent dapat dilihat pada Gambar 6. Gambar 6 menunjukkan bahwa dengan
penambahan asam askorbat dan asam sitrat, total asam produk meningkat, hal ini
dikarenakan asam askorbat dan asam sitrat merupakan jenis asam kuat dan juga
karena kecenderungan penambahan asam akan menyebabkan total asam
meningkat.
Gambar 6. Hubungan antara jenis asam organik terhadap total asam (%)
Pengaruh Perbandingan Sari Markisa dan Terung Belanda terhadap total asam (%)
Dari daftar analisis sidik ragam (Lampiran 3) diketahui bahwa
perbandingan sari markisa dan terung belanda memberikan pengaruh yang
berbeda sangat nyata (P<0,01) terhadap total asam tablet effervescent. Hasil uji
LSR pengaruh perbandingan sari markisa dan terung belanda terhadap total asam
tablet effervescent dapat dilihat pada Tabel 11 berikut ini.
Tabel 11. Uji LSR efek utama pengaruh perbandingan sari markisa dan terung belanda terhadap total asam (%)
Jarak
LSR Perbandingan Sari
Rataan
Notasi
0,05 0,01 Markisa dan Terung
Belanda 0,05 0,01
- - - M1= 90% : 10% 0,340 a A
2 0,010 0,013 M2= 80% : 20% 0,326 b A
3 0,010 0,014 M3= 70% : 30% 0,309 c B
4 0,011 0,015 M4= 60% : 40% 0,292 d C
Keterangan : Notasi huruf yang berbeda menunjukkan pengaruh yang berbeda nyata pada taraf 5% (huruf kecil) dan berbeda sangat nyata pada taraf 1% (huruf besar)
Dari Tabel 11 dapat diketahui bahwa perlakuan M1 berbeda nyata dengan
M2,M3, dan M4. Perlakuan M2 berbeda nyata dengan M3 dan M4. Perlakuan M3
berbeda nyata dengan M4. Total asam tertinggi diperoleh pada perlakuan M1 yaitu
sebesar 0,340% dan terendah pada perlakuan M4 yaitu sebesar 0,292%.
Hubungan antara perbandingan sari markisa dan terung belanda terhadap
total asam tablet effervescent dapt dilihat pada Gambar 7. Gambar 7 menunjukkan
semakin tinggi perbandingan sari markisa maka semakin meningkat total asam
tablet effervescent. Oksidasi tidak akan terjadi bila vitamin C dibiarkan dalam
keadaan asam (Winarno, 2002), sehingga dengan kata lain total asam markisa
sangat tinggi sehingga dengan meningkatnya perbandingan sari markisa, maka
meningkat pula total asam tablet effervescent.
Gambar 7. Hubungan antara perbandingan sari markisa dan terung belanda terhadap total asam (%)
Pengaruh Interaksi Jenis Asam Organik dan Perbandingan Sari Markisa dan Terung Belanda terhadap Total Asam (%)
Dari daftar analisis sidik ragam (Lampiran 3) dapat dilihat bahwa
interaksi jenis asam organik dan perbandingan sari markisa dan terung belanda
memberikan pengaruh berbeda tidak nyata (P<0,05) terhadap total asam tablet
effervescent yang dihasilkan, sehingga uji LSR tidak dilanjutkan.
Daya Larut (%)
Pengaruh Jenis Asam Organik terhadap Daya Larut (%)
Dari daftar analisis sidik ragam (Lampiran 4) diketahui bahwa jenis asam
organik memberikan pengaruh yang berbeda sangat nyata (P<0,01) terhadap daya
larut tablet effervescent. Hasil uji LSR pengaruh jenis asam organik terhadap daya
larut tablet effervescent dapat dilihat pada Tabel 12 berikut ini.
0,26
Perbandingan Sari Markisa dan Terung Belanda (%)
Tabel 12. Uji LSR efek utama pengaruh jenis asam organik terhadap daya larut (%)
Jarak LSR Jenis Asam Organik Rataan Notasi
0,05 0,01 0,05 0,01
- - - A1 = Asam Sitrat 90,31 b B
2 0,40 0,55 A2 = Asam Malat 88,25 c C
3 0,42 0,58 A3 = Asam Tartarat 99,67 a A
4 0,43 0,59 A4 = Asam Askorbat 99,32 a A Keterangan : Notasi huruf yang berbeda menunjukkan pengaruh yang berbeda nyata pada taraf
5% (huruf kecil) dan berbeda sangat nyata pada taraf 1% (huruf besar)
Dari Tabel 12 dapat diketahui bahwa perlakuan A1 berbeda sangat nyata
dengan A2, A3 dan A4. Perlakuan A2 berbeda sangat nyata dengan A3 dan A4.
Perlakuan A3 berbeda tidak nyata dengan A4. Daya larut tertinggi diperoleh pada
perlakuan A3 yaitu sebesar 99,67% dan terendah pada perlakuan A2 yaitu sebesar
88,25%.
Hubungan antara jenis asam organik terhadap daya larut dapat dilihat
pada Gambar 8. Gambar 8 menunjukkan bahwa daya larut tablet effervescent
sangat tinggi dengan penambahan asam tartarat. Dengan menggunakan asam
tartarat saja akan menghasilkan tablet effervescent yang lebih mudah larut dalam
air, karena kelarutan asam tartarat lebih tinggi dari pada asam yang lain
(Candra, 2008).
Gambar 8. Hubungan antara jenis asam organik terhadap daya larut (%)
Pengaruh Perbandingan Sari Markisa dan Terung Belanda terhadap Daya Larut (%)
Dari daftar analisis sidik ragam (Lampiran 4) diketahui bahwa
perbandingan sari markisa dan terung belanda memberikan pengaruh yang
berbeda tidak nyata (P<0,05) terhadap daya larut tablet effervescent yang
dihasilkan, sehingga uji LSR tidak dilanjutkan.
Pengaruh Interaksi antara Jenis Asam Organik dan Perbandingan Sari Markisa dan Terung Belanda terhadap Daya Larut (%)
Dari daftar analisis sidik ragam (Lampiran 4) dapat dilihat bahwa
interaksi antara jenis asam organik dan perbandingan sari markisa dan terung
belanda memberikan pengaruh yang berbeda tidak nyata (P<0,05) terhadap daya
larut tablet effervescent yang dihasilkan, sehingga uji LSR tidak dilanjutkan.
pH
Pengaruh Jenis Asam Organik terhadap pH
Dari daftar analisis sidik ragam (Lampiran 5) diketahui bahwa jenis asam
organik memberikan pengaruh yang berbeda sangat nyata (P<0,01) terhadap pH
tablet effervescent. Hasil uji LSR jenis asam organik terhadap pH tablet
effervescent dapat dilihat pada Tabel 13 berikut ini.
Tabel 13. Uji LSR efek utama pengaruh jenis asam organik terhadap pH
Jarak LSR Jenis Asam Organik Rataan Notasi
0,05 0,01 0,05 0,01
- - - A1 = Asam Sitrat 4,79 a A
2 0,03 0,05 A2 = Asam Malat 4,74 b B
3 0,04 0,05 A3 = Asam Tartarat 4,39 c C
4 0,04 0,05 A4 = Asam Askorbat 4,38 c C Keterangan : Notasi huruf yang berbeda menunjukkan pengaruh yang berbeda nyata pada taraf
5% (huruf kecil) dan berbeda sangat nyata pada taraf 1% (huruf besar)
Dari Tabel 13 dapat diketahui bahwa perlakuan A1 berbeda sangat nyata
dengan A2,A3, dan A4. Perlakuan A2 berbeda sangat nyata dengan A3 dan A4.
Perlakuan A3 berbeda tidak nyata dengan A4. pH tertinggi diperoleh pada
perlakuan A1 yaitu sebesar 4,79 dan terendah pada perlakuan A4 yaitu sebesar
4,38.
Hubungan antara jenis asam organik terhadap pH tablet effervescent dapat
dilihat pada Gambar 9. Gambar 9 menunjukkan bahwa pH tablet effervescent
menurun dengan penambahan asam malat dan asam askorbat. Penambahan asam
malat dapat menyebabkan penurunan pH (Candra, 2008).
Gambar 9. Hubungan antara jenis asam organik terhadap pH
Pengaruh Perbandingan Sari Markisa dan Terung Belanda terhadap pH
Dari daftar analisis sidik ragam (Lampiran 5) diketahui bahwa
perbandingan sari markisa dan terung belanda memberikan pengaruh yang
berbeda sangat nyata (P<0,01) terhadap pH tablet effervescent. Hasil uji LSR
pengaruh perbandingan sari markisa dan terung belanda terhadap pH dapat dilihat
Tabel 14. Uji LSR efek utama pengaruh perbandingan sari markisa dan terung
Keterangan : Notasi huruf yang berbeda menunjukkan pengaruh yang berbeda nyata pada taraf 5% (huruf kecil) dan berbeda sangat nyata pada taraf 1% (huruf besar)
Dari Tabel 14 dapat diketahui bahwa perlakuan M1 berbeda sangat nyata
dengan M2,M3, dan M4. Perlakuan M2 berbeda sangat nyata dengan M3 dan M4.
Perlakuan M3 berbeda tidak nyata dengan M4. pH tertinggi diperoleh pada
perlakuan M4 yaitu sebesar 4,63 dan terendah pada perlakuan M1 yaitu sebesar
4,52.
Hubungan antara perbandingan sari markisa dan terung belanda terhadap
pH tablet effervescent dapat dilihat pada Gambar 10. Gambar 10 menunjukkan
bahwa semakin tinggi perbandingan sari markisa maka semakin rendah pH hal ini
disebabkan markisa merupakan buah yang memiliki kadar vitamin C dan Asam
sitrat yang tinggi.
Gambar 10. Hubungan antara perbandingan sari markisa dan terung belanda terhadap pH
Perbandingan Sari Markisa dan Terung Belanda (%)
Pengaruh Interaksi Jenis Asam Organik dan Perbandingan Sari Markisa dan Terung Belanda terhadap pH
Dari daftar analisis sidik ragam (Lampiran 5) dapat dilihat bahwa
interaksi jenis asam organik dan perbandingan sari markisa dan terung belanda
memberikan pengaruh yang berbeda tidak nyata (P<0,05) terhadap pH tablet
effervescent yang dihasilkan sehingga uji LSR tidak dilanjutkan.
Uji Organoleptik Warna, Aroma dan Rasa (Numerik)
Pengaruh Jenis Asam Organik terhadap Uji Organoleptik Warna, Aroma dan Rasa (Numerik)
Dari daftar analisis sidik ragam (Lampiran 6) diketahui bahwa jenis asam
organik memberikan pengaruh yang berbeda sangat nyata (P<0,01) terhadap uji
organoleptik warna, aroma dan rasa tablet effervescent. Hasil uji LSR pengaruh
jenis asam organik terhadap uji organoleptik warna, aroma dan rasa tablet
effervescent dapat dilihat pada Tabel 15 berikut ini.
Tabel 15. Uji LSR efek utama pengaruh jenis asam organik terhadap uji organoleptik warna aroma dan rasa (numerik)
Jarak LSR Jenis Asam Organik Rataan Notasi
0,05 0,01 0,05 0,01
- - - A1 = Asam Sitrat 2,90 b B
2 0,06 0,08 A2 = Asam Malat 2,92 b B
3 0,06 0,08 A3 = Asam Tartarat 2,94 b B
4 0,06 0,08 A4 = Asam Askorbat 3,05 a A Keterangan : Notasi huruf yang berbeda menunjukkan pengaruh yang berbeda nyata pada taraf
5% (huruf kecil) dan berbeda sangat nyata pada taraf 1% (huruf besar)
Dari tabel 15 dapat diketahui bahwa perlakuan A1 berbeda tidak nyata
dengan A2 dan A3, dan berbeda sangat nyata dengan A4. Perlakuan A2 berbeda
tidak nyata dengan A3, dan berbeda sangat nyata dengan A4. Perlakuan A3
perlakuan A4 yaitu sebesar 3,05 dan terendah pada perlakuan A1 yaitu sebesar
2,90.
Hubungan antara jenis asam organik terhadap uji organleptik warna,
aroma dan rasa tablet effervescent dapat dilihat pada Gambar 11. Gambar 11
menunjukkan bahwa penambahan asam askorbat membuat tablet effervescent
disukai oleh panelis karena asam askorbat yang ditambahkan menghasilkan rasa
yang enak, dimana rasa asam yang dihasilkan dapat meningkatkan cita rasa dari
tablet effervescent yang dihasilkan.
Gambar 11. Hubungan antara jenis asam organik terhadap uji organoleptik warna, aroma dan rasa (numerik)
Pengaruh Perbandingan Sari Markisa dan Terung Belanda terhadap Uji Organoleptik Warna, Aroma dan Rasa (Numerik)
Dari daftar analisis sidik ragam (Lampiran 6) diketahui bahwa
perbandingan sari markisa dan terung belanda memberikan pengaruh yang
berbeda sangat nyata (P<0,01) terhadap warna, aroma dan rasa tablet effervescent.
Hasil uji LSR pengaruh perbandingan sari markisa dan terung belanda terhadap
uji organoleptik warna, aroma dan rasa tablet effervescent dapat dilihat pada tabel