ADSORPSI ASAM LEMAK BEBAS DAN ZAT WARNA
MENGGUNAKAN CAMPURAN KAOLIN-LIMBAH PADAT
TAPIOKA
VICTORIA
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
INSTITUT PERTANIAN BOGOR
ABSTRAK
VICTORIA. Adsorpsi Asam Lemak Bebas dan Zat Warna menggunakan
Campuran Kaolin-Limbah Padat Tapioka. Dibimbing oleh KOMAR SUTRIAH
dan HENNY PURWANINGSIH SUYUTI.
Adsorpsi asam lemak bebas pada minyak goreng bekas dan zat warna biru
metilena dikaji dalam penelitian ini. Hasil penelitian menunjukkan bahwa
campuran kaolin dan limbah padat tapioka merupakan adsorben asam lemak
bebas dan zat warna yang potensial. Pengaruh berbagai perlakuan aktivasi kaolin,
seperti suhu pemanasan dan penggunaan asam juga dipelajari. Hasil aktivasi
terbaik untuk kaolin yang digunakan pada adsorpsi asam lemak bebas adalah
aktivasi dengan suhu 750
°
C dilanjutkan dengan perlakuan H
2SO
430%,
sedangkan untuk adsorpsi biru metilena cukup dengan perlakuan H
2SO
430%.
Aktivasi limbah padat tapioka menggunakan H
3PO
430%. Kondisi optimum
adsorpsi, kapasitas adsorpsi, dan efisiensi penjerapan adsorben campuran kaolin
dan limbah padat tapioka menunjukkan hasil yang berbeda dan khas untuk setiap
jenis adsorbat yang digunakan. Adsorpsi asam lemak bebas dicapai pada waktu 90
menit menggunakan adsorben sebanyak 1 gram dengan nisbah campuran kaolin
dan limbah padat tapioka yang telah diaktivasi adalah 25:75 (1:3). Sementara itu,
adsorpsi biru metilena dicapai pada waktu 30 menit dengan nisbah campuran
kaolin dan limbah padat tapioka yang telah diaktivasi adalah 75:25 (3:1) dengan
jumlah adsorben yang sama. Hasil penelitian menunjukkan bahwa tipe isoterm
untuk adsorpsi asam lemak bebas adalah isoterm Freundlich, sedangkan untuk
adsorpsi biru metilena adalah isoterm Langmuir.
ABSTRACT
VICTORIA. Free Fatty Acid and Dye Adsorption Using Mixture of Activated
Kaolin and Tapioca Solid Waste. Supervised by KOMAR SUTRIAH and
HENNY PURWANINGSIH SUYUTI
Adsorption of free fatty acids in used cooking oil and methylene blue dye is
studied. The results showed that the mixture of kaolin and tapioca solid waste is a
potential adsorbent for the adsorption free fatty acids and dyes. The effect of
kaolin activation treatment, such as heating temperature and the use of acid is also
studied. The best activation results for the kaolin activation used in the free fatty
acid adsorption was heating treatment at 750
°
C followed by treatment with
H
2SO
430%, whereas for methylene blue adsorption by acid treatment only.
Activation of tapioca solid waste was using 30% H
3PO
4treatment. Optimum
ADSORPSI ASAM LEMAK BEBAS DAN ZAT WARNA
MENGGUNAKAN CAMPURAN KAOLIN-LIMBAH PADAT
TAPIOKA
VICTORIA
Skripsi
sebagai salah satu syarat untuk memperoleh gelar
Sarjana Sains pada
Departemen Kimia
DEPARTEMEN ILMU KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
INSTITUT PERTANIAN BOGOR
Judul : Adsorpsi Asam Lemak Bebas dan Zat Warna menggunakan
Campuran Kaolin-Limbah Padat Tapioka
Nama
: Victoria
NIM
: G44050091
Menyetujui
Pembimbing I,
Drs. Komar Sutriah, M.S.
NIP 19630705 199103 1 004
Pembimbing II,
Henny Purwaningsih Suyuti, S.Si, M.Si.
NIP 19741201 200501 2 001
Mengetahui
Ketua Departemen,
Prof. Dr. Ir. Tun Tedja Irawadi, M.S.
NIP 19501227 197603 2 002
PRAKATA
Puji dan syukur penulis panjatkan ke hadirat Tuhan Yang Maha Esa atas
rahmat dan karunia-Nya sehingga penulis dapat menyelesaikan karya ilmiah ini.
Karya ilmiah ini disusun berdasarkan penelitian yang dilaksanakan pada bulan
April sampai Oktober 2009 di Laboratorium Kimia Fisik, Departemen Kimia
FMIPA IPB, dan Laboratorium Terpadu, IPB. Karya ilmiah yang berjudul
Adsorpsi Asam Lemak Bebas dan Zat Warna menggunakan Campuran
Kaolin-Limbah Padat Tapioka ini merupakan salah satu syarat untuk memperoleh gelar
sarjana sains pada Departemen Kimia FMIPA IPB.
Penulis mengucapkan terima kasih kepada Bapak Drs. Komar Sutriah,
M.S. selaku pembimbing pertama dan Ibu Henny Purwaningsih Suyuti, S.Si,
M.Si. selaku pembimbing kedua yang telah memberikan arahan, saran, dan
dorongan selama pelaksanaan penelitian dan penulisan karya ilmiah ini.
Ungkapan terima kasih penulis berikan kepada keluarga tercinta, Bapak, Ibu, dan
adik-adikku (Ita, Risma, dan Eben) yang selalu memberikan semangat, doa, dan
kasih sayang. Terima kasih juga kepada Bapak Nano, Ibu Ai, Bapak Ismail,
Bapak Eman atas fasilitas dan bantuan yang diberikan selama penelitian. Ucapan
terima kasih juga disampaikan kepada
Mbak
Nisha, Dwi, Rita, Mega, Ema, Dian,
Jayanti, Ired, Aurel, dan Maria yang turut membantu, memberikan semangat dan
dukungannya dalam penyusunan karya ilmiah.
Semoga karya ilmiah ini dapat bermanfaat bagi ilmu pengetahuan.
Bogor, Desember 2009
RIWAYAT HIDUP
DAFTAR ISI
Halaman
DAFTAR TABEL ... viii
DAFTAR GAMBAR ... viii
DAFTAR LAMPIRAN ... ix
PENDAHULUAN ...
1
TINJAUAN PUSTAKA
Kaolin ...
2
Limbah Padat Tapioka ...
2
Selulosa ...
3
Adsorpsi ...
3
Isoterm Adsorpsi ...
3
Minyak Goreng ...
4
Asam Lemak Bebas...
4
Zat Warna ...
5
BAHAN DAN METODE
Bahan dan Alat ...
5
Metode...
5
HASIL DAN PEMBAHASAN
Kondisi Optimum Adsorpsi Asam Lemak Bebas ...
8
Kondisi Optimum Adsorpsi Zat Warna ...
9
Kapasitas Adsorpsi dan Efisiensi Penjerapan Adsorben Lain ... 10
Isoterm Adsorpsi ... 11
SIMPULAN DAN SARAN
Simpulan ... 12
Saran ... 13
DAFTAR PUSTAKA ... 13
DAFTAR TABEL
Halaman
1 Komposisi kimia limbah padat tapioka ...
2
2 Komposisi asam lemak minyak kelapa sawit ...
5
3 Modifikasi contoh ...
6
4 Data adsorpsi asam lemak bebas dengan berbagai jenis adsorben ... 11
5 Data adsorpsi biru metilena dengan berbagai jenis adsorben ... 11
6 Nilai konstanta n dan k dari persamaan Freundlich ... 12
7 Nilai konstanta
α
dan
β
dari persamaan Langmuir ... 12
DAFTAR GAMBAR
Halaman
1 Serbuk kaolin ...
2
2 Struktur kaolinit ...
2
3 Limbah padat tapioka ...
2
4 Struktur selulosa ...
3
5 Struktur trigliserida ...
4
6 Struktur biru metilena ...
5
7 Skema interaksi proton dengan struktur kaolin ...
8
8 Waktu optimum adsorpsi asam lemak bebas ...
8
9 Bobot optimum adsorpsi asam lemak bebas ...
8
10 Perlakuan optimum adsorpsi asam lemak bebas ...
9
11 Waktu optimum adsorpsi biru metilena ... 10
12 Bobot optimum adsorpsi biru metilena ... 10
13 Perlakuan optimum adsorpsi biru metilena ... 10
14 Isoterm Langmuir adsorpsi asam lemak bebas ... 11
15 Isoterm Freundlich adsorpsi asam lemak bebas ... 11
16 Isoterm Langmuir adsorpsi biru metilena ... 12
DAFTAR LAMPIRAN
Halaman
1 Diagram alir penelitian ... 16
2 Data optimasi waktu kontak terhadap asam lemak bebas ... 17
3 Data optimasi bobot adsorben terhadap asam lemak bebas ... 18
4 Data optimasi perlakuan adsorben terhadap asam lemak bebas ... 18
5 Data adsorpsi asam lemak bebas dengan adsorben lain ... 20
6 Data asam oleat sebelum dijerap ... 20
7 Data asam oleat setelah dijerap ... 20
8 Data efisiensi penjerapan ... 20
9 Data isoterm Langmuir dan Freundlich untuk adorpsi asam lemak bebas ... 21
10 Data kadar asam lemak bebas pada minyak goreng bekas ... 21
11 Data kadar asam lemak bebas pada minyak goreng baru ... 21
12 Data optimasi waktu kontak adsorben terhadap biru metilena ... 21
13 Data optimasi bobot adsorben terhadap biru metilena ... 22
14 Data optimasi perlakuan adsorben terhadap biru metilena ... 22
15 Data adsorpsi biru metilena dengan adsorben lain ... 23
PENDAHULUAN
Kaolin adalah salah satu golongan mineral aluminasilikat. Kelompok mineral kaolin meliputi kaolinit, nakrit, dikit, dan haloisit. Kaolinit ditemukan dalam jumlah yang paling banyak dalam mineral kelompok kaolin. Kaolinit merupakan mineral liat tipe 1:1 yang paling banyak dijumpai di Indonesia. Mineral kaolinit umumnya terbentuk pada lingkungan reaksi tanah masam dengan drainase tanah yang relatif baik. Kaolinit dapat terbentuk oleh Al dan Si yang dilepaskan oleh mineral-mineral primer ataupun sekunder (Prasetyo et al. 2001). Selain digunakan dalam pengolahan limbah, kaolin juga dapat digunakan sebagai adsorben pada tahap pemucatan (bleaching) dalam pemurnian minyak goreng.
Selain jenis adsorben dari golongan mineral aluminasilikat, saat ini banyak digunakan adsorben yang mengandung selulosa, salah satunya adalah limbah padat tapioka yang dihasilkan pada saat pembuatan tepung tapioka. Ketersediaan limbah padat tapioka terus meningkat sejalan dengan meningkatnya produksi tapioka. Limbah padat tapioka diketahui sebagai bahan sumber energi yang memiliki kadar protein kasar rendah, tetapi kaya akan karbohidrat. Oleh karena itu, limbah padat tapioka dapat digunakan sebagai pakan ternak. Beberapa penelitian tentang pemanfaatan limbah padat tapioka telah dilakukan (Tjiptadi 1985, Rinaldy 1987, Ali 2008, dan Widiarto et al. 2008). Namun demikian, pemanfaatan limbah padat tapioka sebagai adsorben dalam pengolahan minyak goreng bekas belum banyak dilakukan.
Kebutuhan Indonesia terhadap minyak goreng sebagai bahan untuk mengolah makanan semakin meningkat. Penggunaan minyak berulang kali sangat membahayakan kesehatan. Hal ini dikarenakan selain semakin banyaknya kotoran yang terkandung dalam minyak goreng akibat penggorengan bahan makanan sebelumnya dan semakin banyaknya senyawa-senyawa asam karboksilat bebas di dalam minyak serta warna minyak goreng yang semakin tidak jernih jika dipakai berulang kali. Selama proses penggorengan, terjadi pemanasan dan minyak berubah menjadi berwarna gelap karena terjadinya reaksi kimia. Pembuangan minyak goreng bekas secara langsung ke lingkungan akan menimbulkan pencemaran (Buchori dan Widayat 2009).
Minyak goreng bekas tersebut tidak disarankan untuk digunakan kembali dan harus segera diganti dengan minyak goreng yang baru. Frekuensi penggantian minyak goreng ini menjadi salah satu kendala yang dihadapi industri makanan karena akan mempengaruhi biaya operasional. Salah satu cara mengatasi masalah tersebut adalah mengolah minyak goreng bekas dengan metode adsorpsi. Suhu yang tinggi pada proses penggorengan yang berulang-ulang ini akan menghasilkan asam lemak bebas. Asam lemak bebas terbentuk akibat panas dan keberadaan air dari bahan yang akan digoreng sehingga terjadi reaksi hidrolisis (Ketaren 1986). Kadar asam lemak bebas merupakan karakteristik yang paling umum untuk mengendalikan mutu minyak goreng. Minyak goreng dengan kualitas yang baik mengandung asam lemak bebas maksimal 0.6 mg KOH/g (SNI 01-3741-2002). Dengan demikian diperlukan adanya upaya untuk menghilangkan asam lemak bebas yang terdapat dalam minyak goreng bekas tersebut, yaitu dengan cara menjerap asam lemak bebas (Romaria 2008).
Permasalahan industri di Indonesia tidak hanya minyak goreng bekas yang digunakan oleh industri makanan, contoh lainnya adalah masalah limbah yang mengandung zat warna. Masuknya limbah zat warna ke perairan akan mencemari lingkungan. Pengelolaan dan pengolahan limbah tersebut sangat diperlukan untuk mencegah kerusakan lingkungan. Metode yang umum digunakan untuk pengolahan limbah zat warna adalah metode adsorpsi. Beberapa penelitian yang terkait dengan adsorpsi limbah zat warna telah banyak dilakukan di antaranya pemanfaatan tongkol jagung sebagai biosorben zat warna biru metilena (Fahrizal 2008), biosorpsi biru metilena oleh kulit buah kakao (Alamsyah 2007), dan adsorpsi biru metilena oleh kaolin (Ghosh dan Bhattacharyya 2002).
TINJAUAN PUSTAKA
Kaolin
Kaolin termasuk jenis mineral liatdengan rumus kimia Al2O3.2SiO2.2H2O. Kaolin
merupakan batuan yang tersusun dari material lempung atau mineral liat dengan kandungan besi yang rendah dan umumnya berwarna putih atau agak keputihan (Gambar 1).
Gambar 1 Serbuk kaolin.
Kelompok mineral kaolin meliputi kaolinit, nakrit, dikit, dan haloisit. Kaolinit, nakrit, dan dikit mempunyai komposisi kimia yang ideal, yaitu Al2Si2O5(OH)4. Ketiga
mineral tersebut dibedakan oleh susunan lapisan 1:1. Pengertian lapisan 1:1 adalah untuk setiap satuan mineral terdiri atas satu lapisan oksida-Si (lapisan silikat) dan satu lapisan hidroksioksida-Al (lapisan aluminat). Satuan-satuan ini berikatan kuat sesamanya dengan ikatan hidrogen dan van der Waals. Hal ini mengakibatkan kation atau anion dan molekul air tidak dapat masuk ke lapisan silikat maupun aluminat sehingga efektivitas penjerapannya terbatas hanya di permukaan saja. Sifat penukar kation atau anion hanya berasal dari bagian ujung mineral yang mengalami pemutusan/pematahan (Muhdarina dan Linggawati 2003).
Dalam kelompok mineral kaolin, kaolinit ditemukan dalam jumlah yang paling banyak. Komposisi kimia dari kaolinit, yaitu SiO2
46.54%, Al2O3 39.50%, dan H2O 13.96%
(Sarapaa dan Al-Ani 2008). Molekul air dalam struktur kristal kaolinit dapat ditemukan pada ruang antarlapisannya. Struktur kaolin disajikan pada Gambar 2.
Gambar 2 Struktur kaolinit.
Bagian permukaan dari kristal kaolinit mempunyai muatan negatif yang tetap dan tidak bergantung pH (permanent charge).
Muatan negatif tersebut berasal dari subtitusi atom dalam struktur kristal yang tidak mempengaruhi struktur kristal tersebut, misalnya dengan adanya atom Al yang bermuatan +3 yang menggantikan atom Si yang bermuatan +4 menyebabkan kerangka kaolinit kekurangan muatan positif atau kelebihan muatan negatif (Faruqi et al. 1967).
Limbah Padat Tapioka
Proses pengolahan ubi kayu (Manihot utilissima) menjadi tepung tapioka akan menghasilkan limbah padat dan hasil buangan berupa cairan yang disebut sludge. Limbah padat tapioka merupakan limbah padat industri tapioka (solid waste cassava) yang jumlahnya dapat mencapai 30% (b/b) dari bahan baku (Gambar 3). Potensi limbah padat tapioka didukung oleh kadar selulosa yang dapat mencapai 65.9% (Widiarto et al. 2008). Berdasarkan kandungan ini, limbah padat tapioka mempunyai potensi yang besar untuk dimanfaatkan sebagai sumber selulosa maupun untuk menghasilkan produk turunannya.
Gambar 3 Limbah padat tapioka.
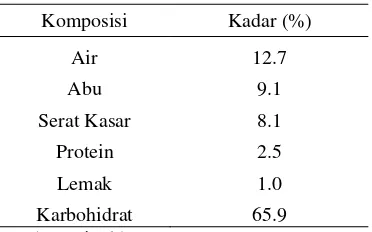
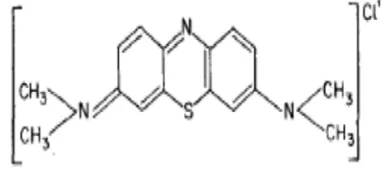
Komponen penting yang terdapat dalam limbah padat tapioka adalah pati dan serat kasar. Komposisi kimia limbah padat tapioka sangat bervariasi tergantung pada mutu bahan baku, efisiensi proses ekstraksi pati, dan penanganan limbah padat tapioka itu sendiri (Tjiptadi 1985). Komposisi kimia limbah padat tapioka berbeda untuk setiap daerah asal dan jenis ubi kayu, serta teknologi yang digunakan dan penanganan limbah padatnya. Komposisi kimia limbah padat tapioka dapat dilihat pada Tabel 1.
Tabel 1 Komposisi kimia limbah padat tapioka
Komposisi Kadar (%)
Air 12.7
Abu 9.1
Serat Kasar 8.1
Protein 2.5
Lemak 1.0
Karbohidrat 65.9
Selulosa
Selulosa merupakan komponen struktural utama tanaman dan senyawa organik yang melimpah di bumi. Selulosa terdiri atas rantai panjang unit-unit glukosa yang terikat dengan ikatan 1- 4β-glukosida. Gambar 4 menyajikan struktur selulosa.
Gambar 4 Struktur selulosa.
Berdasarkan strukturnya, selulosa mempunyai potensi yang cukup besar untuk dijadikan sebagai penjerap karena gugus -OH yang terikat dapat berinteraksi dengan komponen adsorbat. Adanya gugus -OH, pada selulosa menyebabkan adsorben menjadi polar. Dengan demikian selulosa lebih kuat menjerap zat yang bersifat polar dari pada zat yang kurang polar (Sukarta 2008).
Adsorpsi
Adsorpsi merupakan peristiwa terakumulasinya partikel pada suatu permukaan (Atkins 1999). Adsorpsi terjadi karena adanya gaya tarik menarik antarmolekul adsorbat dengan tempat-tempat aktif di permukaan adsorben. Adsorbat adalah senyawa yang terjerap atau senyawa yang akan dipisahkan dari pelarutnya, sedangkan adsorben adalah merupakan suatu media penjerap. Menurut Reynolds yang diacu dalam Wijaya (2008), proses adsorpsi dapat digambarkan sebagai proses saat molekul meninggalkan larutan dan menempel pada permukaan zat adsorben.
Mekanisme penjerapan tersebut dapat dibedakan menjadi dua, yaitu adsorpsi secara fisika (fisisorpsi) dan adsorpsi secara kimia (kimisorpsi). Pada proses fisisorpsi, gaya yang mengikat adsorbat oleh adsorben adalah gaya-gaya van der Waals, sedangkan pada proses adsorpsi kimia terjadi interaksi adsorbat dengan adsorben melalui pembentukan ikatan kimia (Sukarta 2008). Kimisorpsi terjadi dengan diawali adsorpsi secara fisika (fisisorpsi), yaitu partikel-partikel adsorbat mendekat ke permukaan adsorben melalui gaya van der Waals atau melalui ikatan hidrogen, kemudian diikuti oleh adsorpsi
kimia yang terjadi setelah adsorpsi fisika. Pada adsorpsi kimia, partikel yang melekat pada permukaan akan membentuk ikatan kimia (Atkins 1999).
Faktor-faktor yang mempengaruhi adsorpsi, yaitu sifat fisika dan kimia adsorben seperti luas permukaan, pori-pori, dan komposisi kimia. Selain itu juga dipengaruhi sifat fisika dan kimia adsorbat, seperti ukuran molekul, polaritas molekul, komposisi kimia, konsentrasi adsorbat dalam fase cair, sifat fase cair, serta lamanya proses adsorpsi tersebut berlangsung. Semakin kecil ukuran partikel, maka semakin besar luas permukaan padatan persatuan volume tertentu sehingga akan semakin banyak zat yang diadsorpsi (Atkins 1999). Adsorben yang baik memiliki kapasitas adsorpsi dan persentase efisiensi penjerapan yang tinggi. Kapasitas adsorpsi dapat dihitung dengan menggunakan rumus:
Persentase penjerapan dapat dihitung dengan mengunakan rumus:
Keterangan:
Q = kapasitas adsorpsi (mg/g)
V = volume larutan (l)
Co = konsentrasi awal (mg/l) C = konsentrasi akhir (mg/l)
m = massa (g)
Isoterm Adsorpsi
Isoterm adsorpsi merupakan fungsi konsentrasi zat terlarut yang terjerap pada padatan terhadap konsentrasi larutan. Tipe isoterm adsorpsi dapat digunakan untuk mempelajari mekanisme adsorpsi. Adsorpsi fase cair-padat pada umumnya mengikuti tipe isoterm Freundlich dan Langmuir (Atkins 1999).
Isoterm Adsorpsi Langmuir
sehingga permukaan adsorben dapat mengikat adsorbat dengan ikatan kimia. Persamaan isoterm adsorpsi Langmuir dapat diturunkan secara teoritis dengan menganggap terjadinya kesetimbangan antara molekul-molekul zat yang diadsorpsi pada permukaan adsorben dengan molekul-molekul zat yang tidak teradsorpsi sebagai berikut:
Kostanta α dan β dapat ditemukan dari kurva
hubungan terhadap c dengan
persamaan:
Keterangan:
x/m = massa adsorbat yang teradsorpsi per gram adsorben
c = konsentrasi kesetimbangan adsorbat dalam larutan setelah adsorpsi (ppm)
α,β = konstanta empiris
Isoterm Adsorpsi Freundlich
Isoterm Freundlich merupakan proses adsorpsi yang terjadi secara fisisorpsi banyak lapisan. Fisisorpsi adalah adsorpsi yang hanya melibatkan gaya intermolekul dan ikatannya lemah. Persamaan isoterm adsorpsi Freundlich didasarkan atas terbentuknya lapisan monolayer dari molekul-molekul adsorbat pada permukaan adsorben. Namun pada adsorpsi Freundlich tapak-tapak aktif pada permukaan adsorben bersifat heterogen.
Menurut Atkins (1999), pada proses adsorpsi zat terlarut pada permukaan padatan diterapkan isoterm Freundlich yang diturunkan secara empiris dengan bentuk persamaan:
Apabila dilogaritmakan, persamaan isoterm Freundlich dapat dituliskan sebagai berikut:
Keterangan:
x/m = massa adsorbat yang teradsorpsi per gram adsorben
c = konsentrasi kesetimbangan adsorbat dalam larutan setelah adsorpsi (ppm)
k,n = konstanta empiris
Minyak Goreng
Minyak merupakan trigliserida yang tersusun atas tiga unit asam lemak, berwujud cair pada suhu kamar (25°C), dan lebih banyak mengandung asam lemak tidak jenuh sehingga mudah mengalami oksidasi. Minyak yang berbentuk padat biasa disebut dengan lemak. Minyak dapat bersumber dari tanaman, misalnya minyak zaitun, minyak jagung, minyak kelapa, dan minyak bunga matahari. Minyak dapat juga bersumber dari hewan, misalnya minyak ikan sardin, minyak ikan paus dan lain-lain (Ketaren, 1986). Minyak sayur adalah jenis minyak yang digunakan dalam pengolahan bahan pangan, biasanya terbuat dari kelapa maupun kelapa sawit.
Trigliserida merupakan komponen yang relatif sederhana, yaitu ester dari tiga unit asam lemak dan satu unit gliserol. Trigliserida atau gliserida yang terbentuk dari asam lemak jenuh dengan rantai yang panjang, memiliki titik didih atau titik cair lebih tinggi daripada asam lemak jenuh rantai pendek. Rumus molekul dari trigliserida adalah C3H5(COOR)3
(Gambar 5).
Gambar 5 Struktur trigliserida.
Jenis minyak yang digunakan untuk menggoreng biasanya termasuk minyak nabati seperti minyak kelapa, minyak kelapa sawit, dan minyak kacang tanah yang mengandung asam lemak tak jenuh terutama asam oleat dan linoleat. Minyak goreng yang dihasilkan dari bahan yang berbeda mempunyai stabilitas yang berbeda. Faktor yang mempengaruhi stabilitas minyak goreng di antaranya adalah derajat ketidakjenuhan asam lemak, penyebaran ikatan rangkap, dan keberadaan antioksidan yang terdapat secara alami ataupun yang sengaja ditambahkan.
Asam Lemak Bebas
untuk semua lipid pada makhluk hidup. Asam lemak merupakan rantai hidrokarbon yang setiap atom karbonnya mengikat satu atau dua atom hidrogen, kecuali atom karbon terminal mengikat tiga atom hidrogen, sedangkan atom karbon terminal lainnya mengikat gugus karboksil (Pasaribu 2004). Komposisi asam lemak yang terdapat dalam minyak kelapa sawit ditampilkan pada Tabel 2.
Tabel 2 Komposisi asam lemak minyak kelapa sawit
Asam Lemak Jumlah (%)
Asam Kaprilat -
Asam Kaproat -
Asam Miristat 1.1-2.5
Asam Palmitat 40-46
Asam Stearat 3.6-4.7
Asam Oleat 30-45
Asam Laurat -
Asam linolenat 7-11
Sumber : Pasaribu (2004)
Secara alami asam lemak bisa berbentuk bebas (karena lemak yang terhidrolisis) maupun terikat sebagai gliserida. Asam lemak jenuh merupakan asam lemak yang mengandung ikatan tunggal pada rantai hidrokarbonnya. Asam lemak jenuh mempunyai rantai zig-zig yang dapat cocok satu sama lain, sehingga gaya tarik vanderwalls tinggi, sehingga biasanya berwujud padat, sedangkan asam lemak tak jenuh merupakan asam lemak yang mengandung satu ikatan rangkap pada rantai hidrokarbonnya (Herlina dan Ginting 2002).
Hidrolisis merupakan reaksi yang terbentuk antara air dari produk dengan minyak goreng yang dapat membentuk asam lemak bebas. Kecepatan pembentukan asam lemak bebas sangat tergantung dari beberapa faktor, yaitu jumlah air yang dikandung, suhu penggorengan yang digunakan selama proses, kecepatan dari oil turnover system, jumlah partikel/remah-remah dari produk yang digoreng, dan bilangan heating/coolingcycles
dari minyak.
Netralisasi merupakan suatu proses untuk menghilangkan asam lemak bebas dari minyak dengan cara mereaksikan asam lemak bebas dengan basa. Netralisasi dilakukan untuk mengurangi asam lemak bebas, meningkatkan rasa, dan memperbaiki fisik minyak. Netralisasi dilakukan dengan mereaksikan NaOH dengan asam lemak bebas
sehingga membentuk endapan minyak tak larut yang dikenal dengan sabun (soapstock) (Ritonga 2004).
Zat Warna
Zat warna tekstil merupakan senyawa organik yang keberadaannya dalam perairan dapat mengganggu ekosistem di dalamnya sebelum dibuang ke perairan. Limbah cair yang berwarna ini akan diproses terlebih dahulu sampai konsentrasinya cukup aman jika berada di perairan.
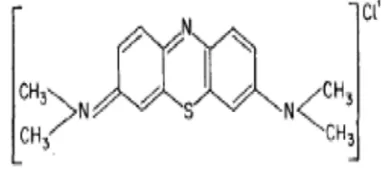
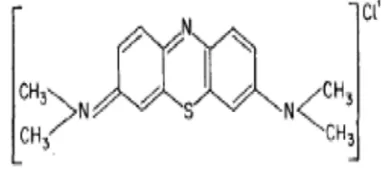
Biru metilena (C16H18ClN3S) yang juga
dikenal sebagai tetrametiltionin merupakan bahan pewarna dasar yang sangat penting dan relatif murah dibandingkan pewarna lainnya (Gambar 6). Biru metilena adalah senyawa kimia berwarna biru dengan bobot molekul 319.86 g/mol. Analisis kadar biru metilena umumnya dilakukan dengan spektroskopi sinar tampak pada kisaran panjang gelombang 609-668 nm.
Gambar 6 Struktur biru metilena.
Biru metilena banyak digunakan pada penelitian bakteri, sebagai pereaksi kimia, campuran indikator, antidot, dan racun sianida (Windholz et al. 1983). Selain itu juga dapat digunakan sebagai pewarna kain dan pewarnaan asam nukleat menggantikan pewarna etidium bromida (Sigma 1996).
BAHAN DAN METODE
Bahan dan Alat
Alat-alat yang digunakan antara lain spektronik 20D+ model Thermo Elektron Coorporation. Bahan-bahan yang digunakan dalam penelitian adalah minyak goreng bekas, kaolin asal Belitung, dan limbah padat tapioka dari PT Sari Alam.
Metode
aktivasi kaolin dan limbah padat tapioka. Tahap ketiga adalah pembuatan campuran adsorben kaolin dan limbah padat tapioka. Tahap keempat adalah optimasi waktu kontak dan bobot adsorben pada adsorpsi asam lemak bebas dan biru metilena. Tahap kelima adalah penentuan tipe isoterm adsopsi asam lemak bebas dan biru metilena.
Tahap Pertama
Perlakuan Awal Kaolin. Serbuk kaolin dicuci dengan akuades dan dikeringkan pada suhu 105 °C selama 3 jam dalam oven, kemudian dihancurkan dan diayak sehingga berukuran ± 200 mesh.
Perlakuan Awal Limbah Padat Tapioka. Serbuk limbah padat tapioka dicuci dengan akuades dan dikeringkan pada 40 °C selama 24 jam dalam oven. Contoh yang telah dikeringkan kemudian dihancurkan dan diayak sehingga berukuran ± 200 mesh.
Tahap Kedua
Aktivasi Kaolin dengan Pemanasan Suhu Tinggi (Arikan et al. 2009). Sebanyak 30 gram kaolin dimasukkan ke dalam cawan porselen, lalu dikalsinasi dalam tanur pada suhu 750 °C selama 2 jam. Kaolin tersebut disimpan dalam desikator untuk pemakaian selanjutnya (Contoh A).
Aktivasi Kaolin dengan Cara Pemanasan dengan Uap Air. Sebanyak 30 gram kaolin dipanaskan dalam autoklaf Contoh kaolin kemudian disimpan dalam desikator untuk pemakaian selanjutnya (Contoh B).
Aktivasi Kaolin dengan Cara Kimia (Modifikasi Koyuncu et al. 2007). Kaolin ditimbang sebanyak 30 gram ke dalam labu bulat dan ditambahkan sebanyak 250 ml larutan H2SO4 30%. Larutan campuran
tersebut digojok dengan pengaduk magnet dan dipanaskan pada suhu 90-100 °C selama 6 jam, kemudian didinginkan dan disaring dengan vakum sehingga dihasilkan residu padat. Kaolin tersebut dicuci beberapa kali dengan akuades untuk mengeluarkan asam, untuk mengetahui adanya ion SO42- dideteksi
menggunakan larutan BaCl2. Kaolin yang
telah dicuci tersebut, dikeringkan pada suhu 105 °C selama 3 jam. Contoh kaolin kemudian disimpan dalam desikator untuk pemakaian selanjutnya (Contoh C).
Aktivasi Kaolin dengan Pemanasan Suhu Tinggi dan Uap Air. Pertama-tama, contoh
kaolin dipanaskan mengikuti metode Arikan
et al. (2009). Selanjutnya kaolin yang telah dipanaskan tersebut dipanaskan kembali dengan autoklaf. Contoh kaolin hasil aktivasi dua kali pemanasan ini selanjutnya disebut Contoh D.
Aktivasi Kaolin dengan Cara Pemanasan Suhu Tinggi dan Kimia. Pertama-tama, contoh kaolin dipanaskan mengikuti metode Arikan et al. (2009). Selanjutnya kaolin yang telah dipanaskan tersebut diaktivasi kembali dengan cara kimia menggunakan asam sesuai metode modifikasi Koyuncu et al. (2007). Contoh ini selanjutnya disebut Contoh E
Aktivasi Limbah Padat Tapioka (Melisya 2009). Limbah padat tapioka ditimbang sebanyak 10 gram ke dalam Erlenmeyer dan ditambahkan sebanyak 50 ml H3PO4 30%.
Campuran tersebut digojok selama 6 jam, kemudian disaring dengan vakum sehingga dihasilkan residu padat. Limbah padat tapioka yang telah diaktivasi tersebut dicuci beberapa waktu dengan akuades untuk mengeluarkan asam, setelah itu dikeringkan pada suhu 40 ºC selama 24 jam.
Tahap Ketiga
Pembuatan Adsorben Kaolin-Limbah Padat Tapioka (Modifikasi dari Chen & Evans 2005). Kaolin yang telah diaktivasi dengan 5 macam variasi perlakuan (Contoh A, B, C, D, dan E) dicampur hingga merata dengan sejumlah limbah padat tapioka yang juga telah diaktivasi dengan asam fosfat. Jumlah total kaolin dan limbah padat tapioka sebanyak 20 gram dengan nisbah kaolin:limbah padat tapioka, yaitu 75:25, 50:50, dan 25:75 (Tabel 3).
Tabel 3 Modifikasi contoh
Contoh Kaolin
Nisbah Kaolin:Limbah Padat Tapioka
75:25 50:50 25:75
A A1 A2 A3
B B1 B2 B3
C C1 C2 C3
D D1 D2 D3
E E1 E2 E3
Tahap Keempat
Adsorpsi Asam Lemak Bebas
fenolftalein, kemudian dititrasi dengan larutan NaOH 0.05 N yang telah distandarisasi sampai warna merah merah muda tidak berubah selama 15 detik. Penetapan bilangan asam lemak bebas dilakukan duplo, serta dilakukan penetapan blanko.
Penentuan Waktu Optimum Adsorpsi. Sebanyak 1 gram adsorben dimasukkan ke dalam 20 gram minyak goreng bekas. Campuran tersebut dikocok dengan variasi waktu adsorpsi 0, 45, 60, 75, 90, 105, dan 120 menit. Setelah itu disaring dan diambil filtratnya, kemudian diukur kadar FFA minyak tersebut.
Penentuan Bobot Optimum Adsorben. Variasi bobot adsorben yang digunakan adalah 0.5, 1.0, 2.0, 3.0, 4.0, dan 5.0 gram. Campuran kaolin dan limbah padat tapioka tersebut dimasukkan ke dalam Erlenmeyer yang berisi 20 gram minyak goreng bekas. Lalu campuran tersebut dikocok selama waktu optimum. Setelah itu disaring dan diambil filtratnya, kemudian diukur kadar FFA minyak tersebut.
Penentuan Rasio Optimum Campuran Kaolin dan Limbah Padat Tapioka. Campuran kaolin dan limbah padat tapioka setiap komposisi ditimbang sebanyak 1 gram dan dimasukkan ke dalam Erlenmeyer yang berisi 20 gram minyak goreng bekas. Campuran tersebut lalu dikocok selama 90 menit. Setelah itu disaring dan diambil filtratnya, kemudian diukur kadar FFA minyak tersebut.
Adsorpsi Zat Warna
Pembuatan Larutan Zat Warna. Larutan stok zat warna sebanyak 1000 mg/l dibuat dengan cara 1000 mg serbuk biru metilena dilarutkan dalam air destilata dan diencerkan hingga 1 liter, kemudian dibuat kurva standar dari larutan biru metilena dengan konsentrasi 5, 10, 20, 30, 40, dan 50 ppm.
Penentuan Panjang Gelombang Maksimum. Panjang gelombang maksimum diukur dengan spektronik 20 D+ pada rentang panjang gelombang 600-700 nm dengan larutan biru metilena 5 mg/l.
Penentuan Waktu Optimum Adsorpsi. Sebanyak 1 gram adsorben dimasukkan ke dalam 100 ml larutan biru metilena dengan konsentrasi 100 mg/l, kemudian larutan digojok dengan alat gojok. Adsorpsi
dilakukan dengan variasi waktu adsorpsi 0, 15, 30, 45, 60, 75, dan 90 menit. Waktu optimum ditentukan dengan menghitung efisiensi dan kapasitas adsorpsi maksimum. Campuran disaring dan absorbansi filtratnya diukur pada panjang gelombang 660 nm.
Penentuan Bobot Optimum Adsorben. Variasi bobot adsorben yang digunakan adalah 0.5, 1.0, 1.5, 2.0, 2.5, dan 3.0 gram. Masing-masing dimasukkan ke dalam 100 ml larutan biru metilena 100 mg/l, kemudian digojok dengan alat gojok selama waktu optimum yang diperoleh. Campuran disaring dan absorbansi filtratnya diukur pada panjang gelombang 660 nm.
Penentuan Rasio Optimum Campuran Kaolin-Limbah Padat Tapioka. Campuran kaolin-limbah padat tapioka dengan perbandingan tertentu ditimbang sebanyak 1 gram dan dimasukkan ke dalam Erlenmeyer yang berisi 100 ml larutan biru metilena 100 mg/l, lalu campuran tersebut dikocok selama 30 menit. Setelah itu disaring dan diambil filtratnya, kemudian diukur dengan spektronik 20D+ pada panjang gelombang 660 nm.
Tahap Kelima
Penentuan Isoterm Adsorpsi Asam Lemak Bebas (Ketaren 1986). Sebanyak 1 gram campuran kaolin dan limbah padat tapioka dimasukkan ke dalam larutan standar asam oleat pada beberapa konsentrasi, yaitu 0, 2000, 6000, 8000, dan 10000 ppm dan digojok selama 90 menit. Setelah itu disaring dan diukur kadar asam lemak bebasnya. Pola isoterm adsorpsi diperoleh dengan membuat persamaan regresi linier menggunakan persamaan Langmuir dan Freundlich untuk menentukan tipe isoterm yang sesuai
HASIL DAN PEMBAHASAN
Kaolin dan limbah padat tapioka dapat dimanfaatkan sebagai adsorben. Penelitian ini menggabungkan kaolin dan limbah padat tapioka kemudian digunakan sebagai adsorben untuk asam lemak bebas dan zat warna biru metilena. Kaolin dan limbah padat tapioka yang digunakan terlebih dahulu diaktivasi sebelum dicampur secara homogen. Kaolin diaktivasi dengan lima variasi perlakuan, yaitu T = 750 ºC (A), autoklaf(B), H2SO4 30% (C),
T = 750 ºC dan autoklaf(D), T = 750 ºC dan H2SO4 30% (E), sedangkan limbah padat
tapioka diaktivasi dengan H3PO4 30%.
Aktivasi limbah padat tapioka dengan H3PO4
30% bertujuan untuk menghilangkan
senyawa-senyawa selain polisakarida yang terdapat di limbah padat tapioka sehingga diharapkan senyawa tersebut tidak ikut berperan dalam mekanisme adsorpsi asam lemak bebas maupun zat warna.
Aktivasi kaolin menggunakan H2SO4 30%
bertujuan untuk melarutkan komponen-komponen seperti Fe2O3, Al2O3, CaO, dan
MgO yang mengisi ruang antarlapisan kaolin, sehingga aktivasi dengan asam akan menambah luas permukaan adsorben, selanjutnya ion-ion Ca2+ dan Mg2+ yang berada pada permukaan kristal adsorben secara berangsur-angsur diganti oleh ion H+ dari H2SO4 (Ketaren 1986). Gambar aktivasi
H2SO4 terlihat pada Gambar 7.
Gambar 7 Skema interaksi proton dengan struktur kaolin. Reaksi yang terjadi pada saat kaolin
diaktivasi dengan asam adalah sebagai berikut:
Al2O3.2SiO2.2H2O + 3H2SO4 → Al2(SO4)3 +
2SiO2 + 5H2O
Aktivasi kaolin dengan pemanasan pada suhu tinggi, yaitu 750 °C mengakibatkan terjadinya perubahan fase kristal kaolin menjadi metakaolin. Pada suhu ini, ikatan antara Si dan Al diharapkan lebih mudah dipisahkan sehingga gabungan aktivasi pemanasan suhu tinggi dengan kimia akan melarutkan aluminium oksida dan meninggalkan residu SiO2 (Purwaningsih 2002).
Pemanasan dengan menggunakan uap air (suhu 121 °C) bertujuan agar perlakukan pemanasan tidak berpengaruh langsung terhadap struktur kaolin sehingga diharapkan struktur kaolin masih dapat dipertahankan dan tidak terjadi pemutusan ikatan antara lapisan silikat dan aluminatnya. Akan tetapi perlakuan tersebut mengakibatkan ada molekul air yang masuk ke dalam ruang antarlapisan kristal kaolin.
Gabungan pemanasan suhu tinggi dan uap air bertujuan agar struktur fase kristal baru (metakaolin) yang terbentuk akibat pemutusan
ikatan antarlapisan silikat dan aluminat yang dihasilkan pada pemanasan suhu tinggi dapat dipertahankan pada pemanasan dengan uap.
Kondisi Optimum Adsorpsi Asam Lemak Bebas
Waktu Adsorpsi
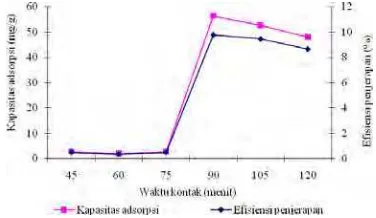
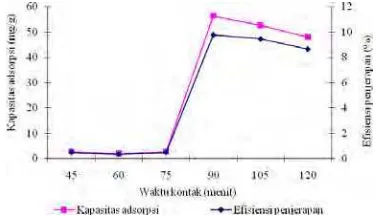
Waktu kontak merupakan salah satu faktor yang mempengaruhi laju dan besarnya adsorpsi. Pengaruh waktu kontak terhadap kapasitas adsorpsi dan efisiensi penjerapan asam lemak bebas dapat dilihat pada Gambar 8.
Lamanya proses adsorpsi ditentukan berdasarkan kapasitas dan persentase efisiensi penjerapannya selama kisaran waktu tertentu. Waktu kontak yang lebih lama memungkinkan proses difusi dan penempelan molekul adsorbat berlangsung lebih baik (Wijaya 2008). Hasil penelitian menunjukkan bahwa kapasitas adsorpsi dan efisiensi penjerapan naik seiring dengan bertambahnya waktu kontak, selanjutnya stabil walaupun terlihat sedikit mengalami penurunan. Waktu optimum adsorpsi yang diperoleh adalah 90 menit dengan kapasitas adsorpsi sebesar 56.38 mg/g artinya untuk setiap 1 g adsorben mampu mengadsorpsi 56.38 mg adsorbat dan efisiensi penjerapan sebesar 9.77%. Data selengkapnya dapat dilihat pada Lampiran 2.
Bobot Adsorben
Bobot adsorben mempengaruhi kapasitas adsorpsi dan efisiensi penjerapan. Hal ini dapat dilihat pada Gambar 9.
Gambar 9 Bobot optimum adsorpsi asam lemak bebas.
Hasil penelitian menunjukkan bahwa semakin banyak jumlah adsorben, maka luas permukaan aktifnya juga meningkat. Semakin luas permukaan adsorben, semakin banyak adsorbat yang dapat dijerap. Hal ini akan meningkatkan efisiensi penjerapan adsorpsi. Data hasil penelitian menunjukkan bahwa efisiensi penjerapan asam lemak bebas meningkat dari 20.09% sampai 29.41% dengan variasi bobot adsorben dari 0.5 g sampai 5 g.
Namun demikian, peningkatan jumlah sisi aktif adsorben akan memperluas penyebaran adsorbat, sehingga kapasitas adsorpsi menjadi lebih rendah dibandingkan dengan jumlah tapak aktif adsorben yang lebih sedikit. Kapasitas adsorpsi dengan bobot adsorben 0.5 gram adalah sebesar 222.59 mg/g mengalami penurunan menjadi 32.70 mg/g dengan bobot adsorben sebesar 5 gram. Hal ini menunjukkan bahwa dengan bobot 0.5 gram
hampir seluruh permukaan adsorben telah terikat dengan adsorbat, sedangkan penambahan bobot adsorben sampai 5 gram menyisakan banyak tapak aktif tidak berikatan dengan adsorbat. Data selengkapnya dapat dilihat pada Lampiran 3.
Perlakuan Optimum Campuran Kaolin-Limbah Padat Tapioka
Adsorben yang dibuat merupakan campuran dari kaolin dan limbah padat tapioka dengan nisbah 75:25 (1), 50:50 (2), dan 25:75 (3). Pengaruh perlakuan adsorben dan perbandingannya terhadap kapasitas adsorpsi dan efisiensi penjerapan dapat dilihat pada Gambar 10.
Gambar 10 Perlakuan optimum adsorpsi asam lemak bebas.
Hasil penelitian menunjukkan bahwa kapasitas adsorpsi dan efisiensi penjerapan paling besar ditunjukkan oleh adsorben E3, yaitu 25% kaolin teraktivasi 750 °C dan H2SO4 30% dicampur dengan 75% limbah
padat tapioka teraktivasi H3PO4 30%. Gambar
10 menunjukkan bahwa penjerapan asam lemak bebas lebih besar saat komposisi dari limbah padat tapioka lebih banyak daripada kaolin. Kapasitas adsorpsi tertinggi ditunjukkan oleh adsorben E3, yaitu sebesar 479.70 mg/g dan efisiensi penjerapan sebesar 89.94%. Data selengkapnya dapat dilihat pada Lampiran 4.
Kondisi Optimum Adsorpsi Zat Warna
Waktu Adsorpsi
kapasitas adsorpsi dan efisiensi penjerapan biru metilena dapat dilihat pada Gambar 11.
Gambar 11 Waktu optimum adsorpsi biru metilena.
Konsentrasi larutan biru metilena menurun dari 100 mg/l menjadi 14.59 mg/l dengan bertambahnya waktu adsorpsi. Waktu optimum adsorpsi yang diperoleh adalah 30 menit dengan kapasitas adsorpsi 8.51 mg/g artinya untuk setiap 1 g adsorben mampu mengadsorpsi 8.51 mg ion biru metilena dalam waktu 30 menit dengan efisiensi penjerapan 85.68%. Setelah melewati 30 menit kapasitas adsorpsi dan efisiensi penjerapan cenderung stabil. Data selengkapnya dapat dilihat pada Lampiran 12.
Bobot Adsorben
Bobot adsorben berpengaruh terhadap kapasitas adsorpsi dan efisiensi penjerapan larutan biru metilena dengan konsentrasi 100 mg/l, hal ini dapat dilihat pada Gambar 12.
Gambar 12 Bobot optimum adsorpsi biru metilena.
Hasil penelitian menunjukkan bahwa semakin banyak jumlah adsorben maka efisiensi penjerapan adsorpsi semakin meningkat dan kapasitas adsorpsi akan menurun. Hal ini terlihat dari efisiensi penjerapan biru metilena yang meningkat dari 66.83% sampai 94.09% dengan variasi bobot dari 0.5 g sampai 3 g. Penambahan jumlah adsorben akan menurunkan kapasitas adsorpsi dari 13.23 mg/g menjadi 3.12 mg/g. Hal ini
disebabkan karena saat bobot 0,5 gram hampir seluruh permukaan adsorben telah terikat dengan adsorbat, sedangkan pada bobot 3 gram masih banyak tapak aktif yang belum berikatan dengan adsorbat. Data selengkapnya dapat dilihat pada Lampiran 13.
Perlakuan Optimum Campuran Kaolin-Limbah Padat Tapioka
Pengaruh perlakuan adsorben dan perbandingannya terhadap kapasitas adsorpsi dan efisiensi penjerapan larutan biru metilena dengan konsentrasi 100 mg/l dapat dilihat pada Gambar 13.
Gambar 13 Perlakuan optimum adsorpsi biru metilena.
Hasil penelitian menunjukkan bahwa kapasitas adsorpsi dan efisiensi penjerapan terbesar dengan menggunakan adsorben C1, yaitu campuran 75% kaolin teraktivasi H2SO4
30% dan 25% limbah padat tapioka teraktivasi H3PO4 30%. Pada nisbah optimum tersebut
diperoleh kapasitas adsorpsi sebesar 9.83 mg/g dan efisiensi penjerapan sebesar 99.53%. Data selengkapnya dapat dilihat pada Lampiran 14.
Kapasitas Adsorpsi dan Efisiensi Penjerapan Adsorben Lain
Kinerja dari adsorben campuran kaolin dan limbah padat tapioka dievaluasi dengan cara membandingkan kemampuan mengad-sorpsinya dengan adsorben komersial, yaitu arang aktif dan adsorben komersial yang diperoleh dari industri pengolahan makanan. Hasil penelitian menunjukkan bahwa nilai kapasitas adsorpsi dan efisiensi penjerapan asam lemak bebas dan biru metilena yang paling besar adalah dengan adsorben campuran kaolin-limbah padat tapioka (komposit). Data hasil penelitian disajikan pada Tabel 4 dan 5.
dalam adsorpsi asam lemak bebas dan zat warna daripada arang aktif dan adsorben komersial. Hal ini disebabkan karena komposit bekerja dengan dua jenis adsorben yang bekerja secara sinergis untuk menjerap asam lemak bebas dan biru metilena.
Tabel 4 Data adsorpsi asam lemak bebas dengan berbagai jenis adsorben
Adsorben Efisiensi Kapasitas Penjerapan Adsorpsi
(%) (mg/g)
Komposit 89.94 479.6968
Arang aktif 70.38 387.5826 Adsorben komersial 59.38 327.0222
Tabel 5 Data adsorpsi biru metilena dengan berbagai jenis adsorben
Adsorben Efisiensi Kapasitas Penjerapan Adsorpsi
(%) (mg/g)
Komposit 99.53 9.83
Arang Aktif 96.79 9.59
Adsorben komersial 78.84 7.87
Onggok 47.26 4.69
Data yang disajikan pada Tabel 4 dan 5 juga mengindikasikan bahwa kapasitas adsorpsi dari asam lemak bebas lebih besar daripada zat warna biru metilena. Hal ini dikarenakan ukuran molekul biru metilena lebih besar daripada asam lemak bebas, sehingga lebih mudah molekul asam lemak bebas masuk ke dalam pori-pori adsorben daripada biru metilena. Data selengkapnya dapat dilihat pada Lampiran 5 dan 15.
Isoterm Adsorpsi
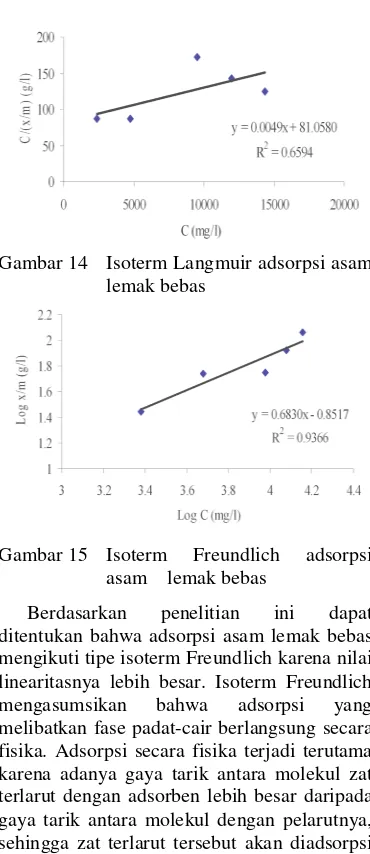
Tipe isoterm adsorpsi dapat digunakan untuk mengetahui mekanisme penjerapan asam lemak bebas dan biru metilena dengan adsorben campuran dari kaolin dan limbah padat tapioka. Isoterm adsorpsi Langmuir dilakukan dengan cara membuat kurva hubungan c/(x/m) terhadap c, sedangkan isoterm adsorpsi Freundlich dilakukan dengan membuat kurva hubungan log x/m terhadap log c. Isoterm adsorpsi asam lemak bebas dapat dilihat pada Gambar 14 dan Gambar 15. Linearitas kedua tipe isoterm adsorpsi berbeda, yaitu 65.94% untuk isoterm Langmuir dan 93.66% untuk isoterm Freundlich.
Gambar 14 Isoterm Langmuir adsorpsi asam lemak bebas
Gambar 15 Isoterm Freundlich adsorpsi asam lemak bebas
Berdasarkan penelitian ini dapat ditentukan bahwa adsorpsi asam lemak bebas mengikuti tipe isoterm Freundlich karena nilai linearitasnya lebih besar. Isoterm Freundlich mengasumsikan bahwa adsorpsi yang melibatkan fase padat-cair berlangsung secara fisika. Adsorpsi secara fisika terjadi terutama karena adanya gaya tarik antara molekul zat terlarut dengan adsorben lebih besar daripada gaya tarik antara molekul dengan pelarutnya, sehingga zat terlarut tersebut akan diadsorpsi ke permukaan adsorben.
Mekanisme adsorpsi asam lemak bebas terjadi melalui gaya tarik-menarik antarmolekuler di antara adsorben dengan asam lemak bebas dalam minyak goreng bekas. Ikatan yang terjadi antara asam lemak bebas dan adsorben diperkirakan terbentuk melalui ikatan hidrogen. Pada kaolin terjadi ikatan hidrogen antara atom O pada SiO2
dengan atom H pada gugus karboksil dalam asam lemak bebas, sedangkan pada limbah padat tapioka terjadi ikatan hidrogen antara atom O pada gugus OH dalam selulosa dengan atom H gugus karboksil dalam asam lemak bebas. Ikatan tersebut sangat lemah sehingga mudah diputuskan.
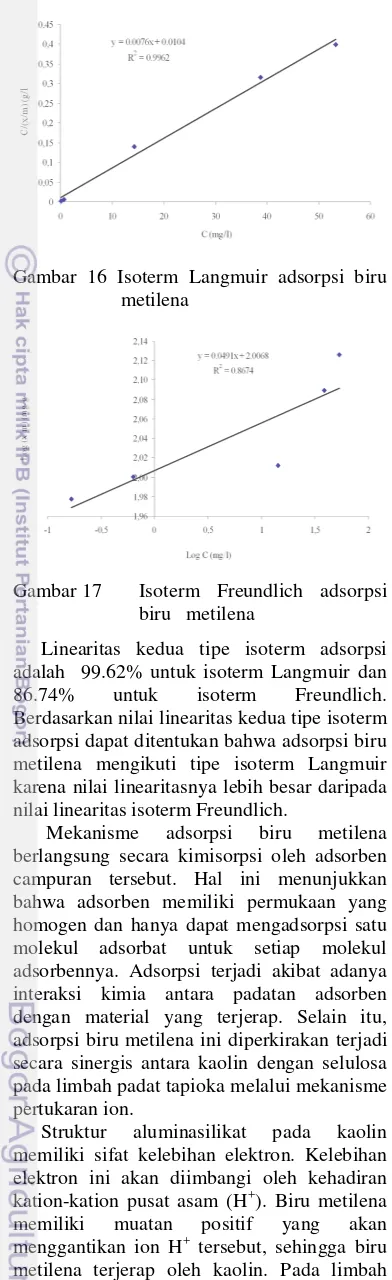
Gambar 16 Isoterm Langmuir adsorpsi biru metilena
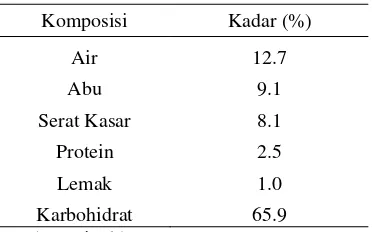
Gambar 17 Isoterm Freundlich adsorpsi biru metilena
Linearitas kedua tipe isoterm adsorpsi adalah 99.62% untuk isoterm Langmuir dan 86.74% untuk isoterm Freundlich. Berdasarkan nilai linearitas kedua tipe isoterm adsorpsi dapat ditentukan bahwa adsorpsi biru metilena mengikuti tipe isoterm Langmuir karena nilai linearitasnya lebih besar daripada nilai linearitas isoterm Freundlich.
Mekanisme adsorpsi biru metilena berlangsung secara kimisorpsi oleh adsorben campuran tersebut. Hal ini menunjukkan bahwa adsorben memiliki permukaan yang homogen dan hanya dapat mengadsorpsi satu molekul adsorbat untuk setiap molekul adsorbennya. Adsorpsi terjadi akibat adanya interaksi kimia antara padatan adsorben dengan material yang terjerap. Selain itu, adsorpsi biru metilena ini diperkirakan terjadi secara sinergis antara kaolin dengan selulosa pada limbah padat tapioka melalui mekanisme pertukaran ion.
Struktur aluminasilikat pada kaolin memiliki sifat kelebihan elektron. Kelebihan elektron ini akan diimbangi oleh kehadiran kation-kation pusat asam (H+). Biru metilena memiliki muatan positif yang akan menggantikan ion H+ tersebut, sehingga biru metilena terjerap oleh kaolin. Pada limbah padat tapioka, molekul biru metilena akan berikatan pada gugus -OH selulosa.
Nilai konstanta n, k, α, dan β dapat dihitung dari persamaan regresi Freundlich dan Langmuir untuk asam lemak bebas (ALB) dan biru metilena (BM) dapat dilihat pada Tabel 6 dan 7.
Tabel 6 Nilai konstanta n dan k dari persamaan Freundlich
Adsorbat n K R
ALB 1.4641 0.1407 93.66 BM 20.3666 101.5781 86.74
Nilai n dan k pada isoterm Freundlich tergantung pada suhu, adsorben, dan unsur-unsur yang dijerap. Nilai n menggambarkan intensitas dari adsorpsi, sedangkan nilai k menunjukkan kapasitas adsorpsi dari adsorben.
Tabel 7 Nilai konstanta α dan β dari persamaan Langmuir
Adsorbat α Β R
ALB 204.0816 0.00006 65.94
BM 131.5789 0.7308 99.62
Nilai α menggambarkan jumlah yang dijerap atau kapasitas adsorpsi untuk membentuk lapisan sempurna pada permukaan adsorben. Nilai β merupakan konstanta yang bertambah dengan kenaikan ukuran molekuler yang menunjukkan kekuatan ikatan molekul adsorbat pada permukaan adsorben.
Nilai-nilai konstanta n, k, α, dan β pada isoterm adsorpsi asam lemak bebas dan biru metilena tidak dapat dibandingkan. Hal ini disebabkan karena asam lemak bebas dan biru metilena merupakan dua senyawa yang memiliki ukuran yang berbeda. Selain itu, metode yang digunakan untuk adsorpsi kedua senyawa juga berbeda.
SIMPULAN DAN SARAN
Simpulan
Adsorben campuran kaolin dan limbah padat tapioka terbukti dapat digunakan sebagai adsorben untuk asam lemak bebas dan zat warna. Kondisi optimum adsorpsi asam lemak bebas dicapai pada waktu 90 menit dengan adsorben campuran 25% kaolin teraktivasi 750 °C serta H2SO4 30% dan 75 %
limbah padat tapioka teraktivasi H3PO4 30%.
dan 25% limbah padat tapioka teraktivasi H3PO4 30%.
Isoterm adsorpsi asam lemak bebas dan zat warna memiliki tipe yang berbeda. Tipe isoterm adsorpsi untuk asam lemak bebas adalah isoterm Freundlich, sedangkan tipe isoterm adsorpsi untuk zat warna adalah isoterm Langmuir.
Saran
Penelitian lanjutan yang perlu dilakukan adalah pencirian sifat fisik dan kimia permukaan adsorben campuran kaolin dan limbah padat tapioka. Selain itu, perlu dilakukan kajian terhadap tahapan modifikasi/aktivasi menggunakan senyawa kimia selain asam.
DAFTAR PUSTAKA
Alamsyah Z. 2007. Biosorpsi Biru Metilena oleh Kulit Buah Kakao [skripsi]. Bogor: Fakultas Matematika dan IPA, Institut Pertanian Bogor.
Ali U. 2008. Pengaruh Penggunaan Onggok dan Isi Rumen Sapi Komplit dalam Pakan Komplit terhadap Penampilan Kambing Peranakan Etawah. Jurusan Nutrisi dan Makanan Ternak, Fakultas Peternakan, Universitas Islam Malang.
Arikan M, Sobolev K, Ertun T, Yeginobali A, Turker P. 2009. Properties Of Blended Cements With Thermally Activated Kaolin. Construction and Building Materials 23: 62–70.
Atkins PW. 1999. Kimia Fisika Jilid 2. Ed ke-4. Jakarta: Erlangga.
Buchori L, Widayat. 2009. Pembuatan Biodiesel Dari Minyak Goreng Bekas dengan Proses Catalytic Cracking.
Prosiding Seminar Nasional Teknik Kimia Indonesia; Bandung, 19-20 Oktober 2009. Semarang: Jurusan Teknik Kimia Fakultas Teknik Universitas Diponegoro.
Chen B, Evans JRG. 2005. Thermoplastic Starch-Clay Nanocomposites and Their Characteristics. Carbohydrate Polymers 6: 455-463.
Dudkin BN, Loukhina IV, Isupov VP, Avvakumov EG. 2005. Mechanical Activation of Kaolinite in the Presence of
Concentrated Sulfuric Acid. Russian Journal of Applied Chemistry 78: 33-37.
Fahrizal. 2008. Pemanfaatan Tongkol Jagung sebagai Biosorben Zat Warna Biru Metilena [skripsi]. Bogor: Fakultas Matematika dan IPA, Institut Pertanian Bogor.
Faruqi FA, Okuda S, Williamson WO. 1967. Chemisorption Of Methylene Blue By Kaolinite. Clay Minerals 7: 19-31.
Ghosh D, Bhattacharyya KG. 2002. Adsorption Of Methylene Blue On Kaolinite. Applied Clay Science 20: 295-300.
Herlina N, Ginting MH. 2002. Lemak dan Minyak. Sumatera Utara: Jurusan Teknik Kimia Fakultas Teknik, Universitas Sumatera Utara.
Ketaren S. 1986. Pengantar Teknologi Minyak dan Lemak Pangan. Jakarta: UI Press.
Ketaren S. 1991. Minyak dan Lemak Nabati. Bogor: IPB Press.
Koyuncu H, Kul AR, Yildiz N, Calimli A, Ceylan H. 2007. Equilibrium and Kinetic Studies for the Sorption of 3-methoxybenzaldehyde on Activated Kaolinites. Hazardous Materials 14: 128-139.
Lynch CT. 1990. Pratical Handbook of Material Science. Ed ke-2. New York: CRC Pr.
Muhdarina, Linggawati A. 2003. Pilarisasi Kaolinit Alam untuk Meningkatkan Kapasitas Tukar Kation. Jurnal Natur Indonesia 6: 20-23.
Melisya N. 2009. Analisa Asam Lemak Bebas Minyak Goreng Bekas Menggunakan Adsorben Berbasis Limbah Padat Tapioka [skripsi]. Bogor: Fakultas Matematika dan IPA, Institut Pertanian Bogor.
Prasetyo BH, Adiningsih JS, Subagyono K, Simanungkalit RDM. 2009. Mineralogi, Kimia, Fisika, Dan Biologi Tanah Sawah. http://www.tekmira.esdm.go.id. [9 Nov 2009].
Purwaningsih H. 2002. Pembuatan Alumina dari Kaolin dan Studi Katalisis Heterogen untuk Sintesis Vanili dari Eugenol Minyak Gagang Cengkeh. [Tesis]. Depok: Fakultas Matematika dan IPA, Universitas Indonesia
Rinaldy W. 1987. Pemanfaatan Onggok Singkong (Manihot esculenta Crantz
Sebagai Bahan Pembuatan Etanol [tesis]. Bogor: Program Pascasarjana, Institut Pertanian Bogor.
Ritonga MY. 2004. Pengaruh Bilangan Asam terhadap Hidrolisa Minyak Kelapa Sawit. Sumatera Utara: Jurusan Teknik Kimia Fakultas Teknik, Universitas Sumatera Utara.
Romaria. 2008. Karakterisasi Fisiko Kimia
Minyak Goreng Pada Proses
Penggorengan Berulang Dan Umur Simpan Kacang Salut Yang Dihasilkan [skripsi]. Bogor: Fakultas Teknologi Pertanian, Institut Pertanian Bogor.
Sarapaa O, Al-Ani T. 2008. Clay and Clay Mineralogy. Finland: GTK Espoo.
[SNI] Standar Nasional Indonesia.1998. SNI 01-3555-1998: Cara Uji Minyak dan Lemak. Jakarta: Dewan Standarisasi Nasional.
[SNI] Standar Nasional Indonesia. 2002. SNI 01-3741-2002: Minyak Goreng. Jakarta: Dewan Standarisasi Nasional.
[Sigma]. 1996. Biochemicals Organic Compound For Research And Diagnostic Reagents. New York : Sigma Clinical Company.
Sukarta N I. 2008. Adsorpsi Ion Cr3+ oleh Serbuk Gergaji Kayu Albizia (Albizia falcata), Studi Pengembangan Bahan Alternatif Penjerap Limbah Logam Berat [tesis]. Bogor: Program Pascasarjana, Institut Pertanian Bogor.
Tjiptadi W. 1985. Telaah Kualitas dan Kuantitas Limbah Industri Tapioka serta Cara Pengendalian di daerah Bogor dan Sekitarnya [disertasi]. Bogor: Program Pascasarjana, Institut Pertanian Bogor.
Widiarto S, Suka IG, Simanjuntak W. 2008. Pembuatan polimer peka lingkungan dengan polimerisasi grafing campuran n-isopropilakrilamida dan asam metakrilat (binary monomer) pada selulosa yang diekstraksi dari onggok. Prosiding Seminar Nasional Sains dan Teknologi-II; Lampung, 17-18 November 2008. Lampung: Jurusan Kimia FMIPA Universitas Lampung. hlm 328-341.
Widiastuti CE. 2009. Kajian Teknologi Aktivitas Bentonit dan Aplikasinya untuk Pemurnian Minyak Kelapa Sawit [skripsi]. Bogor: Fakultas Teknologi Pertanian, Institut Pertanian Bogor.
Wijaya H. 2008. Penggunaan Tanah Laterit sebagai Media Adsorpsi untuk Menurunkan Kadar Chemical Oxygen Demand (COD) pada Pengolahan Limbah Cair di Rumah Sakit Baktiningsih Klepu [skripsi]. Yogyakarta: Jurusan Teknik Lingkungan Fakultas Teknik Sipil dan Perencanaan, Universitas Islam Indonesia.
Wijayanti R. 2009. Arang Aktif dari Ampas Tebu sebagai Adsorben pada Pemurnian Minyak Goreng Bekas [skripsi]. Bogor: Fakultas Matematika dan IPA, Institut Pertanian Bogor.
Lampiran 1 Diagram alir penelitian
Kaolin dan limbah padat tapioka dicuci dengan
akuades
Kaolin dan limbah padat tapioka dikeringkan
Limbah padat tapioka diaktivasi dengan H3PO4 30 %
Kaolin dan limbah padat tapioka dicampur dengan perbandingan
tertentu Kaolin diaktivasi dengan
variasi perlakuan T = 750ºC (A), autoklaf (B), H2SO4 30 %
(C), T = 750ºC dan autoklaf (D), T = 750ºC dan H2SO4 30
% (E)
Penentuan kondisi waktu, bobot, dan perlakuan
optimum
Penentuan isoterm adsorpsi asam lemak bebas dan biru
Densitas Minyak
• Volume piknometer = 25 ml
• Bobot kosong piknometer = 22.6532 gram
• Bobot kosong + minyak = 44.2913 gram Perhitungan :
Lampiran 2 Data optimasi waktu kontak terhadap asam lemak bebas
Waktu Volume Kadar Kadar Rata-Rata Efisiensi Bobot Volume Kapasitas
Kontak NaOH FFA FFA FFA Penjerapan Adsorben Minyak Adsorpsi
(menit) (ml) (%b/v) (ppm) (ppm) (%) (g) (ml) (mg/g)
0 1.0 2.4273 24272.6713 24049.7063 − − − −
1.0 2.3827 23826.7413
45 1.0 2.3781 23780.7526 23931.8227 0.49 1.0177 23.4287 2.7138
1.0 2.4083 24082.8928
60 1.0 2.3896 23896.0588 23965.9849 0.35 1.0098 23.2928 1.9312
1.0 2.4036 24035.9109
75 1.0 2.3818 23817.5294 23931.4110 0.49 1.0309 23.9958 2.7535
1.0 2.4045 24045.2926
90 0.9 2.1717 21717.0528 21700.0664 9.77 1.0098 24.2303 56.3800
0.9 2.1683 21683.0801
105 0.9 2.1768 21768.2119 21776.7652 9.45 1.0146 23.4917 52.6269
0.9 2.1785 21785.3186
120 0.9 2.1841 21841.1013 21971.7039 8.64 1.0285 23.7445 47.9739
0.9 2.2102 22102.3065
Keterangan :
EP = efisiensi penjerapan asam lemak bebas (%)
Q = kapasitas adsorpsi asam lemak bebas (mg/g)
Lampiran 3 Data optimasi bobot adsorben terhadap asam lemak bebas
Bobot Volume Kadar Kadar Rata-Rata Efisiensi Volume Kapasitas
Adsorben NaOH FFA FFA FFA Penjerapan Minyak Adsorpsi
(gram) (ml) (%b/v) (ppm) (ppm) (%) (ml) (mg/g)
0 1.0 2.4273 24272.6713 24049.7063
1.0 2.3827 23826.7413
0.5032 0.8 1.9274 19273.8489 19217.6460 20.09 23.1798 222.5878
0.8 1.9161 19161.4431
1.0456 0.7 1.7218 17218.1385 17161.7919 28.64 23.1347 152.4004
0.7 1.7105 17105.4454
2.0099 0.7 1.7201 17200.9684 17072.5525 29.01 23.1490 80.3593
0.7 1.6944 16944.1367
3.0026 0.7 1.7055 17054.7075 17126.1230 28.79 23.1258 53.3249
0.7 1.7198 17197.5385
4.0066 0.7 1.7215 17214.7017 16979.0899 29.40 23.1871 40.9193
0.7 1.6743 16743.4781
5.0095 0.7 1.7150 17149.6631 16977.5649 29.41 23.1604 32.6966
0.7 1.6805 16805.4668
Lampiran 4 Data optimasi perlakuan adsorben terhadap asam lemak bebas
Jenis Ulangan Volume Kadar Kadar Rata-Rata Efisiensi Bobot Volume Kapasitas
Komposit NaOH FFA FFA FFA Penjerapan Adsorben Minyak Adsorpsi
(ml) (%b/v) (ppm) (ppm) (%) (g) (ml) (mg/g)
A1 1 0.30 0.7221 7221.1641 7163.0952 70.22 1.0716 23.2895 367.0033
2 0.30 0.7135 7135.4488
3 0.30 0.7133 7132.6729
A2 1 0.20 0.4820 4819.8043 4812.5423 79.99 1.0595 23.7028 430.3678
2 0.20 0.4802 4801.8164
3 0.20 0.4816 4816.0062
A3 1 0.20 0.4878 4878.4769 4830.4364 79.91 1.0577 23.5795 428.4587
2 0.20 0.4765 4765.3114
B1 1 0.30 0.7076 7076.2391 7139.2449 70.31 1.0294 23.7635 390.3747
2 0.30 0.7225 7225.4328
3 0.30 0.7116 7116.0627
B2 1 0.20 0.4726 4725.7003 4801.9170 80.03 1.0338 23.1849 431.6677
2 0.20 0.4870 4869.7306
3 0.20 0.4810 4810.3202
B3 1 0.20 0.4856 4856.1874 4795.9167 80.06 1.0300 23.2068 433.8047
2 0.20 0.4771 4770.8914
3 0.20 0.4761 4760.6714
C1 1 0.30 0.7200 7199.8962 7156.6954 70.24 1.1740 23.2055 333.9104
2 0.30 0.7086 7085.8109
3 0.30 0.7184 7184.3792
C2 1 0.20 0.4859 4859.0832 4845.1536 79.85 1.0277 24.0321 449.0860
2 0.20 0.4858 4858.1175
3 0.20 0.4832 4832.1897
C3 1 0.20 0.4775 4774.6187 4826.8449 79.93 1.0195 23.1233 435.9941
2 0.20 0.4826 4826.4654
3 0.20 0.4879 4879.4506
D1 1 0.20 0.4753 4753.2661 4750.4870 80.25 1.0439 23.9884 443.4883
2 0.20 0.4795 4795.2231
3 0.20 0.4703 4702.9718
D2 1 0.20 0.4849 4849.4441 4817.8899 79.97 1.0051 23.3456 446.6994
2 0.20 0.4764 4764.3827 3 0.20 0.4840 4839.8431
D3 1 0.15 0.3591 3590.7825 3583.7707 85.10 1.0604 23.5874 455.2416
2 0.15 0.3580 3579.5657
3 0.15 0.3581 3580.9640
E1 1 0.25 0.5893 5893.4541 5946.0968 75.28 1.0115 23.3391 417.7182
2 0.25 0.5953 5953.1579 3 0.25 0.5992 5991.6783
E2 1 0.20 0.4851 4851.3688 4841.4988 79.87 1.0237 23.3396 437.9329
2 0.20 0.4818 4817.9045
3 0.20 0.4855 4855.2229
E3 1 0.10 0.2431 2430.5078 2419.2122 89.94 1.0448 23.1704 479.6968
2 0.10 0.2399 2398.5525
3 0.10 0.2429 2428.5761
Keterangan :
1 = perbandingan 75:25 2 = perbandingan 50:50 3 = perbandingan 25:75
A = aktivasi kaolin dengan pemanasan 750 ºC B = aktivasi kaolin dengan autoklaf
C = aktivasi kaolin dengan H2SO4 30%
Lampiran 5 Data adsorpsi asam lemak bebas dengan adsorben lain
Sampel Ulangan Volume Kadar Kadar Rata-Rata Efisiensi Bobot Volume Kapasitas
NaOH FFA FFA FFA Penjerapan Adsorben Minyak Adsorpsi
(ml) (%) (ppm) (ppm) (%) (g) (ml) (mg/g)
Arang 1 0.30 0.7161 7160.5294 7123.8549 70.38 1.0158 23.2607 387.5826
aktif 2 0.30 0.7087 7087.1804
Komersil 1 0.35 0.9868 9868.1283 9768.5470 59.38 1.0158 23.2607 327.0222
2 0.35 0.9669 9668.9657
Lampiran 6 Data asam oleat sebelum dijerap
Konsentrasi Volume Kadar Kadar Rata-Rata
Asam Oleat NaOH FFA FFA FFA
(ppm) (ml) (%) (ppm) (ppm)
2000 0.15 0.3589 3588.6740 3571.2837
0.15 0.3554 3553.8933
4000 0.30 0.7208 7208.3883 7241.9988
0.30 0.7276 7275.6094
6000 0.50 1.1925 11924.9012 11967.0801
0.50 1.2009 12009.2589
8000 0.65 1.5572 15572.2568 15576.8378
0.65 1.5581 15581.4188
10000 0.80 1.9287 19286.8225 19325.0142
0.80 1.9363 19363.2059
Lampiran 7 Data asam oleat setelah dijerap
Konsentrasi Volume Kadar Kadar Rata-Rata
Asam Oleat NaOH FFA FFA FFA
(ppm) (ml) (%) (ppm) (ppm)
2000 0.10 0.2392 2392.4494 2408.8262
0.10 0.2425 2425.2031
4000 0.20 0.4748 4747.7272 4790.9140
0.20 0.4834 4834.1008
6000 0.40 0.9540 9539.9210 9524.1510
0.40 0.9508 9508.3810
8000 0.50 1.1976 11976.3117 11978.6596
0.50 1.1981 11981.0074
10000 0.60 1.4397 14396.9655 14346.4499
0.60 1.4296 14295.9342
Lampiran 8 Data efisiensi penjerapan
Konsentrasi Kadar FFA Kadar FFA Efisiensi
Asam Oleat (ppm) terjerap Penjerapan
(ppm) Awal Akhir (ppm) (%)
2000 3571.2837 2408.8262 1162.46 32.55
4000 7241.9988 4790.9140 2451.08 33.85
6000 11967.0801 9524.1510 2442.93 20.41
8000 15576.8378 11978.6596 3598.18 23.10
Lampiran 9 Data isoterm Langmuir dan Freundlich untuk adsorpsi asam lemak bebas
Konsentrasi Asam Oleat Bobot Volume Langmuir Freundlich
(mg/l) Adsorben Minyak x x x/m C/(x/m) Log Log
Awal Akhir (gram) (l) (mg/l) (g) (mg/g) (g/l) C x/m
3571.2837 2408.8262 1.0120 0.0240 1162.4575 0.0279 27.5529 87.4255 3.3818 1.4402 7241.9988 4790.9140 1.0668 0.0238 2451.0848 0.0584 54.7438 87.5152 3.6804 1.7383 11967.0801 9524.1510 1.0552 0.0239 2442.9291 0.0585 55.4113 171.8811 3.9788 1.7436 15576.8378 11978.6596 1.0253 0.0238 3598.1782 0.0857 83.5896 143.3032 4.0784 1.9222 19325.0142 14346.4499 1.0283 0.0238 4978.5643 0.1187 115.4006 124.3187 4.1567 2.0622
Keterangan :
*Cakhir digunakan sebagai variabel c pada rumus Isoterm Langmuir dan Freundlich
*x sebagai konsentrasi yang terjerap
Nilai x = Cteradsorpsi (ppm) x Volume larutan (L) x
• Persamaan garis isoterm Langmuir yang diperoleh y = 0.0049x + 81.0580 dengan r2 = 65.94% maka dari persamaan , diperoleh nilai α = 204.0816 dan β = 0.00006.
• Persamaan garis isoterm Freundlich yang diperoleh y = 0.6830x – 0.8517 dengan r2 = 93.66%
maka dari persamaan log = log k + log C, diperoleh nilai n = 1.4641 dan k = 0.1407
Lampiran 10 Data kadar asam lemak bebas pada minyak goreng bekas
Sampel Ulangan Bobot Volume Kadar Kadar
Minyak NaOH FFA FFA
(gram) (ml) (%) (ppm)
Blanko 0.2
Minyak Bekas 1 0.5076 1.2 2.8047 14236.6572
2 0.5171 1.2 2.7531 14236.2801
Rata-rata 2.7789 14236.4687
Lampiran 11 Data kadar asam lemak bebas pada minyak goreng baru
Sampel Ulangan Bobot Volume Kadar Kadar
Minyak NaOH FFA FFA
(gram) (ml) (%) (ppm)
Blanko 0.20
Minyak Baru 1 0.51 0.30 0.2749 1412.4362
2 0.51 0.30 0.2770 1412.1460
3 0.52 0.30 0.2742 1412.4042
Rata-rata 0.2754 1412.3288
Lampiran 12 Data optimasi waktu kontak adsorben terhadap biru metilena
Waktu A Bobot [Biru Metilena] Co-Ca EP Q
(menit) (gram) (ppm) (ppm) (%) (mg/g)
0 - - 100.0000 - - -
15 0.3979 1.0024 18.3054 81.6946 81.69 8.15
30 0.3170 1.0064 14.3202 85.6798 85.68 8.51
45 0.3686 1.0220 16.8621 83.1379 83.14 8.13
60 0.3507 1.0066 15.9803 84.0197 84.02 8.35
90 0.3324 1.0046 14.5862 85.4138 85.41 8.50
Contoh perhitungan :
Keterangan :
EP = efisiensi penjerapan biru metilena (%)
Q = kapasitas adsorpsi biru metilena (mg/g)
Lampiran 13 Data optimasi bobot adsorben terhadap biru metilena
Bobot A [Biru Metilena] Co-Ca EP Q
(gram) (ppm) (ppm) (%) (mg/g)
0.0000 - 100.0000 - - -
0.5052 0.6996 33.1675 66.8325 66.83 13.23
1.0040 0.4763 22.1675 77.8325 77.83 7.75
1.5075 0.2890 12.9409 87.0591 87.06 5.78
2.0035 0.3170 14.3202 85.6798 85.68 4.28
2.5008 0.2132 9.2069 90.7931 90.79 3.63
3.0150 0.1463 5.9113 94.0887 94.09 3.12
Lampiran 14 Data optimasi perlakuan adsorben terhadap biru metilena
Komposit Rasio Bobot A [Biru Metilena] Co-Ca EP Q
(gram) (ppm) (ppm) (%) (mg/g)
A 1 1.0150 0.0052 0.5061 99.4939 99.49 9.80
2 1.0148 0.0205 0.8197 99.1803 99.18 9.77
3 1.0153 0.0391 1.2008 98.7992 98.80 9.73
B 1 1.0119 0.0223 0.8566 99.1434 99.14 9.80
2 1.0109 0.2503 11.0345 88.9655 88.97 8.80
3 1.0114 0.6091 28.7094 71.2906 71.29 7.05
C 1 1.0130 0.0035 0.4713 99.5287 99.53 9.83
2 1.0129 0.0097 0.5984 99.4016 99.40 9.81
3 1.0145 0.0186 0.7807 99.2193 99.22 9.78
D 1 1.0125 0.0496 1.4160 98.5840 98.58 9.74
3 1.0158 0.6055 28.5320 71.4680 71.47 7.04
E 1 1.0097 0.3788 17.3645 82.6355 82.64 8.18
2 1.0167 0.5317 24.8966 75.1034 75.10 7.39
3 1.0101 0.7496 35.6305 64.3695 64.37 6.37
Keterangan :
1 = perbandingan 75:25 2 = perbandingan 50:50 3 = perbandingan 25:75
A = aktivasi kaolin dengan pemanasan 750 ºC B = aktivasi kaolin dengan autoklaf
C = aktivasi kaolin dengan H2SO4 30%
D = aktivasi kaolin dengan pemanasan 750 ºC dan autoklaf E = aktivasi kaolin dengan pemanasan 750 ºC dan H2SO4 30%
Lampiran 15 Data adsorpsi biru metilena dengan adsorben lain
Adsorben A Bobot [Biru Metilena] EP Q
(gram) (ppm) (%) (mg/g)
Arang Aktif 0.9150 1.0091 3.2118 96.79 9.59
Komersil 0.4559 1.0020 21.1626 78.84 7.87
Onggok 1.0969 1.0087 52.7389 47.26 4.69
Lampiran 16 Data
isoterm Langmuir dan Freundlich untuk adsorpsi biru metilena
Konsentrasi Bobot Langmuir Freundlich
(mg/l) Adsorben x x x/m C/x/m Log Log
A Awal x fp Akhir (gram) (mg/l) (g) (mg/g) (g/l) C x/m
0.4134 953.4500 0.1675 1.0032 953.2825 0.0953 95.0242 0.0018 -0.7760 1.9778 0.4365 1010.3450 0.6305 1.0092 1009.7145 0.1010 100.0510 0.0063 -0.2003 2.0002 0.4535 1052.2150 14.3202 1.0098 1037.8948 0.1038 102.7822 0.1393 1.1559 2.0119 0.5436 1274.1400 38.7291 1.0058 1235.4109 0.1235 122.8287 0.3153 1.5880 2.0893 0.5918 1392.8550 53.2808 1.0014 1339.5742 0.1340 133.7701 0.3983 1.7266 2.1264
Keterangan :
fp : faktor pengenceran 50/1 ( 1 ml dalam 50 ml)
Cakhir : variabel c pada rumus Isoterm Langmuir dan Freundlich
x : konsentrasi yang terjerap
Nilai x = Cteradsorpsi (ppm) x Volume larutan (L) x
• Persamaan garis isoterm Langmuir yang diperoleh y = 0.0076x + 0.0104 dengan r2 = 99.62% maka dari persamaan , diperoleh nilai α = 131.5789 dan β = 0.7308
• Persamaan garis isoterm Freundlich yang diperoleh y = 0.0491x + 2.0068 dengan r2 = 86.74%
ABSTRAK
VICTORIA. Adsorpsi Asam Lemak Bebas dan Zat Warna menggunakan
Campuran Kaolin-Limbah Padat Tapioka. Dibimbing oleh KOMAR SUTRIAH
dan HENNY PURWANINGSIH SUYUTI.
Adsorpsi asam lemak bebas pada minyak goreng bekas dan zat warna biru
metilena dikaji dalam penelitian ini. Hasil penelitian menunjukkan bahwa
campuran kaolin dan limbah padat tapioka merupakan adsorben asam lemak
bebas dan zat warna yang potensial. Pengaruh berbagai perlakuan aktivasi kaolin,
seperti suhu pemanasan dan penggunaan asam juga dipelajari. Hasil aktivasi
terbaik untuk kaolin yang digunakan pada adsorpsi asam lemak bebas adalah
aktivasi dengan suhu 750
°
C dilanjutkan dengan perlaku