PEMANFAATAN LIMBAH BUAH TOMAT UNTUK
PRODUKSI BIOETANOL OLEH Saccharomyces cerevisiae
HELDINNIE GUSTY ATIQAH
DEPARTEMEN TEKNOLOGI INDUSTRI PERTANIAN FAKULTAS TEKNOLOGI PERTANIAN
INSTITUT PERTANIAN BOGOR BOGOR
PERNYATAAN MENGENAI SKRIPSI DAN SUMBER
INFORMASI
Dengan ini saya menyatakan bahwa skripsi berjudul Pemanfaatan Limbah Buah Tomat untuk Produksi Bioetanol Oleh Saccharomyces cerevisiae adalah benar karya saya dengan arahan dari dosen pembimbing dan belum diajukan dalam bentuk apa pun kepada perguruan tinggi mana pun. Sumber informasi yang berasal atau dikutip dari karya yang diterbitkan maupun tidak diterbitkan oleh penulis lain telah disebutkan dalam teks dan dicantumkan dalam Daftar Pustaka di bagian akhir skripsi ini.
Dengan ini saya melimpahkan hak cipta dari karya tulis saya kepada Institut Pertanian Bogor.
Bogor, Agustus 2014
Heldinnie Gusty Atiqah
ABSTRAK
HELDINNIE GUSTY ATIQAH. Pemanfaatan Limbah Buah Tomat untuk Produksi Bioetanol oleh Saccharomyces cerevisiae. Dibimbing oleh MUHAMMAD ROMLI.
Buah tomat mengalami kerusakan setelah panen hingga membentuk limbah dalam jumlah cukup besar yaitu 20-50%. Buah tomat yang menjadi limbah umumnya mengalami kerusakan fisik, dimana masih mengandung karbohidrat yang cukup tinggi sehingga berpotensi untuk digunakan sebagai substrat produksi bioetanol. Penelitian ini bertujuan untuk mengevaluasi potensi pemanfaatan limbah buah tomat untuk produksi bioetanol sebagai sumber energi alternatif. Perlakuan awal bahan dilakukan dengan menghidrolisis buah tomat yang telah diblender dengan enzim selulase untuk mengkonversi karbohidrat menjadi gula pereduksi. Proses fermentasi dilakukan dengan menggunakan ragi Saccharomyces cerevisiae pada suhu kamar selama 72 jam. Kadar etanol, pertumbuhan biomassa, dan kadar gula pereduksi sisa diukur setiap 12 jam. Dalam penelitian ini dilakukan evaluasi terhadap pengaruh jumlah inokulum ragi, yaitu 10% dan 15% (v/v) dan pengaruh penambahan urea untuk memperbaiki rasio C/N media. Hasil penelitian menunjukkan bahwa hidrolisis dengan enzim selulase sebesar 30 IU/g serat kasar pada suhu 60oC dan pH 5 selama 3 hari menghasilkan hidrolisat yang dapat meningkatkan gula pereduksi dari 21.6 g/L menjadi 32.6 g/L. Berdasarkan analisa, kadar etanol meningkat dari 1.26% (v/v) dengan 10% ragi menjadi 1.59% (v/v) dengan 15% ragi. Penambahan urea sebagai nutrien dapat meningkatkan kadar etanol dari 1.59% menjadi 1.86% (v/v) dengan 15% inokulum. Waktu optimum fermentasi adalah 60 jam dengan yield etanol/substrat sebesar 0.49 g/g. Pengembangan usaha bioetanol dari limbah tomat dikatakan layak secara finansial dengan Payback Period (PBP) selama 16 tahun dengan nilai R/C ratio sebesar 1.30.
Kata kunci: Limbah tomat, hidrolisis, enzim selulase, ragi Saccharomyces cerevisiae, bioetanol.
ABSTRACT
HELDINNIE GUSTY ATIQAH. Utilization of Tomato Wastes for Bioethanol Production by Saccharomyces cerevisiae. Supervised by MUHAMMAD ROMLI.
hours. Level of ethanol, growth of biomass, and residual of reducing sugar were measured every 12 hours. This research evaluated the effect of inoculums levels at 10% and 15% (v/v) and the effect of adding urea to improve the ratio of C/N media. The results showed that hydrolysis by cellulose enzyme at 30 IU/g of crude fiber at temperature 60oC and pH 5 for 3 days could increase the reducing sugar from 21.6 g/L to 32.6 g/L. Ethanol content resulted from 15% inoculums was higher compared to 10% inoculums, namely 1.59% (v/v) and 1.26% (v/v) respectively. Addition of urea increased the ethanol from 1.59% (v/v) to 1.96% (v/v) in the case of 15% inoculum. The optimum fermentation time was 60 hours with 0.49 g/g yield of ethanol/substrate. Business development of bioethanol from tomato wastes was assessed viable to be financially with Payback Period (PBP) for 16 years and R/C ratio at 1.30.
PEMANFAATAN LIMBAH BUAH TOMAT UNTUK
PRODUKSI BIOETANOL OLEH Saccharomyces cerevisiae
HELDINNIE GUSTY ATIQAH
Skripsi
sebagai salah satu syarat untuk memperoleh gelar Sarjana Teknologi Pertanian
pada
Departemen Teknologi Industri Pertanian
DEPARTEMEN TEKNOLOGI INDUSTRI PERTANIAN FAKULTAS TEKNOLOGI PERTANIAN
INSTITUT PERTANIAN BOGOR BOGOR
Judul Skripsi : Pemanfaatan Limbah Buah Tomat untuk Produksi Bioetanol Oleh Saccharomyces cerevisiae
Nama : HELDINNIE GUSTY ATIQAH NIM : F34100012
Disetujui oleh
Prof.Dr.Ir.Muhammad Romli, M.Sc.St. Pembimbing
Diketahui oleh
Prof.Dr.Ir.Nastiti Siswi Indrasti Ketua Departemen
PRAKATA
Puji dan syukur penulis panjatkan atas kehadirat Allah SWT yang telah memberikan rahmat dan Karunia-Nya sehingga penulis dapat menyelesaikan
skripsi yang berjudul “Pemanfaatan Limbah Buah Tomat untuk Produksi
Bioetanol oleh Saccharomyces cerevisiae” ini.
Terima kasih penulis ucapkan kepada Prof. Dr. Ir. Muhammad Romli, M.Sc.St. selaku dosen pembimbing atas arahan dan bimbingannya selama penulis menyelesaikan penelitian dan skrispi, kepada Prof. Dr-Ing. Ir. Suprihatin dan Drs. Purwoko, M.Si selaku dosen penguji yang telah memberikan saran dan masukan kepada penulis, kepada kedua orang tua tercinta Drs. Helmi dan Dra.Suswati Monats, Rizka, Yaiza, Nana, Kyka, dan Krisna Cahyo Prastyo, serta semua sahabat atas segala kasih sayang, dukungan, dan doanya selama ini. Terima kasih juga penulis sampaikan kepada Departemen Teknologi Industri Pertanian atas dana bantuan penelitian yang telah diberikan, seluruh staf pengajar dan laboran Laboratorium Teknologi Industri Pertanian atas segala ilmu dan bantuannya, serta kepada seluruh keluarga besar Teknologi Industri Pertanian 47 untuk pelajaran dan pengalamannya selama ini.
Penulis berharap agar skripsi ini dapat bermanfaat bagi semua pihak.
Bogor, Agustus 2014
DAFTAR ISI
DAFTAR TABEL x
DAFTAR GAMBAR x
DAFTAR LAMPIRAN x
PENDAHULUAN 1
Latar Belakang 1
Perumusan Masalah 2
Tujuan 2
Manfaat Penelitian 2
Lingkup Penelitian 3
METODE 3
Bahan 3
Alat 3
Prosedur Penelitian 4
HASIL DAN PEMBAHASAN 6
Persiapan dan Karakterisasi Bahan 6
Penelitian Pendahuluan 8
Penelitian Utama 12
Analisis Kelayakan Finansial 22
SIMPULAN DAN SARAN 25
Simpulan 25
Saran 26
DAFTAR PUSTAKA 26
LAMPIRAN 30
DAFTAR TABEL
1 Variabel perlakuan 6
2 Karakteristik limbah tomat 7 3 Jumlah penambahan enzim dan analisis hasil hidrolisis 9 4 Hasil analisis perbandingan gula pereduksi pada dosis enzim 30 IU/g serat
kasar dengan sampel awal tanpa perlakuan hidrolisis 11 5 Perhitungan jumlah urea dalam media fermentasi 11
6 Komponen biaya investasi 23
7 Rincian biaya mesin dan peralatan 23 8 Komponen biaya operasional 23
9 Rincian penerimaan 24
DAFTAR GAMBAR
1 Diagram alir proses fermentasi hidrolisat limbah tomat menggunakan inokulum ragi Saccharomyces cerevisiae 5
2 Limbah buah tomat 6
3 Hidrolisat limbah buah tomat oleh enzim selulase 10 4 Proses fermentasi bioetanol 13 5 Grafik pembentukan etanol pada berbagai variabel perlakuan (a)
percobaan I (b) percobaan II 14 6 Grafik pertumbuhan biomassa pada berbagai variabel perlakuan (a)
percobaan I (b) percobaan II 16 7 Grafik kadar gula pereduksi sisa pada berbagai variabel perlakuan (a)
percobaan I (b) percobaan II 17 8 Hasil analisis fermentasi menggunakan 15% inokulum dan penambahan
urea 19
9 Kurva laju pertumbuhan spesifik maksimum ragi S. cerevisiae dalam
hidrolisat limbah tomat 21
DAFTAR LAMPIRAN
1 Analisis karakteristik bahan 30
2 Uji aktivitas enzim 32
PENDAHULUAN
Latar Belakang
Tomat merupakan bahan pertanian yang bersifat mudah rusak (perishable), sehingga kuantitas pembuangan limbah tomat cukup tinggi, baik dari petani, distributor, maupun pedagang di pasaran. Berdasarkan data Badan Pusat Statistik (2009), potensi limbah tomat sebagai limbah pasar mencapai 114.90 ton/minggu, sedangkan menurut Winarno (1991), potensi kerusakan buah tomat setelah panen adalah sebesar 20-50%. Berdasarkan hal ini, diperlukan alternatif pemanfaatan limbah untuk meningkatan nilai tambahnya dan menekan laju pembuangan limbah ke lingkungan. Kerusakan buah tomat pada umumnya hanya berupa kerusakan fisik dimana tidak mengubah kandungan karbohidrat didalamnya, sehingga salah satu alternatif pemanfaatan yang dapat dilakukan adalah untuk produksi bioetanol.
Teknologi bioetanol dapat menjadi salah satu alternatif solusi yang menjanjikan, dimana bioetanol merupakan sumber energi alternatif terutama sebagai bahan bakar pengganti bensin. Keberadaan bioetanol juga semakin dibutuhkan melihat tingginya permintaan. Menurut Fatony (2010), terjadi kekurangan pasokan bioetanol sebesar 12.17 KL pada tahun 2013 yang dihitung dari selisih antara persediaan dan permintaan bioetanol, dan kekurangan ini diperkirakan akan terus meningkat. Hal ini menjadi acuan bahwa pengembangan bioetanol penting dilakukan untuk memenuhi kebutuhan nasional.
Bioetanol utamanya berasal dari tumbuhan atau substrat yang mengandung karbohidrat berupa gula, pati, dan selulosa melalui tahapan proses fermentasi. Pemanfaatan bioetanol sebagai bahan bakar memiliki beberapa keunggulan dibandingkan dengan energi alternatif terbarukan lainnya, diantaranya adalah etanol merupakan bahan bakar dengan nilai oktan yang tinggi dan dapat menggantikan timbal sebagai pengikat nilai oktan dalam bensin. Selain itu bioetanol mengandung kadar oksigen yang tinggi yaitu sekitar 35% sehingga proses pembakaran dapat berlangsung lebih sempurna (Kusumaningati et al. 2013). Hal ini akan memberikan dampak positif bagi penekanan jumlah emisi oleh hasil pembakaran bahan bakar.
Peningkatan permintaan bahan bakar alternatif dilatarbelakangi oleh menipisnya sumber energi fosil terutama minyak bumi. Ketergantungan yang tinggi terhadap sumber energi fosil dijelaskan dengan data bahwa selama tahun 2007 konsumsi energi global yang bersumber dari minyak bumi sebesar 36%, batubara 27.4%, dan gas alam 23%. Total penggunaan energi fosil ini mencapai 86.4% (EIA 2007). Penggunaan minyak bumi secara terus menerus mengakibatkan menipisnya cadangan minyak mentah di Indonesia. Menurut Ditjen Migas (2012), cadangan minyak mentah di Indonesia hanya sekitar 3.7 milyar barrel dengan tingkat penggunaan mencapai 830 000 barrel per hari, sehingga diperkirakan akan habis dalam kurun waktu sekitar 12 tahun. Hal ini menjadi dasar utama dibutuhkannya sumber energi alternatif terbarukan yang dapat mensubstitusi kebutuhan dunia akan sumber energi tidak terbarukan.
ini mampu menghasilkan kadar etanol dalam jumlah yang cukup tinggi yaitu sekitar 10-15% (Martini 2003). Selain itu, khamir S. cerevisiae diketahui tahan terhadap kadar alkohol yang tinggi hingga 12-18% (v/v), tahan terhadap kadar gula yang tinggi, dan tetap aktif melakukan fermentasi pada suhu 4-32oC (Harrison dan Graham 1970). Pada penelitian ini digunakan khamir
Saccharomyces cerevisiae berupa ragi roti Fermipankarena mudah diperoleh serta harganya yang relatif murah sehingga mempermudah dalam aplikasinya.
Berdasarkan permasalahan lingkungan berupa tingginya jumlah limbah buah tomat, manfaat pengembangan bioetanol sebagai alternatif energi terbarukan, serta ketersediaan inokulum Saccharomyces cerevisiae dalam bentuk ragi roti, menjadi dasar dilakukannya penelitian dengan judul “Pemanfaatan Limbah Buah Tomat Untuk Produksi Bioetanol oleh Saccharomyces cerevisiae”
ini. Melalui penelitian ini diharapkan dapat menjadi acuan dalam pengembangan bioetanol dengan bahan dasar limbah pertanian terutama limbah buah tomat.
Perumusan Masalah
Mengacu pada fokus penelitian berupa pembentukan limbah buah tomat yang cukup besar dan tingginya kandungan karbohidrat didalamnya, maka perumusan masalah dalam penelitian ini adalah mengembangkan alternatif pemanfaatan limbah buah tomat sebagai media fermentasi bioetanol. Peningkatan
yield etanol dapat dipengaruhi oleh jumlah inokulum dan penambahan nutrisi sehingga dilakukan perbandingan dalam bentuk variabel perlakuan meliputi perbedaan konsentrasi ragi dan penambahan nutrisi dalam media.
Tujuan
Tujuan dilakukannya penelitian ini adalah mengetahui potensi pemanfaatan limbah buah tomat sebagai substrat bioetanol, membandingkan kondisi fermentasi terbaik berdasarkan variasi jumlah ragi dan penambahan nutrisi, mengetahui waktu optimum fermentasi substrat limbah tomat menggunakan ragi Saccharomyces cerevisiae dan yield etanol yang dihasilkan, serta menganalisis kelayakan finansial untuk pengembangan produksi bioetanol limbah buah tomat.
Manfaat Penelitian
Manfaat penelitian Pemanfaatan Limbah Buah Tomat untuk Produksi Bioetanol Oleh Saccharomyces cerevisiae antara lain :
1. Bagi peneliti
2. Bagi peneliti lanjutan
Sebagai sumber informasi awal bagi pengembangan bioetanol dengan memanfaatkan limbah buah tomat yang dapat dikembangkan untuk penelitian selanjutnya.
3. Bagi masyarakat
Sebagai sumber informasi mengenai alternatif pemanfaatan limbah buah tomat sebagai substrat produksi bioetanol.
Lingkup Penelitian
Lingkup penelitian ini adalah :
1. Proses hidrolisis secara enzimatis menggunakan enzim selulase.
2. Fermentasi anaerob oleh khamir Saccharomyces cerevisiae berupa ragi roti. 3. Pengukuran hasil fermentasi tiap 12 jam meliputi analisa kadar etanol,
pertumbuhan biomassa, serta kadar gula pereduksi sisa.
4. Penentuan waktu optimum fermentasi menggunakan variabel perlakuan terpilih.
5. Analisis kelayakan finansial usaha bioetanol dari limbah buah tomat berdasarkan Payback Period (PBP) dan R/C ratio.
METODE
Bahan
Bahan baku yang digunakan untuk membuat bioetanol dalam penelitian ini yaitu limbah buah tomat, Saccharomyces cerevisiae berupa ragi roti Fermipan, serta urea yang diperoleh dari Pasar Dramaga Bogor. Bahan kimia dan bahan penunjang lainnya yang digunakan antara lain H2SO4 0.325 N, NaOH 1.25 N,
etanol 95%, H2SO4 pekat, selen, NaOH 40%, H3BO3 4%, indikator mensel, H2SO4
0.02 N, fenol 5%, asam-3.5-dinitrosalisilat, Na-K Tartarat, Na-Metabisulfit, HCl 0.1 N, buffer fosfat sitrat, CMC , enzim selulase, akuades, H2SO4 10%.
Alat
Peralatan yang digunakan untuk pembuatan bioetanol dalam penelitian ini yaitu fermentor berupa labu erlenmeyer skala 300 ml, leher angsa, erlenmeyer 1000 ml, inkubator, mikro pipet, blender, oven, tabung ulir, kapas, kertas saring
whatman No.40, autoklaf, termometer, cawan alumunium, cawan porselen, tanur, penangas hot plate, saringan 60 mesh, desikator, pipet volumetrik,
Prosedur Penelitian
Penelitian ini dilakukan dalam dua tahap, yaitu penelitian pendahuluan dan penelitian utama.
Penelitian Pendahuluan
Persiapan dan Karakterisasi Bahan
Limbah buah tomat diambil dari Pasar Dramaga Bogor dan dicuci dengan menggunakan air bersih. Limbah buah tomat yang telah dibersihkan kemudian dihancurkan menggunakan blender. Setelah memperoleh kondisi yang halus dan homogen, dilakukan analisis pH awal dan analisis proksimat pada bahan meliputi uji kadar air, kadar serat kasar, kadar abu, kadar protein, kadar karbohidrat by difference, total karbon (C), dan total nitrogen (N) sebagai acuan dalam melakukan penelitian utama. Prosedur analisis awal bahan disajikan pada Lampiran 1.
Uji Aktivitas Enzim
Enzim yang digunakan pada proses hidrolisis limbah tomat adalah enzim selulase dengan tujuan untuk menghidrolisis kandungan selulosa dalam bahan agar membentuk glukosa. Uji aktivitas enzim dilakukan untuk mengetahui jumlah enzim yang dibutuhkan untuk melepas µmol gula pereduksi per menit. Metode penentuan aktivitas enzim mengacu pada penelitian Derosya (2010) yang dapat dilihat pada Lampiran 2.
Penentuan Dosis Enzim Selulase
Hidrolisis selulosa pada limbah buah tomat dilakukan dengan menggunakan metode enzimatis. Enzim yang telah diuji aktivitasnya digunakan untuk menghidrolisis bahan dengan beberapa dosis enzim, diantaranya 10 IU, 20 IU, 30 IU, dan 40 IU/g serat kasar. Proses hidrolisis dilakukan pada inkubator suhu 60oC dengan menambahkan buffer fosfat sitrat pH 5 selama 3 hari untuk mengoptimasi kinerja enzim selulase. Hidrolisat tomat yang dihasilkan kemudian dianalisis meliputi uji total gula dan gula pereduksi sesuai dengan metode pada Lampiran 3. Setelah memperoleh kondisi penambahan jumlah enzim terbaik, hidrolisis dilakukan dalam skala yang lebih besar. Hasil hidrolisis yang diperoleh mengalami penyaringan terlebih dahulu agar diperoleh cairan hidrolisat yang homogen untuk digunakan sebagai media fermentasi.
Penyiapan Inokulum Ragi Roti
Penelitian Utama
Tahapan utama dalam proses pembuatan bioetanol adalah proses fermentasi. Proses fermentasi dilakukan untuk memecah gula dalam substrat oleh khamir
Saccharomyces cerevisiae sehingga menghasilkan etanol. Sebanyak 100 ml substrat cair limbah tomat dimasukkan ke dalam fermentor berupa erlenmeyer 300 ml. Selanjutnya ditambahkan nutrisi berupa urea sesuai dengan perhitungan rasio C/N dan diatur pH media pada 4.8. Kemudian media disterilisasi di dalam autoklaf pada suhu 121oC selama 15 menit. Setelah dingin, dilakukan penambahan S. cerevisiae berupa ragi kering Fermipan sebanyak 10% dan 15% dari volume substrat.
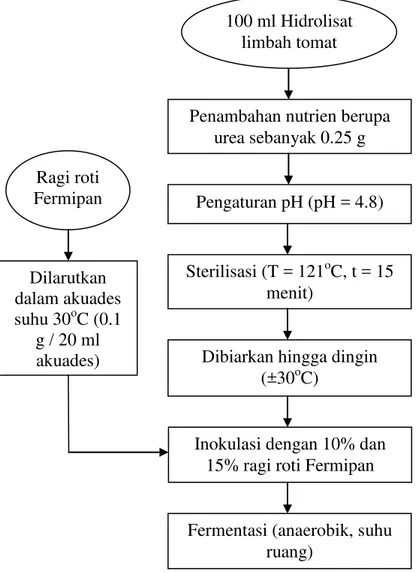
Diagam alir proses fermentasi etanol dari hidrolisat limbah tomat dapat dilihat pada Gambar 1.
Gambar 1 Diagam alir proses fermentasi hidrolisat limbah tomat menggunakan inokulum ragi Saccharomyces cerevisiae
Fermentasi berlangsung pada kondisi anaerob. Fermentor ditutup dengan sumbat dan leher angsa yang diisi dengan asam sulfat encer untuk mencegah kontaminasi dari luar. Proses fermentasi dilakukan pada suhu ruang selama 72 jam. Disamping itu, proses fermentasi diamati setiap 12 jam hingga jam ke-72.
100 ml Hidrolisat limbah tomat
Penambahan nutrien berupa urea sebanyak 0.25 g
Pengaturan pH (pH = 4.8)
Sterilisasi (T = 121oC, t = 15 menit)
Dibiarkan hingga dingin (±30oC)
Inokulasi dengan 10% dan 15% ragi roti Fermipan
Fermentasi (anaerobik, suhu ruang)
Ragi roti Fermipan
Dilarutkan dalam akuades suhu 30oC (0.1
Setelah proses fermentasi selesai, hasilnya dipasteurisasi pada suhu 65oC untuk menginaktifkan mikroorganisme. Tahapan terakhir yang dilakukan adalah analisis kadar etanol, gula pereduksi, dan biomassa dengan prosedur rinci yang terdapat pada Lampiran 4. Variabel perlakuan yang dilakukan pada penelitian ini ditunjukkan pada Tabel 1.
Tabel 1 Variabel perlakuan
Perlakuan Tanpa penambahan nutrisi
Diberi penambahan nutrisi 10% inokulum RATN10 RAN10 15% inokulum RATN15 RAN15
Analisis Kelayakan Finansial
Analisis kelayakan finansial dilakukan untuk melihat potensi pengembangan usaha produksi bioetanol dari limbah buah tomat. Komponen biaya yang dihitung antara lain biaya investasi, biaya tetap, dan biaya variabel. Penerimaan dihitung berdasarkan penjualan output produksi berupa produk utama (bioetanol) dan produk samping (ampas dan sisa hidrolisat). Selanjutnya dilakukan analisis berdasarkan kriteria kelayakan finansial yaitu Payback Period
(PBP) dan Revenue Cost Rasio (R/C ratio).
HASIL DAN PEMBAHASAN
Persiapan dan Karakterisasi Bahan
Limbah buah tomat yang diperoleh dari Pasar Dramaga Bogor mengalami perlakuan pendahuluan berupa pencucian untuk menghilangkan bahan-bahan pengotor, kemudian diblender hingga berukuran halus. Gambar limbah buah tomat yang diperoleh dari Pasar Dramaga Bogor dapat dilihat pada Gambar 2.
Gambar 2 Limbah buah tomat
dikarakterisasi terlebih dahulu, meliputi uji kadar air, kadar abu, kadar protein, dan uji kadar serat kasar. Selain itu, dilakukan pula uji pH dan gula pereduksi dalam bahan untuk mengetahui kesesuaian bahan sebagai media fermentasi agar proses fermentasi dapat berlangsung secara optimal. Karakterisasi limbah buah tomat menghasilkan data yang dapat dilihat pada Tabel 2.
Tabel 2 Karakteristik limbah tomat Parameter analisis Hasil penelitian literatur oleh Direktorat Gizi Departemen Kesehatan (1979) dalam Budiyati dan Haryani (2004) yang menyatakan bahwa kadar air buah tomat masak sebesar 94%. Berdasarkan data tersebut, diketahui kadar air merupakan kandungan paling tinggi dalam buah tomat sehingga menyebabkan buah tomat mudah mengalami kerusakan dan memiliki umur simpan yang rendah.
Perhitungan karbohidrat dilakukan secara by difference tanpa memperhitungkan kadar lemak, karena dianggap sangat kecil dalam limbah buah tomat. Selain komponen air, karbohidrat merupakan komponen tertinggi dalam bahan, yaitu sebesar 3.8% sehingga berpotensi untuk membentuk gula sederhana sebagai substrat fermentasi etanol.
terlalu tinggi maka akan menurunkan efisiensi proses hidrolisis yang terjadi sehingga pada akhirnya akan meningkatkan dosis enzim yang diperlukan.
Kadar protein dilakukan menggunakan metode kjedahl, dimana diperoleh hasil bahwa kadar protein dalam limbah tomat yaitu 0.7%. Apabila dibandingkan dengan data yang diperoleh dari Whfoods.org (2007), kadar protein dalam buah tomat adalah 1.53 g dalam 180 g buah tomat atau setara dengan 0.85%. Hasil ini tidak berbeda jauh dengan hasil penelitian yang telah dilakukan. Total nitrogen (N) diperoleh menggunakan metode yang sama dengan analisis kadar protein sebagai acuan dalam penentuan rasio C/N bahan selanjutnya. Berdasarkan perhitungan, total N dalam buah tomat adalah sebesar 0.12%.
Perhitungan total karbon (C) diperoleh berdasarkan perhitungan “by
difference” sehingga diperlukan perhitungan kadar abu. Kadar abu merupakan kadar residu anorganik dari pembakaran bahan organik pada suhu 550oC (Sudarmadji et al. 1997). Kadar abu limbah buah tomat yang diperoleh berdasarkan hasil uji adalah 0.35%, sehingga melalui perhitungan total C yang dihasilkan adalah 2.47%. Berdasarkan hasil tersebut, maka dapat diketahui total C dan N pada limbah buah tomat yang kemudian digunakan sebagai faktor konversi untuk memperhitungkan kebutuhan penambahan nutrisi berupa urea. Selanjutnya, hasil uji pH menunjukkan bahwa limbah buah tomat berada pada pH 4.98. Analisis pH awal bahan ini diperlukan untuk menyesuaikan kondisi media agar diperoleh kondisi optimum media fermentasi.
Penelitian Pendahuluan
Uji Aktivitas Enzim dan Penentuan Dosis Enzim
Sebelum dilakukan proses hidrolisis limbah buah tomat, terlebih dahulu dilakukan analisis aktivitas enzim selulase yang akan digunakan. Aktivitas enzim diperlukan untuk mengkonversi kebutuhan enzim yang akan ditambahkan kedalam substrat yang dihidrolisis. Satu unit enzim selulase adalah 1 µmol produk yang terbentuk dalam 1 menit (Suyandra 2007). Uji aktivitas enzim dilakukan mengacu pada metode penelitian Derosya (2010) dengan terlebih dahulu membuat kurva standar glukosa menggunakan buffer fosfat sitrat pH 5 dalam berbagai konsentrasi. Perhitungan aktivitas enzim yang diperoleh berdasarkan analisis yang dilakukan adalah sebesar 414 IU/g serat kasar.
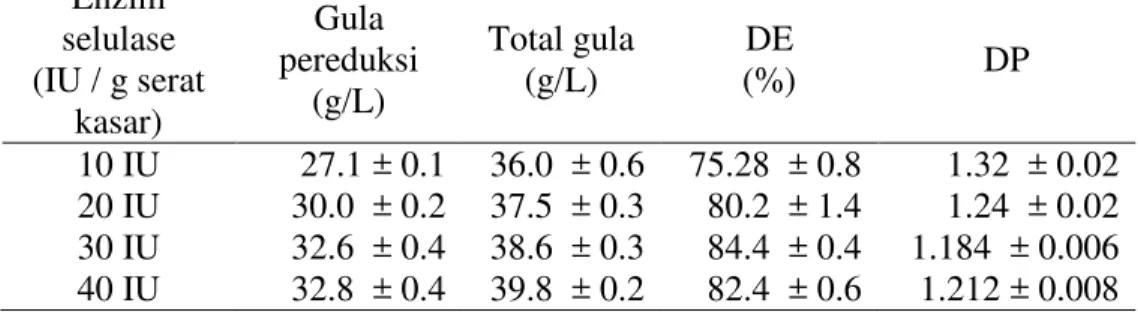
pada Lampiran 3. Kadar gula pereduksi, total gula, nilai DE dan DP yang diperoleh dari hasil hidrolisis limbah buah tomat dapat dilihat pada Tabel 3.
Tabel 3 Jumlah penambahan enzim dan analisis hasil hidrolisis Enzim
Nilai Dextrose Equivalent (DE) diperoleh berdasarkan rasio antara gula pereduksi dengan total gula hidrolisat limbah buah tomat. Kadar gula total menunjukkan jumlah keseluruhan komponen gula dalam bahan yang telah dihidrolisis, sedangkan gula pereduksi menunjukkan jumlah komponen gula yang ujung rantainya mengandung gugus aldehida atau keton bebas. Gula pereduksi terdiri dari semua monosakarida yaitu glukosa, fruktosa, galaktosa, dan disakarida yaitu laktosa dan maltosa. Nilai DE ini diperlukan untuk mengetahui efektivitas enzim selulase dalam menghidrolisis limbah buah tomat membentuk glukosa. Semakin tinggi nilai DE, maka menunjukkan bahwa kandungan glukosa dalam bahan semakin tinggi pula (Palmer 1970). Menurut Tjokroadikoesoemo (1986), konversi sempurna selulosa memberikan nilai DE = 100, sedangkan nilai DE = 0 apabila tidak terjadi hidrolisis.
Berdasarkan perbandingan hasil hidrolisis dari ketiga dosis enzim, hidrolisis menggunakan 30 IU enzim selulase menghasilkan nilai DE paling tinggi dibandingkan perlakuan lainnya. Pada dosis enzim yang lebih tinggi yaitu 40 IU/gr serat kasar, nilai DE justru cenderung menurun. Hal ini menunjukkan bahwa konsentrasi enzim merupakan faktor penentu aktivitas enzim, dimana terdapat batas maksimum konsentrasi enzim sehingga ketika konsentrasi melebihi batasnya, proses hidrolisis tidak berlangsung sempurna. Enzim selulase tetap melakukan hidrolisis pada selulosa, namun tidak sampai pada pembentukan glukosa, melainkan membentuk disakarida berupa selobiosa sehingga menyebabkan penambahan gula total yang lebih tinggi dibandingkan pembentukan gula pereduksi.
Pada dasarnya, enzim selulase merupakan kompleks yang terdiri dari tiga enzim utama yang saling bekerja sama dan bekerja saling berurutan, yaitu enzim endoglukonase, eksoglukonase, dan β-glukosidase. Pada mulanya enzim endoglukonase menguraikan kristal penyusun serat selulosa dengan memutus ikatan pada rantai kristal membentuk selulosa tunggal. Selanjutnya enzim eksoglukonase menguraikan selulosa tunggal membentuk unit-unit selobiosa yang merupakan disakarida. Selobiosa kemudian dikonversi oleh enzim β-glukosidase membentuk glukosa (Jeewon 1997 dalam Farikha 2010).
0.4%. Hal ini menjadi acuan dalam melakukan hidrolisis bahan dalam jumlah lebih besar untuk digunakan sebagai media fermentasi.
Hidrolisis Substrat oleh Enzim Selulase
Proses hidrolisis dilakukan secara enzimatis menggunakan enzim selulase. Enzim selulase merupakan jenis enzim yang bekerja secara spesifik untuk mengkatalisis terjadinya reaksi pemecahan selulosa menjadi glukosa. Hidrolisis secara enzimatis pada dasarnya memiliki beberapa kelebihan dibandingkan dengan hidrolisis asam, diantaranya adalah reaksi yang berlangsung lebih ringan (suhu rendah, tidak mempengaruhi pH), memberikan hasil hidrolisis yang lebih tinggi, tidak menimbulkan degradasi gula hasil hidrolisis, serta membutuhkan biaya pemeliharaan peralatan yang lebih rendah karena tidak terjadi reaksi korosif oleh bahan (Taherzadeh dan Karimi 2007). Selain itu, penggunaan enzim diharapkan dapat mengurangi pencemaran lingkungan akibat asam.
Buah tomat mengandung karbohidrat yang cukup tinggi, dimana terdapat kandungan gula fruktosa dan glukosa, serta pektin, selulosa, dan hemiselulosa (Anonim 2014). Berdasarkan hasil analisis yang telah dilakukan, diperoleh kadar karbohidrat sebesar 3.8% dengan kadar serat kasar yaitu 0.96%. Jumlah kadar serat kasar ini menjadi acuan dalam penambahan konsentrasi enzim selulase pada substrat. Pada dasarnya selulosa merupakan komponen utama penyusun dinding sel tanaman. Berdasarkan hal ini, maka proses hidrolisis selulosa dalam buah tomat dilakukan menggunakan enzim selulase dengan tujuan untuk memperoleh kandungan glukosa yang lebih tinggi pada substrat.
Berdasarkan data total gula pereduksi yang diperoleh dalam beberapa dosis enzim selulase yang digunakan, maka dapat diketahui bahwa penggunaan enzim selulase sebanyak 30 IU/g serat kasar merupakan dosis enzim yang lebih optimum dibandingkan dosis enzim lainnya. Dengan menggunakan data tersebut, selanjutnya dilakukan hidrolisis bahan dalam jumlah yang lebih besar yaitu sejumlah 2 kg limbah tomat dihidrolisis menggunakan 30 IU/g serat kasar enzim selulase. Dari hidrolisis tersebut, dihasilkan hidrolisat limbah tomat sebanyak 2.33 L dengan residu berupa ampas sebesar 280.86 g, atau dengan kata lain rendemen hidrolisat yang dihasilkan adalah sebesar 85.96% (b/b). Hidrolisat limbah buah tomat ditunjukkan pada Gambar 3. Neraca massa proses hidrolisis dilampirkan pada Lampiran 8.
Hidrolisat yang diperoleh kemudian diuji kadar gula pereduksinya sebagai acuan dalam melakukan proses fermentasi. Berdasarkan hasil hidrolisis pada dua kali percobaan, terlihat bahwa terjadi peningkatan kadar gula pereduksi akibat konversi selulosa membentuk gula-gula sederhana. Kadar gula pereduksi dalam limbah buah tomat awal sebelum hidrolisis dengan hasil hidrolisis ditunjukkan pada Tabel 4.
Tabel 4 Hasil analisis perbandingan gula pereduksi pada dosis enzim 30 IU/g serat kasar dengan sampel awal tanpa perlakuan hidrolisis
Percobaan ke- Gula pereduksi
Penentuan Persentase Penambahan Nutrisi Pada Media Fermentasi
Proses fermentasi etanol tidak hanya membutuhkan glukosa sebagai sumber karbon, namun juga membutuhkan sumber nutrisi pendukung lainnya terutama sumber nitrogen. Penambahan nutrien yang cukup dan sesuai dengan kondisi medium akan meningkatkan aktivitas mikroorganisme. Peningkatan aktivitas mikroorganisme tentunya akan berbanding lurus dengan peningkatan produksi etanol yang dihasilkan. Sumber nitrogen yang biasa digunakan dalam proses fermentasi etanol antara lain adalah ekstrak khamir, corn step liquor, ammonium sulfat, urea, protein, ekstrak gandum, dan bahan lainnya yang pada dasarnya memiliki kandungan nitrogen dalam jumlah tinggi. Pada penelitian ini digunakan urea sebagai sumber nitrogen pada proses fermentasi yang dilakukan. Pemilihan urea disebabkan oleh faktor kemudahan dalam memperolehnya serta harganya yang relatif lebih murah dibandingkan sumber nitrogen lainnya.
Penambahan nutrisi berupa urea kedalam media fermentasi menjadi salah satu faktor yang diamati pada penelitian ini. Jumlah penambahan urea ini didasarkan pada kebutuhan nitrogen pada substrat mengacu pada perbandingan total karbon (C) dan total nitrogen (N) pada media tomat. Perbandingan total C/N substrat berdasarkan hasil analisa yang telah dilakukan adalah sebesar 20.58. Menurut Syamsu et al. (2002) dalam Haryani (2008), rasio C/N yang dibutuhkan sebagai media fermentasi etanol adalah sebesar 10, sehingga pada total C dan total N yang masing – masing sebesar sebesar 2.47% dan 0.12%, dibutuhkan 0.12% nitrogen yang harus ditambahkan kedalam substrat. Perhitungan kebutuhan urea yang diperlukan ditampilkan pada tabel 5.
Penelitian Utama
Proses Fermentasi
Proses fermentasi dilakukan secara anaerobik melalui aktivitas khamir
Saccharomyces cerevisiae berupa ragi roti untuk mengkonversi gula dalam substrat membentuk etanol dan CO2. Saccharomyces cerevisiae dapat
memproduksi etanol dari glukosa dalam keadaan anaerob. Penggunaan khamir
Saccharomyces cerevisiae sebagai inokulum dalam produksi etanol telah banyak dilakukan disebabkan beberapa keunggulannya, antara lain dapat menghasilkan etanol dalam jumlah yang tinggi, toleran terhadap kadar etanol dan suhu fermentasi yang tinggi, bersifat stabil terhadap perubahan kondisi fermentasi, serta mampu bertahan hidup pada pH yang rendah (Rehm dan Reed 1981). S.
cerevisiae memiliki sistem metabolisme gula secara anaerobik yang efisien dan memiliki daya toleran terhadap inhibitor yang lebih baik dibanding mikroorganisme lainnya. Reaksi pembentukan etanol dari substrat berupa gula oleh khamir S.cerevisiae adalah sebagai berikut (Oura dalam Dellweg 1983).
C6H12O6 2 C2H5OH + 2 CO2 + 2 ATP + 54 Kkal
Pada dasarnya, proses fermentasi etanol oleh khamir melalui aktivitas metabolisme glukosa membentuk asam piruvat dalam tahapan reaksi pada jalur
Embden Meyerhoff Parnas (EMP) atau glikolisis. Asam piruvat yang dihasilkan dalam jalur EMP kemudian mengalami dekarboksilasi membentuk asetaldehida dan CO2, lalu mengalami proses dehidrogenasi sehingga terkonversi menjadi
etanol (Amerine et al. 1987). Pembentukan etanol dari asam piruvat terjadi melalui reaksi sebagai berikut.
CH3COCO2H CH3CHO C2H5OH
Asam piruvat Asetaldehida Etanol
Proses fermentasi yang dilakukan terhadap substrat limbah buah tomat mengacu pada dua variabel, yaitu penambahan nutrisi dan konsentasi inokulum yang digunakan. Sebanyak 100 ml hidrolisat limbah buah tomat dimasukkan dalam erlenmeyer 300 ml dan diberikan penambahan urea untuk sampel yang diberi perlakuan penambahan nutrisi. Kemudian dilakukan pengaturan pH terlebih dahulu hingga berada tepat pada pH 4.8 untuk mengatur aktivitas fermentasi yang sesuai dengan pertumbuhan khamir didalamnya. Hal ini disebabkan kecepatan fermentasi akan mencapai titik optimum pada pH 4.8 (Rinaldy 1987). Selanjutnya substrat disterilisasi dalam autoklaf selama 15 menit pada suhu 121oC untuk mematikan mikroorganisme lain yang dapat mengganggu proses fermentasi. Setelah proses sterilisasi selesai, substrat kemudian didinginkan pada suhu ruang hingga mencapai suhu sekitar 30oC untuk dilakukan inokulasi.
Inokulasi ragi roti dilakukan sesuai dengan konsentrasi yang telah ditentukan yaitu 10% dan 15% dari jumlah substrat. Ragi roti sebelumnya dilarutkan terlebih dahulu dalam akuades suhu 30oC dengan konsentrasi sebesar 0.1 g ragi roti dalam 20 ml air. Hal ini mengacu pada penelitian Suyandra (2007) yang menyatakan bahwa ragi roti sebanyak 0.1 g dalam 20 ml air memiliki jumlah
sel yang hampir serupa dengan inokulum menggunakan 1 ose khamir
Saccharomyces cerevisiae yaitu sebesar 7.97 x 104 sel/ml inokulum.
Selanjutnya substrat dikondisikan dalam keadaan anaerob melalui penggunaan leher angsa pada labu erlenmeyer yang digunakan. Proses fermentasi dilakukan pada suhu kamar dan dibiarkan selama 72 jam. Menurut Paturau (1981), waktu yang biasa digunakan dalam fermentasi etanol adalah 30 – 72 jam, sedangkan suhu yang optimum digunakan untuk fermentasi adalah berkisar antara 25 – 30oC (Frazier dan Westhoff 1978). Hal ini merupakan acuan pada pelaksanaan proses fermentasi agar diperoleh kondisi optimum produksi etanol. Gambaran proses fermentasi yang dilakukan ditunjukkan pada gambar 4.
Gambar 4 Proses fermentasi bioetanol
Waktu fermentasi substrat limbah buah tomat pada awalnya belum dapat ditentukan karena belum diketahui waktu optimumnya. Oleh sebab itu, dilakukan pengamatan setiap 12 jam untuk melihat kurva produksi etanol yang terbentuk serta pertumbuhan biomassa selama proses fermentasi. Berdasarkan hal tersebut, setiap 12 jam proses fermentasi dilakukan pengamatan terhadap kadar etanol, pertumbuhan biomassa, serta kadar gula pereduksi sisa untuk mengetahui pola konsumsi glukosa oleh khamir Saccharomyces cerevisiae.
Analisis Hasil Fermentasi
Pemilihan Variabel Perlakuan Optimum
(a)
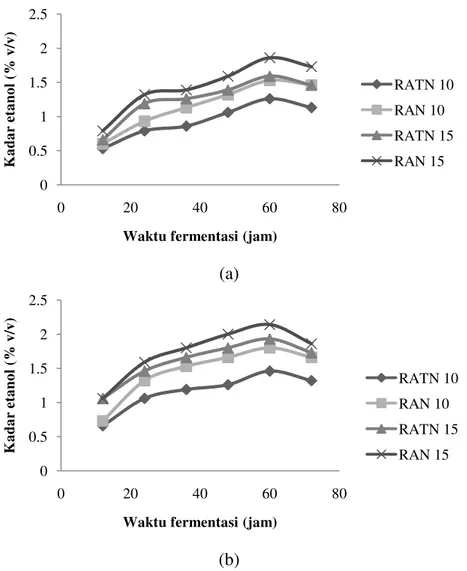
(b)
Gambar 5 Grafik pembentukan etanol pada berbagai variabel perlakuan (a) percobaan I (b) percobaan II
Gambar 5 menunjukkan pola pembentukan etanol pada berbagai waktu yaitu dari 12 – 72 jam waktu fermentasi. Pada grafik dapat pula dilihat pengaruh antar perlakuan terhadap kadar etanol yang dihasilkan. Percobaan I dan II dilakukan menggunakan substrat dengan kadar gula awal yang berbeda. Berdasarkan pola yang terbentuk, secara garis besar dapat terlihat bahwa etanol mengalami peningkatan dimulai dari awal pengamatan hingga jam ke 60, sedangkan pada waktu fermentasi 72 jam terjadi penurunan kadar etanol pada kedua percobaan. Hal ini diduga karena peristiwa inhibitor akibat penghambatan dari kadar etanol yang dihasilkan. Menurut Clark dan Mackie (1984), khamir sangat peka pada etanol ketika konsentrasi etanol telah mencapai 1-2% (v/v) sehingga dapat menghambat proses fermentasi. Pada konsentrasi etanol 10% (v/v), pertumbuhan khamir justru akan berhenti sama sekali. Mengacu pada hasil yang diperoleh, ketika kadar etanol mencapai kadar 1.26 – 2.09% (v/v) pada kedua ulangan, maka akan terjadi penghambatan proses fermentasi yang ditunjukkan pada waktu fermentasi 72 jam.
Perlakuan yang diberikan pada setiap media fermentasi menghasilkan data bahwa perbedaan konsentrasi inokulum mempengaruhi produksi etanol yang terbentuk. Substrat dengan konsentrasi inokulum 15% dapat menghasilkan etanol
yang lebih tinggi yaitu 1.59% (v/v) dibandingkan 10% inokulum yang menghasilkan kadar etanol sebesar 1.26% (v/v) pada percobaan I. Pada percobaan II, konsentrasi inokulum 15% dapat meningkatkan kadar etanol dari 1.46% (v/v) menjadi 1.93% (v/v). Data tersebut menunjukkan bahwa konsentrasi inokulum sebanyak 10% belum dapat mengkonversi gula secara optimal, sehingga pada konsentrasi inokulum yang lebih tinggi kinerja yang terjadi akan semakin baik.
Variabel lainnya yang diamati adalah pengaruh penambahan nutrisi berupa urea dalam media fermentasi. Kebutuhan nutrisi merupakan salah satu faktor penting yang mempengaruhi pertumbuhan dan perkembangan mikroorganisme. Unsur – unsur dasar yang dibutuhkan khamir antara lain adalah karbon yang dapat diperoleh dari gula dalam substrat, serta nitrogen, oksigen, fosfor, kalium, zat besi, dan unsur kelumit lainnya. Nutrisi tambahan ini utamanya diperlukan untuk pemeliharaan sel dan pertumbuhan mikroba. Berdasarkan hal inilah, diperlukan nutrisi tambahan terutama sumber nitrogen yang merupakan makronutrien bagi khamir. Teori tersebut didukung oleh hasil fermentasi yang menunjukkan bahwa penambahan urea dapat meningkatkan kadar etanol dari 1.26% (v/v) menjadi 1.53% (v/v) pada percobaan I dan meningkat dari 1.46% (v/v) menjadi 1.80% (v/v) pada percobaan II menggunakan 10% inokulum. Penambahan urea dengan 15% inokulum mengakibatkan peningkatan etanol dari 1.59% (v/v) menjadi 1.86% (v/v) pada percobaan I dan 1.93% (v/v) menjadi 2.09% (v/v) pada percobaan II.
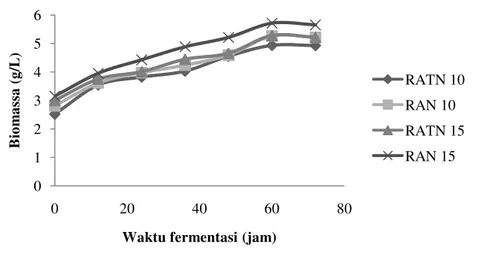
Kinerja fermentasi pada dasarnya dapat pula dianalisis mengacu pada pertumbuhan biomassa serta konsumsi substrat yang dilihat dari kadar gula pereduksi sisa. Biomassa merupakan salah satu analisis yang dibutuhkan untuk mengetahui pola pertumbuhan khamir yang terjadi selama proses fermentasi berlangsung. Secara teoritis, semakin tinggi nilai biomassa menunjukkan bahwa pertumbuhan sel mikroorganisme semakin tinggi. Hal ini disebabkan oleh terjadinya konsumsi substrat oleh khamir sehingga terjadi peningkatan jumlah sel. Biomassa yang terhitung dari hasil analisis menggunakan metode sentrifugasi dan dilanjutkan dengan pengeringan pada suhu 50oC merupakan jumlah sel kering yang terdapat dalam cairan fermentasi (Sari 2009).
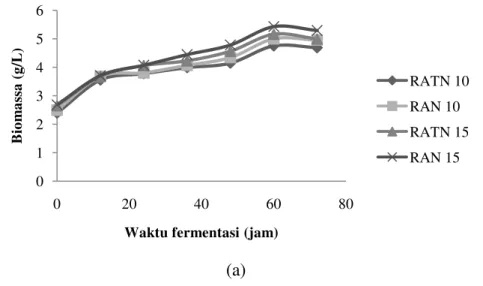
(b)
Gambar 6 Grafik pertumbuhan biomassa pada berbagai variabel perlakuan (a) percobaan I (b) percobaan II
Menurut Fardiaz (1988), pada mulanya mikroorganisme akan mengalami fase adaptasi ketika dipindahkan ke dalam suatu medium untuk menyesuaikan dengan kondisi lingkungannya. Lamanya fase adaptasi dapat dipengaruhi oleh medium dan lingkungan pertumbuhan serta jumlah inokulum yang ditambahkan. Pada Gambar 6, tidak terlihat fase adaptasi khamir S. cerevisiae, yang mungkin disebabkan oleh konsentrasi substrat yang tidak terlalu tinggi sehingga kultur dapat langsung memanfaatkan substrat yang ada. Menurut Wang et al. (1979), konsentrasi substrat mempengaruhi lamanya fase adaptasi oleh kultur, akibat adanya penghambatan pada pertumbuhan mikroorganisme yang digunakan. Kondisi ini disebut sebagai penghambatan oleh substrat (substrate inhibition).
Setelah melalui fase adaptasi, mikroorganisme memasuki fase log atau eksponensial, dimana mikroorganisme membelah dengan cepat. Fase ini merupakan kondisi yang ideal bagi mikroorganisme (Judoamidjojo et al. 1989). Terlihat pada grafik bahwa pertumbuhan mikroorganisme selama fermentasi terus mengalami peningkatan hingga jam ke-12, dan setelahnya pertumbuhan berlangsung statis. Hal ini terjadi karena nutrisi dalam media sudah berkurang serta terakumulasinya hasil metabolisme yang mungkin beracun sehingga dapat menghambat pertumbuhan mikroorganisme. Pada fermentasi hidrolisat tomat ini, pertumbuhan khamir yang terjadi memang tidak terlihat begitu signifikan, hal ini dapat disebakan oleh konsentrasi awal substrat yang hanya ± 3.2% sehingga pertumbuhannya tidak berlangsung secara optimal. Menurut Paturau (1981), konsentrasi gula yang paling baik digunakan sebagai substrat fermentasi berkisar antara 14-18% (b/v).
Berdasarkan grafik pertumbuhan biomassa pada Gambar 6 juga terlihat bahwa pertumbuhan biomassa semakin meningkat dipengaruhi dengan jumlah inokulum dan penambahan nutrien yang ditambahkan dalam media fermentasi. Pada waktu fermentasi 60 jam dimana terjadi fase stasioner menunju fase kematian pada sel, biomassa yang dihasilkan meningkat dari 4.75 g/L pada inokulum 10% menjadi 5.26 g/L pada inokulum 15% untuk percobaan I dan meningkat dari 4.99 g/L menjadi 5.42 g/L untuk percobaan II. Melalui penambahan nutrisi, terjadi pertumbuhan biomassa menjadi 4.99 g/L untuk
percobaan I dan 5.26 g/L untuk percobaan II pada inokulum 10% serta 5.43 g/L untuk percobaan I dan 5.71 g/L untuk percobaan II pada inokulum 15%.
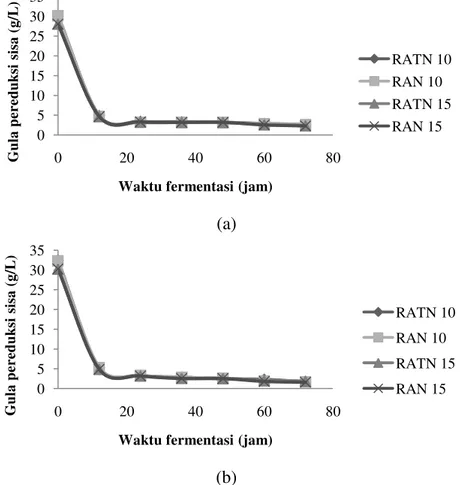
Pola pembentukan produk dan pertumbuhan sel khamir ini merupakan hasil dari konsumsi gula sehingga akan terjadi penurunan kadar gula pereduksi dalam substrat. Pada hasil analisis yang telah dilakukan, diketahui bahwa kadar gula pereduksi sisa terus berkurang dengan bertambahnya waktu fermentasi yang dilakukan. Kadar gula pereduksi sisa antar variabel RATN10, RAN10, RATN15, RAN15 pada jam ke-60 berturut turut adalah 2.88 g/L, 2.83 g/L, 2.59 g/L, 2.55 g/L pada percobaan I dan 2.32 g/L, 2.08 g/L, 1.98 g/L, 1.79 g/L pada percobaan II. Grafik penurunan kadar gula sisa antar perlakuan pada berbagai waktu pengamatan dapat dilihat pada Gambar 7.
(a)
(b)
Gambar 7 Grafik kadar gula pereduksi sisa pada berbagai variabel perlakuan (a) percobaan I (b) percobaan II
Pada dasarnya, semakin tinggi tingkat konsumsi substrat oleh khamir akan meningkatkan kadar etanol yang dihasilkan, karena semakin banyak gula yang terkonversi menjadi produk. Hal ini dapat dikaitkan pada perlakuan RAN 15 yang menghasilkan sisa gula pereduksi terkecil sehingga menghasilkan pertumbuhan biomassa serta kadar etanol yang lebih tinggi dibandingkan perlakuan lainnya. Tingkat konsumsi substrat pada masing- masing perlakuan RATN 10, RAN 10, RATN 15, RAN 15 adalah 91.26%, 91.42%, 92.12%, 92.26% untuk percobaan I. Pada percobaan II, diperoleh tingkat konsumsi substrat berturut-turut adalah
93.54%, 94.22%, 94.46%, 94.98%. Menurut Pacheco et al. (2010), tingkat penggunaan gula pada umumnya berkisar antara 44.8-96.5%.
Mengacu pada kadar etanol yang dihasilkan, pertumbuhan sel, serta tingkat penggunaan gula antar perlakuan, dapat dihitung yield pembentukan produk (Yp/s) dan yield pertumbuhan biomassa (Yx/s) per substrat yang
dikonsumsi. Nilai yield yang terhitung dapat digunakan sebagai acuan dalam penentuan variabel perlakuan paling optimum pada proses fermentasi. Nilai Yp/s
masing-masing variabel perlakuan pada waktu fermentasi 60 jam dimana diperoleh kadar etanol tertinggi yaitu 0.33 g/g, 0.40 g/g, 0.41 g/g, 0.48 g/g berturut-turut pada sampel RATN 10, RAN 10, RATN 15, dan RAN 15 untuk percobaan I. Pada percobaan II, nilai Yp/s terhitung yaitu 0.34 g/g, 0.42 g/g, 0.44
g/g, 0.48 g/g untuk sampel RATN 10, RAN 10, RATN 15, RAN 15. Data tersebut menunjukkan bahwa kadar etanol tertinggi yang terbentuk per g gula yang dikonsumsi diperoleh pada perlakuan fermentasi menggunakan 15% inokulum disertai penambahan urea.
Perhitungan nilai Yx/s juga menunjukkan bahwa pertumbuhan biomassa
tertinggi per g gula yang dikonsumsi oleh khamir adalah pada hasil fermentasi dengan menggunakan 15% inokulum dan penambahan urea. Pada percobaan I, nilai Yx/s untuk sampel RATN 10, RAN 10, RATN 15, RAN 15 adalah 0.078 g/g,
0.083 g/g, 0.086 g/g, dan 0.090 g/g pada waktu fermentasi 60 jam, sedangkan pada percobaan II yaitu 0.072 g/g, 0.073 g/g, 0.073 g/g, dan 0.075 g/g. Mengacu pada data kedua percobaan tersebut (Lampiran 5), dapat ditentukan bahwa jumlah inokulum dan penambahan nutrien dalam media memiliki pengaruh terhadap hasil fermentasi. Semakin banyak inokulum yang ditambahkan dan perlakuan penambahan nutrien berupa urea akan memicu kinerja fermentasi sehingga membentuk hasil yang optimum. Hal ini menjadi dasar bahwa jumlah inokulum 15% dan penambahan urea (RAN 15) merupakan variabel perlakuan paling baik dibandingkan perlakuan lainnya.
Penentuan Waktu Optimum Fermentasi
Perlakuan paling optimum yang telah ditentukan sebelumnya menjadi acuan dalam penentuan waktu optimum fermentasi. Media fermentasi dengan penambahan urea dan inokulasi 15% ragi difermentasi secara duplo selama 72 jam agar diperoleh data yang dapat dianalisis secara statistika. Pengamatan dilakukan pada waktu fermentasi 12, 36, 60, dan 72 jam meliputi kadar etanol, biomassa, serta kadar gula pereduksi sisa. Hasil fermentasi yang dihasilkan dapat terlihat melalui grafik pada Gambar 8.
Menurut Shuler dan Kargi (1992), pertumbuhan berasosiasi dengan pembentukan produk (growth associated) ini terjadi ketika laju pembentukan spesifik produk berbanding lurus dengan laju spesifik pertumbuhan. Pola pertumbuhan tersebut terjadi pada pembentukan produk metabolit primer, misalnya etanol.
Gambar 8 Hasil analisis fermentasi menggunakan 15% inokulum dan penambahan urea
Gambar 8 menunjukkan bahwa pada waktu fermentasi 12 dan 36 jam terjadi pembentukan etanol yang cukup tinggi hingga mencapai kadar etanol maksimumnya pada jam ke-60 sebesar 13.8±0.6 g/L atau setara dengan 1.74±0.08% (v/v). Pada waktu fermentasi 72 jam, terjadi kecenderungan penurunan sintesis produk yang dapat disebabkan terjadinya inhibisi oleh etanol yang terbentuk, dimana kadar etanol sebesar 1.74% tersebut dapat menyebabkan terjadinya denaturasi dinding sel khamir yang menyebabkan rusaknya sel. Hal ini akan menghambat aktivitasnya hingga menyebabkan kematian sel.
Berdasarkan analisis sidik ragam yang dilakukan dengan tingat kepercayaan 95% (Lampiran 6), dihasilkan bahwa pengaruh waktu fermentasi menunjukkan perbedaan yang signifikan pada jam ke 0, 12, 36, dan 60, namun pada waktu fermentasi 60 dan 72 jam tidak terdapat perbedaan nyata. Hal ini memberikan acuan bahwa kadar etanol maksimum mampu dicapai pada jam ke 60, dan tidak adanya perbedaan yang signifikan ketika fermentasi dilanjutkan hingga 72 jam. Oleh sebab itu, waktu optimum fermentasi hidrolisat limbah tomat menggunakan ragi S.cerevisiae adalah 60 jam.
Kinetika Fermentasi
Kinetika fermentasi berkaitan dengan pertumbuhan mikroorganisme, konsumsi substrat, dan pembentukan produk oleh mikroorganisme. Pertumbuhan mikrobial ditunjukkan dengan meningkatnya jumlah massa dan sel, yang dipengaruhi oleh kondisi lingkungan fisik dan kimianya. Pertumbuhan mikroorganisme dapat diartikan sebagai waktu yang dibutuhkan untuk menggandakan massa atau jumlah sel. Pada fase eksponensial, sel telah beradaptasi dengan lingkungannya sehingga sel akan tumbuh dengan cepat. Massa sel dan jumlah sel akan bertambah secara eksponensial terhadap waktu dimana terjadi balance gowth, yaitu semua komponen dalam sel tumbuh dengan kecepatan yang sama. Laju pertumbuhan pada fase eksponensial mengikuti persamaan diferensial orde pertama (Shuler and Kargi 1992).
dX
dt = µ X
Pada fermentasi batch, laju pertumbuhan spesifik adalah konstan dan tidak tergantung pada perubahan konsentrasi nutriennya (Stanbury and Whitaker 1993), sehingga akan terjadi integrasi menghasilkan :
Ln x2
x1 x2
x1 = µ ∆t
Dimana :
µ = laju pertumbuhan spesifik (jam-1) x2 = biomassa sel pada saat t (g/L)
x1 = biomassa sel awal (g/L)
t = waktu (jam)
Parameter lainnya dalam kinetika fermentasi yang menggambarkan efisiensi konversi substrat menjadi biomassa atau produk dan biomassa menghasilkan produk ditunjukkan oleh yield biomassa per substrat (Yx/s), yield
produk per substrat (Yp/s), serta yield produk per biomassa (Yp/x) (Collins dan Walter dalam Bouwkamp 1985).
Y x s=X−Xo
So−S Y
p
s=PSo−−PoS Yp x=PX−−PoXo
Gambar 9 Kurva laju pertumbuhan spesifik ragi S. cerevisiae dalam hidrolisat limbah tomat
Berdasarkan gambar 9, terlihat bahwa laju pertumbuhan spesifik khamir mengalami peningkatan hingga jam ke-12, selanjutnya menurun hingga akhir fermentasi. Ini juga menunjukkan bahwa pada rentang waktu tersebut khamir berada dalam fase eksponensial dan mengalami peningkatan hingga mencapai titik maksimal, yaitu µmaks. Setelah melewati fase eksponensial, laju pertumbuhan
khamir terus menurun yang menandakan bahwa khamir berada dalam pertumbuhan lambat. Penurunan ini terus berlangsung hingga akhirnya terhenti ketika khamir mengalami fase stasioner, dimana nilai µ akan tetap.
Laju pertumbuhan spesifik khamir dalam media fermentasi hidrolisat tomat pada waktu fermentasi 12, 36, 60, dan 72 jam berturut – turut adalah 0.014, 0.012, 0.008, dan 0.007 jam-1, sehingga ditentukan bahwa µmaks khamir yaitu
0.014 jam-1 pada jam ke-12 fermentasi. Selanjutnya ditentukan pula nilai Yp/s dan Yx/s yang dibutuhkan untuk mengetahui jumlah substrat yang dibutuhkan untuk menghasilkan jumlah produk tertentu, guna meningkatkan efisiensi fermentasi. Hasil penelitian menunjukkan nilai Yp/s = 0.49 ± 0.01 g produk/g substrat, Yx/s = 0.062 ± 0.001 g biomassa/g substrat, dan Yp/x = 7.9 ± 0.4 g produk/g biomassa pada jam optimumnya yaitu 60 jam. Menggunakan nilai Yp/x dan Yx/s tersebut, dapat diketahui laju spesifik pembentuk produk (qp) dan laju spesifik penggunaan
substrat (qs) mengacu pada laju pertumbuhan spesifik maksimumnya. Nilai qp dan
qs berturut-turut adalah 0.119 g/g sel.jam-1 dan 0.241 g/g sel.jam-1. Data
perhitungan kinetika fermentasi dapat dilihat pada Lampiran 7.
Apabila dibandingkan dengan penelitian yang dilakukan oleh Suyandra (2007), kinetika fermentasi hidrolisat pati sagu dengan kultur murni S.cerevisiae
menghasilkan Yp/s = 0.2459 g produk/g substrat, Yx/s = 0.0386 g biomassa/g substrat, dan Yp/x = 6.2275 g produk/g substrat. Ini menunjukkan bahwa yield
Analisis Kelayakan Finansial
Potensi pemanfaatan limbah buah tomat sebagai bahan baku produksi bioetanol secara lebih spesifik dapat dianalisis melalui aspek kelayakan finansial. Berdasarkan analisis aspek finansial, dapat diperoleh gambaran terkait struktur pembiayaan dan seluruh kebutuhan modal yang dibutuhkan untuk dapat memenuhi rangkaian aktivitas dari usulan proyek yang direncanakan. Selain itu, dapat pula digunakan untuk mengestimasi penerimaan melalui skala produksi dan harga jual yang telah ditetapkan sebagai asumsi.
Pada perhitungan analisis kelayakan finansial usaha produksi bioetanol dari limbah buah tomat ini diasumsikan bahwa dalam satu minggu dapat diperoleh limbah buah tomat sebanyak 1 ton yang diperoleh dari berbagai sentra, misalnya pedagang, petani, maupun distributor buah tomat. Sebanyak 1 ton limbah buah tomat ini kemudian dijadikan acuan sebagai satuan satu kali proses produksi dengan diagram alir proses yang ditunjukkan pada Lampiran 8.
Berdasarkan neraca massa produksi etanol yang digambarkan pada Lampiran 8, diketahui bahwa dari 1 ton limbah tomat mampu menghasilkan etanol sebanyak 24.62 L. Diasumsikan bahwa kapasitas produksi 24.62 L etanol tersebut dilakukan dalam satu kali proses produksi selama 7 hari dengan mempertimbangkan 3 hari proses hidrolisis dan 60 jam fermentasi. Beberapa asumsi dasar yang digunakan dalam perhitungan finansial usaha produksi bioetanol ini antara lain :
1. Modal yang digunakan dalam pembiayaan usaha adalah modal sendiri
2. Produksi dilakukan sebanyak 47 kali dalam satu tahun (satu kali produksi membutuhkan waktu 1 minggu, dengan kegiatan operasional selama 329 hari dalam 1 tahun)
3. Harga jual bioetanol yang berlaku adalah Rp 17 000/liter
4. Biaya yang dikeluarkan meliputi biaya investasi dan biaya operasional.
5. Produk samping berupa ampas hasil hidrolisis dan sisa hidrolisat hasil fermentasi dijual kepada pihak ketiga seharga Rp 350/kg
6. Kapasitas produksi per siklus adalah 1 ton limbah tomat
Dalam mempertimbangkan aspek finansial, diperlukan perhitungan biaya investasi, biaya tetap dan biaya variabel dalam satu siklus produksi. Berikut akan dirinci terkait biaya yang dibutuhkan.
Biaya Investasi
Tabel 6 Komponen biaya investasi
Total Biaya Investasi 134 769 000
Tabel 7 Rincian biaya mesin dan peralatan No. Mesin/Peralatan Jumlah Harga
satuan
Rincian biaya operasional dapat dilihat pada Tabel 8.
Tabel 8 Komponen biaya operasional No. Komponen Satuan Jumlah Harga
Total biaya tetap/tahun 23 100 000
B. Biaya Variabel
Total Biaya variabel/tahun 4 860 676
Biaya operasional mencakup seluruh biaya yang dikeluarkan untuk menyelenggarakan produksi. Biaya operasional ini dibedakan menjadi dua, yaitu biaya tetap dan biaya variabel yang dirinci pada Tabel 8. Biaya tetap berkaitan dengan biaya yang akan selalu dikenakan selama produksi berlangsung tanpa dipengaruhi oleh kapasitas produksi misalnya upah tenaga kerja, sedangkan biaya variabel merupakan biaya yang dipengaruhi oleh kapasitas produksi yang dilakukan, terkait dengan bahan yang dibutuhkan selama proses. Total biaya operasional yang dibutuhkan selama 1 tahun adalah sebesar Rp 27 960 676.
Penerimaan (Revenue)
Penerimaan dihitung melalui jumlah bioetanol yang mampu dihasilkan dengan harga jual bioetanol yang telah ditetapkan. Sebanyak 24.62 L bioetanol dijual dengan harga Rp 17 000 sehingga diperoleh total penerimaan sebesar Rp 418 540 dalam satu siklus produksi. Selama 1 tahun, maka dapat dihitung total penerimaan yang diperoleh mencapai Rp 19 671 380. Penerimaan juga diperoleh dari penjualan produk samping yang dihasilkan selama produksi, yaitu ampas hasil hidrolisis dan hidrolisat sisa proses fermentasi, dimana kedua produk ini dijual kepada pihak ketiga untuk digunakan sebagai pakan ternak maupun bahan baku pembuatan kompos dengan harg Rp 350/kg. Hasil penjualan produk samping ini memberikan penambahan total penerimaan sebesar Rp 16 683 261/tahun. Berdasarkan hal ini, maka diperoleh total penerimaan selama 1 tahun adalah sebesar Rp 36 354 641. Rincian penerimaan hasil penjualan produk utama maupun produk samping produksi ditunjukkan pada Tabel 9.
Kriteria kelayakan pendirian usaha bioetanol dari limbah buah tomat ini dapat dilihat secara finansial meliputi kriteria Payback Period (PBP) dan Revenue Cost Ratio (R/C Ratio). Payback Period merupakan waktu yang diperlukan untuk mengembalikan investasi awal (Newman 1990). Jangka waktu pengembalian investasi didasarkan pada keuntungan yang diperoleh dari suatu proyek. Pengembalian investasi ini juga dapat diartikan sebagai waktu yang dibutuhkan agar total penerimaan sama dengan jumlah investasi atau biaya. Semakin pendek waktu pengembalian investasi, maka semakin layak suatu pendirian usaha, dalam artian semakin besar laba bersih yang dapat diterima oleh perusahaan. PBP dirumuskan sebagai berikut.
Nilai investasi awal usaha bioetanol adalah Rp 134 769 000, dengan keuntungan bersih per tahun adalah sebesar Rp 8 393 965 yang diperoleh dari selisih total penerimaan hasil penjualan bioetanol dengan biaya operasional yang akan selalu dikeluarkan setiap kali produksi dijalankan. Maka diperoleh nilai PBP sebesar 16.05, yang berarti bahwa investasi awal akan kembali setelah melakukan proses produksi selama 16 tahun. Waktu pengembalian ini masih terbilang cukup lama, karena pada umumnya umur ekonomis mesin dan peralatan adalah berkisar antara 10 – 15 tahun. Hal ini terkait dengan biaya investasi yang besar, terutama pada proses hidrolisis dan sterilisasi yang membutuhkan modal pembelian mesin dan kebutuhan energi panas selama proses.
Selanjutnya ditentukan pula nilai R/C ratio yang dihitung berdasarkan total penerimaan kotor dibagi total biaya operasional meliputi biaya tetap maupun biaya tidak tetap. Menurut Husnan dan Suwarsono (2000), kriteria penilaian
Revenue Cost Ratio yaitu :
a) Jika nilai R/C >1, maka proyek dinyatakan layak secara finansial sehingga dapat dilanjutkan
b) Jika nilai R/C < 1, maka proyek dinyatakan tidak layak secara finansial sehingga tidak dapat dilanjutkan
c) Jika R/C = 1, maka proyek boleh dilaksanakan atau tidak
Berdasarkan perbandingan antara total penerimaan sebesar Rp 36 354 641 /tahun serta total biaya operasional sebesar Rp 27 960 676/tahun, dapat dihitung nilai R/C proyek adalah 1.30. Hal ini menandakan bahwa proyek dinyatakan layak secara finansial sehingga dapat dikembangkan lebih lanjut. Berdasarkan nilai R/C
ratio tersebut, juga dapat disimpulkan bahwa setiap biaya Rp 1 000 000 akan menghasilkan penerimaan sebesar Rp 1 300 000.
Mengacu pada perhitungan kelayakan usaha bioetanol, pada dasarnya usaha ini layak untuk dikembangkan secara finansial mengingat bahwa diperoleh keuntungan pada setiap siklus produksi. Hal ini menjadi dasar bahwa limbah tomat yang terbentuk pada berbagai sentra pengelola buah tomat dapat dimanfaatkan dengan meningkatkan nilai tambahnya melalui produksi bioetanol. Hal ini tentunya memberikan keuntungan bagi berbagai pihak, baik sentra penghasil limbah maupun lingkungan, dimana limbah tomat yang tidak termanfaatkan seringkali hanya terbuang sehingga berpotensi meningkatkan limbah lingkungan. Produksi bioetanol ini tentunya berpotensi dikembangkan baik oleh masyarakat maupun negara mengingat kebutuhan bioetanol semakin meningkat.
SIMPULAN DAN SARAN
Simpulan
hidrolisis oleh enzim selulase dimana dapat meningkatkan kadar gula pereduksi awal sebesar 21.55 g/L menjadi 33 g/L.
Hasil fermentasi menunjukkan bahwa substrat dengan konsentrasi inokulum 15% dapat menghasilkan etanol yang lebih tinggi yaitu 1.59% (v/v) dibandingkan 10% inokulum yang menghasilkan kadar etanol sebesar 1.26% (v/v). Penambahan urea dapat meningkatkan kadar etanol dari 1.26% (v/v) menjadi 1.53% (v/v) menggunakan 10% inokulum, sedangkan penambahan urea dengan 15% inokulum mengakibatkan peningkatan etanol dari 1.59% (v/v) menjadi 1.86% (v/v). Mengacu pada kedua parameter tersebut, dapat ditentukan bahwa penggunaan 15% inokulum dan penambahan urea (RAN 15) merupakan variabel paling optimum pada fermentasi hidrolisat limbah tomat. Berdasarkan analisis sidik ragam pada tingkat kepercayaan 95%, diketahui bahwa waktu optimum fermentasi dengan variabel perlakuan RAN 15 adalah 60 jam dengan
yield etanol sebesar 0.49 ± 0.01 g/g substrat yang dikonsumsi dengan tingkat penggunaan gula 90.7 ± 0.4%.
Analisis kelayakan ekonomi dilakukan untuk melihat potensi pengembangan usaha produksi bioetanol dari hidrolisat limbah tomat. Berdasarkan perhitungan finansial dengan kapasitas bioetanol sebesar 24.62 L / siklus produksi, diperoleh keuntungan bersih per tahun adalah Rp 8 393 965. Nilai Payback Period (PBP) yaitu 16.05, dengan kata lain waktu pengembalian investasi yang dibutuhkan adalah selama 16 tahun. Nilai R/C ratio proyek yang diperoleh adalah 1.30, yang menandakan bahwa pengeluaran biaya operasional sebesar Rp 1 000 000 akan memberikan total penerimaan sebesar Rp 1 300 000.
Saran
Perlu dilakukan penelitian lanjutan untuk mengetahui kinerja proses fermentasi dengan melakukan fermentasi secara simultan untuk lebih menyederhanakan proses. Selain itu, proses sterilisasi dapat disederhanakan dengan cara perebusan selama ±30 menit sehingga dapat menekan kebutuhan investasi berupa mesin sterilisasi dan penggunaan steam.
DAFTAR PUSTAKA
Amerine MA, Berg HW, Kunkee RE, Ough CS, Singleton VI, Webb AD. 1987.
Technology of Wine Making. Conneticut: The AVI Publishing Co. Inc. Anonim. 2014. Tomato. Diakses dari http://foodscience.wikispaces.com.(15 Juli
2014).
[AOAC] Association of Official Analytical Chemistry 1995. Official Method of Analysis of The Association of Official Analytical Chemistry. Washington DS (USA) : AOAC International.
Clark T dan KL Mackie. 1984. Fermentation Inhibition in Word Hydrolysates Derived from the Softwood Pinus radiate. J. Chem. Biotechnol. Vol.34B : 101 – 110.
Collins WW dan WM Walter. 1985. Fresh Roots for Human Consumption. Di dalam Bouwkamp JC. (eds). Sweet Potato Products: A Natural Resource for The Tropics.CRC. Press Inc., Boca Raton.
Derosya V. 2010. Sakarifikasi Empulur Sagu (Metroxylon sagu) dengan Konsorsium Enzim Amilolitik dan Holoselulolitik untuk Produksi Bioetanol. [Skripsi]. Bogor: Departemen Teknologi Indsutri Pertanian, Fateta, IPB.
Direktorat Gizi Departemen Kesehatan. 1979. Kandungan Gizi dalam 100 gram Buah Tomat. Jakarta: Departemen Kesehatan RI.
Ditjen MIGAS. 2012 Statistik Minyak Bumi. Diakses dari www.esdm.go.id. (21 Juni 2014).
Dubois M, Gilles KA, Hmilton JK, Rebers PA, Smith F. 1956. Colorimetric Method for Determination of Sugars and Related Substances. J Anal Chem 28 (3) : 350 – 356.
[EIA] Energy Information Administration. 2007. International Energy Oulook. Washington: US Department of Energy.
Fardiaz S. 1988. Fisiologi Fermentasi. Bogor: Pusat Antar Universitas, Institut Pertanian Bogor.
Fatony MG. 2010. Analisis Kelayakan Investasi Proyek Bioetanol di Jawa Timur. Jakarta: Fakultas Ekonomi, Universitas Indonesia.
Frazier WC dan Westhoff DC. 1978. Food Microbiology. New York: Tata Mc.Gaw-Hill Publ Co.Ltd.
Gaman PM dan KB Sherrington. 1981. Ilmu Pangan: Pengantar Ilmu Pangan, Nutrisi, dan Mikrobiologi (Edisi kedua). Yogyakarta: Gadjah Mada University Press.
Irawadi TT. 1990. Kajian Hidrolisis Limbah Lignoselulosa dari Industri Pertanian. J. Tek. Ind. Pert. 8 (3) : 124-134.
[JICA] Japan International Coorperation Agency. 1978. Methods of Soil Chemcial Analysis. Dokumen. BARISTAN INDAG. Bogor: Japan International Coorperation Agency (JICA).
Jeewon L. 1997. Biological Conversion of Lignocellulosic Biomass to Ethanol : A Review Article. J Bioethanol 56:1-4.
Judoamidjojo RM, Said EG, Hartoto L. 1989. Biokonversi. Bogor: Pusat Antar Universitas Bioteknologi.
Martini A. 2003. Biotechnology of natural and winery associated strains of Saccharomyces cerevisiae. International Microbiology 6: 207-209.
Miller GI. 1959. The Use of Dinitrosalicylic Acid Reagent for Determination of Reducing Sugar. Anal. Chem. 31 (3) : 426 – 428.
Newman DG. 1990. Engineering Economics Analysis. Jakarta: Binarupa Aksara. Oura E. 1983. Reaction Products of Yeasts Fermentations. Di dalam H. Dellweg.
1983. (ed). Biotechnology Vol. III. New York: Academic Press.
Pacheco AM, Gondim DR, Goncalves LRB. 2010. Etahnol Production by Fermentation Using Immobilized Cells of Saccharomyces cerevisiae in Cashew Apple Bagasse. Appl Biochemistry and Biotechnology (161): 209-217.
Palmer TJ. 1970. Acid and Enzyme Hydrolysis of Starch. London: Publishing Company Limited.
Paturau JM. 1981. By-Product of The Cane Sugar Industrial: An Introduction to Their Industrial Utilization. Amsterdam: Elsevier Scientific Publishing Co.
Pons A, Dussap CG, Gross JB. 1990. Xanthan Bath Fermentation: Compared Performance of A Bubble Coloumn and A Stirred Tank Fermentor. Bioprocess Eng 5: 107 – 114.
Rehm HJ dan G Reed. 1981. Biotechnology Vol. I : Microbial Fundamental. Weiheim : Verlag Chemie Gmbh.
Rinaldy W. 1987. Pemanfaatan Onggok Singkong (Manihot esculanta Crantz) Sebagai Bahan Pembuatan Bioetanol. Skripsi. Bogor: Fateta IPB.
Sari FA. 2009. Pengaruh Jenis Asam pada Hidrolisat Pati Sagu (Metroxylon sp.) untuk Pembuatan Etanol. Bogor: Fateta IPB.
Shuler ML dan Kargi KF. 1992. Bioprocess Engineering Basic Concepts. New Jersey : Prentice Hall.
Stanbury PF dan Whitaker A. 1993. Principles of Fermentation Technology. New York: Pergamon Press.
Sudarmadji S, Haryono B, Suhardi. 1997. Prosedur Analisa Untuk Bahan Makanan dan Pertanian. Yogyakarta: Liberty.
Suyandra ID. 2007. Pemanfaatan Hidrolisat Pati Sagu (Metroxylon sp.) Sebagai Sumber Karbon Pada Fermentasi Etanol Oleh Saccharomyces cerevisiae.
[Skripsi]. Bogor: Departemen Teknologi Industri Pertanian, Fakultas Teknologi Pertanian IPB.
Syamsu K, Suryani A, Fauzi AM, Wicaksono BWD. 2003. Optimasi Produksi, Karakterisasi, Aplikasi dan Pengujian Biodegradasi Bioplastik yang Dihasilkan Oleh Ralstonia eutropha pada Substrat Hidrolisat Minyak Sawit. Laporan Akhir Penelitian Hibah Bersaing IX. Pusat Penelitian Bioteknologi. IPB. 189. Hal.
Taherzadeh MJ dan K Karimi. 2007. Acid-Based Hydrolysis Processes for Ethanol From Lignocellulosic Material: A review, J Biores 2: 472-499. Tjokroadikoesoemo OS. 1986. HFS dan Industri Ubi Kayu Lainnya. Jakarta:
Gramedia Pustaka Utama.
Wang NS, Cooney CL, Demain AL, Dunnil P, Humphrey AE, Lolly MD. 1979.
LAMPIRAN
Lampiran 1 Analisis Karakterisasi Bahan
1. Kadar Air (AOAC 1995)
Cawan alumunium yang telah dikeringkan dan diketahui bobotnya, diisi sebanyak 2-3 gram sampel lalu ditimbang (W1) kemudian dimasukkan kedalam
oven suhu 105oC selama 1-2 jam. Cawan alumunium dan sampel yang telah dikeringkan dimasukkan ke dalam desikator kemudian ditimbang. Ulangi pemanasan sampai dihasilkan bobot konstan (W2). Sisa contoh dihitung sebagai
total padatan dan air yang hilang sebagai kadar air.
Kadar air (%) = (�1−�2)
�1 × 100%
2. Kadar Serat Kasar (AOAC 1995)
Contoh sebanyak 5 g dimasukkan ke dalam Erlenmeyer 500 ml kemudian ditambahkan 100 ml H2SO4 0.325 N dan dididihkan selama kurang lebih 30
menit. Ditambahkan lagi 50 ml NaOH 1.25 N dan dididihkan selama 30 menit. Dalam keadaan panas disaring dengan kertas Whatman No.40 setelah diketahui bobot keringnya. Kertas saring yang digunakan dicuci berturut-turut dengan air panas, 25 ml H2SO4 dan etanol 95%. Kemudian dikeringkan di dalam oven
bersuhu 100-110°C sampai bobotnya konstan. Kertas saring didinginkan dalam desikator dan ditimbang.
Kadar serat kasar (%) = bobot endapan kering (g)
bobot contoh (g) � 100%
3. Kandungan nitrogen (N) dengan metode Kjedahl
Sebanyak 0.25 gam sampel dimasukkan ke dalam labu kjedahl dan ditambahkan 2.5 ml H2SO4 pekat dan 1 g katalis. Larutan tersebut kemudian
didestruksi hingga jernih. Selanjutnya ditambahkan NaOH 40% ke dalam larutan dekstruksi dingin sebanyak 15 ml. Disiapkan pula larutan penampung di dalam erlenmeyer 250 ml yang terdiri dari 19 ml H3BO3 4% dan indikator mensel 2-3
tetes. Setelah itu larutan sampel dimasukkan ke dalam labu destilasi. Destilasi dihentikan apabila tidak ada lagi terbentuk gelembung-gelembung yang keluar pada larutan penampung. Hasil destilasi kemudian dititrasi dengan H2SO4 0.02 N.
% N = � � − � � × �2� 4 ×14 ×100
� � 1000
4. Kandungan karbon (C) (JICA 1978)