TESIS
PENGARUH ANTIBODI MATERNAL TERHADAP
HISTOPATOGENESIS VIRUS NEWCASTLE DISEASE
LAPANG PADA AYAM BROILER
I MADE GALIH DIPARAYOGA
PROGRAM PASCASARJANA
UNIVERSITAS UDAYANA
TESIS
PENGARUH ANTIBODI MATERNAL TERHADAP
HISTOPATOGENESIS VIRUS NEWCASTLE DISEASE
LAPANG PADA AYAM BROILER
I MADE GALIH DIPARAYOGA NIM 1492361002
PROGRAM MAGISTER
PROGRAM STUDI KEDOKTERAN HEWAN
PROGRAM PASCASARJANA
PENGARUH ANTIBODI MATERNAL TERHADAP
HISTOPATOGENESIS VIRUS NEWCASTLE DISEASE
LAPANG PADA AYAM BROILER
Tesis untuk Memperoleh Gelar Magister
pada Program Magister, Program Studi Kedokteran Hewan, Program Pascasarjana Universitas Udayana
I MADE GALIH DIPARAYOGA NIM 1492361002
PROGRAM MAGISTER
PROGRAM STUDI KEDOKTERAN HEWAN
PROGRAM PASCASARJANA
UNIVERSITAS UDAYANA
DENPASAR
Lembar Pengesahan
TESIS INI TELAH DISETUJUI
PADA TANGGAL 14 APRIL 2016
Pembimbing I, Pembimbing II
Prof. drh. I Nyoman Mantik Astawa, Ph.D Prof. drh. A. A. Ayu Mirah Adi, M,Si., Ph. D NIP. 196012321 198803 1 003 NIP. 19630826 198803 2 001
Mengetahui
xii
Tesis Ini Telah Diuji pada Tanggal
14 April 2016
Panitia Penguji Tesis Berdasarkan SK Rektor
Universitas Udayana, No.:1505/UN14.4/HK/2016 Tanggal 12 April 2016
Ketua : Prof. drh. I Nyoman Mantik Astawa, Ph.D
Anggota :
1. Prof. drh. A. A. Ayu Mirah Adi, M,Si., Ph. D
2. Prof. Dr. drh. Gusti Ayu Yuniati Kencana, MP
3. Dr. Drh.Ida Bagus Oka Winaya, M. Kes
SURAT PERNYATAAN BEBAS PLAGIAT
Saya yang bertanda tangan di bawah ini :
Nama : I Made Galih Diparayoga
Nim : 1492361002
Program Studi : Kedokteran Hewan
Judul Tesis : Pengaruh Antibodi Maternal terhadap Histopatogenesis
Virus Newcastle Disease Lapang pada Ayam Broiler.
Dengan ini menyatakan bahwa karya ilmiah tesis ini bebas plagiat. Apabila
dikemudian hari terbukti plagiat dalam karya ilmiah ini, maka saya bersedia
menerima sanksi sesuai dengan peraturan Mendiknas RI No. 17 Tahun 2010 dan
Peraturan Perundang-undangan yang berlaku.
Denpasar, 14 April 2016
Yang membuat pernyataan
xiv
DAFTAR RIWAYAT HIDUP
Penulis dilahirkan di kota Denpasar, Bali pada tanggal 8 Februari 1992.
Merupakan anak kedua dari dua bersaudara pasangan Bapak Ir. I Wayan Ekasana
dan Ibu Ni Ketut Kartika Sari. Penulis pertama kali memasuki dunia pendidikan di
TK Panca Darma tahun 1996 – 1997. Kemudian melanjutkan ke SD Negeri 1 Seririt
tahun 1997 – 2003. Selanjutnya masuk SLTP Negeri 1 Seririt tahun 2003 – 2006
dan SMA Negeri 1 Seririt tahun 2006 – 2009. Penulis diterima sebagai mahasiswa
di Fakultas Kedokteran Hewan Universitas Udayana melalui jalur PMDK pada
tahun 2009. Selanjutnya penulis menempuh pendidikan di Kedokteran Hewan
Universitas Udayana, menyelesaikan pendidikan Sarjana Kedokteran Hewan
(SKH) Tahun 2013 dan menyelesaikan Pendidikan Profesi Dokter Hewan Tahun
2014. Penulis diterima menjadi mahasiswa Program Magister Program Studi S2
Kedokteran Hewan di Universitas Udayana Pada Tahun 2014. Selanjutnya penulis
melakukan penelitian di UPT Patobiologi Fakultas Kedokteran Universitas
Udayana berjudul “Pengaruh Titer Antibodi Maternal Terhadap Histopatogenesis
Virus Newcastle Disease pada Ayam Broiler yang Ditantang dengan Virus
Newcastle Disease Lapang”. Penelitian ini dibuat sebagai salah satu syarat untuk
memperoleh gelar Magister Kedokteran Hewan pada Program Magister Program
UCAPAN TERIMA KASIH
Puji syukur penulis panjatkan kepada Tuhan Yang Maha Esa yang telah
memberikan rahmat-Nya sehingga penulisan tesis ini dapat diselesaikan. Pada
kesempatan ini penulis mengucapkan terima kasih kepada Prof. drh. I Nyoman
Mantik Astawa, Ph.D. selaku pembimbing I dan Prof. drh. A. A. Ayu Mirah Adi,
M,Si., Ph. D selaku pembimbing II yang telah memberikan bimbingan dan saran
kepada penulis. Ucapan terima kasih ditujukan kepada Rektor Universitas Udayana
Prof. Dr. dr. Ketut Suastika, Sp.PD-KEMD dan kepada Direktur Program
Pascasarjana Universitas Udayana, Prof. Dr. dr. A.A. Raka Sudewi, Sp.S. (K) atas
kesempatan dan fasilitas yang diberikan kepada penulis untuk mengikuti dan
menyelesaikan pendidikan Program Magister di Universitas Udayana. Terima kasih
penulis sampaikan kepada Prof. Dr. drh. I Ketut Puja, M.Kes. selaku Ketua Program
Studi S2 Kedokteran Hewan Program Pascasarjana Universitas Udayana dan juga
sebagai kesediaannya menjadi penguji. Ucapan terima kasih juga penulis
sampaikan kepada para penguji tesis lainnya, yaitu Prof. Dr. drh. Gusti Ayu Yuniati
Kencana, MP dan Dr. Drh.Ida Bagus Oka Winaya, M. Kes yang telah memberikan
masukan dan saran. Ucapan terima kasih yang tulus penulis sampaikan kepada
Bapak Ir. I Wayan Ekasana dan Ibu Ni Ketut Kartika Sari yang telah memberikan
dukungan dan perhatian dalam penulisan tesis ini. Terima kasih kepada
teman-teman seperjuangan gamers DOTA dan terutama terimakasih banyak kepada Ni
xvi
ABSTRAK
PENGARUH ANTIBODI MATERNAL TERHADAP HISTOPATOGENESIS VIRUS NEWCASTLE DISEASE
LAPANG PADA AYAM BROILER
Tujuan penelitian ini adalah mengetahui pengaruh antibodi maternal terhadap perubahan histopatologis dan imunohistokimia ayam broiler setelah ditantang dengan virus Newcastle disease (ND) APMV-1. Seluruh ayam dibagi atas 3 kelompok perlakuan Kelompok I (titer antibodi < 23 HI Unit), Kelompok II (titer antibodi 23 – 24 HI Unit) dan Kelompok III (titer antibodi > 24 HI Unit). Ayam
Kelompok I, II dan III masing-masing diberi isolat virus ND tipe viscerotropic velogenic 1000 TCID50. Perubahan histopatologis sistem syaraf ayam kelompok
perlakuan menunjukkan endoteliosis dan perivaskular cuffing. Pada pemeriksaan
imunohistokimia sel yang positif mengandung antigen virus ND ditemukan pada kumpulan sel radang. Analisis imunohistokimia mengindikasikan partikel virus ND telah menyebar di organ atau jaringan sistem syaraf, sistem pernafasan dan sistem digesti. Gejala syaraf dan perubahan histopatologis lebih banyak muncul pada kelompok II (titer antibodi 23 – 24 HI Unit).
ABSTRACT
EFFECT OF MATERNAL ANTIBODIES ON HISTOPATHOGENESIS OF NEWCASTLE DISEASE VIRUS IN BROILER CHICKENS
The aims of this research were to overview the effect of maternal antibodies on the histopathological changes and viral antigen distribution of the broiler chickens challenged with ND APMV-1 virus. A total of 100 chicken were allotted into 3 treatment groups consisting of group I (titer antibodies < 23 HI Unit), group
II (titer antibodies 23 – 24 HI Unit) and group III (titer antibodies > 24 HI Unit). All group I, II and III were inoculated with ND virus isolates of type viscerotropic velogenic at the dose of 1000 TCID50. The histopathological changes observed in
nervous system were endotheliosis and perivascular cuffing. Immunohistochemistry staining showed that NDV infected cells were found in most organs both in inflammatory cells and in epithelial cell of many organs mainly in nervous, respiratory and digestive systems. Neurological signs and neural lesions were highest in group II (titer antibodies 23 – 24 HI Unit).
xviii
RINGKASAN
Newcastle Disease (ND) atau penyakit tetelodisebabkan oleh strain virulen avian Paramyxovirus serotipe tipe 1 (AMPV-1) dari genus Avulavirus yang termasuk dalam subfamily Paramyxovirinae, family Paramyxoviridae Berdasarkan hasil uji
Hemagglutination Inhibiton (HI) dan Neuraminidase Inhibition (NI) genus
Avulavirus ini terdiri dari sembilan serotype yakni APMV serotype 1 sampai dengan serotype 9. Virus ND yang ada di Indonesia adalah galur velogenic-viscerotropic.
Unggas yang terinfeksi virus ND terutama dari tipe velogenic Viscerotropic (VVND) gejala klinis yang ditimbulkan antara lain terjadi kelesuan, peningkatan frekuensi pernafasan, kehilangan nafsu makan, penurunan konsumsi air minum, kelemahan dan berakhir kematian. Dilihat dari titer antibodi maternal pada anak ayam, titer antibodi maternal akan menurun sejak hari ke-3 dan menurun terus hingga hari ke-12. Antibodi asal induk ini akan menurun dengan cepat seiring meningkatnya umur ayam.
Salah satu cara untuk mengukur tingkat kekebalan secara serologi dikerjakan melalui uji Hemaglutination Inhibition (HI). Uji HI lebih banyak dipakai karena selain mudah dan murah, uji ini spesifik dan dapat menunjukkan status kekebalan pada ayam. Adapun Metode diagnostik yang berbasis jaringan dan teknik
Immunostaining yaitu Uji imunohistokimia (IHK). Teknik ini dapat melacak distribusi virus pada berbagai organ sehingga dapat dipakai untuk mengetahui pathogenesis infeksi virus, tergolong aman karena dilakukan pada organ yang telah difiksasi dengan formalin sehingga virus yang dilacak adalah virus yang sudah inaktif, penggunaan AbMo sebagai antibodi primer dan metode super sensitive TM Polymere-HRP yang memiliki sensitifitas dan spesifisitas yang tinggi dapat meningkatkan akurasi uji. Atas dasar permasalahan tersebut, penulis melakukan penelitian tentang pengaruh titer antibodi maternal terhadap histopatogenesis virus
Newcastle Disease pada ayam broiler yang ditantang dengan virus Newcastle Disease Lapang. Tujuan dari penelitian ini adalah untuk mengetahui waktu paruh penurunan titer antibodi maternal pada ayam broiler, pengaruh titer antibodi maternal terhadap histopatogenesis virus Newcastle Disease pada ayam broiler khususnya terhadap munculnya gejala syaraf dan untuk mengetahui titer antibodi maternal yang protektif, subprotektif dan tidak protektif terhadap infeksi virus Newcastle Disease
lapang. Hasil penelitian inidiharapkan dapat memberikan informasi kepada peternak tentang pencegahan penyakit Newcastle Disease dalam menentukan efisiensi waktu pemberian vaksinasi pada ternak unggas.
Penelitian ini merupakan penelitian eksperimental dengan RAL . Hewan percobaan yang dipakai dalam penelitian ini adalah Day Old Chicken (DOC) ayam broiler strain Lohman. Sampel yang digunakan adalah 100 ekor ayam, pada umur 12 hari ayam diukur titer maternal antibodi dengan menggunakan uji Hambatan Inhibisi (HI). Setelah didapat titer HI, ayam dikelompokkan menjadi 3 kelompok, kelompok I adalah ayam dengan titer antibodi maternal ≤ 23 HI unit , kelompok II dengan titer antibodi maternal (23-24 HI unit) dan Kelompok III titer antibodi
ND velogenic 1000 TCID50. Dua minggu pasca infeksi dilakukan nekropsi semua
kelainan diamati dan dicatat. Spesimen jaringan dari masing-masing organ kemudian diproses lebih lanjut dengan menggunakan hematoksilin dan eosis (HE). Pewarnaan menggunakan teknik imunohistokimia dengan metode LSAB (Labeled Streptavidin Biotin) dengan antibodi monoklonal terhadap ND. Hasil dinyatakan positif (+) jika terdapat warna kecokelatan dan negatif (-) jika warna tersebut tidak terdeteksi.
Titer antibodi maternal pada ayam umur 12 hari saat uji tantang berkisar antara 21 sampai 25 dengan rerata 22 . Rincian titer antibodi maternal pada ayam adalah 21 (5 ekor ayam), 22 (16 ekor ayam), 23 (4 ekor ayam), 24 (3 ekor ayam) dan 25 (2 ekor ayam). Gejala klinis yang bervariasi dari gejala syaraf (12 ekor ayam),
seperti kejang-kejang, sayap terkulai, kelumpuhan pada kaki, tremor pada kepala, tortikolis yang bersifat sementara sampai dengan yang bersifat permanen. Selain itu, beberapa ayam menunjukkan gejala pernafasan (16 ekor ayam), seperti susah bernafas, ngorok, dan megap-megap. Gejala pencernaan (9 ekor ayam) juga ditemukan pada sebagaian besar ayam yang meliputi gejala diare dari bening sampai diare putih kehijauan. Gambaran histopatologi otak dari tiga kelompok perlakuan ditemukan perivascular cuffing dengan berbagai tingkat. Lesi perivascular cuffing paling luas ditemukan pada kelompok II dengan Titer antibodi 23 – 24 HI unit. Intensitas antigen paling tinggi didapatkan di organ otak pada Kelompok II dengan Titer antibodi 23– 24 HI unit. Berdasarkan analisis statistik menunjukkan bahwa titer antibodi maternal berpengaruh sangat nyata (P<0,01) terhadap nilai rata-rata skoring imunohistokimia pada kelompok II dengan titer antibodi 23– 24 HI unit . Dan pada organ otak, antara titer antibodi maternal < 23 HI Unit dengan 23-24 HI Unit
menunjukkan hasil yang berbeda nyata (P<0,01) terhadap nilai rata-rata skoring imunohistokimia. Antara titer antibodi maternal 23-24 HI Unit dengan > 24 HI Unit menunjukkan hasil yang berbeda nyata (P<0,01) terhadap nilai rata-rata skoring imunohistokimia. Sedangkan antara titer antibodi maternal < 23 HI Unit dengan > 24 HI Unit menunjukkan hasil yang tidak berbeda nyata (P>0,05) terhadap nilai rata-rata skoring imunohistokimia.
Dari hasil penelitian yang didapat dapat ditarik kesimpulan bahwa titer antibodi maternal mempengaruhi pola gejala klinis, histopatologi dan histopatogenesis pada ayam yang terinfeksi virus Newcastle disease pada ayam, titer antibodi maternal mempengaruhi distribusi antigen virus Newcastle disease pada berbagai organ terutama otak, paru-paru dan usus. Titer antibodi maternal 23-24 HI unit dapat memicu munculnya gejala syaraf pada ayam. Didalam penelitian ini gejala saraf pada titer antibodi maternal 23-24 HI unit. Sebaiknya saat melakukan
xx
SUMMARY
Newcastle Disease (ND) caused by a virulent strain of avian paramyxovirus serotype type 1 (AMPV-1) of the genus Avulavirus included in subfamily Paramyxovirinae, family Paramyxoviridae Based on test results Hemagglutination Inhibiton (HI) and Neuraminidase Inhibition (NI) genus Avulavirus this consists of nine serotypes of the apmv serotype 1 to serotype 9. ND virus in Indonesia is velogenic-viscerotropic strain. ND infected poultry, especially of the type velogenic Viscerotropic (VVND) clinical symptoms of lethargy caused, among other things, an increase in the frequency of breathing, loss of appetite, decreased water consumption, weakness and ends in death. Judging from maternal antibody titers in chicks, maternal antibody titer decreases since day 3 and declined steadily until the 12th day.
The origin of the parent antibody decreases rapidly with increasing age of the chicken. One way to measure the level of immune serological test done through Hemaglutination Inhibition (HI). HI test is more widely used because in addition to easy and cheap, this test can indicate specific and immune status in chickens. As a network-based diagnostic methods and techniques Immunostaining namely immunohistochemistry test (IHC). This technique can track the distribution of the virus in various organs that can be used to determine the pathogenesis of viral infection, is safe because it is done on the organs had been fixed in formalin so that the virus being tracked is a virus that has been inactivated, use AbMo as primary antibodies and methods of super sensitive TM polymere -HRP which has a high sensitivity and specificity that can improve test accuracy. On the basis of these problems, the authors conducted a study on the effect of maternal antibody titers against Newcastle Disease virus histopatogenesis in broiler chickens were challenged with Newcastle Disease virus Field. The purpose of this study was to determine the half-life reduction in titer of maternal antibodies in broiler chickens, influence titer of maternal antibodies against histopatogenesis virus Newcastle Disease in broiler chickens in particular to the emergence of neurological symptoms and to determine the titer of maternal antibodies that are protective, subprotektif and not protective against viral infections Newcastle Disease airy. The results of this study are expected to provide information to farmers on the prevention of Newcastle Disease in determining the efficiency of a vaccination in poultry.
This study was an experimental study with a basic RAL design. Experimental animals used in this study is the Day Old Chicken (DOC) Lohman strain broiler chickens. At the age of 12 days chicken maternal antibody titers were measured by using test Barriers Inhibition (HI). Having obtained HI titres, chickens are grouped into three groups, Group I was the chicken with Maternal Antibody
Titer (Ma Ab) ≤ 23 HI unit, group II with Ma Ab Titer (23-24 HI units) and Group
III Ma Ab titer (≥ 25 HI unit). Group I-III is the group that will be infected with a
cutting preparations. Staining using immunohistochemical techniques with methods LSAB (Labeled Streptavidin Biotin) with monoclonal antibodies against ND. The results confirmed positive (+) if there is a brownish color and negative (-) if the color is not detected.
Titers maternal antibody at 12 days old chickens current challenge test ranges from 21 to 25 with a mean of 22. Details of maternal antibody titers in chickens is 21 (5 chickens), 22 (16 chickens), 23 (4 hens), 24 (3 chickens) and 25 (2 chickens). Clinical symptoms vary from neurological symptoms (12 chickens), such as seizures, drooping wings, paralysis of the legs, head tremors, torticollis temporary until permanent. In addition, some chickens showing respiratory symptoms (16 chickens), such as difficulty breathing, snoring and gasping. Gastrointestinal symptoms (9 chickens) are also found on most chickens that includes symptoms of diarrhea from clear white to greenish diarrhea. Histopathologic features of the brain of 3 treatment groups was found perivascular cuffing with different levels. Lesions most extensive perivascular cuffing was found in titer AB 23-24 HI unit. The intensity of the antigen in the brains of most high titer AB 23-24 HI unit. Based on statistical analysis showed that maternal antibody titer was highly significant (P <0.01) to the average value of immunohistochemical scoring. And in the organs of the brain, between the maternal antibody titer <23 with
23-24 HI HI Unit by Unit showed significantly different results (P <0.01) to the average value of immunohistochemical scoring. Maternal antibody titer between 23-24 HI Units with> 24 HI Unit showed significantly different results (P <0.01) to the average value of immunohistochemical scoring. While the maternal antibody titer <23 HI units with> 24 HI Unit showed results that were not significantly different (P> 0.05) to the average value of immunohistochemical scoring.
From the results obtained it can be concluded that the titer of maternal antibodies influence the pattern of clinical symptoms and histopathology in chickens infected with the virus Newcastle disease in chickens, the titer of maternal antibodies influence the distribution of viral antigen Newcastle disease in various organs especially the brain, lungs and intestines and titer maternal antibodies 23-24
HI unit can trigger neurological symptoms in chickens infected with Newcastle disease virus in chickens. In this study the neurological symptoms in titer maternal antibodies 23-24 HI unit. Therefore, when vaccination is done before maternal
xxii
2.1.6 Perubahan patologi anatomi (PA) dan histopa- tologi (HP) ………. 19 2.3.4 Induksi secara aktif melalui vaksinasi………… 30
3.3 Hipotesis……….….….…………. 41
5.1.3 Pengaruh titer antibodi maternal terhadap masa inkubasi, gejala klinis, lama bertahan hidup pasca munculnya klinis ………….……… 51
5.1.4 Histopatologi virus ND pada organ otak, paru-paru dan usus……… 51
5.1.5 Distribusi antigen virus ND pada organ otak, paru-paru dan usus……… 56
5.1.6 Pengaruh titer antibodi maternal terhadap derajat infeksi virus ND pada organ otak, paru dan usus….….….….…….….………….…..…. 57
5.1.7 Perubahan histopatologi dan imunohistokimia pada organ lain.……….….…….. 58
5.2 Pembahasan……… 59
5.2.1 Titer Antibodi Maternal Berperan dalam gejala Klinis ND……… 59
5.2.2 Titer antibodi maternal mempengaruhi derajat infeksi virus ND pada Otak……… 68
BAB VI SIMPULAN DAN SARAN……… 69
DAFTAR PUSTAKA………...…… ……….……….. 69
xxiv
DAFTAR GAMBAR
Halaman
2.1 Virus Newcastle Disease……… 8
2.2 Siklus Hidup dan Mekanisme Infeksi ND ………...………. 15
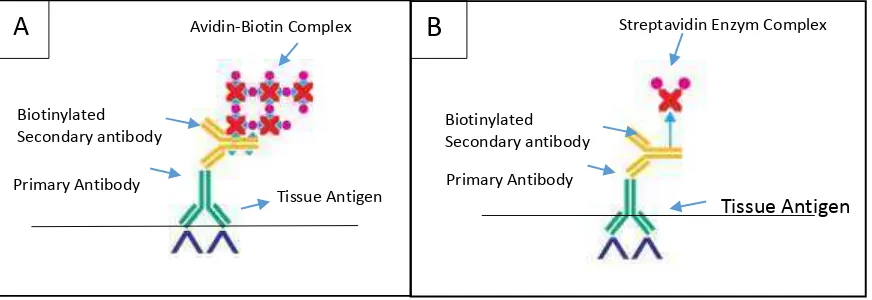
2.3 Metode IHK tidak langsung………..……… 36
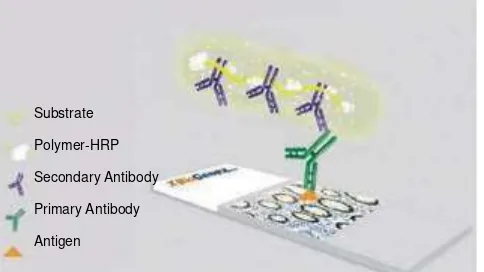
2.4 Super SensitiveTM Polymer-HRP IHC Detection System……….. 37
DAFTAR TABEL
Halaman
5.1 Titer antibodi Maternal dan Gejala Klinis Klinis ND pasca Uji
Tantang……… 49 5.2. Patogenitas Virus Newcastle Disease dosis 1000 TCID50 pada ayam broiler
BAB I PENDAHULUAN 1.1 Latar Belakang
Newcastle Disease (ND) atau penyakit tetelodisebabkan oleh strain virulen
avian Paramyxovirus serotipe tipe 1 (AMPV-1) dari genus Avulavirus yang
termasuk dalam subfamily Paramyxovirinae, family Paramyxoviridae (OIE, 2009).
Berdasarkan hasil uji Hemagglutination Inhibiton (HI) dan Neuraminidase
Inhibition (NI) genus Avulavirus ini terdiri dari sembilan serotype yakni APMV
serotype 1 sampai dengan serotype 9 (Aldous dan Alexander, 2001). Serotype
APMV-4, APMV-5, APMV-6, APMV-7, APMV-8 dan APMV-9 pada umumnya
menyerang itik, angsa, merpati, betet dan beberapa jenis unggas lainnya, tanpa
menimbulkan gejala klinis yang jelas (Saepulloh, 2005). Hanya APMV-2 dan
APMV-3 yang menyebabkan penyakit pernafasan dan penurunan produksi telur
(Alexander, 2000). Penyakit ND sendiri menyerang unggas, khususnya ayam yang
bersifat sangat menular dan akut serta menimbulkan gejala gangguan pencernaan,
pernafasan dan syaraf. (Alexander dan Senne, 2008; Quinn et al., 2011).
Wabah penyakit ND dilaporkanpertama kali tahun 1926 di Jawa (Indonesia)
dan Newcastle (Inggris) (Swayne ang King, 2003; Stenerodon, 2004). Penyakit
akibat virus ini masih merupakan permasalahan yang utama bagi peternak di
Indonesia (OIE, 2009). Di Indonesia, penyakit ND bersifat endemis, yang ditandai
dengan kejadian penyakit yang ditemukan sepanjang tahun (Tabbu, 2000). Tahun
Terdapat tiga pathotype didalam Virus ND yang dikelompokkan berdasarkan
atas waktu kematian embrio, yakni: lentogenic adalah strain virus yang kurang ganas
ditandai dengan kematian embrio lebih dari 90 jam, mesogenic antara 60-90 jam,
sedangkan velogenic kurang dari 60 jam (Saif, 2003). Virus ND tipe lentogenic
menunjukkan gejala klinis pada ternak ayam yang bersifat ringan atau tanpa gejala
klinis. Virus ND tipe mesogenic dengan virulensi moderat (sedang) menunjukkan
gejala yang dari ringan sampai sedang. Sementara itu, virus ND velogenic adalah tipe
yang sangat ganas ditandai dengan penyakit yang bersifat akut dan kematian yang
tinggi sampai 100%. Berdasarkan atas predileksinya dan gejala klinis yang
ditimbulkan, virus ND velogenic dibedakan lagi menjadi bentuk neurotropic dengan
kelainan pada sistem syaraf, pneumotropic dengan kelainan pada sistem pernafasan,
dan Viscerotropic dengan kelainan pada sistem pencernaan (Aldous and Alexander,
2001).
Alexander and Senne (2008b) menyatakan bahwa berdasarkan tanda-tanda
klinis yang terlihat pada ayam yang terinfeksi ND telah dikelompokkan menjadi lima
pathotype. Viscerotropic velogenic: bentuk yang sangat patogen di mana lesi usus
hemoragik sering terlihat; Neurotropic velogenic: bentuk yang ditandai dengan
kematian yang tinggi, biasanya diikuti dengan gejala pernapasan dan saraf;
Mesogenic: bentuk yang ditandai dengan gejala pernapasan, gejala syaraf sesekali,
tapi tingkat kematian rendah; Lentogenic: bentuk yang menunjukkan adanya infeksi
Virus ND yang ada di Indonesia adalah galur velogenic-viscerotropic (Adi et
al., 2010). Tabbu (2000) menjelaskan bahwa unggas yang terinfeksi virus ND
terutama dari tipe velogenic Viscerotropic (VVND) gejala klinis yang ditimbulkan
antara lain terjadi kelesuan, peningkatan frekuensi pernafasan, kehilangan nafsu
makan, penurunan konsumsi air minum, kelemahan dan berakhir kematian. Adi, et
al (2009) menjelaskan bahwa ayam yang terinfeksi virus ND velogenik gejala klinis
yang ditimbulkan dehidrasi, badan mengalami kekurusan dan diare kehijauan yang
menempel di sekitar kloaka.
Penelitian yang dilakukan oleh Tabbu (1996) menyatakan bahwa ayam
broiler yang mendapat vaksinasi dua kali vaksin aktif pada umur 4 dan 18 hari
menunjukkan tingkat proteksi 80% terhadap uji tantang virus velogenic ND pada
umur 45 hari, sedangkan hasil vaksinasi gabungan ND aktif-inaktif yang diberikan
pada umur 4 hari dan dilakukan booster pada umur 18 hari menunjukkan tingkat
proteksi 100%. Penelitian yang dilakukan oleh Nana (2006) tentang program
vaksinasi pada ayam broiler menunjukkan proteksi dari penggunaan vaksin aktif
pada minggu pertama dan minggu kedua adalah 60%. Program vaksinasi
menggunakan vaksin aktif pada minggu pertama dan vaksin inaktif pada minggu
kedua menunjukkan proteksi 100%. Program vaksinasi menggunakan vaksin aktif
pada minggu pertama menunjukkan tingkat proteksi sebesar 40%. Penelitian tentang
uji tantang pada ayam buras yang dilakukan oleh Wibowo and Amanu (2010)
menunjukkan bahwa ayam buras yang diberi vaksin gabungan ND aktif-inaktif pada
umur 7 hari dapat melindungi ayam hingga 100% sedangkan pada ayam yang
proteksinya adalah 60% dari serangan velogenic ND mulai dari munculnya gejala
klinis atau kematian. Penelitian uji tantang pada ayam petelur yang dilakukan oleh
Darminto dan Ronohardjo pada tahun 1996 menunjukkan bahwa pemberian vaksin
ND inaktif pada umur 4 minggu dan dilakukan uji tantang sebanyak 4 kali, yaitu
pada umur 15, 18, 20 dan 26 minggu dapat melindungi ayam dari serangan virus ND
dari munculnya gejala klinis/ kematian hingga 100%. Ayam yang diberi priming
vaksin aktif bersamaan dengan vaksin inaktif memberi proteksi lebih tinggi
dibanding ayam yang diberi priming vaksin aktif karena vaksin inaktif yang ini
diberikan pada DOC dan tidak dipengaruhi oleh antibodi dari induk atau maternal
antibodi, sedangkan vaksin aktif yang diberikan pada hari pertama kemungkinan
terjadi netralisasi oleh maternal antibodi atau antibodi induk sehingga kekebalan
yang terbentuk tidak mencapai maksimal (Tabbu, 2000).
Program vaksinasi yang telah dilakukan seringkali titer antibodi yang
dihasilkan tidak seperti yang diharapkan. Langkah pencegahan seperti program
vaksinasi yang teratur dan kontinyu baik dengan cara suntik, semprot, tetes
mata/hidung, atau air minum serta biosekuriti di lingkungan peternakan tidak
diterapkan dengan baik karena kurangnya perhatian dan pemahaman masyarakat
tentang penyakit ND, sehingga wabah penyakit terus meluas (Malole, 2006;
Suryana, 2006) dan menyebabkan kerugian ekonomi yang signifikan (Antipas et al.,
2012). Hal ini dapat disebabkan oleh berbagai faktor, seperti karena faktor genetik,
Dilihat dari titer antibodi maternal pada anak ayam, titer antibodi maternal
akan menurun sejak hari ke-3 dan menurun terus hingga hari ke-12. Antibodi asal
induk ini akan menurun dengan cepat seiring meningkatnya umur ayam (Allan et al.,
1978). Menurut Gillingham (2006), waktu paruh untuk antibodi asal induk adalah
sekitar 3-5 hari dengan level imunitas protektif hingga 3 minggu. Transfer antibodi
ke embrio terjadi melalui dua tahap. Pertama, antibodi disimpan dalam kuning telur
dan albumin (putih telur) dan setelah itu ditransfer ke embrio. Induk mentransfer
Antibodi Maternal Dapatan (AMD) ke telur dengan cara menyimpan
Imunoglobulin Y (IgY), Imunoglobulin (IgA) dan Imunoglobulin (IgM) ke dalam
kuning telur dan albumin. IgY merupakan Ig isotope yang paling dominan pada
kuning telur. Immunoglobulin ini disekresikan oleh ovarium ayam kedalam ovum
(kuning telur) yang sedang berkembang dalam berbagai tahap. Hamal, et al (2006)
menemukan bahwa 27 sampai 30 % dari IgY induk di transfer ke keturunannya.
IgA dan IgM ditransfer ke embrio melalui albumen oleh usus embrio dan mungkin
memiliki fungsi utama pada anak ayam yang baru menetas sebagai Ig pelindung
disaluran pencernaan atau sebagai tambahan sumber protein.
Salah satu cara untuk mengukur tingkat kekebalan secara serologi
dikerjakan melalui uji Hemaglutination Inhibition (HI). Uji HI lebih banyak dipakai
karena selain mudah dan murah, uji ini spesifik dan dapat menunjukkan status
kekebalan pada ayam (Mirah Adi et a.l., 2012). Adapun Metode diagnostik yang
berbasis jaringan dan teknik Immunostaining yaitu Uji imunohistokimia (IHK).
Teknik ini dapat melacak distribusi virus pada berbagai organ sehingga dapat
dilakukan pada organ yang telah difiksasi dengan formalin sehingga virus yang
dilacak adalah virus yang sudah inaktif, penggunaan AbMo sebagai antibodi primer
dapat meningkatkan akurasi uji. Atas dasar permasalahan tersebut, penulis
melakukan penelitian tentang “pengaruh antibodi maternal terhadap
histopatogenesis virus newcastle disease lapang pada ayam broiler”.
1.2 Rumusan Masalah
1.2.1 Bagaimanakah profil titer antibodi maternal pada ayam broiler ?
1.2.2 Apakah titer antibodi maternal berpengaruh terhadap histopatogenesis virus
Newcastle disease pada ayam broiler khususnya terhadap munculnya gejala
syaraf?
1.2.3 Berapakah titer antibodi maternal yang protektif, subprotektif dan tidak protektif terhadap infeksi virus Newcastle disease lapang?
1.3 Tujuan Penelitian
Tujuan dari penelitian ini adalah untuk mengetahui :
1.3.1 Profil titer antibodi maternal pada ayam broiler.
1.3.2 Pengaruh titer antibodi maternal terhadap histopatogenesis virus Newcastle disease pada ayam broiler khususnya terhadap munculnya gejala syaraf.
1.3.3 Titer antibodi maternal yang protektif, subprotektif dan tidak protektif terhadap infeksi virus Newcastle Disease lapang.
1.4 Manfaat Penelitian
BAB II
TINJAUAN PUSTAKA 2.1 Virus Newcastle disease (ND)
Newcastle Disease (ND) biasa disebut juga sebagai Pseudo-Fowl Pest,
Pseudovogel-Pest, Atypische Gefugelpest, Pseudo-Poultry Plague, Avian Pest,
Avian Distemper, Ranilchet Disease, Tetelo Disease, Korean Fowl Plague, dan
Avian Pneumoencephalitis (Alexander, 2003).
Virus ND diklasifikasikan sebagai superfamily dari Mononegavirales dalam
famili Paramyxoviridae, genus Avulavirus (Mayo, 2002a; b). Family ini tergolong
kedalam virus RNA yang memiliki envelope. Komponen envelope ini merupakan
bagian virus yang bersifat infeksius (Alexander, 1991). Paramyxovirus berbentuk
pleomorfik. Secara umum, virus ini berbentuk bulat dengan diameter 100-500 nm
seperti terlihat pada Gambar 2.1, namun bentukan filament dapat terlihat dengan
panjang 100 nm (Alexander, 2003). Virion terdiri dari susunan helix nukleokapsid
yang berisi asam inti RNA rantai tunggal (ssRNA), dikelilingi envelope atau
membrane tipis yang terdiri dari lipid bilayer, lapisan protein dan glikoprotein yang
berbentuk paku menonjol pada permukaan partikel (Alexander, 1991).
Galur ND terdiri dari 10 grup genetik (I – X) dan dibagi lagi ke dalam
subgenetik (VI a hingga VI h dan VII a hingga VII e). Secara serologi, virus ND
terdiri dari satu (single) grup, avian Paramyxovirus 1. Virusnya merupakan
negative single stranded-genome RNA dengan 15.186 kb (Seal et al., 2000), dengan
kode RNA langsung adalah RNA Polymerase, Hemagglutinin-neuraminidase
OIE mendefinisikan ND sebagai infeksi yang disebabkan oleh virus
APMV-1 dengan indeks ICPI 0,7 atau lebih besar bila disuntik pada ayam umur sehari (OIE,
2000). Virus ND memiliki dua pasang asam amino dasar, yaitu Lysine (K) atau
Arginine (R) (Sudarisman, 2009).
Gambar 2.1. Virus Newcastle disease (Yan, 2008).
Genom virus ini mempunyai 6 protein utama yang menyusunnya yaitu
Nucleocapsid protein (N), Phosphoprotein (P), Matrix protein (M), Fusion protein
(F), Hemagglutinin-neuraminidase protein (HN) dan Large polymerase protein
(L). Protein N, P, HN dan F terletak di bagian luar envelope sedangkan protein M
terdapat di lapisan dalam virion. Protein-protein ini mempunyai peran
masing-masing dalam menentukan virulensi virus ND (Hewajuli and Dharmayanti, 2011).
menyerang berbagai jenis unggas terutama pada ayam. Newcastle Disease
merupakan suatu penyakit yang bersifat komplek, oleh karena isolat dan strain virus
yang berbeda dapat menimbulkan variasi yang besar dalam derajat keparahan dari
penyakit, termasuk pada spesies unggas yang sama, misalnya ayam (Tabbu, 2000).
Virus yang tergolong genus Paramyxovirus dapat dibedakan dari virus
lainnya oleh karena adanya aktifitas neuraminidase yang tidak dimiliki oleh virus
lain pada famili Paramyxoviridae. Virus ND mempunyai aktifitas biologik yaitu
kemampuan untuk mengaglutinasi dan menghemolisis sel darah merah atau fusi
dengan sel-sel tertentu, mempunyai kemampuan neuraminidase dan kemampuan
untuk bereplikasi di dalam sel-sel tertentu (Tabbu, 2000).
Salah satu aktivitas biologis virus ND dapat mengagglutinasi sel darah
merah semua amphibi, reptilia, manusia, tikus dan marmot. Sel darah merah sapi,
kambing, domba, babi dan kuda juga dapat di aglutinasi virus ND tergantung pada
strain virus (Alexander and Senne, 2008). Mekanisme terbentuknya hemaglutinasi
sel darah merah oleh virus ND dengan reseptor sel disebabkan adanya ikatan antara
protein hemagglutinin pada virus ND dengan reseptor yang ada dipermukaan sel
darah merah, yaitu suatu mukoprotein yang terdapat pada permukaan eritrosit
(MacLahlan and Dubovy, 2011).
2.1.1 Serotype avian paramyxovirus (APMV)
Berdasarkan hasil uji Hemagglutination Inhibiton (HI) dan Neuraminidase
Inhibition (NI) genus Avulavirus ini terdiri dari sembilan serotype yakni APMV
serotype 1 sampai dengan serotype 9 (Aldous dan Alexander, 2001). Virus ND
APMV-1 merupakan anggota dari mononegavirales pada family Paramyxoviridae.
Familiy ini dipecah menjadi dua subfamily yaitu Paramyxovirinae dan
Pneumovirinae. Pada Famili Paramyxovirus banyak yang bersifat patogan pada
manusia dan hewan yang dapat menyebabkan penyakit seperti Cacar air/Campak,
Gondok, Virus Nipah, virus pernafasan syncytial pada manusia, virus
parainfluenza, Virus Sendai dan Infeksi NDV. Penataan ulang terhadap Family
Paramyxoviridae oleh Komite Internasional tentang Taksonomi Virus pada tahun
1993 bahwa APMV-1 ditempatkan dalam genus Rubulavirus. Semenjak adanya
perbedaan waktu pada Family Paramyxoviridae menyebabkan pengembangan
genus baru Avulavirus (Hines and Miller, 2012).
Avian Paramyxovirus tipe-2 (APMV-2) dapat ditemukan pada burung,
termasuk burung peliharaan dan jarang pada ayam atau kalkun. Avian
Paramyxovirus tipe-3 (APMV-3) dapat ditemukan pada burung peliharaan dan
kalkun di kanada, USA, UK, Perancis dan Jerman (Fenner, 1993). Serotype
APMV-4, APMV-5, APMV-6, APMV-7, APMV-8 dan APMV-9 pada umumnya menyerang
itik, angsa, merpati, betet dan beberapa jenis unggas lainnya, akan tetapi tidak
menimbulkan gejala klinis (Saepulloh, 2005).
Reaksi silang pada Hambatan Haemaglutinas (HI) dan tes lainnya telah
mendeteksi beberapa serotype APMV. Namun, penggunaan berbagai serologi dan
tes non-serologi cenderung untuk meneguhkan kekhasan dari serotipe APMV.
reaktivitas silang cukup tinggi dengan APMV-1 antisera konvensional yang dapat
menyebabkan masalah. Antibodi terhadap virus APMV-3 terdeteksi pada ayam
dengan tingkat antibodi yang tinggi terhadap NDV sebagai akibat dari vaksinasi
(Alexander, 2000).
Variasi antigenik antara virus dalam APMV serotype sudah pernah
dilaporkan pada sebagian besar serotipe dimana lebih dari beberapa isolat telah
diperoleh. Untuk NDV (APMV-1), perbedaan dideteksi dengan tes HI
konvensional sudah pernah dilaporkan, meskipun jarang. Disebutkan bahwa virus
jenis ini sudah pernah terjadi pada panzootik balapan merpati yang terjadi selama
1980-an. APMV NDV pada merpati terbukti berbeda dengan strain standar dalam
tes HI, meskipun itu tidak cukup berbeda sehingga Vaksin ND yang konvesional
tidak protektif. Variasi yang nyata telah dicatat antara virus yang ditempatkan di
serotipe APMV-2, APMV-3 dan APMV-7. Variasi yang dicatat sering kali
menunjukkan dua virus dengan hubungan satu sama lain, tetapi masing-masing
menunjukkan kemiripan yang kuat pada ketiga virus tersebut (Alexander, 2000).
Dari APMV yang lain, hanya jenis virus APMV-2 dan APMV-3 yang
terbukti menginfeksi dan menyebabkan penyakit pada unggas, meskipun virus
APMV-6 dan APMV-7 telah dikaitkan dengan penyakit klinis pada kalkun. Virus
APMV-2 virus mengakibatkan penyakit pernapasan ringan. Namun, penyakit akan
menjadi lebih serius dan memburuk jika ada infeksi oleh organisme lain. Virus
Avian Paramyxovirus serotipe 2 dikaitkan dengan masalah pernapasan dan
mortalitas tinggi. Penyakit ini biasanya lebih parah pada kalkun dibandingkan
dengan ayam (Alexander, 2000).
Virus Avian Paramyxovirus serotipe 3 dikaitkan dengan penyakit
pernafasan dan masalah produksi telur pada kalkun. Sampai saat ini, tidak ada
infeksi alami yang dilaporkan pada ayam, meskipun infeksi eksperimental
menunjukkan bahwa unggas rentan terhadap serotype ini. Infeksi yang sederhana
pada kalkun, tanda pertama adalah sering mengalami penurunan produksi telur dan
gejala pernafasan yang ringan. Penurunan produksi telur bervariasi sesuai dengan
umur unggas da nada tidaknya infeksi sekunder (Infeksi ganda NDV I Aktif
vaksin), Virus Influenza, Clamydia, Mikoplasma atau bakteri lainnya. Tidak ada
penelitian yang melaporkan adanya lesi yang disebabkan oleh APMV-3 pada
kalkun. Avian Paramyxovirus serotipe 6 telah diisolasi pada kalkun dengan
masalah produksi telur dan pernapasan yang ringan. Virus APMV-7 dilaporkan
sebagai patogen utama dalam wabah penyakit pernapasan dengan mortalitas yang
tinggi pada kalkun. Penyakit pernapasan ringan ditunjukkan pada kalkun terinfeksi
eksperimental (Alexander, 2000).
2.1.2 Cara penularan virus ND
Virus ND yang terutama bereplikasi di dalam saluran pencernaan akan
menyebabkan adanya feses yang tercemar oleh virus tersebut. Penularan virus ND
juga dapat terjadi secara oral akibat ingesti feses yang mengandung virus tersebut
diantara strain Paramyxovirus adalah terletak pada cepat atau lambatnya
perbanyakan virus bersangkutan (Russel, 1993).
Penularan virus ND dapat secara langsung dari ayam yang sakit ke ayam
yang peka, tetapi dapat juga terjadi secara tidak langsung melalui bahan, alat atau
pekerja yang tercemar virus tersebut. Cara penularan virus ND dari ayam yang sakit
ke ayam yang peka tergantung pada tempat bereplikasi dari virus tersebut. Ayam
yang menunjukkan gejala gangguan pernafasan akan menyebabkan adanya udara
bercampur titik air yang mengandung virus ND yang berasal dari mukus ayam sakit.
Penularan virus ND dapat terjadi secara inhalasi (Tabbu, 2000). Penularan penyakit
ND secara aerosol dapat terjadi meskipun jaraknya cukup jauh yakni 64 meter dari
sumber infeksi (Kencana, 2012).
Virus ND dapat ditemukan dalam telur ayam yang terinfeksi virus tersebut
tapi penularan secara transovarial mungkin tidak terjadi oleh karena embrio sudah
mati sebelum telur menetas. Virus ini juga dapat menembus kerabang telur untuk
menginfeksi embrio (Fenner, 1993). Penularan melalui telur ini dapat terjadi akibat
kulit telur terkontaminasi oleh feses yang telah mengandung virus ND (Kencana,
2012).
Penyebaran virus ini sangat cepat, baik dari ayam ke ayam maupun dari
kandang ke kandang. Ayam yang menderita penyakit ini akan akan menghasilkan
telur yang mengandung virus ND, sehingga telur yang mengandung virus tersebut
tidak akan menetas. Dua hari setelah virus menginfeksi ayam, ayam sudah menjadi
sumber penyakit yang siap menebar pada kelompoknya, dan dari kandang ke
sakit dan pada karkas ayam yang mati karena ND. Di samping oleh ayam,
penyebaran penyakit dapat melalui burung piaraan atau burung liar yang ada di
sekitar atau masuk ke dalam kandang. Peranan dari berbagai faktor di atas dalam
penularan virus ND tergantung pada berbagai faktor manajemen dan lingkungan
tempat suatu peternakan beroperasi. Keberhasilan penularan virus ND erat
hubungannya dengan kemampuan virus tersebut bertahan dalam bangkai ayam atau
ekskresi dari ayam sakit. Di dalam bangkai ayam yang terinfeksi, virus ND dapat
bertahan selama beberapa minggu pada temperatur rendah atau selama beberapa
tahun jika disimpan pada temperatur beku. Feses dapat mengandung virus ND
dalam jumlah yang banyak, pada temperatur 37○C virus tersebut masih tetap hidup
selama lebih dari satu bulan (Tabbu, 2000).
Unggas yang terinfeksi ND dapat mengeluarkan virus selama 1 sampai 2
minggu kecuali pada burung psittacine yang dapat mengeluarkan virus selama
beberapa bulan sampai lebih dari setahun. Adanya sekresi virus dalam waktu yang
lama oleh burung psittacine menyebabkan burung ini menjadi sumber penular
penting dari virus ND terutama daerah endemis (Kencana, 2012).
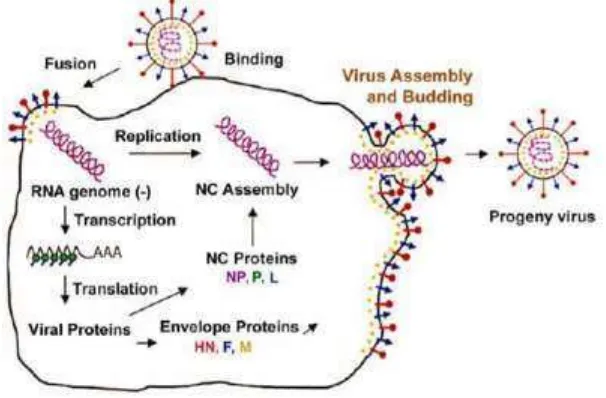
2.1.3 Siklus hidup dan mekanisme infeksi virus ND
Strategi replikasi yang digunakan oleh ND mirip dengan virus RNA
non-segmented negatif lainnya.Langkah awal replikasi adalah adsorpsi dengan reseptor
sel permukaan virus diikuti penyatuan dengan membran sel host. Penyatuan ini
turunan yang sudah matang akan menembus membran plasma (Gambar 2.2) (Yan,
2008).
Gambar 2.2 Siklus Hidup dan Mekanisme Infeksi ND (Yan, 2008).
Amplop virus ND terdiri atas dua glikoprotein, yakni HN dan F yang
berperan amat penting dalam proses infeksi. Protein HN memediasi terjadinya
perlekatan virus dengan sel inang pada reseptor sel inang atau induk semang yang
mengandung sialic acid. Molekul sialic acid ini adalah glycoprotein dan glycolipid.
Protein F berperan dalam pembentukan sinsitia pada sel yang terinfeksi.
Penggabungan amplop virus dengan membran sel target merupakan tahapan yang
paling penting dalam mekanisme infeksi virus ND dan protein F begitu juga HN
memegang peranan penting dalam proses ini. Protein HN bertanggung jawab dalam
pelekatan virion ke sel target, sedangkan protein F berfungsi untuk menghancurkan
sel target serta menginduksi terjadinya penggabungan membran (Mirah Adi et al.,
2008). Penempelan virus dilakukan dengan penyatuan virus dan membran sel yang
terjadi replikasi. Envelope virus masuk ke dalam sel melalui 2 jalan utama yaitu
pertama, penyatuan secara langsung antara envelope virus dengan membran plasma
dan kedua, diperantarai oleh reseptor endositosis. Penetrasi virus melalui reseptor
endositosis tergantung pada kondisi pHnya. Pada Paramyxoviruses, proses
penyatuan membran virus dengan membran plasma inang atau induk semang tidak
tergantung pH. Walaupun demikian, hasil penelitian sebelumnya menunjukkan
bahwa penyatuan virus ND dengan sel mampu meningkatkan pH. Hasil tersebut
mengindikasikan bahwa penetrasi virus ND pada sel inang melalui reseptor
endositosis juga dipengaruhi oleh kondisi pH (Dharmayanti and Hewajuli, 2011).
Kepekaan sel terhadap virus ND yang tidak virulen dipengaruhi oleh
beberapa faktor. Sel tersebut harus mempunyai reseptor yang cocok sehingga virus
dapat melakukan penempelan dan masuk ke dalam sel. Disamping itu, sel tersebut
juga harus memiliki tripsin yang menyerupai protease dimana enzim ini berperan
dalam pemecahan protein F0 menjadi F1 dan F2. Penyebaran reseptor sel pada
ayam yang peka terhadap virus ND bentuk tidak virulen bersifat terbatas dan hanya
ditemukan pada saluran pencernaan dan saluran pernafasan bagian atas (Alexander,
1991). Sedangkan virus bentuk virulen tidak selalu memerlukan enzim protease dan
replikasi virus biasanya terjadi di sebagian besar jaringan induk semang. Replikasi
virus yang terjadi di limfosit menghasilkan suatu respon imun dan produksi antigen
virus yang cukup dibutuhkan untuk meningkatkan efektivitas sistem imun. Di
beberapa bagian saluran pencernaan dapat mengaktifkan virus ND bentuk tidak
virulen setelah virus tersebut dilepaskan dari sel yang kekurangan enzim protease.
Antigen virus ND dideteksi pada sebagian besar sel epitel saluran pencernaan serta
limfosit dan makrofag ditemukan pada lamina propia beberapa jaringan. Hasil
penelitian di atas memperlihatkan bahwa tempat awal replikasi virus ND terutama
terjadi di saluran pencernaan bagian atas yaitu esophagus, tembolok dan
proventrikulus apabila virus ND diinfeksikan melalui mulut, sedangkan replikasi
virus ND pada saluran pencernaan bagian bawah yaitu duodenum, jejunum, ileum
dan caecum kemungkinan terjadi sebagai akibat viremia (Dharmayanti and
Hewajuli, 2011).
2.1.4 Pathotype virus ND
Terdapat tiga pathotype didalam Virus ND yang dikelompokkan berdasarkan
atas waktu kematian embrio, yakni: lentogenic adalah strain virus yang kurang ganas
ditandai dengan kematian embrio lebih dari 90 jam, mesogenic antara 60-90 jam,
sedangkan velogenic kurang dari 60 jam (Saif, 2003). Virus ND tipe lentogenic
menunjukkan gejala klinis pada ternak ayam yang bersifat ringan atau tanpa gejala
klinis. Virus ND tipe mesogenic dengan virulensi moderat (sedang) menunjukkan
gejala yang dari ringan sampai sedang. Sementara itu, virus ND velogenic adalah
tipe yang sangat ganas ditandai dengan penyakit yang bersifat akut dan kematian
yang tinggi sampai 100%. Berdasarkan atas predileksinya dan gejala klinis yang
ditimbulkan, virus ND velogenik dibedakan lagi menjadi bentuk neurotropic dengan
Viscerotropic dengan kelainan pada sistima pencernaan (Aldous and Alexander,
2001).
Alexander and Senne (2008b) menyatakan bahwa berdasarkan tanda-tanda
klinis yang terlihat pada ayam yang terinfeksi NDV telah dikelompokkan menjadi
lima pathotype. Viscerotropic velogenic: bentuk yang sangat patogen di mana lesi
usus hemoragik sering terlihat; Neurotropic velogenic: bentuk yang ditandai dengan
kematian yang tinggi, biasanya diikuti dengan gejala pernapasan dan saraf;
Mesogenic: bentuk yang ditandai dengan gejala pernapasan, gejala saraf sesekali, tapi
tingkat kematian rendah; Lentogenic: bentuk yang menunjukkan adanya infeksi
pernafasan ringan atau subklinis; dan Asimtomatic: bentuk yang biasanya ditandai
dengan infeksi enterik yang bersifat subklinis.
Tabbu (2000) menjelaskan bahwa unggas yang terinfeksi virus ND terutama
dari tipe velogenic viscerotropic (VVND) gejala klinis yang ditimbulkan antara lain
terjadi kelesuan, peningkatan frekuensi pernafasan, kehilangan nafsu makan,
penurunan konsumsi air minum, kelemahan dan berakhir kematian. Adi, et al (2009)
menjelaskan bahwa ayam yang terinfeksi virus ND velogenik gejala klinis yang
ditimbulkan dehidrasi, badan mengalami kekurusan dan diare kehijauan yang
menempel di sekitar kloaka.
2.1.5 Masa inkubasi dan gejala klinis ND
Masa Inkubasi sangat bervariasi tergantung pada strain virus, jenis unggas,
Gejala klinis penyakit ND pada infeksi virus galur velogenik dapat
menimbulkan gejala gangguan pernapasan seperti sesak napas, ngorok, bersin serta
gangguan syaraf seperti kelumpuhan sebagian atau total, tortikolis, serta depresi.
Tanda lainnya adalah adanya pembengkakan jaringan di daerah sekitar mata dan
leher. Infeksi virus galur mesogenik menimbulkan gejala klinis seperti gangguan
pernapasan yaitu sesak napas, batuk, dan bersin. Infeksi virus galur lentogenik
menunjukkan gejala ringan seperti penurunan produksi telur dan tidak terjadinya
gangguan syaraf pada unggas terinfeksi. Morbiditas dan mortalitas tergantung pada
tingkat virulensi dari galur virus, tingkat kekebalan vaksin, kondisi lingkungan, dan
kepadatan ayam di dalam kandang (OIE, 2002).
Tanda - tanda klinis ayam terserang tetelo adalah lemah, nafsu makan
menurun, gangguan pernafasan, gangguan syaraf, minum lebih banyak dan sering
berkerumun atau berkumpul ditempat hangat. Secara patologis, gejalanya antara
lain kantung hawa keruh, proventriculus mengalami pendarahan berupa
bintik-bintik merah, terjadi enteritis dan nekrosa pada usus, eksudat kental berwarna
kehijauan bercampur darah, terdapat peradangan sinus hidung, trakea dan laring,
serta pneumonia (Sudaryani and Santoso, 2003).
2.1.6 Perubahan patologi anatomi dan histopatologi
Perubahan makroskopis pada saluran pencernaan meliputi hemoragi pada
proventrikulus, duodenum dan seka tonsil (Capua and Terregino, 2009). Bagian
yang mendapat perhatian adalah seka tonsil, dimana terdapat nekrosis apabila dibuka
dan perubahan hiperemi di sebagian besar organ terutama otak. Lesi mikroskopik
limpa, timus dan jaringan limfoid mukosa usus), trakheitis, pneumonia, salfingitis,
nekrosis hati, pankreatitis dan konjungtivitis. Beberapa kajian melaporkan tentang
pembentukan ensefalomalasia dan pankreatitis nekrotik pada ND (Tabbu, 2000).
Pada usus halus lesi nekrotik hemoragi bersifat multifokal, secara histopatologi
terlihat nekrosis fokal maupun difus serta infiltrasi sel-sel mononuklear pada jaringan
limpa, hati, ginjal, paru-paru, usus, sekum, proventrikulus dan otak (Oladele et al.,
2008). Meskipun tidak ada lesi patognomonik, hemoragi pada intestinal bisa
digunakan untuk membedakan velogenik viserotropik ND dengan velogenik
neurotropik ND (Alexander 2001).
Akoso (1998) menyatakan bahwa pada kasus ND hasil bedah bangkai
memperlihatkan gejala khas, seperti adanya petechiae pada proventrikulus,
perubahan pada lapisan usus berupa hemoragi dan nekrosa, pada organ pernafasan
akan terjadi eksudasi dan kantung udara menebal. Menurut Tabbu (2000), perubahan
makroskopik yang ditemukan biasanya erat hubungan dengan galur tipe patologik
dari virus ND, pada VVND tersifat oleh adanya nekrosis dan hemoragik pada saluran
pencernaan, meliputi proventrikulus, ventrikulus dan berbagai bagian usus, dimana
lesi tersebut dapat dipakai untuk membedakan VVND dengan NVND. Velogenik
viserotropik ND menimbulkan merah dan bengkak pada konjungtiva, nekrosis
multifokal pada limpa, hemoragi pada mukosa proventrikulus, duodenum, seka
tonsil, atrofi bursa Fabricious dan timus (Nakamura et al., 2010).
semua sampel ayam ditemukan perdarahan yang meluas di proventrikulus dan di
organ usus halus ditemukan fokus nekrotik-hemoragika. Pada pemeriksaan
histopatologi, lumen kelenjar proventrikulus terlihat membesar dan berisi sel-sel
runtuhan, adanya hiperemi hingga hemoragi, nekrosis parah, edema serta endotel
yang rusak (Nuryanto, 2012).
Adi, et al (2010) melaporkan bahwa ayam terserang ND ketika wabah di Bali
menunjukkan atrofi pada organ-organ limfoid seperti bursa Fabrisius, timus dan
limpa; hemoragi intestinal dan edema pada otak. Pemeriksaan histopatologi
menunjukkan meningoensefalomyelitis nonsuppuratif ditandai dengan nekrosis
neuron, gliosis multifokal sampai difus dan perivascular cuffing dari sel-sel
mononuklear, nekrosis hemoragik pada trakhea dan usus serta deplesi dan nekrosis
pada jaringan limfoid termasuk bursa Fabrisius.
2.2Vaksin dan vaksinasi
Vaksin adalah suatu produk biologis yang berisi mikroorganisme agen
penyakit yang telah dilemahkan atau diinaktifkan (atte~zuated). Vaksin secara umum
adalah bahan yang berasal dari mikroorganisme atau parasit yang dapat merangsang
kekebalan terhadap penyakit yang bersangkutan (Malole, 1988). Bahan yang berisi
organisme penyebab penyakit tersebut jika dimasukkan ke dalam tubuh hewan tidak
menimbulkan bahaya penyakit tetapi masih dapat dikenal oleh sistem imun (Kayne
and Jepson, 2004) serta dapat merangsang pembentukan zat-zat kekebalan terhadap
agen penyakit tersebut (Tizard, 1988) dan tindakan ini dikenal dengan istilah
Vaksin terdiri atas vaksin aktifd dan vaksin inaktif. Agen penyakit dalam
vaksin aktifd atau vaksin hidup berada dalam keadaan hidup namun telah
dilemahkan. Agen penyakit pada vaksin inaktif berada dalam keadaan mati dan
biasanya ditambahkan dengan adjuvant (Akoso, 1988). Adjuvan merupakan bahan
kimia yang memperlambat proses penghancuran antigen dalam tubuh serta
merangsang pembentukan kekebalan sehingga menghasilkan antibodi sedikit demi
sedikit (Malole, 1988). Umumnya vaksin aktif lebih baik daripada vaksin inaktif,
karena vaksin aktif dapat memberikan respon kekebalan yang lebih kuat, dapat diberi
tanpa penambahan adjuvan dan dapat merangsang produksi interferon (Tizard,
1988). Namun vaksin aktifd sering memperlihatkan gejala post-vaksinasi yang
kurang baik seperti gangguan pemafasan yang ringan dan menurunnya produksi telur
(Wetsbury et al., 1984).
Keberhasilan vaksinasi dipengaruhi oleh mutu vaksin. Vaksin yang ideal
harus mempunyai mutu yang baik, mutu vaksin akan menurun jika tidak disimpan
dengan baik setelah diterima oleh pengguna. Kondisi yang dapat merusak
keampuhan vaksin antara lain penyimpanan yang tidak sempurna, pengenceran yang
berlebihan saat akan digunakan, serta air pencampuran yang menganduing chlorin
atau bahan sanitasi. Menurut Malole (1988), vaksin yang baik harus memenuhi
beberapa persyaratan, yaitu kemurnian, keamanan, serta vaksin harus dapat
menimbulkan kekebalan terhadap penyakit pada hewan. Suatu vaksin dapat
lebih dari 95% terhadap hewan coba atau tidak lebih dari 5% hewan yang terinfeksi
atau sakit atau mati. Menurut Akoso (1998), selain mutu vaksin, keberhasilan
vaksinasi juga dipengaruhi oleh status kesehatan unggas, keadaan nutrisi unggas,
sanitasi lingkungan dan sistem perkandangan, serta program vaksinasi yang baik.
Vaksin ND dapat berasal dari virus tipe lentogenik, mesogenik, maupun
velogenik. Tipe lentogenik merupakan strain virus ND yang virulensi dan
mortalitasnya rendah yaitu strain B1 (Hitcher), strain La Sota, dan strain F (FA0,
2004). Strain F memiliki tingkat virulensi paling rendah dibandingkan dengan strain
lain pada tipe lentogenik. Vaksin dengan strain ini paling efektif dilakukan secara
individu. Strain B1 rnemiliki tingkat virulensi lebih tinggi dibandingkan dengan
strain F. Aplikasi vaksin strain B1 dilakukan melalui air minum atau penyemprotan.
Pemberian vaksinasi dilakukan pada DOC (Day Old Chick) kemudian diikuti dengan
strain La Sota pada umur 10-14 hari (Fadilah and Polana, 2004).
Tipe mesogenik memberikan kekebalan yang lebih lama dibanding kekebalan
yang dihasilkan oleh tipe lentogenik. Namun pemberian vaksin tipe mesogenik pada
ayam yang belum mempunyai kekebalan dasar dapat menimbulkan reaksi
post-vaksinasi dan penurunan produksi telur (Nugroho, 1981). Tipe mesogenik yang
dipakai sebagai vaksin diantaranya adalah strain Rokain, strain Mukteshwar, strain
Kommarov, dan strain Bankowski (Sudrarjat, 1991). Strain Mukteshwar bersifat
patogenik dan digunakan secara terbatas pada ayam yang sebelumnya telah divaksin
dengan salah satu jenis vaksin tipe lentogenik. Vaksin ini telah diterima secara luas
pada iklim tropis di Asia Tenggara. Strain Kommarov memiliki tingkat virulensi
Bankowski (Tissue Culture Vaccine) sering disebut dengan wing-web vaccine.
Vaksin dengan strain ini tidak bisa digunakan pada ayam muda yang masih memiliki
maternal immunity (Fadilah dan Polana ,2004).
Tipe velogenik dibuat sebagai bahan vaksin dalam bentuk vaksin inaktif
(Nugroho, 1981). Karena tipe velogenik melupakan virus dengan tingkat virulensi
yang sangat tinggi (FAO, 2004). Tipe asiinptomatik yang inempunyai kemampuan
menimbulkan kekebalan tubuh dikenal dengan strain V4 dan Vister 2C. Strain ini
sangat potensial digunakan sebagai vaksin di daerah tropis karena merupakan vaksin
yang mengandung virus tahan panas (Darminto, 2002).
2.3 Sistem Kekebalan Unggas
Sistem kebal adalah bentuk adaptasi dari sistem pertahanan pada vertebrata
sebagai pelindung terhadap serangan mikroorganisme patogen dan kanker. Sistem
ini dapat membangkitkan beberapa macam sel dan molekul yang secara spesifik
mampu mengenali dan mengeliminasi benda asing (Decker, 2000). Menurut Tizard
(2004), tanggap kebal merupakan respon biologis sehingga dapat menyebabkan
variasi tanggap kebal bagi setiap individu. Sistem kekebalan unggas dibagi menjadi
sistem kekebalan non-spesifik dan sistem kekebalan spesifik (Carpenter, 2004).
Mekanisme kedua sistem kekebalan tersebut tidak dapat dipisahkan satu sama
lainnya, keduanya saling meningkatkan efektivitasnya dan terjadi interaksi sehingga
menghasilkan suatu aktivitas biologik yang seirama dan serasi (Fenner and Fransk,
2.3.1 Sistem kekebalan non spesifik unggas
Sistem kekebalan non-spesifik merupakan sistem kekebalan yang secara
alami diperoleh tubuh dan proteksi yang diberikannya tidak terlalu kuat. Semua agen
penyakit yang masuk ke dalam tubuh akan dihancurkan oleh sistem kekebalan
tersebut sehingga proteksi yang diberikannya tidak spesifik terhadap penyakit
tertentu (Butcher and Miles, 2003).
Kekebalan bawaan umumnya bersifat non-spesifik. Kekebalan bawaan
adalah kekebalan yang dibawa oleh individu sejak lahir dan umumnya bersifat tidak
spesifik karena kerjanya tidak tergantung terhadap aktivitas antigen yang spesifik.
Komponen kekebalan bawaan dapat berupa bawaan primer yang terdiri dari (1)
barrier fisik dan kimia seperti bulu dan kulit, lapisan epitel mukosa dan mucus, (2)
sel fagosit, seperti makrofag dan sel pembunuh alami (natural killer) (3) sistem
komplemen dan medistor inflamasi dan (4) sitokin.
Antigen yang berhasil masuk ke dalam tubuh dengan melewati sistem
pertahanan tubuh non-spesifik akan berhadapan dengan makrofag. Makrofag
berfungsi melalui proses fagositosis dengan membunuh, menghancurkan, dan
mengeliminasi antigen dari tubuh. Sel makrofag ini meliputi sel Langerhans di kulit,
sel kupffer di hati, sel debu di paru-paru, sel histiosit di jaringan, dan astrosit di sel
syaraf. Sel mikrofag meliputi sel neutrofil, basofil, dan eosinophil (Wibawan et al.,
2003).
Respon imun bawaan terhadap virus biasanya berlangsung cepat yang
penyebaran virus didalam tubuh. Beberapa respon imun bawaan juga berperan dalam
meningkatkan kekebalan dapatan (Adi and Astawa, 2014).
2.3.2 Sistem kekebalan Spesifik Unggas
Sistem kekebalan spesifik terdiri dari sistem berperantara sel (Cell Mediated Immunity) dan sistem kekebalan berperantara antibodi (Antibody Mediated
Immunity) atau yang lebih dikenal dengan sistern kekebalan humoral (Butcher dan
Miles 2003). Antigen yang berhasil masuk ke dalam tubuh dengan melewati sistem
pertahanan tubuh non-spesifik akan berhadapan dengan makrofag. Selain berfungsi
melakukan fagositosis, makrofag juga berfungsi sebagai Antigen Presenting Cells
(APC) yang dikenal juga sebagai sel penyaji atau sel penadah yang akan
menghancurkan antigen sedemikian rupa sehingga seluruh komponennya dapat
berinteraksi dengan sistem imun spesifik atau antibodi. Makrofag yang berfungsi
sebagai APC ini akan memfragmentasikan dan mempresentasikan antigen tersebut
kepada sel limfosit T-helper (Th) melalui molekul Major Histocompatibility
Complex (MHC) yang terletak dipermukaan makrofag (Wibawan et al., 2003).
Sel limfosit yang berperan penting dalam sistem kekebalan terbagi menjadi
dua, yaitu sel B dan sel T. Sel B di dalam tubuh mamalia secara umum matang dan
berdiferensiasi dalam sumsum tulang, sedangkan dalam tubuh unggas sel B matang
dan berdiferensiasi dalam bursa fabrisius. Sel T di dalam tubuh mamalia dan unggas
matang dan berdiferensiasi pada kelenjar timus. Sel B merupakan bagian dari
menempel pada antigen asing yang memberi tanda agar dapat dihancurkan oleh sel
sistem imun (Darmono, 2006).
Sel B akan mengalami proses perkembangan melalui dua jalur setelah terjadi
rangsangan antigen, yaitu berdiferensiasi menjadi sel plasma dan sel memori. Sel
plasma akan membentuk immunoglobulin. Jumlah immunoglobulin dalam setiap sel
B adalah sekitar l04 sampai 107(Tizard, 1982). Sel plasma akan mati setelah tiga
sampai enam hari, sehingga kadar immunoglobulin akan menurun secara
perlahan-lahan melalui katabolisme. Sel memori hidup berbulan-bulan atau tahunan setelah
pemaparan antigen yang pertama kali. Jika terjadi pemaparan kedua kalinya dengan
antigen yang sama, maka antigen akan merangsang lebih banyak lagi sel peka
antigen daripada pemaparan pertama. Dengan adanya sel memori, maka sistem
pembentukan antibodi memiliki kemampuan untuk mengingat keterpaparan dengan
suatu antigen sebelumnya. Antibodi yang dihasilkan hanya bereaksi dengan antigen
yaug ada di permukaan sel. Tanggap kebal humoral unggas dicirikan dengan antibodi
yang diproduksi oleh sel B yang berada di bawah kontrol bursa Fabrisius. Bursa
Fabrisius merupakan organ limfoid primer yang terletak di bagian dorsal kloaka dan
hanya ada pada unggas (Wibawan et al., 2003). Menurut Azmijah (2005), bursa
fabrisius mengalami perkembangan maksimum ketika berumur tiga sampai enam
minggu.
Sel T yang bersirkulasi dalam darah dan limfe dapat secara langsung
menghancurkan antigen asing. Sel T bertanggung jawab atas cell mediated immunity
atau imunitas seluler. Sel T bergantung pada molekul permukaan yaitu MHC nntuk
yang dapat distimulasi oleh tipe antigen yang berbeda. Antigen virus yang terdapat
pada sel yang terinfeksi akan dipresentasikan bersama-sama dengan MHC kelas I
dan akan menstimulasi sel T CD8+ (sitotoksik). Sedangkan antigen mikroba
ekstraseluler akan diendositosis oleh APC dan dipresentasikan dengan MHC kelas II
dan akan mengaktivasi sel T CD4+ (helper). Antigen yang menempel pada MHC
kelas I1 dan sel T CD4+ akan memacu produksi antibodi dan mengaktifkan
makrofag. Interaksi antara sel Th dengan APC akan menginduksi pengeluaran
sitokin atau interleukin yang merupakan alat komunikasi antar sel sehingga akan
menginduksi pematangan sel B. Sitokin yang dikeluarkan oleh limfosit disebut
limfokin sedangkan sitokin yang dikeluarkan oleh makrofag disebut monokin. Selain
alat komunikasi, sitokin juga berfungsi dalam mengendalikan respon imun dan reaksi
inflamasi dengan cara mengatur pertumbuhan serta mobilitas dan diferensiasi
leukosit maupun sel lain (Puspitasari, 2009).
Kekebalan humoral yang dihasilkan oleh sel B tidak dapat berespon terhadap
antigen yang terdapat didalam sel, sehingga mekanisme kekebalan seluler yang
berperan. Sel yang berperan dalam mekanisme kekebalan seluler adalah sel limfosit
Tcytotoxic (Tc). Sel ini akan mencari sel-sel yang mengalami kelainan fisiologis
untuk kemudian menghancurkan seluruh sel tersebut beserta antigen yang ada di
dalamnya. Tujuan penghancuran ini adalah untuk mencegah penyebaran antigen
intraseluler ke sel-sel sehat lain yang ada di sekitarnya (Wibawan et al., 2003).
lainnya. Pada unggas, antibodi asal induk yang mendapatkan vaksinasi atau
terinfeksi secara alami akan mentransfer antibodi kepada anak melalui telur.
Imunitas pasif ini memiliki durasi yang relatif singkat, biasanya 1-2 minggu dan
umumnya kurang dari 4 minggu dan fungsinya adalah untuk melindungi anak ayam
muda selama periode (pertama beberapa minggu) saat sistem kekebalan tubuh
mereka belum sepenuhnya berkembang untuk menghadapi tantangan awal.
Transfer antibodi maternal dari induk ke anak
Transfer antibodi ke embrio terjadi melalui dua tahap. Pertama, antibodi
disimpan dalam kuning telur dan albumin (putih telur) dan setelah itu ditransfer ke
embrio.
a. Transfer Antibodi Maternal Dapatan (AMD) dari induk ke telur
Induk mentransfer AMD ke telur dengan cara menyimpan antibodi
Imunoglobulin Y (IgY), Imunoglobulin (IgA) dan Imunoglobulin (IgM) ke dalam
kuning telur dan albumin. Molekul IgG ayam lebih panjang daripada mamalia, IgG
ayam disebut oleh beberapa peneliti sebagai IgY. Namun pada IgG (IgY) unggas
secara fungsional homolog dengan IgG mamalia. Jalur penyimpanan
Immunoglobulin (Ig) pada telur berbeda. IgY merupakan Ig isotope yang paling
dominan pada kuning telur. Immunoglobulin ini disekresikan oleh ovarium ayam
kedalam ovum (kuning telur) yang sedang berkembang dalam berbagai tahap.
Berjalannya IgY ke ovum diatur oleh epitel folikular yang mengalami
perubahan morfologis yaitu pembesaran ovum. Epitel ini menjadi lebih datar dan
lebih tipis di ovum yang lebih besar memungkinkan lewatnya IgY dalam jumlah