PEMANFAATAN SIRUP GLUKOSA HASIL HIDROLISA
AMILUM DARI BIJI KWENI (Mangifera odorata Grift) SEBAGAI
PEMANIS PADA PEMBUATAN MANISAN DARI BUAH SALAK
(Salacca edulis reinw)
SKRIPSI
RIRI MARDAWATI
080822012
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
UNIVERSITAS SUMATERA UTARA
MEDAN
2010
PEMANFAATAN SIRUP GLUKOSA HASIL HIDROLISA AMILUM DARI BIJI KWENI (Mangifera odorata Grift) SEBAGAIPEMANIS PADA
SKRIPSI
Diajukan untuk melengkapi tugas dan memenuhi syarat mencapai gelar Sarjana Sains
RIRI MARDAWATI 080822012
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM UNIVERSITAS SUMATERA UTARA
MEDAN 2010
PERSETUJUAN
Judul : PEMANFAATAN SIRUP GLUKOSA HASIL
PADA PEMBUATAN MANISAN DARI BUAH SALAK (Salacca edulis reinw)
Kategori : SKRIPSI
Nama : RIRI MARDAWATI
Nomor Induk Mahasiswa : 080822012
Program Studi : SARJANA (S1) KIMIA EKSTENSI Departemen : KIMIA
Fakultas : MATEMATIKA DAN ILMU PENGETAHUAN
ALAM (FMIPA) UNIVERSITAS SUMATERA UTARA
Diluluskan di Medan, Juni 2010
Komisi Pembimbing
Pembimbing II Pembimbing I
Dr. Rumondang Bulan Nst, M. S Prof. Dr. RA. Harlinah S.P.W,M. Sc NIP 195408301985032001 NIP 130175778
Diketahui/Disetujui oleh
Departemen Kimia FMIPA USU Ketua,
Dr.Rumondang Bulan Nst, M. S NIP 195408301985032001
PEMANFAATAN SIRUP GLUKOSA HASIL HIDROLISA AMILUM DARI
BIJI KWENI (Mangifera odorata Grift) SEBAGAI PEMANIS PADA
PEMBAUATAN MANISAN DARI BUAH SALAK (Salacca edulis reinw)
SKRIPSI
Saya mengakui bahwa skripsi ini adalah hasil kerja saya sendiri, kecuali beberapa kutipan dan ringkasan yang masing-masing disebutkan sumbernya.
Medan, Juni 2010
PENGHARGAAN
Puji dan syukur penulis panjatkan kepada Tuhan Yang Maha Pemurah dan Maha Penyayang, dengan limpahan karunia-Nya kertas kajian ini berhasil diselesaikan dalam waktu yang telah ditetapkan.
ABSTRAK
THE USE OF GLUCOSE SYRUP AS PRODUCT OF STARCH HIDROLYZE
FROM THE SEEDS OF MANGO ( Mangifera odorata Grift ) AS SWEETENER
ON CANDIES PRODUCTION FROM THE ZALACCA PALM ( Salacca edulis
reinw )
ABSTRACT
DAFTAR ISI
2.1.2. Jenis dan Varietas Tanaman Mangga 5
2.8 Manisan 19
3.3.4. Pengukuran Panjang Gelombang Maksimum Larutan Glukosa Standar 26
4.1.2. Pengolahan Data Pengukuran Absorbansi Glukosa Hasil Hidrolisis Amilum Biji Kweni 34
DAFTAR TABEL
Halaman
Tabel 2.1 Kandungan Zat Gizi Buah Mangga 8
Tabel 2.2 Kandungan Zat Gizi Buah Salak 11
Tabel 4.1 Larutan Glukosa Standar Pada Berbagai Konsentrasi 35 Tabel 4.2 Data Hasil Perhitungan Kadar Amilum Biji Kweni 43 Tabel 4.3 Data Absorbansi Larutan Glukosa Standar Pada Berbagai Konsentrasi 43 Tabel 4.4 Data Hasil Perhitungan Kadar Gula Reduksi Berdasarkan Absorbansi
DAFTAR GAMBAR
Halaman
Gambar 2.1 Gambar Buah dan Biji Kweni 4
Gambar 2.2 Gambar Buah Salak 9
ABSTRAK
THE USE OF GLUCOSE SYRUP AS PRODUCT OF STARCH HIDROLYZE
FROM THE SEEDS OF MANGO ( Mangifera odorata Grift ) AS SWEETENER
ON CANDIES PRODUCTION FROM THE ZALACCA PALM ( Salacca edulis
reinw )
ABSTRACT
BAB 1
PENDAHULUAN1.1Latar Belakang
Suatu fakta teramat penting tentang gula belakangan ini adalah harganya yang melambung terus. Kebutuhan gula Indonesia mencapai 3,3 juta ton/tahun, sementara produksi dalam negeri hanya 1,7 juta ton atau 51,5% dari kebutuhan nasional, sehingga impor menjadi pilihan. Ironisnya, harga gula impor lebih murah dibandingkan dengan gula produksi dalam negeri. dalam situasi seperti ini, gula produksi dalam negeri menjadi sulit dipasarkan tanpa kebijakan yang mampu melindunginya dari serbuan gula impor.
Sirup glukosa atau sering juga disebut gula cair dibuat melalui proses hidrolisis pati. Perbedaannya dengan gula pasir atau sukrosa yaitu sukrosa merupakan gula disakarida, terdiri atas ikatan glukosa dan fruktosa, sedangkan sirup glukosa adalah monosakarida, terdiri atas satu monomer yaitu glukosa. Sirup glukosa dapat dibuat dengan cara hidrolisis asam atau dengan cara enzimatis. Dari kedua cara tersebut, pembuatan sirup glukosa secara enzimatis dapat dikembangkan di pedesaan karena tidak banyak menggunakan bahan kimia sehingga aman dan tidak mencemari lingkungan.
Karbohidrat daging buah mangga terdiri dari gula sederhana, tepung, dan selulosa. Gula sederhana yaitu sukrosa, glukosa, dan fruktosa. Gula tersebut memberikan rasa manis dan tenaga yang dapat segera digunakan oleh tubuh. Zat tepung mangga masak lebih sedikit dibandingkan dengan mangga mentah, karena tepung yang ada telah banyak berubah menjadi gula. (Pracaya, 2004)
kentang, ubi kayu, dan sagu. Sirup glukosa telah banyak digunakan untuk kepentingan komersial, antara lain untuk campuran gula jawa, untuk bahan baku pembuatan etanol, pembuatan selai, campuran minuman ringan (soft drink), dan industri permen.
1.2 Permasalahan
Tingginya harga gula dipasaran menjadikan alasan seseorang untuk mencari alternatif bahan pemanis lain sebagai pengganti gula. Gula dari pati mempunyai rasa dan kemanisan hampir sama dengan gula tebu (sukrosa). Dalam hal ini penulis tertarik untuk memanfaatkan amilum pada biji kweni untuk pembuatan manisan salak, sehingga muncul permasalahan apakah amilum pada biji kweni dapat dijadikan pemanis untuk mensubstitusi gula pasir.
1.3 Pembatasan Masalah
Dalam penelitian ini masalah dibatasi sebagai berikut:
1. Perolehan sampel dibatasi hanya buah mangga yang diperoleh dari penjual buah di Pajak Sore Padang Bulan Medan.
2. Varietas buah mangga yang digunakan adalah kweni. 3. Hidrolisis pati dilakukan dengan menggunakan HCl 3%.
4. Jenis polisakarida yang digunakan adalah amilum dari biji kweni.
5. Penentuan kadar glukosa dengan cara spektrofotometri metode Nelson Somogyi.
1.4 Tujuan Penelitian
1.5 Manfaat Penelitian
Untuk memberikan informasi kepada masyarakat tentang kandungan dari biji mangga yang dapat dijadikan bahan pemanis sebagai pengganti gula pasir.
1.6 Lokasi Penelitian
Penelitian ini dilakukan di Laboratorium Biokimia/KBM (Kimia Bahan Makanan) Fakultas Matematika dan Ilmu Pengetahuan Alam Universitas Sumatera Utara.
1.7 Metodologi Penelitian
BAB 2
TINJAUAN PUSTAKA
2.1. Tanaman Mangga
Mangga (Mangifera indica Linn) merupakan buah yang disukai hampir segala bangsa, karena lezat. Sebagai buah konsumsi, mangga terdiri atas tiga lapisan, yaitu kulit, daging, dan biji.
Komponen daging buah mangga yang paling banyak adalah air dan karbohidrat. Selain itu juga mengandung protein, lemak, macam-macam asam, vitamin, mineral, tanin, zat warna, dan zat yang mudah menguap. Zat menguap itu beraroma harum khas mangga.
Karbohidrat daging buah mangga terdiri dari gula sederhana, tepung, dan selulosa. Gula sederhana yaitu sukrosa, glukosa, dan fruktosa. Gula tersebut memberikan rasa manis dan tenaga yang dapat segera digunakan oleh tubuh. Zat tepung mangga masak lebih sedikit dibandingkan dengan mangga mentah, karena tepung yang ada telah banyak yang berubah menjadi gula. (Pracaya, 2004)
2.1.1. Taksonomi dan Morfologi Tanaman Mangga
Dalam tatanama atau sistematik (taksonomi) tumbuhan, tanaman mangga diklasifikasikan sebagai berikut:
Kingdom : Plantae (tumbuh-tumbuhan) Divisi : Spermatophyta (tumbuhan berbiji) Sub-divisi : Angiospermae (berbiji tertutup) Kelas : Dicotiledonae (biji berkeping dua) Ordo : Anacardiales
Famili : Anacardiaceae (mangga-manggaan) Genus : Mangifera
Spesies : Mangifera indica Linn.
Tanaman mangga memiliki pohon yang tingginya mencapai 10 m – 30 m atau lebih dan umurnya dapat mencapai puluhan tahun. Batangnya tumbuh tegak, kokoh, berkayu dan berkulit agak tabal yang warnanya abu-abu kecoklat-coklatan, pecah-pecah serta mengandung cairan semacam damar. Percabangannya banyak yang tumbuh ke segala arah dan tampak rimbun.
Daun tumbuh tunggal pada ranting., letaknya berselang-seling, dan bertangkai panjang. Bentuk daun panjang-lonjong dengan bagian ujung meruncing. Permukaan daun sebelah atas berwarna hijau tua, sedangkan permukaan sebelah bawah berwarna hijau muda.
Bunga mangga tersusun dalam rangkaian bunga (malai). Tiap malai terdapat bunga dalam jumlah yang sangat banyak, yakni sekitar 1.000 – 6.000 kuntum, namun bunga yang berkembang menjadi buah sangat sedikit ± 1%. ( Rukmana, 1997)
2.1.2. Jenis dan Varieatas Tanaman Mangga
pakel, dan kemang. Masing-masing jenis dan varietas memiliki karakter sebagai berikut.
A. Golek
Disebut golek (Mangifera indica L.) karena setelah menikmati rasanya, orang akan mencari lagi buah mangga yang baru saja dimakan. Rasanya memang enak sekali, manis, dan harum aromnya. Golek (bahasa jawa) artinya mencari. Daging buah tebal, lunak dengan warna kuning tua. Daging buahnya boleh dikatakan tidak berserat, tidak berair (kalau diiris tidak banyak mengeluarkan air). Aromanya cukup harum. Rasanya manis lezat.
B. Arumanis
Disebuta mangga arumanis (Mangifera indica L.) karena rasanya manis dan harum (arum) baunya. Daging buah tebal, lunak berwarna kuning, dan tidak berserat (serat sedikit). Aroma harum, tak begitu berair. Rasanya manis, tapi bagian ujung kadang-kadang masih ada rasa asam.
C. Manalagi
Disebut manalagi (Mangifera indica L.) karena sekali makan orang akan mencarinya lagi. Itu karena lezatnya. Kalau orang hanya makan satu buah saja, pasti akan minta yang lainnya. Rasa mangga manalagi seperti perpaduan rasa antara golek dan arumanis. Mungkin pohon manalagi merupakan hasil persilangan alami antara golek dengan arumanis. Buah yang sudah tua walaupun belum masak rasanya sudah enak dan terasa manis. Buah ini sering dimakan dalam keadaan masi keras, tetapi daging buah sudah kelihatan kuning.
D. Endog
E. Lalijiwo
Disebut lalijiwo (Mangifera indica L.) karena setelah makan buah mangga tersebut dan merasakan enaknya, orang bisa lupa terhadap jiwa atau dirinya sendiri. Lali dalam bahasa jawa berarti lupa. Warna daging buah bila masak kuning tua. Air buah hanya sedikit. Aroma kurang harum. Rasa manis lezat. Buah yang amsih muda tak begitu asam rasanya.
F. Madu
Mangga ini disebut madu (Mangifera indica L.) karena rasanya manis seperti madu lebah. Daging buah yang sudah masak warnanya kuning. Bagian dalam kuningnya makin ke dalam makin tua seperti warna madu. Serat daging buah sedikit. Kadar air buah sedang. Rasanya manis seperti madu. Aromanya harum.
G. Kemang
Kemang (Mangifera caesia Jack). Jenis mangga ini buahnya yang sudah masak berwarnya kuning kecokelatan, berbau seperti terpentin. Rasanya ada yang asam atau asam manis, kadang-kadang sepet. Buah dapat dimakan sebagai rujak atau asinan.
H. Kweni
Kweni (Mangifera odorata Grift). Daging buah berwarn kuning, berair, dan berserat kasar. Aroma khas kweni sangat kuat. Rasanya manis dengan sedikit rasa terpentin.
I. Pakel
Pakel (Mangifera foetida Lour) disebut juga bacang, memiliki daging buah yang berserat kasar. Rasanya asam sedikit manis, sedikit rasa terpentin, bau kerasnya menjadi ciri khas. Dikonsumsi sebagai minuman es buah.
J. Jenis-jenis Mangga Lain
2.1.3. Kandungan Zat Gizi Buah Mangga
Mengkonsumsi buah mangga masak maupun buah muda dapat memenuhi gizi dan memelihara kesehatan tubuh. Kandungan gizi buah mangga dapat dilihat pada Tabel 2.1
Tabel 2.1 Kandungan zat gizi buah mangga
Kandungan Zat Nilai Rata-rata Buah Mangga
Mentah Matang
Air (%)
Vitamin B1 (mg/100 gr) Vitamin B2 (mg/100 gr) Vitamin C (mg/100 gr) Asam nicotinat (mg/100 gr) Nilai kalori per 100 gr
90,00
2.2. Tanaman Salak
Salak termasuk famili Palmae, serumpun dengan kelapa, kelapa sawit, aren, (enau), palem, pakis yang bercabang rendah dan tegak. Batangnya hampir tidak kelihatan karena tertutup pelepah daun yang tersususn rapat dan berduri. Dari batang yang berduri itu tumbuh tunas baru yang dapat menjadi anakan atau tunas bunga buah salak dalam jumlah yang banyak. (Soetomo, 2001)
Gambar 2.2. Buah Salak
2.2.1. Taksonomi Buah Salak
Kingdom : Plantae
Divisi : Magnoliophyta Kelas : Liliopsida
Ordo : Arecales
Famili : Arecaceae
Genus : Salacca
Spesies : S. Edulis reinw
2.2.1. Jenis dan Varietas Tanaman Salak
A. Salak Pondoh
Jenis buah salak ini kecil-kecil. Wujudnya tidak menarik, tetapi memiliki daging buah yang rasanya manis dan enak karena sedikit sekali rasa sepet. Daging buahnya tipis sampai agak tebal dengan warna puith susu. Rasanya manis dan enak sejak buah masih muda sampai pada tingkat menjelang masak. Bila buah sudah masak betul (masir) rasa tersebut akan sedikit berkurang.
B. Salak Madu
Jenis buah salak ini besarnya sedang, dalam waktu lima bulan saja buah sudah masak. Buah yang masak berwarna merah-cokelat. Daging buah yang masak rasanya manis.
C. Salak Nangka
Jenis buah salak ini bulat dan kecil. Kulit buahnya berwarna kehitam-hitaman, aromanya seperti buah nangka. Daging buah juga berwarna kuning nangka dan rasanya manis.
D. Salak Kelapa atau Salak Gondok
Jenis buah salak ini besar-besar dengan warna kulit putih kekuningan. Daging buahnya berwarna putih, namun rasanya masam.
E. Salak Gading
Jenis buahnya kecil-kecil dengan warna kulit kuning gading mengkilat. Daging buahnya berwarna putih kekuningan. Rasanya manis dan enak bila sudah masak. Daun salak gading lebih bersih dan agak kekuningan.
F. Salak Putih
Jenis salak ini kulit buahnya berwarna putih kekuningan. Demikian pula pelepah dan daunnya. Buah yang masih muda berwarna hijau dan rasa dagingnya tidak terlalu manis.
G. Salak Lilipan
buahnya manis dan tidak lekas busuk. Jenis salak ini juga disebut ”salak malam”. (Soetomo, 2001)
2.2.2. Kandungan Gizi Buah Salak
Menurut Soetomo (2001), Buah salak mengandung nilai gizi tinggi bila dibandingkan dengan pisang, nanas, dan pepaya. Dalam setiap 100 gram nilai gizinya terdiri dari: Tabel 2.2 Kandungan zat gizi buah salak
Kandungan Zat Nilai Rata-rata Buah Salak Kalori
Berat bahan yang dapat dimakan
77 kal
Sumber : Soetmo, Moch. 2001. Teknik Bertanam Salak.
2.3 Gula Alternatif
produksi dalam negeri menjadi sulit dipasarkan tanpa kebijakan yang mampu melindunginya dari serbuan gula impor.
Pemerintah sebenarnya terus berupaya memihak para petani tebu dengan mengeluarkan kebijakan yang dikenal Surat Keputusan (SK) 643. SK ini mengatur harga minimal pembelian gula petani. Harga pembelian ditingkat petani oleh pabrik gula adalah Rp3.410/kg, sedangkan harga gula di pasaran diusahakan berkisar Rp4.000 – Rp4.500/kg. Namun dengan adanya kenaikan harga BBM, Dewan Gula Nasional mengusulkan harga dasar gula sebesar Rp4.000/kg. Hal ini akan memancing keresahan konsumen karena dengan harga dasar gula Rp3.410/kg yang saat ini berlaku, harga gula dipasaran dapat mencapai Rp6.000/kg atau hampir dua kali lipat harga dasar, walaupun kenaikan harga tersebut lebih disebabkan oleh kekurangan stok gula internasional. Untuk mengurangi impor gula maka produksi gula dalam negeri perlu terus dipacu, disamping mencari alternatif bahan pemanis lain sebagai substitusi gula.
Gula alternatif sekarang yang sudah digunakan antara lain adalah gula siklamat dan stearin yang merupakan gula sintetis, serta gula dari pati seperti sirup gluko sa, fruktosa, maltosa, manitol, sorbitol, dan xilitol. Gula dari pati mempunyai rasa dan kemanisan hampir sama dengan gula tebu (sukrosa), bahkan ada yang lebih manis. Gula tersebut dibuat dari bahan berpati seperti ubi kayu, ubi jalar, sagu, dan pati jagung. Semua bahan tersebut melimpah di Indonesia. Di antara gula dari pati tersebut, sirup glukosa dan fruktosa mempunyai prospek paling baik untuk mensubstitusi gula pasir. September 2009)
2.4 Sirup Glukosa
dengan cara hidrolisis asam atau dengan cara enzimatis. Dari kedua cara tersebut, pembuatan sirup glukosa secara enzimatis dapat dikembangkan di pedesaan karena tidak banyak menggunakan bahan kimia sehingga aman dan tidak mencemari lingkungan. Bahan lain yang diperlukan adalah enzim amilase.
Sirup glukosa pertama kali digunakan sebagai pengganti gula pada masa Napoleon. Sirup glukosa dibuat dengan mereaksikan pati dengan asam dengan menghidrolisis karbohidrat terlebih dahulu untuk memecah gula atau oligosakarida kemudian untuk menggandakan gula maltosa (atau gula gandum) dan hasil akhirnya berupa monosakarida yaitu glukosa. Sirup glukosa dikenal juga dengan nama glukosa konfeksioner atau gula cair.
Sirup glukosa merupakan suatu larutan yang diperoleh dari proses hidrolisis dengan bantuan katalis. Sirup glukosa adalah salah satu produk bahan pemanis makanan dan minuman yang berbentuk cairan, tidak berbau dan tidak berwarna tetapi memiliki rasa manis yang tinggi. Sirup glukosa atau gula cair mengandung D-glukosa, maltosa, dan polimer D-glukosa melalui proses hidrolisis. (Cakebread, 1975)
Bahan baku yang dapat digunakan untuk pembuatan sirup glukosa adalah tapioka, pati umbi-umbian, sagu, jagung, dan serat. Sirup glukosa dapat dibuat dengan cara hidrolisis asam ataupun secara enzimatis.
Industri makanan dan minuman memiliki kecenderungan untuk menggunakan sirup glukosa. Hal ini didasari oleh beberapa kelebihan sirup glukosa dibandingkan sukrosa, diantaranya sirup glukosa tidak mengkristal seperti halnya sukrosa jika dilakukan pemanasan pada suhu tinggi.
disenangi karena dapat mencegah kerusakan oleh mikrobiologis dan memperbaik tekstur. (Dziedzic and Kearsley, 1984)
2.5 Amilum
Polisakarida ini banyak terdapat di alam, yaitu pada sebagian besar tumbuhan. Amilum atau dalam bahasa sehari-hari disebut pati terdapat pada umbi, daun, batang, dan biji-bijian.
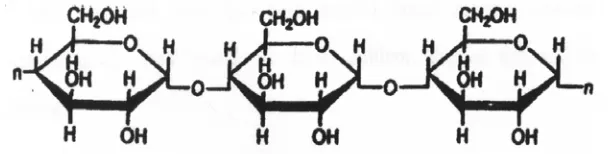
Amilum terdiri atas dua macam polisakarida yang kedua-duanya adalah polimer dari glukosa, yaitu amilosa (kira-kira 20-28%) dan sisanya amilopektin. Amilosa terdiri dari 250-300 unit D-glukosa yang terikat dengan ikatan α 1,4-glikosidik, jadi molekulnya merupakan rantai terbuka.
Gambar 2.3. Struktur Molekul Amilosa
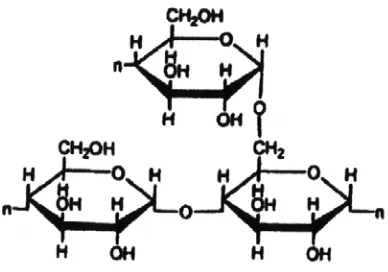
Gambar 2.4. Struktur Molekul Amilopektin
Pati merupakan homopolimer glukosa dengan ikatan α-glikosidik. Berbagai macam pati tidak sama sifatnya, tergantung dari panjang rantai C-nya, serta apakah lurus atau bercabang rantai molekulnya. Pati terdiri dari dua fraksi yang dapat dipisahkan dengan air panas. Fraksi terlarut disebut amilosa dan fraksi tidak terlarut disebut amilopektin. Amilosa mempunyai struktur lurus dengan ikatan α -(1,4)-D-glukosa, sedangkan amilopektin mempunyai cabang dengan ikatan α-(1,4)-D-glukosa sebanyak 4-5% dari berat total. (Winarno, 1997)
Pati tidak dapat larut dalam air jadi dapat dimanfaatkan sebagai depot penyimpanan gluoksa. Tumbuhan yang kelebihan glukosa merubahnya menjadi pati sebagai simpanan. Padi, gandum, dan jagung merupakan sumber utama pati untuk makanan manusia. (Kimball, 1983)
Pati Merupakan sumber kalori yang sangat penting karena sebagian besar karbohidrat dalam dalam makanan terdapat dalam bentuk pati. Amilosa adalah jenis pati berantai lurus tersusun atas 250-350 unit glukosa. Sementara itu, pati berantai cabang yang tersusun atas 20-30 unit glukosa setiap cabangnya disebut amilopektin. (Irianto, 2006)
dengan air. Peristiwa ini disebut dengan proses gelatinasi yang berakibat karbohidrat menjadi lebih mudah dicerna. Pati yang telah mengalami gelatinasi dapat dikeringkan. Bahan yang telah kering tersebut masih dapat menyerap air sehingga sifat ini dimanfaatkan dalam pembuatan produk makanan instan. (Auliana, 1999)
Amilum (zat tepung) adalah homopolimer dari monosakarida tang tersusun dari unsur karbon, hidrogen, dan oksigen dengan rumus kimia (C6H10O5)n dan terdiri
dari dua komponen yaitu sekitar 20% amilosa dan 80% amilopektin. (Fessenden, R. J., Fessenden, J. S., 1999)
2.5.1 Hidrolisis Amilum
Pati atau amilum dapat dihidrolisa dengan cara yang sangat sederhana. Mula-mula pati diekstraksi dan didispersikan menjadi suatu larutan koloidal hingga terpisah dari zat lainnya. Pati yang terdapat dalam dispersi tersebut dapat ditentukan dengan jalan pengendapan dan dilakukan penimbangan. Pati bersifat tidak larut dalam air sehingga mudah dipisahkan dari zat lainnya. (Sudarmadji et al, 1989)
Hidrolisis pati dapat dilakukan oleh asam atau enzim. Jika pati dipanaskan dengan asam akan terurai menjadi molekul-molekul yang lebih kecil secara berurutan, dan hasil akhirnya adalah glukosa.
(C6H10O5)n + nH2O nC6H12O6
Sirup glukosa komersil dihasilkan dengan jalan menghidrolisis pati jagung dengan asam klorida encer. Hidrolisisnya tidak sempurna dan sirup glukosa yang juga dinamakan sirup jagung atau glukosa cair, merupakan campuran glukosa, maltosa, dextrin, dan air. (Gamman, 1992)
panas. Fraksi terlarut disebut amilosa (± 20%), dengan struktur makromolekul linier dengan iodium memberikan warna biru. Sebaliknya, fraksi yang tidak larut disebut amilopektin (± 80%) dengan struktur bercabang. Dengan penambahan iodium, fraksi memberikan warna ungu sampai merah.
Pati dalam suasana asam bila dipanaskan akan terhidrolisis menjadi senyawa-senyawa yang lebih sederhana. Hasil hidrolisis dapat di uji dengan iodium dan menghasilkan warna biru sampai tidak berwarna. Hasil akhir hidrolisis ditegaskan dengan uji Benedict. (Yazid, Nursanti, 2006)
2.6. Metode Analisa Kuantitatif Glukosa
2.6.1. Metode Nelson-Somogyi
Metode ini dapat digunakan untuk mengukur kadar gula reduksi dengan menggunakan pereaksi tembaga-arseno-molibdat. Kupri mula-mula direduksi menjadi bentuk kupro dengan pemansana larutan gula. Kupro yang terbentuk berupa endapan selanjutnya dilarutkan dengan arseno-molibdat menjadi molibdenum berwarna biru yang menunjukkan ukuran konsentrasi gula. Dengan membandingkannya terhadap larutan standar, konsentrasi gula dalam sampel dapat ditentukan. Reaksi Warna yang terbentuk dapat menentukan konsentrasi gula dalam sampel dengan mengukur absorbansi. (Sudarmadji et al, 1984)
2..6.2. Lane-Eynon
keadaan panas menjadi berwarna putih karena kelebihan gula pereduksi diatas jumlah yang dibutuhkan untuk mereduksi semua tembaga.
2.6.3. Metode Shaffer-Somogyi
Metode ini dapat diterapkan untuk segala jenis bahan pangan. Terutama berguna untuk menetapkan sampel yang mengandung sedikit gula pereduksi. Gula reduksi akan mereduksi Cu2+ menjadi Cu+. Cu+ akan dioksidasi oleh I2 (yang terbentuk dari
hasil oksidasi KI oleh KIO3 dalam asam) menjadi Cu2+ kembali. Kelebihan I2 dititrasi
dengan Na2S2O3. Dengan menggunakan blanko, maka kadar gula reduksi dalam
sampel dapat ditentukan.
2.6.4. Metode Anthrone
Metode ini dapat diterapkan untuk semua jenis bahan makanan. Anthrone (9,10-dihydro-9-oxanthracene), merupakan hasil reduksi anthraquinone. Anthrone bereaksi secara spesifik dengan karbohidrat dalam asam sulfat pekat menghasilkan warna biru kehijauan yang khas.
2.6.5. Metode Munson-Walker
Penentuan gula reduksi berdasarkan atas banyaknya endapan Cu2O yang terbentuk,
kemudian dengan melihat tabel Hadmond dapat diketahui jumlah gula pereduksinya. Jumlah Cu2O ditentukan secara gravimetris, yaitu dengan menimbang langsung
endapan Cu2O yang terbentuk. Dan juga ditentukan secara volumetris yaitu dengan
2.7. Metode Analisa Kualitatif Amilum
Reaksi dengan Iodin
Pati yang berikatan dengan iodin (I2) akan menghasilkan warna biru. Sifat ini dapat
digunakan untuk menganalisis adanya pati. Hal ini disebabkan oleh struktur molekul pati yang berbentuk spiral, sehingga akan mengikat molekul iodin dan terbentuklah warna biru. Bila pati dipanaskan, spiral akan merenggang, molekul-molekul iodin terlepas sehingga warna biru akan hilang. (Winarno, 1997)
2.6 Manisan
Manisan adalah salah satu bentuk makanan olahan yang banyak disukai oleh masyarakat. Rasanya yang mains bercampur rasa khas buah sangat cocok untuk dinikmati diberbagai kesempatan. Meskipun jenis manisan buah yang umum dipasarkan ada bermacam-macam bentuk dan rasanya, namun sebenarnya dapat dikelompokkan menajdi 4 golongan yaitu:
1. golongan pertama adalah manisan basah dengan larutan gula encer ( buah dilarutkan dalam gula seperti jambu, mangga, salak, dan kedondong).
2. Golongan kedua adalah manisan gula kental menempel pada buah. Manisan jenis ini adalah pala, lobi-lobi, dan cermai.
3. Golongan ketiga adalah manisan kering dengan gula utuh (sebagian gula tidak larut dan menempel pada buah). Buah yang sering digunakan adalah buah mangga, kedondong, sirsak, dan pala.
2.6.1. Faktor Penentu Kualitas Manisan
Kualitas Produk olahan buah berupa manisan, baik manisan basah maupun manisan kering, sangat menetukan laku tidaknya produk olahan tersebut. Beberapa faktor yang mempengaruhi kualitas manisan adalah sebagai berikut:
A. Penampilan
Penampilan merupakan penentu utama kualitas suatu produk. Penampilan yang menarik menyebabkan konsumen tertarik untuk membelinya. Penampilan suatu produk olahan ditentukan oleh faktor sebagai berikut:
1. Warna
2. Keseragaman bentuk dan ukuran 3. Kemasan
B. Cita Rasa dan Aroma
Cita rasa manisan harus berasal dari cita rasa buah aslinya. Namun, agar cita rasa makin memikat dapat ditambahkan bahan pewangi atau bumbu yang sesuai, seperti kayu Manis, bunga pala, pandan wangi, atau cengkih. Sementara itu, aroma merupakan unsur yang Sangay peka terhadap pemanasan. Karenanya sulit dipertahankan. Namur, cita rasa yang kompak dapat menutupi kekurangan dan unsur aroma ini.
C. Daya Tahan
D. Kandunagn Unsur Gizi dan Kalori
Buah memiliki kandungan gizi, mineral, dan kalori. Beberapa kandungan gizi biasanya akan hilang karena proses pengolahan. Karena itu, proses pengolahan harus memperhatikan teknik atau tata caranya sehingga kandungan gizi dalam buah bisa diselamatkan. Untuk menjaga kualitas manisan tetap baik, biasanya dilakukan penambahan vitamin C ke dalam manisan.
E. Higienis
BAB 3
METODE PENELITIAN
3.1. Alat dan Bahan
3.1.2. Alat-alat
- Neraca Analitik Mettler Toledo - Indikator Universal Merck
- Spektrofotometer Genesys 20
- Inkubator Fisher
- Alat Soklet Pyrex
- Labu takar Pyrex
- Gelas ukur Pyrex
- Gelas beaker Pyrex
- Gelas erlenmeyer Pyrex
- Tabung reaksi Pyrex
- Rak tabung reaksi Pyrex
- Corong Pyrex
- Penangas air Fisons
- Termometer Fisher
3.1.2. Bahan-bahan
- C6H12O6 E. Merck
- Na2CO3 E. Merck
- KNaC4H4O6.4H2O E. Merck
- NaHCO3 E.Merck
- Na2SO4 E. Merck
- CuSO4.5H2O E. Merck
- H2SO4(p) E. Merck
- (NH4)6Mo7O24.4H2O E. Merck
- Na2HAsO4.7H2O E. Merck
- HCl 3% E. Merck
- N-Heksana E. Merck
3.2. Pembuatan Reagen
3.2.1. Larutan Glukosa 20 mg/100 ml
Sebanyak 20 mg glukosa anhidrat dilarutkan dengan akuades dalam labu takar 100 ml sampai garis tanda dan dikocok sampai homogen.
3.2.2. Larutan Pereaksi Nelson
1. Nelson A
Sebanyak 12,5001 g Natrium Karbonat anhidrat, 12,5001 g garam Rochelle (K-Na-Tartrat), 10 g Natrium Bikarbonat, dan 100 g Natrium Sulfat anhidrat dilarutkan dalam 300 ml akuades dan diencerkan sampai 500 ml.
2. Nelson B
Sebanyak 7,5002 g CuSO4.5H2O dilarutkan dalam 50 ml akuades dan
ditambahkan 1 tetes asam sulfat pekat. Pereaksi Nelson dibuat dengan cara mencampur 25 bagian Nelson A dan 1 bagian Nelson B. Pencampuran dilakukan setiap kali digunakan.
3.2.3. Larutan Arsenomolibdat
Sebanyak 25 g Ammonium Molibdat dilarutkan dalam 450 ml akuades dan ditambahkan 25 ml H2SO4. Dilarutkan pada tempat yang lain 3 g
Na2HAsO4.7H2O dalam 25 ml akuades kemudian dituangkan larutan ini
kedalam larutan yang pertama. Disimpan dalam botol berwarna cokelat dan diinkubasi pada suhu 37oC selama 24 jam. Larutan pereaksi ini dapat digunakan setelah masa inkubasi dan berwarna kuning.
3.2.4. Pembuatan Pereaksi Benedict
Dengan bantuan pemanasan, dilarutkan 173 g Na-sitrat dan 100 g Na2CO3
bila perlu). Bila larutan diatas sudah dingin maka perlahan-lahan ditambahkan kedalam larutan I, kemudian diencerkan dengan akuades sampai 1 liter.
3.2.5. Pembuatan Larutan Na2CO3 10%
Sebanyak 100 g NaOH dilarutkan dengan akuades dalam labu takar 1000 ml sampai garis tanda lalu dikocok hingga homogen.
3.2.6. Pembuatan Larutan HCl 3%
3.3. Cara Kerja
3.3.1. Pengambilan Sampel
Sampel berupa biji kweni dan buah salak diperoleh dari 1 lokasi yaitu Pajak Sore Padang Bulan Medan.
3.3.2. Isolasi Amilum dari Biji Mangga
Sebanyak 500 g biji mangga ditimbang dan dihaluskan. Ditambahkan 200 ml akuades sambil diaduk kemudian disaring. Filtrat yang diperoleh kemudian diendapkan selama 24 jam hingga terbentuk pati. Pati yang diperoleh kemudian di ekstraksi dengan alat soklet selama 2 jam pada suhu 225oC. Pati yang telah di ekstraksi kemudian dikeringkan dibawah sinar matahari selama 2 hari. Lalu ditimbang berat pati kering.
3.3.3. Hidrolisis Amilum Biji Mangga serta Uji Gula Reduksi
Sebanyak 0,5002 mg amilum biji mangga yang diperoleh dari isolasi diatas, dimasukkan kedalam labu erlenmeyer kemudian ditambahkan 5 ml akuades lalu dipanaskan pada suhu 72–92 oC. Lalu ditambahkan 10 ml HCl 3% dan dihidrolisis di penangas air selama 2 jam lalu didinginkan. Ditambah NaOH 3% hingga pH 5,0 – 6,0 lalu disaring. Sebanyak 1 ml filtrat dimasukkan kedalam tabung reaksi kemudian ditambahkan 5 ml larutan Benedict dan dipanaskan sampai terbentuk endapan merah bata.
3.3.4. Pengukuran Panjang Gelombang Maksimum Larutan Glukosa Standar
sampai mendidih selama 30 menit lalu didinginkan. Lalu ditambahkan 1 ml larutan Arsenomolibdat lalu dikocok hingga semua endapan larut. Ditambahkan 7 ml akuades lalu dikocok hingga homogen. Diukur serapan panjang gelombang pada 705–725 nm (diperoleh panjang gelombang maksimum).
3.3.5. Penyiapan Kurva Standar Glukosa
Disiapkan larutan glukosa standar dalam beberapa tabung reaksi dengan konsentrasi bertingkat dari 0,02 – 0,20 mg/ml. Ditambahkan 1 ml larutan Nelson kemudian dipanaskan hingga mendidih selama 30 menit dan didinginkan. Ditambahkan 1 ml larutan arsenomolibdat lalu dikocok. Ditambahkan 7 ml akuades lalu dikocok hingga homogen. Diukur serapannya pada panjang gelombang 714 nm. Dibuat kurva standar yang menunjukkan hubungan antara konsentrasi gula standar dan absorbansi.
3.3.6. Analisa Kandungan Glukosa Hasil Hidrolisis Sampel
Diencerkan filtrat hasil hidrolisis pati biji mangga dalam labu takar 250 ml. Kemudian diambil 1 ml dan dimasukkan kedalam tabung reaksi. Ditambahkan 1 ml larutan Nelson kemudian dipanaskan hingga mendidih selama 30 menit dan didinginkan. Ditambahkan 1 ml larutan Arsenomolibdat lalu dikocok. Ditambahkan 7 ml akuades lalu dikocok hingga homogen. Diukur serapanya pada panjang gelombang 714 nm sehingga dapat dihitung kadar gula reduksinya.
3.3.7. Pembuatan Manisan
3.3.8. Uji Organoleptik
Penentuan organoleptik dilakukan dengan menggunakan uji hedonik (uji kesukaan) untuk mengetahui mana yang lebih disukai panelis terhadap rasa, aroma, warna, dan tekstur dari manisan salak. Pengujian dilakukan oleh panelis sebanyak 15 orang. Panelis diberi formulir penilaian organoleptik dengan skala 1 – 5 menurut Elizabeth Larmond, 1977 dengan kriteria:
3.3. Bagan Penelitian
3.3.1. Isolasi Amilum dari Biji Mangga
600 g biji mangga
Dihaluskan
Ditimbang sebanyak 500 g Ditambah 200 ml akuades Disaring
filtrat
Residu
Residu Diendapkan hingga terbentuk pati
Diekstraksi dengan alat soklet selama 2 jam
Filtrat
Ditimbang
Dikeringkan dibawah sinar matahari selama 2 hari Ditimbang
3.3.2. Hidrolisis Amilum serta Uji gula Reduksinya
0,5001 g amilum
Ditambahkan 5 ml akuades sambil diaduk Dipanaskan di penangas air pada suhu 72-90oC Campuran sampel dan air
Ditambah 10 ml HCl 3% Ditutup dengan aluminium foil
Dihidrolisis di penangas air mendidih selama 2 jam Sampel terhidrolisis
Dinetralkan gengan NaOH 3% Disaring
Dipipet 1 ml filtrat kedalam tabung reaksi
Dipanaskan dipenangas air
Residu filtrat
Ditambahkan 5 ml larutan Benedict secara kualitatif
3.3.3. Analisa Kandungan Glukosa Hasil Hidrolisis Amilum Biji Mangga
filtrat hasil hasil hidrolisis amilum biji mangga
Dimasukkan kedalam labu takar 250 ml
Diencerkan dengan akuades sampai garis tanda Dipipet sebanyak 1 ml
1 ml larutan glukosa sampel
Dimasukkan kedalam tabung reaksi Ditambahkan 1 ml pereaksi Nelson Ditutup dengan kapas
Dipanaskan dipenangas air pada suhu 100oC selama 30 menit
Didinginkan dibawah air yang mengalir Larutan dengan endapan merah bata
Diaduk hingga homogen
Ditambahkan 1 ml larutan arsenomolibdat Diaduk hingga endapan larut
Larutan berwarna biru
Ditambahkan 7 ml akuades Diaduk hingga homogen
Diukur absorbansinya pada panjang gelombang 714 nm
3.3.4. Pembuatan Manisan
3.3.5. Uji Organoleptik Buah Salak
Dilakukan sortasi Dikupas kulitnya Dicuci hingga bersih Dirajang
Hasil
Direndam dalam larutan kapur 10% Direndam dalam larutan kapur 10%
Ditiriskan dan dicuci dengan air yang menglir Direndam dalam larutan gula
Penelis dan Manisan Salak
Dilakukan uji kesukaan terhadap warna, cita rasa, aroma, dan tekstur
BAB 4
HASIL DAN PEMBAHASAN
4.1. Hasil Penelitian
4.1.1. Perhitungan kadar amilum biji kweni
Perhitungan kadar amilum biji kweni dapat dihitung dengan rumus sebagai berikut:
%
Dari data perhitungan kadar amilum diperoleh V = kadar amilum
V1 = 6,71 %
V2 = 6,68 %
V3 = 6,41 %
(Hasil pengukuran kadar amilum selengkapnya terdapat pada tabel 4.1)
4.1.2. Pengolahan Data Pengukuran absorbansi Glukosa Hasil Hidrolisis Amilum
Biji Kweni
Pengolahan data pengukuran absorbansi glukosa hasil hidrolisis amilum biji kweni dilakukan secara statistik dengan metode Chauvenet Criterion Test (CCT) yang diambil dari data absorbansi pada tabel 4.3.
Untuk melakukan metode Chauvenet Criterion Test (CCT) perlu harga ht dan hh dapat
dihitung dengan menggunakan rumus:
Untuk A1′ = 0,0044
Sedangkan hhitung adalah
0927
Karena 225,1363 > 103,0927 ( ht > hh ), maka data signifikan dan dapat diterima, data
pengukuran kedua dan ketiga juga signifikan.
4.1.3. Perhitungan Kadar Glukosa Hasil Hidrolisis Amilum Biji Kweni
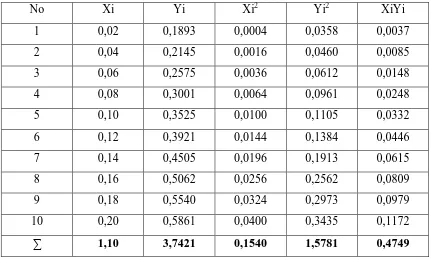
Untuk Menghitung kadar glukosa hasil hidrolisis amilum biji kweni terlebih dahulu harus dicari persamaan garis regresi larutan glukosa standar dari berbagai konsentrasi.
Tabel 4.1. Larutan Glukosa Standar Pada Berbagai Konsentrasi
( )
(
)
Maka persamaan garis regresinya adalah Y = aX + b
Dimana: a = slope b = intersep
Y = 0,1633X + 2,0536
Dimana X = Kadar glukosa (mg/ml)
Y = Absorbansi dari pengukuran serapan glukosa
Setelah diperoleh harga X kemudian disubstitusikan kedalam rumus:
%
Dimana: X = konsentrasi glukosa dari perhitungan regresi V = Volume labu takar (ml)
Contoh:
Absorbansi suatu pengukuran adalah 3,977 dengan volumne labu takar 250 ml dan berat sampel kering 0,5000 g (500 mg), maka:
0,9625 = 0,1633X + 2,0536
Hasil pengukuran kadar gula reduksi hasil hidrolisis amilum biji kweni selengkapnya terdapat pda tabel 4.3.
1705
Sedangkan hhitung adalah :
1476
4.2. Pembahasan
Hidrolisis amilum dapat dilakukan dengan menggunakan asam atau enzim. Jika amilum dipanaskan dengan asam maka akan terurai menjadi molekul-molekul yang lebih kecil dengan tahapan yang berbeda tetapi hasil akhirnya sama yaitu glukosa.
Dari hasil hidrolisis amilum biji kweni dengan menggunakan HCl 3% maka dihasilkan sirup glukosa. Setelah diidentifikasi secara kualitatif dengan reagen Benedict menunjukkan hasil positif bahwa amilum dari biji kweni mengandung glukosa dengan terbentuknya endapan merah bata. Selanjutnya ditentukan kandungan glukosa dengan metode Nelson Somogyi menggunakan alat spektrofotometer pada panjang gelombang 714 nm.
Dari penelitian ini diperoleh kadar amilum sebesar 6,6% untuk 500 gr origin. Kadar glukosa hasil hidrolisis amilum sebesar 19,34%. Hal tersebut menunjukkan bahwa amilum dari biji kweni dapat menjadi salah satu alternatif yang dapat dimanfaatkan menjadi sirup glukosa.
Dari penelitian ini dapat diketahui bahwa sirup glukosa dari amilum biji kweni dapat dijadikan pemanis untuk membuat manisan dari buah salak. Pemanis yang digunakan sebagai pembanding adalah gula pasir dengan perbandingan 1 : 0, 1 : 1, 1 : : 2, dan 1 : 3.
BAB 5
KESIMPULAN DAN SARAN
5.1. Kesimpulan
Dari hasil penelitian dapat disimpulkan bahwa amilum yang terdapat dalam biji kweni dapat dimanfaatkan menjadi sirup glukosa. Kadar glukosa yang diperoleh dari hasil hidrolisis amilum untuk sirup glukosa tersebut adalah 19,34%. Manisan buah salak dengan menggunakan gula pasir lebih disukai panelis dari pada manisan dengan sirup glukosa hasil hidrolisa amailum biji kweni.
5.2. Saran
DAFTAR PUSTAKA
Abdul Fatah, Memet. Bachtiar, Yusuf. 2004. Membuat Aneka Manisan Buah. Jakarta: Agromedia Pustaka.
Apriyanto, A. 1989. Analisis Pangan. Departemen Pendidikan dan Kebudayaan. Jakarta: Institut Pertanian Bogor.
Auliana, Rizqie. 1999. Gizi & Pengolahan Pangan. Yogyakarta: Adicita Karya Nusa. Cakebread, S.H. 1975. Sugar and Chocolate Confectionary. London: Oxford
University Press.
Dziedzic, S. Z. Kearsley, M. W. Glucose Syrups: Science and Technology, England: Elsevier Applied Science Publishers Ltd.
Ermaiza. 2009. Pengaruh Dua Jenis Polisakarida dalam Biji Alpukat (Persea americana mill) Terhadap Kandungan Sirup Glukosa Melalui Proses
Hidrolisis dengan HCl 3%. Skrpsi S1. Jurusan Kimia. Medan: FMIPA USU. Fessenden, R. J., Fessenden, J. S. 1999. Kimia Organik. Edisi Ketiga. Jilid Kedua.
Jakarta: Erlangga.
Gamman, P. M. Sherrington, K. B. 1992. Ilmu Pangan, Pengantar Ilmu
Pangan,Nutrisi dan Mikrobiologi. Edisi Kedua. Yogyakarta: Gadjah Mada University Press.
Irianto, Djoko Pekik, 2006. Panduan Gizi Lengkap Keluarga dan Olahragawan. Yogyakarta: Andi.
Kimball, J. W. 1983.Biologi. Edisi Kelima. Jilid I. Jakarta: PT. Gelora Aksara Pratama.
Larmond, E. 1987. Laboratory Methods For Sensory Evaluation of Food. Canada: Departement of Agriculture
Pracaya. 2004. Bertanam Mangga. Edisi Revisi. Jakarta: Penebar Swadaya. Redaksi Trubus. 2003. Mengebunkan Durian Unggul. Jakarta: Penebar Swadaya. Rukmana, Rahmat. 1997. Mangga: Budidaya dan Pasca Panen. Yogyakarta:
Kanisius.
Santoso, H.B. 1990. Salak Pondoh. Cetakan Pertama. Yogyakarta: Kanisuis. Sianipar, Anthony. 1996. Pengaruh Berbagai Konsentrasi Gula Terhadap Sifat
Organoleptik Manisan Kedondong. Pendidikan Ahli Madya Gizi. Departemen Kesehatan R. I.
Soetomo, Moch. 2001. Teknik Bertanam Salak. Bandung: Sinar Baru Algesindo. S. P. W., Harlinah. 2003. Pemanfaatan Sampah Ampas Kelapa Menjadi Sirup
Glukosa Secara Hidrolisis Oleh HCl. Yogyakarta: Pusat Studi Bioteknologi Universitas Gadjah mada.
Sudarmadji, S. 1984. Prosedur Analisa Untuk Bahan Makanan dan Pertanian. Edisi Ketiga. Yogyakarta: Liberty.
Sudarmadji, S., Haryono, B., Suhadi. 1989. Analisa Bahan Makanan dan Pertanian. Edisi I. Cetakan Pertama. Yogyakarta: Liberty.
Wijayanti, L. 2005. Pengaruh Temperatur dan Durasi Inkubasi Terhadap Kadar Alkohol dari Fermentasi Glukosa Hasil Hidrolisa Rumpu Gajah (Pennisetum purpureum) dengan HCl 3% Menggunakan Saccharomyces cerevisiae. Skripsi S1. Jurusan Kimia. Medan: FMIPA USU.
Winarno, F. G. 1997. Kimia Pangan dan Gizi. Yogyakarta: PT. Gramedia Pustaka Utama.
Yazid, E., Nursanti, L. 2006. Penuntun Praktikum Biokimia untuk Mahasiswa Analis. Yogyakarta: Penerbit Andi.
DAFTAR TABEL
Tabel 1. Data Hasil Perhitungan Kadar Amilum Biji Kweni
Perulangan Berat Amilum ( gr )
Kadar Amilum ( % )
Rata-rata
I 33,5788 6,71
19,34 %
II 33,4272 6,68
II 32,0729 6,41
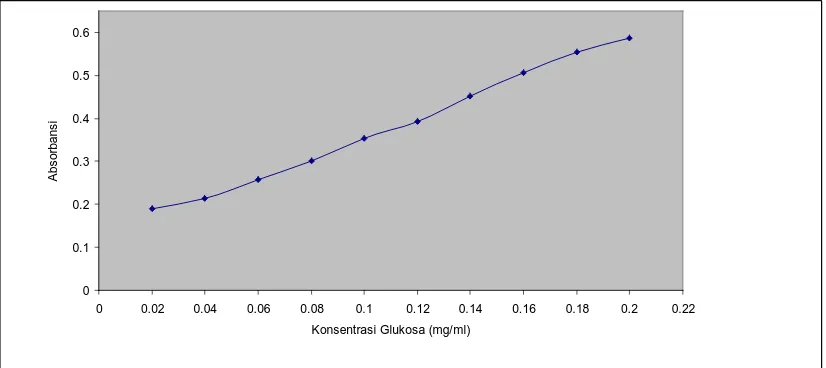
Tabel 2. Data Absorbansi Larutan Glukosa Standar Pada Berbagai Konsentrasi
pada λ Maksimum 714 nm
Konsentrasi ( mg/ml ) Absorbansi
0,02 0,1893
0,04 0,2145
0,06 0,2575
0,08 0,3001
0,10 0,3525
0,12 0,3921
0,14 0,4505
0,16 0,5062
0,18 0,5540
0,20 0,5861
Tabel 3. Data Hasil Perhitungan Kadar Gula Reduksi Berdasarkan Absorbansi
Glukosa Hasil Hidrolisis Amilum Biji Kweni
No Absorbansi Kadar Gula Reduksi
( % )
Ratrata
1 0,9625 19,45
19,34 %
2 0,9501 19,15
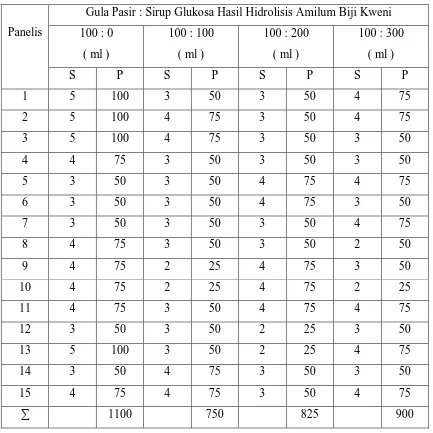
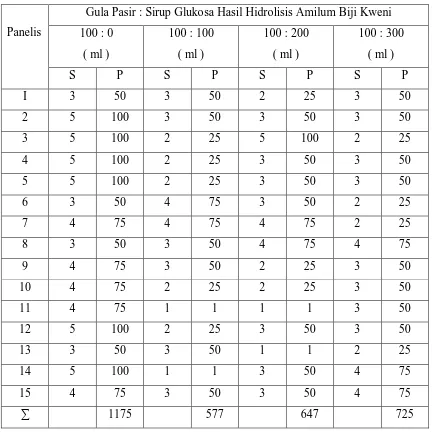
Tabel 5. Data Hasil Pengukuran Organoletik Terhadap Warna Manisan Salak
Panelis
Gula Pasir : Sirup Glukosa Hasil Hidrolisis Amilum Biji Kweni 100 : 0
( ml )
100 : 100 ( ml )
100 : 200 ( ml )
100 : 300 ( ml )
S P S P S P S P
1 5 100 3 50 3 50 4 75
2 5 100 4 75 3 50 4 75
3 5 100 4 75 3 50 3 50
4 4 75 3 50 3 50 3 50
5 3 50 3 50 4 75 4 75
6 3 50 3 50 4 75 3 50
7 3 50 3 50 3 50 4 75
8 4 75 3 50 3 50 2 50
9 4 75 2 25 4 75 3 50
10 4 75 2 25 4 75 2 25
11 4 75 3 50 4 75 4 75
12 3 50 3 50 2 25 3 50
13 5 100 3 50 2 25 4 75
14 3 50 4 75 3 50 3 50
15 4 75 4 75 3 50 4 75
Tabel 6. Data Hasil Pengukuran Organolerptik Terhadap Rasa Manisan Salak
Panelis
Gula Pasir : Sirup Glukosa Hasil Hidrolisis Amilum Biji Kweni 100 : 0
( ml )
100 : 100 ( ml )
100 : 200 ( ml )
100 : 300 ( ml )
S P S P S P S P
I 3 50 3 50 2 25 3 50
2 5 100 3 50 3 50 3 50
3 5 100 2 25 5 100 2 25
4 5 100 2 25 3 50 3 50
5 5 100 2 25 3 50 3 50
6 3 50 4 75 3 50 2 25
7 4 75 4 75 4 75 2 25
8 3 50 3 50 4 75 4 75
9 4 75 3 50 2 25 3 50
10 4 75 2 25 2 25 3 50
11 4 75 1 1 1 1 3 50
12 5 100 2 25 3 50 3 50
13 3 50 3 50 1 1 2 25
14 5 100 1 1 3 50 4 75
15 4 75 3 50 3 50 4 75
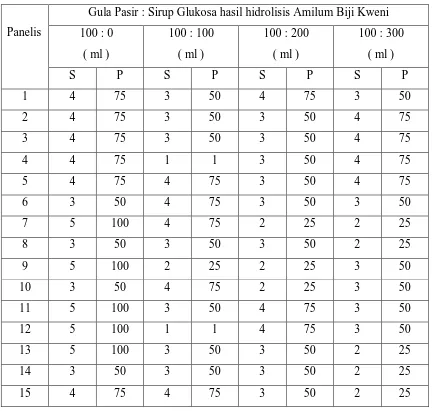
Tabel 7. Data Hasil Pengukuran Organoleptik Terhadap Aroma Manisan Salak
Panelis
Gula Pasir : Sirup Glukosa hasil hidrolisis Amilum Biji Kweni 100 : 0
( ml )
100 : 100 ( ml )
100 : 200 ( ml )
100 : 300 ( ml )
S P S P S P S P
1 4 75 3 50 4 75 3 50
2 4 75 3 50 3 50 4 75
3 4 75 3 50 3 50 4 75
4 4 75 1 1 3 50 4 75
5 4 75 4 75 3 50 4 75
6 3 50 4 75 3 50 3 50
7 5 100 4 75 2 25 2 25
8 3 50 3 50 3 50 2 25
9 5 100 2 25 2 25 3 50
10 3 50 4 75 2 25 3 50
11 5 100 3 50 4 75 3 50
12 5 100 1 1 4 75 3 50
13 5 100 3 50 3 50 2 25
14 3 50 3 50 3 50 2 25
Kurva Absorbansi Larutan Glukosa Standar pada Berbagai Konsentrasi pada λ maksimum 714 nm
0 0.1 0.2 0.3 0.4 0.5 0.6
0 0.02 0.04 0.06 0.08 0.1 0.12 0.14 0.16 0.18 0.2 0.22
Konsentrasi Glukosa (mg/ml)
A
bs
or
bans
i