Hev
vea bras
PA
SE
INST
siliensis
AKAN B
Cyprin
CER
EKOLAH
TITUT P
SEBAG
BENIH I
nus carp
RRIA IN
H PASCA
PERTAN
BOGOR
2011
GAI BAH
IKAN M
pio
Linn
NARA
ASARJA
NIAN BO
R
HAN BA
MAS
n
ANA
OGOR
Dengan ini saya menyatakan bahwa tesis “Kajian Tepung Bungkil Biji Karet (TBBK) Hevea brasiliensis Sebagai Bahan Baku Pakan Benih Ikan Mas Cyprinus carpio Linn” adalah karya saya dengan arahan dari komisi pembimbing dan belum diajukan dalam bentuk apapun kepada perguruan tinggi manapun. Sumber informasi yang berasal atau dikutip dari karya yang diterbitkan maupun tidak diterbitkan dari penulis lain telah disebutkan dalam teks dan dicantumkan dalam Daftar Pustaka di bagian akhir tesis ini.
Bogor, April 2011
Feed Ingredient for Common Carp Fry (Cyprinus carpio Linn) Diet. Under direction of M. AGUS SUPRAYUDI and NUR BAMBANG PRIYO UTOMO.
This research was conducted to study rubber seed meal (Hevea brasiliensis) as a candidate of plant protein source in diet for common carp fry (Cyprinus carpioLinn). This study were divided into 2 experiments: digestibility and growth. Processed rubber seed meal (pRSM) and unprocessed (upRSM) were subjected to digestibility experiment and Cr2O3 at level of 0.05% was used as a tracer. The faeces were daily
collected 30-60 minutes after feeding for 14 days. Dry matter, protein, phosphorus and calcium were used as digestibility parameters. Four treatment diets with isoprotein (30%) were used to evaluate growth performance index. Diet P1 have not
contained protein come from pRSM. Diet P2 and P3 contained 50 and 75% of protein
come from pRSM. Diet P4 contained 50% of protein come from upRSM. Completely
randomized design with 4 treatments and 3 replicates were used to this experiment. Common carp fry 2.19 ± 0.005 g was entered to 18 aquariums at 20/aquarium and feed tested diet at satiation for 40 days of culture period. The evaluated parameter were survival rate, feed consumption, feed efficiency, relative growth, protein and lipid retention, water/lipid/glycogen liver content and hepatosomatic index, histological and haematological blood. The result showed that common carp fry relatively better digested pRSM than upRSM. Moreover, the increasing of protein percentage from pRSM until 50% resulted best growth perfomance indicator and haemotological blood parameter. It is concluded that pRSM can be used as protein source up to 50% in diet common carp fry.
brasiliensis Sebagai Bahan Baku Pakan Benih Ikan Mas Cyprinus carpio Linn. Dibimbing oleh M. AGUS SUPRAYUDI dan NUR BAMBANG PRIYO UTOMO.
Tujuan dan manfaat penelitian ini adalah untuk mengkaji pemanfaatan TBBK sebagai kandidat sumber protein nabati utama berbasis bahan baku lokal dalam pakan benih ikan mas Cyprinus carpio L. Penelitian ini dilaksanakan pada bulan Oktober hingga Desember 2010 yang bertempat di Laboratorium Lapangan dan Teaching Farm Fakultas Perikanan dan Ilmu Kelautan Institut Pertanian Bogor. Analisis kimia, histologi, gambaran darah dan kualitas air dilakukan di Laboratorium Nutrisi Ternak Perah Fakultas Peternakan, Laboratorium Nutrisi Ikan, Laboratorium Kesehatan Ikan, Laboratorium Kualitas Air Fakultas Perikanan dan Ilmu Kelautan Institut Pertanian Bogor dan Laboratorium Balai Besar Penelitian Veteriner Bogor.
Ikan uji yang digunakan adalah benih ikan mas Cyprinus carpio L. ukuran 3-5 cm sebanyak 600 ekor (lebih banyak dari jumlah yang diperlukan) berukuran 2,19 ± 0,005 g. Ikan ini merupakan hasil 1 kali pemijahan dari 1 induk ikan mas Majalaya di Laboratorium Lapangan dan Teaching Farm Fakultas Perikanan dan Ilmu Kelautan Institut Pertanian Bogor. Benih ikan uji ditampung dalam 3 buah bak bervolume 200 l sebagai proses aklimatisasi (lingkungan dan pakan) selama 14 hari. Bahan baku pakan uji berupa 200 kg biji karet yang berasal dari perkebunan karet alam di Desa Pondok Meja, Kecamatan Mestong, Kabupaten Muara Jambi, Propinsi Jambi. Setelah dikeringkan, buah karet dipecahkan dan diambil bijinya selanjutnya diolah menjadi tepung. Proses pengurangan lemak TBBK hingga 15% menggunakan hidrolic press kemudian diekstrak dengan larutan heksan selama 1 hari 1 malam. Setelah diekstrak, TBBK direndam dalam air garam dengan dosis 10 g/100 ml air selama 12 jam dan dilanjutkan dengan perebusan terbuka selama 30 menit untuk mengurangi kandungan sianida.
Penelitian ini terbagi menjadi 2 (dua) bagian, yaitu uji kecernaan dan uji kinerja pertumbuhan. Pakan untuk uji kecernaan menggunakan pakan rujukan dengan kadar protein 28-30%, TBBK diolah dan TBBK tidak diolah, Cr2O3 sebagai indikator dan
CMC sebagai pengikat. Pakan kemudian dianalisis kandungan protein, fosfor, kalsium dan Cr2O3. Pakan untuk uji kinerja pertumbuhan menggunakan 4 perlakuan
dan 3 ulangan dengan Rancangan Acak Lengkap, sebagai berikut: (1) P1, tidak
mendapat sumbangan protein dari TBBK; (2) P2, 50% protein dari TBBK diolah; (3)
P3, 75% protein dari TBBK diolah; dan (4) P4, 50% protein dari TBBK tidak diolah.
Sebelum pakan dibuat, bahan baku pakan dianalisis proksimat kemudian setelah pakan selesai dibuat dilakukan kembali analisis proksimat serta analisis asam aminonya menggunakan metode AOAC.
atasnya yang bertujuan agar feses ikan terkumpul pada bagian dasar akuarium). Pakan diberikan secara at satiation (sekenyang-kenyangnya) dengan frekuensi sebanyak 3 kali sehari, yaitu pada pukul 07.00, 12.00 dan 17.00 WIB selama 14 hari masa pemeliharaan. Pada hari ke-3, feses ikan diambil 30-60 menit setelah pemberian pakan. Feses tersebut disipon dari bagian dasar akuarium kemudian ditampung dalam botol film yang selanjutnya dilakukan analisis kandungan Cr2O3, protein, fosfor dan
kalsium.
Pemeliharaan ikan pada uji kinerja pertumbuhan menggunakan 18 buah akuarium berukuran 50x40x30 cm dengan volume air sebanyak 40 l/akuarium dan padat penebaran sebanyak 20 ekor/akuarium. Pakan diberikan secara at satiation (sekenyang-kenyangnya) dengan frekuensi sebanyak 3 kali sehari, yaitu pada pukul 07.00, 12.00 dan 17.00 WIB selama 40 hari masa pemeliharaan. Jumlah pakan yang diberikan dihitung dengan cara menimbang pakan pada pagi hari dan sisa pakan pada sore hari. Ikan yang mati hingga hari kedua diganti sesuai dengan bobotnya dan setelah itu ikan yang mati ditimbang bobotnya. Pada awal dan akhir pemeliharaan, dilakukan analisis proksimat tubuh ikan uji sedangkan untuk menjaga kualitas air agar tetap baik, feses ikan disipon pada pagi dan sore hari. Selama masa pemeliharaan, nilai kualitas air yang meliputi suhu air berkisar antara 26-27oC, pH 7, DO 4,75-4,95 mg/L dan ammonia-N (NH3-N) 0,93-1,34 mg/l. Pada akhir masa
pemeliharaan, ikan dipuasakan selama 1 hari kemudian ditimbang bobotnya dan beberapa ekor ikan dari setiap perlakuan diambil untuk analisis kadar air, lemak, glikogen hati dan nilai HSI; serta gambaran darah dan histologi.
Proses pengolahan TBBK dengan cara pengurangan lemak mampu meningkatkan kecernaan total dan protein, yaitu 60,07% dan 78,83% menjadi 69,81% dan 84,23%. Nilai tingkat kelangsungan hidup (TKH) benih ikan mas pada berbagai perlakuan pakan tidak berbeda nyata (p>0,05), berkisar 83,33-86,67%. Perlakuan P1
memberikan nilai jumlah konsumsi pakan (JKP) tertinggi sebesar 165,43 g dan terendah pada perlakuan P4 sebesar 131,93 g. Perlakuan P1 dan P2 memberikan
efisisensi pakan (EP) yang tidak berbeda nyata (p>0,05) berkisar 81,72-84,57% dan mencapai nilai terendah pada perlakuan P4 sebesar 65,24%.
Nilai retensi protein (RP) pada perlakuan P1 dan P2 tidak berbeda nyata
(p>0,05), berkisar 37,12-37,94% kemudian menurun pada perlakuan P3 dan P4
(p<0,05), berkisar 19,64-26,03%. Nilai retensi lemak (RL) tertinggi terdapat pada perlakuan P4 (45,67%) dan nilai terendah pada perlakuan P1 sebesar 41,74%. Kadar
air hati tertinggi terdapat pada perlakuan P2 sebesar 77,24% dan terendah pada
perlakuan P4 sebesar 71,72%. Kadar lemak hati tertinggi terdapat pada perlakuan P4
sebesar 12,16% dan terendah pada perlakuan P1 sebesar 9,33%, Nilai glikogen hati
tertinggi terdapat pada perlakuan P2 sebesar 0,105% dan terendah pada perlakuan P4
sebesar 0,022%. Hasil pengukuran nilai hepatosomatik indeks (HSI) menunjukkan nilai tertinggi terdapat pada perlakuan P2 sebesar 0,05 dan terendah pada perlakuan P3
dan P4 sebesar 0,02
Jumlah sel darah merah (SDM) tertinggi terdapat pada perlakuan P1 sebesar
149,01x104 sel/mm3 dan terendah pada perlakuan P4 sebesar 120,51x104 sel/mm3
sedangkan jumlah sel darah putih (SDP) tertinggi terdapat pada perlakuan P4 sebesar
22,84%.
Hasil pengamatan histologi usus bagian depan benih ikan mas pada perlakuan P1 hingga P3 menunjukkan bahwa tidak terdapat kelainan spesifik tetapi pada
perlakuan P4 menunjukkan adanya nekrosis dan desquamasi epitel villi mukosa.
Begitu pula pengamatan histologi usus bagian belakang pada perlakuan P1 hingga P3
menunjukkan bahwa tidak terdapat kelainan spesifik namun terdapat nekrosis, infiltrasi sel mononuklear dan desquamasi epitel villi mukosa pada perlakuan P4.
Pada organ ginjal perlakuan P1 terjadi protein cast, nekrosis pada tubulus dan
hemoraghi ringan, begitu pula pada perlakuan P2 terjadi protein cast serta hemoraghi
ringan. Pada perlakuan P3 terjadi protein cast, hemoraghi dan infiltrasi sel
mononuklear serta pada perlakuan P4 terjadi hemoraghi, nekrosis interstitialis dan
infiltasi sel mononuklear. Selanjutnya pada otot perlakuan P1 dan P2 tidak terdapat
kelainan spesifik hanya saja pada perlakuan P3 dan P4 terjadi hyperemia sedangkan
pada organ hati perlakuan P1 hingga P3 terjadi vakuolisasi sel hati dan pada perlakuan
P4 selain terjadi vakuolisasi hati juga terjadi degenerasi sel epitel hati.
Pemberian TBBK yang diolah memberikan gambaran yang lebih baik berdasarkan sistem pencernaan dan kecernaan ikan, gambaran darah, metabolisme maupun struktur organ dibandingkan TBBK tidak diolah. Hasil penelitian memperlihatkan bahwa TBBK dapat menggantikan peranan tepung bungkil kedelai sebagai sumber protein nabati utama hingga 50% dari total protein pakan pada benih ikan mas Cyprinus carpio L.
© Hak Cipta milik IPB, tahun 2011
Hak Cipta dilindungi Undang-Undang
1. Dilarang mengutip sebagian atau seluruh karya tulis ini tanpa mencantumkan atau
menyebutkan sumber.
a. Pengutipan hanya untuk kepentingan pendidikan, penelitian, penulisan karya
ilmiah, penyusunan laporan, penulisan kritik, atau tinjauan suatu masalah.
b. Pengutipan tidak merugikan kepentingan yang wajar IPB.
2. Dilarang mengumumkan dan memperbanyak sebagian atau seluruh karya tulis dalam
KAJIAN
Hev
N TEPU
vea brasi
PA
Sebagai PrSEK
INSTI
UNG BUN
iliensis
S
AKAN BE
Cyprinu
i salah satu s Magi ogram Studi
CERR
KOLAH
ITUT PE
B
NGKIL
SEBAGA
ENIH IK
us carpio
Tesis syarat untukister Sains p i/Mayor Ilmu
RIA INA
PASCA
ERTANI
BOGOR
2011
BIJI KA
AI BAHA
KAN MA
o
Linn
PAKAN BENIH IKAN MAS Cyprinus carpio Linn Nama : Cerria Inara
NRP : C151080251
Program Studi/Mayor : Ilmu Akuakultur
Disetujui
Komisi Pembimbing
Dr. Ir. M. Agus Suprayudi, M.Si Dr. Ir. Nur Bambang Priyo Utomo, M.Si
Ketua Anggota
Diketahui
Ketua Program Studi/Mayor Ilmu Akuakultur
Dekan Sekolah Pascasarjana
Prof. Dr. Ir. Enang Harris, MS Dr. Ir. Dahrul Syah, M.Sc.Agr
Puji syukur penulis panjatkan ke hadirat Tuhan Yang Maha Kuasa yang selalu memberikan berkat dan anugerah-Nya sehingga penulis dapat menyelesaikan karya ilmiah dengan judul “Kajian Tepung Bungkil Biji Karet (TBBK) Hevea brasiliensis Sebagai Bahan Baku Pakan Benih Ikan Mas Cyprinus carpio Linn”, yang dilaksanakan sejak Oktober-Desember 2010.
Pada kesempatan ini penulis juga mengucapkan terima kasih kepada:
1. Bapak Dr. Ir. M. Agus Suprayudi, M.Si selaku Ketua Komisi Pembimbing dan Bapak Dr. Ir. Nur Bambang Priyo Utomo, M.Si selaku Anggota Komisi Pembimbing serta Bapak Ir. Dedy Yaniharto, M.Sc selaku Penguji Luar Komisi yang telah memberikan dedikasi yang tinggi berupa arahan, bimbingan serta masukan kepada penulis.
2. Kedua orang tua tercinta, Sandin Sidar Antang dan Rayawaty Thius Narang atas segala doa, kesabaran, motivasi serta kasih sayangnya. Kakak-kakakku terkasih Robby Hendra Cyptha, SP dan Arice Sandrayathi, AP, M.Si serta Bryan Marako, S.Sn dan Nellyana, S.STP, M.Si yang telah memberikan dukungan serta nasehatnya.
3. Keluarga Besar Raya Catering dan CV. Inaraya atas segala doa dan motivasi yang diberikan kepada penulis tiada henti.
4. Seluruh rekan-rekan Ilmu Akuakultur 2008 dan rekan-rekan lainnya yang tidak dapat disebutkan satu persatu, atas persaudaraan dan kebersamaannya selama ini.
5. Seluruh staf pengajar, pegawai, laboran, teknisi lapangan, pegawai perpustakaan, petugas keamanan, petugas kebersihan Departemen Budidaya Perairan Fakultas Perikanan dan Ilmu Kelautan serta Sekolah Pascasarjana Institut Pertanian Bogor atas bantuan serta dedikasinya kepada penulis dalam membantu menyelesaikan karya ilmiah ini.
6. Keluarga Besar Unitly-Silahooy atas kasih sayang, motivasi serta doa yang tiada henti diberikan kepada penulis. Terkhususnya kepada Saudara Adrien Jems Akiles Unitly S.Si, M.Si yang telah memberikan kasih sayang, doa, motivasi dan selalu setia menemani sebagai seorang kakak dan sahabat terbaik bagi penulis. God bless you.
Semoga karya ilmiah ini dapat bermanfaat bagi yang membutuhkan.
Penulis dilahirkan di Palangka Raya pada tanggal 15 Juni 1985 dari ayah
Sandin Sidar Antang dan ibu Rayawaty Thius Narang. Penulis merupakan putri
ketiga dari tiga bersaudara.
Tahun 2003 penulis lulus dari SMU Negeri 1 Palangka Raya. Pendidikan
sarjana ditempuh di Jurusan Perikanan Fakultas Pertanian Universitas Palangka
Raya dan lulus pada tahun 2007. Pada tahun 2008 penulis diterima di Program
Studi/Mayor Ilmu Akuakultur Sekolah Pascasarjana Institut Pertanian Bogor.
i
Halaman
DAFTAR TABEL --- ii
DAFTAR GAMBAR --- iii
DAFTAR LAMPIRAN --- iv
PENDAHULUAN --- 1
Latar Belakang --- 1
Perumusan Masalah --- 2
Tujuan dan Manfaat Penelitian --- 3
Hipotesis --- 3
TINJAUAN PUSTAKA --- 4
Kebutuhan Nutrisi Ikan --- 4
Sistem Pencernaan Ikan --- 5
Kecernaan Ikan --- 8
Sumber Protein Nabati Pakan --- 9
Tepung Ikan (TI) --- 10
Tepung Bungkil Kedelai/Soybean Meal (SBM) --- 11
Tepung Bungkil Biji Karet (TBBK) --- 12
Gambaran Darah Ikan dan Histologi --- 17
METODOLOGI --- 20
Waktu dan Tempat --- 20
Ikan Uji --- 20
Persiapan Bahan Baku Biji Karet --- 20
Pakan Uji --- 21
Rancangan Percobaan --- 22
Pemeliharaan Ikan --- 22
Parameter yang Dievaluasi --- 23
Analisis Kimia --- 26
Analisis Statistik --- 27
HASIL DAN PEMBAHASAN --- 28
Hasil --- 28
Pembahasan --- 31
SIMPULAN DAN SARAN --- 41
Simpulan --- 41
Saran --- 41
DAFTAR PUSTAKA --- 43
ii
DAFTAR TABEL
Halaman 1. Komposisi asam amino esensial TI (gr/100 gr protein) --- 10 2. Komposisi proksimat SBM --- 11 3. Komposisi asam amino esensial SBM (%) --- 11 4. Komposisi proksimat daging biji karet dari kebun yang tidak terpelihara
dan cangkang --- 12 5. Komposisi proksimat daging biji karet dari kebun yang terpelihara dan
cangkang --- 13 6. Kandungan nutrisi tepung bungkil biji karet (TBBK) dan tepung
fermentasi biji karet (TFBK) --- 13 7. Komposisi kimia TBBK tidak diolah dan TBBK diolah --- 20 8. Pakan uji kecernaan (%) --- 21 9. Pakan uji kinerja pertumbuhan --- 21 10. Kecernaan TBBK diolah dan tidak diolah pada benih ikan mas --- 28 11. Tingkat kelangsungan hidup (TKH), jumlah konsumsi pakan (JKP),
efisiensi pakan (EP), pertumbuhan relatif (PR), retensi protein (RP) dan
retensi lemak (RL) --- 28 12. Kadar air, lemak, glikogen hati (%) dan nilai HSI --- 29 13. Gambaran darah benih ikan mas Cyprinus carpio L. pada berbagai
iii
iv
DAFTAR LAMPIRAN
Halaman 1. Prosedur analisis proksimat dan kecernaan pada pakan dan feses --- 55 2. Analisis proksimat bahan pakan yang digunakan dalam penelitian (%
bobot kering) --- 61 3. Kecernaan total, protein, fosfor dan kalsium TBBK diolah dan TBBK
tidak diolah --- 62 4. Tingkat kelangsungan hidup (TKH), jumlah konsumsi pakan (JKP),
efisiensi pakan (EP), pertumbuhan relatif (PR), retensi protein (RP) dan
retensi lemak (RL) --- 63 5. Retensi protein dan lemak benih ikan mas Cyprinus carpio L. yang
diberi pakan uji kinerja pertumbuhan selama 40 hari masa pemeliharaan -- 64 6. Kadar air, lemak, glikogen hati dan nilai Hepatosomatik Indeks (HSI) ---- 66 7. Gambaran darah benih ikan mas Cyprinus carpio L. pada berbagai
perlakuan pakan --- 67 8. Hasil pengamatan histologi pada berbagai organ benih ikan mas --- 71 9. Analisis statistik --- 77
Latar Belakang
Ikan mas Cyprinus carpio Linn merupakan salah satu jenis ikan air tawar dan banyak dibudidayakan oleh petani di Indonesia. Data produksi ikan mas pada tahun 2005 sebanyak 216.920 ton meningkat pada tahun 2009 sebanyak 446.800 ton dengan wadah budidaya berupa kolam, keramba, waduk dan sawah. Ciamis, Sukabumi, Tasikmalaya, Bogor, Garut, Bandung, Cianjur, Purwakarta merupakan daerah pusat produksinya (DKP 2009). Produksi perikanan dunia tahun 2010 berada pada angka 144 juta ton masing-masing dari perikanan tangkap sebesar 105 juta ton (63%) sedangkan sisanya berasal dari budidaya sebesar 39 juta ton (37%) dengan jumlah yang dikonsumsi oleh manusia sebesar 114 juta ton (FAO Fishery Statistics 2010).
Dalam usaha budidaya ikan air tawar, biaya pakan sangat mempengaruhi biaya-biaya produksi. Pakan merupakan salah satu komponen yang sangat menentukan koefisien teknis budidaya (efisiensi pakan, laju pertumbuhan dan kelangsungan hidup). Biaya pakan ikan menempati biaya produksi tertinggi dalam kegiatan budidaya yaitu 70-89% dari total biaya produksi (Suprayudi 2010).
2
berkompetisi dengan manusia. Salah satu kandidatnya adalah tepung bungkil biji karet (TBBK).
TBBK dihasilkan dari biji tanaman karet yang merupakan tanaman perkebunan yang paling banyak ditanam di Indonesia. Indonesia memiliki lahan perkebunan karet paling luas di dunia, yaitu 3,3 juta Ha dan 85% diantaranya merupakan perkebunan rakyat (Apriyantono 2007). Menurut Hariyono (1996), bahwa dalam 1 Ha dapat menghasilkan biji karet sebanyak 0,8-1,2 ton/tahun sehingga produksi biji karet setiap tahunnya sebesar 2,7-4,1 juta ton.
Menurut Oyewusi et al. (2007), bahwa biji karet mengandung 10-22% protein dan dalam bentuk bungkilnya mengandung 33-40% protein. Uji coba penggunaan TBBK sebagai bahan baku pakan pada ternak telah dilakukan pada ayam pedaging strain CP 707 hingga 19% (Arossi et al. 1985 dalam Prawirodigdo 2009), 20% fermentasi menggunakan ragi tempe dan oncom pada ayam broiler (Mulyati 2003) dan 10% pada hewan babi (Madubuike et al. 2006). Pemanfaatan TBBK pada organisme akuatik pernah dilakukan dengan menggantikan protein tepung jagung sekitar 10-20% pada lele hibrid (Eyo dan Ezechi 2004).
Pada umumnya pemanfaatan protein nabati dihadapkan pada 2 kendala utama, yaitu kandungan zat anti nutrisi serta kurangnya 1-2 asam amino essensial. Menurut Soltan et al. (2008), bahwa substitusi menggunakan tepung protein asal tanaman seperti jenis leguminosa (kelor dan lamtoro), daun-daunan (mulberry leaf) dan biji-bijian (biji kapas dan biji daun matahari) memiliki kendala seperti zat anti nutrisi yang cukup tinggi dan ketersediaan asam amino lisin dan methionin yang sangat rendah. Menurut Siahaan (2009), bahwa biji karet mengandung sianida sebesar 330 mg/100 g dan lemak sebesar 32,30%.
Perumusan Masalah
penggunaan oksigen (Bahri 1987). Pada dosis rendah, sianida tidak menimbulkan kematian tetapi ikan yang terus menerus teracuni misalnya karena mengkonsumsi pakan yang mengandung sianida dapat menyebabkan diare (Eisler 1991). Selain itu, TBBK memiliki kandungan lemak yang sangat tinggi mencapai hingga 50% bahan. Melihat informasi inilah maka penelitian ini dilakukan agar peranan penting protein TBBK dalam pakan ikan dapat dikaji dengan baik.
Tujuan dan Manfaat Penelitian
Tujuan dan manfaat penelitian ini adalah mengkaji pemanfaatan TBBK sebagai kandidat sumber protein nabati utama berbasis bahan baku lokal dalam pakan benih ikan mas Cyprinus carpio L.
Hipotesis
Hipotesis yang diajukan dalam penelitian ini, sebagai berikut:
Ho : TBBK diolah dan TBBK tidak diolah dalam pakan benih ikan mas Cyprinus carpio L. pada dosis tertentu tidak berpengaruh negatif terhadap sistem pencernaan dan kecernaan ikan, gambaran darah, metabolisme dan kerusakan struktur organ.
TINJAUAN PUSTAKA
Kebutuhan Nutrisi Ikan
Penyusunan pakan ikan yang dapat memenuhi kebutuhan standar maupun
produksi didukung oleh pemenuhan sumber protein dan energinya. Protein dalam
pakan sangat efisien sebagai sumber energi yang akan diserap dan dimanfaatkan
untuk membangun atau memperbaiki sel-sel tubuh yang rusak. Apabila pemenuhan
protein dalam pakan kurang maka protein dalam jaringan tubuh akan dimanfaatkan
untuk mempertahankan fungsi jaringan yang lebih penting. Sebaliknya bila
ketersediaannya berlebihan maka protein tersebut tidak tergunakan dan dalam
sintesisnya akan dikatabolisme dan buangan berupa nitrogen terutama amonia akan
disekresikan ke perairan yang dapat membahayakan kehidupan ikan. Oleh karena itu
pemberian protein yang cukup dalam pakan secara terus menerus perlu dilakukan
agar pakan tersebut dapat diubah menjadi protein tubuh secara efisien (NRC 1983).
Menurut Webster dan Lim (2002), bahwa kebutuhan protein harian untuk
maintanance ikan mas adalah 1 g/kg berat badan sedangkan untuk memperoleh retensi protein optimal pada tubuhnya membutuhkan protein 12 g/kg berat badan.
Protein yang dibutuhkan dalam proses pertumbuhan adalah 7-8 g/berat badan/hari.
Kebutuhan ikan terhadap protein dipengaruhi oleh berbagai faktor antara lain jenis
ikan, umur ikan, ukuran ikan, kualitas protein, pakan, kecernaan pakan dan kondisi
lingkungan. Pemenuhan asam amino esensial yang wajib ada pada komposisi pakan
ikan adalah lisin. Kandungan nutrisi ikan mas yang baik untuk protein adalah
30-38%, kandungan lemak 4-15%, dan karbohidrat 30-40% (Furuichi 1988).
Kebutuhan energi ikan dalam pakan lebih rendah daripada hewan darat. Ikan
mempunyai kebutuhan energi lebih rendah karena ikan tidak mempertahankan suhu
tubuh secara tetap dan ikan relatif memerlukan energi yang kurang untuk
mempertahankan posisi dan bergerak dalam air dibandingkan mamalia dan burung.
Pakan yang dikonsumsi ikan akan menyediakan energi yang sebagian besar
digunakan untuk metabolisme yang meliputi energi untuk beraktivitas, energi untuk
dikeluarkan dalam bentuk feses dan bahan ekskresi lainnya (Webster dan Lim 2002).
Sumber energi lain yang berperan selain karbohidrat adalah lemak. Lemak
mempunyai peranan penting bagi ikan karena berfungsi sebagai sumber energi dan
asam lemak esensial, memelihara bentuk dan fungsi membran atau jaringan yang
penting bagi organ tubuh tertentu, membantu dalam penyerapan vitamin yang larut
dalam lemak serta untuk mempertahankan daya apung tubuh (NRC 1993).
Menurut Furuichi (1988), bahwa kadar optimum karbohidrat pakan untuk
golongan ikan karnivora adalah 10-20% dan golongan omnivora adalah 30-40%.
Karbohidrat dalam pakan digunakan untuk memenuhi kebutuhan energi metabolisme
basal dan maintenance sedangkan protein pakan dapat dipergunakan sepenuhnya
untuk pertumbuhan. Kebutuhan vitamin dan mineral pada pakan ikan mas,
dipengaruhi oleh berbagai faktor seperti ukuran ikan, temperatur media pemeliharaan
dan komposisi pakan. Pada pembuatan pakan komersial, pemberian vitamin dan
mineral dapat dilebihkan menjadi 2-5 kali dari kebutuhan dasar. Hal ini dikarenakan
pada proses pembuatan pelet, mengalami teknik extrution yang menggunakan suhu
tinggi sehingga memungkinkan vitamin dan mineral rusak dan larut (Takeuchi et al. 2002).
Sistem Percernaan Ikan Pencernaan Ikan
Pencernaan merupakan proses pemecahan senyawa kompleks menjadi senyawa
yang lebih kecil, yaitu hidrolisa protein menjadi asam amino atau polipeptida
sederhana dan karbohidrat menjadi gula sederhana serta dari lipid menjadi gliserol
dan asam lemak. Proses pemecahan senyawa tersebut menghasilkan energi yang
penting bagi kebutuhan sel, jaringan, organ dan makhluk hidup. Dalam proses
pencernaan pakan melibatkan beberapa komponen, yaitu: bahan yang dicerna
(pakan); struktur alat/saluran pencernaan (usus) sebagai tempat pencernaan dan
penyerapan nutrien; dan cairan digestif (enzim: protease, lipase dan amilase) yang
disekresikan oleh kelenjar pencernaan (hati dan pankreas) serta dinding usus. Kinerja
6
nutrien dan energi untuk metabolisme sehingga berpengaruh bagi pertumbuhan
(Mohanta et al. 2007).
Alat Pencernaan
Saluran pencernaan ikan mas meliputi segmen-segmen yang meliputi mulut,
rongga mulut, faring, esophagus, pylorus, usus, rektum dan anus. Ikan mas dapat
memakan plankton maupun invertebrata kecil. Atas dasar inilah maka dapat
dikatakan bahwa ikan mas merupakan ikan omnivora yang cenderung herbivora.
Keadaan usus yang sangat panjang pada ikan herbivora merupakan kompensasi
terhadap kondisi makanan yang memiliki kadar serat yang tinggi sehingga
memerlukan pencernaan lebih lama. Hal ini dapat dibuktikan melalui pengamatan
pada organ dalam ikan mas yang tidak ditemukan adanya lambung tetapi bagian
depan usus halus terlihat membesar yang lebih dikenal dengan istilah “lambung
palsu”. Ikan mas memilki panjang usus yang melebihi panjang tubuh ikan. Pada
pengukuran yang telah dilakukan diketahui bahwa tubuh ikan mas yang digunakan
memiliki panjang baku 19 cm sedangkan panjang ususnya mencapai 50 cm atau
hampir tiga kali lipat dari panjang tubuhnya. Usus yang panjang tersebut bertujuan
untuk mendapatkan hasil hidrolisis makromolekul makanan secara maksimal
(Affandi dan Tang 2002).
Kelenjar Pencernaan
Kelenjar pencernaan pada ikan mas terdiri dari hati dan pankreas (Hidayati
2007). Hati merupakan organ penting yang mensekresikan bahan untuk proses
pencernaan. Organ ini merupakan suatu kelenjar yang kompak, berwarna merah
kecoklatan. Posisi hati terletak pada rongga bawah tubuh, di belakang jantung dan di
sekitar usus depan. Pada bagian sekitar hati terdapat organ berbentuk kantung bulat
kecil, oval atau memanjang dan berwarna hijau kebiru-biruan, yang disebut kantung
empedu yang berfungsi untuk menampung cairan empedu. Organ hati tersusun oleh
sel-sel hati (hepatosit) dan di antara sel-sel tersebut banyak dijumpai kapiler-kapiler
y y ( p e p ( O b E u p d a d Pankre yang berper yang berbe (hepatopank pankreatik b eksokrin da pencernaan, (pulau-pulau Oleh karena berhubungan Enzim Penc Enzim untuk memb paling bany ditunjukkan aktivitas enz dalam maka eas merupak
ran dalam p
ntuk komp
kreas). Letak
bermuara di u
an sel endo
yaitu enzim
u langerhans
a sel-sel ters
n dengan kap
cernaan Ika
m merupakan
bantu proses
yak berperan
oleh ikan m
zim amilase
nan akan me
Gam
kan organ ya
proses pence
ak dan ad
k pankreas usus depan. okrin. Hasil m protease, s) merupaka sebut merupa
piler darah (
an
n katalisator
biokimia. M
n dalam hi
mas. Helver
lebih tinggi
eningkatkan
mbar 1. Ikan ma
ang mensekr
ernaan. Sec
a yang dif
berdekatan
Secara sitolo
l utama da
amilase, khi
an kelompok
akan sel pen
(Affandi dan
biologis yan
Menurut Moh
drolisis kar
(2002), men
i daripada pr
daya cerna
as (http://wb3.i
resikan baha
ara anatomi
ffus (menye
n dengan us
ogi, pankrea
ari pankreas
itinase dan
k sel yang a
nghasil horm
n Tang 2002)
ng dihasilka
hanta et al. ( rbohidrat ya
nyatakan ba
rotease dan
ikan terhada
itrademarket.co
an (enzim) d
i-histologis,
ebar) di an
sus depan
as memiliki 2
s eksokrin
lipase. Pank
ada di antara
mon yang po
).
an oleh sel m
(2007), bahw
aitu amilase
ahwa pada ik
lipase. Kebe
ap bahan ma
ompdimage.jpg
dan bikarbon
pankreas a
ntara sel h
sebab salur
2 tipe yaitu s
adalah enz
kreas endokr
a sel eksokr
osisinya sela
makhluk hid
wa enzim ya
e seperti ya
8
Menurut Murni (2004), bahwa enzim berperan dalam mengubah laju reaksi
sehingga kecepatan reaksi yang diperlihatkan dapat dijadikan ukuran keaktifan
enzim. Beberapa peneliti mendapatkan enzim amilase, maltase dan sakharase pada
ekstrak hati, pankreas, esofagus dan usus ikan mas. Amilase ditemukan pada seluruh
jenis ikan dan pada ikan air tawar ditemukan di sepanjang saluran pencernaan
walaupun aktivitasnya berkurang pada usus bagian belakang. Aktivitas amilase pada
ekstrak hati dan pankreas ikan mas sebesar 5,8 dan aktivitas tripsin sebesar 1,7
(Kapoor et al. 1976). Pakan dicerna secara optimal dengan bantuan enzim dalam
pakan dan saluran pencernaan ikan sehingga energi yang dihasilkan dapat digunakan
untuk memacu pertumbuhan ikan (Wirawati 2002).
Kecernaan Ikan
Kecernaan merupakan kombinasi mekanik dan kimia pada proses penghancuran
pakan menjadi bentuk yang lebih sederhana yang siap diserap oleh dinding usus dan
masuk ke dalam sistem pembuluh darah melalui proses menggunakan enzim. Nilai
kecernaan adalah ukuran relatif untuk sebuah pakan yang tercerna maupun yang
dimetabolis oleh ikan (NRC 1983). Kemampuan cerna ikan terhadap suatu pakan
dipengaruhi oleh beberapa faktor, yaitu sifat kimia air, suhu air, jenis pakan, ukuran
dan umur ikan, kandungan nutrisi pakan, frekuensi pemberian pakan serta jumlah dan
macam enzim pencernaan yang terdapat dalam saluran pencernaan pakan (NRC
1977). Nutrien dari bahan yang berbeda mungkin dicerna dengan tingkat yang
berbeda. Hal ini berhubungan dengan sumber dan komposisi bahan-bahan makanan.
Pakan yang berasal dari bahan nabati biasanya lebih sedikit dicerna dibanding
dengan bahan hewani karena bahan nabati umumnya memiliki serat kasar yang sulit
dicerna dan mempunyai dinding sel kuat yang sulit dipecahkan (Hepher 1988).
Kecernaan pakan juga dipengaruhi oleh proses dan metode pengolahan bahan-bahan
tersebut, sebab ada beberapa bahan makanan yang perlu melalui penanganan khusus
karena adanya zat inhibitor dalam bahan makanan tersebut. Menurut Mokoginta
(1997), bahwa perbedaan komposisi bahan dan zat makanan dalam pakan dapat
Analisa kecernaan pakan dapat dilakukan dengan mengumpulkan feses. Ketika
pakan melalui saluran pencernaan, tidak semua pakan dicerna dan diserap. Bagian
yang tidak dicerna dibuang dalam bentuk feses (Hepher 1988). Kecernaan pakan dan
nutrien dapat ditentukan dengan menggunakan indikator yang mempunyai sifat
mudah diindentifikasi atau tidak diserap sehingga dapat melewati saluran pencernaan.
Bahan kromium (Cr2O3) dapat digunakan sebagai indikator dalam menentukan
kecernaan pakan dengan asumsi semua khrom trioksida melalui sistem pencernaan
dan terlihat dalam feses (NRC 1983). Menurut Watanabe dan Pongmaneerat (1988),
menyatakan bahwa Cr2O3 yang digunakan pada penentuan kecernaan ikan adalah
0,5-1,0%.
Sumber Protein Nabati Pakan
Pemenuhan nutrisi pada ikan terdiri dari protein, lemak, karbohidrat, vitamin
dan mineral serta energi untuk melakukan aktivitas. Kebutuhan nutrisi ini dapat
diperoleh dari bahan baku penyusun pakan ikan. Bahan baku pakan ini biasanya
dibagi menjadi 2 golongan, yaitu bahan baku yang berasal dari hewan (hewani) dan
tumbuhan (nabati) (NRC 1977).
Protein dibutuhkan secara terus menerus oleh ikan untuk membentuk jaringan
baru (pertumbuhan dan reproduksi) atau untuk mengganti protein yang hilang
(pemeliharaan). Ketidakcukupan protein dalam makanan akan menghambat
pertumbuhan atau hilangnya bobot badan karena diambilnya protein dari jaringan
yang kurang penting untuk memelihara jaringan yang lebih penting sedangkan jika
protein terlalu banyak maka hanya sebagian kecil yang akan digunakan untuk
membuat protein baru dan sisanya akan dikonversi menjadi energi. Hal ini berarti
pemanfaatan protein untuk pertumbuhan menjadi tidak efisien (Halver 1972).
Salah satu kandidat pengganti tepung bungkil kedelai sebagai sumber protein
nabati dalam pakan adalah dengan memanfaatkan tepung bungkil biji karet (TBBK).
Hanya saja subtitusi sumber protein nabati tidaklah selalu berhasil akibat rendahnya
palatabilitas pakan, pertumbuhan serta efisiensi pakan (Burel et al. 1998 dalam
10
amino esensial, ketersediaan nutrisi, ketersediaan fosfor yang rendah serta dampak
dari metabolisme Antinutritional Factor/ANFs (Medale et al. 1998; Alarcon 1999
dalam Jobling et al. 2002).Beberapa protein nabati mempunyai kekurangan satu atau lebih asam amino esensial sehingga ketersediaannya harus tetap diperhatikan. Hal ini
bertujuan agar kandungan asam amino yang diberikan dalam pakan dapat mendekati
kebutuhan asam amino esensial ikan (Jobling et al. 2002).
Tepung Ikan (TI)
TI merupakan sumber protein dalam pakan buatan yang dapat digunakan secara
efisien (Rumsey 1993). Menurut Lovell (1989), bahwa TI memiliki protein 60-70%
yang hampir 80-90% dapat dicerna oleh ikan serta memiliki lisin dan metionin yang
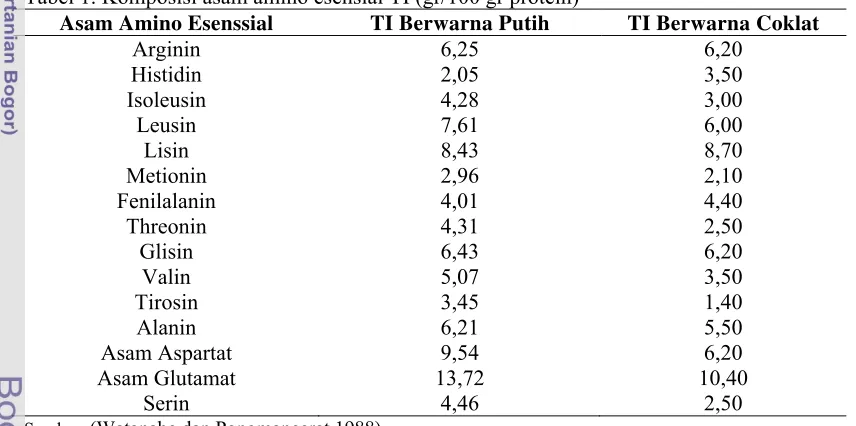
[image:34.612.73.501.359.572.2]tinggi.
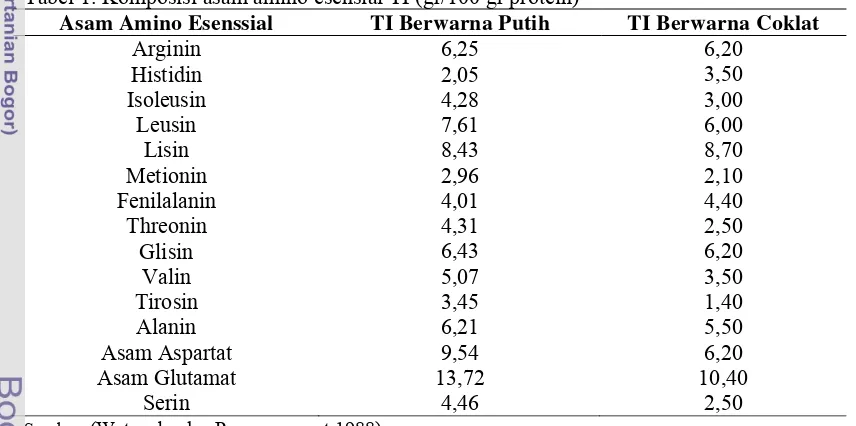
Tabel 1. Komposisi asam amino esensial TI (gr/100 gr protein)
Asam Amino Esenssial TI Berwarna Putih TI Berwarna Coklat
Arginin Histidin Isoleusin Leusin Lisin Metionin Fenilalanin Threonin Glisin Valin Tirosin Alanin Asam Aspartat Asam Glutamat Serin 6,25 2,05 4,28 7,61 8,43 2,96 4,01 4,31 6,43 5,07 3,45 6,21 9,54 13,72 4,46 6,20 3,50 3,00 6,00 8,70 2,10 4,40 2,50 6,20 3,50 1,40 5,50 6,20 10,40 2,50
Sumber: (Watanabe dan Pongmaneerat 1988)
Sebagian besar TI komersial merupakan produk dari berbagai jenis ikan yang
berkualitas dan mengandung sedikit lemak seperti ikan haring dan teri. Dalam
pemberian pakan ada 2 jenis TI yang dapat digunakan, yaitu TI berwarna putih dan TI
dibandingkan dengan TI berwarna coklat tetapi harganya jauh lebih tinggi
(Wiramiharja et al. 2007).
Tepung Bungkil Kedelai/Soybean Meal (SBM)
SBM memiliki kandungan protein dan asam amino esensial yang lebih baik
dibandingakan protein nabati lain (Watanabe dan Pongmaneerat 1988). Menurut
Furuichi (1988), bahwa SBM memiliki ketersediaan asam amino esensial yang cukup
bagi pertumbuhan ikan namun kekurangan metionin dan lisin.
Tabel 2. Komposisi proksimat SBM
Komposisi Proksimat Kandungan (%)
Air Abu Protein Lemak Serat Kasar BETN 10,57 6,95 35,21 3,12 10,57 33,58
Sumber: Hasil analisa (Abidin 2006)
Tabel 3. Komposisi asam amino esensial SBM (%)
Asam Amino Esensial SBM
Arginin Histidin Isoleusin Leusin Lisin Metionin Fenilalanin Threonin Trytophan Valin 7,15 1,93 4,66 8,22 6,28 1,29 5,33 4,09 0,49 4,42
Sumber: Yamamoto et al. (1994)
SBM memiliki makromineral dan mikromineral yang rendah termasuk fosfor
jika dibandingkan dengan tepung ikan (NRC 1983). Selain itu SBM merupakan
sumber vitamin B (Hertrampf dan Felicitas 2000; Bureue 2005; Cheng et al. 2003).
(10,8-12 14,0 M dengan Kandu B keselu Tabel 4 P Keteran Sumber B sebesa Yeong MJ/kg). Pada
n tingkat kec
ungan Nutr
Biji karet te
uruhan (Arito 4. Komposis cangkang Parameter (% Air Lemak Protein Serat Abu pH
ngan: * = tidak r: Siahaan (200
Biji karet m
ar 55-56% da
g 1977).
a ikan chann
cernaan ener
Tepun risi TBBK
erdiri atas k
onang 1988) Gam si proksimat %) Bij k dianalisis 09)
merupakan l
ari daging b
el catfish tin rgi sebesar 5
ng Bungkil
kulit yang k
).
mbar 2. Tanama
daging biji
ji Segar (%)
35,48 41,00 16,49 9,39 3,25 * limbah indu
iji dan 60%
ngkat kecern
51,4% (Hertr
Biji Karet (
keras dan 5
an karet (www
karet dari k
Biji Ker 7,8 44, 17, 10, 2,9 6,4 ustri minyak
dari hasil pe
naan protein
rampf dan F
(TBBK)
7% daging
w.platanum.com
kebun yang
ring (%) C
85 ,50 ,86 ,16 96 47
k biji karet
enggilingan
kasar sebesa
elicitas 2000
biji dari bo
m) tidak terpeli Cangkang (% * 0,48 * * * *
t dengan pe
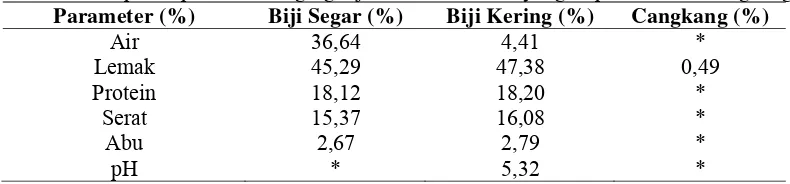
Tabel 5. Komposisi proksimat daging biji karet dari kebun yang terpelihara dan cangkang
Parameter (%) Biji Segar (%) Biji Kering (%) Cangkang (%)
Air 36,64 4,41 *
Lemak 45,29 47,38 0,49
Protein 18,12 18,20 *
Serat 15,37 16,08 *
Abu 2,67 2,79 *
pH * 5,32 *
Keterangan: * = tidak dianalisis Sumber: Siahaan (2009)
Hasil analisa proksimat dan komposisi asam amino pada tepung bungkil biji
karet (TBBK) dan tepung fermentasi biji karet (TFBK) dari beberapa penelitian
tercantum pada Tabel 6.
Tabel 6. Kandungan nutrisi tepung biji karet (TBBK) dan tepung fermentasi biji karet (TFBK)
Komponen
Kandungan
TBBK TFBK
1 2 3 4 5
Energi metabolis (kkal/kg) Berat kering (%)
Protein (%) Serat kasar (%) Lemak (%) Abu (%) BETN (%) Ca (%) P (%) Metionin Lisin Arginin Tritophan Leusin Sistin - 92,00 25,10 15,40 11,60 4,60 35,30 0,30 0,63 - - - - - - 2.550,00 94,11 26,70 12,30 8,20 4,49 4,49 0,09 0,29 0,28 0,70 1,98 - 1,40 0,57 - 90,00-95,00 25,00-33,00 4,40-17,60 4,70 4,50-6,50 24,00-45,00 0,30-0,43 0,29-0,90 0,20-0,30 0,40-0,70 1,50-1,90 - 0,80-1,10 0,20-0,60 - 91,50 33,20 4,60 8,50 5,30 45,30 0,88 0,94 - - - - - - - 31,39 33,40 14,17 11,34 6,19 34,90 0,42 0,66 0,18 1,65 3,14 - 2,12 0,57 Sumber:
[image:37.612.97.542.347.672.2]14
Zat Anti Nutrisi pada TBBK
Menurut Rachmawan (2001), menyatakan bahwa faktor zat anti nutrisi dalam
biji karet adalah “sianogenik glukosida” yang disebut linamarin. Linamarin mengurai
bersama dengan enzim linamarase (β-glukosidase) dan hidroksinitrilliase menjadi
sianida (HCN). Enzim linamarase (β-glukosidase) dan hidroksinitrilliase terletak di
sitosol sedangkan linamarin berada di vakuola sehingga dalam keadaan normal proses
penguraian tidak akan terjadi. Setiap bagian tanaman mempunyai kandungan sianida
yang berkaitan. Kandungan tertinggi terdapat dalam biji, diikuti oleh buah, daun,
batang dan akar (Valkenburg dan Bunyapraphatsara 2001). Apabila biji karet
dihancurkan, diiris ataupun dikunyah sehingga terjadi kerusakan dinding sel
jaringannya, tonoplas akan pecah maka kedua enzim tersebut akan berhubungan
dengan linamarin dan terjadi proses penguraian yang menghasilkan glukosa dan asam
sianida (Liener 1969; Cheeke dan Shull 1985; Kakes 1990; McMahon et al. 1995
dalam Mulyati 2003). Proses terbentuknya HCN dari glukosida dapat dilihat pada Gambar 3.
Sianogenik glukosida β-glukosidase Glukosa + Aglikon
Aglikon Hidroksitrilliase HCN + Aldehid atau keton
Gambar 3. Proses terbentuknya HCN dari glukosida (Cheeke dan Shull 1985; McMahon 1995 dalam Mulyati 2003)
Sianida ini menimbulkan gangguan fisiologik sebagai akibat tidak terbentuknya
kembali ATP selama proses itu masih bergantung pada sitokrom oksidase yang
merupakan tahap akhir dari proses phoporilasi oksidatif. Selama siklus metabolisme
masih bergantung pada sistem transport elektron, sel tidak mampu menggunakan
oksigen sehingga menyebabkan penurunan respirasi serobik dari sel. Hal tersebut
menyebabkan histotoksik seluler hipoksia. Bila hal ini terjadi maka jumlah oksigen
disimpulkan bahwa keracunan sianida terjadi akibat ketidakmampuan jaringan untuk
menggunakan oksigen tersebut (Anonim 2011).
Secara alamiah HCN masuk ke dalam peredaran darah tubuh melalui beberapa
jalur. Biasanya sianida masuk melalui mulut bersama makanan. Sianida di dalam
pencernaan mudah diabsorsi dan didistribusikan ke dalam darah, hati, ginjal atau
otak. Begitu konsentrasi sianida dalam darah meningkat maka laju respirasi menjadi
lambat (menurun) dan terjadi sesak nafas akibat kekurangan oksigen pada otak yang
menyebabkan timbulnya kejang-kejang. Ikatan oksidasi besi ferro dalam hemoglobin
menjadi ferri menghasilkan metHb (Fe3+). Bila hemoglobin berubah menjadi met-Hb,
darah akan kehilangan kemamampuannya untuk mengikat oksigen. Hal ini
menyebabkan terjadinya disosiasi, reaksi berbalik arah sebagai akibatnya timbul
bahaya gangguan fisiologis, yang memungkinkan terjadinya penurunan tekanan darah
karena hadirnya nitrit (Anonim 2011).
Sianida menimbulkan banyak gejala termasuk pada tekanan darah, penglihatan,
saraf pusat, sistem endokrin, sistem otonom dan sistem metabolisme dan kesulitan
bernafas karena mengiritasi mukosa saluran pernafasan karena efek racun dari sianida
adalah memblok pengambilan dan penggunaan dari oksigen maka akan didapatkan
rendahnya kadar oksigen dalam jaringan dan lebam pada tubuh yang berwarna merah
bata (Anonim 2008). Sianida dapat membentuk senyawa tiosianat bersama sulfur
yang menghambat penyerapan iod pada kelenjar thyroid. Kelainan-kelainan yang
terjadi lainnya adalah penyakit ataxic neuropathy pada manusia dan kekerdilan pada tikus (Abrar 2001). Pada manusia meskipun sejumlah kecil sianida masih dapat
ditoleransi oleh tubuh, jumlah sianida yang masuk ke tubuh tidak boleh melebihi 1
mg/berat badan per hari. Gejala keracunan sianida antara lain, meliputi penyempitan
saluran napas, mual, muntah, sakit kepala bahkan pada kasus berat dapat
menimbulkan kematian (Véteer 2000).
Tingkat toksisitas sianida dipengaruhi oleh beberapa faktor, yaitu: ukuran dan
jenis hewan; kecepatan mengunyah makanan; jenis sianogen dalam makanan;
keaktifan enzim dalam degradasi makanan dan detoksifikasi sianida. Mekanisme
16
aktifnya sistem enzim sitokrom oksidase yang terdiri dari sitokrom a-a3 komplek dan
sistem transport elektron. Bilamana sianida mengikat enzim komplek tersebut,
transport elektron akan terhambat sebagai akibatnya akan menurunkan penggunaan
oksigen oleh sel dan mengikat racun (Anonim 2011).
Sianida dalam tubuh dapat diukur pada plasma, sel darah merah atau urin.
Jumlah distribusi dari sianida berubah-ubah sesuai dengan kadar zat kimia lainnya di
dalam darah. Pada percobaan HCN pada tikus didapatkan kadar sianida tertinggi
terdapat pada paru yang diikuti oleh hati kemudian otak. Bila sianida masuk melalui
sistem pencernaan maka kadar tertinggi adalah di hati (Anonim 2008).
Menurut Siahaan (2009), bahwa biji karet mengandung sianida 330 mg/100 g.
Sianida mempunyai sifat autohidrolisis pada suhu 28ºC maka pada suhu kamar sudah
terjadi penguapan (pelepasan sianida) sehingga terjadi penurunan kandungan dan
daya toksiknya (Yuningsih et al. 2004). Menurut Ngoku dan Ononogbu (1998),
bahwa kandungan sianida dalam biji karet dapat dihilangkan dengan cara pemanasan
pada suhu 60oC ataupun dengan perebusan dengan perbandingan biji karet dan air
sebesar 1 : 2-3 (Judoamidjojo et al. 1989). Tingkat kecepatan pelepasan sianida berlainan dari tiap tanaman yang mengandung sianogen tergantung dari penguraian
jenis sianogennya (Everist 1974). Sebagai contoh sianogen amygdalin (dalam biji) mempunyai ikatan sianida lebih kuat (lebih lambat pelepasan sianidanya)
dibandingkan dengan sianogen dhurrin (dalam daun). Selain jenis sianogennya,
pelepasan sianida juga tergantung adanya peluang kontak antara sianogen dengan
enzim (dalam tanaman itu sendiri), misalnya dengan cara pencacahan atau
pemotongan yang dapat mempercepat pelepasan sianida (Tweyongyere dan
Katongole 2002).
Oleh karena itu, biji karet harus diolah menjadi konsentrat terlebih dahulu agar
dapat dimanfaatkan. Konsentrat merupakan hasil pemekatan fraksi protein biji karet
yang kadar proteinnya sudah tinggi menjadi lebih tinggi lagi. Dalam pembuatannya,
fraksi protein akan meningkat lagi dengan cara mengurangi atau menghilangkan
Gambaran Darah Ikan dan Histologi
Gambaran Darah
Darah terdiri dari cairan plasma dan sel-sel darah, yaitu sel darah merah (SDM),
sel darah putih (SDP) dan keping darah (trombosit). Plasma darah merupakan suatu
cairan jernih yang mengandung mineral-mineral terlarut, hasil absorbsi dari
pencernaan makanan, buangan hasil metabolisme oleh jaringan, enzim, antibodi serta
gas terlarut (Lagler et al. 1977). Dalam plasma darah terkandung garam-garam
anorganik (natrium klorida, natrium bikarbonat dan natrium fosfat), protein (dalam
bentuk albumin, globulin dan fibrinogen), lemak (dalam bentuk lesitin dan
kolesterol), hormon, vitamin, enzim dan nutrien. Protein plasma berperan dalam
respon kekebalan tubuh, penyangga perubahan pH darah dan mengatur tekanan
osmotik (Bond 1979).
Sel darah ikan diproduksi di dalam jaringan hematopoietik yang terletak di
ujung anterior ginjal dan limpa. Berbeda dengan mamalia, pada ikan tidak ada
sumsum tulang namun ikan memiliki limfonodus. Pada ikan, darah dibentuk di dalam
organ ginjal, limpa dan timus (Dellman dan Brown 1989). Fungsi darah pada ikan
yaitu untuk mengedarkan zat makanan hasil pencernaan dan oksigen ke sel-sel tubuh
serta membawa hormon dan enzim ke organ yang memerlukannya. Beberapa
parameter yang dapat memperlihatkan perubahan pada darah adalah jumlah sel darah
merah (SDM), sel darah putih (SDP), kadar hemoglobin (Hb) dan kadar hematokrit
(Ht) (Lagler et al. 1977).
SDM pada ikan merupakan sel dengan jumlah paling banyak, mencapai 4x106
sel/mm3 (Moyle dan Cech 2004). Jumlah SDM bervariasi pada tiap spesies dan
biasanya dipengaruhi oleh stres dan suhu lingkungan. Menurut Moyle dan Cech
(2004), bahwa jumlah SDM pada ikan mas Cyprinuscarpio adalah 1,43x106 sel/mm3. SDM mengandung hemoglobin yang merupakan protein-pigmen kompleks yang
18
merah. Sebagai intinya Fe dan rangka protoperphyrin serta globin (tetra phirin) menyebabkan warna darah merah. Memiliki afinitas (daya gabung) terhadap oksigen
dan membentuk oxihemoglobin dalam sel darah merah. Hemoglobin dalam darah
membawa oksigen dari paru-paru ke seluruh jaringan tubuh dan membawa kembali karbondioksida dari seluruh sel menuju paru-paru untuk dikeluarkan dari tubuh.
Penurunan kadar hemoglobin dari normal berarti terjadinya kekurangan darah yang
disebut anemia. Anemia merupakan keadaan menurunnya kadar hemoglobin, hematokrit dan jumlah sel darah merah di bawah nilai normal. Hampir semua gangguan pada sistem peredaran darah disertai dengan anemia yang ditandai dengan warna kepucatan pada tubuh, penurunan kerja fisik dan penurunan daya tahan tubuh (Moyle dan Cech 2004).
Konsentrasi hemoglobin diukur berdasarkan pada intensitas warna dan dinyatakan
dalam satuan gram hemoglobin/100 ml darah (g/100 ml) (Lagler et al. 1977).
Konsentrasi hemoglobin ikan mas (Cyprinus carpio) adalah 6,40 g % (Houston dan
De Wilde 1968 dalam Moyle dan Cech 2004).
SDP dikelompokkan berdasarkan pada ada tidaknya butir-butir (granul) dalam
sitoplasma, yaitu granulosit dan agranulosit. Kelompok granulosit meliputi neutrofil,
eosinofil dan basofil. Jenis ini memiliki sifat reaksi terhadap zat tertentu yaitu
leukosit eosinofil yang bersifat asidofil (berwarna merah oleh eosin), leukosit basofil
berwarna basofil (ungu) dan leukosit netrofil bersifat tidak basofil maupun asidofil
(Dellman dan Brown 1989). Menurut Lagler et al. (1977), jumlah SDP berkisar
antara 20-150 x 104 sel/mm3.
Menurut Alifuddin (1993), bahwa hematokrit merupakan perbandingan antara
plasma dengan padatan darah. Perbandingan antara keduanya dibaca dengan pembaca
mikrohematokrit dalam satuan %. Nilai hematokrit Cyprinus carpio adalah 27,1%
(Houston dan De Wilde 1968 dalam Moyle dan Cech 2004). Pada keadaan hipoksia
akan menyebabkan sel membengkak sehingga meningkatkan nilai hematokrit (Heath
1987).
Histologi merupakan teknik yang digunakan untuk mempelajari jaringan
normal sedangkan untuk pengamatan kelainan-kelainan pada jaringan disebut teknik
histopatologi. Histopatologi secara biologis digunakan untuk mengukur efek stres
lingkungan terhadap hewan (jaringan). Perubahan histopatologi merupakan indikator
perubahan secara biokimia dan fisiologi yang digunakan untuk menentukan efek yang
akan terjadi seperti pada pertumbuhan, reproduksi, pertahanan diri serta stabilitas
populasi (MacKim 1985; Meyer dan Hendricks 1985 dalam Hinton dan Laurtn 1990).
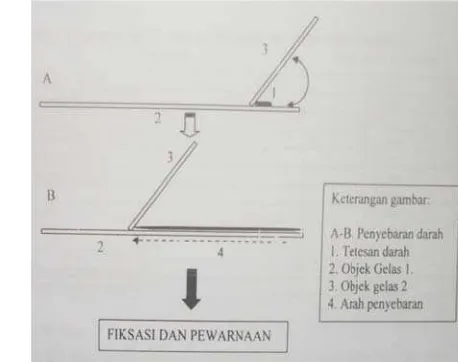
Preparasi jarigan meliputi beberapa langkah termasuk fiksasi jaringan, dehidrasi,
METODOLOGI
Waktu dan Tempat
Penelitian ini dilaksanakan bulan Oktober sampai Desember 2010 yang
bertempat di Laboratorium Lapangan dan Teaching Farm Fakultas Perikanan dan
Ilmu Kelautan Institut Pertanian Bogor. Analisis kimia, histologi, gambaran darah
dan kualitas air dilakukan di Laboratorium Nutrisi Ternak Perah Fakultas Peternakan,
Laboratorium Nutrisi Ikan, Laboratorium Kesehatan Ikan, Laboratorium Kualitas Air
Fakultas Perikanan dan Ilmu Kelautan Institut Pertanian Bogor dan Laboratorium
Balai Besar Penelitian Veteriner Bogor.
Ikan Uji
Ikan uji yang digunakan adalah benih ikan mas Cyprinus carpio L. ukuran 3-5 cm sebanyak 600 ekor (lebih banyak dari jumlah yang diperlukan) berukuran 2,19 ±
0,005 g. Ikan ini merupakan hasil 1 kali pemijahan dari 1 induk ikan mas Majalaya di
Laboratorium Lapangan dan Teaching Farm Fakultas Perikanan dan Ilmu Kelautan
Institut Pertanian Bogor. Benih ikan uji ditampung dalam 3 buah bak bervolume 200
liter air sebagai proses aklimatisasi (lingkungan dan pakan) selama 14 hari.
Persiapan Bahan Baku Biji Karet
Bahan baku pakan uji ini berupa 200 kg biji karet yang berasal dari perkebunan
karet alam di Desa Pondok Meja, Kecamatan Mestong, Kabupaten Muara Jambi,
Propinsi Jambi.
Tabel 7. Komposisi kimia TBBK tidak diolah dan TBBK diolah
Komposisi TBBK Tidak Diolah TBBK Diolah
Protein (%) 21,87 33,82
Lemak (%) 49,30 15,07
Serat Kasar (%) 3,19 15,03
Abu (%) 3,14 5,06
Air (%) 1,50 11,00
BETN (%) 21,00 20,02
Sianida (mg/kg) 18.200 10.920
Setelah dikeringkan, buah karet dipecahkan dan diambil bijinya selanjutnya
diolah menjadi tepung. Proses pengurangan lemak TBBK hingga 15% menggunakan
hidrolic press kemudian diekstrak dengan perendaman dalam larutan heksan selama 1 hari 1 malam. Setelah diekstrak, TBBK direndam dalam air garam dengan dosis 10
g/100 ml selama 12 jam dan dilanjutkan dengan perebusan terbuka selama 30 menit
untuk mengurangi kandungan sianida.
Pakan Uji
Dalam penelitian ini terdapat 2 macam pakan uji, yaitu pakan untuk uji
kecernaan (Tabel 8) dan pakan untuk uji kinerja pertumbuhan (Tabel 9).
Tabel 8. Pakan uji kecernaan (%)
Bahan Baku Pakan Rujukan TBBK Diolah TBBK Tidak Diolah
Pakan Komersial Pengikat (CMC)
Cr2O3
Biji Karet 94,50 5,00 0,50 0 64,50 5,00 0,50 30,00 64,50 5,00 0,50 30,00
Total 100 100 100
Tabel 9. Pakan uji kinerja pertumbuhan (%)
Bahan Baku Perlakuan
P1 P2 P3 P4
Bungkil biji karet Bungkil kedelai Bahan nabati lainnya Premiks 0 28,45 67,25 4,30 41,40 10,20 44,10 4,30 62,09 3,00 30,61 4,30 64,01 28,00 3,69 4,30
Total 100 100 100 100
Sianida 0 0,45 0,67 1,16
Analisis Proksimat Kadar air Protein Lemak Abu Serat kasar BETN 4,72 31,82 8,12 7,75 6,58 41,01 5,00 30,84 10,82 7,30 8,63 37,41 5,11 30,80 11,86 7,43 9,55 35,25 3,37 29,58 31,90 6,34 4,37 24,44
Total 100 100 100 100
22
Pakan untuk uji kecernaan menggunakan pakan rujukan dengan kadar protein
28-30%, TBBK diolah dan TBBK tidak diolah, Cr2O3 sebagai indikator dan CMC
sebagai pengikat. Pakan kemudian dianalisis kandungan protein, fosfor, kalsium dan
Cr2O3. Pakan untuk uji kinerja pertumbuhan menggunakan bahan baku berupa TBBK
diolah dengan berbagai level dan TBBK tidak diolah (Lampiran 1). Sebelum pakan
dibuat, bahan baku pakan akan dianalisis proksimat kemudian setelah pakan selesai
dibuat dilakukan kembali analisis proksimat serta asam aminonya menggunakan
metode AOAC (1984) (Lampiran 2).
Rancangan Percobaan
Penelitian tahap pertama berupa uji kecernaan menggunakan 3 perlakuan, yaitu:
pakan rujukan, TBBK yang diolah dan TBBK yang tidak diolah. Penelitian tahap
kedua berupa uji kinerja pertumbuhan menggunakan 4 perlakuan dan 3 ulangan
dengan Rancangan Acak Lengkap, sebagai berikut:
Perlakuan P1: Tidak mendapat sumbangan protein dari TBBK.
Perlakuan P2: 50% protein dari TBBK diolah.
Perlakuan P3: 75% protein dari TBBK diolah.
Perlakuan P4: 50% protein dari TBBK tidak diolah.
Pemeliharaan Ikan
Pemeliharaan ikan pada uji kecernaan menggunakan 9 buah akuarium
berukuran 50x40x30 cm dengan volume air sebanyak 40 l/akuarium dan padat
penebaran sebanyak 10 ekor/akuarium. Setiap akuarium dilengkapi dengan aerator,
sistem resirkulasi dan diberi penutup plastik agar ikan tidak mudah stres terhadap
lingkungan sekitar. Akuarium diletakkan dalam posisi miring (menanjak bagian
atasnya yang bertujuan agar feses ikan terkumpul pada bagian dasar akuarium).
Pakan diberikan secara at satiation (sekenyang-kenyangnya) dengan frekuensi
sebanyak 3 kali sehari, yaitu pada pukul 07.00, 12.00 dan 17.00 WIB selama 14 hari
masa pemeliharaan. Pada hari ke-3, feses ikan diambil 30-60 menit setelah pemberian
ditampung dalam botol film yang selanjutnya dilakukan analisis kandungan Cr2O3,
protein, fosfor dan kalsium.
Pemeliharaan ikan pada uji kinerja pertumbuhan menggunakan 18 buah
akuarium berukuran 50x40x30 cm dengan volume air sebanyak 40 l/akuarium dan
padat penebaran sebanyak 20 ekor/akuarium. Pakan diberikan secara at satiation
(sekenyang-kenyangnya) dengan frekuensi sebanyak 3 kali sehari, yaitu pada pukul
07.00, 12.00 dan 17.00 WIB selama 40 hari masa pemeliharaan. Jumlah pakan yang
diberikan dihitung dengan cara menimbang pakan pada pagi hari dan sisa pakan pada
sore hari. Ikan yang mati hingga hari kedua diganti sesuai dengan bobotnya dan
setelah itu ikan yang mati ditimbang bobotnya. Pada awal dan akhir pemeliharaan,
dilakukan analisis proksimat tubuh ikan uji sedangkan untuk menjaga kualitas air
agar tetap baik, feses ikan disipon pada pagi dan sore hari. Selama masa
pemeliharaan, nilai kualitas air yang meliputi suhu air berkisar antara 26-27oC, pH 7,
DO 4,75-4,95 mg/l dan ammonia-N (NH3-N) 0,93-1,34 mg/l. Pada akhir masa
pemeliharaan, ikan dipuasakan selama 1 hari kemudian ditimbang bobotnya dan
beberapa ekor ikan dari setiap perlakuan diambil untuk analisis kadar air, lemak,
glikogen hati dan nilai HSI, histologi serta gambaran darah.
Parameter yang Dievaluasi Kecernaan Total, Protein, Fosfor dan Kalsium
Kecernaan total/protein, fosfor (P) dan kalsium (Ca) dihitung menurut Law et al. (1985), yaitu:
Kecernaan total/protein/P/Ca (%) = 1 - IP x NF x 100
IF NP
Ket: IP = Cr2O3 dalam pakan (%)
IF = Cr2O3 dalam feses (%)
NP = Protein, fosfor dan kalsium dalam pakan (%)
NF = Protein, fosfor dan kalsium dalam feses (%)
Tingkat Kelangsungan Hidup
24
TKH (%) = ∑ total ikan akhir (ekor) x 100%
∑ total ikan awal (ekor)
Jumlah Konsumsi Pakan
Jumlah konsumsi pakan dihitung dengan mengurangi total jumlah pakan yang
diberikan pada akhir penelitian dengan awal penelitian.
Efisiensi Pakan
Efisiensi pakan (EP) dihitung menurutTakeuchi (1988), yaitu:
Ket : Wt = bobot total ikan pada akhir pemeliharaan (g)
W0 = bobot total ikan pada awal pemeliharaan (g)
Wd = bobot total ikan yang mati selama pemeliharaan (g)
F = jumlah pakan yang diberikan selama percobaan (g)
Pertumbuhan Relatif
Pertumbuhan relatif (PR) dihitung menurut Takeuchi (1988), yaitu:
PR (%) = Wt - W0 x 100%
W0
Ket : Wt = Biomassa ikan akhir pemeliharaan (g)
W0 = Biomassa ikan awal pemeliharaan (g)
Retensi Protein (RP)
Retensi protein (RP) dihitung menurut Takeuchi (1988), yaitu:
RP (%) = (F - I) x 100%
P
Ket : F = jumlah protein tubuh pada akhir pemeliharaan (g)
I = jumlah protein tubuh pada awal pemeliharaan (g)
P = jumlah protein yang dikonsumsi ikan (g)
Retensi Lemak (RL)
Retensi lemak (RL) dihitung menurut Takeuchi (1988), yaitu: EP (%) = [(Wt + Wd) – W0] x 100%
RL (%) = (F - I) x 100% L
Ket : F = jumlah lemak tubuh pada akhir pemeliharaan (g)
I = jumlah lemak tubuh pada awal pemeliharaan (g)
L = jumlah lemak yang dikonsumsi ikan (g)
Analisis Kadar Air, Lemak, Glikogen Hati dan Nilai Hepatosomatik Indeks (HSI) (Garling dan Wilson 1977)
Analisis ini dilakukan untuk membandingkan keadaan organ hati sebelum dan
sesudah diberi pakan TBBK, yang meliputi kadar air, lemak, glikogen hati serta nilai
hepatosomatik indeks (HSI).
Keterangan: * dalam bobot basah
Gambaran Darah
Pengamatan gambaran darah dilakukan untuk melihat pengaruh pemberian
TBBK dalam pakan yang menimbulkan perubahan komposisi darah pada ikan uji.
Pengambilan darah dilakukan pada awal dan akhir pemeliharaan. Pengamatan
gambaran darah yang dilakukan meliputi sel darah merah (SDM), dan sel darah putih
(SDP), hemoglobin (Hb) dan hematokrit (Ht).
∑ SDM = Jumlah sel
terhitung x
1
volume kotak besar x
faktor pengenceran
= Jumlah sel
terhitung x
1
0,05 x 0,05 x 0,1 mm3
x 200
= ……. sel/mm3
∑ SDP = Jumlah sel
terhitung
x 1
volume kotak besar x
faktor pengenceran = Jumlah sel
terhitung
x 1
0,2 x 0,2 x 0,1 mm3 x 10
= ……. sel/mm3
HSI = Bobot organ hati (g)
*
26
Pengukuran kadar hemoglobin darah dengan menggunakan metode Sahli, yang
didasarkan atas terbentuknya asam hematin (Hb darah dirombak menjadi asam
hematin oleh asam khlorida 0,1 N) dengan satuan pengukuran dalam g %. Tabung
Sahli diisi dengan larutan HCl 0,1 N sampai batas tera 2. Darah dihisap dengan pipet
Sahli sampai skala 20 mm3. Darah kemudian dipindahkan ke dalam tabung sahli yang
telah diisi dengan larutan HCl 0,1 N. Kedua bahan diaduk dan didiamkan sebentar
agar terbentuk asam hematin (berwarna kuning kecoklatan) kemudian tambahkan
aquades hingga warna sampel sama dengan warna standar pada tabung Sahli.
Pembacaan dilakukan dengan melihat permukaan cairan dan warna yang dicocokkan
dengan warna pada skala tabung Sahli yang dilihat pada lajur g % yang berarti
banyaknya hemoglobin dalam g/100 ml darah (Aliffudin 1993).
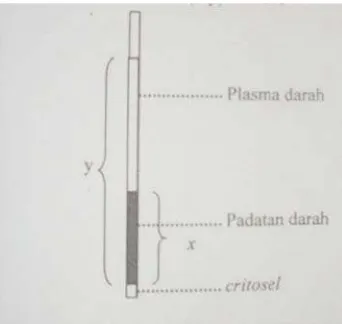
Pengukuran kadar hematokrit dilakukan untuk membandingkan plasma dengan
padatan darah, perbandingan keduanya dibaca dengan pembaca mikrohematokrit
dalam satuan %. Darah dihisap dengan menggunakan tabung mikrohematokrit
berlapis heparin sebanyak 4/5 dari volume tabung kemudian bagian ujung tabung
ditutup dengan menggunakan lilin sumbat (cristosel). Tabung yang berisi darah
kemudian disentrifugasi selama 5 menit dengan kecepatan 3.000 rpm. Pengukuran
dilakukan dengan membandingkan bagian darah yang mengendap dengan seluruh
bagian darah yang ada di dalam tabung mikrohematokrit dan hasilnya dinyatakan
dalam %, yaitu (x/y) x 100% (Aliffudin 1993).
Histologi Usus, Ginjal, Otot dan Hati
Histologi dilakukan untuk melihat terjadinya kerusakan sel, penumpukan lemak
dan perbedaan hepatosit pada setiap perlakuan. Pengambilan sampel dilakukan pada
awal dan akhir pemeliharaan. Pembuatan preparat dilakukan dengan metode
pewarnaan hematoksilin-eosin. Hasil histologi selanjutnya diamati dengan mikroskop pada pembesaran 100x. Pengamatan dilakukan terhadap keberadaan vakuola dan
kerusakan sel usus, ginjal, otot dan hati (Humason 1972).
Kadar air diukur dengan metode pemanasan dalam oven (105-110oC) selama 4
jam. Protein dianalisis dengan metode Kjedahl, lemak dengan metode ekstraksi
menggunakan alat Soxlet, abu dengan pemanasan dalam tanur (400-600oC), serat
kasar diukur dengan pelarutan dalam asam dan basa kuat serta pemanasan. Lemak
tubuh dan hati dianalisis dengan menggunakan metode Folch (Takeuchi 1988).
Pengukuran Cr2O3, fosfor dan kalsium serta HPLC untuk asam amino sesuai prosedur
AOAC (1984). Pengukuran zat anti nutrisinya dilakukan menggunakan alat
spectrofotometer (APHA 1998).
Analisis Statistik
Data dianalisis menggunakan Analysis of Variance (ANOVA) dan dilanjutkan
dengan Uji Duncan dengan selang kepercayaan 95% (α = 0,05) dengan menggunakan
program SAS (Mattjik dan Sumertajaya 2006). Pengamatan histologi dan gambaran
darah dianalisis dengan analisis desriptif ekploratif menggunakan tabel dan grafik.
HASIL DAN PEMBAHASAN
Hasil Uji Kecernaan
Data kecernaan total, protein, fosfor dan kalsium pada TBBK yang diolah dan TBBK tidak diolah pada benih ikan mas tercantum pada Tabel 10 dan Lampiran 3. Proses pengolahan TBBK dengan cara pengurangan lemak mampu meningkatkan kecernaan total dan protein, yaitu 60,07% dan 78,83% menjadi 69,81% dan 84,23%.
Tabel 10. Kecernaan total, protein, fosfor dan kalsium TBBK diolah dan TBBK tidak diolah
Bahan Kecernaan (%)
Total Prote in Fosfor (P) Kalsium (Ca) TBBK diolah 69,81 ± 0,95a 84,23 ± 0,62a 86,51 ± 0,85a 78,09 ± 3,86a TBBK tidak diolah 60,07 ± 2,27b 78,83 ± 2,07b 83,15 ± 1,16b 65,21 ± 0,72b
Keterangan: Nilai yang tertera merupakan rata-rata ± standar deviasi. Huruf di belakang standar deviasi yang berbeda dalam baris yang sama menunjukkan perbedaan nyata (p<0,05).
Uji Kinerja Pertumbuhan
Data uji kinerja pertumbuhan benih ikan mas yang diberi berbagai pakan perlakuan tercantum pada Tabel 12 dan Lampiran 4. Nilai TKH benih ikan mas pada berbagai perlakuan pakan tidak berbeda nyata (p>0,05), berkisar 83,33-86,67%. Perlakuan P1 memberikan nilai JKP tertinggi sebesar 165,43 g dan terendah pada
perlakuan P4 sebesar 131,93 g. Perlakuan P1 dan P2 memberikan EP yang tidak
berbeda nyata (p>0,05) berkisar 81,72-84,57% dan mencapai nilai terendah pada perlakuan P4 sebesar 65,24%.
Tabel 11. Tingkat kelangsungan hidup (TKH), jumlah konsumsi pakan (JKP), efisiensi pakan (EP), pertumbuhan relatif (PR), retensi protein (RP) dan retensi lemak (RL)
Paramete r Perlakuan
P1 P2 P3 P4
TKH (%) 86,67 ± 5,77a 86,67 ± 2,89a 86,67 ± 2,89a 83,33 ± 5,77a JKP (g) 165,43 ± 0,34a 163,54 ± 0,25a 157,50 ± 0,17b 131,93 ± 0,46c EP (%) 81,72 ± 3,88a 84,57 ± 0,44a 67,62 ± 2,80b 65,24 ± 1,53b PR (%) 262,48 ± 21,88a 259,45 ± 11,90a 202,66 ± 11,26b 146,60 ± 21,21c RP (%) 37,94 ± 3,26a 37,12 ± 1,40a 26,03 ± 0,79b 19,64 ± 2,48 c RL (%) 41,74 ± 2,69a 44,19 ± 1,83a 45,27 ± 2,13a 45,67 ± 2,76a
Nilai RP pada perlakuan P1 dan P2 tidak berbeda nyata (p>0,05), berkisar
37,12-37,94% kemudian menurun pada perlakuan P3 dan P4 (p<0,05), berkisar
19,64-26,03% (Lampiran 5). Nilai RL tertinggi terdapat pada P4 (45,67%) dan tidak berbeda
nyata pada perlakuan TBBK diolah lainnya (p>0,05), berkisar 41,74-45,27% dengan nilai RL terendah pada perlakuan P1 sebesar 41,74%.
Kadar Air, Hati, Glikogen Hati dan Nilai Hepatosomatik Indeks (HSI)
Lemak dan glikogen hati benih ikan mas relatif meningkat setelah diberi pakan perlakuan (Tabel 12 dan Lampiran 6). Kadar air hati tertinggi terdapat pada perlakuan P2 sebesar 77,24% lebih tinggi dibandingkan perlakuan P4 sebesar 71,72%. Lemak
hati tertinggi terdapat pada perlakuan P4 sebesar 12,16% dan terendah pada perlakuan
P1 sebesar 9,33% sedangkan untuk glikogen hati tertinggi terdapat pada perlakuan P2
sebesar 0,105% dan terendah pada perlakuan P4 sebesar 0,022% sedangkan hasil
pengukuran HSI menunjukkan nilai tertinggi terdapat pada perlakuan P2 sebesar 0,05
dan terendah pada perlakuan P3 dan P4 sebesar 0,02.
Tabel 12. Kadar air, lemak, glikogen hati (%) dan nilai Hepatosomatik Indeks (HSI)
Paramete r Perlakuan
Awal P1 P2 P3 P4
Kadar air (%) 70,45 74,43 ± 0,86b 77,24 ± 0,57a 73,66 ± 1,33b 71,72 ± 1,19c Lemak (%) 3,03 9,33 ± 0,64b 9,80 ± 0,15b 11,73 ± 0,70a 12,16 ± 1,42a Glikogen (%) 0,0018 0,093 ± 0,007b 0,105 ± 0,002a 0,039 ± 0,004c 0,022 ± 0,003d HSI 0,0044 0,04 ± 0,01a 0,05 ± 0,01a 0,02 ± 0,01b 0,02 ± 0,01b Keterangan: Nilai yang tertera merupakan rata-rata ± standar deviasi. Huruf di belakang
standar deviasi yang berbeda dalam baris yang sama menunjukkan perbedaan nyata (p<0,05).
Gambaran Darah
Pemberian TBBK diolah dan tidak diolah dalam pakan menyebabkan perbedaan gambaran darah. Hasil pengamatan berbagai perlakuan pakan dapat dilihat pada Tabel 13 dan Lampiran 7. Jumlah SDM tertinggi terdapat pada perlakuan P1
sebesar 149,01x104 sel/mm3 dan terendah pada perlakuan P4 sebesar 120,51x104
sel/mm3 sedangkan jumlah SDP tertinggi terdapat pada perlakuan P4 sebesar
30
Jumlah Hb terendah terdapat pada perlakuan P4 sebesar 5,24 g % dan tertinggi pada
perlakuan P1 sebesar 5,84 g % dan jumlah Ht terendah terdapat pada perlakuan P1
sebesar 20,63% dan tertinggi pada perlakuan P4 sebesar 22,84%.
Tabel 13. Gambaran darah benih ikan mas Cyprinus carpio L. pada berbagai perlakuan pakan
Paramete r Perlakuan
Awal P1 P2 P3 P4
SDM 82,80 149,01 ± 0,08a 148,96 ± 0,05a 139,86 ± 0,17b 120,51 ± 0,17c SDP 42,20 97,36 ± 0,07d 98,92 ± 0,08c 99,76 ± 0,13b 100,41 ± 0,14a Hb 2,80 5,84 ± 0,07a 5,83 ± 0,05a 5,57 ± 0,13b 5,24 ± 0,11c Ht 5,80 20,63 ± 0,31d 20,93 ± 0,06c 21,90 ± 0,07b 22,84 ± 0,12a Keterangan: Nilai yang tertera merupakan rata-rata ± standar deviasi. Huruf di belakang standar deviasi yang berbeda dalam baris yang sama menunjukkan perbedaan nyata (p<0,05). Sel darah merah (SDM, x104 sel/mm3), sel darah putih (SDP, x104 sel/mm3), hemoglobin (Hb, g %) dan hematokrit (Ht, %).
Histologi Usus, Ginjal, Otot dan Hati
[image:54.612.72.509.420.663.2]Hasil pengamatan histologi pada beberapa organ pada benih ikan mas terdapat pada Tabel 14 dan Lamp