KARAKTERISASI DAN KESTABILAN PRODUK
KOMBINASI MINYAK IKAN DAN MINYAK
HABBATUSSAUDA
TENNY FARADIBA
DEPARTEMEN TEKNOLOGI HASIL PERAIRAN FAKULTAS PERIKANAN DAN ILMU KELAUTAN
INSTITUT PERTANIAN BOGOR BOGOR
PERNYATAAN MENGENAI SKRIPSI DAN
SUMBER INFORMASI SERTA PELIMPAHAN HAK CIPTA
Dengan ini saya menyatakan bahwa skripsi berjudul “Karakterisasi dan Kestabilan Produk Kombinasi Minyak Ikan dan Minyak Habbatussauda” adalah benar karya saya dengan arahan dari komisi pembimbing dan belum diajukan dalam bentuk apa pun kepada perguruan tinggi mana pun. Sumber informasi yang berasal atau dikutip dari karya yang diterbitkan maupun tidak diterbitkan dari penulis lain telah disebutkan dalam teks dan dicantumkan dalam Daftar Pustaka di bagian akhir skripsi ini.
Dengan ini saya melimpahkan hak cipta dari karya tulis saya kepada Institut Pertanian Bogor.
Bogor, Juni 2013
Tenny Faradiba
ABSTRAK
TENNY FARADIBA. Karakterisasi dan Kestabilan Produk Kombinasi Minyak Ikan dan Minyak Habbatussauda. Dibimbing oleh SUGENG HERI SUSENO dan NURJANAH.
Minyak ikan dan habbatussauda saat ini banyak digunakan dalam meningkatkan kualitas otak dan mencegah berbagai penyakit. Tujuan penelitian ini adalah menentukan karakteristik dan kestabilan produk kombinasi minyak ikan dan habbatussauda. Formulasi minyak ikan dan habbatussauda yaitu sebesar 1:1, 3:1, 5:1, dan 7:1. Analisis profil asam lemak menunjukkan bahwa kandungan terbanyak yang terdapat pada minyak ikan yaitu EPA dan DHA, sedangkan minyak habbatussauda yaitu asam oleat dan asam linoleat. Minyak habbatussauda memiliki aktivitas antioksidan yang lebih tinggi sebesar 551,17 mM AEAC dibandingkan dengan minyak ikan sebesar 61,15 mM AEAC. Berdasarkan uji FFA sebesar 1,68%, bilangan peroksida sebesar 26,67 meq/kg, dan bilangan anisidin 13,65 meq/kg, hasil terbaik yaitu produk kombinasi formulasi 1:1. Hasil terbaik dari uji kestabilan adalah produk kombinasi 3:1 dengan nilai FFA terendah hingga hari ke-9 sebesar 5,94%, dan untuk uji organoleptik formulasi 7:1 paling disukai panelis karena memiliki warna yang paling cerah.
Kata kunci: antioksidan, anisidin, asam lemak bebas, kestabilan, organoleptik, peroksida
ABSTRACT
TENNY FARADIBA. Characterization and Stabilization Product Combination of Fish Oil and Habbatussauda Oil. Supervised by SUGENG HERI SUSENO and NURJANAH.
Fish oil and habbatussauda are currently used to improving the quality of brain and preventing various diseases. The purpose of research is to specify characteristics and stability of product combination of fish oil and habbatussauda. The formulation of fish oil and habbatussauda are 1:1, 3:1, 5:1 and 7:1. The fatty acid profile test showed that most content found on the fish oil are EPA and DHA, while on habbatussauda are oleic and linoleic acid. Test of antioxidant activity showed that habbatussauda has higher antioxidant activity of 551.17 mM AEAC compared with fish oil of 61.15 mM AEAC. Based on free fatty acid test with 1.68%, peroxide value with 26.67 meq/kg, and anisidine value with 13.65 meq/kg, the best result is product combination formulation 1:1. The best results from stabilization test is product combination 3:1 with the lowest FFA value 5.94% in the 9th days, for organoleptic test, formulation 7:1 is the most favourite panelists because it has the brightest color.
Skripsi
sebagai salah satu syarat untuk memperoleh gelar Sarjana Perikanan
pada
Departemen Teknologi Hasil Perairan
DEPARTEMEN TEKNOLOGI HASIL PERAIRAN FAKULTAS PERIKANAN DAN ILMU KELAUTAN
INSTITUT PERTANIAN BOGOR BOGOR
2013
TENNY FARADIBA
KARAKTERISASI DAN KESTABILAN PRODUK
KOMBINASI MINYAK IKAN DAN MINYAK
Judul Skripsi : Karakterisasi dan Kestabilan Produk Kombinasi Minyak Ikan dan Minyak Habbatussauda
Nama : Tenny Faradiba NIM : C34090035
Disetujui oleh
Dr. Sugeng Heri Suseno, S.Pi, M.Si Pembimbing I
Dr. Ir. Nurjanah, MS Pembimbing II
Diketahui oleh
Dr. Ir. Ruddy Suwandi MS.,Mphil Ketua Departemen
PRAKATA
Puji dan syukur penulis panjatkan kepada Allah subhanahu wa ta’ala
atas segala karunia-Nya sehingga karya ilmiah ini berhasil diselesaikan. Tema yang dipilih dalam penelitian yang dilaksanakan sejak bulan Januari 2013 ini minyak ikan, dengan judul Karakterisasi dan Kestabilan Produk Kombinasi Minyak Ikan dan Minyak Habbatussauda.
Terima kasih penulis ucapkan kepada Dr. Sugeng Heri Suseno, S.Pi, MSi dan Dr. Ir. Nurjanah, MS selaku pembimbing. Dr. Ir. Ruddy Suwandi, M.S, M. Phil selaku Ketua Departemen Teknologi Hasil Perairan dan Dr. Ir. Agoes Mardiono Jacoeb, Dipl Biol selaku Ketua Program Studi Teknologi Hasil Perairan.
Terima kasih juga penulis sampaikan kepada Alm. Ayahanda, Mama dan keluarga tercinta serta Antharest atas segala doa dan dukungannya. Penulis juga berterima kasih kepada geng minyak ikan (Mashita, Yoshiara, Saras, Ayu, dan Sri), THP 46, THP 47, THP 48, kontrakkan D1-D2, ex-kostmate Candra, my future penthouse mate Marisky, Eceu Rika atas
peminjaman fasilitas wi-fi nya, teman cacat sepanjang masa Wenny Tiara Andhika Rahayu, my lovely master Dyan Aiy & Niken Eonni, Sistar 91, Goguma Indonesia, dan my idol couple “YongSeo”. I love you all. Semoga
karya ilmiah ini bermanfaat.
Bogor, Juni 2013
DAFTAR ISI
DAFTAR ISI ... i
DAFTAR TABEL ... ii
DAFTAR GAMBAR ... ii
DAFTAR LAMPIRAN ... ii
Latar Belakang ... 1
Perumusan Masalah ... 1
Tujuan Penelitian ... 2
Manfaat Penelitian ... 2
Ruang Lingkup Penelitian ... 2
METODE ... 2
Bahan... 2
Alat ... 3
Prosedur Penelitian... 3
Analisis asam lemak dengan Gas Chromatography ... 3
Uji Aktivitas Antioksidan ... 3
Uji Free Fatty Acid (FFA) ... 4
Uji Bilangan Peroksida ... 4
Uji Bilangan Anisidin ... 4
Uji Stabilitas ... 4
Uji Organoleptik... 5
HASIL DAN PEMBAHASAN ... 5
KESIMPULAN DAN SARAN ... 14
Kesimpulan ... 14
Saran ... 15
DAFTAR PUSTAKA ... 15
LAMPIRAN ... 17
ii
DAFTAR TABEL
1 Profil asam lemak minyak ikan dan minyak habbatussauda ... 6
DAFTAR GAMBAR
1 Minyak ikan dan minyak habbatussauda ... 52 Aktivitas antioksidan ... 8
3 Diagram batang free fatty acid value ... 9
4 Reaksi hidrolisis pada lemak ... 9
5 Diagram batang bilangan peroksida ... 10
6 Diagram batang bilangan anisidin ... 11
7 Grafik kestabilan kadar asam lemak bebas ... 12
8 Diagram batang mean parameter warna ... 13
DAFTAR LAMPIRAN
1 Tabel hasil uji Kruskal-Wallis ... 17PENDAHULUAN
Latar Belakang
Peningkatan kualitas sumberdaya manusia dan kesehatan merupakan dua masalah pokok di negara-negara berkembang, misalnya Indonesia. Status gizi yang kurang baik menyebabkan status kesehatan dan kualitas sumberdaya manusia yang rendah. Sementara itu perubahan pola hidup manusia menimbulkan akibat negatif terhadap kesehatan (Astawan 1998). Gangguan kesehatan yang erat kaitannya dengan perubahan pola hidup manusia, diantaranya yaitu penyakit jantung koroner, tekanan darah tinggi, diabetes, stroke, dan kegemukan (obesitas). Penyakit ini merupakan penyakit yang beresiko tinggi.
Minyak ikan merupakan salah satu sumber yang kaya akan asam lemak omega-3, asam lemak omega-3 terutama asam eikosapentaenoat (EPA) dan asam dokosaheksaenoat (DHA) yang sangat bermanfaat bagi kesehatan, antara lain dapat mencegah penyakit kardiovaskular dan bagian kadar kolesterol darah. Kekurangan asam lemak ini dapat menimbulkan perkembangan psikomotorik menjadi terlambat, dan apabila hal ini terjadi pada masa bayi prenatal akan berlangsung terus sampai dewasa (Astawan 1998). Minyak ikan yang kaya akan asam lemak tak jenuh (PUFA) menyebabkan minyak ikan tersebut mudah teroksidasi dan menimbulkan bau tengik karena kestabilan oksidasi yang rendah.
Minyak habbatussauda yang berasal dari tanaman jintan hitam memiliki khasiat untuk mengobati berbagai penyakit yaitu diabetes, asma, menurunkan kolesterol, dan meningkatkan kinerja jantung (Aldi dan Suhatri 2011). Hadits Riwayat Muslim, Rasulullah SAW bersabda: “Tidak ada satupun penyakit melainkan di dalam habbatussauda terdapat kesembuhan baginya, kecuali kematian.” Menurut Hutapea dalam Rahmi (2011), tanaman jintan hitam memiliki kandungan antioksidan yang cukup tinggi. Kandungan ekstrak minyak jintan hitam antara lain minyak volatil, protein, asam amino, alkaloid, asam anorganik, tanin, resin, metarbin, melatin, vitamin yaitu tiamin, niasin, piridoksin, dan asam folat. Biji dan daun jintan hitam mengandung saponin dan polifenol. Kandungan biji jintan hitam antara lain: thymoquinone, thymohydroquinone, dithymoquinone, thymol, carvacrol, nigellicine, nigellidine, nigellimine-N-oxide dan alpha-hedrin.
Kandungan antioksidan yang tinggi pada minyak habbatussauda dapat diformulasikan dengan minyak ikan yang banyak mengandung asam lemak tak jenuh sehingga tidak mudah teroksidasi. Tujuan dari penelitian ini adalah untuk menentukan karakteristik dan stabilitas produk kombinasi antara minyak ikan dan minyak habbatussauda yang dapat menghasilkan produk kesehatan yang stabil.
Perumusan Masalah
2
minyak ikan dan habbatussauda sebagai suatu produk kombinasi harus diketahui karakteristik dan kestabilannya.
Tujuan Penelitian
1. Menentukan karakteristik produk kombinasi minyak ikan dan habbatussauda
2. Menentukan stabilitas produk kombinasi minyak ikan dan habbatussauda
Manfaat Penelitian
Penelitian ini diharapkan dapat memberikan produk kesehatan berupa produk kombinasi minyak ikan dan minyak habbatussauda dengan karakteristik dan kestabilan yang baik.
Ruang Lingkup Penelitian
Ruang lingkup penelitian ini adalah pencampuran antara minyak ikan dan minyak habbatussauda, analisis profil asam lemak, analisis asam lemak bebas, analisis bilangan peroksida, analisis bilangan anisidin, analisis aktivitas antioksidan, analisis data, serta penulisan laporan.
METODE
Penelitian ini dilaksanakan pada bulan Januari 2013 sampai dengan Mei 2013. Pengujian kadar asam lemak bebas (free fatty acid value) dan bilangan peroksida dilakukan di Laboratorium Biokimia Hasil Perairan, Departemen Teknologi Hasil Perairan, Fakultas Perikanan dan Ilmu Kelautan, IPB. Pengujian kestabilan minyak ikan dilakukan di Laboratorium Bioteknologi Hasil Perairan, Departemen Teknologi Hasil Perairan, Fakultas Perikanan dan Ilmu Kelautan, IPB. Analisis bilangan anisidin dilakukan di Laboratorium Terpadu Fakultas Kedokteran Hewan, IPB. Analisis asam lemak dengan gas chromatography
dilakukan di Laboratorium Kimia Terpadu, Sekolah Pascasarjana, IPB. Pengujian aktivitas antioksidan dilakukan di Pusat Studi Biofarmaka, IPB.
Bahan
larutan isooktan dan p-anisidin. Vitamin C, larutan DPPH, dan etanol adalah bahan yang digunakan dalam uji aktivitas antioksidan dan bahan untuk analisis profil asam lemak.
Alat
Alat yang digunakan uji kadar asam lemak bebas (free fatty acid value)
dan kestabilan adalah oven, statif, biuret, kompor listrik, alumunium foil, erlenmeyer, pipet tetes, pipet volumetrik, timbangan analitik, dan penangas air. Alat yang digunakan untuk uji bilangan peroksida adalah erlenmeyer, gelas ukur, pipet volumetrik, timbangan analitik, statif, biuret, dan alumunium foil. Alat yang digunakan untuk analisis bilangan anisidin adalah spektrofotometer dengan panjang gelombang 350 nm, plate, mikro pipet, erlenmeyer, tabung reaksi,
timbangan analitik, pipet volumetrik, dan alumunium foil. Alat yang digunakan untuk uji aktivitas antioksidan adalah tabung reaksi, mikro pipet, timbangan analitik, plate, dan spektrometer dengan panjang gelombang 515 nm. Analisis
profil asam lemak menggunakan alat gas chromatography.
Prosedur Penelitian Analisis asam lemak dengan Gas Chromatography
Sebanyak 20-40 mg contoh lemak atau minyak dalam tabung bertutup teflon ditambahkan dengan 1 mL NaOH dalam metanol, kemudian dipanaskan dalam
penangas air selama 20 menit. Selanjutnya sebanyak 2 mL BF3 20% serta 5 mg/mL standar internal ditambahkan ke dalam campuran, lalu campuran dipanaskan lagi selama 20 menit. Campuran didinginkan, kemudian ditambahkan 2 mL NaCl jenuh serta 1 mL isooktan, lalu campuran dikocok dengan baik. Lapisan isooktan yang terbentuk dipindahkan dengan bantuan pipet tetes ke dalam tabung berisi sekitar 0,1 gram Na2SO4 anhidrat, lalu dibiarkan 15 menit. Fasa cair yang terbentuk dipisahkan, sedangkan fasa minyak yang terbentuk diinjeksikan sebanyak 1 μL, setelah sebelumnya dilakukan penginjeksian 1 μL campuran standar Supelco 37 Component FAME Mix. Waktu retensi dan puncak masing-masing komponen diukur lalu dibandingkan dengan waktu retensi standar untuk mendapatkan informasi mengenai jenis dan komponen-komponen dalam contoh.
Uji Aktivitas Antioksidan
Sebanyak 100 µL sampel ditambahkan etanol dengan perbandingan 1:1, setelah itu ditambahkan dengan 100 µL larutan DPPH dan diinkubasi selama 30 menit pada suhu ruang. Absorbansi DPPH diukur dengan spektrometer sinar tampak pada panjang gelombang 515 nm. Kemampuan antioksidan diukur sebagai penurunan serapan larutan DPPH akibat adanya penambahan sampel. Nilai serapan larutan DPPH sebelum dan sesudah penambahan ekstrak tersebut dihitung sebagai persen inhibisi (% inhibisi) dengan rumus sebagai berikut:
% Inhibisi = (A�������−A������)
4
Hasil perhitungan dimasukkan ke dalam persamaan regresi dengan konsentrasi ekstrak (mM) sebagai absis (sumbu X) dan nilai % inhibisi (antioksidan) sebagai ordinatnya (sumbu Y), dimana nilai Y = aX + b.
Uji Free Fatty Acid (FFA)
Sebanyak 1 gram sampel dimasukkan dalam erlenmeyer 250 mL ditambah 25 mL alkohol netral. Campuran tersebut dipanaskan diatas kompor listrik sampai mendidih selama lebih kurang 10 menit sambil diaduk. Larutan kemudian dititrasi dengan KOH 0,1N menggunakan indikator phenolptalein sampai terbentuk warna merah jambu yang persisten selama 10 detik. Nilai kadar asam lemak bebas dihitung dengan rumus sebagai berikut:
Uji Bilangan Peroksida
Analisis bilangan peroksida dilakukan dengan menimbang 5 gram sampel dalam Erlenmeyer 250 mL dengan menambahkan 30 mL larutan asam asetat glasial dan kloroform (3:2). Larutan KI jenuh sebanyak 0,5 mL ditambahkan ke dalam sampel tersebut, diikuti dengan penambahan aquades sebanyak 30 mL. Langkah selanjutnya menambahkan 0,5 mL larutan indikator kanji 1% yang akan merubah warna larutan menjadi biru pekat atau hitam, lalu titrasi dengan Na2SO3 0,1N. Penentuan bilangan peroksida dihitung dengan rumus sebagai berikut:
Uji Bilangan Anisidin
Sebanyak 2 gram sampel ditambah dengan 25 mL isooktan dan diukur absorbannya (Ab) pada 350 nm dengan spektrofotometer UV-VIS. Kemudian sebanyak 5 mL larutan tersebut dipipet ke dalam tabung dan ditambahkan 1 mL p-anisidin 0,25% dalam asam asetat glasial, kemudian selanjutnya tabung ditutup, dikocok, dan dibiarkan pada tempat gelap selama 10 menit dan diukur pada panjang gelombang 350 nm sebagai absorban larutan (As). Penentuan bilangan anisidin dihitung menggunakan rumus:
Uji Stabilitas
Uji stabilitas menggunakan metode schaal (Eastman 2010) yang biasa digunakan untuk menguji kestabilan oksidatif lemak atau makanan yang mengandung lemak. Sampel minyak ditempatkan dalam botol dan disimpan pada suhu antara 40°C, lalu sampel dihitung kadar FFA selama 9 hari secara berkala dengan rentang waktu 48 jam.
% FFA = (����������������������) (������������1000)
Bilangan Peroksida = (��Na2SO3�������������Na2SO3�1000)
Uji Organoleptik
Uji organoleptik dilakukan terhadap produk kombinasi minyak ikan dan minyak habbatussauda. Jenis uji yang dilakukan adalah uji tingkat kesukaan dengan skala penilaian 1 sampai 9. Panelis yang digunakan adalah panelis semi terlatih sebanyak 30 orang pada perbedaan formulasi antara minyak ikan dan minyak habbatussauda. Panelis semi terlatih tersebut memberikan penilaian tehadap warna, rasa, dan aroma pada lembar penilaian uji organoleptik.
HASIL DAN PEMBAHASAN
Minyak ikan yang digunakan pada penelitian ini merupakan minyak ikan lemuru yang berasal dari hasil samping pabrik pengalengan di Banyuwangi, Jawa Timur, dan memiliki ciri fisik berwarna kuning keemasan, sedangkan minyak habbatussauda yang digunakan merupakan produk komersial dengan merk “Habasyah” yang didapat dari Pasar Jatinegara, Jakarta Timur, dengan ciri fisik berwarna gelap. Minyak ikan dan minyak habbatussauda yang digunakan dalam penelitian ini dapat dilihat pada Gambar 1a dan 1b.
(a) (b)
Gambar 1 (a) Minyak ikan (b) Minyak habbatussauda
Minyak ikan dan minyak habbatussauda dicampurkan dengan formulasi perbandingan 1:1, 3:1, 5:1, dan 7:1 dan dilakukan uji karakteristik dan stabilitas dari produk kombinasi tersebut.
Menurut Syakiroh (2012), warna akibat oksidasi dan degradasi komponen kimia yang terdapat pada minyak diantaranya warna gelap yang disebabkan oleh proses oksidasi terhadap tokoferol (vitamin E). Warna gelap ini dapat terjadi selama proses pengolahan dan penyimpanan, yang disebabkan beberapa faktor yaitu suhu pemanasan, pengepresan bahan, ekstraksi minyak, kandungan logam, dan oksidasi terhadap fraksi tidak tersabunkan dalam minyak. Warna kuning pada minyak disebabkan adanya kandungan karoten, yaitu zat warna alamiah yang dapat terjadi akibat proses absorbsi dalam minyak tidak jenuh.
Analisis Profil Asam Lemak Bahan Baku
Analisis profil asam lemak dari minyak ikan dan minyak habbatussauda dilakukan dengan menggunakan gas chromatography untuk mengetahui
6
dan asam lemak tak jenuh ganda (Polyunsaturated Fatty Acid/PUFA) yang memiliki dua atau lebih ikatan rangkap (Okuzami dan Tateo 2000). Hasil profil asam lemak dapat dilihat pada Tabel 1.
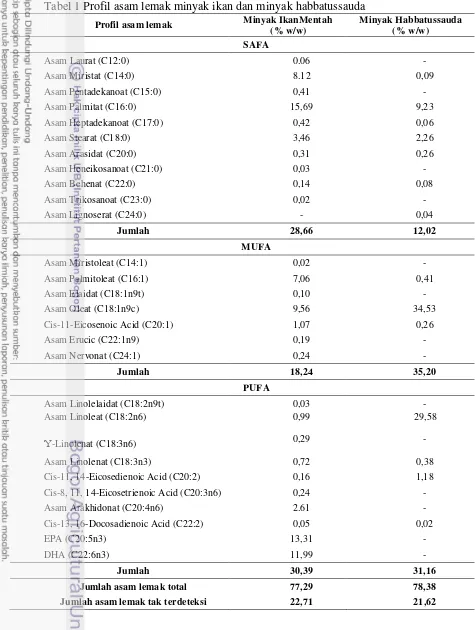
Tabel 1 Profil asam lemak minyak ikan dan minyak habbatussauda
Profil asam lemak Minyak IkanMentah
(% w/w)
Asam Pentadekanoat (C15:0) 0,41 -
Asam Palmitat (C16:0) 15,69 9,23
Asam Heptadekanoat (C17:0) 0,42 0,06
Asam Stearat (C18:0) 3,46 2,26
Asam Arasidat (C20:0) 0,31 0,26
Asam Heneikosanoat (C21:0) 0,03 -
Asam Behenat (C22:0) 0,14 0,08
Asam Palmitoleat (C16:1) 7,06 0,41
Asam Elaidat (C18:1n9t) 0,10 -
Asam Oleat (C18:1n9c) 9,56 34,53
Cis-11-Eicosenoic Acid (C20:1) 1,07 0,26
Asam Erucic (C22:1n9) 0,19 -
Asam Nervonat (C24:1) 0,24 -
Jumlah 18,24 35,20
PUFA
Asam Linolelaidat (C18:2n9t) 0,03 -
Asam Linoleat (C18:2n6) 0,99 29,58
Ƴ-Linolenat (C18:3n6) 0,29 -
Asam Linolenat (C18:3n3) 0,72 0,38
Cis-11, 14-Eicosedienoic Acid (C20:2) 0,16 1,18
Cis-8, 11, 14-Eicosetrienoic Acid (C20:3n6) 0,24 -
Asam Arakhidonat (C20:4n6) 2.61 -
Cis-13, 16-Docosadienoic Acid (C22:2) 0,05 0,02
EPA (C20:5n3) 13,31 -
DHA (C22:6n3) 11,99 -
Jumlah 30,39 31,16
Jumlah asam lemak total 77,29 78,38
Tabel 1 menunjukkan bahwa kandungan asam lemak terbanyak dalam minyak ikan yaitu EPA dan DHA dengan persentasi 13,31% dan 11,99%, sedangkan kandungan asam lemak terbanyak yang terdapat dalam minyak habbatussauda adalah asam oleat dan asam linoleat dengan persentasi 34,53% dan 29,58%.
Pada minyak ikan, asam lemak SAFA (Saturated Fatty Acid) yang
terdeteksi sebanyak 10 jenis, asam lemak MUFA (Monounsaturated Fatty Acid)
sebanyak 7 jenis, dan asam lemak PUFA (Polyunsaturated Fatty Acid) sebanyak 10 jenis. Pada minyak habbatussauda, asam lemak jenis SAFA yang terdeksi sebanyak 6 jenis, asam lemak MUFA sebanyak 3 jenis, asam lemak PUFA sebanyak 4 jenis, dan yang tidak terdeteksi sebanyak 14 jenis.
Minyak habbatusauda banyak mengandung asam lemak oleat dan linoleat, hal tersebut sesuai dengan pernyataan Mardiana (2011) bahwa asam lemak linoleat merupakan asam lemak yang banyak terdapat di alam dan secara khusus banyak dikandung pada seed oil. Asam lemak ini dihasilkan di dalam tubuh
tumbuhan oleh desaturasi Δ12 dan Δ15 asam oleat. Asam lemak ini dapat
diperoleh dari daun tumbuhan dan komponen kecil dari minyak biji. Asam oleat
merupakan produk desaturasi Δ9 asam stearat dan diproduksi pada tumbuhan,
hewan, dan bakteri. Asam oleat merupakan asam paling umum dan merupakan prekursor untuk diproduksi sebagian besar PUFA. Apabila tubuh kekurangan asam linoleat dapat menimbulkan gangguan metabolisme yang menyebabkan
pertumbuhan terhambat, dermatitis, dan gangguan reproduksi (Widjaja dan Utomo 2007). Tubuh apabila kekurangan asam oleat dapat
menyebabkan terjadinya gangguan penglihatan, menurunnya daya ingat serta gangguan pertumbuhan sel otak pada janin dan bayi karena asam oleat memiliki peranan sebagai media pelarut vitamin A, D, E, dan K (Latyshev et al. 2009).
Minyak ikan banyak mengandung asam lemak omega-3 yaitu EPA dan DHA. Hal tersebut diduga karena adanya pengaruh terhadap pakan ikan, asam lemak omega-3 bukanlah merupakan hasil metabolisme pada ikan itu sendiri, tetapi merupakan bahan yang didapat langsung dari pakannya. Sumber pakan alami yang potensial mengandung asam lemak omega-3 adalah phytoplankton, zooplankton, seaweed, oyster, chepapoda, dan shellfish (Mardiana 2011). EPA
banyak berperan dalam penurunan risiko serangan jantung, sedangkan DHA memberikan peranan penting untuk menjaga keseimbangan eikosanoid. DHA berperan penting dalam otak dan retina pada tiga bulan terakhir kehamilan dan tahun pertama pertumbuhan (Syakiroh 2012). EPA dan DHA merupakan komponen utama dari fosfolipid membran sel dan merupakan high unsaturated fatty acid (HUFA) yang berguna untuk sistem saraf pusat (Wu et al. 2010).
Aktivitas Antioksidan Bahan Baku
Uji aktivitas antioksidan untuk menguji potensi aktivitas antioksidan dari minyak habbatussauda yang dicampurkan dengan minyak ikan. Antioksidan
merupakan zat yang dapat menunda atau mencegah oksidasi lipid (Schuler 1990 dalam Amelia 2006). Fardinatri (2007) mengatakan bahwa
8
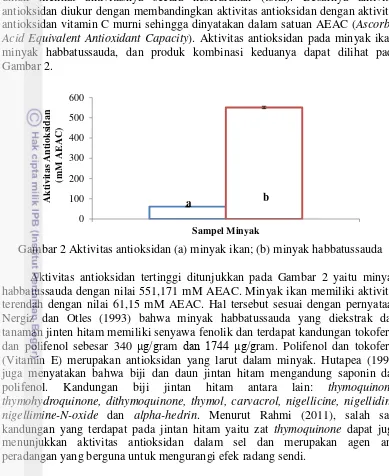
untuk melihat aktivitasnya secara keseluruhan (total). Besarnya aktivitas antioksidan diukur dengan membandingkan aktivitas antioksidan dengan aktivitas antioksidan vitamin C murni sehingga dinyatakan dalam satuan AEAC (Ascorbic Acid Equivalent Antioxidant Capacity). Aktivitas antioksidan pada minyak ikan, minyak habbatussauda, dan produk kombinasi keduanya dapat dilihat pada Gambar 2.
Gambar 2 Aktivitas antioksidan (a) minyak ikan; (b) minyak habbatussauda Aktivitas antioksidan tertinggi ditunjukkan pada Gambar 2 yaitu minyak habbatussauda dengan nilai 551,171 mM AEAC. Minyak ikan memiliki aktivitas terendah dengan nilai 61,15 mM AEAC. Hal tersebut sesuai dengan pernyataan Nergiz dan Otles (1993) bahwa minyak habbatussauda yang diekstrak dari tanaman jinten hitam memiliki senyawa fenolik dan terdapat kandungan tokoferol dan polifenol sebesar 340 μg/gram dan 1744 μg/gram. Polifenol dan tokoferol (Vitamin E) merupakan antioksidan yang larut dalam minyak. Hutapea (1994) juga menyatakan bahwa biji dan daun jintan hitam mengandung saponin dan polifenol. Kandungan biji jintan hitam antara lain: thymoquinone, thymohydroquinone, dithymoquinone, thymol, carvacrol, nigellicine, nigellidine, nigellimine-N-oxide dan alpha-hedrin. Menurut Rahmi (2011), salah satu
kandungan yang terdapat pada jintan hitam yaitu zat thymoquinone dapat juga menunjukkan aktivitas antioksidan dalam sel dan merupakan agen anti peradangan yang berguna untuk mengurangi efek radang sendi.
Kadar Asam Lemak Bebas (Free Fatty Acid Value)
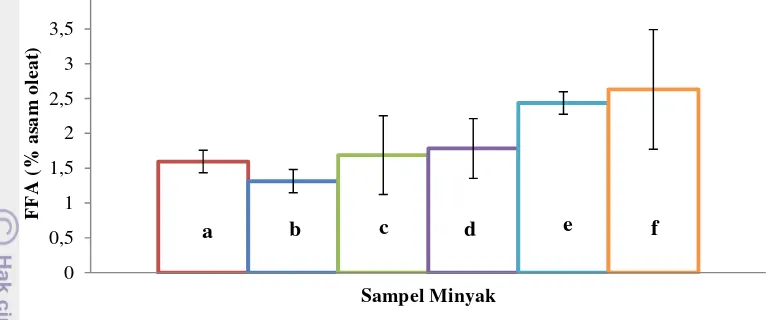
Gambar 3 Diagram batang free fatty acid value (a) minyak ikan; (b) minyak habbatussauda; (c) formulasi 1:1; (d) formulasi 3:1; (e) formulasi 5:1; (f) formulasi 7:1
Gambar 3 menunjukkan bahwa kadar asam lemak bebas pada minyak ikan lebih besar dengan 1,59% dibandingkan dengan kadar asam lemak bebas minyak habbatussauda sebesar 1,31%. Kadar asam lemak bebas untuk produk kombinasi keduanya yang memiliki nilai FFA terendah yaitu produk dengan formulasi 1:1 sebesar 1,68% sedangkan nilai FFA tertinggi yaitu formulasi 7:1 sebesar 2,63%. Nilai kadar asam lemak bebas tersebut memenuhi standar mutu minyak ikan yang baik, menurut Estiasih et al. (2005) nilai asam lemak bebas pada minyak harus berkisar antara 1-7%.
Asam lemak bebas dihasilkan bila terjadi reaksi hidrolisis yang mengubah
lemak dan minyak menjadi asam-asam lemak bebas dan gliserol (Herlina dan Ginting 2002). Peningkatan hidrolisis terhadap minyak akan
meningkatkan jumlah asam lemak bebas yang dihasilkan. Reaksi hidrolisis pada lemak dapat dilihat pada gambar berikut.
Gambar 4 Reaksi hidrolisis pada lemak
Sumber: Herlina dan Ginting (2002)
Asam lemak bebas yang dihasilkan adalah dari jenis asam lemak tidak jenuh, maka ini akan memperbesar terjadinya oksidasi bila tersedia cukup oksigen (Ahmadi 2009). Penyimpanan minyak yang kurang baik dan proses penelitian yang memungkinkan minyak berinteraksi dengan oksigen dapat menyebabkan kadar asam lemak pada minyak tersebut meningkat. Gunawan et al. (2003)
menyatakan bahwa terdapatnya enzim lipase pada lemak atau minyak juga dapat menghidrolisis trigliserida sehingga menghasilkan asam lemak bebas dan gliserol.
10
Hal tersebut sesuai dengan Kusnandar (2010) yang menyatakan bahwa oksidasi asam lemak sangat tergantung pada jumlah ikatan rangkapnya, selain itu dipengaruhi juga oleh suhu, konsentrasi oksigen, logam, aktivitas air, prooksidan, antioksidan, dan katalis. Asam lemak tidak jenuh jamak (MUFA) yang terdapat banyak dalam minyak ikan memiliki jumlah ikatan rangkap yang panjang sehingga mudah untuk teroksidasi, apabila dibandingkan minyak habbatussauda yang memiliki asam lemak tidak jenuh tunggal (PUFA).
Bilangan Peroksida
Menurut AOAC dalam Rasyid (2003), bilangan peroksida didefinisikan
sebagai jumlah peroksida dalam miliekuivalen oksigen aktif yang dikandung dalam 1000 gram senyawa.Bilangan peroksida pada minyak ikan, minyak habbatussauda, dan formulasi keduanya dapat dilihat pada Gambar 5.
Gambar 5 menunjukkan bahwa bilangan peroksida minyak habbatussauda lebih rendah dengan nilai 22,67 meq/kg apabila dibandingkan dengan minyak ikan dengan nilai 24,67 meq/kg dan diantara semua produk kombinasi, yang memiliki nilai bilangan peroksida terendah yaitu produk dengan formulasi 1:1 sebesar 26,67 meq/kg sedangkan produk kombinasi dengan bilangan peroksida tertinggi adalah produk dengan formulasi 3:1 dan 7:1 sebesar 32 meq/kg. Hasil tersebut tidak memenuhi standar bilangan peroksida minyak ikan yang baik yaitu sebesar 3-20 meq/kg (Estiasih et al. 2005).
Gambar 5 Diagram batang bilangan peroksida (a) minyak ikan; (b) minyak habbatussauda; (c) formulasi 1:1; (d) formulasi 3:1; (e) formulasi 5:1; (f) formulasi 7:1
Bilangan oksidasi yang terdapat dalam minyak terjadi akibat dari asam lemak yang mengalami reaksi oksidasi. Stabilitas oksidasi asam lemak sangat tergantung pada jumlah ikatan rangkapnya, selain itu dipengaruhi juga oleh suhu, konsentrasi oksigen, logam, aktivitas air, prooksidan, antioksidan, dan katalis. Reaksi oksidasi terjadi melalui beberapa tahap, yaitu tahap inisiasi, tahap propagasi, dan terminasi. Radikal bebas yang terbentuk pada tahap awal reaksi (tahap inisiasi) dapat bereaksi dengan oksigen dan menghasilkan senyawa peroksida (Kusnandar 2010).
Gunawan et al. (2003) juga menyatakan bahwa adanya kontak langsung dengan udara dan suhu tinggi mengakibatkan asam lemak tidak jenuh terurai.
Rantai karbon dalam ikatan rangkap terputus sehingga asam lemak bebas bertambah. Rantai karbon yang terputus berikatan dengan oksigen sehingga peroksida minyak juga bertambah.
Penambahan minyak habbatussauda terhadap minyak ikan memberikan pengaruh yang tidak terlalu berbeda nyata terhadap bilangan peroksida, akan tetapi penambahan minyak habbatussauda yang terbanyak terhadap minyak ikan memiliki bilangan peroksida terendah. Hal tersebut disebabkan karena minyak habbatussauda memiliki fungsi sebagai antioksidan. Antioksidan tersebut dapat menghalangi terjadinya pembentukan radikal bebas yang terjadi pada tahap inisiasi dengan menyediakan hidrogen kepada radikal bebas sehingga pembentukan radikal bebas dapat direduksi. Menurut Chen dan Tappel (1996)
dalam Hartoyo dan Astuti (2002), gabungan antara antioksidan larut air dan larut
lemak akan lebih efektif dibandingkan antioksidan tunggal, karena gabungan kedua antioksidan tersebut akan mampu menangkal radikal bebas dalam fase cairan dan fase lemak sekaligus.
Bilangan Anisidin
Bilangan anisidin adalah bilangan yang memperkirakan adanya senyawa-senyawa hasil dekomposisi hidroperoksida yang disebabkan oleh oksidasi lanjut. Bilangan anisidin minyak ikan, minyak habbatussauda, dan produk kombinasi keduanya dapat dilihat pada Gambar 6.
Gambar 6 Diagram batang bilangan anisidin (a) minyak ikan; (b) minyak habbatussauda; (c) formulasi 1:1; (d) formulasi 3:1; (e) formulasi 5:1; (f) formulasi 7:1
Gambar 6 menunjukkan bahwa bilangan anisidin yang memiliki nilai terendah pada sampel produk kombinasi dengan formulasi 1:1 sebesar 13,65 meq/kg dan nilai tertinggi pada formulasi 3:1 sebesar 14,75 meq/kg. Minyak ikan dan minyak habbatussauda masing-masing memiliki bilangan anisidin sebesar 12,68 meq/kg dan 9,25 meq/kg. Hasil tersebut memenuhi standar bilangan anisidin yang memiliki nilai maksimum sebesar 60 meq/kg (Estiasih et al. 2005).
Penambahan habbatussauda terhadap minyak ikan tidak memberikan nilai yang berbeda nyata terhadap nilai anisidin, akan tetapi penambahan minyak habbatussauda yang terbanyak terhadap minyak ikan yang memiliki nilai anisidin terendah. Bilangan anisidin merupakan senyawa hasil dekomposisi bilangan peroksida. Hasil anisidin lebih rendah dibandingkan dengan bilangan peroksida diduga karena menurut pernyataan Kusnandar (2010), pembentukan peroksida
12
sebagai senyawa antara dalam oksidasi lemak akan meningkat sampai titik tertentu untuk kemudian menurun kembali dan penurunan ini terjadi karena peroksida yang terbentuk akan terdekomposisi menjadi senyawa dengan berat molekul yang lebih kecil, terutama golongan aldehid dan dinyatakan dengan bilangan anisidin.
Uji Kestabilan
Uji kestabilan dilakukan dengan metode schaal yaitu dengan penyimpanan dalam oven pada suhu 40°C selama 9 hari (Pokorny et al. 2003). Pada hari ke-0
dan ke-1 setiap sampel dihitung kadar asam lemak bebasnya untuk mengetahui kestabilan tiap sampel, setelah hari ke-1 setiap rentang waktu 48 jam tiap sampel dihitung lagi kadar asam lemak bebasnya. Gambar 7 menunjukkan grafik kestabilan dari kadar asam lemak bebas minyak.
Gambar 7 Grafik kestabilan kadar asam lemak bebas minyak ikan; minyak habbatussauda; formulasi 1:1; formulasi 3:1; formulasi 5:1; formulasi 7:1
Penambahan minyak habbatussauda terhadap minyak ikan memberikan pengaruh yang berbeda nyata terhadap kestabilan minyak. Kestabilan yang paling baik dapat dilihat pada hari ke-9 dengan nilai FFA terendah yaitu produk kombinasi 1:1 dan 3:1. Hal ini diduga karena banyaknya penambahan minyak habbatussauda sebagai antioksidan alami terhadap minyak ikan, yang dapat menghalangi terjadinya oksidasi. Antioksidan dapat menghalangi terjadinya pembentukan radikal bebas yang terjadi pada tahap inisiasi dengan menyediakan hidrogen kepada radikal bebas sehingga pembentukan radikal bebas dapat direduksi. Menurut Chen dan Tappel (1996) dalam Hartoyo dan Astuti (2002), gabungan antara antioksidan larut air dan larut lemak akan lebihefektif dibandingkan antioksidan tunggal, karena gabungan kedua antioksidan tersebut akan mampu menangkal radikal bebas dalam fase cairan dan fase lemak sekaligus.
Uji Organoleptik
Uji organoleptik dilakukan untuk melihat respon konsumen terhadap sifat fisik produk kombinasi dari minyak ikan dan minyak habbatussauda. Produk kombinasi minyak ikan dan minyak habbatussauda memiliki formulasi 1:1,
formulasi 3:1, formulasi 5:1, dan formulasi 7:1, untuk mengetahui pengaruh perbedaan formulasi terhadap karakteristik minyak maka dilakukan uji Kruskal-Wallis dengan hipotesa sebagai berikut:
Ho = Perbedaan formulasi memberikan pengaruh terhadap karakteristik minyak Hi = Perbedaan formulasi tidak memberikan pengaruh terhadap karakteristik
minyak
Berdasarkan hasil uji Kruskal-Wallis, parameter warna memiliki nilai P<0,05 yang menunjukkan bahwa perbedaan formulasi mempengaruhi karakteristik warna pada minyak. Sedangkan untuk parameter rasa dan aroma memiliki nilai P>0,05 yang berarti bahwa perbedaan formulasi tidak mempengaruhi karakteristik rasa dan aroma pada minyak.
a) Warna
Perbedaan formulasi mempengaruhi karakteristik warna pada minyak, oleh karena itu diperlukan uji lanjut untuk mengetahui perlakuan mana yang paling disukai oleh panelis. Hasil uji organoleptik pada parameter warna dapat dilihat pada Gambar 8.
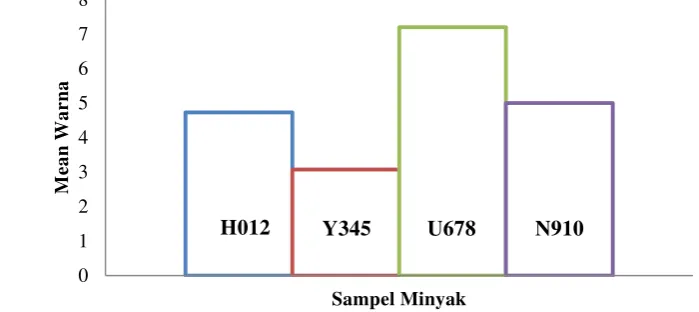
Gambar 8 menunjukkan bahwa minyak dengan kode U678 yaitu formulasi 7:1 paling disukai panelis dengan nilai sebesar 7,20 sedangkan minyak dengan kode Y345 yang merupakan formulasi 1:1 paling tidak disukai oleh panelis. Hal tersebut diduga karena minyak dengan formulasi 1:1 berwarna lebih gelap dibandingkan minyak dengan formulasi 7:1 yang berwarna kuning. Pada formulasi 1:1 perbandingan minyak ikan dengan minyak habbatussauda sepadan sehingga warna gelap pada minyak habbatussauda mendominasi dibandingkan warna kuning keemasan dari minyak ikan. Sedangkan pada formulasi 1:7 dengan perbandingan minyak ikan yang lebih banyak dibandingkan dengan minyak habbatussauda menyebabkan warna kuning keemasan lebih mendominasi dibandingkan warna gelap dari minyak habbatussauda.
Gambar 8 Diagram batang mean parameter warna (H012) formulasi 3:1;
(Y345) formulasi 1:1; (U678) formulasi 7:1; (N910) formulasi 5:1 Menurut Syakiroh (2012) warna pada minyak ikan dan minyak habbatussauda dihasilkan dari oksidasi dan degradasi komponen kimia yang
14
terdapat dalam minyak. Minyak ikan yang memiliki sifat fisik warna kuning disebabkan banyaknya kandungan karoten yaitu zat warna alamiah yang dapat terjadi akibat proses absorbsi dalam lemak atau minyak tidak jenuh, sedangkan minyak habbatussaudah yang memiliki sifat fisik warna gelap dikarenakan proses oksidasi terhadap tokoferol (Vitamin E).
b) Rasa
Secara umum ada 4 citarasa utama yaitu manis, asin, asam dan pahit. Rasa digunakan untuk menerangkan mutu dari kesan yang ditimbulkan oleh senyawa-senyawa yang ada dalam bahan makanan atau minuman. Parameter rasa memiliki nilai P>0,05 yang berarti bahwa perbedaan formulasi tidak memberikan pengaruh terhadap parameter rasa (Lampiran 1). Rasa pada minyak ikan memiliki rasa khas minyak ikan, seperti rasa amis ikan, sedangkan pada minyak habbatussauda memiliki kandungan minyak atsiri dan nigelline yang menyebabkan minyak habbatussauda memiliki rasa sedikit pahit (Rahmi 2011).
c) Aroma
Aroma merupakan sensasi atau kesan yang diterima lewat organ olfaktori ketika mencium atau menghirup senyawa-senyawa volatil. Parameter aroma memiliki nilai P>0,05 yang berarti bahwa perbedaan formulasi tidak memberikan pengaruh terhadap parameter aroma (Lampiran 1). Aroma yang dihasilkan dari minyak ikan dan minyak habbatussauda merupakan hasil dari reaksi hidrolisa. Herlina dan Ginting (2002) menyatakan bahwa reaksi hidrolisa dapat menimbulkan bau tengik pada minyak atau lemak dan produk turunannya. Reaksi tingkat lanjut mengakibatkan terurainya asam lemak menjadi aldehid, keton, alkohol, aromatik, dan hidrokarbon. Reaksi oksidasi minyak dan lemak lebih khusus kepada asam lemak tidak jenuh. Asam lemak tak jenuh semakin reaktif terhadap oksidasi dengan bertambahnya ikatan rangkap pada rantai molekul. Adanya kandungan asam lemak tak jenuh pada minyak ikan dan minyak habbatussauda maka aroma yang dihasilkan relatif sama pada semua sampel.
KESIMPULAN DAN SARAN
Kesimpulan
Saran
Saran untuk penelitian ini adalah dapat dilakukan penelitian lanjutan untuk meningkatkan kualitas dari produk kombinasi dengan formulasi terbaik menjadi
food grade dan diuji umur simpannya, serta dapat menggunakan sumber antioksidan alami yang lainnya, seperti ekstrak teh hijau, daun sirih, mikroalga untuk menambah variasi produk.
DAFTAR PUSTAKA
Ahmadi K. 2009. Pemurnian minyak ikan hasil samping penepungan ikan lemuru (Sardinella longiceps) menggunakan zeolit alam teraktivasi. UPN Jatim Repository 1(1): 93-102.
Aldi Y, Suhatri. 2011. Aktivitas ekstrak etanol biji jintan hitam (Nigella sativa
Linn.) terhadap titer antibodi dan jumlah sel leukosit pada mencit putih jantan. Scientia 1(1): 35-41.
Amelia G. 2006. Potensi Rumput Mutiara (Hedyotis corymbosa Lam.) Sebagai
Antioksidan Alami. [skripsi]. Bogor: Departemen Biokimia, Fakultas Matematika dan Ilmu Pengetahuan Alam, Institut Pertanian Bogor.
Astawan M. 1998. Teknik ekstraksi dan pemanfaatan minyak ikan untuk kesehatan. Buletin Teknologi dan Industri Pangan 9(1): 44-54.
Estiasih T, Nisa FC, Ahmadi K, Umiatun. 2005. Optimasi pemadatan cepat pada pengayaan minyak ikan hasil samping pengalengan lemuru dengan asam
lemak ω-3 menggunakan metode permukaan respon. Jurnal Teknologi dan Industri Pangan 16(3): 230-238.
Fardinatri ID. 2007. Pengembangan dan Evaluasi Tepung dan Tablet Isap Kaya Antioksidan Berbahan Dasar Tomat. [skripsi]. Bogor. Departemen Gizi Masyarakat dan Sumberdaya Keluarga, Fakultas Pertanian, Institut Pertanian Bogor.
Gunawan, Triatmo MMA, Rahayu A. 2003. Analisis pangan: penentuan angka peroksida dan asam lemak bebas pada minyak kedelai dengan variasi menggoreng. Jurnal Staf Kimia Analitik 6(3): 1-6.
Hartoyo A, Astuti M. 2002. Aktivitas antioksidatif dan hipokolesterolemik ekstrak teh hijau dan teh wangi pada tikus yang diberi ransum kaya asam lemak tidak jenuh ganda. Jurnal Teknologi dan Industri Pangan 13(1): 78-85.
Herlina N, Ginting MHS. 2002. Lemak dan Minyak. Medan: Universitas Sumatera Utara.
Hutapea JR. 1994. Inventaris Tanaman Obat Indonesia (III). Jakarta: Badan
Penelitian dan Pengembangan Kesehatan, Departemen Kesehatan Republik Indonesia.
Kusnandar F. 2010. Mengenal Sifat Lemak dan Minyak. Bogor: Departemen Ilmu dan Teknologi Pangan, Institut Pertanian Bogor.
Latyshev NA, Kasyanov SP, Kharlamenko VI, Svetashev VI. 2009. Lipids and of fatty acids of edible crabs of the north-western Pacific. Food Chem
16
Mardiana.2011. Karakteristik Asam Lemak dan Kolesterol Rajungan (Portunus pelagicus) Akibat Proses Pengukusan. [skripsi]. Bogor. Departemen
Teknologi Hasil Perairan, Fakultas Perikanan dan Ilmu Kelautan, Institut Pertanian Bogor.
Nergiz C, Ötles S. 1993. Chemical composition of Nigella Sativa L. seeds. Food Chemistry 48(1): 259-261.
Okuzami, Tateo. 2000. Nutritional and Functional Properties Of Squid And Cuttlefish. Japan: National Cooperative Association.
Pokorny J, Parkanyiova L, Reblova Z, Trojakova L, Sakurai H, Uematsu T, Miyahara M, Yano T. 2003. Changes on storage of peanut oils containing high levels of
tocopherols and β-carotene. Czech Journal Food Science 21(1): 19-27.
Rasyid A. 2003. Asam lemak omega-3 dari minyak ikan. Jurnal Oseana 28(3): 11-16.
Rahmi A. 2011. Pengaruh Pemberian Ekstrak Minyak Jintan Hitam (Nigella sativa) Terhadap Gambaran Histopatologi Organ Testis Mencit (Mus musculus). [skripsi]. Bogor. Fakultas Kedokteran Hewan, Institut Pertanian Bogor.
Syakiroh NM. 2012. Peningkatan Kualitas Asam Lemak Omega-3 Minyak Ikan Limbah Pengalengan Ikan Melalui Proses Degumming, Netralisasi, dan Bleaching Dengan Karbon Aktif Biji Kelor (Moringa oleifera Lamk)
Teraktivasi NaCl. [skripsi]. Malang. Departemen Kimia, Fakultas Sains dan Teknologi, Universitas Islam Negeri Maulana Malik Ibrahim.
Widjaja E, Utomo BN. 2007. Produk samping kelapa sawit sebagai bahan pakan alternatif di Kalimantan Tengah: 2. Pengaruh pemberian solid terhadap kandungan kolesterol, asam lemak dan vitamin A pada ayam broiler. JITV
12(1): 16-21.
LAMPIRAN
Lampiran 1 Tabel hasil uji Kruskal-Wallis
Test Statisticsa,b
Warna Rasa Aroma
Chi-Square
52.211 3.539 2.617
df 3 3 3
Asymp. Sig.
.000 .316 .455
a. Kruskal Wallis Test
b. Grouping Variable: Kode
18