PEMEKATAN KAROTEN DENGAN CARA SOLVOLYTIC MICELLIZATION DARI MINYAK HASIL EKSTRAKSI
LIMBAH SERAT PENGEPRESAN BUAH KELAPA SAWIT
SKRIPSI
Diajukan untuk melengkapi tugas dan memenuhi syarat mencapai gelar Sarjana Sains
FITRI ANGELINA SINAGA 110822015
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM UNIVERSITAS SUMATERA UTARA
PERSETUJUAN
Judul : PEMEKATAN KAROTEN DENGAN CARA
SOLVOLYTIC MICELLIZATIONDARI MINYAK HASIL EKSTRAKSI LIMBAH SERAT PENGEPRESAN BUAH KELAPA SAWIT
Kategori : SKRIPSI
Nama : FITRI ANGELINA SINAGA
Nomor Induk Mahasiswa : 110822015
Program Studi : SARJANA (S1) KIMIA EKSTENSI
Departemen : KIMIA
Fakultas : MATEMATIKA DAN ILMU PENGETAHUAN
ALAM (FMIPA) UNIVERSITAS SUMATERA UTARA
Disetujui di
Medan, Oktober 2015
Komisi Pembimbing :
Pembimbing 2 Pembimbing 1
Dr. Donald Siahaan Dra. Herlince Sihotang, M.Si NIP. 195503251986012002
Diketahui/Disetujui oleh
Departemen Kimia FMIPA USU Ketua,
PERNYATAAN
PEMEKATAN KAROTEN DENGAN CARA SOLVOLYTIC MICELLIZATIONDARI MINYAK HASIL EKSTRAKSI
LIMBAH SERAT PENGEPRESAN BUAH KELAPA SAWIT
SKRIPSI
Saya mengaku bahwa skripsi ini adalah hasil kerja saya sendiri, kecuali beberapa kutipan dan ringkasan yang masing-masing disebutkan sumbernya.
Medan, Oktober 2015
PENGHARGAAN
Segala puji dan syukur penulis panjatkan kepada Tuhan Yang Maha Pengasih, karena berkat kasih dan kemurahan-Nya penulis dapat menyelesaikan penelitian dan penyusunan skripsi dengan judul Pemekatan Karoten dengan Cara Solvolytic Micellization dari Minyak Hasil Ekstraksi Limbah Serat Pengepresan Buah Kelapa Sawit.
Dalam kesempatan ini, penulis juga mengucapkan terima kasih kepada Ibu Dra. Herlince Sihotang, M.Si selaku Dosen Pembimbing I dan Bapak Dr. Donald Siahaan selaku Dosen Pembimbing II yang telah memberikan kesempatan kepada penulis untuk melaksanakan penelitian dan juga yang telah banyak meluangkan waktu untuk memberikan pengarahan, pemikiran serta saran bagi kesempurnaan penelitian dan skripsi ini. Terima kasih kepada Ibu Dr. Rumondang Bulan Nst, MS selaku Ketua Departemen dan Bapak Drs. Albert Pasaribu, M.Sc selaku Sekretaris Departemen. Terima kasih kepada Bapak dan Ibu Dosen Departemen Kimia FMIPA USU yang telah mendidik Penulis selama masa perkuliahan dan Ibu Dra. Emma Zaidar, M.Si selaku penasehat akademik. Bapak dan Ibu staf Laboratorium Pengolahan Hasil dan Mutu (PAHAM) Pusat Penelitian Kelpa Sawit (PPKS) Medan yang telah memberikan arahan dan fasilitas selama penulis melakukan penelitian.
Penulis mempersembahkan rasa terima kasih tak terhingga kepada Bapak tercinta K.Sinaga dan Mamaku tersayang N. Manurung yang selalu memberikan dukungan dan semangat kepada penulis dan juga kepada adik-adikku tersayang : Fandrew Sinaga, Frans Oktavianus Sinaga, dan Finny Chendiawaty Sinaga.
PEMEKATAN KAROTEN DENGAN CARA SOLVOLYTIC MICELLIZATION DARI MINYAK HASIL EKSTRAKSI
LIMBAH SERAT PENGEPRESAN BUAH KELAPA SAWIT
ABSTRAK
Limbah Pabrik Kelapa Sawit (PKS) yaitu serat pengepresan buah kelapa sawit berpotensi sebagai sumber minyak yang mengandung komponen minor yaitu karoten. Untuk memekatkan kadar karoten maka dilakukan dengan metode solvolytic micellization.Penelitian ini bertujuan untuk mengetahui kualitas minyak hasil ekstraksi limbah serat pengepresan buah kelapa sawit dan mengetahui konsentrasi optimum dengan penambahan metil oleat pada proses pemekatan karoten dengan cara solvolytic micellization (SM). Limbah serat pengepresan buah kelapa sawit diektraksi dengan menggunakan pelarut n-heksana selama 24 jam. Minyak hasil ekstraksi ditransesterifikasi dengan menggunakan KOH-metanol dan selanjutnya dilakukan solvolytic micellization dengan berbagai variasi rasio (v/v) yaitu 0,1%; 0,25%; 0,5% dan 0,75%. Kualitas minyak yang diperoleh dari hasil analisis yang telah dilakukan diperoleh kadar Asam Lemak Bebas (ALB) sebesar 9,2502%,kadar air sebesar 6,8175%dan nilai DOBI yang diperoleh yaitu2,38.Kadar karoten minyak hasil ekstraksi limbah serat pengepresan buah kelapa sawit diperoleh sebesar 3384 ppm, pada proses transesterifikasi menjadi 5737 ppmdan pada proses solvolytic micellizationterjadi peningkatan : pada perlakuan 0% (tanpa penambahan metil oleat) kadar karoten diperoleh sebesar 26564 ppm, penambahan metil oleat 0,10% sebesar 27730 ppm, pada penambahan metil oleat 0,25% sebesar 28163 ppm, pada penambahan metil oleat 0,50% sebesar 30406 ppm dan pada penambahan metil oleat 0,75% sebesar 29987 ppm. Konsentrasi optimum metil oleat pada pemekatan karoten dengan cara SM adalah 0,50% dengan kadar karoten 30406 ppm.
PEMEKATAN KAROTEN DENGAN CARA SOLVOLYTIC MICELLIZATION DARI MINYAK HASIL EKTRAKSI
LIMBAH SERAT PENGEPRESAN BUAH KELAPA SAWIT
ABSTRACT
Palm Oil Mill waste is pressed fiber of palm oil which is potentialas source of oil containing a minor component that is carotene. For concentrating carotene then performed method solvolytic micellization. This study aims to determine the quality of extracted pressed palm oil fiber waste and find the optimum concentration with the addition of methyl oleate on carotene concentration process by solvolytic micellization.Pressed palm oil fiber waste extracted using n-hexane solvent for 24 hours. The extraction of pressed palm oilfiber waste in transesterification using KOH-methanol and then performed solvolytic micellization with a variety a ratios is 0,1%; 0,25%; 0,5% dan 0,75%. The quality of the oil obatined from the analysis that has been done obtained free fatty acid contenct amounted 9,2502%, water content amounted 6,8175%, value DOBI 2,38.The extraction of pressed palm oil fiber waste contents 3384 ppm of carotene, 5737 ppm of carotene on transesterified process, and 26564 ppm of carotenesolvolytic micellization process (without the addition of methyl oleate), 27730 ppm of carotene on solvolytic micellizationwith the addition of 0,10% of methyl oleate, 28163 ppm of carotene on solvolytic micellization with the addition of 0,25% of methyl oleate, 30406 ppm of carotene on solvolytic micellization with the addition of 0,50% of methyl oleateand 29987 ppm of carotene on solvolytic micellization with the addition of 0,75% of methyl oleate. The optimum concentration of methyl oleate on carotene concentration process by solvolytic micellization is 0.50% 30406 ppm carotene levels.
DAFTAR ISI
Halaman
Persetujuan ii
Pernyataan iii
Penghargaan iv
Abstrak v
Abstract vi
Daftar Isi vii
Daftar Tabel ix
Daftar Gambar x
Daftar Lampiran xi
BAB 1PENDAHULUAN
1.1.LatarBelakang 1
1.2.Perumusan Masalah 3
1.3.Pembatasan Masalah 3
1.4.Tujuan Penelitian 4
1.5.Manfaat Penelitian 4
1.6.Lokasi Penelitian 4
1.7.Metodologi Penelitian 4
BAB 2 TINJAUAN PUSTAKA
2.1.Kelapa Sawit 6
2.2.Pabrik Pengolahan Kelapa Sawit 7
2.3.Limbah Kelapa Sawit 9
2.3.1. Limbah Padat 9
2.3.2. Limbah Cair 10
2.4.Ekstraksi Minyak Limbah Kelapa Sawit 10
2.5.Transesterifikasi 11
2.6.Komposisi Minyak Kelapa Sawit 13
2.7.Standar Mutu Minyak Kelapa Sawit 14
2.7.1. Kandungan asam lemak bebas 14
2.7.2. Kadar air 14
2.7.3. Nilai DOBI 15
2.8.Karotenoid 15
2.9.Solvolytic Micellization 18
BAB 3 METODE PENELITIAN
3.1. Bahan-Bahan 20
3.2. Alat-alat 20
3.3. Prosedur Penelitian 21
3.3.1.Ekstraksi Minyak 21
3.3.2.1. Penentuan Kadar Asam Lemak Bebas 21
3.3.2.2. Penentuan Kadar Air 22
3.3.2.3. Penentuan Nilai DOBI 22
3.3.2.4. Penentuan Kadar Karoten 22
3.3.3. Transesterifikasi Minyak Serat 23
3.3.4. Solvolytic Micellization (Tanpa Penambahan Metil Oleat) 23 3.3.5. Solvolytic Micellization (Dengan Penambahan
Metil Oleat) 24
3.4. Bagan Penelitian 25
3.4.1. Ekstraksi Minyak 25
3.4.2. Analisa Mutu Minyak 27
3.4.2.1. Penentuan Kadar Asam LemakBebas 27
3.4.2.2. Penentuan Kadar Air 28
3.4.2.3. Penentuan Nilai DOBI 29
3.4.2.4. Penentuan Kadar Karoten 30
3.4.3. Transesterifikasi Minyak Serat 31
3.4.4. Solvoytic Micellization (Tanpa Penambahan
Metil oleat) 32
3.4.5. Solvoytic Micellization (Dengan Penambahan
Metil Oleat ) 33
BAB 4 HASIL DAN PEMBAHASAN
4.1. Hasil 35
4.1.1. Mutu Minyak Serat 35
4.1.2. Hasil Transesterifikasi Minyak Serat 35 4.1.3. Hasil Solvolytic Micellization 35
4.2. Pembahasan 36
4.2.1. Mutu Minyak Serat 36 4.2.2. Hasil Transesterifikasi 37 4.2.3. HasilSolvolytic Micellization 37
BAB 5 KESIMPULAN DAN SARAN
5.1. Kesimpulan 39
5.2. Saran 39
DAFTAR PUSTAKA 40
DAFTAR TABEL
Nomor Judul Halaman Tabel
Tabel 2.1. Standar Kehilangan Minyak Kelapa Sawit Terhadap TBS 8 Tabel 2.2. Standar Kehilangan Minyak Inti Kelapa Sawit Terhadap TBS 8
Tabel 2.3. Rendemen Limbah Padat 9
Tabel 2.4. Komponen Minor Minyak Sawit 13
Tabel 2.5. Komposisi Karotenoid Minyak Sawit dari Berbagai Varietas 14
Tabel 2.6.Standar Mutu Minyak Sawit 15
Tabel 2.7. Perbandingan Aktivitas Vitamin A Minyak Sawit Terhadap
Berbagai Sumber Pangan 18
Tabel 4.1. Mutu Minyak Hasil Ekstraksi 35
Tabel 4.2. Karakteristik Metil Ester Hasil Transesterifikasi 35 Tabel 4.3. Konsentrasi Karoten dan Nilai DOBIHasil Solvolytic
DAFTAR GAMBAR
Nomor Judul Halaman Gambar
Gambar 2.1. Tanaman Kelapa Sawit 6
DAFTAR LAMPIRAN
Nomor Judul Halaman Lamp
Lampiran 1. Hasil Analisis Kadar Air, Kadar Asam Lemak Bebas,
Kandungan Karoten dan DOBI 45
PEMEKATAN KAROTEN DENGAN CARA SOLVOLYTIC MICELLIZATION DARI MINYAK HASIL EKSTRAKSI
LIMBAH SERAT PENGEPRESAN BUAH KELAPA SAWIT
ABSTRAK
Limbah Pabrik Kelapa Sawit (PKS) yaitu serat pengepresan buah kelapa sawit berpotensi sebagai sumber minyak yang mengandung komponen minor yaitu karoten. Untuk memekatkan kadar karoten maka dilakukan dengan metode solvolytic micellization.Penelitian ini bertujuan untuk mengetahui kualitas minyak hasil ekstraksi limbah serat pengepresan buah kelapa sawit dan mengetahui konsentrasi optimum dengan penambahan metil oleat pada proses pemekatan karoten dengan cara solvolytic micellization (SM). Limbah serat pengepresan buah kelapa sawit diektraksi dengan menggunakan pelarut n-heksana selama 24 jam. Minyak hasil ekstraksi ditransesterifikasi dengan menggunakan KOH-metanol dan selanjutnya dilakukan solvolytic micellization dengan berbagai variasi rasio (v/v) yaitu 0,1%; 0,25%; 0,5% dan 0,75%. Kualitas minyak yang diperoleh dari hasil analisis yang telah dilakukan diperoleh kadar Asam Lemak Bebas (ALB) sebesar 9,2502%,kadar air sebesar 6,8175%dan nilai DOBI yang diperoleh yaitu2,38.Kadar karoten minyak hasil ekstraksi limbah serat pengepresan buah kelapa sawit diperoleh sebesar 3384 ppm, pada proses transesterifikasi menjadi 5737 ppmdan pada proses solvolytic micellizationterjadi peningkatan : pada perlakuan 0% (tanpa penambahan metil oleat) kadar karoten diperoleh sebesar 26564 ppm, penambahan metil oleat 0,10% sebesar 27730 ppm, pada penambahan metil oleat 0,25% sebesar 28163 ppm, pada penambahan metil oleat 0,50% sebesar 30406 ppm dan pada penambahan metil oleat 0,75% sebesar 29987 ppm. Konsentrasi optimum metil oleat pada pemekatan karoten dengan cara SM adalah 0,50% dengan kadar karoten 30406 ppm.
PEMEKATAN KAROTEN DENGAN CARA SOLVOLYTIC MICELLIZATION DARI MINYAK HASIL EKTRAKSI
LIMBAH SERAT PENGEPRESAN BUAH KELAPA SAWIT
ABSTRACT
Palm Oil Mill waste is pressed fiber of palm oil which is potentialas source of oil containing a minor component that is carotene. For concentrating carotene then performed method solvolytic micellization. This study aims to determine the quality of extracted pressed palm oil fiber waste and find the optimum concentration with the addition of methyl oleate on carotene concentration process by solvolytic micellization.Pressed palm oil fiber waste extracted using n-hexane solvent for 24 hours. The extraction of pressed palm oilfiber waste in transesterification using KOH-methanol and then performed solvolytic micellization with a variety a ratios is 0,1%; 0,25%; 0,5% dan 0,75%. The quality of the oil obatined from the analysis that has been done obtained free fatty acid contenct amounted 9,2502%, water content amounted 6,8175%, value DOBI 2,38.The extraction of pressed palm oil fiber waste contents 3384 ppm of carotene, 5737 ppm of carotene on transesterified process, and 26564 ppm of carotenesolvolytic micellization process (without the addition of methyl oleate), 27730 ppm of carotene on solvolytic micellizationwith the addition of 0,10% of methyl oleate, 28163 ppm of carotene on solvolytic micellization with the addition of 0,25% of methyl oleate, 30406 ppm of carotene on solvolytic micellization with the addition of 0,50% of methyl oleateand 29987 ppm of carotene on solvolytic micellization with the addition of 0,75% of methyl oleate. The optimum concentration of methyl oleate on carotene concentration process by solvolytic micellization is 0.50% 30406 ppm carotene levels.
BAB 1
PENDAHULUAN
1.1Latar Belakang
Minyak kelapasawit (CrudePalm Oil,
CPO)merupakankomoditasandalanpadasektorindustripertaniandi Indonesiadan
merupakan produsen terbesar di dunia sejak 2007 dengan dominasi yang
cenderung meningkat. Produksi CPO pada 2014mencapai 31,0 juta ton (Indonesia
investment, 2015). Melalui Masterplan Percepatan dan Perluasan Pembangunan
Ekonomi Indonesia (MP3EI), pemerintah telah mencanangkan hilirisasi kelapa
sawit terutama di koridor Sumatera dan Kalimantan sebagai lokasi produksi
utama kelapa sawit di Indonesia.
Minyak kelapa sawit dalam konsumsi minyak dunia mengalami
peningkatan sekitar 9% per tahun, sedangkan pertumbuhan minyak nabati dunia
hanya mampu bertumbuh rata-rata 4,1% per tahun. Peningkatan konsumsi CPO
juga menunjukkan bahwa masyarakat dunia menerima minyak kelapa sawit
sebagai komoditas penting dengan ditemukannya berbagai keunggulan nutrisi
CPO dan keramahan produk CPO terhadap lingkungan (Saragih, 1998).
Produksi CPO akan melewati angka 40 juta pada 2020 sehingga Indonesia
akan menguasai lebih separuh produksi minyak kelapa sawit dunia (Food and
Agricultural Policy Research, 2010). Serapan pasar domestik terhadap produksi CPO relatif terbatas pada angka sekitar 7 juta ton CPO karena pemanfaatannya
yang terbatas dan nilai ekonomi yang diperoleh Indonesia dari kelapa sawit lebih
rendah dibandingkan Malaysia. Hal ini dapat terjadi karena rendahnya tingkat
hilirisasi industri kelapa sawit domestik dan Indonesia sebagai produsen CPO
terbesar, mengalami terpaan black campaign melalui isu lingkungan dan
kesehatan.
Pabrik Kelapa Sawit (PKS) sebagai industri penghasil CPO masih sarat
dengan residu pengolahan dan hanya menghasilkan 25-30% produk utama yaitu
20-23% CPO dan 5-7% inti sawit (kernel). Sementara sisanya dengan jumlahlebih
segar adalah residu pengolahan berupa limbah (Naibaho, 1998). Setiap1 ton
kelapa sawit akan mampu menghasilkan limbah berupa tandan kosong kelapa
sawit (TKKS) sebanyak 23% atau 23 kg, limbah cangkang (shell) sebanyak 6,5%
atau 65 kg, wet decanter solid (lumpur sawit) 4% atau 40 kg, serat (fiber) 13%
serta limbah cair sebanyak 50% (Sunarwan, 2013).
Berdasarkan penelitian oleh Asnawi dkk(2009), limbah cair PKS
umumnya mengandung minyaksekitar 0,5% dengan kadar karoten 100-3500 ppm.
Menurut Choo et al (1996) limbah padat PKS yang berasal dari ampas kempa
mengandung residu minyak 5-6% dengan kadar karoten 4000-6000 ppm, selain
komponen minor lain seperti vitamin E 2400-3500 ppm dan sterol 4500-8500
ppm, limbah padat yang berasal dari tandan kosong hanya mengandung minyak
sekitar 1,9-2%.
Ekstraksi minyak yang berasal dari serat pengepresan adalah salah satu
cara terbaru untuk memanfaatkan limbah dan menghasilkan CPO. Minyak hasil
ekstraksi dari limbah PKS tersebut masih mengandung karoten, senyawa nutrisi
minor yang dapat berfungsi untuk menunjang kesehatan. Karoten yang terdapat
pada CPO secara nutrisi mampu menghasilkan pro-vitamin A (retinol equivalent)
yang sebanding dengan 15 kali lebih besar dari wortel atau 300 kali lebih besar
dari tomat (Sundram et al, 2003). Selain berfungsi untuk menunjang kesehatan,
karoten dari limbah sawit pun berpotensi digunakan sebagai pewarna pangan
(food colorant) bahkan kosmetik (Mahfud dkk. 1991).
Metode ekstraksi karoten dari minyak kelapa sawit telah banyak dilakukan
menggunakan beberapa metode seperti saponifikasi, adsorpsi, solvolytic
micellization (Choo, 2000). Panjaitan dkk (2008) telah mengembangkan proses ekstraksi karoten dari CPO menggunakan metode solvolytic micellization yang
diikuti dengan proses saponifikasi. Masni (2004), mengestraksi karotenoid dari
ekstrak serat sawit dengan menggunakan kromatografi kolom adsorpsi, hasil
konsentrasi karotenoid dapat ditingkatkan enam kali dari konsentrasi awal.
Kembaren & Saputra (2012) mengestrak karotenoid dari serat buah dengan
menggunakan pelarut n-heksana–aseton (10:1 v/v) dan pemurnian menggunakan
kromatografi kolom absorbsi. Asnawi et al (2009), melakukan ekstraksi
pelarut petroleum eter dan n-heksana dan pemurnian dengan menggunakan
bantuan ultrasonic.
Solvolytic micellization (SM) adalah penyisihan zat yang dikehendaki ke dalam fasa rafinat melalui penambahan suatu pelarut. Solvolytic micellization
relatif lebih sederhana, mudah, dapat dilakukan dengan efektif pada kondisi
kamar, dan pelarut utama yang digunakan dapat dengan mudah didaur ulang. Oleh
karena itu peneliti tertarik untuk melakukan penelitian mengenai pemekatan
karoten dengan cara solvolytic micellization dari minyak hasil ekstraksi limbah serat pengepresan buah kelapa sawit.
1.2.Perumusan Masalah
Berdasarkan latar belakang yang telah diuraikan di atas, maka sebagai
perumusan masalah dalam penelitian ini adalah :
1. Berapakah konsentrasi optimum penambahan metil oleat pada proses
pemekatan karoten dengan cara solvolytic micellization ?
1.3.Pembatasan Masalah
Penelitian ini hanya dibatasi pada :
1. Variasi penambahan metil oleat terhadap ester dengan perlakuan v/v : 0%
(sebagai kontrol), 0,10 % ; 0,25%; 0,50%; 0,75%
2. Metil oleat yang digunakan adalah yang diperoleh dari laboratorium
Olekimia PPKS Medan
1.4.Tujuan Penelitian
1. Untuk mengetahui konsentrasi optimum penambahan metil oleat pada
proses pemekatan karoten dengan cara solvolytic micellization
1.5.Manfaat Penelitian
1. Penelitian ini diharapkan dapat memberikan manfaat berupa informasi
kepada Pabrik Kelapa Sawit untuk mengurangi pencemaran lingkungan
2. Memanfaatkan limbah serat pengepressan buah kelapa sawit sebagai
sumber karoten
1.6.Lokasi Penelitian
Pengambilan sampel diambil dari pabrik kelapa sawit (PKS) yaitu, PT
Perkebunan Nusantara IV Pabatu. Penelitian ini dilakukan Laboratorium
Pengolahan Hasil dan Mutu Pusat Penelitian Kelapa Sawit (PPKS) Jl. Brigjen
Katamso No. 51 Medan Sumatera Utara
1.7.Metodologi Penelitian
Penelitian ini bersifat eksperimental laboratorium dimana sampel limbah serat
pengepresan buah kelapa sawit yang diperoleh dari PTPN IV Pabatu. Limbah
serat pengepresan tersebut diekstraksi dengan menggunakan pelarut
n-heksana selama 24 jam kemudian n-n-heksana diuapkan menggunakan rotary
evaporator. Minyak hasil ekstraksi dianalisa mutunya seperti kadar asam
lemak bebas (metode titrasi asam basa), kadar air (gravimetri), nilai DOBI
(Deterioration of Bleachability Index) dengan menggunakan
Spektrofotometer dan juga kadar karotennya dengan menggunakan
Spektrofotometer. Kemudian minyak tersebut ditransesterifikasi dengan
menggunakan KOH-metanol dan selanjutnya dilakukan solvolytic
micellization (SM). Pada proses SM pelarut yang digunakan adalah metanol dengan perbandingan 1:5 (v/v) sebagai pelarut mayor dan air sebanyak 2,5%
dari jumlah larutan dan juga metil oleat sebagai pelarut minor dengan variasi
terhadap ester dengan perlakuan 0 % (sebagai kontrol), 0,10%; 0,25%;
0,50%; 0,75% kemudian dianalisis kandungan ester dan gliserida, DOBI dan
BAB 2
TINJAUAN PUSTAKA
2.1Kelapa Sawit
Kelapa sawit (Elaeis guineensis jacq) merupakan tanaman berkeping satu
penghasil minyak yang berasal dari famili Palmae. Nama genus Elaeis berasal
dari bahasa Yunani Elaion atau minyak, sedangkan nama spesies Guineensis
berasal dari kata guinea, yaitu tempat dimana seorang ahli bernama Jacquin
menemukan tanaman kelapa sawit pertama kali di pantai Guinea (Ketaren, 1986).
Gambar 2.1. Tanaman Kelapa Sawit
Kelapa sawit merupakan tumbuhan tropis yang diperkirakan berasal dari
Nigeria, Afrika Barat karena pertama kali ditemukan di hutan belantara negara
tersebut. Kelapa sawit pertama masuk ke Indonesia pada tahun 1848, kelapa sawit
mulai diperhitungkan sebagai tanaman komoditas (penghasil produk dagangan)
sejak revolusi industri berkembang di Eropa. Pada saat tersebut, mulai
bermunculan industri atau pabrik (sabun dan margarin) yang membutuhkan bahan
baku untuk pembuatannya seperti minyak sawit dan minyak inti sawit
(Hadi,2004).
Kelapa sawit saat ini telah berkembang pesat di Asia Tenggara, khususnya
Indonesia dan Malaysia, dan justru bukan di Afrika Barat yang dianggap sebagai
daerah asalnya. Masuknya bibit kelapa sawit ke Indonesia hanya 4 batang yang
ditanam di Kebun Raya Bogor dan selanjutnya disebarkan ke Deli Sumatera Utara
2.2Pabrik Pengolahan Kelapa Sawit
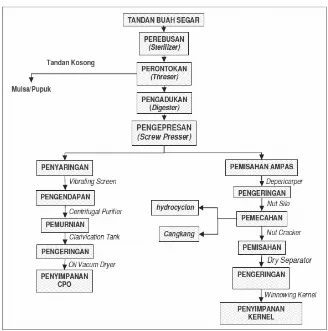
Tujuan utama dari pengolahan kelapa sawit adalah untuk memproduksi
minyak yang diperoleh dari mesokarp atau Crude Palm Oil (CPO) dan inti sawit
(kernel). Stasiun pengolahan tandan buah segar (TBS) menjadi CPO terdiri dari
beberapa stasiun (PTPN, 2009) yaitu :
1.Stasiun Penerimaan Tandan Buah Segar
2. Stasiun Perebusan
3. Stasiun Penebahan
4. Stasiun Pengepresan
5. Stasiun Pemurnian
Diagram alir proses pengolahan CPO dapat dilihat pada Gambar 2.2.
Pengolahan yang baik adalah pengolahan yang menghasilkan minyak dan
inti sawit dengan jumlah mutu yang optimal dan kehilangan (losess) sesuai
dengan yang disyaratkan seperti pada Tabel 2.1 dan Tabel 2.2.
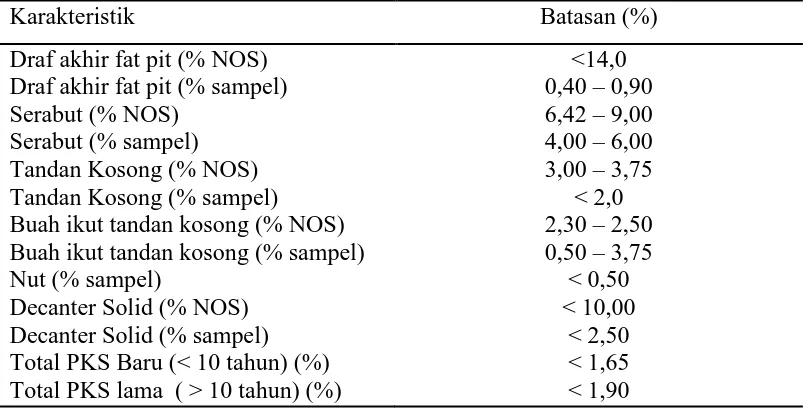
Tabel 2.1 Standar Kehilangan Minyak Kelapa Sawit Terhadap TBS
Karakteristik Batasan (%)
Draf akhir fat pit (% NOS) Draf akhir fat pit (% sampel) Serabut (% NOS)
Serabut (% sampel) Tandan Kosong (% NOS) Tandan Kosong (% sampel) Buah ikut tandan kosong (% NOS) Buah ikut tandan kosong (% sampel) Nut (% sampel)
Decanter Solid (% NOS) Decanter Solid (% sampel) Total PKS Baru (< 10 tahun) (%) Total PKS lama ( > 10 tahun) (%)
<14,0 0,40 – 0,90 6,42 – 9,00 4,00 – 6,00 3,00 – 3,75
< 2,0 2,30 – 2,50 0,50 – 3,75
< 0,50 < 10,00
< 2,50 < 1,65 < 1,90 Sumber : Pahan, 2008
Keterangan : NOS : Non Oil Solid
Tabel 2.2 Standar Kehilangan Minyak Inti Kelapa Sawit Terhadap TBS
Karakteristik Batasan (%)
Serabut (% sampel) LTDS I (% sampel) LTDS II (% sampel) Hydrocyclone (%) Clay bath (%) Total PKS < 15,00 < 2,00 < 1,00 < 5,00 < 1,50 0,60 Sumber : Pahan, 2008
2.3Limbah Kelapa Sawit
Limbah kelapa sawit adalah hasil sisa hasil tanaman kelapa sawit yang
tidak termasuk dalam produk utama atau merupakan hasil ikutan dari proses
pengolahan kelapa sawit. Berdasarkan tempat pembentukannya, limbah kelapa
sawit digolongkan menjadi 2 jenis yaitu limbah perkebunan kelapa sawit dan
limbah industri kelapa sawit.
Limbah perkebunan kelapa sawit merupakan sisa tanaman yang
ditinggalkan waktu panen, peremajaan atau pembukaan areal perkebunan baru.
Contoh limbah perkebunan sawit adalah batang, pelepah, daun dan gulma hasil
penyiangan kebun. Setiap satu hektar tanaman kelapa sawit akan menghasilkan
limbah pelepah daun sebanyak 10,40 ton bobot kering dalam setahun.
Limbah industri kelapa sawit adalah limbah yang dihasilkan pada proses
pengolahan kelapa sawit. Limbah jenis ini digolongkan kedalam dua jenis yaitu
limbah padat dan limbah cair.
2.3.1 Limbah padat
Limbah padat yang dihasilkan oleh pabrik pengolah kelapa sawit ialah
tandan kosong, serat dan tempurung seperti pada Tabel 2.3.
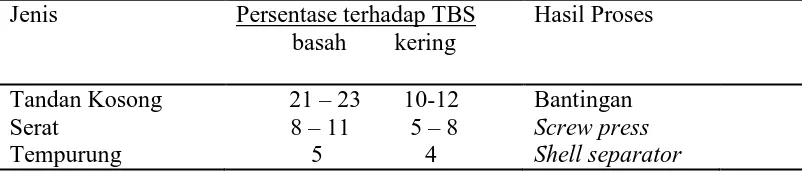
Tabel 2.3. Rendemen limbah padat
Jenis
basah kering
Persentase terhadap TBS Hasil Proses
Tandan Kosong Serat
Tempurung
21 – 23 10-12 8 – 11 5 – 8
5 4
Bantingan Screw press Shell separator Sumber :Naibaho, 1998
Limbah padat tandan kosong kadang-kadang mengandung buah yang tidak
lepas diantara celah-celah ulir dibagian dalam. Kejadian ini timbul, bila perebusan
dan bantingan yang tidak sempurna sehingga pelepasan buah sangat sulit. Hal ini
sering terjadi di pabrik-pabrik yang tekanan kerja ketel rebusan di bawah 2,8 kg
disertai produksi uap yang tidak mencukupi kebutuhan. Perebusan yang tidak
sempurna menghasilkan tandan kosong yang masih mengandung buah hingga 9%
Serat yang merupakan hasil pemisahan dari fibre cyclone mempunyai
kandungan cangkang, minyak dan inti. Kandungan tersebut tergantung pada
proses ekstraksi di srew press dan pemisahan pada fibre cyclone. Kualitas asap
pembakaran pada dapur ketel uap dipengaruhi oleh komposisi serat tersebut.
Ampas serat sekarang ini telah habis terpakai di pabrik sehingga dampak yang
mungkin ditimbulkan pada lingkungan ialah polusi udara (Naibaho,1998).
2.3.2 Limbah cair
Limbah cair yang dihasilkan pabrik pengolah kelapa sawit ialah air drab,
air kondesat, air cucian pabrik, air hidrocyclone atau claybath.Jumlah air buangan
tergantung pada sistem pengolahan, kapasitas olah dan keadaan peralatan
klarifikasi.Air buangan sludge separator umumnya 60% terhadap TBS yang
diolah, akan tetapi ini dipengaruhi oleh :
a. Jumlah air pengencer yang digunakan pada vibrating screen atau pada screw
press
b. Sistem dan instalasi yang digunakan dalam stasiun klarifikasi yaitu klarifikasi
yang menggunakan decanter menghasilkan air limbahnya kecil
c. Efisensi pengamatan minyak dari air limbah yang rendah akan mempengaruhi
karakteristik limbah cair yang dihasilkan (Naibaho, 1998).
2.4Ekstraksi Minyak Limbah Kelapa Sawit
Ekstraksi adalah pemisahan satu atau beberapa bahan dari suatu padatan
atau cairan dengan bantuan pelarut. Pemilihan jenis pelarut didasarkan kepada
kemiripan sifat bahan yang akan diesktrak dengan pelarut ekstrak (like dissolved
like). Ekstraksi pelarut digunakan untuk memisahkan bahan apabila dengan pemisahan mekanis sukar atau tidak dapat dilakukan karena komponen bercampur
saling bercampur sempurna atau jumlah komponen terlalu sedikit (Bernasconi, et.
al., 1995). Berk ( 1983) mengatakan bahwa ekstraksi minyak dari bahan tanaman dilakukan dengan metode pengepresan dan menggunakan pelarut. Apabila bahan
tanaman banyak mengandung minyak seperti biji kedelai dan buah sawit, maka
minyaknya sedikit maka metode ekstraksi yang digunakan adalah metode
ekstraksi pelarut.
Kandungan minyak pada limbah PKS relatif kecil dibandingkan dengan
kandungan minyak pada TBS. Serat mesokarp dari buah sawit matang
mengandung 49% minyak (Naibaho dkk, 2006) sedangkan limbah PKS paling
tinggi 5-6%. Oleh karena itu proses ektraksi minyak dari mesokarp dilakukan
dengan ekstraksi pengepresan, sedangkan pengambilan minyak dari limbah PKS
harus dilakukan melalui ekstraksi dengan pelarut.
Minyak mempunyai sifat non polar, sehingga sifat minyak ditentukan oleh
sifat asam lemak penyusun. Karena minyak bersifat non polar, maka ekstraksi
minyak dengan metode pelarut harus menggunakan pelarut non polar. N-heksana
merupakan pelarut yang sering digunakan untuk mengektraksi minyak dari
tanaman misalnya kacang kedelai, minyak kapas, minyak biji bunga matahari, dan
minyak inti sawit (Sivaraoet al. 2012). Supardan dkk (2011) mengatakan bahwa
ekstraksi minyak dari limbah cair PKS dengan menggunakan n-heksana,
menghasilkan rendemen minyak lebih tinggi dibandingkan dengan menggunakan
petroleum eter hal ini disebabkan kemampuan pelarut untuk mengekstrak minyak
dipengaruhi tingkat polaritas pelarut. Semakin rendah tingkat kepolaritasan
pelarut (semakin non polar) maka daya ekstraksinya semakin tinggi (jumlah
minyak yang terlarut di dalam pelarut semakin besar). Seperti disebutkan diatas
bahwa minyak dan karotenoid mempunyai sifat non polar, sehingga untuk
melarutkan minyak atau lemak pada proses ekstraksi selalu menggunakan pelarut
non polar.
2.5Transesterifikasi
Pembentukanestermerupakansalahsatureaksiyangpentingdalampemberian
nilai
tambahdarilemakhewandanminyaktumbuhan.Reaksipembentukanesterdiklasifika
sikankedalamduareaksiyaitu :
1. Esterifikasi adalah reaksi pembentukan ester
Reaksi ini dapat dilakukan dengan berbagai cara :
RCOOH .+ R’OHRCOOR’+ H2O
b. Reaksi antara halida asam dengan alkohol
RCOCl .+ R’OH RCOOR’ + HCl
c. Reaksi antara anhidrida dengan alkohol
(RCO)2O .+ R’OH RCOOR’ + RCOOH
d. Reaksi antara suatu karboksilat dan alkil halida
RCOOH .+ R’X RCOOR’ + HX
2. Transesterifikasidibagikedalamtigajenis reaksiyaitu:
a. Interesterifikasiyaitupembentukanesterdariesterdenganester
b. Alkoholisisyaitupembentukanesterdarireaksi suatuesterdenganalkohol
c. Asidolisisyaitu reaksiantaraesterdenganasamkarboksilat.
Reaksitransesterifikasimenggunakankatalisheterogenmemilki
parameterpenting untukdiperhatikanseperti
temperatur,luasdarimuatankatalis,perbandinganmol
antarametanoldenganminyakdanwaktureaksi.
Transesterifikasi dariminyaknabati menjadibiodiesel (metil esterasam
lemak, MEAL)dapatdikatalisisdenganbasadan
asam.Katalisbasatermasukkatalisbasa homogen
dankatalisbasaheterogen.Secaraumum menggunakan katalishomogen seperti
NaOH,KOHdanalkosidanya.Keberadaan katalis dapat mempercepat pengaturan
kesetimbangan. Untuk memperoleh yield ester yang tinggi maka digunakan
alkohol berlebih (Manurung, 2006).
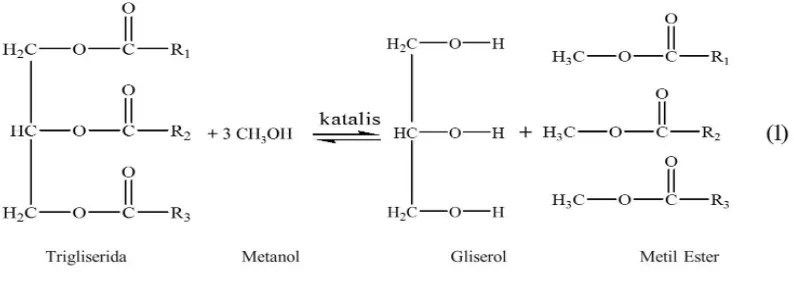
Dalam transesterifikasi minyak nabati, trigliserida bereaksi dengan alkohol
dengan adanya asam kuat atau basa kuat sebagai katalis menghasilkan campuran
metil ester asam lemak dan gliserol (Freedman et al,1986). Reaksi
transesterifikasi antara minyak atau lemak alami dengan metanol digambarkan
Gambar 2. 3. Reaksi transesterifikasi metil ester (Freedman,1984)
2.6Komposisi Minyak Kelapa Sawit
Produk utama yang diperoleh dari tanaman kelapa sawit adalah minyak
sawit dan minyak inti sawit yang mengandung trigliserida (Naibaho, 1998).
Minyak sawit hasil ekstraksi berbentuk kasar sehingga dinamakan Crude Palm
Oil (CPO) yang mengandung bahan-bahan lain (impurities), asam lemak bebas, zat warna, air (ICBS, 2000). Minyak sawit terdiri atas berbagai trigliserida dengan
rantai asam lemak yang berbeda-beda. Minyak sawit memiliki karakteristik yang
unik dibandingkan minyak nabati lainnya. Komposisi asam lemaknya terdiri dari
asam lemak jenuh ± 50%, MUFA ± 40%, serta asam lemak tidak jenuh
(polyunsaturated fatty acid/PUFA) yang relatif sedikit (± 10%). Selain komposisi
asam lemaknya, CPO juga mengandung komponen-komponen minor yang
konsentrasinya mencapai 2% seperti karotenoid, vitamin E (yakni tokoferol dan
Tabel 2.4. Komponen dan kandungan minor minyak sawit
Komponen Minor Kandungan (ppm)
Karotenoid 500-700
Tokoperol dan tokotrienol (vitamin E) 600-1000
Sterol 326-527
Fosfolipid 5-130
Triterpen 40-80
Metyl sterol 40-80
Squalen 200-500
Alkohol alifatik 100-200
Ubiquinon 10-80
Hidrokarbon alifatik 50
Sumber: Choo, 2000. Specialty Products: Carotenoids
CPO mengandung karotenoid sebesar 500 -700 ppm, dimana komponen
utamanya adalah α- dan β-karoten (± 90%). Karoten diketahui memiliki aktifitas
provitamin A yang tinggi, dimana nilai ekuivalen vitamin A dari α- dan β-karoten masing-masing adalah 0,90 dan 1,67 (Choo, 2000; Sundram dan
Chandra-Sekharan, 1997) seperti pada Tabel 2.5
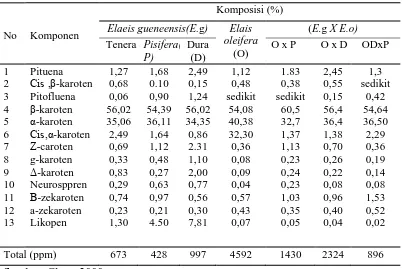
Tabel 2.5. Komposisi karotenoid minyak sawit dari berbagai varietas
No Komponen
Komposisi (%)
Elaeis gueneensis(E.g) Elais oleifera
(O)
(E.g X E.o)
Tenera Pisifera( P)
Dura (D)
O x P O x D ODxP
1 2 3 4 5 6 7 8 9 10 11 12 13 Pituena Cis ,β-karoten Pitofluena β-karoten α-karoten Cis,α-karoten Ζ-caroten g-karoten Δ-karoten Neurosppren Β-zekaroten a-zekaroten Likopen 1,27 0,68 0,06 56,02 35,06 2,49 0,69 0,33 0,83 0,29 0,74 0,23 1,30 1,68 0.10 0,90 54,39 36,11 1,64 1,12 0,48 0,27 0,63 0,97 0,21 4.50 2,49 0,15 1,24 56,02 34,35 0,86 2.31 1,10 2,00 0,77 0,56 0,30 7,81 1,12 0,48 sedikit 54,08 40,38 32,30 0,36 0,08 0,09 0,04 0,57 0,43 0,07 1.83 0,38 sedikit 60,5 32,7 1,37 1,13 0,23 0,24 0,23 1,03 0,35 0,05 2,45 0,55 0,15 56,4 36,4 1,38 0,70 0,26 0,22 0,08 0,96 0,40 0,04 1,3 sedikit 0,42 54,64 36,50 2,29 0,36 0,19 0,14 0,08 1,53 0,52 0,02
Total (ppm) 673 428 997 4592 1430 2324 896
2.7Standar Mutu Minyak Kelapa Sawit
Standar mutu merupakan hal yang paling penting dalam menentukan mutu
minyak kelapa sawit diperdagangan Internasional. Standar mutu diukur
berdasarkan spesifikasi standar mutu Internasional
2.7.1 Kandungan asam lemak bebas
Kandungan asam lemak bebas (Free Fatty Acid, FFA) merupakan
parameter awal yang menentukan kerusakan CPO. FFA yang lebih dari 1% jika
dicicipi akan terasa membentuk film pada permukaan lidah tapi tidak berbau
tengik (Siahaan, dkk., 2008).
2.7.2 Kadar air
Kadar air pada CPO merupakan penentu parameter standar lain. Semakin
banyak kandungan air pada CPO akan mempercepat hidrolisa trigliserida,
memberikan kondisi yang baik bagi pertumbuhan mikroba dan mempengaruhi
densitas CPO, dan merangsang reaksi kontaminasi lain seperti logam. Oleh karena
itu, kadar air pada CPO harus diusahakan sesuai dengan standar (Siahaan, dkk.,
2008).
2.7.3 Kadar DOBI
DOBI (Deterioration of Bleachability Index) atau indeks daya pemucat
merupakan rasio dari kandungan karoten dan produk oksidasi sekunder pada
CPO. Nilai DOBI yang rendah mengindikasikan naiknya kandungan produk
oksidasi sekunder sehingga memiliki daya pemucat yang rendah atau dengan kata
lain membutuhkan lebih banyak bleaching earth karena produk-produk
karotenoid teroksidasi sulit dipucatkan (Siahaan, 2006). Standar Mutu Minyak
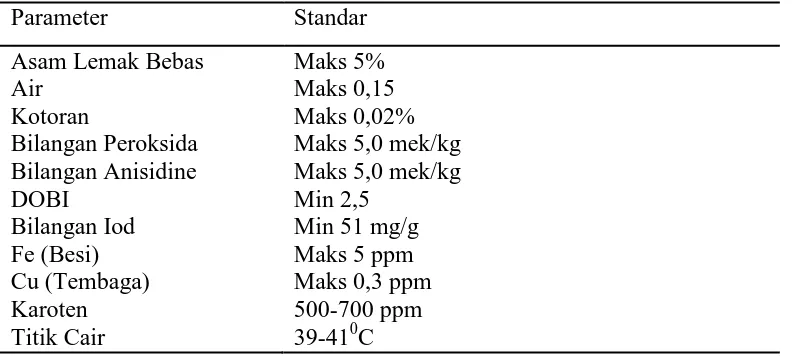
Tabel 2.6. Standar Mutu Minyak Sawit
Parameter Standar
Asam Lemak Bebas Air Kotoran Bilangan Peroksida Bilangan Anisidine DOBI Bilangan Iod Fe (Besi) Cu (Tembaga) Karoten Titik Cair Maks 5% Maks 0,15 Maks 0,02% Maks 5,0 mek/kg Maks 5,0 mek/kg Min 2,5
Min 51 mg/g Maks 5 ppm Maks 0,3 ppm 500-700 ppm 39-410C Sumber : ICBS, 2000
2.8Karotenoid
Terminologi kata karotenoid berasal dari kata carotene yang ditambah
sufiks -oid, yang berarti "senyawa-senyawa sekelompok atau mirip dengan
karoten". Sedangkan kata karoten diturunkan dari bahasa latin carota yaitu
pigmen utama pada akar atau umbi wortel (Daucus carota L). Karoten pertama
sekali diekstrak dari tanaman wortel pada tahun 1831 oleh Wackenroder (Berk,
1983). Kemudian pada tahun 1930, Karrer berhasil menentukan struktur
karoten.Karotenoidadalahsuatukelompokpigmenyangberwarna kuning,orange,atau
merahorange, yangditemukanpadatumbuhan, kulit,cangkang/kerangkaluar
(eksoskeleton)hewan air sertahasillaut lainnyaseperti molusca (calm, oyster,
scallop),crustacea(lobster,kepiting,udang) dan ikan(salmon,trout,seabeam,
kakapmerahdantuna). Karotenoidjuga banyakditemukan pada kelompokbakteri,
jamur, ganggangdan tanaman hijau(Desiana, 2000).
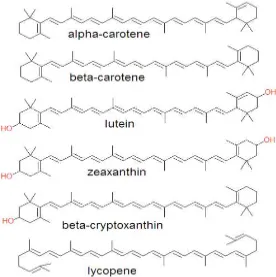
Karotenoid merupakan senyawa tetraterpenoid dengan jumlah atom
karbon 40 yang terdiri atas 8 unit isopronoid C5 (ip). Struktur isopronoid C5 (ip)
dan likopen seperti terlihat pada Gambar 2.4. Rantai lurus karotenoid C40 ini
menjadi kerangka dasar karotenoid. Unit ip tersusun dalam 2 posisi arah yang
berlawanan pada pusat rantainya sehingga berbentuk molekul simetris. Bentuk ini
merupakan bentuk molekul likopen, sehingga likopen sering disebut induk dari
Gambar 2.4 Struktur beberapa jenis karotenoid (Fennema,1996)
Pigmenkarotenoidmempunyaistrukturalifatikataualisiklikyang
padaumumnya disusunolehdelapanunitisoprena,dimana kedua
gugusmetilyangdekatpada molekulpusatterletakpada posisi
C1danC6,sedangkangugusmetillainnyaterletak padaposisi C1dan C5serta
diantaranyaterdapat ikatangandaterkonjugasi.
Karotenoiddibentukolehpenggabungandelapanunitisoprene(C5H8)atau2-metil-1,3-butadienadimanaisoprenayang membentukkarotenoidiniberikatansecara “kepala-ekor” kecualipada pusatmolekulberikatan secara“ekor-ekor”sehingga
menjadikan molekul kerotenoid simetris. Semuasenyawakarotenoidmengandung
sekurang-kurangnyaempatgugusmetildan selalu terdapat ikatan
gandaterkonjugasi diantara gugus metil tersebut. Adanya ikatanganda
terkonjugasidalamikatankarotenoidmenandakanadanyagugus
kromoforayangmenyebabkan terbentuknyawarnapadakarotenoid. Semakin banyak
mengarah kewarnamerah (Heriyanto dan Limantara, 2009).
Istilahkarotendigunakanuntukbeberapazatyang memilikirumusmolekul C40H56.
Secara kimia,karotenadalahterpenayang disintesasecara biokimiadaridelapan
satuan isoprenaC5H8.
Karotenoid mempunyaisifat-sifat tertentu, diantaranyatidak larut dalam
air, larut sedikitdalam minyak, larut dalam hidrokarbonalifatik dan
aromatiksepertiheksana dan benzeneserta larut dalam kloroform danmetilen
klorida. Karotenoidharus selalu disimpan dalamruangangelap (tidak ada cahaya)
dandalam ruanganvakum,pada suhu-200C.Karotenoidyang
terbaikdisimpandalambentukpadatankristaldan
didalamnyaterdapatpelaruthidrokarbonsepertipetroleum,heksanaataubenzena.
Halinibertujuan untuk meminimalkan resikokontaminasidengan air sebelum
dianalisalebih lanjut.
Pada manusia karotenoidsepertiβ-carotene sangatberperansebagai prekusor
darivitaminA,suatupigmenyang sangatpenting untukprosespenglihatan,
karotenoidjugaberperansebagaiantioksidan dalamtubuh(Ravi, Metal.,2010).
Selainitukarotenoidjuga banyakdigunakansebagaibahantambahanpada
makananyaitusebagaipewarnamakanan(Mortensen,A,2006),sepertiekstrakdari
kulitcitrusdigunakansebagai pewarna pada orange jussejakmeningkatnyaharga
pewarna jus.Safronbanyakdimanfaatkansebagaibumbumasakankarena rasanyadan
warnayang diinginkan.Anatoberperanselainsebagaipewarnamakananjuga
dimanfaatkan sebagai pewarna pada industri textile dan kosmetik, Astaxathin
merupakansuatupewarna pada troutdansalmon(Henrikson,2009).
Minyak sawit merupakan sumber karotenoid terutama beta karoten sebagai
precursor vitamin A. Apabila dibandingkan dengan tingkat aktivitas vitamin A
(retinol ekivalen), maka minyak sawit memiliki ativitas vitamin A ekivalen 15
kali lebih besar dari wortel dan 300 kali lebih besar dari tomat ( Choo, 2000).
Perbandingan Aktivitas vitamin A minyak sawit dengan aktivitas vitamin A dari
sumber pangan lain dapat dilihat pada Tabel 2.7 di bawah ini.
Sumber Pangan Aktivitas vitamin A
Perbandingan tingkat aktivitas vitamin A
Minyak sawit 30.000 -
Wortel 2.000 15
Sayur hijau 685 44
Aprikort 250 120
Tomat 100 300
Nenas 30 1.000
Jeruk (juice) 8 3.750
Sumber : Choo (2000).
2.9 Solvolytic Micellization
Solvolytic micellization (SM) yaitu penyisihan zat yang dikehendaki ke dalam fasa rafinat melalui penambahan suatu pelarut. Kelebihan metoda solvolytic
micellization dibandingkan dengan distilasi dalam pemekatan karoten yang terdapat di dalam metil ester sawit antara lain solvolytic micellization relatif
sederhana, mudah, dapat dilakukan dengan efektif pada kondisi suhu kamar, dan
pelarut utama yang digunakan dapat dengan mudah didaur ulang. Selain itu titik
didih metil ester sawit yang relatif tinggi dan jumlah ester alkil di dalam metil
ester sawit mencapai ribuan kali dari jumlah karotennya. Betapa besar energi yang
diperlukan untuk memekatkan karoten walau hanya dari kadar ppm ke 1%
(10.000 ppm) (Lamria dan Soerawidjaja, 2006). Prinsip penjumputan dengan
SMadalah menyisihkan zat yang dikehendaki ke dalam fase rafinat melalui
penambahan suatu pelarut. Setelah minyak diubah menjadi metil ester maka
karotenoid yang tadinya larut di dalam lemak, sekarang berada di dalam metil
ester.Dengan penambahan pelarut tertentu (umumnya pelarut methanol/atau
etanol sebagai pelarut mayor dan air sebagai pelarut minor) maka terjadi proses
penyisihan. Metanol pelarut mayor akan melarutkan metil ester, sementara
karotenoid karena non polar sulit larut dalam metanol (polar). Air bersifat polar,
sehingga dapat membentuk misel antara methanol dengan ester. Lapisan kaya
ester berada di atas, sedangkan lapisan kaya karotenoid yang berada di bawah.
Lapisan kaya karotenoid diambil, lalu dilakukan analisis kandungan
karotenoidnya.
BAB 3
3.1Bahan-bahan
Bahan-bahan yang digunakan dalam penelitian ini adalah
- Limbah serat pengepresan buah kelapa sawit
- n- Heksana teknis
- n-Heksana p.a E- Merck
- KOH teknis
- Etanol p.a E-Merck
- Metanol p.aE-Merck
- Metanol teknis
- KOH p.a E-Merck
- Na-Metilat p.a E-Merck
- Boron Trifluorida p.a E-Merck
- Iso-Oktan p.a E-Merck
- H2O
- Indikator Phenolpthalen
- Alkohol netral 95%
- Metil oleat yang diperoleh dari laboratorium Oleokimia PPKS Medan.
3.2Alat-alat
Alat-alat yang digunakan dalam penelitian ini adalah
- Wadah berukuran 20 liter
- Kain saringan
- Alat Gelas Kimia
- Cawan porselen
- Labu vial
- Pipet tetes
- Labu leher tiga Pyrex
- Labu ukur Pyrex
- Condensor
- Rotary Evaporator Buchi, R210
- Spektrotometer UV-visible Shimadzu, UV-1700
- Kromatografi Gas Shimadzu, GC-14B
- Hot Plate Stirer Termolyne
- Magnetic stirer
- Desikator
- Fortex Fischer Scientific
- Oven Memmert
- Thermometer
3.3Prosedur Penelitian
Adapun prosedur penelitian yang dilaksanakan dalam penelitian ini meliputi
beberapa tahap yaitu sebagai berikut:
3.3.1. Ekstraksi Minyak
Sebanyak 4 kg limbah serat pengepresan buah kelapa sawit dimasukkan
kedalam wadah kemudian ditambahkan n-heksana teknis dengan perbandingan
1:5 (b/v). Ekstraksi dilakukan dengan cara maserasi selama 24 jam lalu kemudian
disaring, minyak hasil ekstraksi dipekatkan menggunakan alat rotary evaporator
untuk memisahkan minyak dengan n-heksana. Hasil minyak yang diperoleh
dianalisis asam lemak bebas (metode titrasi asam basa) , kadar air (gravimetri) ,
DOBI (Deterioration of Bleachability Index) dan kadar karotennya dengan
menggunakan Spektrofotometer UV-Vis.
3.3.2 Analisa Mutu Minyak
3.3.2.1 Penentuan Kadar Asam Lemak Bebas (% ALB) (AOCS Official Methode ca 5a – 40 (1991)
Sampel ditimbang sebanyak 2,5 g didalam gelas Erlenmeyer kemudian
sebanyak 50 ml ditambahkan alkohol netral 95% dan indikator phenolpthalen 1%
sebanyak 3 tetes. Dititrasi hinggga warna merah muda dengan larutan KOH yang
Vol. KOH x N KOH x 25,6 Asam Lemak Bebas =
Berat Sampel (g)
3.3.2.2 Penentuan Kadar Air (SNI 01-0013-1987, AOCS Official Method Ca 2c-25 (1989)
Minyak sebanyak 10 g dimasukkan ke dalam cawan yang sudah
dikeringkan dan diketahui beratnya. Dipanaskan dalam oven pada suhu 1100C
selama 3 jam pada. Kemudian didinginkan dalam desikator dan ditimbang setiap
30 menit periode pengeringan sampai diperoleh berat konstan dan dihitung
dengan :
Wa - Wb
Kadar Air (%) = x 100 Wa
Dimana : Wa = Berat sampel sebelum dikeringkan
Wb = Berat sampel sesudah dikeringkan
3.3.2.3 Penentuan nilai DOBI (Deterioration of Bleachability Index) (MPOB Test Method p2,9:2004, PORIM Test Method 1995)
Sampel minyak ditimbang sebanyak 0,04 g kemudian dimasukkan ke dalam
labu ukur 10 mL lalu ditambahkan n-heksana p.a sampai tanda garis. Absorbansi
dibaca dengan Spektrofotometer pada panjang gelombang ( λ ) 269 nm dan λ 446
nm.
Absorbance λ = 446 nm DOBI=
3.3.2.4 Penentuan Kadar Karoten (MPOB Test Method p2,9:2004)
Sampel sebanyak 0,0400 g ditambahkan n-heksana p.a dan dimasukkan
kedalam labu ukur 10 ml, kemudian dianalisa dengan Spektrofotometer pada λ =
446 nm.
10 x A x 383 Kandungan Karoten =
Wx 100
Dimana : A = Absorbansi Contoh
W = Berat Contoh (g)
3.3.3.Transesterifikasi
Ke dalam labu leher tiga dimasukkan 100 g minyak hasil ekstraksi lalu
ditambahkan 45 g metanol teknis dan 2,4 g KOH sebagai katalis. Kemudian
diaduk dengan menggunakan hot plate strirer pada suhu 70-800C selama 4 jam.
Hasil pemanasan dipindahkan ke corong pisah dan didiamkan selama 1 malam.
Pada corong pisah terjadi pemisahan antara metil ester berwarna merah dibagian
atas dan gliserol di bagian bawah warna agak hitam. Metil ester pada lapisan atas
mengandung karoten. Bagian bawah dibuang, sedangkan bagian atas metil ester
dicuci dengan air hangat pada suhu 40-60 0C. Jumlah air yang digunakan kira-kira
60% dari jumlah metil ester yang diperoleh. Pencucian dilakukan sebanyak 5 kali
sampai air pencuci berwarna putih bening atau sabun dan gliserol telah bebas dari
metil ester. Pencucian bertujuan untuk menyisihkan sabun dari bagian atau lapisan
yang kaya karoten. Kemudian dilanjutkan uji kandungan ester dengan
menggunakan gas kromatografi. Apabila kandungan ester telah mencapai 90-96%
maka tahapan transesterifikasi telah selesai. Namun bila hasil uji menunjukkan
ester di bawah 90%, maka dilakukan transesterifikasi kembali sampai kandungan
ester 90-96%. Kemudian dianalisis kadar gliserida, ester, DOBI dan kadar
3.3.4. Solvolytic micellization ( Tanpa penambahan metil oleat )
Ke dalam gelas Beaker dimasukkan metil ester asam lemak sebanyak 100
ml yang dihasilkan pada tahap transesterifikasi.Lalu ditambahkan metanol p.a
sebanyak 500 ml kemudian diaduk dengan menggunakan hot plate stirer selama 5
menit lalu ditambahkan air sebanyak 15 ml. Kemudian dimasukkan kedalam
corong pisah, setelah terbentuk 2 lapisan kemudian dipisahkan, lapisan bawah
ditampung pada gelas Erlenmeyer (sebagai kontrol). Setelah proses SMselesai
maka dilanjutkan analisis DOBI dan kadar karotennya.
3.3.4.1.Solvolytic micellization ( dengan penambahan metil oleat )
Ke dalam gelas Beaker dimasukkan metil ester asam lemak sebanyak 100
ml yang dihasilkan pada tahap transesterifikasi.Lalu ditambahkan metanol p.a
sebanyak 500 ml kemudian diaduk dengan menggunakan hot plate stirer selama 5
menit lalu ditambahkan air sebanyak 15 ml dan ditambahkan metil oleat 0,10%
(v/v). Kemudian dimasukkan kedalam corong pisah, setelah terbentuk 2 lapisan
kemudian dipisahkan, lapisan bawah ditampung pada gelas erlenmeyer. Setelah
proses SMselesai maka dilanjutkan analisis DOBI dan kadar karotennya.
Kemudian dilakukan hal yang sama dengan penambahan metil oleat dengan
3.4.Bagan Penelitian 3.4.1.Ekstraksi Minyak
dimasukkan kedalam wadah
ditambahkan n-heksana teknis dengan perbandingan 1:5 (b/v)
direndam selama 24 jam
disaring
didestilasi dengan menggunakan rotary evaporator 4 kg limbah serat pengepressan buah kelapa sawit
Minyak n-heksana
Penentuan Kadar Asam Lemak Bebas
Penentuan Kadar Air
Penentuan Nilai DOBI
Penentuan Kadar Karoten
Limbah serat pengepressan dimaserasi dengan menggunakan buah kelapa sawit pelarut n-heksana selama 24 jam
Menguapkan n-heksana dengan Hasil penyaringan Minyak menggunakan alat
Rotary evaporator
Minyak hasil ekstraksi setelah diuapkan
[image:38.595.129.525.90.662.2]dengan n-heksana
3.4.2. Analisa Mutu Minyak
3.4.2.1. Analisa Kadar Asam Lemak Bebas (% ALB) (AOCS Official Methode ca 5a – 40 (1991)
ditimbang sebanyak 1 g
dimasukkan ke dalam gelas Erlenmeyer
ditambahkan 50 ml alkohol 95%
ditambakan indikator phenolftalein Sebanyak 3 tetes
dititrasi dengan KOH yang telah distandarisasi
dicatat volume KOH yang terpakai Minyak
Larutan merah muda
3.4.2.2. Analisa Kadar Air (SNI 01-0013-1987, AOCS Official Method Ca 2c-25 (1989)
ditimbang sebanyak 5 g
dimasukkan kedalam cawan yang sudah dikeringkan dan diketahui beratnya
diuapkan airnya ke dalam oven pada suhu 1050C selama 3 jam
didinginkan dalam desikator
ditimbang setiap 30 menit periode pengeringan sampai diperoleh berat konstan
Minyak
3.4.2.3. Penentuan Nilai DOBI (Deterioration of Bleachability Index) (MPOB Test Method p2,9:2004, PORIM Test Method 1995)
ditimbang sebanyak 0,0400 g
dimasukkan ke dalam labu ukur 10 ml
ditambahkan n-heksana p.a sampai tanda garis
dimasukkan ke dalam kuvet
dibaca absorbansi dengan spektrofotometer pada panjang
gelombang (λ) = 269 nm dan λ= 446nm
Minyak
3.4.2.4. Penentuan Kadar Karoten (MPOB Test Method p2,9:2004)
Dimasukkan ke dalam labu ukur 10 ml
Ditambahkan n-heksana sampai tanda Garis
Dimasukkan ke dalam kuvet
Dibaca absorbansi pada
Spektrofotometer pada λ = 446 nm Minyak (0,0400 g)
3.4.3. Transesterifikasi
dimasukkan kedalam labu leher tiga
ditambahkan 45 g metanol teknis dan 2,4 g KOH
diaduk pada suhu 70-800C selama 4 jam
dipindahkan ke dalam corong pisah dan didiamkan selama 1 malam
dipisahkan
dicuci dengan air hangat dengan suhu 40 – 600C 100 g minyak hasil ekstraksi
Lapisan atas Lapisan bawah
Metil ester asam lemak
Analisis kadar gliserida dan ester dengan menggunakan
kromatografi gas
Analisis DOBI dan kadar karoten dengan menggunakan
3.4.4.Solvolytic Micellization (Tanpa penambahan metil oleat atau sebagai kontrol)
dimasukkan ke dalam gelas Beaker
ditambahkan metanol 500 ml
diaduk dengan menggunakan hot plate
stirerselama 5 menit
ditambahkan air 15 ml
dimasukkan kedalam corong pisah
ditampung
didalam gelas
Erlenmeyer Metil ester asam lemak (100 ml)
Lapisan atas Lapisan bawah
Hasil
Analisis kadar karoten
3.4.4.1.Solvolytic Micellization (dengan penambahan metil oleat )
dimasukkan ke dalam gelas Beaker
ditambahkan metanol 500 ml
diaduk dengan menggunakan hot plate
stirerselama 5 menit ditambahkan air 15 ml
ditambahkan metil oleat 0,10 % (v/v)
dimasukkan kedalam corong pisah
ditampung didalam
gelas Erlenmeyer
• Dilakukan hal yang sama dengan penambahan metil oleat sawit dengan perlakuan (v/v) : 0,25%; 0,50%; 0,75%.
Metil ester asam lemak (100 ml)
Lapisan atas Lapisan bawah
Hasil
Analisis kadar karoten
BAB 4
HASIL DAN PEMBAHASAN
4.1. Hasil
4.1.1. Kualitas Mutu Minyak Serat
[image:47.595.113.493.231.305.2]Hasil analisis mutu minyak hasil ektraksi dapat dilihat pada Tabel 4.1.
Tabel 4.1.Mutu minyak hasil ekstraksi
Mutu Minyak Hasil 1 Hasil 2 Rata-rata
Kadar Air (%) 6,732 6,903 6,817
Asam Lemak Bebas (%) 9,08 9,41 9,25
DOBI 2,49 2,27 2,38
Kadar Karoten (ppm) 3584 3185 3384,5
4.1.2. Hasil Transesterifikasi
[image:47.595.114.495.408.514.2]Hasilproses transesterifikasi dapat dilihat pada Tabel 4.2.
Tabel 4.2.Kandungan yang diperoleh pada proses transesterifikasi
Kandungan Hasil
Trigliserida (%) 0,60
Digliserida (%) (-)
Monogliserida (%) (-)
Ester (%) 93,61
Karoten (ppm) 5737
DOBI 3,13
(-) = tidak terdeteksi
4.1.3. HasilSolvolytic Micellization
Hasil pada proses solvolytic micellizationdapat dilihat pada Tabel 4.3.
Tabel 4.3.Hasil proses solvolytic micellization
Proses Konsentrasi Karoten (ppm) DOBI
[image:47.595.113.489.612.712.2]4.2 Pembahasan
4.2.1. Kualitas Mutu Minyak
Dari hasil analisis yang telah dilakukan, diperoleh kadar asam lemak bebas
(ALB) pada minyak hasil ekstraksi limbah serat pengepresan buah kelapa sawit
sebesar 9,2502%. Berdasarkan ICBS, 2000 (Tabel 2.6) standar maksimal dari
asam lemak bebas adalah 5%, tingginya nilai ALB yang diperoleh dari hasil
ekstraksi limbah dapat disebabkan oleh tingginya kadar air pada minyak hasil
ekstraksi yaitu sebesar 6,8175% sedangkan maksimal standar kadar air
berdasarkan ICBS, 2000 adalah sebesar 0,15%.
Kadarairadalahjumlahairyangterkandungdalam minyakyang menentukan mutu
sampel minyak. Semakin rendah kadar air, maka kualitas minyak tersebut
semakin baik. Hal ini disebabkan, adanya air dalam minyakdapat
memicureaksihidrolisisyangmenyebabkan
penurunanmutuminyak.Reaksihidrolisismenyebabkanpemecahantrigliseridamenja
digliseroldanasam lemak. Reaksi ini dipercepat oleh basa, asam, dan enzim.
Minyak yang terhidrolisis
titikasapnyamenurundanmakananyangdigorengakanmenjadicoklat(Winarno,1997)
. Menurut Siahaan, dkk (2008), semakin banyak kandungan air maka semakin tinggi juga kandungan ALB pada minyak. Hal ini disebabkan kandungan air pada
minyak mempercepat hidrolisa trigliserida, memberikan kondisi yang baik bagi
mikroba dan mempengaruhi densitas minyak.DOBI dan karoten ditentukan untuk
memenuhi standart mutu CPO yang baik, karena semakin tinggi nilai DOBI dan
karoten maka semakin baik kualitas CPO, sehingga daya jual CPO semakin
tinggi. Berdasarkan hasil penelitian yang telah dilakukan bahwasanya kadar
karoten yang diperoleh yaitu 3384 ppm. Nilaiinisudah
beradadiatasnilaiyangdinyatakandalamChoo, 2000 (tabel 2.4.)yaitu500-700 ppm.
Nilai DOBI yang diperoleh untuk hasil ekstraksi minyak dari limbah serat
pengepressan buah kelapa sawit yaitu 2,38 hasil ini menunjukkan bahwa minyak
dari hasil ekstraksi ini masih memenuhi standart. Menurut ICBS, 2000 (Tabel 2.6)
4.2.2. Hasil Transesterifikasi
Pada analisis kandungan ester dan gliserida pada proses transesterifikasi
terlihat bahwa kandungan trigliserida 0,60 % dan tidak mengandung digliserida
dan monogliserida, namun proses tersebut menghasilkan produk ester sebesar
93,61%. Hal tersebut dapat terjadi karena trigliserida telah terkonversi menjadi
gliserida ester (Khalid & Khalid, 2011) dan menurut Hasibuan, dkk (2012), proses
transesterifikasi dengan kadar ester di atas 90% menunjukkan bahwa proses
tersebut telah berhasil.
Kadar karoten yang diperoleh setelah proses transesterifikasi adalah 5737
ppm, kadar karoten pada proses transeterifikasi ini semakin meningkat
dibandingkan dengan kadar karoten yang diperoleh pada proses ekstraksi yang
hanya diperoleh sebesar 3384 ppm. Ini menunjukan bahwa pada proses
transesterifikasi karoten semakin pekat. Hal ini karena proses transesterifikasi
mengubah molekul besar dari trigliserida menjadi molekul lebih sederhana yaitu
metil ester asam lemak yang tingkat kelarutannya jauh lebih tinggi, sehingga
karoten lebih mudah dipisahkan dan dilarutkan (Othman et al, 2010). Nilai DOBI
yang diperoleh pada proses transesterifikasi yaitu sebesar 3,13, nilai DOBI pada
proses ini semakin meningkat dibandingkan dengan nilai DOBI yang diperoleh
pada minyak hasil ektsraksi.
4.2.3. Proses Solvolytic Micellization
Pada analisis kadar karoten yang dimulai dari proses ekstraksi minyak
diperoleh kadar karoten sebesar 3384 ppm dan pada proses transesterifikasi
selanjutnya peningkatan kadar karoten tidak terlalu jauh mengalami peningkatan
yaitu sebesar 5737 ppm, namun lebih terlihat jelas peningkatan kadar karoten
setelah dilanjutkan dengan proses solvolytic micellization dengan penambahan
metil oleat. Pada solvolytic micellization dengan metil oleat 0 % (tanpa
penambahan metil oleat) diperoleh kadar karoten sebesar 26564 ppm, dengan
penambahan metil oleat 0,10% kadar karoten sebesar 27730, dengan penambahan
0,50% sebesar 30406 dan dengan penambahan metil oleat 0,75 % sebesar 29987.
Terlihat jelas bahwa pemekatan karoten pada proses solvolytic
micellizationdengan menggunakan metil oleat 0,50% diperoleh kadar karoten yang tinggi, hal tersebut terjadi karena metil oleat mampu meningkatkan
kestabilan karoten dalam proses SM (Premavalli and Arya, 1985).Metil oleat 0,50
% menghasilkan karoten sebesar 30406 ppm, hasil tersebut karena pemisahan
lapisan ester dari lapisan karoten lebih tinggi dibandingkan konsentrasi metil oleat
BAB 5
KESIMPULAN DAN SARAN
5.1. Kesimpulan
1. Konsentrasi yang optimum yang diperoleh adalah pada penambahan metil oleat 0,50% dengan kadar karoten 30406 ppm.
5.2. Saran
DAFTAR PUSTAKA
AOCS, 1989, Official Methods and Recomended Practices of the American Oil Chemistry Society, 4thed, Broadmaker Drive, Champaign Illinois.
Asnawi,T., M., M. D.Supardandan A,Fuandi.2009.Ekstraksi Karoten DariLimbah Cair PabrikKelapa Sawit Menggunakan GelombangUltrasonik. Laporan Penelitian. Nanggroe Aceh Darusalam. Fakultas Teknik :Universitas Syahkuala.
Berk, Z. 1983. The biochemistry of foods. Elsevier Scientific Publishing Company, New York.
Bernasconi, G., Gerster, H., Hauser, H., Stauble, H., and Schneiter, E. 1995. Teknologi kimia. Bagian 2. Terjemahan Lienda Handojo. Pradnya Paramita: 177-186
Choo, Y. M., S. C. Yap, C. K. Ooi, S. H. Goh, and S. H. Ong. 1996. Recovered Oil From Palm Pressed Fibre. A Good Source of Natural Carotenoids, Vitamin E and sterol. J. Amer. Oil. Chem. Soc. Vol 73:599-602.
Choo, Y., M. 2000. Specialty Products Carotenoids. Advances In Oil Palm Research Vol II (Editor: Y. Basiron, B.S. Jalani, and K.W. Chan) Malaysia Palm Oil Board. pp 1036-1060
Desiana. 2000. Ekstraksi pigmen karotenoid dari limbah udang Windu. Skripsi. Bogor: Institut Pertanian Bogor.
Ditjen PPH Departemen Pertanian. 2006. Pedoman pengelolaan limbah industry sawit, Jakarta.
FennemaO.R.1996.FoodChemistryThirdEdition.MarcelDekkerInc.,New York.
Freedman,B.,Pryde.E.H.,Mounts.T.L.,1984,VariablesAffectingtheYieldsofFattyEs ters from Transesterfied VegetableOils. JAOCS 61 (10) : 1638-1643
Freedman, B., Butterfield, R. O., dan Pryde, E. H. 1986. Transesterification
Kinetics of Soybean Oil, J. Am. Oil Chem. Soc, 63(10): 1375-80
Food and Agricultural Policy Research. 2010. Food and agricultural commodities production statistics: Indonesia and Production Indices (faostat.fao.org).
Adicita Karya Nusa.
Hasibuan, H.A., Herawan, T., and Rivani, M. 2010. Recovery of Palm Fatty Acid Alkyl Ester by Short Part Distillation. Poceedings International Oil Palm Conference. 1-3 June 2010. Jogjakarta. 345-353
Heriyanto dan Limantara, L. 2009. Produksi karotenoid oleh Khamir Rhodotorula sp”. Eksplanasi volume 4 Nomor 7. Hal 1-3
Henrikson,R,(2009),“EarthFoodSpirulinaHowthisremarkablebluegreenalgaecant ransform your health and our planet”,RonoreEnterprises,Inc. , Hawaii, USA.
ICBS.2000.Studi Tentang Produksi, Pemasaran, Konsumsi & Investasi Minyak Kelapa Sawit Indonesia. Jakarta
Indonesia-Investments. 2015. Minyak Kelapa Sawit
Kembaren. R dan I. K Sahputra. 2012. Isolasi dan nanoenkapsulasi karotenoid limbah serat buah kelapa sawit. Prosiding Seminar ilmiah se-Eropah. Berkarya untuk Indonesia. ISBN:9772302690005 hal. 11-13.
Ketaren. 1986. Pengantar minyak dan lemak Pangan (Cetakan I).Jakarta : UI-Press.
Khalid,K.,andKhalid,K.2011.Transesterification of Palm Oil for the Production of Biodiesel. American Journal of Applied Sciences. 8(8): 804-809.
Lamria, M. dan Soerawidjaja, T.H. 2006. Solvolytic Micellization dalam penjumputan karoten dari biodiesel. Bandung: Fakultas Teknologi Industri, ITB.
Lamria, M. Dan Soerawidjaja, T.H., (2005), “Kajian Produksi Terpadu karoten, Vitamin E, dan Biodiesel dari Minyak Sawit Mentah”, Prosiding Seminar Teknik Kimia Soehadi Reksowardojo, Institut Teknologi Bandung, Bandung, 230-237.
Mahfud, M. K., R. Rozanna, dan Hermana. 1991. Emulsi karoten Minyak Kelapa Sawit Sebagai Pewarna Makanan. Vol 14: 99-105
Manurung, R., 2006, Transesterifikasi Minyak Nabati, Jurnal Teknologi Proses USU. 5(1) : 47-52.
MortensenA.,(2006),“CarotenoidsandotherpigmentnaturalColorants”,PureAppl.Ch em., Vol. 78, No. 8, pp. 1477–1491.
MPOB.2004.MPOB Test Method: A Compendium of Test on Palm Oil Products, Palm Kernel Products, Fatty Acids, Food Related Products and Others. Malaysia
Naibaho, P. M. 1998. Teknologi Pengolahan Kelapa Sawit. Pusat Penelitian Kelapa Sawit. Medan. 278 hal
Naibaho, P. M., Siahaan, D dan Yudhanto, B. G. 2006. Pabrik Kelapa Sawit. In: Teknologi pengolahan kelapa sawit dan produk turunannya. Editor: B. Sulistyo, A. Purba, D. Siahaan, dan R. Harahap. Pusat Penelitian Kelapa Sawit, Medan. 147 halaman.
Othman, N., Manan, Z.A., Wan Alwi, S.R., and Sarmidi , M.R. 2010. A Review of Extraction Technology for Carotenoids and Vitamin E Recovery from Palm Oil. Journal of Applied Sciences.10: 1187-1191.
Pahan., I.2008.Panduan Lengkap Kelapa Sawit. Jakarta.Penebar Swadaya
Panjaitan, F. R., Siahaan, D., Herawan, T., Rivani, M dan Hasibuan, H. A. 2008. Studi Awal Penjumputan Karoten Sawit dengan Teknik Solvolytic Micellization Menggunakan Pelarut Mayor Etanol. J. Penelitian Kelapa Sawit.16(3):163-170.
PORIM.1995.PORIM test methods.Palm Oil Research Institute of Malaysia. Ministry of Primary Industries. Malaysia
Premavalli, K.S and Arya, S.S. 1985.Stability of Watermelon Carotenoid Extract in Isolated Model System. Journal of Food Technology. 20 (3) : 359-366
PTPN IV.2009. Buku Panduan Pedoman Operasional Pengolahan Kelapa Sawit.
Ravi,M.,De,SaiL.,Azharuddin, S., Paul, SolomonF.D., (2010), “Thebeneficialeffectsof spirulinafocusingonitsimmunomodulatory andantioxidantproperties”,Nutritionand Dietary Supplements 2010, 2, pp. 73–83, DoveMedical PressLtd.
Risza, S. 1994. Kelapa Sawit ; Upaya Peningkatan Produktivitas. Yogyakarta: Kanisius
Siahaan, D., Hasibuan, H., Panjaitan, F., Rivani, M. 2008. Karakteristik CPO Indonesia. Warta PPKS. Medan .16(1) : 27 -37
Siahaan, D. 2006. Nilai DOBI CPO Indonesia. Laporan Tahunan 2006.PPKS.Medan
Sivarao, Kumar, N., Widodo, W. S., and Haery Sihombing. 2012. Hexane economization in palm oil kernel oil plant: A study after process design improvement. Global Engineers and Technologists Review vol.2 No.12
Sunarwan, B., Juhana, R.,2013.Pemanfaatan Limbah Sawit untuk Bahan Bakar Energi Baru dan Terbarukan (EBT). Jurnal Tekno Insentif Kopwild.7(2):1-14
Sundram, K. And N. Chandrasekharan. 1997. Minor components in edible oils and fats : Their Components of Palm Oil. Malaysian Palm Oil at AOCS 1997, Seattle, Washington.
Sundram, K., R. Sambathamurthi, and Y. A. Tan. 2003. Palm Fruit Chemistry and
Nutrition. Asia Pasific J. Clinical Nutrition,12 (3):355-362
Supardan, M. D., T. M. Asnawi, Y. Putri, dan S. Wahyuni. 2011. Metode ekstraksi pelarut berbantuan ultrasonik untuk recovery minyak dari limbah cair pabrik kelapa sawit. Agritech. Vol.:31 No.4.
Tobing,P.L., Naibaho, P. 1993. Peningkatan Efisiensi Pengolahan Limbah Pabrik Kelapa Sawit (LKPS) dengan Sistem Kolam. Kumpulan Makalah Forum Komunikasi Kelapa Sawit I, Pusat Penilitian Kelapa Sawit. Medan. Hal : 71-81.
Lampiran 1.Hasil analisa kadar air dan kadar asam lemak bebas
1. Kadar air minyak hasil ekstraksi
a. % air = berat minyak sebelum dikeringkan – berat minyak setelah dikeringkan
x100 Berat minyak sebelum dikeringkan
= 5,0226 g – 4,6845 g x 100 5,0226 g
= 6,732 %
b. % air = berat minyak sebelum dikeringkan – berat minyak setelah dikeringkan
x100 Berat minyak sebelum dikeringkan
= 5,0268 g – 4,6798 g x 100 5,0268 g
= 6,903 %
2. Kadar Asam Lemak Bebas ( % ALB)
Vol. KOH x N KOH x 25,6 a. Asam Lemak Bebas (%) =
Berat Sampel (g)
3,2 ml x 0,1151 N x 25,6 =
1,0381 g
= 9,08
Vol. KOH x N KOH x 25,6 b. Asam Lemak Bebas (%) =
3,3 ml x 0,1151 N x 25,6 =
1,0325 g
= 9,41
3. Kandungan Karoten
10 x A x 383
a. Kandungan Karoten =
W x 100
10 x 0,0189 x 383 = 0,000202 x 100
= 3583,51 ppm
10 x A x 383
a. Kandungan Karoten = W x 100
10 x 0,0168 x 383 = 0,0202 x 100
= 3185,34 ppm
4. DOBI
Absorbance λ = 446 nm a. DOBI =
Absorbance λ = 269 nm
0,0189 =
0,0076
= 2,49
Absorbance λ = 446 nm b. DOBI =
Absorbance λ = 269 nm
0,0168 =
0,0074
Lampiran 3. Data Spektrofotometer untuk Analisa Kandungan Karoten
Sampel Berat
Sampel
Berat*100 WL 446 ppm
Karoten Rata-rata Ekstrak Minyak Ester Kontrol 0%
0,1% - Solvo
0,25% - Solvo
0,50% - Solvo
0,75% - Solvo
Lampiran 4.Data Spektrofotometer untuk Analisa DOBI
Sampel WL 446 WL 269 DOBI Rata-rata Deviasi
Ekstrak Minyak
Ester
Kontrol 0%
0,10% - Solvo