ISOLASI DAN ANALISIS KOMPONEN
MINYAK ATSIRI DARI RIMPANG TEMU KUNCI
(Boesenbergia rotunda (L.) Mansf.)
SEGAR DAN KERING SECARA GC-MS
SKRIPSI
OLEH:
KRISTIANTO S. SIMBOLON NIM 081501036
PROGRAM STUDI SARJANA FARMASI
FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA
MEDAN
ISOLASI DAN ANALISIS KOMPONEN
MINYAK ATSIRI DARI RIMPANG TEMU KUNCI
(Boesenbergia rotunda (L.) Mansf.)
SEGAR DAN KERING SECARA GC-MS
SKRIPSI
Diajukan untuk melengkapi salah satu syarat untuk memperoleh gelar Sarjana Farmasi pada Fakultas Farmasi
Universitas Sumatera Utara OLEH:
KRISTIANTO S. SIMBOLON NIM 081501036
PROGRAM STUDI SARJANA FARMASI
FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA
MEDAN
PENGESAHAN SKRIPSI
ISOLASI DAN ANALISIS KOMPONEN
MINYAK ATSIRI DARI RIMPANG TEMU KUNCI
(Boesenbergia rotunda (L.) Mansf.)
SEGAR DAN KERING SECARA GC-MS
OLEH:
KRISTIANTO S. SIMBOLON NIM 081501036
Dipertahankan di hadapan Panitia Penguji Skripsi Fakultas Farmasi Universitas Sumatera Utara
Pada Tanggal : 20 Juli 2013
Pembimbing I, Panitia Penguji,
Dr. M. Pandapotan Nasution, MPS., Apt. Prof. Dr. rer. nat. Effendy De Lux Putra, S.U., Apt.
NIP 194908111976031001 NIP 195306191983031001
Pembimbing II, Dr. M. Pandapotan Nasution, MPS., Apt.
NIP 194908111976031001
Dra. Herawaty Ginting, M.Si, Apt. Dr. Marline Nainggolan, M.S., Apt.
NIP 195112231980032002 NIP 195709091985112001
Drs. Panal Sitorus, M.Si., Apt. NIP 195310301980031002
Medan, Januari 2014 Fakultas Farmasi
Universitas Sumatera Utara Dekan,
KATA PENGANTAR
Puji dan syukur kehadirat Tuhan Yang Maha Esa, karena limpahan
rahmat, kasih dan karuniaNya, sehingga penulis dapat menyelesaikan skripsi ini
yang berjudul ”Isolasi dan Analisis Komponen Minyak Atsiri dari Rimpang Temu
Kunci (Boesenbergia Rotunda (L.) Mansf.) Segar dan Kering Secara GC-MS”.
Skripsi ini diajukan sebagai salah satu syarat untuk memperoleh gelar sarjana
farmasi pada Fakultas Farmasi Universitas Sumatera Utara.
Pada kesempatan ini penulis mengucapkan terima kasih yang tulus dan
ikhlas kepada Bapak Prof. Dr. Sumadio Hadisahputra, Apt., selaku Dekan
Fakultas Farmasi USU Medan yang telah memberikan fasilitas sehingga penulis
dapat menyelesaikan pendidikan. Bapak Dr. M. Pandapotan Nasution, MPS.,
Apt., dan Ibu Dra. Herawaty Ginting, M.Si., Apt., selaku pembimbing yang telah
memberikan waktu, bimbingan, dan nasehat selama penelitian hingga selesainya
penyusunan skripsi ini serta kepada Bapak Drs. Panal Sitorus, M.Si., Apt., selaku
penasehat akademis yang telah memberikan bimbingan kepada penulis. Bapak
Prof. Dr. rer. nat. Effendy De Lux Putra, S.U., Apt., Ibu Dr. Marline Nainggolan,
M.S., Apt., dan Bapak Drs. Panal Sitorus, M.Si., Apt., selaku dosen penguji yang
telah memberikan saran dan arahan kepada penulis dalam menyelesaikan skripsi
ini. Kepada Bapak dan Ibu staf pengajar Fakultas Farmasi USU yang telah
mendidik selama perkuliahan serta Ibu kepala Laboratorium Farmakognosi dan
Laboratorium Penelitian yang telah memberikan bantuan dan fasilitas selama
Penulis juga mengucapkan terima kasih dan penghargaan yang tiada
terhingga kepada Ayahanda dan Ibunda tercinta, O. Simbolon dan L. Hutapea,
yang tiada hentinya berkorban dengan tulus ikhlas bagi kesuksesan penulis, juga
kepada adik-adikku yang selalu setia memberi doa, dukungan dan motivasi selama
melakukan penelitian.
Penulis menyadari skripsi ini masih belum sempurna, oleh karena itu
diharapkan kritik dan saran yang membangun untuk penyempurnaannya. Harapan
saya semoga skripsi ini dapat bermanfaat bagi ilmu pengetahuan kefarmasian.
Medan, Juli 2013 Penulis
ISOLASI DAN ANALISIS KOMPONEN MINYAK ATSIRI DARI RIMPANG TEMU KUNCI (Boesenbergia rotunda (L.) Mansf.)
SEGAR DAN KERING SECARA GC-MS
ABSTRAK
Minyak atsiri merupakan minyak yang mudah menguap dengan komposisi yang berbeda-beda sesuai tumbuhan penghasilnya dan terdiri dari campuran zat yang memiliki sifat fisika kimia yang berbeda-beda. Temu kunci (Boesenbergia rotunda (L.) Mansf.) suku Zingiberaceae adalah tanaman yang mengandung minyak atsiri dan banyak dimanfaatkan masyarakat sebagai bumbu masakan. Penelitian yang dilakukan ini meliputi karakterisasi simplisia, isolasi minyak atsiri dengan cara destilasi air dan analisis komponen minyak atsiri secara Gas Chromatography-Mass Spectrometry (GC-MS) dari rimpang temu kunci segar dan simplisia temu kunci.
Hasil pemeriksaan karakteristik simplisia rimpang temu kunci diperoleh kadar air 6,65%; kadar sari yang larut dalam air 12,45%; kadar sari yang larut dalam etanol 7,95%; kadar abu total 7,19%; kadar abu yang tidak larut dalam asam 2,83%; hasil penetapan kadar minyak atsiri dengan alat Stahl diperoleh kadar minyak atsiri rimpang temu kunci segar sebesar 0,19% v/b, dan kadar minyak atsiri simplisia temu kunci sebesar 1,02% v/b. Hasil penetapan indeks bias minyak atsiri rimpang temu kunci segar diperoleh sebesar 1,488 dan indeks bias minyak atsiri simplisia temu kunci sebesar 1,482. Bobot jenis minyak atsiri rimpang temu kunci segar sebesar 0,9805 dan bobot jenis minyak atsiri simplisia temu kunci sebesar 0,8533.
Hasil analisis GC-MS minyak atsiri yang diperoleh dari rimpang temu kunci segar menunjukkan 31 komponen dan terdapat 11 senyawa sebagai komponen utama yaitu: kamfor (21,20%); 1,8-sineol (14,83%); nerol (10,48%); metil sinamat (8,28%); trans-β-osimen (8,22%); kamfen (6,83%); sitral (5,12%); limonen (4,39%); kamfen hidrat (4,18%); linalool (3,91%); z-sitral (2,39%). Sedangkan hasil analisis GC-MS minyak atsiri yang diperoleh dari simplisia temu kunci menunjukkan 26 komponen dan terdapat 9 senyawa sebagai komponen utama yaitu: trans-β-osimen (25,30%); 1,8-sineol (17,50%); kamfor (16,24%); nerol (13,20%); kamfen (6,81%); 1-limonen (3,65%); metil sinamat (3,52%); linalool (2,48%) dan kamfen hidrat (2,29%). Ternyata terdapat perbedaan komposisi minyak atsiri dari rimpang temu kunci segar dan simplisia.
ISOLATION AND CHEMICAL COMPOSITION OF VOLATILE OIL OF FRESH AND DRIED RHIZOME OF FINGER ROOT
(Boesenbergia rotunda (L.) Mansf.)
ABSTRACT
Essential oils are volatile oils with different composition in accordance with the source and consist of a mixture of compounds of different physicochemical properties. Finger root (Boesenbergia rotunda (L.) Mansf.), of the family Zingiberaceae is one of the plants that contain essential oil which is used as a food flavoring. This research included the characterization of rhizome simplex, isolation of essential oil by water distillation and analysis of essential oil components by Gas Chromatography-Mass Spectrometry (GC-MS) of fresh rhizome and its simplex.
Results of simplex characterization gave water content 6.65%, water-soluble extractive 12.45%, ethanol-soluble extractive 7.95%, total ash value 7.19%, acid insoluble ash 2.83%, the volatile oil content of fresh finger root 0.19% v/w, and the volatile oil content of simplex finger root 1.02% v/w. The refractive index of volatile oil of fresh finger root was 1.488 and the refractive index of volatile oil of simplex finger root was 1.482. Specific gravity of fresh finger root was 0.9805 and specific gravity of simplex finger root was 0.8533.
The result of GC-MS analysis of volatile oil of fresh finger root gave 31 compounds, with 11 main components, i.e. camphor (21.20%), 1.8-cineol (14.83%), nerol (10.48%), methyl cinnamate (8.28%), trans-β-ocimene (8.22%), camphene (6.83%), citral (5.12%), 1-limonene (4.39%), camphene hydrate (4.18%), linalool (3.91%), z-citral (2.39%). Chemical composition of volatile oil from simplex of finger root consisted of 26 compounds, with 9 main components, i.e. trans-β-ocimene (25.30%), 1.8-cineol (17.50%), camphor (16.24%), nerol (13.20%), camphene (6.81%), 1-limonene (3.65%), methyl cinnamate (3.52%), linalool (2.48%), and camphene hydrate (2.29%). It turns out that there are differences of composition the volatile oil of fresh finger root and simplex.
DAFTAR ISI
Halaman
JUDUL ... i
HALAMAN JUDUL ... ii
PENGESAHAN SKRIPSI ... iii
KATA PENGANTAR ... iv
ABSTRAK ... vi
ABSTRACT ... vii
DAFTAR ISI ... viii
DAFTAR TABEL ... xii
DAFTAR GAMBAR ... xiii
DAFTAR LAMPIRAN ... xiv
BAB I PENDAHULUAN ... 1
1.1 Latar Belakang ... 1
1.2 Perumusan Masalah ... 3
1.3 Hipotesis ... 3
1.4 Tujuan Penelitian ... 4
1.5 Manfaat Penelitian ... 4
BAB II TINJAUAN PUSTAKA ... 5
2.1 Uraian Tumbuhan ... 5
2.1.1 Daerah Tumbuh ... 5
2.1.2 Sistematika Tumbuhan ... 5
2.1.4 Morfologi Tumbuhan ... 6
2.1.5 Kandungan Kimia ... 7
2.1.6 Penggunaan Tumbuhan ... 7
2.2 Minyak Atsiri ... 8
2.2.1 Lokalisasi minyak atsiri ... 8
2.2.2 Aktivitas biologi minyak atsiri dan penggunaan ... 8
2.2.3 Komposisi kimia minyak atsiri ... 9
2.3 Cara Isolasi Minyak Atsiri ... 10
2.3.1 Metode penyulingan ... 10
2.3.2 Metode pengepresan ... 11
2.3.3 Ekstraksi dengan pelarut menguap ... 11
2.3.4 Ekstraksi dengan lemak padat ... 11
2.3.5 Metode ecuelle ... 12
2.4 Analisis Komponen Minyak Atsiri dengan GC-MS ... 12
2.4.1 Kromatografi gas ... 13
2.4.1.1 Gas pembawa ... 14
2.4.1.2 Sistem injeksi ... 15
2.4.1.3 Kolom ... 15
2.4.1.4 Fase diam ... 16
2.4.1.5 Suhu ... 16
2.4.1.5.1 Suhu injektor ... 16
2.4.1.5.2 Suhu kolom ... 16
2.4.1.5.3 Suhu detektor ... 17
2.4.2 Spektrometri massa ... 17
BAB III METODE PENELITIAN ... 19
3.1 Alat dan Bahan ... 19
3.1.1 Alat-alat ... 19
3.1.2 Bahan-bahan ... 19
3.2 Pengumpulan dan Pengolahan Sampel ... 20
3.2.1 Pengambilan bahan ... 20
3.2.2 Identifikasi tumbuhan ... 20
3.2.3 Pengolahan simplisia ... 20
3.3 Pemeriksaan Karakteristik Simplisia ... 21
3.3.1 Pemeriksaan makroskopik ... 21
3.3.2 Pemeriksaan mikroskopik ... 21
3.3.3 Penetapan kadar air ... 21
3.3.4 Penetapan kadar sari larut dalam air ... 22
3.3.5 Penetapan kadar sari larut dalam etanol ... 22
3.3.6 Penetapan kadar abu total ... 23
3.3.7 Penetapan kadar abu yang tidak larut dalam asam ... 23
3.3.8 Penetapan kadar minyak atsiri ... 23
3.4 Isolasi Minyak Atsiri ... 24
3.5 Identifikasi Minyak Atsiri ... 24
3.5.1 Penetapan parameter fisika ... 24
3.5.1.1 Penentuan indeks bias ... 24
3.5.1.2 Penentuan bobot jenis ... 25
BAB IV HASIL DAN PEMBAHASAN ... 27
4.1 Identifikasi Tumbuhan ... 27
4.2 Hasil Karakterisasi Simplisia ... 27
4.2.1 Pemeriksaan makroskopik simplisia ... 27
4.2.2 Pemeriksaan mikroskopik serbuk simplisia ... 27
4.2.3 Pemeriksaan karakteristik simplisia ... 27
4.3 Identifikasi Minyak Atsiri ... 30
4.4 Analisis dengan GC-MS ... 31
4.5 Analisis dan Fragmentasi Hasil Spektrometri Massa ... 33
BAB V KESIMPULAN DAN SARAN ... 46
5.1 Kesimpulan ... 46
5.2 Saran ... 47
DAFTAR PUSTAKA ... 48
DAFTAR TABEL
Tabel Halaman
4.1 Hasil karakterisasi serbuk simplisia temu kunci ... 28
4.2 Hasil penetapan kadar minyak atsiri ... 29
4.3 Hasil penentuan indeks bias dan bobot jenis minyak atsiri ... 30
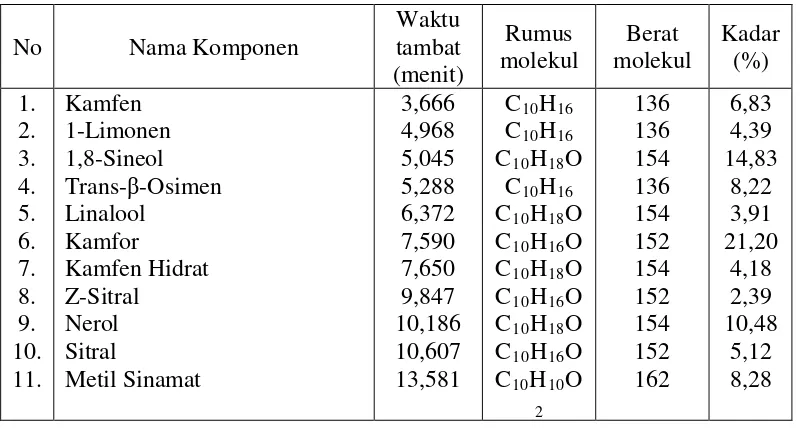
4.4 Waktu tambat dan kadar komponen minyak atsiri hasil analisis
GC-MS dari rimpang temu kunci segar ... 32
4.5 Waktu tambat dan kadar komponen minyak atsiri hasil analisis
DAFTAR GAMBAR
Gambar Halaman
4.1 Rumus bangun Kamfor ... 33
4.2 Rumus bangun 1,8-Sineol ... 34
4.3 Rumus bangun Nerol ... 35
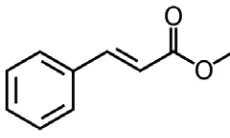
4.4 Rumus bangun Metil Sinamat ... 35
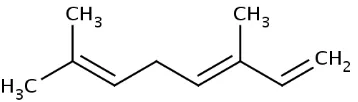
4.5 Rumus bangun Trans-β-Osimen ... 36
4.6 Rumus bangun Kamfen ... 37
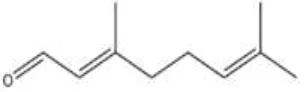
4.7 Rumus bangun Sitral ... 37
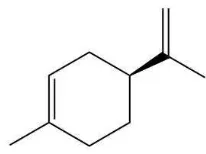
4.8 Rumus bangun 1-Limonen ... 38
4.9 Rumus bangun Kamfen Hidrat ... 39
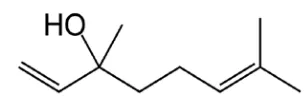
4.10 Rumus bangun Linalool ... 39
DAFTAR LAMPIRAN
5 Gambar mikroskopik serbuk simplisia rimpang temu kunci medium kloralhidrat ... 55
6 Gambar mikroskopik serbuk simplisia rimpang temu kunci medium air ... 56
7 Bagan kerja penelitian ... 57
8 Perhitungan penetapan kadar air dari simplisia rimpang temu kunci ... 58
9 Perhitungan penetapan kadar sari larut air simplisia rimpang temu kunci ... 59
10 Perhitungan penetapan kadar sari larut etanol simplisia rimpang temu kunci ... 60
11 Perhitungan penetapan kadar abu total simplisia rimpang temu kunci ... 61
12 Perhitungan penetapan kadar abu tidak larut asam simplisia rimpang temu kunci ... 62
13 Perhitungan penetapan kadar minyak atsiri ... 63
14 Perhitungan penetapan indeks bias ... 64
15 Penentuan bobot jenis minyak atsiri ... 65
16 Gambar alat yang digunakan ... 66
18 Gambar kromatogram komponen minyak atsiri simplisia rimpang temu kunci ... 70
19 Gambar spektrum massa komponen minyak atsiri rimpang temu
kunci segar ... 72
20 Gambar spektrum massa komponen minyak atsiri simplisia
rimpang temu kunci ... 78
21 Gambar pola fragmentasi komponen minyak atsiri rimpang temu
kunci segar ... 83
22 Gambar pola fragmentasi komponen minyak atsiri simplisia
ISOLASI DAN ANALISIS KOMPONEN MINYAK ATSIRI DARI RIMPANG TEMU KUNCI (Boesenbergia rotunda (L.) Mansf.)
SEGAR DAN KERING SECARA GC-MS
ABSTRAK
Minyak atsiri merupakan minyak yang mudah menguap dengan komposisi yang berbeda-beda sesuai tumbuhan penghasilnya dan terdiri dari campuran zat yang memiliki sifat fisika kimia yang berbeda-beda. Temu kunci (Boesenbergia rotunda (L.) Mansf.) suku Zingiberaceae adalah tanaman yang mengandung minyak atsiri dan banyak dimanfaatkan masyarakat sebagai bumbu masakan. Penelitian yang dilakukan ini meliputi karakterisasi simplisia, isolasi minyak atsiri dengan cara destilasi air dan analisis komponen minyak atsiri secara Gas Chromatography-Mass Spectrometry (GC-MS) dari rimpang temu kunci segar dan simplisia temu kunci.
Hasil pemeriksaan karakteristik simplisia rimpang temu kunci diperoleh kadar air 6,65%; kadar sari yang larut dalam air 12,45%; kadar sari yang larut dalam etanol 7,95%; kadar abu total 7,19%; kadar abu yang tidak larut dalam asam 2,83%; hasil penetapan kadar minyak atsiri dengan alat Stahl diperoleh kadar minyak atsiri rimpang temu kunci segar sebesar 0,19% v/b, dan kadar minyak atsiri simplisia temu kunci sebesar 1,02% v/b. Hasil penetapan indeks bias minyak atsiri rimpang temu kunci segar diperoleh sebesar 1,488 dan indeks bias minyak atsiri simplisia temu kunci sebesar 1,482. Bobot jenis minyak atsiri rimpang temu kunci segar sebesar 0,9805 dan bobot jenis minyak atsiri simplisia temu kunci sebesar 0,8533.
Hasil analisis GC-MS minyak atsiri yang diperoleh dari rimpang temu kunci segar menunjukkan 31 komponen dan terdapat 11 senyawa sebagai komponen utama yaitu: kamfor (21,20%); 1,8-sineol (14,83%); nerol (10,48%); metil sinamat (8,28%); trans-β-osimen (8,22%); kamfen (6,83%); sitral (5,12%); limonen (4,39%); kamfen hidrat (4,18%); linalool (3,91%); z-sitral (2,39%). Sedangkan hasil analisis GC-MS minyak atsiri yang diperoleh dari simplisia temu kunci menunjukkan 26 komponen dan terdapat 9 senyawa sebagai komponen utama yaitu: trans-β-osimen (25,30%); 1,8-sineol (17,50%); kamfor (16,24%); nerol (13,20%); kamfen (6,81%); 1-limonen (3,65%); metil sinamat (3,52%); linalool (2,48%) dan kamfen hidrat (2,29%). Ternyata terdapat perbedaan komposisi minyak atsiri dari rimpang temu kunci segar dan simplisia.
ISOLATION AND CHEMICAL COMPOSITION OF VOLATILE OIL OF FRESH AND DRIED RHIZOME OF FINGER ROOT
(Boesenbergia rotunda (L.) Mansf.)
ABSTRACT
Essential oils are volatile oils with different composition in accordance with the source and consist of a mixture of compounds of different physicochemical properties. Finger root (Boesenbergia rotunda (L.) Mansf.), of the family Zingiberaceae is one of the plants that contain essential oil which is used as a food flavoring. This research included the characterization of rhizome simplex, isolation of essential oil by water distillation and analysis of essential oil components by Gas Chromatography-Mass Spectrometry (GC-MS) of fresh rhizome and its simplex.
Results of simplex characterization gave water content 6.65%, water-soluble extractive 12.45%, ethanol-soluble extractive 7.95%, total ash value 7.19%, acid insoluble ash 2.83%, the volatile oil content of fresh finger root 0.19% v/w, and the volatile oil content of simplex finger root 1.02% v/w. The refractive index of volatile oil of fresh finger root was 1.488 and the refractive index of volatile oil of simplex finger root was 1.482. Specific gravity of fresh finger root was 0.9805 and specific gravity of simplex finger root was 0.8533.
The result of GC-MS analysis of volatile oil of fresh finger root gave 31 compounds, with 11 main components, i.e. camphor (21.20%), 1.8-cineol (14.83%), nerol (10.48%), methyl cinnamate (8.28%), trans-β-ocimene (8.22%), camphene (6.83%), citral (5.12%), 1-limonene (4.39%), camphene hydrate (4.18%), linalool (3.91%), z-citral (2.39%). Chemical composition of volatile oil from simplex of finger root consisted of 26 compounds, with 9 main components, i.e. trans-β-ocimene (25.30%), 1.8-cineol (17.50%), camphor (16.24%), nerol (13.20%), camphene (6.81%), 1-limonene (3.65%), methyl cinnamate (3.52%), linalool (2.48%), and camphene hydrate (2.29%). It turns out that there are differences of composition the volatile oil of fresh finger root and simplex.
BAB I
PENDAHULUAN
1.1 Latar Belakang
Banyak tumbuhan penghasil minyak atsiri yang tumbuh di wilayah
Indonesia sudah dikenal masyarakat. Beberapa diantara jenis-jenis minyak atsiri
menjadi bahan yang sangat penting dalam kehidupan sehari-hari. Minyak atsiri
terdapat pada berbagai bagian tumbuhan antara lain akar, biji, bunga, buah, daun,
kulit kayu, ranting, dan rimpang (Lutony dan Rahmayati, 2000).
Minyak atsiri merupakan zat beraroma yang khas yang terkandung dalam
tumbuhan, disebut juga minyak menguap, minyak eteris atau minyak esensial
karena mudah menguap pada suhu kamar. Minyak atsiri memiliki komposisi yang
berbeda-beda sesuai sumber penghasilnya sehingga mewakili aroma tumbuhan
asalnya (Gunawan dan Mulyani, 2004).
Penggunaan minyak atsiri sangat luas dan beragam, meliputi berbagai
bidang industri, antara lain dalam industri kosmetik seperti: sabun, pasta gigi,
sampo, losion; dalam industri makanan digunakan sebagai bahan penyedap atau
penambah cita rasa; dalam industri parfum sebagai pewangi; dalam berbagai
produk minyak wangi; dalam industri farmasi atau obat-obatan sebagai anti nyeri,
anti infeksi, pembunuh bakteri; dalam industri bahan pengawet, bahkan digunakan
pula sebagai insektisida. Penjajahan negara-negara di Asia, termasuk Indonesia,
oleh negara-negara Barat pada hakekatnya adalah karena rempah-rempah yang
mengandung minyak atsiri, oleh karena itu tidak heran jika minyak atsiri banyak
Boesenbergia rotunda (L.) Mansf. yang dikenal sebagai temu kunci di
Indonesia banyak digunakan sebagai bumbu penyedap masakan dan merupakan
obat tradisional yang mengandung minyak atsiri yang terdiri dari boesenbergin,
cardamonin, pinostrobin, 5,7-dimetoksiflavon, 1,8-sineol, dan panduratin.
Diketahui bahwa minyak atsiri dari rimpang temu kunci efektif sebagai
antimikroba (Taweechaisupapong, et al., 2010). Selain itu temu kunci memiliki
efek sebagai antioksidan dan antikanker (Jing, et al., 2010).
Hasil dari beberapa penelitian yang dilakukan terhadap tumbuhan temu
kunci (Boesenbergia rotunda (L.) Mansf.) seperti manfaatnya sebagai peluruh
dahak atau menanggulangi batuk, penambah nafsu makan, menyembuhkan
sariawan dan sebagai pemacu keluarnya ASI(Syamsuhidayat dan Hutapea, 1991)
juga digunakan sebagai afrodisiak dan untuk pengobatan sakit perut (Kamkaen, et
al., 2006). Menurut Miksusanti, dkk. (2008), minyak atsiri temu kunci terdiri dari
± 50% monoterpen teroksidasi dan ± 50% hidrokarbon. Komponen utama minyak
atsiri rimpang temu kunci dari hasil isolasi minyak atsiri terhadap rimpang temu
kunci secara hidrodestilasi yang dilakukan adalah metil sinamat, kamper, sineol,
dan terpena (Hayani, 2007).
Berdasarkan hal yang telah diuraikan di atas, peneliti tertarik untuk
memanfaatkan rimpang temu kunci sebagai bahan penelitian. Bagian yang akan
digunakan adalah rimpang temu kunci segar dan kering. Proses isolasi minyak
atsiri dilakukan dengan penyulingan air (hidrodestilasi). Tahapan penelitian
meliputi pemeriksaan karakteristik simplisia, penetapan kadar, isolasi, identifikasi
Chromatography-Mass Spectrometry (GC-MS) terhadap rimpang temu kunci
segar dan kering.
Hasil penelitian ini diharapkan bermanfaat bagi ilmu pengetahuan untuk
dapat mengembangkan penelitian tentang bahan alam penghasil minyak atsiri
yang banyak terdapat di Indonesia, dan dapat memberikan informasi komponen
minyak atsiri dari rimpang temu kunci segar dan kering.
1.2 Perumusan Masalah
Berdasarkan latar belakang di atas dapat diambil perumusan masalah
sebagai berikut:
1. Apakah karakteristik simplisia rimpang temu kunci dapat ditentukan
sesuai dengan metode yang terdapat dalam Materia Medika Indonesia
(MMI)?
2. Apakah komponen minyak atsiri rimpang temu kunci segar dan kering
dapat dipisahkan dan dianalisis secara GC-MS?
1.3 Hipotesis
Berdasarkan perumusan masalah di atas maka hipotesisnya adalah:
1. Karakteristik simplisia rimpang temu kunci dapat ditentukan sesuai
dengan metode yang terdapat dalam Materia Medika Indonesia (MMI).
2. Komponen minyak atsiri rimpang temu kunci segar dan kering dapat
1.4 Tujuan Penelitian
1. Untuk mengkarakterisasi simplisia rimpang temu kunci sesuai dengan
metode yang terdapat dalam Materia Medika Indonesia (MMI).
2. Untuk memisahkan dan menganalisis komponen minyak atsiri rimpang
temu kunci segar dan kering secara GC-MS.
1.5 Manfaat Penelitian
Hasil dari penelitian ini diharapkan memberikan informasi tentang
karakterisasi, isolasi dan analisis komponen minyak atsiri secara GC-MS dari
rimpang temu kunci segar dan kering serta bermanfaat bagi ilmu pengetahuan
untuk dapat mengembangkan penelitian tentang bahan alam penghasil minyak
BAB II
TINJAUAN PUSTAKA
2.1 Uraian Tumbuhan
Uraian tumbuhan meliputi daerah tumbuh, sistematika tumbuhan, nama
daerah, morfologi tumbuhan, kandungan senyawa kimia, serta penggunaan
tumbuhan.
2.1.1 Daerah Tumbuh
Temu kunci (Boesenbergia rotunda (L.) Mansf.) ditemukan tumbuh liar
di Jawa terutama di hutan jati di Jawa Tengah dan Jawa Timur (Depkes RI, 1977).
Tumbuh baik pada iklim panas dan lembab pada tanah yang relatif subur dengan
pertukaran udara dan tata air yang baik. Pada tanah yang kurang baik tata airnya
(sering tergenang air atau becek) pertumbuhan akan terganggu dan rimpang akan
cepat busuk (Anonim, 2005).
2.1.2 Sistematika Tumbuhan
Sistematika tumbuhan temu kunci menurut LIPI (2012) adalah sebagai
berikut:
Divisi : Spermatophyta
Sub divisi : Angiospermae
Kelas : Monocotyledoneae
Bangsa : Zingiberales
Suku : Zingiberaceae
Marga : Boesenbergia
2.1.3. Nama Daerah
Nama daerah dari temu kunci adalah tamu kunci (Minangkabau), temu
kunci (Sunda), kunci (Jawa), temmo konce (Madura), koncih (Kangean), temu
konci (Bali), dumu kunci (Bima), tumu konci, tombu konci (Ambon), anipa
waking, uni nowo, uni rawu (Hila-alfuru), aruhu konci (Haruku), rutu kakusi, ene
sitale (Seram), tamputi (Ternate), tamukoaci (Makasar), temu konci (Bugis)
(Depkes RI, 1977).
2.1.4 Morfologi Tumbuhan
Temu kunci merupakan tumbuhan herba rendah, rimpangnya merayap di
dalam tanah. Umumnya batang di atas tanah berupa batang semu (pelepah daun)
dengan rimpang di dalam tanah, berwarna kuning coklat, berbau aromatik,
panjang rimpang 5-30 cm dan garis tengah 0,5-2 cm. Daun umumnya berjumlah
2-7 helai, daun berupa pelepah daun berwarna merah, tangkai daun beralur, tidak
berambut dengan panjang 7-16 cm, pelepah daun sering sama panjang dengan
tangkai daun, helai daun tegak, bentuk lanset lebar atau agak jorong, ujung daun
runcing, permukaan halus tetapi bagian bawah agak berambut terutama sepanjang
pertulangan, warna helai daun hijau muda dengan lebar 5-11 cm. Bunga dengan
susunan bulir tidak berbatas, di ketiak daun, panjang tangkai 4-11 cm, umumnya
tangkai tersembunyi dalam 2 helai daun terujung. Bunga melekat pada bagian
tandan yang pipih sempit. Kelopak berbentuk tabung, bergerigi 1-3 buah, panjang
2.1.5 Kandungan Kimia
Rimpang temu kunci mengandung komponen utama minyak atsiri terdiri
dari monoterpen, seskiterpen, turunan fenilpropan antara lain: geranial, neral,
kamfor, zingiberen, d-pinen, kamfen, 1,8-sineol, d-borneol, geraniol, osimen,
dimetoksi-4(2-propenil), miristin, linalil propanoat, asam sinamat, kamfen hidrat,
propenil guaikol, dihidrokarveol, linalool, etil-sinamat, etil p-metoksi sinamat,
panduratin A, asam kavisinat, pinosembrin (2,3-dihidrokrisin),
2',6'dihidroksi-4'-metoksi kalkon, pinostrobin (5-hidroksi-7-2',6'dihidroksi-4'-metoksi flavanon), alpinetin,
kardamomin, 2',4'-dihidroksi-6'-metoksi kalkon, boesenbergin A,
5,7-dimetoksiflavon (Anonim, 2005). Temu kunci juga mengandung saponin dan
flavonoid di samping minyak atsiri (Hayani, 2007).
2.1.6 Penggunaan Tumbuhan
Rimpang temu kunci yang segar banyak dimanfaatkan sebagai salah satu
bumbu penyedap masakan dan banyak digunakan sebagai obat tradisional oleh
masyarakat sebagai peluruh dahak atau untuk menanggulangi batuk, penambah
nafsu makan, menyembuhkan sariawan dan sebagai pemacu keluarnya ASI
(Syamsuhidayat dan Hutapea, 1991). Rimpang temu kunci juga memiliki khasiat
memperkuat lambung. Apabila dikunyah dengan pinang dapat digunakan sebagai
obat batuk kering dan pharyngitis, obat sakit perut serta obat suka kencing pada
anak-anak. Pada wanita, rimpang temu kunci dapat digunakan sebagai obat
2.2 Minyak Atsiri
Minyak atsiri yang dikenal juga dengan nama minyak eteris atau minyak
terbang (essential oil, volatile oil) dihasilkan oleh tanaman. Minyak tersebut
mudah menguap pada suhu kamar tanpa mengalami dekomposisi, mempunyai
rasa getir, berbau wangi sesuai dengan bau tanaman penghasilnya, umumnya larut
dalam pelarut organik dan tidak larut dalam air (Ketaren, 1985).
2.2.1 Lokalisasi minyak atsiri
Minyak atsiri terkandung dalam berbagai organ, seperti di dalam rambut
kelenjar (pada suku Labiatae), di dalam sel-sel parenkim (misalnya suku
Zingiberaceae dan Piperaceae), di dalam saluran minyak yang disebut vittae (suku
Umbellliferae), di dalam rongga-rongga skizogen dan lisigen (pada suku
Myrtaceae dan Rutaceae), terkandung di dalam semua jaringan (pada suku
Coniferae), pada kayu manis (Lauraceae) banyak ditemui di kulit batang (korteks)
(Gunawan dan Mulyani, 2004).
2.2.2 Aktivitas biologi minyak atsiri dan penggunaan
Pada tanaman, minyak atsiri mempunyai tiga fungsi yaitu: membantu
proses penyerbukan dan menarik beberapa jenis serangga atau hewan, mencegah
kerusakan tanaman oleh serangga atau hewan, dan sebagai cadangan makanan
bagi tanaman (Ketaren, 1985).
Minyak atsiri digunakan sebagai bahan baku dalam berbagai industri,
misalnya industri parfum, kosmetika, farmasi, bahan penyedap (flavoring agent)
2.2.3 Komposisi kimia minyak atsiri
Minyak atsiri terdiri dari berbagai campuran persenyawaan kimia dengan
sifat fisika dan kimia yang juga berbeda. Pada umumnya perbedaan komposisi
minyak atsiri disebabkan perbedaan kondisi iklim, tanah tempat tumbuh, umur
panen, metode ekstraksi yang digunakan, cara penyimpanan minyak dan jenis
tanaman penghasil.
Berdasarkan biosintesis, maka minyak atsiri dibagi atas dua golongan
yaitu terpen dan fenilpropan. Golongan terpen terbagi atas dua lagi yaitu
monoterpen dan seskiterpen. Minyak atsiri biasanya tersusun dari unsur Karbon
(C), Hidrogen (H), dan oksigen (O). Umumnya komponen kimia minyak atsiri
dibagi menjadi dua golongan yaitu: 1) Hidrokarbon, yang terutama terdiri dari
persenyawaan terpen dan 2) Hidrokarbon teroksigenasi.
a. Golongan hidrokarbon
Persenyawaan yang termasuk golongan ini terbentuk dari unsur Karbon
(C) dan Hidrogen (H). Jenis hidrokarbon yang terdapat dalam minyak atsiri
sebagian besar terdiri dari monoterpen (2 unit isopren) dan seskiterpen (3 unit
isopren).
b. Golongan hidrokarbon teroksigenasi
Komponen kimia dari golongan persenyawaan ini terbentuk dari unsur
Karbon (C), Hidrogen (H) dan Oksigen (O). Persenyawaan yang termasuk dalam
golongan ini adalah persenyawaan alkohol, aldehid, keton, ester, eter dan fenol.
Ikatan karbon yang terdapat dalam molekulnya dapat terdiri dari ikatan tunggal
dan ikatan rangkap dua. Terpen mengandung ikatan tunggal dan ikatan rangkap
senyawa hidrokarbon teroksigenasi, sukar larut dalam alkohol encer dan jika
disimpan dalam waktu lama akan membentuk resin. Golongan hidrokarbon
teroksigenasi merupakan senyawa yang penting dalam minyak atsiri karena
umumnya aroma yang lebih wangi (Ketaren, 1985).
2.3 Cara Isolasi Minyak Atsiri
Isolasi minyak atsiri dapat dilakukan dengan beberapa cara yaitu: 1)
penyulingan (distillation), 2) pengepresan (pressing), 3) ekstraksi dengan pelarut
menguap (solvent extraction), 4) ekstraksi dengan lemak, 5) metode ecuelle.
2.3.1 Metode penyulingan
a. Penyulingan dengan air
Pada metode ini, bahan tanaman yang akan disuling mengalami kontak
langsung dengan air mendidih. Bahan dapat mengapung di atas air atau terendam
secara sempurna, tergantung pada berat jenis dan jumlah bahan yang disuling. Ciri
khas model ini yaitu adanya kontak langsung antara bahan dan air mendidih. Oleh
karena itu, sering disebut penyulingan langsung. Penyulingan dengan cara
langsung ini dapat menyebabkan banyaknya rendemen minyak yang hilang (tidak
tersuling) dan terjadi pula penurunan mutu minyak yang diperoleh.
b. Penyulingan dengan uap
Model ini disebut juga penyulingan uap atau penyulingan tak langsung.
Pada prinsipnya, model ini sama dengan penyulingan langsung. Hanya saja, air
penghasil uap dan bahan yang akan disuling berada pada ketel yang berbeda. Uap
c. Penyulingan dengan air dan uap
Pada model penyulingan ini, bahan tanaman yang akan disuling
diletakkan di atas rak-rak atau saringan. Kemudian ketel penyulingan diisi dengan
air sampai permukaannya tidak jauh dari bagian bawah saringan. Ciri khas model
ini yaitu uap selalu dalam keadaan basah, jenuh, dan tidak terlalu panas. Bahan
tanaman yang akan disuling hanya berhubungan dengan uap dan tidak dengan air
panas (Lutony dan Rahmayati, 2000).
2.3.2 Metode pengepresan
Ekstraksi minyak atsiri dengan cara pengepresan umumnya dilakukan
terhadap bahan berupa biji, buah atau kulit buah yang memiliki kandungan
minyak atsiri yang cukup tinggi. Akibat tekanan pengepresan, maka sel-sel yang
mengandung minyak atsiri akan pecah dan minyak atsiri akan mengalir ke
permukaan bahan, misalnya minyak atsiri dari kulit jeruk dapat diperoleh dengan
cara ini (Ketaren, 1985).
2.3.3 Ekstraksi dengan pelarut menguap
Prinsipnya adalah melarutkan minyak atsiri dalam pelarut organik yang
mudah menguap. Ekstraksi dengan pelarut organik pada umumnya digunakan
untuk mengekstraksi minyak atsiri yang mudah rusak oleh pemanasan uap dan air,
terutama untuk mengekstraksi minyak atsiri yang berasal dari bunga misalnya
bunga cempaka, melati, mawar dan kena (Ketaren, 1985).
2.3.4 Ekstraksi dengan lemak padat
Proses ini umumnya digunakan untuk mengekstraksi bunga-bungaan,
untuk mendapatkan mutu dan rendeman minyak atsiri yang tinggi. Metode
a. Ekstraksi dengan lemak tanpa pemanasan (Enfleurage)
Cara ini menggunakan media lemak padat. Metode ini digunakan karena
diketahui beberapa jenis bunga yang telah dipetik, enzimnya masih menunjukkan
kegiatan dalam menghasilkan minyak atsiri sampai beberapa hari/minggu, seperti
bunga melati, sehingga perlu perlakuan yang tidak merusak enzim tersebut secara
langsung. Caranya dengan menaburkan bunga diatas media lilin dan dieramkan
sampai beberapa hari/minggu, selanjutnya lemak padat dikerok (dikenal dengan
pomade) dan diekstraksi menggunakan etanol (Gunawan dan Mulyani, 2004).
b. Ekstraksi dengan lemak panas
Absorbsi minyak atsiri oleh lemak dalam keadaan panas pada suhu 80o
2.3.5 Metode ecuelle
C
selama 1,5 jam. Cara ini dilakukan terhadap bahan tumbuhan yang bila dilakukan
penyulingan atau enfleurasi akan menghasilkan minyak atsiri dengan rendeman
yang rendah. Setelah selesai pemanasan, campuran disaring panas-panas, jika
perlu kelebihan lemak pada ampas disiram dengan air panas, kemudian dilakukan
penyulingan untuk memperoleh minyak atsiri (Ketaren, 1985).
Metode mengeluarkan minyak dengan menusuk kelenjar minyak dan
menggelindingkan buah pada wadah yang memiliki tonjolan tajam yang berjejer.
Tonjolan tersebut cukup panjang untuk menembus epidermis. Tetes minyak yang
jatuh pada wadah kemudian dikumpulkan (Tyler, et al., 1976).
2.4 Analisis Komponen Minyak Atsiri dengan GC-MS
Analisis dan karakterisasi komponen minyak atsiri merupakan masalah
kamar sehingga perlu diseleksi metode yang akan diterapkan untuk menganalisis
minyak atsiri. Sejak ditemukannya kromatografi gas (GC), kendala dalam analisis
komponen minyak atsiri ini mulai dapat diatasi walaupun terbatas hanya pada
analisis kualitatif dan penentuan kuantitatif komponen penyusun minyak atsiri
saja. Pada penggunaan GC, efek penguapan dapat dihindari bahkan dihilangkan
sama sekali. Perkembangan teknologi instrumentasi yang sangat pesat akhirnya
dapat melahirkan suatu alat yag merupakan gabungan dua sistem dengan prinsip
dasar yang berbeda satu sama lain tetapi dapat saling menguntungkan dan saling
melengkapi, yaitu gabungan antara kromatografi gas dan spektrometri massa
(GC-MS). Pada alat GC-MS, kedua alat dihubungkan dengan suatu interfase.
Kromatografi gas disini berfungsi sebagai alat pemisah berbagai komponen
campuran dalam sampel sedangkan spektrometer massa berfungsi untuk
mendeteksi masing-masing molekul komponen yang telah dipisahkan pada
kromatografi gas (Agusta, 2000).
2.4.1 Kromatografi gas
Kromatografi gas digunakan untuk memisahkan komponen campuran
kimia dalam suatu bahan, berdasarkan perbedaan polaritas campuran. Fase gerak
akan membawa campuran sampel menuju kolom. Campuran dalam fase gerak
akan berinteraksi dengan fase diam. Setiap komponen yang terdapat dalam
campuran berinteraksi dengan kecepatan yang berbeda dimana interaksi
komponen dengan fase diam dengan waktu yang paling cepat akan keluar pertama
Waktu yang menunjukkan berapa lama suatu senyawa tertahan di kolom
disebut waktu tambat (waktu retensi) yang diukur mulai saat penyuntikan sampai
saat elusi terjadi (Gritter, et al., 1985).
Menurut Eaton (1989), hal yang mempengaruhi waktu retensi yaitu:
1. Sifat senyawa, semakin sama kepolaran dengan kolom (fasa diam) dan
makin kurang keatsiriannya maka akan tertahan lebih lama di kolom dan
sebaliknya.
2. Sifat adsorben (fase diam), semakin sama kepolaran dengan senyawa maka
senyawa akan semakin lama tertahan dan sebaliknya.
3. Konsentrasi adsorben, semakin banyak adsorben maka semakin besar
kemampuan adsorben (fase diam) mengikat sampel maka senyawa semakin
lama tertahan dan sebaliknya.
4. Temperatur kolom, semakin rendah temperatur kolom maka senyawa
semakin lama tertahan dan sebaliknya.
5. Aliran gas pembawa, semakin kecil aliran gas pembawa maka senyawa
semakin lama tertahan dan sebaliknya.
6. Panjang kolom, semakin panjang kolom akan menahan senyawa lebih lama
dan sebaliknya.
Bagian utama dari kromatografi gas adalah gas pembawa, sistem injeksi,
kolom, fase diam, suhu dan detektor.
2.4.1.1 Gas pembawa
Gas pembawa harus memenuhi persyaratan antara lain harus inert, murni,
dan mudah diperoleh. Pemilihan gas pembawa tergantung pada detektor yang
keadaan murni dan kering yang dapat dikemas dalam tangki bertekanan tinggi.
Gas pembawa yang sering dipakai adalah helium (He), argon (Ar), nitrogen (N2),
hidrogen (H2), dan karbon dioksida (CO2
2.4.1.2 Sistem injeksi
) (Gritter, et al., 1985).
Cuplikan dimasukkan kedalam ruang suntik melalui gerbang suntik,
biasanya berupa lubang yang ditutupi dengan septum atau pemisah karet. Ruang
suntik harus dipanaskan tersendiri, terpisah dari kolom, dan biasanya 10-15o
2.4.1.3 Kolom
C
lebih tinggi dari suhu kolom. Seluruh cuplikan diuapkan segera setelah
disuntikkan dan dibawa ke kolom (Gritter, et al., 1985).
Kolom merupakan tempat terjadinya proses pemisahan karena di
dalamnya terdapat fase diam. Oleh karena itu, kolom merupakan hal sentral dalam
kromatografi gas. Ada dua jenis kolom pada kromatografi gas yaitu kolom kemas
(packing column) dan kolom kapiler (capillary column).
Kolom kemas terdiri atas fase cair yang tersebar pada permukaan
penyangga yang lembam (inert) yang terdapat dalam tabung yang relatif besar
(diameter dalam 1-3mm). Kolom kapiler jauh lebih kecil (0,02 – 0,2 mm) dan
dinding kapiler bertindak sebagai penyangga lembam untuk fase diam cair.
Semakin sempit diameter kolom, maka efisiensi pemisahan kolom semakin besar
atau puncak kromatogram yang dihasilkan semakin tajam. Pada umumnya,
seorang analis akan memilih kolom dengan diameter 0,2 atau yang lebih kecil
ketika menganalisis sampel dengan konsentrasi yang kecil atau untuk memisahkan
2.4.1.4 Fase diam
Banyak macam bahan kimia yang dipakai sebagai fase diam antara lain:
squalen, dietilglikol suksinat. Fase diam yang dipakai dalam kolom kapiler dapat
bersifat non polar, polar atau semi polar. Jenis fase diam akan menentukan urutan
elusi komponen-komponen dalam campuran (Gandjar dan Rohman, 2007).
2.4.1.5 Suhu
Tekanan uap sangat bergantung pada suhu, maka suhu merupakan faktor
utama dalam GC. Pada GC-MS terdapat tiga pengendali suhu yang berbeda, yaitu:
suhu injektor, suhu kolom dan suhu detektor.
2.4.1.5.1 Suhu injektor
Suhu injektor harus cukup panas untuk menguapkan cuplikan dengan
cepat sehingga tidak menghilangkan keefisienan cara penyuntikan. Tetapi
sebaliknya, suhu harus cukup rendah untuk mencegah peruraian atau penataan
ulang akibat panas (McNair dan Bonelli, 1968).
2.4.1.5.2 Suhu kolom
Suhu kolom harus cukup tinggi sehingga analisis dapat diselesaikan
dalam waktu yang sesuai, dan harus cukup rendah sehingga terjadi pemisahan.
Umumnya semakin rendah suhu kolom, semakin tinggi koefisien partisi dalam
fase diam sehingga hasil pemisahan semakin baik. Pada beberapa hal tidak dapat
digunakan suhu kolom yang rendah, terutama bila cuplikan terdiri atas senyawa
dengan rentangan titik didih yang lebar, untuk itu suhu perlu deprogram (McNair
2.4.1.5.3 Suhu detektor
Detektor harus cukup panas sehingga cuplikan dan air atau hasil samping
yang terbentuk pada proses pengionan tidak mengembun (McNair dan Bonelli,
1968).
2.4.1.6 Detektor
Menurut McNair dan Bonelli (1968), ada dua detektor yang popular yaitu
detektor hantar-thermal (thermal conductivity detector) dan detektor pengion
nyala (flame ionization detector).
2.4.2 Spektrometri massa
Suatu spektrometer massa bekerja dengan membangkitkan molekul-
molekul bermuatan atau fragmen-fragmen molekul baik dalam keadaan sangat
hampa atau segera sebelum sampel memasuki ruang sangat hampa (Watson,
2010). Molekul senyawa organik pada spektrometer massa, ditembak dengan
berkas elektron dan menghasilkan ion bermuatan positif yang mempunyai energi
yang tinggi karena lepasnya elektron dari molekul yang dapat pecah menjadi ion
yang lebih kecil (Sastrohamidjojo, 2004).
Menurut Dachriyanus (2004), spektrometer massa pada umumnya
digunakan untuk:
1. Menentukan massa molekul (berat molekul)
2. Menentukan rumus molekul dengan menggunakan Spektrum Massa
Beresolusi Tinggi (High Resolution Mass Spectra)
3. Mengetahui informasi dari struktur dengan melihat pola fragmentasinya
Spektrum massa hasil analisis sistem spektroskopi massa merupakan
komponen kimia (masing-masing puncak pada kromatogram). Setiap fragmen
yang terbentuk dari pemecahan suatu komponen kimia memiliki berat molekul
yang berbeda dan ditampilkan dalam bentuk diagram dua dimensi, m/z (m/e,
massa/muatan) pada sumbu X dan intensitas pada sumbu Y yang disebut dengan
spektrum massa. Pola pemecahan (fragmentasi) molekul yang terbentuk untuk
setiap komponen kimia sangat spesifik sehingga dapat dijadikan sebagai patokan
untuk menentukan struktur molekul suatu komponen kimia. Selanjutnya,
spektrum massa komponen kimia yang diperoleh dari hasil analisis diidentifikasi
dengan cara dibandingkan dengan spektrum massa yang terdapat dalam suatu
bank data (Agusta, 2000).
Spektrometer massa terdiri dari sistem pemasukan cuplikan, ruang
pengion dan percepatan, tabung analisis, pengumpul ion dan penguat dan
pencatat. Keuntungan utama spektrometri massa sebagai metode analisis yaitu
metode ini lebih sensitif dan spesifik untuk identifikasi senyawa yang tidak
diketahui atau untuk menetapkan keberadaan senyawa tertentu. Hal ini disebabkan
adanya pola fragmentasi yang khas untuk setiap senyawa sehingga dapat
memberikan informasi mengenai bobot molekul dan rumus molekul. Puncak ion
molekul penting dikenali karena memberikan bobot molekul senyawa yang
diperiksa. Puncak paling kuat pada spektrum, disebut puncak dasar (base peak),
dinyatakan dengan nilai 100% dan kekuatan puncak lain, termasuk puncak ion
molekulnya dinyatakan sebagai persentase puncak dasar tersebut (Silverstein, et
BAB III
METODE PENELITIAN
Metode penelitian ini meliputi penyiapan sampel, pemeriksaan
karakteristik simplisia, isolasi dan analisis komponen-komponen minyak atsiri
secara GC-MS dari rimpang temu kunci (Boesenbergia rotunda (L.) Mansf.) segar
dan kering.
3.1 Alat dan Bahan 3.1.1 Alat-alat
Alat-alat yang digunakan dalam percobaan adalah alat-alat gelas
laboratorium, cawan porselin berdasar rata, krus porselin bertutup, blender
(National), kaca objek dan kaca penutup, mikroskop, lemari pengering,
refraktometer abbe, piknometer, oven, neraca listrik (Mettler Toledo), neraca
kasar (Ohaus), seperangkat alat Stahl, seperangkat alat destilasi air (Water
Distillation), Gas Chromatograph-Mass Spectrometer (GC-MS) model Shimadzu
QP 2010 Plus.
3.1.2 Bahan-bahan
Bahan-bahan yang digunakan dalam penelitian ini meliputi bahan
tumbuhan dan bahan kimia. Bahan tumbuhan yang digunakan adalah rimpang
temu kunci (Boesenbergia rotunda (L.) Mansf.) segar. Bahan kimia yang
lainnya adalah produksi E-Merck: toluen, kloralhidrat, kloroform, HCl dan
natrium sulfat anhidrat.
3.2 Pengumpulan dan Pengolahan Sampel 3.2.1 Pengambilan bahan
Metode pengambilan bahan dilakukan dengan cara purposif yaitu diambil
dari satu daerah saja tanpa membandingkan dengan tumbuhan yang sama di
daerah lain. Bahan diperoleh dari Pasar Pancur Batu, Kecamatan Pancur Batu,
Provinsi Sumatera Utara. Bahan yang digunakan adalah rimpang temu kunci segar
dan kering.
3.2.2 Identifikasi tumbuhan
Identifikasi tumbuhan dilakukan di Herbarium Bogoriense, Bidang Botani
Pusat, Pusat Penelitian Biologi, Lembaga Ilmu Pengetahuan Indonesia (LIPI)
Bogor. Hasil determinasi dapat dilihat pada Lampiran 1, halaman 50.
3.2.3 Pengolahan simplisia
Pengolahan simplisia dilakukan terhadap rimpang temu kunci. Rimpang
segar dibersihkan dari kotoran yang melekat, disortasi lalu dicuci dengan air
sampai bersih, ditiriskan dan dirajang lalu ditimbang, selanjutnya dilakukan
isolasi minyak atsiri sampel segar.
Sebagian rimpang temu kunci segar dikeringkan dilemari pengering pada
suhu 50oC untuk isolasi minyak atsiri sebagai sampel kering, selanjutnya sebagian
3.3 Pemeriksaan Karakteristik Simplisia
Pemeriksaan karakteristik simplisia meliputi pemeriksaan makroskopik
dan mikroskopik, penetapan kadar air, penetapan kadar sari yang larut dalam air,
penetapan kadar sari larut dalam etanol, penetapan kadar abu total, penetapan
kadar abu yang tidak larut dalam asam, dan penetapan kadar minyak atsiri.
(Depkes RI, 1995; WHO, 1992).
3.3.1 Pemeriksaan makroskopik
Pemeriksaan makroskopik dilakukan dengan mengamati bentuk luar dari
simplisia rimpang temu kunci, meliputi: bentuk, rupa, warna, bau, ukuran, dan
rasa.
3.3.2 Pemeriksaan mikroskopik
Pemeriksaan mikroskopik dilakukan terhadap serbuk simplisia. Serbuk
simplisia diletakkan sedemikian rupa di atas kaca objek yang telah ditetesi kloral
hidrat dan ditutup dengan kaca penutup, kemudian diamati di bawah mikroskop.
Untuk melihat pati serbuk simpisia diletakkan diatas kaca objek yang telah ditetesi
akuades.
3.3.3 Penetapan kadar air
a. Penjenuhan toluen
Sebanyak 200 ml toluen dimasukkan ke dalam labu alas bulat, lalu
ditambahkan 2 ml akuades, kemudian alat dipasang dan dilakukan destilasi selama
2 jam. Destilasi dihentikan dan dibiarkan dingin selama 30 menit, kemudian
b. Penetapan kadar air simplisia
Dimasukkan 5 g serbuk simplisia yang telah ditimbang seksama ke dalam
labu tersebut, dipanaskan secara hati-hati selama 15 menit. Kecepatan tetesan
diatur 2 tetes per detik setelah toluen mendidih sampai sebagian besar air
terdestilasi, kemudian kecepatan destilasi dinaikkan sampai 4 tetes per detik.
Bagian dalam pendingin dibilas dengan toluene setelah semua air terdestilasi.
Destilasi dilanjutkan selama 5 menit, tabung penerima dibiarkan mendingin pada
suhu kamar. Volume air dibaca setelah air dan toluene memisah sempurna dengan
ketelitian 0,5 ml. Selisih kedua volume air yang dibaca sesuai dengan kadar air
yang terdapat dalam bahan yang diperiksa. Kadar air dihitung dalam persen
(WHO, 1992).
3.3.4 Penetapan kadar sari larut dalam air
Sebanyak 5 g serbuk simplisia, direndam selama 24 jam dalam 100 ml
air-kloroform (2,5 ml air-kloroform dalam air suling hingga 1000 ml) dalam labu
bersumbat sambil sesekali dikocok selama 6 jam pertama, kemudian dibiarkan
selama 18 jam, lalu disaring. Sejumlah 20 ml filtrat pertama diuapkan sampai
kering dalam cawan penguap rata yang telah dipanaskan dan ditara. Sisa
dipanaskan pada suhu 105ºC sampai bobot tetap. Kadar dalam persen sari yang
larut dalam air dihitung terhadap bahan yang telah dikeringkan (Depkes RI, 1995).
3.3.5 Penetapan kadar sari larut dalam etanol
Sebanyak 5 g serbuk simplisia, direndam selama 24 jam dalam 100 ml
etanol 95% dalam labu bersumbat sambil sekali-sekali dikocok selama 6 jam
pertama, kemudian dibiarkan selama 18 jam, lalu disaring. Sejumlah 20 ml filtrat
dan ditara. Sisa dipanaskan pada suhu 105ºC sampai bobot tetap. Kadar dalam
persen sari yang larut dalam etanol dihitung terhadap bahan yang telah
dikeringkan (Depkes RI, 1995).
3.3.6 Penetapan kadar abu total
Sebanyak 2 g serbuk simplisia ditimbang seksama dimasukkan kedalam
krus porselin yang telah dipijar dan ditara, kemudian diratakan. Krus porselin
dipijar perlahan-lahan sampai arang habis, pemijaran dilakukan pada suhu
500-600ºC selama 3 jam kemudian didinginkan dan ditimbang sampai diperoleh bobot
tetap. Kadar abu dihitung terhadap bahan yang telah dikeringkan (WHO, 1992).
3.3.7 Penetapan kadar abu yang tidak larut dalam asam
Abu yang telah diperoleh dalam penetapan kadar abu dididihkan dalam 25
ml asam klorida encer selama 5 menit, bagian yang tidak larut dalam asam
dikumpulkan, disaring melalui kertas saring dan dipijar sampai bobot tetap,
kemudian didinginkan dan ditimbang. Kadar abu yang tidak larut dalam asam
dihitung terhadap bahan yang dikeringkan (Depkes RI, 1995).
3.3.8 Penetapan kadar minyak atsiri
Penetapan kadar minyak atsiri dilakukan dengan menggunakan alat Stahl.
Cara: Sebanyak 10 g rimpang temu kunci yang sudah kering dan sudah dihaluskan
dimasukkan dalam labu alas bulat berleher pendek, ditambahkan air suling
sebanyak 300 ml, labu diletakkan diatas pemanas listrik. Hubungkan labu dengan
pendingin dan alat penampung berskala, buret diisi air sampai penuh. Didihkan isi
labu dengan pemanasan yang sesuai untuk menjaga pendidihan berlangsung
lambat tetapi teratur sampai minyak atsiri terdestilasi sempurna dan tidak
setelah penyulingan selesai, catat volume minyak atsiri pada buret. Hitung kadar
minyak atsiri dalam % v/b (Depkes RI, 1995).
3.4 Isolasi Minyak Atsiri
Isolasi minyak atsiri rimpang temu kunci segar dan kering dilakukan
dengan metode penyulingan air (water distillation).
Caranya: 100 g sampel yang telah dirajang dimasukkan dalam labu alas
datar berleher panjang 2 liter ditambahkan akuades sampai sampel terendam.
Kemudian dirangkai alat destilasi air. Destilasi dilakukan selama 4 jam. Minyak
atsiri yang diperoleh ditampung dalam corong pisah setelah itu dipisahkan antara
minyak dan air. Kemudian minyak atsiri yang diperoleh ditambahkan natrium
sulfat anhidrat, dikocok dan didiamkan selama 1 hari. Minyak atsiri dipipet dan
disimpan dalam botol berwarna gelap (Ketaren, 1985).
3.5 Identifikasi Minyak Atsiri 3.5.1 Penetapan paramater fisika 3.5.1.1 Penentuan indeks bias
Penentuan indeks bias dilakukan menggunakan alat Refraktometer Abbe.
Caranya: Alat Refraktometer Abbe dihidupkan. Prisma atas dan prisma bawah
dipisahkan dengan membuka klem dan dibersihkan dengan mengoleskan kapas
yang telah dibasahi dengan alkohol. Cuplikan minyak diteteskan ke prisma bawah
kemudian ditutup. Melalui teleskop dapat dilihat adanya bidang terang dan gelap
gelap terbagi atas dua bagian yang sama secara vertikal. Indeks biasnya dapat
dibaca dengan melihat skala.
3.5.1.2 Penentuan bobot jenis
Penentuan bobot jenis dilakukan dengan menggunakan piknometer.
Caranya: Piknometer dibersihkan dan dikeringkan, diisi dengan air suling lalu
ditimbang dengan seksama. Kemudian piknometer dikosongkan dan dibilas
beberapa kali dengan alkohol kemudian dikeringkan dengan bantuan hairdryer
dan ditimbang seksama. Piknometer diisi dengan minyak selanjutnya dilakukan
seperti pengerjaan pada air suling. Bobot minyak atsiri diperoleh dengan
mengurangkan bobot piknometer yang diisi minyak atsiri dengan bobot
piknometer kosong. Bobot jenis minyak atsiri adalah hasil yang diperoleh dengan
membagi bobot minyak atsiri dengan bobot air suling dalam piknometer. Kecuali
dinyatakan lain dalam monograf keduanya ditetapkan pada suhu kamar (Depkes
RI, 1995).
3.5.2 Analisis komponen minyak atsiri
Penentuan komponen minyak atsiri yang diperoleh dari rimpang temu
kunci segar dan kering dilakukan di Laboratorium Penelitian Fakultas Farmasi
USU dengan menggunakan seperangkat alat GC-MS model Shimadzu QP-2010
Plus dan Auto Injecto AOC-20i.
Kondisi analisis adalah jenis kolom kapiler Rtx - 5MS, panjang kolom 30
m, diameter kolom dalam 0,25 mm, suhu injektor 250oC, gas pembawa He dengan
laju alir 0,5 ml/menit. Suhu kolom terprogram (temperature programming)
kenaikan 5,0oC/menit sampai suhu akhir 280o
Cara identifikasi komponen minyak atsiri adalah dengan membandingkan
spektrum massa dan komponen minyak atsiri yang diperoleh (unknown) dengan
data library yang memiliki tingkat kemiripan (similary index) tertinggi.
C yang dipertahankan (Zaeoung, et
BAB IV
HASIL DAN PEMBAHASAN
4.1 Identifikasi Tumbuhan
Identifikasi tumbuhan yang dilakukan di Herbarium Bogoriense, Bidang
Botani Pusat, Pusat Penelitian Biologi, Lembaga Ilmu Pengetahuan Indonesia
(LIPI) Bogor menunjukkan bahwa sampel adalah benar temu kunci (Boesenbergia
rotunda (L.) Mansf.) dari suku Zingiberaceae. Data selengkapnya dapat dilihat
pada Lampiran 1, halaman 51.
4.2 Hasil Karakterisasi Simplisia
4.2.1 Pemeriksaan makroskopik simplisia
Pemeriksaan makroskopik simplisia rimpang temu kunci dicirikan bentuk
hampir bulat, berkerut, irisan rimpang berwarna coklat muda kekuningan, berbau
khas aromatik, rasa agak pahit. Gambar hasil pemeriksaan makroskopik dapat
dilihat pada Lampiran 3, halaman 53.
4.2.2 Pemeriksaan mikroskopik serbuk simplisia
Pemeriksaan mikroskopik serbuk simplisia rimpang temu kunci berwarna coklat
muda kekuningan. Terdapat adanya pembuluh kayu dengan penebalan jala dan
spiral, periderm, parenkim dengan sel sekresi, dan butir pati. Gambar hasil
pemeriksaan mikroskopik dapat dilihat pada Lampiran 5-6, halaman 55-56.
4.2.3 Pemeriksaan karakteristik simplisia
Karakteristik simplisia dari rimpang temu kunci dapat dilihat pada Tabel
Tabel 4.1 Hasil karakterisasi serbuk simplisia rimpang temu kunci
No Karakteristik Hasil pemeriksaan (%)
1.
Kadar sari larut air Kadar sari larut etanol Kadar abu total
Kadar abu tidak larut asam
6,65 12,45
7,95 7,19 2,83
Kadar air dalam simplisia menunjukkan jumlah air yang terkandung dalam
simplisia yang digunakan. Kadar air simplisia berhubungan dengan proses
pengeringan simplisia. Pengeringan merupakan suatu usaha untuk menurunkan
kadar air bahan sampai tingkat yang didinginkan. Kadar air yang cukup aman,
maka simplisia tidak mudah rusak dan dapat disimpan dalam jangka waktu yang
cukup lama. Apabila simplisia yang dihasilkan tidak cukup kering maka
kemungkinan akan terjadi pertumbuhan jamur dan jasad renik lainnya. Hasil dari
penelitian diperoleh kadar air simplisia temu kunci adalah 6,65% dan memenuhi
peryaratan literatur untuk kadar air simplisia yaitu kurang dari 10% (Depkes RI,
1986).
Penetapan kadar sari dilakukan terhadap 2 pengujian yaitu kadar sari larut
dalam etanol dan air. Penetapan kadar sari simplisia menyatakan jumlah zat yang
tersari dalam air dan dalam etanol. Dalam hal ini simplisia rimpang temu kunci
kadar sari yang larut dalam air diperoleh lebih besar dari kadar sari yang larut
dalam etanol. Penetapan kadar sari yang larut dalam air dan dalam etanol
dilakukan untuk mengetahui jumlah senyawa yang dapat tersari dalam air dan
etanol dari suatu simplisia. Senyawa yang bersifat polar dan larut dalam air akan
tersari oleh air sedangkan senyawa-senyawa yang tidak larut dalam air dan larut
Penetapan kadar abu dimaksudkan untuk mengetahui kandungan mineral
internal yang terdapat didalam simplisia yang diteliti serta senyawa organik yang
tersisa selama pembakaran. Abu total terbagi dua, yang pertama abu fisiologis
adalah abu yang berasal dari jaringan tumbuhan itu sendiri dan abu non fisiologis
adalah sisa setelah pembakaran yang berasal dari bahan-bahan dari luar yang
terdapat pada permukaan simplisia. Kadar abu tidak larut asam untuk menentukan
jumlah silika, khususnya pasir yang ada pada simplisia dengan cara melarutkan
abu total dalam asam klorida (WHO, 1992).
Penetapan kadar minyak atsiri dengan menggunakan alat Stahl diketahui
bahwa minyak atsiri rimpang temu kunci segar adalah 0,19% v/b, sementara pada
simplisia temu kunci 1,02% v/b, dari hasil ini diketahui bahwa minyak atsiri lebih
banyak terdapat pada simplisia temu kunci. Hal ini disebabkan oleh kadar air pada
simplisia temu kunci lebih sedikit dibandingkan kadar air pada rimpang temu
kunci segar sehingga berpengaruh pada bobot sampel. Hasil penetapan kadar
minyak atsiri dari rimpang temu kunci dapat dilihat pada Tabel 4.2 (data
selengkapnya dapat dilihat pada Lampiran 13, halaman 63).
Tabel 4.2 Hasil penetapan kadar minyak atsiri
No Sampel
Kadar minyak atsiri (% v/b)
Hasil praktek Hasil berdasarkan
literatur
Minyak atsiri yang terdapat pada rimpang temu kunci yaitu berada di dalam
sel-sel parenkim. Kadar minyak atsiri rimpang temu kunci yang diperoleh dari hasil
sampel (sumber sampel), umur panen, lingkungan, dan faktor genetik (Ditjen
POM, 2000).
4.3 Identifikasi Minyak Atsiri
Hasil penentuan indeks bias dan bobot jenis minyak atsiri hasil isolasi dari
rimpang temu kunci dapat dilihat pada Tabel 4.3 (data selengkapnya dapat dilihat
pada Lampiran 14-15, halaman 64-65).
Tabel 4.3 Hasil penentuan indeks bias dan bobot jenis minyak atsiri
No Sampel Indeks bias Bobot jenis
Dapat dilihat bahwa indeks bias minyak atsiri dari rimpang temu kunci segar
sebesar 1,488 dan simplisia temu kunci sebesar 1,482. Hal ini menunjukkan
bahwa perubahan kecil pada komposisi komponen minyak atsiri tidak terlalu
mempengaruhi harga indeks bias.
Indeks bias merupakan perbandingan antara kecepatan cahaya di dalam udara
dengan kecepatan cahaya di dalam zat tersebut pada suhu tertentu. Indeks bias
berguna untuk identifikasi kemurnian dan berhubungan erat dengan
komponen-komponen yang tersusun dalam minyak atsiri yang dihasilkan. Sama halnya
dengan berat jenis dimana komponen penyusun minyak atsiri dapat
mempengaruhi nilai indeks biasnya (Armando, 2009).
Hasil dari penelitian diperoleh bahwa terdapat perbedaan nilai bobot jenis dari
minyak atsiri yang berasal dari rimpang temu kunci segar dan yang kering. Bobot
atsiri dari simplisia temu kunci adalah sebesar 0,8533. Hal ini disebabkan pada
identifikasi minyak atsiri dengan GC-MS diperoleh komponen senyawa kimia
dari minyak atsiri rimpang temu kunci segar lebih banyak dibandingkan dengan
minyak atsiri simplisia temu kunci. Menurut Armando, bobot jenis merupakan
salah satu kriteria paling penting dalam menentukan mutu dan kemurnian minyak
atsiri. Bobot jenis sering dihubungkan dengan berat komponen yang terkandung
di dalamnya. Semakin besar fraksi berat yang terkandung dalam minyak, semakin
besar pula nilai bobot jenisnya.
4.4 Analisis dengan GC-MS
Hasil analisis dengan GC-MS minyak atsiri dari rimpang temu kunci segar
diperoleh 11 puncak utama dari 31 puncak pada kromatogram GC yaitu kamfor,
1,8-sineol, nerol, metil sinamat, trans-β-osimen, kamfen, sitral, 1-limonen, kamfen
hidrat, linalool, z-sitral.
Hasil analisis dengan GC-MS minyak atsiri dari simplisia temu kunci diperoleh 9
puncak utama dari 26 puncak pada kromatogram GC yaitu β-osimen, 1,8-sineol,
kamfor, nerol, kamfen, 1-limonen, metil sinamat, linalool, dan kamfen hidrat.
Hasil analisis dengan GC-MS minyak atsiri dari rimpang temu kunci segar dan
kering dapat dilihat pada Tabel 4.4 dan Tabel 4.5 (data selengkapnya dapat dilihat
pada Lampiran 19-20, halaman 72-82).
No Nama Komponen
Tabel 4.5 Waktu tambat dan kadar komponen minyak atsiri hasil analisis GC-MS dari simplisia temu kunci
No Nama Komponen
Berdasarkan Tabel 4.4 dan Tabel 4.5 di atas dapat disimpulkan bahwa
komponen minyak atsiri dari simplisia temu kunci kehilangan komponen z-sitral
dan sitral dari rimpang temu kunci segar. Dapat dilihat pula adanya perbedaan
kadar antara komponen yang satu dengan yang lain. Salah satu contohnya adalah
kamfor pada minyak atsiri rimpang temu kunci segar memiliki kadar 21,20%
sementara pada minyak atsiri simplisia temu kunci mengalami penurunan kadar
memiliki kadar yang berbeda. Hal ini dapat di sebabkan oleh lamanya sampel
terpapar dengan udara yang dapat menyebabkan sampel mengalami penguapan
sehingga terjadi penguapan pada komponen minyak atsiri yang lebih mudah
menguap. Perubahan minyak atsiri juga dapat terjadi karena adanya proses reaksi
konjugasi, hidrolisis, reduksi dan juga oksidasi. Tempat penyimpanan sampel
dapat mempengaruhi penyusutan dan komponen dari minyak atsiri (Guenther,
1987).
4.5 Analisis dan Fragmentasi Hasil Spektrometri Massa
Analisis dan fragmentasi hasil spektrometri massa komponen utama minyak atsiri
dari rimpang temu kunci segar adalah sebagai berikut:
Pola fragmentasi dari masing-masing senyawa, selengkapnya dapat dilihat pada
Lampiran 21 halaman 83-86.
1. Puncak dengan waktu tambat 7,592 menit
Mempunyai M+ 152 diikuti fragmen m/z 152, 137, 123, 95, 81, 55, 41].
Berdasarkan perbandingan antara spektrum MS unknown dengan data library,
maka senyawa ini disimpulkan sebagai Kamfor dengan tingkat kemiripan
(similarity index) = 98% dan rumus molekulnya C10H16O dengan rumus bangun
seperti pada Gambar 4.1.
Spektrum massa unknown memberikan puncak ion molekul M+ 152 yang
merupakan berat molekul dari C10H16O. Pelepasan CH3 menghasilkan fragmen
[C9H13O]+ dengan m/z 137. Pelepasan CH2 menghasilkan fragmen [C8H11O]+
dengan m/z 123. Pelepasan CO menghasilkan fragmen [C7H11]+ dengan m/z 95.
Pelepasan CH2 menghasilkan fragmen [C6H9]+ dengan m/z 81. Pelepasan C2H2
menghasilkan fragmen [C4H7]+ dengan m/z 55. Pelepasan CH2 menghasilkan
fragmen [C3H5]+
2. Puncak dengan waktu tambat 5,042 menit dengan m/z 41.
Mempunyai M+ 154 diikuti fragmen m/z 154, 139, 125, 84, 69, 41, 27].
Berdasarkan perbandingan antara spektrum MS unknown dengan data library,
maka senyawa ini disimpulkan sebagai 1,8-Sineol dengan tingkat kemiripan
(similarity index) = 97% dan rumus molekulnya C10H18O dengan rumus bangun
seperti pada Gambar 4.2.
Gambar 4.2 Rumus bangun 1,8-Sineol
Spektrum massa unknown memberikan puncak ion molekul M+ 154 yang
merupakan berat molekul dari C10H18O. Pelepasan CH3 menghasilkan fragmen
[C9H15O]+ dengan m/z 139. Pelepasan CH2 menghasilkan fragmen [C8H13O]+
dengan m/z 125. Pelepasan C3H5 menghasilkan fragmen [C5H8O]+ dengan m/z
84. Pelepasan CH3 menghasilkan fragmen [C4H5O]+ dengan m/z 69. Pelepasan
CO menghasilkan fragmen [C3H5]+ dengan m/z 41. Pelepasan CH2 menghasilkan
3. Puncak dengan waktu tambat 10,183 menit
Mempunyai M+ 154 diikuti fragmen m/z 154, 136, 121, 80, 53, 27]. Berdasarkan
perbandingan antara spektrum MS unknown dengan data library, maka senyawa
ini disimpulkan sebagai Nerol dengan tingkat kemiripan (similarity index) = 96%
dan rumus molekulnya C10H18O dengan rumus bangun seperti pada Gambar 4.3.
Gambar 4.3 Rumus bangun Nerol
Spektrum massa unknown memberikan puncak ion molekul M+ 154 yang
merupakan berat molekul dari C10H18O. Pelepasan H2O menghasilkan fragmen
[C10H16]+ dengan m/z 136. Pelepasan CH3 menghasilkan fragmen [C9H13]+
dengan m/z 121. Pelepasan C3H5 menghasilkan fragmen [C6H8]+ dengan m/z 80.
Pelepasan C2H3 menghasilkan fragmen [C4H5]+ dengan m/z 53. Pelepasan C2H2
menghasilkan fragmen [C2H3]+
4. Puncak dengan waktu tambat 13,583 menit dengan m/z 27.
Mempunyai M+ 162 diikuti fragmen m/z 162, 117, 91, 77]. Berdasarkan
perbandingan antara spektrum MS unknown dengan data library, maka senyawa
ini disimpulkan sebagai Metil Sinamat dengan tingkat kemiripan (similarity
index) = 98% dan rumus molekulnya C10H10O2 dengan rumus bangun seperti
pada Gambar 4.4.
Spektrum massa unknown memberikan puncak ion molekul M+ 162 yang
merupakan berat molekul dari C10H10O2. Pelepasan C2H5O menghasilkan
fragmen [C8H5O]+ dengan m/z 117. Pelepasan C2H2 menghasilkan fragmen
[C6H3O]+ dengan m/z 91. Pelepasan CH2 menghasilkan fragmen [C5HO]+
5. Puncak dengan waktu tambat 5,292 menit dengan m/z 77.
Mempunyai M+ 136 diikuti fragmen m/z 136, 121, 93, 79, 53, 38]. Berdasarkan
perbandingan antara spektrum MS unknown dengan data library, maka senyawa
ini disimpulkan sebagai Trans-β-Osimen dengan tingkat kemiripan (similarity
index) = 97% dan rumus molekulnya C10H16 dengan rumus bangun seperti pada
Gambar 4.5.
Gambar 4.5 Rumus bangun Trans-β-Osimen
Spektrum massa unknown memberikan puncak ion molekul M+ 136 yang
merupakan berat molekul dari C10H16. Pelepasan CH3 menghasilkan fragmen
[C9H13]+ dengan m/z 121. Pelepasan C2H4 menghasilkan fragmen [C7H9]+
dengan m/z 93. Pelepasan CH2 menghasilkan fragmen [C6H7]+ dengan m/z 79.
Pelepasan C2H2 menghasilkan fragmen [C4H5]+ dengan m/z 53. Pelepasan CH3
menghasilkan fragmen [C3H2]+
6. Puncak dengan waktu tambat 3,667 menit dengan m/z 38.
Mempunyai M+ 136 diikuti fragmen m/z 136, 121, 107, 93, 79, 53, 27].
maka senyawa ini disimpulkan sebagai Kamfen dengan tingkat kemiripan
(similarity index) = 97% dan rumus molekulnya C10H16 dengan rumus bangun
seperti pada Gambar 4.6.
Gambar 4.6 Rumus bangun Kamfen
Spektrum massa unknown memberikan puncak ion molekul M+ 136 yang
merupakan berat molekul dari C10H16. Pelepasan CH3 menghasilkan fragmen
[C9H13]+ dengan m/z 121. Pelepasan CH2 menghasilkan fragmen [C8H11]+
dengan m/z 107. Pelepasan CH2 menghasilkan fragmen [C7H9]+ dengan m/z 93.
Pelepasan CH2 menghasilkan fragmen [C6H7]+ dengan m/z 79. Pelepasan C2H2
menghasilkan fragmen [C4H5]+ dengan m/z 53. Pelepasan C2H2 menghasilkan
fragmen [C2H3]+
7. Puncak dengan waktu tambat 10,608 menit dengan m/z 27.
Mempunyai M+ 152 diikuti fragmen m/z 152, 137, 123, 109, 83, 69, 41, 27].
Berdasarkan perbandingan antara spektrum MS unknown dengan data library,
maka senyawa ini disimpulkan sebagai Sitral dengan tingkat kemiripan (similarity
index) = 97% dan rumus molekulnya C10H16O dengan rumus bangun seperti pada
Gambar 4.7.