KARAKTERISASI SIMPLISIA DAN ISOLASI SERTA ANALISIS KOMPONEN MINYAK ATSIRI SECARA GC-MS DARI SIMPLISIA RIMPANG TANAMAN
TEMU PUTIH (Kaemferia rotunda L.)
SKRIPSI
OLEH:
DESMI WARDANI NASUTION NIM 091524026
PROGRAM EKSTENSI SARJANA FARMASI FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA MEDAN
KARAKTERISASI SIMPLISIA DAN ISOLASI SERTA ANALISIS KOMPONEN MINYAK ATSIRI SECARA GC-MS DARI SIMPLISIA RIMPANG TANAMAN
TEMU PUTIH (Kaemferia rotunda L.)
SKRIPSI
Diajukan Untuk Melengkapi Salah Satu Syarat Untuk Mencapai Gelar Sarjana Farmasi pada Fakultas Farmasi
Universitas Sumatera Utara
OLEH:
DESMI WARDANI NASUTION NIM 091524026
FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA MEDAN
LEMBAR PENGESAHAN
KARAKTERISASI SIMPLISIA DAN ISOLASI SERTA ANALISIS KOMPONEN MINYAK ATSIRI
SECARA GC-MS DARI SIMPLISIA RIMPANG TANAMAN TEMU PUTIH (Kaemferia rotunda L.)
OLEH:
DESMI WARDANI NASUTION NIM 091524026
Dipertahankan di Hadapan Panitia Penguji Fakultas Farmasi
KATA PENGANTAR
Puji dan syukur kehadirat Allah SWT yang telah melimpahkan rahmat
dan hidayahNya sehingga penulis dapat menyelesaikan penelitian dan penulisan
skripsi yang berjudul “Karakterisasi Simplisia dan Isolasi serta Analisis
Komponen Minyak Atsiri secara GC-MS dari Simplisia Temu Putih (Kaemferia
rotunda L.)” untuk memenuhi syarat guna mencapai gelar sarjana farmasi pada
Fakultas Farmasi Universitas Sumatera Utara.
Pada kesempatan ini dengan segala kerendahan hati penulis mengucapkan
terimakasih yang tak terhingga kepada Ayahanda Noyan Nasution dan ibunda
Tiopan Lubis tercinta, serta kakanda semua yang tersayang yang telah dengan
penuh kesabaran dan kasih sayang selalu memberi dorongan, bimbingan, nasehat
serta do’a.
Melalui tulisan ini ucapan terimakasih yang tulus dan ikhlas atas
bimbingan, petunjuk, pemberian fasilitas serta saran dan bantuan lainnya, sebelum
dan selama penelitian juga disampaikan kepada:
1. Bapak Drs. Ismail M.Si, Apt., dan Drs. Panal Sitorus M.Si, Apt., selaku
dosen pembimbing yang telah membimbing penulis dengan penuh
kesabaran selama penelitian hingga selesainya skripsi ini.
2. Bapak Dr. M. Pandapotan Nasution, MPS., Apt., Drs. Ismail M.Si, Apt.,
Dra. Saleha Salbi, M.Si.,Apt.dan Drs. Syahrial Yoenoes, S.U.,Apt. selaku
penguji yang telah menguji dan memberikan masukan kepada penulis
3. Bapak Prof. Dr. Sumadiohadisahputra, Apt., selaku Dekan Fakultas
Farmasi Universitas Sumatera Utara yang telah mensyahkan dan
memberikan pengarahan dalam penyusunan skripsi ini.
4. Ibu Prof. M.Timbul selaku dosen wali yang selama ini telah banyak
membina dan membimbing penulis selama masa pendidikan.
5. Asisten Laboratorim Farmakognosi dan staf – staf farmasi khususnya Deni
yang banyak memberikan dorongan dan bantuan selama penelitian.
6. Teman-teman penulis khususnya Tentuwin (emil, sri, winda, ipit, nita,
rika, pipi, iza, k’ira, k’ve yang telah memberikan dukungan dalam
menyelesaikan penelitian dan penulisan skripsi
7. Semua mahasiswa/wi farmasi khususnya farmasi ekstensi 2009 yang tidak
disebutkan satu persatu, terimakasih untuk semangat dan do’a nya.
Semoga skripsi ini dapat menjadi sumbangan yang berarti bagi ilmu
pengetahuan khususnya pada ilmu farmasi. Penulis mengharapkan kritik dan saran
demi kesempurnaan skripsi ini.
Medan, Juni 2011
Penulis
Karakterisasi Simplisia dan Isolasi serta Analisis Komponen Minyak Atsiri Secara GC-MS dari Rimpang Tanaman Temu Putih
(Kaemferia rotunda L.) Abstrak
Minyak atsiri merupakan minyak yang mudah menguap dengan komposisi yang berbeda– beda sesuai sumber penghasilnya dan terdiri dari campuran zat yang memiliki sifat fisika kimia berbeda-beda. Temu putih (Kaemferia rotunda L.) famili Zingiberaceae adalah salah satu tanaman yang mengandung minyak atsiri dan banyak dimanfaatkan masyarakat sebagai obat anti kanker.
Penelitian yang dilakukan meliputi karakterisasi simplisia, isolasi minyak atsiri dengan cara destilasi air dan analisis komponen minyak atsiri secara Gas Chromatography-Mass Spectrophotometry (GC-MS) dari simplisia temu putih.
Hasil karakterisasi simplisia rimpang temu putih diperoleh kadar air 7,33%; kadar sari yang larut dalam air 18,91%; kadar sari yang larut dalam etanol 7,62%; kadar abu total 3,77%; kadar abu yang tidak larut dalam asam 0,15%; hasil penetapan kadar minyak atsiri dengan alat Stahl diperoleh kadar minyak atsiri rimpang temu putih sebesar 1,09 % v/b. Hasil penetapan indeks bias minyak atsiri rimpang temu putih diperoleh sebesar 1,5020 bobot jenis minyak atsiri rimpang temu putih sebesar 0,9144.
Hasil analisis GC-MS minyak atsiri yang diperoleh dari rimpang temu putih menunjukkan 31 komponen dan terdapat 6 senyawa sebagai komponen utama yaitu: Benzyl benzoat (60,71%), Hexadecane (29,22%), pentadecane (2,11%), Camphene (1,60%), Bornyl acetate (1,19%), dan Siklopropazulen (0,08%).
Characteristic of Simplex and Isolation and Analyzed Volatile Oil Component by GC-MS from Rhizome of White Ginger
(Kaemferia rotunda L.) Abstract
Volatile oil represents the essential oil with the different composition with chemical physics different. White Ginger (Kaemferia
rotunda L.) of the family Zingiberaceae is one part of species that contain
volatile oil and a lot of exploited asanti cancer.
The purpose of this research include simplex characteritation, isolation of volatile oil was accomplished by water destillation and analyzed volatile oil components by Gas Cromatography-Mass
Spectrophotometry (GC-MS) from simplex of white ginger (Kaemferia rotunda L.).
The result of simplex characteritation from simplex of white ginger obtained water value 7,33%, water soluable extract value 18,91%, ethanol soluble extract value 7,62%, total ash value 3,77%, acid insoluble ash value 0,15%, the volatile oil content of White Ginger 1,09 % v/b, the refractive index volatile oil of white ginger is 1,5020 and specific gravity is 0,9144.
The result of GC-MS analyzed of volatile oil from white ginger of obtained 31 compounds, 6 compounds of them was main compound, i.e. Benzyl benzoic (60,71%), Hexadecane (29,22%), Pentadecane (2,11%), Camphene (1,60%), Bornyl acetate (1,19%) and Siklopropazulen (0,08%).
DAFTAR ISI
Halaman
JUDUL ... i
LEMBAR PENGESAHAN ... ii
KATA PENGANTAR ... iv
ABSTRAK ... vi
ABSTRACT ... vii
DAFTAR ISI ... viii
DAFTAR TABEL ... xii
DAFTAR GAMBAR... xiii
DAFTAR LAMPIRAN ... xiv
BAB I PENDAHULUAN ... 1
1.1 Latar Belakang ... 1
1.2 Perumusan masalah ... 3
1.3 Hipotesis... 3
1.4 Tujuan penelitian ... 3
1.5 Manfaat penelitian ... 3
BAB II TINJAUAN PUSTAKA ... 4
2.1. Uraian Tanaman ... 4
2.1.1. Nama Daerah ... 4
2.1.2. Taksonomi Tanaman ... 5
2.1.3. Morfologi Tumbuhan ... 5
2.1.4. Kandungan Senyawa Kimia ... 6
2.2. Minyak Atsiri ... 6
2.2.1. Lokalisasi Minyak Atsiri ... 7
2.2.2. Aktivitas Biologi Minyak Atsiri dan Penggunaan ... 7
2.2.3. Komposisi kimia minyak atsiri ... 7
2.3 Cara isolasi minyak atsiri ... 9
2.3.1. Metode Penyulingan ... 9
2.3.2. Metode Pengepresan ... 10
2.3.3. Ekstraksi dengan Pelarut Menguap ... 10
2.3.4. Ekstraksi dengan Lemak ... 10
2.4 Analisa Komponen Minyak Atsiri dengan GC-MS ... 11
2.4.1. Kromatografi Gas ... 11
2.4.1.1. Gas Pembawa ... 12
2.4.1.2. Sistem Injeksi ... 12
2.4.1.3 Kolom ... 12
2.4.1.4. Fase diam ... 13
2.4.1.5. Suhu ... 13
2.4.1.5.1. Suhu injektor ... 13
2.4.1.5.2. Suhu kolom ... 14
2.4.1.5.3. Suhu detektor ... 14
2.4.1.6 Detektor ... 14
BAB III METODOLOGI PENELITIAN... 16
3.1 Alat-alat ... 16
3.2 Bahan-bahan ... 16
3.3 Penyiapan Bahan Tumbuhan ... 16
3.3.1. Pengambilan Bahan Tumbuhan ... 17
3.3.2.Identifikasi Tumbuhan ... 17
3.3.3. Pembuatan Simplisia ... 17
3.4 Pemeriksaan Karakteristik Simplisia... 17
3.4.1. Pemeriksaan Makroskopik ... 17
3.4.2. Pemeriksaan Mikroskopik ... 17
3.4.3. Penetapan Kadar Air... 18
3.4.4. Penetapan Kadar Sari Larut dalam Air ... 18
3.4.5. Penetapan Kadar Sari yang Larut dalam Etanol ... 19
3.4.6. Penetapan Kadar Abu Total ... 19
3.4.7. Penetapan Kadar Abu yang Tidak Larut dalam Asam ... 19
3.4.8. Penetapan Kadar Minyak Atsiri ... 20
3.5. Isolasi Minyak Atsiri ... 20
3.6. Identifikasi Minyak Atsiri... 21
3.6.1. Penetapan Parameter Fisika ... 21
3.6.1.1. Penentuan Indeks Bias ... 21
3.6.1.2. Penentuan Bobot Jenis ... 21
BAB IV HASIL DAN PEMBAHASAN ... 23
4.1. Identifikasi Tumbuhan ... 23
4.2. Karakterisasi Simplisia Temu Putih ... 23
4.3. Identifikasi Minyak Atsiri ... 25
4.4. Analisis dengan GC-MS ... 27
4.5. Analisis dan Fragmentasi Hasil spektrofotometri massa ... 29
BAB V KESIMPULAN DAN SARAN ... 34
5.1. Kesimpulan ... 34
5.2. Saran ... 34
DAFTAR PUSTAKA ... 35
DAFTAR TABEL
Tabel 4.1. Hasil Karakterisasi Serbuk Simplisia Temu Putih ... 23
Tabel 4.2. Hasil Penetapan Kadar Minyak Atsiri ... 25
Tabel 4.3. Hasil Penentuan Indeks Bias dan Bobot Jenis Minyak Atsiri... 26
DAFTAR GAMBAR
Gambar 1. Kromatogram GC-MS Minyak Atsiri Temu Putih ... 27
Gambar 2. Rumus Bangun dari Senyawa Benzyl benzoate ... 29
Gambar 3. Rumus Bangun dari Senyawa Hexadecane ... 30
Gambar 4. Rumus Bangun dari Senyawa Camphene... 31
Gambar 5. Rumus Bangun dari Senyawa Pentadecane... 31
Gambar 6. Rumus Bangun dari Senyawa Bornyl acetate... 32
DAFTAR LAMPIRAN
Halaman
Lampiran 1. Hasil Identifikasi Tumbuhan ... 37
Lampiran 2. Foto Morfologi Tanaman Temu Putih ... 38
Lampiran 3. Foto Simplisia Temu Putih ... 39
Lampiran 4. Hasil Pemeriksaan Mikroskopik ... 40
Lampiran 5. Alat- alat Yang Digunakan Dalam Penelitian ... 41
Lampiran 6. Hasil Pemeriksaan Karakterisasi Simplisa ... 44
Lampiran 7. Bagan Kerja Penelitian ... 52
Lampiran 8. Kromatogram GC-MS Minyak Atsiri Temu Putih ... 53
Lampiran 9. Spektrum Massa Minyak Atsiri Temu Putih ... 55
Karakterisasi Simplisia dan Isolasi serta Analisis Komponen Minyak Atsiri Secara GC-MS dari Rimpang Tanaman Temu Putih
(Kaemferia rotunda L.) Abstrak
Minyak atsiri merupakan minyak yang mudah menguap dengan komposisi yang berbeda– beda sesuai sumber penghasilnya dan terdiri dari campuran zat yang memiliki sifat fisika kimia berbeda-beda. Temu putih (Kaemferia rotunda L.) famili Zingiberaceae adalah salah satu tanaman yang mengandung minyak atsiri dan banyak dimanfaatkan masyarakat sebagai obat anti kanker.
Penelitian yang dilakukan meliputi karakterisasi simplisia, isolasi minyak atsiri dengan cara destilasi air dan analisis komponen minyak atsiri secara Gas Chromatography-Mass Spectrophotometry (GC-MS) dari simplisia temu putih.
Hasil karakterisasi simplisia rimpang temu putih diperoleh kadar air 7,33%; kadar sari yang larut dalam air 18,91%; kadar sari yang larut dalam etanol 7,62%; kadar abu total 3,77%; kadar abu yang tidak larut dalam asam 0,15%; hasil penetapan kadar minyak atsiri dengan alat Stahl diperoleh kadar minyak atsiri rimpang temu putih sebesar 1,09 % v/b. Hasil penetapan indeks bias minyak atsiri rimpang temu putih diperoleh sebesar 1,5020 bobot jenis minyak atsiri rimpang temu putih sebesar 0,9144.
Hasil analisis GC-MS minyak atsiri yang diperoleh dari rimpang temu putih menunjukkan 31 komponen dan terdapat 6 senyawa sebagai komponen utama yaitu: Benzyl benzoat (60,71%), Hexadecane (29,22%), pentadecane (2,11%), Camphene (1,60%), Bornyl acetate (1,19%), dan Siklopropazulen (0,08%).
Characteristic of Simplex and Isolation and Analyzed Volatile Oil Component by GC-MS from Rhizome of White Ginger
(Kaemferia rotunda L.) Abstract
Volatile oil represents the essential oil with the different composition with chemical physics different. White Ginger (Kaemferia
rotunda L.) of the family Zingiberaceae is one part of species that contain
volatile oil and a lot of exploited asanti cancer.
The purpose of this research include simplex characteritation, isolation of volatile oil was accomplished by water destillation and analyzed volatile oil components by Gas Cromatography-Mass
Spectrophotometry (GC-MS) from simplex of white ginger (Kaemferia rotunda L.).
The result of simplex characteritation from simplex of white ginger obtained water value 7,33%, water soluable extract value 18,91%, ethanol soluble extract value 7,62%, total ash value 3,77%, acid insoluble ash value 0,15%, the volatile oil content of White Ginger 1,09 % v/b, the refractive index volatile oil of white ginger is 1,5020 and specific gravity is 0,9144.
The result of GC-MS analyzed of volatile oil from white ginger of obtained 31 compounds, 6 compounds of them was main compound, i.e. Benzyl benzoic (60,71%), Hexadecane (29,22%), Pentadecane (2,11%), Camphene (1,60%), Bornyl acetate (1,19%) and Siklopropazulen (0,08%).
BAB I PENDAHULUAN 1.1. Latar Belakang
Minyak atsiri yang juga disebut minyak eteris merupakan minyak yang
mudah menguap dengan komposisi yang berbeda-beda sesuai sumber
penghasilnya. Minyak atsiri bukan merupakan zat kimia tunggal murni, melainkan
merupakan campuran zat-zat yang memiliki sifat fisika dan kimia berbeda-beda
(Lutony dan Rahmayanti, 1994).
Peranan paling utama dari minyak atsiri terhadap tanaman itu sendiri adalah
sebagai pengusir serangga serta sebagai pengusir hewan-hewan pemakan daun
lainnya. Namun sebaliknya minyak atsiri berfungsi sebagai penarik serangga guna
membantu terjadinya penyerbukan silang dari bunga (Tyler,et al,1970).
Kegunaan minyak atsiri sangat luas dan spesifik, khususnya dalam berbagai
bidang industri, antara lain industri makanan digunakan sebagai bahan penyedap,
industri parfum sebagai pewangi, industri farmasi, bahkan digunakan pula sebagai
insektisida. Salah satu tanaman penghasil minyak atsiri adalah temu putih
(Lutony, 1994)
Temu putih (Kaemferia rotunda L.) di Jawa Tengah dikenal dengan nama
kunir putih. Daunnya berbentuk bundar menjorong lebar, berwarna hijau muda.
Bunganya bermunculan diatas batang semu yang amat pendek. Akarnya
berdaging seolah membengkak, membentuk umbi yang tidak terlalu besar, yakni
hanya seukuran telur puyuh, rimpang temu putih berwarna pucat, banyak serat,
Sebagai obat-obatan temu putih ini lebih banyak digunakan untuk
mengatasi gangguan pencernaan, penurun panas, perangsang nafsu makan
termasuk juga sebagai antineoplastik (antikanker).
Minyak atsiri dapat diproduksi dengan beberapa metode, namun sebagian
besar minyak atsiri diperoleh dengan metode penyulingan yang dikenal dengan
hidrodestilasi. Cara lain adalah metode ekstraksi yang menggunakan pelarut dan
metode pengempaan (Lutony & Rahmayati, 1994).
Pada beberapa literatur metode penyulingan minyak atsiri dari rimpang temu
putih dilakukan dengan cara destilasi uap (steam destillation). Komponen utama
minyak atsiri dari temu putih ini diantaranya adalah benzyl benzoate (30,61%)
dan siklopropazulen (26,85%) (Anonim, 2005).
Dalam hal ini penulis ingin meneliti salah satu tanaman penghasil minyak
atsiri yaitu temu putih (Kaemferia rotunda L.) yang layak untuk dikembangkan
karena kandungan minyak atsiri didalamnya cukup banyak.
Oleh karena itu penulis ingin melakukan penyulingan minyak atsiri dari
temu putih dengan metode destilasi air (water distillation) dan ingin melihat
apakah ada perbedaan hasil komponen minyak atsiri yang ditemukan.
Pada metode ini, tanaman yang akan disuling mengalami kontak langsung
dengan air mendidih. Bahan terendam secara sempurna, sehingga penyulingan
minyak atsiri dapat berlangsung secara sempurna.
Hasil penelitian ini diharapkan bermanfaat bagi ilmu pengetahuan untuk
dapat mengembangkan penelitian tentang bahan alam penghasil minyak atsiri
yang banyak terdapat di Indonesia, dan dapat memberikan informasi komponen
1.2. Perumusan Masalah
Berdasarkan latar belakang masalah di atas dapat diambil perumusan
masalah sebagai berikut :
1. Apakah cara destilasi air dapat digunakan untuk mengisolasi minyak
atsiri rimpang temu putih (Kaemferia rotunda L.)?
2. Apakah komponen minyak atsiri rimpang temu putih (Kaemferia
rotunda L.) dapat dipisahkan dan dianalisis secara GC-MS ?
1.3. Hipotesis
Berdasarkan perumusan masalah di atas maka hipotesisnya adalah :
1. Cara destilasi air dapat digunakan untuk mengisolasi minyak atsiri
rimpang temu putih (Kaemferia rotunda L.)
2. Komponen minyak atsiri rimpang temu putih (Kaemferia rotunda L.)
dapat dipisahkan dan dianalisis secara GC-MS.
1.4. Tujuan Penelitian
Adapun tujuan dari penelitian ini adalah untuk mengisolasi serta
menganalisis komponen minyak atsiri rimpang temu putih (Kaemferia rotunda L.)
secara GC-MS.
1.5. Manfaat Penelitian
Hasil dari penelitian ini diharapkan memberikan informasi tentang
komponen minyak atsiri rimpang temu putih (Kaemferia rotunda L.) serta
bermanfaat bagi ilmu pengetahuan untuk dapat mengembangkan penelitian
BAB II
TINJAUAN PUSTAKA 2.1. Uraian Tanaman
Kunci pepet termasuk kerabat temu-temuan, tanaman ini masih satu genus
dengan temu kunci, yakni genus Kaemferia. Kunci pepet (Kaemferia rotunda L.)
di Jawa Tengah dikenal dengan nama temu putih atau kunir putih. Daunnya
berbentuk bundar menjorong lebar, berwarna hijau muda. Bunganya bermunculan
diatas batang semu yang amat pendek dengan daun yang menutupi permukaan
tanah, bunga tumbuh bergerombolan. Rimpang temu putih tumbuh pendek, ada
beberapa rimpang yang sekaligus tumbuh bergerombolan. Akarnya berdaging
seolah membengkak, membentuk umbi yang tidak terlalu besar, yakni hanya
seukuran telur puyuh, rimpang temu putih berwarna pucat, banyak serat, dan
rasanya pahit.
2.1.1. Nama Daerah
Nama daerah dari temu putih adalah kunir putih, ardong, kunci pepet
(Jawa), temu putri (Jakarta), konce pet (Madura). Namun soal nama ini perlu
berhati-hati, karena kunir putih atau kunyit putih juga merupakan nama dari
Curcuma zedoaria dan kunci pepet juga digunakan untuk menyebut Kaempferia
angustifolia. Dalam bahasa Inggris Kaempferia rotunda dikenal sebagai
2.1.2 Taksonomi Tanaman
Menurut Johnny ria hutapea (2002), sistematika tanaman temu putih adalah
sebagai berikut:
Devisi : Spermatophyta
Subdivisi : Angiospermae
Kelas : Monocotyledoneae
Bangsa : Zingiberales
Suku : Zingiberaceae
Marga : Kaemferia
Jenis : Kaemferia rotunda L.
2.1.3 Morfologi Tumbuhan
Tanaman temu putih merupakan habitus semak, semusim yang tingginya
30-70 cm. Ciri-ciri morfologi tanaman temu putih sebagai berikut:
Batang : lunak, berpelepah, membentuk rimpang, hitam keabu-abuan
Daun : tunggal, lanset, ujung runcing, pangkal berpelepah, tepi rata, ibu
tulang daun menonjol, panjang ± 70 cm, hijau muda.
Bunga : majemuk, bentuk tabung, kelopak lanset, panjang 4-8 cm, lebar
2-3, 5 cm, mahkota panjang 10-19 cm, benang sari dan putik kecil,
putih.
Akar : serabut, putih.
Rimpang : rimpang kunyit rasanya agak pahit dan getir dengan bau yang
khas, warnanya jingga kecoklatan dari luar, sedangkan bagian
2.1.4 Kandungan Senyawa Kimia
Rimpang dan daun Kaemferia rotunda mengandung kurkuminoid,
saponin, tanin dan minyak atsiri. Minyak temu putih mengandung 0,15 % minyak
atsiri yang terdiri dari 11 senyawa dan terdapat 2 sebagai komponen utama, yaitu
benzyl benzoate (30,61%), dan siklopropazulen (26,85%) (Agusta, 2000).
2.1.5 Kegunaan Tanaman
Kunyit putih dapat membantu mencegah kerusakan sel. Sedangkan
kandungan minyak atsiri, kunyit putih dapat dipakai untuk menjaga kesehatan
saluran pernafasan dan pencernaan. Kunyit Putih sangat bermanfaat untuk :
Kanker, Tumor, Kista, dan Kolesterol. Selain itu oleh peracik jamu dan insustri
obat-obatan digunakan sebagai campuran obat-obatan, campuran jamu-jamu,
kosmetik tradisional, dan minuman dari ramuan temu lawak, selain itu enak
dijadikan lalap (Fauziah, 1987).
2.2 Minyak Atsiri
Minyak atsiri yang dikenal juga dengan nama minyak eteris atau minyak
terbang ( essential oil, volatile oil) dihasilkan oleh tanaman. minyak tersebut
mudah menguap pada suhu kamar tanpa mengalami dekomposisi, mempunyai
rasa getir, berbau wangi sesuai dengan bau tanaman penghasilnya, umumnya larut
dalam pelarut organik dan tidak larut dalam air (Ketaren, 1985).
2.2.1 Lokalisasi minyak atsiri
Minyak atsiri terkandung dalam berbagai organ, seperti di dalam rambut
kelenjar (pada famili Labiatae), di dalam sel-sel parenkim (misalnya famili
Piperaceae), di dalam saluran minyak yang disebut vittae (famili Umbellliferae),
Rutaceae), terkandung di dalam semua jaringan (pada famili Coniferae), pada
kayu manis (Lauraceae) banyak ditemui di kulit batang (korteks) (Gunawan &
Mulyani, 2004).
2.2.2 Aktivitas Biologi Minyak Atsiri dan Penggunaan
Pada tanaman, minyak atsiri mempunyai tiga fungsi yaitu: membantu
proses penyerbukan dan menarik beberapa jenis serangga atau hewan, mencegah
kerusakan tanaman oleh serangga atau hewan, dan sebagai cadangan makanan
bagi tanaman (Ketaren, 1985).
Minyak atsiri digunakan sebagai bahan baku dalam berbagai industri,
misalnya industri parfum, kosmetika, farmasi, bahan penyedap (flavoring agent)
dalam industri makanan dan minuman (Ketaren, 1985).
2.2.3 Komposisi kimia minyak atsiri
Minyak atsiri terdiri dari berbagai campuran persenyawaan kimia dengan
sifat fisika dan kimia yang juga berbeda. Pada umumnya perbedaan komposisi
minyak atsiri disebabkan perbedaan kondisi iklim, tanah tempat tumbuh, umur
panen, metode ekstraksi yang digunakan, cara penyimpanan minyak dan jenis
tanaman penghasil.
Minyak atsiri biasanya tersusun dari unsur Karbon (C), Hidrogen (H), dan
oksigen (O). Pada umumnya komponen kimia minyak atsiri dibagi menjadi dua
golongan yaitu: 1) Hidrokarbon, yang terutama terdiri dari persenyawaan terpen
dan 2) Hidrokarbon teroksigenasi.
a. Golongan hidrokarbon
Persenyawaan yang termasuk golongan ini terbentuk dari unsur Karbon
sebagian besar terdiri dari monoterpen (2 unit isopren), sesquiterpen (3 unit
isopren) dan diterpen (4 unit isopren)
b. Golongan hidrokarbon teroksigenasi
Komponen kimia dari golongan persenyawaan ini terbentuk dari unsur
Karbon (C), Hidrogen (H) dan Oksigen (O). Persenyawaan yang termasuk dalam
golongan ini adalah persenyawaan alkohol, aldehid, keton, ester, eter dan fenol.
Ikatan karbon yang terdapat dalam molekulnya dapat terdiri dari ikatan tunggal,
ikatan rangkap dua dan ikatan rangkap tiga. Terpen mengandung ikatan tunggal
dan ikatan rangkap dua.
Senyawa terpen memiliki aroma kurang wangi, sukar larut dalam alkohol encer
dan jika disimpan dalam waktu lama akan membentuk resin. Golongan
hidrokarbon teroksigenasi merupakan senyawa yang penting dalam minyak atsiri
karena umumnya aroma yang lebih wangi (Ketaren, 1985).
2.3 Cara isolasi minyak atsiri
Isolasi minyak atsiri dapat dilakukan dengan beberapa cara yaitu: 1) penyulingan
(distillation), 2) pengepresan (pressing), 3) ekstraksi dengan pelarut menguap
(solvent extraction), 4) ekstraksi dengan lemak.
2.3.1 Metode penyulingan
a. Penyulingan dengan air
Pada metode ini, bahan tanaman yang akan disuling mengalami kontak
langsung dengan air mendidih. Bahan dapat mengapung di atas air atau terendam
khas model ini yaitu adanya kontak langsung antara bahan dan air mendidih. Oleh
karena itu, sering disebut penyulingan langsung.
Penyulingan dengan cara langsung ini dapat menyebabkan banyaknya
rendemen minyak yang hilang (tidak tersuling) dan terjadi pula penurunan mutu
minyak yang diperoleh.
b. Penyulingan dengan uap
Model ini disebut juga penyulingan uap atau penyulingan tak langsung.
Pada prinsipnya, model ini sama dengan penyulingan langsung. Hanya saja, air
penghasil uap dan bahan yang akan disuling berada pada ketel yang berbeda. Uap
yang digunakan berupa uap jenuh.
c. Penyulingan dengan air dan uap
Pada model penyulingan ini, bahan tanaman yang akan disuling diletakkan
di atas rak-rak atau saringan. Kemudian ketel penyulingan diisi dengan air sampai
permukaannya tidak jauh dari bagian bawah saringan. Ciri khas model ini yaitu
uap selalu dalam keadaan basah, jenuh, dan tidak terlalu panas. Bahan tanaman
yang akan disuling hanya berhubungan dengan uap dan tidak dengan air panas
(Lutony & Rahmayati, 2000).
2.3.2 Metode pengepresan
Ekstraksi minyak atsiri dengan cara pengepresan umumnya dilakukan
terhadap bahan berupa biji, buah atau kulit buah yang memiliki kandungan
minyak atsiri yang cukup tinggi. Akibat tekanan pengepresan, maka sel-sel yang
permukaan bahan, misalnya minyak atsiri dari kulit jeruk dapat diperoleh dengan
cara ini (Ketaren, 1985).
2.3.3 Ekstraksi dengan pelarut menguap
Prinsipnya adalah melarutkan minyak atsiri dalam pelarut organik yang
mudah menguap. Ekstraksi dengan pelarut organik pada umumnya digunakan
untuk mengekstraksi minyak atsiri yang mudah rusak oleh pemanasan uap dan air,
terutama untuk mengekstraksi minyak atsiri yang berasal dari bunga misalnya
bunga cempaka, melati, mawar dan kena (Ketaren, 1985).
2.3.4 Ekstraksi dengan lemak padat
Proses ini umumnya digunakan untuk mengekstraksi bunga-bungaan,
untuk mendapatkan mutu dan rendeman minyak atsiri yang tinggi. Metode
ekstraksi dapat dilakukan dengan dua cara yaitu enfleurasi dan maserasi (Ketaren,
1985).
2.4 Analisa Komponen Minyak Atsiri dengan GC-MS
2.4.1 Kromatografi gas
Kromatografi gas digunakan untuk memisahkan komponen campuran
kimia dalam suatu bahan, berdasarkan perbedaan polaritas campuran. Fase gerak
akan membawa campuran sampel menuju kolom. Campuran dalam fase gerak
akan berinteraksi dengan fase diam. Setiap komponen yang terdapat dalam
campuran berinteraksi dengan kecepatan yang berbeda dimana interaksi
komponen dengan fase diam dengan waktu yang paling cepat akan keluar pertama
Waktu yang menunjukkan berapa lama suatu senyawa tertahan di kolom
disebut waktu tambat (waktu retensi) yang diukur mulai saat penyuntikan sampai
saat elusi terjadi (Gritter, dkk., 1991).
Menurut Eaton (1989), hal yang mempengaruhi waktu retensi yaitu:
1. Sifat senyawa, semakin sama kepolaran dengan kolom dan makin kurang keatsiriannya maka akan tertahan lebih lama di kolom dan sebaliknya.
2. Sifat adsorben, semakin sama kepolaran maka senyawa akan semakin lama tertahan dan sebaliknya.
3. Konsentrasi adsorben, semakin banyak adsorben maka senyawa semakin lama tertahan dan sebaliknya.
4. Temperatur kolom, semakin rendah temperatur maka senyawa semakin lama tertahan dan sebaliknya.
5. Aliran gas pembawa, semakin kecil aliran gas maka senyawa semakin lama tertahan dan sebaliknya.
6. Panjang kolom, semakin panjang kolom akan menahan senyawa lebih lama dan sebaliknya.
Bagian utama dari kromatografi gas adalah gas pembawa, sistem injeksi, kolom,
fase diam, suhu dan detektor.
2.4.1.1 Gas Pembawa
Gas pembawa harus memenuhi persyaratan antara lain harus inert, murni,
dan mudah diperoleh. Pemilihan gas pembawa tergantung pada detektor yang
dipakai, semua gas yang dipakai ini harus tidak reaktif, dapat dibeli dalam
Gas pembawa yang sering dipakai adalah helium (He), argon (Ar), nitrogen (N2),
hidrogen (H2), dan karbon dioksida (CO2) (Gritter, 1991).
2.4.1.2 Sistem Injeksi
Cuplikan dimasukkan kedalam ruang suntik melalui gerbang suntik,
biasanya berupa lubang yang ditutupi dengan septum atau pemisah karet. Ruang
suntik harus dipanaskan tersendiri, terpisah dari kolom, dan biasanya pada suhu
10-15oC lebih tinggi dari suhu maksimum. Jadi seluruh cuplikan diuapkan segera
setelah disuntikkan dan dibawa ke kolom (Gritter, dkk., 1991).
2.4.1.3 Kolom
Kolom merupakan tempat terjadinya proses pemisahan karena di
dalamnya terdapat fase diam. Oleh karena itu, kolom merupakan hal sentral dalam
kromatografi gas. Ada dua jenis kolom pada kromatografi gas yaitu kolom kemas
(packing column) dan kolom kapiler (capillary column).
Kolom kemas terdiri atas fase cair yang tersebar pada permukaan
penyangga yang lembam (inert) yang terdapat dalam tabung yang relatif besar
(diameter dalam 1-3mm). Kolom kapiler jauh lebih kecil (0,02 – 0,2 mm) dan
dinding kapiler bertindak sebagai penyangga lembam untuk fase diam cair.
Semakin sempit diameter kolom, maka efisiensi pemisahan kolom semakin besar
atau puncak kromatogram yang dihasilkan semakin tajam. Pada umumnya,
seorang analis akan memilih kolom dengan diameter 0,2 atau yang lebih kecil
ketika menganalisis sampel dengan konsentrasi yang kecil atau memisahkan
2.4.1.4 Fase diam
Banyak macam bahan kimia yang dipakai sebagai fase diam antara lain:
squalen, DEGS (Dietilglikol suksinat). Fase diam yang dipakai dalam kolom
kapiler dapat bersifat non polar, polar atau semi polar. Jenis fase diam akan
menentukan urutan elusi komponen – komponen dalam campuran. Seorang analis
harus memilih fase diam yang mampu memisahkan komponen – komponen dalam
sampel (Rohman, 2007).
2.4.1.5 Suhu
Tekanan uap sangat bergantung pada suhu, maka suhu merupakan faktor utama
dalam GC. Pada GC-MS terdapat tiga pengendali suhu yang berbeda, yaitu: suhu
injektor, suhu kolom, suhu detektor.
2.4.1.5.1 Suhu injektor
Suhu injektor harus cukup panas untuk menguapkan cuplikan dengan cepat
sehingga tidak menghilangkan keefisienan cara penyuntikan. Tetapi sebaliknya,
suhu harus cukup rendah untuk mencegah peruraian atau penataan ulang akibat
panas (McNair and Bonelli, 1988).
2.4.1.5.2 Suhu kolom
Suhu kolom harus cukup tinggi sehingga analisis dapat diselesaikan dalam
waktu yang sesuai, dan harus cukup rendah sehingga terjadi pemisahan.
Umumnya semakin rendah suhu kolom, semakin tinggi koefisien partisi dalam
fase diam sehingga hasil pemisahan semakin baik. Pada beberapa hal tidak dapat
digunakan suhu kolom yang rendah, terutama bila cuplikan terdiri atas senyawa
2.4.1.5.3 Suhu detektor
Detektor harus cukup panas sehingga cuplikan dan air atau hasil samping
yang terbentuk pada proses pengionan tidak mengembun (McNair and
Bonelli,1988).
2.4.1.6 Detektor
Menurut McNair dan Bonelli (1988) ada dua detektor yang popular yaitu
detektor hantar-thermal (DHB) dan detektor pengion nyala (DPN).
2.4.2 Spektrometri massa
Spektrofotometer massa pada umumnya digunakan untuk:
1. Menentukan massa molekul
2. Menentukan rumus molekul dengan menggunakan Spektrum Massa
Beresolusi Tinggi (High Resolution Mass Spectra)
3. mengetahui informasi dari struktur dengan melihat pola fragmentasinya (Dachriyanus,2004)
Spektrometer massa terdiri dari sistem pemasukan cuplikan, ruang pengion
dan percepatan, tabung analisis, pengumpul ion dan penguat, dan pencatat.
Keuntungan utama spektrometri massa sebagai metode analisis yaitu metode ini
lebih sensitif dan spesifik untuk identifikasi senyawa yang tidak diketahui atau
untuk menetapkan keberadaan senyawa tertentu. Hal ini disebabkan adanya pola
fragmentasi yang khas sehingga dapat memberikan informasi mengenai bobot
BAB III
METODOLOGI PENELITIAN
Metodologi penelitian ini meliputi penyiapan sampel, pemeriksaan
karakteristik simplisia, isolasi dan analisis komponen – komponen minyak atsiri
dari rimpang temu putih (Kaemferia rotunda L.) secara GC – MS.
3.1. Alat – Alat
Alat – alat yang digunakan dalam percobaan adalah alat – alat gelas
laboratorium, timbangan kasar (Ohaus), lemari pengering, neraca analitik (Mettler
Toledo), seperangkat alat Stahl, seperangkat alat destilasi air (Water Destillation),
oven, mikroskop, Gas Chromatograph – Mass Spectrometer (GC-MS) model
Shimadzu QP 2010 S.
3.2. Bahan – Bahan
Bahan – bahan yang digunakan dalam percobaan ini adalah rimpang temu
putih (Kaemferia rotunda L.), air suling, etanol 96%, sudan III, toluen pro analisa
(E.Merck), kloroform pro analisa (E.Merck), dan natrium sulfat anhidrat pro
analisa (E.Merck), kloralhidrat (E.Merck), kloroform (E.Merck), HCl pro analisa
(E.Merck).
3.3. Penyiapan Bahan Tumbuhan
Penyiapan bahan tumbuhan meliputi pengambilan bahan tumbuhan,
3.3.1. Pengambilan Bahan Tumbuhan
Pengambilan bahan tumbuhan dilakukan secara purposif yaitu diambil dari
satu daerah saja tanpa membandingkan dengan tumbuhan yang sama di daerah
lain. Temu putih ada 2 jenis, tumbuhan yang digunakan dalam penelitian ini
adalah jenis temu putih yang daunnya berwarna sedikit ungu. Bahan diperoleh
dari Pasar Sentral Pajak Sambu Kecamatan Medan Kota Provinsi Sumatera Utara.
3.3.2. Identifikasi Tumbuhan
Identifikasi tumbuhan dilakukan di Pusat Penelitian Biologi LIPI Bogor.
3.3.3. Pembuatan Simplisia
Rimpang dibersihkan dari tanah yang melekat dan dicuci dengan air
hingga bersih, lalu ditiriskan. Kemudian rimpang dirajang secara melintang
dengan ketebalan 3-4 mm, lalu ditimbang. Selanjutnya dikeringkan di lemari
pengering pada suhu 50-60 oC sampai simplisia rapuh (sekitar satu minggu)
kemudian ditimbang.
3.4. Pemeriksaan Karakteristik Simplisia 3.4.1. Pemeriksaan Makroskopik
Pemeriksaan makroskopik dilakukan dengan mengamati bentuk luar dari
simplisia rimpang temu putih.
3.4.2. Pemeriksaan Mikroskopik
Pemeriksaan mikroskopik dilakukan terhadap serbuk simplisia rimpang
temu putih. Serbuk simplisia ditaburkan diatas kaca objek yang telah ditetesi
dengan larutan kloralhidrat dan ditutup dengan kaca penutup, kemudian diamati di
kaca objek yang telah ditetesi sudan III. Sedangkan untuk melihat pati serbuk
simpisia diatas kaca objek yang telah ditetesi air.
3.4.3. Penetapan Kadar Air a. Penjenuhan Toluen
Sebanyak 200 ml toluen dimasukkan kedalam labu alas bulat, lalu
ditambahkan 2 ml air suling, kemudian alat dipasang dan dilakukan destilasi
selama 2 jam. Destilasi dihentikan dan dibiarkan dingin selama ± 30 menit,
kemudian volume air dalam tabung penerima dibaca dengan ketelitian 0,1 ml.
b. Penetapan Kadar Air Simplisia
Dimasukkan 5 g serbuk simplisia ke dalam labu tersebut, lalu dipanaskan
hati – hati selama 15 menit. Setelah toluen mendidih, kecepatan tetesan diatur 2
tetes per detik sampai sebagian besar air terdestilasi, kemudian kecepatan destilasi
dinaikkan sampai 4 tetes per detik. Setelah semua air terdestilasi, bagian dalam
pendingin dibilas dengan toluen. Destilasi dilanjutkan selama 5 menit, kemudian
tabung penerima dibiarkan mendingin pada suhu kamar. Setelah air dan toluen
memisah sempurna, volume air dibaca dengan ketelitian 0,1 ml. Selisih kedua
volume air yang dibaca sesuai dengan kadar air yang terdapat dalam bahan yang
diperiksa. Kadar air dihitung dalam persen (WHO,1992).
3.4.4. Penetapan Kadar Sari Larut dalam Air
Sebanyak 5 g serbuk simplisia yang telah dikeringkan, dimaserasi selama
24 jam dalam 100 ml air – kloroform (2,5 ml kloroform dalam air suling sampai 1
liter) dalam labu bersumbat sambil sesekali dikocok selama 6 jam pertama,
diuapkan sampai kering dalam cawan penguap yang rata yang telah dipanaskan
dan ditara. Sisa dipanaskan pada suhu 1050C sampai bobot tetap.
Kadar dalam persen sari yang larut dalam air dihitung terhadap bahan yang telah
dikeringkan (Depkes,1977).
3.4.5. Penetapan Kadar Sari yang Larut dalam Etanol
Sebanyak 5 g serbuk simplisia yang telah dikeringkan, dimaserasi selama
24 jam dalam 100 ml etanol 96% dalam labu bersumbat sambil sesekali dikocok
selama 6 jam pertama, kemudian dibiarkan selama 18 jam, lalu disaring. Sejumlah
20 ml filtrat pertama diuapkan sampai kering dalam cawan penguap yang rata
yang telah dipanaskan dan ditara. Sisa dipanaskan pada suhu 1050C sampai bobot
tetap. Kadar dalam persen sari yang larut dalam etanol 96% dihitung terhadap
bahan yang telah dikeringkan (Depkes, 1977).
3.4.6. Penetapan Kadar Abu Total
Sebanyak 2 g serbuk simplisia yang telah digerus dan ditimbang seksama
dimasukkan dalam krus porselin yang telah dipijar dan ditara, kemudian
diratakan. Krus dipijar perlahan – lahan sampai arang habis, pemijaran dilakukan
pada suhu 500 - 6000C selama 3 jam kemudian didinginkan dan ditimbang sampai
diperoleh bobot tetap. Kadar abu dihitung terhadap bahan yang telah dikeringkan
(WHO, 1992).
3.4.7. Penetapan Kadar Abu yang Tidak Larut dalam Asam
Abu yang telah diperoleh dalam penetapan kadar abu didihkan dalam 25
ml asam klorida encer selama 5 menit, bagian yang tidak larut dalam asam
kemudian didinginkan dan ditimbang. Kadar abu yang tidak larut dalam asam
dihitung terhadap bahan yang dikeringkan (WHO, 1992).
3.4.8. Penetapan Kadar Minyak Atsiri
Penetapan kadar minyak atsiri dilakukan dengan menggunakan alat Stahl.
Gambar alat dapat dilihat pada lampiran 5 halaman 28.
Caranya : Sebanyak 10 g serbuk simplisia dimasukkan dalam labu alas bulat
berleher pendek, tambahkan air suling sebanyak 300 ml, letakkan labu di atas
pemanas listrik. Labu dihubungkan dengan pendingin dan alat penampung
berskala, isi buret dengan air sampai penuh. Didihkan isi labu dengan pemanasan
yang sesuai untuk menjaga pendidihan berlangsung lambat tetapi teratur sampai
minyak atsiri terdestilasi sempurna dan tidak bertambah lagi dalam alat berskala
(6 jam). Setelah penyulingan selesai, biarkan tidak kurang dari 15 menit, catat
volume minyak atsiri pada buret. Hitung kadar minyak atsiri dalam % v/b
(Depkes, 1977).
3.5. Isolasi Minyak Atsiri
Isolasi minyak atsiri dilakukan dengan metode penyulingan air.
Penyulingan dilakukan dengan menggunakan alat destilasi air.
Caranya: Sebanyak 200 g serbuk simplisia dimasukkan kedalam labu alas bulat
berleher panjang 2 L ditambahkan air suling sampai sampel terendam. Kemudian
dirangkai alat destilasi air. Destilasi dilakukan selama 6 jam. Minyak atsiri yang
diperoleh ditampung dalam corong pisah, setelah itu dipisahkan antara minyak
dan air. Kemudian minyak atsiri yang diperoleh ditambahkan natrium sulfat
anhidrat, dikocok dan didiamkan selama 1 hari. Minyak atsiri dipipet dan
dianalisis dengan GC-MS. Kemudian dilakukan penetapan parameter fisika yang
meliputi penentuan indeks bias dan penentuan bobot jenis.
3.6. Identifikasi Minyak Atsiri 3.6.1. Penetapan Parameter Fisika 3.6.1.1. Penentuan Indeks Bias
Penentuan indeks bias dilakukan menggunakan alat Refraktometer Abbe.
Caranya: Alat Refraktometer Abbe dihidupkan. Prisma atas dan prisma bawah
dipisahkan dengan membuka klem dan dibersihkan dengan mengoleskan kapas
yang telah dibasahi dengan alkohol. Cuplikan minyak diteteskan ke prisma bawah
lalu ditutup. Melalui teleskop dapat dilihat adanya bidang terang dan bidang gelap
lalu skrup pemutar prisma diputar sedemikian rupa, sehingga bidang terang dan
gelap terbagi atas dua bagian yang sama secara vertikal. Dengan melihat skala
dapat dibaca indeks biasnya.
3.6.1.2. Penentuan Bobot Jenis
Penentuan bobot jenis dilakukan dengan menggunakan alat Piknometer.
Caranya: Piknometer kosong ditimbang dengan seksama, lalu diisi dengan air
suling dan ditimbang. Kemudian piknometer dikosongkan dan dibilas beberapa
kali dengan alkohol dan dikeringkan dengan bantuan hairdryer. Piknometer diisi
dengan minyak, selanjutnya dilakukan seperti pengerjaan pada air suling. Hasil
bobot minyak atsiri diperoleh dengan mengurangkan bobot piknometer yang diisi
minyak atsiri dengan bobot piknometer kosong. Bobot jenis minyak atsiri adalah
hasil yang diperoleh dengan membagi bobot minyak atsiri dengan bobot air suling
3.6.2. Analisis Komponen Minyak Atsiri
Penentuan komponen minyak atsiri yang diperoleh dari rimpang temu
putih dilakukan di Laboratorium Penelitian Fakultas Farmasi USU dengan
menggunakan seperangkat alat Gas Cromatograph–Mass Spectrometer (GC-MS)
model Shimadzu QP 2010 S. Gambar alat dapat dilihat pada lampiran 5 halaman
30.
Kondisi analisis adalah jenis kolom kapiler Rtx - 5MS, panjang kolom 30
m, diameter kolom dalam 0,25 mm, suhu injektor 1500C, gas pembawa He dengan
laju alir 0,5 ml/menit. Suhu kolom terprogram (temperature programming)
dengan suhu awal 500C selama 2 menit, lalu dinaikkan perlahan – lahan dengan
rute kenaikan 20C/menit sampai suhu akhir 2000C selama 13 menit yang
dipertahankan. Cara identifikasi komponen minyak atsiri adalah dengan
membandingkan spektrum massa dan komponen minyak atsiri yang diperoleh
(unknown) dengan data library yang memiliki tingkat kemiripan (similary index)
BAB IV
HASIL DAN PEMBAHASAN
4.1 Identifikasi Tumbuhan
Hasil identifikasi yang dilakukan di Pusat Penelitian Biologi – LIPI Bogor
terhadap rimpang tumbuhan temu putih yang diteliti adalah jenis Kaemferia
rotunda L. dari suku Zingiberaceae (Data selengkapnya dapat dilihat pada
lampiran 1 halaman 24).
4.2 Karakterisasi Simplisia Rimpang Tumbuhan Temu Putih
Hasil pemeriksaan makroskopik rimpang tumbuhan temu putih dicirikan
dengan rimpang yang agak kecil, irisan rimpang berwarna putih dengan tepi
berwarna kuning muda, beraroma aromatik serta berasa pahit. Diameter kira-kira
2 cm.
Hasil pemeriksaan mikroskopik serbuk simplisia temu putih terdapat
fragmen sel-sel parenkim berisi minyak yang berwarna kuning muda, fragmen
parenkim yang berisi butir-butir pati, jaringan gabus, serta berkas pembuluh kayu.
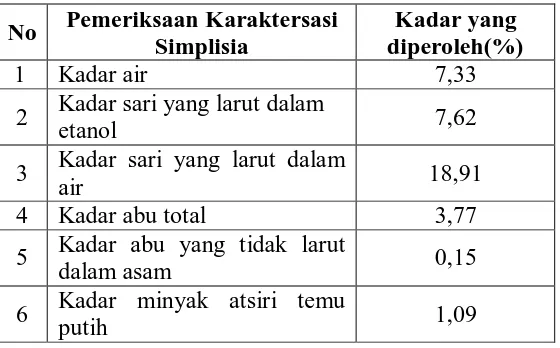
Tabel 4.1. Hasil Karakterisasi Serbuk Simplisia Temu Putih No Pemeriksaan Karaktersasi
Simplisia
Kadar yang diperoleh(%)
1 Kadar air 7,33
2 Kadar sari yang larut dalam
etanol 7,62
3 Kadar sari yang larut dalam
air 18,91
Kadar air dalam simplisia menunjukkan jumlah air yang terkandung dalam
simplisia yang digunakan, dari hasil penelitian diperoleh kadar air simplisia temu
putih adalah 7,33%. Kadar air simplisia berhubungan dengan proses pengeringan
simplisia. Pengeringan merupakan suatu usaha untuk menurunkan kadar air bahan
sampai tingkat yang didinginkan. Kadar air yang cukup aman, maka simplisia
tidak mudah rusak dan dapat disimpan dalam jangka waktu yang cukup lama.
Apabila simplisia yang dihasilkan tidak cukup kering maka kemungkinan akan
terjadi pertumbuhan jamur dan jasad renik lainnya. Simplisia dinilai cukup aman
bila mempunyai kadar air kurang dari 10% (Depkes, 1985).
Penetapan kadar sari yang larut dalam air dan dalam etanol dilakukan
untuk mengetahui jumlah senyawa yang dapat tersari dalam air dan dalam etanol
dari suatu simplisia. Senyawa yang bersifat polar dan larut dalam air akan tersari
oleh air. Sedangkan senyawa yang larut dalam etanol akan tersari oleh etanol.
Penetapan kadar abu dimaksudkan untuk mengetahui kandungan mineral
internal yang terdapat dalam simplisia yang diteliti.
Abu total terbagi dua yang pertama abu fisiologis adalah abu yang berasal
dari jaringan tumbuhan itu sendiri dan yang kedua abu non fisiologis adalah sisa
setelah pembakaran yang berasal dari bahan – bahan dari luar (seperti pasir dan
4.3 Identifikasi Minyak Atsiri
Pemeriksaan organoleptis pada minyak atsiri yang diisolasi dari simplisia
rimpang tumbuhan temu putih adalah memiliki warna putih kekuningan, bau
aromatik, dan rasa pahit.
Tabel 4.2. Hasil Penetapan Kadar Minyak Atsiri
No Sampel Kadar Praktek (% v/b) Kadar berdasarkan literatur
(% v/b)
1 Simplisia rimpang
temu putih
1,09 % v/b Tidak kurang dari 0,15% v/b
Data selengkapnya dapat dilihat pada lampiran 6 halaman 44
Minyak atsiri dapat terkandung dalam beberapa organ tumbuhan (Tyler,et
al,1970):
1. Terdapat dalam rambut kelenjar contoh: famili Labiatae dan Moraceae
2. Terdapat di dalam sel-sel parenkim contoh: famili Piperaceae dan
Zingiberaceae
3. Terdapat di dalam saluran minyak yang disebut vittae contoh: famili
Umbelliferae
4. Terdapat di dalam rongga skizogen dan lisigen contoh: famili Pinaceae dan
Rutaceae
Minyak atsiri yang terdapat pada rimpang temu putih yaitu berada di
dalam sel-sel parenkim.
Kadar minyak atsiri yang terkandung di dalam rimpang temu putih
dipengaruhi oleh umur panen, lingkungan, dan faktor genetik dimana minyak
Tabel 4.3. Hasil Penentuan Indeks Bias dan Bobot Jenis Minyak Atsiri
No Sampel
Indeks bias Bobot jenis
Hasil Penetapan Hasil Penetapan
1 Minyak atsiri
temu putih
1,5020 0,9144
(Data selengkapnya dapat dilihat pada lampiran 6 halaman 49-50)
Bobot jenis minyak atsiri merupakan perbandingan antara bobot minyak
dengan bobot air pada volume air yang sama dengan volume minyak. Bobot jenis
sering dihubungkan dengan jumlah komponen yang terkandung didalamnya.
Semakin besar jumlah komponen yang terkandung dalam minyak, semakin besar
pula nilai densitasnya (Armando, 2009).
Indeks bias merupakan perbandingan antara kecepatan cahaya didalam
udara dengan kecepatan cahaya didalam zat tersebut pada suhu tertentu. Indeks
bias minyak atsiri berhubungan erat dengan komponen-komponen yang
terkandung dalam minyak atsiri yang dihasilkan, sama halnya dengan berat jenis
dimana komponen penyusun minyak atsiri dapat mempengaruhi nilai indeks
biasnya (Armando, 2009).
Pada penentuan bobot jenis, piknometer yang digunakan adalah Sprengel
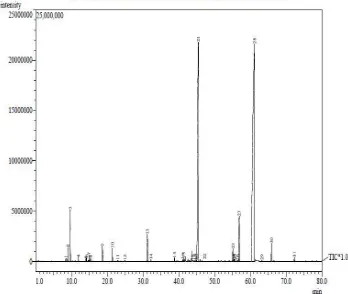
4.4. Analisis dengan GC-MS
Hasil analisis dengan GC-MS minyak atsiri dari rimpang temu putih
diperoleh 31 puncak pada kromatogram GC, Hasil selengkapnya dapat dilihat
pada gambar 1 di bawah ini.
Hasil analisis dengan GC-MS dari 31 puncak menunjukkan 6 komponen
utama minyak atsiri yang diperoleh dari simplisia rimpang temu putih yaitu
Benzyl benzoate, Hexadecane, Pentadecane, Camphene, Bornyl acetate dan
Siklopropazulen. Hasil selengkapnya dapat dilihat pada lampiran 10 halaman
58-63.
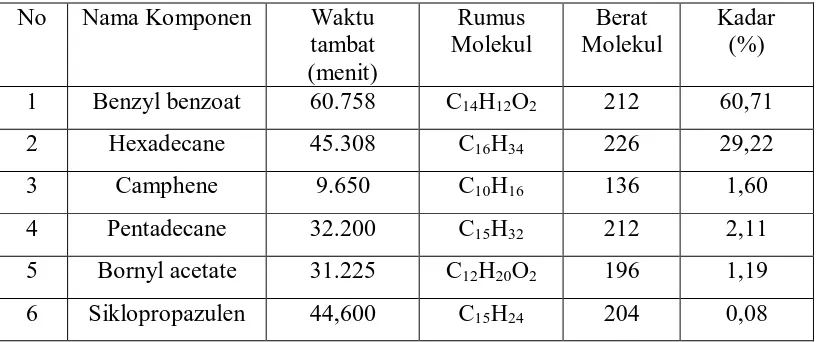
Tabel 4.4. Waktu Tambat dan Kadar Komponen Minyak Atsiri Hasil
Analisis GC-MS dari Simplisia Rimpang Temu Putih
No Nama Komponen Waktu
tambat (menit)
Rumus Molekul
Berat Molekul
Kadar (%)
1 Benzyl benzoat 60.758 C14H12O2 212 60,71
2 Hexadecane 45.308 C16H34 226 29,22
3 Camphene 9.650 C10H16 136 1,60
4 Pentadecane 32.200 C15H32 212 2,11
5 Bornyl acetate 31.225 C12H20O2 196 1,19
6 Siklopropazulen 44,600 C15H24 204 0,08
4.5 Analisis dan Fragmentasi Hasil Spektrofotometri Massa
Analisis dan fragmentasi hasil spektrofotometri massa komponen utama
minyak atsiri dari simplisia rimpang temu putih adalah sebagai berikut:
Pola fragmentasi dari masing-masing senyawa, selengkapnya dapat dilihat pada
lampiran 10 halaman 58-63.
1. Puncak dengan waktu tambat 60.758 menit
Mempunyai M+212 diikuti fragmen m/z 212, 194, 167, 152, 105, 91, 77,
65]. Berdasarkan perbandingan antara spectrum MS unknown dengan data library,
maka senyawa ini disimpulkan sebagai Benzyl benzoate dengan tingkat kemiripan
(similarity index) = 97% dan rumus molekulnya C14H12O2 dengan rumus bangun
seperti pada gambar 2:
Spektrum massa unknown memberikan puncak ion molekul M+ 212 yang
merupakan berat dari C14H12O2. Fragmentasi dapat terjadi dengan cara pelepasan
H2Odari puncak ion molekul C14H12O2 menghasilkan fragmen C14H10O]+. dengan
m/z 194. Pelepasan C2H3]+ menghasilkan fragmen C12H7O]+ dengan m/z 167.
]Pelepasan CH3]+ menghasilkan fragmen C11H4O]2+ dengan m/z 152. Pelepasan
C5H2 dari puncak ion molekul C12H7O menghasilkan fragmen C7H5O]+ dengan
m/z 105. Pelepasan CH2 menghasilkan fragmen C6H3O]+ dengan m/z 91.
Pelepasan CH2 menghasilkan fragmen C5HO]3+ dengan m/z 77. Pelepasan C
2. Puncak dengan waktu tambat 45.308 menit
Mempunyai M+226 diikuti fragmen m/z 197, 182, 169, 99, 85, 71, 57, 43,
27. Berdasarkan perbandingan antara spectrum MS unknown dengan data library,
maka senyawa ini disimpulkan sebagai Hexadecane dengan tingkat kemiripan
(similarity index)= 97% dan rumus molekulnya C16H34 dengan rumus bangun
seperti pada gambar 3:
Spektrum massa unknown memberikan puncak ion molekul M+ 226 yang
merupakan berat dari C16H34. Fragmentasi dapat terjadi dengan pelepasan C2H5]+
dari puncak ion molekul C16H34 menghasilkan fragmen C14H29]+ dengan m/z 197.
Pelepasan CH3]+ menghasilkan fragmen C13H26]+ dengan m/z 182. Pelepasan
CH]+ menghasilkan fragmen C12H25]+ dengan m/z 169. Pelepasan C5H10
menghasilkan fragmen C7H15]+ dengan m/z 99. Pelepasan CH2 menghasilkan
fragmen C6H13]+ dengan m/z 85. Pelepasan CH2 menghasilkan fragmen C5H11]+
dengan m/z 71. CH2 menghasilkan fragmen C4H9]+ dengan m/z 57. CH2
menghasilkan fragmen C3H7]+ dengan m/z 43. CH4 menghasilkan fragmen C2H3]+
dengan m/z 27.
3. Puncak dengan waktu tambat 9.650 menit
Mempunyai M+136 diikuti fragmen m/z 136, 121, 107, 93, 79, 67, 53, 41,
27. Berdasarkan perbandingan antara spectrum MS unknown dengan data library,
maka senyawa ini disimpulkan sebagai Camphene dengan tingkat kemiripan
(similarity index) = 96% dan rumus molekulnya C10H16 dengan rumus bangun
Spektrum massa unknown memberikan puncak ion molekul M+ 136 yang
merupakan berat dari C10H16. Fragmentasi dapat terjadi dengan pelepasan CH3]+
dari puncak ion molekul C10H16 menghasilkan fragmen C9H13]+ dengan m/z 121.
Pelepasan CH2 menghasilkan fragmen C8H11]+ dengan m/z 107. Pelepasan CH2
menghasilkan fragmen C7H9]+ dengan m/z 93. Pelepasan CH2 menghasilkan
fragmen C6H7]4+ dengan m/z 79. Pelepasan C menghasilkan fragmen C5H7]+
dengan m/z 67. Pelepasan CH2 menghasilkan fragmen C4H5]+ dengan m/z 53.
Pelepasan C menghasilkan fragmen C3H5]+ dengan m/z 41. Pelepasan CH2
menghasilkan fragmen C2H3]+ dengan m/z 27.
4. puncak dengan waktu tambat 32.200 menit
Mempunyai M+212 diikuti fragmen m/z 183, 169, 154, 141, 127, 113, 99,
85, 71, 43, 41. berdasarkan perbandingan antara spectrum MS unknown dengan
data library, maka senyawa ini disimpulkan sebagai Pentadecane dengan tingkat
kemiripan (similarity index) = 96% dan rumus molekulnya C15H32 dengan rumus
bangun seperti pada gambar 5:
Spektrum massa unknown memberikan puncak ion molekul M+ 212 yang
merupakan berat dari C15H32. Fragmentasi dapat terjadi dengan pelepasan C2H5]+
dari puncak ion molekul C15H32 menghasilkan fragmen C13H27]+ dengan m/z 183.
Pelepasan CH2 menghasilkan fragmen C12H25 dengan m/z 169. Pelepasan CH2
fragmen C10H21]+ dengan m/z 141. Pelepasan CH2 menghasilkan fragmen C9H19]+
dengan m/z 127. Pelepasan CH2 menghasilkan fragmen C8H17]+dengan m/z 113.
Pelepasan CH2 menghasilkan fragmen C7H15]+ dengan m/z 99. Pelepasan CH2
menghasilkan fragmen C6H13]+ dengan m/z 85. Pelepasan CH2 menghasilkan
fragmen C5H11]+ dengan m/z 71. Pelepasan CH2 menghasilkan fragmen C3H7]+
dengan m/z 43. Pelepasan CH4 menghasilkan fragmen C2H3]+dengan m/z 41.
5. Puncak dengan waktu tambat 31.225 menit
Mempunyai M+ 196 diikuti fragmen m/z 154, 136, 121, 108, 95, 79.
Berdasarkan perbandingan antara spectrum MS unknown dengan data library,
maka senyawa ini disimpulkan sebagai Bornyl acetate dengan tingkat kemiripan
(similarity index) = 96% dan rumus molekulnya C12H20O2 dengan rumus bangun
seperti pada gambar 6:
Spektrum massa unknown memberikan puncak ion molekul M+ 196 yang
merupakan berat dari C12H20O2. Fragmentasi dapat terjadi dengan pelepasan C3H6
dari puncak ion molekul C12H20O2menghasilkan fragmen C9H14O2]2+dengan m/z
154. Pelepasan CH4 + H2 menghasilkan fragmen C8H8O2]2+ dengan m/z 136.
Pelepasan CH3]+ menghasilkan fragmen C7H5O2]3+ dengan m/z 121. Pelepasan
CH]+ menghasilkan fragmen C6H4O2]3+ dengan m/z 108. Pelepasan CH]+
menghasilkan fragmen C5H3O2]2+dengan m/z 95. Pelepasan CH]+ menghasilkan
6. Puncak dengan waktu tambat 44.600 menit
Mempunyai M+ 204 diikuti fragmen m/z 189, 175, 161, 147, 133, 119,
105, 91, 79, 67, 55, 41. Berdasarkan perbandingan antara spectrum MS unknown
dengan data library, maka senyawa ini disimpulkan sebagai Siklopropazulene
dengan tingkat kemiripan (similarity index) = 93% dan rumus molekulnya C15H24
dengan rumus bangun seperti pada gambar 7:
Spektrum massa unknown memberikan puncak ion molekul M+ 196 yang
merupakan berat dari C12H20O2. Fragmentasi dapat terjadi dengan pelepasan C3H6
dari puncak ion molekul C12H20O2menghasilkan fragmen C9H14O2]2+dengan m/z
154. Pelepasan CH4 + H2 menghasilkan fragmen C8H8O2]2+ dengan m/z 136.
Pelepasan CH3]+ menghasilkan fragmen C7H5O2]3+ dengan m/z 121. Pelepasan
CH]+ menghasilkan fragmen C6H4O2]3+ dengan m/z 108. Pelepasan CH]+
menghasilkan fragmen C5H3O2]2+dengan m/z 95. Pelepasan CH]+ menghasilkan
BAB V
KESIMPULAN DAN SARAN
5.1. Kesimpulan
Hasil karakterisasi simplisia rimpang temu putih (Kaemferia rotunda L.)
diperoleh kadar abu total 3,77%; kadar abu yang tidak larut dalam asam 0,15%;
kadar sari yang larut dalam air 18,91%; kadar sari yang larut dalam etanol 7,62%;
dan kadar air 7,33%. Hasil penetapan kadar minyak atsiri dari simplisia rimpang
temu putih dengan alat Stahl diperoleh kadar minyak atsiri sebesar 1,09% v/b.
Hasil penetapan indeks bias diperoleh sebesar 1,5020 dan bobot jenis diperoleh
sebesar 0,9144.
Hasil analisis GC-MS minyak atsiri dari simplisia rimpang tanaman temu
putih diperoleh 31 puncak dengan 6 komponen utama yaitu: Benzyl benzoate
(60,71%), Hexadecane (29,22%), Pentadecane (2,11%), Camphene (1,60%)
Bornyl acetate (1,19%) dan Siklopropazulen (0,08%).
5.2. Saran
Dari hasil penelitian ini disarankan kepada peneliti selanjutnya untuk
melakukan isolasi komponen aktif tunggal dari minyak atsiri temu putih
DAFTAR PUSTAKA
Agusta, A. (2000). Minyak Atsiri Tumbuhan Tropika Indonesia. Bandung : Penerbit ITB. Hal. 105-106.
Claus, E. P, Tyler, V.E, dan Brady, L.R. (1970). Pharmacognosy. Philadelphia: Lea & Febiger. Hal. 162.
Depkes. (2000). Parameter Standar Umum Ekstrak Tumbuhan Obat. Jakarta: Departemen Kesehatan RI. Hal. 4.
Depkes. (1995). Farmakope Indonesia. Edisi IV. Jakarta: Departemen Kesehatan RI. Hal. 1030-1031.
Depkes. (1977). Materia Medika Indonesia. Jilid I. Jakarta: Departemen Kesehatan RI. Hal. 129-135.
Eaton, D.C. (1989). Laboratory Investigations in Organic Chemistry. USA: McGraw-Hill, Inc. Hal. 152-157.
Gritter, R.J, Bobbit, J.M, dan Schwarting, A.E. (1985). Introduction of
Chromatography. Penerjemah: K. Padmawinata. Pengantar Kromatografi.
Edisi III. Bandung: Penerbit ITB. Hal. 36-39.
Guenther, E. (1987). The Essential Oils. Penerjemah: Ketaren, R.S. Minyak Atsiri. Jilid I. Jakarta: Penerbit Universitas Indonesia. Hal. 41-50.
Gunawan, D. dan Mulyani, S. (2004). Ilmu Obat Alam (Farmakognosi). Jilid I. Jakarta: Penerbit Penebar Swadaya. Hal. 107.
Haris, R. (1987). Tanaman Minyak Atsiri. Jakarta: Penerbit Penebar Swadaya. Hal.4-5.
Ketaren, S. (1985). Pengantar Teknologi Minyak Atsiri. Jakarta: Penerbit Balai Pustaka. Hal. 37, 45-47, 61-67.
Lutony, T.L, dan Rahmayanti, Y. (1994). Produksi Dan Perdagangan Minyak
Atsiri. Jakarta: Penerbit Penebar Swadaya. Hal. 1-3, 32-51.
McLafferty, F.W. (1980). Interpretasi Spektra Massa.
Penerjemah: H. Sastrohamidjojo. Edisi III. Yogyakarta: Gadjah Mada University Press. Hal. 25-30.
McNair, H dan Bonelli E.J. (1988). Basic Gas Chromatography.
Muhlisah, F. (1999). Temu- temuan dan Empon- empon Budi Daya dan
Manfaatnya. Yogyakarta: Penerbit Kanisius. Hal. 34-36.
Noerdin, D. (1985). Elusidasi Struktur Senyawa Organik dengan Cara
Spektroskopi Ultralembayung dan Inframerah. Bandung: Penerbit
Angkasa. Hal. 73-75.
Rukmana, R. (2004). Apotik Hidup di Pekarangan. Yogyakarta: Penerbit Kanisius. Hal. 33-36.
Sastrohamidjojo, H. (1985). Dasar-dasar Spektroskopi. Edisi I. Yogyakarta: Liberty. Hal. 161.
Sastrohamidjojo, H. (2004). Kimia Minyak Atsiri. Yogyakarta: Penerbit Universitas Gadjah Mada. Hal. 1-15.
Silverstein, R.M, Bassler, G.C, dan Morrill, T.C. (1986). Laboratory
Investigations in Organic Chemistry. Penerjemah: Hartono, dkk. Penyidikan Spektrometrik Senyawa Organik. Jakarta: Erlangga. Hal. 3-81,
305-308.
Simon, S. (1981). Tables Of Spectral Data for Structure Determination of
Organic Compounds. Translated from the German by K. Biemann. Berlin:
J.G. Hal. 5-50.
Lampiran 2. Foto Morfologi Tanaman Temu Putih
A
B
Keterangan:
A : Tanaman Temu Putih
Lampiran 3. Foto Simplisia Temu Putih
A
B
C
Keterangan:
A : Irisan Rimpang Temu Putih B : Simplisia Rimpang Temu Putih
Lampiran 4. Hasil Pemeriksaan Mikroskopik Rimpang Tanaman Temu Putih
Keterangan:
1. Jaringan gabus 2. Jaringan parenkim 3. Butir pati
4. Pembuluh kayu 2. Jaringan parenkim
1. Jaringan gabus
3. Butir pati
Lampiran 5. Alat – alat yang digunakan dalam penelitian
A
A
B
Keterangan: A : Alat Stahl
(lanjutan)
A
B
Keterangan:
(lanjutan)
A
A
B
B
Keterangan:
A : Alat Piknometer
Lampiran 6. Hasil Perhitungan Karakterisasi Simplisia
6.1 Penetapan Kadar Air
Kadar Air = x100%
1. Simplisia temu putih
Lampiran 6. (Lanjutan)
6.2 Penetapan Kadar Minyak Atsiri
Kadar Minyak Atsiri= x100%
sampel
1. Simplisia Temu Putih
Lampiran 6. (Lanjutan)
6.3 Penetapan Kadar Sari yang Larut dalam Air
Lampiran 6. (Lanjutan)
6.4 Kadar Sari Larut dalam Etanol
Kadar sari larut dalam etanol = x100%
Lampiran 6. (Lanjutan)
6.5 Penetapan Kadar Abu Total
Lampiran 6. (Lanjutan)
6.6 Penetapan Kadar Abu yang Tidak Larut dalam Asam
Lampiran 6. (Lanjutan)
6.7 Penetapan Indeks Bias
1. Simplisia Temu Putih
Sampel I = 1,5020
Sampel II = 1,5020
Sampel III = 1,5020
Indeks bias rata-rata =
3
1,5020 1,5020
1,5020+ +
Lampiran 6. (Lanjutan)
6.8 Penentuan Bobot Jenis Minyak Atsiri
Bobot jenis minyak atsiri =
Keterangan : A : Bobot piknometer kosong
B : Bobot piknometer + minyak atsiri
C : Bobot piknometer + air sulin
Lampiran 7. Bagan Kerja Penelitian
Minyak atsiri dan air
Air Minyak atsiri dengan
kemungkinan adanya air
Na2SO4 x H2O
Minyak atsiri
ditambah Na2SO4 anhidrat (1,0009
dipisahkan
Lampiran 8.(Lanjutan)
Lampiran 9. Spektrum Massa Minyak Atsiri Temu Putih
Keterangan: puncak dengan waktu tambat 60.758
Lampiran 9. (Lanjutan)
Keterangan: puncak dengan waktu tambat 32.200
Lampiran 9. (Lanjutan)