ADAPTASI
Saccharomyces cerevisiae
TERHADAP
HIDROLISAT ASAM UBI KAYU UNTUK PRODUKSI
BIOETANOL
DESSY MAULIDYA MAHARANI
SEKOLAH PASCASARJANA
INSTITUT PERTANIAN BOGOR
PERNYATAAN MENGENAI TESIS DAN SUMBER INFORMASI
Dengan ini saya menyatakan bahwa tesis “Adaptasi Saccharomyces cerevisiae terhadap Hidrolisat Asam Ubi Kayu untuk Produksi Bioetanol” adalah karya saya dengan arahan dari komisi pembimbing dan belum diajukan dalam bentuk apapun kepada perguruan tinggi manapun. Sumber informasi yang berasal atau dikutip dari karya yang diterbitkan maupun tidak diterbitkan dari penulis lain telah disebutkan dalam teks dan dicantumkan dalam Daftar Pustaka di bagian akhir dari tesis ini.
Bogor, Juli 2011
Dessy Maulidya Maharani
© Hak Cipta milik IPB, tahun 2011 Hak Cipta dilindungi Undang-Undang
Dilarang mengutip sebagian atau seluruh karya tulis ini tanpa mencantumkan atau menyebutkan sumbernya. Pengutipan hanya untuk kepentingan pendidikan, penelitian, penulisan karya ilmiah, penyusunan laporan, penulisan kritik, atau tinjauan suatu masalah; dan pengutipan tersebut tidak merugikan kepentingan yang wajar IPB
ADAPTASI
Saccharomyces cerevisiae
TERHADAP
HIDROLISAT ASAM UBI KAYU UNTUK PRODUKSI
BIOETANOL
DESSY MAULIDYA MAHARANI
Tesis
sebagai salah satu syarat untuk memperoleh gelar Magister Sains pada
Program Studi Teknologi Industri Pertanian
SEKOLAH PASCASARJANA
INSTITUT PERTANIAN BOGOR
ABSTRACT
DESSY MAULIDYA MAHARANI. F351080101. Adaptation of Saccharomyces
cerevisiae to Cassava Acid Hydrolisates for Bioethanol Production. Under
direction of DWI SETYANINGSIH and GAYUH RAHAYU.
Acid hydrolisates of cassava contain toxic substances i.e. 3,55 g/l HMF and 0,72 g/l furfural to ethanol producing yeast, Saccharomyces cerevisiae. This study is aiming at screening four strains of S. cerevisiae for their tolerance capacity to that acid hydrolisates. Out of four strains, S. cerevisiae IPBCC 05.548 showed the highest tolerance on the bases of ethanol production. It produced 4,1% (b/v) ethanol. Prior to adaptation, optimum sugar concentration and starter dosage were determined in sequence. Out of 15%, 18%, 20% and 24% concentration. S. cerevisiae IPBCC 05.548 showed the highest ethanol production (4,10% b/v) at 15% of total sugar. Among starter dosage (1, 2 and 3 times of 0,23% of sugar concentration), that were tested on optimal sugar concentration indicated that the twice of dosage was the best for ethanol production. Adaptation was then performed for 72 hours for each cycle. Of the cycles, the 9th cycle (648 hours) showed the highest specific growth rate (0,14g.h-1) as well as ethnol yield (4,13% b/v). Comparison of the adapted strain to unadapted strain proved that the adapted strain produced 30,78% higher ethanol yield than those of unadapted strain.
RINGKASAN
DESSY MAULIDYA MAHARANI. F351080101. Adaptasi Saccharomyces
cerevisiae terhadap Hidrolisat Asam Ubi Kayu untuk Produksi Bioetanol.
Dibimbing oleh DWI SETYANINGSIH and GAYUH RAHAYU.
Bioetanol merupakan salah satu sumber energi hasil fermentasi yang dapat diperbaharui, ramah lingkungan dan paling cepat berkembang. Saccharomyces
cerevisiae adalah mikroorganisme paling umum digunakan dalam proses
fermentasi. Dua hal yang berperan dalam fermentasi adalah agen fermentasi dan substrat. Ada tiga kategori bahan baku yaitu bahan bergula, berpati dan berserat. Bahan berpati dan berserat dapat diolah dengan hidrolisis asam encer. Cara ini memiliki beberapa kelebihan antara lain harganya lebih murah, lebih cepat dalam menghidrolisis, mudah didapat dan rendemen gula lebih tinggi jika dibandingkan dengan hidrolisis enzim. Permasalahan timbul karena cara ini menghasilkan senyawa-senyawa penghambat. Senyawa tersebut bersifat toksik bagi mikroorganisme fermentasi. Tujuan penelitian ini adalah mendapatkan galur S. cerevisiae yang paling adaptif terhadap hidrolisat asam ubi kayu yang mengandung inhibitor, mendapatkan teknologi adaptasi S. cerevisiae hidrolisat asam ubi kayu yang mengandung inhibitor dan mendapatkan teknologi bioproses produksi etanol ubi kayu menggunakan S. cerevisiae yang adaptif terhadap hidrolisat asam sehingga mampu meningkatkan konversi gula menjadi etanol.
Tahap awal penelitian adalah persiapan bahan baku untuk dihidrolisis. Selanjutnya hidrolisis dilakukan satu tahap dengan total padatan ubi kayu 18%, H2SO4 1M, waktu 15 menit, suhu 121oC dan netralisasi menggunakan NH4OH
furfural 0,022 g/l. Fermentasi menggunakan hidrolisat asam tersebut mempengaruhi kinerja 4 galur yang diseleksi. Dari seleksi tersebut didapat bahwa galur IPBCC 05.548 memproduksi etanol terbanyak yaitu 4,1 % (b/v). Galur ini selanjutnya menghasilkan etanol tertinggi pada optimasi dengan gula awal 15% dan dosis S. cerevisiae 2x 0,23% konsentrasi total gula awal. Pada proses selajutnya IPBCC 05.548 dengan gula awal 15% dan dosis S. cerevisiae 2x 0,23% konsentrasi total gula menghasilkan laju pertumbuhan spesifik dan etanol tertinggi pada adaptasi ke-9. Kemampuan S. cerevisiae yang telah teradaptasi lebih baik dari yang tidak adaptif, yang ditunjukkan oleh rendemen etanol yang dari galur teradaptasi lebih tinggi 30,78 % dari yang tidak teradaptasi.
LEMBAR PENGESAHAN
Judul Tesis : Adaptasi Saccharomyces cerevisiae terhadap Hidrolisat Asam Ubi Kayu untuk Produksi Bioetanol
Nama : Dessy Maulidya Maharani
NRP : F351080101
Disetujui
Komisi Pembimbing
Dr. Ir. Dwi Setyaningsih, M.Si. Dr. Ir. Gayuh Rahayu
Ketua Anggota
Diketahui
Ketua Program Studi Dekan Sekolah Pascasarjana
Teknologi Industri Pertanian
Dr. Ir. Machfud, MS Dr. Ir. Dahrul Syah M,Sc.Agr
PRAKATA
Puji syukur penulis panjatkan hanya pada ALLAH SWT, karena atas
rahmat dan hidayahNya penulis dapat menyelesaikan tesis ini dengan baik.
Penulisan tesis ini diajkan sebagai salah satu syarat untuk memperoleh gelar
Magister Sains pada Program Studi Teknologi Industri Pertanian, Fakultas
Teknologi Pertanian, Institut Pertanian Bogor. Ucapan terima kasih penulis
saimpaikan kepada semua pihak yang telah membantu diantaranya :
1. Ibu Dr. Ir. Dwi Setyaningsih, M.Si. dan Ibu Dr. Ir. Gayuh Rahayu, selaku dosen
pembimbing.
2. Bapak Dr. Ir. Machfud, MS., selaku Ketua Program Studi.
3. Ibu Dr. Ir. Liesbetini Haditjaroko, MS selaku penguji .
4. Ibu Dr. Ir Titi Candra, MSi selaku wakil Program Studi.
5. Departemen Teknologi Industri Pertanian, FATETA IPB, yang telah membantu
sebagian dana penelitian .
6. Kedua orang tua, Ibu Hj Gusti Darnelia, SH, Ayah H Achmad Bunyamin, SH
dan Adik Meirinda Ramadhani, SE yang selalu memberikan dukungAN materi,
kasih sayang, do’a dan nasehat.
7. Suami Arief Hermawan ST dan Anak Nadhira Anindya yang selalu
memberikan semangat, dukungan dan do’a.
8. Keluarga besar H. Gusti Ibrahim Aman di Banjarmasin, Khususnya Om Gusti
Perdana Kesuma yang telah memberikan support dana kuliah dan penelitian
Om Gusti Suryanata SH, Tante Martha Kirana, S.kom, yang telah memberi
semangat dan dukungannya agar cepat menyelesaikan studi di bogor.
9. Ibu Rini, ibu Ega, ibu Sri, bapak Edi, bapak Sugi, bapak Dicky, Saiful, Wiwin
(LAB SBRC), ibu Ari (LAB Mikrobiologi PAU) dan laboran lain.
10.Teman-teman TIP, IPB angkatan 2008 serta semua pihak yang telah membantu
dalam penelitian maupun penyelesaian tesis ini.
Penulis menyadari sepenuhnya bahwa penelitian ini masih jauh dari
sempurna. Oleh karena itu dengan segala ketulusan dan kerendahan hati, penulis
menerima saran, kritik serta masukan untuk menjadikan tulisan ini lebih baik lagi.
Semoga hasil penelitian ini bermanfaat.
Bogor, Juli 2011
RIWAYAT HIDUP
Penulis dilahirkan di Banjarmasin, Kalimantan Selatan pada tanggal 18 Desember 1982 dari ayah H Achmad Bunyamin, SH dan ibu Hj Gusti Darnelia, SH. Penulis merupakan anak pertama dari dua bersaudara.
Penulis menyelesaikan pendidikan sekolah dasar (SD) sampai sekolah menengah atas (SMA) di Kota Banjarmasin pada tahun 2001. Penulis lulus dari SMUN 2 Banjarmasin dan pada tahun yang sama diterima di Universitas Lambung Mangkurat pada program Agronomi. Pada tahun 2007 penulis menyelesaikan program S1 dan meraih gelar Sarjana Agronomi. Pada tahun 2002-2007 penulis bekerja sebagai pegawai honor di Dinas Pendapatan Daerah Kabupaten Banjar Kalimantan Selatan. Pada tahun 2008 penulis melanjutkan pendidikan di program studi Teknologi Industri Pertanian, Sekolah Pascasarjana Institut Pertanian Bogor.
Halaman
2.4 Proses Pembuatan Etanol... 9
2.5 Hidrolisis Asam ... 10
2.6 Fermentasi... 11
2.7 Saccharomyces cerevisiae... 14
2.8 Pengaruh Furfural dan HMF terhadap S. cerevisiae... 15
2.9 Seleksi Galur S. cerevisiae... 17
2.10 Adaptasi S. cerevisiae... 18
3. METODE PENELITIAN... 19
3.1 Waktu dan Tempat ... 19
3.3.3 Hidrolisis Asam dan Karakterisasi Hidrolisat ... 20
3.3.4 Seleksi S. cerevisiae... 20
3.3.4.1 Persiapan Inokulum... 20
3.3.4.2 Seleksi Toleransi Galur S. cerevisiae Terhadap Hidrolisat Asam ... 20
3.3.4.3 Seleksi Total Gula Awal dan Dosis Starter... 21
ii
3.3.5 Produksi etanol ... 23
3.4 Teknik Analisis Data ... 23
3.4.1 Seleksi Toleransi Galur S. cerevisiae terhadap Hidrolisat Asam... 23
3.4.2 Seleksi Penentuan Total Gula Awal dan Dosis Starter ... 24
3.4.3 Adaptasi S. cerevisiae terhadap Hidrolisat Asam ... 24
3.4.4 Produksi Etanol ... 25
4. HASIL DAN PEMBAHASAN ... 27
4.1 Karakterisasi Ubi Kayu ... 27
4.2 Karakterisasi Hidrolisis Asam... 29
4.3 Seleksi S. cerevisiae... 31
4.3.1 Persiapan Starter... 31
4.3.1 Seleksi Toleransi Galur S. cerevisiae terhadap Hidrolisat Asam... 32
4.3.1 Seleksi Total Gula Awal dan Dosis Starter ... 36
4.4 Adaptasi S. cerevisiae Terhadap Hidrolisat Asam ... 40
4.5 Produksi Etanol ... 45
5. SIMPULAN DAN SARAN ... 49
5.1 Simpulan... 49
5.2 Saran ... 49
DAFTAR PUSTAKA... 51
1. Komposisi kimia ubi kayu segar dan tepung ubi kayu ... 5
2. Sifat fisika etanol ... 8
3. Perbandingan produksi dan produktivitas S. cerevisiae adaptasi dengan non-adaptasi ... ... 18
4. Komposisi kimia ubi kayu segar ... 25
5. Komposisi kimia hidrolisat asam ... 29
6. Jumlah sel S. cerevisiae pada masing-masing galur ... 31
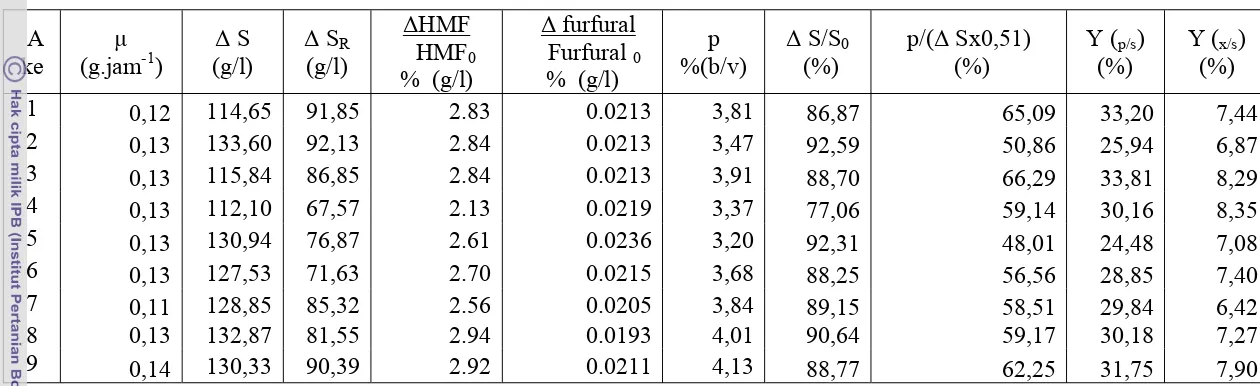
7. Laju pertumbuhan spesifik S. cerevisiae, penurunan gula total, penurunan gula reduksi, penurunan HMF, penurunan furfural dan kadar etanol proses adaptasi.. ... ... 44
1. Komposisi serat dalam batang barley dan senyawa inhibitor turunannya ... 11
2. Kurva pertumbuhan S.cerevisiae... 14
3. Perubahan HMF menjadi HMF alkohol... 16
4. Skema jalur metabolisme S. cerevisiae dan kemungkinannya berinteraksi dengan furfural . ... 16
5. Perubahan total gula dan pH selama fermentasi s1, s2, s3, dan s4 ... 33
6. Kadar etanol masing-masing galur ... 35
7. Pengaruh masing-masing galur terhadap efisiensi substrat, efisiensi
fermentasi dan rendemen ... 36
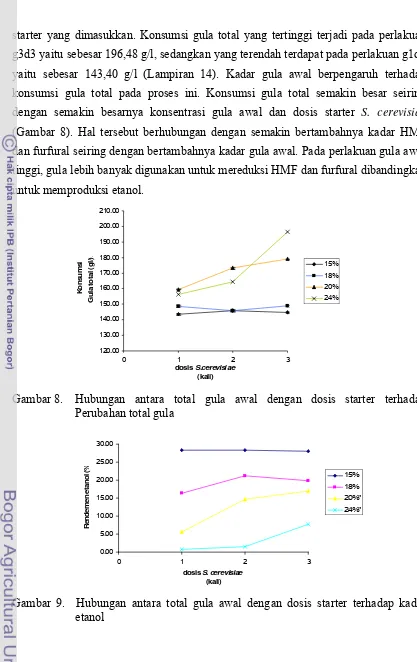
8. Hubungan antara total gula awal dengan dosis starter terhadap konsumsi gula total ... 37
9. Hubungan antara total gula awal dengan dosis starter terhadap kadar
etanol ... 37
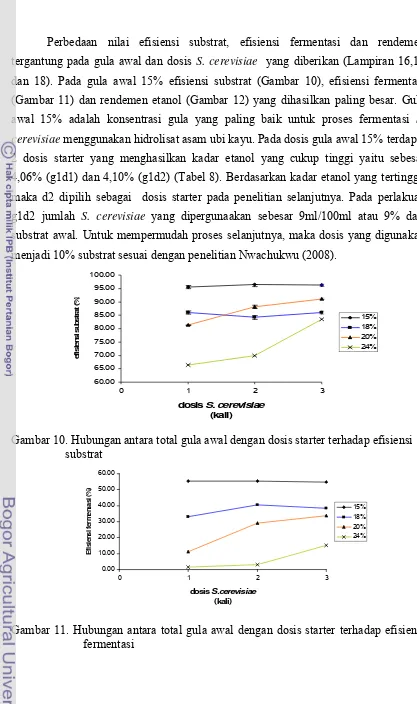
10. Hubungan antara total gula awal dengan dosis starter terhadap efisiensi substrat ... 39
11. Hubungan antara total gula awal dengan dosis starter terhadap efisiensi fermentasi... ... 39
12. Hubungan antara total gula awal dengan dosis starter terhadap rendemen etanol ... ... ... 40
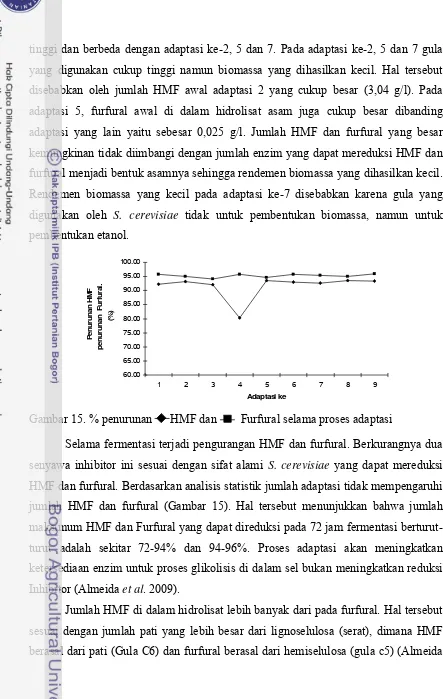
13. Konsumsi gula total dan gula reduksi selama proses adaptsi ... 41
14. Laju pertumbuhan spesifik S. cerevisiae dan etanol adaptasi ... 41
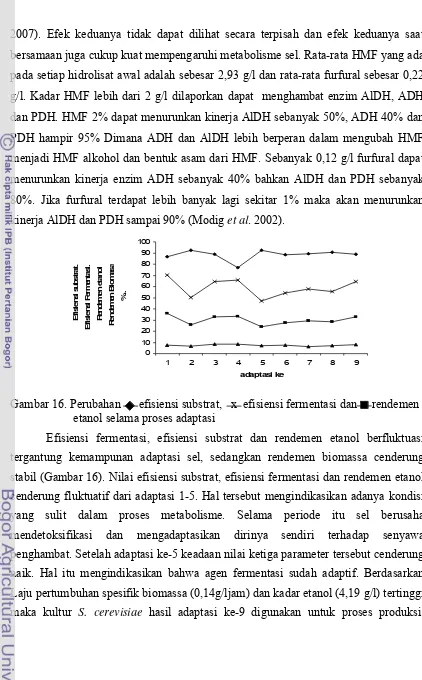
15. Perubahan HMF dan furfural adaptasi ... 42
16. Perubahan efisiensi substrat, efisiensi fermentasi, rendemen etanol dan rendemen biomassa adaptasi ... 43
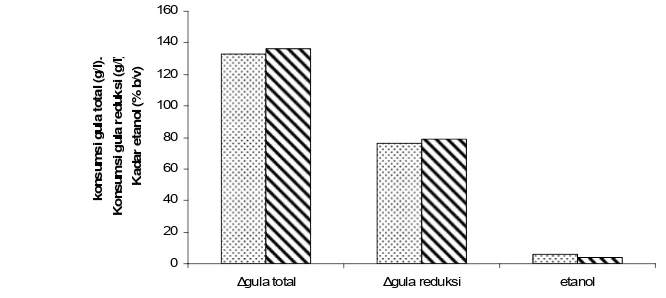
17. Konsumsi total gula, konsumsi gula reduksi, dan etanol pada tahapan
produksi dengan perlakuan adaptasi dan non-adaptasi ... 45
18. Efisiensi fermentasi, efisiensi substrat, rendemn etanol dan rendemen
1. Pohon industri ubi kayu ... 60
2. Diagram alir tahapan penelitian ... 61
3. Prosedur analisa parameter-parameter percobaan... 62
4. Contoh perhitungan hidrolisis ... 68
5. Contoh perhitungan dosis starter S. cerevisiae... 69
6. Perhitungan efisiensi pemanfaatan substrat, efisiensi fermentasi
rendemen etanol dan rendemen biomassa... 70
7. Konsumsi total gula seleksi toleransi galur terhadap hidrolisat... 71
8. Konsumsi gula reduksi seleksi toleransi galur terhadap hidrolisat ... 72
9. Perubahan pH seleksi toleransi galur terhadap hidrolisat ... 73
10. Produksi etanol seleksi toleransi galur terhadap hidrolisat ... 74
11.Efisiensi penggunaan substrat seleksi toleransi galur terhadap hidrolisat ... 75
12.Efisiensi fermentasi toleransi galur terhadap hidrolisat ... 76
13.Rendemen etanol toleransi galur terhadap hidrolisat ... 77
14.Perubahan total gula optimasi gula dan dosis starter ... 78
15.Produksi etanol optimasi gula dan dosis starter S. cerevisiae... 79
16.Efisiensi penggunaan substrat optimasi gula dan dosis starter S. cerevisiae.. 80
17.Efisiensi fermentasi optimasi gula dan dosis starter S. cerevisiae... 81
18.Rendemen etanol optimasi gula dan dosis starter S. cerevisiae... 82
19. Konsumsi total gula adaptasi ... 83
20. Konsumsi gula reduksi adaptasi ... 84
21. Biomassa Adaptasi ... 85
22. Reduksi HMF adaptasi... 86
23. Reduksi furfural adaptasi ... 87
24. Produksi etanol adaptasi ... 88
25. Efisiensi penggunaan substrat adaptasi... 88
26. Efisiensi fermentasi adaptasi... 89
27. Rendemen etanol adaptasi... 89
28. Rendemen bobot biomassa adaptasi... 89
viii
30. Etanol proses produksi etanol...90
31. Bobot biomassa proses produksi etanol ...90
32. Jumlah sel S. cerevisiae proses produksi etanol ...91
33. Efisiensi substrat proses produksi etanol...91
34. Efisiensi fermentasi proses produksi etanol ...92
35. Rendemen etanol proses produksi ...92
36. Rendemen bobot biomassa proses produksi...93
1.1 Latar Belakang
Bioetanol mulai dikembangkan pada tahun 1950 dan merupakan salah satu
sumber energi yang dapat diperbaharui dan ramah lingkungan (Thomas 2005).
Berdasarkan peraturan Kementrian Energi dan Sumber Daya Mineral No 32 tahun
2008, pada tahun 2008 sampai 2010 etanol harus mensubstitusi premium sebanyak
3% untuk transportasi dan akan meningkat menjadi 5% di tahun 2015, 10% pada
tahun 2020 dan 15% pada tahun 2025 (Sutarto 2009). Industri bioetanol terdiri dari
tiga skala industri yaitu skala besar, skala menengah dan skala kecil. Produsen skala
besar adalah produsen yang memproduksi etanol lebih dari 60 kilo liter (kL) perhari,
sedangkan produsen skala kecil adalah produsen dengan skala etanol kurang dari 1
kL/hari (Rama et al. 2007).
Bioetanol dapat berasal dari berbagai macam bahan baku. Ada tiga kategori
bahan baku bioetanol yaitu bahan bergula, bahan berpati dan bahan berserat. Bahan
baku berpati dan berserat dapat diolah dengan hirolisis asam encer, hidrolisis
enzimatis atau menggabungkan keduanya. Hidrolisis asam encer biasanya
menggunakan asam seperti H2SO4 dan HCl untuk menghasilkan gula, sedangkan
hidrolisis enzim dapat menggunakan enzim α-amilase dan amiloglukosidase.
Hidrolisis enzim memiliki kelebihan yaitu lebih ramah lingkungan dan tidak
menghasilkan senyawa penghambat untuk proses fermentasi, namun enzim juga
memiliki kelemahan yaitu tidak bisa disimpan dalam waktu yang lama, harganya
mahal, merupakan produk impor dan memerlukan waktu lebih lama dalam
menghidrolisis. Kerugian tersebut membuat metode hidrolisis enzim kurang cocok
digunakan dalam pembuatan bioetanol skala kecil.
Hidrolisis asam encer memiliki beberapa kelebihan, yaitu harganya lebih
murah, lebih cepat dalam menghidrolisis, mudah didapat dan rendemen gula lebih
tinggi jika dibandingkan dengan hidrolisis enzim. Dari keuntungan tersebut maka
para produsen bioetanol skala kecil sangat cocok untuk menerapkan hidrolisis asam
2
yaitu cenderung korosif terhadap alat, toksik terhadap lingkungan dan dapat
menghasilkan senyawa-senyawa penghambat. Senyawa tersebut bersifat toksik
bagi mikroorganisme yang berperan dalam proses fermentasi (Taherzadeh dan
Karimi 2007).
Efek inhibitor dalam hidrolisat dapat dikurangi dengan empat cara yaitu :
menggunakan asam konsentrasi rendah 0,4 M sampai 1 M untuk menghidrolisis
ubi kayu, detoksifikasi hidrolisat sebelum fermentasi, mengubah komponen yang
toksik menjadi produk yang tidak mengganggu metabolisme dan mengembangkan
mikroorganisme fermentasi yang tahan terhadap inhibitor (Solanges 2004;
Taherzadeh et al. 2000; Schneider 1996; Gong et al. 1993).
Pada penelitian ini dilakukan strategi pengembangan mikroorganisme
yang tahan terhadap inhibitor. Mikroorganisme yang paling umum digunakan
dalam proses fermentasi adalah Saccharomyces cerevisiae (Jeffries dan Shi 1999).
Selain umum digunakan, pemilihan khamir tersebut didasarkan pada Generally
Recognized as Safe (GRAS). GRAS adalah bagian dari undang-undang yang
dibuat oleh Food, Drug, and Cosmetic Act (FDA) Amerika pada tahun 1958.
Undang-undang ini dibuat untuk melindungi konsumen terhadap zat berbahaya
yang ditambahkan ke dalam bahan makanan. (FDA 2011). Pemilihan berdasarkan
GRAS akan membuat khamir ini lebih mudah diaplikasikan pada masyarakat
sebagai produsen etanol.
Adanya inhibitor seperti furfural dan 5-hidroksimetilfurfural (HMF) yang
terbentuk dalam hidrolisis asam menghambat metabolisme S. cerevisiae sehingga
mengakibatkan penurunan biomassa dan produksi etanol. S. cerevisiae yang tahan
terhadap inhibitor bisa didapatkan dengan proses penapisan dan adaptasi.
Beberapa penelitian telah melaporkan bahwa dengan proses adaptasi S. cerevisiae
pada media hidrolisat asam akan meningkatkan kemampuan S. cerevisiae dalam
memfermentasi substrat yang mengandung inhibitor (Felipe et al. 1996; Parajό et
al. 1998; Sene et al. 2001). Di Indonesia terdapat beberapa galur S. cerevisiae
yang tersedia di pasaran atau yang menjadi koleksi di laboratorium. Galur-galur
ini belum diketahui kemampuannya dalam menggunakan hidrolisat asam ubi kayu
1.2 Rumusan Masalah
Hidrolisis menggunakan asam encer dapat menghasilkan gula total cukup
tinggi setara dengan hidrolisis enzim. Saat fermentasi menggunakan hidrolisat
asam, kandungan gula dalam sisa fermentasi masih tinggi dan kadar etanol lebih
rendah dibandingkan menggunakan hidrolisat enzim. Hal tersebut mungkin
disebabkan adanya hambatan oleh inhibitor terhadap agen fermentasi. Untuk itu,
sebelum fermentasi, S. cerevisiae perlu diadaptasikan pada lingkungan yang
mengandung komponen inhibitor berupa HMF dan furfural. Pengaruh adaptasi S.
cerevisiae terhadap hidrolisat asam ubi kayu belum diketahui, sehingga perlu
dipelajari lebih lanjut mengenai hal tersebut.
1.3 Tujuan
1. Mendapatkan galur S. cerevisiae yang paling adaptif terhadap hidrolisat
asam ubi kayu yang mengandung inhibitor.
2. Mendapatkan teknologi adaptasi S. cerevisiae pada hidrolisat asam ubi
kayu yang mengandung inhibitor.
3. Mendapatkan teknologi bioproses produksi etanol ubi kayu
menggunakan S. cerevisiae yang adaptif terhadap hidrolisat asam
sehingga mampu meningkatkan konversi gula menjadi etanol.
1.4 Hipotesa
1. S. cerevisiae dari galur yang berbeda memiliki kemampuan yang
berbeda pula dalam mentoleransi hidrolisat asam ubi kayu.
2. Proses adaptasi bertahap dapat meningkatkan kemampuan S. cerevisiae
mentoleransi senyawa toksik hasil hidrolisis asam (HMF dan furfural).
3. S. cerevisiae yang telah diadaptasi terhadap hidrolisat asam akan
menghasilkan etanol lebih tinggi dari yang tidak teradaptasi.
1.5 Ruang Lingkup
1. Penapisan galur-galur S. cerevisiae dari berbagai sumber berdasarkan
kemampuan memproduksi etanol tertinggi menggunakan hidrolisat asam
ubi kayu.
2. Menentukan konsentrasi gula total awal dan dosis starter.
3. Mengadaptasinya galur S. cerevisiae terpilih di dalam hidrolisat asam
ubi kayudalam fermentasi sistem batch bertahap.
2. TINJAUAN PUSTAKA
2.1 Ubi Kayu (Manihot utilissima)
Ubi kayu berasal dari Brazil. Tanaman ini menyebar ke Asia pada awal abad
ketujuh belas dibawa oleh pedagang Spanyol dari Meksiko ke Fhilipina. Kemudian
ubi kayu menyebar ke Asia Tenggara, termasuk Indonesia (Ekanayake et al. 1997).
Sebagai komoditi perdagangan, ubi kayu dapat dibuat menjadi berbagai olahan antara
lain gaplek, pakan ternak, etanol, gula cair, sorbitol, tepung aromatik dan beberapa
produk (Lampiran 1).
Akar ubi kayu berfungsi menjadi tempat penyimpanan makanan atau lebih
dikenal dengan umbi. Pati dan serat diakumulasi di akarnya. Umbinya
merupakan sumber karbohidrat yang mengandung air sekitar 60%, pati, protein,
mineral, serat, selulosa, hemiselulosa dan lignin (Tabel 1) (Pandanou et al. 2005;
Wargiono et al. 2006; Arnata 2009).
Tabel 1. Komposisi kimia ubi kayu segar dan tepung ubi kayu
Jumlah (%) Komponen
Ubi kayua Tepung ubi kayub
Air 62-65 11,5
Abu 0,3-1,3 0,7
Karbohidrat 32-35 83,8
Protein 0,7-2,6 1,0
Lemak 0,2-0,5 0,9
Serat kasar 0,8-1,3 2,1
Selulosa - 0,36c
Hemiselulosa - 1,88c
Lignin - 0,02c
Sumber : a. Kay (1973), b. Depperin (1989), c. Arnata (2009)
Selama ini untuk membuat bioetanol para produsen hanya memanfaatkan
patinya saja, sedangkan seratnya tidak diperhitungkan. Rendemen yang dihasilkan
dengan mengolah pati dan seratnya lebih tinggi jika dibandingkan dengan mengolah
patinya saja (Susmiati 2009; Nurdyastuti 2005). Sebagai bahan baku bioetanol, ubi
kayu memiliki dua keuntungan. Pertama, ubi kayu dapat tumbuh dengan baik pada
tumbuh dengan baik. Kedua, ubi kayu bukan makanan pokok penduduk Indonesia,
sehingga dapat digunakan sebagai bahan baku bioetanol (Dai et al. 2006). Ubi kayu
yang tidak layak digunakan sebagai bahan pangan seperti ubi kayu yang mengandung
HCN tinggi (50-80 mg/kg) (Ciptadi dan Nasution, 1974), serat tinggi, ukurannya
kecil dan tidak segar (Syarief 1974) dapat digunakan sebagai bahan baku etanol.
Penggunaan ubi kayu tidak layak konsumsi menjadi bahan baku etanol dapat
mengurangi limbah pertanian dan dapat memberikan nilai tambah bagi petani.
Ubi kayu jika ditinjau dari segi teknis, finansial dan industri layak
dikembangkan sebagai bahan baku bioetanol (Anonim 2007). Kelayakan teknis dapat
dilihat dari peningkatan produktivitas ubi kayu dengan laju produksi 1,3 sampai 37%
pertahun, tersedianya varietas unggul untuk industri bioetanol, dan masih banyak
terdapat lahan tidur serta lahan sawah tadah hujan yang sebagian besar hanya
ditanami padi satu kali setahun. Kelayakan finansial ditandai oleh rasio B/C 1,49 dan
1,98 pada tingkat hasil 15 ton dan 20 ton/hektar dengan harga ubi segar di tingkat
petani Rp 250/kg (Anonim 2007).
2.2 Polisakarida Dalam Ubi Kayu
Polisakarida merupakan molekul-molekul monosakarida yang dapat berantai
lurus atau bercabang serta dapat dihidrolisis dengan enzim-enzim yang kerjanya
spesifik. Sebagian polisakarida akan dihidrolisis menjadi oligosakarida. Susunan
oligosakarida dapat digunakan utuk menentukan struktur molekul polisakarida.
Polisakarida dalam bahan makanan berfungsi sebagai penguat tekstur (selulosa,
hemiselulosa, pektin dan lignin) dan sebagai sumber energi (pati, dekstrin, glikogen,
dan fruktan) (Winarno 1997).
Komposisi utama polisakarida ubi kayu adalah pati, selulosa, dan
hemiselulosa. Pati disimpan sebagai cadangan makanan di akar. Pati merupakan salah
satu sumber karbohidrat dari tumbuhan. Semua pati yang berasal dari tumbuhan
berbentuk granula dengan ukuran dan karakteristik fisik yang spesifik (Prasad et al.
2007). Di negara-negara tropis seperti Indonesia, Thailand, Vietnam, dan Brazil,
7
keunggulan jika dibandingkan dengan pati jagung atau kentang. Keunggulan tersebut
antara lain kandungan pati lebih tinggi (± 90 % basis kering), kandungan protein dan
mineral lebih rendah, temperatur gelatinisasi lebih rendah, dan kelarutan amilosa
lebih tinggi. Sifat-sifat tersebut sangat penting untuk hidrolisis pati secara enzimatis
(Widiasa 2005).
Pati pada dasarnya terdiri dari dua polimer yang terkait di berbagai proporsi
menurut sumbernya yaitu amilosa (16%-30%) dan amilopektin (65%-85%) (Prasad et
al. 2007). Amilosa mempunyai struktur lurus dengan ikatan α-(1,4)-D-glikosidik,
sedangkan amilopektin mempunyai struktur bercabang dengan ikatan α
-(1,6)-D-glikosidik sebanyak 4%-6% dari bobot total.
Selulosa merupakan komponen terbesar (33-51%) dalam lignoselulosa yang
berfungsi sebagai struktur dasar dinding sel tanaman (Holtzapple 1993). Komponen
ini terdiri dari unit monomer D-glukosa yang terikat melaui ikatan β-1,
4-D-glukopiranosa. Struktur kimia selulosa berupa polisakarida linear yang tersusun dari
pengulangan unit β-1, 4-D-glukopiranosa dan berasosiasi dengan hemiselulosa (Hayn
et al. 1993.). Rumus molekul polisakarida adalah (C6H10O5)n dan n menyatakan
jumlah unit glukosa pembentuk rantai polimer atau derajat polimerisasi.
Selulosa dapat larut dalam asam pekat seperti H2SO4 72%. Asam tersebut
akan menghidrolisis selulosa menjadi glukosa. Peningkatan temperatur dan tekanan
akan meningkatkan laju hidrolisis. Hidrolisis selulosa dapat dihambat oleh lignin dan
hemiselulosa (Sjostrom 1994).
Hemiselulosa adalah polimer dari lignoselulosa. Di dalam lignocelulosa
terdapat 19%-34% hemiselulosa (Ingram 1975). Polimer ini termasuk dalam
kelompok polisakarida heterogen yang terbentuk melalui biosintetis yang berbeda
dari selulosa. Komponen ini mudah terhidrolisis dengan asam menjadi
komponen-komponen monomernya yang terdiri dari glukosa, manosa, galaktosa,
xilosa, L-arabinosa, dan sejumlah kecil L-ramnosa disamping menjadi asam
D-glukuronat, asam 4-0-metil-glukuronat dan asam D-galakturonat (Saha et al. 2005).
Lignin merupakan polimer alkohol aromatik yang terdapat di dalam
kontribusi dalam proses fermentasi, bahkan lebih berpotensi menjadi penghambat
dalam proses tersebut (Antonius et al. 2006; Ingram 1975).
Pektin adalah komponen terkecil di dalam lignoselulosa (2%-20%). Pektin
tersusun atas α-(1,6)-D-glikosidik yang terhubung pada asam galakturonat. Asam
galakturonat sendiri bisa teresterifikasi dengan senyawa metil dan kelompok asetil.
Pektin mengandung polisakarida bercabang seperti rhamnogalakturonan I,
rhamnogalakturonan II dan xylogalakturonan (Antonius et al. 2006; Ingram 1975).
2.3 Etanol
Etanol merupakan senyawa yang sering digunakan dalam industri kimia
antara lain sebagai pelarut (40%), untuk membuat asetaldehid (36%), eter, glikol eter,
etilasetat dan membuat kloral (CL3CCHO) (9%) (Lily et al. 2008). Etanol adalah
cairan yang bening, tidak berwarna dan memiliki bau yang khas. Etanol
mengeluarkan bau yang agak manis ada pengenceran menjadi cairan encer, tetapi
mengeluarkan bau terbakar saat konsentrasinya ditambahkan. Etanol (CH3CH2OH)
termasuk dalam kelompok alkohol dengan gugus hidroxil (–OH ) yang berikatan
dengan atom karbon dengan karakteristik tertentu (Tabel 3).
Tabel 2. Sifat fisika dan etanol
Besaran Nilai
Titik beku, oC -114,1
Titik didih normal, oC +78,32
Temperatur kritis, oC 243,1
Tekanan kritis, kPa 6383,48
Volume kritis, L/mol 0,167
Faktor kompresibilitas kritis, z 0,248
Densitas, pada 20 oC , g/ml 0,7893
Viskositas, pada 20 oC, mPa.s (=cP) 1,17
Kelarutan dalam air, pada 20 oC Larut
Panas penguapan, pada t.d normal, J/g 839,31
Panas pembakaran, pada 25 oC, J/g 29676,69
Panas pembentukan 104,6
Panas spesifik, pada 20oC, J/g.C.s Berat molekul
2,42 0,79 Sumber : Othmer (1969).
Etanol untuk minuman telah dibuat sejak zaman dahulu menggunakan
9
maksimal sekitar 14% etanol. Etanol dengan kadar lebih tinggi dapat dihasilkan
dengan distilasi larutan. Komposisi larutan distilasi adalah 96% etanol dan 4% air.
Etanol komersial mengandung 95% etanol dan 5% air. Etanol murni tidak dapat
diperoleh dengan penyulingan, tetapi diperoleh dengan penambahan agen dehidrasi
untuk menghilangkan sisa air. Etanol dapat bercampur dengan sebagian besar pelarut
organik. Hal ini berguna sebagai dalam pembuatan parfum, cat, pernis, dan bahan
peledak (Anshory 2004).
Bioetanol dapat dijadikan bahan bakar pengganti bensin, namun sampai saat
ini penggunaannya di Indonesia masih sangat terbatas. Di Indonesia penggunaan
bioetanol sebagai bahan bakarkendaraan bermotor masih dicampur dengan bensin.
Pencampuran bioetanol absolut sebanyak 10 % dengan bensin (90%), sering disebut
Gasohol E-10. Gasohol singkatan dari gasoline (bensin) dan alkohol (bioetanol).
Etanol absolut memiliki angka oktan (ON) 117, sedangkan Premium hanya 87-88.
Gasohol E-10 secara proporsional memiliki ON 92 atau setara Pertamax. Pada
komposisi ini bioetanol dikenal sebagai octan enhancer (aditif) yang paling ramah
lingkungan dan di negara- negara maju telah menggeser penggunaan Tetra Ethyl
Lead (TEL) maupun Methyl Tertiary Buthyl Ether (MTBE) (BPPT, 2005). Produksi
bioetanol dari tanaman dan penggunaannya pada mesin mobil akan menciptakan
keseimbangan siklus karbondioksida, yang berarti akan mengurangi laju pemanasan
global.
2.4 Proses Pembuatan Bioetanol
Produksi bioetanol dengan bahan baku pati atau karbohidrat, dilakukan
melalui proses konversi karbohidrat menjadi gula (glukosa) larut air (Lily et al.
2008). Teknologi proses produksi bioetanol tersebut dapat dibagi dalam tiga tahap,
yaitu hidrolisis, fermentasi, dan distilasi. Proses hidrolisis bergantung pada bahan
baku yang digunakan, misalnya dari bahan bergula, bahan berpati atau bahan
berserat. Sebelum dihidrolisis bahan baku harus dipersiapkan terlebih dahulu mulai
dari pengupasan, pencucian sampai pengecilan ukuran. Adapun tujuan setiap
teknologi persiapan atau pretreatment adalah untuk mengubah atau menghapus faktor
dinding sel polisakarida untuk menjadi monomer gula(Mosier et al. 2005). Hidrolisis
asam digunakan untuk menghidrolisis hemiselulosa menjadi pentosa (xilosa dan
arabinosa) dan heksosa (galaktosa, mannosa dan glukosa). Hidrolisis selulosa dan
hemiselulosa (terutama xylan) menjadi gula dapat dikatalis oleh bermacam-macam
asam termasuk asam sulfat, asam hidroksida, sam hidrokloroda, dan nitrat.
Tahap fermentasi merupakan tahap kedua dalam proses produksi bioetanol.
Pada tahap ini, monomer gula seperti glukosa dan xilosa diubah menjadi etanol
dengan bantuan mikroorganisme. Proses fermentasi menggunakan dua jenis khamir
yang berbeda untuk mengubah secara bersamaan xilosa dan glukosa disebut
co-fermentation antara lain dengan menggunakan S. cerevisiae dan Pichia stipitis
(Merida dan Figueroa 2009).
2.5 Hidrolisis Asam
Hidrolisis menggunakan asam telah dikembangkan di Jerman sejak awal abad
19. Asam yang paling banyak digunakan adalah jenis asam sulfat encer. Bahan ini
digunakan karena murah. Selain asam sulfat sering juga digunakan asam oksalat dan
asam asetat. Perlakuan asam sulfat encer dapat digunakan dengan baik untuk
bahan-bahan hasil pertanian, seperti tongkol jagung dan jerami padi atau gandum. Asam
dapat memecah hemiselulosa yang merupakan bahan yang bersifat rekalsitran (sulit
terurai) dalam hidrolisis. Hidrolisat asam dapat digunakan sebagai substrat utama
produksi bioetanol. Hal ini disebabkan karena hidrolisat asam mengandung glukosa.
Glukosa dapat digunakan sebagai sumber energi dan sumber karbon untuk
membentuk material penyusun sel baru (Voet dan Voet 2004). Hidrolisis asam dapat
menggunakan berbagai macam katalis asam pada berbagai macam konsentrasinya.
Umumnya asam yang digunakan adalah H2SO4 atau HCl (Mussatto dan Roberto,
2004) dengan konsentrasi berkisar antara 2-5% (Iranmahboob et al. 2002; Sun dan
Cheng 2002) dan suhu reaksi ± 160oC. Asam sulfat encer (1% atau pH 1,5) dan suhu
180-190oC digunakan untuk menghidrolisis tongkol jagung skala pilot. Waktu
11
xylosa dihidrolisis menjadi monomernya, 15% xilan menjadi furfural dan 15%
sisanya hilang selama hidrolisis (Zhu et al. 2004).
Gambar 1. Komposisi serat dalam batang barley dan senyawa inhibitor turunannya Sumber: Almeida et al.(2007)
Hidrolisis asam digunakan pada bahan-bahan yang berlignoselulosa karena
lebih dapat memecah hemiselulosa dan selulosa menjadi bahan bergula. Metode ini
memiliki kelemahan yaitu membentuk furfural dan senyawa inhibitor lainnya yang
dapat menghambat porses fermentasi (Taherzadeh dan Karimi 2007). Komponen
toksik yang teridentifikasi berjumlah lebih dari tiga puluh lima senyawa. Komponen
ini terbagi atas tiga kelompok utama (Gambar 1) yaitu kelompok asam-asam organik
(asam asetat, format dan levulinat), turunan furan (furfural dan
5-hidroksimetilfurfural), dan komponen-komponen fenolik (Luo et al. 2002).
2.6 Fermentasi
Proses fermentasi adalah proses pembebasan energi tanpa adanya oksigen, nama
lainnya adalah respirasi anaerob. Dari hasil akhirnya, fermentasi dibedakan menjadi
fermentasi asam laktatdan fermentasi alkohol. Pada beberapa mikroba pembebasan
energi dapat terjadi karena asam piruvat diubah menjadi asam asetat dan CO2
mannosa
xilosa arabinosa furfural
asam asetat fenol
selanjutanya asam asetat diubah menjadi alkohol. Dalam fermentasi alkohol, 1
molekul glukosa hanya dapat menghasilkan 2 molekul ATP. Jumlah ATP yang
dihasilkan lebih kecil dari respirasi aerob. Pada respirasi aerob 1 molekul glukosa
mampu menghasilkan 38 molekul ATP. Reaksi biokimia fermentasi bervariasi
tergantung jenis gula yang digunakan dan produk yang dihasilkan. Tahap akhir dari
fermentasi adalah konversi piruvat ke produk fermentasi akhir. Tahap ini tidak
menghasilkan energi tetapi sangat penting bagi sel anaerobik karena tahap ini
meregenerasi nicotinamide adenine dinucleotide (NAD+), yang diperlukan untuk
glikolisis.
Reaksinya :
1. Gula (C6H12O6) ————> asam piruvat (glikolisis) + ATP
2. Dekarboksilasi asam piruvat.
Asam piruvat————————————————————>asetaldehid + CO2.
piruvat dekarboksilase (CH3CHO)
3. Asetaldehid oleh alkohol dihidrogenase diubah menjadi etanol.
2 CH3CHO + 2 NADH2————————> 2 C2H5OH + 2 NAD.
alcohol dehidrogenase enzim
Secara singkat, glukosa (C6H12O6) yang merupakan gula paling sederhana,
melalui fermentasi akan menghasilkan etanol (2C2H5OH). Reaksi fermentasi ini
dilakukan oleh khamir seperti S. cerevisiae, yang bersifat fakultatif anaerobik. Pada
kondisi aerobik oksigen digunakan sebagai akseptor elektron terakhir pada jalur
reaksi bioenergetik. Pemanfaatan oksigen pada keadaan ini menghasilkan
penambahan biomassa sel dengan persamaan reaksi sebagai berikut:
Biomassa sel + C6H12O6 Æ CO2 + H2O + biomassa sel
Pada kondisi anaerobik di jalur reaksi bioenergetik, S cerevisiae menggunakan
senyawa organik sebagai akseptor elektron terakhir. Glukosa digunakan sebagai
substrat dengan hasil akhir berupa alkohol, CO2, aldehid dan asam organik. Reaksi
yang berlangsung dalam keadaan anaerobik tersebut adalah sebagai berikut:
13
Proses pertumbuhan mikroba sangat dinamik dan kinetikanya dapat digunakan
untuk meramal produksi biomassa dalam suatu proses fermentasi. Faktor utama yang
mempengaruhi pertumbuhan dan perilaku mikroba dapat digolongan dalam faktor
intraseluler dan faktor ekstraselular. Faktor intraselular meliputi struktur, mekanisme,
metabolisme, dan genetika. Sedangkan faktor ekstraselular meliputi kondisi
lingkungan seperti pH, suhu, tekanan (Hidayat et al .2006).
Proses pertumbuhan mikroba merupakan proses yang memiliki batas tertentu.
Pada saat tertentu, setelah melewati tahap minimum, mikroba akan mengalami fase
kematian. Faktor-faktor yang dapat menyebabkan berhentinya pertumbuhan mikroba
antara lain:
1. Penyusutan konsentrasi nutrisi yang dibutuhkan dalam pertumbuhan
mikroba karena habis terkonsumsi.
2. Produk akhir metabolisme yang menghambat pertumbuhan mikroba karena
terjadinya inhibisi dan represi.
Pertumbuhan kultur mikroba umumnya dapat digambarkan dalam suatu kurva
pertumbuhan. Pertumbuhan mikroba dapat terbagi dalam beberapa tahap yaitu:
1. Fase adaptasi atau fase lag. Pada fase ini mikroba menyesuaikan diri dengan
lingkungan dan medium baru. Mikroba berusaha merombak materi-materi dalam
medium agar dapat digunakan sebagai nutrisi untuk pertumbuhannya. Bila dalam
medium ada komponen yang tidak dikenal, mikroba akan memproduksi enzim
ekstraselular untuk merombak komponen tersebut. Pada fase ini juga berlangsung
seleksi. Hanya mikroba yang dapat mencerna nutrisi yang dapat bertahan hidup.
Fase lag bisa berlangsung lebih lama pada media yang mengandung inhibitor.
2. Fase log atau pertumbuhan dipercepat adalah fase pertumbuh dan
perkembangbiakkan mikroba dimana jumlahnya meningkat dengan cepat. Pada
fase ini mikroba sudah dapat menggunakan nutrisi dalam medium fermentasinya.
3. Fase stationer adalah fase dimana laju pertumbuhan tetap yaitu pada laju
pertumbuhan maksimum (µmaks), Namun jumlah mikroba yang mati juga
bertambah. Kematian ini diakibatkan oleh berkurangnya nutrien dan akumulasi
4. Fase kematian atau fase menurun adalah fase terhentinya pertumbuhan disertai
meningkat jumlah mikroba yang. Pada proses fermentasi secara komersil etanol
dipanen sebelum memasuki fase ini. (Crueger dan Crueger 1984; Hidayat et al.
2006).
Gambar 2. Kurva pertumbuhan Saccharomyces cerevisiae
2.7 Saccharomyces cerevisiae
S. cerevisiae (Saccharomycetes) adalah salah satu jenis khamir yang termasuk
dalam kingdom fungi dengan karakteristik dinding sel banyak mengandung kitin dan
manan (Moore 2001). Khamir bereproduksi dengan membentuk sel baru secara serial.
Pertumbuhannya disetarakan dengan pertumbuhan tunas yang mencapai ukuran sel
dewasa pada saat memisahkan diri dari sel induk. Siklus selnya biasanya terdiri dari
tahapan berikut G1, S, G2 dan M yang merupakan tahap mitosis (Moore 2001).
Waktu generasinya pendek yaitu 1,5-2 jam dan dapat dengan mudah dikulturkan.
Khamir hidup di alam dalam keadaan terbatas pada habitat yang dapat ditempatinya
(Moore 2001). Hidup optimum pada pH 4,0-4,5, pada suhu 30°C dan akan mati jika
terkena radiasi ultraviolet sebesar 3 sampai 4 mW detik x 103 (Hidayat et al. 2006).
S. cerevisiae merupakan khamir yang paling banyak digunakan dalam
fermentasi, dan merupakan mikroorganisme yang sangat dikenal oleh masyarakat
luas sebagai khamir roti (baker’s yeast). Khamir roti ini digunakan dalam pembuatan
15
makanan, minuman dan juga dalam industri etanol (Russel et al. 1991). Khamir ini
digunakan dalam proses fermentasi alkohol karena mampu memproduksi etanol
dalam jumlah yang besar, toleran terhadap etanol yang cukup tinggi 12-18% (v/v),
toleran terhadap kadar gula tinggi dan tetap aktif melakukan fermentasi pada suhu
4-23oC (Harrisson dan Graham 1970).
Bahan baku dan perlakuan yang berbeda akan mengakibatkan perbedaan
produksi etanol yang dihasilkan. Fermentasi Jerusalem artichoke menggunakan kultur
tunggal S. cerevisiae menghasilkan etanol sebanyak 0,45 g/g, rendemen sebesar 88,1
g/l, hasil dan produktivitas etanol sebanyak 1,84 g/l (Pakhvirun et al. 2007).
Semua galur S. cerevisiae dapat tumbuh aerobik pada glukosa, maltosa, dan
trehalosa namun tidak dapat tumbuh pada laktosa dan selobiosa. Pertumbuhannya
pada gula lain dapat berubah-ubah. Dua jenis gula yang paling baik untuk
difermentasikan adalah glukosa dan fruktosa (Martini dan Martini 2001).
Fermentasi substrat terhambat apabila di dalam substrat tersebut terdapat
inhibitor berupa furfural, 5-hidroksimetil furfural (HMF) dan asam asetat (Nevoight
2008). Jika dibandingkan dengan mikroorganisme yang lain seperti Zymomonas,
Pichia stipitis dan Escherichia coli, species ini lebih toleran terhadap inhibitor (asam
asetat, furfural dan HMF) (Olsson dan Hahn-hagerdal 1996).
Laju fermentasi pada hidrolisat asam oleh S. cerevisiae lebih lambat daripada
laju fermentasi pada hidrolisat enzim. Hal tersebut mungkin disebabkan oleh adanya
senyawa inhibitor. Sanches dan Baustista (1988) menyatakan bahwa waktu atau fase
lag bisa berlangsung lebih lama dengan adanya konsentrasi HMF sebesar 2 g/L.
Selain HMF, furfural dengan konsentrasi 4 g/l dapat menurunkan laju pembentukan
CO2 sekitar 35% pada. HMF dan furfural dapat menghambat laju pertumbuhan
spesifik dan laju produksi etanol baik pada kondisi aerob maupun anerob pada sistem
kultivasi dan fermentasi S. cerevisiae secara curah (Taherzadeh et al. 1999).
Beberapa penelitian mencoba mengatasi hal tersebut antara lain dengan cara seleksi
dan adaptasi galur yang tahan terhadap senyawa inhibitor.
2.8Pengaruh Furfural dan HMF Terhadap S. cerevisiae
Furfural dan HMF dalam konsentrasi tinggi dapat menghambat pertumbuhan
dapat menghambat aktivitas enzim glikolitik seperti piruvat dehidrogenase (PDH),
fosfat dehidrogenase, alkohol dehidrogenase (ADH), dan aldehid dehidrogenase
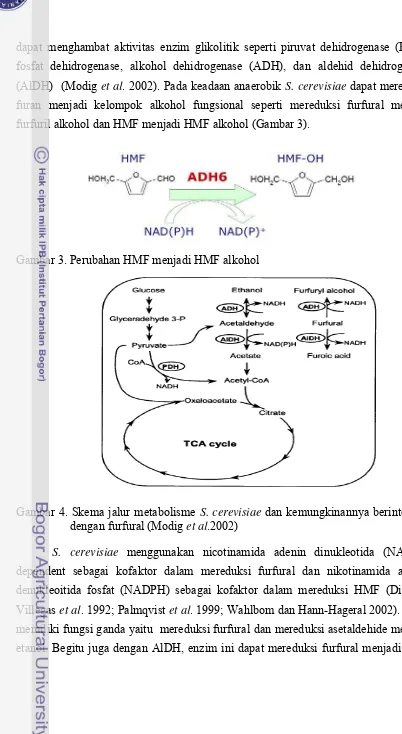
(AlDH) (Modig et al. 2002). Pada keadaan anaerobik S. cerevisiae dapat mereduksi
furan menjadi kelompok alkohol fungsional seperti mereduksi furfural menjadi
furfuril alkohol dan HMF menjadi HMF alkohol (Gambar 3).
Gambar 3. Perubahan HMF menjadi HMF alkohol
Gambar 4. Skema jalur metabolisme S. cerevisiae dan kemungkinannya berinteraksi
dengan furfural (Modig et al.2002)
S. cerevisiae menggunakan nicotinamida adenin dinukleotida
(NADH)-dependent sebagai kofaktor dalam mereduksi furfural dan nikotinamida adenin
denukleoitida fosfat (NADPH) sebagai kofaktor dalam mereduksi HMF (Diaz de
Villegas et al. 1992; Palmqvist et al. 1999; Wahlbom dan Hann-Hageral 2002). ADH
memiliki fungsi ganda yaitu mereduksi furfural dan mereduksi asetaldehide menjadi
17
furoat namun juga berfungsi mereduksi asetaldehid menjadi asam asetat. Adanya
fungsi ganda ADH dan AlDH menyebabkan kompetisi penggunaan enzim antara dua
substrat (Gambar 4) (Modig et al. 2002).
Kompetisi tidak hanya pada penggunaan enzim saja tetapi juga penggunaan
kofaktor (Palmqvist et al. 1999). Konsekuensi dari kompetisi tersebut adalah kofaktor
NADH dan NADPH bebas harus tersedia untuk mendetoksifikasi inhibitor tersebut.
Oleh karena itu, keteraturan jalur oksidasi dan reduksi menjadi sangat penting untuk
toleransi furfural (Gorsich et al. 2006). Reaksi-reaksi tersebut dapat dijelaskan dalam
persamaan berikut :
asetaldehid + NADH +H+ ⎯⎯ →ADH⎯ etanol + NAD+ (1)
furfural + NADH +H+ ⎯⎯ →ADH⎯ furfuril alkohol + NAD+ (2) asetaldehid + NAD+ ⎯⎯ →AlDH⎯ asam asetat + NADH + H+ (3)
furfural + NAD+ ⎯⎯ →AlDH⎯ asam furoat + NADH +H+ (4)
2.9SeleksiGalurS. cerevisiae
Inhibitor menyebabkan berkurangnya produktivitas S. cerevisiae. Seleksi
galur adalah cara yang dapat dilakukan untuk mengatasi masalah tersebut, selain
detoksifikasi terhadap hidrolisat asam (Martin dan Jonsson 2003). Seleksi galur
berdasarkan perbedaan toleransi tiap galur terhadap inhibitor sehingga berpotensi
menghasilkan konsentrasi etanol yang tinggi. Seleksi ini sangat penting untuk
optimalisasi proses produksi (Brandberg et al. 2004).
Beberapa galur S. cerevisiae dianggap memiliki kemampuan toleransi
terhadap inhibitor sehingga Martin dan Johnsson (2003) menyeleksi sepuluh galur S.
cerevisiae yang salah satunya adalah ragi roti dan dua strain Zygosaccharomyces.
Fermentasi dilakukan pada medium sintetik dengan menambahkan campuran
inhibitor yang mengandung 3,5g/l asam format, 4,5g/l asam asetat 2,9g/l furfural,
3,8g/l HMF, 0,15 g/l asam sinamat dan 0,18 g/l koniferyl aldehid. Pada fermentasi
didapat bahwa ragi roti pada keadaan tanpa inhibitor sampai level inhibitor 50%
menghasilkan etanol yang paling tinggi baik setelah 12 jam dan 24 jam fermentasi.
Etanol yang dihasilkan sebesar 0,42 g/g dan 0,106 g/g. Artinya bahwa kemampuan ragi roti dalam menghasilkan etanol dapat diandalkan bila dibandingkan dengan galur
dengan menyeleksi sembilan galur S. cerevisiae. Seleksi dilakukan melalui proses
fermentasi hidrolisat asam potongan kayu yang mengandung senyawa inhibitor
berupa furfural sebanyak 0,61 g/l, HMF sebanyak 2,3 g/l, dan asetat 2,8 g/l. Proses
fermentasi lakukan secara curah dan semi curah. Dari penelitian tersebut didapat satu
strain yang paling tolerant yaitu S. cerevisiae ATCC 96581.
2.10AdaptasiS. cerevisiae
Metode adaptasi merupakan metode yang paling murah dan mudah untuk
meningkatkan kinerja S. cerevisiae pada saat fermentasi dibandingkan metode fisika,
kimia dan biologis yang lain (Silva dan Roberto, 2001). Peningkatan toleransi
dikaitkan dengan peningkatan kemampuan NADH- dan NADPH menkonversi
furfural dan HMF ke masing-masing bentuk alkoholnya. Studi-studi terdahulu telah
meningkatan potensi detoksifikasi in situ dan menunjukkan bahwa aktivitas reduktase
tinggi dapat menjadi dasar bagi toleransi (Tabel 3).
Tabel 3. Perbandingan hasil dan produktivitas dari galur S. cerevisiae yang terdaptasi terhadap galur tidak teradatasi
No Parameter Non adaptasi Teradaptasi
1 Hasil (g/g) 0,18 0,38
2 Produktivitas (g/g.h-1) 1,15 2,55
Sumber : Martin et al. 2007
Galur yang adaptif biasanya mengkonsumsi glukosa sebanyak 2,0 g per gram
biomassa pada 8 jam pertama. Etanol yang terbentuk adalah 0,1 g/g per jam selama
periode fermentasi (Brandberg et al. 2004). Martin et al. (2007) mengadaptasi S.
cerevisiae yang telah direkayasa dengan penambahan gen dari Pichia stipitis pada
media yang mengandung inhibitor konsentrasi tinggi secara bertahap selama 353 jam
menggunakan bahan baku bagas. Hasilnya menunjukkan 74% furfural dan 40% HMF
dapat dikonversi menjadi furfuril alkohol dan HMF alkohol oleh galur yang
teradaptasi. Galur yang tidak teradaptasi hanya mengkonversi furfural sebanyak 22%
dan HMF sebanyak 20%. Etanol yang didapat dari galur teradaptasi lebih tinggi dari
non adaptasi sebesar 47,37% (Tabel 3). Hal tersebut diduga karena adaptasi telah
meningkatkan kemampuan S. cerevisiae dalam mentoleransi dan mengubah seyawa
3. METODE PENELITIAN
3.1 Waktu dan Tempat Penelitian
Penelitian ini dilaksanakan dari bulan Mei 2010 sampai Februari 2011,
bertempat di laboratorium Bioindustri Teknologi Industri Pertanian IPB dan
laboratorium SBRC IPB Bogor.
3.2 Bahan dan Alat
3.2.1 Bahan
Bahan baku yang digunakan dalam penelitian ini adalah ubi kayu, S.
cerevisiae berupa ragi curah dari pasar bogor, ragi kering Fermipan™, kultur koleksi
PAU (ATCC 9763) dan IPB Culture Colection (IPBCC 05.548), pupuk NPK, H2SO4
pekat teknis, NH4OH 21%, media Yeast Malt Glukose Pepton (YMGP)
3.2.2 Alat
Peralatan utama yang digunakan di dalam penelitian ini antara lain peralatan
gelas, neraca analitik, shaker, hemasitometer, autoklaf, pH universal, brix meter,
HPLC, Spektrofotometer UV-Vis, GC, Densitometer, seperangkat alat inokulasi
khamir dan seperangkat alat produksi bioetanol skala laboratorium.
3.3 Tahapan Penelitian
Tahapan penelitian adalah: 1) persiapan bahan baku, 2) karakterisasi ubi kayu
dan hidrolisat, 3) seleksi, 4) adaptasi S. cerevisiae dan 4) produksi etanol (Lampiran
2).
3.3.1 Persiapan Bahan Baku
Bahan baku yang masih segar dipisahkan kulit ari dengan daging umbinya.
Setelah kulit ari bersih daging umbi dicuci untuk membuang kotoran yang masih
menempel. Selanjutnya ubi kayu diparut sehingga menjadi bubur ubi kayu.
3.3.2 Karakterisasi Ubi Kayu
Sifat kimia bubur ubi kyu selanjutnya dianalisa dengan analisa proximat
(Lampiran 3). Parameter yang diukur antara lain komponen air, abu, lemak protein,
(1995), sedangkan pati dan komponen serat diukur menurut metode Van Soetst
(1963).
3.3.3 Hidrolisis Asam dan Karakterisasi Hidrolisat
Hidrolisis dalam penelitian ini dilakukan satu tahap menggunakan autoklaf
sederhana. Padatan yang digunakan pada saat hidrolisis adalah 18% dengan
konsentasi H2SO4 1M (Lampiran 4). Campuran ubi kayu, H2SO4 dan air dihidrolisis
selama 15 menit dengan suhu 121oC. Setelah dihidrolisis, hidrolisat ditambahkan
NH4OH teknis 21% untuk menaikkan pH hidrolisat menjadi 4-5. Karakterisasi
hidrolisat dilakukan dengan tujuan untuk mengetahui karakteristik hidrolisat dengan
analisis gula total dengan metode fenol H2SO4, analisis gula pereduksi dengan
metode DNS, furfural dan HMF dengan metode HPLC (Lampiran 3).
1.3.4Seleksi
1.3.4.1Persiapan Inokulum
Perlakuan pendahuluan untuk kelompok ragi kering seperti ragi curah dan
Merk ”F” berbeda dengan S. cerevisiae yang berbentuk biakan segar. Adapun
perlakuan untuk biakan segar adalah sebagai berikut :
Sebanyak 1 ose biakan segar dimasukkan ke dalam labu erlenmeyer yang
berisi 5 ml media YMGP yang telah disterilisasi pada suhu 121oC dan tekanan 1 atm
selama 15 menit. yang terdiri dari 5g/l ekstrak khamir, 5g/l malt, 40g/l glukosa, 5g/l
pepton dan 1L aquadest, Inkubasi dilakukan pada suhu 30oC selama 48 jam dan di
shaker (Arnata 2009). Setelah dibiakkan jumlah populasi akan dihitung dengan
metode hitung langsung menggunakan hemasitometer. Isolat ragi kering dihitung
tanpa proses penyegaran, namun hanya dilakukan pengenceran serial saja sampai 10
-3
. Kuantitas S. cerevisiae (Lampiran 5) yang dimasukkan ke dalam hidrolisat harus
seragam untuk menciptakan lingkungan yang homogen.
1.3.4.2Seleksi Toleransi Galur S. cerevisiae terhadap Hidrolisat Asam
Tujuan penelitian ini adalah untuk menyeleksi beberapa galur S. cerevisiae,
yang paling toleran terhadap hidrolisat asam ubi kayu. Sebelum digunakan, hidrolisat
disaring dengan kertas saring dan pompa vakum sehingga terpisah padatan dan
21
Selanjutnya kedalam hidrolisat ditambahkan masing-masing satu galur S. cerevisiae
dengan populasi yang sama. S. cerevisiae kering galur ”F” dijadikan acuan jumlah
galur yang lainnya. Starter 0,23% gula awal dan NPK 0,06% gula awal (Arnata 2009)
ditambahkan ke dalam hidrolisat. Campuran hidrolisat diinkubasi di dalam labu
erlenmeyer 250 ml menggunakan orbital shaker 128 rpm selama 24 jam pertama.
Labu erlenmeyer ditutup dengan sumbat karet dan labu leher angsa secara aseptis.
Total waktu inkubasi selama 72 jam. Pengamatan dilakukan setiap 12 jam terhadap
total gula, gula pereduksi, dan etanol yang terbentuk pada akhir fermentasi (Lampiran
6).
Parameter yang diukur dan dihitung sebagai indikator kinerja proses seleksi
toleransi galur S. cerevisiae terhadap hidrolisat asam adalah :
1. Substrat awal berupa gula total (So)
2. Sisa substrat setiap 12 jam
3. Kadar etanol sebagai produk (P)
4. % Efisiensi pemakaian substrat ((S0-S)/S0)
5. % Efisiensi fermentasi (P/P teoritis)
6. % Rendemen etanol (Yp/s)
Galur yang toleran adalah galur yang menunjukkan efisiensi pemanfaatan
substrat, efisiensi fermentasi dan rendemen etanol (Lampiran 6) tertinggi. Galur yang
paling toleran digunakan untuk penelitian selanjutnya.
1.3.4.3Seleksi Total Gula Awal dan Dosis Starter Terbaik
Pada penetuan ini fermentasi hidrolisat asam ditetapkan kadar gula dan dosis
starter minimum yang paling efektif bagi galur terpilih. Keadaan fermentasi sama
seperti seleksi toleransi galur, namun jumlah gula yang dimasukkan adalah 15%,
18%, 20% dan 24%. Dosis starter yang dimasukkan adalah 1x, 2x dan 3x (0,23% gula
awal). Pengamatan yang dilakukan adalah jumlah total gula pada awal dan akhir
fermentasi, serta etanol yang terbentuk pada akhir fermentasi.
Parameter yang diukur dan dihitung sebagai indikator kinerja proses seleksi
total gula awal dan dosis starter terbaik adalah :
2. Sisa substrat pada akhir fermentasi
3. Kadar etanol sebagai produk (P)
4. % Efisiensi pemakaian substrat ((S0-S)/S0)
5. % Efisiensi permentasi (P/P teoritis)
6. % Rendemen etanol terhadap total gula (Yp/s)
Kadar gula dan dosis starter yang menghasilkan etanol terbanyak akan
digunakan pada proses selanjutnya.
1.3.5Adaptasi S. cerevisiae terhadap Hidrolisat Asam
Prosedur adaptasi menggunakan metode batch. Dosis starter terpilih
dimasukkan ke dalam 250 ml labu erlenmeyer yang berisi 100% hidrolisat (kultur
sel 1). Setaah 72 jam, starter sejumlah dosis terpilih dikeluarkan dengan pipet
kemudian dimasukkan kembali ke kultur sel 2. Penambahan starter ke dalam
hidrolisat baru diulang 9x. Pengamatan jumlah biomassa, kadar etanol, total gula,
gula pereduksi, HMF dan furfural (Lampiran 3). Pengamatan dilakukan setiap 72
jam.
Parameter yang diukur dan dihitung sebagai indikator kinerja proses adaptasi
S. cerevisiae terhadap hidrolisat asam adalah :
1. Konsumsi gula total (S0-S)
2. Kadar etanol sebagai produk (P)
3. Laju pertumbuhan spesifif (µ= bobot biomassa/72 jam)
4. % Penurunan HMF ((H0-H)/H0)
5. % Penurunan Furfural ((F0-F)/F0)
6. % Efisiensi pemakaian substrat ((S0-S)/S0)
7. % Efisiensi fermentasi (P/P teoritis)
8. % Rendemen etanol terhadap total gula(Yp/s)
10 % Rendemen bobot biomassa terhadap total gula (Yx/s)
Kondisi adaptasi dengan µ dan etanol tertinggi akan digunakan untuk proses
23
3.3.5 Produksi Bioetanol
Proses ini merupakan proses verifikasi terhadap galur yang adaptif. Proses ini
dilakukan dengan membandingkan kemampuan galur yang telah adaptif dengan
kontrol yaitu strain yang tidak adaptif dalam menghasilkan etanol. Isolat yang adaptif
dan kontrol di masukkan ke dalam 300 ml hidrolisat asam untuk proses fermentasi
selama 96 jam pada suhu ruang dan agitasi 128 rpm untuk 24 jam pertama.
Parameter yang diukur dan dihitung sebagai indikator kinerja proses produksi
etanol adalah :
1. Konsumsi gula total (S0-S)
2. Kadar etanol sebagai produk (P)
3. ∆ biomassa (x0-x)
4. % Efisiensi pemakaian substrat ((S0-S)/S0)
5. % Efisiensi fermentasi (P/P teoritis)
6. % Rendemen etanol terhadap total gula(Yp/s)
7. % Rendemen bobot biomassa terhadap total gula (Yx/s)
3.4. Teknik Analisis Data
3.4.1 Seleksi Toleransi Galur S. cerevisiae terhadap Hidrolisat
Untuk mengetahui pengaruh hidrolisat asam terhadap kinerja S. cerevisiae
dilakukan uji F dengan Rancangan Acak Lengkap (RAL) faktor tunggal. Faktor yang
mempengaruhi adalah 4 sumber galur yaitu ragi curah (s1), merk ”F” (s2), koleksi
PAU (s3) dan koleksi IPBCC(s4). Percobaan diulang 2x. Apabila ada salah satu
perlakukan berpengaruh nyata maka analisis dilanjutkan dengan uji Duncan (Gomez
dan Gomez 1995). Parameter yang diuji adalah jumlal gula total yang digunakan,
gula reduksi yang digunakan, etanol yang terbentuk, efisiensi fermentasi, efisiensi
substrat dan rendemen etanol.
Persamaan model rancangannya sebagai berikut :
Yij = µ+ si + ε(ij)
Yij = variabel respon karena pengaruh taraf ke i faktor S,
pengamatan/unit perlakuan ke n
µ = pengaruh rata-rata yang sebenarnya (nilai konstan)
ε(ij) = pengaruh sebenarnya unit eksperimen ke i disebabkan oleh kombinasi perlakuan (ij).
i = taraf galur (1, 2, 3 dan 4)
j = taraf ulangan (1dan 2)
3.4.1 Seleksi Total Gula Awal dan Dosis Starter Terbaik
Untuk mengetahui pengaruh Jumlah gula dan dosis starter terhadap proses
fermentasi dilakukan uji F dengan RAL dua faktor. Faktor yang mempengaruhi
adalah gula awal sebanyak empat taraf yaitu 15% (g1), 18% (g2), 20%(g3) dan
24%(g4). Percobaan diulang sebanyak 2x. Faktor kedua adalah dosis agen fermentasi
sebanyak tiga taraf yaitu 1kali (d1), 2 kali (d2) dan 3 kali (d3). Apabila ada salah satu
perlakukan atau interaksinya berpengaruh nyata maka analisis dilanjutkan dengan uji
Duncan (Gomez dan Gomez 1995). Parameter yang diuji adalah adalah jumlal gula
total yang digunakan etanol yang terbentuk, efisiensi fermentasi, efisiensi substrat,
dan rendemen etanol.
Persamaan model rancangannya sebagai berikut :
Yikj = µ+ gi + di + (gd) ij + ε(ijk)
Yijk = variabel respon karena pengaruh taraf ke-i faktor g dan taraf ke-J
faktor d
µ = pengaruh rata-rata yang sebenarnya (nilai konstan) gi = pengaruh sebenarnya dari taraf ke i faktor g
dj = pengaruh sebenarnya dari taraf ke J faktor d
ε(ijk) = pengaruh sebenarnya unit eksperimen ke-ki disebabkan oleh
kombinasi perlakuan (ij). i = taraf jumlah gula (1, 2, 3 dan 4) j = taraf dosis agen fermentasi (1, 2 dan3) k = taraf ulangan (1 dan 2)
3.4.2 Adaptasi S. cerevisiae terhadap Hidrolisat Asam
Untuk mengetahui pengaruh hidrolisat asam terhadap kinerja S. cerevisiae
dilakukan uji F dengan RAL faktor tunggal. Faktor yang mempengaruhi adalah siklus
adaptasi yaitu 1x – 9x (t1-t9). Percobaan diulang sebanyak 2x. Apabila ada salah satu
perlakukan berpengaruh nyata maka dilanjutkan dengan uji Duncan (Gomez dan
25
reduksi, etanol yang terbentuk, jumlah biomassa, efisiensi fermentasi, efisiensi
penggunaan substrat, rendemen etanol dan rendemen bobot biomassa (Lampiran 6).
Persamaan model rancangannya sebagai berikut :
Yij = µ+ ti + ε(ij)
Yij = variabel respon karena pengaruh taraf ke i faktor t,
pengamatan/unit perlakuan ke n
µ = pengaruh rata-rata yang sebenarnya (nilai konstan)
ti = pengaruh sebenarnya dari taraf ke i faktor t
ε(ij) = pengaruh sebenarnya unit eksperimen ke i disebabkan oleh
kombinasi perlakuan (ijkl).
i = taraf waktu (1, 2, dan 3)
j = taraf ulangan (1 dan 2)
3.4.3 Produksi Etanol
Untuk mengetahui pengaruh kondisi S. cerevisiae yang telah diadaptasi
terhadap proses fermentasi, maka dilakukan uji F dengan RAL faktor tunggal. Faktor
yang mempengaruhi adalah kondisi S. cerevisiae sebanyak 2 taraf yaitu Kondisi
teradaptasi (A) dan tanpa Adapatasi (NA). Diulang sebanyak 2x. Apabila ada salah
satu perlakukan berpengaruh nyata maka analisis dilanjutkan dengan uji Duncan
(Gomez dan Gomez 1995). Parameter yang diuji adalah perubahan gula total, etanol
yang terbentuk, biomassa, jumlah sel, efisiensi fermentasi, efisiensi substrat,
rendemen etanol dan rendemen bobot biomassa (Lampiran 6).
Persamaan model rancangannya sebagai berikut :
Yij = µ+ ai + ε(ij)
Yij = variabel respon karena pengaruh taraf ke i faktor a,
pengamatan/unit perlakuan ke n
µ = pengaruh rata-rata yang sebenarnya (nilai konstan)
ai = pengaruh sebenarnya dari taraf ke i faktor a
ε(ij) = pengaruh sebenarnya unit eksperimen ke i disebabkan oleh
kombinasi perlakuan (ij). i = taraf kondisi S. cerevisiae (1,2)
Ubi kayu yang dipergunakan dalam penelitian ini mempunyai ciri-ciri fisik
antara lain umbinya berbentuk silinder memanjang, kulit berwarna coklat tua dengan
daging umbi berwarna putih. Bubur ubi kayu mengandung banyak air dan pati
dengan sedikit lemak, protein dan serat (Tabel 4).
Tabel. 4 Komposisi kimia ubi kayu segar
Komposisi
Pati (karbohidrat by difference) Serat Kasar Keterangan : bb = berat basah, bk = berat kering
Hasil analisis menunjukkan kadar air ubi kayu segar adalah 66,74%. Hasil
tersebut lebih tinggi dari yang didapatkan Susmiati (2010) yaitu sebesar 57% dan dari
Pandanou et al. (2005) sebesar 60,30%. Menurut Priadi (2009), beberapa jenis ubi
kayu di Indonesia memiliki kandungan air sebesar 58% sampai 66%. Hal tersebut
kemungkinan dipengaruhi perbedaan jenis ubi kayu, daerah penanaman dan waktu
panen (Hartadi et al.1986).
Pengukuran kadar air penting dilakukan karena hasil pengukuran akan
digunakan dalam perhitungan pengenceran asam dan kadar padatan dalam proses
hidrolisis. Kadar air pada ubi kayu diharapkan dapat mengurangi penggunaan air.
Selain menghemat air juga menghemat biaya untuk proses pengeringan, namun ubi
kayu segar memiliki keterbatasan yaitu tidak dapat disimpan terlalu lama.
Kadar abu dalam bahan menggambarkan kandungan mineral-mineral
anorganik sisa pembakaran bahan organik pada suhu 550oC (Apriyantono et al.
2,52% pada bobot kering. Hasil yang didapat tidak jauh berbeda dengan yang
dilaporkan Arnata (2009) yaitu sebesar 2,55% pada bobot keringnya.
Kadar lemak dan protein bahan berturut-turut 1,33% (bk) dan 3,94% (bk)
Kadar Lemak lebih rendah dari yang dilaporkan Arnata (2009) yaitu sebesar 6,54%
(bk) sedangkan kadar proteinnya lebih tinggi dari yang dilaporkan Arnata (2009)
yaitu sebesar 1,81% (bk)
Polisakarida yang penting dalam ubi kayu adalah pati dan serat. Monomer
keduanya digunakan oleh agen fermentasi sebagai sumber energi untuk mensintesis
ATP dalam proses fermentasi. Pati merupakan bagian terpenting yang dapat
digunakan menjadi bahan dasar pembuatan etanol. Pati akan terhidrolisis menjadi
monomer glukosa dan manosa. Pada hidrolisis asam, glukosa dapat terdegradasi lebih
lanjut manjadi HMF yang dapat mengambat pembentukan etanol pada proses
fermentasi (Gambar 1). Kadar pati yang didapat pada penelitian ini adalah sebesar
30,42% (bb) dan 89,35% (bk) (Tabel 2). Hasil tersebut lebih tinggi dari yang
dilaporkan oleh Tokuari (2004) sebesar 24% (bb) dan Arnata (2009) sebesar 62,54%
(bk).
Kadar serat kasar yang didapat dalam penelitian ini adalah sebesar 0,77%.
Kadar serat yang kecil berpengaruh terhadap proses hidrolisis. Serat lebih sulit
terdegradasi dibanding pati karena mengandung selulosa, hemiselulosa dan lignin.
Subagio (2006) melaporkan serat ubi kayu adalah sebesar 0,60% sedangkan pada
keadaan kering serat yang didapat adalah sebesar 2,87%. Keadaan ini lebih besar dari
yang dilaporkan Arnata (2009) yaitu sebesar 2,69%
Kadar selulosa, hemiselulosa dan lignin dianalisa dengan menentukan nilai
Acid Detergent Fiber (ADF) dan Neutral Detergen Fiber (NDF) (Van Soetst 1963).
Pada penelitian ini komponen yang terbesar dari ubi kayu adalah hemiselulosa
sebesar 11,67% diikuti selulosa sebesar 3,15% dan lignin 0,67%. Kadar hemiselulosa
yang tinggi berpotensi menjadi monomer gula yang tinggi pula. Namun, hemiselulosa
juga berpotensi terdegradasi menjadi menjadi senyawa penghambat berupa furfural
penelitian ini berwarna merah kecoklatan dengan nilai pH 1-2. Hidrolisis dilakukan
dengan tujuan untuk memecah pati, selulosa dan hemiselulosa menjadi gula-gula
sederhana yang dapat digunakan oleh S. cerevisiae dalam proses fermentasi.
Tabel 5. Komposisi kimia hidrolisat asam ubi kayu setelah netralisasi
Parameter Komposisi HA Komposisi HA yang
diinginkan (g/l)
Susmiati (2009) telah menghidrolisis tepung ubi kayu dengan H2SO4 dan
melaporkan bahwa hidrolisis satu tahap dengan kadar padatan 30% dan konsentrasi
H2SO41 M selama 10 menit pada suhu 121oC. menghasilkan gula tertinggi. Pada
proses hidrolisis konsentrasi asam dan suhu reaksi merupakan variabel penting yang
dapat mempengaruhi terbentuknya senyawa-senyawa ini. Suhu moderat (<160oC)
diperlukan untuk dapat menghidrolisis hemiselulosa dan menekan dekomposisi gula
sedehana. Suhu yang lebih tinggi akan mempermudah dekomposisi gula sederhana
dan senyawa lignin (Mussatto dan Roberto 2004). Pada penelitian ubi kayu segar
digunakan sebagai substrat. Adanya kandungan air yang lebih banyak menyebabkan kadar padatan dan konsentrasi H2SO4 yang digunakan juga berbeda. Penggunaan ubi
kayu segar sebagai substrat telah dilaporkan oleh Rusdianto (2010). Rusdianto (2010)
melaporkan bahwa hidrolisis menggunakan H2SO4 1 M selama 15 menit, suhu 121oC
dengan kadar padatan 18% mendekati hasil hidrolisis tepung ubi kayu yang
dilaporkan Susmiati (2010), sehingga cara hidrolisis tersebut dipergunakan dalam
penelitian ini. Setelah semua kondisi hidrolisis terpenuhi maka didapat hidrolisat
dengan komposisi tertentu seperti pada Tabel 5.
Kadar gula total yang didapat pada hidrolisat asam setelah dilakukan