ABSTRAK
SINTESIS ZEOLIT BERBASIS SILIKA SEKAM PADI DENGAN METODE ELEKTROKIMIA SEBAGAI KATALIS
TRANSESTERIFIKASI MINYAK KELAPA
Oleh
FARADILLA SYANI
Telah dilakukan transesterifikasi minyak kelapa dengan metanol menggunakan zeolit sintetik yang dihasilkan dengan metode elektrokimia. Untuk membuat zeolit dengan komposisi yang berbeda, percobaan sintesis dilakukan dengan pH yang berbeda yakni 4, 5, 6, 8, 10 dan waktu elektrolisis yang berbeda yakni 15, 30, 45, 60 menit dengan potensial tetap sebesar 8V. Uji katalis pada reaksi transesterifikasi dilakukan dengan variabel kinetis yakni waktu reaksi transesterifikasi. Kondisi optimum percobaan adalah penggunaan zeolit sebesar 5% terhadap berat reaktan, dengan perbandingan mol minyak kelapa dan metanol 1:4, pada suhu 70 oC selama 2 jam dengan persen konversi sebesar 100%. Analisis GC-MS menunjukkan adanya sepuluh puncak utama dengan komposisi tertinggi adalah metil miristat dengan jumlah relatif sebesar 21,03%. Berdasarkan analisis parameter biodiesel diperoleh produk transesterifikasi yang memenuhi standar SNI 04-7182-2006 yakni massa jenis 0,8895 g/mL, angka cetana 73,4, dan viskositas 5,49 mm2/s. Zeolit dengan unjuk kerja terbaik dikarakterisasi dengan SEM-EDX, BET dan XRD.
TRANSESTERIFICATION CATALYST
By
FARADILLA SYANI
This study was carried out to invistigate transesterification of coconut oil with methanol using synthetic zeolite produced by electrochemical method as catalyst. Preparation of synthetis zeolites was undertaken at varied pHs of 4, 5, 6, 8, 10 and electrolysis times of 15, 30, 45, 50 minutes, with specified potential of 8V. A series of transesterification reaction was performed to select the zeolites capable to catalyse transesterification, and reaction time. The optimum conditions obtained for the transesterification reaction are the use of zeolite 5% by weight of reactant, the mole ratio of coconut oil to methanol of 1: 4, temperature of 70 ° C, and reaction time of 2 hours with the percent conversion of 100%. GC-MS analysis showed the presence of ten major peaks with the highest peak belongs to methyl myristate with relative amount of 21.03%. Transesterification product was found to meet some of the standards of SNI 04-7182-2006 for biodiesel, includes density (0.8895 g/mL), cetane number (73.4), and viscosity (5.49 mm2/s). Zeolite with the best performance was characterized by SEM-EDX, BET, and XRD techniques.
RIWAYAT HIDUP
Penulis menyelesaikan pendidikan dasar di SDN 1 Gotong
Royong Bandar Lampung dan menyelesaikannya tahun 2004,
pendidikan tingkat menengah hingga tahun 2007 di SMP
Negeri 9 Bandar Lampung. Kemudian penulis melanjutkan
pendidikan di SMTI Tanjung Karang Bandar Lampung dan
menyelesaikannya tahun 2010. Pada tahun yang sama, penulis diterima sebagai
mahasiswa Jurusan Kimia FMIPA Universitas Lampung melalui jalur Seleksi
Nasional Masuk Perguruan Tinggi Negeri (SNMPTN).
Selama menempuh pendidikan di kampus, penulis pernah menjadi Juara 5 Tingkat
Nasional Lomba Invitasi Nasional KSCSR Lampung tahun 2011, Finalis Youth
Power UGM Tahun 2012, Peringkat 3 GIS-Competition UGM 2012, Juara Poster
Terfavorit Tingkat Provinsi Lampung Olimpiade Sains Nasional Pertamina
(OSN-Pertamina) tahun 2013 Kategori Proyek Sains, 5 Besar Lomba Inovasi Teknologi
BAPPEDA Lampung 2014 dan Juara Poster Terfavorit Tingkat Provinsi Lampung
Olimpiade Sains Nasional Pertamina (OSN-Pertamina) tahun 2014 Kategori
Proyek Sains. Penulis juga pernah menjadi Juri LKIR GEMPITA Himasakta
Aktivitas organisasi penulis dimulai sejak menjadi Kader Muda Himaki, Brigade
Muda BEM FMIPA, Kader Muda ROIS FMIPA dan Anggota Muda UKM
Penelitian Unila tahun 2010-2011. Penulis juga pernah menjadi Anggota Biro
Penerbitan Himaki FMIPA Unila tahun 2011–2012, Anggota Depertemen
Pemberdayaan Sumber Daya Mahasiswa (PSDM) BEM FMIPA Unila tahun
2011–2012, Anggota Bidang Kaderisasi ROIS FMIPA Unila tahun 2011–2012,
Sekretaris Umum UKM Penelitian Unila tahun 2011–2012, Anggota Biro Usaha
Mandiri Himaki FMIPA Unila tahun 2012–2013, Wakil Ketua Umum UKM
Penelitian Unila tahun 2012–2013 dan Bendaraha Umum Ikatan Lembaga
Penalaran dan Penelitian Mahasiswa Indonesia (ILP2MI) tahun 2013–2015.
Penulis juga pernah menjadi asisten praktikum Sains Dasar tahun 2013 untuk
mahasiswa Kimia, praktikum Kimia Dasar tahun 2013 untuk mahasiswa Teknik
Geofisika, dan praktikum Kimia Dasar, Sains Dasar dan Kimia Fisik tahun 2014
untuk mahasiswa Kimia. Pada tahun 2013 penulis menyelesaikan Kerja Praktek
Lapangan (PKL) yang berjudul ” Pengaruh Potensial Terhadap Komposisi Zeolit
Sintetis Berbasis Silika Sekam Padi yang Dihasilkan dengan Metode
Elektrokimia” di Laboratorium Polimer Universitas Lampung. Penulis juga
pernah menulis beberapa karya ilmiah antara lain Kawasan Usaha Agro Terpadu
(KUAT) Sebuah Konsep Grand Design Menuju Revitalisasi “Lampung Black Pepper”tahun 2012, Desain Bangun Trapping CO2 dan Nikotin Untuk Ruangan
Khusus Merokok Di Tempat Umum tahun 2013, dan Preparasi Zeolit Sintetik
Berbasis Silika Sekam Padi Dengan Metode Elektrokimia Sebagai Katalis Unggul
Tersenyumlah dalam mengawali hari, karena itu menandakan
bahwa kamu siap menghadapi hari dengan penuh semangat
Jangan takut mencoba, karena kesalahan adalah guru terbaik jika kamu jujur mengakuinya dan mau belajar
darinya
Tidak ada balasan kebaikan kecuali kebaikan (pula). Maka nikmat Tuhan kamu yang manakah yang kamu dustakan?
(QS. Ar-Rahman (55):60-61
Sesungguhnya ilmu itu diperoleh dengan belajar, kesantunan itu
diperoleh dengan kerendahan hati, sedangkan kesabaran itu
diperoleh dengan keteguhan hati.
(HR. Ibnu Fajar).
Jangan pernah takut untuk mencoba, karena dengan
mencoba kita dapat mengukur seberapa besar kekuatan,
Puji syukur kepada Allah SWT atas limpahan Karunia-Nya,
sehingga terciptalah sebuah karya tulisku yang kupersembahkan
untuk:
Papa dan Mama tercinta atas doa, kasih sayang, dukungan,
keikhlasan dan kesabaran dalam mendidikku.
Adinda Robin, Khasandra dan Laras Oktaviani atas doa dan
dukunganya
Keluarga besar yang selalu mendoakan keberhasilanku
Prof. Wasinton Simanjuntak, Ph.D dan Bapak Ibu Dosen
Jurusan Kimia atas semua dedikasinya selama ananda menempuh
pendidikan di kampus
SANWACANA
Segala Puji bagi Allah, Rabb semesta alam atas nikmat-Nya yang tak terhingga,
kasih sayang-Nya yang tak terbilang, serta nikmat persaudaraan yang senantiasa
terjaga hingga hari ini sehingga penulis dapat menyelesaikan skripsi yang berjudul
SINTESIS ZEOLIT BERBASIS SILIKA SEKAM PADI DENGAN METODE ELEKTROKIMIA SEBAGAI KATALIS
TRANSESTERIFIKASI MINYAK KELAPA
Shalawat teriring salam semoga tersampaikan kepada Rasulullah SAW beserta
keluarga dan sahabat serta umatnya di akhir zaman, Aamiin.
Teriring doa nan tulus jazaakumullah khaiiran katsir, penulis mengucapkan
terima kasih kepada:
1. Bapak Prof. Wasinton Simanjuntak, Ph. D. selaku Pembimbing I penulis atas
seluruh dedikasi yang beliau berikan selama menempuh pendidikan di
kampus, atas semua kesabaran, keikhlasan, bimbingan dan nasihat yang
diberikan hingga penelitian dan skripsi ini dapat terselesaikan.
2. Bapak Prof. Simon Sembiring, Ph. D. selaku Pembimbing II yang telah
membimbing penulis dengan penuh kesabaran, keikhlasan, serta bimbingan
3. Ibu Kamisah D Pandiangan, M.Si. selaku Pembahas dalam penelitian penulis
atas semua bimbingan, nasihat, dan kesabaran beliau sehingga skripsi ini
dapat terselesaikan. Semoga Allah membalasnya dengan kebaikan.
4. Ibu Dian Septiani Pratama, M.Si. selaku pembimbing akademik atas nasehat,
bimbingan serta motivasi yang diberikan kepada penulis.
5. Bapak Dr. Eng. Suripto Dwi Yuwono, M. T. selaku Ketua Jurusan Kimia
FMIPA Unila.
6. Bapak dan Ibu Dosen Jurusan Kimia FMIPA Universitas Lampung atas
seluruh dedikasi dan ilmu yang diberikan selama penulis menempuh
perkuliahan.
7. Bapak Prof. Suharso, Ph.D selaku dekan Fakultas Matematika dan Ilmu
Pengetahuan Alam Universitas Lampung.
8. Teriring syukur ananda untuk Papa dan Mama atas seluruh kasih sayang,
kesabaran, keikhlasan, doa, nasehat serta semua dedikasi dalam mendidik
ananda, semoga Allah membalas cintanya dengan jannah-Nya, aamiin
Allahuma aamiin.
9. Adikku Robin, Khasandra dan Laras Oktaviani terima kasih atas doa dan
dukungannya kepada penulis.
10. Teruntuk keluarga besar Makudun, Maete Ad, Uncu, Ante Li, Ante Yul dan
Ante Mel terima kasih atas doa, nasehat dan dukungannya kepada penulis.
11. Teruntuk sahabat terbaikku Chintia Yolanda terima kasih untuk persaudaraan,
doa, nasehat dan dukungannya. Semoga persahabatan kita terjalin dengan
dukungan, dan motivasinya selama penelitian.
13. Rekan kerja lab polimer Leni Astuti, S.Si., Funda Elisya, S.Si., Mbak Ruth
Meta M, S.Si., Mbak Juwita Ratna Sari, S.Si., Mbak Luh Gede Rai P., S.Si.,
Mbak Nurjanah, S.Si., Bu Laila, S.Si., Bu Rina, S.Pd., serta adik-adik satu
bimbingan Umi Fadilah, Endah Pertiwi, dan Jelita P.S. Terima kasih untuk
semua kerjasama dan bantuannya.
14. Rekan-rekan Kimia Angkatan 2010 Agung Supriyanto, M. Nurul Fajri,
M. Prasetio Ersa, Rahmat Kurniawan, S.Si., Wynda Dwi Anggraini, S.Si.,
Desi Meriyanti, S.Si., Rina R Sutisna, S.Si., Widya Afriliani W, S.Si.,
Putri Heriyani Utami, S.Si., Sevina Silvi, S.Si., Purniawati, S.Si., Rully
Prayetno, Lailatul Hasanah, Ariyanti, Sifa Kusuma W., Fajria Faiza,
Putri Sari Dewi, Juni Julhijjah, Kristi Arina, Martha Selvini Gultom.,
Rini Handayani R., Fauziyyah Mu’min S., S.Si., Rani Anggraini.,
Nur Robiah, Indah Aprianti, Silvana Maya P, Hapin Afliyani S.Si.,
Chyntia Gustianda P., Lolita Napatilova A.K., Sutini Karlina Sari,
Adetia Fatmawati dan Ely Setiawati terima kasih untuk persaudaraan,
cerita dan kenangan yang dibina selama menempuh pendidikan di kampus.
Semoga kebersamaan yang telah terangkai tak lekang oleh waktu meskipun
suatu saat kita akan berpisah.
15. Rekan-rekan UKM Penelitian dan ILP2MI terima kasih untuk persaudaraan,
kenangan, kerja sama, dukungan dan nasihat kepada penulis.
16. Uni Kidas, Mb Liza, Mb Nora, Mas Nomo dan Pak Gani terima kasih atas
17. Seluruh keluarga besar Jurusan Kimia Angkatan 2011 – 2014.
18. Almamater tercinta, Universitas Lampung.
Penulis menyadari bahwa dalam penulisan skripsi ini masih terdapat kekurangan
dan kesalahan, untuk itu penulis mengharapkan kritik dan saran yang membangun
demi perbaikan penulisan di masa datang. Semoga bermanfaat.
Bandar Lampung, September 2014 Penulis
DAFTAR ISI
3. Karakteristik Biodiesel ... 10
B.Katalis Transesterifikasi … ... 12
1. Katalis Homogen … ... 12
2. Katalis Heterogen ….… ... 13
3. Karakterisasi Katalis Heterogen ... 14
1. Difraksi Sinar-X (X-Ray Diffraction) ... 14
2. Scanning Electron Microscopy-Energy Dispersive X-ray Spektrometer (SEM-EDX) ... 17
1. Faktor-Faktor yang Mempengaruhi Elektrolisis ... 31
2. Reaksi Pada Elektroda ... 31
ii
2. Ekstraksi Silika dengan Metode Presipitasi … ... 34
3. Pembuatan Sol Silika Sekam Padi …… ... 35
4. Pembuatan Zeolit dengan Metode Elektrolisis dan Sol-Gel .... 35
5. Kalsinasi Katalis ... 36
3. Analisis GasChromathography-Mass Spectroscopy (GC-MS) ... 41
7. Karakterisasi Katalis ... 43
a. Karakterisasi dengan XRD (X-Ray Diffraction) ... 43
b. Karakterisasi dengan SEM/EDX (Scanning Electron Microscope-Energy Dispersive Spectrometer) ... 44
c. Karakterisasi dengan BET (Brunauer-Emmett-Teller) ... 45
E. Pembuatan Zeolit dengan Metode Elektrokimia ... 50
F. Uji Reaksi Transesterifikasi ... 53
1. Penentuan Waktu Reaksi Optimum ... 54
2. Hasil Reaksi Transesterifikasi ... 55
G. Uji Kelayakan Biodiesel ... 55
1. Kromatografi Gas-Spektroskopi Massa (KG-SM)... 56
2. Kualitas Biodiesel ... 62
H. Karakterisasi Katalis ... 63
1. Scanning Electron Microscope-Energy Dispersive Spectrometer (SEM/EDX) ... 63
V. SIMPULAN DAN SARAN ... 69
A. Simpulan ... 69
B. Saran ... 70
DAFTAR TABEL
Tabel Halaman
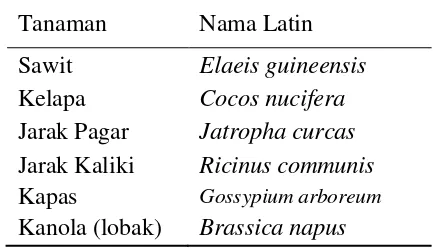
1. Beberapa tanaman penghasil minyak nabati... 7
2. Contoh zeolit alam yang umum ditemukan ... 22
3. Rumus oksida beberapa jenis zeolit sintetik ... 24
4. Komposisi sekam padi ... 26
5. Karakteristik silika sekam padi yang dihasilkan dengan dengan metode IPSIT (Indian Institute of Science Precipitate Silica Technology). ... 30
6. Hasil reaksi transesterifikasi minyak kelapa dengan tiga katalis yang berbeda... 55
7. Hasil analisis GC-MS produk transesterifikasi minyak kelapa... 57
DAFTAR GAMBAR
Gambar Halaman
1. Reaksi transesterifikasi ... 8
2. Reaksi transesterifikasi antara trigliserida dan metanol ... 8
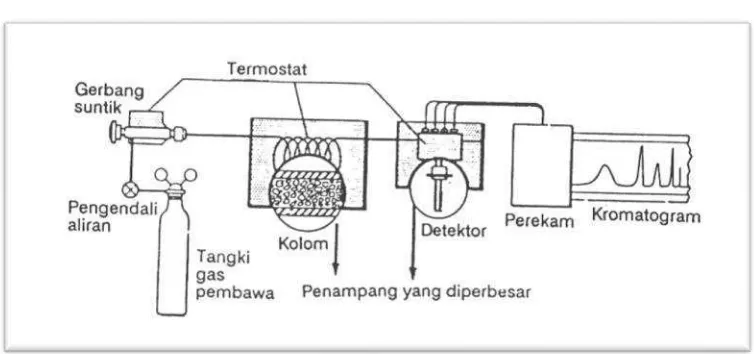
3. Bagian dasar kromatografi gas ... 11
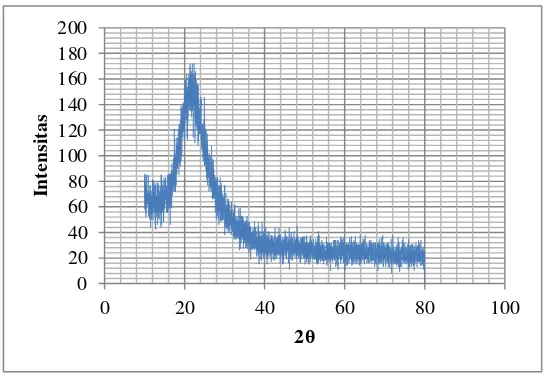
4. Pola difraksi sinar-X pada sampel silika sekam padi setelah kalsinasi 550 ºC ... 16
5. Mikrostruktur silika sekam padi ... 17
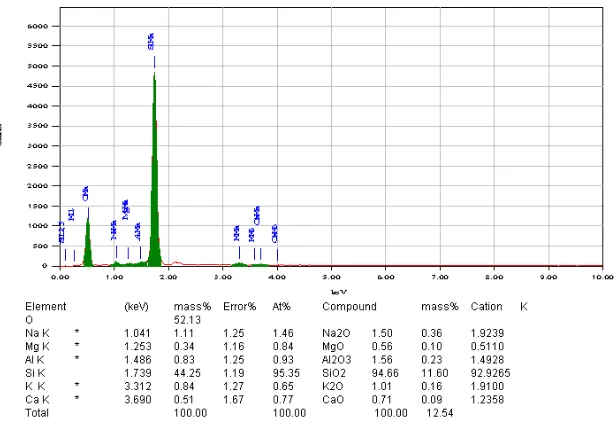
6. Hasil analisis EDX silika sekam padi ... 18
7. Enam tipe adsorpsi dan desorpsi isotermis pada padatan atau bahan mesopori dan mikropori ... 21
8. Viskometer Ostwald (alat untuk mengukur viskositas) ... 39
9. Sekam padi ... 47
10. Proses ekstraksi silika sekam padi ... 49
11. Sol silika ... 49
12. Reaktor sintesis zeolit ... 50
13. Mekanisme sintesis zeolit ... 51
14. Proses sintesis ... 52
15. Reaktor transesterifikasi ... 53
16. Kurva penentuan waktu reaksi optimum ... 54
ii
18. Spektrum massa ... 58
19. Fragmentasi metil palmitat ... 62
20. Mikrogram katalis zeolit sintetik yang di kalsinasi pada 300 ºC ... 64
21. Spektrum EDX zeolit sintetik yang di kalsinasi pada 300 ºC ... 64
22. Pola difraksi sinar-x untuk zeolit pH 10 dengan waktu elektrolisis 30 menit ... 65
23. Kurva dan hasil multi-point BET zeolit sintetik ... 67
I. PENDAHULUAN
A. Latar Belakang
Peningkatan jumlah kendaraan dan industrialisasi telah berdampak langsung pada
peningkatan kebutuhan akan bahan bakar. Hal ini yang menjadi pendorong
perkembangan sumber energi alternatif dan terbarukan untuk mengurangi dampak
negatif akibat semakin terbatasnya ketersediaan bahan bakar, terutama bahan
bakar fosil. Untuk tujuan tersebut, dewasa ini berbagai sumber energi alternatif
terus diteliti dan dikembangkan, antara lain bioetanol (Sari, 2013; Septarini,
2013), biogas (Syarif, 2009), dan biodiesel (Nurjannah, 2014).
Dari beberapa sumber energi alternatif tersebut, salah satu yang paling berpotensi
untuk dikembangkan di Indonesia adalah biodiesel. Hal ini dikarenakan
Indonesia memiliki berbagai sumber penghasil minyak nabati seperti kelapa,
kelapa sawit, kedelai, bunga matahari, dan jarak pagar yang merupakan bahan
baku pembuatan biodiesel.
Dalam pembuatan biodiesel, salah satu aspek yang terus diteliti adalah
pengembangan katalis heterogen, sebagai pengganti katalis homogen yang telah
digunakan secara tradisionil. Pengembangan katalis heterogen dimaksudkan
2
basa. Kelemahan katalis homogen yaitu dapat bercampur dengan produk
sehingga sulit dipisahkan. Disamping itu, katalis asam maupun basa bersifat
korosif sehingga tidak ramah lingkungan. Dibanding dengan katalis homogen,
katalis heterogen memiliki keuntungan antara lain biaya pembuatannya murah,
tidak korosif, ramah lingkungan (Bangun, 2007), mudah untuk digunakan dalam
berbagai media, mudah untuk dipisahkan katalis dari campuran reaksi, dan
penggunaan ulang katalis (Moffat, 1990; Frenzer and Maier, 2006).
Katalis heterogen pada prinsipnya terdiri dari dua komponen utama, yakni
penyangga dan situs aktif. Penyangga katalis heterogen adalah zat padat berpori,
dimana situs aktif ditempelkan. Banyak bahan yang telah diaplikasikan sebagai
penyangga katalis seperti alumina aktif (Wang and Liu, 1998), zeolit (Breck,
1974; Hideyuki et al., 2004), dan silika (Benvenutti and Yoshitaka, 1998; Yang et
al., 2006; Pandiangan dkk., 2009).
Situs aktif merupakan logam-logam transisi yang memiliki orbital d kosong atau
memiliki elektron tunggal yang akan disumbangkan pada molekul reaktan
sehingga terbentuk ikatan baru dengan kekuatan ikatan tertentu (Campbell, 1998).
Berbagai logam telah diaplikasikan sebagai situs aktif diantaranya Fe (Kusworo,
2013), Ni (Tadeus, 2013), Cr (Trisunaryanti dkk., 2002 ), Ti (Pandiangan dkk.,
2010), Co (Trisunaryanti dan Emmanuel, 2009), Cu (Sasarahan, 2013), Zn
(Trisunaryantidkk., 2008).
Dalam bidang katalis heterogen, zeolit merupakan bahan yang sangat menarik,
karena zeolit diketahui merupakan padatan berpori dan sudah memiliki aktivitas
keunggulan dibanding zeolit alam, antara lain kandungan dari zeolit dapat
divariasikan sesuai dengan kebutuhan. Sesuai dengan komponen pembentuknya,
silika sekam padi merupakan bahan baku zeolit sintetik yang sangat potensil
karena didukung oleh berbagai faktor.
Sekam padi merupakan residu pertanian yang jumlahnya melimpah di Indonesia,
termasuk Provinsi Lampung. Sebagai gambaran, data Biro Pusat Statistik (BPS)
Provinsi Lampung menunjukkan bahwa pada tahun 2012 produksi padi mencapai
3 juta ton. Hasil penelitian (Widowati, 2001) menunjukkan, sekitar 20% dari
gabah kering adalah sekam, dengan demikian potensi sekam yang ada di Provinsi
Lampung ada sekitar 600.000 ton. Hasil penelitian Sharma (1984) juga
menunjukkan, bahwa sekam padi mengandung silika sekitar 22%. Dengan
demikian, potensi silika sekam padi yang dimiliki Provinsi Lampung mencapai
136.000 ton. Silika sekam padi diketahui larut dalam larutan alkali, sehingga
dapat diperoleh dengan mudah menggunakan metode ekstraksi alkalis misalnya
dengan NaOH dan KOH (Kalaphathy et al., 2000; Daifullah dkk., 2003;
Pandiangan dkk., 2008; Suka dkk., 2008).
Komponen lain dari zeolit sintetik adalah alumina. Umumnya alumina yang
digunakan untuk pembuatan zeolit sintetik adalah senyawa alumina, antara lain
aluminium nitrat (Wang et al., 2010), aluminium klorida (Dirdianti, 2011)
4
Dikaitkan dengan potensi dan sifat silika sekam padi di atas, dalam penelitian ini
digagas untuk membuat zeolit sintetik dengan metode elektrokimia. Prinsip dasar
gagasan ini adalah elektrolisis logam aluminium yang ditempatkan dalam sol
silika sekam padi. Dalam proses ini, logam aluminium akan teroksidasi menjadi
kation Al3+, yang akan terlarut secara merata dalam sol silika. Dengan demikian,
diharapkan akan diperoleh produk yang sangat homogen. Di samping itu, secara
umum telah diketahui bahwa proses elektrokimia dapat dikendalikan dengan
mengatur variabel elektrokimia yang diterapkan, dua yang paling utama adalah
pH dan waktu. Hal ini berarti, jumlah kation Al3+ yang terbentuk dalam proses
elektrolisis dapat diatur dengan mengatur kedua variabel di atas, yang berarti juga,
bahwa nisbah Al/Si dapat diatur dengan mengatur variabel elektrokimia tersebut.
Sesuai dengan latar belakang yang dipaparkan di atas, masalah utama yang akan
dipelajari dalam penelitian ini adalah bagaimana pengaruh waktu dan pH terhadap
nisbah Al/Si zeolit sintetik yang dihasilkan dan bagaimana hubungan komposisi
ini dengan unjuk kerja zeolit sebagai katalis transesterifikasi.
B. Tujuan Penelitian
Berdasarkan latar belakang masalah yang telah dipaparkan di atas, penelitian ini
dilakukan dengan beberapa tujuan spesifik sebagai berikut:
1. Mendapatkan informasi tentang pengaruh waktu dan pH terhadap nisbah
Al/Si zeolit sintetik yang dihasilkan.
2. Mendapatkan informasi tentang potensi zeolit sintetik yang dihasilkan
C. Manfaat Penelitian
Penelitian ini diharapkan dapat memberikan manfaat sebagai berikut :
1. Menjadi dasar untuk mengembangkan metode produksi biodiesel yang
lebih efisien dan ramah lingkungan.
2. Membuka peluang pemanfaatan silika sekam padi dalam skala industri.
6
II. TINJAUAN PUSTAKA
A. Biodiesel
1. Bahan Baku Biodiesel
Biodiesel adalah bahan bakar alternatif yang dapat digunakan secara langsung
atau dicampur dengan solar untuk mesin diesel. Dewasa ini keterkaitan terhadap
biodiesel terus meningkat karena selain dapat diperbarui, bahan bakar alternatif ini
juga diketahui memiliki sifat-sifat yang lebih baik dibandingkan diesel
petrokimia. Pada dasarnya biodiesel merupakan alkil ester asam lemak yang
dapat dihasilkan dari rangkaian reaksi esterifikasi dan transesterifikasi asam lemak
yang terkandung dalam minyak nabati maupun minyak hewani.
Meskipun kedua jenis bahan baku di atas dapat digunakan, namun hingga dewasa
ini bahan baku yang paling umum digunakan adalah minyak nabati. Bahan baku
ini masih menjadi andalan dan potensial karena keberadaannya yang dapat
diperbaharui. Selain itu, terdapat beberapa kelebihan biodiesel antara lain adalah
tidak beracun, dapat dibiodegradasi, mempunyai bilangan setana yang tinggi,
mengurangi emisi karbon monoksida, hidrokarbon dan NOx. Dan memiliki flash
minyak hewani. Tabel.1 menunjukkan berbagai penghasil minyak nabati yang
dapat dimanfaatkan sebagai bahan baku pembuatan biodiesel.
Tabel.1 Beberapa tanaman penghasil minyak nabati
Tanaman Nama Latin Sawit Elaeis guineensis
Kelapa Cocos nucifera
Jarak Pagar Jatropha curcas
Jarak Kaliki Ricinus communis
Kapas Gossypium arboreum
Kanola (lobak) Brassica napus
Sumber: Soerawidjaja, 2006; Tambun, 2006.
Di Indonesia khususnya di Provinsi Lampung tanaman kelapa merupakan sumber
minyak nabati yang sangat pontensil untuk industri biodiesel didukung oleh luas
perkebunan kelapa yang mencapai 377.350 Ha (BPS, 2012) selain kelapa, kelapa
sawit, jarak pagar, dan jarak kaliki juga merupakan tanaman penghasil minyak
nabati yang sangat potensil di Indonesia.
2. Reaksi Pembuatan Biodiesel
Seperti dipaparkan sebelumnya, biodiesel pada hakekatnya adalah produk reaksi
transesterifikasi minyak nabati atau minyak hewani. Transesterifikasi merupakan
reaksi perubahan suatu ester menjadi ester lain dengan mereaksikannya dengan
suatu alkohol. Secara umum transesterifikasi dapat dituliskan dengan persamaan
8
ester alkohol ester alkohol
Gambar 1. Reaksi transesterifikasi
Dikaitkan dengan biodiesel, transesterifikasi merupakan pengubahan gliserida
menjadi ester yang lebih sederhana dengan mereaksikannya dengan alkohol
terutama metanol dan etanol. Dalam reaksi ini, gugus gliserida digantikan oleh
gugus metil atau etil dari alkohol dan gliserida diubah menjadi gliserol sebagai
hasil samping.
Secara garis besar, gliserida yang terkandung dalam minyak nabati dapat
dibedakan menjadi tiga golongan yakni monogliserida, digliserida, dan
trigliserida. Ketiga jenis trigliserida tersebut dapat mengalami transesterifikasi
mengikuti persamaan reaksi yang dicontohkan dalam Gambar 2.
metanol ester metil gliserol asam-asam lemak
Gambar 2. Reaksi transesterifikasi antara trigliserida dan metanol
Seperti terlihat pada Gambar 2, transesterifikasi mengakibatkan pemutusan ikatan
rangkap pada digliserida dan trigliserida menghasilkan metil ester asam lemak.
biodiesel menjadi bahan bakar yang lebih baik dari minyak nabati asalnya.
Reaksi transesterifikasi minyak nabati dengan alkohol (metanol) berlangsung
sangat lambat. Oleh karena itu, katalis menjadi kebutuhan yang mutlak harus ada
dalam reaksi tersebut. Beberapa peneliti telah melaporkan pembuatan biodiesel
dengan menggunakan katalis asam atau basa kuat. Katalis asam atau basa yang
umum digunakan dalam pembuatan biodiesel yaitu H2SO4 (Widyan and
Al-Shyouk, 2002), HCl (Al-Widyan and Al-Al-Shyouk, 2002), NaOH (Haryanto, 2002;
Utami dkk, 2007) dan KOH (Prakoso, 2004).
Penggunaan katalis asam atau basa masih memiliki beberapa kelemahan.
Penggunaan katalis asam diketahui membutuhkan waktu reaksi yang cukup lama
(Schuarddt et al., 1998) dan pemisahan katalis dan produk sangat sulit sehingga di
butuhkan perlakuan khusus untuk memisahkannya. Di samping itu, reaksi harus
dilangsungkan tanpa air karena adanya air akan meningkatkan pembentukan asam
karboksilat sehingga mengurangi rendemen reaksi. Dibanding dengan asam,
katalis basa menghasilkan reaksi dengan laju yang lebih tinggi. Namun demikian,
penggunaan katalis ini dapat menghasilkan air dari reaksi antara hidroksida dan
alkohol. Pembentukan air ini akan mengakibatkan terjadinya reaksi hidrolisis
ester yang sudah terbentuk, menghasilkan sabun yang tidak hanya mengurangi
rendemen reaksi akan tetapi juga menyulitkan pemisahan gliserol akibat
10
Karena alasan tersebut, banyak peneliti menggagaskan penggunaan katalis
heterogen dalam reaksi transesterifikasi untuk pembuatan biodiesel diantaranya
adalah abu tandan kosong sawit (Imadudin dkk, 2008), Nb2O5-ZAA
(Padmaningsih dkk, 2006), Fe-SiO2 (Pandiangan dkk, 2009). Penggunaan katalis
heterogen dalam reaksi transesterifikasi minyak nabati mununjukkan konversi
yang cukup besar, yaitu mencapai 92% meggunakan abu tandan kosong sawit
(Imadudin dkk, 2008), 76,6% menggunakan Nb2O5-ZAA (Padmaningsih dkk,
2006), dan 70 % menggunakan Fe-SiO2 (Pandiangan dkk, 2009). Disamping
persen konversi yang cukup besar, katalis heterogen memiliki beberapa kelebihan
diantaranya yaitu ketahanannya terhadap reaksi bersuhu tinggi (Shriver etal.,
1990), kemudahan pemisahan katalis dari campuran reaksi, serta dapat digunakan
berulang-ulang (Moffat, 1990; Frenzer and Maier, 2006).
3. Karakteristik Biodiesel
Seperti dipaparkan sebelumnya, biodiesel pada hakekatnya adalah metil atau etil
ester asam lemak, tergantung pada jenis alkohol yang digunakan. Untuk
mengetahui komposisinya, biodiesel umumnya dianalisis menggunakan
kromatografi gas spektrometri massa (GC-MS), dengan memanfaatkan volatilitas
ester yang tinggi sehingga dapat diubah menjadi gas dengan mudah dalam
perangkat GC-MS.
Perangkat GC-MS pada dasarnya merupakan paduan perangkat GC, yang
berperan untuk memisahkan komponen yang ada dalam suatu sampel, dan
3.
Gambar 3. Bagian dasar kromatografi gas
Komponen penting dalam kromatografi gas adalah:
1. Tangki pembawa gas yang dilengkapi dengan pengatur tekanan
2. Tempat injeksi sampel
3. Kolom
4. Detektor yang dilengkapi termostat
5. Pemerkuat arus (amplifier)
6. Rekorder atau integrator
Fungsi gas pembawa adalah mengangkut cuplikan dari kolom menuju detektor,
gas tersebut haruslah inert dan murni, gas pembawa yang sering digunakan adalah
nitrogen, hidrogen, helium, dan argon. Kolom kromatografi terdiri dari tiga
bagian yaitu wadah luar, isi kolom yang terdiri dari padatan pendukung dan fasa
12
B. Katalis Transesterifikasi
1. Katalis Homogen
Katalis homogen merupakan katalis yang mempunyai fasa sama dengan reaktan
dan produk. Penggunaan katalis homogen ini mempunyai kelemahan yaitu:
mencemari lingkungan, tidak dapat digunakan kembali, bersifat korosif,
berbahaya karena dapat merusak kulit, mata, paru-paru bila tertelan, sulit
dipisahkan dari produk sehingga terbuang pada saat pencucian (Widyastuti,
2007). Selain itu katalis homogen juga umumnya hanya digunakan pada skala
laboratorium ataupun industri bahan kimia tertentu, sulit dilakukan secara
komersil, oprasi pada fase cair dibatasi pada kondisi suhu dan tekanan, sehingga
peralatan lebih kompleks dan diperlukan pemisahan antara produk dan katalis.
Katalis basa homogen seperti NaOH (natrium hidroksida) dan KOH (kalium
hidroksida) merupakan katalis yang paling umum digunakan dalam proses
pembuatan biodiesel karena dapat digunakan pada temperatur dan tekanan operasi
yang relatif rendah serta memiliki kemampuan katalisator yang tinggi. Akan
tetapi, katalis basa homogen sangat sulit dipisahkan dari campuran reaksi
sehingga tidak dapat digunakan kembali dan pada akhirnya akan ikut terbuang
sebagai limbah yang dapat mencemarkan lingkungan (Kirk and Othmer, 1980).
Keunggulan katalis homogen adalah konversi reaksi yang dihasilkan lebih besar
dibandingkan katalis heterogen, tidak membutuhkan suhu dan tekanan yang tinggi
Katalis heterogen merupakan katalis yang memiliki fasa berbeda dengan reaktan.
Katalis heterogen berada pada fasa padat sedangkan reaktan berada pada faca cair.
Katalis heterogen memiliki berbagai keunggulan dibandingkan katalis homogen,
antara lain biaya pembuatannya murah, tidak korosif, ramah lingkungan (Bangun,
2007), efisiensinya yang tinggi, kemudahan untuk digunakan dalam berbagai
media, kemudahan pemisahan katalis dari campuran reaksi, dan penggunaan
ulang katalis (Moffat, 1990; Frenzer and Maier, 2006).
Dalam reaksi transesterifikasi katalis akan memecahkan rantai kimia minyak
nabati sehingga rantai ester minyak nabati akan terlepas, begitu ester terlepas
alkohol akan segera bereaksi dengannya dan membentuk biodiesel, sedangkan
gliserin dan katalis yang tersisa akan mengendap setelah reaksi selesai.
Penggunaan katalis tidak boleh terlampau banyak ataupun terlampau sedikit,
penggunaan katalis yang terlampau banyak reaksi transesterifikasi akan
menghasilkan emulsi, dan jika sedikit mengakibatkan pemisahan gliserol dan
metil ester tidak sempurna.
Aktivitas suatu katalis juga sangat bergantung pada komponen penyusunnya.
Katalis heterogen terdiri atas penyangga dan situs aktif (dopan). Situs aktif
merupakan logam-logam transisi yang memiliki orbital d kosong atau memiliki
elektron tunggal yang akan disumbangkan pada molekul reaktan sehingga
terbentuk ikatan baru dengan kekuatan ikatan tertentu (Campbell, 1998).
14
Berbagai logam telah diaplikasikan sebagai situs aktif diantaranya Fe, Ni, Ti, Al,
Co, Cu, Zn dan lain-lain. Terlepas dari peranan situs aktif, penyangga katalis
mengambil peranan penting dalam aktivitas katalisis suatu katalis heterogen.
Banyak bahan yang telah diaplikasikan sebagai penyangga katalis seperti alumina
aktif (Wang and Liu, 1998), zeolit (Breck, 1974; Hideyuki et al., 2004), dan silika
(Benvenutti and Yoshitaka, 1998; Yang et al., 2006; Pandiangan dkk, 2009).
3. Karakterisasi Katalis Heterogen
1. Difraxi Sinar-X (X-Ray Diffraction)
Karakterisasi X-Ray Diffraction (XRD) dimaksudkan untuk mengidentifikasi fasa
bulk suatu katalis dan untuk menentukan sifat kristal atau kristalinitas dari suatu
katalis. Kebanyakan dari katalis adalah berbentuk padatan kristal seperti oksida
logam, zeolit, dan logam yang berpenyangga. XRD menjadi teknik yang cukup
handal dan mendasar untuk mengevaluasi sifat-sifat fasa kristal dan ukuran kristal
(Leofanti et al., 1997).
Di dalam analisis XRD, kristal katalis memantulkan sinar-X yang dikirimkan dari
sumber dan diterima oleh detektor. Dengan melalukan sudut kedatangan sinar-X
maka spektrum pantulan adalah spesifik yang berhubungan langsung dengan
lattice spacing dari kristal yang dianalisis. Pola difraksi diplotkan berdasarkan
intensitas peak yang menyatakan peta parameter kisi kristal atau indeks Miller
(hkl) sebagai fungsi 2θ, dimana θ menyatakan sudut difraksi berdasarkan
adalah datar.
nλ= 2d sin θ
Dimana d menyatakan jarak antar lapisan atom atau ion yang berdekatan, yang
menyatakan panjang gelombang radiasi sinar-X, dan n adalah urutan pantulan.
Kristalinitas dapat juga ditentukan dengan XRD melalui pembandingan intensitas
atau luasan peak sampel dengan intensitas atau luasan peak standar yang
ditunjukkan pada persamaan :
Lebar peak XRD adalah merupakan fungsi dari ukuran partikel, maka ukuran
kristal (crystallite size) dinyatakan dalam Persamaan Scherrer berikut
(Richardson, 1989):
Dimana K=1.000, B adalah lebar peak untuk jalur difraksi pada sudut 2θ, b adalah
1nstrument peak broadening (0.1o), dan adalah panjang gelombang pada 0.154
nm (Wolfovich et al., 2004; Richardson, 1989). Suku (B2-b2)½ adalah lebar peak
untuk corrected instrumental broadening.
Metode XRD banyak digunakan untuk mengidentifikasi dan mengkarakterisasi
material yang digunakan sebagai katalis, karena banyak material katalis yang
16
mengidentifikasi dan menentukan besarnya bagian fasa dalam padatan, film tipis,
dan sample multi fasa. Salah satu alat XRD yang biasa digunakan adalah Siemen
D5000 yang menggunakan radiasi Cu-Kα radiation. Tabung X-ray dioperasikan
pada 40 kV dan 30 mA.
Karakteristik yang paling penting dari katalis logam berpenyangga adalah:
Ukuran dan dispersi kristal, yang merupakan fraksi atau jumlah bagian
atom logam yang berhubungan dengan jumlah situs aktif
Distribusi di dalam granul penyangga, yang menentukan akses ke
situs-situs aktif.
Rasio antar permukaan kristal, yang mempunyai peran penting dalam
reaksi sebagai struktur yang sensitif.
Berikut ini disajikan contoh difraktogram silika sekam padi yang dikalsinasi pada
suhu 550 oC.
Gambar 4. Pola difraksi sinar-X pada sampel silika sekam padi setelah kalsinasi
Untuk menganalisis komposisi kimia suatu permukaan secara kualitatif dan
kuantitatif digunakan perangkat alat SEM (Scanning Electron Microscopy) yang
dirangkaikan dengan EDX (Energy Dispersive X-ray Spectrometer). Pada SEM
(Scannng Electron Microscopy) dapat diamati karakteristik bentuk, struktur, serta
distribusi pori pada permukaan bahan, sedangkan komposisi serta kadar unsur
yang terkandung dalam sampel dapat diamati dengan EDX (Sartono, 2007).
Analisis EDX dimaksudkan untuk mengetahui ketidakhomogenan pada sampel
dan menganalisis secara kualitatif dan kuantitatif jenis unsur atau oksida logam M
yang masuk ke dalam matriks silika sekam padi pada pembuatan katalis heterogen
berbasis silika sekam padi dengan metode sol-gel. Berikut ini disajikan gambar
yang diperoleh dari hasil uji karakteristik silika sekam padi menggunakan
SEM-EDX (Yuliyati, 2011) pada Gambar 5 dan 6.
18
Gambar 6. Hasil analisis EDX silika sekam padi
3. BET (Brunauer-Emmett-Teller)
Luas permukaan, volume total pori, dan rata-rata jari-jari pori merupakan faktor
penentu unjuk kerja suatu katalis. Suatu bahan padat seperti katalis, memiliki luas
permukaan yang dapat dibedakan menjadi luas permukaan eksternal
(makroskopik) dan internal (mikroskopik). Luas permukaan eksternal hanya
meliputi permukaan luar bahan, sedangkan luas permukaan internal meliputi
semua pori-pori kecil, celah, dan rongga pada padatan (Nurwijayadi, 1998).
Luas permukaan katalis pada penelitian ini ditentukan melalui pengukuran
menggunakan Surface Area Analyzer Quantachrome NOVA-1000 versi 2.2 yang
didasarkan pada metode BET yaitu adsorpsi dan desorpsi isotermis dari gas yang
diserap (nitrogen). Kuantitas gas yang diserap dapat dihitung dengan persamaan
(1)
Dimana:
W = Berat gas yang diserap (adsorbed) pada tekanan relatif P/Po
Wm = Berat gas nitrogen (adsorbed) pada lapis tunggal P = Tekanan kesetimbangan adsorpsi
Po = Tekanan uap jenuh adsorpsi P/ Po = Tekanan relatif adsorpsi C = Konstanta energi
Persamaan BET di atas akan merupakan garis lurus apabila dibuat grafik 1/ [W
(P/Po – 1)] versus P/Po (Lowell and Shields,1984). Selanjutnya untuk
pengukuran luas permukaan dengan metode BET berdasarkan pada persamaan
berikut:
(2)
Dimana:
St = luas permukaan total (m2) Wm = berat gas nitrogen (g)
M = berat molekul dari gas nitrogen
N = bilangan Avogadro (6,023 x 1023 molekul/mol) Acs = luas molekul cross sectional gas nitrogen (16,2 Å)
Pengukuran luas permukaan spesifik ditentukan dengan menggunakan persamaan
20
Volume total pori adalah volume gas yang teradsorpsi pada tekanan jenuh, untuk
menghitung volume total pori digunakan persamaan berikut:
(4)
Dimana:
Vρ = volume total pori (cc/g)
Wa = berat nitrogen yang teradsorpsi pada P/Po = 0,99 = densitas nitrogen pada 77oK
Perhitungan ukuran pori dilakukan dengan asumsi bahwa geometri pori berbentuk
silindris sehingga rata-rata jari-jari pori dihitung dari perbandingan volume total
pori dan luas permukaan spesifik, dengan menggunakan persamaan berikut:
(5)
Dimana:
Rp = rata-rata jari-jari pori Vρ = volume total pori
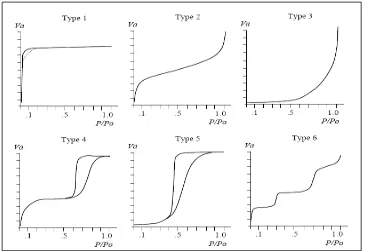
Terdapat enam tipe adsorpsi isotermis pada metode BET bila volume total gas
adsorpsi (Va) diplotkan sebagai fungsi P/Po, hasil adsorpsi isotermis tersebut
Gambar 7. Enam tipe adsorpsi dan desorpsi isotermis pada padatan atau bahan
mesopori dan mikropori
Tipe I merupakan karakteristik padatan mikropori seperti zeolit, yang
menunjukkan kapasitas adsorpsi yang tinggi dan cepat. Tipe II menunjukkan
adsorpsi isotermis pada material atau bahan yang tak berpori, sedangkan pada tipe
III untuk bahan yang makropori. Ciri utama isotermis pada tipe IV adalah adanya
hysteresis loop dan kenaikan grafik yang tinggi pada P/Po. Isotermis tipe ini
umumnya terdapat pada bahan mesopori seperti silika gel. Pada tipe V
menujukkan adsorpsi nitrogen yang rendah pada tekanan relatif rendah, kenyataan
ini mengindikasikan bahwa interaksi rendah antara adsorben dengan adsorben.
Isotermis tipe VI sangat jarang ditemukan, tipe ini dapat dihasilkan pada nitrogen
22
C. Zeolit
1. Zeolit Alam
Zeolit alam ditemukan dalam bentuk mineral dengan komposisi yang berbeda,
terutama dalam nisbah Al/Si dan jenis logam yang menjadi komponen minor,
seperti diperlihatkan dalam Tabel 2.
Tabel 2. Contoh zeolit alam yang umum ditemukan (Subagjo, 1993)
No Zeolit Alam Komposisi
1 Analsim Na16(Al16Si32O96).16H2O
Zeolit alam terbentuk karena adanya proses kimia dan fisika yang kompleks dari
batuan-batuan yang mengalami berbagai macam perubahan di alam. Para ahli
geokimia dan mineralogi memperkirakan bahwa zeolit merupakan produk gunung
berapi yang membeku menjadi batuan vulkanik, batuan sedimen dan batuan
metamorfosa yang selanjutnya mengalami proses pelapukan karena pengaruh
panas dan dingin (Lestari, 2010). Sebagai produk alam, zeolit alam diketahui
memiliki komposisi yang sangat bervariasi, namun komponen utamanya adalah
alumina dan silika. Di samping komponen utama ini, zeolit juga mengandung
zeolit klinoptilolit (Lestari, 2010).
Zeolit klinoptilolit memiliki diameter pori 0,45-0,65 nm (Bogdanov, 2009).
Klinoptilolit memiliki sifat stabil di berbagai media kaustik, stabil terhadap suhu
tinggi, dan tingkat kesetimbangan sorpsinya tinggi, sehingga banyak digunakan
dalam perlindungan kimia lingkungan dan industri (Korkuna, 2006). Dewasa ini
klinoptilolit banyak digunakan dalam bidang pengolahan air dan limbah cair
(Hrenovi, 2003; Erdem, 2004), adsorpsi (Polat, 2004), pengolahan limbah nuklir
(Prikryl, 1999), pertanian (Főldesová, 2007), dan pengobatan (Pavelic, 2002;
Zarkovic, 2003).
Terlepas dari aplikasinya yang luas, zeolit alam memiliki beberapa kelemahan,
diantaranya mengandung banyak pengotor seperti Na, K, Ca, Mg dan Fe serta
kristalinitasnya kurang baik. Keberadaan pengotor-pengotor tersebut dapat
mengurangi aktivitas dari zeolit. Untuk memperbaiki karakter zeolit alam
sehingga dapat digunakan sebagai katalis, adsorben, atau aplikasi lainnya,
biasanya dilakukan aktivasi dan modifikasi terlebih dahulu (Mockovciakova et
al., 2007; Setiadi dan Pertiwi 2007; Yuanita, 2010).
2. Zeolit Sintetik
Zeolit sintetik adalah zeolit yang dibuat secara rekayasa yang sedemikian rupa
sehingga didapatkan karakter yang lebih baik dari zeolit alam. Prinsip dasar
produksi zeolit sintetik adalah komponennya yang terdiri dari alumina dan silika,
24
komponen di atas. Komponen minor dalam zeolit juga dapat ditambahkan dengan
mudah menggunakan senyawa murni, sehingga zeolit sintetik memiliki komposisi
yang tetap dengan tingkat kemurnian yang tinggi. Dengan perkembangan
penelitian, dewasa ini telah dikenal beragam zeolit sintetik, dan beberapa
diantaranya disajikan dalam Tabel 3.
Tabel 3. Rumus oksida beberapa jenis zeolit sintetik (Georgiev, 2009).
Zeolit Rumus Oksida
Dewasa ini zeolit sintetik terus dikembangkan, dengan dua fokus utama yaitu
bahan baku dan metode. Dari segi bahan baku utama, digunakan dua jenis bahan
baku yakni bahan baku sintetik dan bahan baku limbah. Wongkasemjit (2002)
mensintesis zeolit ANA dan GIS dari bahan baku sintetik alumatran dan silatran
dengan proses sol-gel dan teknik microwave. Alumatran dan silatran digunakan
sebagai prekursor untuk menghasilkan aluminosilikat melalui proses sol-gel. NaCl
dan NaOH digunakan sebagai agen hidrolisis. Konsentrasi NaOH mempengaruhi
bentuk kristalnya, kristal yang sangat baik terbentuk pada konsentrasi NaOH yang
tinggi. Proses pembentukan gel adalah reaksi endotermik. Menggunakan
differential scanning calorimetry (DSC), pertumbuhan kristal maksimum terjadi
hidrotermal selama 3 jam pada suhu 110 0C, sedangkan analcime (ANA)
terbentuk pada suhu 130 0C selama 8 jam. Ukuran partikel yang terbentuk, GIS
4,55 µm dan ANA berukuran 9,96 µm.
Sunardi (2007) melaporkan telah mensintesis zeolit dengan bahan baku abu
layang batu bara dengan metode peleburan menggunakan NaOH serta aplikasinya
sebagai adsorben logam merkuri (II). Abu layang dan NaOH dicampur dan
dihomogenkan lalu dilebur pada temperatur 550 0C selama 60 menit. Hasil
peleburan ditambahkan akuades, diaduk selama 12 jam dan dihidrotermalkan pada
temperatur 90 0C selama 24 jam. Hasil karakterisasi menggunakan Fourrier
Transform Infra Red (FTIR) dan X-Ray Diffraction (XRD) menunjukkan bahwa
telah terbentuk zeolit tipe faujasit.
Dengan bahan baku yang sama, Laosiripojana (2010) berhasil mensintesis zeolit
dengan metode fusi. Abu layang dicampur dengan NaOH kondisi udara pada
suhu 450 0C di dalam furnace. Produk yang dihasilkan dilarutkan dengan akuades
kemudian diaduk dengan mesin pengaduk selama 12 jam. Kristal yang dihasilkan
dicuci dengan akuades dan dikeringkan semalaman dengan suhu 105 0C.
Karakterisasi zeolit menggunakan X-Ray Diffraction (XRD) diketahui bahwa
zeolit hasil sintesis memiliki rumus oksida 1.08Na2O.Al2O3.1.68SiO2.1.8H2O.
Bahan baku lain yang digunakan dalam sintesis zeolit adalah silika sekam padi.
Kamarudin (2004) melaporkan telah mensintesis zeolit dari silika sekam padi,
mula-mula sekam padi dibakar dalam furnace pada suhu 450, 600 dan 800 0C
26
NaOH pada suhu 80 0C selama 2 jam, kemudian dicampurkan dengan gel
(natrium aluminat dan natrium hidoksida) dan dipanaskan pada suhu 100 0C
selama 14 jam. Zeolit yang terbentuk dikarakterisasi dengan X-Ray Diffraction
(XRD), diketahui zeolit yang terbentuk bertipe zeolit Y dan P. Analisis adsorbsi
nitrogen diketahui luas permukaannya 39-211 m2/g, volume pori 0,014-0,075
cm3/g dan rata-rata diameter pori 2,95-6 nm.
D. Silika Sekam Padi
Sekam merupakan hasil samping penggilingan padi tertinggi sekitar 20%
(Widowati, 2001). Hasil penelitian Sharma (1984) menunjukkan bahwa dalam
sekam padi terkandung silika dengan kadar sekitar 22%, di samping komponen
lain seperti ditunjukkan dalam Tabel 4.
Tabel 4. Komposisi sekam padi (Sharma, 1984).
Komposisi Kandungan (% Berat)
Senyawa-senyawa organik 73,87
Karena kandungan silikanya yang tinggi, sekam padi merupakan salah satu
sumber silika nabati yang berpotensi untuk dimanfaatkan sebagai alternatif silika
mineral sebagai bahan baku pembuatan zeolit sintetik. Potensi ini juga didasarkan
luas untuk pembuatan keramik (Sitorus, 2009; Wittayakun, 2011), katalis (Adam,
2006), berbagai material komposit (Marlina, 2012; Suka, 2009; Handayani, 2009),
dan zeolit sintetik (Prasetyoko, 2007). Pemanfaatan silika yang demikian luas
juga didukung kemudahan untuk memperoleh silika dari sekam padi, yakni
dengan cara ekstraksi atau dengan pengabuan.
Suka dkk. (2008) berhasil mengkarakterisasi sekam padi Provinsi Lampung
dengan metode ekstraksi. Mula-mula sekam padi dipreparasi, sekam padi
direndam dalam air panas selama 2 jam dan dicuci berulang-ulang dengan air
panas untuk menghilangkan pengotor organiknya. Kemudian, sekam padi yang
telah bersih direndam ke dalam KOH 5% selama 60 menit. Filtrat yang diperoleh
diasamkan dengan HCl hingga pH mencapai 7,0. Karakterisasi dengan FTIR,
muncul puncak Si-OH, dan Si-O-Si yang menunjukkan adanya gugus fungsi
siloksan, yang mengindikasikan bahwa silika sekam padi merupakan silika
reaktif. Sifat reaktif silika ini juga didukung hasil karakterisasi menggunakan
XRD, yang menunjukkan bahwa silika adalah amorf dengan fase kristobalit.
Karakterisasi dengan EDX menunjukkan unsur unsur yang terkandung, meliputi
O, Na, Mg, Al, Si, K dan Ca. Hasil yang di dapatkan, sekam padi yang
diekstraksi memiliki kadar silika 40,8% dengan kemurnian sekitar 95,53%.
Menurut Mittal (1997) reaksi yang terjadi antara SiO2 yang terkandung dalam abu
sekam padi dengan larutan alkali, larutan KOH adalah sebagai berikut:
28
Kemudian, dalam larutan tersebut ditambahkan asam, larutan HCl yang
digunakan untuk mengikat kalium sehingga dihasilkan SiO2. Reaksi yang terjadi
sebagai berikut:
K2SiO3 + HCl SiO2 + KCl + H2O
Selain ekstraksi menggunakan alkali, Zulhajri (2000) mengekstrak silika dari
sekam padi dengan cara perendaman di dalam larutan asam klorida dengan
konsentrasi 0%, 1%, 3%, 5%, dan 10% selama 24 jam dilanjutkan dengan
pengabuan pada suhu pemanasan 900 oC selama 2 jam dan pengekstrakan dengan
asam nitrat encer. Residu kemudian dipanaskan pada suhu 900 oC selama 2 jam.
Penggunaan asam klorida, karena cenderung bereaksi dengan oksida logam
sehingga kadar logam dalam sekam padi dapat berkurang. Peningkatan
konsentrasi asam klorida dapat meningkatkan kadar (kemurnian) silika yang
terdapat pada abu sekam padi sampai 99,68% dengan konsentrasi asam klorida
10%.
Karena teknologi dalam pembuatan silika dari sekam padi mengalami
perkembangan dari tahun ke tahun. Sebuah institut di India dengan nama IPSIT
(Indian Institute of Science Precipitate Silica Technology) membuat sebuah
metode dalam pengendapan silika dari abu sekam padi (Subbukrishna, 2007),
dimana metode ini dapat diaplikasikan dalam skala industri. Secara garis besar,
teknologi ini melibatkan tiga proses, seperti disajikan di bawah ini.
Digesti
Na2O.xSiO2 (l) + CO2 (g) xSiO2(s) + Na2CO3(l)
Regenerasi
Na2CO3(l) + Ca(OH)2(s) CaCO3(s) + NaOH (l)
Dengan metode ini tahap pertama adalah digesti, mula mula abu sekam padi
dilarutkan ke dalam larutan NaOH agar terbentuk natrium silikat kemudian
disaring dan filtrat yang bersih siap untuk diendapkan. Langkah selanjutnya
adalah presipitasi, pada langkah ini bertujuan untuk mengendapkan silika dari
larutan natrium silikat. Gas karbon dioksida dengan laju alir tertentu dilewatkan
ke larutan silikat. Diaduk terus menerus dan endapan silika disaring dan dicuci
dengan air untuk menghilangkan garam anorganik. Filtrat yang dihasilkan
digunakan untuk tahap regenerasi.
Regenerasi adalah tahap dimana penambahan kalsium akan bereaksi natrium
karbonat membentuk kalsium karbonat dan natrium hidroksida. Filtrat hasil
proses pengendapan ditambahkan kalsium dan akan membentuk kalsium karbonat
dan natrium hidroksida, kemudian disaring untuk menghilangkan kalsium
karbonat dan larutan natrium hidroksida yang dihasilkan digunakan untuk proses
digesti. Kalsium karbonat dicuci dengan air dan dikeringkan, kalsium karbonat
dikalsinasi untuk mendapatkan kalsium oksida untuk proses regenerasi kembali.
Penerapan metode ini menghasilkan silika dengan sifat-sifat seperti disajikan
30
Tabel 5. Karakteristik silika sekam padi yang dihasilkan dengan dengan metode IPSIT (Indian Institute of Science Precipitate Silica Technology).
Sifat Bubuk Amorf
Penampilan Bubuk Putih
Kemurnian >98%
Luas Permukaan Area 50-300 m2/gm Berat jenis kotor 120-400 g / liter Pengurangan pengapian 3,0-6,0%
pH dari 5% bubur 6,4 ± 0,5
Kehilangan panas 4,0-7,0%
E.Elektrolisis
Elektrolisis adalah proses penggunaan energi listrik menjadi energi kimia. Dalam
proses elektrolisis, larutan yang dihasilkan tidak hanya menghantarkan arus
listrik, melainkan juga mengalami perubahan kimia. Perubahan kimia yang
terjadi selama proses elektrolisis mudah dilihat di sekitar elektroda, walaupun
perubahan ini hanya berupa penguraian sederhana (Svehla, 1985).
Aliran listrik melalui suatu konduktor (penghantar) melibatkan perpindahan
elektron dari potensial negatif tinggi ke potensial lainnya yang lebih rendah.
Mekanisme dari transfer ini tidak sama untuk berbagai konduktor. Dalam
penghantar elektronik, seperti padatan dan lelehan logam, penghantaran
berlangsung melalui perpindahan elektron langsung melalui penghantar dari
tersebut. Akan tetapi penghantar elektrolistik yang mencangkup larutan elektrolit
dan lelehan garam-garam. Penghantaran berlangsung melalui perpindahan
ion-ion baik positif maupun negatif menuju elektroda-elektroda. Migrasi ini tidak
hanya melibatkan perpindahan listrik dari suatu elektroda ke elektroda lainnya
tetapi juga melibatkan adanya transport materi dari suatu bagian konduktor ke
bagian lainnya (Mulyati, 2003).
1. Faktor-Faktor yang Mempengaruhi Elektrolisis
Faktor-faktor yang mempengaruhi proses elektrolisis yaitu kerapatan listrik,
waktu, tegangan, kadar keasaman (pH), ketebalan plat dan jarak antar elektroda
(Putero, 2008). Pemilihan elektroda juga berpengaruh dalam proses elektrolisis.
Faktor-faktor yang dipertimbangkan ketika memilih bahan elektroda adalah
stabilitas fisik dan kimiawi yang meliputi ketahanan terhadap korosi,
pembentukan oksida dan hidrida tertentu, laju dan selektivitas produk yang akan
terbentuk, konduktivitas listrik, ketahanan dan harga faktor, serta kesesuaian
dengan desain sel atau sistem (Artadi, 2007).
2. Reaksi pada Elektroda
Apabila listrik dialirkan melalui lelehan senyawa ion maka senyawa ion itu akan
diuraikan. Kation direduksi di katoda, sedangkan anion dioksidasi di anoda.
Reaksi elektrolisis dalam larutan elektrolit berlangsung lebih kompleks. Spesi
32
elektrodanya. Hal itu bergantung pada potensial spesi-spesi yang terdapat dalam
larutan (Keenan, 1984). Pada proses elektrolisis air dengan elektroda aluminium,
pada anoda terjadi oksidasi Al menjadi Al3+ dan pada katoda air mengalami
reduksi menghasilkan gas hidrogen (H2) (Holt et al., 2002).
3. Hukum Faraday
Akibat aliran arus listrik searah ke dalam larutan elektrolit akan terjadi perubahan
kimia dalam larutan tersebut. Menurut Michael Faraday (1834) lewatnya arus 1
F mengakibatkan oksidasi 1 massa ekivalen suatu zat pada suatu elektroda
(anoda) dan reduksi 1 massa ekivalen suatu zat pada elektroda yang lain (katoda)
(Mollah et al., 2004).
Hukum Faraday I : Massa zat yang timbul pada elektroda karena elektrolisis
berbanding lurus dengan jumlah listrik yang mengalir melalui larutan.
Keterangan:
W = massa zat yang diendapkan (g) Ar = Massa atom relatif
n = valensi ion t = waktu (dt)
III. METODOLOGI PENELITIAN
A. Tempat dan Waktu Penelitian
Penelitian ini telah dilakukan selama 3 bulan yaitu dari bulan Mei hingga Agustus
2014, bertempat di Laboratorium Polimer Jurusan Kimia Fakultas MIPA Universitas
Lampung. Sedangkan analisis produk transesterifikasi dilakukan di Laboratorium
Biomassa Universitas Lampung. Analisis SEM-EDX, XRD, dan BET dilakukan di
Institut Teknologi Bandung, Bandung dan GC-MS di Universitas Gajah Mada,
Yogyakarta.
B. Alat dan Bahan
1. Alat-alat yang digunakan
Alat-alat yang digunakan dalam penelitian ini antara lain, Scanning Electron
Microscope-Energy Dispersive X-Ray Spectroscopy (SEM-EDX) MA10-14-37 ZEI
SS EVO, X-Ray Diffraction (XRD), Brunauer-Emmett-Teller (BET) NOVA-1000
versi 2.2, GasChromathography -Mass Spectroscopy (GC-MS), viskometer,
perangkat elektrokimia, penangas, magnetic stirrer, oven, alat vakum, thermometer,
34
2. Bahan-bahan yang digunakan
Bahan-bahan yang digunakan dalam penelitian ini antara lain : sekam padi, larutan
HNO3 10 %, akuades, indikator universal, kertas saring, metanol, larutan NaOH
1,5 %,batangan aluminium dan minyak kelapa.
C. Prosedur Penelitian
1. Preparasi Sekam Padi
Langkah awal dalam penelitian ini adalah preparasi sampel sekam padi. Sebanyak
100 gram sekam padi direndam dalam air panas selama 2 jam untuk mengekstrak
bahan organik larut air yang merupakan bahan pengotor dalam proses ekstraksi silika.
Sekam padi kemudian disaring dan dicuci lagi secara berulang dengan cara disiram
dengan air panas untuk menghilangkan pengotor bahan organik larut air yang masih
diperkirakan menempel pada permukaan sekam padi. Kemudian, sekam padi yang
telah bebas dari pengotor dikeringanginkan dan selanjutnya sekam padi siap
digunakan untuk ekstraksi silika.
2. Ekstraksi Silika dengan Metode Presipitasi
Metode ekstraksi silika dalam penelitian ini mengadopsi metode ekstraksi yang telah
digunakan sebelumnya oleh Daifullah dkk (2003) dan Pandiangan dkk (2008).
Sebanyak 50 gram sekam padi yang telah bebas dari pengotor bahan organik larut air
filtrat yang mengandung silika terlarut ditampung. Untuk mengendapkan silika,
filtrat kemudian ditambahkan larutan asam HNO3 10% secara bertahap hingga
terbentuk endapan silika dalam bentuk gel dan pH pengendapan silika mencapai 7,0.
Gel silika kemudian didiamkan (dituakan) selama 24 jam pada suhu kamar.
Selanjutnya gel silika disaring dan dicuci dengan akuades panas di dalam pompa
vakum hingga air cucian bersifat netral. Silika yang diperoleh kemudian dikeringkan
dalam oven pada suhu 110 °C selama 24 jam dan dihaluskan.
3. Pembuatan Sol Silika Sekam Padi
Sebanyak 20 gram silika sekam padi hasil ekstraksi dimasukkan ke dalam 600 mL
larutan NaOH 1,5% kemudian dipanaskan sambil diaduk menggunakan hotplate
stirer hingga larut.
4. Pembuatan Zeolit dengan Metode Elektrolisis dan Sol-Gel
Sebanyak 600 mL sol silika yang telah dibuat, diasamkan dengan larutan HNO3 10%
secara bertahap hingga pH yang telah ditentukan. Selanjutnya dimasukkan ke dalam
tabung elektrolisis untuk dielektrolisis dengan menggunakan alumunium sebagai
elektroda. Proses elektrolisis dilakukan dengan potensial 8 volt dalam variasi waktu
15, 30, 45, dan 60 menit serta variasi pH 4, 5, 6, 8, dan 10. Sol zeolit yang terbentuk
selanjutnya dikeringkan pada suhu 110 oC selama 24 jam untuk menghilangkan air.
36
5. Kalsinasi Katalis
Proses kalsinasi dilakukan dengan menggunakan furnace Lento 3508 yang dapat
disesuaikan dengan perlakuan yang diinginkan. Kalsinasi katalis zeolit yang
berbentuk serbuk dilakukan dengan suhu 300 oC dan ditahan selama 2 jam untuk
dapat memastikan apakah silika masih dalam fasa amorf dan katalis bersifat kristalin.
Berikut ini adalah langkah-langkah pengunaan furnace :
1. Sampel disiapkan.
2. Sampel dimasukkan ke dalam tungku pemanas (furnace).
3. Alat tungku dihubungkan dengan sumber tegangan, kemudian setting
alat dalam keadaan hidup atau "ON".
4. Tungku diatur (setting) sesuai dengan perlakuan pada sampel.
5. Tungku pemanas dimatikan ketika proses telah selesai.
6. Sampel dikeluarkan dari tungku pemanas.
Sampel dipanaskan dari suhu 25 oC hingga mencapai suhu 300 oC dengan kenaikan
suhu 5 oC/menit. Setelah mencapai suhu yang diinginkan (300 oC) suhu ditahan
selama 2 jam (120 menit). Selanjutnya alat furnace akan menghentikan pemicu
kenaikan dan penahanan suhu, kemudian secara otomatis suhu di dalam furnace akan
Untuk mengevaluasi aktivitas katalitik zeolit, dilakukan serangkaian percobaan
transesterifikasi menggunakan metode yang telah digunakan sebelumnya (Darnoko et
al., 2000; Ogawa et al., 2004; Abreua et al., 2004; Kusmiyati, 1999).
a. Pengaruh Nisbah Katalis Terhadap Minyak Kelapa
Percobaan ini dilakukan dengan menggunakan jumlah katalis sebesar 5% yang
ditambahkan ke dalam minyak kelapa dan metanol dengan perbandingan mol 1:4 dan
dilakukan pengadukan sambil direfluks dengan suhu 70 oC selama 120 menit.
Parameter keberhasilan reaksi adalah rendemen produk yang dihasilkan.
b. Pengaruh Waktu
Percobaan ini dilakukan dengan waktu yang berbeda, yakni selama 30, 60, 90 dan
120 menit, untuk mendapatkan waktu terbaik.
c. Analisis Biodiesel
Untuk menguji kelayakan biodiesel sebagai bahan bakar aplikasi, sampel yang sama
juga dianalisis untuk menentukan parameter teknis meliputi flash point, cetane
38
1. Analisis Flash Point Biodiesel
Langkah-langkah untuk analisis flash point biodiesel adalah sebagai berikut :
1. Sampel dimasukkan ke dalam mangkok uji hingga garis batas pengujian
2. Suhu sampel dan mangkok uji diatur sekitar 18 0C di bawah kisaran perkiraan
suhu flash point sampel
3. Mangkok uji ditutup
4. Cahaya nyala dihidupkan dan diatur intensitasnya (kenaikan suhu diatur
sebesar 5 - 6 oC/menit dan sampel diaduk dengan menggunakan alat pengaduk
pada kecepatan 90 – 120 rpm)
5. Pengadukan dihentikan dan gas pembakar ditambahkan dengan
mengoperasikan penutup mangkok uji.
2. Analisis Viskositas Biodiesel
Viskositas diukur dengan menggunakan viskometer Oswald di bawah pengaruh
gravitasi pada suhu yang telah ditentukan. Langkah-langkah untuk analisis viskositas
biodiesel adalah sebagai berikut :
1. Sampel disaring dengan filter berukuran 75 m
2. Viskometer diisi dengan contoh lalu diletakkan di dalam bak (suhu bak
viskometer dinaikkan pada 15-100 oC hingga diperoleh kisaran waktu 30
ketinggian sampel dengan kapiler disesuaikan dengan menggunakan pompa
hisap hingga melebihi sedikit garis batas (m)
4. Sampel dibiarkan turun serta dihitung waktu sampai tanda batas (n) (waktu
yang diukur adalah waktu miniskus untuk melewati waktu dari sasaran
pertama (m) menuju waktu sasaran kedua (n).
40
Pengukuran dilakukan dua kali. Nilai viskositas kemudian dihitung dengan
rumus :
= C x t
Keterangan :
μ viskositas kinematik (mm2/s)
C : konstanta kalibrasi viskometer (mm2/s2)
t : waktu alir sampel dari batas atas ke batas bawah (s)
3. Analisis Densitas Biodiesel
Prinsip kerja dari penentuan densitas adalah perbandingan massa contoh tanpa udara
pada suhu dan volume tertentu dengan massa air pada suhu dan volume yang sama.
Langkah-langkah untuk analisis densitas biodiesel adalah sebagai berikut :
1. Piknometer kosong dikeringkan di dalam oven kemudian ditimbang terlebih
dahulu
2. Lalu piknometer diisi dengan aquadest suhu 20 oC kemudian disimpan dalam
water bath pada suhu 25 oC selama 30 menit
3. Piknometer kemudian diangkat, dikeringkan, dan ditimbang (berat akuades
diperoleh dari selisih berat piknometer berisi akuades dan berat piknometer
kosong)
dibersihkan dan dikeringkan hingga meluap dan tidak terbentuk gelembung
udara
6. Bagian luar piknometer dikeringkan dan piknometer ditempatkan di dalam
water bath pada suhu konstan 25 oC selama 30 menit
7. Piknometer diangkat dari water bath lalu dikeringkan, dan ditimbang (berat
sampel diperoleh dengan menghitung selisih berat piknometer berisi sampel
dan berat piknometer kosong)
Densitas dihitung dengan rumus :
Densitas =
x ρair
Keterangan :
W1 : berat sampel (g)
W2 : berat aquadest (g)
ρair : densitas air (g/mL)
4. Analisis Gas Chromathography-Mass Spectroscopy (GC-MS)
Produk yang dihasilkan dari kondisi optimum reaksi transesterifikasi minyak kelapa
dianalisis dengan menggunakan GasChromathography-Mass Spectroscopy
(GC-MS). Analisis ini dilakukan untuk mengidentifikasi komponen dalam produk, dan
42
nabati mampu diubah menjadi mono ester. Adapun langkah-langkah penggunaan
GC-MS sebagai berikut:
1. Transformator/power supply dinyalakan, kemudian tombol “on” ditekan pada
alat GC-MS, berturut-turut untuk power pada Ion Gauge (I.G.), MS, dan GC.
Gas He dialirkan, dan dihidupkan pula komputer, monitor, dan printer.
2. dipilih menu Class-5000, klik vacuum control, dan auto start up dijalankan.
3. GC-MS monitor diaktifkan, set temperatur injector, kolom, dan detector.
Kemudian ditunggu hingga tekanan vakum di bawah 5 kPa
4. Tuning diaktifkan, diklik auto tune, load method yang akan digunakan,
kemudian diklik start dan ditunggu beberapa saat sampai hasilnya diprint-out,
setelah selesai diklik close tuning
5. Method development diaktifkan, set GC parameter, set MS parameter, save
method yang telah dideskripsikan, kemudian diklik exit.
6. Real Time Analysis diaktifkan, dipilih single sample parameter, kemudian
diisi dengan deskripsi yang diinginkan
7. Dilakukan Send Parameter. ditunggu sampai GC dan MS ready, kemudian
dilakukan injeksi sampel.
8. ditunggu sampai analisa selesai
9. Post Run Analysis diaktifkan, kemudian dipilih Browser untuk analisis sampel
secara kualitatif.
10.Dilakukan pengaturan peak top comment (peak label), dan reintegrasiLoad
file yang dianalisa. Kemudian dipilih display spectrum search pada peak
didinginkan sampai temperatur ruangan (30 oC). Bila sudah tercapai, vacum control
diklik dan dilakukan auto shut down. Perangkat alat dimatikan dengan urutan :
komputer, GC, MS, IG, dan gas He.
7. Karakterisasi Katalis
a. Karakterisasi dengan XRD (X-Ray Diffraction)
Karakterisasi dengan XRD dilakukan untuk menganalisis pengaruh suhu kalsinasi
terhadap struktur kristalografi sampel zeolit, apakah sampel bersifat amorf atau
kristalin. Sumber sinar radiasi menggunakan Kα dari Cu. Langkah-langkah yang
dilakukan dalam analisis menggunakan XRD adalah sebagai berikut:
1. Sampel yang akan dianalisis disiapkan dan direkatkan pada kaca,
kemudian dipasang pada tempatnya yang berupa lempeng tipis berbentuk
persegi panjang (sampel holder) dengan bantuan malam (lilin perekat).
2. Sampel yang disimpan dipasang pada sampel holder kemudian dilekatkan
pada sampel stand dibagian goniometer.
3. Parameter pengukuran dimasukkan pada software pengukuran melalui
komputer pengontrol, yaitu meliputi penentuan scan mode, penentuan
rentang sudut, kecepatan scan cuplikan, memberi nama cuplikan dan
44
4. Alat difraktometer dioperasikan dengan perintah “Start” pada menu
komputer, dimana sinar-X akan meradiasi sampel yang terpancar dari
target Cu dengan panjang gelombang 1,5406 Å.
5. Hasil difraksi dapat dilihat pada komputer dan intensitas difraksi pada
sudut 2 tertentu dapat dicetak oleh mesin printer.
6. Sampel dari sampel holder diambil setelah pengukuran cuplikan selesai.
b. Karakterisasi dengan SEM-EDX (Scanning Electron Microscopy-Energy Dispersive X-ray Spektrometer)
Analisis menggunakan SEM dilakukan untuk mengetahui morfologi permukaan
sampel dan ukuran partikel. Analisis menggunakan SEM-EDX ini dilakukan pada
semua sampel zeolit yang dihasilkan. Adapun langkah-langkah dalam uji SEM-EDX
ini adalah sebagai berikut:
1. Sampel yang akan dianalisis disiapkan dan direkatkan pada spesimen
holder (Dolite, double sticy tape).
2. Sampel yang telah dipasang pada holder kemudian dibersihkan dengan
Hand Blower.
3. Sampel dimasukkan dalam mesin couting untuk diberi lapisan tipis yang
berupa gold-poladium selama 4 menit sehingga menghasilkan lapisan
dengan ketebalan 200-400 Å.
mengatur pembesaran yang diinginkan.
6. Penentuan spot untuk analisis pada layer SEM-EDX.
7. Pemotretan gambar SEM-EDX.
c. Karakterisasi dengan BET (Brunauer-Emmett-Teller)
Untuk mengetahui luas permukaan spesifik, volume total pori, dan rata-rata jari-jari
pori sampel silika (kontrol) dan sampel katalis logam-silika yang mempunyai
aktivitas terbaik dalam reaksi esterifikasi maka dilakukan analisis menggunakan
BET. Langkah-langkah kerjanya adalah sebagai berikut :
1. Tombol pemilih adsorbat dipastikan pada arah tank.
2. Gas nitrogen dari tabung dialirkan dengan memutar (berlawanan arah
jarum jam) kran tabung gas.
3. Listrik dihidupkan dengan menghidupkan stabilizer.
4. Pompa vakum dihidupkan dengan menekan tombol merah pada magnetik
kontaktor.
5. Power alat (NOVA-1000) dihidupkan, kemudian ditunggu sampai muncul
menu utama pada layar LCD.
6. Pengukuran yang diinginkan dilakukan dengan mengikuti menu program