ABSTRAK
PENGEMBANGAN ZEOLIT SINTETIK BERBASIS SILIKA SEKAM PADI SECARA ELEKTROKIMIA SEBAGAI KATALIS UNTUK
PENGOLAHAN MINYAK NABATI MENJADI BIODIESEL
Oleh
LAILA SUSANTI
Dalampenelitian ini, telah disintesis prekusorzeolitdarisilikasekam padidanlogamaluminiummenggunakan metodeelektrokimia dengan variasipHdanpotensial yang kemudiandiuji sebagai katalis dalam reaksi transesterifikasiminyak kelapa dan minyak jarak. Katalis dengan unjuk kerja terbaik dalam transesterifikasi minyak kelapa yakni prekusor zeolit yang disintesis pada pH 10 dan potensial 8 volt (prek-zeo10:8) suhu kalsinasi 300 oC menghasilkan morfologi permukaan yang homogen dengan distribusi ukuran partikel 172-252,6 nm, biodiesel diperoleh persen konversi 94% dan dianalisis dengan GC-MS terbentuk metil ester dengan komponen tertinggi metil laurat. Katalis dengan unjuk kerja terbaik dalam transesterifikasi minyak jarak yakni prekusor zeolit yang disintesis pada pH 10 dan potensial 10 volt (prek-zeo10:10) suhu kalsinasi 500 oC menghasilkan morfologi permukaan relatif tidak homogen dengan distribusi ukuran partikel 901,9-1399,7 nm, biodiesel diperoleh dengan persen konversi 98% dianalisis dengan GC-MS terbentuk metil ester dengan komponen tertinggi metil ricinoleat. Kedua jenis biodiesel yang dihasilkan memenuhi standar SNI 04-7182-2006 untuk nilai viskositas, titik nyala dan massa jenis. Data XRD menunjukkan bahwa prek-zeo10:8 suhu kalsinasi 300 oC mempunyai fasa albite dan nepheline. Katalis prek-zeo10:10 suhu kalsinasi 500 oC mempunyai fasa albite.
ABSTRACT
DEVELOPMENT
OFSYNTHETICZEOLITESILICAFROMRICEHUSKSILICA USINGELECTROCHEMICAL METHODASA
CATALYSTFORPROCESSINGOF VEGETABLE OILTO BIODIESEL
By
LAILA SUSANTI
In this study, a series of synthetic zeolites synthesized from rice husk silica and aluminum metal using an electrochemical method was tested with the potential variations in pH and then tested for transesterification of coconut oil and castor oil. Catalysts with different Si/Al ratios were prepared through application of different pHs and potentials, and the catalysts were subjected to calcination treatments at 300 and 500 oC before use. The results of transesterification experiments revealed that the best catalyst for transesterification of coconut oil was the catalyst prepared at pH 10 and potential 8 volt, calcined at 300 oC, with the yield of 94%. For castor oil, the best catalysts was that prepared at pH 10 and potential 10 volt, calcined at 500 oC, with the yield of 98%. The conversion of fatty acids in oils into coresponding methyl esters were confirmed using GC-MS method. Characterizations of the best catalysts for transesterification of coconut oil indicate the particle size distribution from 172 to 252.6 nm, and from 901.9 to 1399.7 nm for the best catalyst for ransterification of castor oil. The XRD data showed the presence of albite and nepheline phases.
PENGEMBANGAN ZEOLIT SINTETIK BERBASIS SILIKA SEKAM PADI SECARA ELEKTROKIMIA SEBAGAI KATALIS UNTUK
PENGOLAHAN MINYAK NABATI MENJADI BIODIESEL
Oleh Laila Susanti
TESIS
Diajukan Sebagai Salah Satu Syarat Untuk Memperoleh Gelar Magister Sains
Program Pasca Sarjana Magister Kimia
Fakultas Matematika dan Ilmu Pengetahuan Alam
Universitas Lampung
Bandar Lampung
RIWAYAT HIDUP
Penulis dilahirkan di Jakarta pada tanggal 27 Agustus 1980 dan merupakan anak ke dua dari tiga bersaudara.dari Bapak H. Marisidi dan Ibu Hj. Marisah. Penulis menyelesaikan pendidikan dasar di SDN Tri Rawa Bakti 1 tahun 1992, kemudian melanjutkan pendidikan tingkat menengah di SMP N 4 Bekasi hingga tahun 1995. Kemudian penulis melanjutkan pendidikan tingkat atas di SMK Analis Kimia Caraka Nusantara, Jakarta (program studi : 4 tahun) hingga 1999. Pada tahun yang sama penulis diterima sebagai mahasiswa Jurusan Kimia FMIPA Universitas Lampung melalui jalur Ujian Masuk Perguruan Tinggi Negeri (UMPTN). Pada tahun 2013 penulis terdaftar sebagai mahasiswa program studi Magister Kimia FMIPA Universitas Lampung.
Ku Persembahkan Hasil Karya ini Teruntuk yang
Tercinta :
1.
Orang Tua ku Bpk H. Marsidi dan Ibu Hj.
Marisah atas segala cinta, doa dan
dukungannya dari buaian hingga saat ini.
2.
Suamiku Dimyati, S.Si atas semua cinta,
doa, nasehat, dukungan moril dan materil.
Love you cause Alloh SWT.
3.
Anak-anakku Musyaffa Mumtaz
Ramadhan dan Muhammad Arkan Danish,
lihatlah bundamu yang tak pernah berhenti
belajar, begitu juga kalian, raih masa
depan cemerlang kalian, doa Ayah Bunda
selalu menyertai.
27 Juni 2015
Dihargai atau tidak oleh manusia,
Dipandang atau tidak oleh manusia,
Janganlah kita merasa bangga atau
khawatir...
Karenaseharusnya kita patut malu dan
khawatir karena ada sang
Al-Khaliq
disana yang menilai kadar
keikhlasan dan kesungguhan atas
setiap hal yang kita kerjakan....
Maka, tetap teruslah bergerak,
teruslah menghasilkan karya, dan tak
lupa selipkan hati ikhlas dan
sungguh-sungguh di dalamnya...
SANWACANA
Alhamdulillahirabbil ‘alamin, segala puji bagi Allah, Tuhan semesta alam yang
selalu melimpahkan rahmat, hidayah dan kasih sayang yang tak terhingga sehingga penulis dapat menyelesaikan tesis yang berjudul
PENGEMBANGAN ZEOLIT SINTETIK BERBASIS SILIKA SEKAM PADI SECARA ELEKTROKIMIA SEBAGAI KATALIS UNTUK
PENGOLAHAN MINYAK NABATI MENJADI BIODIESEL
Shalawat dan salam penulis haturkan kepada manusia terbaik suri tauladan umat Rasulullah SAW beserta keluarga dan sahabat serta umatnya yang selalu istiqomah di jalan-NYA semoga dipertemukan kelak di yaumil akhir, Aamin.
Dengan segala kerendahan hati, izinkanlah penulis menyampaikan terima kasih yang sebesar-besarnya kepada :
1. Bapak Prof. Wasinton Simanjuntak, Ph.D. selaku pembimbing I dan Pembimbing Akademik atas dedikasi yang luar biasa dalam memberikan saran dan ide selama penelitian berlangsung, memberikan pointer dan petunjuk tata bahasa dalam penulisan tesis disemua bab, serta memberikan motivasi untuk segera menyelesaikan penelitian dan tesis.
PSAdan memberikan pointer-pointer pada bab IV yang berguna untuk memperbaiki hasil penelitian di tesis saya.
3. Bapak Dr. Rudy TM Situmeang, M.Sc. selaku Pembahas atas semua kritik dan saran terhadap kaidah penulisan dan substansi tesis ini, demi menjadikan tesis ini lebih baik lagi.
4. Bapak Prof. Sutopo Hadi, Ph.D. selaku ketua Program Studi Magister Kimia yang telah sabar memberikan informasi, layanan akademik dan arahan kepada mahasiswa Magister Kimia.
5. Bapak Dr. Eng. Suripto Dwi Yuwono, M.T. selaku Ketua Jurusan Kimia FMIPA yang telah memberikan fasilitas akademik selama penulis menempuh perkuliahan dan penelitian.
6. Bapak Prof. Suharso, Ph.D. selaku Dekan FMIPA yang telah memberikan fasilitas akademik selama penulis menempuh perkuliahan dan penelitian. 7. Bapak Prof. John Hendri, Ph.D dan Bunda Aspita Laila, M.Si, terimakasih
atas perhatiannya yang selalu menanyakan “kapan sidang?” meskipun
beliau bukan pembimbing saya.
8. Kedua orang tua ku tersayang, Bapak H. Marsidi dan Ibu Hj. Sumiyarsih atas seluruh cinta, do’a, dan kasih sayang kepada penulis dari masih dalam
buaian hingga saat ini. Rabighfirlii waliwalidayya warhamhuma kamma Rabbayani saghiraa. Semoga Allah tetap menjaga masa tua kalian dengan tetap istiqomah di jalan-NYA dan mengumpulkan kita di Jannah-NYA. 9. Suamiku tercinta, Dimyati, S.Si sebagai tempat curhat berbagai masalah
atas seluruh cinta, do’a, dukungan, kesabaran, motivasi, nasihat, yang
Semoga Allah tetap menjaga cinta kita dan menjodohkan kita kembali di Jannah-NYA.
10.Anak-anakku tersayang, „guru-guru kecil’ kami Musyaffa Mumtaz Ramadhan dan Muhammad Arkan Danish, kalianlah amanah Allah yang selalu menjadi pembelajaran untuk kami, semoga do’a anak sholeh seperti
kalian menjadi penolong kami di akhirat kelak.
11.Mas Fajar Miyarhadi, Astri Nur Andini serta semua kakak ipar dan adik ipar, tak lupa semua keponakan-keponakan yang telah menjadi bagian keluarga besar Bapak Marsidi dan Bapak Bunyani (alm).
12.Bapak Doni Permana, S.Si, selaku Kepala Cabang Ganesha Operation Lampung, terima kasih atas motivasi dan kesempatan yang diberikan kepada penulis untuk menempuh pendidikan magister dan tetap bekerja. 13.Mbak Nora dan Pak Gani, terima kasih atas kemudahan dan kelancaran
yang diberikan dalam pengurusan administrasi akademik.
14.Uni Noor dan Mbak Liza selaku Laboran Kimia Dasar dan Laboran Kimia An Organik-Fisik, terima kasih atas kemudahan dan kelancaran yang diberikan dalam pengurusan peminjaman alat-alat laboratorium.
15.Ibu Nurhasanah, M.Si, Ibu Dr. Dian Herasari dan Ibu Kamisah D Pandingan, M.Si yang telah membantu karakterisasi sampel.
16.Teman satu tim ku : jeng Rina Mediasari, S.Pd. terima kasih atas kerja sama selama penelitian yang dimulai dari nol sampai selesai sehingga dapat terkumpul cerita dengan judul „Suka Duka Wanita Bekerja, Ibu
17.Teman-teman satu peer grup kimia fisik : Tutik, S.Si., Rodhiansyah, S.Si., Iip Sugiharta, S.T., Septian Dwi S.Si., Raffel Stevano, S.Si, terima kasih atas kerja sama yang saling memotivasi, keceriaan dan keriangan selama perkuliahan.
18.Teman-teman program studi Magister Kimia angkatan 2013 kelas A dan B, serta angkatan 2014, terima kasih telah memberikan pengalaman-pengalaman hebat, berkumpul dengan mereka telah memberikan wawasan baru akan arti sebuah perjuangan, senang telah mengenal Bapak dan Ibu semua.
19.Teman-teman laboratorium Kimia Polimer : Faradilla Syani, S.Si., Hanif Amrullah, S.Si, Funda Elisya, S.Si., Leni Astuti, S.Si., Tata, Gege, Lusi, Vevi, Umi, Debo, Rully, Ferdinand dan lain-lain yang telah membantu penulis selama penelitian.
20.Semua pihak yang telah membantu dan tidak bisa disebutkan satu persatu, semoga Allah memberikan balasan yang baik atas kebaikan yang diberikan kepada penulis.
Penulis menyadari bahwa laporan tesis ini masih terdapat banyak kekurangan, namun penulis berharap penelitian ini dapat bermanfaat dan bisa dilanjutkan untuk kajian baru yang lebih mutakhir, sehingga ilmu ini selalu akan berkembang hingga akhir zaman.
Bandar Lampung, Juni 2015
i
3. Reaksi Pembuatan Biodiesel ... 14
B. Katalis Reaksi Transesterifikasi … ... 19
D. Karakterisasi Katalis Zeolit ... 36
1. SEM/EDS ... 36
ii
3. XRD ... 38
E. Karakterisasi Biodiesel ... 41
1. Uji Kelayakan Biodiesel ... 41
4. Pembuatan Prekusor Zeolit Dengan Metode Elektrokimia ... 46
5. Kalsinasi Katalis ... 47
6. Seleksi Katalis Pada Reaksi Transesterifikasi ... 48
7. Analisis Produk Transesterifikasi (Biodiesel) ... 49
8. Karakterisasi Katalis ... 51
a. Karakterisasi Dengan SEM/EDS ... 51
b. Karakterisasi Dengan PSA ... 52
c. Karakterisasi Dengan XRD ... 52
IV. HASIL DAN PEMBAHASAN ... 54
A.Pengantar ... 54
B. Ekstraksi Silika Sekam Padi ... 55
C.Preparasi Prekusor Zeolit Sintetik ... 57
D.Uji Aktivitas Katalis Prekusor Zeolit Sintetik ... 60
1. Transesterifikasi Minyak Kelapa ... 61
2. Transesterifikasi Minyak Jarak ... 64
E. Analisis Biodiesel ... 69
1. Analisis GC-MS Hasil Transesterifikasi Minyak Kelapa ... 69
2. Analisis GC-MS Hasil Transesterifikasi Minyak Jarak ... 76
3. Kualitas Biodiesel ... 82
F. Karakterisasi Katalis ... 83
1. Analisis Mikrostruktur dan Distribusi Ukuran Partikel ... 83
iii 1.2 Analisis SEM-EDS Katalis Transesterifikasi Minyak
Jarak ... 86
1.3 Analisis Dengan PSA ... 89
2. Karakterisasi Dengan XRD ... 92
2.1 Analisis XRD Katalis Transesterifikasi Minyak Kelapa ... 93
2.2 Analisis XRD Katalis Transesterifikasi Minyak Jarak ... 96
V. SIMPULAN DAN SARAN ... 100
A. Simpulan ... 100
B. Saran ... 102
iv
7. Massa prekusor zeolit yang dihasilkan dari percobaan dengan pH dan potensial (E) yang berbeda ... 59
8. Massa jenis, viskositas, dan % konversi hasil transesterifikasi Minyak kelapa dengan katalis prekusor zeolit pH 10 suhu kalsinasi 300 oC ... 63
9. Massa jenis, viskositas dan % konversi hasil transesterifikasi 50 mL Minyak jarak dengan volume koreaktan 10 mL, katalis prekusor zeolit pH 10 suhu kalsinasi 500 oC ... 67
10. Massa jenis, viskositas dan % konversi hasil transesterifikasi minyak jarak dengan variasi koreaktan, katalis zeolit pH 10 dan potensial 10 volt suhu kalsinasi 500oC (prek-zeo10:10 suhu 500 oC) ... 67
11. Profil biodiesel hasil transesterifikasi minyak kelapa dengan katalis prek-zeo10:4 suhu kalsinasi 300 oC ... 70
12. Profil biodiesel hasil transesterifikasi minyak kelapa dengan katalis prek-zeo10:8 suhu kalsinasi 300oC ... 71
v
14. Profil komponen senyawa hasil transesterifikasi minyak jarak variasi koreaktan 20 mL dengan katalis prek-zeo10:10 suhu kalsinasi
500 oC ... 78 15. Karakteristik biodiesel hasil transesterifikasi minyak kelapa dan
minyak jarak dengan katalis terbaik... 83 16. Komposisi prekusor zeolit sintetik pH 10 suhu kalsinasi 500 oC berdasarkan spektra EDS ... 88
17. Profil distribusi ukuran partikel zeolit pH 10 suhu kalsinasi
500 oC yang dihasilkan dengan potensial yang berbeda ... 91 18. Puncak-puncak representatif dari difraktogram prek-zeo10:8 suhu
kalsinasi 300 oC ... 93 19. Puncak-puncak representatif dari difraktogram referensi
I. PENDAHULUAN
A. Latar Belakang
Bertambahnya populasi manusia dan jumlah kendaraan serta perkembangan industrialisasi menyebabkan kebutuhan akan bahan bakar semakin meningkat. Hal ini menyebabkan ketersediaan bahan bakar menjadi semakin menipis, terutama bahan bakar fosil yang masih menjadi andalan saat ini. Dampak utama adalah harga bahan bakar fosil yangterus naiksehingga diperlukan terobosan baru agar ketersediaan bahan bakar dapat memenuhi berbagai kebutuhan. Masalah lain yang terkait dengan bahan bakar fosil adalah emisi gas CO2 dari hasil pembakaran yang berdampak langsung pada pemanasan global.
Dua masalah utama di atas menjadi faktor pendorong pengembangan bahan bakar alternatif dan terbarukan di seluruh dunia, termasuk di Indonesia. Dari berbagai upaya yang telah dilakukan dewasa ini telah dikenal berbagai jenis bahan bakar alternatif, salah satunya adalah biodiesel. Di Indonesia, bahan bakar alternatif ini berpeluang besar menjadi komoditas unggulan, bukan hanya untuk memenuhi kebutuhan dalam negeri tetapi menjadi komoditas ekspor sebagai sumber devisa.
2 sulfur yang bersifat karsinogen, jumlah CO2 yang dihasilkan pada pembakarannya lebih sedikit dibanding dengan bahan bakar fosil, serta memiliki angka cetane yang lebih tinggi dari minyak diesel yang dihasilkan dari industri petrokimia. Di samping itu, industri biodisel juga didukung ketersediaan bahan baku yang cukup melimpah di Indonesia, yaitu minyak nabati yang dapat diperoleh dari berbagai sumber antara lain biji bunga matahari, kedelai, biji kapas, kelapa, kelapa sawit, dan biji jarak.
Secara kimia, pembuatan biodiesel pada hakekatnya adalah reaksi transesterifikasi minyak nabati menjadi ester yang lebih sederhana dengan menggunakan alkohol, terutama metanol (Crabbe et al., 2001) dan etanol (Al-Widyan and Al-Shyoukh., 2002). Karakteristik utama reaksi transesterifikasi adalah merupakan reaksi reversibel dan kedua reaktan merupakan senyawa yang tidak reaktif, sehingga untuk mendorong reaksi ke arah produk dibutuhkan katalis.
3 ester yang sudah terbentuk akan mengalami reaksi hidrolisis, selain itu air juga mengakibatkan pembentukan sabun dan buih yang tidak hanya akan mengurangi rendemen reaksi tetapi juga akan meningkatkan viskositas, dan mempersulit pemisahan gliserol. Disamping itu, residu katalis homogen seringkali masih terdapat dalam produk, sehingga mengurangi kelayakgunaan produk karena sifat korosif asam maupun basa, dan katalis tersebut pada umumnya tidak dapat digunakan ulang.
Kelemahan katalis homogen seperti dipaparkan di atas telah mendorong pengembangan katalis heterogen. Katalis heterogen mempunyai fasa berbeda dengan reaktan, yaitu katalis berbentuk padat sedangkan reaktan pada fasa cair. Penggunaan katalis heterogen mempunyai beberapa keunggulan diantaranya, tahan terhadap reaksi bersuhu tinggi, kemudahan pemisahan katalis dari campuran reaksi, dapat digunakan ulangdan tidak korosif (Moffat, 2002; Frenzer et al., 2006).
4 tidak seragam, dan kekuatan asamnya juga sulit di kontrol.Kelemahan tersebut merupakan faktor pendorong pengembangan zeolit sintetik karena memiliki kemurnian yang tinggi dan komposisi yang sangat homogen.
Pada umumnya, zeolit sintetik diproduksi dari bahan baku berupa senyawa silika yang mudah larut dalam air misalnya tetra methyl ortho silicate(TMOS) dan tetra ethyl ortho silicate (TEOS), sedangkan senyawa alumina didapatkan dari garam aluminium terutama aluminium nitrat (Wang et al., 2010) dan aluminum klorida (Dirdianti, 2011) yang juga mudah larut dalam air. Dari bahan baku tersebut, zeolit dapat dibuat dengan metode sol-gel. Bahan baku lain yang sudah dimanfaatkan adalah berupa padatan, misalnya fume silika (Tomiyama et al., 2003; Barrault et al., 2002) dan alumino silikat (Dirdianti, 2011), untuk bahan baku ini metode yang digunakan adalah hidrotermal (Wustoni, 2011). Teknik lainnya adalah microwave, pada teknik ini gelombang elektromagnetik dengan frekuensi 300 MHz – 300 GHz dialirkan ke dalam campuran larutan aluminat dan silikat sampai terbentuk campuran yang homogen (Musthofa dan Lukman, 2010).
5 Dalam upaya menekan biaya produksi zeolit sintetik, penelitian ini digagas untuk memanfaatkan silika dari sekam padi sebagai bahan baku.Sekam padi diketahui merupakan residu pertanian yang melimpah di Indonesia, termasuk Provinsi Lampung.Sekitar 20 % sekam padi akan diperoleh dari padi yang digiling. Hasil penelitian Harsono(2002) juga menunjukkan, bahwa sekam padi mengandung silikasekitar 85-97 %.Kandungan silika dan kelimpahan yang tinggi, memberi peluang untuk dimanfaatkan sebagai sumber silika menggantikan sumber silika lain yang lebih mahal. Silika sekam padi diketahui larut dalam larutan alkali, sehingga dapat diperoleh dengan mudah menggunakan metode ekstraksi alkalis misalnya dengan NaOH dan KOH (Kalaphathy et al., 2000; Suka dkk., 2008; Daifullah et al., 2003; Pandiangan dkk., 2009).
Pada penelitian ini, zeolit sintetikdibuat dengan metode elektrokimia menggunakan batangan alumina sebagai elektrodanya. Metode ini memiliki keunggulan antara lain peralatan yang digunakan sederhana, biaya operasional alat relatif murah, bisa digunakan pada sistem alir (Yatmaz et al., 2009) dan yang paling utama adalah proses dapat dikendalikan dengan mengatur variabel elektrokimia seperti waktu dan potensial. Prinsip dasar gagasan ini adalah, elektrolisis logam alumina yang ditempatkan dalam sol silika sekam padi. Logam Al yang digunakan sebagai anoda akan teroksidasi menjadi kation Al3+, yang akan terlarutdalam sol silika.Dengan mengatur variabel potensial, pH dan waktu maka akan didapatkan zeolit sintetik dengan nisbah Si/Al yang berbeda-beda.
6 dijelaskan sebelumnya, reaksi transesterifikasi merupakan reaksi pembuatan biodiesel yang membutuhkan katalis. Katalis zeolit sintetik dengan nisbah Si/Al berbedaakan memberikan perbedaan unjuk kerja dalam reaksi transesterifikasi, sehingga akan terpilih katalis terbaik dengan nisbah Si/Al tertentu.
Beberapa peneliti menggunakan zeolit sintetik untuk uji transesterifikasi diantaranya adalah Santoso dkk (2012) melakukan sintesis katalis zeolit dari sekam padi dengan metode sol gel yang digunakan untuk uji transesterifikasi minyak biji kapuk diperoleh rendemen metil ester sebesar 21,94 %. Wirasito dkk (2014) melakukan sintesis katalis zeolit termodifikasi abu tandan kosong kelapa sawit untuk uji transesterifikasi minyak goreng bekas dengan diperoleh rendemen metil ester sebesar 91,58%.
Terkait dengan pembuatan zeolit sintetik secara elektrokimia untuk reaksi transesterifikasi, Syani (2014) melakukan sintesis zeolit dari sekam padi secara elektrokimia sebagai katalis untuk reaksi transesterifikasi minyak kelapa, diperoleh rendemen metil ester sebesar 100%. Liani (2014) mensintesis alumina dengan metode elektrokimia yang digunakan sebagai bahan baku zeolit sintetik faujasit dengan metode hidrotermal.
7 menjadi ester dengan GC-MS, yang tujuannya adalah untuk mengidentifikasi jenis ester yang terbentuk, serta uji biodiesel umum seperti viskositas, berat jenis dan flash point.
Sesuai dengan latar belakang yang dipaparkan diatas, masalah utama yang akan dipelajari dalam penelitian ini adalah bagaimana pengaruh potensial, waktu dan pH terhadap nisbah Si/Al zeolit sintetik yang dihasilkan dan bagaimana hubungan komposisi ini dengan unjuk kerja zeolit sebagai katalis transesterifikasi. Dari rangkaian percobaan yang akan dilakukan, diharapkan akan diperoleh zeolit sintetik dengan unjuk kerja yang baik sebagai katalis transesterifikasi, dan berpeluang untuk dikembangkan sebagai katalis aplikasi hingga ke skala yang lebih besar.
B.TUJUAN PENELITIAN
Berdasarkan latar belakang yang telah dipaparkan diatas, berikut ini beberapa tujuan spesifik dari penelitian ini antara lain :
1. Mensintesis zeolit melalui penerapan potensial dan pH yang berbeda, sehingga akan dihasilkan nisbah Si/Al yang berbeda-beda.
2. Menguji aktivitas zeolit sebagai katalis untuk reaksi transesterifikasi minyak kelapa dan minyak jarak untuk mendapatkan katalis dengan unjuk kerja terbaik.
8 antara karakteristik dengan unjuk kerja zeolit sebagai katalis reaksi transesterifikasi.
4. Menentukan jenis zeolit sintetik yang memberikan unjuk kerja terbaik melalui karakterisasi SEM-EDS dan XRD
5. Mengkarakterisasi biodiesel yang dihasilkandengan GC-MS, viskositas, massa jenis dan flash pointuntuk melihat kelayakannya sebagai bahan bakar.
C. MANFAAT PENELITIAN
Penelitian ini diharapkan dapat memberikan manfaat sebagai berikut :
1. Meningkatkan pemanfaatan silika sekam padi, untuk perolehan nilai tambah dari sektor pertanian
2. Memberikan informasi pembuatan zeolit sintetik dengan metoda baru, yaitu metoda elektrokimia
3. Memberikan informasi ilmiah tentang jenis katalis zeolit sintetik yang yang efektif dalam pembuatan biodiesel.
9
II. TINJAUAN PUSTAKA
A. Biodiesel
1. Sifat Umum Biodiesel
Biodiesel merupakan bahan bakar terbarukan yang dapat digunakan untuk menggantikan bahan bakar diesel yang berasal dari minyak bumi.Secara kimia, biodiesel merupakan alkil ester asam lemak yang dapat dibuat dengan rangkaian reaksi esterifikasi dan transesterifikasi asam lemak yang bersumber dari minyak nabati maupun minyak hewani.
Biodiesel merupakan cairan dengan warna yang bervariasi antara kuning keemasan hingga coklat gelap tergantung dari bahan baku yang digunakan. Biodiesel tidak dapat bercampur dengan air. Memiliki titik didih tinggi dan dan titik uap yang rendah. Titik pembakaran biodiesel (>130 °C) sangat signifikan lebih tinggi dari petrodiesel (64 °C) atau premium (−45 °C).Biodiesel memiliki kerapatan ~ 0.88 g/cm³ lebih rendah dari air.
10
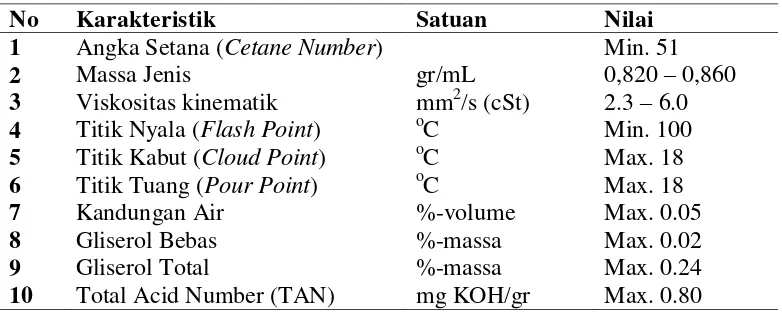
dieselstandar, tidak beracun dan dapat dibiodegradasi.Untuk penggunaannya, biodiesel harus memenuhi sejumlah parameter teknis, dan di Indonesia diatur dalam Standar Nasional Indonesia (SNI) nomor 04-7182-2006 seperti dicantumkan dalam Tabel 1.
Tabel 1. SNI biodiesel
No Karakteristik Satuan Nilai
1 Angka Setana (Cetane Number) Min. 51 Sumber : Standard Nasional Indonesia (SNI), 2006
Saat ini biodiesel telah dikembangkan secara luas karena semakin terbatasnya persediaan minyak bumi seiring meningkatnya jumlah kendaraan dan aktifitas industrialisasi.Penggunaan biodiesel sangat menguntungkan karena terbuat dari bahan bakuyang mudah terbaharui dan mudah didapatkan di Indonesia.
2. Bahan Baku Biodiesel
11
misalnya minyak goreng bekas (waste cooking oils) (Baharta, 2006). Lemak hewani juga dapat diolah menjadi biodiesel, namun untuk skala industri terkendala oleh kesulitan mendapatkan bahan baku yang cukup.
Tabel 2 di bawah ini menunjukkan berbagai macam tanaman penghasil minyak nabati yang dapat dimanfaatkan sebagai bahan baku pembuatan biodiesel.
Tabel 2. Berbagai macam tanaman penghasil minyak nabati Nama Indonesia Nama Latin
Sawit Elais guinensis
Kelapa Cocos nucifra
Alpukat Persea americana
Jarak Kaliki Ricinus communis
Jojoba Simmondsia califor
Zaitun Olea europea
Kanola Brassica napus
Sumber : Soerawidjaja, 2006
12
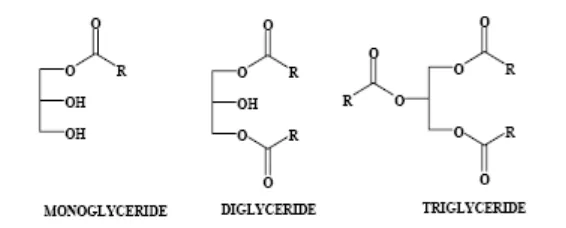
Gambar 1. Struktur molekul monogliserida, digliserida dan trigliserida
Trigliserida adalah ester dari tiga asam lemak rantai panjang (C8 sampai dengan C22) yang terikat pada satu gugus gliserol, dan merupakan komponen terbesar penyusun minyak nabati dengan kadar 90-98%.
2.1 Minyak Kelapa
Buah kelapa (Cocos nucifera) merupakan sumber minyak nabati yang sangat potensial dan terdapat di seluruh daerah Indonesia. Selain mempunyai kandungan minyak yang tinggi, buah kelapa juga sangat mudah diolah untuk memisahkan minyak dari daging buah.Komponen penyusun minyak kelapa disajikan dalam Tabel 3.
Tabel 3.Kandungan asam lemak minyak kelapa
Sumber : Tambun, 2006
Asam Lemak Rumus Kimia Jumlah (%)
Asam laurat C11H23COOH 44,0 – 52,0
Asam miristat C13H27COOH 13,2 – 19,0
Asam palmitat C15H31COOH 7,5 – 10
Asam Kaprilat C7H15COOH 5,5 – 9,5
Asam oleat C17H33COOH 5,0 – 8,0
Asam kaprat C9H19COOH 4,5 – 9,5
Asam linoleat C17H31COOH 1,5 – 2,5
13
Dari Tabel 3terlihat bahwa komponen utama dalam minyak kelapa adalah asam laurat dan asam miristat. Beberapa peneliti telah mengembangkan minyak kelapa sebagai bahan baku biodiesel, diantaranya Alamu et al., (2010) menggunakan 100 gram minyak kelapa menghasilkan persen konversi sebesar 10,4%. Peneliti lain Velasquezet al., (2009) melaporkan dengan persen konversi sebesar91,5-95,7 % dan Syani (2014) mendapatkan persen konversi minyak sebesar 100%.
2.2Minyak Jarak
Kandungan minyak pada biji jarak cukup tinggi yaitu sekitar 30-50% dan sangat potensial untuk dimanfaatkan sebagai bahan baku biodiesel karena minyak jarak pagar tidak termasuk kategori minyak untuk makanan (edible oil) sehingga tidak menganggu ketersediaan kebutuhan minyak pangan. Berikut komposisi asam lemak pada minyak jarak disajikan dalam tabel di bawah ini.
Tabel 4. Kandungan asam lemak minyak jarak
Asam lemak Rumus Kimia Jumlah (%)
Asam Ricinoleat C17H33COOH 35 – 64
Asam Linoleat C17H31COOH 19 – 42
Asam Palmitat C15H31COOH 12 – 17
Asam Stearat C17H35COOH 5 – 10
Asam Linolenat C17H32COOH 2 – 4
Sumber : Sudrajat R, 2006
14
biodiesel dengan persen konversi sebanyak 93% dan Endalew et al., (2011) melaporkan persen konversi sebanyak 66,4%.
3. Reaksi Pembuatan Biodiesel
Pembuatan biodiesel umumnya menggunakan 2 tahap yakni reaksi esterifikasi dan transesterifikasi dengan bantuan katalis asam maupun basa. Kedua proses reaksi ini dapat mengkonversi asam lemak bebas menjadi biodiesel berupa metil ester (Crabbe et al., 2001) ataupun etil ester (Al-Widyan and Al-Shyoukh, 2002) tergantung dari jenis alkohol yang digunakan (metanol atau etanol).
Proses reaksi esterifikasi adalah reaksi reversibel dimana asam lemak bebas (free fatty acid/FFA) dikonversi menjadi alkil ester melalui katalis asam (HCl atau H2SO4).Esterifikasi umumnya dilakukan untuk membuat biodiesel dari minyak
berkadar FFA tinggi (angka asam 5 mg-KOH/g). Pada tahap ini, asam lemak
bebas akan dikonversikan menjadi metil ester. Reaksi esterifikasi dapat dilihat pada reaksi berikut :
R-COOH + R-OH R-COO-R’ + H2O
15
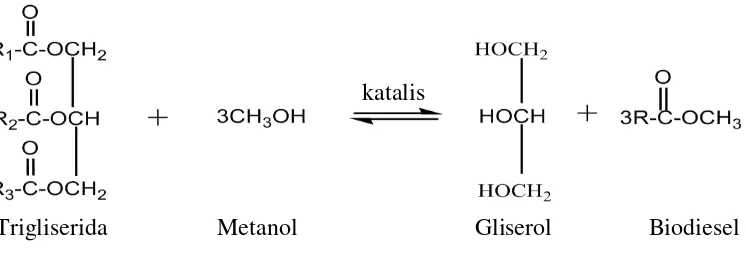
Gambar 2. Reaksi Transesterifikasi
Untuk mengolah minyak nabati menjadi biodiesel, ada beberapa faktor yang harus diperhatikan diantaranya adalah reaksi minyak nabati (trigliserida) dan alkohol merupakan reaksi yang tidak reaktif satu terhadap lainnya, sehingga katalis menjadi kebutuhan mutlak karena tanpa katalis reaksi membutuhkan suhu hingga 250°C. Dengan penggunaan katalis, suhu reaksi dapat diturunkan secara
signifikan hingga kisaran 65-75°C tergantung dari jenis minyak dan katalis yang
digunakan (Darnoko and Cheryan, 2000; Al-Widyan and Al-Shyoukh, 2002; Dermibas, 2003).
Faktor kedua adalah reaksi transesterifikasi merupakan reaksi kesetimbangan, sehingga untuk mendorong reaksi ke arah produk diperlukan alkohol berlebih. Berdasarkan stoikiometri reaksi, proses transesterifikasi memerlukan 3 mol alkohol untuk setiap mol trigliserida supaya menghasilkan 3 mol biodiesel dan 1 mol gliserol. Namun pada beberapa penelitian, perbandingan mol trigliserida dan alkohol tidak selalu 1 :3. Sebagai contoh, Darnoko dan Cheryan (2000) menggunakan perbandingan 1 : 6 untuk transesterifikasi minyak kelapa, Padmaningsih dkk (2006) menggunakan perbandingan 1 : 12 untuk transesterifikasi minyak goreng bekas.
katalis
16
Faktor ketiga adalah laju reaksi transesterifikasi dipengaruhi oleh panjang rantai hidrokarbon dan posisi gugus hidroksil dalam molekul alkohol. Laju reaksi diketahui menurun secara signifikan dengan pertambahan panjang rantai karbon. Sifat inilah yang menjadi alasan penggunaan metanol dan etanol sebagai alkohol utama dalam industri biodiesel. Penggunaan kedua jenis alkohol tersebut juga didukung keberadaannya sebagai alkohol primer yang jauh lebih reaktif dibanding alkohol sekunder dan tersier. Selain dipengaruhi jenis alkohol, laju reaksi transesterifikasi juga dipengaruhi oleh suhu dan waktu. Seperti telah diketahui, kenaikan suhu akan meningkatkan laju reaksi secara umum.
Waktu reaksi juga merupakan variabel penting suatu reaksi karena untuk memberikan kesempatan reaktan untuk bertumbukan satu sama lain. Namun demikian pada reaksi transesterifikasi pengaruh suhu dapat disesuaikan dengan sifat reaktan yang digunakan dan pengaruh waktu juga tidak mempengaruhi jika kesetimbangan reaksi telah dicapai. Sebagai contoh hasil penelitian sebelumnya Liu et al (2008) menunjukkan suhu efektif untuk transesterifikasi minyak kedelai adalah 65°C dengan persen konversi 95% dengan waktu reaksi selama 3 jam. Zhu
et al(2006) melakukan transesterifikasi minyak jarak pada suhu efektif 70°C
selama 2,5 jam dengan persen konversi sebesar 93%. Suhu reaksi 70°C juga
digunakan dalam transesterifikasi minyak sawit bekas pakai yang dilakukan oleh Padmaningsih dkk (2006) dengan persen konversi 76,76%.
17
tersebut, reaksi transesterfikasi harus dilangsungkan menggunakan alkohol absolut serta asam pekat atau basa dalam bentuk kristal sebagai katalis.
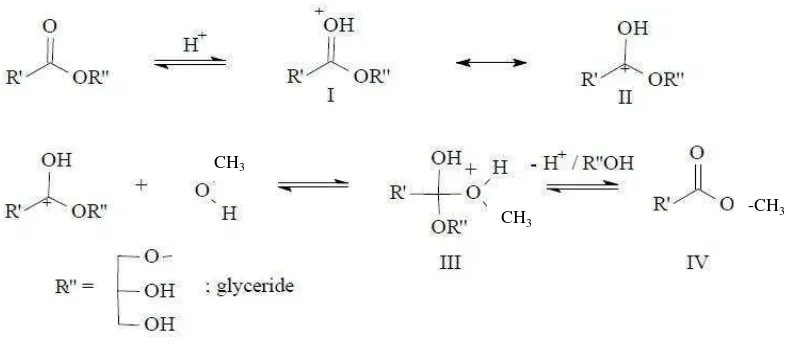
Secara garis besar, reaksi transesterifikasi minyak nabati dengan metanol menggunakan katalis asam disajikan pada Gambar 3.
Gambar 3. Mekanisme reaksi transesterifikasi minyak nabati dengan metanolmenggunakan katalis asam (Schuchardtet al., 1998)
Berdasarkan Gambar 3 diatas terlihat bahwa reaksi berlangsung secara bertahap, diawali dengan protonasi gugus karbonil ester sehingga akan terbentuk karbokation (struktur II). Karbokation ini selanjutnya mengalami serangan nukleofilik oleh metanol menghasilkan produk intermediate tetrahedral (struktur III) yang menyebabkan gliserol terlepas dan terbentuk ester baru (struktur IV) dan melepaskan katalis H+.
Dari mekanisme diatas, asam karboksilat dapat dibentuk dari reaksi karbokation II dengan air yang ada dalam campuran reaksi. Hal ini menunjukkan bahwa reaksi transesterifikasi dengan katalis asam harus dilakukan tanpa adanya air, untuk menghindari pembentukan asam karboksilat yang bisa mengurangi konversi alkil ester.
CH3
18
Seperti telah dijelaskan sebelumnya, transesterifikasi juga dapat dikatalisis oleh basa. Dalam penelitian sebelumnya telah diketahui bahwa reaksi transesterifikasi yang menggunakan katalis basa berjalan lebih cepat dibandingkan dengan katalis asam (Fredman et al., 1986). Contoh reaksi transesterifikasi dengan katalis basa disajikan pada Gambar 4.
Gambar 4. Mekanisme reaksi transesterifikasi minyak nabati dengan metanol menggunakan katalis basa (Schuchardt et al., 1998)
Dari mekanisme reaksi di atas dapat dilihat bahwa tahap 1 adalah reaksi antara katalis basa dengan metanol menghasilkan metoksida dan katalis yang terprotonasi. Pada tahap 2 terjadi serangan nukleofilik metoksida terhadap gugus karbonil pada gliserida menghasilkan senyawa intermediate tetrahedral, yang selanjutnya berubah menjadi alkil ester dan suatu anion gliserida pada tahap 3. Tahap 4 merupakan tahap akhir, yaitu katalis akan mengalami deprotonasi
CH3OOCR’’
(4)
CH3 - OH B CH3O- + B H+
OCH3
-OCH
3
(1)
(3)
OCH3
19
sehingga katalis yang masih memiliki situs aktif akan dihasilkan kembali. Digliserida dan trigliserida juga dapat dikonversi dengan mekanisme reaksi yang sama untuk menghasilkan campuran alkil ester dan gliserol (Schuchardt et al., 1998).
Transesterifikasi trigliserida dengan katalis basa homogen merupakan aspek kimia biodiesel yang paling penting. Spesies reaktif dalam transesterifikasi menggunakan katalis basa homogen alkoksida yang terbentuk ketika alkohol dan katalis bereaksi. Alkoksida yang sangat reaktif kemudian terlibat dalam serangan nukleofilik pada gugus karbonil dari asam lemak sehingga memungkinkan serangan nukleofilik oleh alkohol melalui oksigen yang bersifat elektronegatif.
B. Katalis Reaksi Transesterifikasi Dalam Pembuatan Biodiesel
Katalis merupakan suatu zat atau substansi yang dapat mempercepat reaksi tanpa mengalami perubahan secara kimiawi pada akhir reaksi, reaksi yang berlangsung dengan bantuan katalis secara umum dikenal dengan reaksi katalisis. Katalis dapat mempercepat reaksi dengan cara menurunkan energi aktivasi reaksi. Energi aktivasi reaksi merupakan banyaknya energi minimum yang dibutuhkan oleh reaksi agar reaksi dapat berlangsung. Penurunan energi aktivasi reaksi disebabkan oleh terjadinya pembentukan alur atau mekanisme reaksi yang berbeda darialur reaksi tanpa katalis.
20
yang dapat mengakibatkan terjadinya deaktivasi katalis. Sehingga untuk setiap reaksi yang dikatalisisnya, katalis harus mempunyai aktivitas kimia yang sama, selektivitas dan stabilitas yang cukup tinggi.
Secara umum, katalis dikelompokkan dalam dua kelompok besar yaitu katalis homogen dan heterogen. Katalis homogen adalah katalis yang mempunyai fasa sama dengan reaktan, sehingga reaksi berlangsung dalam keseluruhan sistem karena dapat bercampur merata. Namun, katalis jenis ini terkadang menyulitkan dalam pemisahan dari produk pada akhir reaksi, sehingga tidak dapat digunakan ulang dan seringkali bersifat korosif dan berbahaya bagi lingkungan.
Jenis katalis yang kedua adalah katalis heterogen. Dewasa ini, katalis heterogen menjadi andalan dalam beberapa reaksi, karena sifat fasanya berbeda dengan reaktan sehingga dapat dipisahkan dari produk serta bisa digunakan kembali, dengan demikianini akan memberikan nilai efisiensi proses. Disamping itu, hasil akhir proses ini tidak bersifat korosif sehingga aman bagi lingkungan. Namun, pada prosesnya dibutuhkan pengadukan secara kontinyu karena katalis ini tak dapat bercampur merata dengan reaktan.
21
1. Katalis Homogen
Pada awalnya, katalis yang umum digunakan pada reaksi transesterifikasi adalah katalis homogen yaitu cairan asam kuat atau basa kuat. Penggunaan katalis asam diketahui menghasilkan kelimpahan alkil ester yang tinggi, namun membutuhkan waktu reaksi yang cukup lama (Schuchardt et al., 1998) karena reaksi yang terjadi adalah reversible (bolak-balik) dan pemisahan katalis dari produk sangat sulit sehingga di butuhkan perlakuan khusus memisahkannya.Sebagai contoh, Canakci et al., (1999) melakukan proses transesterifikasi minyak kedelai menggunakan katalis H2SO4 menghasilkan kenaikan persen konversi dari 87,8% menjadi 95,1 % setelah waktu reaksi ditambah dari 48 jam menjadi 96 jam.
Di samping itu, reaksi harus dilangsungkan tanpa air karena adanya air akan meningkatkan pembentukan asam karboksilat sehingga mengurangi rendemen reaksi.Beberapa peneliti lain yang telah melakukan reaksi transesterifikasi menggunakan katalis asam kuat H2SO4 (Edwardet al., 2000 ; Widyan and Al-Shyouk, 2002) dan HCl (Al-Widyan and Al-Al-Shyouk, 2002 ; Tashtoush et al., 2002).
22
rendemen reaksi akan tetapi juga menyulitkan pemisahan gliserol akibat pembentukan emulsi.
Hossain et al (2012) melakukan transesterifikasi minyak kelapa dengan katalis NaOH memerlukan pencucian hingga 4 kali untuk menghilangkan sabun yang terbentuk. Disamping itu, residu katalis homogen seringkali masih terdapat dalam produk, sehingga mengurangi kelayakgunaan produk karena sifat korosif asam maupun basa, dan katalis tersebut pada umumnya tidak dapat digunakan berulang-ulang. Beberapa peneliti telah melakukan transesterifikasi menggunakan katalis basa kuat KOH (Alamu et al., 2010 ; Komintarachat et al., 2010) dan NaOH (Alamu et al., 2008).
Adanya berbagai kelemahan katalis homogen untuk reaksi transesterifikasi yang telah dipaparkan diatas mendorong pengembangan katalis heterogen.
2. Katalis Heterogen
Katalis heterogen mendapat perhatian yang luas karena secara prinsip memiliki keunggulan dibandingkan katalis homogen. Katalis heterogen memiliki berbagai keunggulan dibandingkan katalis homogen, antara lain efisiensi yang tinggi, kemudahan untuk digunakan dalam berbagai media, kemudahan pemisahan katalis dari campuran reaksi, dan penggunaan ulang katalis (Moffat, 1990; Frenzer and Maier, 2006).
23
penyangga umumnya berupa zat padat berpori yang berfungsi untuk memberikan luas permukaan yang lebih besar bagi situs aktif.Penyangga yang baik adalah yang mempunyai stabilitas termal dan kimia yang tinggi, luas permukaan yang besar dan sebaiknya juga merupakan senyawa inert.
Dewasa ini dikenal beberapa penyangga yang sudah umum digunakan antara lain magnesia (Ramirez-Olivia et al., 2006), zeolit (Yagiz et al., 2007; Ramos et al., 2008), alumina (Wang and Liu, 1998; Asri, 2012) dan silika (Benvenutti and Yoshitaka, 1998; Pandiangan dkk., 2008). Berbagai oksida logam telah diaplikasikan sebagai situs aktif diantaranya CaO untuk transesterifikasi minyak jarak(Zhu et al., 2006; Endalew et al., 2011), CaO-ZnO untuk transesterifikasi minyak sawit (Chantara et al., 2012), TiO2/SiO2 untuk transesterifikasi minyak kelapa (Pandiangan dkk, 2013), dan MgO untuk transesterifikasi minyak kelapa (Syani, 2014).
24
2.1 Zeolit Alam
Zeolit alam terbentuk karena adanya proses kimia dan fisika yang kompleks dari batuan-batuan yang mengalami berbagai macam perubahan di alam. Para ahli geokimia dan mineralogi memperkirakan bahwa zeolit merupakan produk gunung berapi yang membeku menjadi batuan vulkanik, batuan sedimen dan batuan metamorfosa yang selanjutnya mengalami proses pelapukan karena pengaruh panas dan dingin.
Berdasarkan asal pembentukannya, zeolit alam dibedakan menjadi dua yakni (1) zeolit yang terdapat diantara lapisan dan celah-celah batuan, zeolit jenis ini biasanya terdiri dari beberapa jenis mineral zeolit yang tergabung dengan mineral lain seperti kalsit, kwarsa, renit, klorit, fluorit dan mineral sulfida. (2) Zeolit yang berupa batuan, zeolit jenis ini diantaranya adalah klipnotilolit, analsim, laumonit, modernit, filipsit, kabasit dan heulandit. Secara umum zeolit alam ditemukan dalam komposisi berbeda, dan secara umum dinyatakan dengan rumus :
Mn[(AlO2)x(SiO2)y].wH2O,
25
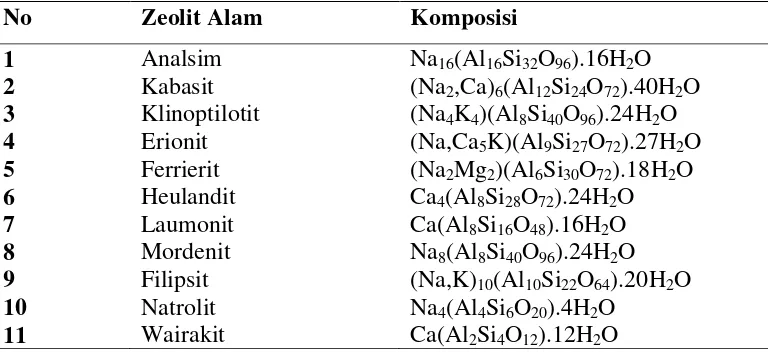
Tabel 5. Contoh mineralzeolit yang umum ditemukan di alam
No Zeolit Alam Komposisi
1 Analsim Na16(Al16Si32O96).16H2O
Lestari (2010) melaporkan bahwa zeolit alam Indonesia (Malang dan Wonosari) banyak mengandung jenismordenit dan klinoptilolit. Klinoptilolit dan mordenit memiliki sifat stabil di berbagai media kaustik, mampu mempertahankan
strukturnya hingga suhu tinggi hingga 800-900°C, dan tingkat kesetimbangan
sorpsinya tinggi, sehingga banyak digunakan dalam perlindungan kimia lingkungan dan industri (Korkuna, 2006).
Dewasa ini klinoptilolit dan mordenit banyak digunakan dalam bidang pengolahan air dan limbah cair, adsorpsi, pengolahan limbah nuklir, pertanian, pengobatan, dan pengolahan biodiesel (Kusuma dkk, 2012).
26
zeolit.Disamping itu, ukuran pori-pori pada permukaan zeolit juga tidak seragam, kristalinitasnya kurang baik dan kekuatan asamnya sulit dikontrol. Untuk memperbaiki karakter zeolit alam sehingga dapat digunakan sebagai katalis, adsorben, atau aplikasi lainnya, biasanya dilakukan aktivasi dan modifikasi. Yuanita (2009) melakukan modifikasi terhadap zeolit alam jenis mordenit dan klinoptilolit dengan perlakuan asam menggunakan HCl dan penyisipan Si pada kerangka zeolit menggunakan natrium silikat.
Atas dasar beberapa kelemahan zeolit alam tersebut, maka mulai dikembangkan zeolit sintetikkarena lebih unggul dalam stabilitas termal, memiliki kemurnian yang tinggi dan komposisi nisbah Si/Al nya mudah dikontrol.
2.2 Zeolit Sintetik
27
Dengan perkembangan penelitian, dewasa ini telah dikenal beragam zeolit sintetik, dan beberapa diantaranya disajikan dalam Tabel 6.
Tabel 6. Rumus oksida beberapa jenis zeolit sintetik
Zeolit Rumus Oksida
Zeolit A Na2O.Al2O3.2SiO2.4,5H2O
Zeolit N-A (Na,TMA)2O.Al2O3.4,8SiO2.7H2O TMA – (CH3)4N+ Zeolit H K2O.Al2O3.2SiO2.4H2O Zeolit Ω (Na,TMA)2O.Al2O3.7SiO2.5H2O TMA – (CH3)4N+ Zeolit ZK-4 0,85Na2O.0,15(TMA)2O.Al2O3.3,3SiO2.6H2O Zeolit ZK-5 (R,Na2)O.Al2O3.4-6SiO2.6H2O
Sumber : (Georgiev, 2009)
Seperti telah dijelaskan sebelumnya, prinsip dasar produksi zeolit sintetik adalah komponennya yang terdiri darisilika dan alumunium. Berdasarkan komposisi tersebut, berbagai penelitian untuk menghasilkan zeolit sintetik telah dilakukan dan difokuskan pada dua aspek, yakni bahan baku dan metode preparasi. Pada umumnya, zeolit sintetik diproduksi dari bahan baku berupa senyawa silika yang mudah larut dalam air seperti tetra methyl ortho silicate (TMOS) dan tetra ethyl ortho silicate (TEOS), sedangkan untuk senyawa alumina didapatkan darialumunium nitrat (Wang et al., 2010) dan alumunium klorida (Dirdianti, 2011). Dari bahan baku tersebut, zeolit dapat dibuat dengan metode sol-gel.
28
hidrotermal (Wustoni, 2011). Teknik lainnya adalah microwave, pada teknik ini gelombang elektromagnetik dengan frekuensi 300 MHz – 300 GHz dialirkan ke dalam campuran larutan aluminat dan silikat sampai terbentuk campuran zeolit yang homogen (Musthofa dan Lukman, 2010).
Dari beberapa jenis bahan baku dan metoda sintesis yang telah disebutkan di atas, terdapat beberapa kelemahan, diantaranya adalah bahan baku silika TEOS dan TMOS merupakan produk impor yang harganya mahal, metode preparasi zeolit dengan hidrothermal memerlukan waktu lama dan banyak bahan kimia yang terbuang, dan teknik pembuatan zeolit dengan microwavemasih dipertanyakan mengenai keamanan dan efek kesehatan bagi pengguna karena tingginya frekuensi yang digunakan (Conner, 2004).
Terkait dengan bahan baku dan metode preparasi yang di paparkan diatas, dalam penelitian ini digagas pembuatan zeolit sintetik dari bahan baku sekam padi dengan metode elektrokimia. Metode ini digagas berdasarkan dua latar belakang yakni pemanfaatan silika sekam padi dan pemanfaatan logam alumunium.
2.2.1 Silika Sekam Padi
29
Sebagai gambaran, silika sekam padi telah dimanfaatkan secara luas untuk pembuatan keramik (Sitorus, 2009; Wittayakun, 2011), katalis (Adam, 2006), berbagai material komposit (Marlina, 2012; Suka, 2009; Handayani, 2009), dan pembuatan zeolit sintetik ( Kristiyani, 2012; Fuadi dkk, 2012; Tepamat et al., 2012; Syani, 2014). Pemanfaatan silika yang demikian luas juga didukung kemudahan untuk memperoleh silika dari sekam padi, yakni dengan cara ekstraksi atau dengan pengabuan.
Suka (2008) berhasil mensintesis silika dari sekam padi Provinsi Lampung dengan metode ekstraksimenggunakan KOH. Filtrat yang dihasilkan diasamkan dengan HCl hingga didapatkan gel silika pada pH 7, hasil yang diperoleh didapatkan kadar silika 40,8 % dengan kemurnian sekitar 95,53%.Peneliti lain Agung M (2013) mengekstraksi silika dari abu sekam padi yang telah dipanaskan dalam
furnace selama 4 jam pada suhu 700oC, hasil yang didapat diperoleh rendemen silika sekitar 50,97% pada konsentrasi KOH 10% dengan waktu ekstraksi 90 menit.
Menurut Mittal (1997) reaksi yang terjadi antara SiO2 yang terkandung dalam abu sekam padi dengan larutan alkali, larutan KOH adalah sebagai berikut:
SiO2 + 2KOH K2SiO3 + H2O
Kemudian, dalam larutan tersebut ditambahkan asam, larutan HCl yang digunakan untuk mengikat kalium sehingga dihasilkan SiO2. Reaksi yang terjadi sebagai berikut:
30
Terkait dengan produksi zeolit sintetik, beberapa peneliti telah mensintesis zeolit sintetik menggunakan bahan baku sekam padi dengan berbagai metode. Kamarudin (2004) melaporkan telah mensintesis zeolit dari silika sekam padi, mula-mula sekam padi dibakar dalam furnace pada suhu 450, 600 dan 800°C
dengan rata-rata pemanasan 5°C/menit.Abu yang terbentuk dicuci dengan NaOH
pada suhu 80°C selama 2 jam, kemudian dicampurkan dengan gel (natrium
aluminat dan natrium hidoksida) dan dipanaskan pada suhu 100°C selama 14 jam.
Zeolit yang terbentuk dikarakterisasi dengan X-Ray Diffraction (XRD), diketahui zeolit yang terbentuk bertipe zeolit Y dan P.
Wittayakun (2008) melaporkan telah mensintesis zeolit NaP dari NaY dari silika sekam padi dengan metode hidrothermal.Dalam pelaksanaannya, proses dilakukan
secara hidrotermal pada suhu 100°C dengan rasio optimum dari SiO2, Al2O3 dan
31
Fuadi dkk (2012) melakukan pencampuran abu sekam padi dengan natrium silikat, air dan NaOH yang dimasukkan kemicrowave pada berbagai variasi suhu dan waktu, dihasilkan zeolit dengan kristalinitas tinggi setelah 60 menit pada suhu rendah. Tepamat et al., (2013) melakukan sintesis zeolit jenis NaA menggunakan abu sekam padi dengan metode hidrotermal pada suhu 100°C selama 4 jam, dari
perlakuan ini dihasilkan bentuk kristal dari zeolit NaA adalah kubik.
Terkait dengan penelitian ini, yaitu pembuatan zeolit sintetik dari bahan baku sekam padi sebagai katalis untuk reaksi transesterifikasi,Artkla(2008) melakukan sintesis sejenis material mesoporos RH-MCM-41 yang berasal dari sekam padi dengan metode hidrotermal sebagai dopan K2O. Katalis K2O/RH-MCM-41 digunakan untuk reaksi transesterifikasi minyak sawit. Katalis dengan muatan K2O sebesar 8% memberikan persen konversi metil ester sebesar 84% pada suhu 100°C.
Atas dasar berbagai kemudahan dalam penggunaan sekam padi, dengan mengadopsi penelitian Suka (2008), penelitian ini mengekstraksi silika dari sekam padi dengan larutan NaOH 1,5%yang diasamkan hingga menjadi gel silika pada pH 7. Silika yang dihasilkan digunakan sebagai bahan baku zeolit sintetik menggunakan metode elektrokimia dengan logam alumunium sebagai elektroda.
2.2.2 Logam Alumunium
32
ekonomis tinggi sehingga sering dijumpai dalam alat rumah tangga, bingkai jendela dan sebagainya.Alumunium ditemukan dialam berupa mineral-mineral, salah satu mineral yang umum digunakan untuk pengolahan alumunium adalah bijih bauksit (Al2O3). Proses pemurnian alumunium terjadi pada dua tahap yakni, proses Bayer dan dan proses Hall-Herault. Proses Bayer merupakan proses pemurnian bijih bauksit untuk memperoleh alumunium oksida, untuk proses Hall-Herault merupakan proses peleburan alumunium oksida untuk menghasilkan alumunium murni.
Pada proses Bayer, bijih bauksit yang mengandung 50-60% Al2O3 yang bercampur dengan zat-zat pengotor terutama Fe2O3, SiO2 dan TiO2. Untuk memisahkan Al2O3 dari zat-zat pengotor tersebut, maka bijih bauksit tersebut dilarutkan dalam NaOH, melalui reaksi berikut :
Al2O3(s) + 2NaOH(aq) + 3H2O(l)2NaAl(OH)4(aq)
Aluminium oksida dapat larut dalam NaOH dikarenakan sifat amfoter dari Al2O3 sehingga zat-zat pengotor lainnya yang tidak larut dapat dipisahkan melalui proses penyaringan. Larutan NaAl(OH)4yang terbentuk dialirkan dengan gas CO2 untuk mendapatkan endapan Al(OH)3.
2NaAl(OH)4(aq) + CO2(g)2Al(OH)3(s) + Na2CO3(aq) + H2O(l)
Endapan Al(OH)3 disaring, kemudian dikeringkan dan dipanaskan sehingga diperoleh aluminium oksida murni (Al2O3).
2Al(OH)3(s) Al2O3(s) + 3H2O(g)
33
Al2O3menjadi suhu 850-950°C, sehingga leburan tersebut bisa dielektrolisis
menggunakan grafit sebagai anoda dan katodanya. Ketika listrik dijalankan ion-ion Al3+ yang ada dalam larutan bergerak menuju katoda, yang direduksi menjadi alumunium cair, sedangkan O2- akan bergerak menuju anoda yang selanjutnya dioksidasi menjadi gas oksigen. Alumunium yang dihasilkan di katoda dialirkan keluar dari sel dan suhunya diturunkan sehingga diperoleh alumunium padat. Reaksi yang terjadi pada katoda dan anoda dapat dilihat sebagai berikut :
Al2O3(l) 2Al3+(l) + 3O2-(l) Katoda : 2Al3+ + 6e- 2Al(l) Anoda : 3O2-(l) 3/2O2(g) + 6e
-Terkait dengan beberapa keunggulan dari logam alumunium, pada penelitian inidigunakan logam alumuniummurni besertasilika yang telah diekstrak dari sekam padi untuk membuat zeolit sintetik menggunakan metode elektrosintesis.
C. Elektrosintesis
Selain pemanfaatan yang sudah umum (konvensional), pemanfaatan lain dari metode elektrokimia adalah elektrosintesis. Meskipun bidang elektrosintesis ini masih relatif terbatas, ada beberapa contoh senyawa organik yang telah disintesis dengan metode ini, seperti yang dilakukan oleh Wu et al ( 2012) yang mensintesis organik karbonat dari CO2 dengan alkohol dibawah kondisi galvanistik pada suhu kamar dan tekanan normal dalam DMF/MeCN tanpa penambahan katalis.
34
senyawa multi karbon dengan efisiensi penggunaan elektron tertinggi hingga 80 %.Selain senyawa organik, senyawa anorganik juga dapat dihasilkan dengan metode elektrosintesis khususnya bahan-bahan atau senyawa berbasis logam, misalnya komposit PANI-Nano TiO2sebagai pelapis anti korosi telah berhasil di elektrosintesis dari anilin dalam larutan asam oksalat yang mengandung nano TiO2 menggunakan voltametrik siklik. (Karpakam et al., 2011).
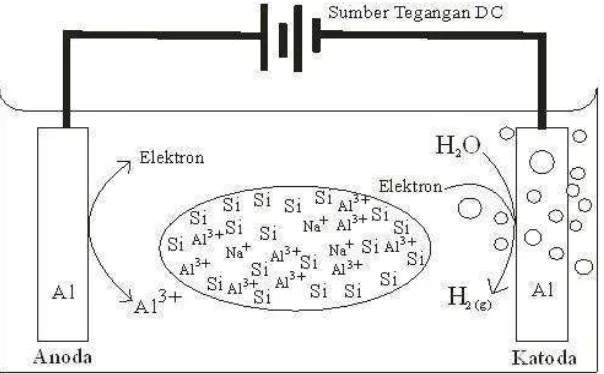
Terkait dengan penelitian ini, zeolit sintetik dihasilkan dengan metode elektrosintesis menggunakan sol silika sekam padi yang dilarutkan dalam larutan NaOH dan batangan logam alumunium sebagai anoda dan katoda. Secara garis besar pembuatan zeolit sintetik dengan metode elektrosintesis dapat dijelaskan dalam Gambar 5 dan Gambar 6.
Gambar 5. Mekanisme pembentukan zeolit dalam reaktor elektrosintesis
Na + Si
O
OH
OH Na O Si OH O
Katoda : 2H2O(l) + 2e- H2(g) + 2OH-(aq) Anoda : Al(s)Al3+(aq) + 3e-
35
Al3+ + Si
O
OH
OH
Al O Si
O
O
Al
Gambar 6. Mekanisme reaksi pembuatan zeolit sintetik dengan ekstraksi NaOH dan elektrosintesis
Pada tahap 1 silika sekam padi diekstraksidengan larutan alkali NaOH hingga mendidih. Fitrat yang dihasilkan ditambahkan HNO3 10% hingga menjadi gel pada pH 7. Gel silika yang terbentuk kemudian dikeringkan dan dihaluskan. Serbuk silika dilarutkan kembali dengan NaOH kemudian dielektrosintesis menggunakan batangan logam alumunium sebagai anoda dan katoda. Pada tahap 2 reaksi yang terjadi pada katoda dihasilkan gas hidrogen, dan dianoda melepaskan ion Al3+, ion Al3+akan bereaksi dengan sol silika membentuk senyawa alumina silika (tahap 3). Melalui penerapan berbeda pada pH, potensial dan waktu, maka dihasilkan zeolit sintetik yang beragam (tahap 4).
36
D. Karakterisasi Katalis Zeolit
1. Scanning Electron Microscopy-Energi Dispersive X-ray Spektrometer
(SEM-EDS)
Untuk menganalisis komposisi kimia suatu permukaan secara kualitatif dan kuantitatif digunakan perangkat alat SEM (Scanning Electron Microscopy) yang dirangkaikan dengan EDS (Energy Dispersive X-ray Spectrometer). Pada SEM (Scanning Electron Microscopy) dapat diamati karakteristik bentuk, struktur, serta distribusi pori pada permukaan bahan, sedangkan komposisi serta kadar unsur yang terkandung dalam sampel dapat diamati dengan EDS. Analisis EDS dimaksudkan untuk mengetahui ketidakhomogenan pada sampel dan menganalisis secara kualitatif dan kuantitatif jenis unsur atau oksida logam M yang masuk ke dalam matriks silika sekampadi. Ghasemi dan Younesi (2010) melakukan sintesis zeolit NaA dari sekam padi menggunakan metode hidrotermal tanpa penambahan zat tambahan organik. Hasil analisis SEM menunjukkan nanozeolit NaA berhasil disintesis dengan ukuran partikel50-120 nm dengan perbandingan Na2O/SiO2 sebesar 6 seperti ditunjukkan dalam Gambar 7.
37
Terkait dengan penelitian ini, Simanjuntak, dkk (2013) berhasil mensintesis zeolit dari sekam padi menggunakan metode elektrosintesis dan dihasilkan morfologi partikel dengan ukuran nano dan relatif seragam, terdistribusi secara merata dan menghasilkan permukaan yang cukup homogen. Hasil morfologi dari zeolit tersebut disajikan dalam Gambar 8.
Gambar 8. Morfologi permukaan zeolit sintetik dari sekam padi dengan metode Elektrosintesis (Simanjuntak, dkk., 2013)
2. Particle Size Analyser (PSA)
Perkembangan ilmu pengetahuan lebih mengarah ke era nanoteknologi, para peneliti mulai menggunakan Laser Diffraction (LAS), metode ini lebih akurat bila dibandingkan dengan metode analisa gambar maupun metode ayakan (sieve
analyses), terutama untuk sample-sampel dalam skala nanometer maupun submicron. Contoh alat yang menggunakan metode LAS adalah particle size
38
partikel dan membawanya ke sensing zone. Metode ini baik digunakan untuk ukuran yang kasar, dimana hubungan antarpartikel lemah dan kemungkinan untuk beraglomerasi kecil.
Pengukuran partikel dengan menggunakan PSA biasanya menggunakan metode basah. Metode ini dinilai lebih akurat jika dibandingkan dengan metode kering karena partikel didispersikan ke dalam media sehingga partikel tidak saling beraglomerasi (menggumpal). Dengan demikian ukuran partikel yang terukur adalah ukuran dari single particle. Selain itu hasil pengukuran dalam bentuk distribusi, sehingga hasil pengukuran dapat diasumsikan sudah menggambarkan keseluruhan kondisi sampel.
3. X-Ray Diffraction (XRD)
Metode XRD banyak digunakan untuk mengidentifikasi dan mengkarakterisasi material yang digunakan sebagai katalis, karena banyak material katalis yang berwujud kristal. Teknologi XRD ini jugamempunyai kemampuan untuk mengidentifikasi dan menentukan besarnya bagian fasa dalam padatan, film tipis, dan sample multi fasa.
Di dalam analisis XRD, kristal katalis memantulkan sinar-X yang dikirimkan dari sumber dan diterima oleh detektor. Dengan memantulkan sudut kedatangan sinar-X maka spektrum pantulan adalah spesifik yang berhubungan langsung dengan
39
persamaan Bragg Richardson. Pada persamaan interpretasi Hukum Bragg dilakukan berdasarkan asumsi bahwa permukaan dari mana sinar X dipantulkan adalah datar.
nλ= 2d sin θ
Dimana d menyatakan jarak antar lapisan atom atau ion yang berdekatan, λ menyatakan panjang gelombang radiasi sinar-X, dan n adalah urutan pantulan. Kristalinitas dapat juga ditentukan dengan XRD melaluiperbandingan intensitas atau luasan peak sampel dengan intensitas atau luasan peak standar yang ditunjukkanpadapersamaan:
Lebar peak XRD merupakan fungsi dari ukuran partikel, maka ukuran kristal(crystallite size) dinyatakan dalam Persamaan Scherrer berikut (Richardson, 1989)
Dimana K=1.000, B adalah lebar peak untuk jalur difraksi pada sudut 2θ, b adalah instrument peak broadening (0.1o), dan λ adalah panjang gelombang pada 0.154 nm. Suku (B2-b2)½ adalah lebar peak untuk corrected instrumental broadening.
40
kristal, yang mempunyai peran penting dalam reaksi sebagai struktur yang sensitif.
Liani (2014)melakukan sintesis zeolit dari alumina yang dihasilkan dengan metode elektrokimia yang digunakan sebagai bahan baku untuk pembuatan zeolit sintetik faujasit dengan metode hidrotermal. Zeolit yang terbentuk dikalsinasi pada suhu yang berbeda, yakni 350, 450, dan 550 oC, kemudian dikarakterisasi menggunakan difraksi sinar X (XRD) untuk mempelajari proses pembentukan fasa zeolit. Contoh hasil karakterisasi disajikan dalam Gambar 9.
Gambar 9. Difraktogram sampel zeolit yang dikalsinasi pada suhu yang berbeda. (A) 350 oC, (B) 450 oC (Liani, 2014).
(A)
41
Dari kedua gambar di atas menunjukkan pola yang praktis sama, yang mengindikasikan bahwa pembentukan zeolit jenis faujasit sudah mencapai tahap yang sempurna pada suhu 350oC. Suhu pembentukan zeolit yang tergolong rendah ini mengindikasikan bahwa alumina yang dihasilkan secara elektrokimia dan silika sekam padi yang digunakan sebagai bahan baku, keduanya mampu bereaksi dengan energi yang kecil.
E. Karakterisasi Biodiesel
1. Uji Kelayakan Biodiesel
Biodiesel didefinisikan sebagai alkil ester asam lemak yang berasal dari minyak nabati. Biodiesel harus memenuhi standar kelayakan sebelum digunakan sebagai bahan bakar mesin diesel. Standar kelayakan didasarkan atas “An American
National Standard Specification for Biodiesel Fuel Blend Stock (B100) for Middle Distillate Fuels” dan SNI 04-7182-2006. Berikut ini data standar dan sifat fisika dan kimia berdasarkan An American National Standard for Biodiesel (B100) dan Standard Nasional Indonesia (SNI).
2. Gas Chromatography – Mass Spectrofotometry (GC-MS)
42
Perangkat GC-MS pada dasarnya merupakan paduan perangkat GC, yang berperan untuk memisahkan komponen yang ada dalam suatu sampel, dan perangkat MS yang berperan sebagai detektor. Komponen penting dalam kromatografi gas adalah tangki pembawa gas yang dilengkapi dengan pengatur tekanan, tempat injeksi sampel, kolom, detektor yang dilengkapi thermostat, amplifier dan rekorder.
Fungsi gas pembawa adalah mengangkut cuplikan dari kolom menuju detektor, gas tersebut haruslah inert dan murni, gas pembawa yang sering digunakan adalah nitrogen, hidrogen, helium, dan argon. Kolom kromatografi terdiri dari tiga bagian yaitu wadah luar, isi kolom yang terdiri dari padatan pendukung dan fasa cairan.
Spektroskopi massa dapat digunakan untuk mengidentifikasi senyawa yang dipengaruhi oleh kestabilan senyawa dalam bentuk ion. Puncak paling tinggi disebut base peak, pola fragmentasi dalam bentuk deretan garis, puncak pendek dan kecil yang disebut isotop. Perpaduan spektroskopi massa dengan kromatografi gas akan menghasilkan analisis yang lebih baik. Berkas elektron yang ditembakkan ke molekul senyawa biasanya 7-15 mV yang menyebabkan senyawa mengalami ionisasi.
43
III. METODE PENELITIAN
A. Tempat dan Waktu Penelitian
Penelitian ini akan dilakukan selama 4 bulan yaitu dari bulan November2014 hingga Maret 2015 bertempat di Laboratorium Polimer Jurusan Kimia Fakultas MIPA Universitas Lampung.Analisis flash point, viskositas dan berat jenis produk transesterifikasibiodiesel dilakukan diLaboratorium Biomassa Universitas Lampung. Karakterisasi katalis dengan SEM-EDS, dan XRD dilakukan di Institut Teknologi Bandung, dan analisis PSA di lakukan dilaboratorium pusat LIPI Serpong, dan analisis biodiesel GC-MS dilakukan di Universitas Gajah Mada, Yogyakarta.
B. Alat dan Bahan
1. Alat-alat yang digunakan
45
SHIMADZU,viskometer ostwald,perangkat elektrokimia, penangas, magnetic stirrer, oven, alat vakum, thermometer, dan peralatan gelas.
2. Bahan-Bahan Yang Digunakan
Bahan-bahan yang digunakan dalam penelitian ini antara lain : sekam padi, larutan larutan HNO3 10 %, aquades, indikator universal, kertas saring, larutan NaOH 1,5 %,batangan aluminium, minyak kelapa, dan minyak jarak.
C.Prosedur Penelitian
1. Preparasi Sekam Padi
Langkah awal dalam penelitian ini adalah preparasi sampel sekam padi.Sebanyak 500 gram sekam padi direndam dalam air panas selama 2 jam untuk mengekstrak bahan organik larut air yang merupakan bahan pengotor dalam proses ekstraksi silika. Sekam padi kemudian disaring dan dicuci lagi secara berulang dengan cara disiram dengan air panas untuk menghilangkan pengotor bahan organik larut air yang masih diperkirakan menempel pada permukaan sekam padi.Kemudian, sekam padi yang telah bebas dari pengotor dikeringanginkan dan siap digunakan untuk ekstraksi silika.
2. Ekstraksi Silika Dari Sekam Padi
46
direndam dalam 500 mL larutan NaOH 1,5% kemudian dipanaskan sampai mendidih selama 30 menit. Selanjutnya, sampel disaring dan filtrat yang mengandung silika terlarut ditampung. Untuk mengendapkan silika, filtrat kemudian ditambahkan larutan asam HNO3 10% secara bertahap hingga terbentuk endapan silika dalam bentuk gel dan pH pengendapan silika mencapai 7,0. Gel silika kemudian didiamkan (aging) selama 24 jam pada suhu kamar. Selanjutnya gel silika disaring dan dicuci dengan akuades panas hingga bersih, lalu silika gel di rendam dengan larutan pemutih (bayclin) untuk menghilangkan sisa-sisa pengotor organik. Dilakukan pencucian lagi dengan air suling panas hingga bau bayclin hilang. Selanjutnya silika gel yang telah bersih dan bebas pengotor organik kemudian dikeringkan dalam oven pada suhu 110°C selama 24 jam dan dihaluskan.
3. Pembuatan Sol Silika Sekam Padi
Sebanyak 20 gram silika sekam padi hasil ektraksi yang telah dihaluskan dimasukkan ke dalam 600 ml larutan NaOH 1,5% hingga larut sempurnasambil diaduk menggunakan hotplate stirer.
4. Pembuatan Prekusor Zeolit Dengan Metode Elektrokimia
47
elektrolisis pada variasi potensial 4, 6, 8 dan 10 volt selama 30 menit. Zeolit yang terbentuk selanjutnya disaring kemudian dikeringkan pada suhu 110oC selama 24 jam lalu digerus dan diayak dengan ayakan berukuran 200 mesh. Rancangan alat untuk proses elektrosintesis zeolit dapat diberikan pada Gambar 10.
Gambar 10. Rancangan reaktor elektrokimia silika sekam padi menjadi zeolit
5. Kalsinasi Katalis
Proses kalsinasi dilakukan dengan menggunakan furnace Lento 3508 yang dapat disesuaikan dengan perlakuan yang diinginkan. Kalsinasi katalis zeolit yang berbentuk serbuk halus dilakukanpada suhu konstan 300oC selama 2 jam.Berikut ini adalah langkah-langkah pengunaan furnace :
1. Sampel disiapkan.
2. Sampel dimasukkan ke dalam tungku pemanas (furnace).
5 Keterangan :
A. Potensial meter B. Reaktor kaca C. Batang alumunium D. Hot Plate Stirrer E. Kabel penghubung
48
3. Alat tungku dihubungkan dengan sumber tegangan, kemudian setting alat dalam keadaan hidup atau "ON".
4. Tungku diatur (setting) sesuai dengan perlakuan pada sampel. 5. Tungku pemanas dimatikan ketika proses telah selesai.
6. Sampel dikeluarkan dari tungku pemanas.
Sampel dipanaskan dari suhu 25oC hingga mencapai suhu 300oC dengan kenaikan suhu 5oC/menit. Setelah mencapai suhu yang diinginkan (300oC) suhu ditahan selama 2 jam (120 menit).Selanjutnya alat furnace akan menghentikan pemicu kenaikan dan penahanan suhu, kemudian secara otomatis suhu di dalam furnace akan turun kembali secara perlahan hingga mencapai suhu kamar (25oC).
6. Seleksi Katalis Pada Reaksi Transesterifikasi
Untuk mendapatkan zeolit dengan unjuk kerja terbaik sebagai katalis, zeolit yang dihasilkan dari metode elektrosintesis diujicobakan pada reaksi transesterifikasi minyak nabati. Sebanyak 50 mL minyak nabati dicampurkan dengan 20 mL metanol dan katalis zeolit sintetik sebanyak 2 gram. Campuran diaduk secara kontinyu menggunakan Hot Plate Stirrer pada suhu 75-80°C selama 120 menit dalam kondisi
49
Gambar 11. Rancangan proses transesterifikasi
7. Analisis Produk Transesterifikasi (Biodiesel)
Produk yang dihasilkan pada kondisi optimum reaksi transesterifikasi minyak nabati dilakukan uji kelayakan sebagai bahan bakar antara lainflash point,cetane number, viskositas dan massa jenisberdasarkan SNI 04-7182-2006. Sedangkan untuk identifikasi komponen dalam produk, dan secara khusus untuk melihat apakah semua trigliserida yang terdapat dalam minyak nabati mampu diubah menjadi mono ester dilakukan analisis GasChromathografy-Mass Spectroscopy (MS).Analisis GC-MS menggunakan model GC-GC-MS QP2010S SHIMADZU, yang dilengkapi dengan kolom AgilentJ%W DB-1 yang panjangnya 30 meter dan diameter internal 0,25 mm. Fragmentasi berlangsung dengan bantuan sumber elektron berupa electron impact(EI)
E D B
A