ABSTRAK
PEMANFAATAN EKSTRAK BIJI PINANG SEBAGAI INHIBITOR KERAK KALSIUM KARBONAT (CaCO3) DENGAN METODE
UNSEEDED EXPERIMENT
Oleh
Fauziyyah Mu’min Shiddiq
Dalam penelitian ini telah dilakukan penambahan inhibitor ekstrak biji pinang pada kerak kalsium karbonat (CaCO3) menggunakan metode unseeded experiment
pada konsentrasi CaCO3 sebesar 0,00,100 M serta variasi inhibitor sebesar
50-250 ppm. Hasil penelitian berdasarkan analisis data menggunakan Microsoft Excel menunjukkan bahwa konsentrasi optimum inhibitor dalam menghambat laju pembentukan inti serta pertumbuhan kerak CaCO3 0,05 M adalah 250 ppm
dengan hasil persentase kemampuan menghambat sebesar 20%. Hal ini didukung dengan analisis kualitatif menggunakan Scanning Electron Microscopy (SEM)
yang secara umum memperlihatkan perbedaan yang signifikan pada morfologi permukaan kerak CaCO3. Analisis kuantitatif menggunakan Particle Size
Analyzer (PSA) menunjukkan bahwa distribusi ukuran partikel kerak CaCO3
menjadi lebih kecil dengan adanya penambahan inhibitor yang dinilai berdasarkan pada nilai tengah dan nilai rata-rata ukuran partikel kerak CaCO3 yakni tanpa
penambahan inhibitor memiliki nilai tengah sebesar 0,30 µm dan nilai rata-rata sebesar 1,28 µm, sedangkan setelah penambahan inhibitor memiliki nilai tengah sebesar 0,22 µm dan nilai rata-rata sebesar 0,98 µm.
ABSTRACT
UTILIZATION OF BETEL NUT SEED EXTRACT AS INHIBITOR OF CALCIUM CARBONATE (CaCO3) SCALE FORMATION WITH
UNSEEDED EXPERIMENT METHOD
By
Fauziyyah Mu’min Shiddiq
In this research, it has been conducted addition of betel nut seed extract on the calcium carbonate (CaCO3) scale using unseeded experiment method at various
concentrations of growth solutions from 0.050 to 0.100 M. The various concentrations of inhibitor added were around 50 to 250 ppm. The results based on data analysis using Microsoft Excel that indicate the optimum concentration of inhibition in inhibiting formation and growth of CaCO3 0.050 M scale is 250 ppm
with percentage of inhibitor ability 20%. This is supported by qualitative analysis using Scanning Electron Microscopy (SEM), which generally showed a significant difference in the surface morphology of CaCO3 scale. The quantitative
analysis using a Particle Size Analyzer (PSA) showed that the distribution of particle size of CaCO3 crystals with the addition of inhibitor is smaller than
without the addition of inhibitor based on the median and the average value. Particle size of CaCO3 scale without the addition of inhibitor has the median value
of 0.30 µm and average value of 1.28 µm. After the addition of inhibitor, it has the median value of 0.22 µm and average value of 0.98 µm.
PEMANFAATAN EKSTRAK BIJIPINANGSEBAGAI INHIBITORKERAK KALSIUM KARBONAT (CaCO3) DENGAN METODE UNSEEDED
EXPERIMENT
Oleh
FAUZIYYAH MU’MIN SHIDDIQ
Skripsi
Sebagai Salah Satu Syarat untuk Mencapai Gelar SARJANA SAINS
Pada Jurusan Kimia
Fakultas Matematika dan Ilmu Pengetahuan Alam
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM UNIVERSITAS LAMPUNG
RIWAYAT HIDUP
Penulis dilahirkan di Bandar Lampung, pada tanggal 10
Maret 1992 sebagai anak ketiga dari enam bersaudara dari
pasangan Bapak Yanto dan Ibu Eti Yuningsih. Penulis
menyelesaikan pendidikan di TQ Qurrota Ayun pada
tahun 1998, Sekolah Dasar Muhammadiyah 1 Bandar
Lampung pada tahun 2004, SMP Negeri 8 Bandar Lampung pada tahun 2007, dan
SMA Negeri 14 Bandar Lampung pada tahun 2010. Penulis terdaftar sebagai
mahasiswa Jurusan Kimia Fakultas Matematika dan Ilmu Pengetahuan Alam pada
tahun 2010 melalui jalur Seleksi Nasional Masuk Perguruan Tinggi Negeri
(SNMPTN).
Pada tahun 2013 penulis melakukan Praktek kerja lapangan di Laboratorium
Anorganik Universitas Lampung. Selama menjadi mahasiswa penulis pernah
menjadi asisten pratikum S1 Kimia mata kuliah Sains Dasar, S1 Matematika mata
kuliah Sains Dasar dan S1 Kehutanan mata kuliah Kimia Dasar. Penulis aktif di
Himpunan Mahasiswa Kimia (HIMAKI) FMIPA Unila sebagai anggota Kader
Muda Himaki (KAMI) kepengurusan 2010/2011 dan di Badan Eksekutif
Mahasiswa sebagai sekretaris bidang Sains dan Teknologi kepengurusan
MOTO
... karena, sesungguhnya sesudah kesulitan ada
kemudahan (QS. 94 : 5-6)
Maka apabila kamu telah selesai (dari suatu urusan),
kerjakanlah dengan sungguh-sungguh (urusan) yang
lain (QS. 94 : 7)
Aku tidak punya bakat turunan, oleh karenanya aku
terus berkata pada diri sendiri bahwa aku harus
berusaha keras dalam mencapai semua
cita-cita/tujuanku (Lee Seung Gi)
Kupersembahkan karya kecilku ini kepada...
Ummi (Eti Yuningsih) dan Abi (Yanto) tercinta yang
tiada hentinya selalu memberi dan berdoa yang terbaik
untukku
serta kakak-kakakku dan adik-adikku tersayang,
Afifah, Hanif, Yahya, Halimah dan Salma
SANWACANA
Puji syukur kehadirat Allah SWT yang telah memberikan segala bentuk rahmat,
hidayah dan ridho-Nya yang tak bertepi. Shalawat serta salam teruntuk Nabi
Muhammad SAW. Berbekal pengetahuan dan pengalaman yang telah diperoleh,
penulis mampu menyelesaikan skripsi yang berjudul "Pemanfaatan Ekstrak Biji Pinang sebagai Inhibitor Kerak Kalsium Karbonat (CaCO3) dengan Metode Unseeded Experiment" Dengan segenap jiwa yang dilandasi dengan
ketulusan hati, penulis mengucapkan terima kasih kepada :
1. Ummiku dan Abiku tercinta yang telah menguliahkanku hingga selesai serta
doa dan pengorbanannya selama ini.
2. Bapak Prof. Suharso, Ph.D selaku Dekan Fakultas Matematika dan Ilmu
Pengetahuan Alam Universitas Lampung, dosen pembimbing I yang telah
bersedia membimbing penulis, memberikan saran dan kritik hingga penulis
dapat menyelesaikan penelitian;
3. Ibu Prof. Dr. Buhani, M.Si selaku dosen pembimbing II yang telah berkenan
membimbing penulis, memberikan saran dan kritik pada skripsi yang
4. Bapak Prof. Sutopo Hadi, Ph.D selaku dosen pembahas, yang telah
memberikan banyak masukan, baik saran maupun kritik kepada penulis;
5. Ibu Dian Septiani, M.Si yang telah memberikan pengarahan dan bimbingan,
terimakasih banyak;
6. Bapak Dr. Eng. Suripto Dwi Yuwono selaku Ketua Jurusan Kimia FMIPA
Universitas Lampung;
7. Seluruh dosen kimia FMIPA Unila yang telah dengan senang hati
memberikan ilmu pengetahuan yang sangat berguna kepada penulis selama
kuliah;
8. Keluarga tercinta dan tersayang keberadaan kalian merupakan anugerah
terindah dalam hidupku;
9. Sahabat-sahabatku tersayang, Indah Aprianti , Lailatul Hasanah, Putri
Heriyani Utami, Rina Rachmawati Sutisna dan Widya Afriliani Wijaya,
yang selalu menemaniku dan memberikan arahan, semoga kita masih bisa
berkumpul bersama, aamiin;
10. Patner Tercinta, Silvana Maya Pratiwi yang telah menemani di
Laboratorium Anorganik selama ini;
11. Teman-teman 2010, kakak tingkat, dan adik tingkat yang telah meberi
motivasi pada penulis;
12. Aprian Agung Budiman yang selalu memberikan semangat dan waktu
dalam penyelesaian skripsi ini. Semoga selesainya skripsi ini jadi awal yang
13. Seluruh karyawan/karyawati Jurusan Kimia, Mba Nora, Mba Liza, Uni
Kidas, Mb Iin, Mas Udin, Mas Nomo, Pak Man, Mba Win atas bimbingan,
dan perhatian yang telah diberikan kepada penulis;
14. Seluruh teman-teman kimia 2007-2013;
15. Semua pihak yang telah membantu dan mendukung penulis dalam
penelitian dan penyusunan skripsi ini.
Akhir kata, penulis menyadari bahwa skripsi ini masih jauh dari kesempurnaan,
akan tetapi sedikit harapan semoga skripsi yang sederhana ini dapat berguna dan
bermanfaat bagi kita semua. Amiin
Bandar Lampung, 21 Agustus 2014 Penulis
DAFTAR ISI A. Proses Pengendapan Senyawa Anorganik pada Peralatan Industri ... 5
B. Kristalisasi ... 5
C. Kerak ... 7
D. Faktor Pembentukan Kristal ... 9
E. Kalsium Karbonat (CaCO3) ... 10
F. Pengaruh Terbentuknya Kerak Kalsium Karbonat ... 11
G. Metode Pencegahan Terbentuknya Kerak CaCO3 ... 12
1. Pengendalian pH ... 12
2. Pelunakan dan Pembebasan Mineral Air ... 13
3. Penggunaan Inhibitor Kerak ... 13
H. Tanaman Pinang dan Kandungan di dalamnya ... 16
I. KomponenKimia Biji Pinang ... 17
J. Asam Tanat ... 18
K. Analisis Menggunakan Metode Seeded Experiment,Scanning Electron Microscopy (SEM) dan Instrument Particle Size Analyzer (PSA) ... 19
2. Instrumentasi SEM ... 19
a. Penentuan Laju Pertumbuhan CaCO3 tanpa Penambahan Inhibitor pada Konsentrasi yang Berbeda ... 25
b. Penentuan Laju Pertumbuhan CaCO3 dengan Penambahan Inhibitor pada Konsentrasi yang Berbeda ... 26
4. Analisis Data ... 27
IV. HASIL PENGAMATAN DAN PEMBAHASAN A. Analisis Ekstrak Biji Pinang dengan Menggunakan Spektrofotometer Infra Merah (IR) ... 28
B. Penentuan Laju Pertumbuhan Kristal Kalsium Karbonat (CaCO3) dengan Variasi Konsentrasi Larutan Pertumbuhan dan Tanpa Penambahan Inhibitor ... 30
C. Penentuan Laju Pertumbuhan Kristal Kalsium Karboat (CaCO3) dengan Variasi Konsentrasi Inhibitor dan Variasi Konsentrasi Larutan Pertumbuhan ... 31
1. Penentuan Laju Pertumbuhan Inti Kristal Kalsium Karbonat (CaCO3) dengan Variasi Konsentrasi Inhibitor pada Larutan Pertumbuhan 0,050 M ... 31
2. Penentuan Laju Pertumbuhan Inti Kristal Kalsium Karbonat (CaCO3) dengan Variasi Konsentrasi Inhibitor pada Larutan Pertumbuhan 0,075 M ... 34
3. Penentuan Laju Pertumbuhan Inti Kristal Kalsium Karbonat (CaCO3) dengan Variasi Konsentrasi Inhibitor Pada Larutan Pertumbuhan 0,100 M ... 35
D. Analisis Distribusi Ukuran Partikel Kerak CaCO3 Menggunakan PSA ... 38
E. Analisis Permukaan Kerak CaCO3 Menggunakan SEM ... 40
LAMPIRAN
DAFTAR TABEL
Halaman
1. Data persentase efektivitas inhibitor pada larutan
pertumbuhan0,050 M ... 33
2. Data persentase efektivitas inhibitor pada larutan
pertumbuhan0,075 M ... 35
3. Data persentase efektivitas inhibitor pada larutan
DAFTAR GAMBAR
Halaman
1. Tahapan Kristalisasi ... 7
2. Skema Umum Mekanisme Pembentukan Deposit Kerak Air ... 9
3. Reaksi Hidrolisis Polifosfat ... 15
4. Biji pinang ... 17
5. Struktur Asam Tanat ... 18
6. Skema Bagan SEM ... 20
7. Diagram Proses Fraksinasi Massa Dalam Sedigraf ... 22
8. Hasil Analisis IR Ekstrak Biji Pinang ... 28
9. Grafik Perbandingan Pola Pertumbuhan Inti Kristal CaCO3 dengan Variasi Konsentrasi Larutan Pertumbuhan dan Tanpa Penambahan Inhibitor ... 30
10. Grafik Pola Pertumbuhan Inti Kristal CaCO3 pada Konsentrasi Larutan Pertumbuhan 0,050 M dengan dan tanpa Penambahan Inhibitor Ekstrak Biji Pinang ... 32
11. Grafik Pola Pertubuhan Inti Kristal CaCO3 pada Konsentrasi Larutan Pertumbuhan 0,075 M dengan dan tanpa Penambahan Inhibitor Ekstrak Biji Pinang ... 34
Larutan Pertumbuhan 0,100 M dengan dan tanpa Penambahan
Inhibitor Ekstrak Biji Pinang ... 36
13. Mekanisme Dispersancy ... 38
14. Grafik Distribusi Ukuran Partikel CaCO3 0,05 M dengan dan tanpa
Penambahan Inhibitor Ekstrak Biji Pinang 250 ppm dengan
Menggunakan Metode Unseeded Experiment dalam % Volume ... 39
15. Morfologi Kerak CaCO3 0,05 M dengan Metode Unseeded
Experiment dengan dan tanpa Penambahan Ekstrak Biji Pinang
1
I. PENDAHULUAN
A. Latar Belakang
Endapan kerak merupakan salah satu masalah yang serius dalam dunia
perindustrian dan umumnya banyak dijumpai pada peralatan-peralatan industri
minyak dan gas, proses desalinasi, ketel serta industri kimia (Badr and Yassin,
2007; Lestari dkk., 2004).
Kerak adalah tumpukan keras dari bahan anorganik yang disebabkan oleh
pengendapan partikel mineral dalam air terutama pada permukaan perpindahan
panas. Seperti air menguap dalam menara pendingin, uap yang murni hilang dan
konsentrasi padatan terlarut dalam air yang tersisa. Jika konsentrasi siklus ini
dibiarkan berlanjut, berbagai kelarutan padat akhirnya akan terlampaui. Padatan
kemudian akan menetap di dalam pipa atau pada permukaan pertukaran panas, di
mana ia sering membeku menjadi kerak (Bhatia, 2003).
Terbentuknya kerak tersebut telah menjadi masalah yang cukup serius di bidang
industri terutama industri minyak dan gas. Salah satu contoh yang merasakan
dampak dari terbentuknya kerak tersebut adalah perusahaan minyak Indonesia
yakni perusahaan pertamina yang harus mengeluarkan dana sebesar 6-7 juta dolar
2
mengatasi masalah kerak (Suharso et al., 2010). Terbentuknya kerak pada
pipa-pipa industri tersebut akan memperkecil diameter dan menghambat aliran
fluida pada sistem pipa tersebut. Terganggunya aliran fluida ini akan
menyebabkan suhu semakin naik dan tekanan semakin tinggi sehingga
kemungkinan pipa akan pecah semakin tinggi (Asnawati, 2001).
Dampak negatif yang ditimbulkan karena adanya penimbunan kerak antara lain
menyebabkan sumur pipa pada industri panas bumi pembangkit tenaga listrik
hanya berumur 10 tahun. Setelah itu perusahaan harus membuat kembali sumur
pipa dengan biaya 6-7 juta dolar per sumur atau setara dengan Rp 60-70 milyar.
Akibatnya biaya dan kerugian yang ditimbulkan sangat besar untuk oprasional
biaya perawatan (Suharso et al., 2010). Kerak juga dapat dicegah menggunakan
asam untuk menurunkan pH larutan, rentang pH efektif untuk mencegah
pengendapan kerak adalah 6,5 sampai 8,0. Namun menghilangkan kerak
menggunakan asam dengan konsentrasi tinggi tidak efektif karena dapat
meningkatnya laju korosi yang cukup tinggi, serta mempunyai bahaya yang cukup
tinggi dalam penangannya (Lestari, 2008).
Adapun komponen-komponen kerak yang sering dijumpai pada peralatan industri
yaitu, kalsium karbonat (CaCO3), kalsium dan seng fosfat, kalsium sulfat
(CaSO4), serta silika dan magnesium silikat (Lestari dkk., 2004). Beberapa
metode yang pernah dilakukan untuk mencegah terbentuknya kerak kalsium sulfat
pada peralatan-peralatan industri yaitu dengan menurunkan pH larutan melalui
penambahan asam, penggunaan senyawa-senyawa anorganik (Zhang and Dawe,
3
(Donachy and Sikes, 1994 dan Jones et al., 2005) dan senyawa-senyawa organik
lain (He et al., 1999). Selain beberapa metode di atas, pembentukkan kerak dapat
dikontrol dengan cara pelunakkan dan pembebasan mineral air, akan tetapi
penggunaan air bebas mineral dalam industri-industri besar membutuhkan biaya
yang cukup tinggi. Hal ini karena sebagian besar biaya ditujukan untuk
menyediakan air bebas mineral. Penghambatan pertumbuhan kristal tampaknya
menjadi metode yang paling efisien mengendalikan kerak CaCO3, CaF2,
CaSO4.2H2O dan BaSO4. Efektivitas inhibitor kerak tergantung pada kemampuan
sebuah aditif untuk mengganggu langkah-langkah pembentukan kerak, yaitu baik
dengan langkah nukleasi atau dengan pertumbuhan kristal (Tzotzi et al., 2007).
Berdasarkan penelitian yang telah dilakukan sebelumnya (Asmarani, 2011),
diketahui bahwa asam tanat (tanin) yang terdapat pada tanaman, seperti tanaman
gambir dapat digunakan sebagai inhibitor pertumbuhan kerak kalsium karbonat.
Seperti halnya gambir, senyawa yang dominan pada biji pinang adalah tanin dan
alkaloid. Kandungan tanin sekitar 15 dan alkaloid 0,3-0,6% sehingga
memungkinkan tanaman ini untuk dijadikan inhibitor yang cukup efektif dalam
menghambat laju pertumbuhan kerak kalsium karbonat pada pipa-pipa industri.
Karena alasan tersebut maka pada penelitian ini telah mempelajari pengaruh
penambahan senyawa ekstrak biji pinang sebagai inhibitor pada pembentukan
kerak CaCO3 dengan metode unseeded experiment pada konsentrasi larutan
4
B. Tujuan Penelitian
Adapun tujuan dilakukannya penelitian ini adalah :
1. mengetahui manfaat penambahan senyawa ekstrak biji pinang sebagai
inhibitor kerak CaCO3 pada konsentrasi yang berbeda;
2. mendapatkan perbandingan efektifitas penambahan senyawa ekstrak biji
pinang sebagai inhibitor kerak CaCO3.
C. Manfaat Penelitian
Manfaat dari penelitian ini adalah untuk memberikan pengetahuan mengenai
pencegahan timbulnya kerak CaCO3 dengan metode unseeded experiment, dan
dapat dikembangkan untuk memperoleh inhibitor kerak yang efektif, terutama
untuk mencegah pembentukan kerak pada peralatan-peralatan industri supaya
5
II. TINJAUAN PUSTAKA
Dalam tinjauan pustaka ini akan diuraikan mengenai hal-hal yang berhubungan
dengan kerak, proses pembentukkan kerak, pencegahan dan jenis-jenis analisis,
antara lain:
A. Proses Pengendapan Senyawa Anorganik Pada Peralatan Industri
Prosespengendapan senyawa-senyawa anorganik biasa terjadi pada
peralatan-peralatan industri yang melibatkan air garam seperti industri minyak dan gas,
proses desalinasi dan ketel serta industri kimia. Hal ini disebabkan karena
terdapatnya unsur-unsur anorganik pembentuk kerak seperti logam kalsium dalam
jumlah yang melebihi kelarutannya pada keadaan kesetimbangan.
Terakumulasinya endapan-endapan dari senyawa anorganik tersebut dapat
menimbulkan masalah seperti kerak (Weijnen et al.,1983 ; Maley, 1999).
B. Kristalisasi
Kristalisasi merupakan peristiwa pembentukan partikel-partikel zat padat dalam
suatu fase homogen. Kristalisasi dari larutan dapat terjadi jika padatan terlarut
dalam keadaan berlebih (di luar kesetimbangan), maka sistem akan mencapai
6
Kristalisasi senyawa dalam larutan langsung pada permukaan transfer panas
dimana kerak terbentuk memerlukan tiga faktor simultan yaitu konsentrasi lewat
jenuh (supersaturation), nukleasi (terbentuknya inti kristal) dan waktu kontak
yang memadai. Pada saat terjadi penguapan, kondisi jenuh (saturation) dan
kondisi lewat jenuh (supersaturation)dicapai secara simultan melalui pemekatan
larutan dan penurunan daya larut setimbang saat kenaikan suhu menjadi suhu
penguapan. Dalam keadaan larutan lewat jenuh beberapa molekul akan bergabung
membentuk inti kristal.Inti kristal ini akan terlarut bila ukurannya lebih kecil dari
ukuran partikel kritis (inti kritis), sementara itu kristal-kristal akan berkembang
bila ukurannya lebih besar dari partikel kritis. Apabila ukuran inti kristal menjadi
lebih besar dari inti kritis, maka akan terjadi pertumbuhan kristal.
Laju pertumbuhan kristal ditentukan oleh laju difusi zat terlarut pada permukaan
kristal dan laju pengendapan zat terlarut pada kristal tersebut. Daya dorong difusi
zat-zat terlarut adalah perbedaan antara konsentrasi zat-zat terlarut pada
permukaan kristal dan pada larutan. Kristal-kristal yang telah terbentuk
mempunyai muatan ion lebih rendah dan cenderung untuk menggumpal sehingga
7
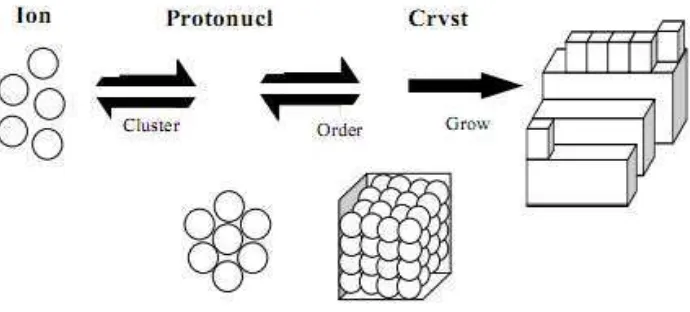
Proses pembentukkankristalisasi ditunjukkan pada gambar berikut:
Gambar 1.Tahapan kristalisasi(Zeiheret al., 2003).
C. Kerak
Kerak didefinisikan sebagai suatu deposit dari senyawa-senyawa anorganik yang
terendapkan dan membentuk timbunan kristal pada permukaan suatu subtansi
(Kemmer, 1979). Kerak terbentuk karena tercapainya keadaan larutan lewat
jenuh.Kerak juga dapat terbentuk karena campuran air yang digunakan tidak
sesuai. Campuran air tersebut tidak sesuai jika air berinteraksi secara kimia dan
mineralnya mengendap jika dicampurkan. Contoh tipe air yang tidak sesuai
adalah air laut dengan konsentrasi SO42- tinggi dan konsentrasi Ca2+ rendah dan
air formasi dengan konsentrasi SO42- sangat rendah tetapi konsentrasi Ca2+ tinggi.
Campuran air ini menyebabkan terbentuknya endapan CaSO4 (Badr andYassin,
2007).
Pembentukan kerak pada sistem perpipaan di industri maupun rumah tangga
menimbulkan banyak permasalahan teknis dan ekonomis.Hal ini disebabkan
8
sekaligus menghambat proses perpindahan panas pada peralatan penukar panas.
Sehingga,kerak yang terbentuk pada pipa-pipa akan memperkecil diameter dan
menghambat aliran fluida pada sistem pipa tersebut.
Terganggunya aliran fluida menyebabkan suhu semakin naik dan tekanan semakin
tinggi maka kemungkinan pipa akan pecah dan rusak (Patton, 1981). Adapun
komponen-komponen kerak yang sering dijumpai pada peralatan industri
yaitu,kalsium sulfat (CaSO4), kalsium karbonat (CaCO3 turunan dari kalsium
bikarbonat),kalsium dan seng fosfat, kalsium fosfat, silika dengan konsentrasi
tinggi, besi dioksida (senyawa yang disebabkan oleh kurangnya kontrol korosi
atau alami berasal dari besi yang teroksidasi), besi fosfat ( senyawa yang
disebabkan karena pembentukan lapisan film dari inhibitor fosfat), mangan
dioksida (mangan teroksidasi tingkat tinggi) magnesium silika, silika dan
magnesium pada konsentrasi tinggi dengan pH tinggi, magnesium karbonat,
magnesium dengan konsentrasi tinggi dan pH tinggi serta CO2 tinggi (Lestari,
2008; Nunn, 1997).
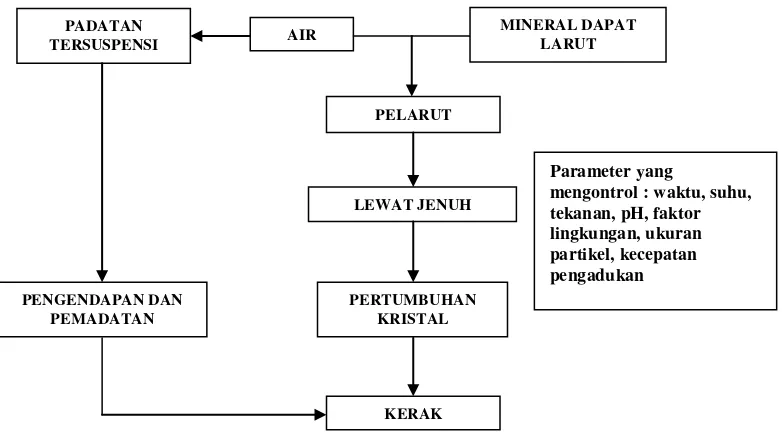
Skema mekanisme pembentukan kerak yang dilengkapi parameter-parameter
9
Gambar 2. Skema umum mekanisme pembentukan deposit kerak air(Salimin dan Gunandjar, 2007).
D. Faktor Pembentuk Kristal
Ukuran kristal yang terbentuk selama pengendapan, tergantung terutama pada dua
faktor penting, yaitu laju pembentukkan inti (nukleasi) dan laju pertumbuhan
kristal. Laju pembentukkan inti dapat dinyatakan dengan jumlah inti yang
terbentuk dalam satuan waktu. Jika laju pembentukkan inti tinggi, banyak sekali
kristal yang akan terbentuk yang terdiri dari partikel-partikel kecil. Laju
pembentukkan inti tergantung pada derajat lewat jenuh dari larutan. Semakin
tinggi derajat lewat jenuh maka semakin besar kemungkinan untuk membentuk
inti baru sehingga akan semakin besar laju pembentukkan inti. Laju pertumbuhan
kristal merupakan faktor penting lainnya yang akan mempengaruhi ukuran kristal
yang terbentuk selama pengendapan berlangsung. Semakin tinggi laju
pertumbuhan maka akan kristal yang terbentuk akan besar. Laju pertumbuhan
kristal juga tergantung pada derajat lewat jenuh (Svehla, 1990).
10
E. Kalsium Karbonat (CaCO3)
Kalsium karbonat (CaCO3) merupakan suatu zat padat putih, tak berbau, tak
berasa, terurai pada 825oC, tak beracun, larut dalam asam dengan melepas CO2,
dan dijumpai di alam sebagai kalsit, napal, aragonit, travertin, marmer, batu
gamping, dan kapur, juga ditemukan bersama mineral dolomit (CaCO3.MgCO3).
Benar-benar tidak larut dalam air (hanya beberapa bagian per juta), kristalnya
berwujud rombik/rombohedral dan dimanfaatkan sebagai obat penawar asam,
dalam pasta gigi, cat putih, pembersih, bahan pengisi kertas, semen, kaca, plastik,
dan sebagainya.
Kalsium karbonat (CaCO3) merupakan salah satu endapan penyusun kerak yang
menjadi masalah serius pada sebagian besar proses industri yang melibatkan air
garam (Amjad, 1995) dan pada operasi produksi minyak bumi
(Halimatuddahliana, 2003). Kalsium karbonat(CaCO3) dibuat dari reaksi CaCl2 +
Na2CO3dalam air, atau melewatkan CO2 melalui suspensi Ca(OH)2 dalam air yang
murni. Kalsium karbonat (CaCO3) berupa endapan amorf putih terbentuk dari
reaksi antara ion kalsium (Ca2+) dalam bentuk CaCl2 dengan ion karbonat (CO32-)
dalam bentuk Na2CO3 (Svehla, 1990).
Ca2+ + CO32- CaCO3
Karbonat dari kalsium tidak larut dalam air dan hasil kali kelarutannya menurun
11
Kelarutan CaCO3 yang sedikit dapat terbentuk jika larutan lewat jenuh dalam
tempat pengolahannya terjadi kesetimbangan kimia dengan lingkungannya pada
tekanan dan temperatur yang sebenarnya.Kesetimbangan CaCO3 dapat diganggu
dengan pengurangan gas CO2 dari aliran selama proses produksi berlangsung. Ini
akan mengakibatkan pengendapan sehingga terbentuk kerak. Pengendapan
CaCO3 dapat dihasilkan dari reaksi sebagai berikut :
CO2 + 2 OH- CO32- + H2O
Ca(OH)2 Ca2+ + 2 OH-
Ca2+ + CO32- CaCO3
(Zhang et al., 2002).
F. Pengaruh Terbentuknya Kerak Kalsium Karbonat (CaCO3)
Kerak kalsium karbonat (CaCO3) yang sering dijumpai pada pipa-pipa peralatan
industri dapat menimbulkan masalah-masalah seperti mengecilnya diameter pipa
sehingga menghambat aliran fluida pada sistem pipa tersebut. Terganggunya
aliran fluida menyebabkan suhu semakin naik dan tekanan semakin tinggi
sehingga kemungkinan pipa akan pecah (Asnawati, 2001). Pada operasi produksi
minyak bumi, pembentukan kerak dapat mengurangi produktivitas sumur akibat
tersumbatnya penorasi, pompa, valve, dan fitting (Halimatuddahliana, 2003).Oleh
karena itu, perlu dilakukan pencegahan pembentukan kerak untuk mengurangi
atau menghilangkan kerak kalsium karbonat yang terdapat pada
12
G. Metode Pencegahan Terbentuknya Kerak CaCO3
Beberapa metode yang digunakan untuk mencegah terbentuknya kerak kalsium
karbonat pada peralatan-peralatan industri adalah sebagai berikut :
1. Pengendalian pH
Pengendalian pH dengan penginjeksian asam (asam sulfat atau asam klorida) telah
lama diterapkan untuk mencegah pertumbuhan kerak oleh garam-garam kalsium,
garam logam bivalen dan garam fosfat (Lestari dkk.,2004). Asam sulfat yang
biasa digunakan pada metode ini akan bereaksi dengan ion karbonat yang ada di
air menghasilkan H2O dan CO2 sehingga pembentukan kerak CaCO3 dapat
dicegah (Al-Deffeeri, 2006).
CaCO3 + 2H+ Ca2+ + H2O + CO2
Kelarutan bahan pembentuk kerak biasanya meningkat pada pH yang lebih
rendah. Namun pada pH 6,5 atau kurang, korosi pada baja, karbon, tembaga, dan
paduan tembaga dengan cepat akan berlangsung sehingga pH efektif untuk
mencegah pengendapan kerak hanyalah pada pH 7 sampai 7,5.
Oleh karena itu, suatu sistem otomatis penginjeksian asam diperlukan untuk
mengendalikan pH secara tepat.Selain itu, asam sulfat dan asam klorida
mempunyai tingkat bahaya yang cukup tinggi dalam penanganannya. Saat ini,
penghambatan kerak dengan hanya penginjeksian asam semakin jarang digunakan
13
2. Pelunakan dan Pembebasan Mineral Air
Untuk mencegah terjadinya kerak pada air yang mengandung kesadahan tinggi
(±250 ppm CaCO3) perlu adanya pelunakan dengan menggunakan kapur dan soda
abu (pengolahan kapur dingin). Masalah kerak tidak akan dijumpai jika yang
digunakan adalah air bebas mineral karena seluruh garam-garam terlarut dapat
dihilangkan. Oleh karena itu, pemakaian air bebas mineral merupakan metode
yang tepat untuk menghambat kerak di dalam suatu sistem dengan pembebanan
panas tinggi dimana pengolahan konvensional dengan bahan penghambat kerak
tidak berhasil (Lestari dkk., 2004). Namun penggunaan air bebas mineral dalam
industri-industri besar membutuhkan biaya yang cukup tinggi sehingga dapat
menurunkan efisiensi kerja.
3. Penggunaan Inhibitor Kerak
Inhibitor kerak pada umumnya merupakan bahan kimia yang sengaja ditambahkan
untuk mencegah atau menghentikan terbentuknya kerak bila ditambahkan dengan
konsentrasi yang kecil ke dalam air (Halimatuddahliana, 2003). Prinsip kerja dari
inhibitor kerak adalah pembentukan senyawa kompleks (kelat) antara inhibitor
dengan unsur-unsur penyusun kerak.Senyawa kompleks yang terbentuk larut
dalam air sehingga menutup kemungkinan pertumbuhan kristal yang besar dan
mencegah kristal kerak untuk melekat pada permukaan pipa (Patton, 1981).
Biasanya, penggunaan bahan kimia tambahan untuk mencegah pembentukan
14
mekanis permukaan bagian dalam pipa.Syarat yang harus dimiliki senyawa kimia
sebagai inhibitor kerak adalah sebagai berikut:
1. inhibitor kerak harus menunjukkan kestabilan termal yang cukup dan
efektif untuk mencegah terbentuknya air sadah dari pembentukkan
kerak;
2. inhibitor kerak juga harus dapat merusak struktur kristal dan padatan
tersuspensi lain yang mungkin akan terbentuk;
3. selain itu, inhibitor kerak juga harus memiliki tingkat keamanan yang
tinggi dalam penggunaannya sehingga tidak menimbulkan efek samping
yang berbahaya bagi lingkungan sekitar (Al-Deffeeri, 2006).
Pada umumnya inhibitor kerak yang digunakan di ladang-ladang minyak atau
pada peralatan industri dibagi menjadi dua macam yaitu inhibitor kerak anorganik
dan inhibitor kerak organik.Senyawa anorganik fosfat yang umum digunakan
sebagai inhibitor adalah kondesat fosfat dan dehidrat fosfat. Pada dasarnya
bahan-bahan kimia ini mengandung grup P-O-P dan cenderung untuk melekat
pada permukaan kristal. Inhibitor kerak organik yang biasa digunakan adalah
organofosfonat organofosfat ester dan polimer-polimer organik. Inhibitor kerak
yang pernah digunakan yaitu polimer-polimer yang larut dalam air dan senyawa
fosfonat (Asnawati, 2001).
Salah satu inhibitor kerak dari polimer-polimer yang larut dalam air yaitu
polifosfat.Polifosfat merupakan inhibitor kerak yang murah namun keefektifannya
15
(CaCO3) antara lain karena kemampuannya untuk menyerap pada permukaan
kristal yang mikroskopik, menghambat pertumbuhan kristal pada batas
konsentrasi rendah dan strukturnya yang mampu merusak padatan tersuspensi.
Hal ini dapat mencegah pertumbuhan kristal lebih lanjut, atau setidaknya
memperlambat proses pertumbuhan kerak. Namun, polifosfat memiliki
kelemahan utama yaitu mudah terhidrolisis pada temperatur di atas 90°C
menghasilkan ortofosfat.
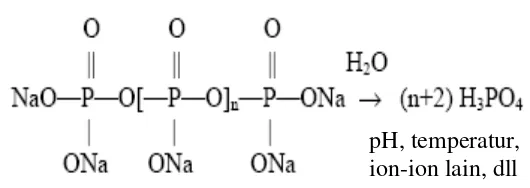
Gambar 3.Reaksi hidrolisis polifosfat (Gill, 1999).
Reaksi di atas adalah reaksi hidrolisis polifosfat yang merupakan fungsi dari
temperatur, pH, waktu, dan adanya ion-ion lain.Ortofosfat yang dihasilkan dapat
menyebabkan menurunnya kemampuan untuk menghambat pertumbuhan kerak
dan menyebabkan terbentuknya kerak baru dari presipitasi kalsium fosfat (Gill,
1999), sehingga penggunaan polifosfat sebagai inhibitor kerak hanya efektif pada
temperatur rendah (Al-Deffeeri, 2006).
Fosfonat merupakan inhibitor yang sangat baik bila dibandingkan dengan
polifosfat. Namun fosfonat masih memiliki kelemahan yaitu struktur fosfonat pH, temperatur,
16
yang monomerik sehingga tidak efektif jika digunakan sebagai dispersing
agents(bahan pembantu untuk mendispersi)(Al-Deffeeri, 2006).
Penggunaan senyawa-senyawa anorganik (Zhang and Dawe, 2000), asam amino
(Manoli et al., 2003), polimer-polimer yang larut dalam air seperti poliaspartat
(Donachy and Sikes, 1994), polifosfat dan senyawa-senyawa lain seperti fosfonat,
karboksilat (Al-Deffeeri, 2006), dan sulfonat telah diketahui sangat efektif sebagai
inhibitor endapan kalsium karbonat (CaCO3) (He et al., 1999).
H. Tanaman Pinang dan Kandungan di dalamnya
Pinang sirih (Areca catechu L), merupakan salah satu tanaman obat yang banyak
dimanfaatkan untuk tujuan komersial karena memiliki nilai ekonomis yang tinggi
dalam berbagai bidang, hanya belum banyak dikelola.Biji pinang mengandung 0,3
– 0,6 % alkaloid, seperti arekolin (C8H13NO2), arekolidine, arekain, guvakolin,
guvasine dan isoguvasine. Selain itu juga mengandung red tanin 15 %, lemak 14
%, kanji dan resin. Biji segar mengandung kira-kira 50 % lebih banyak alkaloid
dibandingkan biji yang telah diproses (Sugianto, 2010). Tanin adalah salah satu
senyawa yang terkandung dalam buah pinang yang kadarnya cukup tinggi. Tanin
diperoleh dengan cara ekstraksi dengan pelarut air dan etanol karena tanin dapat
larut dalam pelarut tersebut.Tanin merupakan senyawa yang sangat penting
17
Gambar 4. Biji Pinang.
Klaifikasi Tanaman Pinang :
Regnum : Plantae
Divisi : Magnoliophyta
Kelas : Liliopsida
Ordo : Arecaceae
Genus : Areca
Spesis : Areca catechu L.
I. Komponen Kimia Biji Pinang
Biji buah pinang mengandung alkaloid, seperti arekolin (C8 H13 NO2),
arekolidine, arekain, guvakolin, guvasine dan isoguvasine, tanin terkondensasi,
tanin terhidrolisis, flavan, senyawa fenolik, asam galat, getah, lignin, minyak
menguap dan tidak menguap, serta garam (Wang and Lee, 1996). Nonaka (1989)
18
tanin terkondensasi yang termasuk dalam golongan flavonoid. Proantosianidin
mempunyai efek antibakteri, antivirus, antikarsinogenik, inflamasi,
anti-alergi, dan vasodilatasi (Fine, 2000).
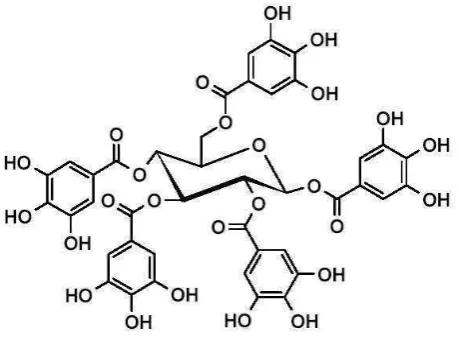
J. Asam Tanat
Asam tanat merupakan unsur dasar dalam zat warna kimia tanaman.Asam tanat
banyak terdapat dalam kayu oak, walnut, mahogani, dan gambir.Asam tanat
merupakan salah satu golongan tanin terhidrolisis dan termasuk asam
lemah.Rumus kimia dari asam tanat adalah C41H32O26.Pusat molekul dari asan
tanat adalah glukosa, dimana gugus hidroksil dari karboksilat terestrifikasi dengan
gugus asam galat.Ikatan ester dari asam tanat mudah mengalami hidrolisis dengan
bantuan katalis asam, basa, enzim, dan air panas. Hidrolisis total dari asan tanat
akan menghasilkan karboksilat dan asam galat (Hagerman,2002).
19
K. Analisis Menggunakan Metode Unseeded Experiment,Scanning Electron Microscopy (SEM) dan Instrument Particle Size Analyzer (PSA)
Pada penelitian ini dilakukan beberapa analisis terhadap kristal CaCO3 yang
terbentuk. Analisis tersebut meliputi analisis unseeded experiment, analisis
morfologi permukaan kristal CaCO3menggunakan SEM, dan analisis distribusi
ukuran partikel menggunakan PSA. Hal ini bertujuan untuk mengetahui seberapa
efektif ekstrak biji pinangdalam menghambat pembentukkan kerak CaCO3.
A. Unseeded experiment
Unseeded Experiment merupakan salah satu metode pembentukkan kristal dengan
cara tanpa menambahkan bibit kristal ke dalam larutan pertumbuhan. Hal ini
dilakukan untuk melihat laju pertumbuhan kerak kalsium karbonat setelah
ditambahkan senyawa ekstrak biji pinang tanpa penambahan bibit kristal
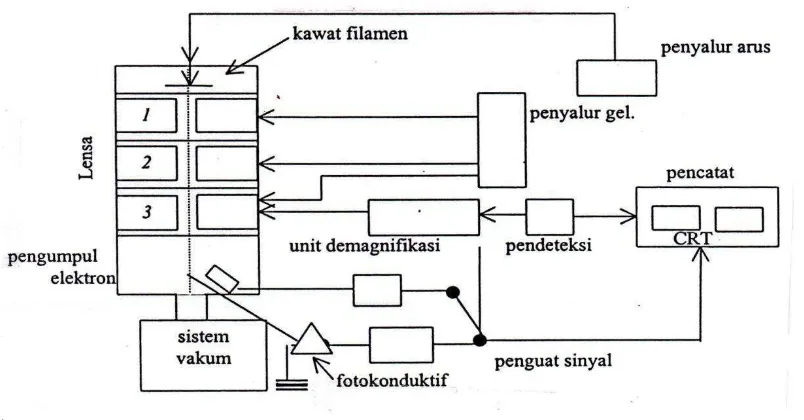
2. Instrumentasi SEM
SEM adalah salah satu jenis mikroskop elektron yang dapat mengamati dan
menganalisis karakteristik struktur mikro dari bahan padat yang konduktif
maupun yang nonkonduktif. Sistem pencahayaan pada SEM menggunakan
radiasi elektron yang mempunyai λ = 200 – 0,1 Å, daya pisah (resolusi) yang
tinggi sekitar 5 nm sehingga dapat dicapai perbesaran hingga ± 100.000 kalidan
menghasilkan gambar atau citra yang tampak seperti tiga dimensi karena
20
gambar atau citra yang lebih baik dibandingkan dengan hasil mikroskop
optik.Aplikasi mikroskop elektron ini tidak hanya terbatas pada analisis logam
dan paduan di bidang metalurgi, melainkan dapat diaplikasikan di berbagai bidang
lain, seperti farmasi, pertanian, biologi, kedokteran, dan industri bahan
elektronika, komponen mesin serta pesawat terbang.
Pada prinsipnya mikroskop elektron dapat mengamati morfologi, struktur mikro,
komposisi, dan distribusi unsur.Untuk menentukan komposisi unsur secara
kualitatif dan kuantitatif perlu dirangkaikan satu perangkat alat EDS (Energy
Dispersive X-ray Spectrometer) atau WDS (Wavelength Dispersive X-ray
Spectrometer) (Handayani dkk., 1996).
`
21
3. Instrumentasi PSA (Sedigraf)
Metode sedigraf digunakan untuk menentukan distribusi ukuran partikel yang
secara luassudah dipakai dalam berbagai aplikasi sejak tahun 1967. Instrumentasi
ini sudah melalui pembuktian dalam kecepatan, kemampuan penanganan sampel,
dan reduksi data dan presentasi sejak diperkenalkan. Dasar metode analisis,
pengukuran partikel dengan mengukur kecepatan dan penentuan fraksinasi massa
dengan kerelatifan absorbsi sinar-X pada energi yang rendah.Sedigraf
menggunakan sinar-X sebagai tanda horizontal tipis untuk mengukur konsentrasi
partikel massa secara langsung dalam medium cairan. Ini dilakukan pada
pengukuran pertama intensitas massa, Imax dari garis dasar atau keterangan atau
informasi yang ditransmisikan sinar-X yang sudah diproyeksikan melalui medium
cairan sebelum pengenalan sampel. Sebagai sirkulasi cairan yang berkelanjutan,
sampel berupa padatan dimasukkan ke wadah cairan dan dicampur sampai
penyebaran aliran suspensi sampel berupa padatan homogen dan penyebaran
cairan dipompa melalui sel.
Sampel berupa padatan lebih banyak mengabsorbsi sinar-X daripada cairan, oleh
karena itu transmisi sinar-X dikurangi. Sejak pencampuran suspensi yang
homogen, intensitas diasumsikan sebagai nilai konstan, Imin, untuk transmisi
sinar-X dalam skala pengurangan yang penuh.
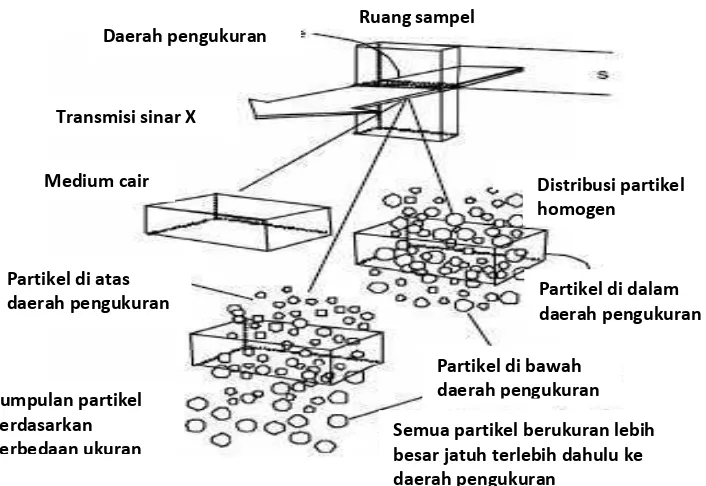
Aliran pencampuran dihentikan dan penyebaran yang homogen dimulai untuk
menyelesaikan pentransmisian intensitas sinar-X yang dimonitor pada depth - s.
Selama proses sedimentasi, partikel yang besar menempati tempat pertama di
22
dan yang tertinggal hanya cairan yang bersih. Semakin banyak partikel besar yang
menempati di bawah zona pengukuran dan tidak digantikan dengan ukuran
partikel yang sama yang menempati dari atas, maka pelemahan sinar-X berkurang
(Webb, 2002).
Gambar 7. Diagram proses fraksinasi massa dalam sedigraf (Webb, 2002).
Ruang sampel besar jatuh terlebih dahulu ke daerah pengukuran
23
III. METODOLOGI PENELITIAN
A. Waktu dan Tempat Penelitian
Penelitian ini dilakukan di Laboratorium Kimia Anorganik Fakultas Matematika
dan Ilmu Pengetahuan Alam Universitas Lampung pada bulan April sampai Juni
2014. Analisis menggunakan Mikroskop Optik dilakukan di Laboratorium
Biologi Universitas Lampung. Selain itu, analisis morfologi menggunakan
instrument SEM (Jeol JSM-6360la) dilakukan di Laboratorium PTBIN BATAN
Serpong dan analisis menggunakan instrument PSA (Coulter LS 1000) dilakukan
di Laboratorium Biomassa Terpadu Universitas Lampung.
B. Alat dan Bahan
Alat-alat yang digunakan pada penelitian ini, yaitu alat-alat gelas yang sering
digunakan di laboratorium, water bath, botol-botol plastik, pengaduk magnet,
oven, neraca analitik merek Airshwoth AA-160, Spektrofotometer IR, Scanning
Electron Microscopy (SEM) merek JEOL jsm-6510la serta Particle Size Analyzer
(PSA) merek Coulter LS 100Q.
Bahan-bahan yang digunakan dalam penelitian ini, yaitu CaCl2 anhidrat, Na2CO3,
24
C. Prosedur Penelitian
1. Pembuatan Ekstrak Biji Pinang
Ekstrak biji pinang dibuat dengan cara mengeringkan buah pinang
dengan menggunakan sinar matahari kurang lebih selama 2 minggu
kemudian dikupas kulitnya dan dipotong-potong bijinya menjadi
kecil-kecil. Untuk menghilangkan kadar air yang masih tersisa pada biji
pinang, biji dikeringkan kembali dengan menggunakan oven dan
ditimbang hingga beratnya konstan, kemudian dihaluskan dengan
menggunakan blender. Selanjutnya dibuat larutan biji pinang dengan
konsentrasi 1000 ppm, sebanyak 1 gram serbuk biji pinang dilarutkan
dalam akuades hingga volumenya mencapai 1 liter dalam gelas bejana.
Larutan tersebut diaduk menggunakan pengaduk magnet selama 2-3 jam
dengan suhu 90 °C kemudian larutan disaring menggunakan kertas
saring. Larutan yang telah disaring tersebut adalah ekstrak dari biji
pinang. Untuk mengetahui kandungan yang terdapat dari ekstrak biji
pinang, dilakukan analisis gugus fungsi menggunakan spektrofotometer
25
2. Pengujian Ekstrak Biji Pinang Sebagai Inhibitor dalam Pengendapan Kristal CaCO3
Tahapan untuk menguji ekstrak biji pinang sebagai inhibitor dalam
pengendapan kristal CaCO3 dengan metode unseeded experiment
dilakukan dengan rangkaian percobaan sebagai berikut:
a. Penentuan Laju Pertumbuhan CaCO3 tanpa Penambahan Inhibitor pada Konsentrasi yang Berbeda
Larutan pertumbuhan dibuat dengan cara melarutkan 0,050 M CaCl2 dan
0,050 M Na2CO3 masing-masing dalam akuades hingga mencapai
volume 200 mL. Masing-masing larutan dimasukkan ke dalam gelas
kimia dan diaduk menggunakan pengaduk magnet selama 10-15 menit
dengan suhu 90 °C untuk menghomogenkan larutan. Selanjutnya, kedua
larutan tersebut dicampur agar terbentuk kerak CaCO3 kemudian
dimasukkan ke dalam 6 gelas plastik masing-masing 50 mL dan
diletakkan dalam water bath pada suhu 90 °C selama 10-15 menit untuk
mencapai kesetimbangan. Pengamatan akan dilakukan setiap lima menit
sekali. Dalam lima menit sekali, satu botol diambil kemudian larutan
dalam botol tersebut disaring menggunakan kertas saring, dicuci dengan
akuades, dan dikeringkan menggunakan oven pada suhu 80 °C selama
3-4 jam. Percobaan ini diulang dengan variasi konsentrasi larutan CaCl2
26
ditimbang untuk mengetahui berat kristal yang terbentuk dan didiamkan
selama 1 hari untuk melihat morfologi kristal yang terbentuk.
b. Penentuan Laju Pertumbuhan CaCO3 dengan Penambahan Inhibitor pada Konsentrasi yang Berbeda
Larutan pertumbuhan dibuat dengan cara melarutkan 0,050 M CaCl2 dan
0,050 M Na2CO3 masing-masing dalam larutan ekstrak biji pinang 50
ppm hingga mencapai volume 200 mL. Masing-masing larutan
dimasukkan ke dalam gelas kimia dan diaduk menggunakan pengaduk
magnet selama 10-15 menit dengan suhu 90 °C untuk menghomogenkan
larutan. Selanjutnya, kedua larutan tersebut dicampur agar terbentuk
kerak CaCO3 kemudian dimasukkan ke dalam 6 gelas plastik
masing-masing 50 mL dan diletakkan dalam water bath pada suhu 90 °C selama
10-15 menit untuk mencapai kesetimbangan. Pengamatan akan
dilakukan setiap lima menit sekali. Dalam lima menit sekali, satu botol
diambil kemudian larutan dalam botol tersebut disaring menggunakan
kertas saring, dicuci dengan akuades, dan dikeringkan menggunakan
oven pada suhu 80 °C selama 3-4 jam. Percobaan ini diulang dengan
variasi konsentrasi larutan CaCl2 dan Na2CO3 sebesar 0,075, 0,100 M.
Selanjutnya, endapan tersebut ditimbang untuk mengetahui berat kristal
yang terbentuk dan didiamkan selama 1 hari untuk melihat morfologi
27
3. Analisa Data
Data yang diperoleh berupa jumlah endapan terhadap waktu dengan
variasi konsentrasi larutan pertumbuhan dan variasi konsentrasi inhibitor,
masing-masing diplot sebagai jumlah endapan terhadap waktu
menggunakan Microsoft Excel. Nilai slope yang diperoleh dari
masing-masing grafik merupakan pertumbuhan kerak CaCO3. Morfologi kerak
CaCO3 sebelum atau sesudah penambahan inhibitor dianalisis
menggunakan SEM. Perubahan ukuran partikel dari kelimpahan kalsium
karbonat pada masing-masing endapan dari setiap percobaan yang
43
V. SIMPULAN DAN SARAN
A. Simpulan
Berdasarkan penelitian yang telah dilakukan, maka diperoleh kesimpulan sebagai
berikut:
1. Senyawa ekstrak biji pinangdapat digunakan sebagai inhibitor
kerakCaCO3.Hal ini dilihat dari perbedaan nilai laju pertumbuhan, morfologi,
dan ukuran partikel inti kristal CaCO3.
2. Pada penelitian ini konsentrasi optimum inhibitor ekstrak biji pinangdalam
menghambat laju pembentukan inti serta pertumbuhan kerak CaCO3
0,05 M adalah 250 ppm dengan keefektifan sebesar 20 %.
3. Analisis menggunakan SEM menunjukkan bahwa morfologi permukaan
kerak CaCO3 sebelum penambahan inhibitor lebih tebal dan besar
permukaannya dibandingkan sesudah penambahan inhibitorsenyawa ekstrak
biji pinang yang terlihat lebih rapuh.
4. Analisis menggunakan PSA menunjukkan bahwa distribusi ukuran partikel
kerak CaCO3 mengalami penurunan setelah ditambahkan inhibitorsenyawa
44
B. Saran
Dengan keterbatasan zat aktif yang terdapat pada inhibitor dalam menghambat
kerak CaCO3, maka penulis memberikan saran yaitu perlu dilakukannya
DAFTAR PUSTAKA
Al-Deffeeri, N. S. 2006. Heat Transfer Measurement as a Criterion For Performance Evaluation of Scale Inhibition in MSF Plants in Kuwait. Desalination. Vol. 204. pp. 423-436.
Amjad, Z. 1995. Kinetics of crystal growth of calcium sulfate dihydrate, The influence of polymer composition, molecular weight, and solution pH. Can. J. Chem. Vol. 66.
Asmarani, D. 2011. Pengaruh Penambahan Senyawa Turunan Kaliksarena dan Ekstrak Gambir Sebagai Inhibitor Kerak Kalsium Sulfat (CaSO4).
(Skripsi Tidak Diterbitkan). Jurusan Kimia FMIPA Universitas
Lampung. Lampung.
Asnawati. 2001. Pengaruh Temperatur Terhadap Reaksi Fosfonat dalam
Inhibitor Kerak pada Sumur Minyak. Jurnal ILMU DASAR. Vol.2.
No.1:20.
Badr, A. and A. A. M. Yassin. 2007. Barium Sulfate Scale Formation in Oil Reservoir During Water Injection at High-Barium Formation Water.
Journal of Applied Sciences. 7 (17) ; 2393-2403.
Bhatia, A. 2003. Cooling Water Problems and Solutions, Continuing Education
and Development, Inc. 9 Greyridge Farm Court Stony Point, NY 10980. Course no: M05-009.
Cotton, F. A dan G. Wilkinson. 1989. Kimia Anorganik Dasar. UI-Press. Jakarta.
Dewi, D.F. dan M. Ali . 2003. Penyisihan Fosfat dengan Proses Kristalisasi dalam Reaktor Terfluidasi Menggunakan Media Pasir Silika. Jurnal
Donachy, J. E. and C. S. Sikes. 1994. Thermal Polycondensation Synthesis of Biomimetic Serine-Containing Derivatives Polyaspartate: Potent Inhibitors of Calsium Carbonate Phosphate Crystallisation. J. Polymer Science. Vol. 32. pp. 789-795.
Engleson, J. 2008. Scale Inhibitors. Avista Technologies, Inc. 133 North Pacific
Street, San Marcos.
Fine, A.M. 2000. Oligomeric Proanthocyanidin Complexes: History, Structure, and phytopharmaceutical Applications, Altern Med
Rev,5(2):144-151.
Gabriel, Bl. 1985. SEM : A User’s Manual for Material Science. American Society for Metal.
Gill, J. S. 1999. A Novel Inhibitor For Scale Control in Water Desalination.
Desalination. Vol. 124. pp. 43-50.
Hagerman, A.E. 2002. Condensed Tannin Structural Chemistry. Department of
Chemistry and Biochemistry, Miami University, Oxford, Ohio 45056.
Halimatuddahliana. 2003. Pencegahan Korosi dan Scale Pada Proses Produksi Minyak Bumi. Laporan Penelitian Universitas Sumatera Utara.
Medan.
Handayani, A., Sumaryo and A. Sitompul. 1996. Teknik Pengamatan
Strukturmikro dengan SEM-EDAX. Makalah Kunjungan dan Demo PTBIN BATAN. Serpong.
Hasson, D. and R. Semiat. 2005. Scale Control in Saline and Wastewater Desalination. Israel Journal of Chemistry. Vol. 46. pp. 97-104.
He, S., A. T. Kan and M. B. Tomson. 1999. Inhibition of Calsium Carbonate Precipitation in NaCl Brines From 25 to 90°C. Applied
Jones, F., M. Mocerino, M. Ogden, A. Oliveria and G. Parkinson. 2005. Bio-inspired Calix[4]Arene Additives for Crystal Growth Modification of Inorganic Materials. Crystal Growth and Design. 5: 2336-2343.
Kemmer, F. N. 1979. The Nalco Water Hand Book. Nalco Chemical Co. Mc
Graw Hill Book CO. New York, 20. pp. 1-19.
Lestari, D. E., G. R. Sunaryo, Y. E. Yulianto, S. Alibasyah dan S. B. Utomo. 2004. Kimia Air Reaktor Riset G.A.Siwabessy. Makalah Penelitian P2TRR dan P2TKN BATAN. Serpong.
Lestari, D.E. 2008. Kimia Air, Pelatihan Operator dan Supervisor Reaktor Riset.
Pusat Pendidikan dan Pelatihan BATAN. Serpong.
Maley, M. 1999. Inhibition of Calcite Nucleation and Growth Using
Phosphonate. Curtin University of Technology Western Australia.
Australia.
Manoli, F., J. Kanakis, P. Malkaj and E. Dalas. 2003. The Effect of Aminoacids on The Crystal Growth of Calsium Carbonate. Journal of Crystal Growth. Vol. 53. pp. 105-111.
Miksic, B. A., A. Y. Furman dan M. A. Kharshan. 2005. Biodegradable and Renewable Raw Materials in a New Generation of Water-Treatment Products. Cortec Corporation. Saint Paul.
Nonaka, G. 1989. Isolation and structure elucidation of tannins. Pure & Appl,
Chem. 61 (3): 357-360.
Nunn, R.G. 1997. Water Treatment Essentials far Boiler Plant Operation. Mc
Graw Hill. New York.Capillary Zone Electrophoresis. Elsevier B.V. Journal of Chromatography A, 934. 113-122.
Patton, C. 1981. Oilfield Water System. 2 ed. Cambeel Petroleum Series.
Salimin, Z., dan Gunandjar. 2007. Penggunaan EDTA sebagai Pencegah
Timbulnya Kerak pada Evaporasi Limbah Radioaktif Cair. Prosiding PPI – PDIPTN. Pustek Akselerator dan Proses Bahan – BATAN.
Yogyakarta.
Sikiric, M.D. dan H. F. Milhofer. 2007. Advances in Colloid and Interface Science. 128-130(2006). Hal 135-158.
Sugianto, R. 2010. http://ridwansugianto.blogspot.com/2010/02/jambe.html. Diakses tanggal 26 maret 2014.
Suharso, Buhani, S. Bachri and T. Endaryanto. 2010. The Use of Gambier
Extracts from West Sumatra as a Green Inhibitor of Calcium Sulfate (CaSO4) Scale Formation. Asian J. Research Chem. Vol. 3(1). pp.
183-187.
Suryadi, E. 1984. Penelitian Pembuuatan Tepung Pinang dan Sifat – Sifat Fisika
Kimianya.Balai Penelitian dan Pengembangan Industri. Banda Aceh
Svehla, G. 1990. Buku Teks Analisis Anorganik Kualitatif Makro dan Semimikro.
Alih Bahasa Oleh L. Setiono dan A. H pudjaatmaka. PT. Kalman Media Pustaka. Jakarta.
Tzotzi, C., T. Pahiadaki, S. G. Yiantsios, A. J. Karabelas, N. Andritsos. 2007. A study of CaCO3 scale formation and inhibition in RO and NF membrane Processes, desalination, vol 296, pp;171-184.
Wang, C.K. and W. H. Lee. 1996. Separation, Characteristics, and Biological Activities of Phenolics in Areca Fruit, J. Agric. Food Chem.,
44(8):2014 -2019.
Webb, P. A., 2002. Interpretation of Particle Size Reported by Different Analytical Technique Diakses melalui www.micromeristics.com
pada tanggal 5 Maret 2009 Pukul 14.00 WIB.
Weijnen, M. P. C., W. G. J. Marchee, and Rosmalen G. M. V. 1983.
Zeiher, E.H.K., H. Bosco, and K. D. Williams. 2003. Novel Antiscalant Dosing Control. Desalination 157. 209-216.
Zhang, Y and R. A. Dawe. 2000. Influence of Mg2+ on The Kinetics of Calcite Precipication and Calcite Crystal Morphology. Chemical Geology.
Vol. 163. pp. 129-138.