KULTUR DAUN PUCUK TANAMAN KEMENYAN (Styrax benzoin
Dryander) PADA MEDIA MS DENGAN PEMBERIAN ATONIK
DAN BAP
SKRIPSI
RICO PRANATA TARIGAN
050805005
DEPARTEMEN BIOLOGI
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
UNIVERSITAS SUMATERA UTARA
KULTUR DAUN PUCUK TANAMAN KEMENYAN (Styrax benzoin
Dryander) PADA MEDIA MS DENGAN PEMBERIAN ATONIK
DAN BAP
SKRIPSI
Diajukan untuk melengkapi tugas dan memenuhi syarat mencapai gelar Sarjana Sains
RICO PRANATA TARIGAN
050805005
DEPARTEMEN BIOLOGI
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
UNIVERSITAS SUMATERA UTARA
PERSETUJUAN
Judul : KULTUR DAUN PUCUK TANAMAN KEMENYAN
(Styrax benzoin Dryander) PADA MEDIA MS DENGAN PEMBERIAN ATONIK DAN BAP
Kategori : SKRIPSI
Nama : RICO PRANATA TARIGAN
Nomor Induk Mahasiswa : 050805005
Program Studi : SARJANA (S1) BIOLOGI
Departemen : BIOLOGI
Fakultas : MATEMATIKA DAN ILMU PENGETAHUAN ALAM
(FMIPA) UNIVERSITAS SUMATERA UTARA
Diluluskan di
Medan, September 2010
Komisi Pembimbing :
Pembimbing 2 Pembimbing 1
Riyanto Sinaga S.Si, M.Si
NIP. 197108 311997 022001 NIP. 196005 231985 022001
Dra. Isnaini Nurwahyuni M.Sc.
Diketahui/Disetujui oleh
Departemen Biologi FMIPA USU Ketua,
PERNYATAAN
KULTUR DAUN PUCUK TANAMAN KEMENYAN (Styrax benzoin Dryander) PADA MEDIA MS DENGAN PEMBERIAN ATONIK DAN BAP
SKRIPSI
Saya mengakui bahwa skripsi ini adalah hasil kerja saya sendiri, kecuali beberapa kutipan dan ringkasan yang masing-masing disebutkan sumbernya.
Medan, September 2010
PENGHARGAAN
Dengan segala kerendahan hati, puji dan syukur penulis panjatkan ke hadirat Tuhan Yesus Kristus yang dengan kasih dan anugerahNya sehingga skripsi ini dapat diselesaikan. Hasil penelitian ini berjudul: ” Kultur Daun Pucuk Tanaman
Kemenyan (Styrax benzoin Dryander) pada Media MS dengan Pemberian Atonik dan BAP”.
Terima kasih penulis sampaikan kepada Ibu Dra. Isnaini Nurwahyuni M.Sc. selaku pembimbing I dan Bapak Riyanto Sinaga S.Si, M.Si selaku pembimbing II yang telah memberikan bimbingan, arahan dan masukannya kepada penulis dalam penyusunan hasil penelitian ini. Penulis juga tidak lupa mengucapkan terima kasih kepada Ketua Departemen Biologi FMIPA USU, Dekan, Pembantu Dekan, dan seluruh pegawai FMIPA USU, Ibu Dra. Elimasni M.Si. selaku Pembimbing Akademik yang telah banyak membimbing penulis selama pendidikan. Ucapan terima kasih juga saya tujukan kepada Bapak dan Ibu dosen di Departemen Biologi FMIPA USU yang telah mendidik dan memberikan ilmu pengetahuan yang bermanfaat selama masa perkuliahan, serta Ibu Roslina Ginting, Abang Raswin, Ibu Nurhasni Muluk dan Bapak Sukirmanto selaku pegawai di Departemen Biologi, FMIPA USU.
Rekan-rekan asisten Lab. Genetika: Siti, Simlah, Riris, Delni, Julita, Kakak Maria dan Ruth. Kepada Abang Franhot atas dukungannya dan Abang David Napitupulu selaku kakak asuh. Terima kasih kepada teman-teman seperjuangan angkatan 2005: Susanti Siagian, Elfrida, Diana, Wulan, Toberni, Ummi, Ochid, Nikma, Masrayanti, Dwi, Sri Zulyani, Seneng, Sarah, Valentyna, Susi, Andini S., Putri, Rebecca, Erna, Erni, Dini, Patimah, Maysarah, Irfan, Misran, Taripar, Efendi, Andi, Dahin, Rahmad, Verta, Kabul, Juned. Saudari dalam dosen penasehat akademik yang sama: Kurniayanti, Widya, Mustika, Susanty SarMut, Fifi, Fitria, Gustin, dan Winda. Adik-adik di Biologi: Raymond (adik asuh), Hilda, Jane, Desmina dan Tetty. Kepada rekan-rekan seluruh saudara-saudari di PKBKB FMIPA USU maju dan tetaplah penuh semangat. Terima kasih untuk tiap tawa dan tangis yang kita lalui bersama, kiranya Tuhan Yesus memberkati.
Tak ada gading yang tak retak. Demikian pula halnya dengan penelitian ini.
Penulis menyadari bahwa penelitian ini masih jauh dari kesempurnaan. Oleh karena itu, penulis mengharapkan kritik dan saran yang bersifat membangun demi kesempurnaan skripsi ini. Akhir kata, demikianlah yang dapat disampaikan. Semoga penelitian ini bermanfaat.
Medan, September 2010
ABSTRAK
Penelitian tentang “Kultur Daun Pucuk Tanaman Kemenyan (Styrax Benzoin
Dryander) Pada Media MS Dengan Pemberian Atonik Dan BAP” telah dilakukan
di Laboratorium Kultur jaringa n Tumbuhan Departemen Biologi Fakultas Matematika dan Ilmu Pengetahuan Alam Universitas Sumatera Utara dari bulan Januari 2010 sampai Mei 2010. Penelitian yang bertujuan untuk mengetahui pengaruh kombinasi atonik dan BAP terhadap pertumbuhan kultur daun pucuk kemenyan (Styrax benzoin Dryander) ini menggunakan Rancangan Acak Lengkap Faktorial dengan 5 taraf atonik yaitu: 0,0; 0,5; 1,0; 1,5; 2,0 ml/L dan 4 taraf BAP yaitu: 0,0; 0,05; 0,5; 5,0 mg/L. Hasil analisis statistik menunjukkan bahwa interaksi kedua zat pengatur tumbuh Atonik dan BAP memberikan pengaruh yang tidak nyata terhadap kultur yang membentuk kalus dan berat basah kultur. Perlakuan yang terbaik berdasarkan kalus yang terbentuk dan berat basah terbaik adalah A2B3 (1 ml/L Atonik + 5 mg/l BAP).
THE LEAF TISSUE CULTURE OF BENZOIN (Styrax Benzoin Dryander) IN MEDIA MS WITH ATONIK AND BAP
ABSTRACT
The research about “The Leaf Tissue Culture Of Benzoin (Styrax Benzoin
Dryander) In MS Media With Atonik And BAP” has been done in Plant Tissue
Culture Laboratory of Biology Department at Faculty of Mathematics and Natural Science, University of Sumatera Utara from Januari 2010 until May 2010. The aim of the research was to obtain the effect of combination Atonik and BAP to the growth of the leaf tissue culture of benzoin (Styrax benzoin Dryander) using Complete Randomized Design and two factors which are 5 level of Atonik concentrations: 0,0; 0,5; 1,0; 1,5; 2,0 ml/L and 4 concentrations of BAP: 0,0; 0,05; 0,5; 5,0 mg/L. The result of statistic analysis indicated that the interaction of Atonic and BAP gives nonsignificant effect to the percentage of callus growth and callus fresh wight. The best treatment of callus growth and callus fresh weight found in media A2B3 (1ml/L
Atonik + 5 mg/l BAP).
DAFTAR ISI
DAFTAR LAMPIRAN vii
DAFTAR GAMBAR viii
BAB 1. Pendahuluan
1.1Latar Belakang 1
1.2Permasalahan 3
1.3Tujuan 3
1.4Hipotesis 3
1.5Manfaat 3
BAB 2. Tinjauan Pustaka
2.1 Botani Kemenyan (Styrax benzoin Dryander) 4
2.2 Teknik Kultur Jaringan 5
2.3 Kultur Daun Pucuk 6
2.8 Kultur Jaringan Kemenyan 11
BAB 3. Bahan dan Metoda
BAB 4. Hasil dan Pembahasan
4.1 Saat Terbentuknya Kalus 18
4.2 Persentase kulur yang membentuk kalus (%) 20
4.4. Warna Kalus 24 4.5 Persentase Terkontaminasi 26
BAB 5. Kesimpulan dan Saran
5.1 Kesimpulan 28
5.2 Saran 28
DAFTAR PUSTAKA 29
DAFTAR TABEL
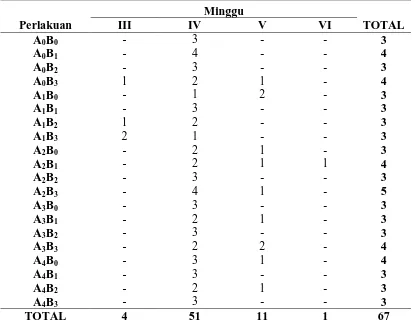
Tabel 4.1.1 Jumlah Kultur yang membentuk kalus per minggu. 19
Tabel 4.2.1 Persentase Kultur yang membentuk kalus (%) 20
DAFTAR GAMBAR
Gambar 1 Tanaman Kemenyan (Styrax benzoin Dryander) 13
Gambar 2 Eksplan Daun Kemenyan 15
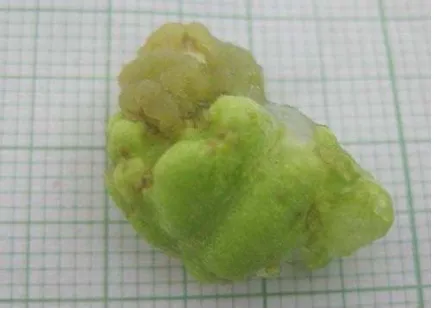
Gambar 3 Kalus Kemenyan 18
Gambar 4 Kalus dengan berat basah tertinggi pada perlakuan A2B3 22
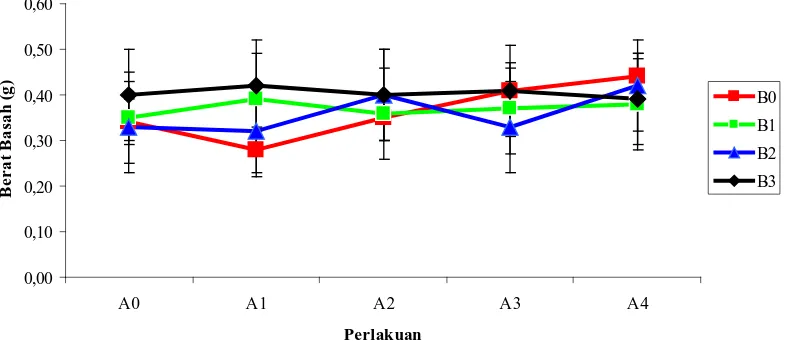
Gambar 5 Hubungan rata-rata berat basah kalus dengan kombinasi ZPT 23
Gambar 6 Warna Kalus 25
DAFTAR LAMPIRAN
Lampiran A Data pengamatan persentase kultur yang hidup 33
Lampiran B Data pengamatan berat basah kultur 34
Lampiran C Data pengamatan persentase kultur terkontaminasi 36
ABSTRAK
Penelitian tentang “Kultur Daun Pucuk Tanaman Kemenyan (Styrax Benzoin
Dryander) Pada Media MS Dengan Pemberian Atonik Dan BAP” telah dilakukan
di Laboratorium Kultur jaringa n Tumbuhan Departemen Biologi Fakultas Matematika dan Ilmu Pengetahuan Alam Universitas Sumatera Utara dari bulan Januari 2010 sampai Mei 2010. Penelitian yang bertujuan untuk mengetahui pengaruh kombinasi atonik dan BAP terhadap pertumbuhan kultur daun pucuk kemenyan (Styrax benzoin Dryander) ini menggunakan Rancangan Acak Lengkap Faktorial dengan 5 taraf atonik yaitu: 0,0; 0,5; 1,0; 1,5; 2,0 ml/L dan 4 taraf BAP yaitu: 0,0; 0,05; 0,5; 5,0 mg/L. Hasil analisis statistik menunjukkan bahwa interaksi kedua zat pengatur tumbuh Atonik dan BAP memberikan pengaruh yang tidak nyata terhadap kultur yang membentuk kalus dan berat basah kultur. Perlakuan yang terbaik berdasarkan kalus yang terbentuk dan berat basah terbaik adalah A2B3 (1 ml/L Atonik + 5 mg/l BAP).
THE LEAF TISSUE CULTURE OF BENZOIN (Styrax Benzoin Dryander) IN MEDIA MS WITH ATONIK AND BAP
ABSTRACT
The research about “The Leaf Tissue Culture Of Benzoin (Styrax Benzoin
Dryander) In MS Media With Atonik And BAP” has been done in Plant Tissue
Culture Laboratory of Biology Department at Faculty of Mathematics and Natural Science, University of Sumatera Utara from Januari 2010 until May 2010. The aim of the research was to obtain the effect of combination Atonik and BAP to the growth of the leaf tissue culture of benzoin (Styrax benzoin Dryander) using Complete Randomized Design and two factors which are 5 level of Atonik concentrations: 0,0; 0,5; 1,0; 1,5; 2,0 ml/L and 4 concentrations of BAP: 0,0; 0,05; 0,5; 5,0 mg/L. The result of statistic analysis indicated that the interaction of Atonic and BAP gives nonsignificant effect to the percentage of callus growth and callus fresh wight. The best treatment of callus growth and callus fresh weight found in media A2B3 (1ml/L
Atonik + 5 mg/l BAP).
BAB 1
PENDAHULUAN
1.1 Latar Belakang
Tanaman kemenyan merupakan tanaman penghasil getah yang merupakan produk
hasil hutan non kayu memiliki nilai ekonomis tinggi. Getah kemenyan sangat
potensial sebagai produk unggulan karena diperlukan sebagai bahan baku obat,
industri parfum, kosmetik, bahan tambahan pembuatan rokok. Getah kemenyan bukan
hanya dibutuhkan secara lokal, akan tetapi sudah merupakan komoditas ekspor (BPS,
2003). Salah satu jenis tanaman kemenyan yang paling baik kualitasnya adalah
kemenyan Toba yang terdapat di daerah Tapanuli Utara. Kemenyan Toba memiliki
beberapa keunggulan kualitas getah yang jauh lebih baik dibandingkan dengan getah
yang berasal dari daerah lain yaitu warna getah yang putih mengkilap dan aroma yang
khas sehingga memiliki harga jual yang cukup tinggi sehingga membuat kemenyan
Tapanuli Utara terkenal di seluruh dunia (Siregar, 2001).
Banyak penduduk di sekitar hutan Tapanuli Utara yang menggantungkan
hidup dari getah kemenyaan, yang pada umumnya masih dijual dalam bentuk bahan
baku mentah. Walaupun kemenyan sudah termasuk komoditas unggulan akan tetapi
budidayanya belum dilakukan dengan baik (Nurwahyuni, 2005). Dalam proses
ekstensifikasi pembudidayaan kemenyan salah satu masalah yang dihadapi petani
adalah kurangnya ketersediaan bibit yang bermutu baik. Penyedian bibit kemenyan
yang masih dilakukan hingga kini adalah dengan menggunakan biji. Penanaman
dengan biji melalui proses perkecambahan biji yang relatif lama sehingga dapat
mempengaruhi waktu produksi kemenyan (Siregar, 2001). Selain itu perbanyakan
dengan perkecambahan biji mungkin mendapatkan tanaman yang tidak seragam dan
rentan terhadap penyakit. Kelemahan tersebut dapat diatasi dengan perbanyakan
secara kultur jaringan. Kultur jaringan dikembangkan untuk membantu
secara generatif. Perbanyakan secara kultur jaringan dapat menghasilkan bibit dengan
jumlah yang besar dalam waktu yang singkat, bibit yang steril, kecepatan tumbuh
yang lebih cepat dan memiliki sifat yang identik dengan induknya (Widaryanto &
Hugeng, 2004).
Kultur jaringan memiliki manfaat yang sangat penting dalam pelestarian plasma
nutfah, karena kultur jaringan membantu untuk penyediaan bibit dalam jumlah besar,
seragam dan dengan kualitas baik (Triatminingsih, 2008). Teknik kultur jaringan juga
termasuk cara yang sangat baik untuk perbaikan kualitas tanaman, khususnya tanaman
yang potensil seperti tanaman-tanaman hortikultura dan tanaman hutan (Chaturvedi, et
al., 1982). Apabila penanaman kemenyan tidak digalakkan maka diperkirakan suatu
saat potensi ekonomi tanaman kemenyan akan menurun dan bahkan akan dilupakan.
Penelitian awal menunjukkan kemampuan jaringan tanaman untuk membentuk
kalus sangat dipengaruhi oleh konsentrasi zat pengatur tumbuh kinetin dan α
-napthaleneacetic acid (NAA) dalam media MS (Nurwahyuni, 2002). Penelitian lain
yang dilakukan oleh Harahap (2004), menunjukan perlakuan media MS dengan BAP
1 mg/l memberikan hasil terbaik terhadap persentase bertunas. Dalam kultur daun
pucuk biasanya digunakan zat pengatur tumbuh auksin dan sitokinin, karena
kombinasi tersebut dapat memberikan respon ataupun pengaruh terhadap kultur
pucuk. Secara umum konsentrasi auksin yang biasa digunakan berkisar antara
0,1-10mg/l dan untuk sitokinin berkisar antara 0,01-0,1-10mg/l (Vasil,1995; Pierik, 1987).
Kelebihan kultur tunas adalah mampu menghasilkan bibit tanaman yang identik
dengan induknya dan bebas virus. Rice et al. (1992) mengatakan bahwa kultur tunas
daun mampu meningkatkan laju induksi dan penggandaan sel/tunas, mampu
memperbaiki mutu bibit yang dihasilkan, mampu mempertahankan sifat-sifat
morfologi yang positif. Menurut Suyadi (2003), selain itu penggunaan tunas aksiler
juga banyak menghasilkan tunas-tunas baru yang masih aktif membelah.
Berdasarkan hal tersebut maka perlu dilakukan penelitian untuk mengetahui
pertumbuhan kultur pucuk daun kemenyan menggunakan media MS dan dengan zat
1.2 Permasalahan
Potensi ekonomi yang besar dari getah kemenyan Sumatera Utara yang selama ini di
budidayakan secara tradisional perlu ditingkatkan dengan lebih baik lagi melalui
kultur jaringan, namun hal tersebut masih terkendala dengan belum diketahuinya
formula zat pengatur tumbuh yang sesuai untuk kultur jaringan kemenyan.
1.3 Tujuan
Penelitian ini bertujuan untuk mengetahui pengaruh pemberian zat pengatur tumbuh
Atonik dan BAP terhadap pertumbuhan kultur daun pucuk kemenyan pada media MS.
1.4 Hipotesis
Penambahan zat pengatur tumbuh Atonik dan BAP dalam media MS berpengaruh
terhadap pertumbuhan daun pucuk aksiler kemenyan.
1.5 Manfaat
Penelitian ini bermanfaat sebagai bahan informasi bagi yang memerlukan, khususnya
BAB 2
TINJAUAN PUSTAKA
2.1 Botani Kemenyan ( Styrax benzoin Dryander)
Kemenyan termasuk dalam genus Styrax adalah jenis pohon yang tumbuh di
lereng-lereng bukit dan pada tanah berpasir pada ketinggian 1000-5000 m di atas
permukaan laut. Pohon ini banyak di temui di Kabupaten Tapanuli Utara yang di
kenal dengan nama Haminjon atau Kemenyan Toba (Brahmana, 1981). Menurut
Tjitrosoepomo (2000) kedudukan tanaman kemenyan dalam sistematika adalah
sebagai berikut:
Kingdom : Plantae
Divisio : Spermatophyta
SubDivisio : Angiospermae
Kelas : Dicotyledoneae
Ordo : Ebenales
Famili : Styracaceae
Genus : Styrax
Spesies : Styrax benzoin Dryander
Kemenyan merupakan jenis pohon yang berukuran besar, tingginya dapat
mencapai 40 m dengan diameter batang mencapai 100 cm. Batang berbentuk lurus
dengan percabangan relatif sedikit dan kulit berwarna merah anggur (Oetomo, 1974
dalam Harahap, 2004). Batangnya mengandung resin yang bila dibakar berbau wangi.
Daunnya tersusun spiral dan pada permukaan bagian bawah berambut putih.
Bunganya berbentuk tandan dan berbau wangi, buah berbentuk bulat keras dan kulit
Tanaman kemenyan dikelola dan diusahakan oleh penduduk Toba dinamakan
tobbak. Penanaman dilakukan dengan cara memindahkan anakan pada lahan yang
telah ditumbuhi oleh kemenyan yang sudah tua dan tidak menghasilkan getah lagi.
Untuk sementara tanaman induk dibiarkan hidup untuk dapat melindungi bibit yang
baru ditanam. Tetapi setelah bibit berumur satu tahun atau lebih pohon kemenyan
yang telah tua harus dialal. Dialal merupakan suatu pekerjaan untuk memisahkan atau
membuang kulit dari batang kemenyan supaya makanan yang diserap akar tidak
dibawa keseluruh batang dan ranting kemenyan. Sehingga lambat laun daun-daun
pohon yang dialal berjatuhan disekitar bibit yang ditanam dan akan menjadi penyubur
bagi bibit kemenyan (Siregar, 2001)
2.2 Teknik Kultur Jaringan
Teknik kultur jaringan adalah suatu cara yang dilakukukan untuk memperbanyak
tanaman dengan mengisolasi bagian-bagian tanaman seperti sel, jaringan atau organ
serta menumbuhkannya dalam media buatan aseptik dan kaya akan nutrisi serta
dengan zat pengatur tumbuh, yang semua pengerjaannya dilakukan secara aseptis.
Menurut Hendaryono & Wijayani (1994), mengatakan bahwa kultur jaringan berarti
membudidayakan suatu jaringan tanaman menjadi tanaman kecil yang mempunyai
sifat seperti induknya.
Kultur jaringan menggunakan dasar sel seperti yang dikemukakan oleh
Schleiden dan Schwann, bahwa sel mempunyai kemampuan otonom (mampu tumbuh
mandiri), bahkan mempunyai kemampuan totipotensi (Nugroho & Sugito, 2000).
Totipotensi sel yaitu setiap sel tanaman yang hidup di lengkapi dengan informasi
genetik dan perangkat fisiologis yang lengkap untuk tumbuh dan berkembang menjadi
tanaman utuh, jika kodisinya sesuai (Yusnita, 2003). Sel atau jaringan tanaman
tersebut dapat berorganogenesis menjadi tunas dan akar atau dapat tumbuh menjadi
kumpulan sel yang merismatik dalam jumlah yang tak terhingga yang disebut kalus.
Kalus tersebut dapat diarahkan untuk tumbuh menjadi tunas dan akar tanaman atau
menjadi embrio somatik tergantung dari komposisi media dan lingkungan tumbuhnya
Kultur jaringan memberikan informasi pengetahuan yang sengat bermanfaat di
bidang fisiologi tanaman dan juga usaha penyedian bibit dengan jumlah yang besar
dan keseragaman sifat yang tinggi. Sampai saat ini sudah banyak sekali dikenal
perbanyakan tanaman secara in vitro baik tanaman hias, tanaman buah, bahkan
tanaman perkebunan (Hendaryono & Wijayani, 1994). Di samping itu, perbanyakan
tanaman secara kultur jaringan sangat bermanfaat untuk memperbanyak tanaman
introduksi, tanaman klon unggul baru, dan tanaman bebas patogen yang perlu
diperbanyak dalam jumlah besar dalam waktu yang relatif singkat (Widiastuty, 2001).
Perkembangan bioteknologi tanaman juga mensyaratkan dikuasainya regenerasi
tanaman secara in vitro, yang merupakan salah satu penyebab banyaknya penelitian
dan dana yang dicurahkan untuk mendapatkan prosedur regenerasi in vitro untuk
berbagai tanaman bernilai ekonomi tinggi (Yusnita, 2003).
2.3 Kultur Daun Pucuk
Bagian tanaman yang dapat digunakan sebagai eksplan adalah daun pucuk. Kultur
tunas aksiler hampir sama dengan kultur meristem hanya perbedaannya terletak pada
ukuran eksplan yang digunakan. Eksplan yang digunakan pada kultur tunas aksiler
lebih besar dibanding dengan ukuran eksplan dalam kultur meristem. Eksplan yang
digunakan untuk kultur pucuk aksiler dapat berasal dari pucuk apikal atau pun aksilar
(Katuuk, 1989).
Perbanyakan tanaman yang dihasilkan secara kultur jaringan dengan
menggunakan pucuk aksiler memiliki keuntungan tersendiri yaitu dimungkinkannya
untuk mengontrol eksplan bebas virus, tanaman secara genetik seragam dan pada
tanaman laju perbanyakan lebih tinggi (Rosmayati, 1993). Menurut Irawati (2005), di
dalam suatu tumbuhan, kemampuan regenarasi dari jaringan tergantung dari umur
fisiologis, karakter dan kualitas selnya. Jaringan yang muda umumnya mempunyai
kemampuan berdiferensiasi dan tumbuh lebih baik dalam suatu medium hara (Wetter
Menurut Katuuk (1989), perbanyakan dengan menggunakan pucuk aksiler
dapat dilaksanakan pada tiap jenis tanaman yang mempunyai pucuk aksiler. Pucuk ini
akan berkembang dengan baik bila dalam media diberikan sitokinin seperti BAP, 2-iP,
dan Zeatin. Hal ini terjadi pada tanaman berkayu terutaman buah-buahan dan tanaman
kehutanan. Menurut Irawati (2005), dalam kultur pucuk biasanya media mengandung
auksin dan sitokinin dengan konsentrasi sitokinin lebih tinggi dari auksin karena
sitokinin dapat mengatasi kemunduran daya tumbuh apabila pertumbuhan terganggu.
2.4 Eksplan (Bahan Tanaman)
Sebelum melakukan kultur jaringan untuk suatu tanaman, kegiatan yang pertama
harus dilakukan adalah memilih tanaman induk yang hendak diperbanyak. Tanaman
tersebut harus jelas jenis, spesies, dan varietasnya, serta harus sehat dan bebas dari
hama penyakit. Umumnya bagian tanaman yang digunakan sebagai eksplan adalah
jaringan muda yang sedang tumbuh aktif (Yusnita, 2003). Eksplan adalah bagian
tanaman yang digunakan dalam kulturisasi. Eksplan ini menjadi bahan dasar bagi
pembentukan kalus (bentuk awal calon tunas yang kemudian mengalami proses
perlengkapan bagian tanaman seperti daun, batang, dan akar) (Nugroho & Sugito,
2000). Agar pertumbuhan bibit secara kultur jaringan berlangsung mudah, sebaiknya
di ambil sel yang berasal dari bagian meristem tanaman yang masih muda. Misalnya
daun muda, ujung akar, ujung batang, dan keping biji. Bagian meristem dipilih, karena
bagian tersebut memiliki sifat pertumbuhan yang agresif (Yusnita, 2003).
Menurut Murashige (1974 dalam Bayu, 2002), ada lima faktor yang harus
diperhatikan dalam regenerasi in vitro dari eksplan yaitu : organ yang digunakan,
umur fisiologis, umur saat diambil dari tanaman asal, ukuran eksplan dan kualitas
tanaman asal. Dalam hal ini ukuran eksplan yang paling baik digunakan adalah antara
0,5-1 cm, namun hal ini dapat juga terjadi (tumbuh) tergantung pada tanaman yang
dipakai dan juga jenis tanamannya (Katuuk, 1989). Selain itu ekspalan yang
digunakan harus bebas kontaminan (dengan menggunakan sterilan) sebelum ditransfer
ke dalam kultur, serta media tempat kultur ditanam harus steril dan aseptik (George &
2.5 Media Kultur Jaringan
Media tanamam dalam kultur jaringa adalah tempat tumbuh untuk eksplan. Media
tanam tersebut dapat berupa larutan (cair) atau padat. Media tanam harus berisi semua
zat yang diperlukan untuk menjamin pertumbuhan eksplan. Bahan-bahan yang diramu
berisi campuran garam mineral sumber unsur makro dan mikro, gula, protein, vitamin,
dan hormon tumbuh. Dengan demikian keberhasilan kultur jaringan jelas ditentukan
oleh media tanam dan macam-macam tanaman (Hendaryono & Wijayani, 1994).
Menurut Yusnita (2003), komponen media kultur yang lengkap adalah air
destilata (akuades), hara-hara makro dan mikro, gula (umumnya sukrosa) sebagai
sumber energi, vitamin, asam amino, bahan organik lain, zat pengatur tumbuh,
suplemen berupa bahan-bahan alami, agar-agar atau gelrite sebagai pemadat media.
Menurut Hartmann & Ketser (1983), media yang paling sering digunakan
dalam kultur jaringan adalah media MS (Murashige dan Skoog). Media dengan
formulasi MS adalah media yang paling cocok untuk perkembangan kultur dan
organogenesis (Vasil, 1985). Selain itu media ini memiliki keistimewaan, karena
mengandung nitrat, kalium, dan amonianya tinggi (Wetter & Constabel, 1991).
2.6 Zat Pengatur Tumbuh
Zat pengatur tumbuh merupakan salah satu komponen media yang nentukan
keberhasilan kultur jaringan (Yusnita, 2003). Zat pengatur tumbuh adalah senyawa
organik bukan hara, yang dalam jumlah sedikit dapat mendukung, meghambat dan
merubah proses fisiologis tumbuhan. Zat pengatur tumbuh dalam tanaman terdiri dari
lima kelompok yaitu Auksin, Giberelin, Sitokinin, Etilen dan In hibitor dengan ciri
khas serta pengaruh berlainan terhadap proses fisiologis (Hendaryono & Wijayani,
Zat pengatur tumbuh sangat diperlukan bagi komponen medium bagi
pertumbuhan dan diferensiasi. Tanpa pembelahan zat pengatur tumbuh dalam
medium, pertumbuhan sangat terhambat bahkan mungkin tidak tumbuh sama sekali
(Hendaryono & Wijayani, 1994). Faktor lain yang perlu mandapat perhatian dalam
penggunaan zat pengatur tumbuh antara lain jenis zat pengatur tumbuh yang
digunakan, konsentrasi, urutan penggunaan, dan periode masa induksi dalam kultur
tertentu (Gunawan, 1995).
2.6.1 Zat Pengatur Tumbuh BAP (Benzil Amino Purin)
Sitokinin merupkan hormon tumbuhan turunan adenin dan berfungsi untuk
merangsang pembelahan sel dan diferensiasi mitosis, disintesis pada ujung akar dan
ditranslokasi melalui pembuluh xilem. Golongan sitokinin yang sering ditambahkan
dalam medium antara lain adalah : Kinetin, Zeatin, BAP (Benzil Amino Purin)
(Hendaryono & Wijayani, 1994). BAP sering digunakan karena BAP mempunyai
efektifitas untuk perbanyakan tunas, mudah didapat dan harganya relatif murah
(Imelda, 2007). Menurut Mariani (2003) zat pengatur tumbuh sitokinin berperanan
dalam pembelahan sel dan morfogenesis, sedang auksin berperanan dalam mengatur
pertumbuhan dan pemanjangan sel. Pemanjangan sel, pembelahan sel, morfogenesis
dan pengaturan pertumbuhan merupakan proses yang sangat penting dalam
pembetukan kalus dan selanjutnya diikuti pembentukan tunas. Menurut Suyadi (2003)
apabila kondisi auksin dan sitokinin endogen berada pada kondisi sub optimal, maka
diperlukan penambahan auksin dan sitokinin secara eksogen, sehingga diperoleh
perimbangan auksin dan sitokinin optimal.
BAP mempunyai struktur yang sama dengan kinetin, akan tetapi lebih efektif
bila dibandingkan dengan kinetin karena memiliki gugus benzil (Winarsih, 2002).
Umumnya tanaman memiliki respon yang lebih baik terhadap BAP dibandingkan
kinetin sehingga BAP lebih efektif untuk produksi tunas in vitro pada banyak
tanaman. Contohnya pada tanaman kehutanan Acacia sp., Eucalyptus ficifolia,
2.6.2 Zat Pengatur Tumbuh Atonik
Atonik adalah suatu zat pengatur tumbuh sintetik berbentuk larutan dalam air,
berwarna cokelat dan berbau khas (Wuryaningsih, 1993). Atonik adalah gabungan
garam-garam natrium dari S-nitroquiocol dan garam natrium dari paranitrophenol
(Kusumo, 1990). Atonik mengandung zat aktif natrium orto nitrofenol, natrium para
nitrofenol, natrium 2,4 di nitrofenol, dan natrium 5 nitroguaiakol (Saptarini, et al,
2001).
Atonik bukan merupakan hormon tanaman (fitohormon) atau pestisida tetapi
suatu zat kimia yang dapat merangsang proses biokimia dan fisiologis tanaman,
sehingga atonik termasuk zat pengatur tumbuh (Kusumo, 1990). Atonik biasanya
digunakan untuk merangsang pertumbuhan akar tanaman terhadap unsur hara,
meningkatkan daya serap daun, keluarnya bunga, pembentukan buah, dan
meningkatkan jumlah dan bobot buah (Saptarini, et al, 2001)
2.7 Glutamin
Asam amino sebagai sumber nitrogen organil relatif jarang diperlukan, karena sumber
nitrogen utama dalam media biasanya NO3- dan NH4+. Namun, jika diperlukan sebagai
sumber nitrogen organik, asam amino yang sering digunakan adalah glutamin
(Yusnita, 2003). Karena glutamin merupakan penyimpan nitrogen yang utama pada
tumbuhan dan juga mudah di sintesis oleh tumbuhan (Salisbury & Ross, 1991).
Glutamin berperan dalam metabolisme asam amino karena dapat menjadi
pembawa amonia untuk sintesis asam-asam amino baru dalam jaringan (Hendaryono
& Wijayani, 1994). Keberadaan asam amino dalam bentuk D-asam glutamat
mempunyai berbagai pengaruh terhadap pertumbuhan dan metabolisme tumbuhan.
(Robinson, 1991). Glutamin juga sangat penting untuk inisiasi dan perkembangan
embrio somatik. Penambahan asam amino dapat merangsang terjadi-nya komunikasi
inisiasi dan pendewasaan embrio somatik diperlukan keseimbangan yang tepat antara
NH4+ dan NO3- (Robinson, 1991).
2.8 Kultur Jaringan Tanaman Kemenyan
Penelitian awal dalam perbanyakan Kemenyan melalui kultur pucuk telah dilakukan
oleh peneliti (Nurwahyuni, 2002). Hasil penelitian menunjukkan tahapan yang
menggembirakan. Beberapa hasil penelitian ini yaitu diperoleh pengaruh pemberian
zat tumbuh terhadap pertumbuhan eksplan kultur daun pucuk di dalam media kultur.
Dari penelitian ini diperoleh kesimpulan semakin tinggi kinetin dalam media, kualitas
eksplan akan semakin baik. Penelitian yang dilakukan oleh Harahap (2004),
menggunakan BAP dengan kosentrasi 0-4 mg/l dengan variasi media yaitu media MS
dan WMP. Perlakuan media MS dengan BAP 1 mg/l memberikan hasil terbaik
BAB 3
BAHAN DAN METODA
3.1 Waktu dan Tempat
Penelitian ini dilakukan pada bulan Januari sampai dengan Mei 2010 di laboratorium
Kultur Jaringa n Departemen Biologi, Fakultas Matematika dan Ilmu Pengetahuan
Alam, Univeritas Sumatera Utara. Bahan tanaman yang digunakan sebagai eksplan
penelitian ini adalah tunas aksiler tanaman kemenyan. Kemenyan ini diambil dari
Desa Aji Nembah Kecamatan Merek, Kabupaten Karo.
3.2 Persiapan Bahan Tanaman
Bibit kemenyan dipindahkan ke dalam polibag plastik dengan media pasir : tanah
(1:1). Kemudian tanaman/bibit dipangkas pada setiap ujung batangnya untuk
menumbuhkan tunas aksiler. Setiap seminggu sekali dilakukan penyemprotan dengan
fungisida untuk mencegah penyakit dan mengurangi terjadinya kontaminasi. Setelah
tunas aksiler yang dipergunakan mencukupi untuk dipanen selanjutnya akan ditanam
secara in vitro di laboratorium kultur jaringan Departemen Biologi Fakultas
Gambar 1. Tanaman Kemenyan (Styrax benzoin Dryander)
3.3 Metode Penelitian
Penelitian ini menggunakan metode percobaan dengan Rancangan Acak Lengkap
(RAL) faktorial dengan 2 faktor, yaitu:
I. Faktor tingkat konsentrasi atonik (A)
A0= 0 (tanpa atonik)
A1= 0,5 ml/L atonik
A2= 1 ml/L atonik
A3= 1,5 ml/L atonik
A4= 2 ml/L atonik
II. Faktor konsentrasi BAP (B)
Terdiri dari 4 taraf yaitu:
B0= 0 (tanpa BAP)
B1= 0,05 mg/L BAP
B2= 0,5 mg/L BAP
Dengan demikian diperoleh 20 kombinasi perlakuan, yaitu:
A0B0 A1B0 A2B0 A3B0 A4B0
A0B1 A1B1 A2B1 A3B1 A4B1
A0B2 A1B2 A2B2 A3B2 A4B2
A0B3 A1B3 A2B3 A3B3 A4B3
Jumlah ulangan pada setiap perlakuan adalah 5 maka jumlah total percobaan
seluruhnya adalah 100 satuan percobaan.
3.4 Cara Kerja
3.4.1 Sterilisasi Alat
Semua alat gelas dan alat diseksi yang akan digunakan dicuci dengan bersih dan
dikeringkan. Lalu cawan petri yang telah bersih diisi dengan kertas saring. Kemudian
alat-alat tersebut dibungkus dengan kertas, sterilisasi dalam autoklaf pada suhu 121oC
dengan tekanan 15 psi selama 60 menit. Bersamaan dengan itu akuades dalam
erlenmeyer yang telah ditutup dengan aluminium foil yang juga ikut disterilisasi.
3.4.2 Pembuatan Media
Media yang digunakan adalah media dasar MS (Murashige dan Skoog, 1962) dengan
penambahan atonik dan BAP dengan konsentrasi yang disesuaikan dengan perlakuan.
Tahap awal pembuatan media adalah pembuatan stok, yang terdiri dari stok hara
mikro, iron, vitamin dan zat pengatur tumbuh. Sementara unsur hara makro,
myo-inositol, sukrosa dan agar dapat ditimbang langsung sesuai dengan kebutuhan tanpa
harus dijadikan stok.
Larutan MS dibuat dengan cara memasukkan hara makro, myo-inositol dan
sukrosa ke dalam gelas ukur 1000 ml yang terlebih dahulu telah berisi akuades.
Selanjutnya dimasukan hara mikro, iron, vitamin masing-masing 1 ml dari larutan
perlakuan. Setiap bagian diberi zat pengatur tumbuh atonik dan BAP sesuai dengan
perlakuan kemudian pH larutan diukur dengan menggunakan pH meter sebesar 5,8.
Untuk mendapatkan pH yang optimal ditambahkan NaOH 0,1 N atau HCl 0,1 N.
Kedalam larutan ditambahkan agar dan dipanaskan hingga mendidih. Larutan media
dituang ke dalam botol kultur steril dan dibagi sesuai dengan banyaknya ulangan,
ditutup dengan aluminium foil, diikat dengan karet gelang dan disterilisasi dalam
autoklaf bertekanan 15 psi pada suhu 121oC selama 20 menit. Selanjutnya media
disimpan di dalam ruang kultur sebelum digunakan.
3.4.3 Sterilisasi Eksplan
Eksplan tanaman berupa pucuk daun kemenyan dicuci di bawah air yang mengalir
kemudian direndam dengan detergen sebanyak 3 g/l selama 60 menit. Selanjutnya
pucuk dibilas dengan akuades steril. Pucuk kemenyan kemudian dishaker dalam
larutan benlate sebanyak 2 g/l dan di tetesi tween 80 sebanyak dua tetes selama 3 jam.
Kemudian pucuk dibilas dengan akuades steril. Tahap selanjutnya direndam dalam
larutan alkohol 70% selama 1 menit, lalu berturut-turut disterilkan dalam larutan
bayclin 10% selama 20 menit, larutan bayclin 20% selama 10 menit. Kemudian dicuci
bersih dengan akuades steril. Tahap akhir dilakukan perendaman dalam larutan
Betadine 10% selama 5 menit dan dikeringkan di atas cawan petri steril yang berisi
kertas saring (Nurwahyuni, 2005).
3.4.4 Penanaman Eksplan
Sebelum melakukan penanaman diupayakan agar ruangan dalam keadaan bersih.
Penanaman dilakukan di dalam enkas. Alat-alat diseksi, lampu bunsen dan alkohol
70% dipersiapkan terlebih dahulu. Eksplan yang akan ditanam dipotong pada bagian
basal sehingga ukuran eksplan ±1cm kemudian ditanam delam media kultur. Setiap
botol kultur berisi satu eksplan. Penanaman dilakukan dengan aseptik sehingga setiap
kali menggunakan pisau dan pinset terlebih dahulu dicelupkan ke dalam alkohol 96%
kemudian dibakar diatas lampu bunsen. Botol berisi eksplan kemudian ditutup dengan
aluminium foil dan dikencangkan dengan karet gelang.
3.4.5 Pemeliharaan Eksplan
Botol-botol berisi eksplan kemudian disusun dengan rapi di atas rak kultur sesuai
dengan layout penelitian. Ruang pemeliharaan kultur harus senantiasa dalam keadaan
bersih dan aseptik dengan cara disemprot dengan alkohol 70% setiap hari. Suhu dijaga
berkisar 25±2 oC dengan pengaturan AC. Pada rak kultur intensitas cahaya dengan
penyinaran lampu neon 500 lux. Lama inkubasi 2 bulan dan dilakukan pengamatan
setiap 2 hari sekali.
3.4.6 Parameter Pengamatan
Parameter yang diamati dalam penelitian ini adalah :
a. Saat terbentuk kalus
Saat terbentuknya kalus diamati pada hari awal hingga akhir terbentuknya
kalus.
b. Persentase kultur yang membentuk kalus (%)
Persentase kultur yang berkalus = Jumlah eksplan yang berkalus Jumlah eksplan seluruh perlakuan
x 100 %
c. Berat basah kultur (g)
Berat basah kultur dihitung pada akhir penelitian.
e. Persentase kultur yang terkontaminasi (%)
Persentase kultur yang terkontaminasi dihitung setiap hari sejak awal hingga
akhir penelitian dengan rumus:
Persentase terkontaminasi = Jumlah ekspalan yang terkontaminasi Jumlah eksplan seluruh perlakuan
x 100 %
3.5 Analisis Data
Data yang didapatkan dari masing-masing parameter dianalisis dengan Analysis of
Variance (ANOVA) dan jika terdapat perbedaan yang nyata dilanjutkan dengan
BAB 4
HASIL DAN PEMBAHASAN
4.1 Saat Terbentuknya Kalus
Kalus merupakan suatu kumpulan sel yang tidak terorganisir dan tidak berbentuk,
kalus terjadi karena pembelahan yang sangat aktif. Pada tanaman utuh kalus dapat
terbentuk karena pelukaan, serangan serangga atau mikroorganisme. Secara in vitro
kalus diinisiasi dengan meletakkan bagian kecil tanaman (eksplan) pada medium
pertumbuhan pada kondisi aseptik. Dengan adanya rangsangan dan zat pengatur
tumbuh endogen atau eksogen menyebabkan metabolisme sel menjadi aktif sehingga
akan terbentuk kalus (George & Sherington, 1984). Dari pengamatan langsung hasil
kultur pucuk kemenyan ini diperoleh bahwa pertumbuhan kalus dimulai dari minggu
ke-3 (hari ke 21) sampai minggu ke-6 setelah penanaman. Pertumbuhan kalus pada
tanaman kemenyan relatif lama dibanding dengan tanaman lain yang pada umumnya
kalus muncul pada hari ke 12 setelah inokulasi. Santoso dan Nursadi (2004)
menyatakan bahwa pada umumnya eksplan pucuk dan daun mempunyai kemampuan
tumbuh lebih cepat dibanding dengan eksplan batang utama, cabang batang, atau
tangkai bunga. Pada media MS, eksplan daun muncul kalus umumnya berkisaar pada
hari ke-12 setelah inokulasi, sedangkan eksplan batang pada 26 hari setelah inokulasi.
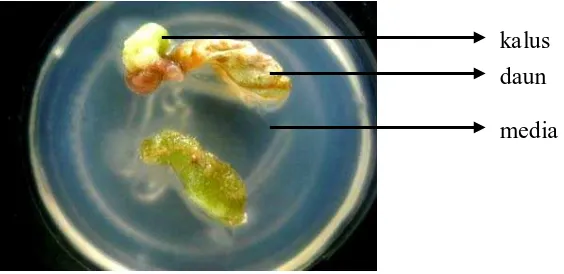
kalus
daun
media
Dari Tabel 4.1.1 dapat dilihat bahwa pertumbuhan kalus paling banyak terjadi
pada minggu ke-4 pengamatan dibanding minggu yang lain. Pada minggu ke-4 kultur
yang hidup sebanyak 51 botol kultur, sedangkan pada minggu ke-3 ada 4 botol kultur,
minggu ke-5 sebanyak 11 botol, dan minggu ke-6 sebanyak 1 botol. Hal ini
menunjukkan bahwa minggu ke-4 yakni berkisar antara 30-35 hari merupakan waktu
dimana kalus kemenyan mulai tumbuh dengan seragam, sedangkan minggu ke ke-6
kemampuan eksplan beregenerasi semakin menurun dan tidak menghasilkan kalus.
Tabel 4.1.1 Jumlah Kultur yang membentuk kalus per minggu.
Ket: A0= 0 (tanpa ZPT) A1= 0,5 ml/L atonik A2= 1 ml/L atonik A3= 1,5 ml/L atonik A4= 2 ml/L atonik B0= 0 (tanpa ZPT) B1= 0,05 mg/L BAP B2= 0,5 mg/L BAP B3= 5 mg/L BAP
Dari hasil penelitian ini dapat dilihat bahwa regenerasi tanaman belum
diperoleh secara maksimal. Perbanyakan tanaman baik secara embriogenesis maupun
organogenesis belum tercapai. Hasil yang dicapai masih dalam tahap inisasi kalus.
Menurut Hartman et al. (2002), regenerasi tanaman pada kultur in vitro dapat terjadi
melalui dua cara yatu organogenesis dan embriogenesis somatik. Menurut Kaatuk
(1989), organogenesis tergantung pada hal berikut: media dan lingkungan, namun
perbandingan zat pengatur tumbuh auksin dan sitokinin juga mempengaruhi derajat
organogenesis.
Penelitian sebelumnya telah dilakukan oleh Erika (2007) dengan menggunakan
2,4-D dan BAP, diketahui bahwa kalus mulai terbentuk pada hari ke-16 setelah
inokulasi tetapi ada yang pertumbuhannya lambat sampai hari ke-30. Sedangkan pada
penelitian ini diketahui bahwa bahwa pertumbuhan kalus dimulai dari minggu ke-3
(hari ke 21) sampai minggu ke-6 setelah penanaman. Faktor yang mempengaruhi lebih
lamanya pertumbuhan kalus pada penelitian kemenyan ini dimungkinkan oleh
perbandingan antara zat pengatur tumbuh auksin dan sitokinin yang tidak tepat dan
strilisasi yang terlalu keras (Kaatuk,1989).
4.2 Persentase kulur yang membentuk kalus (%)
Persentase kultur yang membentuk kalus adalah banyaknya kalus yang terbentuk dari
seluruh eksplan yang ditanam. Data pengamatan persentase kultur dapat dilihat pada
tabel 4.2.1. Dari data tersebut didapat bahwa jumlah kultur yang hidup sebesar 67%
yaitu sebanyak 67 botol dari 100 botol perlakuan.
4.2.1 Persentase Kultur yang membentuk kalus (%)
Secara umum pemberian kombinasi Atonik dan BAP memberikan pengaruh
tidak nyata terhadap pertumbuhan kalus. Pada Tabel 4.2.1 dapat dilihat bahwa hampir
pada semua perlakuan terdapat kultur yang hidup. Pada A0B0 yang tidak diberikan zat
pengatur tumbuh juga menghasilkan jumlah kalus yang tidak jauh berbeda dengan
perlakuan yang di berikan zat pengatur tumbuh. Pada perlakuan A2B3 memiliki kultur
hidup yang paling tinggi yaitu sebesar 100%. Hal ini menunjukkan bahwa kombinasi
perlakuan atonik 1 ml/L dan BAP 5 mg/L juga dapat memacu kultur hidup kalus.
Menurut Sri Hutami (2003), selain hara makro dan mikro dalam kultur in vitro zat
pengatur tumbuh sitokinin dan auksin berperan dalam pertumbuhan dan morfogenesis.
Keseimbangan kedua zat pengatur tumbuh tersebut sangat berperan dalam
pembentukan kalus. Menurut Pierik (1987), apabila digunakan pada konsentrasi tinggi
yaitu berkisar 1-10 mg/l dapat menginduksi pembentukan kalus tetapi pada umumnya
dapat menghambat pembentukan akar. Dan menurut George dan Sherington (1984),
auksin digunakan secara luas dan sangat baik dalam kultur jaringan untuk merangsang
pertumbuhan kalus.
Penelitian ini juga menunjukkan bahwa hubungan kombinasi pemberian zat
pengatur tumbuh dengan pertumbuhan kalus bersifat fluktuatif. Walau ada
kecenderungan bahwa semakin tinggi konsentrasi atonik yang di berikan pada media
dcenderung menurunkan jumlah kalus yang terbentuk. Sedangkan pemberian BAP,
memberikan kecenderungan semakin tinggi konsentrasi BAP maka kalus yang
terbentuk semakin banyak. Rata-rata jumlah kalus yang terbentuk karena penambahan
BAP lebih besar dibandingkan dengan penambahan atonik bahkan pada perlakuan B0
kalus yang terbentuk lebih besar bila dibandingkan dengan semua tingkat konsentrasi
atonik.
Penggunaan BAP untuk perbanyakan pisang telah banyak dilaporkan, antara
lain oleh Yusnita et. al. (1996) yang menyatakan bahwa penggunaan BAP 2 mg/l
menghasilkan hasil yang terbaik untuk perbanyakan pisang ambon kuning secara in
vitro yang menghasilkan tunas. Pada penelitian yang dilakukan Sudarmaji (2003)
penggunaan BAP pada kultur kapas, menghasilkan berat kalus yang terbesar pada
konsentrasi 2 mg/l. Sedangkan pada penelitian ini penggunaan BAP yang terbaik
telah digunkan dalam perbanyakan tanaman, diantaranya pada perbanyakan buah naga
dimana atonik berperan di dalam pembentukan tunas buah naga, pada penggunaan 4
ml/l (Dini et. al., 2007). Pada penelitian tanaman Kopi yang dilakukan Johanes
(2004), atonik berpengaruh dalam pembelahan sel dan perkembangan tunas ada pada
konsentrasi 6 ml/l.
Kombinasi dari kombinasi atonik dan BAP belum pernah dilakukan pada
tanaman-tanaman lain. Sehingga pengaruh kombinasi kedua zat pengatur tumbuh ini
masih diketahui hanya sampai proses pembentukan kalus. Sehingga masih dibutuhkan
penelitian-penelitian lain untuk memastikan pengaruh kombinasi dari zat pengatur
tumbuh Atonik dan BAP terhadap tanaman atau pun eksplan.
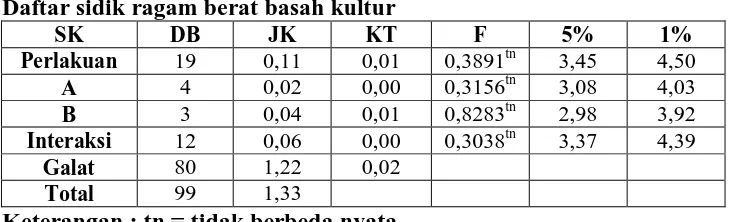
4.3. Berat basah kalus (g)
Hasil analisis sidik ragam pada basah kalus (Lampiran 2) ternyata kombinasi
pemberian ZPT (atonik dan BAP) tidak berpengaruh nyata terhadap berat basah
kultur. Hubungan antara kombinasi pemberian ZPT (atonik dan BAP) dengan berat
basah kultur dapat dilihat pada grafik:
0,00
Gambar 5. Hubungan rata-rata berat basah kalus dengan kombinasi ZPT
Ket: A0= 0 (tanpa ZPT) A1= 0,5 ml/L atonik A2= 1 ml/L atonik A3= 1,5 ml/L atonik A4= 2 ml/L atonik B0= 0 (tanpa ZPT) B1= 0,05 mg/L BAP B2= 0,5 mg/L BAP B3= 5 mg/L BAP
Dari grafik di atas dapat dilihat bahwa hubungan antara perlakuan kombinasi
pemberian ZPT (atonik dan BAP) dengan berat basah kultur bersifat fluktuatif.
Perlakuan A4B0 (0,44 g) memberikan hasil tertinggi terhadap berat basah kultur,
sedangkan perlakuan A1B0 (0,28 g) menunjukkan berat kultur yang terendah. Hal
tersebut menunjukkan bahwasanya peningkatan berat basah kalus lebih dipengaruhi
oleh pemberian atonik dan bukan BAP. Menurut Sallisbury dan Ross (1995), zat
pengatur tumbuh yang diberikan dalam jumlah yang tepat dapat memberikan
pengaruh terhadap berat kultur. Auksin berperan pada perbesaran sel, sedangkan
sitokinin merangsang pembelahan sel. Interaksi antara kedua zat pengatur tumbuh
tersebut akan meningkatkan jumlah dan ukuran sel dalam jaringan sehingga dapat
Menurut George dan Sherrington (1984), auksin dapat meningkatkan
pertumbuhan kalus terutama jika dikombinasikan dengan sitokinin. Jika sitokinin dan
auksin dikombinasikan secara bersama-sama maka akan terbentuk kalus yaitu massa
sel yg belum berdiferensiasi (Hartmann et al., 1983). Namun pada penelitian ini dapat
dilihat kecenderungan BAP memberikan dampak berbeda terhadap berat basah kalus
yaitu menurunkan berat basah kalus, pada perlakuan B0 semakin tinggi konsentrasi
atonik maka semakin besar berat basah kalus, sedangkan pada perlakuan B3 ada
kecenderungan semakin tinggi konsentrasi atonik semakin kecil berat basah kalus
seiring dengan peningkatan atonik.
4.4. Warna Kalus
Pengamatan warna kalus dilakukan pada umur 5 minggu sesudah inokulasi karena
pada minggu ke-5 hampir semua kalus sudah tumbuh dan tidak ada lagi terjadi
perubahan warna. Data pengamatan warna kalus dapat dilihat pada Tabel 4.4.1
4.4.1 Tabel Warna Kalus
Perlakuan KH KP HC Total
Dari Tabel di atas menunjukkan bahwa warna kalus yang tumbuh tidak
seragam, diperoleh warna kalus berwarna kuning kehijauan sebanyak 45 botol atau
sebanyak 67,2 % dari kultur yang hidup, kuning pucat sebanyak 15 botol atau
sebanyak 22,4 % dari kultur yang hidup, dan hijau kecokelatan sebanyak 7 botol atau
sebanyak 10,4 % dari kultur yang hidup. Dengan hasil tersebut diketahui bahwa
pemberian atonik dan BAP memberi dampak yang baik untuk warna kalus. Menurut
George dan Sherrington (1984), tanaman yang berasal dari varietas yang sama dapat
membentuk kalus yang berbeda baik tekstur dan warna. Menurut Keese et al. (1991),
warna kalus yang terbaik adalah kuning kehijauan dengan struktur friabel ataupun
kompak. Hal ini sesuai dengan pendapat Bayu (2005), jaringan embriogenik yang
berkualitas tinggi adalah berwarna hijau, homogen dan friabel atau pun kompak.
Lebih lanjut dijelaskan bahwa kalus kuning pucat dan kecokelatan, lembek dan
kadang-kadang berair kurang bagus. Hal ini terjadi karena eksplan sudah mengalami
penuaan sehingga eksplan mengeluarkan cairan cokelat ke medium dan membutuhkan
subkultur ke media yang baru.
Menurut Kardhinata (1999), perubahan warna dan kesegaran kalus erat
kaitannya dengan ketahanan hidup dari kalus. Kalus yang berwarna cokelat
menyebabkan pertumbuhan dan perkembangan kalus menjadi terhambat. Apabila
kalus telah berubah menjadi cokelat maka kalus tidak dapat melakukan aktifitas
sehingga menyebabkan kematian. Hal ini kemungkinan disebabkan oleh nutrisi telah
habis, terhambatnya difusi nutrien, dan penguapan air yang mengakibatkan
penimbunan metabolit yang bersifat racun bagi kalus. Kalus berwarna kuning
4.5 Persentase Terkontaminasi
Kultur yang bebas dari kontaminasi adalah salah satu yang penting dalam menentukan
keberhasilan kultur in vitro. Data pengamatan kultur terkontaminasi dapat dilihat pada
lampiran C. Dari data tersebut dapat diketahui bahwa persentase kultur terkontaminasi
sebesar 15%, yaitu sebanyak 15 botol dari 100 botol. Dan dapat diketahui juga bahwa
kultur yang tidak tumbuh sebesar 18%, hal ini bisa di sebabkan eksplan yang kurang
baik dan tidak mampu menyerap unsur-unsur hara pada media. Rata-rata kultur
terkontaminasi terjadi setelah 2-3 minggu setelah penanaman yakni berkisar antara
14-21 hari setelah penanaman.
Dari hasil pengamatan menunjukkan penyebab kontaminasi lebih banyak
disebabkan oleh jamur. Jamur ini dapat berkembang dengan cepat dan menghambat
aktivitas pertumbuhan eksplan. Menurut Kaatuk (1989), kontaminasi yang sering
terjadi disebabkan oleh spora jamur yang ada dimana-mana, karena massa yang ringan
dan ukuran yang sangat kecil memungkinkan spora untuk berpindah hanya dengan
gerakan udara yang lambat. Selanjutnya Pnadey dan Chadha (1996), mengatakan
bahwa media tanam kebanyakan terdiri atas garam-garam anorganik (makro elemen
dan mikro elemen), juga vitamin dan sukrosa. Media kultur yang kaya akan nutrisi ini
dapan mendukung pertumbuhan dari mikroorganisme yang akhirnya mencegah
pertumbuhan jaringan tanaman.
Kontaminasi dapat berasal dari eksplan, organisme kecil yang masuk ke dalam
media, botol-botol kultur serta alat-alat yang kurang steril, lingkungan kerja dan ruang
kultur yang kotor, serta kecerobohan dalam pelaksanaan kultur jaringan (Katuuk,
1989). Kontaminasi yang terjadi kemungkinan juga disebabkan karena adanya
beberapa botol kultur lain yang telah terkontaminasi dan masih berada di dalam ruang
kultur. Apabila kultur sudah terkontaminasi, maka botol yang berisi eksplan tersebut
harus segera dikeluarkan dari ruang inkubasi agar kultur yang terkontaminasi tidak
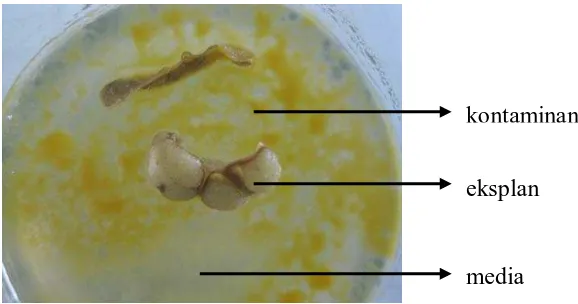
Gambar 7. Eksplan yang terkena kontaminasi
Pemilihan tanaman sebagai sumber eksplan juga merupakan salah satu hal
yang sangat penting dalam mendukung keberhasilan kultur jaringan. Eksplan yang
berasal dari lapangan terbuka lebih besar membawa kontaminasi karena bahan
tanaman banyak mengandung debu, kotoran dan berbagai kontaminan lainnya.
Menurut Pierik (1987), eksplan yang digunakan untuk kultur jaringan apabila berasal
dari tanaman yang ada di lapangan akan memiliki resiko yang sangat tinggi untuk
terinfeksi bila dibandingkan dengan eksplan yang diambil dari tanaman yang tumbuh
di rumah kaca. Hartmann et al. (2002), menyatakan bahwa walaupun ukuran eksplan
sangat kecil, namun ukuran ini sudah memberikan kesempatan kehadiran virus serta
patogen sistemik lain. Beberapa eksplan mengandung patogen internal yang tidak
muncul sampai kultur berumur beberapa lama. Organisme mikro akan menyerang
eksplan melalui luka-luka akibat pemotongan dan penanganan waktu sterilisasi
sehingga menyebabkan kematian jaringan eksplan (Gunawan, 1995). Selanjutnya
Yusnita (2003), menambahkan bahwa kontaminasi kebanyakan juga berasal dari
komponen media dan faktor manusia.
kontaminan
eksplan
BAB 5
KESIMPULAN DAN SARAN
5.1 Kesimpulan
Adapun kesimpulan yang dapat diperoleh dari penelitian ini adalah:
1. Pemberian zat pengatur tumbuh Atonik dan BAP memberikan pengaruh yang
tidak nyata terhadap pertumbuhan kultur daun pucuk kemenyan.
2. Kombinasi zat pengatur tumbuh pada perlakuan A0B4 memberikan pengaruh
terhadap berat basah kalus tertinggi.
3. Jumlah kalus yang berwarna kuning kehijauan sebagai indikasi kualitas kalus yang
baik sebanyak 67,2 % dari kultur yang hidup.
5.2. Saran
Untuk penelitian selanjutnya sebaiknya dilakukan pemilihan eksplan yang lebih baik
dan seragam, seperti tunas yang masih aktif membelah dan bebas dari kontaminan
dengan melakukan sterilisasi yang benar sehingga dapat mengurangi resiko terjadinya
DAFTAR PUSTAKA
Badan Koordinasi dan Pemetaan Nasional (Bakosurtanal). 2001. Atlas Flora dan
Fauna Indonesia. Jakarta: PT. Grasindo. hal. 23
Bayu, E. S. 2002. Pengaruh Zat Pengatur Tumbuh Jenis Auksin dan Varietas Terhadap Inisiasi Kalus Pada Kultur Embrio Kedelai (Glycine max L. Merr)
Tessis. Medan: Program Pascasarjana Universitas Sumatera Utara. hal. 11
BPS. 2003. Statistik Hasil Hutan Indonesia Tahun 1991-1993, Komoditi Kemenyan, Biro Pusat Statistik, Indonesia. hal. 3
Brahmana, H.R., Bangun, N. dan Ginting M. 1981. Penentuan Kadar Asam Sinamat dari Kemenyan Tapanuli (Styrax sumatrana). Laporan Penelitian. Medan: Fakultas Matematika dan Ilmu Pengetahuan Alam Universitas Sumatera Utara. hal. 3
Chaturvedi, H.C.; Sharma, A.K.; Sharma, M. dan Prasad, R.N., (1982),
Morphogenesis, micropropagation and germplasm preservation of some economic plants by tissue cultures. In: Plant Tissue Culture, (A.Fugiwara,
eds), Maruzen, Tokyo, Page: 687-688
Elimasni dan Nurwahyuni, I. 2005. Perbanyakan Bibit Kemenyan Sumaterana (Styrax
benzoin Dryander). Laporan Penelitian. Medan: Fakultas Matematika dan
Ilmu Pengetahuan Alam Universitas Sumatera Utara. hal. 5-6
Evivi. S., & Ikrarwati 2004.Mikropropagasi Pisang Abaca (Musa Textillis Nee) melalui Teknik Kultur Jaringan. Ilmu Pertanian. 11( 2): hal. 27-34
George, E.T & Sherrington, P.D. 1984. Plant Propagation by Tissue Culture. Handbook and Directory of commercial laboratories. Exegetics limited. Eastern Press. England. Page: 184
Gunawan, L.W. 1995. Teknik kultur In vitro Dalam Holtikultura. Jakarta: Penebar Swadaya. hal. 43
Harahap, T. 2004. Kultur Pucuk Tanaman Kemenyan Toba (Styrax sumatrana) Pada perlakuan BAP dan Media Secara in vitro. Skripsi. Medan: Fakultas Pertanian Universitas Sumatera Utara. hal. 3, 24
Hartmann, H.T. dan Kester, D. E. 1983. Plant Propagation Principle and Practices. Fourth Edition. New Jersey: Prentince-Mall, Inc. Englewood Cliffs. Page: 536
Hendaryono, D. P. S. dan Wijayani, A. 1994. Teknik Kultur Jaringan Pengenalan dan
Petunjuk Perbanyakan Tanaman Secara Vegetaif Modern. Yogyakarta:
Hutami, S. & Lestari, E. G. 2005. Produksi Bibit Kencur (Kaempferia galanga L.) Melalui Kultur Jaringan. Berita Biologi. 7 (6): hal. 319-328
Hutami, S & Ragapadmi, P. 2003. Perbanyakan Klonal Temu Mangga (Curcuma
mangga) melalui Kultur In Vitro. Buletin Plasma Nutfah. 9(1): hal. 39-44
Imelda, M, & Aida W. 2007. Regenerasi Tunas dari Kultur Tangka i Daun Iles-iles (Amorphophallus muelleri Blume) BIODIVERSITAS 9(3): hal. 173-176
Irawati. 2005. Pembentukan Kalus dan Embriogenesis Kultur Pelepah Daun Calladium hibrida. Berita Biologi 7(5): hal. 258
Kardhinata, E. H. 1999. Induksi Kalus Embrio Kedelai Pada Media MS Dengan
Penambahaan NAA dan Air Kelapa. Laporan Penelitian. Medan: Universitas
Sumatera Utara
Katuuk, J.R.P. 1989. Teknik Kultur Jaringan Dalam Mikropogasi Tanaman. Jakarta: Departemen Pandidikan dan Kebudayaan. hal. 65-68, 78, 80
Keese, J. R., Rupert, E. A. dan Carter, G. E. Physiologia Plantarum. An International Journal for Plant Biology. 81(4): hal. 513-520
Kusumo, S. 1990. Zat Pengatur Tumbuh Tanaman. Cet-2. Jakarta: Yasaguna. hal. 71
Mariani, Y., 2005. Penggandaan Tunas Krisan Melalui Kultur Jaringan. Ilmu
Pertanian 12(1): hal. 51 - 55
Marlin. 2005. Regenerasi in vitro Planlet Bebas Penyakit Layu Bakteri Pada Beberapa Taraf Konsentrasi BAP dan NAA. Junrnal Ilmu Pertanian Indonesia. 7(1): hal. 9-16
Mastalin Mandiri, 1994. Brosur Zat Pengatur Tumbuh Atonik. Jakarta
Murashige T and Skoog F., 1962. A Revised Medium For Rapid Growth And Bioassays With Tobacco Tissue Cultures. Physiol Plant 15(3): hal. 473-497.
Nasir, M. 2002. Bioteknologi: Potensi dan Keberhasilannya dalam Bidang Pertanian. Cetakan petama. Jakarta: PT. Raja Grafindo Persada. hal. 33
Nugroho, A & H. Sugito. 2004. Pedoman Pelaksanaan Teknik Kultur Jaringan. Cetakan kelima. Jakarta: Penebar Swadaya. hal. 41
Nurwahyuni, I., 2002. Upaya Perbanyakan Tanaman Kemenyan Sumatrana (Styrax
Benzoin Dryander) Melalui Kultur Pucuk, Laporan Hasil Penelitian, PPD
HEDS - FMIPA USU Medan
Pandey, S. N. Dan Chandha, A. 1996. Plant Anatomy and Embryology. New Delhi: Vikas Publishing House PVT LTD. hal. 78
Pierik, R.L.M. 1987. In vitro Culture of Higher Plants. Martinus Nijhoff Publisher. Netherland. hlm: 70, 197
Rosmayati. 1993. Penggunaan BA dan NAA Pada Kultur Mata Tunas Gladiolus hybridus Secara Kultur Jaringan. Laporan Penelitian. Medan Fakultas Pertanian Universitas Sumatera Utara. hal. 8
Robinson, T. 1995. Kandungan Organik Tumbuhan Tinggi. Edisi ke-6. Bandung: Institut Teknologi Bandung. hal. 225
Salisbury, F. B. Dan Ross. C.W. 1995. Fisiologi Tumbuhan. Jilid ke-3. Edisi ke-4 Bandung: Institut Teknologi Bandung. hal. 1, 6
Santoso, U. & F. Nursadi 1995. Kultur Jaringan Tanaman. Malang: UMM Press. Sibuea, P. 2002. Potensi Andaliman Sebagai Antioksidan Alami. http://www.compas.com. Diakses tangga l 13 April 2007
Saptarini, N., Diah P., Endang P. 2001. Membuat Tanaman Cepat Berbuah. Jakarta: Penebar Swadaya. hal. 16
Sastrosupadi, A. 2002. Rancangan Percobaan Praktis Bidang Pertanian. Edisi Revisi. Yogyakarta: Kansius. hal.102
Siregar, M. 2001. Analisis Kesejahtraan Petani Kemenyan Sebagai Komuditi Unggulan Kabupaten Tapanuli Utara. Tesis. Medan. Program Pasca Sarjana Universitas Sumatera Utara. hal. 41-42, 46
Sudarmadji, 2003. Penggunaan Benzil Amino Purine Pada Pertumbuhan Kalus Kapas Secara in vitro. Buletin Teknik Pertanian 8(1): hal 8-10
Suryowinoto, M. 1996. Pemuliaan Tanaman Secara In vitro. Cetakan pertama. Yogyakarta: Kanisius. hal. 43
Suyadi, A., Purwantoro, A. dan Trisnowati, S. 2003. Penggadaan Tunas Abaca Melalui Kultur Meristem. Ilmu Pertanian 10 (2): hal. 11 – 16
Tjitrosoepomo, G. 2000. Taksonomi Tumbuhan (Spermatophyta). Cetakan kedua. Yogyakarta: Universitas Gajah Mada. hal. 328
Triatminingsih. R , 2008. Perbanyakan bibit jeruk Citromelo dan JC (Japanese
Citroen) secara in vitro. Indonesian Agricultural Research Abstracts 25(2):
hal. 103-105
Wetter, L.R. & F. Constabel. 1991. Metode Kultur Jaringan Tanaman. Edisi ke-2. Bandung: Institut Teknik Bandung. hal. 1-3
Widaryanto, MM., Hugeng, S. 2004. Kajian Kelayakan Pemanfaatan Bibit jati Hasil Kultur Jaringan di Kawasan Transmigrasi. http://www.nakertrans.go.id. Diakses tanggal 5 agustus 2005
Widiastuty., D. 2001. Perbaikan Genetik dan Perbanyakan Bibit Secara in vitro Dalam mendukung Perkembangan Anggrek di Indonesia. Jurnal Penelitian dan
Pengembangan Pertanian 20(4): hal. 141-152
Winarsih, S. dan Priyono. 2002. Pengaruh Zat Pengatur Tumbuh Terhadap Pembentukan dan Pengakaran Tunas Mikro pada Asparagus Secara in vitro.
Badan Penelitian dan Pengembengan Pertanian. 10(1): hal 12-19
Wuryaningsih, S. dan T. Sutater.1993. Pengaruh Zat Pengatur Tumbuh dan Pupuk N terhadap Pertumbuhan dan Produksi Bunga Krisan Standard Warna Putih.
Jurnal Holtikultura. 1(1): hal 47 -56
Yusnita. 2003. Kultur Jaringan Cara Memperbanyak Tanaman Secara Efisien. Cetakan pertama. Jakarta: agromedia Pustaka. hal. 2, 9-10, 59-60
Yusnita, K. Mantja, dan D. Hapsoro. 1996. Pengaruh benziladenin, adenine, dan asam indolasetat terhadap perbanyakan tunas pisang ambon kuning secara in
LAMPIRAN A: DATA PENGAMATAN PERSENTASE KULTUR YANG HIDUP
Perlakuan Ulangan Jumlah
1 2 3 4 5
Jumlah kultur yang hidup = Jumlah eksplan yang hidup
Jumlah eksplan seluruh perlakuan
= 67
100
= 67%
X 100%
LAMPIRAN B : DATA PENGAMATAN BERAT BASAH KULTUR
Data pengamatan berat basah kultur sebelum di transformasi
Perlakuan ULANGAN Total Rataan
I II III IV V
Data pengamatan berat basah kultur setelah di transformasi (y+0,5)0,5
Perlakuan ULANGAN Total Rataan
Tabel Dua Arah
Perlakuan B0 B1 B2 B3
A0 0,34 0,35 0,33 0,40
A1 0,28 0,39 0,32 0,42
A2 0,35 0,36 0,40 0,40
A3 0,41 0,37 0,33 0,41
A4 0,44 0,38 0,42 0,39
Daftar sidik ragam berat basah kultur
SK DB JK KT F 5% 1%
Perlakuan 19 0,11 0,01 0,3891tn 3,45 4,50
A 4 0,02 0,00 0,3156tn 3,08 4,03
B 3 0,04 0,01 0,8283tn 2,98 3,92
Interaksi 12 0,06 0,00 0,3038tn 3,37 4,39
Galat 80 1,22 0,02
Total 99 1,33
LAMPIRAN C: DATA PENGAMATAN PERSENTASE KULTUR TERKONTAMINASI
Perlakuan Ulangan Jumlah
1 2 3 4 5
Persentase Kontaminasi = Jumlah kontaminasi
LAMPIRAN D. KOMPOSISI MEDIA MS
Bahan Kimia Konsentrasi dalam Media (mg/l)
Makro Nutrien
Nicotine Acid 0.500
Pyrodoxin HCl 0.500
Thyamine HCl 0.100
Myo-inositol 100.000
Sukrosa 30000.000
Agar 7000.000