KETAHANAN TANAMAN PANGAN TERHADAP APLIKASI
BIOLIGNOHERBISIDA BERBAHAN BAKU LIMBAH PERTANIAN
DENGAN PROSES HIDROLISA TERMAL
INDAH MAWARNI SUSENO
DEPARTEMEN AGRONOMI DAN HORTIKULTURA FAKULTAS PERTANIAN
INSTITUT PERTANIAN BOGOR BOGOR
PERNYATAAN MENGENAI SKRIPSI DAN
SUMBER INFORMASI SERTA PELIMPAHAN HAK CIPTA
*Dengan ini saya menyatakan bahwa skripsi berjudul Ketahanan Tanaman Utama Semusim terhadap Aplikasi ‘Biolignoherbisida’ Berbahan Baku Limbah Pertanian dengan Proses Hidrolisa Termal adalah benar karya saya dengan arahan dari komisi pembimbing dan belum diajukan dalam bentuk apa pun kepada perguruan tinggi mana pun. Sumber informasi yang berasal atau dikutip dari karya yang diterbitkan maupun tidak diterbitkan dari penulis lain telah disebutkan dalam teks dan dicantumkan dalam Daftar Pustaka di bagian akhir skripsi ini.
Dengan ini saya melimpahkan hak cipta dari karya tulis saya kepada Institut Pertanian Bogor.
Bogor, September 2015
ABSTRAK
INDAH MAWARNI SUSENO. Ketahanan Tanaman Utama Semusim terhadap
Aplikasi ‘Biolignoherbisida’ Berbahan Baku Limbah Pertanian dengan Proses Hidrolisa Termal. Dibimbing oleh HERDHATA AGUSTA.
Limbah pertanian dapat dimanfaatkan menjadi bioherbisida. Aplikasi bioherbisida di lapangan diinginkan bersifat selektif terhadap tanaman utama. Terdapat beberapa hal yang dipelajari melalui penelitian ini. Pertama, mempela-jari pengaruh ‘biolignoherbisida’ terhadap tanaman utama. Kedua, mempelajari ketahanan tanaman utama terhadap ‘biolignoherbisida’ pada beberapa fase per -tumbuhan. Ketiga, mempelajari toksisitas ‘biolignoherbisida’ dari berbagai bahan baku.
Hasil pengujian menunjukkan bioherbisida berbahan baku cangkang sawit, gambut, sekam, cangkang sawit + SO2, gambut + SO2, dan sekam + SO2
konsen-trasi 10 % tidak menghambat pertumbuhan tanaman jagung, kedelai, padi, dan kacang tanah pada aplikasi fase pratumbuh, kecambah, dan 1 MST. Bioherbisida berbahan baku cangkang sawit, cangkang sawit + SO2, gambut dan gambut + SO2,
sekam, dan sekam + SO2 konsentrasi 10 % tidak menghambat pertumbuhan
tanaman jagung, kedelai, padi, dan kacang tanah pada uji persistensi 2 MSA, 4 MSA, dan 8 MSA. Benih padi, jagung, dan kedelai pada uji bioasai tidak memi-liki ketahanan terhadap paparan seluruh ‘biolignoherbisida’ uji. Benih kacang tanah pada uji bioasai tidak memiliki ketahanan terhadap paparan bioherbisida berbahan baku cangkang sawit, sekam, cangkang sawit + SO2, dan sekam + SO2.
Benih kacang tanah memiliki ketahanan terhadap paparan bioherbisida berbahan baku gambut dan gambut + SO2.
ABSTRACT
INDAH MAWARNI SUSENO. Resistance of Annual Crops to ‘ Biolignoherbi-cides’ from Several Agricultural Wastes by The Thermal Hydrolysis. Supervised by HERDHATA AGUSTA.
Agricultural waste can be used as bioherbicide. Practically, bioherbicide application is desired to be selective to the crops. There are several things which are learned from this research. The first is effect of biolignoherbicide to the crops. Second is resistance of crops to biolignoherbicide in some growth phases. Third is biolignoherbicide toxicity from various materials.
The result of this experiment show that bioherbicide from oil palm shell, peat, paddy husk, oil palm shell + SO2, peat + SO2, and paddy husk + SO2 10% did not inhibit the growth of maize, soybean, paddy, and peanut on pre-emergence phase, emergence phase, and one week after planting (WAP). Bioherbicide from oil palm shell, peat, paddy husk, oil palm shell + SO2, peat + SO2, and paddy husk + SO2 10% did not inhibit the growth of maize, soybean, paddy, and peanut from the persistance test on 2 weeks after application (WAA), 4 WAA, and 8 WAA. Based on bioassay test, it is known that paddy, maize, and soybean are not resistant to all tested biolignoherbicides. Peanut seeds are not resistant to bioherbicide from oil palm shell, paddy husk, oil palm shell + SO2, and paddy husk + SO2 10%. Peanut seeds are resistant to bioherbicide from peat and peat + SO2.
Skripsi
sebagai salah satu syarat untuk memperoleh gelar Sarjana Pertanian
pada
Departemen Agronomi dan Hortikultura
KETAHANAN TANAMAN UTAMA SEMUSIM TERHADAP
APLIKASI BIOLIGNOHERBISIDA BERBAHAN BAKU LIMBAH
PERTANIAN DENGAN PROSES HIDROLISA TERMAL
INDAH MAWARNI SUSENO
DEPARTEMEN AGRONOMI DAN HORTIKULTURA FAKULTAS PERTANIAN
INSTITUT PERTANIAN BOGOR BOGOR
PRAKATA
Puji dan syukur penulis panjatkan kepada Allah subhanahu wa ta’ala atas segala karunia-Nya sehingga karya ilmiah ini berhasil diselesaikan. Tema yang dipilih dalam penelitian yang dilaksanakan sejak bulan Oktober 2013 sampai Januari 2014 ini ialah bioherbisida, dengan judul Ketahanan Tanaman Utama Semusim terhadap Aplikasi ‘Biolignoherbisida’ Berbahan Baku Limbah Pertanian dengan Proses Hidrolisa Termal.
Terima kasih penulis ucapkan kepada Pembimbing Akademik Bapak Dr Ir Iskandar Lubis MS dan Bapak Dr Ir Herdhata Agusta selaku Pembimbing Skripsi. Ucapan terimakasih turut penulis ucapkan kepada seluruh pihak yang membantu selama proses penelitian, pengolahan data dan skripsi, dan atas segala dukungan moral dan materiil selama penulis mengenyam pengetahuan di IPB hingga lulus.
Semoga karya ilmiah ini bermanfaat.
Bogor, September 2015
DAFTAR ISI
DAFTAR TABEL xii
DAFTAR GAMBAR xiii
DAFTAR LAMPIRAN xiii
PENDAHULUAN 1
TINJAUAN PUSTAKA 2
Biolignoherbisida 2
Fisiologi Herbisida 3
METODE 5
Tempat dan Waktu 5
Bahan dan Alat 5
Metode Penelitian 5
HASIL DAN PEMBAHASAN 8
Kondisi Umum 8
Ketahanan Tanaman Uji pada Fase Pratumbuh 8
Ketahanan Tanaman Uji pada Fase Kecambah 10
Ketahanan Tanaman Uji pada Fase 1 MST 12
Uji Persistensi ‘Biolignoherbisida’ 2 MSA di Media Tanam 14 Uji Persistensi ‘Biolignoherbisida’ 4 MSA di Media Tanam 17 Uji Persistensi ‘Biolignoherbisida’ 8 MSA di Media Tanam 19
Ketahanan Tanaman Uji pada Bioasai 21
Pembahasan Umum 26
SIMPULAN DAN SARAN 27
Simpulan 27
Saran 28
DAFTAR PUSTAKA 29
DAFTAR TABEL
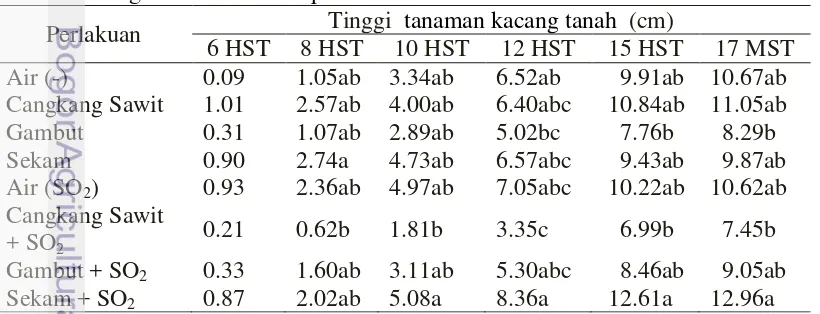
1 Tinggi tanaman kacang tanah pada aplikasi beberapa bahan baku
‘biolignoherbisida’ fase pratumbuh 8
2 Tinggi tanaman kedelai pada aplikasi beberapa bahan baku
‘biolignoherbisida’ fase pratumbuh 9
3 Tinggi tanaman jagung pada aplikasi beberapa bahan baku
‘biolignoherbisida’ fase pratumbuh 9
4 Tinggi tanaman padi pada aplikasi beberapa bahan baku
‘biolignoherbisida’ fase pratumbuh 10
5 Tinggi tanaman kacang tanah pada aplikasi beberapa bahan baku
‘biolignoherbisida’ fase kecambah 11
6 Tinggi tanaman kedelai pada aplikasi beberapa bahan baku
‘biolignoherbisida’ fase kecambah 11
7 Tinggi tanaman jagung pada aplikasi beberapa bahan baku
‘biolignoherbisida’ fase kecambah 12
8 Tinggi tanaman padi pada aplikasi beberapa bahan baku
‘biolignoherbisida’ fase kecambah 12
9 Tinggi tanaman kacang tanah pada aplikasi beberapa bahan baku
‘biolignoherbisida’ fase 1 MST 13
10 Tinggi tanaman kedelai pada aplikasi beberapa bahan baku
‘biolignoherbisida’ fase 1 MST 13
11 Tinggi tanaman jagung pada aplikasi beberapa bahan baku
‘biolignoherbisida’ fase 1 MST 14
12 Tinggi tanaman padi pada aplikasi beberapa bahan baku
‘biolignoherbisida’ fase 1 MST 14
13 Tinggi tanaman padi pada uji persistensi 2 MSA beberapa bahan
baku ‘biolignoherbisida’ 15
14 Tinggi tanaman kacang hijau pada uji persistensi 2 MSA
beberapa bahan baku ‘biolignoherbisida’ 15
15 Tinggi tanaman jagung pada uji persistensi 2 MSA beberapa
bahan baku ‘biolignoherbisida’ 16
16 Tinggi tanaman kedelai pada uji persistensi 2 MSA beberapa
bahan baku ‘biolignoherbisida’ 16
17 Tinggi tanaman padi pada uji persistensi 4 MSA beberapa bahan
baku ‘biolignoherbisida’ 17
18 Tinggi tanaman kacang hijau pada uji persistensi 4 MSA
beberapa bahan baku ‘biolignoherbisida’ 17
19 Tinggi tanaman jagung pada uji persistensi 4 MSA beberapa
bahan baku ‘biolignoherbisida’ 18
20 Tinggi tanaman kedelai pada uji persistensi 4 MSA beberapa
bahan baku ‘biolignoherbisida’ 18
21 Tinggi tanaman padi pada uji persistensi 8 MSA beberapa bahan
baku ‘biolignoherbisida’ 19
22 Tinggi tanaman kacang hijau pada uji persistensi 8 MSA beberapa
bahan baku ‘biolignoherbisida’ 19
23 Tinggi tanaman jagung pada uji persistensi 8 MSA beberapa
24 Tinggi tanaman kedelai pada uji persistensi 8 MSA beberapa
bahan baku ‘biolignoherbisida’ 20
25 Panjang akar dan jumlah benih berakar pada benih padi pada uji
bioasai beberapa bahan baku ‘biolignoherbisida’ 21 26 Panjang plumula dan jumlah benih berplumula pada benih padi
pada uji bioasai beberapa bahan baku ‘biolignoherbisida’ 22 27 Panjang akar dan jumlah benih berakar pada benih kacang tanah
pada uji bioasai beberapa bahan baku ‘biolignoherbisida’ 22 28 Panjang plumula dan jumlah benih berplumula pada benih kacang
tanah pada uji bioasai beberapa bahan baku ‘biolignoherbisida’ 23 29 Panjang akar dan jumlah benih berakar pada benih kedelai pada
uji bioasai beberapa bahan baku ‘biolignoherbisida’ 24 30 Panjang plumula dan jumlah benih berplumula pada benih kedelai
pada uji bioasai beberapa bahan baku ‘biolignoherbisida’ 24 31 Panjang akar dan jumlah benih berakar pada benih jagung pada
uji bioasai beberapa bahan baku ‘biolignoherbisida’ 25 32 Panjang plumula dan jumlah benih berplumula pada benih jagung
pada uji bioasai beberapa bahan baku ‘biolignoherbisida’ 25 33 Panjang akar seminal dan jumlah akar seminal per cawan pada
benih jagung pada uji bioasai beberapa bahan baku
‘biolignoherbisida’ 26
DAFTAR GAMBAR
1 Proses pembuatan ‘biolignoherbisida’ 6
DAFTAR LAMPIRAN
1 Uji bioasai ketahanan tanaman utama terhadap ‘biolignoherbisida’
dari beberapa bahan baku 32
2 Ketahanan tanaman utama terhadap aplikasi ‘biolignoherbisida’
PENDAHULUAN
Latar belakang
Teknik budidaya pertanian saat ini seperti penanaman dalam baris, jarak tanam yang lebar, mekanisasi, pengairan, dan pupuk sintetik memacu pertumbuh-an gulma lebih cepat. Kondisi iklim seperti suhu ypertumbuh-ang relatif tinggi dpertumbuh-an cahaya matahari melimpah mendorong pertumbuhan dan perkembangan gulma. Pertum-buhan dan perkembangan gulma yang pesat menjadi masalah dalam budidaya tanaman (Mustopa 2011). Kerugian akibat gangguan gulma diantaranya adalah penurunan produksi akibat kompetisi sumber daya (nutrisi, air, cahaya, dan CO2),
memproduksi senyawa penghambat pertumbuhan (alelopati), inang hama dan penyakit, serta menurunkan kualitas hasil karena adanya kontaminasi dari bagian-bagian gulma (Murni 1995). Pengendalian gulma karena permasalahan tersebut menjadi hal penting. Salah satu cara pengendalian gulma adalah dengan cara kimiawi seperti menggunakan herbisida.
Frekuensi dan volume penggunaan herbisida semakin meningkat seiring budidaya pertanian yang semakin intensif. Disisi lain penggunaan herbisida bersifat toksik bagi organisme lain dan lingkungan. Risiko akibat herbisida men-desak agar dalam pengendalian gulma menggunakan strategi baru dalam penggu-naan herbisida yang berisiko rendah (Bailey 2014).
Bioherbisida adalah produk pengendali gulma yang berasal dari organisme yang mampu menekan populasi gulma dan termasuk stategi pengendalian yang berisiko rendah. Keuntungan dalam penggunaan bioherbisida adalah mudah terdegradasi di lingkungan, memiliki lebih dari satu cara kerja dalam mengendali-kan gulma sehingga menurumengendali-kan risiko resistensi gulma terhadap herbisida, dan toksisitas rendah (Bailey 2014).
Pengendalian gulma menggunakan cara kimiawi pada masa pertumbuhan tanaman budidaya berisiko terhadap pertumbuhan dan perkembangan. Salah satu pertimbangan aplikasi herbisida pada masa produksi tanaman adalah mendapatkan pengendalian yang selektif, yaitu mematikan gulma tetapi tidak mengakibatkan kerusakan terhadap tanaman budidaya. Pengetahuan tentang dosis dan konsentrasi yang optimum pada tanaman oleh karena itu diperlukan, supaya kelebihan pemakaian herbisida dapat dihindari (Yakup 2002). Waktu yang tepat pada masa produksi untuk mengendalikan gulma kimiawi pun perlu diketahui. Pada bibit padi umur 21 hari lebih tahan terhadap keracunan gulma. Tanaman yang lebih muda lebih peka terhadap keracunan gulma (Pane 2003).
Tujuan
Terdapat beberapa hal yang dipelajari melalui penelitian ini. Pertama, mempelajari pengaruh ‘Biolignoherbisida’ terhadap tanaman utama Kedua, mem-pelajari pengaruh penggunaan katalisator SO2 terhadap toksisitas bioherbisida.
2
Hipotesis
Terdapat beberapa hipotesis yang diajukan pada penelitian ini. Pertama,
‘biolignoherbisida’ menghambat pertumbuhan dan merusak fisiologi tanaman utama. Kedua, ‘biolignoherbisida’ dengan katalisator SO2 lebih toksik terhadap
tanaman. Ketiga, semakin panjang fase pertumbuhan semakin besar ketahanan
tanaman utama terhadap ‘biolignoherbisida’. Keempat, semakin tinggi kandungan
lignin bahan baku maka semakin toksik ‘Biolignoherbisida’ yang dihasilkan
TINJAUAN PUSTAKA
Biolignoherbisida
Biolignoherbisida merupakan bioherbisida berasal dari dekomposisi lignin yang dihasilkan dari bagian tanaman. Lignin pada tanaman dibedakan menjadi tiga yaitu dari tanaman berkayu lunak (gymnospermae), berkayu keras (angiospermae), dan rumput atau tanaman semusim (graminae) (Pearl 1967). Lignin (20% pada kayu), selulosa (50 %), dan hemiselulosa adalah tiga komponen dominan penyusun biomassa tanaman (Bobleter 1994). Perbedaan lignin terdapat pada bagian fenilpropane atau monolignol yang bertanggung jawab pada biosintesis lignin. Proses hidrolisis lignin akan menghasilkan senyawa fenol (Freudenberg 1968).
Lignin mengandung senyawa metoksil, fenol, dan aldehid sehingga pada dekomposisi lignin akan menghasilkan senyawa tersebut. Fenol berikut susunannya merupakan senyawa kimia yang banyak dimanfaatkan sebagai insektisida, herbisida, dan fungisida. Fenol sebagai herbisida bersifat toksisitas tinggi, non selektif, dan bekerja efektif. Fenol merupakan herbisida organik dan sebagian besar bersifat rancun kontak (Oudejans 1991).
Asam fenolat merupakan salah satu dari belasan alelokimia (senyawa penyebab alelopati yang dapat menghambat pertumbuhan tanaman lain disekitarnya) (Einhellig 1995). Asam fenolat dapat bersifat racun bagi tanaman sehingga mengganggu pertumbuhan tanaman (Salisbury dan Ross 1995). Alelokimia dari senyawa fenol menghambat pertumbuhan tanaman melalui beberapa cara, antara lain dengan menghambat pembelahan dan pemanjangan sel, menghambat kerja hormon, mengubah pola kerja enzim, menghambat proses respirasi, menurunkan kemampuan fotosintesis, mengurangi pembukaan stomata, menghambat penyerapan air dan hara serta menurunkan permeabilitas membran (Devi et al. 1997).
3 suhu 270-372 oC), diperoleh produk berupa lebih dari 50 % pelarut air, 90 % pelarut aseton. Pada fase pelarut air dari degradasi hidrotermal lignin kayu Poplar pada suhu 251 oC diperoleh tujuh hidrolisat yang teridentifikasi berupa senyawa cincin tunggal (4-hydroxybenzoic acid, vanillic acid, syringic acid, vanilin, coniferyl alcohol, syringaldehyde, sinapyl alcohol) (Pecina et al 1986).
Lignoselulosa sangat sulit dihidrolisis menggunakan enzim. Salah satu cara untuk mengurai monosakarida dari struktur selulosa dan hemiselulosa adalah dengan menggunakan beberapa cara praperlakuan yang kemudian dihidrolisis dengan enzim. Fungsi dari praperlakuan adalah agar enzim dapat masuk ke selulosa dan menghidrolis hemiselulosa. Beberapa contoh teknik praperlakuan yaitu dilarutkan dalam asam (Ohgren et al. 2005). Pengayaan SO2 pada
pengukus-an Pinus radiata bermanfaat untuk meningkatkan hidrolisis hemiselulosa dan selulosa (Clark et al. 1989).
Fisiologi Herbisida
Umur tumbuhan mempengaruhi kepekaan tumbuhan terhadap herbisida. Umur tumbuhan yang lebih muda memiliki persentase pertumbuhan jaringan me-ristematik yang lebih tinggi sehingga aktivitas biologisnya lebih tinggi. Tumbuhan yang masih muda kurang mampu bertahan dibandingkan dengan tumbuhan yang sudah tua. Umur tumbuhan pada umumnya menentukan respons terhadap herbisida. Stadium pertumbuhan gulma yang sudah hampir menyelesaikan siklus hidupnya kurang peka terhadap herbisida, tetapi sebaliknya gulma yang sedang aktif tumbuh lebih peka dan mudah dikendalikan oleh herbisida. Keadaan kepe-kaan tumbuhan terhadap herbisida menentukan waktu aplikasi herbisida yang tepat (Klingman dan Ashton 1982).
Pada konsentrasi tertentu senyawa alelokimia dapat menghambat dan mengurangi hasil pada proses-proses utama tumbuhan. Hambatan tersebut misalnya terjadi pada pembentukan asam nukleat, protein, dan ATP. Jumlah ATP yang berkurang dapat menekan hampir seluruh proses metabolisme sel, sehingga sintesis zat-zat lain yang dibutuhkan oleh tumbuhan pun akan berkurang (Rice 1984; Salisbury dan Ross 1995).
Senyawa allelopati dan air yang masuk ke dalam biji akan menghambat induksi hormon pertumbuhan seperti asam giberelin (GA) dan asam indolasetat (IAA) (Yuliani 2000). Sintesis giberelin yang terhambat menyebabkan tidak
terjadi pemacuan enzim α-amilase, sehingga proses hidrolisis pati menjadi glukosa di dalam endosperma atau kotiledon berkurang. Jumlah glukosa yang ditransportasikan ke titik-titik tumbuh menjadi lebih sedikit (Rice 1984). Komponen makromolekul yang berkurang mengakibatkan sintesis protein terhambat dan akan berakibat pada terhambatnya sintesis protoplasma (Yuliani 2000). Sintesis protoplasma yang terhambat mengakibatkan proses pembelahan dan pemanjangan sel terhambat, kemudian berakibat pada terhambatnya proses perkecambahan dan pertumbuhan. Proses perkecambahan yang akan banyak kecambah yang tidak normal atau cacat (Einhellig 1986).
4
(Ardi 1999). Hambatan ini menyebabkan pembelahan sel pada bagian meristem pucuk terganggu sehingga menghambat pertumbuhan tinggi gulma maman ungu (Cleome rutidospermae) (Pebriani et al. 2013). Pemanjangan ruas batang dipe-ngaruhi oleh aktivitas hormon giberelin. Senyawa alelokimia menghambat akti-vitas giberelin, yang menyebabkan pembelahan sel pada bagian meristem inter-kalar terganggu, sehingga pemanjangan ruas batang gulma terhambat (Gardner et al. 1991).
Senyawa alelokimia dapat menyebabkan hambatan penyerapan air dan penghambatan proses fotosintesis (Sastroutomo 1990). Hambatan penyerapan air menyebabkan hambatan proses fotosintesis, karena mengakibatkan kadar air pada tanaman menjadi rendah sehingga terjadi penutupan stomata. Pengambilan CO2 menjadi terhambat karena stomata tertutup. Senyawa fenol dapat merusak struktur klorofil. Struktur klorofil yang rusak akan menghambat penyerapan cahaya yang diperlukan pada proses fotosintesis (May dan Ash 1990). Kemampuan fotosintesis yang menurun akan diikuti penurunan laju pembentukan bahan organik tanaman sehingga menurunkan nilai berat kering tanaman (Kristanto 2006).
Penghambatan pertumbuhan oleh senyawa alelokimia bersifat selektif tergantung dari jenis gulma dan sumber alelokimia, sehingga tidak semua pertumbuhan organ tumbuhan dapat dihambat oleh senyawa alelokimia (Tekcen 1974). Senyawa fenol sebagai salah satu senyawa alelokimia dapat berfungsi sebagai herbisida organik yang bersifat kontak (Oudejans 1991). Sukman dan Yakup (2002) menyatakan bahwa herbisida kontak hanya mematikan bagian yang kontak langsung dengan herbisida. Penyemprotan bioherbisida dilakukan pada bagian tajuk, sehingga hanya bagian atas tumbuhan yaitu batang dan daun yang mengalami hambatan pertumbuhan.
Cara kerja herbisida kontak dalam mematikan tumbuhan dengan merusak membran sel (Ross dan Childs [tahun tidak diketahui]). Senyawa fenol merusak gugus fosfat pada fospolipid membran sel sehingga molekul fospolipid akan terurai menjadi gliserol, asam karboksilat, dan asam fosfat dan dapat menyebabkan keluarnya zat-zat penyusun sel dan metabolit dari dalam sel (Gilman et al. 1991). Golongan herbisida kontak mengakibatkan kerusakan membran sel cepat dan mematikan tumbuhan sangat cepat. Golongan bipyridylium dan difenil eter masuk kedalam sitoplasma dan membentuk peroksida dan elektron bebas (syarat adanya cahaya) yang segera akan merusak membran sel. Kandungan minyak pada formulasi herbisida melarutkan membran sel. Kerusakan membran sel yang cepat mencegah translokasi herbisida ke bagian lain pada tumbuhan. Kerusakan tumbuhan yang parah akan tampak pada beberapa jam setelah aplikasi herbisida, gejala awal seperti busuk basah dan gejala lanjut menjadi kuning atau coklat. Waktu maksimum herbisida kontak mematikan gulma selama satu minggu atau kurang. Penyemprotan herbisida pada sebagian area hanya mematikan area yang disemprot herbisida dan muncul seperti spot-spot pada area aplikasi. Pada tanaman yang mampu bertahan akan tumbuh kembali normal (Ross dan Childs [tahun tidak diketahui]).
5 dalam tanah pada konsentrasi yang cukup untuk mempengaruhi pertumbuhan, produktivitas, dan kualitas tanaman (Alberta 2001).
METODE
Tempat dan Waktu
Penelitian ini dilaksanakan di Laboraturium Ecotoxycology Waste & Bioagents IPB Bogor. Waktu pelaksanaan penelitian pada bulan Oktober 2013 sampai Januari 2014.
Bahan dan Alat
Bahan yang digunakan adalah gas N2, gas SO2, benih jagung varietas P1,
padi varietas IPB 3S, kedelai varietas Willis, kacang tanah varietas Kingkong, furadan, aquades, dan media tanam dengan komposisi pupuk kandang, tanah, dan
sekam. Bioherbisida yang digunakan adalah ‘biolignoherbisida’ yang berasal dari
cangkang sawit, sekam, dan gambut halus. Peralatan yang digunakan adalah reaktor hidrotermal, timbangan digital, gerinda, gelas ukur, pengayak/saringan, tray, cawan petri, kertas buram, handsprayer, dan penggaris.
Metode Penelitian
Percobaan disusun dalam Rancangan Acak Lengkap. Biolignoherbisida yang digunakan berasal dari cangkang sawit, gambut, sekam, cangkang sawit + SO2, gambut + SO2, dan sekam + SO2, dan kontrol yaitu air dan air (SO2). Setiap
ulangan terdiri dari enam biolignoherbisida berbeda dan dua kontrol yang diaplikasikan secara acak. Kedelapan satuan uji tersebut diulang sebanyak delapan ulangan pada uji fase tanaman pratumbuh, kecambah, dan 1 MST (minggu setelah tanam). Pada uji fase tanaman pratumbuh, kecambah, 1 MST, dan persistensi satu petak percobaan terdiri dari 64 tanaman pada petak percobaan tray ukuran 16 x 4 lubang. Setiap tanaman uji terdiri dari delapan tanaman dalam satu petak percobaan. Pada uji bioasai diulang sebanyak empat ulangan. Setiap cawan jagung, padi, dan kedelai terdiri dari sepuluh benih. Setiap cawan kacang tanah terdiri dari lima benih. Satu petak percobaan terdiri dari enam belas cawan dan masing-masing benih uji terdiri empat cawan. Biolignoherbisida diproduksi dari bahan baku cangkang sawit, sekam, dan gambut dengan konsentrasi 20 gr bahan baku per 200 ml aquades atau konsentrasi 10 % (b/v). Pada masing-masing bahan baku diproduksi dengan dua cara yaitu dengan katalisator SO2 dan tanpa katalisator SO2.
Model liniear rancangan ini adalah sebagai berikut:
Yij = μ + Ri + Cj + Eij
Yij = nilai pengamatan tanaman terhadap aplikasi ‘biolignoherbisida’ ke-i,
dan ulangan ke-k
6
Ri = pengaruh aplikasi ‘biolignoherbisida’ ke-i, i = 1, 2, 3, 4, 5, 6, 7, 8
Cj = pengaruh ulangan ke-j, j = 1, 2, 3, 4
Eij = pengaruh galat pada aplikasi ‘biolignoherbisida’ ke-i, ulangan ke-j
Eijk = galat percobaan
Produksi Biolignoherbisida
Gambar 1 Proses pembuatan ‘biolignoherbisida’
a: penggilingan limbah pertanian; b: pengayakan hasil gilingan; c: tepung limbah pertanian hasil ayakan; d: menimbang tepung limbah pertanian sebanyak 20 g; e: mengukur aquades sebanyak 200 ml; f: reaktor hidrotermal untuk memproses bahan baku ‘biolignoherbisida’; g: alat vakum, mengeluarkan udara dari dalam reaktor; h: mengisi reaktor dengan gas N2, gas
7 Penelitian diawali dengan produksi ‘biolignoherbisida’ yang digambarkan pada Gambar 1. Pembuatan ‘biolignoherbisida’ diawali dengan grinding (penggilingan) limbah pertanian hingga berbentuk tepung. Tepung limbah pertanian diayak untuk mendapatkan ukuran partikel 20 – 30 mesh. Tepung lim-bah pertanian 20 g dan 200 ml aquades dimasukkan ke dalam tabung reaktor kemudian diaduk. Reaktor terpasang lengkap, gas O2 keluar dari reaktor untuk
membuat keadaan anaerob menggunakan alat vakum. Reaktor berisi katalisator gas N2 dan SO2 selama 1-2 menit hingga tekanan > 50 bar. Alat pengatur suhu
dalam pengaturan suhu 280 oC. Limbah pertanian didalam reaktor mengalami pemanasan pada suhu konstan kisaran 280 oC selama 30 menit.
Penyiapan media tanam seluruh petak percobaan pada tray ukuran 8 x 16 lubang untuk dua satuan percobaan. Pada pengujian ketahanan terhadap bio-herbisida pada beberapa fase pertumbuhan benih ditanam serempak. Aplikasi bioherbisida menggunakan dosis 0,6 ml/tanaman pada fase yang telah ditetapkan yaitu fase pratumbuh, kecambah, dan 1 MST (minggu setelah tanam).
Pada pengujian persistensi bioherbisida aplikasi bioherbisida serempak pada media tanam pada awal penyiapan media tanam. Benih ditanamkan pada waktu yang telah ditetapkan yaitu 2 MSA (minggu setelah aplikasi), 4 MSA, dan 8 MSA. Pada pengujian bioasai media tanam berupa lembaran kertas buram yang diletakkan dalam cawan petri. Jumlah benih padi, jagung, dan kedelai per cawan adalah sepuluh benih. Jumlah benih kacang tanah per cawan adalah lima benih. Benih di letakkan diatas cawan petri dan diaplikasikan bioherbisida.
Pengamatan
Fase pratumbuh, kecambah, dan 1 MST
Pengamatan dilakukan dengan pengukuran tinggi tanaman sejak tanaman tumbuh hingga satu minggu setelah aplikasi ‘biolignoherbisida’. Tinggi tanaman jagung dan padi diukur dari permukaan tanah sampai ujung tertinggi dengan meluruskan daun. Pada kedelai dan kacang tanah tinggi diukur sampai titik tumbuh.
Uji Persistensi
Pengamatan dilakukan dengan pengukuran tinggi tanaman sejak tanaman tumbuh hingga umur dua minggu setelah tanam. Tinggi tanaman jagung dan padi diukur dari permukaan tanah sampai ujung tertinggi dengan meluruskan daun. Pada kedelai dan kacang tanah tinggi diukur sampai titik tumbuh.
Uji Bioasai
8
HASIL DAN PEMBAHASAN
Kondisi Umum
Perkecambahan benih pada seluruh percobaan memiliki daya berkecambah 87 % hingga 100 %. Setiap satuan percobaan diusahakan mendapat pemberian air yang sama. Pada percobaan fase pertumbuhan dan persistensi setiap tanaman mendapat air rata-rata 4 mm per hari. Pada percobaan cawan ‘biolignoherbisida’ dan air diirigasikan sesuai kapasitas media tanam yang berupa lembaran kertas buram. Pada percobaan cawan ‘biolignoherbisida’ dan air diberikan hanya sekali pada saat tanam.
Serangan hama penyakit pada tanaman uji selama percobaan tidak terjadi. Hal ini terjadi terutama karena masa pertumbuhan tanaman uji singkat dan tidak ditanam dilapangan. Umur tanaman uji paling lama pada percobaan adalah 19 HST (hari setelah tanam). Kondisi lingkungan tanaman uji yang berada di teras bangunan sehingga sedikit adanya sumber hama dan penyakit. Benih uji percobaan bioasai dilakukan pada cawan tertutup.
Ketahanan Tanaman Uji pada Fase Pratumbuh
Bioherbisida diaplikasikan di permukaan tanah pada saat penanaman benih. Pengamatan diawali pada 6 HST (hari setelah tanam) menunjukkan ketahanan tanaman kacang tanah terhadap seluruh bioherbisida uji (Tabel 1). Tanaman yang diaplikasikan bioherbisida masing-masing menunjukkan pertumbuhan tinggi tanaman yang tidak berbeda. Berikutnya, pada pengamatan 17 HST pertumbuhan tinggi tanaman masing-masing bioherbisida tidak terpengaruh dibandingkan air (-) dan air (SO2) (Tabel 1). Bioherbisida berbahan baku cangkang sawit, gambut, sekam, cangkang sawit + SO2, gambut + SO2, dan sekam + SO2 pada konsentrasi
10 % (b/v) tidak berpengaruh terhadap tinggi kacang tanah pada fase pratumbuh (Tabel 1).
Tabel 1 Tinggi tanaman kacang tanah pada aplikasi beberapa bahan baku ‘biolignoherbisida’ fase pratumbuh
Keterangan: Nilai yang diikuti oleh huruf yang sama tidak berbeda nyata berdasarkan taraf uji 5% (DMRT)
Perlakuan Tinggi tanaman kacang tanah (cm)
9
Pada pengamatan awal 4 HST menunjukkan tinggi tanaman kedelai masing-masing bioherbisida tidak terpengaruh dibandingkan air (-) dan air (SO2) (Tabel 2). Selanjutnya hingga pengamatan pada 13 HST menunjukkan masing-masing bioherbisida tidak berpengaruh terhadap tinggi tanaman kedelai dibandingkan air (-) dan air (SO2) (Tabel 2). Bioherbisida berbahan baku cangkang sawit, gambut, sekam, cangkang sawit + SO2, gambut + SO2, dan sekam + SO2 pada konsentrasi
10 % (b/v) tidak berpengaruh terhadap tinggi kedelai pada fase pratumbuh (Tabel 2).
Tabel 2 Tinggi tanaman kedelai pada aplikasi beberapa bahan baku ‘bioligno
-herbisida’ fase pratumbuh
Keterangan: Nilai yang diikuti oleh huruf yang sama tidak berbeda nyata berdasarkan taraf uji 5% (DMRT)
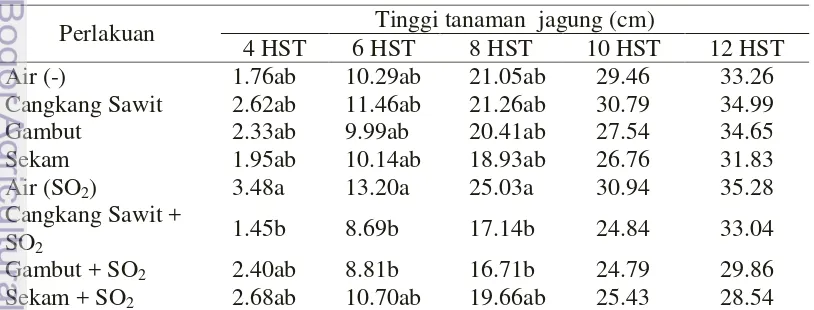
Pada 12 HST akhir pengamatan tinggi tanaman jagung menunjukkan pertumbuhan tanaman jagung tidak terpengaruh setelah aplikasi masing-masing bioherbisida (Tabel 3). Bioherbisida berbahan baku cangkang sawit, gambut, sekam, cangkang sawit + SO2, gambut + SO2, dan sekam + SO2 pada konsentrasi
10 % (b/v) tidak berpengaruh terhadap tinggi jagung pada fase pratumbuh (Tabel 3). Karena itu, tanaman jagung memiliki ketahanan terhadap seluruh bioherbisida uji.
Tabel 3 Tinggi tanaman jagung pada aplikasi beberapa bahan baku ‘bioligno
-herbisida’ fase pratumbuh
Keterangan: Nilai yang diikuti oleh huruf yang sama tidak berbeda nyata berdasarkan taraf uji 5% (DMRT)
Perlakuan Tinggi tanaman kedelai (cm)
4 HST 7 HST 10 HST 13 HST
Perlakuan Tinggi tanaman jagung (cm)
10
Bioherbisida berbahan baku cangkang sawit, gambut, sekam, cangkang sawit + SO2, gambut + SO2, dan sekam + SO2 pada konsentrasi 10 % (b/v) tidak
berpengaruh terhadap tinggi padi pada fase pratumbuh (Tabel 4). Penelitian Arifin (2015) menunjukkan bioherbisida berbahan baku sekam padi 133 g l-1 + SO2 dan cangkang sawit 133 g l-1 + SO2 menghambat perkecambahan gulma padi F. miliacea. Pertumbuhan akar F. miliacea 11.3 mm dan 12.5 mm pada aplikasi sekam padi 133 g l-1 + SO2 dan cangkang sawit 133 g l-1 + SO2 terhadap kontrol 17.3 mm pada 3 MSA. Gulma terhambat pertumbuhannya dan padi yang memiliki ketahanan terhadap bioherbisida menjadi hasil efektif untuk tujuan pengendalian gulma pada masa penanaman padi.
Tabel 4 Tinggi tanaman padi pada aplikasi beberapa bahan baku ‘
bioligno-herbisida’ fase pratumbuh
Keterangan: Nilai yang diikuti oleh huruf yang sama tidak berbeda nyata berdasarkan taraf uji 5% (DMRT)
Ketahanan Tanaman Uji pada Fase Kecambah
Bioherbisida masing-masing diaplikasikan pada 3 HST ketika tanaman uji berupa kecambah. Pada konsentrasi tertentu senyawa alelokimia dapat menghambat dan mengurangi hasil pada proses-proses utama tumbuhan (Rice 1984). Pengamatan akhir dilakukan sekitar 2 MST untuk mengetahui pengaruh bioherbisida terhadap pertumbuhan tanaman uji sejak aplikasi bioherbisida.
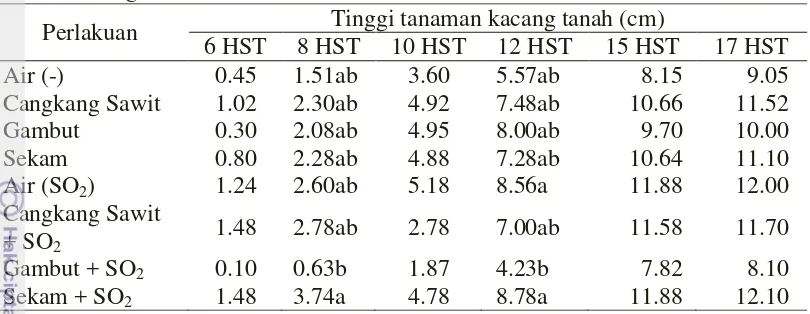
Pengamatan tinggi tanaman kacang tanah pada 17 HST menunjukkan tidak terpengaruh terhadap masing-masing bioherbisida (Tabel 5). Bioherbisida berba-han baku cangkang sawit, gambut, sekam, cangkang sawit + SO2, gambut + SO2,
dan sekam + SO2 pada konsentrasi 10 % (b/v) tidak berpengaruh terhadap tinggi
kacang tanah pada fase kecambah (Tabel 5). Jadi, tanaman kacang tanah memi-liki ketahanan terhadap seluruh bioherbisida uji.
Perlakuan Tinggi tanaman padi (cm)
11 Tabel 5 Tinggi tanaman kacang tanah pada aplikasi beberapa bahan baku
‘biolignoherbisida’ fase kecambah
Keterangan: Nilai yang diikuti oleh huruf yang sama tidak berbeda nyata berdasarkan taraf uji 5% (DMRT)
Tanaman kedelai pada 13 HST menunjukkan pertumbuhan yang tidak terpengaruh terhadap seluruh bioherbisida uji (Tabel 6). Bioherbisida berbahan baku cangkang sawit, gambut, sekam, cangkang sawit + SO2, gambut + SO2, dan
sekam + SO2 pada konsentrasi 10 % (b/v) tidak berpengaruh terhadap tinggi
kedelai pada fase kecambah (Tabel 6). Oleh sebab itu, tanaman kedelai tahan terhadap aplikasi seluruh bioherbisida uji pada fase kecambah.
Tabel 6 Tinggi tanaman kedelai pada aplikasi beberapa bahan baku ‘bioligno
-herbisida’ fase kecambah
Keterangan: Nilai yang diikuti oleh huruf yang sama tidak berbeda nyata berdasarkan taraf uji 5% (DMRT)
Tanaman jagung pada 12 HST tidak terpengaruh pertumbuhannya setelah aplikasi bioherbisida uji pada 3 HST (Tabel 7). Bioherbisida berbahan baku cangkang sawit, gambut, sekam, cangkang sawit + SO2, gambut + SO2, dan sekam
+ SO2 pada konsentrasi 10 % (b/v) tidak berpengaruh terhadap tinggi jagung pada
fase kecambah (Tabel 7). Jadi, tanaman jagung tahan terhadap aplikasi seluruh bioherbisida uji pada fase kecambah.
Perlakuan Tinggi tanaman kacang tanah (cm)
6 HST 8 HST 10 HST 12 HST 15 HST 17 HST
Perlakuan Tinggi tanaman kedelai (cm)
12
Tabel 7 Tinggi tanaman jagung pada aplikasi beberapa bahan baku ‘bioligno
-herbisida’ fase kecambah
Keterangan: Nilai yang diikuti oleh huruf yang sama tidak berbeda nyata berdasarkan taraf uji 5% (DMRT)
Bioherbisida berbahan baku cangkang sawit, gambut, sekam, cangkang sawit + SO2, gambut + SO2, dan sekam + SO2 pada konsentrasi 10 % (b/v) tidak
berpengaruh terhadap tinggi padi pada fase kecambah (Tabel 8). Penelitian Arifin (2015) menunjukkan bioherbisida berbahan baku baku sekam padi 133 g l-1 + SO2 dan cangkang sawit 133 g l-1 + SO2 menyebabkan kerusakan daun gulma F. miliacea, L. octovalvis, dan L. chinensis. Jumlah daun rusak F. miliacea, L. octovalvis, dan L. chinensis pada aplikasi bioherbisida sekam padi 133 g l-1 + SO2 berturut-turut 3.7, 6.0, dan 3.3 helai dibandingkan kontrol tidak ada kerusakan daun. Aplikasi gulma dilakukan pada fase post emergence padi dan gulma berumur sekitar satu bulan.
Tabel 8 Tinggi tanaman padi pada aplikasi beberapa bahan baku ‘bioligno
-herbisida’ fase kecambah
Keterangan: Nilai yang diikuti oleh huruf yang sama tidak berbeda nyata berdasarkan taraf uji 5% (DMRT)
Ketahanan Tanaman Uji pada Fase 1 MST
Uji pada fase 1 MST bioherbisida diaplikasikan 7 HST ke masing-masing tanaman uji. Pengamatan tinggi tanaman kacang tanah menujukkan tanaman
Perlakuan Tinggi tanaman jagung (cm)
4 HST 6 HST 8 HST 10 HST 12 HST Air (-) 2.38ab 10.81ab 21.04ab 28.74abc 33.23ab Cangkang Sawit 2.75ab 10.99ab 23.86ab 30.09ab 34.39ab
Gambut 1.44bc 8.11bc 17.76bc 24.40bc 29.28b
Perlakuan Tinggi tanaman padi (cm)
13 pertumbuhan kacang tanah tidak terpengaruh akibat aplikasi herbisida 10 hari setelah aplikasi (Tabel 9). Bioherbisida berbahan baku cangkang sawit, gambut, sekam, cangkang sawit + SO2, gambut + SO2, dan sekam + SO2 pada konsentrasi
10 % (b/v) tidak berpengaruh terhadap tinggi kacang tanah pada fase 1 MST (Tabel 9). Jadi, tanaman kacang tanah tahan terhadap seluruh bioherbisida pada aplikasi fase 1 MST.
Tabel 9 Tinggi tanaman kacang tanah pada aplikasi beberapa bahan baku
‘biolignoherbisida’ fase 1 MST
Keterangan: Nilai yang diikuti oleh huruf yang sama tidak berbeda nyata berdasarkan taraf uji 5% (DMRT)
Pengamatan tinggi tanaman kedelai 13 HST menununjukkan tanaman kedelai tidak terpengaruh terhadap aplikasi bioherbisida (Tabel 10). Bioherbisida berbahan baku cangkang sawit, gambut, sekam, cangkang sawit + SO2, gambut +
SO2, dan sekam + SO2 pada konsentrasi 10 % (b/v) tidak berpengaruh terhadap
tinggi kedelai pada fase 1 MST (Tabel 10). Oleh sebab itu, tanaman kedelai memiliki ketahanan terhadap seluruh aplikasi bioherbisida.
Tabel 10 Tinggi tanaman kedelai pada aplikasi beberapa bahan baku
‘biolignoherbisida’ fase 1 MST
Keterangan: Nilai yang diikuti oleh huruf yang sama tidak berbeda nyata berdasarkan taraf uji 5% (DMRT)
Pertumbuhan tanaman jagung tidak terpengaruh terhadap aplikasi seluruh bioherbisida (Tabel 11). Bioherbisida berbahan baku cangkang sawit, gambut,
Perlakuan Tinggi tanaman kacang tanah (cm)
6 HST 8 HST 10 HST 12 HST 15 HST 17 HST
Perlakuan Tinggi tanaman kedelai (cm)
14
sekam, cangkang sawit + SO2, gambut + SO2, dan sekam + SO2 pada konsentrasi
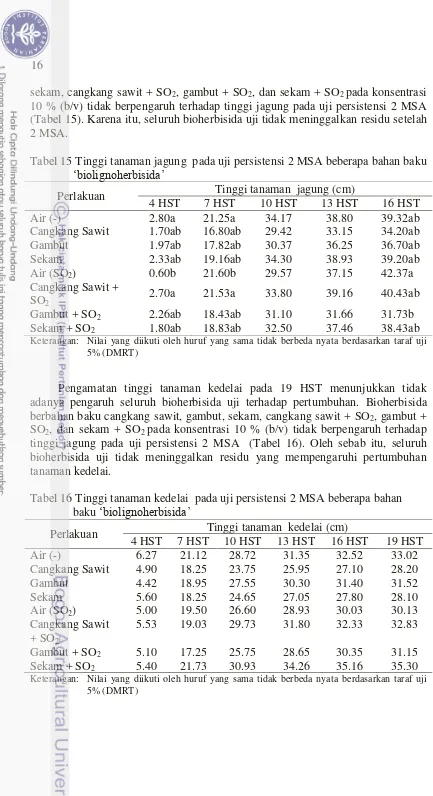
10 % (b/v) tidak berpengaruh terhadap tinggi jagung pada fase 1 MST (Tabel 11). Karena itu, tanaman jagung memiliki ketahanan terhadap seluruh bioherbisida uji. Tabel 11 Tinggi tanaman jagung pada aplikasi beberapa bahan baku
‘biolignoherbisida’ fase 1 MST
Keterangan: Nilai yang diikuti oleh huruf yang sama tidak berbeda nyata berdasarkan taraf uji 5% (DMRT)
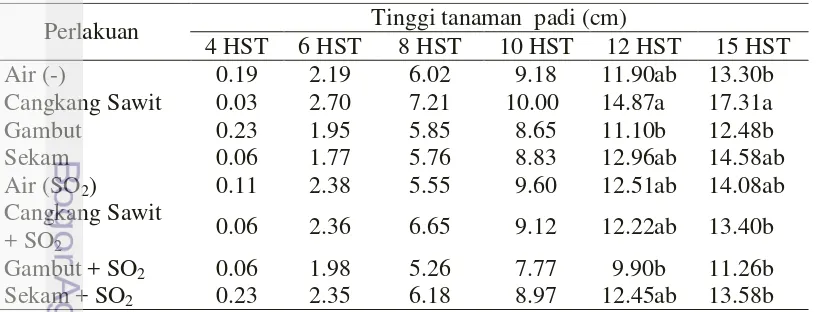
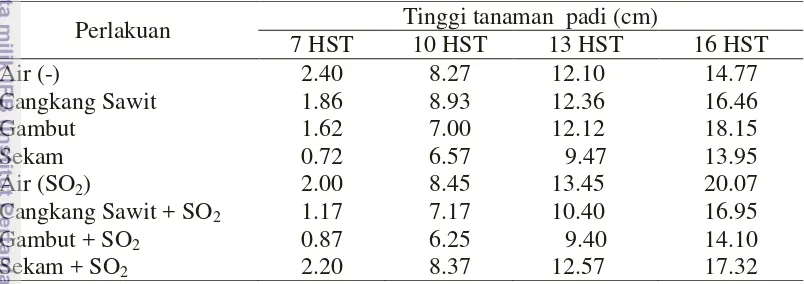
Pengamatan tinggi tanaman padi pada 15 HST menunjukkan pertumbuhan tanaman padi tidak terpengaruh terhadap aplikasi seluruh bioherbisida uji (Tabel 12). Bioherbisida berbahan baku cangkang sawit, gambut, sekam, cangkang sawit + SO2, gambut + SO2, dan sekam + SO2 pada konsentrasi 10 % (b/v) tidak
berpengaruh terhadap tinggi padi pada fase 1 MST (Tabel 12). Oleh sebab itu, tanaman padi memiliki ketahanan terhadap seluruh bioherbisida uji.
Tabel 12 Tinggi tanaman padi pada aplikasi beberapa bahan baku
‘biolignoherbisida’ fase 1 MST
Keterangan: Nilai yang diikuti oleh huruf yang sama tidak berbeda nyata berdasarkan taraf uji 5% (DMRT)
Uji Persistensi ‘Biolignoherbisida’ 2 MSA di Media Tanam
Bioherbisida berbahan baku cangkang sawit, gambut, cangkang sawit + SO2,
gambut + SO2, dan sekam + SO2 pada konsentrasi 10 % (b/v) tidak berpengaruh
Perlakuan Tinggi tanaman jagung (cm)
4 HST 6 HST 8 HST 10 HST 12 HST
Perlakuan Tinggi tanaman padi (cm)
15 terhadap tinggi padi pada uji persistensi 2 MSA (Tabel 13). Bioherbisida berbahan baku sekam pada konsentrasi 10 % (b/v) berpengaruh terhadap tinggi padi pada uji persistensi 2 MSA (Tabel 13). Media tanam yang mengandung residu bioherbisida berbahan baku sekam menyebabkan tanaman padi terhambat pertumbuhannya dibandingkan kontrol.
Tabel 13 Tinggi tanaman padi pada uji persistensi 2 MSA beberapa bahan baku
‘biolignoherbisida’
Keterangan: Nilai yang diikuti oleh huruf yang sama tidak berbeda nyata berdasarkan taraf uji 5% (DMRT)
Pengamatan tinggi tanaman kacang hijau menunjukkan tidak adanya pengaruh bioherbisida uji terhadap pertumbuhan (Tabel 14). Oleh sebab itu, bioherbisida uji tidak meninggalkan residu. Bioherbisida berbahan baku cangkang sawit, gambut, sekam, cangkang sawit + SO2, gambut + SO2, dan sekam + SO2
pada konsentrasi 10 % (b/v) tidak berpengaruh terhadap tinggi kacang hijau pada uji persistensi 2 MSA (Tabel 14).
Tabel 14 Tinggi tanaman kacang hijau pada uji persistensi 2 MSA beberapa bahan baku ‘biolignoherbisida’
Keterangan: Nilai yang diikuti oleh huruf yang sama tidak berbeda nyata berdasarkan taraf uji 5% (DMRT)
Pengamatan tinggi tanaman jagung menunjukkan tidak adanya pengaruh seluruh bioherbisida uji. Bioherbisida berbahan baku cangkang sawit, gambut,
Perlakuan Tinggi tanaman padi (cm)
7 HST 10 HST 13 HST 16 HST 19 HST
Air (-) 5.22 10.02ab 14.20ab 19.25abc 23.90a
Cangkang Sawit 5.30 10.87ab 13.35ab 17.10abc 18.85abc
Gambut 6.15 11.80a 16.02a 20.80a 22.57ab
Perlakuan Tinggi tanaman kacang hijau (cm)
16
sekam, cangkang sawit + SO2, gambut + SO2, dan sekam + SO2 pada konsentrasi
10 % (b/v) tidak berpengaruh terhadap tinggi jagung pada uji persistensi 2 MSA (Tabel 15). Karena itu, seluruh bioherbisida uji tidak meninggalkan residu setelah 2 MSA.
Tabel 15 Tinggi tanaman jagung pada uji persistensi 2 MSA beberapa bahan baku
‘biolignoherbisida’
Keterangan: Nilai yang diikuti oleh huruf yang sama tidak berbeda nyata berdasarkan taraf uji 5% (DMRT)
Pengamatan tinggi tanaman kedelai pada 19 HST menunjukkan tidak adanya pengaruh seluruh bioherbisida uji terhadap pertumbuhan. Bioherbisida berbahan baku cangkang sawit, gambut, sekam, cangkang sawit + SO2, gambut +
SO2, dan sekam + SO2 pada konsentrasi 10 % (b/v) tidak berpengaruh terhadap
tinggi jagung pada uji persistensi 2 MSA (Tabel 16). Oleh sebab itu, seluruh bioherbisida uji tidak meninggalkan residu yang mempengaruhi pertumbuhan tanaman kedelai.
Tabel 16 Tinggi tanaman kedelai pada uji persistensi 2 MSA beberapa bahan baku ‘biolignoherbisida’
Keterangan: Nilai yang diikuti oleh huruf yang sama tidak berbeda nyata berdasarkan taraf uji 5% (DMRT)
Perlakuan Tinggi tanaman jagung (cm)
4 HST 7 HST 10 HST 13 HST 16 HST
Perlakuan Tinggi tanaman kedelai (cm)
17 Uji Persistensi ‘Biolignoherbisida’ 4 MSA di Media Tanam
Bioherbisida uji diaplikasikan pada permukaan media tanam. Selanjutnya, 4 MSA dilakukan penanaman tanaman pangan. Pengamatan akhir tanaman padi pada 16 HST menunjukkan seluruh bioherbisida uji tidak mempengaruhi pertumbuhan tanaman padi (Tabel 17). Bioherbisida berbahan baku cangkang sawit, gambut, sekam, cangkang sawit + SO2, gambut + SO2, dan sekam + SO2
pada konsentrasi 10 % (b/v) tidak berpengaruh terhadap tinggi padi pada uji persistensi 4 MSA (Tabel 17). Karena itu, seluruh bioherbisida uji tidak meninggalkan residu.
Tabel 17 Tinggi tanaman padi pada uji persistensi 4 MSA beberapa bahan baku
‘biolignoherbisida’
Keterangan: Nilai yang diikuti oleh huruf yang sama tidak berbeda nyata berdasarkan taraf uji 5% (DMRT)
Pengamatan tinggi tanaman kacang hijau pada 16 HST menunjukkan tidak adanya pengaruh bioherbisida uji terhadap pertumbuhan tanaman kacang hijau (Tabel 18). Bioherbisida berbahan baku cangkang sawit, gambut, sekam, cangkang sawit + SO2, gambut + SO2, dan sekam + SO2 pada konsentrasi 10 %
(b/v) tidak berpengaruh terhadap tinggi kacang hijau pada uji persistensi 4 MSA (Tabel 18). Jadi, seluruh bioherbisida uji tidak meninggalkan residu setelah 4 MSA.
Tabel 18 Tinggi tanaman kacang hijau pada uji persistensi 4 MSA beberapa bahan baku ‘biolignoherbisida’
Keterangan: Nilai yang diikuti oleh huruf yang sama tidak berbeda nyata berdasarkan taraf uji 5% (DMRT)
Perlakuan Tinggi tanaman padi (cm)
7 HST 10 HST 13 HST 16 HST
Perlakuan Tinggi tanaman kacang hijau (cm)
18
Bioherbisida berbahan baku cangkang sawit, gambut, sekam, cangkang sawit + SO2, gambut + SO2, dan sekam + SO2 pada konsentrasi 10 % (b/v) tidak
berpengaruh terhadap tinggi jagung pada uji persistensi 4 MSA (Tabel 19).
Tabel 19 Tinggi tanaman jagung pada uji persistensi 4 MSA beberapa bahan baku
‘biolignoherbisida’
Keterangan: Nilai yang diikuti oleh huruf yang sama tidak berbeda nyata berdasarkan taraf uji 5% (DMRT)
Pengamatan tinggi tanaman kedelai pada 16 HST menunjukkan seluruh bioherbisida uji tidak mempengaruhi pertumbuhan tanaman kedelai (Tabel 20). Bioherbisida berbahan baku cangkang sawit, gambut, sekam, cangkang sawit + SO2, gambut + SO2, dan sekam + SO2 pada konsentrasi 10 % (b/v) tidak
berpengaruh terhadap tinggi kedelai pada uji persistensi 4 MSA (Tabel 20). Karena itu, seluruh bioherbisida uji tidak meninggalkan residu setelah 4 MSA.
Tabel 20 Tinggi tanaman kedelai pada uji persistensi 4 MSA beberapa bahan baku
‘biolignoherbisida’
Keterangan: Nilai yang diikuti oleh huruf yang sama tidak berbeda nyata berdasarkan taraf uji 5% (DMRT)
Perlakuan Tinggi tanaman jagung (cm)
4 HST 7 HST 10 HST 13 HST 16 HST
Perlakuan Tinggi tanaman kedelai (cm)
19 Uji Persistensi ‘Biolignoherbisida’ 8 MSA di Media Tanam
Bioherbisida uji diaplikasikan ke permukaan media tanam pada 14 HST. Selanjutnya, tanaman uji tumbuh di media tanam setelah 8 MSA. Pengamatan tinggi tanaman padi pada 14 HST menunjukkan seluruh bioherbisida uji tidak mempengaruhi pertumbuhan tanman padi (Tabel 21).. Bioherbisida berbahan baku cangkang sawit, gambut, sekam, cangkang sawit + SO2, gambut + SO2, dan
sekam + SO2 pada konsentrasi 10 % (b/v) tidak berpengaruh terhadap tinggi padi
pada uji persistensi 8 MSA (Tabel 21). Oleh sebab itu, seluruh bioherbisida uji tidak meninggalkan residu setelah 8 MSA.
Tabel 21 Tinggi tanaman padi pada uji persistensi 8 MSA beberapa bahan baku
‘biolignoherbisida’
Keterangan: Nilai yang diikuti oleh huruf yang sama tidak berbeda nyata berdasarkan taraf uji 5% (DMRT)
Pengamatan tanaman kacang hijau pada 17 HST menunjukkan seluruh bioherbisida uji tidak mempengaruhi pertumbuhan tanaman kacang hijau. Bioherbisida berbahan baku cangkang sawit, gambut, sekam, cangkang sawit + SO2, gambut + SO2, dan sekam + SO2 pada konsentrasi 10 % (b/v) tidak
berpengaruh terhadap tinggi kacang hijau pada uji persistensi 8 MSA (Tabel 22). Jadi, seluruh bioherbisida uji tidak meninggalkan residu setelah 8 MSA.
Tabel 22 Tinggi tanaman kacang hijau pada uji persistensi 8 MSA beberapa bahan baku ‘biolignoherbisida’
Keterangan: Nilai yang diikuti oleh huruf yang sama tidak berbeda nyata berdasarkan taraf uji 5% (DMRT)
Perlakuan Tinggi tanaman padi (cm)
6 HST 8 HST 11 HST 14 HST
Perlakuan Tinggi tanaman kacang hijau (cm)
20
Pengamatan tinggi tanaman jagung pada 17 HST menunjukkan seluruh bioherbisida uji tidak berpengaruh nyata terhadap pertumbuhan tanaman jagung (Tabel 23). Bioherbisida berbahan baku cangkang sawit, gambut, sekam, cangkang sawit + SO2, gambut + SO2, dan sekam + SO2 pada konsentrasi 10 %
(b/v) tidak berpengaruh terhadap tinggi tanaman jagung pada uji persistensi 8 MSA (Tabel 23). Karena itu, seluruh bioherbisida uji tidak meninggalkan residu setelah 8 MSA.
Tabel 23 Tinggi tanaman jagung pada uji persistensi 8 MSA beberapa bahan baku
‘biolignoherbisida’
Keterangan: Nilai yang diikuti oleh huruf yang sama tidak berbeda nyata berdasarkan taraf uji 5% (DMRT)
Pengamatan tanaman kedelai menunjukkan seluruh bioherbisida uji tidak mempengaruhi pertumbuhan tanaman kedelai (Tabel 24). Bioherbisida berbahan baku cangkang sawit, gambut, sekam, cangkang sawit + SO2, gambut + SO2, dan
sekam + SO2 pada konsentrasi 10 % (b/v) tidak berpengaruh terhadap tinggi
tanaman kedelai pada uji persistensi 8 MSA (Tabel 24). Oleh sebab itu, seluruh bioherbisida uji tidak meninggalkan residu.
Tabel 24 Tinggi tanaman kedelai pada uji persistensi 8 MSA beberapa bahan baku
‘biolignoherbisida’
Keterangan: Nilai yang diikuti oleh huruf yang sama tidak berbeda nyata berdasarkan taraf uji 5% (DMRT)
Perlakuan Tinggi tanaman jagung (cm)
6 HST 8 HST 11 HST 14 HST 17 HST
Perlakuan Tinggi tanaman kedelai (cm)
21
Ketahanan Tanaman Uji pada Bioasai
Bioasai merupakan metode langsung untuk menentukan keamanan pertumbuhan tanaman utama saat terpapar herbisida yang tidak diketahui atau sejarah lahan tidak diketahui pernah terkena herbisida. Bioasai dapat mendeteksi jika herbisida atau residu bahan kimia terkandung dalam tanah pada konsentrasi yang cukup untuk mempengaruhi pertumbuhan, produktivitas, dan kualitas tanaman (Alberta 2001). Benih uji menyerap larutan bioherbisida untuk perke-cambahan pada uji bioasai. Selanjutnya, pengamatan dilakukan untuk mengetahui ketahanan tanaman pangan terhadap masing-masing bioherbisida.
Bioherbisida berbahan baku cangkang sawit, gambut, sekam, cangkang sawit + SO2, gambut + SO2, dan sekam + SO2 (Tabel 25) mampu menghambat
panjang akar padi dibandingkan kontrol. Bioherbisida berbahan baku cangkang sawit, gambut, sekam, cangkang sawit + SO2, dan sekam +SO2 (Tabel 25)
mam-pu menghambat jumlah benih padi berakar dibandingkan kontrol. Padi yang ter-papar bioherbisida gambut + SO2 jumlah benih berakarnya tidak berbeda
diban-dingkan kontrol (Tabel 25). Benih padi pada uji bioasai tidak memiliki ketahanan terhadap paparan seluruh ‘biolignoherbisida’ uji.
Tabel 25 Panjang akar dan jumlah benih berakar pada benih padi pada uji bioasai beberapa bahan baku ‘biolignoherbisida’
Keterangan: Nilai yang diikuti oleh huruf yang sama tidak berbeda nyata berdasarkan taraf uji 5% (DMRT)
Bioherbisida berbahan baku cangkang sawit, gambut, sekam, cangkang sawit + SO2, gambut + SO2, dan sekam + SO2 (Tabel 26) menghambat panjang
plumula padi dibandingkan kontrol. Bioherbisida berbahan baku cangkang sawit, sekam, cangkang sawit + SO2, dan sekam +SO2 (Tabel 26) menghambat jumlah
benih padi berplumula dibandingkan kontrol. Padi yang terpapar bioherbisida gambut dan gambut + SO2 jumlah benih berplumulanya tidak berbeda
diban-dingkan kontrol (Tabel 26). Benih padi pada uji bioasai tidak memiliki ketahanan terhadap paparan seluruh ‘biolignoherbisida’ uji.
Perlakuan Panjang akar (mm) Jumlah benih berakar
22
Tabel 26 Panjang plumula dan jumlah benih berplumula pada benih padi pada uji bioasai beberapa bahan baku ‘biolignoherbisida’
Keterangan: Nilai yang diikuti oleh huruf yang sama tidak berbeda nyata berdasarkan taraf uji 5% (DMRT)
Bioherbisida berbahan baku cangkang sawit, sekam, cangkang sawit + SO2,
dan sekam + SO2 (Tabel 27) mampu menghambat panjang akar kacang tanah
dibandingkan kontrol. Benih kacang tanah yang terpapar bioherbisida gambut dan gambut + SO2 panjang akarnya tidak berbeda dibandingkan kontrol (Tabel 27).
Bioherbisida berbahan baku cangkang sawit, sekam, cangkang sawit + SO2, dan
sekam + SO2 (Tabel 27) menghambat jumlah benih kacang tanah berakar
dibandingkan kontrol. Kacang tanah yang terpapar bioherbisida gambut dan gambut + SO2 jumlah benih berakarnya tidak berbeda dibandingkan kontrol
(Tabel 27). Benih kacang tanah pada uji bioasai tidak memiliki ketahanan terhadap paparan bioherbisida berbahan baku cangkang sawit, sekam, cangkang sawit +SO2, dan sekam + SO2. Benih kacang tanah memiliki ketahanan terhadap
paparan bioherbisida berbahan baku gambut dan gambut + SO2.
Tabel 27 Panjang akar dan jumlah benih berakar pada benih kacang tanah pada uji bioasai beberapa bahan baku ‘biolignoherbisida’
Keterangan: Nilai yang diikuti oleh huruf yang sama tidak berbeda nyata berdasarkan taraf uji 5% (DMRT)
Bioherbisida berbahan baku cangkang sawit, sekam, cangkang sawit + SO2,
dan sekam + SO2 (Tabel 28) menghambat panjang plumula kacang tanah
Perlakuan Panjang plumula (mm) Jumlah benih berplumula 48 Jam 90 Jam 48 Jam 90 Jam
Perlakuan Panjang akar (mm) Jumlah benih berakar
23 dibandingkan kontrol. Benih kacang tanah yang terpapar bioherbisida gambut dan gambut + SO2 panjang plumulanya tidak berbeda dibandingkan kontrol (Tabel 28).
Oleh sebab itu, pertumbuhan plumula kacang tanah mampu tumbuh baik hanya pada bioherbisida gambut dan gambut + SO2.
Bioherbisida berbahan baku cangkang sawit, sekam, cangkang sawit +SO2,
dan sekam +SO2 (Tabel 28) menghambat jumlah benih kacang tanah berplumula
dibandingkan kontrol. Kacang tanah yang terpapar bioherbisida gambut dan gambut + SO2 jumlah benih berplumulanya tidak berbeda dibandingkan kontrol
(Tabel 28). Benih kacang tanah pada uji bioasai tidak memiliki ketahanan terhadap paparan bioherbisida berbahan baku cangkang sawit, sekam, cangkang sawit +SO2, dan sekam +SO2. Benih kacang tanah memiliki ketahanan terhadap
paparan bioherbisida berbahan baku gambut dan gambut + SO2.
Tabel 28 Panjang plumula dan jumlah benih berplumula pada benih kacang tanah pada uji bioasai beberapa bahan baku ‘biolignoherbisida’
Keterangan: Nilai yang diikuti oleh huruf yang sama tidak berbeda nyata berdasarkan taraf uji 5% (DMRT)
Bioherbisida berbahan baku cangkang sawit, gambut, sekam, cangkang sawit + SO2, gambut + SO2, dan sekam + SO2 (Tabel 29) mampu menghambat
panjang akar kedelai dibandingkan kontrol. Bioherbisida berbahan baku cangkang sawit, sekam, cangkang sawit + SO2, dan sekam + SO2 (Tabel 29) mampu
menghambat jumlah benih kedelai berakar dibandingkan kontrol. Kedelai yang terpapar bioherbisida gambut dan gambut + SO2 jumlah benih berakarnya tidak
terpengaruh dibandingkan kontrol (Tabel 29). Selanjutnya, kemampuan perkecambahan kedelai terhadap bioherbisida gambut dan gambut + SO2 yang
baik. Walau demikian, benih kedelai terpengaruh pertumbuhan akarnya terhadap seluruh bioherbisida. Oleh sebab itu, benih kedelai pada uji bioasai tidak memiliki ketahanan terhadap paparan seluruh ‘biolignoherbisida’ uji.
Perlakuan Panjang plumula (mm) Jumlah benih berplumula 48 Jam
Air (-) 8.15a 4.25a
Cangkang Sawit 0.50b 0.25c
24
Tabel 29 Panjang akar dan jumlah benih berakar pada benih kedelai pada uji bioasai beberapa bahan baku ‘biolignoherbisida’
Keterangan: Nilai yang diikuti oleh huruf yang sama tidak berbeda nyata berdasarkan taraf uji 5% (DMRT)
Bioherbisida berbahan baku cangkang sawit, gambut, sekam, cangkang sawit + SO2, gambut + SO2, dan sekam + SO2 (Tabel 30) mampu menghambat
panjang plumula kedelai dibandingkan kontrol. Bioherbisida berbahan baku cang-kang sawit, sekam, cangcang-kang sawit + SO2, dan sekam + SO2 (Tabel 30) mampu
menghambat jumlah benih kedelai berplumula dibandingkan kontrol. Kedelai yang terpapar bioherbisida gambut dan gambut + SO2 jumlah benih
berplu-mulanya tidak berbeda dibandingkan kontrol (Tabel 30). Benih kedelai pada uji bioasai tidak memiliki ketahanan terhadap paparan seluruh ‘biolignoherbisida’ uji.
Tabel 30 Panjang plumula dan jumlah benih berplumula pada benih kedelai pada uji bioasai beberapa bahan baku ‘biolignoherbisida’
Keterangan: Nilai yang diikuti oleh huruf yang sama tidak berbeda nyata berdasarkan taraf uji 5% (DMRT)
Bioherbisida berbahan baku cangkang sawit, sekam, cangkang sawit + SO2,
dan sekam + SO2 (Tabel 31) mampu menghambat panjang akar jagung
dibandingkan kontrol. Benih jagung yang terpapar bioherbisida gambut dan gambut + SO2 panjang akarnya tidak berbeda dibandingkan kontrol (Tabel 31).
Bioherbisida berbahan baku cangkang sawit, sekam, cangkang sawit + SO2, dan
sekam + SO2 (Tabel 31) mampu menghambat jumlah benih jagung berplumula
dibandingkan kontrol. Jagung yang terpapar bioherbisida gambut dan gambut + SO2 jumlah benih berakarnya tidak berbeda dibandingkan kontrol (Tabel 31).
Perlakuan Panjang akar (mm) Jumlah benih berakar
24 36 48 72 24 36 48 72
Perlakuan Panjang plumula (mm) Jumlah benih berplumula 48 Jam
Air (-) 25.60a 9.75a
Cangkang Sawit 0.00c 0.00c
25 Benih jagung pada uji bioasai tidak memiliki ketahanan terhadap paparan bioherbisida berbahan baku cangkang sawit, sekam, cangkang sawit + SO2, dan
sekam + SO2. Benih jagung memiliki ketahanan terhadap paparan bioherbisida
berbahan baku gambut dan gambut + SO2.
Tabel 31 Panjang akar dan jumlah benih berakar pada benih jagung pada uji bioasai beberapa bahan baku ‘biolignoherbisida’
Perlakuan Panjang akar (mm) Jumlah benih berakar
36 48 72 36 48 72
Keterangan: Nilai yang diikuti oleh huruf yang sama tidak berbeda nyata berdasarkan taraf uji 5% (DMRT)
Bioherbisida berbahan baku cangkang sawit, sekam, cangkang sawit +SO2,
dan sekam + SO2 (Tabel 32) mampu menghambat panjang plumula jagung
dibandingkan kontrol. Benih jagung yang terpapar bioherbisida gambut dan gambut + SO2 panjang plumulanya tidak berbeda dibandingkan kontrol (Tabel 32).
Bioherbisida berbahan baku cangkang sawit, sekam, cangkang sawit + SO2, dan
sekam + SO2 (Tabel 32) mampu menghambat jumlah benih jagung berplumula
dibandingkan kontrol. Jagung yang terpapar bioherbisida gambut dan gambut + SO2 jumlah benih berakarnya tidak berbeda dibandingkan kontrol (Tabel 32).
Tabel 32 Panjang plumula dan jumlah benih berplumula pada benih jagung pada uji bioasai beberapa bahan baku ‘biolignoherbisida’
Keterangan: Nilai yang diikuti oleh huruf yang sama tidak berbeda nyata berdasarkan taraf uji 5% (DMRT)
Bioherbisida berbahan baku cangkang sawit dan cangkang sawit + SO2
(Tabel 33) mampu menghambat panjang akar seminal jagung dibandingkan kontrol. Benih jagung yang terpapar bioherbisida gambut, sekam, gambut + SO2,
dan sekam + SO2 panjang akar seminalnya tidak berbeda dibandingkan kontrol
(Tabel 33). Bioherbisida berbahan baku cangkang sawit (Tabel 33) mampu Perlakuan Panjang plumula (mm) Jumlah benih berplumula
48 Jam
Air (-) 7.67a 6.00a
Cangkang Sawit 0.00c 0.00b
26
menghambat jumlah benih jagung berakar seminal dibandingkan kontrol. Jagung yang terpapar bioherbisida gambut, sekam, cangkang sawit + SO2, gambut + SO2,
dan sekam + SO2 jumlah benih berakar seminal tidak berbeda dibandingkan
kontrol (Tabel 33). Benih jagung pada uji bioasai tidak memiliki ketahanan terhadap paparan seluruh bioherbisida uji. Hal tersebut karena panjang akar dan panjang plumula jagung terhambat oleh seluruh bioherbisida uji gambut dan gambut + SO2 pada pengukuran faktor vegetatif lain tidak berpengaruh .
Tabel 33 Panjang akar seminal dan jumlah akar seminal per cawan pada benih jagung pada uji bioasai beberapa bahan baku ‘biolignoherbisida’
Keterangan: Nilai yang diikuti oleh huruf yang sama tidak berbeda nyata berdasarkan taraf uji 5% (DMRT)
Pembahasan Umum
Bioherbisida dengan bahan baku tertentu pada fase pertumbuhan tertentu yang mampu menghambat pertumbuhan masing-masing tanaman uji menunjuk-kan tanaman tidak tahan. Tanaman yang tidak tahan pada fase tersebut tidak boleh terpapar bioherbisida yang mampu menghambat pertumbuhannya. Hambatan per-tumbuhan pada karakter vegetatif akan menghambat produktivitas tanaman.
Bioherbisida dengan bahan baku tertentu yang tidak berpengaruh terhadap pertumbuhan tanaman uji menunjukkan ketahanan tanaman uji. Pada fase pertum-buhan tersebut aplikasi herbisida diperbolehkan. Pada fase pertumpertum-buhan tersebut aplikasi herbisida diharapkan mampu mengendalikan gulma namun tidak mempengaruhi pertumbuhan tanaman utama.
Pada uji persistensi seluruh bioherbisida pada konsentrasi 10 % (b/v) tidak meninggalkan residu sejak 2 MSA. Hal tersebut ditunjukkan oleh tidak adanya hambatan pertumbuhan seluruh tanaman uji sejak 2 MSA. Pada umumnya persistensi herbisida di dalam tanah lebih pendek daripada insektisida dan bervariasi dari beberapa minggu hingga beberapa tahun, bergantung pada struktur dan sifat tanah serta kandungan air di dalam tanah. Herbisida persistensi rendah menandakan lamanya aktivitas biologi herbisida dalam tanah termasuk rendah (Soerjandono 2005).
Bioherbisida dengan bahan baku tertentu yang tidak berpengaruh terhadap pertumbuhan tanaman utama pada uji bioasai menunjukkan ketahanan tanaman uji. Ketahanan tanaman utama pada uji bioasai memproyeksikan tanaman tidak akan
Perlakuan Panjang akar seminal (mm)
27
terhambat pertumbuhannya jika terpapar ‘biolignoherbisida’ tersebut pada fase pertumbuhan selanjutnya. Ketahanan tanaman utama dapat berubah jika
konsentrasi ‘biolignoherbisida’ meningkat pada taraf toksik terhadap tanaman utama.
Bioherbisida dengan bahan baku tertentu yang berpengaruh terhadap penghambatan pertumbuhan tanaman utama pada uji bioasai menunjukkan tanaman tidak tahan. Tanaman yang tidak tahan pada uji bioasai diproyeksikan akan terhambat pertumbuhannya jika terpapar ‘biolignoherbisida’ konsentrasi 10 % tersebut pada fase selanjutnya. Tanaman utama diproyeksikan lebih tidak
tahan jika terpapar ‘biolignoherbisida’ tersebut pada konsentrasi lebih tinggi.
Panjang akar berhubungan dengan penyerapan air dan hara. Akar semakin panjang maka penyerapan air dan hara semakin besar. Air dan hara yang diserap tanaman berhubungan dengan metabolisme tanaman, semakin besar air dan hara semakin besar metabolisme tanaman. Metabolisme tanaman yang besar menyebabkan pertumbuhan dan perkembangan tanaman semakin baik. Pertumbuhan yang baik pada uji bioasai ditunjukkan dengan panjang akar dan panjang plumula. Jumlah benih berakar dan berplumula berhubungan dengan jumlah benih yang tumbuh. Herbisida pratumbuh mencegah perkecambahan benih salah satunya dengan menghambat enzim, sehingga menurunkan aktivitas enzim (Pujisiswanto et al. 2014). Hasil penelitian Pott (2008) bahwa benih selada yang terpapar langsung asam asetat pada konsentrasi 1-10 % tidak menghasilkan kecambah dan akar.
‘Biolignoherbisida’ berbahan bakugambut dan gambut + SO2 berdasarkan
uji bioasai (Tabel 25-33) memiliki toksisitas lebih rendah dibandingkan
‘biolignoherbisida’ cangkang sawit, sekam, cangkang sawit + SO2, dan sekam +
SO2. Uji bioasai (Tabel 25-33) menginterpretasikan tanaman yang terpapar
‘biolignoherbisida’ berbahan baku gambut dan gambut + SO2 memiliki nilai
pengukuran lebih besar dibandingkan ‘biolignoherbisida’ cangkang sawit, sekam, cangkang sawit + SO2, dan sekam + SO2.
SIMPULAN DAN SARAN
Simpulan
Bioherbisida berbahan baku cangkang sawit, gambut, sekam, cangkang sawit + SO2, gambut + SO2, dan sekam + SO2 konsentrasi 10 % tidak
mengham-bat pertumbuhan tanaman jagung, kedelai, padi, dan kacang tanah pada aplikasi fase pratumbuh, kecambah, dan 1 MST. Bioherbisida berbahan baku cangkang sawit, gambut, sekam, cangkang sawit + SO2, gambut + SO2, dan sekam + SO2
konsentrasi 10 % tidak menghambat pertumbuhan tanaman jagung, kedelai, padi, dan kacang tanah pada uji persistensi 2 MSA, 4 MSA, dan 8 MSA.
28
kacang tanah memiliki ketahanan terhadap paparan bioherbisida berbahan baku gambut dan gambut + SO2.
Saran
Penelitian lanjutan pada dosis ‘biolignoherbisida’ yang lebih tinggi karena penelitiaan ini sejalan dengan pengujian ‘biolignoherbisida’ pada beberapa tingkat
dosis. Serta adanya ketahanan tanaman terhadap ‘biolignoherbisida’. Pengujian
29
DAFTAR PUSTAKA
Alberta Research Council (Alberta). 2001. Plant bioasai techniques for detecting and identifying herbicide residues in soil. Agri-fact [internet]. Tersedia pada: http://ucanr.edu/blogs/UCDWeedScience/blogfiles /8850.pdf. [08 Mei 2015].
Ardi. 1999. Potensi alelopati akar rimpang alang- alang (Imperata cylindrica L.) terhadap Mimosa pudica L. Stigma. Volume 7(1): 66-68.
Arifin B. 2015. Pemanfaatan hidrolisat lignoselulosa sebagai bioherbisida untuk pengendalian gulma pada padi sawah dan kelapa sawit. [Tesis]. Bogor (ID): Institut Pertanian Bogor.
Bailey KL. 2014. Integrated pest management: current concepts and ecological
perspective. Massachusetts (US): Academic Press [internet]. [diunduh 14
Okt 2013]; 13: 245-266. Tersedia pada: http://www.sciencedirect.com/ science/article/pii/B9780123985293000142.
Bobleter O. 1994. Hydrothermal degradation of polymers derived from plants. Jurnal Progress in Polymer Science. Vol 19(5): 797–841.
Bobleter O, Concin R. 1979. Degradation of poplar lignin by hydrothermal treatment. Jurnal Cellulose chemistry and technology. Vol 13(5): 583–593. Clark T A, K L Mackie, P H Dare. 1989. Steam explosion of the softwood Pinus
radiata with sulphur dioxide addition. Journal of Wood Chemistry and Technology. Volume 9: 135-166.
Devi SR, Pellisier, Prasad. 1997. Plant Ecophysiology: Allelochemical. Prasad MNV, editor. Canada (US): John Willey and Sons, inc. hlm 253-303
Einhellig, FA. 1986. In The Science of Allelopathy: Mechanisms and modes of action of allelochemicals. 171-188. Putnam AR, Tang CS, editor. John Wiley and Sons, Inc.
___________. 1995. Allelophaty: current status and future growth. Washington DC (US): American Chemical Society. Hlm: 216
Fang Z, Takafumi S, Richard L S Jr. 2008. Reaction chemistry and phase behavior of lignin in high-temperature and supercritical water. Jurnal Bioresource Technology. Vol 99: 3424-2430.
Fitter AH, Hay RKM. 1991. Fisiologi Lingkungan Tanaman. Andani S, penerjemah. Yogyakarta (ID): Gadjah Mada Press.
Freudenberg K, Neish AC. 1968. Constitution and Biosynthesis of Lignin. Springer GF, Kleinzeller A, editor. New York (US): Springer-Verlag. hlm 129.
Gardner FP, Pearce RB, Mitchel RL. 1991. Fisiologi Tanaman Budidaya, Herawati S, penerjemah. Jakarta (ID): Universitas Indonesia Press. hlm: 129, 134, 276, 346.
Gilman AG, Hardman JG, Limbird LE. 1991. The Pharmacological Basis of
Therapeutics. Vol.I, Singapore (SG): Pergamon Press.
Klingman GC, Ashton RM. 1982. Weed science : Principles and practices. New York (US): John Wiley & Sons.
Kristanto BA. 2006. Perubahan karakter tanaman jagung (Zea mays L.) akibat alelopati dan persaingan teki (Cyperus rotundus L.). J.Indon.Trop.Anim.