PENETAPAN KADAR BORAKS PADA MIE BASAH YANG BEREDAR DI PASAR CIPUTAT
DENGAN METODE SPEKTROFOTOMETRI UV-VIS MENGGUNAKAN PEREAKSI KURKUMIN
Skripsi
Diajukan sebagai salah satu syarat untuk memperoleh gelar Sarjana Farmasi
OLEH : RAISANI RUSLI NIM : 105102003340
PROGRAM STUDI FARMASI
FAKULTAS KEDOKTERAN DAN ILMU KESEHATAN UNIVERSITAS ISLAM NEGERI (UIN) SYARIF HIDAYATULLAH
LEMBAR PERSETUJUAN SKRIPSI
NAMA : RAISANI RUSLI NIM : 105102003340
JUDUL : PENETAPAN KADAR BORAKS PADA MIE BASAH YANG BEREDAR DI PASAR CIPUTAT DENGAN METODE SPEKTROFOTOMETRI UV-VIS MENGGUNAKAN PEREAKSI KURKUMIN
Menyetujui,
Pembimbing I Pembimbing II
Drs. M. Yanis Musdja, M.Sc, Apt Zilhadia M.Si, Apt NIP. 1956010619851010001 NIP. 150408672
Mengetahui,
Ketua Program Studi Farmasi FKIK UIN Syarif Hidayatullah Jakarta
Skripsi dengan judul
PENETAPAN KADAR BORAKS PADA MIE BASAH YANG BEREDAR DI PASAR CIPUTAT
DENGAN METODE SPEKTROFOTOMETRI UV-VIS MENGGUNAKAN PEREAKSI KURKUMIN
Telah disetujui, diperiksa dan dipertahankan di hadapan penguji oleh RAISANI RUSLI
NIM 105102003340
Pembimbing
Drs. M. Yanis Musdja, M.Sc, Apt Zilhadia M.Si, Apt NIP. 1956010619851010001 NIP. 150408672
Penguji
Supandi, M.Si,Apt Azri Fitria, M.Si, Apt Eka Putri, M.Si, Apt
Penguji I Penguji II Penguji III
Mengetahui,
Ketua Program Studi Farmasi UIN Syarif Hidayatullah Jakarta
Drs. M. Yanis Musdja, M.Sc, Apt
Dekan Fakultas Kedokteran dan Ilmu Kesehatan UIN Syarif Hidayatullah Jakarta
LEMBAR PERNYATAAN
DENGAN INI SAYA MENYATAKAN BAHWA SKRIPSI INI BENAR- BENAR KARYA SENDIRI YANG BELUM PERNAH DIAJUKAN SEBAGAI SKRIPSI ATAU KARYA ILMIAH PADA PERGURUAN TINGGI ATAU PADA LAMBAGA PENDIDIKAN MANAPUN.
Jakarta, Desember 2009
KATA PENGANTAR
Alhamdulillah, puji dan syukur kehadirat Allah SWT yang telah melimpahkan rahmat dan karunia-Nya serta shalawat dan salam selalu tercurah kepada junjungan kita Nabi Muhammad SAW karena dengan segala rahmat dan karunia-Nya penulis dapat menyelesaikan penelitian dan penulisan skripsi dengan judul “PENETAPAN KADAR BORAKS PADA MIE BASAH YANG BEREDAR DI PASAR CIPUTAT DENGAN METODE SPEKTROFOTOMETRI UV-VIS MENGGUNAKAN PEREAKSI KURKUMIN”. Skripsi ini disusun untuk memenuhi tugas akhir sebagai salah satu syarat untuk memperoleh gelar Sarjana Farmasi pada Fakultas Kedokteran dan Ilmu Kesehatan Program Studi Farmasi UIN Syarif Hidayatullah, Jakarta.
Pada kesempatan ini perkenankanlah penulis menyampaikan ucapan terima kasih yang sebesar-besarnya kepada:
1. Bapak Prof. DR. (hc) dr. M.K Tadjudin Sp.And, selaku Dekan Fakultas Kedokteran dan Ilmu Kesehatan UIN Syarif Hidayatullah Jakarta.
2. Bapak Drs. Muhammad Yanis Musdja, M.Sc, Apt, selaku Ketua Program studi Farmasi FKIK UIN Syarif Hidayatullah Jakarta sekaligus pembimbing 1 yang telah memberikan ilmu dan bimbingan selama penulisan skripsi ini . 3. Ibu Zilhadia M.Si, Apt, selaku pembimbing II yang telah memberikan waktu,
semangat, ilmu, dan bimbingan selama penulisan skripsi ini.
4. Kedua orang tua, Ayahanda H.Rusli Gucci dan Ibunda tercinta Hj.Mariah yang selalu memberikan kasih sayang, doa, dan dukungan baik moril maupun materil. Tiada apapun di dunia ini yang dapat membalas semua kebaikan, cinta dan kasih sayang yang telah engkau berikan.
5. Kakak-kakakku, Dra. Ratnawati Rusli, H. Deny Rusli dan Istri, Letkol Heri Rusli dan istri, Rasti Rusli, Temy Rusli dan Istri, Rini Rusli, Jimmy Rusli, Amd.Par dan istri atas doa, dukungan baik moril maupun materil.
7. Para staf dan karyawan program studi Farmasi. Staf Administrasi Farmasi yang telah banyak membantu selama penelitian dan penyelesaian skripsi. 8. Kakak Erlis dan Kakak Nurul selaku asisten laboratorium kimia farmasi UIN
Syarif Hidayatullah dan Kakak Prita dan Kakak Pipit selaku asisten laboratorium pangan PLT UIN Syarif Hidayatullah yang telah banyak membantu selama penelitian berlangsung.
9. Kepada teman-teman Farmasi angkatan 2005, terimakasih untuk kebersamaan, dukungan, saran dan kritiknya. Kebersamaan kita didalam suka dan duka akan selalu terkenang di dalam hati sanubari.
10. Kepada adik-adik Farmasi 2007 dan Tim Saman 02-03 yang telah membantu dan menemani melewati semua perjuangan ini dengan berbagi tangis dan tawa, serta semua kisah selama penelitian dan penulisan skripsi ini.
11. Teman-teman Farmasi UP Lena dan Farmasi UNAIR Ratna terimakasih untuk bantuan, dukungan, saran dan kritiknya selama penelitian dan penulisan skripsi ini.
12. Serta semua pihak yang tidak dapat disebutkan satu persatu yang turut membantu menyelesaikan skripsi ini.
Penulis menyadari bahwa penyusunan skripsi ini masih belum sempurna. Oleh karena itu kritik dan saran yang bersifat membangun sangat penulis harapkan guna tercapainya kesempurnaan skripsi ini.
Akhirnya, dengan segala kerendahan hati, penulis berharap semoga hasil penelitian ini dapat bermanfaat baik bagi kalangan akademis, khususnya bagi mahasiswa farmasi, masyarakat pada umumnya dan bagi dunia ilmu pengetahuan.
Jakarta, Desember 2009
DAFTAR ISI
1.2. Perumusan masalah ……….3
1.3. Hipotesa………...3
1.4. Tujuan Penelitian………..4
1.5. Manfaat Penelitian………... 4
BAB II TINJAUAN PUSTAKA TINJAUAN PUSTAKA 2.1. Bahan tambahan makanan………... 5
2.1.1. Peranan Bahan Tambahan Makanan………. 5
2.1.2. Jenis dan Golongan Bahan Tambahan Makanan…..7
2.2. Boraks ………... 8
2.2.1. Sifat Kimia Boraks………. 8
2.2.2. Sifat Farmakologi ………. 9
2.3. Spektrofotometer UV-Vis……….. 11
2.4. Metode Validasi ………. 19
2.5. Metode Analisa Boraks ……… 24
2.5.1. Kurkumin ………27
2.6. Teknik sampling ……… 29
BAB III KERANGKA KONSEP ... 33
BAB IV METODE PENELITIAN 4.1. Pengambilan Sampel ……….. 34
4.2. Tempat dan Waktu Penelitian ………. 34
4.3. Alat dan Bahan Penelitian ………...34
4.3.1. Alat ……….. 34
4.3.2. Bahan ……….. 35
4.4. Prosedur Penelitian ………. 35
4.4.4. Analisa sampel pasar……….. 38
A. Uji Kualitatif …..……… ……... 38
B. Uji kuantitatif ……….. 39
BAB V HASIL DAN PEMBAHASAN 5.1. Hasil Penelitian ………... 41
5.2. Pembahasan ………. 42
BAB VI KESIMPULAN DAN SARAN 6.1. Kesimpulan ……… 51
6.2. Saran ……….. 51
DAFTAR PUSTAKA... 53
DAFTAR TABEL
Halaman Tabel 1. Pengukuran serapan konsentrasi larutan boraks pada panjang
gelombang 545,95 nm………... ……… 66 Tabel 2. Hasil penentuan batas deteksi dan batas kuantitasi boraks
pada mie basah simulasi... 67 Tabel 3. Hasil uji perolehan kembali mie basah simulasi...……… 68 Tabel 4. Hasil uji presisi mie basah simulasi…….……….. 69 Tabel 5. Hasil identifikasi boraks pada empat sampel mie basah
DAFTAR GAMBAR
Halaman
Gambar 1. Spektrum Elektromagnit………. 12
Gambar 2. Skema instrument UV-Vis………... 13
Gambar 3. Skema spektrofotometri UV-Vis tipe single beam………. 15
Gambar 4. Skema spektrofotometri UV-Vis tipe double beam………. 15
Gambar 5. Rumus Bangun Kurkumin……… 27
Gambar 6. Kurva kalibrasi boraks pada mie basah……… 41
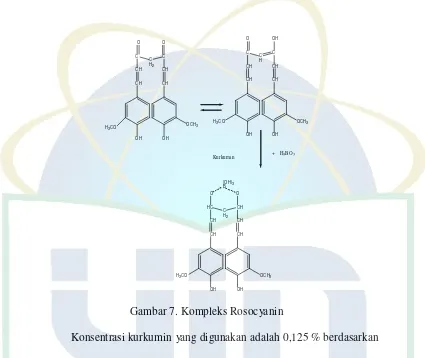
Gambar 7. Kompleks Rosocyanin…..……… 45
Gambar 8. Dinatrium tetraborat……… 56
Gambar 9. Skema pembuatan larutan uji dan pereaksi………. 57
Gambar 10. Skema pembuatan mie basah simulasi…..……….. 58
Gambar 11. Skema pembuatan larutan dari 11 mie basah simulasi yang mengandung boraks dengan kadar 6,25-50 µg/ml……….. 59
Gambar 12. Skema penetuan panjang gelombang maksimum pada larutan mie basah simulasi dengan kadar 25 µ g/ml.….….. 60
Gambar 13. Skema pembuatan kurva kalibrasi dan validasi metode…. 61 Gambar 14. Skema pengujian sampel mie basah pasar secara kualitatif.. 62
Gambar 15. Skema pengujian sampel mie basah pasar secara kuantitatif. 64 Gambar 16. Kurva absorbs boraks dengan pereaksi kurkumin……….. 65
Gambar 17. Spektrofotometri UV-Vis……… 71
Gambar 18. Penggiling adonan mie……… 71
Gambar 19 Pencetak mie……… 71
DAFTAR LAMPIRAN
Halaman
Lampiran 1 sampel boraks……….. 56
Lampiran 2. Skema kerja... 57
Lampiran 3. Penentuan panjang gelombang maksimum………... 65
Lampiran 4. Pembuatan kurva kalibrasi………... 66
Lampiran 5. Penentuan batas deteksi dan batas kuantitasi boraks pada mie basah simulasi ………..……….. 67
Lampiran 6. Uji perolehan kembali mie basah simulasi………. 68
Lampiran 7. Uji presisi simulasi mie basah……….……….... 69
Lampiran 8. Penetapan kadar boraks pada mie basah yang beredar di pasar Ciputat ... 70
Lampiran 9. Alat yang digunakan dalam penelitian……….. 71
Lampiran 10. Sampel mie basah dari pasar Ciputat... 72
ABSTRAK
Judul : Penetapan Kadar Boraks pada Mie Basah yang Beredar di Pasar Ciputat Dengan Metode Spektrofotometri UV-Vis Menggunakan Pereaksi Kurkumin
Analisa boraks dalam mie basah dilakukan dengan menggunakan pereaksi kurkuin sebagai pereaksi warna yang menghasilkan kompleks rosocyanin dan diamati dengan menggunakan spektrofotometri UV-Vis pada panjang gelombang maksimum 545,95 nm. Sebelum digunakan terhadap sampel yang diambil dari pasar Ciputat metode ini divalidasi. Hasil dari penelitian menunjukkan kurva kalibrasi linier pada rentang 6,25-50 µ g/ml dengan persamaan regresi y = 0,008 + 0,012x dan koevisien korelasi (r) = 0,9994. Metode ini memberikan batas deteksi sebesar 3,1132 µg/ml dan batas kuantitasi sebesar 10,3775 µg/ml. Persen perolehan kembali dari larutan mie basah simulasi yang diperoleh dalam penelitian ini sebesar 99,767±1,114 %. Hasil pemeriksaan sampel mie basah yang beredar di pasar Ciputat empat diantaranya diantaranya mengandung senyawa boraks 3,76112±0,0451, 108,592±0,02185, 117,9461±0,01455, dan 6,275±0,0221.
ABSTRACT
Title : Determination of Borax contain in wet noodles which distributed in Ciputat market by spectrofotometri UV-Vis method using curcumin reagent.
Determining of borax contain in wet noodles done by curcumin reagent as color regent which produced rosocyanin complexs and monitor by using spectrofotometri UV-Vis in maximum wave length in 545,95 nm. Before it was used in sample which taken from Ciputat market this method was validated. The result showed that calibration curve in linier 6,25-50 µg/ml with regression equal y = 0,008 + 0,012x and corelation coevision (r) = 0,9994. this method gave detection limit at 3,1132 µg/ml and qualification limit at 10,3775 µg/ml. The recovery of wet nodles simulation was 99,767±1,114 %. The result of examination wet noodles sample which was marketed in Ciputat market that four of five contain 3,76112±0,0451, 108,592±0,02185, 117,9461±0,01455, and 6,275±0,0221 borax.
BAB I
PENDAHULUAN
1.1 Latar Belakang
Boraks yang berasal dari bahasa arab yaitu Bouraq pada awal mula dikenal mempunyai aktivitas sebagai bahan antiseptik yang digunakan sebagai
bahan pembersih, pengawet kayu, dan herbisida. Namun saat ini boraks tidak digunakan sebagai pembersih, tetapi umum sebagai pengenyal atau pengawet
makanan. Dengan adanya boraks, adonan dapat lebih liat dan elastis, sehingga
tidak cepat molor atau sagging. Boraks banyak digunakan oleh industri kecil
atau industri rumah tangga, dalam pembuatan adonan mie, gendar, atau kerupuk gendar (kerupuk nasi). Mie merupakan salah satu produk makanan
yang sangat digemari oleh masyarakat, baik anak–anak maupun orang dewasa, terbuat dari tepung gandum, tepung beras, atau tepung tapioka. Pada proses
pembuatannya terutama pada mie basah yang memiliki kadar air 51 % sering
ditambahkan boraks untuk memperpanjang daya tahannya terhadap kerusakan dan kebasian. (Winarno et al,1994).
Meskipun jumlah yang ditambahkan tidak terlalu banyak, namun boraks
mempunyai efek akumulasi yang berbahaya. Dalam air, boraks merupakan campuran natrium metaborat dan asam borat. Sedangkan dalam suasana asam
boraks terurai menjadi asam borat. Dengan demikian, baik waktu pengolahan
makanan dengan air maupun karena dimakan dan melalui lambung yang bersifat asam, didalam tubuh akan ditemukan asam borat setelah
akut meliputi rasa mula, muntah-muntah, diare, kejang perut, bercak–bercak
pada kulit, temperatur tubuh menurun, ruam eritema kulit yang menyerupai
campak dan kerusakan pada ginjal, gelisah, dan lemah juga dapat terjadi, kematian terjadi akibat kolaps pernapasan. Sedangkan pada keracunan kronik
dapat menyebabkan demam, anoreksia, anuria, kerusakan ginjal, depresi dan bingung (Haddad et al,1990; Dreisbach,1974; Gosselin et al).
Kasus keracunan boraks yang bukan dari makanan, dilaporkan pertama
kali pada tahun 1907. Menurut laporan tersebut, banyak anak usia dini
menderita sariawan pada mulut, kemudian dioleskan campuran madu dan boraks. Ternyata kelainan pasca pengolesan pada kulit, terjadi eritema, dan
wajah tampak keriput. Di Indonesia tepatnya di Palembang Sumatera Selatan terjadi kasus keracunan boraks yang berasal dari makanan pada pertengahan
tahun 1994. Dilaporkan 5 orang meninggal dunia dan 56 orang terpaksa di
rawat di rumah sakit (Goodman,1975; Akmal,1995). Pada tahun 2009 Dinas Kesehatan kota Depok mengumumkan hasil pengujian di kantin Sekolah
Dasar yang rata-rata menjajakan jajanan khas sekolah, terbukti 30 persen
mengandung boraks dan 16 persen mengandung formalin.
Larangan penggunaan boraks juga diperkuat dengan adanya Permenkes RI No. 1168/MENKES/PER/X/1999 menyatakan bahwa salah satu BTM yang dilarang digunakan dalam makanan adalah boraks (Depkes,1999).
Karena hal-hal tersebut maka pada penelitian ini akan dilakukan
Hidayatullah dan merupakan pasar tradisional besar sehingga penelitian ini
dilakukan sebagai dharma UIN terhadap masyarakat sekitar.
Penetapan kadar boraks dilakukan dengan metode spektrofotometri sinar tampak, dimana pada metode ini ada dua pereaksi pembentuk kompleks warna
yaitu Quinalizarin dan Kurkumin. Pada penelitian–penelitian sebelumnya,
peraksi yang banyak digunakan adalah kurkumin dimana kompleks warna yang terjadi adalah rosocyanin yang berwarna rosa. (Dibble,1965)
Berdasarkan hal tersebut, maka identifikasi dan penetapan kadar boraks
dapat dilakukan dengan menggunakan metode spektrofotometri UV-Vis dengan menggunakan pereaksi kurkumin dan perlu dilakukan penelitian
terhadap beberapa mie basah yang dijual dipasar Ciputat, Karena
kemungkinan mie tersebut juga menggunakan boraks pada pembuatannya.
1.2 Perumusan Masalah
Pada penelitian ini yang menjadi perumusan masalah adalah sebagai berikut :. 1. Apakah validasi metode penetapan kadar boraks menggunakan
spektrofotometer UV-Vis dapat memenuhi persyaratan.
2. Apakah mie basah yang beredar di pasar Ciputat mengandung boraks
sebagai bahan tambahan makanan.
1.3 Hipotesis
1. Validasi metode pada boraks dengan menggunakan Spektrofotometer UV-
2. Mie Basah yang dijual di pasar Ciputat mengandung bahan tambahan
makanan boraks sebagai pengenyal
1.4 Tujuan Penelitian
Tujuan dari penelitian ini adalah mengetahui adanya boraks pada mie basah
dan mengetahui kadar boraks pada mie basah yang dijual di pasar Ciputat.
1.5 Manfaat Penelitian
1. Penelitian ini diharapkan memberikan informasi kepada masyarakat
tentang bahaya penggunaan boraks pada makanan.
2. Hasil penelitian diharapkan meningkatkan kewaspadaan mayarakat pada produk yang mengandung boraks di pasar Ciputat
BAB II
TINJAUAN PUSTAKA
2.1 Bahan Tambahan Makanan
Pengertian atau definisi bahan tambahan makanan (BTM) cukup
bervariasi. Secara umum yang dimaksud dengan bahan tambahan makanan adalah bahan-bahan yang ditambahkan ke dalam makanan selama
produksi, pengolahan, pengemasan atau penyimpanan untuk tujuan
tertentu.
2.1.1 Peranan Bahan Tambahan Makanan
Peranan BTM pada dasarnya sebagai senyawa yang ditambahkan
dalam bahan pangan untuk memperbaiki penampilan, cita rasa, tekstur, atau sifat-sifat penyimpanannya serta untuk mempengaruhi kualitas yang
dikehendaki. BTM digunakandi industri-industri makanan untuk
meningkatkan mutu pangan olahan penggunaan. Bahan tambahan makanan tersebut hanya dibenarkan jika ditujukan untuk keperluan
berikut:
1. Mempertahankan nilai gizi makanan.
Sebagai contoh, penambahan bahan antioksidan seperti BHA (butyl
hidroksianisol) dalam pengolahan vitamin A akan mempertahankan potensi vitamin tersebut bila ditambahkan pada makanan.
2. Sebagai konsumsi segolongan orang tertentu yang memerlukan
5. Membuat makanan menjadi lebih tambahan makanan, seperti pewarna
Misalnya penambahan bahan pemanis buatan seperti sakarin ke dalam
makanan atau minuman, sehingga tidak menambah kalori kedalam makanan tersebut.
3. Mempertahankan mutu atau kestabilan makanan atau untuk
memperbaiki sifat-sifat organoleptiknya hingga tidak menyimpang dari sifat alamiahnya, dan dapat membantu mengurangi makanan yang
dibuang. Bahan pengawet memegang peranan penting dalam memperpanjang daya simpan berbagai jenis makanan, sehingga
memungkinkan bagi makanan-makanan tersebut ditransportasikan
dalam jarak yang jauh, disimpan untuk waktu yang lama, tetapi masih
dapat dikonsumsi secara aman.
4. Sebagai keperluan pembuatan, pengolahan, penyediaan, perlakuan,
pewadahan, pembungkusan, pemindahan, atau pengangkutan.
Beberapa makanan dalam proses pengolahannya membutuhkan penggunaan bahan-bahan, seperti bahan penstabil, bahan penjernih, dan
bahan pengikat logam. Penggunaan bahan-bahan tersebut
memungkinkan bagi industri dalam skala besar memproduksi makanan dengan komposisi dan mutu yang konstan sepanjang tahun.
menarik Penggunaan bahan dan bahan pemantap tekstur memperbaiki bahan baku yang bervariasi sehingga nantinya produk akhir mempunyai penampakan, rasa, serta penampilan yang selalu sama
2.1.2 Jenis dan Penggolongan Bahan Tambahan Makanan (BMT)
Pada umunya Bahan Tambahan Makanan (BTM) dapat dibagi
menjadi dua golongan besar, yaitu :
1. BTM yang ditambahkan dengan sengaja ke dalam makanan.
BTM ini dibagi lagi berdasarkan fungsinya dalam pengolahan makanan, antara lain sebagai anti oksidan; pemanis buatan; pemutih tepung;
pengemulsi dan pengental; pengeras; pewarna serta penyedap rasa dan
aroma.
2. BTM yang tidak sengaja tidak ditambahkan pada makanan.
BTM ini tidak mempunyai fungsi dalam makanan, terdapat secara fisik sengaja baik dalam jumlah sedikit atau cukup banyak akibat perlakuan
selama proses produksi, pengolahan dan pengemasan. Bahan ini dapat
pula merupakan residu atau kontaminan dari bahan yang sengaja yang ditambahkan untuk tujuan produksi bahan mentah atau penanganannya
yang masih terus terbawa ke dalam makanan yang akan dikonsumsi.
Contoh BTM dalam golongan ini adalah residu pestisida (termasuk insektisida, herbisida, dan fungisida), kontaminan radio aktif, logam
berat, residu obat ternak (termasuk hormone dan antibiotic), serta migrasi komponen–komponen plastik dari pembungkus ke dalam
makanan.
Menurut sumbernya, BTM dapat dibedakan menjadi dua, yaitu : a) Alamiah, seperti lesitin dan asam sitrat.
sifat metabolismenya, seperti asam askorbat.Pada umunya bahan
sintetik mempunyai kelebihan yaitu lebih pekat, lebih stabil dan lebih murah. Walaupun demikian terdapat kelemahan yaitu sering
terjadi ketidaksempurnaan proses sehingga mengandung zat–zat
yang berbahaya bagi kesehatan, kadang bersifat karsinogenik (Winarno,1988).
2.2 Boraks
2.2.1 Sifat Kimia Boraks
Rumus Molekul : Na2B4O7. 10H2O
Nama Kimia : Natrium Tetraborat Berat Molekul : 381,37
Berat Jenis : 1,68 – 1,72 Titik Leleh : 750 C
Boraks merupakan senyawa kimia yang mengandung unsur boron (B). Boraks merupakan kristal lunak tidak berwarna, terjadi dalam suatu deposit hasil proses penguapan hot spring (pancuran air panas) atau danau garam. Boraks termasuk kelompok mineral borat, suatu jenis senyawa
kima alami yang terbentuk dari boron (B) dan oksigen (O2). Beberapa
jenis boraks jarang ditemui, dan terjadi pada daerah tertentu saja, sebaliknya beberapa diantaranya, misalnya boraks, kernite
(Na2B4O74H2O) dan colemanite (Ca2B6O11.5H2O) secara komersil
Boraks berupa hablur transparan tidak berwarna atau serbuk hablur
putih dan tidak berbau. Larutannya bersifat basa terhadap fenoftalen. Pada udara kering merapuh. Hablur sering dilapisi serbuk warna putih. Larut
dalam 20 bagian air, 0,6 bagian air mendidih dan 1 bagian gliserol, praktis
tidak larut dalam etanol (Reynold,1982; Farmakope IV,1995; Farmakope III,1979).
2.2.2 Sifat Farmakologi A. Absorbsi
Boraks diabsorpsi secara cepat oleh saluran cerna, kulit yang terbakar dan pada kulit yang terluka. Namun boraks tidak diabsorpsi
secara baik pada kulit yang utuh. Boraks didistribusikan ke seluruh tubuh
dan memiliki afinitas yang besar terhadap hati, otak dan ginjal, sehingga dapat terakumulasi pada organ tersebut. (Goodman,1975; Winarno,1994;
Haddad et al,1990)
Pada keadaan normal, konsentrasi boraks didalam serum sebesar 7
mg/l, tetapi pada keracunan berat konsentrasinya 20–150 mg/l. Sedangkan
pada kasus kematian dapat terjadi pada konsentrasi 200–15000 mg/l
(Flanaga et al,1995). B. Ekskresi
Boraks diekskresikan sebagian besar melalui ginjal. Lebih dari 50% dosis oral diekskresikan tanpa perubahan melalui ginjal selama 24
jam dan 90% setelah 96 jam. Sebagian kecil dikeluarkan melalui kelenjar keringat. Waktu paruh boraks dilaporkan bervariasi, antara 5–21 jam
C. Toksisitas.
Keracunan boraks terjadi karena absorpsi yang berlangsung dengan
segera dari saluran pencernaan makanan, kulit yang terluka, lecet, atau terbakar yang mendapat pengobatan secara berulang–ulang dengan serbuk
atau larutan asam borat. Selain itu, ekskresi boraks yang lambat juga memperbesar terjadinya akumulasi akibat penggunaan berulang. Pada bayi
dan anak-anak keracunan lebih mudah terjadi dibanding orang dewasa,
dan kematian dapat terjadi setelah penggunaan topikal dari serbuk boraks untuk mengobati ruam. Keracunan dapat bersifat akut maupun kronis
dengan manifestasinya yang utama adalah kulit mengelupas, demam, dan
anuria.
Gejala keracunan boraks akut meliputi rasa mula, muntah-muntah,
diare, kejang perut, bercak–bercak pada kulit, temperatur tubuh menurun,
ruam eritema kulit yang menyerupai campak dan kerusakan pada ginjal, gelisah, dan lemah juga dapat terjadi, kematian terjadi akibat kolaps
pernapasan. Sedangkan pada keracunan kronik dapat menyebabkan
demam, anoreksia, anuria, kerusakan ginjal, depresi dan bingung (Haddad
et al,1990; Dreisbach,1974; Gosselin et al).
Untuk boraks nilai LD50 (Letal Death 50 ) pada tikus melalui
penggunaan oral adalah 3,0 g/kg berat badan. Uji yang dilakukan terhadap 10 orang dewasa menunjukkan bahwa dengan penyuntikan 20 g boraks
tidak menimbulkan kematian, tetapi, mengakibatkan mual, muntah–
muntah, diare, atau gangguan mental selama beberapa hari. Anak kecil
yang baru lahir yang diberi asam borat pada makanannya, karena 5 anak
yang mendapatkan 4,5–14 g meninggal dalam waktu 2-3 hari, sedangkan 6 bayi lainnya mendapat 2–4,5 g dapat bertahan (Winarno,Titi,1994).
2.3 Spektrofotometer UV –Vis
Pada awalnya, spektroskopi adalah ilmu yang mempelajari tentang radiasi sinar tampak yang berinteraksi dengan molekul pada panjang
gelombang tertentu dan menghasilkan suatu spektra, yang merupakan hasil
interaksi antara energi radian dengan panjang gelombang atau frekuensi. Kemudian pengertian ini dikembangkan tidak hanya untuk radiasi sinar
tampak, tapi juga jenis radiasi elektromagnetik yang lain seperti sinar X,
ultraviolet, inframerah, gelombang mikro, dan radiasi frekuensi radio. Ilmu yang berhubungan dengan pengukuran spektra tersebut dinamakan
spektrofotometer (Skoog,West,Holler,1996). Spektrofotometri UV-Vis
adalah alat yang digunakan untuk mengukur serapan yang dihasilkan dari interaksi kimia antara radiasi elektromagnetik dengan molekul atau atom
dari suatu zat kimia pada daerah UV-Vis (FI edisi IV, 1995).
Jangkauan panjang gelombang yang tersedia untuk pengukuran membentang dari panjang gelombang pendek ultraviolet sampai ke garis
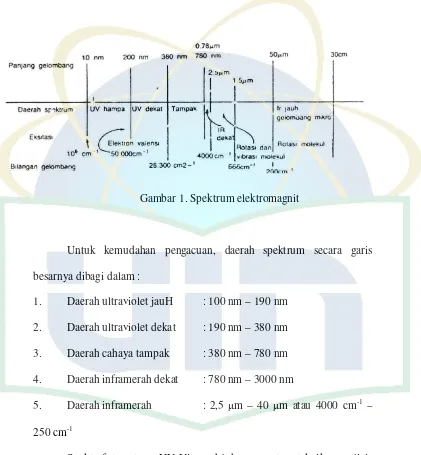
Gambar 1. Spektrum elektromagnit
Untuk kemudahan pengacuan, daerah spektrum secara garis besarnya dibagi dalam :
1. Daerah ultraviolet jauH : 100 nm – 190 nm 2. Daerah ultraviolet dekat : 190 nm – 380 nm 3. Daerah cahaya tampak : 380 nm – 780 nm
4. Daerah inframerah dekat : 780 nm – 3000 nm
5. Daerah inframerah : 2,5 m – 40 m atau 4000 cm-1 –
250 cm-1
Spektrofotometer UV-Vis adalah anggota teknik analisis
spektroskopik yang memakai sumber radiasi elektromagnetik ultraviolet (190-380 nm) dan sinar tampak (380-780 nm) dengan memakai instrument
spektrofotometer.
Spektrofotometer UV–Vis merupakan metoda analisa yang
penggunaannya cukup luas, baik untuk analisa kualitatif maupun kuantitatif. Untuk analisa kuantitatif yang diperhatikan adalah :
b) Membandingkan serapan (A), daya serap (a), . c) Membandingkan spektrum serapannya
Prinsip dari spektrofotometri UV-Vis adalah mengukur jumlah cahaya yang diabsorbsi atau ditransmisikan oleh molekul-molekul di
dalam larutan. Ketika panjang gelombang cahaya ditransmisikan melalui
larutan, sebagian energi cahaya tersebut akan diserap (diabsorpsi). Besarnya kemampuan molekul-molekul zat terlarut untuk mengabsorbsi
cahaya pada panjang gelombang tertentu dikenal dengan istilah absorbansi
(A), yang setara dengan nilai konsentrasi larutan tersebut dan panjang
berkas cahaya yang dilalui (biasanya 1 cm dalam spektrofotometri) ke
suatu point dimana persentase jumlah cahaya yang ditransmisikan atau
diabsorbsi diukur dengan phototube.
Gambar 2. Skema instrument UV-Vis Spektrofotometri sederhana terdiri dari : 1. Sumber radiasi
2. Monokromator
Monokromator merupakan alat yang berfungsi sebagai penyeleksi
cahaya dengan panjang gelombang tertentu. Monokromator akan memisahkan radiasi cahaya putih yang polikromatis menjadi
cahaya monokromatis (mendekati monokromatis). 3. Kuvet
Pada umumnya spektrofotometri melibatkan larutan, dengan
demikian diperlukan wadah/ sell untuk menempatkan larutan.
4. Detektor
Fungsinya mengubah energi radiasi yang jatuh mengenainya
menjadi suatu besaran yang dapat diukur. 5. Amplifier
Fungsinya untuk memperkuat sinyal listrik. 6. Recorder
Alat untuk mencatat, dapat berupa gambar/angka-angka. Tipe instrumentasi dari spektrofotometri UV-Vis (Harmita, 2006) :
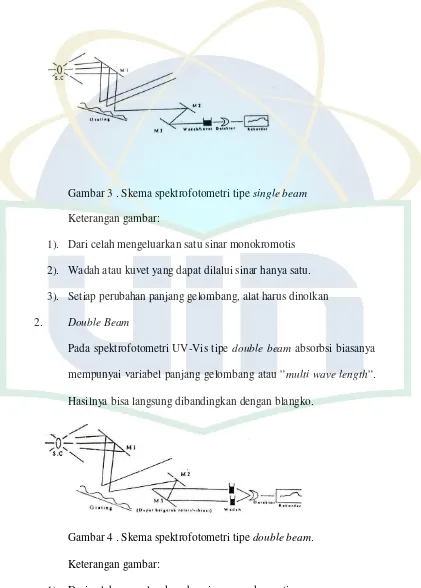
1. Single Beam
Pada spektrofotometri UV-Vis tipe single beam absorbsi
berdasarkan pada sinar tunggal dimana sampel akan ditentukan jumlahnya pada satu panjang gelombang atau fix wave lenght.
Gambar 3 . Skema spektrofotometri tipe single beam
Keterangan gambar:
1). Dari celah mengeluarkan satu sinar monokromotis 2). Wadah atau kuvet yang dapat dilalui sinar hanya satu. 3). Setiap perubahan panjang gelombang, alat harus dinolkan
2. Double Beam
Pada spektrofotometri UV-Vis tipe double beam absorbsi biasanya
mempunyai variabel panjang gelombang atau ”multi wave length”.
Hasilnya bisa langsung dibandingkan dengan blangko.
Gambar 4 . Skema spektrofotometri tipe double beam.
Keterangan gambar:
1). Dari celah mengeluarkan dua sinar monokromotis. 2). Sinar melaui 2 wadah atau kuvet yang sekaligus.
3). Alat hanya di auto zero satu kali dengan cara mengisi kedua kuvet
Persyaratan suatu sampel dapat dianalisa menggunakan Spektrofotometri UV Vis adalah :
1. Bahan mempunyai gugus kromofor
2. Bahan tidak mempunyai gugus kromofor tapi berwarna
3. Bahan tidak mempunyai gugus kromofor dan tidak berwarna, maka ditambahkan pereaksi warna (Vis)
4. Bahan tidak mempunyai gugus kromofor dibuat turunannya yang mempunyai gugus kromofor (UV).
Dasar dari metoda ini karena adanya perubahan sifat fisikokimia dari bahan yang diperiksa dengan jalan mengamati sifat serapannya terhadap energi cahaya atau radiasi elektromagnetik. Spectrum UV-Vis
merupakan hasil interaksi antara radiasi elektromagnetik (REM) dengan
molekul. REM merupakan bentuk energi radiasi yang mempunyai sifat gelombang dan partikel (foton). Karena bersifat sebagai gelombang maka
beberapa parameter perlu diketahui, misalnya panjang gelombang ( ),
frekuensi (v), bilangan gelombang (v), dan serapan (A).
REM mempunyai vektor listrik dan vektor magnet yang bergetar
dalam bidang-bidang yang tegak lurus satu sama lain dan masing-masing
tegak lurus pada arah perambatan radiasi.
Bila suatu cahaya monokromatis atau bukan monokromatis jatuh
pada medium homogen, maka sebagian dari cahaya ini akan dipantulkan,
sebagian akan diabsorbsi dan sisanya akan diteruskan, sehingga dalam hal ini dapat dinyatakan sebagai berikut:
Dimana :
I0 = intensitas cahaya yang datang
Ir = intensitas cahaya yang dipantulkan
Ia = intensitas cahaya yang diserap
It = intensitas cahaya yang diteruskan
Pengaruh Ir dapat dihilangkan dengan menggunakan
blanko/kontrol, sehingga :
I0 = Ia + It
Dua hukum empiris telah merumuskan tentang intensitas serapan.
Hokum Lambert telah menyatakan bahwa fraksi penyerapan sinar tidak bergantung dari intensitas sumber cahaya. Hukum Beer mengatakan
bahwa penyerapan sebanding dengan jumlah molekul yang menyerap (Sudjadi, 1983)
Gabungan dari hukum Lambert-Beer menurunkan secara empiris hubungan antara intensitas cahaya yang ditransmisikan dengan tebalnya
larutan, dan hubungan antara intensitas tadi dengan konsentrasi zat (Depkes,1995).
Rumus :
A = log (Io/It) = . b . c = a.b.c Dimana : A = Serapan
Io = Intensitas sinar yang datang It = Intensitas sinar yang diteruskan
b = Tebal larutan / kuvet (cm) c = Konsentrasi zat (g/L, mg/mL)
Sampel yang sering dianalisis dengan metode spektrofotometer
UV-Vis adalah senyawa organik. Senyawa organik yang dapat memberikan serapan adalah senyawa yang memiliki gugus kromofor dan
auksokrom. Gugus kromofor adalah gugus fungsional tidak jenuh yang memberikan serapan pada daerah ultraviolet atau cahaya tampak. Hampir
semua kromofor mempunyai ikatan rangkap seperti alkena (C=C), C=O, -
NO2, benzene, dan lain-lain.
Sedangkan auksokrom adalah gugus fungsional seperti –OH, -NH2,
-X, yaitu gugus yang mempunyai elektron nonbonding dan tidak
mengabsorbsi radiasi pada diatas 200 nm, akan tetapi mengabsorbsi radiasi UV jauh (Harmita, 2006).
Ruang lingkup spektroskopi serapan dapat diperluas dengan
menggunakan reaksi warna, yang seringkali diiringi dengan peningkatan sensitivitas atau selektivitas. Reaksi warna digunakan untuk memodifikasi
spektrum dari molekul pengabsorbsi sehingga dapat dideteksi pada daerah
visible, dan terpisah dari senyawa pengganggu lain yang memiki serapan di daerah UV. Selain itu, modifikasi kimia ini dapat digunakan untuk
mengubah molekul yang tidak mengabsorbsi menjadi senyawa turunan
yang stabil yang memiliki serapan yang bermakna.
menghitung jumlah senyawa dalam sampel. Jika konsentrasi senyawa
semakin tinggi maka lebih banyak cahaya yang diabsorbsi oleh sampel.
2.4 Metode Validasi
Validasi metode analisis adalah suatu tindakan penilaian terhadap
parameter tertentu, berdasarkan percobaan laboratorium, untuk membuktikan bahwa parameter tersebut memenuhi persyaratan untuk
penggunaanya.
Parameter tersebut adalah : 1. Kecermatan (Accuracy)
Kecermatan adalah kedekatan hasil penetapan yang diperoleh
dengan hasil sebenarnya. Kecermatan dinyatakan sebagai hasil
perolehan kembali dari analit yang ditambahkan.
Cara penentuan akurasi dapat dilakukan dengan cara absolute dan cara audisi. Syarat akurasi yang baik : 98 – 102 %, untuk sampel hayati (biologis atau nabati) : ±10 %. Beberapa pendapat mangatakan antara 95-105 %, dan beberapa berpendapat antara 80-120 %. Hal ini
dikarenakan semakin kompleks penyiapan sampel dan semakin sulit
metode analisis yang digunakan, maka recovery yang diperbolehkan semakin rendah atau kisarannya semakin lebar. Perhitungannya sebagai
berikut :
Dianjurkan untuk melakukan penentuan akurasi dengan 5 konsentrasi berbeda. ( (Harmita, 2006 ; Snyder, dkk, 1988 ; Gandjar,
2009)
2. Keseksamaan (precision)
Keseksamaan adalah ukuran yang menunjukkan derajat kesesuaian
antara hasil uji individual, diukur melalui penyebaran hasil individual dari rata – rata jika prosedur diterapkan secara berulang pada sampel –
sampel yang diambil dari campuran yang homogen. Keseksamaan diukur sebagai simpangan baku atau simpangan baku relatif (koefisien
variasi). Keseksamaan dapat dinyatakan sebagai keterulangan
(repeatability) atau ketertiruan (reproducibility). Kriteria seksama
diberikan jika metode memberikan simpangan baku relatif atau
koefisien variasi 2% atau kurang.
Keseksamaan dapat dihitung dengan cara sebagai berikut :
a. Hasil analisis adalah x1, x2, x3, x4,……….xn
maka simpangan bakunya adalah : SD = ( (x – x )2 )
n – 1
b. Simpangan baku relatif atau koefisien variasi (KV) adalah : KV = SD x 100 % (Harmita, 2006)
x
3. Selektivitas (specificity)
Selektivitas atau spesifisitas suatu metode adalah kemampuannya yang
hanya mengukur zat tertentu saja secara cermat dan seksama dengan
Selektivitas seringkali dapat dinyatakan sebagai derajat penyimpangan
(degree of bias) metode yang dilakukan terhadap sampel yang
mengandung bahan yang ditambahkan berupa cemaran, hasil urai, senyawa sejenis, senyawa asing lainnya, dan dibandingkan terhadap
hasil analisis sampel yang tidak mengandung bahan lain yang ditambahkan. Pada metode analisa yang melibatkan kromatografi,
selektivitas ditentukan melalui perhitungan daya resolusinya (Rs).
Pemisahan kromatogram yang baik diperoleh bila nilai resolusinya
lebih besar dari 1,5 (Harmita, 2006).
4. Linearitas dan Rentang
Linearitas adalah kemampuan metode analisis yang memberikan respon
yang secara langsung atau dengan bantuan transformasi matematik yang baik, proporsional terhadap konsentrasi analit dalam sampel.
Rentang metode adalah pernyataan batas terendah dan tertinggi analit
yang sudah ditunjukkan dapat ditetapkan dengan kecermatan, keseksamaan, dan linearitas yang dapat diterima. Penentuan linearitas
dalam praktek, digunakan satu seri larutan yang berbeda konsentrasinya
antara 50 – 150% kadar analit dalam sampel. Di dalam pustaka, sering ditemukan rentang konsentrasi yang digunakan antara 0 – 200%.
Jumlah sampel yang dianalisis sekurang-kurangnya delapan buah sampel blanko. Sebagai parameter adanya hubungan linier digunakan
koefisien korelasi r pada analisis regresi linier Y = a + bx. Untuk
memperoleh nilai a dan b digunakan metode kuadrat terkecil (least
a =
Linieritas ditentukan berdasarkan nilai koefisien (r) r = N( xy) - ( x) ( y)
[ (N ( x2) – ( x) 2) (N ( y2) ( y)2) ]1/2
Hubungan linear yang ideal dicapai jika nilai b = 0 dan r = +1 atau -1 bergantung pada arah garis. Sedangkan nilai a menunjukkan kepekaan
analisis terutama instrument yang digunakan. Parameter lain yang harus dihitung adalah simpangan baku residual (Sy).
Sy = (y1 – 1)
a) Koefisien korelasi (r) r 0,9990
b) Jumlah kuadrat sisa masing-masing titik temu (ri) mendekati nol (0)
(ri)2 sekecil mungkin 0
ri = yi – (b x i + a)
c) Koefisien fungsi regresi
5,0% (sediaan biologi)
d) Kepekaan analisis ( y/ x)
y/ x = y2 – y1 y3 – y2 y4 – y5 yn – yn-1
X2 – x1 X3 – x2 x4 – x5 xn – xn-1 (Harmita, 2006)
5. Batas Deteksi dan Batas Kuantitasi
Batas deteksi didefinisikan sebagai konsentrasi analit terendah dalam
sampel yang masih dapat dideteksi, meskipun tidak selalu dapat dikuantitasi. Batas deteksi merupakan batas uji yang secara spesifik
menyatakan apakah analit di atas atau di bawah nilai tertentu. Batas kuantitasi merupakan parameter pada analisis renik dan diartikan
sebagai kuantitas terkecil analit dalam sampel yang masih dapat
memenuhi kriteria cermat dan seksama. Pada analisis instrument batas
deteksi dapat dihitung dengan mengukur respon blangko beberapa kali lalu dihitung simpangan baku respon blangko dan formula di bawah ini
dapat digunakan untuk perhitungan
Q =
1
Keterangan :
Q = LOD (batas deteksi) atau LOQ (batas kuantitasi) k = 3 untuk batas deteksi atau 10 untuk batas kuantitasi
Sb = simpangan baku respon analitik dari blangko
S1 = arah garis linear (kepekaan arah) dari kurva antara respon terhadap
Batas deteksi dan kuantitasi dapat dihitung secara statistik melalui garis
regresi linier dari kurva kalibrasi. Nilai pengukuran akan sama dengan nilai b pada persamaan garis linier y = a+bx, sedangkan simpangan
baku blangko sama dengan simpangan baku residual(Sy/x)
a. Batas deteksi (Q) karena k = 3 atau 10
Simpangan baku (Sb) = Sy/x, maka
Q = 3 /
1
b. Batas kuantitasi (Q)
Q = 1 0 /
1 (Harmita, 2006; Gandjar, 2009;Snyder, dkk, 1988)
2.5 Metoda Analisa Boraks
1. Kualitatif
Metoda analisa boraks/asam borat secara kualitatif dapat dilakukan
dengan beberapa cara, antara lain sebagai berikut :
a. Penambahan asam sulfat pekat dengan bantuan panas. Ketika
dipanaskan, asap putih asam borat dilepaskan. Reaksi yang terjadi :
Na2B4O7 + H2SO4 + 5 H2O 4 H3BO3 + 2 Na+ + SO4
2-(Setiono, et al 1985)
nyala hijau, disebabkan oleh pembentukan etil borat atau
metal borat. (Setiono, et al 1985; Basir, 1992)
c. Uji kertas kunyit (Turmeri). Menggunakan sehelai kertas
kunyit yang dicelup ke dalam larutan suatu borat yang diasamkan dengan asam klorida encer kemudian dikeringkan.
Apabila suatu sample mengandung boraks dan diidentfikasi menggunakan kertas kurkumin dilihat melalui perubahan
warna kertas dari kuning menjadi hijau biru gelap setelah
ditambah amonia encer. (Wiliam,2002)
d. Menggunakan natrium karbonat dan penambahan asam
klorida dengan bantuan pemanasan akan mengidentifikasi
adanya boraks melalui perubahan residu dari berwarna merah ceri berubah menjadi hijau kehitaman.
e. Metoda Titrasi (Wisnu 2008; Slamet,2007).
1) Titrasi langsung basa kuat
Di dalam larutan air boraks merupakan campuran natrium
metaborat dan asam borat. Asam borat adalah asam sangat
lemah sehingga tidak dapat dititrasi langsung. Dengan adanya
senyawa poli-ol seperti gliserol dan manitol asam borat dapat membentuk kompleks yang mempunyai keasaman yang lebih
tinggi. Oleh karena itu, boraks dapat dititrasi dengan adanya gliserol atau manitol menggunakan fenolftalen sebagai
Na2B4O7 + 10H2 2NaBO2 + 2 H3BO3 + 7 H2O
2H3BO3 + 2 NaOH 2NaBO2 + 4H2O
2) Titrasi dengan asam.
Penetapan kadar dilakukan dengan menggunkana HCL untuk membentuk asam borat dan mengunakan merah metal
sebagai indicator. Reaksi yang terbentuk :
Na2B4O7 + 10H2 + 2HCL 4 H3BO3 + 2 NaCl + H2O
2. Kuantitatif
Penentuan kadar boraks dapat dilakukan dengan metode asam- basa. Spektrofotometri dan AAS (Atomic Absorption
Spectrophotometric ). Pada metode asam-basa dapat dikerjakan
dengan cepat namun terbatas untuk sampel dengan kadar yang relatif cukup besar, pada metode AAS dapat digunakan untuk
menetapkan sample dengan kadar yang sangat kecil namun jarang
laboratorium yang memiliki alat tersebut. Sedangkan pada metode spektrofotometri UV-Vis dapat digunakan untuk penetapan sample
dengan kadar yang sangat kecil dan beberapa laboratorium banyak yang memiliki alat tersebut.
Pada penetapan kadar boraks (secara spektrofotometri)
dilakukan dengan metoda spektrofotometri sinar tampak, dimana pada metoda ini ada dua pereaksi pembentuk kompleks warna yaitu
digunakan karena bentuk kompleks warna yang terjadi harus
dilarutkan terlebih dahulu dalam asam sulfat yang pekat yang memberikan kesulitan pada saat pengamatannya. Yang sering
digunakan pada penelitian-penelitian sebelumnya adalah kurkumin
dimana kompleks warna yang terjadi yaitu rosocyanin yang berwarna rosa. Rosocyanin ini pada penetapan secara
spektrofotometri sinar tampak dilakukan dengan melarutkannya
dalam alkohol 96% dan diamati pada panjang gelombang 548 nm (Dibble,1965).
2.5.1 Kurkumin
Nama Kimia : 1,7 – Bis – ( 4 – hydroxyl – 3 – methoxyphenyl ) – 1,6 – diene – 3,5 dione
Rumus molekul : C21H20O6
Berat molekul : 368,39
Titik leleh : 1790 C – 1820 C
Rumus bangun :
Gambar 5. Rumus bangun Kurkumin
Kurkumin merupakan senyawa alam yang terdapat di dalam
Curcuma domestica Val, sedangkan nama daerahnya adalah kunir,
kunyit, atau temu kuning (Anonim,1992).
Dalam keadaan murni dapat berupa Kristal berbentuk batang
atau prisma, berwarna kuning jingga. Larut dalam etanol dan asam
asetat glacial, tidak larut dalam air dan dietil eter. Dalam alkali
berwarna merah kecoklatan, dan dalam asam berwarna kuning (Windholz et al,1983).
Kurkumin merupakan zat warna alam, digunakan untuk
pewarna makanan dan kosmetik, juga sebagai penunjuk boraks. Dimana kurkumin akan bereaksi dengan asam borat atau boraks
membentuk kompleks kelat rosasianin yang berwarna merah (Roth,1978).
Kurkumin atau diferuloyl methane pertama kali diisolasi pada
tahun 1815. Kemudian tahun 1910, kurkumin didapatkan
berbentuk Kristal dan bisa dilarutkan dengan pelarut alkohol. Banyak hasil penelitian menunjukkan bahwa kurkumin aman dan
tidak toksik bila dikonsumsi oleh manusia. Jumlah kurkumin yang
aman dikonsumsi manusia adalah 100 mg/hari.
Kunyit merupakan salah satu tanaman obat potensial penghasil
kurkumin. Selain sebagai bahan baku obat dapat juga dipakai sebagai bumbu dapur dan zat pewarna alami. Rimpangnya sangat
bermanfaat sebagai anti koagulan, menurunkan tekanan darah, obat
diare dan reumatik. Kandungan kurkumin didalam kunyit berkisar 3–4% (Joe et al; 2004; Eighner dan Schulz, 1999).
2.6 Teknik Sampling
Sampel adalah bagian dari populasi yang menjadi objek penelitian (sampel sendiri secara harfiah berarti contoh). Alasan perlunya
pengambilan sampel adalah sebagai berikut : keterbatasan waktu, tenaga
dan biaya; lebih cepat dan lebih mudah; memberi informasi yang lebih banyak dan dalam; dapat ditangani lebih teliti (Nasution R, 2003).
Populasi penelitian terdiri dari populasi sampling dan populasi sasaran.
Populasi sampling adalah keseluruhan objek yang diteliti, sedangkan
populasi sasaran adalah populasi yang benar-benar dijadikan sumber data. Pemilihan teknik pengambilan sampel merupakan upaya penelitian
untuk mendapat sampel yang representatif (mewakili), yang dapat menggambarkan populasinya. Teknik pengambilan sampel tersebut dibagi
atas 3 kelompok besar, yaitu :
1. Sampel Acak atau Random Sampling / Probability Sampling : pada
pengambilan sampel secara random, setiap unit populasinya
mempunyai kesempatan yang sama untuk diambil sebagai sampel.
Keuntungan pengambilan sampel dengan probability sampling adalah sebagai berikut :
- Derajat kepercayaan terhadap sampel dapat ditentukan.
- Beda penaksiran parameter populasi dengan statistik sampel, dapat diperkirakan.
Ada 5 cara pengambilan sampel yang termasuk secara random, yaitu
sebagai berikut :
a. Sampel Random Sederhana (Simple Random Sampling) :
Proses pengambilan sampel dilakukan dengan memberi
kesempatan yang sama pada setiap anggota populasi untuk menjadi anggota sampel.
Keuntungan : prosedur mudah dan sederhana
Kerugian : membutuhkan daftar seluruh anggota populasi,
biaya transportasi besar.
b. Sampel Random Sistematik (Systematic Random Sampling) :
Proses pengambilan sampel, setiap urutan dari titik awal yang
dipilih secara random.
Keuntungan : perencanaan dan penggunaannya mudah, sampel tersebar di daerah populasi.
Kerugian : membutuhkan daftar populasi.
c. Sampel Random Berstrata (Stratified Random Sampling) :
Populasi dibagi strata-strata (sub populasi), kemudian pengambilan sampel dilakukan dalam setiap strata baik secara simple random
sampling,maupun secara systematik random sampling.
Keuntungan : taksiran mengenai karakteristik populasi lebih
tepat.
Kerugian : daftar populasi setiap strata diperlukan.
Pengambilan sampel dilakukan terhadap sampling unit, dimana
sampling unitnya terdiri dari satu kelompok (cluster). Tiap item (individu) di dalam kelompok yang terpilih akan diambil sebagai
sampel.
Keuntungan : tidak memerlukan daftar populasi Kerugian : prosedur sulit
e. Sampel Bertingkat (Multi Stage Sampling) : Proses pengambilan
sampel dilakukan bertingkat, baik bertingkat dua maupun lebih.
Keuntungan : biaya transportasi kurang
Kerugian :prosedur sulit,prosedur pengambilan sampel memerlukan perencanaan yang lebih cermat.
2. Non Probability Sample (Selected Sample) : pemilihan sampel tidak
secara random. Cara ini dipergunakan : bila biaya sangat sedikit, hasil yang diminta segera, tidak memerlukan ketepatan yang tinggi.
Ada 3 cara yang dikenal :
a. Pusposive Sampling : Pengambilan sampel dilakukan hanya atas dasar
pertimbangan penelitinya saja yang menganggap unsur-unsur yang
dikehendaki telah ada dalam anggota sampel yang diambil.
b. Accidental Sampling : Sampel diambil atas dasar seandainya saja, tanpa
direncanakan lebih dahulu. Juga jumlah sampel yang dikehenadaki
tidak berdasarkan pertimbangan yang dapat dipertanggung jawabkan, asal memenuhi keperluan saja. Kesimpulan yang diperoleh bersifat
c. Quota Sampling : Pengambilan sampel hanya berdasarkan pertimbangan peneliti
saja, hanya disini besar dan kriteria sampel telah ditentukan lebih dahulu. Cara ini dipergunakan kalau peneliti mengenal betul daerah dan situasi
daerah dimana penelitian akan dilakukan.
3. Investigatif Sampel : pemilihan sampel diambil secara acak dan dilihat dari nomor registrasi yang berbeda untuk setiap sampel serta
peminatan masyakarakat yang cukup tinggi terhadap produk tersebut.
BAB III
KERANGKA KONSEP
Boraks bukan merupakan senyawa yang digunakan pada makanan atau sebagai bahan tambahan
Boraks memilik efek akumulasi yang berbahaya jika dikonsumsi karena menimbulkan keracunan akut maupun
kronis bahkan kematian
Berdasarka penelitian-penelitian masih banyak ditemukan produk mie yang mengandung boraks
Boraks tidak boleh digunakan boraks pada mie yang beredar
di pasar Ciputat
Tes Nyala Api Tes Warna dengan Peraksi
Kurkumin
BAB IV
METODOLOGI PENELITIAN
4.1 Pengambilan Sampel
Sampel yang digunakan terdiri dari 5 Mie basah yang beredar di pasar Ciputat. Mie basah yang diambil berdasarkan teknik sampling investigativ, yaitu mencari
tahu secara langsung asal pabrik pembuat mie basah yang dijual para pedagang
tersebut. Dari hasil investigasi seluruh pedagang mie basah yang berjumlah ± 20
pedagang didapatkan 5 pabrik utama yaitu pabrik di daerah Bandung, pabrik di daerah Parung, pabrik dari Tangerang, dan 2 sampel dari pabrik di Ciputat
dengan bentuk dan warna yang berbeda.
4.2 Tempat dan Waktu Penelitian
Penelitian dilakukan di laboratorium Kimia Farmasi Fakultas Kedokteran dan
Ilmu Kesehatan (FKIK) UIN Syarif Hidayatullah Jakarta . Penelitian ini
berlangsung dari bulan Agustus 2009 sampai dengan bulan November 2009.
4.3 Alat dan Bahan 4.3.1 Alat
Alat yang digunakan dalam penelitian ini, yaitu:
Alat gelas yang umum terdapat dilaboratorium, timbangan listrik, mesin penggiling mie sederhana, oven, tanur, alat refluks, kertas saring, Bunsen,
4.3.2 Bahan
Bahan- bahan yang digunakan dalam penelitian ini, yaitu :
Boraks proanalisa (Merck), Kurkumin proanalisa (Merck), tepung terigu merk cakra
kembar, telur, garam dapur, soda kue (natrium karbonat), Alkohol 96%, asam asetat
pekat, asam sulfat pekat, NaOH 10%, H2O2 30%, Ca(OH)2, asam oksalat, mie basah,
aquades,
4.4 Prosedur Penelitian
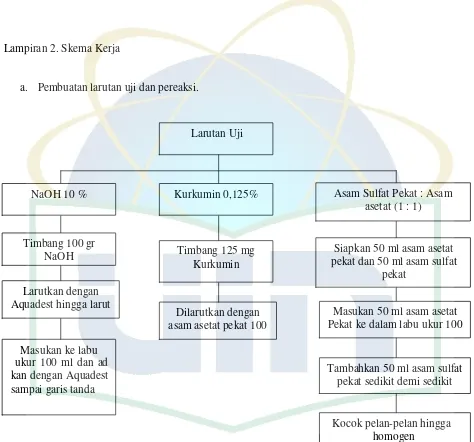
4.4.1 Penyiapan Bahan Baku dan Pereaksi 1. Pembuatan Larutan kurkumin 0,125%
Ditimbang kurkumin sebanyak 125 mg, dimasukkan ke dalam labu ukur 100 ml, ditambahkan asam asetat pekat sampai larut dan ditambahkan
asam asetat tersebut sampai larut dan sampai garis tanda.
2. Pembuatan larutan asam sulfat pekat-asam asetat (1 : 1)
Diukur 100 ml larutan asam asetat pekat, dimasukkan ke dalam Erlenmeyer 250 ml. diukur asam sulfat pekat 100 ml, dicampurkan
sedikit–sedikit pada asam asetat pekat sampai homogen.
3. Pembuatan larutan NaOH 10%
Ditimbang NaOH 10 gram dilarutkan dengan air suling sampai larut dimasukkan ke dalam labu ukur 100 ml, ditambahkan aquadest sampai
garis tanda.
4. Pembuatan mie basah dengan penambahan boraks
Ditimbang 250 gram tepung terigu, 1 buah telur ayam (62,5 gram),
tercampr rata. Timbang adonan 20 gram sebanyak 12 buah. Kemudian
setiap 20 gram adonan mie ditambahkan dengan boraks sesuai dengan
kadar (2.5 mg boraks untuk 6,25 µg/ml, 4 mg boraks untuk 10 µ g/ml, 5 mg boraks untuk 12,5 µ g/ml, 7mg boraks untuk 18,75 µ g/ml, 8mg
boraks untuk 20 µg/ml, 10 mg boraks untuk 25 µg/ml, 12 mg boraks
untuk 30 µg/ml, 12,5 mg boraks untuk 31,25 µ g/ml, 15 mg boraks untuk 37 µg/ml, 17,5 mg boraks untuk 43,75 µg/ml, 20 mg boraks untuk 50 µg/ml. Kemudian masing-masing adonan dihaluska dan di cetak seperti
mie.
5. Pembuatan larutan Mie basah yang sudah ditambahkan boraks
Ditimbang mie yang sudah dicampur boraks dengan kadar 6,25 µg/ml
sebanyak 5 gram Dimasukkan ke dalam labu alas bulat 250 ml, kemudian ditambahkan 20 ml H2SO4 pekat. Labu ditutup dengan alat
refluks sederhana dan dipanaskan selama 5 menit untuk meratakan
larutan asam, sampai permukaan larutan mulai bergerak dan larutan akan menjadi hitam dan licin kemudian labu tersebut didinginkan dalam air es dan bila terdapat asap dibiarkan terbuka beberapa saat. Kemudian larutan dengan cepat ditambahkan 20 ml H2O2 30 %, larutan akan bergolak
sehingga mie yang padat berubah menjadi cairan, dan akan keluar asap keunguan, dibiarkan hingga asap berkurang, kemudian di refluks kembali selama 15 detik, dinginkan didalam air es, didiamkan pada suhu ruangan.
dengan boraks pada kadar 10 µ g/ml, 12,5 µg/ml, 18,75 µ g/ml, 20 µ g/ml, 25 µg/ml, 30 µg/ml, 31,25 µ g/ml, 37 µg/ml, 43,75 µg/ml, 50 µg/ml.
4.4.2 Penentuan panjang gelombang maksimum.
Dari larutan mie dengan kadar 25 µg/ml dipipet 1 ml kemudian dimasukkan ke dalam cawan porselin dan ditambahkan 1 ml larutan NaOH 10%, dipanaskan di atas penangas air sampai kering, kemudian pemanasan dilanjutkan
dengan oven pada suhu 1000 ± 50 C selama 5 menit, didinginkan. Ditambahkan 3 ml larutan kurkumin 0,125% dipanaskan sambil diaduk selama 5 menit, didinginkan lagi. Kemudian ditambahkan 3 ml larutan asam sulfat–asetat (1:1) dipanaskan sambil diaduk sampai tidak ada warna kuning, baik pada cawan
maupun pada pengaduk, didiamkan selama 15 menit.
Ditambahkan sedikit alkohol kemudian dimasukkan ke dalam labu kur
100 ml, diencerkan dengan alkohol sampai garis tanda. Kemudian larutan disaring dengan kertas penyaring. Hasil saringan dikumpulkan dan diamati serapannya pada panjang gelombang antara 400 sampai 600 nm.
4.4.3 Pembuatan kurva kalibrasi dan validasi metoda
Dari larutan 6,25 µg/ml dipipet 1 ml kemudian dimasukkan ke dalam cawan porselin dan ditambahkan 1 ml larutan NaOH 10%, dipanaskan di atas penangas air sampai kering, kemudian pemanasan dilanjutkan dengan oven pada
suhu 1000 ± 50 C selama 30 menit, kemudian didinginkan pada suhu ruangan. Ditambahkan 3 ml larutan kurkumin 0,125% dipanaskan sambil diaduk selama 5 menit, didinginkan lagi. Kemudian ditambahkan 3 ml larutan asam sulfat–asetat (1:1) dipanaskan sambil diaduk sampai tidak ada warna kuning,
Ditambahkan sedikit alkohol kemudian dimasukkan ke dalam labu kur 100 ml, diencerkan dengan alkohol sampai garis tanda. Disaring dengan kertas
saring. Hasil saringan dikumpulkan dan diamati serapannya pada panjang
gelombang 545,95 nm. Lakukan hal yang sama pada
,
12,5 µ g/ml, 18,75 µ g/ml, ,25 µg/ml, , 31,25 µg/ml, 37 µg/ml, 43,75 µg/ml, 50 µ g/ml untuk kurva kalibrasi
dan 10 µg/ml, 20 µ g/ml, 30 µg/ml untuk validasi metoda.
4.4.4 Analisa sampel pasar secara kualitatif dan kuantitatif a. Analisa kualitatif
1.
Uji nyala api
Ditimbang 5gram sampel dan masukkan dalam cawan porselen
ditambahkan 10 tetes asam sulfat pekat, kemudian ditambah 2 ml methanol dan dibakar. Bila timbul nyala hijau akan terdapat senyawa
boron sebagai metal borat atau etil borat.
2.
Uji kurkumin
Lebih kurang 20 gram sampel dibubuhi hablur natrium karbonat
secukupnya. Arangkan di atas nyala api Bunsen dan abukan didalam
tanur listrik. Dinginkan, lalu tambahkan air dan beberapa tetes asam klorida 5 N, saring. Tambahkan 4 tetes asam oksalat jenuh dan1 ml
ekstak etil alkohol dan kurkumin. Uapkan di atas penangas air, bila
b.
Analisa Kuantitatif dengan Spektrofotometri Uv-Vis
Ditimbang sampel mie basah dari pasar sebanyak 5 gram Dimasukkan ke dalam labu alas bulat 250 ml, kemudian ditambahkan 20
ml H2SO4 pekat. Labu ditutup dengan alat refluks sederhana dan
dipanaskan selama 5 menit untuk meratakan larutan asam, sampai permukaan larutan mulai bergerak dan larutan akan menjadi hitam dan licin kemudian labu tersebut didinginkan dalam air es dan bila terdapat
asap dibiarkan terbuka beberapa saat.
Kemudian larutan dengan cepat ditambahkan 20 ml H2O2 30 %,
larutan akan bergolak sehingga mie yang padat berubah menjadi cairan, dan akan keluar asap keunguan, dibiarkan hingga asap berkurang, kemudian di refluks kembali selama 15 detik, dinginkan didalam air es, didiamkan pada suhu ruangan. Kemudian di masukkan ke dalam labu
ukur 100 ml, dan diencerkan dengan aquadest pada suhu ruangan.
Dari larutan tersebut dipipet 1 ml kemudian dimasukkan ke dalam cawan porselin dan ditambahkan 1 ml larutan NaOH 10%, dipanaskan di atas penangas air sampai kering, kemudian pemanasan
dilanjutkan dengan oven pada suhu 1000 ± 50 C selama 5 menit, didinginkan.
Ditambahkan 3 ml larutan kurkumin 0,125% dipanaskan sambil diaduk selama 5 menit, didinginkan lagi. Kemudian ditambahkan 3 ml
larutan asam sulfat–asetat (1:1) dipanaskan sambil diaduk sampai tidak ada warna kuning, baik pada cawan maupun pada pengaduk, didiamkan
Ditambahkan sedikit alkohol kemudian dimasukkan ke dalam
labu ukur 100 ml, diencerkan dengan alkohol sampai garis tanda.
Disaring dengan kertas saring. Hasil saringan dikumpulkan dan diamati serapannya pada panjang gelombang 545,95 nm
BAB V
HASIL DAN PEMBAHASAN
5.1 Hasil
Dari penelitian yang dilakukan didapatkan hasil sebagai berikut :
1. Pada penentuan panjang gelombang didapatkan panjang gelombang serapan maksimum boraks sebesar 545,9 nm. Data selengkapnya dapat
dilihat pada lampiran 3.
2. Hasil uji liniearitas dan pembuatan kurva kalibrasi
Pada pembuatan kurva kalibrasi dilakukan dengan menggunakan deret
konsentrasi pada kisaran 6,25-50 µ g/ml, dan didapatkan kurva kalibrasi boraks sebagai berikut :
0.6
Gambar 6. Kurva kalibrasi boraks pada mie basah Persamaan garis : y = 0,008 + 0,012x
3. Pada Pengujian batas deteksi boraks dengan mie basah simulasi pada
percobaan ini adalah sebesar 3,1132 µ g/ml sedangkan untuk batas
kuantitasi sebesar 10,3775 µg/ml. Data selengkapnya dapat dilihat pada lampiran 5.
4. Hasil Uji Perolehan Kembali (Akurasi) dari 3 konsentrasi boraks
dalam mie basah simulasi yaitu 99,767±1,114 %. Data selengkapnya dapat dilihat pada lampiran 6.
5. Hasil uji keseksamaan (presisi) pada 3 konsentrasi boraks dalam mie basah simulasi yang diuji pada percobaan ini memberikan nilai
koefisien variasi dibawah 2%. Data selengkapnya dapat dilihat pada
lampiran 7.
6. Pada 2 uji kualitatif sampel mie basah yang beredar di pasar Ciputat dari lima sampel yang beredar, pada penelitian ini negativ
mengandung boraks. Data selengkapnya dapat dilihat pada lampiran 11.
7. Penetuan kadar sampel mie basah yang beredar di pasar Ciputat dari
lima sampel yang beredar, terdapat empat mie basah yang mengandung boraks. Mie tersebut memiliki kadar boraks yang
berbeda-beda. Data selengkapnya dapat dilihat pada lampiran 8.
5.2 Pembahasan
Boraks pada awal mula dikenal sebagai bahan antiseptik yang
digunakan sebagai bahan pembersih, pengawet kayu, dan herbisida namun sekarang banyak digunakan sebagai bahan tambahan makanan pada mie,
pengawet. Pada penelitian ini menggunakan sampel mie basah yaitu mie
yang mengandung kadar air 51 % dan sering ditambahkan boraks sebagai
pengenyal. Absorbsi boraks secara berulang atau absorpsi berlebihan dapat mengakibatkan toksik (keracunan). Dalam air, boraks merupakan
campuran natrium metaborat dan asam borat. Sedangkan dalam suasana
asam boraks terurai menjadi asam borat. Dengan demikian, baik waktu pengolahan makanan dengan air maupun karena dimakan dan melalui
lambung yang bersifat asam, didalam tubuh akan ditemukan asam borat setelah mengkonsumsi makanan yang mengandung boraks. Gejala dapat
berupa mual, muntah, diare, suhu tubuh menurun, lemah, sakit kepala,
rash erythematus, bahkan dapat menimbulkan shock.
Metode pada penelitian ini terdiri dari beberapa tahap sehingga sampel yang berupa padatan dapat dijadikan larutan yang dapat dibaca
pada alat spektrofotometri UV-Vis. Tahap awal yaitu mendestruksi sampel mie basah menggunakan larutan H2SO4 pekat yang ditutup dengan refluks
dan dipanaskan dengan suhu kecil 500-700 C untuk meratakan larutan asam selama 30 menit atau sampai larutan menjadi hitam dan licin. Kemudian ditambahkan oksidator H2O2 30 % yang berguna untuk mereduksi
senyawa organik menjadi C02 dan H2O sehingga larutan akan menjadi
jernih. Penggunaan H2SO4 dan H2O2 30 % dilakukan dengan perbandingan
1:1. Selanjutnya di encerkan dengan aquadest.
Dari larutan tersebut dipipet 1 ml dan ditambahkan NaOH sebagai pengikat unsur boron. Kemudian dipanaskan dengan water bath selama 90
Hal ini dilakukan karena senyawa kompleks ini mudah terhidrolisis oleh
adannya air, sehingga diusahakan untuk menghilangkan air yang ada
dengan jalan pemanasan.
Larutan boraks merupakan larutan yang tidak berwarna, hal ini
menjadi kendala karena larutan yang akan digunakan dengan
spektrofotometri UV-Vis harus memiliki gugus kromofor yang ditandai dengan warna. Sehingga pada penelitian ini boraks direaksikan dengan
dengan kurkumin sebagai pembentuk kompleks warna rosocyanin yang menghasilkan warna rosa.
Kurkumin merupakan zat warna alam, selain digunakan untuk
pewarna makanan dan kosmetik, juga dapat digunakan sebagai penunjuk
adanya boraks pada makanan. Oleh asam kuat, boraks terurai dari ikatan- ikatannya menjadi asam borat dan diikat oleh kurkumin membentuk
kompleks warna rosa yang sering disebut kelat rosasianin atau senyawa Boron Cyano Kurkumin Kompleks. yaitu suatu zat yang berwarna merah,
O OH
Konsentrasi kurkumin yang digunakan adalah 0,125 % berdasarkan penelitian terdahulu, bahwa pada kisaran 0,100%-0,150% kurkumin dapat
larut sempurna dalam asam asetat tanpa proses penyaringan. Stabilitas
kompleks warna yaitu 2 jam setelah kompleks warna yang terjadi dilarutkan dalam alkohol dalam keadaan asam, sehingga dalam percobaan
ini pengamatan pada spektrofotometer tidak lebih dari 2 jam setelah
kompleks tersebut dilarutkan dalam alkohol.
Penentuan nilai serapan suatu sampel harus berada pada panjang
gelombang maksimum sehingga didapatkan nilai yang maksimal. Pada
penelitian sebelumnya panjang gelombang maksimum boraks yaitu 548 nm. Namun dikarenakan kondisi preparasi sampel yang berbeda sehingga
perlu dilakukan penetapan panjang gelombang maksimum pada penelitian
kadar boraks sebesar 25 µ g/ml. Dari hasil pengukuran panjang gelombang
serapan maksimum boraks tersebut adalah sebesar 545,95 nm berdasarkan
nilai tertinggi dari data serapan.
Suatu metode penelitian perlu dilakukan validasi untuk
membuktikan bahwa hasil yang diperoleh merupakan hasil yang akurat
dan memenuhi persyaratan untuk penggunaannya. Validasi metode analisis merupakan suatu tindakan penilaian terhadap parameter tertentu
yang bertujuan untuk menjamin bahwa metode analisa yang digunakan akurat, spesifik, dan tahan pada kisaran analit yang akan dianalisis dan
sesuai dengan . Dalam penelitian ini, parameter- parameter validasi yang
dilakukan yaitu liniearitas, batas deteksi dan batas kuantisasi, kecermatan,
dan keseksamaan. Menggunakan sampel mie yang dibuat sendiri dengan penambahan boraks pada kadar tertentu, hal ini dimaksudkan agar tidak
terjadi penyimpangan yang terlalu jauh.
Tahap pertama yaitu pembuatan kurva kalibrasi. Kurva kalibrasi
dihitung berdasarkan persamaan yang diperoleh dari nilai absorban pada
berbagai deret konsentrasi. Deret konsentrasi yang dibuat yaitu 6,25-50
µg/ml dan kurva kalibrasi ini untuk memperoleh hasil-hasil uji secara langsung proporsional dengan konsentrasi analit pada kisaran yang
diberikan. Dari kurva kalibrasi tersebut didapat persamaan regresi y = 0.012x + 0.008 dengan koefisien korelasi (r) sebesar 0,9994. Kriteria
penerimaan dari koefisien korelasi adalah (r) sebesar 0,9995 yang berarti