EFEK IMUNOSTIMULATOR EKSTRAK
DAUN SAMBUNG NYAWA (Gynura procumbens (Lour.) Merr)
TERHADAP RESPON HIPERSENSITIVITAS TIPE LAMBAT
DAN TITERANTIBODI SEL IMUN PADA MENCIT JANTAN
SKRIPSI
OLEH:
AMBAR WIRATMI
NIM 111524041
PROGRAM EKSTENSI SARJANA FARMASI
FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA
MEDAN
EFEK IMUNOSTIMULATOR EKSTRAK
DAUN SAMBUNG NYAWA (Gynura procumbens (Lour.)
Merr) TERHADAP RESPON HIPERSENSITIVITAS TIPE
LAMBAT DAN TITER ANTIBODI SEL IMUN PADA
MENCIT JANTAN
SKRIPSI
Diajukan untuk melengkapi salah satu syarat untuk memperoleh Gelar Sarjana Farmasi pada
Fakultas Farmasi Universitas Sumatera Utara
OLEH:
AMBAR WIRATMI
NIM 111524041
PROGRAM EKSTENSI SARJANA FARMASI
FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA
MEDAN
PENGESAHAN SKRIPSI
EFEK IMUNOSTIMULATOR EKSTRAK DAUN SAMBUNG
NYAWA (Gynura procumbens (Lour.) Merr) TERHADAP
RESPON HIPERSENSITIVITAS TIPE LAMBAT DAN
TITER ANTIBODI SEL IMUN PADA MENCIT JANTAN
OLEH:
AMBAR WIRATMI NIM 111524041
Dipertahankan di Hadapan Panitia Penguji Skripsi Fakultas Farmasi Universitas Sumatera Utara
Pada tanggal: 7 Februari 2014
Pembimbing I, Panitia Penguji,
Drs. Saiful Bahri, M.S., Apt. Prof. Dr. Rosidah, M.Si., Apt.
NIP 195208241983031001 NIP 195103261978022001
Pembimbing II, Drs. Saiful Bahri, M.S., Apt.
NIP 195208241983031001
Drs. Suryadi Achmad M.Sc., Apt. Aminah Dalimunthe, S.Si., M.Si., Apt.
NIP 195109081985031002 NIP 197806032005012004
Dra. Herawaty Ginting, M.Si., Apt.
NIP 195112231980032002
Medan, 17 April 2014 Fakultas Farmasi
Universitas Sumatera Utara Dekan,
KATA PENGANTAR
Puji dan syukur penulis ucapkan kehadirat Allah SWT yang Maha
Kuasa yang telah melimpahkan nikmat, rahmat, karunia, dan kasih
sayang-Nya, sehingga penulis dapat menyelesaikan skripsi ini, yang berjudul “Efek
Imunostimulator Ekstrak Daun Sambung Nyawa (Gynura procumbens (Lour.)
Merr) terhadap Respon Hipersensitivitas Tipe Lambat dan Titer Antibodi Sel
Imun pada Mencit Jantan”. Skripsi ini diajukan sebagai salah satu syarat untuk
memperoleh gelar Sarjana Farmasi pada Fakultas Farmasi Universitas
Sumatera Utara.
Pada kesempatan ini penulis mengucapkan terima kasih kepada Bapak
Prof. Dr. Sumadio Hadisahputra, Apt., selaku Dekan Fakultas Farmasi
Universitas Sumatera Utara yang telah memberikan bantuan dan fasilitas
selama masa pendidikan. Penulis juga mengucapkan terima kasih yang
sebesar-besarnya kepada Bapak Drs. Saiful Bahri, M.S., Apt., dan Bapak Drs.
Suryadi Achmad M.Sc., Apt., selaku pembimbing yang telah memberikan
banyak waktu, bimbingan, dan nasehat selama penelitian hingga selesainya
penyusunan skripsi ini. Selain itu, penulis juga mengucapkan terima kasih
kepada Ibu Prof. Dr. Rosidah, M.Si., Apt., Ibu Aminah Dalimunthe, S.Si.,
M.Si., Apt., dan Ibu Dra. Herawaty Ginting, M.Si., Apt., selaku penguji yang
telah memberikan evaluasi dan masukan kepada penulis dalam penyusunan
skripsi ini. Juga kepada Bapak Drs. Awaluddin Saragih, M.Si., Apt., selaku
dosen pembimbing akademik penulis selama menjalani perkuliahan di Fakultas
Penulis mengucapkan terima kasih dan rasa sayang yang tak terhingga
kepada Ayahanda Suroso dan Ibunda Suharni tercinta atas segala-galanya, juga
kepada ketiga adik penulis Renaldy Zulfikhri, Wahyu Ramadhan dan Rezkia
Amelia Putri atas doa dan dukungannya dalam penyelesaian skripsi ini.
Penulis juga mengucapkan terima kasih sebesar-besarnya kepada para
sahabat dan rekan-rekan seperjuangan angkatan 2011: Ayu, Dewi, Iza, Leni,
Suci, Difa, Martko, Uya, dan juga kepada semua Kepala Laboratorium di
Laboratorium Farmakologi Farmasi, Laboratorium Fitokimia Farmasi,
Laboratorium Botani Farmasi, dan asisten atas semua dukungan dan doa
dalam penyelesaian skripsi ini.
Penulis menyadari bahwa skripsi ini masih jauh dari kesempurnaan,
sehingga penulis mengharapkan kritik dan saran yang bersifat membangun.
Akhir kata, semoga tulisan ini dapat bermanfaat bagi pembaca dan menjadi
sumbangan yang berarti bagi ilmu pengetahuan khususnya dalam bidang ilmu
farmasi.
Medan, 17 April 2014
Penulis,
EFEK IMUNOSTIMULATOR EKSTRAK DAUN SAMBUNG NYAWA (Gynura procumbens (Lour.) Merr) TERHADAP RESPON
HIPERSENSITIVITAS TIPE LAMBAT DAN TITER ANTIBODI SEL IMUN MENCIT JANTAN
ABSTRAK
Sistem imun pada manusia berperan penting untuk mempertahankan kondisi tubuh dari serangan agen-agen penyebab infeksi, seperti mikroorganisme patogen. Dalam keadaan sistem imun tidak mampu bekerja dengan baik, peningkatan sistem imun menjadi sangat penting agar sistem imun tetap bekerja dengan maksimal. Peningkatan sistem imun dapat dilakukan dengan menggunakan imunomodulator, khususnya yang bersifat imunostimulan.
Tujuan dari penelitian ini adalah untuk mengetahui efek imunostimulator ekstrak daun sambung nyawa. Pada penelitian ini dilakukan uji efek imunostimulator ekstrak daun sambung nyawa terhadap respon hipersensitivitas tipe lambat dan titer antibodi sel imun mencit jantan. Ekstrak etanol daun sambung nyawa diberikan secara oral dengan dosis 125 mg/kg bb, 250 mg/kg bb, 500 mg/kg bb. Levamisole dosis 25 mg/kg bb sebagai kontrol positif, suspensi CMC Na 1% sebagai kontrol negatif dan sel darah merah sapi digunakan sebagai antigen.
Hasil uji efek imunostimulator ekstrak daun sambung nyawa terhadap respon hipersensitivitas tipe lambat dan titer antibodi sel imun mencit jantan menunjukkan bahwa ekstrak daun sambung nyawa dosis 125, 250, 500 mg/kg bb memberikan peningkatan respon hipersensitivitas tipe lambat dan titer antibodi sel imun dibandingkan kontrol negatif. Hanya dosis 250 mg/kg bb yang memberikan hasil yang tidak berbeda nyata dengan kontrol positif (p < 0,05). Pemberian ekstrak daun sambung nyawa dosis 500 mg/kg bb memberikan hasil yang lebih baik dibandingkan dengan pada pemberian dosis 125 dan 250 mg/kg bb. Dengan demikian disimpulkan bahwa ekstrak daun sambung nyawa mempunyai efek imunostimulator terhadap respon hipersensitivitas tipe lambat dan titer antibodi sel imun mencit jantan.
THE IMMUNOSTIMULATORY EFFECT OF SAMBUNG NYAWA LEAVES EXTRACT TO DELAYED TYPE HYPERSENSITIVITY
RESPONE AND IMMUNITY CELLS ANTIBODY TITER OF MALE MICE
ABSTRACT
The immune system plays an important role in the human body to maintain the condition of attack infectious agents, such as pathogenic microorganisms. In the state of the immune system can not work properly, increase immune system becomes very important in order to keep the immune system working optimally. Improved immune system can be done by using immunomodulators particularly one which is immunostimulatory.
The objective of this study was to determine the immunostimulatory effect of extracts of leaves of the sambung nyawa. This study tested the immunostimulatory effect of extracts of leaves of the sambung nyawa of the delayed type hypersensitivity response and antibody titer immune cells of male mice. Ethanol extract of leaves of sambung nyawa given orally at a dose of 125 mg/kg bw, 250 mg/kg bw, 500 mg/kg bw. Levamisole dose of 25 mg/kg bw as a positive control, 1% CMC Na suspension as a negative control and bovine red blood cells are used as antigen.
Based on the result of immunostimulatory effect of extracts of leaves of the sambung nyawa of the delayed type hypersensitivity response and antibody titer immune cells of male mice showed that the leaf extract dose god 125, 250, 500 mg/kg bw provides enhanced delayed-type hypersensitivity response and immune cell antibody titer compared negative control. Only the dose of 250 mg/kg bw which gives results that are not significantly different from the positive control (p < 0,05). Sambung nyawa leaf extract dose of 500 mg/kg bw gives better results as compared to the administration dose 125 and 250 mg/kg bw. Thus, it is concluded that sambung nyawa leaf extract has immunostimulatory effects on delayed-type hypersensitivity response and antibody titer immune cells of male mice .
DAFTAR ISI
Halaman
JUDUL ... i
LEMBAR PENGESAHAN ... iii
KATA PENGANTAR ... iv
ABSTRAK ... vi
ABSTRACT ... vii
DAFTAR ISI ... viii
DAFTAR TABEL ... xi
DAFTAR GAMBAR ... xii
DAFTAR LAMPIRAN ... xiii
BAB I PENDAHULUAN ... 1
1.1 Latar Belakang ... 1
1.2 Perumusan Masalah ... 3
1.3 Hipotesis ... 3
1.4 Tujuan Penelitian ... 4
1.5 Manfaat Penelitian ... 4
1.6 Diagram Kerangka Pikir Penelitian ... 5
BAB II TINJAUAN PUSTAKA ... 6
2.1 Uraian Tumbuhan ... 6
2.1.1 Habitat ... 6
2.1.2 Morfologi ... 6
2.1.4 Sinonim ... 7
2.1.5 Nama Asing ... 7
2.1.6 Nama Daerah ... 7
2.1.7 Kandungan Kimia ... 7
2.1.8 Khasiat Tumbuhan ... 8
2.2 Ekstraksi ... 8
2.3 Cara-cara Ekstraksi ... 9
2.4 Sistem Imun ... 10
2.4.1 Respon Imun Nonspesifik ... 11
2.4.2 Respon Imun Spesifik ... 11
2.4.3 Imunomodulator ... 17
2.5 Metode Pengujian Efek Imunomodulator ... 19
BAB III METODE PENELITIAN ... 21
3.1 Alat dan Bahan ... 21
3.1.1 Alat-alat ... 21
3.1.2 Bahan-bahan ... 22
3.2 Hewan Percobaan ... 22
3.3 Pembuatan Larutan Pereaksi ... 22
3.4 Prosedur Pembuatan Simplisia ... 24
3.5 Karakterisasi Simplisia ... 25
3.5.1 Pemeriksaan Makroskopik ... 25
3.5.2 Pemeriksaan Mikroskopik ... 25
3.5.4 Penetapan Kadar Sari yang Larut dalam Air ... 26
3.5.5 Penetapan Kadar Sari yang Larut dalam Etanol ... 26
3.5.6 Penetapan Kadar Abu Total ... 27
3.5.7 Penetapan Kadar Abu Tidak Larut Asam ... 27
3.6 Skrining Fitokimia ... 28
3.7 Pembuatan Ekstrak Etanol Daun Sambung Nyawa ... 31
3.8 Uji Efek Imunomodulator ... 31
3.8.1 Penyiapan Hewan Percobaan ... 31
3.8.2 Penyiapan Kontrol, Bahan Uji, dan Antigen ... 32
3.8.2.1 Penyiapan CMC Na 1% ... 32
3.8.2.2 Penyiapan Suspensi Levamisole ... 32
3.8.2.3 Penyiapan Suspensi Ekstrak Daun Sambung Nyawa ... 33
3.8.2.4 Penyiapan Sel Darah Merah Sapi ... 33
3.8.3 Uji Respon Hipersensitivitas Tipe Lambat ... 34
3.8.4 Uji Titer Antibodi ... 35
3.9 Analisis Statistik ... 36
BAB IV HASIL DAN PEMBAHASAN ... 37
4.1 Simplisia dan Ekstrak ... 37
4.2 Pengujian Efek Imunomodulator ... 40
4.2.1 Respon Hipersensitivitas Tipe Lambat ... 42
4.2.2 Titer Antibodi ... 45
BAB V KESIMPULAN DAN SARAN ... 50
5.1 Kesimpulan ... 50
DAFTAR PUSTAKA ... 52
DAFTAR TABEL
Tabel Halaman
4.1 Hasil Pemeriksaan Karakterisasi Simplisia ... 38
4.2 Hasil Pemeriksaan Skrining Simplisia ... 39
DAFTAR GAMBAR
Gambar Halaman
1.1 Diagram Kerangka Pikir Penelitian ... 5
4.1 Volume Pembengkakan Kaki Mencit Pada Berbagai Perlakuan
(Rerata ± SEM) ... 43
4.2 Titer Antibodi Sel Imun Mencit ... 46
DAFTAR LAMPIRAN
Lampiran Halaman
1. Hasil identifikasi Daun Sambung Nyawa ... 55
2. Gambar Karakteristik Sampel ... 56
3. Gambar Mikroskopik Serbuk Simplisia Daun Sambung Nyawa, Perbesaran 10 x 40 ... 58
4. Perhitungan Hasil Pemeriksaan Karakterisasi Simplisia ... 60
5. Bagan Alur Penelitian ... 65
6. Gambar Alat-alat ... 66
7. Gambar Hewan Percobaan ... 68
8. Pembengkakan Kaki Mencit dan Hemaglutinasi ... 69
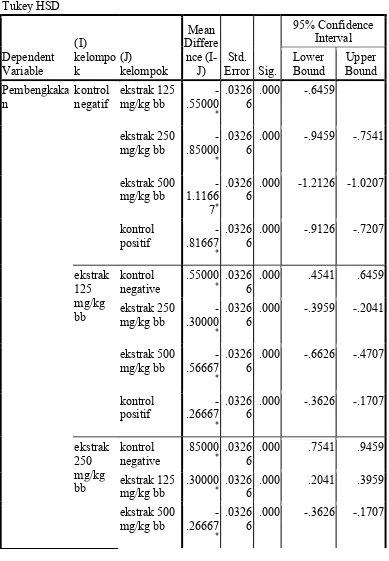
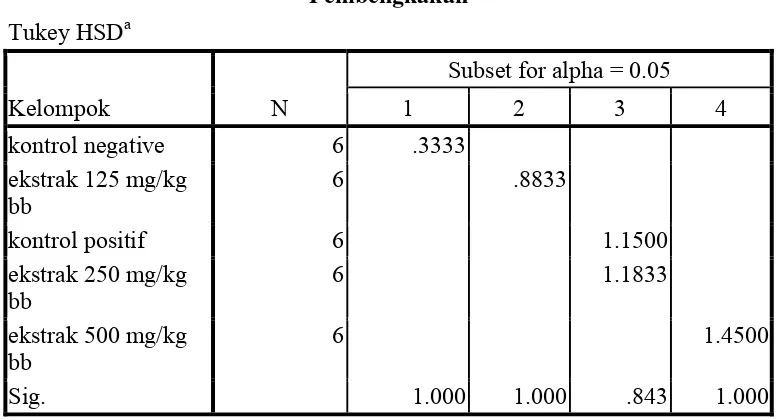
9. Tabel Hasil Perhitungan Statistik ... 71
EFEK IMUNOSTIMULATOR EKSTRAK DAUN SAMBUNG NYAWA (Gynura procumbens (Lour.) Merr) TERHADAP RESPON
HIPERSENSITIVITAS TIPE LAMBAT DAN TITER ANTIBODI SEL IMUN MENCIT JANTAN
ABSTRAK
Sistem imun pada manusia berperan penting untuk mempertahankan kondisi tubuh dari serangan agen-agen penyebab infeksi, seperti mikroorganisme patogen. Dalam keadaan sistem imun tidak mampu bekerja dengan baik, peningkatan sistem imun menjadi sangat penting agar sistem imun tetap bekerja dengan maksimal. Peningkatan sistem imun dapat dilakukan dengan menggunakan imunomodulator, khususnya yang bersifat imunostimulan.
Tujuan dari penelitian ini adalah untuk mengetahui efek imunostimulator ekstrak daun sambung nyawa. Pada penelitian ini dilakukan uji efek imunostimulator ekstrak daun sambung nyawa terhadap respon hipersensitivitas tipe lambat dan titer antibodi sel imun mencit jantan. Ekstrak etanol daun sambung nyawa diberikan secara oral dengan dosis 125 mg/kg bb, 250 mg/kg bb, 500 mg/kg bb. Levamisole dosis 25 mg/kg bb sebagai kontrol positif, suspensi CMC Na 1% sebagai kontrol negatif dan sel darah merah sapi digunakan sebagai antigen.
Hasil uji efek imunostimulator ekstrak daun sambung nyawa terhadap respon hipersensitivitas tipe lambat dan titer antibodi sel imun mencit jantan menunjukkan bahwa ekstrak daun sambung nyawa dosis 125, 250, 500 mg/kg bb memberikan peningkatan respon hipersensitivitas tipe lambat dan titer antibodi sel imun dibandingkan kontrol negatif. Hanya dosis 250 mg/kg bb yang memberikan hasil yang tidak berbeda nyata dengan kontrol positif (p < 0,05). Pemberian ekstrak daun sambung nyawa dosis 500 mg/kg bb memberikan hasil yang lebih baik dibandingkan dengan pada pemberian dosis 125 dan 250 mg/kg bb. Dengan demikian disimpulkan bahwa ekstrak daun sambung nyawa mempunyai efek imunostimulator terhadap respon hipersensitivitas tipe lambat dan titer antibodi sel imun mencit jantan.
Kata kunci: imunostimulator, respon hipersensitivitas tipe lambat, titer antibodi, daun sambung nyawa.
THE IMMUNOSTIMULATORY EFFECT OF SAMBUNG NYAWA LEAVES EXTRACT TO DELAYED TYPE HYPERSENSITIVITY
RESPONE AND IMMUNITY CELLS ANTIBODY TITER OF MALE MICE
ABSTRACT
The immune system plays an important role in the human body to maintain the condition of attack infectious agents, such as pathogenic microorganisms. In the state of the immune system can not work properly, increase immune system becomes very important in order to keep the immune system working optimally. Improved immune system can be done by using immunomodulators particularly one which is immunostimulatory.
The objective of this study was to determine the immunostimulatory effect of extracts of leaves of the sambung nyawa. This study tested the immunostimulatory effect of extracts of leaves of the sambung nyawa of the delayed type hypersensitivity response and antibody titer immune cells of male mice. Ethanol extract of leaves of sambung nyawa given orally at a dose of 125 mg/kg bw, 250 mg/kg bw, 500 mg/kg bw. Levamisole dose of 25 mg/kg bw as a positive control, 1% CMC Na suspension as a negative control and bovine red blood cells are used as antigen.
Based on the result of immunostimulatory effect of extracts of leaves of the sambung nyawa of the delayed type hypersensitivity response and antibody titer immune cells of male mice showed that the leaf extract dose god 125, 250, 500 mg/kg bw provides enhanced delayed-type hypersensitivity response and immune cell antibody titer compared negative control. Only the dose of 250 mg/kg bw which gives results that are not significantly different from the positive control (p < 0,05). Sambung nyawa leaf extract dose of 500 mg/kg bw gives better results as compared to the administration dose 125 and 250 mg/kg bw. Thus, it is concluded that sambung nyawa leaf extract has immunostimulatory effects on delayed-type hypersensitivity response and antibody titer immune cells of male mice .
Keywords: immunostimulatory, delayed-type hypersensitivity response, antibody titer, sambung nyawa leaves.
BAB I
PENDAHULUAN
1.1 Latar Belakang
Tumbuhan merupakan keragaman hayati yang selalu ada di sekitar kita,
baik itu yang tumbuh secara liar maupun yang sengaja dibudidayakan. Sejak
zaman dahulu, tumbuhan sudah digunakan sebagai tanaman obat, walaupun
penggunaannya disebarkan secara turun-temurun (Yuniarti, 2008).
Sistem imun terdiri atas imunitas nonspesifik dan spesifik. Kedua
sistem imun bekerja sama dalam mempertahankan keseimbangan badan.
Penyembuhan infeksi akan lebih cepat bila fungsi sistem imun tubuh
ditingkatkan. Berbagai bahan tanaman dapat memacu fungsi berbagai
komponen sistem imun nonspesifik (fagosit, sel NK) dan sistem imun spesifik
(proliferasi sel T, sel B yang memproduksi antibodi) serta produksi sitokin
sehingga dapat digunakan dalam klinik sebagai ajuvan untuk meningkatkan
penyembuhan berbagai penyakit infeksi (Baratawidjaya, 2006; Anderson,
1999). Salah satu dari bahan tanaman yang dapat memacu fungsi berbagai
komponen sistem imun ialah tumbuhan sambung nyawa.
Tumbuhan sambung nyawa (Gynura procumbens) termasuk dalam
familia Asteraceae, kandungan kimianya antara lain steroid/triterpenoid,
glikosida, flavonoid, saponin, tanin, dan minyak atsiri. Kandungan flavonoid,
terpenoid dan polifenol merupakan senyawa yang membantu peran daun
tersebut berperan sebagai komponen yang dapat mencegah peradangan sel
(Utami, 2013). Studi preklinis menunjukan bahwa ekstrak Gynura procumbens
(Lour) Merr dapat meningkatkan pengeluaran sel imunitas tubuh yang
terinfeksi oleh Salmonella typhimurium (Lia, 2006; Utami, 2013).
Tanaman ini tumbuh dan berkembang dengan baik pada daerah
ketinggian 100-1000 m diatas permukaan laut, suhu udara berkisar 20-30ºC,
intensitas cahaya sekitar 40-50%, dan curah hujan 1.500-2.500 mm/tahun.
Daun yang digunakan adalah daun tua yang belum menguning. Daun sambung
nyawa memiliki fungsi pengobatan antara lain sebagai antipiretik, hipotensif,
hipoglikemik, mencegah dan meluruhkan batu ginjal dan batu kandung kemih,
antihiperlipidemia, antibakteri, sitostatik, serta mencegah dan memperbaiki
kerusakan sel-sel jaringan ginjal (Winarto, 2003).
Berdasarkan uraian di atas, peneliti tertarik untuk melakukan uji efek
ekstrak daun sambung nyawa terhadap respon hipersensitivitas tipe lambat dan
titer antibodi sel imun mencit jantan sehingga dapat digunakan sebagai
1.2 Perumusan Masalah
Berdasarkan uraian di atas maka perumusan masalah pada penelitian ini
adalah:
a.apakah karakteristik simplisia daun sambung nyawa yang diteliti
memenuhi persyaratan mutu simplisia?
b.apa sajakah golongan senyawa kimia yang terdapat pada serbuk
simplisia daun sambung nyawa?
c.apakah ekstrak daun sambung nyawa dapat meningkatkan respon
hipersensitivitas tipe lambat pada mencit jantan?
d.apakah ekstrak daun sambung nyawa dapat meningkatkan titer antibodi
sel imun mencit jantan?
1.3 Hipotesis
Berdasarkan perumusan masalah di atas, maka dibuat hipotesis sebagai
berikut:
a. karakteristik serbuk simplisia daun sambung nyawa yang diteliti
memenuhi persyaratan simplisia.
b. golongan senyawa kimia yang terdapat pada serbuk simplisia daun
sambung nyawa yaitu golongan steroid/triterpenoid, alkaloid,
glikosida, flavonoid, saponin, dan tanin.
c. ekstrak daun sambung nyawa dapat meningkatkan respon
hipersensitivitas tipe lambat mencit jantan.
d. ekstrak daun sambung nyawa dapat meningkatkan titer antibodi sel
1.4 Tujuan Penelitian
Adapun tujuan dari penelitian ini adalah untuk mengetahui sebagai
berikut:
a. karakteristik dari serbuk simplisia daun sambung nyawa.
b. golongan senyawa kimia yang terdapat dalam simplisia daun sambung
nyawa.
c. efek imunostimulator ekstrak daun sambung nyawa dengan
meningkatkan respon hipersensitivitas tipe lambat mencit jantan.
d. efek imunostimulator ekstrak daun sambung nyawa dengan
meningkatkan titer antibodi sel imun mencit jantan.
1.5 Manfaat Penelitian
Adapun manfaat dari penelitian ini adalah sebagai berikut:
a. membuat daun sambung nyawa menjadi suatu sediaan herbal terstandar
dengan efek imunostimulator.
b. menambah inventaris tanaman obat yang berkhasiat sebagai
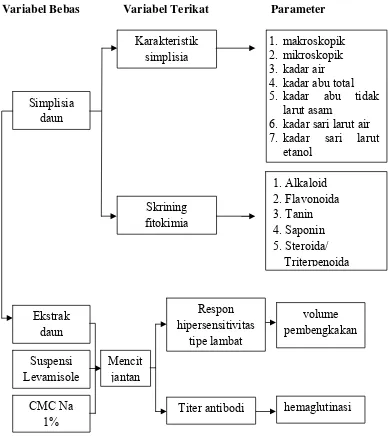
1.6 Kerangka Pikir Penelitian
Adapun kerangka pikir penelitian ini ditunjukkan pada Gambar 1.1.
Variabel Bebas Variabel Terikat Parameter
Gambar 1.1 Diagram Kerangka Pikir Penelitian
Simplisia
6. kadar sari larut air
7. kadar sari larut
BAB II
TINJAUAN PUSTAKA
2.1 Uraian Tumbuhan Sambung Nyawa
Uraian tumbuhan meliputi habitat, morfologi, sistematika tumbuhan,
sinonim, nama asing, nama daerah, kandungan kimia dan khasiatnya.
2.1.1 Habitat
Habitat tumbuhan ini berada di hutan belantara, termasuk semak
belukar. Hidupnya pada ketinggian 1-1200 meter diatas permukaan laut.
Namun akan tumbuh baik pada ketinggian 300-500 m diatas permukaan laut.
Dengan naungan, tanaman ini dapat tumbuh baik pada ketinggian 1-300 m
diatas permukaan laut (Winarto, 2003).
2.1.2 Morfologi
Tumbuhan ini merupakan tumbuhan semak semusim dengan tinggi
sekitar 20-60 cm. Berbatang lunak dengan penampang bulat dan berwarna
ungu kehijauan. Berdaun tunggal, berbentuk bulat telur, berwarna hijau, tepi
daun rata atau agak bergelombang, serta panjangnya bias mencapai 15 cm dan
lebar 7 cm. Daun bertangkai, letak berseling, berdaging, ujung dan pangkal
meruncing, serta pertulangan menyirip. Tumbuhan sambung nyawa berakar
2.1.3 Sistematika Tumbuhan
Sistematika dari tumbuhan daun sambung nyawa menurut Winarto
(2003) adalah sebagai berikut:
Divisio : Spermatophyta
Subdivision : Angiospermae
Classsis : Dicotyledonae
Ordo : Asterales
Familia : Asteraceae
Genus : Gynura
Spesies : Gynura procumbens (Lour.) Merr.
2.1.4 Sinonim
Sinonim : Gynura sarmentosa DC (Dalimartha, 2006),
Calacia procumbens Lour (Dalimartha, 2006),
Gynura divaricata DC(Yuniarti, 2008).
2.1.5 Nama Asing
Nama asing dari tumbuhan ini adalah: san qi cao (Cina), akar sabiak
(Malaysia) ) (Yuniarti, 2008).
2.1.6 Nama Daerah
Tanaman ini memiliki nama daerah: sambung nyawa, beluntas cina
(Melayu), daun sambung nyawa (Sumatera), ngokilo (Jawa) (Redaksi Trubus,
2011).
2.1.7 Kandungan Kimia
Tanaman daun sambung nyawa mengandung: senyawa golongan
glikosida, flavonoid, minyak atsiri, saponin, tannin, dan triterpen steroida
2.1.8 Khasiat Tumbuhan
Tanaman ini berkhasiat antara lain sebagai antipiretik, hipotensif,
hipoglikemik, mencegah dan meluruhkan batu ginjal dan batu kandung kemih,
antihiperlipidemia, antibakteri, sitostatik, serta mencegah dan memperbaiki
kerusakan sel-sel jaringan ginjal (Winarto, 2003). Kandungan flavonoid,
terpenoid dan polifenol merupakan senyawa yang membantu peran daun
sambung nyawa dalam menumpas kanker. Kandungan steroid dalam daun
tersebut berperan sebagai komponen yang dapat mencegah peradangan sel
(Utami, 2013).
2.2 Ekstraksi
Ekstraksi adalah kegiatan penarikan kandungan kimia yang dapat larut
sehingga terpisah dari bahan yang tidak dapat larut dengan pelarut cair (Ditjen
POM, 2000). Hasil dari ekstraksi disebut dengan ekstrak yaitu sediaan kental
yang diperoleh dengan mengekstraksi zat aktif dari simplisia nabati atau
simplisia hewani menggunakan pelarut yang sesuai, kemudian semua atau
hampir semua pelarut diuapkan dan massa atau serbuk yang tersisa
diperlakukan sedemikian sehingga memenuhi baku yang telah ditetapkan
(Ditjen POM, 1995).
Farmakope Indonesia menetapkan bahwa cairan penyari untuk
ekstraksi adalah air, etanol, dan etanol-air atau eter. Penyarian pada perusahaan
obat tradisional masih terbatas pada penggunaan penyari air, etanol, atau
etanol-air (Ditjen POM, 1989).
2.3 Cara-cara Ekstraksi
Ekstraksi dengan menggunakan pelarut terdiri dari 2 cara, yaitu:
1. Cara dingin
Ekstraksi menggunakan pelarut dengan cara dingin terdiri dari:
a. Maserasi
Maserasi adalah proses perendaman simplisia dengan menggunakan
pelarut dengan beberapa kali pengocokan atau pengadukan pada temperatur
ruangan.
b. Perkolasi
Perkolasi adalah ekstraksi dengan pelarut yang selalu baru sampai
sempurna yang umumnya dilakukan pada temperatur ruangan. Proses terdiri
dari tahapan penyerbukan simplisia, pengembangan bahan, tahap maserasi
antara, tahap perkolasi sebenarnya (penetesan/penampungan ekstrak),
terus-menerus sampai diperoleh ekstrak (perkolat).
2. Cara panas
Ekstraksi menggunakan pelarut dengan cara panas terdiri dari:
a. Refluks
Refluks adalah ekstraksi dengan pelarut pada temperatur titik
didihnya, selama waktu tertentu dan jumlah pelarut terbatas yang relatif
konstan dengan adanya pendingin balik.
b. Sokletasi
Sokletasi adalah ekstraksi menggunakan pelarut yang selalu baru
kontinu dengan jumlah pelarut relatif konstan dengan adanya pendingin
balik.
c. Digesti
Digesti adalah maserasi kinetik (dengan pengadukan kontinu) pada
temperatur yang lebih tinggi dari temperatur kamar (40-50ºC).
d. Infus
Infus adalah ekstraksi dengan pelarut air pada temperatur penangas
air (bejana infus tercelup dalam penangas air mendidih, temperatur terukur
90ºC) selama waktu tertentu (15-20 menit).
e. Dekok
Dekok adalah infus pada waktu yang lebih lama (30 menit) dan
temperatur sampai 90ºC (Ditjen POM, 2000).
2.4 Sistem Imun
Sistem imun adalah sistem pertahanan tubuh yang terdiri dari sel atau
gabungan sel, molekul-molekul, dan atau jaringan yang berperan dalam
penolakan mikroorganisme penyebab infeksi. Sistem imun berguna sebagai
perlindungan terhadap infeksi molekul lain seperti virus, bakteri, protozoa dan
parasit (Salmon, 1989).
Bila sistem imun bekerja pada zat yang dianggap asing, maka ada dua
jenis respon imun yang mungkin terjadi, yaitu respon imun nonspesifik dan
2.4.1 Respon Imun Nonspesifik
Respon imun nonspesifik fisiologik berupa komponen normal tubuh,
selalu ditemukan pada individu sehat dan siap mencegah mikroba masuk tubuh
dan dengan cepat menyingkirkannya. Disebut nonspesifik karena tidak
ditujukan terhadap mikroba tertentu, telah ada dan siap berfungsi sejak lahir.
Mekanismenya tidak menunjukan spesifisitas terhadap bahan asing dan mampu
melindungi tubuh terhadap banyak patogen potensial. System tersebut
merupakan pertahanan terdepan dalam menghadapi serangan berbagai mikroba
dan dapat memberikan respon langsung (Baratawidjaja,2012).
2.4.2 Respon Imun Spesifik
Respon imun spesifik merupakan imunitas yang didapat (adaptive
immunity) dimulai dari pengenalan zat asing hingga penghancuran zat asing
tersebut dengan berbagai mekanisme (Subowo, 1993). Dalam respon imun
spesifik, limfosit merupakan sel yang memainkan peranan penting karena sel
ini mampu mengenali setiap antigen yang masuk ke dalam tubuh, baik yang
terdapat intraseluler maupun ekstraseluler. Secara umum, limfosit dibedakan
menjadi dua jenis yaitu limfosit T dan limfosit B. Respon imun spesifik dapat
dibagi dalam 3 golongan, yaitu respon imun seluler, respon imun humoral dan
interaksi antara respon imun selular dengan respon imun humoral (Kresno,
2010).
Limfosit T dan B (sel T dan B) berasal dari sel induk yang sama yaitu
bermigrasi ke timus dan mengalami pengolahan lebih lanjut menjadi limfosit
T. Limfosit yang matang di tempat lain selain timus akan menjadi limfosit B.
Sel B berasal dari limfosit yang matang dan berdiferensiasi di sumsum
tulang, sedangkan sel T berasal dari limfosit yang berasal dari sumsum tulang
tetapi matang di timus. Sel T dan B yang matang mengalir melalui darah dan
berdiam di jaringan limfoid perifer dan membentuk koloni. Kedua sel ini akan
berproliferasi setelah mendapat stimulasi dengan adanya invasi asing.
Sel T
Sel T adalah sel yang bertanggung jawab dalam respon imun selular.
Sel T dapat dibedakan sebagai berikut:
a. Sel Thelper (Sel Th)
Sel Th adalah sel yang membantu meningkatkan perkembangan sel B
aktif menjadi sel plasma, memperkuat aktivitas sel T sitotoksik dan sel T
supresor yang sesuai, dan mengaktifkan makrofag. Sel Th dapat dibedakan
menjadi sel Th1 dan Th2. Sel Th1 berperan sebagai limfosit yang akan
melepaskan sitokin yang bersifat proinflamasi, sedangkan sel Th2 berperan
dalam memproduksi antibodi dengan menstimulasi sel B menjadi sel plasma
(Sherwood, 2001).
b. Sel Tsuppresor (Sel Ts)
Sel Ts adalah sel yang berperan dalam membatasi reaksi imun melalui
mekanisme “check and balance”dengan limfosit yang lain. Sel Ts menekan
aktivitas sel T lainnya dan sel B. Sel Th dan sel Ts akan berinteraksi dengan
menekan sel T lainnya. Dengan demikian sel Ts dapat menghambat respon
imun yang berlebihan dan bersifat antiinflamasi (Sherwood, 2001).
c. Sel Tcytotoxic (Sel Tc)
Sel Tc adalah sel yang mampu menghancurkan sel cangkokan dan sel
yang terinfeksi virus dengan mengeluarkan zat-zat kimiawi sebelum replikasi
virus terjadi (Sherwood, 2001).
Sel B
Sel B terdapat kurang lebih 25% dari jumlah limfosit total. Pada
membran sel B terdapat reseptor khas untuk mengikat antigen. Cytokin
berperan penting pada aktivasi dan pemasakan (maturasi) dari sel B menjadi
sel plasma dan sel memori (Tan dan Rahardja, 2007).
Antibodi
Antibodi adalah immunoglobulin (Ig) yang merupakan golongan yang
dibentuk oleh sel plasma yang berasal dari proliferasi sel B akibat adanya
kontak dengan antigen. Menurut perbedaan struktur dan aktivitas biologis,
antibodi dibedakan menjadi 5 subkelas:
a. Imunoglobulin G
Paling banyak ditemukan dalam cairan tubuh terutama ektravaskular
untuk memerangi mikroorganisme dan toksiknya. Ig G merupakan komponen
utama imunoglobulin serum, dengan berat molekul 160.000 dalton. Kadarnya
dalam serum sekitar 13 mg/ml, merupakan 75% dari semua imunoglobulin. Ig
sampai umur 6-9 bulan. Ig G dan komplemen bekerja saling membantu sebagai
opsoninbpada pemusnahan antigen.
b. Imunoglobulin A
Ig A dengan berat molekul 165.000 dalton ditemukan dalam serum
dengan jumlah sedikit. Kadarnya terbanyak ditemukan dalam cairan sekresi
saluran nafas, cerna dan kemih, air mata, keringat, ludah dan dalam air susu ibu
yang lebih berupa Ig A sekretori (sIgA) yang merupakan bagian terbanyak. Ig
A dapat bekerja sebagai opsonin, yaitu dapat meningkatkan efek bakteriolitik
komplemen dan menetralisasi toksin serta dapat mengaglutinasikan kuman,
mengganggu motilitasnya sehingga memudahkan fagositosis.
c. Imunoglobulin M
Berat molekul Ig M adalah 900.000 dalton. Ig M merupakan Ig paling
efisien dalam aktivasi komplemen. Ig M dibentuk paling dahulu pada respon
imun primer terhadap kebanyakan antigen disbanding dengan Ig G. Ig M dapat
mencegah gerakan mikroorganisme patogen, memudahkan fagositosis dan
merupakan aglutinator poten antigen.
d. Imunoglobulin D
Ig D ditemukan dalam serum dengan kadar yang sangat rendah. Ig D
merupakan komponen permukaan utama sel B dan pertanda dari diferensiasi
sel B yang lebih matang. Ig D merupakan 1% dari total imunoglobulin dan
banyak ditemukan pada membrane sel B bersama Ig M yang dapat berfungsi
e. Immunoglobulin E
Ig E mudah diikat sel mast, basofil dan eosinofil yang memiliki reseptor
untuk fraksi Fc dari Ig E. Ig E dibentuk setempat oleh sel plasma dalam
selaput lender saluran nafas dan cerna (Baratawidjaja, 2012).
Akibat sifat bivalen dari antibody dan banyaknya tempat antigen pada
sebagian besar agen penyebab penyakit, maka antibodi dapat mematikan
aktivitas agen penyebab penyakit tersebut dengan salah satu cara berikut ini:
a. Aglutinasi, dimana berbagai partikel besar dengan antigen pada
permukaannya, seperti bakteri atau sel darah merah terikat bersama-sama
menjadi satu kelompok. Apabila kompleks antigen-antibodi semacam itu
melibatkan antigen yang larut, kisi-kisi yang terbentuk dapat berukuran
sedemikian besar, sehingga menyebabkan pengendapan.
b. Presipitasi, dimana kompleks molekular dari antigen yang larut dan
antibodi menjadi begitu besar sehingga berubah menjadi tak larut dan
membentuk presipitat.
c. Netralisasi, dimana antibodi menutupi tempat-tempat yang toksik dari agen
yang bersifat antigenik.
d. Lisis, dimana beberapa antibodi yang sangat kuat kadang-kadang mampu
langsung menyerang membran sel agen penyebab penyakit sehingga
2.4.2.1 Respon imun selular
Respon imun selular merupakan fungsi dari limfosit T. Antigen akan
menyebabkan proliferasi dan diferensiasi sel T menjadi beberapa subpopulasi.
Subpopulasi sel T yang disebut sel T-helper (Th) akan mengenali antigen pada
permukaan sel makrofag atau sel yang terinfeksi melalui T-cell receptors
(TCR) dan molekul major histocompatibility complex (MHC) kelas-II. Sinyal
yang diberikan oleh sel terinfeksi akan menginduksi limfosit untuk
memproduksi berbagai jenis limfokin yang dapat membantu menghancurkan
antigen tersebut. Subpopulasi sel T lain yang disebut sel T-cytotoxic (Tc) akan
menghancurkan antigen melalui MHC kelas-I dengan cara kontak langsung
dengan sel (cell to cell contact). Selain itu, sel Tc memproduksi γ-interferon
yang mencegah penyebaran antigen lebih jauh (Kresno, 2001).
2.4.2.2 Respon imun humoral
Respon imun humoral dilakukan oleh sel B dan produknya, yaitu
antibodi. Respon ini diawali dengan diferensiasi limfosit B menjadi suatu
populasi sel plasma yang meproduksi dan melepaskan antibodi spesifik ke
dalam darah. Diferensiasi sel B dibantu oleh sel Th2. Adanya sinyal yang
diberikan oleh makrofag, sel Th2 akan merangsang sel B untuk memproduksi
antibodi. Sel T-supresor juga ikut berperan dalam pengaturan produksi antibodi
agar seimbang dan sesuai dengan kebutuhan. Antibodi yang terbentuk akan
berikatan dengan antigen membentuk kompleks antigen-antibodi yang akan
respon imun humoral juga terjadi respon primer yang membentuk populasi sel
B memory (Kresno, 2001).
2.4.2.3 Interaksi antara respon imun selular dengan respon imun humoral
Salah satu interaksi antara respon imun selular dengan respon imun
humoral adalah antibody dependent cell mediated cytotoxicity (ADCC). Pada
interaksi ini sitolisis terjadi dengan bantuan antibodi yang berfungsi melapisi
antigen sasaran (opsonisasi), sehingga sel natural killer (NK) yang mempunyai
reseptor pada fragmen Fc antibodi tersebut dapat melekat pada antigen sasaran
dan menghancurkan antigen tersebut (Kresno, 2001).
2.4.3 Imunomodulator
Imunomodulator adalah obat yang dapat mengembalikan dan
memperbaiki sistem imun yang fungsinya terganggu atau untuk menekan yang
fungsinya berlebihan. Obat golongan imunomodulator bekerja menurut 3 cara,
yaitu melalui:
- Imunosupresi
- Imunorestorasi
- Imunostimulasi
Imunorestorasi dan imunostimulasi disebut imunopotensiasi atau up
regulation, sedangkan imunosupresi disebut down regulation (Baratawidjaja,
2012).
A. Imunosupresi
Merupakan suatu tindakan untuk menekan respons imun. Kegunaannya
pada berbagai penyakit inflamasi yang menimbulkan kerusakan atau gejala
sistemik, seperti autoimun atau auto-inflamasi. Obat-obat imunosupresi
digunakan pada penderita yang akan menjalani transplantasi dan penyakit
autoimun oleh karena kemampuannya yang dapat menekan respon imun
seperti azatioprin, dan siklofosfamid (Baratawidjaja, 2012).
B. Imunorestorasi
Merupakan suatu cara untuk mengembalikan fungsi sistem imun yang
terganggu dengan memberikan berbagai komponen sistem imun, seperti:
immunoglobulin dalam bentuk Immune Serum Globulin (ISG), Hyperimmune
Serum Globulin (HSG), plasma, plasmapheresis, leukopheresis, transplantasi
sumsum tulang, hati dan timus (Baratawidjaja, 2012).
C. Imunostimulasi
Imunostimulasi yang disebut juga imunopotensiasi adalah cara
memperbaiki fungsi sistem imun dengan menggunakan bahan yang
merangsang sistem imun, seperti: levamisole, isoprenosin, hidroksiklorokin,
dan arginin (Baratawidjaja, 2012).
Salah satu obat yang dapat meningkatkan sistem kekebalan tubuh yaitu:
Levamisole
Levamisole HCl
N N
S H
Levamisole adalah derivate tetramizol, obat cacing yang dapat
meningkatkan proliferasi sitotoksisitas sel T serta mengembalikan anergi pada
beberapa penderita dengan kanker (imunostimulasi nonspesifik). Levamisol
dapat meningkatkan efek antigen, mitogen, limfokin, dan faktor kemotaktik
untuk merangsang limfosit, granulosit dan makrofag (Baratawidjaja, 2012)
Levamisole suatu obat imunomodulasi yang sedang diteliti untuk
menentukan kemanjurannya dalam berbagai kanker, penyakit autoimun,
infeksi bakteri menahun dan keratitis herpetika. Ia mempengaruhi pertahanan
hospes dengan mengatur respon imun seluler, termasuk fungsi leukosit
polimononuklear, makrofag dan sel T. Reaktivitas imun segera meningkat
setelah pemberian hanya satu dosis dan dianggap menetap beberapa hari
sampai beberapa bulan (Katzung, 1989).
2.5 Metode Pengujian Efek Imunomodulator
Ada beberapa metode yang digunakan dalam pengujian efek
imunomodulator. Beberapa di antaranya adalah uji respon hipersensitivitas tipe
lambat, pengukuran antibodi (titer antibodi), uji transformasi limfosit T, uji
komplemen, indeks migrasi makrofag, uji granulosit, bioluminisensi radikal,
respon fagositik, respon proliferasi limfosit.
2.5.1 Uji Respon Hipersensitivitas Tipe Lambat
Uji respon hipersensitivitas merupakan pengujian efek
imunomodulator terkait dengan respon imun spesifik. Respon
hipersensitivitas tipe lambat merupakan respon imun seluler yang
meningkatkan aktivitas makrofag sehingga dapat meningkatkan reaksi
inflamasi yang ditandai dengan pembengkakan kaki hewan uji
(Roit,1989).
2.5.2 Titer Antibodi
Respon imun spesifik dapat berupa respon imun seluler dan
respon imun humoral. Penilaian titer antibodi merupakan pengujian
terhadap respon imun humoral yang melibat pembentukan antibodi.
Peningkatan nilai titer antibodi terjadi karena peningkatan aktivitas sel
Th yang menstimulasi sel B untuk pembentukan antibodi dan
peningkatan aktivitas sel B dalam pembentukan antibodi (Roit, 1989).
BAB III
METODE PENELITIAN
Penelitian ini menggunakan metode eksperimental dengan tahapan
penelitian yaitu penyiapan sampel, skrining simplisia, karakterisasi simplisia,
pembuatan ekstrak, penyiapan hewan percobaan dan pengujian respon
hipersensitivitas tipe lambat dan titer antibodi pada hewan percobaan. Data
hasil penelitian dianalisis secara ANAVA (analisis variansi) dan dilanjutkan
dengan uji Post Hoc Tukey menggunakan program SPSS (Statistical Product
and Service Solution) versi 17.0.
3.1 Alat dan Bahan
3.1.1 Alat-alat
Alat-alat yang digunakan dalam penelitian ini adalah alat-alat gelas
laboratorium, aluminium foil, kertas saring, lampu spritus, lemari pengering,
mikroskop (Boeco), microtitration plate, microtube, mortir dan stamfer, neraca
hewan (Presica), neraca kasar, neraca listrik (Vibra), oral sonde, perkolator,
pipet mikro (Brand), pletismometer air raksa, rotary evaporator (Heidolph
VV-300), seperangkat alat destilasi penetapan kadar air, spuit 1 ml (Terumo), tanur,
dan velocity 18R refrigerated centrifuge (Dynamic). Gambar alat-alat yang
3.1.2 Bahan-bahan
Bahan-bahan yang digunakan dalam penelitian ini adalah daun
sambung nyawa, karboksi metil selulosa (CMC), sel darah merah sapi
(SDMS), levamisole, larutan fisiologis, etanol 96%, toluen, kloroform, besi
(III) klorida 1%, Bouchardat, Dragendorff, Mayer, Molish, asam klorida 2 N,
asam sulfat 2 N, kloralhidrat, natrium hidroksida 2 N, Liebermann-Bouchard,
timbal (II) asetat 0,4 M, heparin, dan air suling.
3.2 Hewan Percobaan
Hewan percobaan yang digunakan dalam penelitian adalah mencit
jantan dengan berat badan 20-35 gram berumur 2-3 bulan. Sebelum
digunakan, mencit dipelihara selama 2 minggu dalam kandang yang baik untuk
menyesuaikan diri dengan lingkungannya, dan diberi makan pelet hewan serta
air. Gambar hewan percobaan dapat dilihat pada Lampiran 7, halaman 68.
3.3 Pembuatan Larutan Pereaksi
Pembuatan larutan pereaksi terdiri dari asam klorida 2N, asam sulfat
2N, besi (III) klorida 1%, Bouchardat, Dragendorff, kloralhidrat, Mayer,
Molish, natrium hidroksida 2N dan timbal (II) asetat 0,4M (Depkes RI,1995).
Liebermann-Burchard menurut Harborne (1987).
3.3.1 Besi (III) klorida 1%
Sebanyak 1 g besi (III) klorida dilarutkan dalam air suling hingga 100
3.3.2 Bouchardat
Sebanyak 4 g kalium iodida ditimbang, kemudian dilarutkan dalam air
suling, ditambahkan iodium sebanyak 2 g dan dicukupkan dengan air suling
hingga 100 ml.
3.3.3 Dragendorff
Sebanyak 0,85 g bismut (III) nitrat ditimbang, kemudian dilarutkan
dalam 100 ml asam asetat glasial ditambahkan 40 ml air suling. Kemudian
pada wadah lain ditimbang 8 g kalium iodida lalu dilarutkan dalam 20 ml air
suling, lalu dicampurkan kedua larutan sama banyak. Kemudian ditambahkan
20 ml asam asetat glasial dan diencerkan dengan air suling hingga 100 ml.
3.3.4 Mayer
Sebanyak 1,35 g raksa (II) klorida dilarutkan dalam 60 ml air suling.
Kemudian pada wadah lain sebanyak 5 g kalium iodida dilarutkan dalam 10
ml air lalu dicampurkan keduanya dan ditambahkan air suling hingga 100 ml.
3.3.5 Molish
Sebanyak 3 g α-naftol ditimbang, kemudian dilarutkan dalam asam
nitrat 0,5 N hingga volume 100 ml.
3.3.6 Asam klorida 2 N
Sebanyak 7,3 ml asam klorida pekat dilarutkan dalam air suling hingga
volume 100 ml.
3.3.7 Asam sulfat 2 N
Sebanyak 9,8 ml asam sulfat pekat kemudian diencerkan dengan air
3.3.8 Natrium hidroksida 2 N
Sebanyak 8,002 g kristal natrium hidroksida dilarutkan dalam air suling
hingga 100 ml.
3.3.9 Kloralhidrat
Sebanyak 50 g kloralhidrat dilarutkan dalam 20 ml air.
3.3.10 Liebermann-Bouchard
Sebanyak 5 ml asam asetat anhidrida dicampurkan dengan 5 ml asam
sulfat pekat kemudian ditambahkan etanol hingga 50 ml
3.3.11 Timbal (II) asetat 0,4 M
Sebanyak 15,17 g timbal (II) asetat dilarutkan dalam air bebas
karbondioksida hingga 100 ml.
3.4 Prosedur Pembuatan Simplisia
3.4.1 Pengambilan Bahan
Pengumpulan sampel dilakukan secara purposif yaitu tanpa
membandingkan dengan tumbuhan yang sama dari daerah lain. Sampel yang
digunakan adalah daun sambung nyawa. Daun yang digunakan adalah daun tua
yang belum menguning maksimum pada daun ke-8 dari pucuk (Winarto,
2003). Sampel diambil dari Jl. Penghasilan Dalam, Kota Berastagi, Kabupaten
Karo, Sumatera Utara.
3.4.2 Identifikasi Tumbuhan
Identifikasi tumbuhan dilakukan di Herbarium Bogoriense, Bidang
Botani Pusat Penelitian Biologi LIPI-Bogor. Hasil identifikasi sampel dapat
3.5Karakteristik Simplisia
3.5.1 Pemeriksaan makroskopik
Pemeriksaan makroskopik dan organoleptik dilakukan dengan
mengamati bentuk, warna, bau dan rasa dari simplisia daun sambung nyawa
dan daun sambung nyawa segar. Gambar makroskopik dapat dilihat pada
Lampiran 2, halaman 56-57.
3.5.2 Pemeriksaan mikroskopik
Pemeriksaan mikroskopik dilakukan terhadap daun segar dengan cara
memotong tipis secara melintang diatas kaca preparat lalu diteteskan larutan
kloralhidrat dan dipanaskan diatas api bunsen kemudian ditutup dengan kaca
penutup dan diamati di bawah mikroskop. Gambar mikroskopik dapat dilihat
pada Lampiran 3, halaman 58-59.
Pemeriksaan mikroskopik dilakukan terhadap serbuk simplisia dengan
cara menaburkan serbuk simplisia di atas kaca objek yang telah ditetesi dengan
kloralhidrat kemudian ditutup dengan kaca penutup setelah itu dilihat dibawah
mikroskop.
3.5.3 Penetapan kadar air
Penetapan kadar air dilakukan dengan metode azeotropi (destilasi
toluen). Cara penetapan: ke dalam labu alas bulat dimasukkan 200 ml toluena
dan 2 ml aquades, didestilasi selama 2 jam. Setelah toluena didinginkan dan
volume air pada tabung penerima dibaca. Kemudian kedalam labu dimasukkan
5 g serbuk simplisia yang telah ditimbang seksama, dipanaskan hati – hati
lebih 2 tetes tiap detik, hingga sebagian air tersuling, kemudian naikkan
kecepatan penyulingan hingga 4 tetes tiap detik. Setelah semua tersuling,
bagian dalam pendingin dibilas dengan toluena yang telah jenuh. Penyulingan
dilanjutkan selama 5 menit, kemudian tabung penerima dibiarkan mendingin
sampai suhu kamar. Setelah air dan toluena memisah sempurna, volume
dibaca. Selisih kedua volume air dibaca sesuai dengan kandungan air yang
terdapat dalam bahan yang diperiksa (WHO, 1992). Perhitungan penetapan
kadar air dapat dilihat pada Lampiran 4, halaman 60.
3.5.4 Penetapan kadar sari larut dalam air
Sebanyak 5 g serbuk dimaserasi selama 24 jam dalam 100 ml
air-kloroform (2,5 ml air-kloroform dalam akuades sampai 1 liter) dengan
menggunakan botol bersumbat warna coklat sambil sekali-kali dikocok selama
6 jam pertama, kemudian dibiarkan selama 18-24 jam dan disaring, sejumlah
20 ml filtrat pertama diuapkan hingga kering dalam cawan yang telah
dipanaskan dan ditara. Residu dipanaskan dalam oven pada suhu 105ºC sampai
diperoleh bobot tetap. Kadar sari yang larut dalam air dihitung terhadap bahan
yang telah dikeringkan diudara (Depkes, 1989). Perhitungan penetapan kadar
sari yang larut air dapat dilihat pada Lampiran 4, halaman 61.
3.5.5 Penetapan kadar sari larut dalam etanol
Sebanyak 5 g serbuk dimaserasi selama 24 jam dalam 100 ml etanol
96% dengan menggunakan botol bersumbat berwarna coklat sambil sekali-kali
dikocok selama 6 jam pertama, kemudian dibiarkan selama 18-24 jam dan
yang telah dipanaskan dan ditara. Residu dipanaskan dalam oven pada suhu
105ºC sampai diperoleh bobot tetap. Kadar sari larut dalam etanol dihitung
terhadap bahan yang telah dikeringkan diudara (Depkes, 1989). Perhitungan
penetapan kadar sari yang larut etanol dapat dilihat pada Lampiran 4, halaman
62.
3.5.6 Penetapan kadar abu total
Lebih kurang 2 g zat yang telah digerus dan ditimbang seksama,
dimasukkan kedalam krus porselin yang telah dipijar dan ditara, kemudian
diratakan. Krus porselen bersama isinya dipijarkan perlahan–lahan hingga
arang habis, didinginkan, ditimbang sampai diperoleh bobot yang tetap. Kadar
abu dihitung terhadap bahan yang telah dikeringkan diudara (Depkes, 1989).
Perhitungan penetapan kadar abu total dapat dilihat pada Lampiran 4, halaman
63.
3.5.7 Penetapan kadar abu yang tidak larut dalam asam
Abu yang diperoleh pada penetapan kadar abu total dididihkan dengan
25 ml asam klorida encer selama 5 menit, dikumpulkan bagian yang tidak larut
dalam asam, disaring dengan kertas saring, lalu dicuci dengan air panas.
Kemudian residu dan kertas saring dipijarkan sampai diperoleh bobot tetap,
didinginkan dan ditimbang beratnya. Kadar abu yang tidak larut dalam asam
dihitung terhadap bahan yang telah dikeringkan diudara (Depkes, 1989).
Perhitungan penetapan kadar abu yang tidak larut dalam asam dapat dilihat
3.6 Skrining Fitokimia
Skrining fitokimia serbuk simplisia meliputi pemeriksaan senyawa
golongan flavonoid, alkaloid, saponin, tanin, glikosida, steroid/triterpenoid,
dan antrakinon.
3.6.1 Pemeriksaan Flavonoid
Serbuk simplisia ditimbang 0,5 g, lalu ditambahkan 10 ml metanol,
direfluks selama 10 menit, disaring panas-panas dengan kertas saring. Filtrat
diencerkan dengan 10 ml air suling, setelah dingin ditambahkan 5 ml
petroleum eter, dikocok hati-hati, lalu didiamkan sebentar. Lapisan metanol
diambil, diuapkan pada temperatur 40ºC, sisanya dilarutkan dalam 5 ml etil
asetat, disaring. Filtratnya digunakan untuk uji flavonoid dengan cara berikut:
sebanyak 1 ml filtrat diuapkan sampai kering, sisa dilarutkan dalam 1-2 ml
etanol 96%, lalu ditambah 0,1 g serbuk Mg dan 10 tetes asam klorida pekat.
Jika terjadi warna merah jingga sampai warna merah unggu menunjukkan
adanya flavonoid. Jika terjadi warna kuning jingga menunjukkan adanya
flavon, kalkon dan auron (Depkes,1995).
3.6.2 Pemeriksaan Alkaloid
Serbuk simplisia ditimbang sebanyak 0,5 g kemudian ditambahkan 1
ml asam klorida 2 N dan 9 ml air suling, dipanaskan diatas penangas air selama
2 menit, didinginkan dan disaring. Filtrat yang diperoleh dipakai untuk tes
alkaloid. Diambil 3 tabung reaksi, lalu ke dalamnya dimasukkan 0,5 ml filtrat.
a. ditambahkan 2 tetes pereaksi Mayer
b. ditambahkan 2 tetes pereaksi Bouchardat
c. ditambahkan 2 tetes pereaksi Dragendorff
Alkaloid positif jika terjadi endapan atau kekeruhan pada dua dari tiga
percobaan diatas (Depkes, 1995).
3.6.3 Pemeriksaan saponin
Sebanyak 0,5 g serbuk simplisia dimasukkan ke dalam tabung reaksi,
ditambahkan 10 ml air panas, didinginkan kemudian dikocok kuat-kuat selama
10 detik, jika terbentuk buih yang mantap setinggi 1-10 cm yang stabil tidak
kurang dari 10 menit dan tidak hilang dengan penambahan 1 tetes asam klorida
2 N menunjukkan adanya saponin (Depkes, 1989).
3.6.4 Pemeriksaan tanin
Sebanyak 0,5 g serbuk simplisia disari dengan 10 ml air suling lalu
disaring, filtratnya diencerkan dengan air sampai tidak berwarna. Larutan
diambil 2 ml dan ditambahkan 1-2 tetes pereaksi besi (III) klorida 1%. Jika
terjadi warna biru atau hijau kehitaman menunjukkan adanya tanin (Depkes,
1989).
3.6.5 Pemeriksaan glikosida
Sebanyak 3 g serbuk simplisia ditimbang kemudian disari dengan 30 ml
campuran etanol 96% dengan air (7:3) dan 10 ml asam klorida 2 N, direfluks
selama 2 jam, didinginkan dan disaring. Diambil 20 ml filtrat ditambahkan 25
ml air suling dan 25 ml timbal (II) asetat 0,4 M, dikocok, didiamkan 5 menit
(2:3), dilakukan berulang sebanyak 3 kali. Pada kumpulan sari lapisan
isopropanolol diuapkan pada suhu tidak lebih dari 50ºC. Sisanya dilarutkan
dalam 2 ml metanol untuk larutan percobaan 0,1 ml larutan percobaan
diuapkan diatas penangas air, pada sisa ditambahkan 2 ml air dan 5 tetes
pereaksi Molish. Kemudian secara perlahan-lahan ditambahkan 2 ml asam
sulfat pekat melalui dinding tabung terbentuknya cincin berwarna ungu pada
batas kedua cairan menunjukkan adanya ikatan gula (Depkes, 1995).
3.6.6 Pemeriksaan steroida/triterpenoida
Sebanyak 1 g serbuk simplisia dimaserasi dengan 20 ml eter selama 2
jam, disaring, filtrat diuapkan dalam cawan penguap, dan pada sisanya
ditambahkan 20 tetes asam asetat anhidrat dan 1 tetes asam sulfat pekat
(pereaksi Liebermann-Burchard). Apabila terbentuk warna ungu atau merah
yang berubah menjadi biru hijau menunjukkan adanya steroida/triterpenoida
(Harborne, 1987).
3.6.7 Pemeriksaan antrakinon
Sebanyak 0,2 g serbuk simplisia ditimbang, dicampur dengan 5 ml
asam sulfat 2 N, dipanaskan sebentar, setelah dingin ditambahkan 10 ml
benzen, dikocok dan didiamkan. Lapisan benzen dipisahkan dan disaring,
kemudian kocok dengan 2 ml NaOH 2 N, didiamkan. Lapisan air berwarna
merah dan lapisan benzen tidak berwarna menunjukkan adanya antrakinon
3.7 Pembuatan Ekstrak Etanol Daun Sambung Nyawa
Sebanyak 500 gram serbuk simplisia dimasukkan kedalam bejana
tertutup, etanol 96% dituangkan ke dalam bejana sampai seluruh simplisia
terendam, diaduk, dibiarkan sekurang-kurangnya selama 3 jam. Dipindahkan
massa sedikit demi sedikit kedalam perkolator sambil tiap kali ditekan
hati-hati, dituangkan cairan penyari secukupnya sampai cairan mulai menetes dan
di atas simplisia masih terdapat selapis cairan penyari, ditutup perkolator,
dibiarkan selama 24 jam. Dibiarkan cairan menetes dengan kecepatan 1 ml per
menit, ditambahkan berulang-ulang cairan penyari secukupnya hingga selalu
terdapat selapis cairan penyari diatas simplisia. Perkolasi dihentikan setelah
tetesan terakhir perkolat tidak berwarna lagi atau apabila sebanyak 500 mg
cairan perkolat diuapkan di atas penangas air tidak meninggalkan sisa. Perkolat
yang diperoleh dipekatkan dengan alat penguap vakum putar (rotary
evaporator). Kemudian dikeringkan dengan menggunakan freeze dryer (Ditjen
POM, 1995).
3.8 Uji Efek Imunomodulator
Uji efek imunomodulator meliputi penyiapan hewan percobaan,
penyiapan kontrol, bahan uji, antigen, uji respon hipersensitivitas tipe lambat,
dan uji titer antibodi.
3.8.1 Penyiapan Hewan Percobaan
Hewan yang digunakan adalah mencit jantan dengan berat 20-35 g
dibagi 5 kelompok, 1 kelompok untuk kontrol negatif, 1 kelompok untuk
Sebelum digunakan sebagai hewan percobaan, semua mencit dipelihara
terlebih dahulu selama kurang lebih satu minggu dalam kandang yang baik
pada suhu ruangan untuk penyesuaian lingkungan, pengontrolan kesehatan dan
berat badan. Mencit diberi makan pelet hewan dan tetap diberi air minum.
3.8.2 Penyiapan Kontrol, Bahan Uji, dan Antigen
Penyiapan kontrol, bahan uji, dan antigen meliputi penyiapan CMC
1%, penyiapan suspensi levamisole, penyiapan suspensi ekstrak daun sambung
nyawa 2%, dan penyiapan sel darah merah sapi.
3.8.2.1 Penyiapan CMC Na 1%
Pembuatan suspensi CMC Na 1% (b/v) dilakukan dengan cara sebagai
berikut: sebanyak 1 g CMC Na ditaburkan kedalam lumpang yang berisi air
panas sebanyak 20 ml. Didiamkan selama 15 menit hingga diperoleh massa
yang transparan, digerus hingga berbentuk gel dan diencerkan dengan sedikit
air, kemudian dituang ke dalam labu tentukur 100 ml, ditambahkan air suling
sampai batas tanda.
3.8.2.2 Penyiapan Suspensi Levamisole
Pengambilan sampel tablet levamisole yaitu dengan cara ditimbang dan
diserbukhaluskan tidak kurang dari 20 tablet. Ditimbang serbuk yang telah
dihaluskan tersebut kemudian ditimbang seksama sejumlah serbuk setara
dengan lebih kurang 25 mg levamisole (Depkes, 1995).
Pembuatan suspensi levamisole dilakukan dengan cara sebagai berikut:
ditimbang serbuk levamisole 29,46 mg (setara dengan 25 mg levamisole) dan
CMC Na 1% secukupnya. Digerus hingga homogen dan dituangkan kedalam
labu tentukur 25 ml, dan kemudian ditambahkan suspensi CMC Na 1% sampai
batas tanda.
3.8.2.3 Penyiapan Suspensi Ekstrak Daun Sambung Nyawa (SEDSN) 2%
Pembuatan suspensi ekstrak daun sambung nyawa 2% (b/v) dilakukan
dengan cara sebagai berikut: sebanyak 500 mg ekstrak daun sambung nyawa
dimasukkan kedalam lumpang, ditambahkan suspensi CMC Na 1%
secukupnya kemudian digerus sampai homogen. Dituang ke dalam labu
tentukur 25 ml, ditambahkan suspensi CMC Na 1% sampai batas tanda.
3.8.2.4 Penyiapan Sel Darah Merah Sapi (SDMS)
Penyiapan dan pembuatan SDMS didasarkan pada penelitian yang
dilakukan oleh Yufri (2011). Darah segar dikumpulkan dari sapi yang
disembelih, diperoleh 500 ml. kemudian ditambahkan 1,5 ml heparin dan
dimasukan kedalam termos yang berisi es. Darah dicuci dengan larutan NaCl
fisiologis (1:1) masing-masing sebanyak 5 ml dan diaduk homogen kemudian
disentrifus dengan kecepatan 2000 rpm selama 15 menit, dibuang
supernatannya, diulangi 3 kali dengan menambahkan 5 ml NaCl fisiologis
setiap pengulangan. Setelah didapatkan eritrosit ditambahkan larutan NaCl
fisiologis dengan volume yang sama, hingga diperoleh SDMS 50%. Kemudian
diambil 0,2 ml SDMS 50%, ditambahkan larutan NaCl fisiologis hingga 10 ml,
3.8.3 Uji Respon Hipersensitivitas Tipe Lambat
Efek imunomodulator ekstrak daun sambung nyawa ditentukan dengan
mengukur volume respon hipersensitivitas tipe lambat menggunakan uji
pembengkakan telapak kaki hewan uji (foot paw swelling test) (Lakshmi, et al.,
2003; Ray, et al., 1996).
Sebanyak 30 ekor mencit dibagi menjadi 5 kelompok dengan
pembagian sebagai berikut:
a. Kelompok I diberi suspensi CMC Na 1% (b/v) sebagai kontrol negatif.
b. Kelompok II diberi Suspensi Ekstrak Daun Sambung Nyawa (SEDSN)
dengan dosis 125 mg/kg BB.
c. Kelompok III diberi SEDSN dengan dosis 250 mg/kg BB.
d. Kelompok IV diberi SEDSN dengan dosis 500 mg/kg BB
e. Kelompok V diberi Suspensi Levamisole dengan dosis 25 mg/kg BB
sebagai kontrol positif.
Tiap kelompok diinjeksikan dengan 0,1 ml sel darah merah sapi
(SDMS) 1% dalam dalam larutan NaCl fisiologis secara intraperitoneal pada
hari ke-0. Perlakuan dimulai dari hari ke-0 dan diberikan setiap hari selama 7
hari. Pada hari ke-7, sendi kaki mencit sebelah kanan diberi tanda batas
pengukuran volume kaki mencit. Volume kaki mencit diukur sebagai volume
awal (V0). Kemudian mencit diinjeksikan dengan 0,1 ml suspensi SDMS 1%
dalam dalam larutan NaCl fisiologis secara intraplantar pada telapak kaki
Pada hari kedelapan (setelah 24 jam) diukur volume pembengkakan
kaki mencit dengan pletismometer air raksa. Pengukuran dilakukan dengan
mencelupkan kaki mencit ke dalam tabung yang berisi air raksa sampai tanda
batas pengukuran. Perubahan volume air raksa terlihat pada kenaikan skala
pada pletismometer sebagai volume waktu tertentu (Vt) kaki mencit. Volume
pembengkakan kaki mencit ditentukan berdasarkan selisih antara volume
waktu tertentu (Vt) dengan volume awal (V0) (Shivaprasad, 2006).
3.8.4 Uji Titer Antibodi
Tiap kelompok diinjeksikan dengan 0,1 ml sel darah merah sapi
(SDMS) 1% dalam larutan NaCl fisiologis secara intraperitoneal pada hari
ke-0. Perlakuan dimulai dari hari ke-0 dan diberikan satu kali setiap hari selama 7
hari. Pada hari ke-7, sampel darah masing-masing mencit diambil melalui
pembuluh darah vena di bagian ekor. Sampel darah dikumpulkan dalam tabung
mikro (microtube), kemudian dilakukan pemusingan 1900 rpm dengan alat
sentrifugasi pada suhu 4C selama 10 menit dan diambil serumnya.
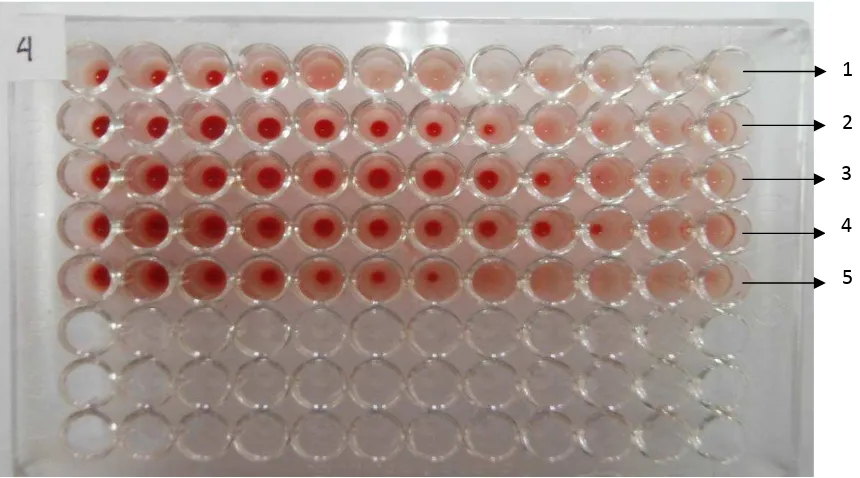
Nilai titer antibodi ditentukan dengan teknik hemaglutinasi. Duapuluh
lima mikroliter (25 μl) serum diteteskan ke dalam sumur microtitration plate
96 lubang, ditambahkan dalam larutan NaCl fisiologis dan SDMS dengan
volume yang sama, dan diencerkan dua kali lipat (1:2; 1:4; 1:8; 1:16; 1:32;
1:64; 1:128; 1:256; 1:512; 1:1024; 1:2048) kemudian diamati penggumpalan
yang terjadi (Makare, et al., 2001; Puri, et al., 1993). Nilai titer antibodi
ditentukan berdasarkan pengenceran terakhir dimana antibodi masih terdeteksi
selanjutnya ditransformasikan dengan [2log(titer)+1] (Hargono, 2000; Eldiza,
2011).
3.9 Analisis Data
Data hasil penelitian dianalisis dengan menggunakan program SPSS
versi 17.0. Data ditentukan homogenitas dan normalitasnya untuk menentukan
analisis statistik yang digunakan. Data dianalisis dengan menggunakan uji
ANAVA satu arah (One-Way ANOVA) untuk menentukan perbedaan rata-rata
di antara perlakuan. Jika terdapat perbedaan, dilanjutkan dengan menggunakan
uji Post Hoc Tukey untuk mengetahui variabel mana yang memiliki perbedaan.
Berdasarkan nilai signifikansi, P < 0,05 dianggap signifikan. Data hasil
statistik ANAVA satu arah (One-Way ANOVA) dapat dilihat pada Lampiran
BAB IV
HASIL DAN PEMBAHASAN
4.1 Simplisia dan Ekstrak
Tumbuhan yang digunakan telah diidentifikasi di Herbarium
Bogoriense, Bidang Botani Pusat Penelitian Biologi LIPI-Bogor. Hasil
identifikasi tumbuhan dapat dilihat pada Lampiran 1, halaman 55.
Hasil pemeriksaan organoleptik terhadap daun sambung nyawa segar
yaitu daun berwarna hijau, berbau aromatik, rasa kelat dan sedikit manis.
Sedangkan hasil pemeriksaan organoleptik simplisia daun sambung nyawa
adalah berwarna hijau pekat, berbau aromatik, dan rasa kelat. Hasil
pemeriksaan makroskopik terhadap daun sambung nyawa segar adalah daun
berwarna hijau, bertangkai, letaknya saling berhadapan dan bersilang, helaian
daun bulat telur dengan pangkal daun membulat dan ujung daun runcing,
pinggir daun bergerigi dangkal, panjang daun sampai 21 cm, lebar daun sampai
9 cm, kedua permukaan daun berambut halus dengan pertulangan menyirip.
Hasil pemeriksaan makroskopik dapat dilihat pada Lampiran 2, halaman
56-57.
Hasil pemeriksaan mikroskopik penampang melintang pada daun
sambung nyawa segar yaitu adanya: sel kelenjar, trakea, kutikula, epidermis
atas, jaringan palisade, jaringan bunga karang (spons), epidermis bawah dan
rambut penutup. Hasil pemeriksaan mikroskopik serbuk simplisia pada daun
mesofil, dan stomata. Hasil pemeriksaan mikroskopik dapat dilihat pada
Lampiran 3, halaman 58-59.
Hasil pemeriksaan karakteristik simplisia daun sambung nyawa
diperoleh kadar air 9,2%, kadar sari yang larut dalam air 23,67%, kadar sari
yang larut dalam etanol 13,64%, kadar abu total 6,39% dan kadar abu yang
tidak larut dalam asam 0,62%. Persyaratan umum pada Farmakope Herbal
adalah kadar air tidak lebih dari 10%, kadar sari yang larut dalam air tidak
kurang dari 7,9%, kadar sari yang larut dalam etanol tidak kurang dari 3,9%,
kadar abu tidak lebih dari 7,2%, dan kadar abu yang tidak larut dalam asam
tidak lebih dari 1,2%. Dengan demikian hasil penetapan kadar air, kadar sari
yang larut dalam etanol, kadar abu total, kadar abu yang tidak larut asam dan
kadar air memenuhi persyaratan pada Farmakope Herbal (2010). Data hasil
pemeriksaan karakteristik simplisia ditunjukkan pada Tabel 4.1.
Tabel 4.1 Hasil Pemeriksaan Karakteristik Simplisia
No. Penetapan / Karakteristik Simplisia
5 Kadar abu tidak larut dalam
asam 0,62 < 1,2
Pemeriksaan skrining fitokimia serbuk simplisia daun sambung nyawa
yang dilakukan untuk mengetahui adanya kandungan alkaloida, glikosida,
Tabel 4.2 Hasil Pemeriksaan Skrining Simplisia
No Senyawa Serbuk simplisia
1 Alkaloida -
2 Glikosida +
3 Saponin +
4 Flavonoid +
5 Tanin +
6 Steroid/Triterpenoid +
Keterangan :
+ = Mengandung golongan senyawa - = Tidak mengandung golongan senyawa
Berdasarkan hasil pemeriksaan skrining fitokimia terhadap serbuk
simplisia daun sambung nyawa terdapat kandungan senyawa kimia golongan
alkaloida, glikosida, saponin, flavonoid, tanin, dan steroida/triterpenoida.
Standarisasi diperlukan karena kandungan bahan aktif yang terkandung dalam
jenis tanaman yang sama dapat bervariasi, dengan standarisasi diharapkan
bahan aktif yang terkandung di dalam bahan baku tersebut cukup konsisten,
sehingga takaran yang digunakan untuk pengujian memiliki kandungan aktif
yang setara.
Hasil penyarian 500 g serbuk simplisia daun sambung nyawa dengan
pelarut etanol 96% diperoleh ekstrak kental yang kemudian diuapkan dengan
menggunakan rotary evaporator dan dikeringkan, diperoleh 98,32 g ekstrak
4.2 Pengujian Efek Imunomodulator
Pengujian efek imunomodulator ekstrak daun sambung nyawa
dilakukan dengan metode respon hipersensitivitas tipe lambat dan titer antibodi
yang digunakan untuk melihat pengaruh ekstrak terhadap aktivitas dan
mekanisme sistem imun humoral yang melibatkan sel T dan sel B. Menurut
Makare, et al., (2001), kombinasi kedua metode tersebut mempunyai
keuntungan yaitu memungkinkan dua komponen respon imun diukur pada
spesies yang sama dibawah kondisi ideal, relatif sederhana dan tidak mahal.
Penentuan dosis dilakukan dengan orientasi dari dosis 50 mg/kg bb
hingga 1 g/kg bb. Dari orientasi yang dilakukan diperoleh bahwa dosis 125
mg/kg bb, 250 mg/kg bb, dan 500 mg/kg bb sudah memberikan efek yg lebih
dari normal dan pembanding. Pembanding yang digunakan ialah levamisole
dengan dosis 25 mg/kg bb. Dosis levamisole tertinggi yang dapat digunakan
tinggi pada mencit ialah 25 mg/kg bb (Katzung, 1989). Data hasil penelitian
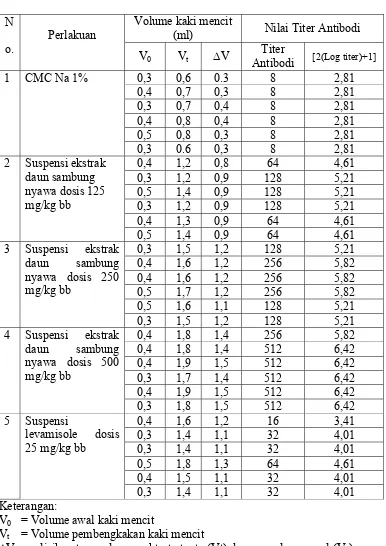
Tabel 4.3 Volume Pembengkakan Kaki Mencit dan Nilai Titer Antibodi
N
o.
Perlakuan
Volume kaki mencit
(ml) Nilai Titer Antibodi
V0 Vt ∆V
Titer
Antibodi [2(Log titer)+1]
1 CMC Na 1% 0,3 0,6 0.3 8 2,81
2 Suspensi ekstrak
daun sambung nyawa dosis 125 mg/kg bb
3 Suspensi ekstrak daun sambung nyawa dosis 250 mg/kg bb
4 Suspensi ekstrak daun sambung nyawa dosis 500 mg/kg bb
Vt = Volume pembengkakan kaki mencit
4.2.1 Respon Hipersensitivitas Tipe Lambat
Respon hipersensitivitas tipe lambat dikenali dengan reaksi
imuno-inflamasi karena makrofag dan sel T helper (Th1) berperan besar dalam proses
tersebut (Mukherjee, 2010). Reaksi ini ditandai dengan adanya pembengkakan
pada tempat terjadinya induksi antigen.
Pembengkakan terkait langsung dengan cell mediated immunity (CMI),
karena antigen mengaktivasi sel T terutama sel Th1. Aktivasi sel T
menyebabkan pelepasan beberapa sitokin yang bersifat proinflamasi. Sitokin
tersebut akan menarik makrofag ke tempat terjadinya induksi dan
mengaktivasinya sehingga menyebabkan peningkatan aktivitas fagositik untuk
melawan antigen yang masuk (Fulzele, et al., 2002). Penarikan makrofag ini
terjadinya pembengkakan. Semakin besar pembengkakan menunjukkan
semakin tinggi respon hipersensitivitas tipe lambat sehingga dapat
menggambarkan peningkatan aktivitas sistem imun.
Pengujian dilakukan dengan cara menginduksi mencit dengan sel darah
merah sapi (SDMS) sebagai antigen secara intraperitoneal pada hari ke-0.
Respon hipersensitivitas tipe lambat diketahui dari volume pembengkakan kaki
mencit yang diukur pada hari ke-8. Setelah sehari sebelumnya mencit diberi
tanda batas pengukuran volume kaki mencit pada sendi kaki mencit sebelah
kanan, volume kaki mencit diukur sebagai volume awal (V0). Kemudian
mencit diinjeksikan dengan 0,1 ml suspensi SDMS 1% dalam dalam larutan
NaCl fisiologis secara intraplantar pada telapak kaki sebelah kanan.