EKSPRESI VASCULAR ENDOTHELIAL GROWTH
FACTOR PADA KARSINOMA NASOFARING
Tesis
Diajukan untuk Melengkapi Tugas dan Memenuhi Salah Satu Syarat untuk Mencapai Spesialis dalam Bidang
Ilmu Kesehatan Telinga Hidung Tenggorok Bedah Kepala Leher
Oleh
M. PAHALA HANAFI HARAHAP
PROGRAM PENDIDIKAN DOKTER SPESIALIS BIDANG ILMU KESEHATAN TELINGA HIDUNG TENGGOROK
BEDAH KEPALA LEHER FAKULTAS KEDOKTERAN UNIVERSITAS SUMATERA UTARA
KATA PENGANTAR
Puji dan syukur kehadirat Allah Subhanahu Wata’ala atas rahmat, karunia dan
hidayahNya, sehingga penulis dapat menyelesaikan tesis ini sebagai salah satu tugas
akhir dalam menyelesaikan pendidikan spesialis dalam bidang Ilmu Kesehatan Telinga
Hidung Tenggorok Bedah Kepala Leher Fakultas Kedokteran Universitas Sumatera
Utara/RSUP H. Adam Malik Medan.
Berkat dukungan dan bimbingan dari berbagai pihak, akhirnya tesis ini dapat
diselesaikan. Untuk itu perkenankanlah penulis menyampaikan ucapan terima kasih dan
penghargaan yang setinggi-tingginya kepada :
Rektor Universitas Sumatera Utara, Bapak Prof. Chairuddin Panusunan Lubis, dr,
Sp.A (K), DTM&H, yang telah memberikan kesempatan kepada penulis untuk mengikuti
Program Pendidikan Dokter Spesialis di Departemen THT-KL Fakultas Kedokteran
Sumatera Utara.
Bapak Dekan Fakultas Kedokteran Universitas Sumatera Utara Prof. Gontar
Alamsyah, dr, Sp.PD-KGEH dan mantan dekan Prof. Sutomo Kasiman, dr, Sp.JP (K)
dan Prof. T. Bahri Anwar, dr, Sp.JP (K) yang telah memberikan kesempatan kepada
penulis untuk mengikuti Program Pendidikan di Fakultas Kedokteran Universitas
Sumatera Utara.
Bapak Direktur Rumah Sakit Umum Pusat H. Adam Malik Medan yang telah
memberikan kesempatan kepada penulis untuk belajar dan bekerja di Rumah Sakit ini.
Prof. Abdul Rachman Saragih, dr, Sp.THT-KL (K) sebagai Kepala Departemen
bimbingan dan arahan sejak penulis mengikuti pendidikan di Departemen THT-KL FK
USU/RSUP H. Adam Malik Medan.
Prof. Askaroellah Aboet, dr, Sp.THT-KL (K) sebagai Ketua Program Studi
Pendidikan Dokter Spesialis di Departemen THT-KL FK USU/RSUP H. Adam Malik
Medan atas bimbingan, arahan, dorongan dan nasehat selama penulis mengikuti
pendidikan di Departemen THT-KL FK USU/RSUP H. Adam Malik Medan.
Dr. dr. Delfitri Munir, Sp.THT-KL (K) sebagai pembimbing utama tesis, Prof.
Ramsi Lutan, dr. Sp.THT-KL (K) dan dr. Farhat, Sp.THT-KL sebagai pembimbing
pendamping tesis, yang telah banyak memberikan waktu, bimbingan, arahan dan
motivasi sehingga penulis dapat menyelesaikan tesis ini.
Ucapan terima kasih yang sebesar-besarnya saya tujukan kepada semua
guru-guru di Departemen THT-KL FK USU/RSUP H. Adam Malik Medan, dr. Asroel Aboet,
Sp.THT-KL (K), Prof. Ramsi Lutan, dr. Sp.THT-KL (K), dr. Yuritna Haryono, Sp.THT-KL
(K), Prof. Askaroellah Aboet, dr, Sp.THT-KL (K), Prof. Abdul Rachman Saragih, dr,
KL (K), Dr. Muzakkir Zamzam, KL (K), dr. Mangain Hasibuan,
Sp.THT-KL, dr. T. Sofia Hanum, Sp.THT-KL (K), Dr. dr. Delfitri Munir, Sp.THT-KL (K), dr. Linda I
Adenin, Sp.THT-KL, dr. Hafni, Sp.THT-KL (K), dr. Ida Sjailendrawati H, Sp.THT-KL, dr.
Adlin Adnan, KL, dr. Rizalina A. Asnir, KL, dr. Ainul Mardhiah,
Sp.THT-KL, dr. Siti Nursiah, Sp.THT-Sp.THT-KL, dr. Andrina YM Rambe, Sp.THT-Sp.THT-KL, dr. Harry Agustaf
A, Sp.THT-KL, dr. Farhat, Sp.THT-KL, dr. T. Siti Hajar Haryuna, Sp.THT-KL, dr. Aliandri,
Sp.THT-KL dan dr. Ashri Yudhistira, Sp.THT-KL yang telah memberikan bimbingan, ilmu
Yang terhormat Prof. H. M. Nadjib Dahlan Lubis, dr, Sp. PA(K), para staf
Departemen Patologi Anatomi FK USU/RSUP H. Adam Malik Medan yang telah banyak
membantu, memberikan masukan, perhatian dan bimbingan di bidang patologi anatomi
terutama mengenai pemeriksaan imunohistokimia dalam penulisan tesis ini.
Yang terhormat dr. Arlinda Sari Wahyuni, M.Kes, staf Departemen Ilmu
Kesehatan Masyarakat / Ilmu Kedokteran Komunitas yang telah banyak membantu saya
di bidang statistik dalam pengolahan data tesis ini.
Bapak Kepala Departemen/Staf Radiologi FK USU/RSUP H. Adam Malik Medan,
Kepala Departemen/Staf Anastesiologi dan Reanimasi FK USU/RSUP H. Adam Malik
Medan, Kepala Departemen/Staf Patologi Anatomi FK USU/RSUP H. Adam Malik
Medan yang telah memberikan bimbingan kepada penulis selama menjalani stase
pendidikan di Departemen tersebut.
Direktur dan seluruh staf THT-KL RSUD Lubuk Pakam, RS PTP XI Tembakau
Deli Medan, Rumah Sakit DAM-I/Bukit Barisan Medan dan RSU Dr. Pirngadi Medan,
yang telah memberikan kesempatan dan bimbingan kepada penulis untuk belajar
selama pendidikan di rumah sakit tersebut.
Kedua orangtua tercinta, Ibunda Salismi dan ayahanda dr. Amran Harahap, serta
kakak dan adik penulis mengucapkan terima kasih atas limpahan kasih sayang dan tak
henti-hentinya memberikan dorongan serta doa kepada penulis.
Istriku Ns. Cholina Trisa Siregar MKep. Sp. KMB terima kasih atas dukungan dan
perhatiannya sehingga penulis dapat menyelesaikan tesis ini. Ananda M. Faiz Zuhairi
Teman-teman sejawat peserta pendidikan Ilmu Kesehatan THT Bedah Kepala
Leher terima kasih atas persahabatan dan kerjasama yang terjalin selama mengikuti
pendidikan.
Paramedis dan karyawan Departemen THT Bedah Kepala Leher FK USU/RSUP
H. Adam Malik Medan yang telah membantu dan bekerja sama selama penulis
menjalani pendidikan.
Semoga segala bantuan dan bimbingan yang diberikan kepada penulis menjadi
amal ibadah. Akhirnya penulis berharap semoga tulisan ini dapat bermanfaat bagi
semua pihak, dan semoga Allah Subhanahu Wata’ala selalu melimpahkan rahmat dan
hidayahNya kepada kita semua.
Medan, Maret 2009
Ekspresi Vascular Endothelial Growth Factor Pada Karsinoma Nasofaring
Abstrak
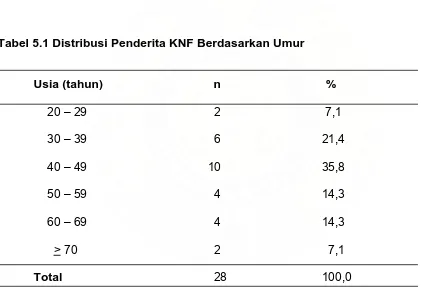
Latar Belakang : Karsinoma Nasofaring (KNF) adalah tumor ganas yang cenderung didiagnosa pada stadium lanjut, sehingga angka survival rendah dan prognosis
penderita jelek. Salah satu faktor yang diduga berperan dalam progresivitas tumor dan
metastase tumor adalah overekspresi vascular endothelial growth factor (VEGF) yang
berperan penting dalam proses angiogenesis tumor. Penelitian ini dilakukan untuk
melihat ekspresi VEGF pada KNF, serta melihat hubungan ekspresi VEGF dengan
stadium dan jenis histopatologi KNF.
Metode Penelitian : Penelitian dilakukan dengan studi potong lintang (cross sectional study) di Departemen THT-KL FK USU / RSUP H. Adam Malik Medan, secara non
probability consecutive sampling mulai Maret 2008. Terhadap penderita KNF dilakukan
pemeriksaan histopatologi dan imunohistokimia dari jaringan nasofaring yang diperoleh
dari biopsi. Ekspresi VEGF dinilai pada sitoplasma yang terwarnai merah kecoklatan .
Data dianalisa dengan uji korelasi Spearman dan uji chi square dengan batas
kebermaknaan p < 0,05.
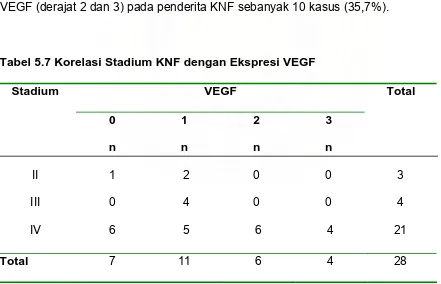
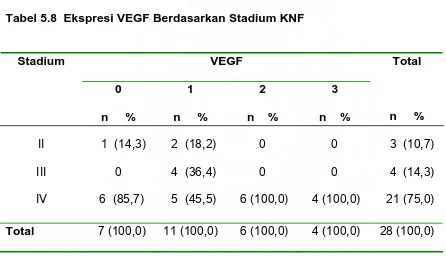
Hasil Penelitian : Sebanyak 21 dari 28 kasus KNF (75,0%) memiliki ekspresi VEGF positif. Overekspresi VEGF dijumpai pada 10 dari 28 kasus KNF (35,7%). Tidak dijumpai
korelasi yang bermakna antara stadium tumor dengan ekspresi VEGF pada KNF (p >
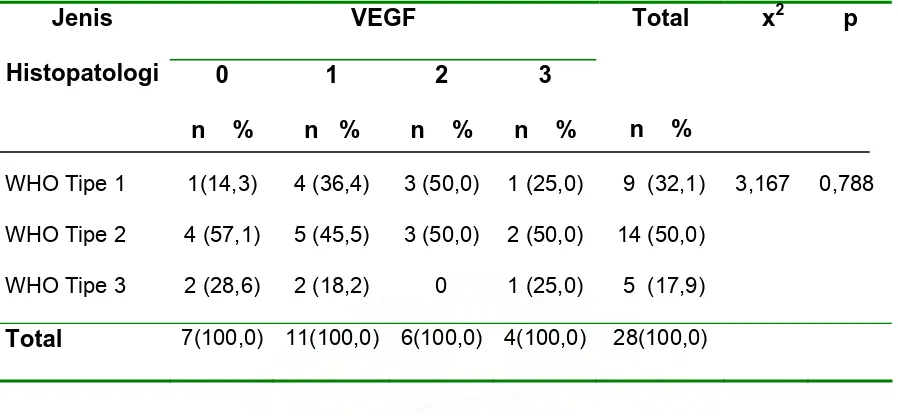
0,05). Tidak dijumpai hubungan yang bermakna antara jenis histopatologi dengan
Kesimpulan : Ekspresi VEGF cukup tinggi pada penderita KNF. Kemungkinan VEGF berperan dalam proses angiogenesis pada KNF.
Kata Kunci : KNF, VEGF, stadium, histopatologi
Abstract
Background : Nasopharyngeal Carcinoma (NPC) is a malignancy that tend to diagnosed at advanced stage with low survival and prognosis rate. One of the factor that
may play a role in progresivity and metastasis of tumour is overexpression of vascular
endothelial growth factor (VEGF) which is a key role in tumour angiogenesis. The aim of
this study is to learn the expression of VEGF in NPC, and to learn the association of
VEGF expression with tumour stage and histopathologic type of NPC.
Study design and methods : This is a cross sectional study performed in ENT-HNS Department of Medical School of University of North Sumatera / H. Adam Malik Hospital.
Sample was collected by non probability consecutive sampling, starting from March
2008. NPC patients underwent histophatologic examination and immunohistochemical
analysis from nasopharyngeal biopsy. VEGF expression analysed by red-brown stained
cytoplasm. Data was analysed by Spearman’s correlation test and chi square test.
Results : VEGF positive expression was found in 21 of 28 (75.0%) NPC cases. VEGF overexpression was found in 10 of 28 (35.7%) NPC cases. No significance correlation
found between tumour stage and VEGF expression (p > 0.05). No significance
Conclusions : VEGF expression is relatively high in NPC patient. VEGF may play a role in the angiogenesis of NPC.
BAB 4 : METODE PENELITIAN ... ……… 55
4.3.1. Klasifikasi Variabel Penelitian... 57
4.3.2. Definisi Operasional Variabel... . 57
4.4. Bahan Penelitian ... 58
Lampiran 1. Data Sampel Penelitian ... ... 87
Lampiran 2. Status Penelitian ... 88
Lampiran 3. Lembar Penjelasan Kepada Subyek Penelitian... 92
Lampiran 4. Lembar Persetujuan Setelah Penjelasan... 94
Lampiran 5. Persetujuan Komite Etik Penelitian ... 95
BAB 1 PENDAHULUAN
1.1 Latar Belakang
Karsinoma Nasofaring (KNF) adalah tumor ganas yang berasal dari sel epitel
yang melapisi nasofaring, tidak termasuk tumor kelenjar atau limfoma (Wei dan Sham,
2005; Brennan, 2006). Di Indonesia KNF merupakan tumor ganas kepala dan leher
yang paling banyak ditemukan. Menurut data patologi tahun 1990 KNF menduduki
urutan ke-4 dari seluruh keganasan setelah kanker mulut rahim, payudara dan kulit.
Prevalensi penderita KNF 4,7 orang per 100.000 penduduk pertahun yang diambil dari
data resmi Departemen Kesehatan tahun 1980 (Roezin, 1995). Penelitian Fachiroh di
Yogyakarta menyatakan insiden penderita KNF 3,9 orang per 100.000 penduduk
(Fachiroh et al. 2004). Di Bagian THT FK-UI RSCM selama periode 1988-1992 didapati
511 penderita baru KNF (Roezin, 1995). Di RSUP H. Adam Malik Medan pada tahun
1998-2000 ditemukan 130 penderita KNF dari 1370 pasien baru onkologi kepala dan
leher (Lutan, 2003). Sementara pada periode 1 Juli 2005 – 30 Juni 2006 ditemukan 79
orang penderita baru KNF (Aliandri, 2007).
Diagnosis dini sangat menentukan prognosis penderita. Hal ini sukar dicapai
karena nasofaring tersembunyi di belakang tabir langit-langit dan terletak di bawah
dasar tengkorak serta berhubungan dengan banyak daerah penting di dalam tengkorak
maupun leher (Roezin, 1995). Diagnosis dini yaitu menemukan kasus KNF pada
stadium I dan II, dimana belum terjadi metastase regional. Keadaan ini sangat sulit
Indonesia dan di luar negeri, kasus dini hanya ditemukan antara 3,8%-13,9%,
dibandingkan dengan kasus lanjut (stadium III dan IV) sekitar 88,1%-96,2% (Soetjipto,
1993). Di RSUP HAM periode Juli 2005-Juni 2006 dari 79 penderita KNF seluruhnya
berada pada stadium lanjut, tidak dijumpai penderita dengan stadium dini (Aliandri,
2007).
Radioterapi tetap merupakan modalitas terapi primer terhadap KNF (Cottrill dan
Nutting, 2005; Wei dan Sham, 2005). Penderita dengan stadium I dan II mempunyai
angka kesembuhan tinggi dengan pemberian radioterapi saja, dimana prognosis bagi
penderita dengan metastase jauh masih buruk. Bagi penderita dengan stadium III dan
IV, peran pembedahan terbatas dan pemberian radioterapi yang dikombinasikan
dengan kemoterapi telah menjadi standar terapi (Agulnik dan Siu, 2005). Akan tetapi,
regimen obat kemoterapi yang optimal untuk dikombinasikan dengan radioterapi masih
kontroversial. Beberapa studi random telah dilakukan untuk mengevaluasi pemberian
kemoterapi neoadjuvan, concurrent dan adjuvan dalam berbagai kombinasi dengan
radioterapi (Cottrill dan Nutting, 2003; Agulnik dan Siu, 2005).
Kanker yang kecil pada KNF memiliki angka survival yang tinggi dengan
pemberian radioterapi dan kemoterapi sekitar 80%-90%. Lesi yang lebih luas tanpa
penyebaran ke kelenjar limfe leher sering dapat disembuhkan dengan angka survival
50%-70%. Penderita dengan lesi lanjut, terutama dengan penyebaran ke kelenjar limfe
leher, keterlibatan syaraf kranial dan destruksi tulang, sulit dilakukan kontrol lokal
dengan radioterapi dengan / tanpa pembedahan dan sering berkembang menjadi
metastase jauh. Walau rekurensi biasanya terjadi dalam 5 tahun setelah diagnosis,
Beberapa target molekuler telah diidentifikasi dalam spesimen tumor penderita
KNF. Ekspresi atau overekspresi reseptor-reseptor berikut telah dievaluasi pada KNF :
EGFR, cKIT c-erbB-2 (HER-2) dan VEGF (Vascular Endothelial Growth Factor), yang
merupakan faktor proangiogenik, yang berperan dalam angiogenesis untuk
pertumbuhan tumor, invasi dan metastase tumor (Agulnik dan Siu, 2005).
Angiogenesis adalah pembentukan pembuluh darah baru yang berasal dari
pembuluh darah yang telah ada (Josko et al. 2000; Rosen, 2002). Angiogenesis sangat
dibutuhkan dalam pembentukan organ baru serta untuk diferensiasi saat embriogenesis,
penyembuhan luka dan fungsi reproduksi wanita (Josko et al. 2000; Rosen, 2002).
Dalam kondisi patologi, angiogenesis dibutuhkan pada proses pertumbuhan tumor solid
dan pada proses metastase (Rosen, 2002; Medinger dan Drevs, 2005; Hicklin dan Ellis,
2005). Tumor membutuhkan angiogenesis untuk tumbuh di atas ukuran 1-2 mm3
(Rosen, 2002). Angiogenesis diperlukan untuk suplai oksigen, nutrien, faktor
pertumbuhan dan hormon, enzim proteolitik, mempengaruhi faktor hemostatik yang
mengontrol koagulasi dan sistem fibrinolitik, dan penyebaran sel-sel tumor ke tempat
jauh (Hicklin dan Ellis, 2005).
Angiogenesis merupakan proses yang sangat kompleks, yang diregulasi secara
ketat oleh faktor-faktor proangiogenik (VEGF) dan faktor-faktor antiangiogenik (Rosen,
2002; Hicklin dan Ellis, 2005). VEGF berperan penting dalam angiogenesis tumor.
Ekspresi VEGF dalam sel-sel tumor distimulasi oleh hipoksia, onkogen (ras) dan
inaktivasi gen supresor tumor (p53) dan oleh berbagai sitokin (Rosen, 2002). Aktivasi
aksis VEGF/VEGF reseptor (VEGFR) memicu jaringan sinyal multipel yang
vaskular serta mobilisasi sel-sel progenitor endotel dari sumsum tulang ke sirkulasi
perifer (Hicklin dan Ellis, 2005).
Overekspresi VEGF telah dihubungkan dengan progresivitas tumor dan
prognosis buruk dalam berbagai macam tumor, termasuk karsinoma kolorektal,
karsinoma lambung, karsinoma pankreas, kanker payudara, kanker paru dan
melanoma, acute myeloid leukemia, karsinoma hepar dan kanker ovarium (Rosen,
2002; Hicklin dan Ellis, 2005). Ekspresi VEGF dibandingkan antara sampel jaringan
yang diambil dari nasofaring normal, tumor jinak nasofaring dan KNF, dengan nilai
ekspresi VEGF 10%, 40% dan 80%. Ekspresi VEGF meningkat pada KNF stadium
lanjut dengan perbandingan statistik yang signifikan terhadap KNF stadium dini (dikutip
oleh Agulnik dan Siu, 2005 dari Guang Wu, 2000). Satu studi di China dari 127
spesimen KNF dengan pemeriksaan imunohistokimia didapati nilai positif VEGF 66,9%
(Sha dan He, 2006). Penelitian di India didapati overekspresi VEGF 67% dari 103
penderita KNF (Khrisna et al. 2006). Penelitian sebelumnya di Singapura dari 42 pasien
KNF yang diperiksa secara imunohistokimia dijumpai overekspresi VEGF pada seluruh
sampel (Soo et al. 2005).
Karena peran sentralnya dalam angiogenesis tumor, jalur VEGF/VEGFR telah
menjadi fokus utama riset dasar dan pengembangan obat-obatan di bidang onkologi
(Hicklin dan Ellis, 2005). Dari beberapa penelitian telah disimpulkan kombinasi anti
VEGF dengan kemoterapi atau radioterapi menghasilkan efek antitumor yang lebih baik
daripada pemberian kemoterapi/radioterapi sendiri (Ferrara et al. 2004).
Di Departemen THT KL FK USU/RSUP HAM, penderita KNF sebagian besar
datang dengan stadium lanjut (Stadium III dan IV). Penderita KNF stadium lanjut
memiliki prognosa yang jelek, dengan kemungkinan besar terjadi rekurensi dan
metastase jauh. Peneliti tertarik untuk mengetahui ekspresi VEGF pada KNF, dimana
overekspresi VEGF telah dihubungkan dengan progresivitas dan prognosis tumor yang
buruk.
1.3 Tujuan Penelitian 1.3.1Tujuan Umum
Mengetahui ekspresi Vascular Endothelial Growth Factor pada Karsinoma
Nasofaring
1.3.2Tujuan Khusus
1.3.2.1 Mengetahui ekspresi VEGF pada penderita KNF
1.3.2.2 Mengetahui hubungan stadium tumor dengan ekspresi VEGF pada KNF
1.3.2.3 Mengetahui hubungan jenis histopatologi dengan ekspresi VEGF pada KNF
1.4 MANFAAT PENELITIAN 1.4.1 Manfaat teoritik
Dapat memahami peran VEGF pada KNF dalam progresivitas dan prognosis
penyakit.
1.4.2Manfaat praktis
Sebagai dasar penelitian selanjutnya dalam pemberian anti VEGF terhadap
BAB 2
TINJAUAN PUSTAKA
2.1 Karsinoma Nasofaring 2.1.1 Anatomi Nasofaring
Nasofaring merupakan ruang berbentuk trapezoid dengan ukuran tinggi 4 cm,
lebar 4 cm dan anteroposterior 3 cm. Permukaan dilapisi epitel pseudostratified
columnar tipe pernafasan dan epitel non keratinizing stratified squamous. Dinding
anterior dibentuk oleh koana dan batas posterior septum nasi. Lantai dibentuk oleh
permukaan atas palatum mole. Bagian atap dan dinding posterior dibentuk oleh
permukaan yang melandai dibatasi oleh badan sfenoid, basioksiput dan vertebra
cervical I dan II hingga batas palatum mole. Dinding lateral terdapat muara tuba
Eustachius. (Chew, 1997; Cottrill dan Nutting, 2003; Wei, 2006).
Atap dan dinding posterior nasofaring
Bagian atap melandai yang menyatu dengan dinding posterior. Keduanya
dibentuk oleh lantai sinus sfenoid di medial dan fibrokartilago foramen lacerum di lateral.
Sinus kavernosus dengan arteri karotis interna dan syaraf kranial III, IV, V dan VI
terletak di atas foramen laserum pada kedua sisi. Dinding posterior menutupi bagian
basilar tulang oksipital dan arkus anterior atlas di inferior. Dibagian atas dinding
posterior melekat jaringan limfoid pada membran mukosa (tonsil nasofaring atau
adenoid). Fascia prevertebra dan otot memisahkan adenoid dengan tulang vertebra
Dinding lateral nasofaring
Tuba Eustachius bermuara ke nasofaring melalui dinding lateral. Tuba dibentuk
oleh fascia faringobasilar yang diperkuat di inferior oleh otot konstriktor superior. Dilihat
dari cavum nasi, aspek anterior dan aspek posterior orificium tuba Eustachius ditandai
dengan elevasi kartilago tuba, dimana di belakangnya terletak fossa Rosenmuller. Di
sebelah dalam dinding lateral terdapat ruang parafaring yang berisikan arteri karotis
interna, syaraf kranial IX, X, XI dan XII, vena jugularis interna dan kelenjar limfe
retrofaring (Chew, 1997; Cottrill dan Nutting, 2003).
Fascia faring dan jaringan ikat foramen laserum menyebabkan kerentanan
terhadap invasi langsung tumor ganas nasofaring. Keadaan ini serta seringnya
keterlibatan kelenjar limfe retrofaring menjelaskan seringnya keterlibatan syaraf kranial
(Cottrill dan Nutting, 2003).
Dasar nasofaring
Dasar nasofaring dibentuk oleh permukaan superior palatum molle, yang
berhubungan dengan spingter palatofaring berperan untuk menutup ismus faring saat
menelan, memisahkan nasofaring dengan orofaring di bawahnya (Chew, 1997; Cottrill
dan Nutting, 2003).
Saluran limfe dan persyarafan nasofaring
Mukosa terbentuk dari beberapa lipatan otot dibawahnya dan mengandung
berbagai kumpulan jaringan limfoid. Jaringan limfoid yang paling menonjol, terutama
menonjol ke depan dari pertemuan atap dan dinding posterior. Lokasi aliran limfe
kelompok pertama adalah kelenjar retrofaring yang terletak di ruang antara dinding
nasofaring posterior, fascia faringobasilar dan fascia prevertebra. Kelompok kelenjar
Rouviere (node of Rouviere) membentuk kelompok kelenjar lateral utama. Kelenjar
tersebut terletak di anterior sebelah lateral atlas di batas lateral m. capitis longus,
sebelah anteromedial arteri karotis interna. Pembuluh eferen mengalir ke rantai jugular
interna dalam pada bagian paling atas di dasar tengkorak di ruang kompartemen
parafaring retrostiloid disebelah dalam ujung atas otot sternomastoid. Kelenjar ini
kemudian mengalir ke bawah di posterior dari kelompok syaraf aksesorius dan di
anterior kelompok jugulodigastrik. (Chew, 1997; Cottrill dan Nutting, 2003).
Suplai syaraf ke mukosa nasofaring berasal dari n. trigeminal divisi maksilla
melalui cabang kecil, n. faringeal yang berasal dari fossa pterigopalatina, di dekat
ganglion pterigopalatina (Cottrill dan Nutting, 2003).
2.1.2 Epidemiologi
Karsinoma Nasofaring (KNF) adalah tumor ganas yang berasal dari sel epitel
yang melapisi nasofaring, tidak termasuk tumor kelenjar atau limfoma (Wei dan Sham,
2005; Brennan 2006). Di Indonesia KNF merupakan tumor ganas kepala dan leher
yang paling banyak ditemukan. Menurut data patologi tahun 1990 KNF menduduki
urutan ke-4 dari seluruh keganasan setelah kanker mulut rahim, payudara dan kulit.
Prevalensi penderita KNF 4,7 orang per 100.000 penduduk pertahun yang diambil dari
data resmi Departemen Kesehatan tahun 1980 (Roezin, 1995). Penelitian Fachiroh di
(Fachiroh et al. 2004). Di Bagian THT FK-UI RSCM selama periode 1988-1992 didapati
511 penderita baru KNF (Roezin, 1997). Di RSUP H. Adam Malik Medan pada tahun
1998-2000 ditemukan 130 penderita KNF dari 1370 pasien baru onkologi kepala dan
leher (Lutan, 2003). Sementara pada periode 1 Juli 2005 – 30 Juni 2006 ditemukan 79
orang penderita baru KNF (Aliandri, 2007).
Pada daerah Barat (Amerika dan Eropa) kejadian KNF jarang dengan insiden
sekitar 0,5/100.000, dengan angka 1-2% dari seluruh kanker kepala dan leher. Di Cina
Selatan dan Hongkong penyakit ini endemik dengan angka insiden meningkat hingga
50/100.000. Perbedaan ini berhubungan dengan subtipe patologis, di Amerika Utara
terdapat WHO tipe 1 (keratinizing squamous cell carcinoma) pada 68% kasus,
sementara di Timur Jauh lebih 95% merupakan WHO tipe 2-3. Insidensi WHO tipe 3
juga tinggi di Eskimo dan Alaska, dan juga meningkat di Malaysia, Afrika Utara dan
Eropa Selatan (Cottrill dan Nutting, 2003).
Secara umum KNF ditemukan pada populasi yang lebih muda dari kanker kepala
dan leher di tempat lain. Pada daerah endemik insiden meningkat sejak usia 20 tahun
dan mencapai puncak pada dekade IV dan dekade V. Pada daerah resiko rendah usia
terbanyak pada dekade V dan dekade VI tapi masih terdapat insidensi yang signifikan
pada usia di bawah 30 tahun, sehingga didapati distribusi usia bimodal, dengan puncak
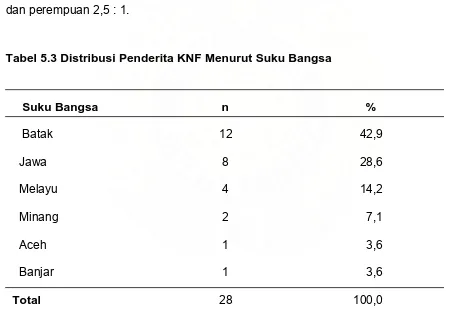
awalnya antara usia 15-25 tahun. KNF lebih sering dijumpai pada pria dengan
perbandingan pria dan wanita 3 : 1 (Chew, 1997; Cottrill dan Nutting, 2003; Ganguly et
2.1.3 Etiologi
KNF kemungkinan merupakan hasil interaksi kompleks faktor-faktor genetik, virus
dan lingkungan (Ganguly et al. 2003). Beberapa faktor yang dianggap berpengaruh
terhadap KNF :
1. Infeksi virus Epstein-Barr
Terdapat peningkatan antibodi IgA terhadap viral capsid antigen (VCA) dan early
antigen compleks (EA) dan ditemukannya genom virus pada sel tumor (McDermott et
al. 2001 Ahmad, 2002; Cottrill dan Nutting; 2003. Lutzky et al. 2008). Virus
Epstein-Barr (VEB) terdeteksi secara konsisten pada pasien KNF di daerah dengan insidensi
tinggi dan daerah dengan insidensi rendah. Sinyal RNA yang dikode VEB dengan
metode hibridisasi in situ dijumpai pada hampir seluruh sel tumor, dimana RNA yang
dikode VEB tidak dijumpai pada jaringan normal di sekitar tumor, kecuali pada
jaringan limfoid yang terbatas. Lesi premaligna di epitel nasofaring telah
menunjukkan kandungan VEB, yang menunjukkan infeksi terjadi pada fase awal
karsinogenesis. Terdeteksinya bentuk tunggal DNA viral menyarankan bahwa tumor
merupakan proliferasi klonal dari sel tunggal yang pada awalnya terinfeksi VEB.
Gen-gen laten spesifik VEB secara konsisten diekspresikan pada karsinoma
nasofaring pada lesi awal dan lesi displastik. Protein viral laten (latent membrane
protein 1 dan 2) memiliki efek yang substansial pada ekspresi gen selular dan
pertumbuhan selular, menghasilkan pertumbuhan yang sangat invasif serta
pertumbuhan yang ganas dari karsinoma (McDermott et al. 2001; Cottrill dan Nutting,
2. Ikan asin, makanan yang diawetkan dan nitrosamin
Beberapa penelitian epidemiologik dan laboratorium menyokong hipotesa yang
menyebutkan bahwa konsumsi dini ikan asin menyebabkan KNF di Cina Selatan dan
Hongkong. Suatu studi kasus kontrol menunjukkan bahwa hanya konsumsi ikan asin
yang sering sebelum usia 10 tahun yang berhubungan dengan peningkatan resiko
terjadinya KNF (Ahmad, 2002; Ganguly et al. 2003; Cottrill dan Nutting, 2003; Wei,
2006).
Selain ikan asin, uap nitrosamin tingkat tinggi juga ditemukan pada berbagai bahan
makanan yang diawetkan di China, Tunisia dan Greenland, dimana beberapa bahan
makanan tersebut mengandung prekursor nitrosamin tingkat tinggi yang
menghasilkan uap nitrosamin setelah dicerna di lambung (Chew, 1997).
3. Sosial ekonomi, lingkungan dan kebiasaan hidup.
Udara yang penuh asap dan uap di rumah-rumah dengan ventilasi kurang baik di
Cina, Indonesia dan Kenya juga meningkatkan insiden KNF. Pembakaran dupa di
rumah-rumah juga dianggap berperan dalam menimbulkan KNF di Hongkong (Chew,
1997; McDermott et al. 2001; Ahmad, 2002). Perokok berat meningkatkan resiko
KNF pada daerah endemik (Cottrill dan Nutting, 2003; Ganguly et al. 2003).
4. Sering kontak dengan bahan karsinogen antara lain : benzopyren, benzo
anthracene, gas kimia, asap industri, asap kayu, debu kayu, formaldehid, asap
rokok, dan beberapa ekstrak tumbuhan. Penelitian di Swedia menunjukkan pembuat
gelas, pembuat sepatu, pembuat buku serta pekerja di pembakaran tanaman
mempunyai risiko tinggi untuk KNF. Di Selandia Baru peningkatan resiko KNF terjadi
suatu studi kasus kontrol menunjukkan resiko tinggi KNF pada pekerja yang terpapar
bahan-bahan hasil pembakaran batu bara, arang, pengelasan serta bahan bakar cair
(Chew, 1997; McDermott et al. 2001; Ganguly et al. 2003).
5. Ras dan keturunan.
Insiden tertinggi di dunia ternyata terdapat pada ras Cina, baik di daerah asal
ataupun di perantauan. Insiden tertinggi terutama di Provinsi Guangdong dan
Daerah Otonom Guangxi (Roezin, 1995; Chew, 1997; Ahmad, 2002). Insiden KNF
tetap tinggi pada penduduk Cina yang berimigrasi ke Asia Tenggara atau Amerika
Utara, tapi lebih rendah pada penduduk Cina yang lahir di Amerika Utara daripada
yang lahir di Cina Selatan (Chew, 1997; Ahmad, 2002; Wei dan Sham, 2005).
Insiden sedang dijumpai pada ras Asia Tenggara (Malaysia, Indonesia, Thailand,
Vietnam, Filipina), Eskimo (Kanada, Alaska, Greenland) dan Afrika Utara. Insiden
yang jauh lebih rendah daripada insiden di Asia dijumpai di Malta, Tunisia, Aljazair,
Maroko dan Sudan, tetapi insiden tetap lebih tinggi daripada di Amerika dan Eropa
(Chew, 1997; Cottrill dan Nutting, 2003).
6. Radang kronis di nasofaring
Dengan adanya peradangan menahun di nasofaring, mukosa nasofaring menjadi
lebih rentan terhadap karsinogen penyebab KNF (McDermott, et al. 2001; Ahmad,
2002). Proses peradangan dan kondisi-kondisi benigna di telinga, hidung dan
tenggorokan merupakan faktor predisposisi terjadinya transformasi pada mukosa
7. Profil HLA.
Hubungan antara profil HLA dan KNF ditemukan pada pasien KNF di berbagai
negara. Pada etnik Cina, KNF dihubungkan dengan ditemukannya HLA tipe A2 dan
Bw46 (Chew, 1997; Cottrill dan Nutting, 2003). Penelitian di bagian THT FKUI/RSCM
tahun 1997 didapatkan fenotip antigen HLA kelas 1, HLA-A24 dan HLA-B63 untuk
kemungkinan faktor penyebab bagi orang Indonesia asli (Roezin, 1996; Ahmad,
2002). Penelitian di Medan menemukan alel gen paling tinggi pada penderita KNF
suku Batak adalah alel gen HLA-DRB1*12 dan HLA-DQB*0301 dimana alel gen
yang potensial sebagai penyebab kerentanan timbulnya KNF pada suku Batak
adalah alel gen HLA-DRB1*08 (Delfitri M, 2007)
2.1.4 Gejala Klinik
Dari segi penderita gejala dini KNF tidak khas bahkan lebih banyak menyerupai
gejala rhinitis atau sinusitis. Keluhan penderita KNF sering meragukan dan baru jelas
setelah tumor membesar dan stadium sudah lanjut. Kesulitan ini akibat sulitnya
pemeriksaan nasofaring (Ahmad, 2002).
Gejala yang timbul berhubungan erat dengan lokasi tumor di nasofaring dan
derajat penyebaran. Gejala dini sering tidak disadari oleh penderita maupun dokter
sendiri. Gejala yang sering ditemukan :
1. Pembesaran kelenjar leher
Gejala ini paling sering ditemukan dan membawa penderita berkonsultasi dengan
dokter, sebagian besar penderita datang dengan pembesaran kelenjar leher baik
terdekat secara limfogen dari KNF. Kelenjar limfe retrofaring lateral (node of
Rouviere) adalah penyaring limfatik pertama akan tetapi tidak dapat diraba.
Pembesaran kelenjar yang agak khas akibat metastasis adalah lokasi pada ujung
prosesus mastoideus di belakang angulus mandibula yaitu kelenjar jugulodigastric
dan kelenjar cervical posterior (atas dan tengah), kemudian diikuti kelenjar cervical
tengah. Tumor biasa teraba keras, tidak nyeri. Dapat terfiksir atau mudah
digerakkan (Chew, 1997; Ahmad, 2002; Cottrill dan Nutting, 2003; Thompson, 2005)
2. Gejala hidung
Gejala pada hidung dapat merupakan gejala dini KNF akan tetapi gejala ini tidak
khas, karena dapat juga dijumpai pada penyakit infeksi biasa seperti rhinitis kronis
atau sinusitis. Gejala dapat berupa ingus yang dinodai darah serta ludah yang
bercampur darah saat membersihkan tenggorokan. Perdarahan dapat timbul
berulang-ulang, jumlah sedikit, bercampur ingus sehingga berwarna merah jambu
atau terdapat garis-garis darah halus. Epistaksis biasanya dijumpai pada KNF
stadium lanjut dengan atau tanpa erosi dasar tengkorak. Sumbat hidung biasanya
gejala pada stadium lanjut. Jika dijumpai pada stadium dini biasanya akibat infeksi
sekunder. Ozaena terjadi akibat nekrosis tumor dan merupakan ciri KNF stadium
lanjut. (Chew, 1997; Ahmad, 2002; Cottrill dan Nutting, 2003)
3. Gejala telinga
Dapat berupa gangguan pendengaran seperti tuli hantar, rasa penuh di telinga,
seperti ada cairan, tinitus atau berdenging. Hal ini karena umumnya tumor pertama
kali timbul di fossa Rosenmuller dan menyumbat muara tuba Eustachius. Gejala ini
pasien KNF yang didiagnosa dini. Jika seorang Cina dewasa datang dengan
keluhan ini, seorang ahli THT harus mempertimbangkan kemungkinan KNF (Chew,
1997; Ahmad, 2002; Wei, 2006).
4. Gejala neurologis
a. Sindroma petrosfenoidal
Gejala timbul akibat perluasan tumor ke intrakranial melalui foramen laserum.
Syaraf kranial yang terlibat berturut-turut adalah : n.VI, n. III, n.IV sedang n. II
paling akhir mengalami gangguan. Parese n. II menyebabkan gangguan
visus. Parese n. III menyebabkan kelumpuhan m. levator palpebra dan otot
tarsalis superior sehingga menimbulkan ptosis. Parese n. III, IV dan VI akan
menyebabkan gangguan berupa diplopia karena syaraf-syaraf tersebut
berperan dalam pergerakan bola mata. Parese n. V akan menimbulkan gejala
parestesi atau hipestesi pada separuh wajah. Apabila semua syaraf grup
anterior (n. II – n. VI) terkena, maka akan timbul gejala : neuralgia trigeminal
unilateral, oftalmoplegi unilateral, serta gejala nyeri kepala hebat yang timbul
akibat penekanan tumor pada duramater (Sudyartono dan Wiratno, 1996;
Ahmad, 2002)
b. Sindroma parafaring
Gejala ini timbul akibat gangguan syaraf kranial grup posterior (n. IX, X, XI
dan XII) karena penjalaran retroparotidean dimana tumor tumbuh ke
belakang masuk ke dalam foramen jugularis dan kanalis nervus hipoglosus.
Manifestasi kelumpuhan ialah : n. IX : kesulitan menelan karena hemiparese
disfoni, disfagia dan spasme esofagus. Gangguan sensorik berupa nyeri
daerah laring dan faring, dyspnoe dan hipersalivasi. N. XI : kelumpuhan atau
atrofi m. trapezius, sternokleidomastoideus serta hemiparese palatum molle.
N. XII : hemiparese dan atrofi sebelah lidah. N. VII dan n. VIII jarang terkena
KNF karena letaknya agak tinggi (Sudyartono dan Wiratno, 1996; Ahmad,
2002).
5. Gejala akibat metastase jauh.
Sel-sel kanker dapat menjalar bersama aliran darah (hematogen) atau bersama
aliran limfe (limfogen) mengenai organ tubuh yang letaknya jauh dari nasofaring.
Metastase jauh dijumpai pada 3-6% penderita saat pertama kali datang, tetapi dapat
berkembang hingga 40% dari penderita KNF. Organ yang sering dikenai adalah
tulang (48%), diikuti paru (27%) dan hati (11%). Sumsum tulang jarang terlibat akan
tetapi membawa prognosis yang buruk. Metastase kelenjar limfe diluar leher jarang
terjadi dan biasanya timbul pada kasus relaps. Metastase jauh merupakan stadium
lanjut dan KNF dengan prognosis buruk. (Chiesa dan Paoli, 2001; Ahmad, 2002;
Cottrill dan Nutting, 2003).
2.1.5 Diagnosis
Dari sebuah penelitian pada 4768 penderita KNF, gejala yang dikeluhkan pada
saat pertama datang adalah benjolan di leher (76%), gangguan hidung (73%),
gangguan telinga (62%), sakit kepala (35%), penglihatan ganda (11%), rasa kebas di
wajah (8%), penurunan berat badan (7%) dan trismus (3%). Tanda klinis yang
(75%) dan kelainan syaraf kranial (20%). Syaraf kranial yang sering terkena adalah
syaraf kranial III, V, VI dan XII. Bila secara klinis dicurigai menderita KNF dan tumor
tidak terlihat pada pemeriksaan endoskopi, harus dilakukan pencitraan dengan
potongan lintang (CT Scan atau MRI). Diagnosis pasti KNF ditegakkan melalui biopsi
nasofaring yang didukung oleh visualisasi melalui endoskopi atau pencitraan dengan
potongan lintang (Wei dan Sham, 2005).
Jika penderita datang dengan gejala KNF, penderita harus dievaluasi secara
klinis adanya tanda-tanda fisik KNF (kelenjar limfe leher, cairan di telinga tengah,
keterlibatan syaraf kranial). Anamnesa lengkap, terutama gejala neurologi dan keluhan
yang menyarankan adanya metastase jauh sangat penting untuk ditanyakan kepada
penderita. Karena radioterapi adalah terapi utama sangat penting untuk menanyakan
faktor-faktor yang berpotensi terjadinya komplikasi yaitu riwayat radiasi sebelumnya,
merokok, alkohol, gizi buruk dan kelainan gigi (Cottrill dan Nutting, 2003; Wei, 2006).
Pemeriksaan yang dianjurkan untuk penderita KNF :
Untuk seluruh penderita :
- Nasofaringoskopi langsung dan biopsi pada tumor primer
- Pemeriksaan darah
- Profil biokimia termasuk tes fungsi hati dan laktat dehidrogenase (LDH)
- Serologi virus Epstein-Barr (IgA anti VCA, IgA anti EA)
- X-ray dada
- CT resolusi tinggi (dengan kontras intravena) atau scan MRI pada fossa cranii media,
nasofaring, sinus paranasal, leher dan inlet dada
Untuk penderita dengan keterlibatan kelenjar limfe lanjut (N3) atau diduga adanya
metastase jauh :
- Scan tulang dan radiografi polos pada daerah yang abnormal atau daerah yang
menunjukkan gejala.
- Scan ultrasound hati (Cottrill dan Nutting, 2003).
Pemeriksaan penunjang :
- Audiometri (jika ada indikasi klinis atau pada pemberian kemoterapi platinum)
- Bersihan kreatinin atau bersihan EDTA (pada pemberian kemoterapi platinum) (Cottrill
dan Nutting, 2003).
Pemeriksaan Fisik
Pemeriksaan fisik harus diarahkan ke cavum nasi dan nasofaring. Pemeriksaan
tidak langsung daerah nasofaring dapat dilakukan dengan cermin (rinoskopi posterior),
tetapi variasi anatomi pada penderita akan menganggu evaluasi yang adekwat pada
daerah nasofaring. Rinoskopi posterior juga dibatasi oleh refleks faring, kerjasama
penderita dan ketidakmampuan membuka mulut. Akan tetapi, pemeriksaan dengan
cermin masih tetap cara tercepat untuk menilai nasofaring. Dengan bantuan
nasoendoskopi kaku atau nasoendoskopi fleksibel dapat dilihat perluasan tumor primer,
yang dapat tumbuh eksofitik, atau tampak hanya berkurangnya batas dari fossa
Rosenmuller. Perluasan ke palatum mole, dinding faring dan orofaring harus dilihat
dengan inspeksi dan palpasi. Bukti adanya defisit syaraf kranial dapat dilihat dari
dilakukan pemeriksaan visual dan pemeriksaan membran timpani (Chew, 1997; Cottrill
dan Nutting, 2003; Wei, 2006)
Biopsi nasofaring
Konfirmasi pasti diagnosa KNF diperoleh dengan hasil biopsi positif yang diambil
dari tumor di nasofaring. Prosedur standar adalah biopsi transnasal dengan panduan
endoskopi. Teleskop kaku Hopkins 0° dan 30° memberikan pandangan yang baik dari
nasofaring. Jika terdapat deviasi septum, endoskop 70° dimasukkan melalui cavum nasi
yang berlawanan dapat memberikan visualisasi tumor yang adekwat. Endoskop 70°
yang dimasukkan di belakang palatum molle dapat memberikan visualisasi atap
nasofaring dan kedua muara tuba Eustachius. Endoskop kaku tidak mempunyai jalur
penghisap atau jalur biopsi. Darah dan mukus yang menutupi tumor harus dibuang
dengan penghisap terpisah untuk mendapatkan pandangan yang jelas pada daerah
patologis. Forsep biopsi harus dimasukkan bersebelahan dengan endoskop untuk
mendapatkan biopsi tumor dibawah pandangan langsung (Chew, 1997; Cottrill dan
Nutting, 2003; Wei, 2006).
Endoskop fleksibel memberikan pemeriksaan yang teliti pada seluruh nasofaring,
walau dimasukkan melalui satu sisi cavum nasi. Ujungnya dapat bermanuver di
belakang septum nasi ke sisi sebelah. Endoskop ini memiliki jalur penghisap dan forsep
biopsi dapat dimasukkan melaluinya untuk mengambil biopsi tumor dibawah pandangan
langsung. Walaupun demikian, gambaran visual yang diperoleh dari endoskop fleksibel
kurang baik dibandingkan endoskop kaku dan ukuran forsep biopsi kecil, sehingga
Pada beberapa keadaan seperti : keadaan umum kurang baik, penderita tidak
kooperatif, faring terlalu sensitif, trismus atau pada anak, dilakukan eksplorasi
nasofaring dimana selain dilakukan biopsi, juga dilakukan kuretase daerah nasofaring.
Hal ini juga dilakukan pada penderita yang telah dilakukan biopsi dengan anestesi lokal
tetapi tidak menunjukkan hasil positif sedangkan gejala dan tanda yang ditemukan
menunjukkan ciri KNF (Ahmad, 2002).
Pada kasus KNF yang tidak dapat dikonfirmasi dengan biopsi endoskopi
konvensional, dapat dilakukan biopsi aspirasi jarum halus di nasofaring. Tumor yang
terletak dalam yang tidak dapat diambil dengan biopsi konvensional dapat dicapai oleh
biopsi aspirasi jarum halus dengan hasil yang cukup akurat (Lubis, 1993).
Biopsi nasofaring tetap dilaksanakan walaupun tumor primer tidak terlihat di
nasofaring pada keadaan :
1. Limfadenopati kelenjar leher akibat metastase tumor ganas.
2. Parese/paralise unilateral n.IV dan n.VI dengan sebab yang tidak jelas.
3. Asimetri nasofaring pada CT scan.
4. Terdapat 2 dari 3 gejala yaitu gejala telinga, gejala hidung dan gejala neurologis
(Ahmad, 2002).
Pemeriksaan Radiologi
Pemeriksaan foto polos dapat menilai destruksi tulang dan massa jaringan lunak
yang menutupi jalan nafas atas. Akan tetapi teknik ini memiliki sensitivitas dan
spesifisitas yang rendah dan hanya sedikit memberikan keterangan tentang invasi dan
Pemeriksaan fisik (termasuk endoskopi) dapat memberikan informasi yang
bernilai mengenai keterlibatan mukosa dan perluasan tumor ke hidung dan orofaring,
tetapi tidak dapat menilai perluasan ke dalam, erosi dasar tengkorak, atau penyebaran
intrakranial, kecuali terdapat gejala dan tanda ekstensi yang luas melalui jalur tersebut
(Wei dan Sham, 2005).
Pencitraan potong lintang telah meningkatkan efektivitas terapi pada penderita
KNF. Pencitraan tumor primer yang sesuai sangat penting bukan hanya untuk
menentukan stadium tetapi juga untuk perencanaan radioterapi yang akurat. Dalam
menentukan stadium, CT dapat mengidentifikasi penyebaran paranasofaring yaitu jenis
penyebaran yang paling sering pada KNF, dan dapat menunjukkan penyebaran
perineural melalui foramen ovale yang merupakan jalur penyebaran intrakranial yang
penting. Penyebaran perineural melalui foramen ovale juga diperhitungkan sebagai bukti
CT adanya keterlibatan sinus kavernosa tanpa erosi dasar tengkorak (Cottrill dan
Nutting 2003; Wei dan Sham, 2005)
MRI lebih baik dari CT dalam memperlihatkan jaringan lunak nasofaring
superfisial atau dalam dan untuk membedakan tumor dengan jaringan lunak. MRI juga
lebih sensitif untuk menilai metastase kelenjar retrofaring dan kelenjar leher dalam.
Akan tetapi MRI kemampuannya terbatas dalam detail tulang dan CT harus dilakukan
bila status dasar tengkorak tidak dapat ditentukan dengan jelas oleh MRI. Dalam
penentuan stadium, MRI dapat mendeteksi infiltrasi tumor ke sumsum tulang, dimana
CT tidak dapat mendeteksinya kecuali dijumpai erosi tulang yang terlibat. Infiltrasi ke
sumsum tulang dihubungkan dengan peningkatan resiko metastase jauh. Pada suatu
dengan pemeriksaan CT dibandingkan MRI (Cottrill dan Nutting 2003; Wei dan Sham,
2005).
Deteksi metastase jauh saat diagnosa dengan radiografi konvensional, CT dan
MRI biasanya tidak berhasil. Beberapa laporan telah menyimpulkan bahwa scan tulang,
scintigrafi hati, ultrasonografi abdominal dan biopsi sumsum tulang memiliki nilai yang
kecil dalam pemeriksaan stadium rutin dan direkomendasikan untuk tidak digunakan
(Wei dan Sham, 2005).
Saat digunakan untuk memonitor kondisi penderita setelah terapi, baik CT dan
MRI memiliki sensitivitas rendah dan spesifisitas sedang dalam mendeteksi rekurensi
tumor, walaupun secara umum MRI lebih baik dari CT dalam menunjukkan rekurensi
tumor dan komplikasi post radiasi (Wei dan Sham, 2005).
Pemeriksaan Serologi
Virus Epstein-Barr dapat mempengaruhi manusia dalam berbagai bentuk. Virus
ini dapat menyebabkan infeksi mononukleosis dan juga berhubungan dengan limfoma
Burkitt dan KNF. VEB tergolong virus herpes dan antigen spesifik VEB dapat
dikelompokkan menjadi antigen replikatif awal, antigen fase laten dan antigen akhir.
Pada pasien KNF, antibodi imunoglobulin A (IgA) memberikan respon terhadap early
antigen (EA) dari kelompok pertama, dan viral capsid antigen (VCA) dari kelompok
ketiga memiliki nilai diagnostik. Keduanya juga berperan dalam skrining bagi penderita
KNF asimtomatik pada populasi resiko tinggi. IgA anti VCA lebih sensitif tetapi kurang
spesifik dibandingkan IgA anti EA. Walau kurang spesifik, peninggian LDH serum juga
2.1.6 Histopatologi dan Stadium
WHO menetapkan KNF sebagai kanker yang berasal dari sel skuamous dan
dibedakan berdasarkan mikroskop cahaya menjadi 3 tipe :
Tipe 1 : keratinizing squamous cell carcinoma, menunjukkan differensiasi skuamosa
dengan adanya jembatan interseluler dan/atau keratinisasi di atasnya.
Tipe 2 : differentiated non keratinizing carcinoma, sel tumor menunjukkan diferensiasi
dengan rangkaian maturasi yang terjadi di dalam sel, dimana diferensiasi
skuamosa tidak terlihat pada mikroskop cahaya.
Tipe 3 : undifferentiated carcinoma, sel-sel tumor memiliki inti vesikuler yang oval atau
bulat dan nukleolus yang menonjol. Batas sel tidak terlihat, dan tumor
menunjukkan gambaran sinsitial.
Tumor tipe 2 dan tipe 3 biasanya lebih radiosensitif dan memiliki hubungan
yang kuat dengan virus Epstein-Barr (Thompson, 2005; Wei dan Sham, 2005;
Lutzky et al. 2008).
Terdapat berbagai klasifikasi untuk KNF, yang paling sering digunakan adalah
menurut UICC (2002) dan Ho (1978). (Marzaini, 2002; Mould dan Tai, 2002; Cottrill
dan Nutting, 2003).
Klasifikasi menurut AJCC/UICC 2002 : (Brennan, 2006)
Tumor Primer (T)
TX Tumor primer tidak dapat dinilai
T0 Tidak terbukti adanya tumor primer
Nasofaring
T1 Tumor terbatas di nasofaring
T2 Tumor meluas ke jaringan lunak orofaring dan/atau rongga hidung
T2a Tanpa perluasan ke daerah parafaring
T2b Dengan perluasan ke daerah parafaring
T3 Tumor menginvasi struktur tulang dan/atau sinus paranasal
T4 Tumor dengan perluasan intrakranial dan/atau terlibatnya syaraf kranial, rongga
infratemporal, hipofaring, orbita atau ruang mastikator.
KGB Regional (N)
NX KGB regional tidak dapat dinilai
N0 Tidak ada metastase ke KGB regional
N1 Metastase KGB unilateral, diameter terbesar kurang dari 6 cm, di atas fossa
supraklavikular.
N2 Metastase KGB bilateral, diameter terbesar kurang dari 6 cm, di atas fossa
supraklavikular
N3 Metastase pada KGB :
N3a Diameter terbesar lebih dari 6 cm
N3b Meluas ke fossa supraklavikular
Metastase Jauh (M)
Mx Metastase jauh tidak dapat dinilai
M1 Metastase jauh
Kelompok stadium :
0 Tis N0 M0
I T1 N0 M0
IIA T2a N0 M0
IIB T1 N1 M0
T2a N1 M0
T2b N0 M0
T2b N1 M0
III T1 N2 M0
T2a N2 M0
T2b N2 M0
T3 N0 M0
T3 N1 M0
T3 N2 M0
IVA T4 N0 M0
T4 N1 M0
T4 N2 M0
IVB setiap T N3 M0
2.1.7 Terapi Radioterapi
Radioterapi masih tetap merupakan modalitas terapi primer untuk KNF dan
kelenjar regional yang membesar (Cottrill dan Nutting, 2003; Wei dan Sham, 2005). Ini
disebabkan lokasi nasofaring berdekatan dengan struktur yang penting, serta sifat
infiltrasi KNF, sehingga pembedahan sulit dilakukan. Selain itu KNF memiliki sensitivitas
tinggi terhadap radiasi maupun kemoterapi dibandingkan kanker kepala dan leher
lainnya (Wei, 2006; Lin, 2006; Guigay et al. 2006).
Pada pasien KNF stadium dini (stadium I dan II), terapi pilihan adalah radioterapi
definitif. Pada KNF stadium lanjut (stadium III dan IV) pemberian kemoterapi
dikombinasikan dengan radioterapi merupakan pilihan, walau masih kontroversial sebab
masih didapati perbedaan-perbedaan dalam laporan studi di literatur (Licitra et al. 2003;
Lin, 2006)
Dosis radiasi untuk tumor primer biasanya diberikan 65-75 Gy dan pada kelenjar
leher 65-70 Gy. Dosis untuk terapi profilaktik pada leher dengan kelenjar negatif adalah
50-60 Gy (Wei dan Sham, 2005). Dosis radiasi perfraksi yang diberikan adalah 200 cGy
DT (dosis tumor) diberikan 5 kali seminggu untuk tumor primer maupun kelenjar.
Setelah itu radiasi dilanjutkan untuk tumor primer sehingga dosis total adalah 6000-7000
cGy pada tumor (Marzaini, 2002; Mould dan Tai, 2002; Licitra et al. 2003).
Dengan pemberian radioterapi saja telah berhasil mengontrol tumor T1 dan T2
pada 75-90% kasus dan tumor T3 dan T4 pada 50-75% kasus. Kontrol kelenjar leher
mencapai 90% pada kasus N0 dan N1, tapi tingkat kontrol berkurang menjadi 70% pada
Kemoterapi
Pemberian kemoterapi pada KNF diindikasikan pada kasus penyebaran ke
kelenjar getah bening leher, metastasis jauh dan kasus-kasus residif. Pemberian
kemoterapi terutama diberikan pada KNF dengan penyakit lokoregional tingkat lanjut
dikombinasikan dengan radioterapi. Kemoterapi dapat diberikan sebelum (neoadjuvan),
selama (concurrent) atau setelah (adjuvan) pemberian kemoterapi. Regimen kemoterapi
aktif antara lain : cisplatin, 5-fluorouracil (5-FU), doxorubicin, epirubicin, bleomycin,
mitoxantron, methotrexate dan alkaloid vinca (Zakifman, 2002; Cottrill dan Nutting,
2003; Lin, 2006).
Sebanyak 70% pasien yang baru terdiagnosa KNF datang pada stadium III dan
IV, dengan penyakit lokal lanjut tanpa metastase. Standar pengobatan adalah
radioterapi dikombinasikan dengan kemoterapi. Akan tetapi, waktu pemberian, dosis,
durasi dan regimen obat kemoterapi yang optimal masih tetap kontroversial sebab
masih didapati perbedaan-perbedaan dalam laporan studi di literatur (Agulnik dan Siu,
2005; Lin, 2006).
Dasar pemberian kemoterapi neoadjuvan/induksi kemoterapi dengan radioterapi
ada 2. Pertama : reduksi sitotoksik tumor primer dan kelenjar dapat meningkatkan
kontrol lokoregional. Kedua : eradikasi mikrometastase sistemik pada stadium dini dapat
mengurangi relaps metastase jauh. Pemberian kemoterapi saat siklus radioterapi
(concomitant) menawarkan potensi sensitisasi tumor terhadap radiasi dan juga
kemungkinan eradikasi mikrometastase. Akan tetapi juga menawarkan peningkatan
tidak berperan secara signifikan terhadap kontrol lokoregional (Mould dan Tai, 2002;
Cottrill dan Nutting, 2003).
Berdasarkan berbagai uji random yang telah dipublikasikan dengan tujuan
menilai penambahan kemoterapi pada radioterapi pada KNF lokal stadium lanjut, telah
diambil persetujuan umum bahwa kemoradioterapi concurrent sangat berguna, secara
konsisten menghasilkan keuntungan survival dibandingkan pemberian radioterapi saja,
mencapai tingkat overall survival (OS) 5 tahun sebesar 70% (Agulnik dan Siu, 2005;
Wei, 2006; Guigay et al. 2006).
Pemberian kemoterapi lanjutan terhadap kemoradioterapi concurrent, baik
sebagai neoadjuvan ataupun adjuvan, diperkirakan akan memperkuat kontrol penyakit.
Berdasarkan laporan-laporan terakhir, dipertimbangkan kombinasi kemoterapi
induksi/neoadjuvan diikuti terapi concurrent. Penggabungan bahan-bahan antikanker
terbaru yang kurang toksik dan lebih efektif seperti gemcitabine, taxane dan
bahan-bahan target molekular sebagai kombinasi regimen modalitas memerlukan eksplorasi
lebih lanjut dalam terapi KNF lokal stadium lanjut (Agulnik dan Siu, 2005)
Sampai sekarang, regimen dengan dasar platinum merupakan standar
kemoterapi pada pasien KNF dengan metastase, dan terapi lini pertama yang paling
banyak digunakan adalah kombinasi cisplatin dan 5-FU, yang mencapai ratio respon
66%-76% (Guigay et al. 2006; Wei, 2006). Kombinasi platinum dengan bahan baru
seperti gemcitabine atau paclitaxel telah menunjukkan respon yang baik (Guigay et al.
Pembedahan
Pembedahan hanya sedikit berperan dalam penatalaksanaan KNF. Terbatas
pada diseksi leher radikal untuk mengontrol kelenjar yang radioresisten dan metastase
leher setelah radioterapi, pada pasien tertentu pembedahan penyelamatan (salvage
treatment) dilakukan pada kasus rekurensi di nasofaring atau kelenjar leher tanpa
metastase jauh (Chew, 1997; Wei, 2003; Wei, 2006; Lutzky et al. 2008).
Terapi Target Molekuler
Dengan tujuan untuk meningkatkan proporsi survival jangka panjang pada pasien
KNF yang rekuren atau dengan metastase jauh, bahan sistemik yang lebih baik
diperlukan untuk meningkatkan respon komplet. Dengan potensi indeks terapetik yang
lebih tinggi, bahan-bahan target melokuler menampilkan senyawa-senyawa yang dapat
melengkapi penggunaan kemoterapi konvensional (Agulnik dan Siu, 2005).
Beberapa target molekuler telah diidentifikasi dalam spesimen tumor penderita
KNF. Ekspresi atau overekspresi reseptor-reseptor berikut telah dievaluasi pada KNF
yaitu : EGFR, cKIT c-erbB-2 (HER-2) dan VEGF (Vascular Endothelial Growth Factor),
yang merupakan faktor proangiogenik, yang berperan dalam angiogenesis untuk
pertumbuhan tumor, invasi dan metastase tumor (Agulnik dan Siu, 2005).
Saat ini target terapi dengan cetuximab (antibodi monoklonal EGFR) sedang
dalam perkembangan untuk pasien KNF rekuren atau dengan metastase (Agulnik dan
Siu, 2005; Guigay et al. 2006; Licitra et al. 2006). Terapi multitarget inhibitor tyrosine
kinase VEGF untuk KNF dengan metastase telah menunjukkan aktivitas pada studi fase
Manajemen Pada KNF Persisten atau Rekuren
Komplikasi lambat dapat timbul pada pasien yang bertahan hidup lama sebagai
akibat radiasi pada daerah sekitar nasofaring dan kelenjar leher. Komplikasi yang dapat
timbul yaitu pada neuroendokrin dan otologi, xerostomia, fibrosis jaringan lunak,
stenosis arteri karotid. Komplikasi neurologi yang menyulitkan seperti nekrosis lobus
temporal dan kelumpuhan syaraf kranial. Kemoterapi dengan cisplatin akan
meningkatkan efek samping otologi (Cottrill dan Nutting, 2003; Wei, 2006).
Remisi komplet KNF setelah terapi dapat dimonitor dengan pemeriksaan fisik,
pemeriksaan endoskopi dengan atau tanpa biopsi, dan pencitraan. Pemeriksaan
dengan PET lebih baik dibandingkan dengan CT atau MRI untuk mendeteksi tumor
yang persisten atau rekuren. Deteksi dini adanya relaps lokoregional sangat penting
karena tumor ini masih dapat ditolong jika dideteksi dini. Pada kasus persisten, baik
pada nasofaring ataupun kelenjar leher 10 minggu setelah terapi inisial telah komplet,
dapat dipertimbangkan terapi penyelamatan (salvage treatment) (Wei, 2006).
Walau kemoradioterapi concomitant cukup efektif pada terapi KNF, kegagalan
lokal atau regional sebagai tumor yang persisten atau rekuren dapat terjadi. Untuk
mempertahankan tingkat survival yang tinggi dibutuhkan deteksi dan terapi dini. Berikut
terapi yang dapat diberikan :
1. Tumor persisten atau rekuren pada kelenjar limfe leher : diseksi leher radikal, dapat
ditambahkan dengan brakiterapi bila tumor telah menyebar keluar batas kelenjar
leher.
2. Tumor persisten atau rekuren di nasofaring : radioterapi eksternal siklus kedua
radioterapi eksternal siklus kedua dikombinasi dengan kemoterapi concurrent ( Cottrill
dan Nutting, 2003; Wei, 2003; Wei, 2006).
2.2 Vascular Endothelial Growth Factor 2.2.1 Angiogenesis
Angiogenesis adalah pembentukan pembuluh darah baru yang berasal dari
pembuluh darah yang telah ada (Josko et al. 2000; Rosen, 2002). Angiogenesis sangat
dibutuhkan dalam pembentukan organ baru serta untuk diferensiasi saat embriogenesis,
penyembuhan luka dan fungsi reproduksi wanita (Josko et al. 2000; Rosen, 2002).
Angiogenesis kompensatori ditunjukkan dengan pembentukan pembuluh darah kolateral
jika terjadi kekurangan oksigen dan kekurangan nutrisi pada jaringan normal (Rosen,
2002). Angiogenesis dapat dipicu oleh berbagai kondisi patologis, seperti reumatoid
artritis, retinopati diabetik, degenerasi makular, psoriasis dan pertumbuhan serta
metastasis tumor (Rosen, 2002; Plank dan Sleeman, 2003).
Tumor membutuhkan angiogenesis untuk tumbuh di atas ukuran 1-2 mm3
(Rosen, 2002). Angiogenesis diperlukan untuk suplai oksigen, nutrien, faktor
pertumbuhan dan hormon, enzim proteolitik, mempengaruhi faktor hemostatik yang
mengontrol koagulasi dan sistem fibrinolitik, dan penyebaran sel-sel tumor ke tempat
jauh (Hicklin dan Ellis, 2005).
Angiogenesis merupakan proses yang sangat kompleks, yang diregulasi secara
ketat oleh faktor-faktor proangiogenik (VEGF, FGF, PDGF) dan faktor-faktor
antiangiogenik (Rosen, 2002; Hicklin dan Ellis, 2005). Suatu tumor avaskular
pembuangan produk sisa. Kebutuhan tumor terhadap nutrien berkembang sesuai
dengan volumenya, tetapi kemampuannya mengabsorbsi bahan-bahan melalui difusi
dari jaringan sekitar sesuai dengan luas permukaan tumor. Karena itu tumor tumbuh
hingga suatu ukuran maksimum hingga tumor mengalami defisiensi nutrien (biasanya di
bagian tengah tumor, dimana tingkat nutrien paling rendah) yang akan manghambat
proliferasi tumor hingga tumor berada dalam status diam. Hal ini membatasi ukuran
tumor sampai sekitar 2 mm, yang disebut keadaan dorman. Sel-sel tumor yang hipoksik
akan memproduksi faktor-faktor pertumbuhan angiogenik, termasuk VEGF. Tumor juga
memproduksi inhibitor endogen angiogenesis, seperti TGF- . Mulanya inhibitor melebihi
faktor pertumbuhan angiogenik dan sel endotel tetap diam. Akan tetapi, saat tumor
mampu memproduksi cukup faktor pertumbuhan dan/atau menekan ekspresi inhibitor,
akan terjadi ‘angiogenic switch’ menuju proses angiogenesis. (Plank dan Sleeman,
2003). ‘Angiogenic switch’ merupakan pertanda proses malignansi (Hicklin dan Ellis,
2005).
2.2.2 Angiogenesis Yang Diinduksi Tumor
Model terkini proses angiogenesis tumor menyarankan bahwa proses ini
melibatkan tumbuhnya tunas pembuluh dari pembuluh darah yang ada dan menyatunya
progenitor endotel menjadi pembuluh vaskular baru. Proses ini meliputi berbagai
kejadian yaitu proliferasi, migrasi dan invasi sel-sel endotel, organisasi sel-sel endotel
menjadi struktur tubular yang fungsional, maturasi pembuluh, dan regresi pembuluh.
(Detmar, 2000; Hicklin dan Ellis, 2005). Pada jaringan normal, kestabilan vaskular
terhadap stimulus angiogenik, sebaliknya angiogenesis tumor diinduksi oleh
peningkatan sekresi faktor angiogenik dan/atau oleh penurunan regulasi inhibitor
angiogenesis (Detmar, 2000).
Permulaan Angiogenesis
Pada permulaan angiogenesis, stimulus angiogenik yang diterima menyebabkan
sel endotel kapiler sekitar tumor teraktivasi, kontak yang erat dengan sel sekitar akan
menghilang dan mensekresi enzim proteolitik (protease) yang mempunyai efek
mendegradasi jaringan ekstraseluler. Ada banyak jenis enzim proteolitik tersebut, tetapi
secara garis besar dibagi menjadi matrix metalloproteases (MMPs) dan plasminogen
activator (PA)/sistem plasmin. Target awal protease adalah membran dasar. Setelah
terdegradasi, sel endotel akan dapat bergerak melalui gap yang ada pada membran
dasar menuju matriks ekstraseluler. Sel-sel endotel sekitar akan bergerak mengisi gap
pada membran dasar dan mengikuti sel-sel endotel sebelumnya menuju matriks
ekstraseluler. Karena itu, fungsi pertama faktor pertumbuhan angiogenik adalah
menstimulasi produksi protease oleh sel-sel endotel. Hal ini merupakan faktor kunci
pada rangkaian angiogenesis, sebab tanpa adanya aktivitas proteolitik, sel-sel endotel
akan dihambat oleh membran dasar hingga tidak dapat keluar dari kapiler (pembuluh)
induk (Plank dan Sleeman, 2003).
Migrasi Sel Endotel, Proliferasi dan Pembentukan Pembuluh
Setelah ekstravasasi, sel endotel terus mensekresi enzim proteolitik, yang akan
induk menuju tumor, membentuk tunas kecil. Sel endotel akan bertambah dari
pembuluh induk hingga tunas memanjang. Awalnya tunas-tunas ini bergerak paralel
satu sama lain, akan tetapi pada jarak tertentu dari pembuluh induk, mulai condong
menuju tunas lainnya. Hal ini akan membentuk loop tertutup (anastomose), yang akan
memungkinkan dimulainya sirkulasi pada pembuluh yang baru. Ini merupakan peristiwa
penting dalam pembentukan jaringan vaskular fungsional, akan tetapi stimulus yang
pasti terhadap perubahan arah tunas dan anastomosis masih belum diketahui (Plank
dan Sleeman, 2003).
Fase Vaskular
Dalam fase vaskular, pada angiogenesis fisiologis, ketika jaringan target telah
tervaskularisasi, ekspresi faktor pertumbuhan angiogenik akan berkurang. Migrasi,
proliferasi dan proteolisis sel-sel endotel akan berhenti dan pembuluh darah yang baru
terbentuk mengalami proses maturasi. Ikatan yang kuat antar sel distabilkan di endotel
dan sel endotel mensekresi protein (laminin, kolagen) untuk membentuk membran
dasar. Akhirnya sel-sel penyokong periendotel (perisit) direkrut dan pembuluh darah
baru menjadi bagian sistem vaskular yang stabil. Proses maturasi biasanya tidak terjadi
pada angiogenesis tumor, karena masih tetap terdapat daerah hipoksik di dalam tumor
yang tetap memproduksi faktor angiogenik. Selain itu, ketika daerah vaskularisasi yang
baru pada tumor terus bertambah, akan melebihi suplai darahnya sendiri sehingga
menimbulkan daerah hipoksik sendiri. Angiogenesis akan terus berlangsung dan
kapiler-kapiler baru terus tumbuh, meningkatkan suplai darah ke tumor yang sekarang
Akan tetapi, berlanjutnya angiogenesis akan meningkatkan pertumbuhan tumor,
yang akan membutuhkan suplai darah baru. Pada tumor yang sangat ganas, kebutuhan
akan pembuluh darah baru biasanya tidak pernah terpenuhi (Plank dan Sleeman, 2003).
Kapiler tumor biasanya tidak matang dan tidak stabil karena tidak terbentuknya
membran dasar, disebabkan faktor angiogenik terus diproduksi. Pembuluh baru akan
berbentuk ireguler, rapuh dan berliku-liku (Plank dan Sleeman, 2003).
2.2.3 Famili VEGF
Famili VEGF yang secara genetik berhubungan sebagai faktor pertumbuhan
angiogenik dan limfangiogenik terdiri dari 6 glikoprotein yaitu VEGF-A (biasa disebut
VEGF), VEGF-B, VEGF-C, VEGF-D, VEGF-E, dan placenta growth factor (PlGF)
(Hicklin dan Ellis, 2005).
In vivo, ekspresi VEGF-A telah menunjukkan peran kuncinya dalam
vaskulogenesis fisiologik dan angiogenesis. Pada tikus, delesi homozigot dan
heterozigot pada gen VEGF secara embrionik letal, menimbulkan defek pada
vaskulogenesis dan abnormalitas kardiovaskular. VEGF-A juga berperan penting dalam
proses angiogenik postnatal, termasuk penyembuhan luka, ovulasi, menstruasi,
mempertahankan tekanan darah serta kehamilan. VEGF-A juga telah dihubungkan
dengan berbagai kondisi patologis yang berkaitan dengan peningkatan angiogenesis,
seperti artritis, psoriasis, degenerasi makular dan retinopati diabetik (Hicklin dan Ellis,
2005).
Pada tikus, ketiadaan VEGF-B dan PlGF menunjukkan tidak ada defek pada
menyarankan bahwa peran VEGF-B dan PlGF mungkin berlebihan. Akan tetapi tidak
adanya PlGF akan mengganggu angiogenesis, ekstravasasi plasma, dan pertumbuhan
kolateral saat iskemia, peradangan, penyembuhan luka dan pertumbuhan tumor yang
menyarankan bahwa peran PlGF pada keadaan patologis yang terjadi pada orang
dewasa (Hicklin dan Ellis, 2005).
Homolog VEGF yaitu VEGF-C dan VEGF-D memegang peran kunci pada
limfangiogenesis saat embrionik dan postnatal. Delesi homozigot gen VEGF-C pada
tikus bersifat letal embrionik dan delesi heterozigot akan menyebabkan defek postnatal
yang berhubungan dengan defek perkembangan limfatik. VEGF-C dan VEGF-D
mungkin juga berperan dalam pertumbuhan pembuluh darah baru, terutama pada
keadaan patologik seperti pertumbuhan tumor. Akan tetapi perannya pada angiogenesis
tumor masih belum jelas. VEGF-E bukan homolog VEGF mamalia, tetapi protein viral
yang dikode virus Orf parapoxvirus (Hicklin dan Ellis, 2005; Guang, 2007).
2.2.4 Reseptor VEGF
Ligan VEGF menengahi efek angiogeniknya melalui reseptor yang berbeda. Dua
reseptor diidentifikasi pada sel endotel dikenal sebagai reseptor tirosin kinase spesifik
VEGFR-1 (fms-like tyrosine kinase1/Flt-1) dan VEGFR-2 (KDR/Flk-1). Saat ini VEGFR-3
(fms-like tyrosine kinase 4/Flt-4) telah diidentifikasi dan dihubungkan dengan proses
limfangiogenesis (Neufeld et al. 1999; Hicklin dan Ellis, 2005; Shibuya, 2006).
VEGFR-1 merupakan reseptor untuk VEGF-A dan mempunyai kemampuan untuk
mengikat VEGF-B dan PlGF. VEGFR-1 sangat penting untuk angiogenesis fisiologik
mempunyai peran fungsional positif pada beberapa tipe sel, yang berpartisipasi pada
migrasi monosit, rekrutmen progenitor sel endotel, meningkatkan sifat adesif sel-sel
natural killer, dan menginduksi faktor pertumbuhan dari sel-sel sinusoidal hati (Hicklin
dan Ellis, 2005; Shibuya, 2006).
Studi oleh Autiero dkk. menunjukkan aktivasi VEGFR-1 oleh PlGF menyebabkan
transfosforilasi VEGFR-2 pada sel endotel sehingga terjadi koekspresi terhadap
reseptor tersebut. Studi lain menunjukkan bahwa pada kondisi patologik seperti
tumorigenesis, VEGFR-1 merupakan regulator angiogenesis yang positif dan poten.
Bukti terakhir menyarankan fungsi VEGFR-1 berbeda sesuai tahap perkembangan,
berbagai kondisi patologik dan fisiologik, dan tipe sel dimana dia diekspresikan (Hicklin
dan Ellis, 2005; Shibuya, 2006).
VEGFR-2 menengahi mayoritas efek akhir VEGF-A pada angiogenesis, termasuk
permeabilitas mikrovaskular, proliferasi, invasi, migrasi dan survival sel endotel. Aktivasi
spesifik VEGFR-2 dengan VEGF-E telah menunjukkan aktivitas sel endotel yang poten
in vitro dan in vivo, dengan kuat menyokong gagasan bahwa aktivasi VEGFR-2 sendiri
dapat secara efisien menstimulasi angiogenesis. Seperti telah dijelaskan sebelumnya,
aktivasi dan sinyal VEGFR-2 dapat secara positif atau negatif dipengaruhi ko-ekspresi
dan aktivasi VEGFR-1 (Hicklin dan Ellis, 2005; Shibuya, 2006; Tabernero, 2007).
VEGFR-3 adalah reseptor tirosin kinase yang berasal dari klon lapisan sel
leukemia dan plasenta manusia. VEGFR-3 condong berikatan dengan VEGF-C dan
VEGF-D. VEGFR-3 diekspresikan melalui vaskulatur embrionik, tapi saat perkembangan
dan ketika dewasa, ekspresinya terbatas pada sel-sel endotel limfatik. Pada manusia
kardiovaskular dan pembentukan jaringan vaskular primer saat embriogenesis, dan
memfasilitasi limfangiogenesis ketika dewasa. Aktivasi dan peningkatan regulasi ligan
VEGFR-3 telah diobservasi pada beberapa neoplasma, seperti kanker payudara dan
melanoma, dengan peningkatan level VEGF-C dan VEGF-D yang berhubungan dengan
metastase kelenjar limfe pada pasien. Inhibisi sinyal VEGFR-3 dengan menggunakan
VEGFR-3 solubel menunjukkan pengurangan limfangiogenesis dan metastase kelenjar
limfe tumor (Hicklin dan Ellis, 2005; Shibuya, 2006).
2.2.5 Peran VEGF Pada Angiogenesis
Vascular Endothelial Growth Factor merupakan golongan faktor angiogenik
terbaik. Telah jelas ditemukan bahwa VEGF adalah kekuatan utama dibalik
angiogenesis tumor dan pembentukan seluruh pembuluh darah. Tiga aktivitas pokok sel
endotel dalam angiogenesis yaitu sekresi protease, migrasi dan proliferasi. VEGF
mampu memicu ketiga proses tersebut dan bekerja secara spesifik pada sel endotel
(VEGFR secara eksklusif terekspresi pada sel endotel). VEGF juga bertindak sebagai
faktor survival sel endotel dengan menghambat apoptosis. (Rosen, 2002; Plank dan
Sleeman, 2003). Fungsi VEGF pada sel endotel yaitu meningkatkan permeabilitas
vaskular 50.000 kali lebih poten dari histamin. VEGF mengaktivasi sel endotel dengan
efek perubahan morfologi sel endotel, perubahan cytoskeleton, dan menstimulasi
migrasi dan pertumbuhan sel endotel. VEGF bersifat mitogen terhadap sel endotel yang
menyebabkan proliferasi sel. VEGF juga menginduksi berbagai enzim dan protein yang
migrasi dan invasi yang merupakan tahap penting pada angiogenesis (Hicklin dan Ellis,
2005).
Permeabilitas
VEGF sebenarnya ditemukan karena kemampuannya membuat vena dan vena
kecil hiperpermeabel terhadap molekul makro dalam sirkulasi, sehingga pertama kali
disebut sebagai vascular permeability factor (VPF). Faktanya VEGF salah satu
penginduksi permeabilitas vaskular yang paling poten, 50.000 kali lebih poten dari
histamin. Kemampuannya untuk meningkatkan permeabilitas mikrovaskular merupakan
salah satu peran yang paling penting untuk VEGF, terutama dengan
mempertimbangkan hipermeabilitas pembuluh tumor yang diperkirakan berperan besar
untuk ekspresi VEGF pada sel-sel tumor (Hicklin dan Ellis, 2005).
Mekanisme pasti bagaimana VEGF meningkatkan permeabilitas mikrovaskular
belum sepenuhnya jelas. Studi terakhir menyarankan bahwa VEGF menginduksi
permeabilitas mungkin dimediasi via jalur calcium dependent yang melibatkan produksi
oksida nitrat dan aktivasi jalur Akt dan peningkatan cGMP, dengan aktivasi jalur Erk1/2
dengan cara stimulasi prostaglandin PGI2 (Hicklin dan Ellis, 2005).
Aktivasi Sel Endotel
VEGF menghasilkan berbagai efek yang berbeda pada sel-sel endotel dan
endotel vaskular. Efek-efek tersebut termasuk perubahan dalam morfologi sel endotel,
perubahan cytoskeleton, dan stimulasi pertumbuhan dan migrasi sel endotel. VEGF