SINTESIS NANOKOMPOSIT KAOLIN/TiO
2TEREMBAN
Fe
2O
3UNTUK ADSORPSI-FOTODEGRADASI
BIRU METILENA
INDRI DWI HANDAYANI
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM INSTITUT PERTANIAN BOGOR
PERNYATAAN MENGENAI SKRIPSI DAN
SUMBER INFORMASI SERTA PELIMPAHAN HAK CIPTA*
Dengan ini saya menyatakan bahwa skripsi berjudul Sintesis Nanokomposit Kaolin/TiO2 Teremban Fe2O3 untuk Adsorpsi-Fotodegradasi Biru Metilena adalah benar karya saya dengan arahan dari komisi pembimbing dan belum diajukan dalam bentuk apa pun kepada perguruan tinggi mana pun. Sumber informasi yang berasal atau dikutip dari karya yang diterbitkan maupun tidak diterbitkan dari penulis lain telah disebutkan dalam teks dan dicantumkan dalam Daftar Pustaka di bagian akhir disertasi ini.
Dengan ini saya melimpahkan hak cipta dari karya tulis saya kepada Institut Pertanian Bogor.
Bogor, Januari 2014
Indri Dwi Handayyani
ABSTRAK
INDRI DWI HANDAYANI. Sintesis Nanokomposit Kaolin/TiO2 Teremban Fe2O3 untuk Adsorpsi-Fotodegradasi Biru Metilena. Dibimbing oleh SRI SUGIARTI dan AHMAD SJAHRIZA.
Kaolin merupakan sejenis mineral lempung yang memiliki daya adsorpsi. Percobaan menunjukkan hasil pengukuran kapasitas adsorpsi kaolin sebesar 20.6 mg/g. Nilai ini lebih rendah dibandingkan zeolit yang umumnya memiliki kapasitas adsorpsi di atas 100 mg/g. Pencampuran kaolin dengan material lain membentuk nanokomposit, diharapkan dapat memperbaiki sifat adsorpsinya. Nanokomposit yang telah disintesis adalah nanokomposit kaolin/TiO2 yang teremban Fe2O3 menggunakan 2 metode sintesis. Nanokomposit disintesis dengan metode ball milling dan pasta. Nanokomposit dengan metode ball milling mampu meningkatkan daya adsorpsi yang lebih tinggi, yaitu 23.6 mg/g. Nanokomposit kaolin/TiO2 mampu mengadsorpsi sekaligus menguraikan limbah zat warna pada daerah ultraviolet. Tambahan Fe2O3 pada nanokomposit kaolin/TiO2 mampu meningkatkan kinerja nanokomposit dengan bereaksi di bawah sinar tampak. Maka, kinerja nanokomposit kaolin/TiO2 teremban Fe2O3 lebih efektif karena sinar tampak merupakan bagian terbesar dari sinar matahari.
Kata kunci: adsorpsi, fotodegradasi, kaolin, nanokomposit kaolin/TiO2/Fe2O3.
ABSTRACT
INDRI DWI HANDAYANI. Synthesis of Kaolin/TiO2 nanocomposite with Fe2O3 as Dopant for Adsorption-Photodegradation of Methylene Blue. Supervised by SRI SUGIARTI and AHMAD SJAHRIZA
Kaolin is a type of clay mineral that has adsorption capacity. The experiment shows that the adsorption capacity of kaolin was 20.6 mg/g. This value is lower than zeolite adsorption capacity that in general has value above 100 mg/g. Mixing kaolin with other materials to form nanocomposite, may improve its adsorption properties. Nanocomposites that had been synthesized were kaolin/TiO2 nanocomposites with the addition of Fe2O3 using 2 synthetic methods, namely using ball milling and paste methods. The nanocomposite synthesized using ball milling method had higher adsorption capacity value, i.e. 23.6 mg/g. The nanocomposite of kaolin/ TiO2 was able to adsorb and degrade waste dyes in ultraviolet range. Furthermore, addition of Fe2O3 to the kaolin/TiO2 nanocomposite improved the performance of the nanocomposite by reacting under the visible rays. Therefore, the performance of nanocomposite of kaolin/TiO2 added with Fe2O3 was is more effective since visible ray is the major part of the sun light. .
Skripsi
sebagai salah satu syarat untuk memperoleh gelar Sarjana Sains
pada
Departemen Kimia
SINTESIS NANOKOMPOSIT KAOLIN/TiO
2TEREMBAN
Fe
2O
3UNTUK ADSORPSI-FOTODEGRADASI
BIRU METILENA
INDRI DWI HANDAYANI
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
INSTITUT PERTANIAN BOGOR
Judul Skripsi : Sintesis Nanokomposit Kaolin/TiO2 Teremban Fe2O3 untuk Adsorpsi-Fotodegradasi Biru Metilena
Nama : Indri Dwi Handayani NIM : G44090078
Disetujui oleh
Sri Sugiarti, PhD Pembimbing I
Drs Ahmad Sjahriza Pembimbing II
Diketahui oleh
Prof Dr Dra Purwantiningsih Sugita, MS Ketua Departemen
PRAKATA
Puji dan syukur penulis panjatkan kepada Allah subhanahu wa ta’ala atas segala karunia-Nya sehingga karya ilmiah ini berhasil diselesaikan. Tema yang dipilih dalam penelitian yang dilaksanakan sejak bulan Maret 2013 ini ialah kaolin, dengan judul Sintesis Nanokomposit Kaolin/TiO2 Teremban Fe2O3 untuk Adsorpsi-Fotodegradasi Biru Metilena.
Terima kasih penulis ucapkan kepada Ibu Sri Sugiarti, PhD dan Bapak Drs Ahmad Sjahriza selaku pembimbing, dan Bapak Budi Arifin. Di samping itu, penghargaan penulis sampaikan kepada Shinta Purwasih dan Sara Aisyah Syafira selaku teman satu tema yang telah membantu selama penelitian dan pengumpulan data. Ungkapan terima kasih juga disampaikan kepada ayah, ibu, teman-teman Puri Fikriyyah (Yulia, Irma, Kania, Yuni, dan Sisil), teman-teman Primagama Quantumkids (Ka Nabil, Ka aga, Ka Wika, dan lainnya), teman-teman KIMIA 46, serta seluruh keluarga, atas segala doa dan dukungan semangatnya.
Semoga karya ilmiah ini bermanfaat.
Bogor, Januari 2014
DAFTAR ISI
DAFTAR GAMBAR vii
DAFTAR LAMPIRAN viii
PENDAHULUAN 1
Latar Belakang 1
Tujuan Penelitian 2
Manfaat Penelitian 2
Waktu dan Tempat 3
METODE 3
Alat dan Bahan 3
Prosedur Percobaan 3
HASIL DAN PEMBAHASAN 4
Nanokomposit Kaolin/TiO2/Fe2O3 4
Pencirian dengan difraktometer sinar-X (XRD) 5
Hasil Analisis Scanning Electron Microskop (SEM) 8
Kapasitas Adsorpsi Nanokomposit/TiO2 9
Kapasitas Adsorpsi Nanokomposit/TiO2/Fe2O3 10
Sifat Fotokatalis nanokomposit kaolin/TiO2 11
Sifat fotokatalis nanokomposit kaolin/TiO2/Fe2O3 14
Penyinaran di bawah sinar tampak 15
SIMPULAN DAN SARAN 18
Simpulan 18
Saran 18
DAFTAR PUSTAKA 18
LAMPIRAN 21
DAFTAR GAMBAR
1 Struktur kaolin (Sunardi 2011) 1
2 Struktur biru metilena (Hang dan Brindley 2006) 1 3 Pola difraksi XRD kaolin (Benea 2004) (a), TiO2 (Thamapat
2008) (b), dan Fe2O3 (Yue 2007) (c) 6
4 Reaksi perubahan kaolin menjadi metakaolin 6
5 Pola difraktogram nanokomposit kaolin/TiO2/Fe2O3 7 6 Morfologi nanokomposit (a) NKP dan (b) NKP-F 8 7 Kapasitas adsorpsi nanokomposit kaolin/TiO2 9 8 Kapasitas adsorpsi nanokomposit kaolin/TiO2 dengan Fe2O3 10
9 Kapasitas adsorpsi optimum 11
10 Filtrat uji fotokatalisis dibawah sinar UV; a=biru metilena, b=TiO2, c=Fe2O3, d=nanokomposit NBCa1, e=nanokomposit
NBCa0, dan f=nanokomposit NKP. 12
11 Spektrum uji fotokatalisis nanokomposit NBCa1 (A), nanokomposit NBCa0 (B), nanokomposit NKP (C) dengan sinar
UV 12
12 Endapan hasil uji fotokatalisis dibawah sinar UV; a= biru metilena, b=TiO2, c=Fe2o3, d= nanokomposit NBCa1, e= nanokomposit NBCa0, dan f= nanokomposit NKP. 13 13 Filtrat uji fotokatalisis dibawah sinar UV; a= biru metilena, b=
nanokomposit NBCa1-F, c= nanokomposit NBCa0-F, dan d=
nanokomposit NKP-F. 14
14 Spektrum uji fotokatalisis nanokomposit NBCa1-F(A1), nanokomposit NBCa0-F(B1), dan nanokomposit NKP-F(C1)
dengan sinar UV 15
15 Endapan hasil uji fotokatalisis dibawah sinar UV; a= nanokomposit NBCa1-F, b= nanokomposit NBCa0-F, dan c=
nanokomposit NKP-F 15
16 Filtrat uji fotokatalisis; a= biru metilena, b=nanokomposit NBCa1-F, c= nanokomposit NBCa0-F, dan d= nanokomposit
NKP-F dibawah sinar tampak. 16
17 Spektrum uji fotokatalisis nanokomposit a=NBCa1-F, b=nanokomposit NKP-F, dan c= nanokomposit NBCa0-F
dibawah sinar tampak 16
18 Endapan hasil uji fotokatalisis dibawah sinar tampak; a= nanokompositNBCa1-F, b=nanokomposit NBCa0-F, dan
c=nanokomposit NKP-F. 17
DAFTAR LAMPIRAN
1 Lingkup Kerja 21
2 Panjang gelombang maksimum biru metilena 22
3 Konsentrasi dan absorbans larutan biru metilena pada kurva standar 23
4 Kapasitas adsorpsi kaolin 24
5 Kapasitas adsorpsi TiO2 25
6 Kapasitas adsorpsi Fe2O3 26
7 Kapasitas adsorpsi Kaolin - Bahan Pengikat 27
8 Kapasitas adsorpsi K:B:T (7:2:1) ball milling (Nanokomposit
NBCa1) 28
9 Kapasitas adsorpsi K:T (9:1) ball milling (Nanokomposit NBCa0) 29 10 Kapasitas adsorpsi K:B:T (7:2:1) pasta (Nanokomposit NKP) 30 11 Kapasitas adsorpsi K:B:T (7:2:1) ball milling/Fe2O3 (Nanokomposit
NBCa1-F) 31
12 Kapasitas adsorpsi K:T (9:1) ball milling/Fe2O3 (Nanokomposit
NBCa0-F ) 32
13 Kapasitas adsorpsi K:B:T (7:2:1) pasta/Fe2O3 (Nanokomposit
PENDAHULUAN
Latar Belakang
Kaolin merupakan endapan lempung yang sebagian besar terdiri atas mineral kaolinit, dengan rumus Al2O3.2SiO2.2H2O. Struktur kaolin berupa lapisan 1:1 dari lapisan oksida-Si (lapisan silikat) dan lapisan hidroksida-Al (lapisan aluminat) (Gambar 1).
Gambar 1 Struktur kaolin (Sunardi 2011)
Kaolin digunakan dalam industri seperti industri kertas sebagai filler dalam kertas, bahan campuran keramik, bahan untuk memutihkan dan meningkatkan kecerahan warna cat, dan sebagai aditif dalam industri kosmetik. Beberapa tahun terakhir, kaolin juga telah banyak digunakan dalam insektisida, pupuk, dan plastik (Jalaluddin 2005). Selain itu, kaolin juga dimanfaatkan dalam proses adsorpsi limbah zat warna industri tekstil. Zat warna yang sering dijerap salah satunya adalah zat warna biru metilena (Gambar 2).
Gambar 2 Struktur biru metilena (Hang dan Brindley 2006)
Biru metilena merupakan zat warna dasar yang penting dalam proses pewarnaan kulit, kain mori, kain katun, dan tanin (Hamdaoui and Chiha, 2006). Pada kenyataannya, kaolin belum banyak digunakan untuk adsorpsi karena daya adsorpsinya kecil dan zat warna tekstil yang diadsorpsi masih terakumulasi di dalam adsorben sehingga di kemudian hari berpotensi menimbulkan persoalan baru. Hal inilah yang menjadi dasar pengolahan kaolin lebih lanjut dengan modifikasi metode adsorpsi-fotodegradasi.
2
Saat ini, TiO2 lebih banyak digunakan dalam aplikasi fotokatalisis khususnya pengolahan limbah, karena mempunyai celah pita (band gap/Eg) yang besar (3.2 eV), stabil terhadap sinar, tidak beracun, oksidasi tinggi, dan tidak larut dalam kondisi percobaan (Linsebigler 1995). Suatu fotokatalis dengan band gap
yang besar mengindikasikan bahwa bahan tersebut mempunyai fotoaktivitas yang tinggi (Kunarti 2009).
Nisaa (2011) telah menyintesis nanokomposit kaolin/TiO2 yang dapat mengadsorpsi sekaligus mendegradasi limbah zat warna biru metilena di bawah sinar UV yang memiliki panjang gelombang lebih kecil dari sinar tampak. Pada kenyataannya, sinar tampaklah yang paling banyak terdapat dalam sinar matahari (50%), sedangkan sinar UV hanya terdapat sekitar 5%. Ketidakmampuan untuk memanfaatkan sinar tampak telah membatasi efisiensi reaksi fotokatalitik dengan energi matahari. Hal ini mendasari dibutuhkannya suatu bahan pengemban atau doping agar proses adsorpsi-fotodegradasi ini dapat berlangsung pada sinar tampak.
Bahan pengemban atau doping yang ditambahkan ke dalam sistem katalis dibagi menjadi 2 jenis, yaitu dopan non-logam dan logam. Oksida logam transisi, misalnya Fe2O3 dengan Eg = 2.2 eV (Wu et al. 2012) telah dilaporkan dapat berfungsi sebagai semikonduktor fotokatalis sehingga dapat mempercepat reaksi oksidasi yang diinduksi oleh sinar (Mondestov 1997). Choi et al. (1994) melaporkan bahwa dopan ion logam dapat memperbesar respons TiO2 terhadap spektrum sinar tampak. Penelitian Zhang et al. (2010) melaporkan bahwa penambahan dopan Fe2O3 ke dalam komposit N-TiO2 dapat meningkatkan daya adsorpsi foton pada rentang panjang gelombang yang lebih lebar.
Pada penelitian ini kaolin yang keberadaannya melimpah di alam digunakan dalam bentuk nanokomposit dengan TiO2 dan diemban dengan Fe2O3 agar memiliki sifat fotokatalis yang baik. Adsorben yang dihasilkan diharapkan dapat mengadsorpsi sekaligus mendegradasi zat warna biru metilena menjadi senyawa yang aman di lingkungan di bawah sinar tampak.
Tujuan Penelitian
Penelitian ini bertujuan menyintesis nanokomposit kaolin/TiO2 dengan Fe2O3 sebagai pengemban, uji adsorpsi dan uji fotodegradasi nanokomposit kaolin/TiO2/Fe2O3 terhadap zat warna biru metilena.
Manfaat Penelitian
3 Waktu dan Tempat
Penelitian dilaksanakan pada April sampai Juli 2013 di Laboratorium Kimia Anorganik, Laboratorium Kimia Organik, dan Laboratorium Biokimia, Balai Pengujian dan Identifikasi Barang Jakarta, Laboratorium Diklat Kehutanan, dan Laboratorium Bersama, Institut Pertanian Bogor.
METODE
Alat dan Bahan
Alat-alat yang digunakan pada penelitian ini adalah neraca analitik, peralatan kaca, oven, ball milling, sentrifuga, lampu biru 14 watt, spektrofotometer UV-tampak, mikroskop elektron pemayaran (SEM), dan difraktometer sinar-X (XRD).
Bahan yang digunakan pada penelitian ini antara lain kaolin dari Bangka Belitung, serbuk biru metilena, bahan pengikat, serbuk TiO2, serbuk Fe2O3 p.a Merck, dan kertas aluminium.
Prosedur Percobaan Sintesis Nanokomposit Kaolin/TiO2 (Nisaa 2011)
Nanokomposit kaolin/TiO2 dibuat dengan metode pasta dengan komposisi campuran kaolin-bahan pengikat-TiO2 (7:2:1). Campuran dibuat pasta dengan cara menambahkan akuades, kemudian pasta diaduk hingga homogen dan dikeringkan pada suhu 100 ºC selama 2 jam. Nanokomposit tersebut kemudian digerus menjadi bentuk serbuk (nanokomposit NKP). Nanokomposit dengan komposisi yang sama juga dibuat dengan menggunakan ball milling dengan kecepatan 300 rpm selama 4 jam (nanokomposit NBCa1). Metode ball milling
yang sama juga digunakan untuk menyintesis nanokomposit kaolin/TiO2 tanpa bahan pengikat, yaitu campuran kaolin-TiO2 (9:1) (nanokomposit NBCa0). Ketiga nanokomposit kaolin/TiO2 kemudian dianalisis dengan menggunakan SEM dan XRD.
Sintesis Nanokomposit Kaolin/TiO2 dengan Fe2O3 sebagai Pengemban (Calle
et al. 2008)
4
Penentuan Kapasitas Adsorpsi (Nisaa 2011)
Sebanyak 50 mg sampel nanokomposit dimasukkan ke dalam vial kemudian ditambahkan larutan biru metilena 25, 50, 75, 100, 150, 200, dan 300 mg/L sebanyak 15 mL. Larutan digojok selama 2 jam, kemudian disentrifugasi selama 15 menit. Konsentrasi supernatan (biru metilena) ditentukan dengan spektrofotometer UV-tampak pada panjang gelombang maksimum.
Larutan stok biru metilena 1000 mg/L dibuat dengan cara melarutkan 1000 mg serbuk biru metilena dalam air suling dan diencerkan hingga 1 L. Deret larutan standar dibuat dari larutan tersebut dengan konsentrasi 0.5, 1, 1.5, 2, 2.5, dan 3 mg/L. Panjang gelombang maksimum ditentukan dengan mengukur serapan larutan biru metilena dengan spektrofotometer UV-tampak pada rentang 600-700 nm.
Uji Sifat Fotokatalis (Nisaa 2011)
Sebanyak 100 mg nanokomposit dimasukkan ke dalam cawan petri kemudian ditambahkan 15 mL larutan biru metilena 100 mg/L. Sampel kemudian diletakkan dalam kotak tertutup dan disinari dengan lampu biru 14 watt dan lampu UV pada λ = 365 nm. Filtrat sampel dianalisis serapannya dengan spektrofotometer UV-Vis pada panjang gelombang 200-700 nm. Uji fotodegradasi nanokomposit juga dilakukan pada kaolin, TiO2, Fe2O3, dan bahan pengikat.
HASIL DAN PEMBAHASAN
Nanokomposit Kaolin/TiO2/Fe2O3
Nanokomposit kaolin/TiO2 disintesis dengan 2 cara pencampuran secara fisik, yaitu pasta dan ball milling. Nanokomposit merupakan material padat multifase dan setiap fase memiliki sedikitnya 1 dimensi dengan ukuran kurang dari 100 nm (Salim 2010). Hasil sintesis dalam penelitian ini dapat dikatakan nanokomposit karena salah satu bahan, yaitu TiO2 yang dicampurkan dengan kaolin berukuran kurang dari 100 nm.
Komposisi TiO2 hanya 10% dari total nanokomposit karena jika lebih dari itu, nanokomposit akan terurai dalam larutan. Penambahan bahan pengikat digunakan untuk mengikat kedua bahan agar nanokomposit lebih homogen dan tidak mudah terurai dalam larutan. Nanokomposit dengan penambahan bahan pengikat kurang dari 20% akan hancur saat dilarutkan dalam air (Nisaa 2011).
Nanokomposit yang diperoleh dengan metode ball milling terlihat lebih homogen dan tercampur secara merata dibandingkan dengan metode pasta. Kecepatan ball milling saat sintesis ialah 300 rpm selama 4 jam. Menurut Alfatah (2012), pada kecepatan 300 rpm, energi dari ball milling cukup untuk menghancurkan serbuk menjadi lebih kecil sehingga luas permukaan bertambah dan dapat meningkatkan daya adsorpsi kaolin.
5 komponen doblet. Satu komponen sekstet menunjukkan adanya logam besi atau hematit yang berasal dari serbuk Fe2O3, sementara 2 komponen doblet dihasilkan dari Fe2+ dan Fe3+ pada posisi oktahedral. Doblet Fe3+ dapat berasal dari Fe yang masuk ke dalam struktur TiO2 dan ion Fe2+ yang menempel pada permukaan TiO2 atau besi yang menyebar di seluruh bagian TiO2 (Calle et al 2008). Komposisi bahan pengemban yang kecil diharapkan mampu meningkatkan sifat fotodegradasi nanokomposit sehingga dapat bergeser ke arah sinar tampak.
Spektrum XRD
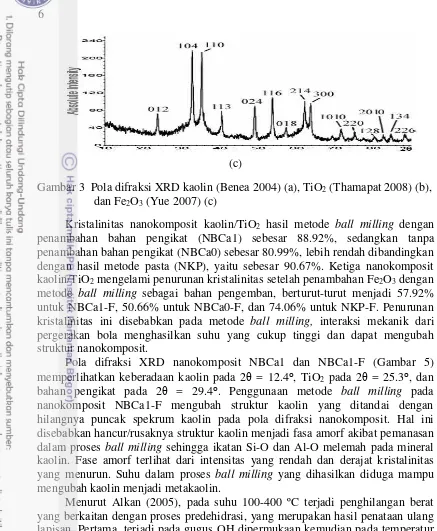
Analisis XRD nanokomposit kaolin/TiO2 dapat mengindetifikasi terbentuknya nanokomposit dan kristalinitasnya berdasarkan nilai 2θ dan intensitas puncak-puncak dalam spektrum dari setiap sampel (Kunarti 2009). Setiap puncak XRD mewakili 1 bidang kristal yang memiliki orientasi tertentu dalam sumbu tiga dimensi. Pola difraksi kaolin (Gambar 3a) menunjukkan puncak khas pada 2θ = 12⁰ dan 24⁰. Spektrum TiO2 murni (Gambar 3b) memiliki puncak pada 2θ = 25⁰, dan spekrum Fe2O3 murni (Gambar 3c) menunjukkan puncak khas pada 2θ = 33⁰ dan 48⁰.
.
(a)
6
(c)
Gambar 3 Pola difraksi XRD kaolin (Benea 2004) (a), TiO2 (Thamapat 2008) (b), dan Fe2O3 (Yue 2007) (c)
Kristalinitas nanokomposit kaolin/TiO2 hasil metode ball milling dengan penambahan bahan pengikat (NBCa1) sebesar 88.92%, sedangkan tanpa penambahan bahan pengikat (NBCa0) sebesar 80.99%, lebih rendah dibandingkan dengan hasil metode pasta (NKP), yaitu sebesar 90.67%. Ketiga nanokomposit kaolin/TiO2 mengelami penurunan kristalinitas setelah penambahan Fe2O3 dengan metode ball milling sebagai bahan pengemban, berturut-turut menjadi 57.92% untuk NBCa1-F, 50.66% untuk NBCa0-F, dan 74.06% untuk NKP-F. Penurunan kristalinitas ini disebabkan pada metode ball milling, interaksi mekanik dari pergerakan bola menghasilkan suhu yang cukup tinggi dan dapat mengubah struktur nanokomposit.
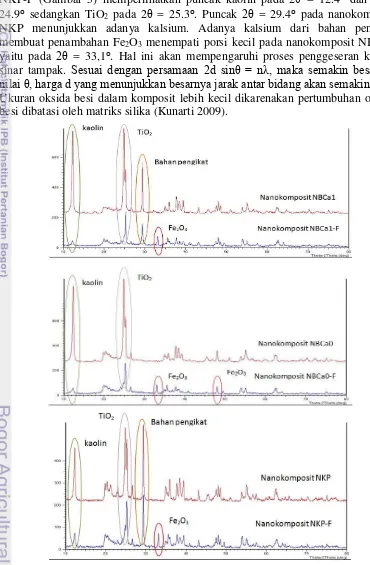
Pola difraksi XRD nanokomposit NBCa1 dan NBCa1-F (Gambar 5) memperlihatkan keberadaan kaolin pada 2θ = 12.4⁰, TiO2 pada 2θ = 25.3⁰, dan bahan pengikat pada 2θ = 29.4⁰. Penggunaan metode ball milling pada nanokomposit NBCa1-F mengubah struktur kaolin yang ditandai dengan hilangnya puncak spekrum kaolin pada pola difraksi nanokomposit. Hal ini disebabkan hancur/rusaknya struktur kaolin menjadi fasa amorf akibat pemanasan dalam proses ball milling sehingga ikatan Si-O dan Al-O melemah pada mineral kaolin. Fase amorf terlihat dari intensitas yang rendah dan derajat kristalinitas yang menurun. Suhu dalam proses ball milling yang dihasilkan diduga mampu mengubah kaolin menjadi metakaolin.
Menurut Alkan (2005), pada suhu 100-400 ºC terjadi penghilangan berat yang berkaitan dengan proses predehidrasi, yang merupakan hasil penataan ulang lapisan. Pertama, terjadi pada gugus OH dipermukaan kemudian pada temperatur 400-800 ºC terjadi proses dehidroksilasi penghilangan gugus OH pada kaolin dan terjadi pembentukan metakaolin dengan fasa amorf. Reaksi yang terjadi (Sudaryo 2011):
Gambar 4 Reaksi perubahan kaolin menjadi metakaolin
7 ditempati oleh Fe2O3 sehingga porsi untuk Fe2O3 menjadi labih banyak pada nanokomposit NBCa0-F.
Nanokomposit NKP dengan metode pasta memiliki kristalinitas 90.67%. Metode pasta mamliki kristalinitas paling besar dibandingkan dengan metode ball milling. Hal ini terjadi karena tidak adanya pengaruh interaksi mekanik yang dapat merusak struktur nanokomposit. Pola difraksi nanokomposit NKP dan NKP-F (Gambar 5) memperlihatkan puncak kaolin pada 2θ = 12.4⁰ dan 2θ = 24.9⁰ sedangkan TiO2 pada 2θ = 25.3⁰. Puncak 2θ = 29.4⁰ pada nanokomposit NKP menunjukkan adanya kalsium. Adanya kalsium dari bahan pengikat membuat penambahan Fe2O3 menempati porsi kecil pada nanokomposit NKP-F, yaitu pada 2θ = 33,1⁰. Hal ini akan mempengaruhi proses penggeseran kearah sinar tampak. Sesuai dengan persamaan 2d sinθ = nλ, maka semakin besarnya
nilai θ, harga d yang menunjukkan besarnya jarak antar bidang akan semakin kecil.
Ukuran oksida besi dalam komposit lebih kecil dikarenakan pertumbuhan oksida besi dibatasi oleh matriks silika (Kunarti 2009).
8
Penambahan Fe2O3 pada nanokomposit menyebabkan menyatu atau bergabungnya semua ion Fe pada nanokomposit kaolin/TiO2 dan menggantikan sebagian posisi nanokomposit tersebut (Nguyen et al. 2011). Fernandez (2012) menyatakan keberhasilan terlapisinya Fe2O3 pada nanokomposit ditandai dengan terjadinya pengurangan intensitas dan pergeseran puncak serapan. Intensitas puncak difraksi yang tidak cukup tinggi disebabkan karena diperolehnya struktur amorf atau stuktur kristal dengan tingkat keteraturan yang rendah (Toifur 2004). Dapat dikatakan bahwa intensitas yang rendah pada nanokomposit setelah penambahan Fe2O3 merubah struktur kaolin menjadi metakaolin yang bersifat amorf karena pengaruh suhu pada proses ball milling.
Morfologi SEM
Analisis menggunakan SEM dapat memperlihatkan morfologi, kehomogenan permukaan, dan distribusi partikel pada nanokomposit. Hasil analisis SEM diujikan pada nanokomposit NKP dan NKP-F (Gambar 6). Hal ini dimaksudkan untuk melihat perubahan struktur permukaan nanokomposit NKP dengan metode pasta yang selanjutnya ditambahkan Fe2O3 sebagai pengemban dengan metode ball milling. Nanokomposit NKP terlihat bongkahan seperti serabut lembaran warna putih dengan ukuran yang hampir seragam.
(a) (b)
Gambar 6 Morfologi nanokomposit (a) NKP dan (b) NKP-F
9 Kapasitas Adsorpsi Nanokomposit/TiO2
Kapasitas adsorpsi untuk kaolin sebesar 20.6122 mg/g (Lampiran 4). Adsorpsi kaolin masih terbilang rendah karena bentuk struktur kaolin yang terdiri atas lapisan 1:1. Pengertian lapisan 1:1 adalah untuk setiap satuan mineral terdiri atas satu lapisan oksida-Si (lapisan silikat) dan satu lapisan hidroksida-Al (lapisan aluminat) berikatan kuat sesamanya. Hal ini mengakibatkan kation atau anion dan molekul air tidak dapat masuk ke lapisan silikat maupun aluminat sehingga efektivitas penjerapannya terbatas hanya di permukaan saja (Muhdarina dan Linggawati 2003).
Nilai kapasitas adsorpsi TiO2 sebesar 5.3572 mg/g (Lampiran 5), untuk Fe2O3 sebesar 1.0244 mg/g (Lampiran 6), dan kaolin/bahan pengikat sebesar 19.4220 mg/g (Lampiran 7). Penurunan kapasitas adsorpsi optimum kaolin setelah penambahan bahan pengikat mengindikasikan bahwa bahan pengikat dapat menutupi sebagian permukaan kaolin yang dapat menurunkan daya adsorpsi kaolin.
Hasil sintesis kaolin dengan TiO2 menyebabkan penurunan daya adsorpsi dari masing-masing nanokomposit. Kenaikan konsentrasi biru metilena tidak diikuti dengan kenaikan kapasitas adsorpsi nanokomposit. Kapasitas adsorpsi maksimum dari nanokomposit NBCa1 sebesar 17.7978 mg/g, nanokomposit NBCa0 sebesar 17.9938 mg/g, dan nanokomposit NKP sebesar 16.0516 mg/g. Penurunan kapasitas adsorpsi nanokomposit kaolin/TiO2 dimungkinkan terjadi karena TiO2 tidak menyebar secara merata pada permukaan kaolin dan sebagian dari TiO2 menutupi pori kaolin sehingga memperkecil daya adsorpsi kaolin.
Gambar 7 Kapasitas adsorpsi nanokomposit kaolin/TiO2
Hasil penentuan kapasitas adsorpsi dari ketiga nanokomposit (Gambar 7) terlihat bahwa nonokomposit NKP dengan metode pasta memiliki kapasitas adsorpsi yang paling kecil, yaitu 16.0516 mg/g. Hal ini dapat diartikan bahwa metode ball milling dapat memperkecil ukuran partikel nanokomposit kaolin/TiO2 sehingga daya adsorpsi dengan biru metilena menjadi lebih baik.
Dalam kajian adsorpsi, waktu kontak yang cukup diperlukan untuk mencapai kesetimbangan adsorpsi. Jika fase cair yang berisi adsorben dalam
10
keadaan diam, maka difusi adsorbat melalui permukaan adsorben akan lambat dan merupakan tahap penentu kecepatan adsorpsi sehingga diperlukan penggojokan untuk mempercepat proses adsorpsi. Kecepatan penggojokan diperlukan dalam adsorpsi karena berpengaruh pada kecepatan interaksi antara adsorbat dengan adsorben.
Kapasitas Adsorpsi Nanokomposit/TiO2/Fe2O3
Penambahan Fe2O3 sebagai bahan pengemban dengan metode ball milling
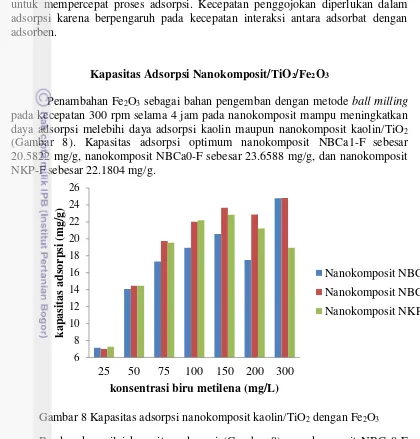
pada kecepatan 300 rpm selama 4 jam pada nanokomposit mampu meningkatkan daya adsorpsi melebihi daya adsorpsi kaolin maupun nanokomposit kaolin/TiO2 (Gambar 8). Kapasitas adsorpsi optimum nanokomposit NBCa1-F sebesar 20.5822 mg/g, nanokomposit NBCa0-F sebesar 23.6588 mg/g, dan nanokomposit NKP-F sebesar 22.1804 mg/g.
Gambar 8 Kapasitas adsorpsi nanokomposit kaolin/TiO2 dengan Fe2O3 Berdasarkan nilai kapasitas adsorpsi (Gambar 8), nanokomposit NBCa0-F dengan metode ball milling memiliki daya adsorpsi paling tinggi. Nilai kapasitas adsorpsi ini terkait dengan hasil XRD nanokomposit NBCa0-F dengan keberadaan Fe2O3 yang menempati porsi yang lebih besar karena ketiadaan bahan pengikat sehingga tidak ada bahan lain yang menutupi pori nanokomposit yang dapat menurunkan daya adsorpsi.
Perbedaan metode pasta dengan ball milling dapat terlihat dari hasil daya adsorpsi masing-masing nanokomposit. Pada Gambar 9 terlihat bahwa metode
11
Gambar 9 Kapasitas adsorpsi optimum
Keterkaitan kapasitas adsorpsi dengan hasil SEM terlihat pada luas permukaan spesifik dan volume total pori yang bertambah, oleh karena proses pembentukan oksida besi di dalam antarlapis dan permukaan nanokomposit. Dengan pertambahan ukuran pori ini, adsorpsi biru metilena lebih efektif dan fotodegradasi yang terjadi lebih efektif juga.
Sifat Fotokatalis Nanokomposit Kaolin/TiO2
Pada penelitian ini dilakukan uji sifat fotokatalisis dari nanokomposit perpaduan antara kaolin yang memiliki daya adsorpsi dengan kemampuan TiO2 dalam menguraikan zat warna sehingga nanokomposit kaolin/TiO2 ini mampu mengadsorpsi sekaligus menguraikannya menjadi komponen-komponen yang lebih sederhana dan aman bagi lingkungan. Uji sifat fotokatalis dilakukan di bawah penyinaran lampu UV pada panjang gelombang 365 nm dan penyinaran di bawah sinar tampak menggunakan lampu biru.
Konsentrasi larutan biru metilena yang digunakan sebesar 100 mg/L dengan lama penyinaran 6 jam. Semakin lama waktu penyinaran, maka waktu kontak antara biru metilena dengan nanokomposit semakin lama. Hal ini akan meningkatkan efektivitas proses fotodegradasi nanokomposit.
Filtrat hasil penyinaran selama 6 jam memperlihatkan warna biru yang lebih pudar dibandingkan warna biru metilena (Gambar 10). Filtrat kemudian diukur spektrumnya dengan menggunakan spektrofotometer UV-Vis pada panjang gelombang 200-700 nm. Puncak spektrum serapan biru metilena berada pada λ = 664,5 nm. Serapan spektrum ketiga nanokomposit NBCa1, NBCa0, NKP (Gambar 11) berada dibawah puncak biru metilena yang menandakan telah berkurangnya keberadaan biru metilena di dalam filtrat nanokomposit.
14 16 18 20 22 24
12
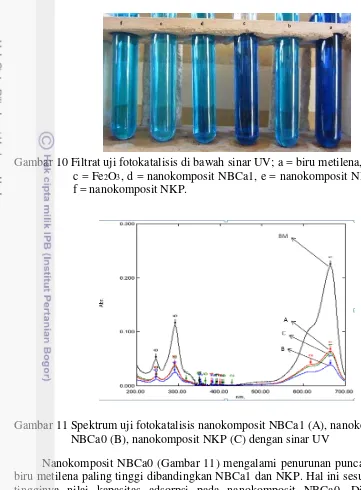
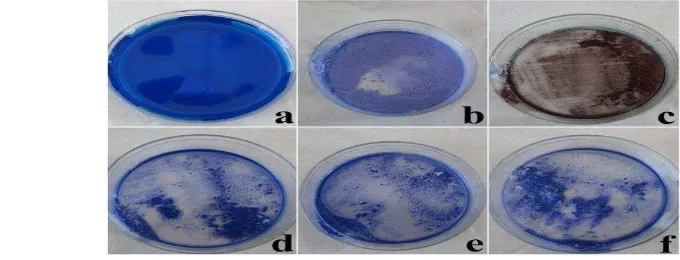
Gambar 10 Filtrat uji fotokatalisis di bawah sinar UV; a = biru metilena, b = TiO2, c = Fe2O3, d = nanokomposit NBCa1, e = nanokomposit NBCa0, dan f = nanokomposit NKP.
Gambar 11 Spektrum uji fotokatalisis nanokomposit NBCa1 (A), nanokomposit NBCa0 (B), nanokomposit NKP (C) dengan sinar UV
Nanokomposit NBCa0 (Gambar 11) mengalami penurunan puncak serapan biru metilena paling tinggi dibandingkan NBCa1 dan NKP. Hal ini sesuai dengan tingginya nilai kapasitas adsorpsi pada nanokomposit NBCa0. Dilihat dari komposisi nanokomposit NBCa0 tanpa bahan pengikat memungkinkan tidak adanya bahan lain selain kaolin dan TiO2 yang dapat menghambat proses adsorpsi nonokomposit tersebut.
Menurut Wijaya (2006) reaksi fotodegradasi terkatalisis pada sampel nanokomposit memerlukan empat komponen yaitu, sumber sinar (foton) dari sinar UV dan sinar tampak, senyawa target berupa zat warna biru metilena, oksigen sebagai penangkap elektron, dan fotokatalis nanokomposit kaolin/TiO2. Fase anatase pada TiO2 dikenal sebagai kristal yang paling reaktif terhadap sinar. Anatase memiliki aktivitas fotokatalitik terbaik, eksitasi elektron ke pita konduksi dapat dengan mudah terjadi apabila kristal ini dikenai sinar dengan energi yang lebih besar dari pada celah energinya (Setiawati 2006).
13 dari pita valensi ke pita konduksi yang akan menghasilkan elektron (e-cb) dan menyebabkan adanya kekosongan atau hole (h+vb) (Wijaya et al. 2006). Selanjutnya, hole (h+vb) akan bereaksi dengan air yang akan membentuk radikal hidroksida logam (HO●) sebagai oksidator kuat untuk mengoksidasi biru metilena. Elektron (e-cb) pada permukaan semikonduktor dapat terjebak dalam hidroksida logam dan bereaksi dengan O2 akan menghasilkan radikal superoksida (O2-●) sebagai reduktor yang akan mereduksi biru metilena di dalam larutan. Radikal-radikal ini akan terus-menerus terbentuk selama biru metilena masih dikenai sinar ultraviolet dan selama itu pula radikal-radikal tersebut akan menyerang biru metilena di permukaan katalis (Nogueira et al. 1993). Mekanisme reaksi yang terjadi pada proses fotodegradasi dengan TiO2 adalah sebagai berikut:
TiO2 + UVTiO2 (e- cb + h+ vb) TiO2 (h+) + H2O TiO2 + HO● + H+ TiO2 (e-) + O2 TiO2 + O2-*
zat warna + O2 -● produk degradasi
Hasil fotodegradasi tidak hanya terlihat dari warna filtrat dan spektrum hasil spektrofotometer UV-Vis yang diujikan setelah penyinaran dibawah sinar UV. Cara lain yang dilakukan untuk melihat hasil degradasi dari nanokomposit terlihat dari warna endapan yang dihasilkan. Perubahan warna pada endapan setelah dilakukan penyinaran dibawah sinar UV dapat dijadikan salah satu indikator terjadinya fotodegradasi.
Endapan berwarna biru menunjukkan bahwa nanokomposit hanya mengalami adsorpsi, sedangkan bila endapan berwarna putih maka nanokomposit tidak hanya mengalami adsorpsi tetapi sekaligus mengalami fotodegradasi. Endapan yang terjadi pada TiO2, Fe2O3, dan nanokomposit NBCa1, NBCa0, NKP (Gambar 12) terlihat warna biru yang lebih memudar dari larutan biru metilena yang menandakan bahwa nanokomposit mengalami proses adsorpsi. Endapan warna putih terlihat dalam jumlah yang sangat kecil menandakan nanokomposit mengalami fotodegradasi yang rendah pada konsentrasi 100 ppm dibawah sinar UV.
14
Sifat Fotokatalis Nanokomposit Kaolin/TiO2/Fe2O3
Penambahan Fe2O3 sebagai bahan pengemban pada nanokomposit juga dilakukan uji fotokatalisis dibawah penyinaran lampu UV selam 6 jam. Filtrat yang dihasilkan (Gambar 13) terlihat memiliki warna biru yang semakin memudar dari warna larutan biru metilena.dapat dikatakan bahwa keberadaan biru metilena pada nanokomposit NBCa1-F, NBCa0-F, dan NKP-F sudah jauh menurun dibawah sinar UV.
Gambar 13 Filtrat uji fotokatalisis di bawah sinar UV; a = biru metilena, b= nanokomposit NBCa1-F, c = nanokomposit NBCa0-F, dan d= nanokomposit NKP-F.
15
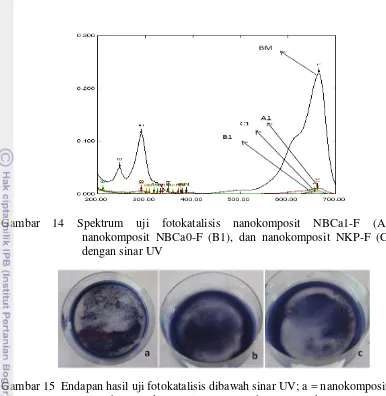
Gambar 14 Spektrum uji fotokatalisis nanokomposit NBCa1-F (A1), nanokomposit NBCa0-F (B1), dan nanokomposit NKP-F (C1) dengan sinar UV
Gambar 15 Endapan hasil uji fotokatalisis dibawah sinar UV; a = nanokomposit NBCa1-F, b = nanokomposit NBCa0-F, dan c = nanokomposit NKP-F Hasil penelitian menunjukkan bahwa efektivitas fotodegradasi terkatalisis nanokomposit kaolin/TiO2 dengan penambahan Fe2O3 lebih tinggi dibandingkan dengan nanokomposit kaolin/TiO2. Hal ini menunjukkan terdispersinya oksida besi dalam silika pada nanokomposit. Dengan oksida besi yang terdispersi dalam nanokomposit maka ukuran oksida besi lebih kecil atau luas permukaannya lebih besar daripada oksida besi tanpa nanokomposit. Hal ini berpengaruh dalam peningkatan fotoaktivitas.
Menurut Kunarti (2009), Fe2O3 mudah mengalami fotoreduksi yang berakibat pada pelarutan oksida yang menyebabkan larutan menjadi keruh sehingga mengganggu proses penyerapan sinar oleh fotokatalis. Pencegahan pelarutan dapat dilakukan dengan cara mengombinasikan oksida besi dengan matriks seperti kaolin dengan membuatnya menjadi komposit oksida besi-silika.
Penyinaran Di bawah Sinar Tampak
16
serapannya dengan spektrofotometer UV-Vis pada panjang gelombang 200-700 nm. Spektrum serapan yang dihasilkan dibawah sinar tampak berada dibawah serapan biru metilena.
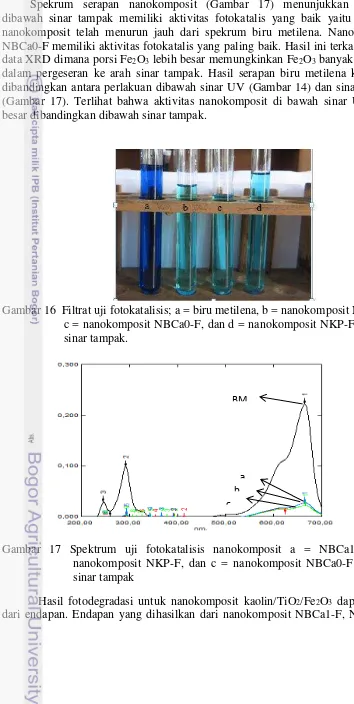
Spekrum serapan nanokomposit (Gambar 17) menunjukkan aktivitas dibawah sinar tampak memiliki aktivitas fotokatalis yang baik yaitu spekrum nanokomposit telah menurun jauh dari spekrum biru metilena. Nanokomposit NBCa0-F memiliki aktivitas fotokatalis yang paling baik. Hasil ini terkait dengan data XRD dimana porsi Fe2O3 lebih besar memungkinkan Fe2O3 banyak berperan dalam pergeseran ke arah sinar tampak. Hasil serapan biru metilena kemudian dibandingkan antara perlakuan dibawah sinar UV (Gambar 14) dan sinar tampak (Gambar 17). Terlihat bahwa aktivitas nanokomposit di bawah sinar UV lebih besar dibandingkan dibawah sinar tampak.
Gambar 16 Filtrat uji fotokatalisis; a = biru metilena, b = nanokomposit NBCa1-F, c = nanokomposit NBCa0-F, dan d = nanokomposit NKP-F dibawah sinar tampak.
Gambar 17 Spektrum uji fotokatalisis nanokomposit a = NBCa1-F, b = nanokomposit NKP-F, dan c = nanokomposit NBCa0-F dibawah sinar tampak
Hasil fotodegradasi untuk nanokomposit kaolin/TiO2/Fe2O3 dapat dilihat dari endapan. Endapan yang dihasilkan dari nanokomposit NBCa1-F, NBCa0-F,
BM
17 dan NKP-F (Gambar 18) menunjukkan warna biru kemerahan. Hasil endapan yang dihasilkan dapat diartikan bahwa nanokomposit mampu mengadsorpsi biru metilena tetapi tidak mengalami proses fotodegradasi dibawah sinar tampak pada konsentrasi biru metilena 100 ppm. Hal ini dapat diartikan bahwa nanokomposit NBCa1-F, NBCa0-F, dan NKP-F mampu bereaksi di bawah sinar tampak yaitu mampu bereaksi pada panjang gelombang yang lebih besar dengan energi yang lebih kecil.
Gambar 18 Endapan hasil uji fotokatalisis dibawah sinar tampak; a = nanokompositNBCa1-F, b = nanokomposit NBCa0-F, dan c = nanokomposit NKP-F.
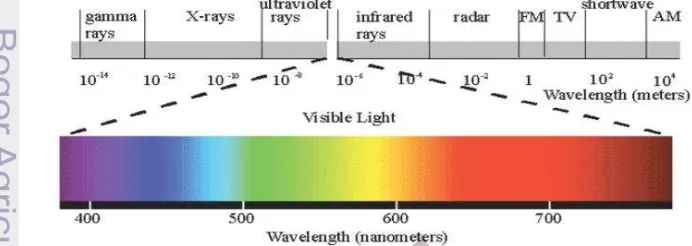
Sinar tampak adalah sebagian dari spektrum gelombang elektromagnet yang mempunyai panjang gelombang antara 400-800 nm (Gambar 19). Panjang gelombang yang berbeda-beda diinterpretasikan oleh otak manusia sebagai warna, dengan merah adalah panjang gelombang terpanjang (frekuensi paling rendah) hingga ke violet dengan panjang gelombang terpendek (frekuensi paling tinggi). Sinar dengan panjang gelombang di bawah 400 nmdan di atas 800 nmtidak dapat dilihat manusia dan disebut ultraviolet pada batas panjang gelombang pendek dan inframerah pada batas panjang gelombang terpanjang (Dewi 2006). Sinar tampak (380-780) nm, seperti yang dapat dilihat pada spektrum elektromagnetik, menyatakan gelombang pada daerah sempit yang terletak di antara ultraviolet
(UV) dan inframerah. Pada daerah inilah panjang gelombang tersebut dapat ditangkap oleh mata manusia dan direpresentasikan dalam bentuk warna. Selain itu, sinar tampak merupakan sinar yang keberadaannya paling banyak pada matahari. Salah satu sumber sinar tampak yang digunakan adalah lampu biru dengan kisaran panjang gelombang 492-455 nm (Ardy et al. 2007).
18
menyebabkan penyempitan band gap. Fe2O3 menyebabkan formasi dasar yang baru mendekat ke pita konduksi. Hal ini terjadi karena penambahan bahan pengemban Fe2O3 membuat struktur TiO2 anatase dapat berespon terhadap sinar tampak dengan memperkecil band gap. Oleh karena itu, doping oleh ion besi sangat meningkatkan aktivitas fotokatalisis di daerah sinar tampak. Nanokomposit kaolin/TiO2/Fe2O3 mampu mengadsorpsi biru metilena dengan baik dibawah sinar tampak tetapi tidak diikuti dengan kemampuan mendegradasi biru metilena.
SIMPULAN DAN SARAN
Simpulan
Nanokomposit kaolin/TiO2 dengan penambahan Fe2O3 sebagai bahan pengemban berhasil disintesis menggunakan metode ball milling dan metode pasta. Hal ini didukung dengan adanya puncak spekrum kaolin, TiO2, Fe2O3, dan bahan pengikat pada pola difraksi XRD. Kapasitas adsorpsi optimum pada kaolin sebesar 20.61 mg/g. Nanokomposit kaolin/TiO2/Fe2O3 menggunakan metode ball milling mampu meningkatkan daya adsorpsi yang lebih tinggi, yaitu sebesar 23.66 mg/g. Hasil fotodegradasi nanokomposit NBCa1-F, NBCa0-F, NKP mampu mengadsorpsi biru metilena dengan sangat baik tetapi proses fotodegradasinya yang masih rendah pada konsentrasi 100 ppm dibawah sinar ultraviolet. Penggunaan lampu biru pada uji fotokatalisis berhasil membuat nanokomposit kaolin/TiO2/Fe2O3 bereaksi di bawah sinar tampak.
Saran
Metode ball milling dapat dijadikan metode dalam mensistesis suatu nanokomposit karena dapat meningkatkan kapasitas adsorpsi. Diperlukan adanya variasi penambahan massa Fe2O3 sebagai bahan pengemban agar dihasilkan massa optimum yang dapat meningkatkan sifat fotodegradasi ke arah sinar tampak.
DAFTAR PUSTAKA
Akbar AG, Widyastuti. 2012. Pengaruh variasi penambahan Ni pada Mg dan variasi kecepatan milling dengan metode mechanical alloying terhadap sifat absorpsi dan desorpsi Mg sebagai material penyimpan hydrogen.
Jurnal Teknik Material dan Metalurgi POMITS. 1(1):1-4.
19 zeolite NaA from natural kaolinite. Microporous and Mesoporous Materials 86:176-184.
Ardi F, Suseno JE, Sofyan F. 2007. Pembuatan perangkat lunak untuk menentukan panjang gelombang berdasarkan spekrum cahaya tampak dengan metode jaringan syaraf tiruan menggunakan matlab 7.0 [catatan penelitian]. Semarang (ID): Universitas Diponegoro.
Benea M, Gorea M. 2004. Mineralogy and technological properties of some kaolin types used in the ceramic industry. Geologia. XLIX:33-39.
Calle AM, Sanchez LC, Arboleda JD, Beltran JJ, Barrero CA, Osorio J, Nomura K. 2008. Mixtures of iron and anatase TiO2 by mechanical alloying.
Microelectronics Journal. 39:1322–1323. www.elseiver.com/locate/mejo. Choi WY, Termin A, Hoffmann MR. 1994. The role of metal ion dopants in
quantumsized TiO2 correlation between photoreactivity and charge carrier recombination dynamics. Journal Phys Chem. 84:13669–13679. Dewi LA, Purwanto A, Kuswanto H. 2006. Pergeseran spektrum pada filamen
lampu wolfram. Di dalam: [nama editor tidak diketahui], editor. Seminar Nasional MIPA; 2006 Agu 01; Yogyakarta, Indonesia. Yogyakarta (ID): UNY Press. hlm 1-10.
Dhamayanti Y, Karna W, Tahir I. 2005. Fotodegradasi zat warna methyl orange menggunakan Fe2O3-montmorillonit dan sinar ultraviolet. Di dalam: [nama editor tidak diketahui], editor. Seminar Nasional DIES ke 50 FMIPA UGM; 2005 Sept 17; Yogyakarta, Indonesia. Yogyakarta (ID): UGM Press. hlm 1-8.
Fernandez BR. 2012. Sintesis, pelapisan dan stabilitas senyawa oksida besi oleh silika dan aplikasinya untuk amobilisasi protein [catatan penelitian]. Padang (ID): Pascasarjana Universitas Andalas.
Jalaluddin, Jamaludin T. 2005. Pemanfaatan kaolin sebagai bahan baku pembuatan aluminium sulfat dengan metode adsorpsi. Jurnal Sistem Teknik Industri. 6:5.
Hamdaoui O, Chiha M, 2006, Removal of methylene blue from aqueous solutions by wheat bran. Acta Chim.54:407–418.
Hang PT, Brindley GW. 2006. Methylene blue absorption by clay minerals determination of surface areas and cation exchange capacities (clay-organic studies XVIII). J. Clay Minerals. 18:203-212.
Khalil LB, Mourad WE, Rophael MW. 1998. Photocatalytic reduction of environmental pollutans Cr(VI) over some semiconductor under uv/visible light illumination. Appl Catal B:Environ. 173:267-273.
Kunarti ES, Wahyuni ET, Hermawan FE. 2009. Pengujian aktivitas komposit Fe2O3-SiO2 sebagai fotokatalis pada fotodegradasi 4-klorofenol. Jurnal Manusia dan Lingkungan. 16(1):54-64.
Linsebigler, Amy L. 1995. Photocatalysis on TiO2 surface: principle, mechanism, and selected result. Chemistry Revolusion. 95:735-758.
Muhdarina, Linggawati A. 2003. Pilarisasi kaolinit alam untuk meningkatkan kapasitas tukar kation. J Natur Indo. 6:20-23.
20
Nogueira RFP, Jardim WF. 1993. Photodegradation of methlene blue using solar light and semikonduktor (TiO2). J Chem Edu. 70(10):861-862. Nguyen VN, Nguyen NKT, Nguyen PH. 2011. Hydrothermal synthesis of
Fe-doped TiO2 nanostructure photocatalyst. Adv Nat Sci: Nanosci. Nanotechnol. 2:1-4.doi:10.1088/2043-6262/2/3/035014.
Nisaa Shofwatun. 2011. Adsorpsi Biru Metilena pada Kaolin dan Nanokomposit Kaolin/TiO2 serta Uji Sifat Fotokatalisis [skripsi]. Bogor(ID): Institut Pertanian Bogor.
Salim AA. 2010. Sintesis dan karakterisasi katalis nanokomposit berbasis titania untuk produksi hidrogen dari gliserol dan air [tesis]. Depok (ID): Universitas Indonesia.
Setiawati TS, Amalia IS, Sulistioso GS, Wisnu AA. 2006. Sintesis lapisan tipis TiO2 dan analisis sifat fotokatalisnya. Indonesian Journal of Materials Science. Edisi Khusus Oktober:141 – 146.
Sunardi, Irawati U, Wianto T. 20011. Karakterisasi kaolin lokal Kalimantan Selatan hasil kalsinasi. Jurnal Fisika FLUX. 8 (1):59-65.
Thamaphat K, Pichet L, Boonlaer N. Phase characterization of TiO2 powder by XRD and TEM. Kasetsart Journal Natural Science. 42(5).
Toifur Muhammad, Prayoto, Abraha Kamsul, dan Ridwan. 2004. Penghalusan kurva latar data spekrum XRD lapisan tipis Ni80Fe20. Prosiding of the First Jogja Regional Physics Conference.
Wijaya Karna, Sugiharto, Fatimah, Sudiono, Kurniyasih. 2006. Utilisasi TiO2-zeolit dan sinar UV untuk fotodegradasi zat warna congo red. Berkala MIPA. 16(3).
Wu HC, Li SH, Lin SW. 2012. Effect of Fe concentration on Fe-doped anatase TiO2 from GGA + U calculations. Internatioanl Journal of Photoenergy. 2012: 1-6.doi:10.1155/2012/frame,823498.
Yue W, Wuzong Z. 2007. Porous Crystals of Cubic metal oxides template by cage-containing mesoporous Silica. J Mater Chem. This journal is (c) The Royal Society of Chemistry 2007.
21 Lampiran 1 Lingkup Kerja
Kaolin, TiO2, Fe2O3, dan Bahan Pengikat
XRD dan SEM Nanokomposit
Kaolin/TiO2
XRD dan SEM
Sintesis Nanokomposit Kaolin/TiO2 dengan
Fe2O3
XRD dan SEM
Penentuan Kapasitas Adsorpsi
22
Lampiran 2 Panjang gelombang maksimum biru metilena
Panjang gelombang
(nm)
Absorbansi
660 0,068
660,5 0,068
661 0,069
661,5 0,069
662 0,069
662,5 0,07
663 0,07
663,5 0,07
664 0,07
664,5 0,07
665 0,07
665,5 0,07
666 0,07
666,5 0,069
667 0,069
667,5 0,069
668 0,068
668,5 0,068
23 Lampiran 3 Konsentrasi dan absorbans larutan biru metilena pada kurva standar
Sample Type Konsentrasi Absorbans
std 1 Standard 0,5 0,052
std 2 Standard 1,0 0,102
std 3 Standard 1,5 0,163
std 4 Standard 2,0 0,219
std 5 Standard 2,5 0,281
std 6 Standard 3,0 0,341
Gambar Kurva standar zat warna biru metilena
y = 0,1165x - 0,0108 R² = 0,9991
0 0,05 0,1 0,15 0,2 0,25 0,3 0,35 0,4
0,0 0,5 1,0 1,5 2,0 2,5 3,0 3,5
A
b
sor
b
an
s
24
Lampiran 4 Kapasitas adsorpsi kaolin
Co
25 0.0508 0.160 1.46757 0 1.4676 23.5324 6.9486
6.9254
25 0.0506 0.189 1.71669 0 1.7167 23.2833 6.9022
50 0.0503 0.314 2.79048 0 2.7905 47.2095 14.0784
14.0481
50 0.0506 0.305 2.71317 0 2.7132 47.2868 14.0178
75 0.0504 0.097 0.92638 10 9.2638 65.7362 19.5643
19.8058
75 0.0506 0.075 0.73739 10 7.3739 67.6261 20.0473
100 0.0501 0.158 1.45039 20 29.0078 70.9922 21.2551
20.6122
100 0.0501 0.183 1.66515 20 33.3030 66.6970 19.9692
150 0.0503 0.186 1.69092 50 84.5460 65.4540 19.5191
19.1989
150 0.0503 0.191 1.73387 50 86.6936 63.3064 18.8787
200 0.0500 0.305 2.71317 50 135.6584 64.3416 19.3025
20.3551
200 0.0505 0.287 2.55854 50 127.9272 72.0728 21.4078
300 0.0501 0.256 2.29224 100 229.2243 70.7757 21.1903
19.3724 300 0.0502 0.270 2.41251 100 241.2508 58.7492 17.5546
Contoh perhitungan:
Co : Konsentrasi awal larutan biru metilena (mg/L)
Ce : Konsentrasi akhir larutan biru metilena (mg/L)
25 Lampiran 5 Kapasitas adsorpsi TiO2
Co
25 0.0504 0.120 1.12396 10 11.2396 13.7604 4.0954
4.2793
25 0.0500 0.107 1.01228 10 10.1228 14.8772 4.4631
50 0.0505 0.169 1.54488 20 30.8977 19.1023 5.6740
5.3572
50 0.0502 0.182 1.65656 20 33.1312 16.8688 5.0405
75 0.0507 0.139 1.28717 50 64.3587 10.6413 3.1483
3.1514
75 0.0506 0.139 1.28717 50 64.3587 10.6413 3.1545
100 0.0507 0.097 0.92638 100 92.6381 7.3619 2.1781
2.0567
100 0.0504 0.098 0.93497 100 93.4971 6.5029 1.9354
150 0.0505 0.160 1.46757 100 146.7572 3.2428 0.9632
0.5805
150 0.0505 0.163 1.49334 100 149.3342 0.6658 0.1977
200 0.0504 0.226 2.03453 100 203.4533 -3.4533 -1.0278
-0.7711
200 0.0506 0.224 2.01735 100 201.7352 -1.7352 -0.5144
300 0.0502 0.176 1.60502 200 321.0034 -21.0034 -6.2759
-6.0135
300 0.0503 0.175 1.59643 200 319.853 -19.2853 -5.7511
Contoh perhitungan:
Co : Konsentrasi awal larutan biru metilena (mg/L)
Ce : Konsentrasi akhir larutan biru metilena (mg/L)
26
Lampiran 6 Kapasitas adsorpsi Fe2O3
Co
25 0.0507 0.113 1.06383 20 21.2765 3.7235 1.1016
1.0244
25 0.0508 0.116 1.08960 20 21.7919 3.2081 0.9473
50 0.0507 0.099 0.94356 50 47.1781 2.8219 0.8349
0.1982
50 0.0504 0.109 1.02946 50 51.4732 -1.4732 -0.4385
75 0.0504 0.086 0.83189 100 83.1887 -8.1887 -2.4371
-2.6987
75 0.0502 0.088 0.84907 100 84.9068 -9.9068 -2.9602
100 0.0501 0.116 1.08960 100 108.9597 -8.9597 -2.6825
-2.5396
100 0.0507 0.115 1.08101 100 108.1007 -8.1007 -2.3967
150 0.0504 0.090 0.86625 200 173.2497 -23.2497 -6.9196
-7.1679 150 0.0505 0.091 0.87484 200 174.9678 -24.9678 -7.4162
200 0.0502 0.118 1.10678 200 221.3556 -21.3556 -6.3811
-7.1121 200 0.0507 0.121 1.13255 200 226.5098 -26.5098 -7.8431
300 0.0503 0.172 1.57066 200 314.1311 -14.1311 -4.2140
-6.2225 300 0.0508 0.180 1.63938 200 327.8756 -27.8756 -8.2310
Contoh perhitungan:
Co : Konsentrasi awal larutan biru metilena (mg/L)
Ce : Konsentrasi akhir larutan biru metilena (mg/L)
27 Lampiran 7 Kapasitas adsorpsi Kaolin - Bahan Pengikat
Co
25 0.0506 0.083 0.80612 0 0.8061 24.1939 7.1721
7.2012
25 0.0503 0.077 0.75457 0 0.7546 24.2454 7.2302
50 0.0503 0.093 0.89202 5 44.601 45.5399 13.5805
13.7396
50 0.0504 0.066 0.66008 5 33.004 46.6996 13.8987
75 0.0505 0.171 156.207 10 156.207 59.3793 17.6374
17.8955
75 0.0502 0.155 142.462 10 142.462 60.7538 18.1535
100 0.0504 0.189 171.669 20 343.338 65.6662 19.5435
19.4220
100 0.0501 0.196 177.682 20 355.365 64.4635 19.3005
150 0.0501 0.195 176.823 50 884.116 61.5884 18.4396
18.4396
150 0.0501 0.195 176.823 50 884.116 61.5884 18.4396
200 0.0503 0.171 156.207 100 1.562.065 43.7935 13.0597
12.4076 200 0.0504 0.176 160.502 100 1.605.017 39.4983 11.7555
300 0.0501 0.290 258.431 100 2.584.314 41.5686 12.4457
9.0964
300 0.0502 0.316 280.766 100 2.807.663 19.2337 5.7471
Contoh perhitungan:
Co : Konsentrasi awal larutan biru metilena (mg/L)
Ce : Konsentrasi akhir larutan biru metilena (mg/L)
28
Lampiran 8 Kapasitas adsorpsi K:B:T (7:2:1) ball milling (Nanokomposit NBCa1)
25 0.0503 0.132 1.22704 0 1.2270 23.7730 7.0894
7.1362
25 0.0502 0.101 0.96074 0 0.9607 24.0393 7.1830
50 0.0502 0.091 0.87484 0 0.8748 49.1252 14.6788
14.6760
50 0.0500 0.116 1.08960 0 1.0896 48.9104 14.6731
75 0.0504 0.197 1.78541 10 17.8541 57.1459 17.0077
17.1057
75 0.0502 0.192 1.74246 10 17.4246 57.5754 17.2038
100 0.0503 0.210 1.89709 20 37.9418 62.0582 18.5064
17.7978
100 0.0504 0.237 2.12903 20 42.5805 57.4195 17.0891
150 0.0502 0.206 1.86273 50 93.1363 56.8637 16.9911
16.7493
150 0.0505 0.209 1.88850 50 94.4249 55.5751 16.5075
200 0.0501 0.157 1.44180 100 144.1801 55.8199 16.7126
16.7293 200 0.0500 0.157 1.44180 100 144.1801 55.8199 16.7460
300 0.0502 0.138 1.27858 200 255.7169 44.2831 13.2320
13.7454 300 0.0502 0.136 1.26140 200 252.2807 47.7193 14.2587
Contoh perhitungan:
Co : Konsentrasi awal larutan biru metilena (mg/L)
Ce : Konsentrasi akhir larutan biru metilena (mg/L)
29
Lampiran 9 Kapasitas adsorpsi K:T (9:1) ball milling (Nanokomposit NBCa0)
Co
25 0.0502 0.191 1.73387 0 1.7339 23.2661 6.9520
6.8647
25 0.0506 0.238 2.13762 0 2.1376 22.8624 6.7774
50 0.0504 0.374 3.30590 0 3.3059 46.6941 13.8971
13.9533
50 0.0504 0.330 2.92793 0 2.9279 47.0721 14.0095
75 0.0502 0.204 1.84555 10 18.4555 56.5445 16.8958
16.9641
75 0.0501 0.200 1.81118 10 18.1118 56.8882 17.0324
100 0.0504 0.216 1.94863 20 38.9726 61.0274 18.1629
17.9938
100 0.0502 0.224 2.01735 20 40.3470 59.6530 17.8246
150 0.0506 0.199 1.80259 50 90.1297 59.8703 17.7481
17.7257
150 0.0500 0.201 1.81977 50 90.9887 59.0113 17.7034
200 0.0501 0.165 1.51052 100 151.0523 48.9477 14.6550
14.3418 200 0.0505 0.167 1.52770 100 152.7704 47.2296 14.0286
300 0.0501 0.301 2.67881 100 267.8808 32.1192 9.6165
11.1597 300 0.0501 0.289 2.57572 100 257.5724 42.4276 12.7029
Contoh perhitungan:
Co : Konsentrasi awal larutan biru metilena (mg/L)
Ce : Konsentrasi akhir larutan biru metilena (mg/L)
30
Lampiran 10 Kapasitas adsorpsi K:B:T (7:2:1) pasta (Nanokomposit NKP)
Co
25 0.0503 0.164 1.50193 0 1.5019 23.4981 7.0074
6.9077
25 0.0506 0.226 2.03453 0 2.0345 22.9655 6.8079
50 0.0501 0.080 0.78035 10 7.8035 42.1965 12.6337
12.9298
50 0.0500 0.058 0.59136 10 5.9136 44.0864 13.2259
75 0.0502 0.134 1.24422 20 24.8845 50.1155 14.9748
14.9086
75 0.0503 0.136 1.26140 20 25.2281 49.7719 14.8425
100 0.0503 0.109 1.02946 50 51.4732 48.5268 14.4712
14.8403
100 0.0504 0.103 0.97792 50 48.8961 51.1039 15.2095
150 0.0506 0.103 0.97792 100 97.7923 52.2077 15.4766
16.0516
150 0.0502 0.099 0.94356 100 94.3562 55.6438 16.6266
200 0.0501 0.167 1.52770 100 152.7704 47.2296 14.1406
13.2404 200 0.0501 0.174 1.58784 100 158.7836 41.2164 12.3402
300 0.0501 0.144 1.33013 200 266.0253 33.9747 10.1721
9.6395 300 0.0503 0.146 1.34731 200 269.4614 30.5386 9.1069
Contoh perhitungan:
Co : Konsentrasi awal larutan biru metilena (mg/L)
Ce : Konsentrasi akhir larutan biru metilena (mg/L)
31 Lampiran 11 Kapasitas adsorpsi K:B:T (7:2:1) ball milling/Fe2O3 (Nanokomposit
NBCa1-F)
25 0.0507 0.135 1.25281 0 1.2528 23.7472 7.0258
7.1523
25 0.0500 0.075 0.73739 0 0.7374 24.2626 7.2788
50 0.0501 0.060 0.60854 5 3.0427 46.9573 14.0591
14.0719
50 0.0501 0.058 0.59136 5 2.9568 47.0432 14.0848
75 0.0501 0.186 1.69092 10 16.9092 58.0908 17.3925
17.3320
75 0.0506 0.184 1.67374 10 16.7374 58.2626 17.2715
100 0.0504 0.190 1.72528 20 34.5056 65.4944 19.4924
18.9335
100 0.0501 0.214 1.93145 20 38.6290 61.3710 18.3746
150 0.0501 0.180 1.63938 50 81.9689 68.0311 20.3686
20.5822
150 0.0500 0.177 1.61361 50 80.6804 69.3196 20.7959
200 0.0506 0.154 1.41603 100 141.6030 58.3970 17.3114
17.4911 200 0.0503 0.153 1.40744 100 140.7439 59.2561 17.6708
300 0.0500 0.236 2.12044 100 212.0436 87.9564 26.3869
24.7942 300 0.0502 0.248 2.22352 100 222.3520 77.6480 23.2016
Contoh perhitungan:
Co : Konsentrasi awal larutan biru metilena (mg/L)
Ce : Konsentrasi akhir larutan biru metilena (mg/L)
32
25 0.0503 0.151 1.39026 0 1.3903 23.6097 7.0407
7.0038
25 0.0505 0.169 1.54488 0 1.5449 23.4551 6.9669
50 0.0503 0.161 1.47616 0 1.4762 48.5238 14.4703
14.4519
50 0.0505 0.153 1.40744 0 1.4074 48.5926 14.4334
75 0.0500 0.091 0.87484 10 8.7484 66.2516 19.8755
19.7327
75 0.0504 0.096 0.91779 10 9.1779 65.8221 19.5899
100 0.0506 0.141 1.30436 20 26.0871 73.9129 21.9109
22.0092
100 0.0505 0.138 1.27858 20 25.5717 74.4283 22.1074
150 0.0502 0.153 1.40744 50 70.3720 79.6280 23.7932
23.6588
150 0.0505 0.154 1.41603 50 70.8015 79.1985 23.5243
200 0.0506 0.133 1.23563 100 123.5633 76.4367 22.6591
22.8777 200 0.0502 0.132 1.22704 100 122.7042 77.2958 23.0963
300 0.0503 0.238 2.13762 100 213.7617 86.2383 25.7172
24.8206 300 0.0503 0.245 2.19775 100 219.7749 80.2251 23.9240
Contoh perhitungan:
Co : Konsentrasi awal larutan biru metilena (mg/L)
Ce : Konsentrasi akhir larutan biru metilena (mg/L)
33
25 0.0501 0.071 0.70303 0 0.7030 24.2970 7.2745
7.2498
25 0.0503 0.079 0.77176 0 0.7718 24.2282 7.2251
50 0.0505 0.155 1.42462 0 1.4246 48.5754 14.4283
14.4685
50 0.0503 0.146 1.34731 0 1.3473 48.6527 14.5088
75 0.0504 0.091 0.87484 10 8.7484 66.2516 19.7177
19.5517
75 0.0502 0.107 1.01228 10 10.1228 64.8772 19.3856
100 0.0503 0.286 2.54995 10 25.4995 74.5005 22.2168
22.1804
100 0.0500 0.294 2.61868 10 26.1868 73.8132 22.1440
150 0.0505 0.158 1.45039 50 72.5195 77.4805 23.0140
22.8451
150 0.0504 0.161 1.47616 50 73.8081 76.1919 22.6762
200 0.0503 0.131 1.21845 100 121.8452 78.1548 23.3066
21.2003 200 0.0506 0.147 1.35590 100 135.5897 64.4103 19.0940
300 0.0502 0.270 2.41251 100 241.2508 58.7492 17.5546
18.9461 300 0.0503 0.259 2.31801 100 231.8014 68.1986 20.3376
Contoh perhitungan:
Co : Konsentrasi awal larutan biru metilena (mg/L)
Ce : Konsentrasi akhir larutan biru metilena (mg/L)
34
RIWAYAT HIDUP
Penulis dilahirkan di Jakarta pada tanggal 30 September 1992 dari ayah Srijono dan ibu Siti Zakiyah. Penulis adalah putri kedua dari dua bersaudara. Tahun 2009 penulis lulus dari SMA Negeri 80 Jakarta dan pada tahun yang sama penulis lulus seleksi masuk Institut Pertanian Bogor dan diterima di Departemen Kimia, Fakultas Matematika dan Ilmu Pengetahuan Alam.