DAN PENGKONSENTRASIAN KARAGINAN
DENGAN MEMBRAN MIKROFILTRASI
OLEH:
UJU
SEKOLAH PASCASARJANA
INSTITUT PERTANIAN BOGOR
BOGOR
SURAT PERNYATAAN
Dengan ini saya menyatakan bahwa tesis yang berjudul :
Kajian Proses Pemurnian dan Pengkonsentrasian Karaginan dengan Membran Mikrofiltrasi
adalah benar hasil karya saya sendiri dan belum pernah dipublikasikan. Semua sumber data dan informasi yang digunakan telah dinyatakan secara jelas dan dapat diperiksa kebenarannya
Bogor, Desember 2005
Uju
ABSTRAK
UJU. Kajian Proses Pemurnian dan Pengkonsentrasian Karaginan dengan Membran Mikrofiltrasi. Dibimbing oleh SUPRIHATIN, PRAYOGA SURYADARMA dan LINAWATI HARDJITO.
Proses pemurnian karaginan secara komersial dilakukan dengan cara pengendapan dengan KCl atau alkohol. Metode pengendapan dengan KCl lebih murah, tetapi metode pengendapan dengan alkohol akan menghasilkan mutu yang lebih baik, namun butuh biaya tinggi. Tingginya biaya proses pemurnian tersebut terkait dengan jumlah penggunaan volume alkohol yang diperlukan dan kebutuhan energi tambahan untuk proses recovery alkohol melalui proses evaporasi atau distilasi. Saat ini teknologi proses membran telah banyak diaplikasikan untuk pemurnian beberapa polimer seperti protein, polisakarida, oligosakarida, nukleotida dan gula. Keuntungan yang akan diperoleh dari penggunaan teknologi membran antara lain lebih hemat dalam penggunaan energi dan bahan kimia. Dalam penelitian ini dikaji pengaruh tekanan transmembran dan laju alir umpan terhadap nilai fluks dan rejeksi pada filtrasi karaginan, analisis mendalam dilakukan terhadap tahanan filtrasi dan fluks. Penelitian dilakukan dengan menggunakan rancangan Response Surface Methodology.
Proses prefiltrasi ekstrak rumput laut dengan filter 0,3 mikron menghasilkan warna filtrat rumput yang lebih jernih dibandingkan dengan hasil filtrasi 350 mesh dan 1 mikron. Penggunaan filter ukuran 0,3 mikron dapat menurunkan kadar selulosa dari 6,57 menjadi 0,90 % (84,00%), sedangkan nilai absorbansi figmen fikosianin dan fikoeritin menurun dari 0,24 menjadi 0,07 pada fikosianin dan 0,31 menjadi 0,09 pada fikoeritin, degan viskositas 23,89 cP.
Pada proses pemurnian larutan karaginan dengan membran mikrofilrtasi 0,1 mikron, fluks meningkat sebesar 8,05 l m2 jam-1 untuk setiap kenaikan tekanan transmembran 1 kPa, sedangkan laju alir umpan pada kondisi ini tidak berpengaruh signifikan dalam meningkatkan fluks. Tekanan transmembran dan laju alir umpan tidak berpengaruh signifikan terhadap nilai rejeksi pigmen fikosianin dan fikoeritin serta karaginan.
Besarnya fluks ditentukan oleh nilai tahanan membran internal (Rm), tahanan fouling (Rf) dan tahanan polarisasi (Rp). Nilai Rf mencapai 2-3 kali lebih tinggi dibandingkan nilai Rm dan selama proses filtrasi kedua jenis tahanan tersebut tidak mengalami perubahan yang signifikan. Nilai tahanan polarisasi konsentrasi (Rp) besanya tergantung pada perkalian indeks tahanan polarisasi (Ф) dan tekanan transmembran (P). Pada tekanan transmembran rendah (kurang dari 27,6 – 40,0 kPa) nilai tahanan didominasi oleh Rm dan Rf, sedangkan diatas nilai tekanan transmembran tahanan membran didominasi oleh Rp. Model tahanan seri dapat menjelaskan perilaku fluks baik pada daerah yang dikendalikan oleh tekanan maupun pada daerah yang dikendalikan oleh transfer massa.
KAJIAN PROSES PEMURNIAN DAN
PENGKONSENTRASIAN KARAGINAN DENGAN
MEMBRAN MIKROFILTRASI
UJU
Tesis
sebagai salah satu syarat untuk memperoleh gelar Magister Sains
pada Program Studi Teknologi Industri Pertanian
SEKOLAH PASCA SARJANA
INSTITUT PERTANIAN BOGOR
PRAKATA
Alhamdulillah puji syukur penulis panjatkan kehadirat Allah SWT, karena berkat karunia dan rahmatNya penulis dapat menyelesaikan tesis ini. Pada kesempatan ini penulis mengucapkan terimakasih kepada :
1. Dr. Ir. Suprihatin, Dipl.Ing, Bapak Prayoga Suryadarma STP, MT dan Dr. Ir. Linawati Hardjito, M.Sc selaku dosen pembimbing yang telah memberikan bimbingan dan arahan
2. Dr. Ir. Nastiti Siwi Indrasti selaku dosen penguji yang telah memberikan masukan dan pencerahan terhadap tesis ini
3. Dr. Ir. Erliza Noor dan Keluarga Dr. Ir. Anang Kristatnto M.Sc yang telah memberikan pinjaman dan pengadaan peralatan penelitian.
4. Pimpinan dan Staf WR IV dan Direktorat Kerjasama-IPB terima kasih atas tenaga bantuan peralatan selama seminar dan ujian.
5. Mr Benk, Sotong, Zaki, Eful, Ismail, atas bantuan teknis selama penelitian 6. Ema dan Bapak serta Mimi terimakasih atas doa dan dukunganya
7. Istri dan Anak tercinta atas doa, dukungan, motovasi serta pengorbanannya
Semoga tesis dapat bermanfaat.
Bogor, Desember 2005
RIWAYAT HIDUP
Penulis dilahirkan di Haurgeulis-Indramayu pada tanggal 12 Juni 1973 dari Ibu Ratinah dan Ayah Sadi. Penulis merupakan anak pertama dari dua bersaudara.
Penulis menyelesaikan pendidikan Sekolah Dasar pada SD Negeri Haurgeulis Kolot, Indramayu tahun 1987, Sekolah Menengah Pertama pada SMP Negeri Haurgeulis, Indramayu pada tahun 1990 dan Sekolah Menengah Atas pada SMA Negeri 2 Cirebon tahun 1993. Pada tahun 1994 penulis diterima di Institut Pertanian Bogor melalui jalur UMPTN dan tahun 1995 penulis memilih Program Studi Teknologi Hasil Perikanan, Fakultas Perikanan IPB. Penulis menyelesaikan studinya pada progam studi tersebut pada tahun 1999.
Terhitung bulan Desember 2000 sampai sekarang penulis diterima sebagai staf pengajar Jurusan Teknologi Hasil Perikanan, Fakultas Perikanan dan Ilmu Kelautan IPB. Pada tahun 2002 penulis melanjutkan pendidikan Magister (S2) pada Program Studi Teknologi Industri Pertanian IPB dengan beasiswa BPPS.
DAFTAR ISI
Halaman
DAFTAR TABEL... viii
DAFTAR GAMBAR ... ix
DAFTAR LAMPIRAN... xi
1. PENDAHULUAN ... 1
1.1 Latar Belakang ... 1
1.2 Tujuan ... 1.3 Ruang Lingkup... 4
1.4 Tempat dan Waktu Penelitian ... 4
2. TINJAUAN PUSTAKA ... 5
2.1 Komponen Rumput Laut... 5
2.2 Karakteristik Karaginan ... 8
2.2.1 Kelarutan... 9
2.2.2 Viskositas ... 9
2.2.3 Pembentukan gel ... 10
2.2.4 Stabilitas... 11
2.3 Proses Produksi Karaginan ... 12
2.4 Standar Mutu Karaginan ... 15
2.5 Proses Filtrasi dengan Membran... 17
2.6 Model Fluks Hagen Poisuille... 18
2.7 Fouling dan Polarisasi Konsentrasi ... 20
2.7.1 Fouling... 20
2.7.2 Polarisasi konsentrasi... 21
2.8 Model Transfer Massa (Teori Film) ... 21
2.9 Model Tahan Seri... 23
2.10 Faktor-faktor yang Mempengaruhi Fluks ... 25
2.10.1 Tekanan transmembran ... 25
2.10.2 Konsentrasi umpan... 26
2.10.3 Laju alir umpan cross-flow... 26
2.10.4 Suhu ... 26
3. METODOLOGI PENELITIAN... 27
3.1 Bahan dan Alat... 28
3.2 Prosedur Penelitian ... 29
3.2.1 Preparasi bahan ... 29
3.2.2 Proses pemurnian dan pengkonsentrasian dengan mikrofiltrasi... 29
3.2.3 Analisis dan karakterisasi ... 30
3.2.4 Penentuan permeabilitas dan tahanan membran internal.. 30
3.2.5 Penentuan waktu tunak fluks ... 31
3.2.6 Penentuan pengaruh tekanan transmembran dan laju alir umpan rerhadap nilai fluks dan rejeksi... 31
3.2.7 Penentuan respon permukaan pengaruh tekanan transmembran dan laju alir umpan ... 32
3.2.8 Penentuan nilai fluks dengan model tahanan seri ... 32
3.3 Rancangan Percobaan ... 33
3.3.1 Penentuan pengaruh tekanan transmembran dan laju alir umpan terhadap nilai fluks dan rejeksi ... 33
3.3.2 Penentuan permukaan respon fluks ... 33
3.3.3 Penentuan tahanan proses membran dengan model tahanan seri... 33
4. HASIL DAN PEMBAHASAN... 35
4.1 Karakterisasi Rumput Laut ... 35
4.2 Karaktersitik Ekstrak dan Filtrat Rumput Laut... 37
4.2.1 Warna ... 37
4.2.2 Kadar selulosa ... 38
4.2.3 Konsentrasi pigmen ... 39
4.2.4 Viskositas ... 41
4.2.4.1 Hubungan konsentrasi karaginan terhadap viskositas 42 4.2.5 Rendemen ... 45
4.3 Permeabilitas dan Tahanan Membran... 46
4.4 Pengaruh Tekanan Transmembran dan Laju Alir Umpan terhadap Nilai Fluks dan Rejeksi ... 48
4.4.1 Pengaruh tekanan transmembran dan laju alir umpan terhadap nilai fluks... 49
4.4.2 Pengaruh tekanan transmembran dan laju alir umpan terhadap nilai rejeksi ... 50
4.5 Permukaan Respon Fluks ... 51
4.6 Analisis Susunan dan Nilai Tahanan Membran... 54
4.6.1 Nilai tahanan fouling (Rf) ... 55
4.6.2 Rasio tahanan membran internal (Rm) terhadap Rf ... 55
4.6.3 Nilai indeks tahanan polarisasi konsentrasi (Ф) ... 56
4.6.4 Nilai tahanan polarisasi konsentrasi (Rp) ... 57
4.7 Peta dan Kontribusi Rm, Rf dan Rp terhadap Tahanan Total (Rt) . 58 4.8 Prediksi Fluks dengan Model Tahanan Seri ... 60
4.9 Pengaruh Faktor Konsentrasi ... 62
4.10 Analisis Karakteristik Karaginan ... 64
4.10.1 Kadar selulosa ... 65
4.10.2 Viskositas ... 66
4.10.3 Tingkat kecerahan ... 66
4.10.4 Rendemen ... 66
5. KESIMPULAN DAN SARAN... 67
5.1 Kesimpulan ... 67
5.2 Saran ... 68
DAFTAR PUSTAKA ... 69
LAMPIRAN... 75
DAFTAR TABEL
Halaman
1 Komponen penyusun alga merah... 7
2 Sifat-sifat kelarutan karaginan pada berbagai medium... 10
3 Karakteristik gel kappa, iota dan lamda karaginan ... 11
4 Stabilitas jenis karaginan pada pH alkali dan asam ... 12
5 Pengaruh penggunaan konsentrasi NaOH pada proses ekstraksi terhadap beberapa parameter mutu karaginan ... 13
6 Analisis kadar logam berat terhadap sampel refined carrageenan dan PNG komersil... 15
7 Standar mutu semi refined carrageenan dan refined carrageenan... 16
8 Pengelompokan proses membran berdasarkan kisaran ukuran partikel yang direjeksi ... 17
9 Penentuan taraf nilai sebenarnya dari variabel-varibel bebas ... 32
10 Parameter regresi pengaruh tekanan transmembran dan laju alir umpan terhadap nilai fluks... 50
11 Nilai parameter operasi, data hasil percobaan dan nilai dugaan dengan metode RSM... 52
12 Nilai-nilai koefisien variabel proses dan tingkat kesignifikanannya ... 53
13 Analisis komponen dan nilai tahanan membran pada proses filtrasi ekstrak rumput laut pada laju alir umpan 2,97; 3,47 dan 3,97 m s-1... 55
14 Data, nilai prediksi fluks dan indikator keakuratan model tahan seri ... 62
15 Perbandingan karakteristik karaginan yang dihasilkan melaui proses konvensional, membran mikrofiltrasi dan standar parameter yang ditetapkan oleh FAO ... 64
DAFTAR GAMBAR
Halaman
1 Struktur molekul pigmen fikosianin dan fikoeritin (Anonim 2004) ... 5
2 Spesies rumput laut penghasil karaginan (Velde dan De Ruiter 2004) .. 6
3 Struktur karaginan yang terdiri dari ikatan (1- 3) -D-galaktosa dan β(1-4) D-galaktosa (cPKelco ApS 2004) ... 8
4 Struktur monomer karaginan jenis kappa, iota dan lamda (Tojo dan Prodo 2003) ... 8
5 Mekanisme pembentukkan gel pada karaginan (Smidsrod dan Grasdalen 1982) ... 11
6 Diagram alir proses produksi karaginan ( McHugh 2003; Imeson 2002) 14 7 Proses operasi filtrasi membran dengan sistem cross-flow... 18
8 Profil kecepatan aliran zat cair yang melewati suatu membran (Krijgsman 1992) ... 18
9 Lokasi terjadinya fouling pada membran (Paulson 1995) ... 20
10 Profil konsentrasi selama proses filtrasi dengan membran (Mulder 1996) 22 11 Mekanisme penyumbatan pori membran oleh partikel terlarut (Roorda dan van der Graaf 2001) ... 24
12 Diagram alir tahapan proses penelitian ... 27
13 Unit cross-flow filtrasi membran ... 28
14 Diagram alir proses membran ... 29
15 Kerangka pemodelan proses membran dengan pendekatan model tahanan seri ... 32
16 Rumput laut Kappaphycus alvarezii kering... 35
17 Karakterstik, kadar air, kadar abu dan kadar selulosa rumput laut kering Kappaphycus alvarezii... 36
18 Pengaruh ukuran pori filter terhadap warna ekstrak dan filtrat ekstrak rumput laut. Dari kiri ke kanan adalah ekstrak, penyaringan 350 mesh, penyaringan 1 mikron dan penyaringan 0,3 mikron ... 37
19 Pengaruh ukuran filter terhadap kadar selulosa dalam ekstrak dan filtrat ekstrak rumput laut... 38
20 Pengaruh ukuran pori filter terhadap nilai absorbansi pigmen fikoeritin (ג = 530 nm) dan fikosinin (ג = 620) nm pada ekstrak dan filtrat ekstrak rumput laut... 40
21 Pengaruh perlakuan ukuran pori filter terhadap nilai viskositas filtrat... 42
22 Hubungan antara konsentrasi dan viskositas karaginan pada suhu 45 oC dan 55 oC... 44
23 Pengaruh perlakuan ukuran pori filter terhadap nilai rendemen
filtrat ekstrak rumput laut... 45 24 Pengaruh tekanan membran dan suhu umpan air distilasi terhadap
nilai fluks ... 46 25 Pengaruh suhu umpan air distilasi terhadap nilai tahanan membran
internal ... 47 26 Pola perubahan nilai fluks permeat yang disebabkan oleh perubahan tekanan transmembran dan laju alir umpan ... 48 27 Respon permukaan tekanan transmembran (ΔP) dan laju alir umpan (v)
terhadap nilai fluks permeat... 54 28 Pengaruh laju alir umpan terhadap nilai indeks tahanan polarisasi (Ф) . 57 29 Pengaruh tekanan transmembran terhadap nilai tahan polarisasi
konsentrasi (Rp)... 58
30 Perubahan nilai komponen tahanan membran menurut fungsi tekanan
transmembran pada laju alir umpan 2,97 m s-1... 59 31 Nilai data dan prediksi fluks dengan model tahanan seri pada laju alir
umpan (v) 2,97; 3,47 dan 3,97 m s-1... 61 32 Perubahan nilai fluks yang disebabkan oleh faktor konsentrasi ... 63 33 Viskositas larutan karaginan pada kondisi sebelum dan sesudah
pengkonsentrasian dengan membran mikrofiltrasi 0,1 mikron... 64 34 Karakteristik karaginan yang dihasilkan melalui proses mikrofiltrasi
dan konvensional ... 65
DAFTAR LAMPIRAN
Halaman
1 Prosedur ekstraksi karaginan (Gliksman 1983 yang dimodifikasi) ... 75
2 Analisis fluks dan rejeksi ... 76
3 Prosedur analisis karakterisasi bahan dan produk... 77
4 Data dan hasil analisis statistik kadar selulosa... 81
5 Data dan hasil analisis statistik abosorbansi fikosianin ... 82
6 Data dan hasil analisis statistik absorbansi fikoeritin ... 83
7 Data dan hasil analisis statistik viskositas ... 84
8 Data hubungan antara konsentrasi karaginan dengan nilai viskositas dan analisis statitsiknya... 85
9 Data hubungan antara tekanan transmembran (ΔP) dan fluks (J) dengan menggunakan air distilasi pada suhu umpan 27 oC, 45 oC dan 55 oC 86 10 Data hubungan antara tekanan transmembran (ΔP) dan laju alir umpan (v) terhadap fluks (J) serta analisis statistiknya ... 86
11 Data dan hasil analisis statistik pigmen fikosianin dan fikoeritin... 87
12 Analisis ragam pengaruh tekanan transmembran (ΔP) dan laju alir umpan (v) terhadap nilai fluks (J) dengan respons surface methodology. 88 13 Menentukan komponen dan nilai tahanan selama proses membran ... 89
14 Data perubahan faktor konsentrasi terhadap fluks... 90
14 Data dan hasil analisis karakteristik karaginan ... 91
1. PENDAHULUAN
1.1 Latar Belakang
Karaginan merupakan biopolimer yang diperoleh dari rumput laut yang bernilai ekonomis tinggi. Tingkat permintaan produk ini setiap tahunnya selalu mengalami peningkatan secara eksponensial dengan kenaikan rata-rata sekitar 5% (Bixler 1996; McHugh 2003). Nilai jual rumput laut Kappaphycus alvarezii
kering US$ 0,3 per kilogram, dalam bentuk semi refined carrageenan berharga US$ 6/kg dan menjadi US$ 10/kg dalam bentuk jadi sebagai refined carrageenan
(Kompas 23 Juli 2003), dengan demikian nilai tambah karena pengolahan adalah 20-30 kali lipat. Hal tersebut menyebabkan perusahaan-perusahaan besar karaginan dunia lebih tertarik dan memfokuskan produksinya pada refined carrageenan hingga mencapai 80 - 85 % dari total kapasitasnya (McHugh 2003).
Proses produksi refined carrageenan meliputi proses pencucian, ekstraksi, penyaringan kasar, penyaringan halus dengan menambahkan filter aid, pemurnian/pengkonsentrasian, pengeringan dan penepungan. Proses pemurnian bertujuan untuk menghilangkan komponen tidak larut air seperti selulosa, hemiselulosa, β-glucan, senyawa protein, senyawa lemak dan polimer lainnya (Zamorano et al. 2002). Selulosa dan pigmen yang tidak dapat dipisahkan akan meyebabkan karaginan yang dihasilkan berwarna keruh (Bixler dan Jhondro 2000; Zamorano et al. 2002).
Proses pemurnian karaginan secara komersial dilakukan dengan cara pengendapan KCl atau dengan alkohol. Ditinjau dari aspek ekonomis metode pengendapan dengan KCl lebih murah, tetapi dari segi kualitas metode pengendapan dengan alkohol akan menghasilkan mutu yang paling baik (Gliksman 1983). Tingginya biaya proses pemurnian karaginan dengan metode pengendapan alkohol terkait jumlah penggunaan volume alkohol dan penggunaan energi tambahan untuk proses recovery alkohol agar dapat digunakan kembali melalui proses destilasi. Jumlah volume alkohol yang dibutuhkan untuk proses pemurnian berkisar antara 1,5 – 4 kali volume filtrat (Gliksman 1983).
gula (DeFrees 2003; Yeh dan Dong 2003). Membran ultrafiltrasi berhasil memekatkan serta memurnikan larutan arabinoxylan dan rhamnogalacturonan dengan nilai rejeksi retentat mencapai 90% dan nilai fluks 14,5 l/m2 jam pada kondisi steady state (Jorda et al. 2002). Noor dan Kusumawardani (2002) memekatkan sirup glukosa menggunakan membran mikrofiltrasi pada fluks 75-90 l/m2 jam dengan nilai rejeksi 55-68%. Gan et al. (2001) menggantikan dan menemukan proses klarifikasi bir yang optimum dengan menggunakan membran mikrofiltrasi 0,5 mikron. Proses klarifikasi dengan proses membran dapat menghilangkan penggunaan filter aid seperti diatome, celite, atau alumunium aktif serta dapat mengurangi masalah pencemaran lingkungan akibat residu bahan-bahan tersebut.
Keuntungan yang diperoleh dari penggunaan teknologi membran adalah lebih hemat dalam penggunaan energi dan bahan kimia. Hasil studi Kessler (1986) menunjukkan bahwa proses pemekatan jus dengan menggunakan freeze concentration, evaporasi dan teknologi membran reverse osmosis masing-masing membutuhkan energi sebanyak 855, 1754 dan 120 kJ untuk setiap kilogram air yang dipisahkan. Kebutuhan energi yang digunakan pada proses membran adalah untuk menggerakan pompa dan meningkatkan suhu umpan jika diperlukan (Yeh dan Tsai 1997). Pada proses membran tidak terdapat perubahan fase bahan seperti yang terjadi pada evaporasi dan pembekuan. Perubahan fase suatu zat atau senyawa akan membutuhkan energi yang lebih besar.
Proses membran mikrofiltrasi dan ultrafiltrasi memanfaatkan prinsip penyaringan dalam memisahkan bahan dengan menggunakan tekanan transmembran sebagai driving force (Yeh dan Dong 2003; Andersen 2004). Pada proses ini partikel dengan berat molekul dibawah Molecule Weight Cut Off
Laju fluks permeat akan semakin meningkat secara linier dengan meningkatnya tekanan transmembran tetapi setelah mencapai tekanan tertentu fluks akan menurun jika tekanan transmembran ditingkatkan lagi (Kirk et al.
1983). Peningkatan tekanan transmembran akan menyebabkan pembentukan partikel terejeksi pada permukaan membran, dan semakin padat jika tekanan transmembran ditingkatkan lagi (Bian et al. 2000).
Laju fluks akan semakin meningkat dengan semakin tingginya kecepatan alir umpan. Kecepatan alir yang tinggi dapat membentuk aliran turbulen sehingga dapat menyapu pratikel-partikel yang terejeksi pada permukaan membran dan dapat mengurangi tingkat ketebalan polarisasi konsentrasi dan lapisan gel (Eakin et al. 1978; Bian et al. 2000). Menurut Dornier et al. (1994) penggunaan kecepatan alir umpan yang terlalu tinggi akan menjadi tidak ekonomis dalam skala industri.
Berdasarkan permasalahan tersebut, pemahaman yang lebih baik terhadap faktor-faktor yang mempengaruhi kinerja proses membran akan lebih ekonomis diaplikasikan pada setiap proses. Teknik optimasi response surface methodology
(RSM) dapat digunakan untuk mengetahui titik optimum dari suatu proses yang dipengaruhi beberapa variabel proses. Teknik RSM telah banyak diaplikasikan pada proses-proses optimasi baik skala laboratorium maupun dalam skala pilot plan (Dornier et al. 1994; Montgomery 2001). Di lain pihak, untuk mengevaluasi kinerja proses membran, model tahanan seri telah berhasil menjelaskan mekanisme proses pemisahan dengan baik (Chiang dan Cheryan 1986;Viadero et al. 1999).
1.2 Tujuan
Penelitian ini dilakukan dengan tujuan untuk :
1. Mengetahui informasi tentang pengaruh tekanan transmembran dan laju alir umpan terhadap fluks dan rejeksi (serta kurva permukaan respon terhadap fluks) pada proses pemurnian karaginan dengan membran mikrofiltrasi. 2. Mendapatkan bentuk model tahanan seri proses pemurnian karaginan
3. Mengetahui data tentang karakteristik karaginan yang dihasilkan dari proses pemurnian dan pengkonsentrasian dengan membran mikrofiltrasi.
1.3 Ruang Lingkup
1. Menentukan bentuk hubungan antara konsentrasi karaginan dengan viskositasnya.
2. Menentukan pengaruh variabel tekanan transmembran dan laju alir umpan terhadap fluks dan rejeksi.
3. Menentukan bentuk model proses membran pemurnian dan pengkonsentrasian karaginan dengan membran mikrofiltrasi melalui pendekatan model tahanan seri.
4. Melakukan karakterisasi refined carrageenan yang dihasilkan dengan proses membran mikrofiltrasi.
1.4 Tempat dan Waktu Penelitian
2. TINJAUAN PUSTAKA
Rumput laut (seaweed) merupakan bentuk poliseluler dari ganggang (algae) yang hidup dilaut dan tergolong dalam divisio Thalllophyta. Berdasarkan kandungan pigmennya, rumput laut dikelompokkan menjadi 4 kelas yaitu kelas Chlorophyceae (alga hijau), Phaeophyceae (alga coklat), Cyanophyceae (alga hijau biru) dan Rhodophyceae (alga merah). Untuk saat ini baru Rhodophyceae dan Phaeophyceae yang memiliki produk metabolit primer dengan nilai yang cukup berarti dalam dunia perdagangan.
2.1 Komponen Rumput Laut
Warna merah pada alga kelas Rhodophyceae disebabkan oleh dominasi pigmen yang membentuk warna merah yaitu fikosianin dan fikoeritin. Fikosianin dan fikoeritin bersifat larut dalam air tetapi tidak larut dalam pelarut organik. Fikosianin memiliki berat molekul 100 – 220 kDa, sedangkan berat molekul fikoeritin adalah 240 kDa (Anonim 2004). Struktur molekul kimia kedua jenis pigmen tersebut disajikan pada Gambar 1.
Salah satu produk metabolit primer yang dihasilkan rumput laut kelas Rhodophyceae adalah karaginan. Beberapa spesies rumput laut penghasil karaginan berdasarkan sistematikanya disajikan pada Gambar 2.
Fikoeritin Fikosianin
Rhodophycaea (Red algae)
Florideophycidae Gigartinales
Furcellariaceae
Hypneaceae
Sollariaceae
Gigartinaceae
Phyllophonaceae
Furcellaria
Hypnea
Eucheuma
Kappaphycus
Chondrus
Iridaea
Gigartina
Phyllophora
Gymnogongrus
Annfellia
F. lumbricalis F. fastigiata
H. musciformis H. cervicois
E. denticulatum
K. alvarezii
C. crispus C. ocellatus
I. cordata I. undulosa I. boryana
G. radula G. stellata G. acticularis G. pistillata G. charmissol G. skottsbergii G. canaliculata
Kelas Subkelas Ordo Famili Genus Spesies
Rumput laut Kappaphycuss alvarezii mengandung karaginan 39%, sedangkan sisanya merupakan garam anorganik 49%, selulosa 8%, protein kasar 3% serta lemak 1% (Bixler 1996). Komposisi dan proporsi komponen rumput laut kelas Rhodophyceae secara umum disajikan pada Tabel 1.
Tabel 1 Komponen penyusun alga merah
Komponen Berat Molekul Keterangan
Galaktosida 266 Sangat banyak
2-D-asam gluiserat-α-D-mannopriranosida 268 Td
3-o-fluoridosida α-D- mannopriranosida 415 Td
1-o-gliserol- α-D-galaktopiranosida 254 Td
D-glukosa 176 Td
D-galaktosa 180 2,5 **
D-manosa 180 Td
L-galaktosa 180 0,85**
D-xilosa 390 1,0**
Ester sulfat 96 3,5**
D-asam glukoronat 193 9,5 – 11%
D-asam galakturonat 194 6%
Selulosa 2.464.000 1 - 9%
Xylan 5.850 29 – 45%*
Mannan 2.928 3,8%*
Klorofil a 1.972 +++
Fikosianin 232.000 +
Asam poliuronat 2.005 Td
Β-karoten 536 Td
Lutein 568 ++
Karaginan
Kappa karaginan pada Kappaphycuss alvarezii
100.000 - 1.000.000 260.000 – 320.000
35,1 – 80% 61,52%
Trace element (I, Mg, Na, K) 254, 24, 23, 39
Klorofil d 1972 +
α-karoten 536 +
Fikoeritin 240.000 +++
+++ : Pembentuk pigmen utama
++ : Komponen pigmen yang kurang dari setengah dari jumlah total pigmen + : Sebagaian kecil komponen pigmen
* : Basis kering
** : Perbandingan molar dalam Porphyra sp td : Tidak ada
2 Karakteristik Karaginan
Karaginan merupakan polisakarida berantai lurus yang dibentuk oleh unit-unit α(1-3)-D-galaktosa dan β(1-4) D-galaktosa secara berselang seling (Glicksman 1983). Struktur ikatan kimia, dan komponen penyusunan karaginan disajikan pada Gambar 3.
Karaginan dikelompokkan berdasarkan gugus 3,6-anhidro-D-galaktosa dan
jumlah serta posisi dari gugus ester sulfatnya. Berdasarkan cara pengelompokan tersebut, karaginan dapat dibedakan menjadi 3 jenis yaitu karaginan jenis kappa, iota dan lamda (Gliksman 1983). Struktur monomer-monomer karaginan jenis kappa, iota dan lamda disajikan pada Gambar 4.
Berat molekul (BM) karaginan bervariasi mulai dari 100 – 800 kDa. Berat molekul optimum karaginan mutu makanan berkisar antara 100–500 kDa (FAO 1990). Pada berat molekul dibawah 100 kDa sifat fungsional gel karaginan akan banyak yang hilang (Imeson 2000). Secara spesifik Towle (1973) menyatakan bahwa BM kappa karaginan dan lamda karaginan masing-masing berkisar antara 262 – 320 kDa dan 33 – 79 kDa.
Gambar 3 Struktur karaginan yang terdiri dari ikatan α(1-3)-D-galaktosa dan
β(1-4) D-galaktosa (cPKelco ApS 2004)
2.2.1 Kelarutan
Karakteristik kelarutan karaginan dalam air dipengaruhi oleh sejumlah faktor penting antara lain tipe karaginan, temperatur, pH, kehadiran ion tandingan, dan zat-zat terlarut lain. Gugus hidroksil dan sulfat pada karaginan bersifat hidrofilik sedangkan gugus 3,6-anhydro-D-galaktosa lebih hidrofobik. Lamda karaginan mudah larut pada semua kondisi karena tanpa unit 3-6 anhydro-D-galaktosa dan mengandung gugus sulfat yang tinggi. Karaginan jenis iota bersifat lebih hidrofilik karena adanya gugus 2-sulfat dapat menetralkan 3-6 anhydro-D-galaktosa yang kurang hidrofilik. Karaginan jenis kappa kurang hidrofilik karena lebih banyak memiliki gugus 3-6 anhydro-D-galaktosa (Towle 1983; cPKelco ApS 2004).
Karakteristik daya larut karaginan juga dipengaruhi oleh bentuk garam dari gugus ester sulfatnya. Jenis sodium umumnya lebih mudah larut, sementara jenis potasium lebih sukar larut. Hal ini menyebabkan kappa karaginan dalam bentuk garam potasium lebih sulit larut dalam air dingin dan diperlukan panas untuk mengubahnya menjadi larutan, sedangkan dalam bentuk garam sodium lebih mudah larut. Lambda karaginan larut dalam air dan tidak tergantung jenis garamnya (cPKelco ApS 2004).
Kehadiran zat lain dalam larutan akan mempengaruhi sifat kelarutan karaginan, hal ini terjadi karena adanya persaingan penggunaan air dalam mengubah keadaan polihidrasi. Garam-garam organik lebih efektif dalam mengubah hidrasi karaginan, khususnya jika kationnya garam potasium. Sifat-sifat kelarutan karaginan pada berbagai medium disajikan pada Tabel 2.
2.2.2 Viskositas
Tabel 2 Sifat-sifat kelarutan karaginan pada berbagai medium
Medium Kappa Iota Lamda
Air panas Larut diatas 60oC Larut diatas 70oC*
Larut diatas 60oC Larut diatas 70oC*
Larut
Air dingin Larut dalam garam sodium, potasium dan kalsium tidak larut
Larut dalam garam sodium, garam kalsium menghasilkan dispersi
thixotropic
Larut
Susu panas Larut Larut Larut
Susu dingin Tidak larut dalam garam sodium, potasium dan kalsium tetapi mengembang dengan baik
Tidak larut Larut
Larutan konsentrat gula
Larut pada panas Tidak mudah larut Larut pada
panas
Larutan konsentrat garam
Tidak larut Larut pada panas Larut
Sumber: cPKelco ApS 2004 * Glicksman 1983
2.2.3 Pembentukan gel
Karaginan memiliki kemampuan membentuk gel pada saat larutan panas menjadi dingin. Proses pembentukan gel bersifat thermoreversible, artinya gel dapat mencair pada saat pemanasan dan membentuk gel kembali pada saat pendinginan (Gliksman 1983; Imeson 2000). Larutan kappa karaginan yang dipanaskan dan kemudian didinginkan akan membentuk gel pada suhu 40 – 60oC, dan gel akan mencair kembali jika dipanaskan 5 – 20oC diatas titik cairnya (Imeson 2000).
Adanya ion monovalen K+, NH4+, Rb+, dan Cs+ dapat membantu
pembentukan gel. Kappa karaginan dapat membentuk gel yang paling kuat. Iota akan membentuk gel yang kuat dan stabil jika terdapat ion Ca2+, sedangkan ion Na+ dapat menghambat pembentukan gel karaginan jenis kappa dan lamda (Gliksman 1983)
Tabel 3 Karakteristik gel kappa, iota dan lamda karaginan
Keterangan Kappa Iota Lamda
Efek kation Gel lebih kuat dengan ion potassium
Gel lebih kuat dengan ion kalsium
Tidak membentuk gel
Tipe gel Kuat dan rapuh
dengan sineresi
Elastis dan kohesif tanpa sineresis
Tidak membentuk gel
Efek sinergis dengan locus gum
Tinggi Tinggi Tidak
Stabilitas Freezing thawing
Tidak Stabil Tidak
Sumber: cPKelco ApS 2004.
2.2.4 Stabilitas
Karaginan dalam larutan memiliki stabilitas maksimum pada pH 9 dan tidak boleh berada pada pH dibawah 3,5 karena akan terhidrolisis. Pada pH 6 atau lebih Gambar 5 Mekanisme pembentukan gel pada karaginan (Smidsrod dan
Grasdalen 1982)
Sol Gel II
Gel I Pemanasan
Pendinginan
umumnya larutan karaginan dapat mempertahankan kondisi proses (cPKelco 2004). Hidrolisis asam akan terjadi jika karaginan berada dalam bentuk larutan, hidrolisis akan meningkat sesuai dengan peningkatan suhu. Larutan karaginan akan menurun viskositasnya jika pHnya diturunkan dibawah 4,3 (Imeson 2003). Stabilitas jenis karaginan yang disebabkan oleh perubahan pH disajikan pada Tabel 4.
Tabel 4 Stabilitas jenis karaginan pada pH alkali dan asam
Stabilitas Kappa Iota Lamda
Pada pH netral dan alkali
Stabil Stabil Stabil
Pada pH asam Terhidrolisis dalam larutan ketika dipanaskan. Stabil dalam bentuk gel
Terhidrolisis dalam larutan. Stabil dalam bentuk gel
Terhidrolisis
Sumber: Moraino 1977
2.3 Proses Produksi Karaginan
Proses produksi karaginan terdiri dari tahap penyiapan bahan baku, ekstraksi, pemisahan karaginan dari ekstraknya, pemurnian, pengeringan dan penepungan.
1. Penyiapan bahan baku
Sebelum proses ekstraksi dilakukan, rumput laut dicuci dahulu. Proses pencucian dilakukan untuk menghilangkan pasir, garam dan benda-benda asing lainnya.
2. Ekstraksi
Karaginan dapat diekstrak dengan cara memecah dinding sel rumput laut pada suhu 90 – 100 oC. Untuk memperoleh kekuatan gel yang tinggi proses ekstraksi dilakukan dalam suasana pH alkalis. Jenis basa yang digunakan adalah NaOH atau Ca(OH)2. Penggunaan NaOH 1% dengan volume air
Tabel 5 Pengaruh penggunaan konsentrasi NaOH pada proses ekstraksi terhadap beberapa parameter mutu karaginan.
Spesies Konsentrasi alkali
Yield (%)
Kekuatan gel (g/cm2)
Suhu Pembentukan gel (°C) So4 (%) 3, 6-Ag (%)
Air 74,6 57 39,3 14,7 22,4
0.5% NaOH 65,7 114 40,1 14,0 27,6
1.0% NaOH 62,8 187 44,4 11,0 28,6
2.0% NaOH 58,9 244 47,4 10,2 29,9
Eucheuma gelatinae
NaOH pekat 43,7 346 48,9 11,4 29,5
Air 49,4 22 34,1 22,8 21,6
0.5% NaOH 35,1 44 32,0 19,6 22,7
1.0% NaOH 34,8 129 32,3 18,4 27,8
2.0% NaOH 35,2 145 32,6 17,7 27,6
Eucheuma cottonii
NaOH pekat 29,6 521 32,1 13,2 33,6
Catatan : 3,6 –Ag merupakan gugus 3,6-anhydro-D-galaktosa Sumber : Shi et al 1986 dalam FAO 1990
3. Penyaringan
Proses penyaringan ekstrak rumput laut dilakukan dua kali, yaitu penyaringan kasar dan penyaringan halus. Penyaringan kasar mengunakan kain saring atau rotary filter, sedangkan penyaringan halus dengan filter press atau door-oliver vacuum filter. Untuk menghindari terjadinya pembentukan gel, proses penyaringan dilakukan dalam keadaan panas. Untuk membantu mempermudah proses penyaringan dan menjernihkan filtrat dapat ditambahkan filter aid (Gliksman 1983). Jenis filter aid yang biasa digunakan adalah celite, atau alumunium aktif dengan konsentrasi berkisar antara 3 – 4 % (Anonim 2004)
4. Pemurnian
serat-serat koagulan yang selanjutnya dipisahkan dengan menggunakan
sentrifuge atau penyaring halus (McHugh 2003). 5. Pengeringan dan penepungan
Karaginan basah hasil pengendapan dengan alkohol dikeringkan dengan menggunakan oven. Pengeringan dengan oven dilakukan pada suhu 60 oC. Karaginan yang telah dikeringkan kemudian ditepung dan diayak. Diagram alir proses produksi karaginan secara ringkas disajikan pada Gambar 6 .
Perendaman
Ekstraksi
Penyaringan kasar
Penyaringan halus
Pengkonsentrasian
Pengendapan dengan alkohol Pengepresan gel
Pengeringan
Pengeringan
Recovery
alkohol
Penepungan
Penggilingan
Refined carrageenan
Ampas (residu)
Filter aid
Rumput Laut Pencucian
Air
Pengendapan dengan KCL
2.4 Standar Mutu Karaginan
Berdasarkan tingkat kemurniannya, karaginan dapat dibedakan menjadi dua jenis, yaitu semi refined carrageenan dan refined carrageenan. Perbedaan yang mendasar antara keduanya yaitu terletak pada kadar selulosa, kadar garam dan logam beratnya. Kadar selulosa pada semi refined carrageenan lebih tinggi, sedangkan kadar garamnya lebih rendah dibanding refined carrageenan. Adanya selulosa pada karaginan menyebabkan penampakan karaginan menjadi gelap (Jhondro 2000; Zamorano et al. 2002).
Tinggi rendahnya kandungan selulosa dapat ditentukan dari nilai bahan tidak larut asamnya. Kadar bahan tidak larut asam pada refined carrageenan umumnya 0,1% sedangkan semi refined carrageenan mengandung 10 – 15%. Kadar logam berat pada semi refined carrageenan lebih tinggi dari pada refined carrageenan
(Bixler dan Jhondro 2000). Pada Tabel 6 disajikan hasil analisis logam berat pada
refined carrageenan dan Philipphine Natural Grade (PNG), salah satu jenis produk semi refined carrageenan.
Tabel 6 Analisis kadar logam berat terhadap sampel refined carrageenan dan PNG komersial
Konsentrasi (mg/kg)
Refined carrageenan (39 sampel) PNG (30 sampel) Logam
Rata-rata Std. dev Rata-rata Std. dev
As 0,066 0,046 0,150 0,119
Cd 0,107 0,091 0,263 0,279
Hg 0,025 0,024 0,141 0,193
Pb 0,203 0,121 0,561 0,391
Std. dev = Standar deviasi Sumber : Bixler dan Jhondro 2000
Tabel 7 Standar mutu semi refined carrageenan dan refined carrageenan
Semi refined carrageenan Refined
carrageenan Kriteria European Commision* Codex Alimentarius* Food Chemical Codex* FAO** FAO***
Residu alkohol 0,1% total - - ≤ 1% ≤ 1%
pH - 8 - 11 - 8 - 11 8 - 11
Viskositas 1,5% pada 75oC
≥ 5 mPa/s ≥ 5 mPa/s ≥ 5 mPa/s ≥ 5 mPa/s ≥ 5 mPa/s
Susut pengeringan setalah 4 jam pada 105oC
Max 12% Max 12% Max 12% Max 12% Max 12%
Sulfat 15% - 40% 15% - 40% 18% - 40% 15% - 40% 15% - 40%
(basis kering) Total abu pada
550oC 1% – 40% 15% – 30% ≥35% 15% – 30%
15% - 40% (basis kering Abu tidak larut
asam (dalam 10% HCl)
≤ 1% ≤ 1% ≤ 1% ≤ 1% ≤ 1%
Bahan tidak larut asam (dalam 1% H2SO4)
8% - 15% 8% - 15% - 8% – 15% ≤ 2%
Arsen ≤ 3 mg/kg ≤ 3 mg/kg ≤ 3 mg/kg ≤ 3 mg/kg ≤ 3 mg/kg
Lead ≤ 5 mg/kg ≤ 2 mg/kg ≤ 10 mg/kg ≤ 5 mg/kg ≤ 5 mg/kg
Mercury ≤ 1 mg/kg ≤ 1mg/kg - ≤ 1mg/kg ≤ 1mg/kg
Cadmium ≤ 1 mg/kg ≤ 1 mg/kg - ≤ 2 mg/kg ≤ 1 mg/kg
Logam berat
sebagai Pb ≤ 20 mg/kg - ≤40 mg/kg - -
TPC ≤ 500 cfu/g ≤ 500 cfu/g - ≤ 500 cfu/g ≤ 500 cfu/g
Ragi dan jamur ≤ 300 cfu/g - - - -
E.coli Negatif
dalam 5 g
Negatif dalam 1 g
Negatif dalam 1 g
Negatif dalam 1 g
Negatif dalam 1 g
Salmonella spp Negatif
dalam 10 g negatif negatif negatif negatif
Sumber :
*) Bixler dan Jhondro, 2000
**) http://apps3.fao.org/jecfa/additive_specs/docs/9/additive-0830.htm
2.5 Proses Filtrasi dengan Membran
Membran merupakan lapisan tipis dari suatu material berpori yang dapat digunakan untuk proses pemisahan. Pori-pori yang kecil pada membran dapat berfungsi sebagai penghalang secara fisik, sehingga mampu meloloskan dan menghalangi molekul/senyawa tertentu. Menurut Renner dan El-Salam (1991), proses membran dikelompokan kedalam tiga kelas yaitu mikrofiltrasi, ultrafiltasi, dan reverse osmosis. Beberapa parameter yang menjadi indikator pengelompokkan tersebut disajikan pada Tabel 8.
Tabel 8 Pengelompokan proses membran berdasarkan kisaran ukuran partikel yang direjeksi.
Parameter Mikrofiltrasi Ultrafiltrasi Reverse osmosis
Ukuran partikel tertahan
> 106 Da 0,01-10 μm
103 - 106 Da 0,001 -0,02 μm
< 103 Da < 0,001μm
Tekanan (bar) <2 1 - 15 >20
Mekanisme penahanan
Penyaringan molekul
Penyaringan molekul
Difusi/ Penyaringan molekul
Fluks (l m-2 h-1) >300 30 - 300 3 - 30
Sumber : Renner dan El-Salam 1991
Membran mikrofiltrasi dan ultrafiltrasi telah banyak diaplikasikan dalam industri pangan untuk tujuan pengkonsentrasian, pemurnian biopolimer pada suatu larutan makromolekul seperti protein,dan polisakarida (Carrere et al. 1998; Jorda et al. 2002; Yeh dan Dong 2003; Cho et al. 2003).
Sistem operasi filtrasi membran dapat dilakukan dengan dua cara, yaitu sistem dead-end dan sistem cross-flow. Pada sistem dead-end umpan dilewatkan secara tegak lurus dengan membran sedangkan pada sistem cross-flow, umpan berupa larutan dialirkan sejajar dengan permukaan membran. Hasil proses pada sistem cross-flow terdiri dari dua fraksi, yaitu molekul-molekul yang dapat melewati pori-pori membran yang disebut permeat dan molekul berukuran besar yang tidak dapat melewati pori disebut retentat atau kosentrat (Gambar 7). sedangkan sistem dead-end hanya satu fraksi saja yaitu retentat. Sistem operasi
Gambar 7 Proses operasi filtrasi membran dengan sistem cross-flow
2.6 Model Fluks Hagen Poisuille.
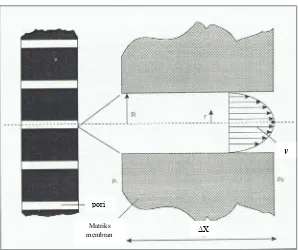
Bila membran memiliki ketebalan ΔX dan pori-pori diasumsikan berbentuk lingkaran dengan jari-jari R serta menyebar seragam dengan porositas . Jika suatu cairan dilewatkan pada permukaan membran dengan tekanan di bagian dalam membran P1 dan bagian luarnya P2. Jika P1>P2, maka sebagian cairan akan
keluar melewati pori membran dengan profil kecepatan aliran cairan (v) pada pori membran berbentuk seperti yang ditunjukkan pada Gambar 8.
Gambar 8 Profil kecepatan aliran zat cair yang melewati suatu membran (Krijgsman 1992)
Pori membran
membran Permeat
Permukaan membran
Molekul besar
Molekul kecil
Umpan Retentat
ΔX pori
Matriks membran
[image:32.595.159.457.458.708.2]Kecepatan aliran permeat akan semakin kecil dengan semakin dekatnya dengan dinding pori membran dan mencapai nilai nol ketika pada permukaan dinding pori membran. Adanya bentuk profil kecepatan aliran permeat yang demikian disebabkan oleh gaya gesek antara dinding pori membran dengan komponen molekul penyusun zat cair (Singh dan Heldman 1984). Besarnya nilai koefisien gaya gesek tersebut dinyatakan sebagai viskositas (η).
Jika fluks permeat (J) didefinisikan sebagai jumlah volume cairan yang melewati membran per satuan luas permukaan membran dan satuan waktu, model Hagen-Poiseuille memprediksi besarnya nilai fluks permeat tersebut seperti yang disajikan dalam persamaaan (1)
Keterangan :
J = Fluks permeat (m s-1) = Porositas membran R = Jari-jari pori membran (m)
ΔP = Selisih tekanan dalam membran dengan luar membran (Pa)
η = Viskositas cairan yang melewati pori membran (Pa s)
ΔX = Ketebalan membran (m)
Asumsi-asumsi yang dibuat dalam model tersebut adalah (Cheryan 1998):
1. Aliran yang melalui pori bersifat laminar (bilangan Renold kurang dari 2100). 2. Densitas konstan
3. Aliran independen terhadap waktu 4. Fluida bersifat Newtonian
Berdasarkan model tersebut terlihat bahwa fluks berbanding lurus dengan tekanan dan berbanding terbalik dengan viskositas bahan yang dipisahkan, hal ini berarti semakin tinggi tekanan operasi yang digunakan maka fluks yang dihasilkan akan semakin tinggi juga.
Ketebalan membran, porositas, dan jari-jari pori merupakan karakter yang unik dari suatu membran dan biasanya digabungkan menjadi satu yang biasa disebut dengan tahanan membran internal (Bai dan Leow 2002). Jika K merupakan koefisien permeabilitas membran (m Pa-1 s-1) dan Rm merupakan
(1) R2 ΔP
J =
tahanan membran internal (Pa s m-1), dan hubungan Rm = 1/K dan harga Rm dinyatakan dengan persamaan (2) sebagai berikut :
Maka melalui substitusi nilai Rm pada persamaan fluks (persamaan (1)) akan diperoleh persamaan persamaan (3):
Nilai fluks juga dapat dinyatakan dalam bentuk fungsi dari koefisien permeabilitas dan tekanan transmembran dengan persamaan (4) sebagai berikut:
2.7 Fouling dan Polarisasi Konsentrasi
Masalah utama dalam proses filtrasi dengan membran adalah menurunnya fluks selama proses filtrasi berlangsung. Secara umum dua faktor yang menyebabkan menurunnya fluks adalah fouling dan polarisasi konsentrasi.
2.7.1 Fouling
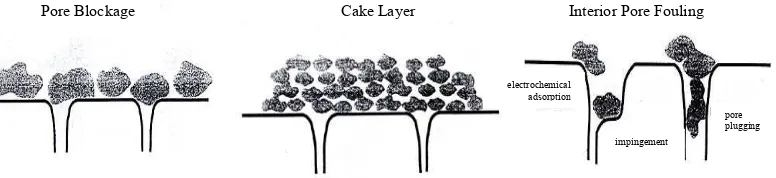
Fouling merupakan perubahan yang bersifat ireversibel yang disebabkan oleh interaksi secara fisik dan kimia antara membran dan partikel yang terdapat dalam larutan yang dipisahkan. Menurut Gould et al. (2004), fouling pada membran dapat terjadi pada 3 lokasi yaitu didekat, pada, atau dalam membran yang berupa penyumbatan pori (pore blocking), pembentukan lapisan cake dan penyumbatan pori membran bagian dalam atau interior pore fouling (Gambar 9).
ΔP J =
η Rm
(3)
J = K.ΔP (4)
8ΔX Rm =
R2
[image:34.595.130.518.628.717.2](2)
Gambar 9 Lokasi terjadinya fouling pada membran (Paulson 1995)
electrochemical adsorption
pore plugging impingement
2.7.2 Polarisasi konsenstrasi
Fenomena polarisasi konsentrasi muncul ketika proses mikrofiltrasi atau ultrafiltrasi dilakukan untuk memisahkan bahan-bahan seperti hidrokoloid, protein dan molekul besar lainnya. Molekul-molekul ini akan terejeksi dan menumpuk serta akan menutupi permukaan membran atau bahkan sampai membentuk lapisan gel atau cake (Cheryan 1998). Pada kondisi ini fluks tidak dipengaruhi lagi oleh tekanan tetapi dikendalikan oleh mekanisme perpindahan massa. Penggunaan tekanan yang lebih tinggi lagi tidak akan dapat meningkatkan besarnya fluks. Fenomena tingkah laku fluks pada daerah yang dikendalikan oleh transfer massa (mass transfer controlled region), dapat dijelaskan dengan menggunakan model transfer massa atau teori film.
2.8 Model Transfer Massa (Teori Film)
Model Hagen-Poiseuille hanya bisa menerangkan dengan tepat apabila kondisi operasi membran berlangsung pada tekanan rendah, konsentrasi rendah, dan laju alir yang tinggi. Pada kondisi tersebut fluks dikendalikan oleh tekanan operasi yang digunakan (pressure controlled region) dimana pengaruh polarisasi konsentrasi sangat kecil. Ketika proses operasi menyimpang jauh dari kondisi tersebut, maka fluks menjadi tidak dipengaruhi lagi oleh tekanan operasi (Cheryan 1998). Salah satu bentuk model yang dapat digunakan untuk memprediksi fluks pada kondisi pressure controlled region adalah model teori film.
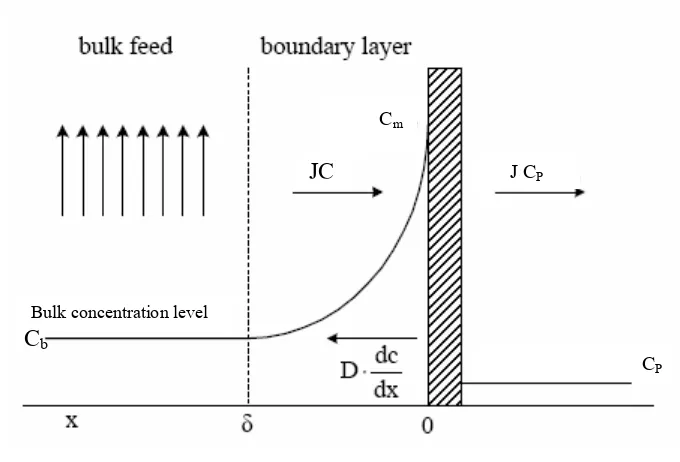
Jika suatu larutan yang terdiri dari sejumlah pelarut dan zat terlarut dengan konsentrasi Cb dilewatkan pada suatu membran dengan tekanan tertentu. Adanya
tekanan pada sisi umpan yang cukup tinggi akan menyebabkan sebagian pelarut dan zat terlarut melewati pori membran dan keluar sebagai permeat dengan konsentrasi Cp. Kondisi demikian menyebabkan konsentrasi lokal pada
permukaan membran (Cm) lebih tinggi dari konsentrasi umpan (Cb) dan permeat
(Cp) (Gambar 10).
Gambar 10 Profil konsentrasi selama proses filtrasi dengan membran (Mulder 1996)
Jika besarnya laju alir konvektif zat terlarut menuju permukaan membran dinyatakan Js dan nilainya equivalen dengan JC (persamaan 5).
Keterangan :
JS = Laju alir konvektif (m s-1) J = Laju fluks permeat (m s-1) C = Konsentrasi bahan terlarut (kg kg!)
Adanya akumulasi partikel zat terlarut yang tertahan pada permukaan membran akan meningkatkan konsentrasi padatan pada permukaan membran sehingga akan muncul gradien konsentrasi. Gradien konsentrasi ini menyebabkan aliran difusi balik (Jsb) yang arahnya berlawanan dengan aliran konvektif yaitu
menuju umpan yang besarnya dinyatakan dengan persamaan (6):
dimana D merupakan koefisien difusitas (m2 s-1) dan dC/dx merupakan gradien konsentrasi (kg kg-1 m-1). Kondisi kesetimbangan terjadi jika laju alir konvektif menuju permukaan membran (JC) sama dengan laju alir permeat (J Cp) ditambah
laju alir difusi balik (Jsb) persamaan (7) : dC
Jsb = -D
dx
(6)
JS = J C (5)
Cb
Bulk concentration level
JC
Cm
J CP
Apabila pada jarak tertentu misalnya x =
δ
merupakan jarak dari permukaan membran (m) dimana pencampuran homogen masih terjadi (Cb) dan kearah lebihdekat lagi dengan permukaan membran konsentrasi semakin meningkat dan mencapai pada permukaan membran pada x = 0. Melalui substitusi nilai-nilai tersebut dan mengintegralkan pada persamaan 8 maka akan diperoleh persamaan :
Nilai D/ diketahui sebagai koefisien transfer massa (m s-1), sehingga persaman tersebut menjadi persamaan (9):
Berdasarkan persamaan model diatas terlihat bahwa besarnya fluks dipengaruhi oleh koefisien transfer massa dan karakteristik fisikokimia larutan umpan (Cheryan 1998).
2.9 Model Tahan Seri
Pada model transfer massa terlihat bahwa, tidak ada komponen tekanan transmembran dalam model tersebut karena itu model ini tepat jika hanya digunakan pada daerah bebas pengaruh tekanan (pressure-independt region) dan sebaliknya tidak cocok untuk digunakan pada daerah yang dikendalikan oleh tekanan. Salah satu model yang bisa menjelaskan tingkah laku fluks untuk daerah yang dikendalikan oleh tekanan dan dikendalikan oleh transfer mass adalah model tahanan seri.
Pendekatan model tahanan seri dalam memprediksi fluks adalah lapisan partikel pada permukaan membran merupakan penghalang laju aliran permeat. Hal ini dapat dinyatakan dengan persamaan (10) sebagai berikut :
Dimana J merupakan laju fluks permeat (m s-1), ΔP merupakan tekanan transmembran (Pa) dan Rt merupakan nilai tahanan total (Pa s m-1)terhadap laju
Cw
J = (D/ ) ln Cb
(8)
Cw
J = K ln Cb
(9)
ΔP J = Rt
(10) dC
JC + ( - D ) = J Cp
dx
alir permeat. Adanya peristiwa fouling dan polarisasi konsentrasi menyebabkan tahanan membran bertambah, sehingga nilai total tahanan membran (Rt) merupakan penggabungan dari tahanan membran internal (Rm), tahanan membran karena fouling (Rf) dan tahanan membran karena proses polarisasi konsentrasi (Rp), seperti yang dinyatakan dalam persamaan 11.
Keterangan :
Rt = Tahanan total (P a s m-1)
Rm = Tahanan membran internal (Pa s m-1) Rf = Tahanan membran fouling (Pa s m-1) RP = Tahanan polarisasi konsentrasi (Pa s m-1)
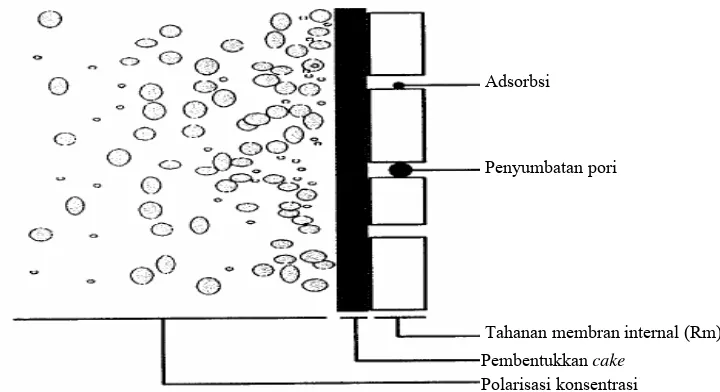
Secara visual posisi dan komponen penyusun tahanan pada proses filtrasi membran dapat dilihat pada Gambar 11. Chen et al. (1997) mengelompokkan proses penyumbatan pori dan pembentukan cake pada membran kedalam klasifikasi fouling, proses adsorbsi oleh membran pada proses mikrofiltrasi pengaruhnya diabaikan (Choi et al. 2005).
Nilai tahanan membran internal dapat ditentukan dengan menggunakan air murni sebagai umpan, sedangkan nilai Rf muncul akibat interaksi dari sifat membran dan partikel terlarut. Nilai Rf tidak dipengaruhi oleh parameter operasi dan biasanya Rf disatukan dengan nilai Rm menjadi R’m seperti pada
persamaan 12 (Cheryan 1998).
Rt = Rm+Rf+Rp (11)
Adsorbsi
Penyumbatan pori
Tahanan membran internal (Rm) Pembentukkan cake
[image:38.595.147.507.406.602.2]Polarisasi konsentrasi
Rp merupakan fungsi dari permeabilitas dan ketebalan gel yang merupakan fungsi dari tekanan, sehingga nilai tahanan membran karena polarisasi dapat dinyatakan dengan persamaan 13 :
Nilai Φ merupakan variabel yang mempengaruhi transfer massa seperti viskositas,
shear rate/laju alir dan suhu. Melalui subtitusi persamaan 12 dan 13 kedalam persamaan 10 maka model tahan seri dapat dinyatakan dengan persamaan (14) :
Keterangan :
J = Fluks permeat (m s-1)
R’m = Jumlah nilai tahanan membran internal dan tahanan fouling (Pa s m-1) Φ = Indeks tahanan polarisasi konsentrasi (s m-1)
P = Tekanan transmembran (Pa)
Model tahanan seri dapat digunakan baik pada daerah yang bertekanan rendah (pressure dependent) dan daerah yang bertekanan tinggi (pressure independent). Pada daerah yang dikendalikan oleh tekanan (pressure dependent) konsentrasi polarisasi terjadi sangat tipis (Rp<< R’m) dan J merupakan fungsi
linier dari ΔP. Pada daerah yang tidak dikendalikan oleh tekanan (pressure independent) ketebalan dan densitas lapisan polarisasi semakin bertambah dan Rp>> R’m. Pada kondisi ini J menjadi independen terhadap ΔP dengan nilai
pembatas 1/Φ.
2.10 Faktor-faktor yang Mempengaruhi Fluks 2.10.1 Tekanan transmembran
Tekanan transmembran merupakan driving force dalam proses filtrasi dengan menggunakan membran. Tekanan transmembran didefinisikan sebagai perbedaan tekanan antara sisi rententat dan permeat (persamaan (15)).
R’m = Rm+Rf (12)
Rp = ΦΔP (13)
P J =
R’m + Φ P
dimana : Pin = Tekanan pada saat masuk (Pa) Pout = Tekanan pada saat keluar (Pa)
Fluks permeat akan meningkat dengan semakin meningkatnya tekanan transmembran, tetapi korelasi ini hanya berlaku pada umpan air murni atau pada kondisi, tekanan rendah, konsentrasi umpan rendah, dan laju alir umpan yang tinggi (Mulder 1996). Jika umpan berupa larutan lain, maka besarnya fluks akan naik sampai batas tertentu, tetapi setelah mencapai tekanan tertentu fluks tidak akan meningkat walaupun tekanan dinaikkan.
2.10.2 Konsentrasi umpan
Model teori film menyatakan bahwa fluks akan menurun secara eksponensial jika konsentrasi umpan meningkat dan fluks akan mencapai nol jika terjadi konsentrasi umpan sama dengan konsentrasi gel (Mulder 1996). Kondisi ini berlaku pada setiap suhu dan tipe aliran yang berbeda
2.10.3 Laju alir umpan cross-flow
Laju alir umpan yang tinggi akan lebih banyak menghilangkan deposit material pada permukaan membran sehingga tahanan hidrolik dapat dikurangi dan fluks akan lebih besar. Laju alir umpan yang tinggi juga akan mengurangi fenomena polarisasi konsentrasi dengan semakin meningkatnya koefisien transfer massa. Tipe laju alir turbulensi akan menimbulkan efek pengadukan atau pemompaan fluida pada daerah mass transfer-controlled region (Mulder 1996). 2.10.4 Suhu
Suhu yang lebih tinggi akan menyebabkan fluks yang lebih besar baik pada
pressure controlled region maupun mass transfer controlled region. Suhu yang lebih tinggi akan menyebabkan penurunan viskositas bahan dan proses difusi akan menjadi lebih besar.
Pin + Pout
P = 2
3. METODOLOGI PENELITIAN
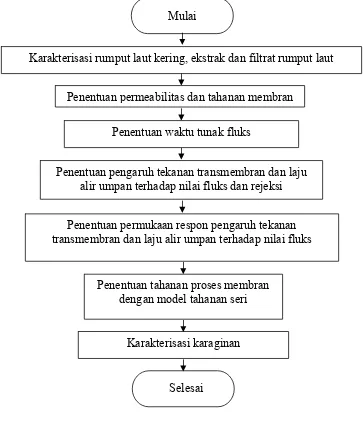
[image:41.595.124.487.299.727.2]Penelitian ini dilaksanakan dalam 7 tahap meliputi karakterisasi ekstrak rumput laut, penentuan permeabilitas dan tahanan membran, penentuan waktu tunak fluks, penentuan pengaruh tekanan transmembran dan laju alir umpan terhadap nilai fluks dan rejeksi, penentuan permukaan respon pengaruh tekanan transmembran dan laju alir umpan terhadap nilai fluks dan rejeksi, penentuan proses mikrofiltrasi dengan model tahanan seri dan karakterisasi karaginan. Diagram alir tahap penelitian disajikan pada Gambar 12.
Gambar 12. Diagram alir tahapan proses penelitian Karakterisasi karaginan
Selesai
Karakterisasi rumput laut kering, ekstrak dan filtrat rumput laut Mulai
Penentuan permeabilitas dan tahanan membran
Penentuan pengaruh tekanan transmembran dan laju alir umpan terhadap nilai fluks dan rejeksi
Penentuan permukaan respon pengaruh tekanan transmembran dan laju alir umpan terhadap nilai fluks
3.1 Bahan dan Alat
Bahan baku yang digunakan pada penelitian ini adalah Kappaphycuss alvarezii. Bahan-bahan kimia yang diperlukan pada tahap perendaman dan ekstraksi adalah : NaOH 0,1%, HCl 1%, sodium hipoklorit, dan aquades. Bahan kimia yang digunakan pada proses analisis adalah HCl, barium klorida, H2O2,
NaOH, dan H2SO4 95 -97%.
[image:42.595.156.475.433.648.2]Peralatan utama yang digunakan pada penelitian ini adalah satu unit membran cross-flow filtrasi (Gambar 13). Membran yang digunakan adalah mikrofiltrasi 0,1 mikron dengan bahan polysulfon. Jenis modul membran adalah tubular, yang terdiri dari 6 buah pipa dengan diameter 1,5 mm dan total luas permukaan efektif 26 cm2. Untuk keperluan preparasi bahan digunakan beberapa peralatan seperti blender, pemanas listrik, gelas ukur, pH meter, stop watch dan termometer, filter ukuran 350 mesh, 1 mikron dan 0,3 mikron. Untuk keperluan analisis dibutuhkan alat-alat: cawan porselen, desikator, timbangan analitik, labu erlenmeyer, gelas piala, gelas pengaduk, viskometer, spektrofotometer, tanur, pipet, curd tensionmeter, dan pH meter.
3.2 Prosedur Penelitian 3.2.1 Preparasi bahan
Tahapan proses preparasi bahan penelitian meliputi tahapan ekstraksi rumput laut dan tahapan prefiltrasi. Prosedur tahapan proses ekstraksi disajikan pada Lampiran 1.
3.2.2 Proses pemurnian dan pengkonsentrasian karaginan dengan mikrofiltrasi
Sistem proses pemurnian dan pengkonsentrasian karaginan dengan mikrofiltrasi ini disajikan dalam Gambar 14. Proses pemurnian dan pengkonsentrasian dilakukan dengan menggunakan membran mikrofiltrasi 0,1 mikron.
Pada proses pemurnian sejumlah filtrat ekstrak rumput laut (250 – 350 cm3) dimasukkan kedalam tangki umpan, kemudian dipanaskan hingga mencapai suhu 55 ± 1 oC. Untuk memanaskan dan mempertahankan umpan pada suhu tersebut,
3
1
2
6
8
9 7
10 4
8 5
Keterangan :
1. Tangki umpan 6. Pompa
2. Pemanas 7. Flow meter
3. Pengaduk 8. Pressure gauge
4. Termometer 9. Membrane mikrofiltrasi
5. Valve 10. Wadah permeat
tangki umpan dilengkapi dengan pemanas listrik. Produk hasil proses membran (permeat dan retentat) diresirkulasikan kedalam tangki umpan. Pada waktu tertentu dilakukan sampling terhadap permeat untuk pengukuran fluks dan nilai rejeksi.
Proses pemurnian dan pengkonsentrasian karaginan dilakukan dengan cara memasukkan 800 cm3 ekstrak rumput laut kedalam tangki umpan. Selama proses berlangsung fraksi permeat yang berupa air tidak resirkulasikan tetapi dibiarkan dalam wadahnya, sehingga fraksi retentat sebagai konsentrat menjadi semakin pekat. Indikator proses dievaluasi dengan melihat hubungan antara faktor konsentrasi dengan nilai fluks. Menurut Cheryan (1998) faktor konsentrasi didefinisikan sebagai perbadingan antara volume umpan diawal proses dengan volume retentatnya
Setiap proses membran selesai dilakukan, membran dicuci dengan cara meresirkulasikan larutan pembersih yang mengandung sodium hypochlorite. Sodium hypoclorite dari 200 ppm larutan klorin ditambah dengan NaOH 1% sehingga pH larutan menjadi 10,5 – 11,0. Fluks membran diuji kembali hingga mencapai fluks semula.
Variabel operasi yang dipilih meliputi tekanan transmembran (ΔP) dan laju alir umpan (v). Indikator kinerja membran dilihat dengan mengukur fluks permeat, sedangkan indikator kualitas produk yang dihasilkan ditentukan dengan mengukur nilai rejeksi membran. Sampling dan pengukuran nilai rejeksi pigmen dilakukan pada keadaan kondisi fluks steady state.
Nilai rejeksi yang diukur meliputi rejeksi karaginan (Robs (carr)) dan rejeksi
pigmen. Dua jenis pigmen yang diukur nilai rejeksinya meliputi fikoeritin (Robs(PE)) dan fikosianin (Robs(PS)) yang ditentukan secara spektrofotometri pada
panjang gelombang 530 dan 620 nm. Prosedur pengukuran fluks dan rejeksi disajikan pada Lampiran 2.
3.2.3 Analisis dan karakterisasi
dan kadar selulosa, sedangkan pada ekstrak dan filtrat meliputi kadar selulosa, nilai absorbansi pigmen fikosianin dan fikoeritin, rendemen serta viskositas. Parameter mutu karaginan yang diukur meliputi kadar air, kadar abu, kadar selulosa, kadar sulfat, kekuatan gel, viskositas, derajat kecerahan dan nilai rendemen. Prosedur analisis disajikan pada Lampiran 3.
3.2.4 Penentuan permeabilitas dan tahanan membran internal
Permeabilitas membran dan tahanan membran internal diukur dengan cara menggunakan air destilasi sebagai umpan. Proses pengukuran dilakukan pada suhu 30, 45 dan 55 oC dengan kisaran tekanan transmembran yang digunakan 69 – 103,5 kPa. Pada setiap suhu dan tekanan transmembran yang diujikan, besarnya fluks permeat air diukur.
Nilai permeabilitas membran (K) ditentukan dengan cara menghitung gradien plot grafik antara nilai fluks (Jw) sebagai sumbu Y dan tekanan transmembran
(ΔP) sebagai sumbu X. Penentuan nilai tahanan membran internal (Rm) dilakukan dengan cara membuat plot grafik nilai 1/Jw sebagai sumbu Y (ordinat)
dan 1/ΔP sebagai sumbu X (absis). Nilai tahanan membran diperoleh dengan cara menghitung gradien pada persamaan garis dari nilai plot 1/Jw dan 1/ΔP.
3.2.5 Penentuan waktu tunak fluks
Waktu tunak fluks ditentukan dengan menghitung fluks permeat sejak kondisi variabel proses terpasang. Jeda waktu pengukuran dan penghitungan fluks permeat dilakukan setiap satu menit sekali. Fluks dianggap tunak jika 5-10 kali pengukuran memperoleh nilai yang sama.
3.2.6 Penentuan pengaruh tekanan transmembran dan laju alir umpan terhadap nilai fluks dan rejeksi
3.2.7 Penentuan respon permukaan pengaruh tekanan transmembran dan laju alir umpan terhadap nilai fluks
Pada tahap ini kurva respon fluks dilakukan dengan rancangan CCD (Central Composite Design). Analisis parameter koefisein dan visualisasi grafik tiga dimensi dilakukan dengan menggunakan software Minitab 13.
3.2.8 Penentuan nilai fluks dengan model tahanan seri
Pendugaan nilai fluks sebagai fungsi dari tekanan transmembran pada laju alir umpan 2,97, 3,47 dan 3,97 m s-1 dilakukan dengan pendekatan model tahanan seri. Pada tahap ini dilakukan pengukuran dan penghitungan nilai-nilai komponen tahanan proses membran.
Nilai dan komponen tahanan proses membran yang diukur atau dihitung meliputi tahanan membran internal (Rm), tahanan fouling (Rf), dan tahanan polarisasi konsentrasi (Rp). Jumlah nilai Rm dan Rf ditentukan dengan cara menghitung nilai gradien dari plot garfik antara (1/J) sebagai sumbu Y dan (1/ΔP) sebagai sumbu X, sedangkan intersep dari grafik tersebut ditentukan sebagai nilai indeks tahanan polarisasi konsentrasi (Φ). Nilai Rp ditentukan dengan cara mengalikan indeks tahanan seri dengan tekanan transmembran (Rp = ΦΔP).
3.3 Rancangan Percobaan
3.3.1 Penentuan pengaruh tekanan transmembran dan laju alir umpan terhadap nilai fluks dan rejeksi
Rancangan percobaan yang digunakan dalam tahap penelitian ini adalah
two level factorial design (Box et al. 1979; Montgomery 2001). Dua parameter atau variabel yang dipilih meliputi tekanan transmembran (ΔP) dan laju alir umpan (v), sedangkan respon yang diukur adalah fluks (J) dan rejeksi (Robs).
Parameter, nilai taraf dan pengkodean variabel percobaan disajikan pada Tabel 9. Tabel 9 Penentuan taraf nilai sebenarnya dari variabel-varibel bebas
Nilai pengkodean dan taraf sebenarnya Parameter
Model rancangan percobaan untuk mengetahui hubungan linier dari variabel tekanan transmembran dan laju alir umpan terhadap respon nilai fluks dan rejeksi diberikan pada persamaan (17).
∑
+
∑
+
=
<j i j i ij i i io
a
x
a
x
x
a
Y
(17)Keterangan:
Y = Respon dari masing-masing perlakuan
ao, ai, aij, aii = Parameter regresi
xi = Pengaruh linier variabel utama
xixj = Pengaruh linier dua variabel
3.3.2 Penentuan permukaan respon fluks
Percobaan yang digunakan untuk menentukan model kuadratik pengaruh faktor terhadap respon adalah metoda permukaan respon (Response Surface) (Box et al. 1979; Montgomery 2001) dengan rancangan CCD (Central Composite Design). Model rancangan percobaan tersebut diberikan pada persamaan 18.
=
+
∑
+
∑
+
∑
<j i
i i i ii j i ij i i
o
a
x
a
x
x
a
x
a
Y
2(18 )
Keterangan :
Y = Respon dari masing-masing perlakuan
ao, ai, aij, aii = Parameter regresi
xi = Pengaruh linier variabel utama
xixj = Pengaruh linier dua variabel
2 i
x = Pengaruh kuadratik variabel utama
3.3.3 Penentuan tahanan proses membran dengan model tahanan seri
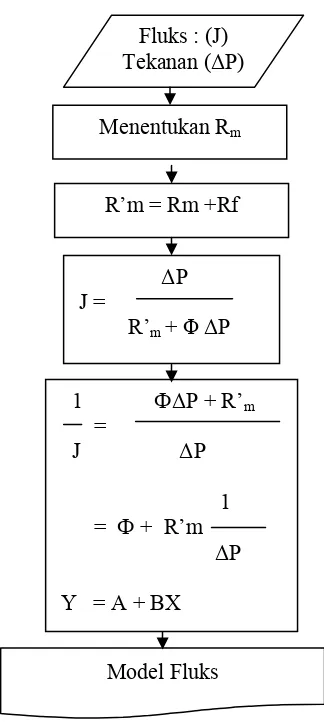
Gambar 15 Kerangka pemodelan proses membran dengan pendekatan model tahanan seri
1 ФΔP + R’m
= J ΔP
1 = Ф + R’m ΔP
Y = A + BX Menentukan Rm
Fluks : (J) Tekanan (ΔP)
Model Fluks ΔP J =
R’m + ΦΔP
4. HASIL DAN PEMBAHASAN
4.1 Karakterisasi Rumput Laut
Rumput laut Kappaphycus alvarezii merupakan salah satu spesies penghasil karaginan dari kelas Rhodophyceae. Rumput laut ini dalam keadaan kering berwarna merah agak kecoklatan dan terdapat bercak-bercak putih (Gambar 16). Warna merah disebabkan oleh adanya kandungan pigmen fikosianin dan fikoeritin yang dapat membentuk warna merah, sedangkan warna bercak putih timbul karena garam-garam yang terbawa pada saat pemanenan dan tidak semuanya dapat dihilangkan dengan proses pencucian.
[image:49.595.137.487.315.524.2]
Gambar 16 Rumput laut Kappaphycus alvarezii kering
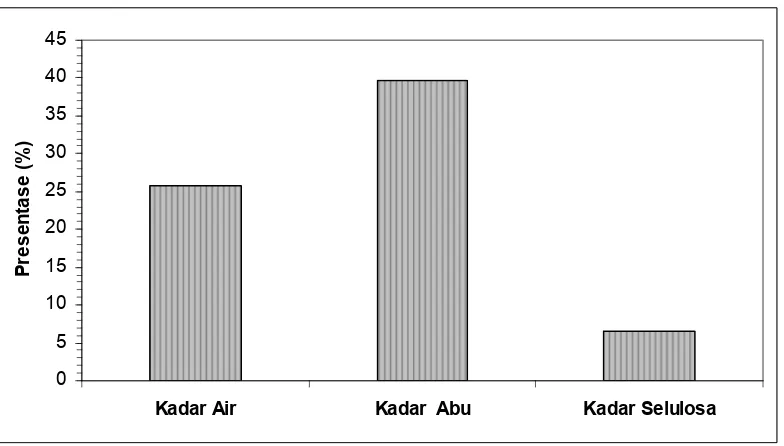
Pada Gambar 17 disajikan karakteristik fisika-kimia rumput laut kering tersebut. Kadar air rumput laut 25,86 ± 0,51 %, nilai ini masih memenuhi standar rumput laut kering yang disyaratkan SNI 01-2690-1998 yaitu maksimum 35 %. Kadar air dalam rumput laut akan bepengaruh terhadap mutu karaginan yang dihasilkan dan proses kecepatan penurunan mutu produk. Kadar air yang
tinggi dapat menyebabkan kekuatan gel, viskositas dan kandungan 3,6-anhidrogalaktosa menjadi turun (Anggadireja 1985). Selain hal tersebut,
0 5 10 15 20 25 30 35 40 45
Kadar Air Kadar Abu Kadar Selulosa
P
re
sen
ta
se (
%
[image:50.595.116.508.85.308.2])
Gambar 17 Karakterstik, kadar air, kadar abu dan kadar selulosa rumput laut kering Kappaphycus alvarezii
Kadar abu rumput laut mencapai 39,69 ± 0,21 % dan merupakan parameter paling tinggi diantara parameter lainnya yang diukur. Nilai kadar abu yang tinggi diduga berasal dari garam yang berasal dari mineral air laut dan pasir laut. Adanya pasir pada rumput laut dapat berasal dari dua sumber, yaitu pasir yang menempel pada subtrat dan yang terbawa pada saat penjemuran. Kadar abu dalam rumput laut dapat di kurangi dengan melakukan pencucian terlebih dahulu sebelum dikeringkan. Pencucian dan perendaman sebelum proses ekstraksi dapat membantu dalam menurunkan kadar abu pada karaginan.
4.2 Karakteristik Ekstrak dan Filtrat Rumput Laut
Karakterisasi dilakukan terhadap ekstrak dan filtrat hasil filtrasi yang diperoleh dengan penyaringan beberapa ukuran pori filter yang berbeda sebagai prefiltrasi. Parameter yang diamati meliputi warna ekstrak dan filtrat, kadar selulosa, viskositas dan rendemen. Proses prefiltrasi pada penelitian ini dilakukan untuk meningkatkan kinerja proses membran yaitu mengurangi intensitas polarisasi konsentrasi dan fouling serta dapat memperbaiki kualitas produk akhir. Proses prefiltrasi dilakukan melalui sistem dead-end dengan menggunakan ukuran pori 350 mesh, 1 mikron dan 0,3 mikron.
4.2.1 Warna
Ukuran pori filter yang digunakan untuk menyaring ekstrak rumput laut berpengaruh signifikan terhadap warna filtrat yang dihasilkan. Ekstrak rumput laut sebelum mendapat perlakuan filtrasi berwarna coklat-keruh dan masih terlihat serat-serat kasarnya. Setelah melewati filter 350 mesh, 1 mikron dan 0,3 mikron serat-serat kasar tersebut hilang dan warna filtrat menjadi semakin lebih jernih (Gambar 18). Munculnya warna coklat atau keruh pada ekstrak dan filtrat diduga disebabkan oleh masih adanya selulosa, pigmen fikoeritin, pigmen fikosianin, serta adanya konversi D-glukosa menjadi 5-hidroksilmetil furfural yang terbentuk selama proses pemanasan (Susanto dan Saneto, 1994).
0 1 2 3 4 5 6 7
Ekstrak 350 mesh 1 mikron 0,3 mikron
K
a
d
a
r Se
lu
lo
s
a
(
%
)
4.2.2 Kadar selulosa
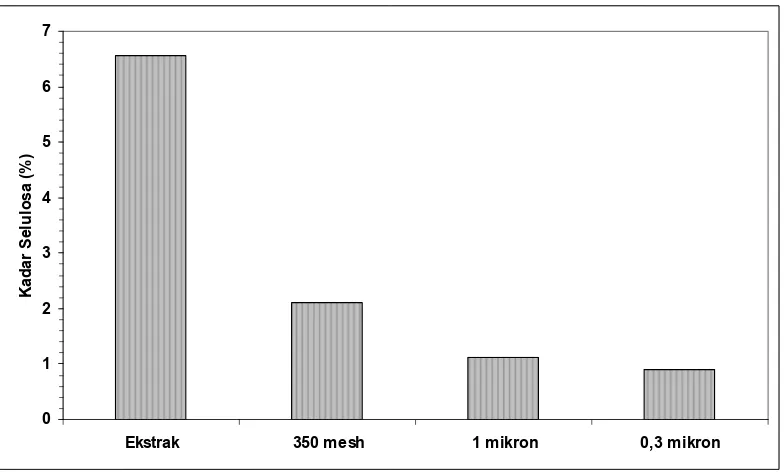
Kadar selulosa tertinggi diperoleh pada ekstrak rumput laut dengan nilai 6,57%, sedangkan kadar selulosa dalam filtrat rumput laut setelah melalui penyaringan dengan filter ukuran 350 mesh , 1 mikron dan 0,3 mikron masing-masing 2,10%, 1,12% dan 0,90 (Gambar 19). Kadar selulosa menurun dengan semakin halusnya ukuran filter. Besarnya nilai penurunan kadar selulosa yang disebabkan oleh perlakuan penyaringan dengan filter ukuran 350 mesh, 1 mikron dan 0,3 mikron dibandingkan dengan ekstraknya beturut-turut 68,04, 82,95 dan 86,30%.
[image:52.595.117.509.468.705.2]Kadar selulosa pada ekstrak hampir sama dengan kadar selulosa rumput laut kering (6,55%), hal tersebut menunjukkan bahwa proses ekstraksi tidak dapat mereduksi kadar selulosa dalam bahan. Berdasarkan hasil tersebut diketahui bahwa penggunaan filter ukuran 350 mesh sudah mendekati standar selulosa FAO dan filter ukuran 1 mikron sudah memenuhi kadar selulosa maksimum yang ditetapkan FAO. FAO telah menetapkan kadar selulosa maksimum dalam refined carrageenan paling tinggi 2%. Penggunaan filter ukuran 0,3 mikron dapat menghasilkan refined carrageenan dengan kadar selulosa jauh lebih rendah yang ditetapkan FDA yaitu maksimum1% (Bixler 1996).
Hasil analisis ragam pada α = 0,05 (Lampiran 4b) menunjukkan bahwa perlakuan ukuran pori berpengaruh signifikan terhadap nilai penurunan kadar selulosa dalam filtrat. Hasil analisis perbandingan berganda dengan uji Tukey menunjukkan bahwa penggunaan ukuran pori filter 350 mesh, 1 mikron dan 0,3 mikron berbeda nyata dalam menurunkan kadar selulosa dibandingkan dengan kadar selulosa dalam ekstraknya. Penggunaan filter ukuran 350 mesh, 1 mikr