SKRIPSI
LANGKAH AWAL PENGGANDAAN SKALA TEPUNG UBI
JALAR DAN BEBERAPA KARAKTERISTIKNYA
Oleh :
SENDHI DHANIA
F24101112
2006
FAKULTAS TEKNOLOGI PERTANIAN
INSTITUT PERTANIAN BOGOR
Finally I could get through one step
But it’s not the end
To me, this should be the beginning
From something bigger
Or maybe the biggest…
Sendhi Dhania. F24101112. Langkah Awal Penggandaan Skala Tepung Ubi Jalar dan Beberapa Karakteristiknya. Di bawah bimbingan Tien R. Muchtadi dan Dahrul Syah (2006).
Ringkasan
Ubi jalar merupakan salah satu tanaman palawija yang banyak terdapat di Indonesia. Ubi jalar memiliki kandungan nutrisi yang baik, umur yang relatif pendek, produksi yang tinggi, dan potensi lainnya. Ubi jalar juga dianggap murah, lebih manis, dan banyak mengandung komponen kalori, vitamin A dibandingkan dengan tepung terigu. Selain itu, ubi jalar juga merupakan salah satu komoditas lokal sumber serat pangan. Hal tersebut di atas terlihat bahwa ubi jalar mempunyai potensi untuk dikembangkan dengan berbasiskan kepada produk tepung.
Tujuan penelitian ini adalah untuk mengetahui pemetaan penelitian tepung ubi jalar hingga saat ini, memverifikasi proses pembuatan tepung ubi jalar dan merumuskan langkah awal untuk penggandaan skala produksi tepung ubi jalar yang memenuhi syarat dengan lokasi di Cibungbulang, Bogor- Barat dan mengetahui mutu tepung ubi jalar melalui sifat fisik dan kimianya. Penelitian ini meliputi studi pustaka yaitu pemetaan pemanfaatan tepung-tepungan yang berasal dari umbi-umbian, perumusan langkah awal penggandaan skala yang meliputi pembuatan tepung ubi jalar, pembuatan air klorinasi, pembuatan chips ubi jalar, penentuan kadar airnya, penentuan residu klorin yang akan digunakan dalam pembersihan ubi jalar dan penentuan Total Plate Count (TPC), Penentuan karakteristik fisik (pengukuran amilograf dan farinograf) dan kimia tepung ubi jalar (analisis proksimat dan serat).
Pemetaan pemanfaatan tepung-tepungan meliputi penentuan jenis komoditi, rekayasa proses, karakteristik dan aplikasi. Pembuatan tepung ubi jalar dalam penelitian ini menggunakan 3 jenis ubi jalar yaitu ubi jalar putih varietas sukuh (CIP-2 : AB94001), ubi jalar merah (Klon BB 00105.10) dan ubi jalar ungu (lokal). Pada pembuatan tepung ubi jalar, untuk skala industri, direkomendasikan digunakan ubi jalar putih untuk dijadikan tepung, karena memiliki nilai rendemen yang tinggi yaitu 30.21%. Hal ini disebabkan ubi jalar putih memilki kadar air yang rendah yaitu 62.59%.
Hasil analisis kimia menunjukkan kandungan gizi tertinggi adalah karbohidrat baik dalam bentuk segar maupun tepung. Untuk ubi jalar segar putih, merah dan ungu kandungan karbohidratnya masing-masing sebesar 8.84 Kg, 8.82 Kg dan 7.41 Kg (dalam basis kering), sedangkan untuk tepung ubi jalar putih, merah dan ungu masing-masing sebesar 2.67 Kg, 1.75 Kg dan 1.6 Kg (dalam basis kering). Selain itu, kandungan serat makanan yang tertinggi di dalam ubi jalar adalah serat makanan tidak larut, yaitu untuk tepung ubi jalar putih, tepung ubi jalar merah dan tepung ubi jalar ungu masing-masing sebesar 0.33 Kg, 0.22 Kg dan 0.21 Kg (dari berat awal).
Analisis sifat fisik berupa uji amilograf menghasilkan data untuk tepung ubi jalar putih, merah dan ungu yaitu parameter suhu awal gelatinisasi masing-masing 77.25oC, 61.5oC dan 77.25oC. Parameter suhu puncak gelatinisasi masing-masing 95.25oC, 81oC dan 97.13oC. Sedangkan untuk parameter viskositas maksimum sebesar 511 BU, 89.5 BU dan 297.5 BU. Analisis reologi berikutnya adalah uji farinograf. Uji farinograf dilakukan dengan penambahan air sebanyak 60.2% dan 67%, tetapi data tidak dapat dibaca dikarenakan adonan tidak elastis. Tidak terbacanya data pada uji farinograf juga menyebabkan tidak dapat dilakukannya uji ekstensograf.
LANGKAH AWAL PENGGANDAAN SKALA TEPUNG UBI
JALAR DAN BEBERAPA KARAKTERISTIKNYA
SKRIPSI
Sebagai salah satu syarat untuk memperoleh gelar
SARJANA TEKNOLOGI PERTANIAN
Pada Departemen Ilmu dan Teknologi Pangan
Fakultas Teknologi Pertanian
Institut Pertanian Bogor
Oleh
Sendhi Dhania
F24101112
2006
DEPARTEMEN ILMU DAN TEKNOLOGI PANGAN
FAKULTAS TEKNOLOGI PERTANIAN
FAKULTAS TEKNOLOGI PERTANIAN
INSTITUT PERTANIAN BOGOR
LANGKAH AWAL PENGGANDAAN SKALA TEPUNG UBI
JALAR DAN BEBERAPA KARAKTERISTIKNYA
SKRIPSI
Sebagai salah satu syarat untuk memperoleh gelar
SARJANA TEKNOLOGI PERTANIAN
Pada Departemen ILMU DAN TEKNOLOGI PANGAN
Fakultas Teknologi Pertanian
Institut Pertanian Bogor
Oleh:
SENDHI DHANIA
F24101112
Dilahirkan pada tanggal 30 Juni 1983
Di Jakarta
Tanggal lulus:
Mengetahui
Bogor, 2006
Prof. Dr. Ir. Tien R. Muchtadi, MS Dr. Ir. Dahrul Syah,MSc Dosen Pembimbing I Dosen Pembimbing II
Dr. Ir. Dahrul Syah,MSc
KATA PENGANTAR
Puji syukur penulis ucapkan kepada Allah SWT yang telah memberi karunia dan kebesaranNya sehingga penelitian dan penulisan skripsi ini dapat terlaksana dengan baik. Penulis juga ingin mengucapkan terimakasih kepada banyak pihak yang telah banyak membantu, yaitu:
1. Prof. Dr. Ir. Tien R. Muchtadi, MS selaku dosen pembimbing pertama yang telah membimbing dan mendidik penulis serta memberikan banyak pelajaran hidup. Terima kasih untuk kesempatan dan perhatian yang Ibu berikan, semoga Ibu selalu diberikan kebahagiaan oleh Allah SWT.
2. Dr. Ir. Dahrul Syah, MSc selaku dosen pembimbing kedua yang telah membimbing dan banyak membantu dalam pelaksanaan penelitian juga penulisan skripsi. Terimakasih atas kesabaran, perhatian, dan kesempatan yang diberikan untuk bergabung dengan RUSNAS (Riset Unggulan Strategis Nasional) dan mengikuti segala kegiatannya, semoga Bapak sehat dan bahagia selalu.
3. Dr. Yadi Haryadi, MSc selaku dosen penguji yang telah meluangkan waktu untuk menguji dan memberikan masukan-masukan untuk memperbaiki skripsi ini.
4. Kantor Kementrian Riset dan Teknologi melalui program RUSNAS DIVERSIFIKASI PANGAN, yang telah mendanai penelitian sehingga penelitian dapat berjalan dengan lancar.
5. Mamah, ayah, Fifi, serta keluarga besar yang telah begitu banyak memberikan semangat, kasih sayang, sumbangan tenaga dan materi untuk kelancaran penelitian. Terimakasih semuanya…..
6. Hendra Syahputra, yang selalu ada dan siap membantu. Terima kasih untuk kesabaran, kasih sayang , semangat dan dukungannya.
7. Desta, Vennia, Agnes, Rina, Hilda, Piesca, Ella, Dian, Harti dan Blobers. Tarima kasih atas semangat, perhatian, bantuan dan dukungannya selama penulis melakukan penelitian dan terimakasih untuk keceriaannya selama empat tahun.
9. Hendry dan Octa. Terimakasih atas semangat dan dukungannya serta telah menjadi temen sebimbingan yang baik.
10. Irus dan Udin. Terima kasih atas kerjasama dan bantuannya selama penelitiaan dalam satu tim.
11. Anak-anak golongan D : Inggrid, Pande, Reni dan Astri. Terimakasih untuk empat tahun indahnya.
12. Anto, Zen, Firzi, Sidik, Aulia, Kanyaka, Dedi, Endang, Eko, Mbak Erna. Terimakasih telah menjadi saudara satu bimbingan yang selalu memberikan keceriaan dan dukungan kepada penulis
13. Yuanita, Fanny, Via, Aya, Christina dan Putri. Terimakasih atas bantuannya selama penelitiaan di lab.
14. Joan, Merry, Vany, BarQ, Pipal, Joe dan Tanto. Terimakasih untuk kenangan indahnya selama dua bulan (KKN) di desa tercinta Sirna galih yang telah banyak memberikan pelajaran dan perubahan hidup terhadap diri penulis serta menjadi keluarga kedua . Sukses buat semuanya.
15. Ningrum, Lina dan Novi. Terimakasih untuk waktu indahnya selama di bangku kuliah dan semangatnya.
16. Firman, Elia, Bang Fahmy,A’Budi, A’Dede.Terimakasih untuk semangatnya 17. Pak Ade dan Teh Yuli. Terimakasih atas kebaikan dan bantuannya.
18. Pak Ilyas, Pak Jun, Pak Chamdani, Pak Mashudi, Pak Sobirin, dan laboran lainnya yang telah banyak membantu pelaksanaan penelitian.
19. Teman–teman TPG 38 dan 39 lainnya yang telah membuat kampus menyenangkan.
Penulis menyadari bahwa tulisan (skripsi) ini masih jauh dari sempurna. Penulis Sangat terbuka menerima saran dan kritik membangun untuk perbaikan. Semoga tulisan ini memberikan manfaat bagi yang membacanya.
Bogor, Februari 2006
RIWAYAT HIDUP
Penulis bernama Sendhi Dhania, dilahirkan di Jakarta pada tanggal 30 Juni 1983. Penulis merupakan anak pertama dari dua bersaudara dari pasangan Iwan Budhi Setyawan dan Endang Kardinah.
Riwayat pendidikan penulis dimulai dari TK Islam Al-Muhajirin (1987-1989). Penulis menyelesaikan pendidikan dasar di SD Madrasah Pembangunan IAIN Jakarta (1989-1995), dilanjutkan ke jenjang berikutnya yaitu Sekolah Menengah Pertama Negeri 19 Jakarta (1995-1998), kemudian Sekolah Menengah Umum Negeri 6 Jakarta (1998-2001). Penulis masuk ke Institut Pertanian Bogor (IPB), Departemen Ilmu dan Teknologi Pangan melalui jalur UMPTN (Ujian Masuk Perguruan Tinggi Negeri).
Selama di IPB penulis merupakan anggota dari HIMITEPA (Himpunan Mahasiswa Teknologi Pangan (2001-2006), pengurus harian HIMITEPA Divisi Kesekretariatan (2003-2004), pengurus Food Chat tahun 2003-2004 disamping itu penulis pernah menjadi panitia BAUR TPG tahun 2003, panitia LCTIP (Lomba Cepat Tepat Ilmu Pangan) tahun 2003, panitia Open House dan Pameran RUSNAS (Riset Unggulan Strategis Nasional ) Kementerian Riset dan Teknologi tahun 2003 dan tahun 2005, panitia pelatihan HACCP (Hazard and Analytical Control Point) tahun 2004 dan panitia NSPC (National Students Paper Competition) tahun 2003-2004. Pada Tahun 2004 penulis pernah menjadi asisten untuk praktikum Teknologi Pengolahan Bumbu dan Rempah. Penulis melakukan Kuliah Kerja Nyata pada tahun 2004 di desa Sirna Galih Kecamatan Taman Sari Kabupaten Bogor.
DAFTAR ISI
Halaman
KATA PENGANTAR... I RIWAYAT HIDUP...
DAFTAR ISI...
iii iv DAFTAR TABEL... Vi DAFTAR GAMBAR... Vii DAFTAR LAMPIRAN... Viii
I. PENDAHULUAN... 1
A. Latar Belakang... 1
B. Tujuan, Sasaran dan Manfaat Penelitian... 2
II. TINJAUAN PUSTAKA... 3
A. UBI JALAR... 3
1. Botani Ubi Jalar... 3
2. Produksi Ubi Jalar... 4
3. Komposisi Kimia Ubi Jalar... 6
4. Pengolahan Ubi Jalar... 10
5. Tepung Ubi Jalar... 11
B. SIFAT REOLOGI ADONAN... 13
C. SERAT PANGAN... 14
1. Selulosa... 14
2. Hemiselolosa... 15
3. Pektin... 15
4. Lignin... 16
D. KLORINASI AIR... 17
III. METODOLOGI... 22
A. BAHAN DAN ALAT... 22
B. METODE PENELITIAN... 22
1. Studi Pustaka Pemanfaatan Tepung-Tepungan... 24
2. Langkah Awal Penggandaan Skala... 24
SKRIPSI
LANGKAH AWAL PENGGANDAAN SKALA TEPUNG UBI
JALAR DAN BEBERAPA KARAKTERISTIKNYA
Oleh :
SENDHI DHANIA
F24101112
2006
FAKULTAS TEKNOLOGI PERTANIAN
INSTITUT PERTANIAN BOGOR
Finally I could get through one step
But it’s not the end
To me, this should be the beginning
From something bigger
Or maybe the biggest…
Sendhi Dhania. F24101112. Langkah Awal Penggandaan Skala Tepung Ubi Jalar dan Beberapa Karakteristiknya. Di bawah bimbingan Tien R. Muchtadi dan Dahrul Syah (2006).
Ringkasan
Ubi jalar merupakan salah satu tanaman palawija yang banyak terdapat di Indonesia. Ubi jalar memiliki kandungan nutrisi yang baik, umur yang relatif pendek, produksi yang tinggi, dan potensi lainnya. Ubi jalar juga dianggap murah, lebih manis, dan banyak mengandung komponen kalori, vitamin A dibandingkan dengan tepung terigu. Selain itu, ubi jalar juga merupakan salah satu komoditas lokal sumber serat pangan. Hal tersebut di atas terlihat bahwa ubi jalar mempunyai potensi untuk dikembangkan dengan berbasiskan kepada produk tepung.
Tujuan penelitian ini adalah untuk mengetahui pemetaan penelitian tepung ubi jalar hingga saat ini, memverifikasi proses pembuatan tepung ubi jalar dan merumuskan langkah awal untuk penggandaan skala produksi tepung ubi jalar yang memenuhi syarat dengan lokasi di Cibungbulang, Bogor- Barat dan mengetahui mutu tepung ubi jalar melalui sifat fisik dan kimianya. Penelitian ini meliputi studi pustaka yaitu pemetaan pemanfaatan tepung-tepungan yang berasal dari umbi-umbian, perumusan langkah awal penggandaan skala yang meliputi pembuatan tepung ubi jalar, pembuatan air klorinasi, pembuatan chips ubi jalar, penentuan kadar airnya, penentuan residu klorin yang akan digunakan dalam pembersihan ubi jalar dan penentuan Total Plate Count (TPC), Penentuan karakteristik fisik (pengukuran amilograf dan farinograf) dan kimia tepung ubi jalar (analisis proksimat dan serat).
Pemetaan pemanfaatan tepung-tepungan meliputi penentuan jenis komoditi, rekayasa proses, karakteristik dan aplikasi. Pembuatan tepung ubi jalar dalam penelitian ini menggunakan 3 jenis ubi jalar yaitu ubi jalar putih varietas sukuh (CIP-2 : AB94001), ubi jalar merah (Klon BB 00105.10) dan ubi jalar ungu (lokal). Pada pembuatan tepung ubi jalar, untuk skala industri, direkomendasikan digunakan ubi jalar putih untuk dijadikan tepung, karena memiliki nilai rendemen yang tinggi yaitu 30.21%. Hal ini disebabkan ubi jalar putih memilki kadar air yang rendah yaitu 62.59%.
Hasil analisis kimia menunjukkan kandungan gizi tertinggi adalah karbohidrat baik dalam bentuk segar maupun tepung. Untuk ubi jalar segar putih, merah dan ungu kandungan karbohidratnya masing-masing sebesar 8.84 Kg, 8.82 Kg dan 7.41 Kg (dalam basis kering), sedangkan untuk tepung ubi jalar putih, merah dan ungu masing-masing sebesar 2.67 Kg, 1.75 Kg dan 1.6 Kg (dalam basis kering). Selain itu, kandungan serat makanan yang tertinggi di dalam ubi jalar adalah serat makanan tidak larut, yaitu untuk tepung ubi jalar putih, tepung ubi jalar merah dan tepung ubi jalar ungu masing-masing sebesar 0.33 Kg, 0.22 Kg dan 0.21 Kg (dari berat awal).
Analisis sifat fisik berupa uji amilograf menghasilkan data untuk tepung ubi jalar putih, merah dan ungu yaitu parameter suhu awal gelatinisasi masing-masing 77.25oC, 61.5oC dan 77.25oC. Parameter suhu puncak gelatinisasi masing-masing 95.25oC, 81oC dan 97.13oC. Sedangkan untuk parameter viskositas maksimum sebesar 511 BU, 89.5 BU dan 297.5 BU. Analisis reologi berikutnya adalah uji farinograf. Uji farinograf dilakukan dengan penambahan air sebanyak 60.2% dan 67%, tetapi data tidak dapat dibaca dikarenakan adonan tidak elastis. Tidak terbacanya data pada uji farinograf juga menyebabkan tidak dapat dilakukannya uji ekstensograf.
LANGKAH AWAL PENGGANDAAN SKALA TEPUNG UBI
JALAR DAN BEBERAPA KARAKTERISTIKNYA
SKRIPSI
Sebagai salah satu syarat untuk memperoleh gelar
SARJANA TEKNOLOGI PERTANIAN
Pada Departemen Ilmu dan Teknologi Pangan
Fakultas Teknologi Pertanian
Institut Pertanian Bogor
Oleh
Sendhi Dhania
F24101112
2006
DEPARTEMEN ILMU DAN TEKNOLOGI PANGAN
FAKULTAS TEKNOLOGI PERTANIAN
FAKULTAS TEKNOLOGI PERTANIAN
INSTITUT PERTANIAN BOGOR
LANGKAH AWAL PENGGANDAAN SKALA TEPUNG UBI
JALAR DAN BEBERAPA KARAKTERISTIKNYA
SKRIPSI
Sebagai salah satu syarat untuk memperoleh gelar
SARJANA TEKNOLOGI PERTANIAN
Pada Departemen ILMU DAN TEKNOLOGI PANGAN
Fakultas Teknologi Pertanian
Institut Pertanian Bogor
Oleh:
SENDHI DHANIA
F24101112
Dilahirkan pada tanggal 30 Juni 1983
Di Jakarta
Tanggal lulus:
Mengetahui
Bogor, 2006
Prof. Dr. Ir. Tien R. Muchtadi, MS Dr. Ir. Dahrul Syah,MSc Dosen Pembimbing I Dosen Pembimbing II
Dr. Ir. Dahrul Syah,MSc
KATA PENGANTAR
Puji syukur penulis ucapkan kepada Allah SWT yang telah memberi karunia dan kebesaranNya sehingga penelitian dan penulisan skripsi ini dapat terlaksana dengan baik. Penulis juga ingin mengucapkan terimakasih kepada banyak pihak yang telah banyak membantu, yaitu:
1. Prof. Dr. Ir. Tien R. Muchtadi, MS selaku dosen pembimbing pertama yang telah membimbing dan mendidik penulis serta memberikan banyak pelajaran hidup. Terima kasih untuk kesempatan dan perhatian yang Ibu berikan, semoga Ibu selalu diberikan kebahagiaan oleh Allah SWT.
2. Dr. Ir. Dahrul Syah, MSc selaku dosen pembimbing kedua yang telah membimbing dan banyak membantu dalam pelaksanaan penelitian juga penulisan skripsi. Terimakasih atas kesabaran, perhatian, dan kesempatan yang diberikan untuk bergabung dengan RUSNAS (Riset Unggulan Strategis Nasional) dan mengikuti segala kegiatannya, semoga Bapak sehat dan bahagia selalu.
3. Dr. Yadi Haryadi, MSc selaku dosen penguji yang telah meluangkan waktu untuk menguji dan memberikan masukan-masukan untuk memperbaiki skripsi ini.
4. Kantor Kementrian Riset dan Teknologi melalui program RUSNAS DIVERSIFIKASI PANGAN, yang telah mendanai penelitian sehingga penelitian dapat berjalan dengan lancar.
5. Mamah, ayah, Fifi, serta keluarga besar yang telah begitu banyak memberikan semangat, kasih sayang, sumbangan tenaga dan materi untuk kelancaran penelitian. Terimakasih semuanya…..
6. Hendra Syahputra, yang selalu ada dan siap membantu. Terima kasih untuk kesabaran, kasih sayang , semangat dan dukungannya.
7. Desta, Vennia, Agnes, Rina, Hilda, Piesca, Ella, Dian, Harti dan Blobers. Tarima kasih atas semangat, perhatian, bantuan dan dukungannya selama penulis melakukan penelitian dan terimakasih untuk keceriaannya selama empat tahun.
9. Hendry dan Octa. Terimakasih atas semangat dan dukungannya serta telah menjadi temen sebimbingan yang baik.
10. Irus dan Udin. Terima kasih atas kerjasama dan bantuannya selama penelitiaan dalam satu tim.
11. Anak-anak golongan D : Inggrid, Pande, Reni dan Astri. Terimakasih untuk empat tahun indahnya.
12. Anto, Zen, Firzi, Sidik, Aulia, Kanyaka, Dedi, Endang, Eko, Mbak Erna. Terimakasih telah menjadi saudara satu bimbingan yang selalu memberikan keceriaan dan dukungan kepada penulis
13. Yuanita, Fanny, Via, Aya, Christina dan Putri. Terimakasih atas bantuannya selama penelitiaan di lab.
14. Joan, Merry, Vany, BarQ, Pipal, Joe dan Tanto. Terimakasih untuk kenangan indahnya selama dua bulan (KKN) di desa tercinta Sirna galih yang telah banyak memberikan pelajaran dan perubahan hidup terhadap diri penulis serta menjadi keluarga kedua . Sukses buat semuanya.
15. Ningrum, Lina dan Novi. Terimakasih untuk waktu indahnya selama di bangku kuliah dan semangatnya.
16. Firman, Elia, Bang Fahmy,A’Budi, A’Dede.Terimakasih untuk semangatnya 17. Pak Ade dan Teh Yuli. Terimakasih atas kebaikan dan bantuannya.
18. Pak Ilyas, Pak Jun, Pak Chamdani, Pak Mashudi, Pak Sobirin, dan laboran lainnya yang telah banyak membantu pelaksanaan penelitian.
19. Teman–teman TPG 38 dan 39 lainnya yang telah membuat kampus menyenangkan.
Penulis menyadari bahwa tulisan (skripsi) ini masih jauh dari sempurna. Penulis Sangat terbuka menerima saran dan kritik membangun untuk perbaikan. Semoga tulisan ini memberikan manfaat bagi yang membacanya.
Bogor, Februari 2006
RIWAYAT HIDUP
Penulis bernama Sendhi Dhania, dilahirkan di Jakarta pada tanggal 30 Juni 1983. Penulis merupakan anak pertama dari dua bersaudara dari pasangan Iwan Budhi Setyawan dan Endang Kardinah.
Riwayat pendidikan penulis dimulai dari TK Islam Al-Muhajirin (1987-1989). Penulis menyelesaikan pendidikan dasar di SD Madrasah Pembangunan IAIN Jakarta (1989-1995), dilanjutkan ke jenjang berikutnya yaitu Sekolah Menengah Pertama Negeri 19 Jakarta (1995-1998), kemudian Sekolah Menengah Umum Negeri 6 Jakarta (1998-2001). Penulis masuk ke Institut Pertanian Bogor (IPB), Departemen Ilmu dan Teknologi Pangan melalui jalur UMPTN (Ujian Masuk Perguruan Tinggi Negeri).
Selama di IPB penulis merupakan anggota dari HIMITEPA (Himpunan Mahasiswa Teknologi Pangan (2001-2006), pengurus harian HIMITEPA Divisi Kesekretariatan (2003-2004), pengurus Food Chat tahun 2003-2004 disamping itu penulis pernah menjadi panitia BAUR TPG tahun 2003, panitia LCTIP (Lomba Cepat Tepat Ilmu Pangan) tahun 2003, panitia Open House dan Pameran RUSNAS (Riset Unggulan Strategis Nasional ) Kementerian Riset dan Teknologi tahun 2003 dan tahun 2005, panitia pelatihan HACCP (Hazard and Analytical Control Point) tahun 2004 dan panitia NSPC (National Students Paper Competition) tahun 2003-2004. Pada Tahun 2004 penulis pernah menjadi asisten untuk praktikum Teknologi Pengolahan Bumbu dan Rempah. Penulis melakukan Kuliah Kerja Nyata pada tahun 2004 di desa Sirna Galih Kecamatan Taman Sari Kabupaten Bogor.
DAFTAR ISI
Halaman
KATA PENGANTAR... I RIWAYAT HIDUP...
DAFTAR ISI...
iii iv DAFTAR TABEL... Vi DAFTAR GAMBAR... Vii DAFTAR LAMPIRAN... Viii
I. PENDAHULUAN... 1
A. Latar Belakang... 1
B. Tujuan, Sasaran dan Manfaat Penelitian... 2
II. TINJAUAN PUSTAKA... 3
A. UBI JALAR... 3
1. Botani Ubi Jalar... 3
2. Produksi Ubi Jalar... 4
3. Komposisi Kimia Ubi Jalar... 6
4. Pengolahan Ubi Jalar... 10
5. Tepung Ubi Jalar... 11
B. SIFAT REOLOGI ADONAN... 13
C. SERAT PANGAN... 14
1. Selulosa... 14
2. Hemiselolosa... 15
3. Pektin... 15
4. Lignin... 16
D. KLORINASI AIR... 17
III. METODOLOGI... 22
A. BAHAN DAN ALAT... 22
B. METODE PENELITIAN... 22
1. Studi Pustaka Pemanfaatan Tepung-Tepungan... 24
2. Langkah Awal Penggandaan Skala... 24
b. Pembuatan Air Klorinasi... 25
c. Pembuatan Chips Ubi Jalar Menggunakan Air Klorinasi. 26 d. Pengukuran Residu Klorin... 26
e. Uji Total Plate Count (TPC)... 27
3.Karakteristik Tepung Ubi Jalar... 27
a. Sifat Kimia Tepung Ubi Jalar………... 27
b. Sifat Fisik Tepung Ubi Jalar... 32
IV. HASIL DAN PEMBAHASAN……….. 35
A. Studi Pustaka Pemanfaatan Tepung-Tepungan... 35
B. Langkah Awal Penggandaan Skala... 36
1. Pembuatan Tepung Ubi Jalar... 36
2. Klorinasi Air dan Penentuan Residu Klorin... 39
3. Pembuatan Chips Ubi Jalar Menggunakan Air Klorinasi.... 41
4. Pengukuran Total Plate Count (TPC)... 43
5. Pengukuran Kadar Air Chips Ubi Jalar... 47
C. Karakteristik Tepung Ubi Jalar... 47
1. Sifat Kimia Tepung Ubi Jalar………... 47
a. Kandungan Air... 48
b. Kandungan Abu... 49
c.Kandungan Protein... 50
d. Kandungan Lemak... 51
e. Kandungan Karbohidrat... 53
f. Kandungan Serat Pangan... 53
2. Sifat Fisik Tepung Ubi Jalar... 54
a. Uji Pengukuran Viskositas (Amilograf)………... 54
b. Uji Ketahanan Adonan (Farinograf) dan Kemampuan Penyerapan Air pada Tepung (Ekstensograf )... 58
V KESIMPULAN DAN SARAN... 61
A. Kesimpulan... 61
B. Saran... 62 DAFTAR PUSTAKA...
LAMPIRAN...
DAFTAR TABEL
Halaman
Tabel 1.
Tabel 2.
Data perkembangan produksi ubi kayu dan ubi Jalar di Indonesia dari tahun 2001 hingga tahun 2004...
Spesifikasi jenis ubi jalar merah, putih dan ungu…………
5
6
Tabel 3. Komposisi kimia ubi jalar per 100 gram bahan segar... 7
Tabel 4. Komponen serat pangan ubi jalar mentah asal Tonga... 9
Tabel 5. Komposisi umum karbohidrat ubi jalar yang telah diolah
dengan pemanasan (pemasakan)………... 9
Tabel 6. Sifat reologi adonan tepung ubi jalar dengan menggunakan
amilograf... 14
Tabel 7. Analisis jumlah total padatan dan rendemen ubi jalar... 38
Tabel 8. Konsentrasi, residu dan harga klorin (Rp/ g)... 40 Tabel 9. Pengeringan sawut ubi jalar dengan menggunakan bed
dryer... 43 Tabel 10. Total Plate Count (TPC) chips ubi jalar menggunakan air
PT.FITS terklorinasi ... 43
Tabel 11. Total Plate Count (TPC) air yang digunakan untuk pembuatan Chips ubi jalar………... 44 Tabel 12. Total Plate Count (TPC) chips ubi jalar putih dengan
menggunakan berbagai sumber air... 45
Tabel 13. Kadar air Chips ubi jalar dengan menggunakan berbagai
sumber air... 47
Tabel 14. Karakteristik kimia (analisis proksimat) ubi jalar segar
(dalam Kg basis kering)... 48
Tabel 15. Karakteristik kimia (analisis proksimat) tepung ubi jalar
(dalam Kg basis kering)... 48
Tabel 16. Analisis serat makanan tepung ubi jalar (dalam Kg basis
kering)... 48
DAFTAR GAMBAR
Halaman
Gambar 1. Struktur kimia selulosa... 14
Gambar 2. Struktur kimia hemiselulosa... 15
Gambar 3. Struktur kimia pektin... 16
Gambar 4. Struktur kimia lignin... 17
Gambar 5. Reaksi klorin dalam air... 19
Gambar 6. Proses pembuatan tepung ubi jalar ... 24
Gambar 7. Proses pembuatan air klorinasi... 25
Gambar 8. Proses pembuatan chips ubi jalar... 26 Gambar 9. Tepung ubi jalar putih hasil pengayakan 60 mesh ... 37
Gambar 10. Tepung ubi jalar merah hasil pengayakan 60 mesh... 37
Gambar 11. Tepung ubi jalar ungu hasil pengayakan 60 mesh... 37
Gambar 12. Grafik hubungan dosis klorin dengan residu klorin... 40
Gambar 13. Histogram Jumlah TPC dengan Berbagai Konsentrasi
Klorin (g/lt)………... 44
Gambar 14. Histogram jumlah TPC dari sumber air yang digunakan
untuk pembuatan chips ubi jalar………... 45 Gambar15. Histogram TPC chips ubi jalar dengan menggunakan
DAFTAR LAMPIRAN
Halaman
Lampiran 1. Pemetaan pemanfaatan tepung-tepungan... 71
Lampiran 2. Komoditi yang digunakan untuk tepung, potensi, peluang
dan kepercayaan dalam masyarakat... 78
Lampiran 3. Jenis-jenis Ubi jalar yang digunakan untuk pembuatan
tepung ………... 80
Lampiran 4. Mikrochlorine test yang digunakan untuk mengukur residu
klorin ………... 81
Lampiran 5. Pembuatan larutan stok klorin ………. 82
Lampiran 6. Perhitungan absolut (g) dan harga klorin Rp/g ………... 83 Lampiran 7. Rekapitulasi Total Plate Count (TPC) air PT.FITS ……. 85 Lampiran 8. Rekapitulasi Total Plate Count (TPC) air Cibungbulang... 86
Lampiran 9. Rekapitulasi Total Plate Count (TPC) air Cibungbulang
dengan menggunakan residu klorin 200 ppm……….. 87 Lampiran 10. Rekapitulasi Total Plate Count(TPC) chips ubi jalar
dengan menggunakan air PT.FITS………. 88
Lampiran 11. Rekapitulasi Total Plate Count (TPC) chips ubi jalar dengan menggunakan air PT.FITS dengan klorinasi………... 89
Lampiran 12. Rekapitulasi Total Plate Count(TPC) chips ubi jalar
dengan menggunakan air Cibungbulang………... 90
Lampiran 13. Rekapitulasi Total Plate Count (TPC) chips ubi jalar
menggunakan air Cibungbulang dengan residu klorinasi . 91
Lampiran 14. Rekapitulasi hasil analisis amilograf tepung ubi jalar……. 92 Lampiran 15. Kurva amilograf tepung ubi jalar putih pada beberapa kali
ulangan... 93
Lampiran 16. Kurva amilograf tepung ubi jalar putih pada beberapa
kali ulangan (Lanjutan)……… 94
Lampiran 17. Kurva amilograf tepung ubi jalar merah pada beberapa
I. PENDAHULUAN
A. LATAR BELAKANG
Ubi jalar merupakan salah satu tanaman palawija yang banyak terdapat di Indonesia. Plasma nutfah ubi jalar yang dimiliki Indonesia adalah sekitar 5000 klon lokal. Hampir seluruh produksi ubi jalar nasional digunakan sebagai bahan makanan. Ubi jalar memiliki kandungan nutrisi yang baik, umur yang relatif pendek, produksi yang tinggi, dan potensi lainnya (Widodo, 1989). Ubi jalar juga dianggap murah, lebih manis, dan banyak mengandung komponen kalori, vitamin A dibandingkan dengan tepung terigu (Villareal dan Griggs, 1982). Selain itu, ubi jalar juga merupakan salah satu komoditas lokal sumber serat pangan. Hal tersebut di atas terlihat bahwa ubi jalar mempunyai potensi untuk dikembangkan dengan berbasiskan kepada produk tepung.
Tepung ubi jalar dapat diolah kembali menjadi produk olahan lainnya seperti roti, cookies dan mie, tetapi harus diperhatikan juga kualitas dari tepung itu sendiri. Sifat yang dimiliki tepung adalah gelatinisasi dan reologi adonan, diantaranya sifat pada saat pembentukan adonan dan kekuatan adonan. Menurut Wirakartakusumah et.al. (1992), sifat reologi makanan memusatkan perhatiaannya pada aliran (flow) dan perubahan bentuk (deformasi) pada adonan makanan. Adonan makanan adalah suatu bentuk produk dengan kandungan air rendah dari campuran air dan tepung. Sifat reologi adonan sangat penting dalam menentukan kualitas panggang suatu tepung (De man, 1989).
Salah satu strategi optimal adalah memposisikan pengembangan ubi jalar secara selaras dengan pengembangan ekonomi daerah. Hal ini menjadi lebih penting dalam era otonomi daerah. Dengan kata lain pengembanagn dilaksanakan secara terkait dari hulu hingga hilir dengan memberi penekanan pada aneka produk bernilai tambah yang dapat diserap oleh pasar. Salah satu pola yang sesuai dalam skema pengembangan ini adalah pola klaster.
yang kemudian dilakukan pengujian sifat reologi dan fungsional tepung ubi jalar serta beberapa langkah awal untuk penggandaan skala.
B. TUJUAN, SASARAN DAN MANFAAT PENELITIAN
Berangkat dari latar belakang tersebut di atas, maka tujuan penelitian ini adalah :
a.Mengetahui pemetaan penelitian tepung ubi jalar hingga saat ini
b.Memverifikasi proses pembuatan tepung ubi jalar dan merumuskan langkah awal untuk penggandaan skala produksi tepung ubi jalar yang memenuhi syarat dengan lokasi di Cibungbulang, Bogor- Barat
c.Mengetahui mutu tepung ubi jalar melalui sifat fisik dan kimianya melalui sifat reologi dan kandungannya
Sasaran dari penelitian ini adalah menghasilkan tepung ubi jalar dengan sifat reologi yang terukur dan menghasilkan chips ubi jalar dengan kadar air maksimal 6% serta TPC (Total Plate Count) maksimal 103 CFU/gr dengan menggunakan air dari Cibungbulang.
II. TINJAUAN PUSTAKA
A. UBI JALAR
1. Botani Ubi Jalar
Ubi jalar atau ketela rambat berasal dari benua Amerika. Para ahli botani dan pertanian memperkirakan daerah asal tanaman ubi jalar adalah Selandia Baru, Polinesia dan Amerika bagian Tengah (Rukmana, 1997). Tanaman ubi jalar dapat beradaptasi luas terhadap lingkungan tumbuh karena daerah penyebaran terletak pada 30 OC LU dan 30 OC LS. Daerah yang paling ideal untuk mengembangkan ubi jalar adalah daerah bersuhu antara 21 OC - 27 OC, yang mendapat sinar matahari 11-12 jam/hari, kelembaban udara (RH) 50-60%, dengan curah hujan 750-1500 mm/tahun. Pertumbuhan dan produksi yang optimal untuk usaha tani ubi jalar tercapai pada musim kering (kemarau) (Rukmana, 1997).
Menurut Rukmana (1997), klasifikasi lengkap taksonomi tumbuhan adalah kingdom Plantae (tumbuh-tumbuhan), divisi Spermatophyta (tumbuhan berbiji), subdivisi Angiospermae (berbiji tertutup), kelas Dicotyledonae (biji berkeping dua), ordo Convolvulales, famili Convolvulaceae, genus Ipomoea dan spesies Ipomoea batatas L. Pada umumnya ubi jalar dibagi dalam dua golongan yaitu ubi jalar yang berumbi lunak karena banyak mengandung air dan umbi jalar yang berumbi keras karena banyak mengandung pati ( Lingga et al., 1986). Warna kulit umbi ada yang berwarna putih, putih merah tua, jingga dan dagingnya ada yang berwarna putih kekuningan (Steinbauer dan Kushman, 1971).
lebih rapat sehingga jumlah populasi persatuan luas akan lebih banyak (Ega, 2002). Produksi ubi jalar varietas sukuh adalah sebesar 21.30 ton/Ha Sedangkan ubi jalar merah (Klon BB 00105.10) yang dikembangkan oleh International Potato Center (CIP) merupakan hasil persilangan tanaman ubi jalar berproduktivitas tinggi dan tanaman ubi jalar yang berproduktivitas rendah.
Ubi jalar merupakan tanaman palawija penting di Indonesia setelah jagung dan ubi kayu. Komoditas ubi jalar sangat layak untuk dipertimbangkan dalam menunjang program diversifikasi pangan berdasarkan kandungan nutrisi, umur yang relatif pendek, produksi tinggi dan potensi lainnya. Sehingga apabila ditangani secara sungguh-sungguh, ubi jalar akan dapat menjadi sumber devisa yang potensial ( Widodo, 1989).
Ubi jalar memiliki keistimewaan dibanding tanaman pangan lainnya. Ubi jalar termasuk salah satu tanaman yang paling tinggi daya penyesuaiannya terhadap kondisi lingkungan yang buruk, seperti angin kencang, musim kering yang panjang serta telah terbukti besar perannya dalam musim paceklik dan bencana alam sebagai makanan alternatif. Dengan daya adaptasi yang luas, tanaman ini dapat ditanam sepanjang tahun asalkan kebutuhan air pada awal pertumbuhannya cukup.
2. Produksi Ubi Jalar
Negara-negara berkembang di dunia merupakan produsen utama dari tanaman ubi jalar. Dengan produksi sekitar 90 juta ton per tahunnya. Secara kasar, 80% total tanaman ubi jalar di dunia dibudidayakan di Asia dan kurang dari 15% dibudidayakan di Afrika. Hanya sekitar 5% dari populasi tersebut dibudidayakan di Afrika. Cina merupakan produsen ubi jalar yang paling besar. Sementara Indonesia menempati peringkat kedua setelah Cina dengan jumlah produksi 2.5 juta ton per tahun.
dan tingkat konsumsi ubi jalar. Di Jepang, peningkatan pendapatan rumah tangga akan menyebabkan penurunan konsumsi ubi jalar yang dianggap sebagai bahan pangan inferior (Mackay et al., 1989).
Menurut catatan Badan Pusat Statistik (2005), produksi ubi jalar dari tahun ke tahun tidak mengalami kenaikan yang signifikan dan jumlah produksinya jauh di bawah tanaman umbi-umbian lain seperti ubi kayu. Ubi jalar mempunyai prospek yang baik bila dikelola dengan pola agribisnis dan agroindustri yang baik. Data perkembangan produksi ubi jalar dapat dilihat pada Tabel 1.
Tabel 1. Data perkembangan produksi ubi kayu dan ubi Jalar di Indonesia dari tahun 2001 hingga tahun 2004
Tahun Ubi kayu (ton) Ubi jalar (ton)
2001 17,054,648 1.749.070
2002 16,913,104 1.771.642
2003 18,523,810 1.991.478 2004 19,263,978 1.889.222 Sumber : Badan Pusat Statistik (2005)
maupun keuangan dan (3) kurangnya akses untuk mencapai masyarakat, ubi jalar umumnya hanya ditemui di pasar-pasar tradisional saja sehingga distribusinya tidak menyebar luas.
Dengan melihat kenyataan tersebut di atas, ini merupakan suatu tantangan bagi pemerintah dan kita untuk dapat mengembangkan dan memasyarakatkan ubi jalar sebagai bahan pangan yang bernilai gizi serta terjangkau oleh semua masyarakat. Salah satu usaha untuk meningkatkan konsumsi ubi jalar adalah melakukan penganekaragaman produk pangan berbasis ubi jalar.
[image:30.612.163.509.318.568.2]Selain hambatan yang disebutkan diatas, ubi jalar juga mempunyai spesifikasi seperti tercantum pada Tabel 2.
Tabel 2. Spesifikasi Jenis Ubi Jalar Merah, Putih dan Ungu
Ubi jalar putih Ubi jalar merah Ubi jalar Ungu - Banyak terdapat di
pasar
- Mengandung pati yang tinggi, berkisar 5.30 sampai 28.40[1] - Rasanya lebih manis,
banyak mengandung sukrosa [2]
- Mempunyai rendemen yang tinggi 25-40% 3 - Biasanya umbi
berukuran besar[3] - Mengandung serat yang
tinggi sanpai 1.95%[3] - Sumber vitamin C yang
baik[4]
- Merupakan varietas yang bertekstur lunak[1]
- Tanamannya tahan terhadap kekeringan dan memproduksi umbi dalam jumlah yang banyak[1] - Memiliki kandungan
vitamin–vitamin seperti prekursor vitamin A[2]
- Mengandung antosianin yang berperan sebagai antioksidan [5] - Mengandung anti
hipertensi[6] - Mengandung anti
hiperglisemik[6]
Sumber :
[1]
Zuraida, 2005. [2]
. Rajiv, 2005. [3]
O'Hair, S. K. 1990. [4]
. Anonim , 2006a. [5]
Anonim , 2001a. [6]
Suda, 2003.
3. Komposisi Kimia Ubi Jalar
energi yang baik dalam bentuk karbohidrat. Ubi jalar merupakan sumber energi sebesar 215 kal/ha/hari, sedangkan padi dan jagung hanya 176 kal/ha/hari (Rukmana, 1997). Komposisi kimia ubi jalar seperti tercantum pada Tabel 3.
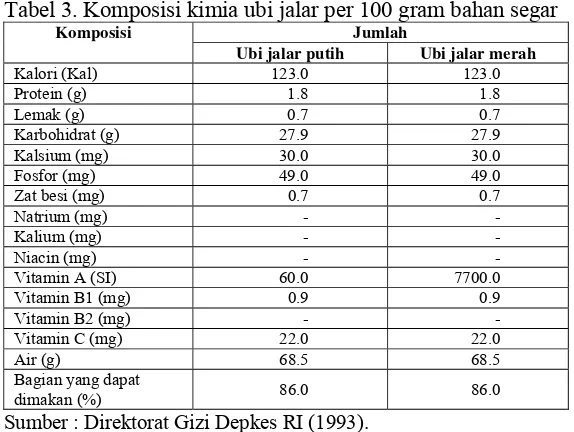
Tabel 3. Komposisi kimia ubi jalar per 100 gram bahan segar Komposisi Jumlah
Ubi jalar putih Ubi jalar merah
Kalori (Kal) 123.0 123.0
Protein (g) 1.8 1.8
Lemak (g) 0.7 0.7
Karbohidrat (g) 27.9 27.9
Kalsium (mg) 30.0 30.0
Fosfor (mg) 49.0 49.0
Zat besi (mg) 0.7 0.7
Natrium (mg) - -
Kalium (mg) - -
Niacin (mg) - -
Vitamin A (SI) 60.0 7700.0
Vitamin B1 (mg) 0.9 0.9
Vitamin B2 (mg) - -
Vitamin C (mg) 22.0 22.0
Air (g) 68.5 68.5
Bagian yang dapat
dimakan (%) 86.0 86.0
Sumber : Direktorat Gizi Depkes RI (1993).
Menurut Kementerian Negara Urusan Pangan yang bekerjasama dengan Pusat Pengembangan Teknologi Pangan Lembaga Pengabdian kepada Masyarakat (1999), vitamin terbanyak dalam ubi jalar adalah beta karoten (provitamin A) dan asam askorbat (vitamin C). Beta karoten merupakan gabungan antara dua molekul retinol sehingga memiliki aktivitas provitamin A maksimum. Kandungan β karoten ubi jalar mencapai 7100 IU, namun tidak semua jenis ubi jalar mengandung β-karoten yang tinggi. Ubi jalar yang mengandung β-karoten tinggi hanya varietas ubi jalar yang warna daging ubinya jingga kemerah-merahan. Sedangkan varietas ubi jalar yang daging ubinya berwarna kuning atau putih memiliki kandungan β-karoten yang lebih rendah (Juanda et al., 2000). Sukirwan (2000) juga melaporkan bahwa vitamin A dapat menghaluskan kulit dan sebagai antioksidan yang dapat mencegah penuaan dini.
kalorinya, yaitu sekitar dua kali lipat dari jumlah yang dibutuhkan manusia. Potasium merupakan mineral utama yang terkandung pada komoditas ini dan kandungan zat besi (0.8 mg/100 g) dapat memenuhi kebutuhan zat besi bila ubi jalar dikonsumsi setidaknya 2 kg per hari (Villareal dan Griggs, 1982).
Serat makanan didefinisikan sebagai kelompok polisakarida dan polimer-polimer lain yang tidak dapat dicerna oleh sistem gastrointestinal bagian atas tubuh manusia. Istilah serat makanan juga harus dibedakan dari istilah serat kasar yang biasa digunakan dalam analisis proksimat makanan. Serat kasar (crude fiber) adalah bagian dari makanan yang tidak dapat dihidrolisa oleh bahan-bahan kimia yang digunakan untuk menentukan kadar serat kasar, yaitu asam sulfat dan natrium hidroksida, sedangkan serat makanan adalah bagian dari makanan yang tidak dapat dihidrolisis enzim-enzim pencernaan. Oleh karena itu kadar serat kasar nilainya lebih rendah dibandingkan dengan serat makanan, karena asam sulfat dan natrium hidroksida mempunyai kemampuan yang lebih besar untuk menghidrolisis komponen-komponen makanan dibandingkan dengan enzim-enzim pencernaan (Muchtadi, 1989).
Penelitian mutakhir diketahui bahwa serat makanan total (total dietary fiber, TDF) terdiri dari komponen serat makanan larut (soluble dietary fiber, SDF) dan serat makanan tidak larut (insoluble dietary fiber, IDF) (Muchtadi, 2001). Kelompok makanan yang termasuk ke dalam kelompok SDF adalah gum, pektin dan sebagian hemiselulosa larut air. Sementara komponen serat makanan yang termasuk ke dalam komponen IDF adalah selulosa, lignin, dan pektat. Biasanya jumlah IDF selalu lebih banyak dari SDF dan jumlah SDF biasanya adalah satu per tiga TDF (Muchtadi,2001).
sel tanaman. Komponen ini termasuk senyawa struktural seperti selulosa, hemiselulosa, pektin, dan lignin (Southgate, 1982).
[image:33.612.165.507.333.420.2]Mengkonsumsi serat makanan dalam jumlah tinggi akan memberi pertahanan pada manusia terhadap timbulnya berbagai penyakit, misalnya kanker usus besar (colon), penyakit divertikulasi, penyakit kardiovaskuler dan obesitas (kegemukan) (Muchtadi, 1989). Pola konsumsi yang kurang serat dipengaruhi oleh adanya perubahan pola makan dari pola tradisional yang mengandung pati dan serat menjadi pola modern dengan kandungan protein, lemak, gula dan garam yang tinggi tetapi kurang serat. Kecukupan asupan (adequate intake/AI) untuk orang dewasa adalah 25-30 gram serat makanan per orang per hari (Zakaria, 2003). Komponen serat makanan yang telah diolah disajikan pada Tabel 4.
Tabel 4. Komponen serat makanan ubi jalar mentah asal Tonga
Komponen % berat kering % berat basah
SNSP 4.4 1.4
Pektin 2.5 0.8
Hemiselulosa 3.8 1.2
Selulosa 1.9 0.6
Lignin 1.4 0.4
Keterangan : SNSP (Soluble non-starch polysaccharides)
Sumber : Holloway et al. (1985)
Kandungan karbohidrat yang banyak terdapat pada ubi jalar adalah pati, gula dan serat makanan. Komposisi umum karbohidrat ubi jalar yang telah diolah dengan pemanasan (pemasakan) dapat dilihat pada Tabel 5.
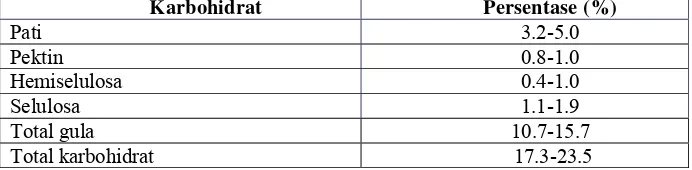
Tabel 5. Komposisi umum karbohidrat ubi jalar yang telah diolah dengan pemanasan (pemasakan)
Karbohidrat Persentase (%)
Pati 3.2-5.0 Pektin 0.8-1.0 Hemiselulosa 0.4-1.0 Selulosa 1.1-1.9 Total gula 10.7-15.7
Total karbohidrat 17.3-23.5
[image:33.612.161.507.558.643.2]Pati yang tersusun atas amilosa dan amilopektin merupakan komponen karbohidrat utama pada ubi jalar. Rasio amilosa dan amilopektin pada ubi jalar cukup bervariasi, tetapi secara umum adalah 1: 3 atau 1: 4. Kandungan amilopektin yang tinggi dan amilosa yang rendah diduga bertanggung jawab terhadap karakteristik ubi jalar. Pati ubi jalar tergelatinisasi pada suhu antara 65 0C hingga 80 0C (Woolfe, 1999).
Karakteristik ubijalar yang berhubungan dengan kandungan karbohidrat adalah kecenderungan timbulnya flatulensi setelah mengkonsumsi ubi jalar. Flatulensi disebabkan oleh gas flatus yang merupakan hasil samping fermentasi karbohidrat yang tidak dicerna dalam tubuh, yang dilakukan oleh mikroflora usus. Menurut Darmadjati (2003), karbohidrat yang tidak dicerna tersebut antara lain pati tidak tercerna (resistant starch), oligosakarida tak tercerna (non digestibility oligosaccharides) dan polisakarida non pati ((non starch polisaccharides) seperti komponen-komponen serat makanan.
Karbohidrat tak tercerna menyediakan substrat bagi pertumbuhan dan metabolisme mikriflora usus. Substrat tersebut mempercepat pertumbuhan bakteri sehingga menghasilkan metabolit yang berfungsi sebagai penjaga kesehatan usus halus dan kolon, terutama melalui mekanisme antagonisme dengan bakteri patogen, metabolit asam lemak rantai pendek dan peningkatan respon imun usus halus (Zakaria, 2003). Selain asam lemak, proses fermentasi karbohidrat tak tercerna juga menghasilkan gas H, CH4 dan CO2 yang bersama-sama membentuk gas flatus. Metabolit terakhir ini
yang menyebabkan terjadinya flatulensi. Makanan yang tidak dapat dicerna tetapi menguntungkan bakteri kolon dengan cara meningkatkan peryumbuhan dan keaktifan satu atau lebih jenis bakteri tersebut dikenal sebagai prebiotik (Johnson dan Southgate, 1994).
4. Pengolahan Ubi Jalar
makanan ringan ataupun pencuci mulut dan umumnya dikonsumsi dalam bentuk segarnya yang telah direbus, dipanggang ataupun dimasak dengan bahan-bahan lainnya. Komoditas ini juga dapat diolah menjadi keripik dengan bentuk potongan ataupun seperti bentuk kentang goreng (Mackay et al., 1989).
Pengeringan oleh sinar matahari pada ubi jalar yang telah diblansir merupakan proses pengolahan tradisional yang dilakukan negara-negara berkembang untuk menghasilkan chips ubi jalar. Pengeringan adalah suatu cara untuk mengurangi kadar air suatu bahan, sehingga diperoleh hasil akhir yang kering. Pengeringan ini bertujuan untuk memperpanjang masa simpan bahan pangan. Menurut Desrosier (1963), pengeringan adalah suatu proses pindah panas dan pindah massa. Sekarang ini banyak digunakan juga alat pengering lainnya seperti cabinet drier dan vertical bed drier.
Ubi jalar segar di Indonesia terkadang direndam dalam larutan garam 8-10% selama sekitar satu jam sebelum dipotong menjadi bentuk chips dan dikeringkan. Perlakuan perendaman tersebut dilaporkan dapat mencegah pertumbuhan mikroba selama proses pengeringan (Villareal dan Griggs, 1982). Perlakuan perendaman chips dalam sulfur sebelum dikeringkan pada dasarnya bertujuan untuk mempertahankan warna, cita rasa, mencegah kerusakan oleh mikroba atau aktifitas insekta dan mempertahankan mutu selama penyimpanan produk kering.
Proses pemasakan akan menyebabkan perubahan pada tekstur dan flavor ubi jalar dan juga dapat meningkatkan daya cerna berupa zat gizi khususnya pati. Proses pemasakan juga dapat mengurangi jumlah toksin pada ubi jalar (toxic terpenoid phytoalexins) dan jumlah zat anti nutrisi berupa tripsin inhibitor. Namun, proses pemasakan yang terlalu lama akan menyebabkan hilangnya beberapa zat gizi melalui proses degradasi thermal, oksidasi dan reduksi ketersediaan biologis (Woolfe, 1993).
5. Tepung Ubi Jalar
jalar dapat dibuat dengan dua cara yaitu pertama, ubi jalar diiris tipis lalu dikeringkan kemudian ditepungkan dan kedua, ubi jalar diparut atau dibuat pasta lalu dikeringkan dan ditepungkan.
Jenis bahan yang akan dikeringkan, mutu hasil akhir yang dikeringkan dan pertimbangan ekonomi mempengaruhi pemilihan alat dan kondisi pengering yang akan digunakan misalnya untuk jenis bahan padatan atau yang berbentuk lempeng maka alat yang sesuai untuk mengeringkan bahan tersebut adalah pengering cabinet atau tray drier. Sedangkan untuk bahan yang berbentuk pasta atau puree maka alat yang sesuai untuk mengeringkan adalah pengering drum (Brennan et.al., 1974).
Pembuatan tepung ubi jalar pada penelitian ini menggunakan pengering cabinet (cabinet drier) yang terdiri dari suatu ruangan yang terisolasi dengan baik untuk mencegah kehilangan panas. Pengering cabinet umumnya digunakan untuk potongan-potongan buah atau umbi dengan kecepatan aliran udara 500-1000 ft/menit. Pengeringan akan memakan waktu 5-10 jam atau kurang tergantung dari jenis bahan dan tingkat kadar air yang diinginkan (De Leon, 1988).
Menurut De Leon (1988), bahan yang akan dikeringkan dapat diletakkan di atas nampan yang berlubang-lubang atau loyang sebagai lapisan yang tipis. Pada pengering kabinet yang besar nampan diletakkan diatas trolley untuk memudahkan penanganan. Untuk ukuran yang lebih kecil dapat diletakkan di atas penompang yang permanen. Kipas yang berada dalam pengering cabinet mengalirkan udara melalui elemen-elemen pemanas dan menyebarkannya secara merata melalui nampan-nampan yang berisi bahan yang akan dikeringkan. Alat pengering ini dilengkapi sebuah saluran untuk mengeringkan udara yang penuh dengan uap air sebelum proses resirkulasi.
B. SIFAT REOLOGI ADONAN
Dalam pembuatan suatu produk, sebelumnya terlebih dahulu perlu diketahui sifat reologi adonan, sehingga dapat menghasilkan produk dengan karakteristik yang sesuai. Dalam industri pangan, sifat-sifat reologi dan teknik pengukuran sifat-sifat reologi adonan makanan merupakan hal yang sangat penting tidak hanya dalam pengoperasian bahan tetapi juga dalam menentukan mutu pangan yang dapat diukur secara objektif, desain model proses dengan scale up. Reologi makanan menitikberatkan pada aliran (flow) dan perubahan bentuk (deformasi) pada adonan makanan. Alat-alat yang digunakan untuk mengetahui karakterisasi deformasi adonan adalah farinograf, amilograf dan ekstensograf. Alat-alat ini hanya dapat digunakan untuk menentukan sifat-sifat reologi adonan secara kualitatif dan tidak dapat digunakan untuk menentukan sifat-sifat reologi secara kuantitatif / ilmu keteknikan. Hal ini disebabkan karena sifat-sifat aliran dalam peralatan sangat kompleks, sehingga sukar untuk mengetahui sifat-sifat dasar bahan (Wirakartakusumah et al.,1992).
Tabel 6. Sifat reologi adonan tepung ubi jalar dengan menggunakan amilograf
Komoditi Suhu Awal (0C)
Viskositas Maksimum (Vp) (BU)
Viskositas Pada Saat 950C (BU)
Viskositas Pada Saat Awal Pendinginan (Vr) (BU) Viskositas Pada Akhir Pendinginan (Ve) (BU) Viskositas Balik (BU) Stabilitas (Vp-Vr) (BU) Indeks Gelatinis asi (Ve-Vr) (BU) Tepung Ubi Jalar Putih
82.5 250 150 250 700 450 0 450
Tepung Ubi Jalar Merah
50 450 450 380 715 265 50 335
C. SERAT PANGAN 1. Selulosa
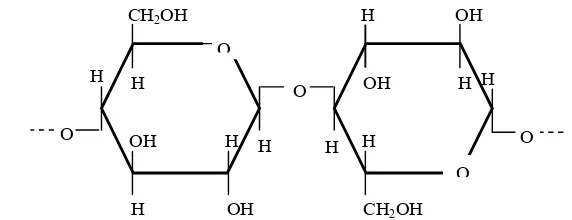
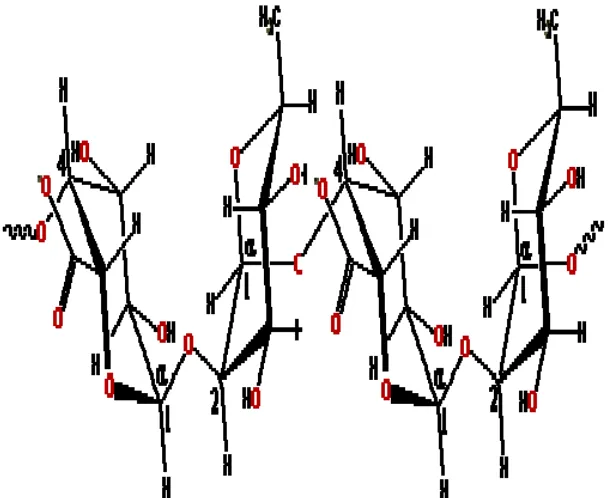
Selulosa merupakan serat-serat panjang yang bersama-sama hemiselulosa, pektin, dan protein membentuk jaringan yang memperkuat dinding sel tanaman (Winarno, 1997). Seperti juga amilosa, selulosa adalah polimer berantai lurus α-(1,4)-D-glukosa. Bedanya dengan amilosa adalah pada jenis ikatan glukosidanya. Selulosa bila dihidrolisis oleh enzim selulobiase, yang cara kerjanya serupa dengan β-amilase, akan terhidrolisis dan menghasilkan dua molekul glukosa dari ujung rantai, sehingga dihasilkan selobiosa (β-(1,4)-G-G). Struktur kimia selulosa dapat dilihat pada Gambar 1.
Gambar 1. Struktur kimia selulosa (Dreher, 1987)
Dalam dinding sel, senyawa ini terdapat dalam bentuk mikrofibril yang terdiri dari beberapa rantai molekul. Konfigurasi molekulnya yang berupa suatu kumpulan yang sangat kokoh tersebut disebabkan oleh ikatan hidrogen yang kuat diantara rantai molekul yang paralel. Ciri-ciri struktural selulosa inilah yang menyebabkan mempunyai kekuatan mekanis yang Sumber : Osundahunsi et al. (2003)
H O CH2OH H H OH OH H O
[image:38.612.182.468.470.580.2]tinggi dan bersifat tahan terhadap reaksi-reaksi kimia (Southgate dan Englyst, 1985).
2. Hemiselulosa
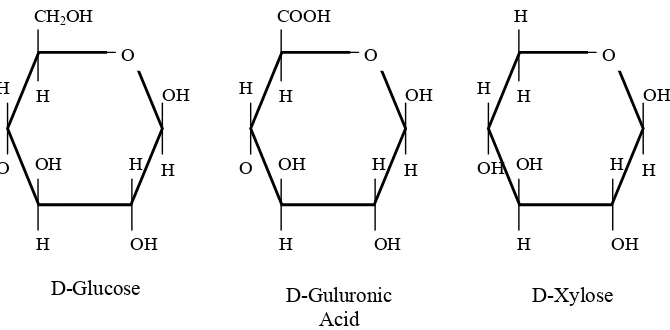
[image:39.612.156.491.340.505.2]Beda hemiselulosa dengan selulosa yaitu hemiselulosa mempunyai derajat polimerisasi rendah dan mudah larut alkali tapi sukar larut dalam asam, sedangkan selulosa sebaliknya. Hemiselulosa tidak merupakan serat-serat yang panjang seperti selulosa, juga suhu bakarnya tidak setinggi selulosa. Hasil hidrolisis selulosa akan menghasilkan D-glukosa, sedangkan hemiselulosa akan menghasilkan D-xilosa dan monosakarida lainnya (Winarno, 1997). Hasil Struktur kimia hemiselulosa dapat dilihat pada Gambar 2.
Gambar 2. Struktur kimia hemiselulosa (Dreher, 1987)
3. Pektin
Pektin secara umum terdapat di dalam dinding sel primer tanaman, khususnya di sela-sela antara selulosa dan hemiselulosa. Senyawa-senyawa pektin juga berfungsi sebagai bahan perekat antara dinding sel yang satu dengan yang lain. Bagian antara dua dinding sel yang berdekatan tersebut disebut lamela tengah (middle lamella).
Senyawa-senyawa pektin merupakan polimer dari asam D-galakturonat yang dihubungkan dengan ikatan β- (1,4)-glukosida; asam
H O CH2OH H H OH OH H
O H
OH H
O COOH H H OH OH H
O H
OH H
O H H H OH OH H
OH H
OH
galakturonat merupakan turunan dari galaktosa (Winarno, 1997). Struktur kimia pektin dapat dilihat pada Gambar 3.
[image:40.612.181.487.137.386.2]
Gambar 3. Struktur kimia pektin (Anonim ,1999a)
Selain ditemukan pada dinding sel tanaman, pektin juga ditemukan di dalam sel sebagai senyawa semen interseluler dan sering dikelompokkan sebagai gum tanaman dan pektin dapat larut dalam air panas (Schneeman, 1989).
4. Lignin
Gambar 4. Struktur kimia lignin (Sipila et al.,1999)
D. KLORINASI AIR
Air dapat merupakan medium pembawa mikroorganisme patogenik yang berbahaya bagi kesehatan. Jumlah dan jenis mikroorganisme yang terdapat di dalam air bervariasi tergantung dari berbagai faktor. Faktor-faktor tersebut adalah sebagai berikut (Frazier dan Westhoof, 1978)
1. Sumber air
Jumlah dan jenis mikroorganisme di dalam air dipengaruhi oleh sumber air tersebut, misalnya air atmosfer (air hujan, salju), air permukaan (danau, sungai), air tanah (sumur, mata air), air tergenang, air laut dan sebagainya.
2. Komponen nutrien dalam air
3. Komponen beracun
Komponen beracun yang terdapat di dalam air mempengaruhi jumlah dan jenis mikroorganisme dalam air tersebut. Sebagai contoh komponen-komponen metalik, asam-asam organik maupun anorganik, alkohol, antibiotik, khlorin dan sebagainya dapat membunuh organisme dan kehidupan lainnya di dalam air.
4. Organisme air
Adanya organisme di dalam air dapat mempengaruhi jumlah dan jenis mikroorganisme air. Sebagai contoh adanya protozoa dan bakteriophage mengurangi jumlah bakteri di dalam air karena kedua organisme tersebut dapat membunuh bakteri.
5. Faktor fisik
Jumlah dan jenis mikroorganisme juga dipengaruhi oleh faktor-faktor fisik air seperti suhu, pH, tekanan osmotik, tekanan hidrostatik, aerasi dan penetrasi sinar matahari.
Untuk mereduksi jumlah mikroorganisme di dalam air maka perlu ditambahkan desinfektan seperti penggunaan klorin. Tujuan utama penambahan klorin terhadap air adalah melakukan desinfeksi air dengan kontaminasi yang tidak terlalu berat. Efek desinfeksi didapatkan melalui in-aktivasi organisme-organisme bakteri dan virus patogenik yang dapat dipindahkan melalui air (Jenie, 1988).
Menurut Naidu dan Khanna (2000), diantara berbagai jenis sanitaiser dipakai di industri, seperti garam amonium quartenary, ozon, iodophor, gluteraldehid, dan etilen oksida, senyawa klorin mempunyai pangsa pasar yang terbesar. Hal-hal yang menyebabkan sangat populer adalah (1) tingginya efektifitas antimikrobialnya, (2) sifat toksin yang rendah terhadap manusia, (3) aplikasi yang mudah, (4) harga murah dan (5) penanganan yang mudah.
sedikit di dalam larutan. Klorin dalam jumlah yang berlebihan dapat menyebabkan iritasi terhadap paru-paru, membaran-membran hidung dan tenggorokan. Klorin telah digunakan sebagai desinfektan untuk air sejak tahun 1896. Fungsi klorin dalam penanganan air tidak hanya untuk desinfeksi, tetapi juga untuk kontrol terhadap ganggang yang hidup dalam reservoir dan kontrol terhadap pertumbuhan bakteri pembentuk lendir (Jenie, 1988).
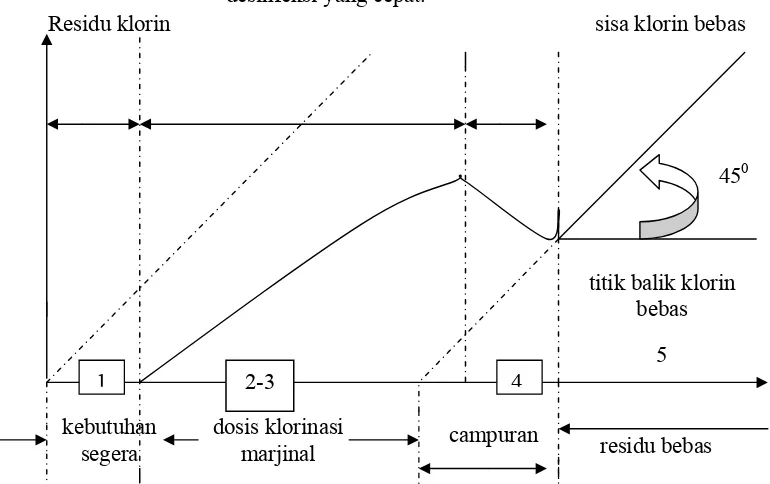
Bila senyawa klorin ditambahkan ke dalam air akan mengalami tahap-tahap sebagai berikut (sesuai dengan Gambar 5):
Reaksi (1) : terjadi destruksi senyawa - senyawa pereduksi klorin, tidak ada desinfeksi.
Reaksi (2) : bila klorin ditambahkan lagi, terbentuk senyawa - senyawa kloro-organik
Reaksi (3) :terbentuk senyawa ammonia-klorin yang mempunyai desinfeksi lambat
Reaksi (4) : terjadi penghancuran senyawa amonia-klorin
Reaksi (5) : klorin bebas terdapat dalam rasio tertentu dengan kelebihan klorin yang ditambahkan, klorin bebas ini mempunyai kerja desinfeksi yang cepat.
[image:43.612.110.495.440.682.2]
Gambar 5. Reaksi klorin dalam air (Jenie, 1988) dosis klorinasi
marjinal kebutuhan
segera campuran
titik balik klorin bebas
residu bebas 5
Residu klorin sisa klorin bebas
1 2-3 4
Davidson dan Branen (1993) menyatakan bahwa klorin dalam berbagai bentuknya merupakan sanitaiser kimia yang paling luas digunakan dalam industri makanan. Senyawa-senyawa klorin yang berfungsi sebagai sanitaiser dapat dikelompokkan menjadi klorin cair, hipoklorit, kloramin anorganik, kloramin organik dan klorin dioksida. Di dalam air, klor sebagai gas Cl2 akan bereaksi membentuk asam hipoklorit (HOCl), H+ dan klorida
(Cl-) :
Cl2 + H2O HOCl + H+ + Cl-
Pada suhu air yang normal, reaksi tersebut telah selesai secara lengkap hanya dalam beberapa detik saja. Pada pH rendah keseimbangan akan berjalan ke kanan, karena itu hanya sedikit sekali Cl2 yang berada
dalam larutan.
Sedang asam hipoklorit akan mengalami disosiasi sesuai dengan reaksi berikut :
HOCl OCl- + H+ (hipoklorit)
Ion klorida (Cl-) tidak aktif, sedangkan Cl2, HOCl dan OCl- dianggap
sebagai bahan yang aktif. HOCl yang tidak terpecah adalah zat pembasmi yang paling efisien pada kondisi pH agak rendah sampai suasana netral (Alaerts dan Santika, 1984).
Di samping reaksi klorin dengan bahan-bahan impurities, apabila air yang akan didesinfeksi mengandung amonia, maka terjadi reaksi antara asam hipoklorit dengan amonia membentuk kloramin. Reaksinya adalah sebagai berikut :
NH3 + HOCl NH2Cl + H2O pH > 7
(monokloramin)
NH2Cl + HOCl NHCl2 + H2O 4 < pH < 6
NHCl2 + HOCl NCl3 + H2O pH < 3
(trikloramin)
Semua klor yang tersedia di dalam air sebagai kloramin disebut “klor tersedia terikat” (combined available chlorine), sedang klor yang terbentuk sebagai Cl2, OCl- dan HOCl disebut (free available chlorine). Klor yang
terikat maupun bebas sama-sama memiliki daya desinfeksi, hanya pada klor yang terikat kemampuannya lebih rendah dibanding pada keadaan bebas (Alaerts dan Santika, 1984).
Hipoklorit merupakan agen anti mikrobial yang tertua dan paling banyak digunakan untuk sanitasi dan desinfeksi. Hipoklorit biasa dikenal dengan nama bleach dan banyak diaplikasikan dalam penanganan air minum dan limbah (Naidu dan Khanna, 2000). Klorin mampu menyebabkan reaksi mematikan pada membran sel dan dapat mempengaruhi DNA. NaOCl bereaksi dengan DNA sel hidup, menyebabkan mutasi oleh reaksi oksidasi basa purin dan pirimidin. Klorin daapt diperhitungkan termasuk dalam germisida berspektrum luas (Davidson dan Branen, 1993).
Konsentrasi klorin yang digunakan dalam kehidupan sehari-hari berbeda-beda tergantung dari tujuan dan pemanfaatan klorin itu sendiri. Klorin pada konsentrasi 3000-150000 ppm digunakan sebagai pemutih, sedangkan klorin pada konsentrasi 1000 ppm digunakan sebagai pembersih darah (Anonim , 19964). Menurut Jay (2000), klorin 2000 ppm mempunyai kemampuan menurunkan jumlah mikroba sebanyak 2.3 log 10 dengan waktu
kontak 1-10 menit.
Konsentrasi klorin dapat dikurangi dengan semakin meningkatnya waktu kontak yang digunakan. Konsentrasi klorin yang tinggi dapat menyebabkan korosi, sehingga waktu kontak yang digunakan pun tidak boleh melebihi 30 menit. Efek dari korosi ini dapat dikurangi dengan menurunkan waktu kontak, menurunkan temperatur atau dengan meningkatkan pH (Marriot, 1999).
III. METODOLOGI
A. BAHAN DAN ALAT
Bahan yang digunakan adalah air dari sumber di Cibungbulang (air yang tanpa diklorinasi), air dari PT. FITS, ubi jalar, K2SO4, HgO, H2SO4,
NaOH-Na2O3, indikator (metil merah dan metil biru), H3BO3, Na2S2O5,
petroleum eter, buffer fosfat, enzim α-amilase, amiloglikoksidase, etil alkohol 75% dan 95%, aseton, NaOH 4%, natrium hipoklorit, akuades, Plate Count Agar (PCA), alkohol, buffer natrium fosfat pH 6.4 HCl, NaOH 4 M, etanol teknis 95%, etanol 78%, aseton puriss, enzim termamyl, Pepsin, dan pankreatin. Alat yang digunakan untuk pembuatan adalah cabinet drier, pisau, baskom, penggiling tepung, brabender amilograph, brabender ekstensograf, brabender farinograf, buret, filter, gelas ukur, termometer, timbangan analitik, lap basah, pengaduk/sendok, gelas piala, erlenmeyer 500 ml, peralatan untuk ekstraksi lemak (sokhlet), cawan aluminium, cawan porselin, oven, desikator, labu Kjedahl, batu didih kondensor inkubator, tanur, penangas air, pH meter, alumunium foil, kertas saring whatman no 40, bunsen, pipet mikro 100-1000 µL, cawan petri, plastik tahan panas, autoklaf, stomacher, tips dan tabung reaksi bertutup .
B. METODE PENELITIAN
1. Studi Pustaka Pemanfaatan Tepung-Tepungan
Studi pustaka pemanfaatan tepung-tepungan meliputi pencarian komoditi yang digunakan untuk pembuatan tepung-tepungan, Rekayasa proses pembuatan tepung, karakter fisik maupun kimia, aplikasi, potensi dan peluang dan kepercayaan dalam masyarakat.
2. Langkah Awal penggandaan Skala a. Pembuatan Tepung Ubi Jalar
Pembuatan tepung ubi jalar meliputi pencucian ubi jalar dengan air untuk menghilangkan kotoran-kotoran. Lalu ubi jalar diiris-iris dengan ketebalan ± 1.5 mm dengan menggunakan slicer. Ubi jalar direndam dalam larutan metabisulfit untuk menghindari pencoklatan. Proses selanjutnya ubi jalar digiling dengan disc mill diayak. Proses pembuatan tepung ubi jalar dapat dilihat pada Gambar 6.
Ubi jalar
Dicuci dan dikupas
Direndam dalam larutan metabisulfit 0.3% tahap I
Dipotong-potong dengan slicer dengan ketebalan ±1.5 mm
Direndam dalam larutan metabisulfit 0.3% selama 5 menit tahap II
Dikeringkan dengan cabinet drier 60 OC
Digiling dengan disc mill
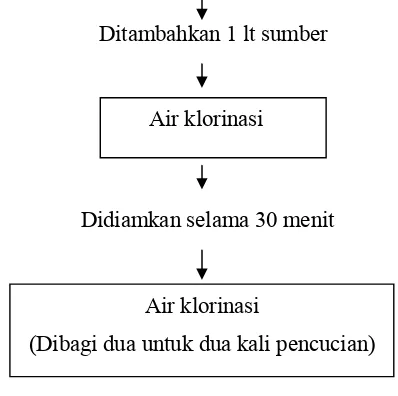
b. Pembuatan Air Klorinasi
Tepung ubi jalar
Diayak dengan saringan 60 mesh
Gambar 6. Proses Pembuatan Tepung ubi Jalar (Modifikasi Kadarisman et al.,1992)
@
Larutan stok klorin 709.52 ml Natrium hipoklorit
Air klorinasi
Air klorinasi
(Dibagi dua untuk dua kali pencucian) Diencerkan dengan 290.48 ml
Ditambahkan 1 lt sumber
[image:49.612.218.417.446.644.2]Didiamkan selama 30 menit
Gambar 7. Proses pembuatan air klorinasi
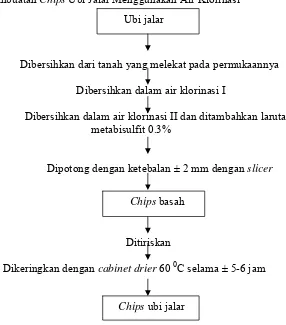
c. Pembuatan Chips Ubi Jalar Menggunakan Air Klorinasi
Dibersihkan dari tanah yang melekat pada permukaannya
Dibersihkan dalam air klorinasi I
Dibersihkan dalam air klorinasi II dan ditambahkan larutan metabisulfit 0.3%
Dipotong dengan ketebalan ± 2 mm dengan slicer
Ditiriskan
Dikeringkan dengan cabinet drier 60 0C selama ± 5-6 jam
d. Pengukuran Residu Klorin
Alat yang digunakan untuk mengukur residu klorin adalah pHydron Microchlorine Test Kit ( Lampiran 9). Alat ini berupa gulungan kertas indikator yang dapat dibaca dengan mencelupkan indikator ke dalam sampel. Konsentrasi residu klorin yang dapat terbaca berkisar dari 10, 50, 100 dan 200 ppm. Kertas dicelupkan ke dalam cairan yang terdapat pada sampel kemudian kertas dilihat dan dicocokkan dengan contoh warna yang menunjukkan konsentrasi residu klorin dalam ppm.
Ubi jalar
[image:50.612.188.474.87.412.2]Chips ubi jalar Chips basah
e. Uji Total Plate Count (TPC) (AOAC, 1992)
Sampel ditimbang sebanyak 10 gram dan dimasukkan ke dalam kantung plastik steril lalu dimasukkan larutan pengencer sebanyak 90 ml. Sampel tersebut kemudian di stomacher selama 1 menit. Dari hasil hancuran sampel tersebut dilakukan pengenceran dan pemupukan sampai tingkat yang dikehendaki. Larutan pengencer yang digunakan adalah NaCl 0.1 % (w/v).
Satu ml sampel dipipet dari pengenceran yang dikehendaki ke dalam cawan petri kemudian di tuang media Plate Count Agar (PCA) sebanyak ± 12-15 ml. Cawan petri tersebut segera digerakkan dengan gerakan melingkar atau gerakan seperti angka delapan untuk menyebarkan sel-sel mikroba secara merata. Setelah media agar membeku, cawan diinkubasi dengan posisi terbalik pada suhu 37 0C selama ± 48 jam. Jumlah koloni yang terbentuk pada cawan dihitung berdasarkan Standar Plate Count (SPC).
3. Karakteristik Tepung Ubi Jalar a. Sifat Kimia Tepung Ubi Jalar
1) Kadar air, metode oven (AOAC, 1995)
Mula-mula cawan kosong dikeringkan dengan oven selama 15 menit dan didinginkan dalam desikator, kemudian ditimbang. Sebanyak 4 – 5 gram (a) contoh dimasukkan dalam cawan yang telah ditimbang dan selanjutnya dikeringkan dalam oven bersuhu 100 – 105 0C selama 6 jam. Cawan yang telah berisi contoh tersebut dipindahkan ke desikator, didinginkan, dan ditimbang. Pengeringan dilakukan kembali sampai diperoleh berat konstan (b). Kadar air dihitung berdasarkan kehilangan berat yaitu selisih berat awal dengan berat akhir.Penetapan kadar air berdasarkan perhitungan:
100%
) ( )
(% x
a b a bb air
Kadar = −
% 100 ) ( )
(% x
b b a
bk = −
dimana : bb = berat basah bk = berat kering a = berat bahan awal b = berat bahan akhir
2) Kadar abu, metode tanur (AOAC, 1995)
Pengukuran kadar abu ditentukan dengan alat tanur. Cawan porselin dipanaskan dahulu dalam oven, kemudian didinginkan dalam desikator dan ditimbang. Sebanyak 3 – 5 gram sampel dimasukkan dalam cawan porselin lalu dibakar sampai tidak berasap lagi dan diabukan dalam tanur suhu 600 0C sampai berwarna putih (semua contoh menjadi abu) dan berat konstan. Setelah itu didinginkan dalam desikator dan ditimbang. Penetapan kadar abu berdasarkan perhitungan :
3 ) Kadar protein, metode mikro-kjedahl (AOAC, 1995)
Penentuan kadar protein dilakukan dengan metode mikro kjedahl. Ditimbang sejumlah kecil contoh (0.1 – 0.2 gram) lalu dimasukkan ke dalam labu Kjedahl. Setelah itu ditambahkan 1.9 ± 0.1 gram K2SO4, 10 ± mg HgO, dan 2.0 ± 0.1 ml H2SO4 . Ditambahkan
pula beberapa batu didih. Sampel didihkan selama 1-1.5 jam sampai cairan menjadi jernih. Dilakukan pendinginan cairan yang dihasilkan untuk kemudian ditambahkan 8-10 ml NaOH – Na2S2O3 dan
dimasukkan ke alat destilasi. Di bawah kondensor alat destilasi diletakkan erlenmeyer yang berisi 5 ml larutan H3BO3 dan beberapa
tetes indikator (campuran 2 bagian metil merah 0.2 % dalam alkohol %
100 )
(% x
sampel berat
abu berat bb
abu
Kadar =
% 100 ker
)
(% x
ing sampel berat
abu berat bk =
dan 1 bagian methylen blue 0.2 % dalam alkohol). Ujung selang kondensor harus terendam larutan tersebut untuk menampung hasil destilasi sekitar 15 ml. Hasil destilasi kemudian dititrasi oleh HCl 0.02 M sampai terbentuk warna abu-abu. Prosedur yang sama juga dilakukan terhadap blanko (yang tidak mengandung sampel). Penetapan kadar protein berdasarkan perhitungan :
Kadar Protein (%) = % N x FK
Dimana : a = ml titrasi HCl pada sampel b = ml titrasi HCl pada blanko
FK = faktor konversi (6.25 untuk tepung ubi jalar)
4) Kadar lemak, Metode Sokhlet (AOAC, 1995)
Metode yang digunakan dalam analisis lemak adalah metode ekstraksi sokhlet. Pertama kali labu lemak yang akan dikeringkan di dalam oven, kemudian didinginkan dalam desikator dan ditimbang beratnya. Sampel sebanyak 5 gram dibungkus dengan kertas saring. Setelah itu kertas saring yang berisi contoh tersebut dimasukkan ke dalam alat ekstraksi sokhlet. Alat kondensor diletakkan di atasnya dan labu lemak diletakkan di bawahnya. Pelarut heksana dimasukkan ke dalam labu lemak secukupnya. Selanjutnya dilakukan refluks selama minimal 5 jam sampai pelarut yang turun kembali ke dalam labu lemak berwarna jernih.
Pelarut yang ada di dalam labu lemak didestilasi dan pelarut ditampung kembali. Labu lemak yang berisi lemak hasil ekstraksi kemudian dipanaskan di dalam oven pada suhu 105 0C hingga mencapai berat tetap dan setelah itu didinginkan dalam desikator.
% 100 007 . 14 ) ( ) (% x sampel mg x HCl N x b a bb N
Kadar = −
% 100 ker 007 . 14 ) ( ) (% x ing sampel mg x HCl N x b a bk = −
Selanjutnya, labu beserta lemak di dalamnya ditimbang dan berat lemak dapat diketahui. Penetapan kadar lemak berdasarkan perhitungan :
5) Kadar karbohidrat by difference ( Apriyantono et.al., 1989) Kadar karbohidrat ( % bb) = 100% - (P + A + KA + L)
( % bk) = 100% - (P + A + L)
Dimana : P = kadar protein KA = kadar air A = abu
L = kadar lemak
6) Kadar serat pangan (AOAC, 1995)
Sebanyak 1 gram sampel bebas lemak dimasukkan ke dalam erlenmeyer, ditambahkan 25 ml buffer natrium fosfat pH 6.0 dan dibuat menjadi suspensi. Setelah itu ditambahkan 0.1 ml enzim termamyl, ditutup dan diinkubasikan pada suhu 100 0C selama 15 menit, sambil sesekali diaduk. Setelah selesai erlenmeyer diangkat dan didinginkan. Pada suspensi kemudian ditambah air destilata sebanyak 20 ml dan diatur pH-nya menjadi 1.5 dengan menambahkan HCl 4M. Selanjutnya ditambahkan 100 mg pepsin dan diinkubasikan pada suhu 40 0C, diagitasi selama 60 menit.
Setelah selesai, ditambah air destilata sebanyak 20 ml dan pH diatur menjadi 6.8 dengan NaOH. Ditambahkan 100 mg enzim pankreatin, ditutup dan diinkubasikan pada suhu 40 0C selama 60 menit sambil diagitasi. Selanjutnya pH diatur 4.5 dengan HCl,
% 100 ) (% x sampel berat lemak berat bb lemak Kadar = % 100 ker ) (% x ing sampel berat lemak berat bk =
Bobot lemak (kg)= %kadar lemak x ∑bobot bahan
suspensi disaring melalui crucible kering yang telah ditimbang beratnya (porositas 2) dan ditambah 0.5 g celite kering (berat tepat diketahui). Pada penyaringan dilakukan pencucian dengan 2 x 10 ml air destilata.
Untuk perhitungan serat makanan tidak larut (IDF), residu dicuci dengan 2 x 10 ml etanol 95 % dan 2 x 10 ml aseton. Selanjutnya residu dikeringkan pada suhu 105 0C sampai berat tetap. Setelah ditimbang (D1), pada residu kering dilakukan analisa kadar
abu (I1).
Untuk perhitungan serat makanan larut (SDF), volume filtrat diatur dengan air sampai 100 ml, ditambah 400 ml etanol 95 % hangat (60 0C) dan diendapkan selama 1 jam. Selanjutnya filtrat dengan endapannya disaring dengan crucible kering (porositas 2) yang mengandung 0.5 g celite kering. Setelah itu dicuci dengan 2 x 10 m