PERBEDAAN TAMPILAN IMUNOHISTOKIMIA P63 ANTARA NEOPLASIA INTRAEPITEL PROSTAT DENGAN ADENOKARSINOMA PROSTAT
TESIS
HENDRIANTO
NIM.087108002
PROGRAM PENDIDIKAN DOKTER SPESIALIS PATOLOGI ANATOMI
FAKULTAS KEDOKTERAN UNIVERSITAS SUMATERA UTARA
MEDAN
PERBEDAAN TAMPILAN IMUNOHISTOKIMIA P63 ANTARA NEOPLASIA INTRAEPITEL PROSTAT DENGAN ADENOKARSINOMA PROSTAT
TESIS
Untuk Memperoleh Gelar Spesialis Patologi Anatomi Dalam Program Pendidikan
Dokter Spesialis I Pada Fakultas Kedokteran Universitas Sumatera Utara
HENDRIANTO
NIM.087108002
PROGRAM PENDIDIKAN DOKTER SPESIALIS PATOLOGI ANATOMI
FAKULTAS KEDOKTERAN UNIVERSITAS SUMATERA UTARA
MEDAN
Judul Penelitian : Perbedaan tampilan imunohistokimia p63 antara
neoplasia intraepitel prostat dengan adenokarsinoma
prostat
Nama : Hendrianto
Nomor Induk Mahasiswa : 087108002
Program Studi : Program Pendidikan Dokter Spesialis I
Departemen Patologi Anatomi
Menyetujui
Pembimbing I Pembimbing II
Prof.Dr.H.M.Nadjib D.Lubis,Sp.PA(K) Dr. H. Joko S. Lukito,Sp PA NIP.130 318 033 NIP.19460308 197802 1 001
Ketua Program Studi Ketua Departemen
Patologi Anatomi FK-USU Patologi Anatomi FK- USU
PERNYATAAN
Judul Tesis : Perbedaan Tampilan Imunohistokimia p63 Antara Neoplasia
Intraepitel Prostat Dengan Adenokarsinoma Prostat
Dengan ini saya menyatakan bahwa dalam tesis ini tidak terdapat karya yang
pernah diajukan untuk memperoleh gelar kesarjanaan di suatu perguruan tinggi dan
sepanjang pengetahuan saya juga tidak terdapat karya atau pendapat orang lain yang
pernah ditulis atau diterbitkan oleh orang lain, kecuali yang secara tertulis diacu dalam
naskah ini dan disebutkan dalam referensi.
Yang Menyatakan,
Peneliti
Telah diuji pada
Tanggal: 3 Mei 2011
PANITIA PENGUJI TESIS
Penguji I : Dr.H.Delyuzar,Sp.PA(K)
UCAPAN TERIMA KASIH
Puji syukur ke hadirat Tuhan Yang Maha Esa atas berkat dan rahmatNya, sehingga
penulis dapat menyelesaikan penelitian dengan judul ”Perbedaan Tampilan
Imunohistokimia p63 Antara Neoplasia Intraepitel Prostat Dengan Adenokarsinoma Prostat”.
Tesis ini merupakan salah satu syarat yang harus dilaksanakan penulis dalam
rangka memenuhi persyaratan untuk meraih gelar Spesialis Patologi Anatomi dalam
program Pendidikan Dokter Spesialis I pada Fakultas Kedokteran Universitas
Sumatera Utara.
Dengan selesainya tesis ini, perkenankanlah penulis mengucapkan terima kasih
yang sebesar-besarnya kepada:
Rektor Universitas Sumatera Utara, Prof.Dr.H.Sjahrir Pasaribu,DTM&H,Sp.A(K)
dan seluruh jajarannya yang telah memberi kesempatan pada penulis untuk mengikuti
pendidikan di program Pendidikan Dokter Spesialis I pada Fakultas Kedokteran
Universitas Sumatera Utara.
Dekan Fakultas Kedokteran Universitas Sumatera Utara, Prof.Dr.Gontar
A.Siregar,Sp.PD(KGEH), atas kesempatan dan fasilitas yang diberikan kepada penulis
untuk mengikuti dan menyelesaikan pendidikan program Pendidikan Dokter Spesialis
Terima kasih yang tidak terhingga dan penghargaan setinggi-tingginya penulis
sampaikan kepada Prof.Dr.H.M.Nadjib D.Lubis,Sp.PA(K) (pembimbing I); Dr.H.Joko
S.Lukito,Sp.PA (pembimbing II) yang dengan penuh perhatian dan kesabaran telah
mengorbankan waktu untuk memberikan dorongan, bimbingan, bantuan serta
saran-saran yang bermanfaat kepada penulis mulai dari persiapan penelitian sampai pada
penyelesaian tesis ini.
Terima kasih yang sebesar-besarnya kepada Prof.Dr.H.M.Nadjib
D.Lubis,Sp.PA(K), Dr.A.Harkingto Wibisono,Sp.PA, Dr.H.Soekimin,Sp.PA,
Dr.H.Joko S.Lukito,Sp.PA, Dr.Sumondang M.Pardede,Sp.PA, Dr.Jamaluddin
Pane,Sp.PA, Dr.Neni Wahyu Hastuti,Sp.PA, Dr.Lidya Imelda Laksmi,Sp.PA dan
Dr.Jessy Chrestella,Sp.PA yang telah mengizinkan penulis untuk mengambil sampel
penelitian pada laboratorium Patologi Anatomi yang dipimpin.
Terima kasih kepada Dr.H.Delyuzar,Sp.PA(K) dan Dr.H.T.Ibnu Alferraly,Sp.PA
yang telah bersedia menguji tesis penelitian saya dan tidak lupa saya mengucapkan
terima kasih kepada seluruh staf pengajar dan analis laboratorium di Departemen
Patologi Anatomi Fakultas Kedokteran Universitas Sumatera Utara dan RS.H.Adam
Malik Medan yang telah membantu penulis dalam menyelesaikan tesis ini.
Persembahan terima kasih tulus, rasa hormat dan sembah sujud kepada ayahanda
dan ibunda tercinta (alm.Basuki L.A. dan Rismawaty), yang telah membesarkan
menjalani pendidikan dokter spesialis Patologi Anatomi. Semoga Tuhan Yang Maha
Esa mengampuni dan selalu merahmati kedua ayahanda dan ibunda ini.
Kepada ayah dan ibu mertua (Taufik dan Si A Eng), istriku tercinta Yanti, ananda
tersayang Christine Maria Friska dan Gladys Carlene, tiada kata yang setara untuk
mengutarakan terima kasih dan penghargaan setinggi-tingginya atas cinta, kasih
sayang, pengertian, pengorbanan, kesabaran dan dorongan serta doa yang diberikan
kepada penulis. Adinda Suryanto,ST dan istri, saya ucapkan terima kasih atas
dorongan moral, doa dan selalu mengingatkan penulis untuk dapat menjalani
pendidikan sampai menyelesaikan tesis ini dengan baik.
Akhirnya penulis menyadari bahwa isi hasil penelitian ini masih perlu mendapat
koreksi dan masukan untuk kesempurnaan. Oleh karena itu penulis berharap adanya
kritik serta saran untuk penyempurnaan tulisan ini. Semoga penelitian ini bermanfaat
bagi kita semua. Amin.
Medan, 2 Mei 2011
Penulis
DAFTAR ISI
Halaman
Lembar Persetujuan Penelitian….…...……….…... ii
Lembar Pernyataan ... iii
Ucapan Terima Kasih ... v
Daftar Isi...……….…….….…..…..….…. viii
Daftar Gambar.……….…... xiii
Daftar Tabel ... xvi
Daftar Singkatan………….…….….…... xvii
Abstrak ... xviii
Abstract ... xix
BAB 1. PENDAHULUAN………...….….…... 1
1.1. Latar Belakang………..…... 1
1.2. Identifikasi Masalah...….….…... 2
1.3. Hipotesis ... 3
1.4. Tujuan Penelitian………...…... 3
1.5. Manfaat penelitian...…….…..……. 3
BAB 2. STUDI PUSTAKA …...…….……….…….…....…. 5
2.1. Embriologi dan Perkembangan Prostat... 5
2.2. Anatomi dan Histologi Kelenjar Prostat Normal... 5
2.4. Hiperplasia Prostat Jinak... 10
2.5. Neoplasia Intraepitel Prostat ... 12
2.6. Adenokarsinoma Prostat ... 13
2.6.1. Etiologi... 14
2.6.2. Gejala Klinis... 16
2.6.3. Diteksi Dini... 17
2.6.4. Gambaran Makroskopis... 17
2.6.5. Histopatologi... 18
2.6.5.1. Gambaran Arsitektur... 19
2.6.5.2. Gambaran Inti... 19
2.6.5.3. Gambaran Sitoplasma... 20
2.6.5.4. Gambaran Intraluminal... 21
2.6.5 5. Varian Atrophic... 22
2.6.5.6. Varian Pseudohyperplastic... 23
2.6.5.7. Varian Foamy Gland... 23
2.6.5.8. Varian Colloid dan Signet Ring... 24
2.6.5.9. Varian Oncocytic... 25
2.6.5.10. Varian Yang Menyerupai Lymphoepithelioma... 25
2.6.5.11.Varian Sarcomatoid... 26
2.6.6. Gleason Grade... 26
2.6.7.1. Klasifikasi TNM... 31
2.6.7.2. Tingkat Diferensiasi Kanker... 33
2.6.7.3. Tingkat PSA Dalam Serum... 34
2.6.8. Imunohistokimia... 35
2.6.8.1. PSA ... 35
2.6.8.2. PAP ... 36
2.6.8.3. Keratin 34ΒE12... 36
2.6.8.4. P63 ... 37
2.6.8.5. Alpha Methylacyl CoA Racemase... 41
2.6.8.6. Receptor Androgen... 41
2.6.8.7. P53 ... 42
2.6.9. Pengobatan... 44
2.7. Kerangka Konsep ... 45
BAB 3. METODE PENELITIAN ………..………...…. 46
3.1. Rancangan Penelitian... 46
3.2. Tempat Dan Waktu Penelitian...…….….…... 46
3.2.1. Tempat Penelitian …………... 46
3.2.2. Waktu Penelitian ………... 46
3.3. Subjek Penelitian………... 46
3.3.1. Populasi …………....………..….…... 46
3.4. Kriteria Inklusi Dan Eksklusi.….………..…... 47
3.4.1. Kriteria Inklusi ………... 47
3.4.2. Kriteria Eksklusi ………... 47
3.5. Jumlah Sampel ...… ..……….……….……... 47
3.6. Cara Kerja... 48
3.6.1. Pembuatan Sediaan Mikroskopis ... 49
3.6.2. Prosedur Sebelum Pulasan Antibodi Primer... 50
3.6.3. Protokol Pulasan Imunohistokimia p63 Dengan Menggunakan Metode REAL En Vision ... 51
3.7. Alat Dan Bahan Penelitian ... 52
3.7.1. Alat-Alat Penelitian ... 52
3.7.2. Bahan Penelitian ... 52
3.8. Instrumen Penelitian ... 54
3.9. Kerangka Operasional ...55
3.10. Variabel Penelitian ...56
3.10.1. Variabel Bebas ... 56
3.10.2. Variabel Terikat ...56
3.11. Pengolahan Data... 56
3.12. Analisa Data ... 57
3.13. Definisi Operasional ... 57
BAB 4. HASIL PENELITIAN ... 60
4.1. Distribusi Data Berdasarkan Jenis Kelainan Prostat ... 60
4.2. Distribusi Data Berdasarkan Umur Penderita Pada Kelompok Neoplasia Intraepitel Prostat ... 61
4.3. Distribusi Data Berdasarkan Umur Penderita Pada Kelompok Adenokarsinoma Prostat ... 62
4.4. Distribusi Data Berdasarkan Gleason Score Pada Kelompok Adenokarsinoma Prostat ... 63
4.5. Distribusi Data Tampilan Imunohistokimia p63 Di Inti Sel Basal... 64
4.6. Distribusi Data Tampilan Abberant p63 Di Sitoplasma Sel Luminal .. 65
4.7. Distribusi Data Tampilan Abberant p63 Di Sitoplasma Sel Luminal Berdasarkan Gleason Score Pada Kelompok Adenokarsinoma Prostat..66
4.8. Tampilan p63 Pada Neoplasia Intraepitel Prostat Dan Adenokarsinoma Prostat ... 67
4.9. Korelasi Abberant p63 Dengan Gleason Score ... 69
BAB 5. PEMBAHASAN ... 72
BAB 6. KESIMPULAN DAN SARAN ... 82
6.1. Kesimpulan ... 82
6.2. Saran ... 83
Referensi ...………..………... 84
DAFTAR GAMBAR
Halaman
Gambar 2.1.Anatomi zona dari kelenjar prostat yang dideskripsi oleh
McNeal... 7
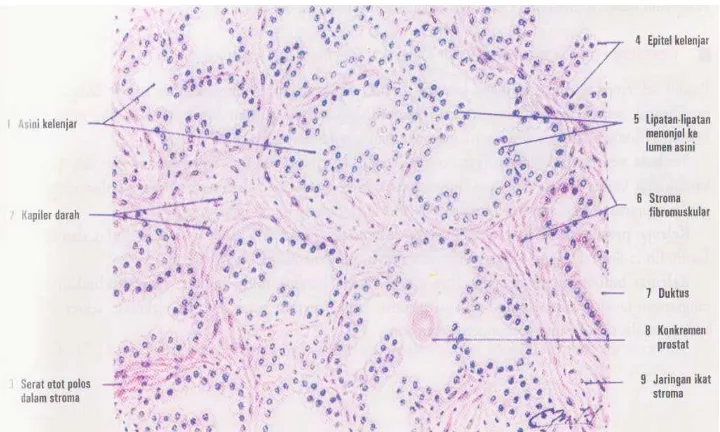
Gambar 2.2. Histologi kelenjar prostat dengan pewarnaan haematoksilin dan eosin... 8
Gambar 2.3. Jenis-jenis sel prostat ... 9
Gambar 2.4. Diferensiasi sel-sel stem prostat ... 9
Gambar 2.5. Makroskopis dan mikroskopis hiperplasia prostat jinak... 12
Gambar 2.6. Gambar perubahan atipia epitel pada PIN... 13
Gambar 2.7. A. Kelenjar prostat yang normal (kiri) dan kelenjar prostat yang mengalami PIN (kanan) ; B. Inti yang membesar dengan nukleoli yang menonjol pada PIN... 13
Gambar 2.8. Makroskopis adenokarsinoma prostat... 18
Gambar 2.9. Adenokarsinoma prostat dengan sitoplasma yang amphophilic dan inti membesar serta nukleoli yang menonjol... 20
Gambar 2.10. Kristaloid intraluminal pada adenokarsinoma prostat yang low grade ... 21
Gambar 2.11. Varian atrophic... 22
Gambar 2.13. Varian foamy gland... 24
Gambar 2.14. Varian colloid... 25
Gambar 2.15. Varian signet ring... 25
Gambar 2.16. Varian sarcomatoid (A) dengan formasi osteoid (B)... 26
Gambar 2.17. Gleason grade 1………..……….…...………... 28
Gambar 2.18. Gleason grade 2………....………...………... 29
Gambar 2.19. Gleason grade 3………...…..………... 29
Gambar 2.20. Gleason grade 4………....…... 30
Gambar 2.21. Gleason grade 5………..…..………... 30
Gambar 2.22. Gleason grade pada adenokarsinoma prostate... 31
Gambar 2.23. Imunohistokimia PSA pada epitel kelenjar prostat yang normal (A) dan adenokarsinoma prostat yang poorly differentiated (B)…... 36
Gambar 2.24. Imunohistokimia keratin 34βE12 pada epitel kelenjar prostat yang normal(A); PIN (B); adenokarsinoma prostat……… 37
Gambar 2.25. Struktur p63 ……… 39
Gambar 2.26. Tampilan p63 pada sel basal kelenjar prostat normal; B. Pewarnaan p63 negatif baik di sitoplasma maupun inti pada adenokarsinoma prostat; C dan D. Pewarnaan p63 positif di sitoplasma pada adenokarsinoma prostat……… 40
differentiated... 43
Gambar 2.28. Pewarnaan imunohistokimia p53 yang kuat (a)
dan sedang (b)... 44
Gambar 5.1. Histopatologi neoplasia intraepitel prostat dengan pewarnaan
hematoksilin eosin ……….. 73
Gambar 5.2. Histopatologi neoplasia intraepitel prostat dengan pewarnaan
imunohistokimia p63 yang memberikan tampilan negatif ..……… 74
Gambar 5.3. Histopatologi adenokarsinoma prostat dengan pewarnaan
hematoksilin eosin ….…...………... 75
Gambar 5.4. Histopatologi adenokarsinoma prostat dengan pewarnaan
imunohistokimia p63 yang memberikan tampilan positif sedang
dan kuat ….……….. 76
Gambar 5.5. Tampilan p63 positif pada preparat yang diduga suatu
adenokarsinoma prostat dengan metaplasia sel transitional
atau urothelial carcinoma ……… 77
Gambar 5.6. A. p63 tertampil di inti sel basal pada setempat yang menunjukkan
neoplasia intraepitel prostat, B. p63 tidak tertampil pada
adenokarsinoma prostat ………...……… 78
Gambar 5.7. Histopatologi adenokarsinoma prostat dengan pewarnaan p63
yang menunjukkan tampilan aberrant p63 pada berbagai Gleason
DAFTAR TABEL
Tabel 4.1. Distribusi Data Berdasarkan Jenis Kelainan Prostat ... ... 60
Tabel 4.2. Distribusi Data Berdasarkan Umur Penderita Pada Kelompok Neoplasia Intraepitel Prostat ... ... 61
Tabel 4.3. Distribusi Data Berdasarkan Umur Penderita Pada Kelompok Adenokarsinoma Prostat ... 62
Tabel 4.4. Distribusi Data Berdasarkan Gleason Score Pada Kelompok Adenokarsinoma Prostat ... 63
Tabel 4.5. Distribusi Data Tampilan Imunohistokimia p63 Di Inti Sel Basal... 64
Tabel 4.6. Distribusi Data Tampilan Abberant p63 Di Sitoplasma Sel Luminal..65
Tabel 4.7. Distribusi Data Tampilan Abberant p63 Di Sitoplasma Sel Luminal Berdasarkan Gleason Score Pada Kelompok Adenokarsinoma Prostat ... 66
Tabel 4.8. Tampilan p63 Pada Neoplasia Intraepitel Prostat Dan Adenokarsinoma Prostat ... 67
Tabel 4.9. Uji Chi-square ... 67
Tabel 4.10. Uji Diagnostik Imunohistokimia p63 ... 68
DAFTAR SINGKATAN
FKUI Fakultas Kedokteran Universitas Indonesia
RSCM Rumah Sakit Cipto Mangunkusumo
BPH Benign Prostate Hyperplasia
HPC1 Hereditary Prostate Cancer 1
PCAP Predisposing for Cancer of the Prostate
ASCO American Society of Clinical Oncology
PSA Prostate Specific Antigen
DRE Digital Rectal Examination
PIN Prostate Intraepithelial Neoplasia
LGPIN Low Grade Prostate Intraepithelial Neoplasia
HGPIN High Grade Prostate Intraepithelial Neoplasia
TNM Tumor, Node, Metastasis
PAP Prostatic Acid Phosphatase
AMACR Alpha Methylacyl CoA Racemase
H&E Haematoxyline Eosine
TRUS Transrectal Ultrasonografi
Perbedaan tampilan imunohistokimia p63 antara neoplasia intraepitel
prostat dengan adenokarsinoma prostat (Hasil Penelitian)
Hendrianto, H.M.Nadjib Dahlan Lubis, Joko S.Lukito
Departemen Patologi Anatomi Fakultas Kedokteran Universitas Sumatera Utara
Abstrak
Kadangkala adenokarsinoma prostat terutama yang well differentiated sulit dibedakan dengan neoplasia intraepitel prostat secara histopatologi dengan pewarnaan hematoksilin eosin. Untuk membedakannya diperlukan pewarnaan lain yang lebih akurat, seperti menggunakan salah satu imunohistokimia petanda sel basal seperti p63.
Tujuan penelitian ini adalah membuktikan adanya perbedaan tampilan imunohistokimia p63 antara neoplasia intraepitel prostat dengan adenokarsinoma prostat.
Penelitian ini merupakan penelitian deskripsi analitik dengan rancangan cross
sectional. Sampel penelitian sebanyak 49 blok paraffin jaringan prostat dari TURP
(transurethral resection of prostate) atau surgical prostatectomy yang telah didiagnosa dengan pewarnaan hematoksilin eosin.
Pemeriksaan imunohistokimia p63 ini memiliki sensitifitas sebesar 68%, spesifitas sebesar 75%, nilai prediktif positif sebesar 74%, nilai prediktif negatif sebesar 69% dan likelihood ratio + sebesar 2,72. Terdapat perbedaan tampilan p63 yang bermakna antara neoplasia intraepitel prostat dengan adenokarsinoma prostat (p<0.05) dimana p63 lebih tertampil pada neoplasia intraepitel prostat. Terdapat korelasi yang sangat bermakna antara tampilan aberrant p63 dengan Gleason score pada adenokarsinoma prostat (p<0.001).
Kata-kata kunci: imunohistokimia p63, aberrant p63, neoplasia intraepitel prostat,
Expression difference of p63 immunohistochemistry among prostate intraepithelial neoplasia with prostate adenocarcinoma
(Research Result)
Hendrianto, H.M.Nadjib Dahlan Lubis, Joko S.Lukito
Anatomy Pathology Department of Medical Faculty of North Sumatra University
Abstract
Sometimes prostate adenocarcinoma especially well differentiated was very difficult to differentiate with prostate intraepithelial neoplasia by histopathology examination with hematoxylin eosine staining. To differentiate it needful more other accurate stain, as utilizes one of immunohistochemistry of basal cell markers such as p63.
The purpose of this research is to prove distinctive of p63 immunohistochemistry expression among prostate intraepithelial neoplasia and prostate adenocarcinoma.
This research constitute analytic descriptive research with design cross sectional. Observational sample contain 49 paraffin blocks of prostate tissue from TURP (
transurethral resection of prostate ) or surgical prostatectomy have been diagnosed by
hematoxylin eosin's staining.
This p63 immunohistochemistry assay has sensitivity 68%, specificity 75%, positive predictive value 74%, negative predictive value 69% and likelihood ratio + 2,72. It has significant difference of p63 expression among prostate intraepithelial neoplasia with prostate adenocarcinoma (p<0.05) which p63 expression in prostate intraepithelial neoplasia is more stronger. It has very significant correlation among aberrant p63 expression with Gleason score in prostate adenocarcinoma (p<0.001).
Key words: p63 immunohistochemistry, aberrant p63, prostate intraepithelial
Perbedaan tampilan imunohistokimia p63 antara neoplasia intraepitel
prostat dengan adenokarsinoma prostat (Hasil Penelitian)
Hendrianto, H.M.Nadjib Dahlan Lubis, Joko S.Lukito
Departemen Patologi Anatomi Fakultas Kedokteran Universitas Sumatera Utara
Abstrak
Kadangkala adenokarsinoma prostat terutama yang well differentiated sulit dibedakan dengan neoplasia intraepitel prostat secara histopatologi dengan pewarnaan hematoksilin eosin. Untuk membedakannya diperlukan pewarnaan lain yang lebih akurat, seperti menggunakan salah satu imunohistokimia petanda sel basal seperti p63.
Tujuan penelitian ini adalah membuktikan adanya perbedaan tampilan imunohistokimia p63 antara neoplasia intraepitel prostat dengan adenokarsinoma prostat.
Penelitian ini merupakan penelitian deskripsi analitik dengan rancangan cross
sectional. Sampel penelitian sebanyak 49 blok paraffin jaringan prostat dari TURP
(transurethral resection of prostate) atau surgical prostatectomy yang telah didiagnosa dengan pewarnaan hematoksilin eosin.
Pemeriksaan imunohistokimia p63 ini memiliki sensitifitas sebesar 68%, spesifitas sebesar 75%, nilai prediktif positif sebesar 74%, nilai prediktif negatif sebesar 69% dan likelihood ratio + sebesar 2,72. Terdapat perbedaan tampilan p63 yang bermakna antara neoplasia intraepitel prostat dengan adenokarsinoma prostat (p<0.05) dimana p63 lebih tertampil pada neoplasia intraepitel prostat. Terdapat korelasi yang sangat bermakna antara tampilan aberrant p63 dengan Gleason score pada adenokarsinoma prostat (p<0.001).
Kata-kata kunci: imunohistokimia p63, aberrant p63, neoplasia intraepitel prostat,
Expression difference of p63 immunohistochemistry among prostate intraepithelial neoplasia with prostate adenocarcinoma
(Research Result)
Hendrianto, H.M.Nadjib Dahlan Lubis, Joko S.Lukito
Anatomy Pathology Department of Medical Faculty of North Sumatra University
Abstract
Sometimes prostate adenocarcinoma especially well differentiated was very difficult to differentiate with prostate intraepithelial neoplasia by histopathology examination with hematoxylin eosine staining. To differentiate it needful more other accurate stain, as utilizes one of immunohistochemistry of basal cell markers such as p63.
The purpose of this research is to prove distinctive of p63 immunohistochemistry expression among prostate intraepithelial neoplasia and prostate adenocarcinoma.
This research constitute analytic descriptive research with design cross sectional. Observational sample contain 49 paraffin blocks of prostate tissue from TURP (
transurethral resection of prostate ) or surgical prostatectomy have been diagnosed by
hematoxylin eosin's staining.
This p63 immunohistochemistry assay has sensitivity 68%, specificity 75%, positive predictive value 74%, negative predictive value 69% and likelihood ratio + 2,72. It has significant difference of p63 expression among prostate intraepithelial neoplasia with prostate adenocarcinoma (p<0.05) which p63 expression in prostate intraepithelial neoplasia is more stronger. It has very significant correlation among aberrant p63 expression with Gleason score in prostate adenocarcinoma (p<0.001).
Key words: p63 immunohistochemistry, aberrant p63, prostate intraepithelial
BAB 1 PENDAHULUAN
1.1. Latar belakang
Adenokarsinoma prostat masih menjadi permasalahan kesehatan di seluruh
dunia, baik dari segi insiden maupun mortalitasnya. Sembilan puluh lima
persen dari keganasan pada kelenjar prostat adalah adenokarsinoma prostat.1
Sekitar satu dari setiap lima laki-laki Amerika didiagnosa kanker prostat
pada kehidupannya dan sekitar 3% akan meninggal. American Cancer
Society memperkirakan 220.900 kasus baru dari adenokarsinoma prostat dan
28.900 kematian dari penderita ini pada tahun 2003, dengan urutan kedua
setelah kanker paru-paru.1,2
Dalam beberapa tahun terakhir ini, adenokarsinoma prostat merupakan
keganasan tersering pada pria di Amerika Serikat, sedangkan di negara Asia
insidensinya masih termasuk peringkat rendah. Di subbagian Urologi,
bagian bedah FKUI/RSCM, selama periode 1995-1998 ditemukan rata-rata
17 kasus pertahun dan menduduki peringkat kedua setelah kanker buli-buli
(kandung kemih).3
Insiden adenokarsinoma prostat yang dijumpai pada otopsi meningkat
sesuai dengan pertambahan umur dan bervariasi tergantung pada metode
pengambilan sampel dari kelenjar prostat. Khususnya pada laki-laki dengan
umur di bawah 50 tahun terdapat peningkatan jumlah adenokarsinoma
section dari kelenjar prostat. Laki-laki muda yang menjalani prostatektomi
radikal tidak memiliki prognosis yang jelek setelah operasi dibandingkan
dengan laki-laki yang lebih tua. Mereka biasanya didiagnosa dengan keluhan
genitourinaria yang tidak berhubungan dengan prostat atau karena riwayat
keluarga kanker prostat.1,2
Perubahan keganasan pada prostat tidak terjadi secara menyeluruh dan
serentak, akan tetapi secara bertahap sehingga kadangkala sulit untuk
membedakan perubahan keganasan pada prostat yang masih awal seperti
neoplasia intraepitel prostat dengan adenokarsinoma prostat. Semakin awal
dijumpai keganasan pada prostat, maka semakin baik prognosisnya. Oleh
karena itu, hal ini yang membuat peneliti berkeinginan untuk meneliti
pemeriksaan keganasan prostat dengan menggunakan imunohistokimia.
1.2. Identifikasi Masalah
Adenokarsinoma prostat merupakan tipe keganasan pada organ prostat
yang paling banyak dan kadangkala tidak terditeksi terutama pada Gleason
grade 1 atau 2, dimana sulit dibedakan dengan neoplasia intraepitel prostat
pada pewarnaan hematoksilin eosin. Di bagian Patologi Anatomi FK USU,
kadangkala pada beberapa sediaan jaringan prostat ditemukan keraguan
dalam menegakkan diagnosa apakah sediaan tersebut masih merupakan
neoplasia intraepitelial prostat atau suatu adenokarsinoma prostat terutama
yang well differentiated. Untuk itu diperlukan adanya pemeriksaan
prostat dari neoplasia intraepitel prostat, sehingga tidak terjadi
underdiagnosis.
1.3. Hipotesis
Ada perbedaan tampilan imunohistokimia p63 antara neoplasia intraepitel
prostat dengan adenokarsinoma prostat.
1.4. Tujuan Penelitian 1.4.1. Tujuan umum
Untuk membuktikan adanya perbedaan tampilan imunohistokimia p63
antara neoplasia intraepitel prostat dengan adenokarsinoma prostat.
1.4.2. Tujuan khusus
1. Untuk melakukan uji diagnostik pemeriksaan imunohistokimia p63
terhadap pemeriksaan histopatologi dengan pewarnaan hematoksilin
eosin pada neoplasia intraepitel prostat dan adenokarsinoma prostat.
2. Untuk mengetahui korelasi tampilan aberrant p63 di sitoplasma pada
adenokarsinoma prostat dengan Gleason score.
1.5. Manfaat Penelitian
1. Sebagai diagnostik penunjang yang lebih akurat dalam menegakkan
penanganan yang lebih awal dengan konsekuensi prognosis yang
lebih baik.
2. Dapat dipergunakan untuk menyingkirkan diagnosa yang ragu-ragu.
3. Dapat dikembangkan untuk penelitian lebih lanjut mengenai biologi
molekuler gen p63 dalam karsinogenesis yang berhubungan dengan
BAB 2 STUDI PUSTAKA
2.1. Embriologi dan Perkembangan Prostat
Selama kehamilan bulan ketiga, kelenjar prostat berkembang dari
invaginasi epithelial dari sinus urogenital posterior di bawah pengaruh
mesenkim. Pembentukan normal dari kelenjar prostat membutuhkan
pengaruh 5α-dihidrotestosteron yang disintesa dari testosteron fetal oleh 5α
-reduktase. Enzim ini dijumpai pada sinus urogenital dan genitalia ekternal.
Konsekuensinya, defisiensi 5α-reduktase akan menyebabkan prostat yang mengecil atau sama sekali tidak ada, walaupun epididimis, vasa deferentia
dan vesikel seminal tetap normal.
Selama masa prepubertas, terjadi perubahan prostat menuju fenotipe
dewasa. Kelenjar membesar secara kontinu mencapai berat sekitar 20 gram
pada usia 25-30 tahun.4
2.2. Anatomi dan Histologi Kelenjar Prostat Normal
Prostat normal memiliki berat sekitar 20 gram dan mengelilingi bagian
atas dari uretra (prostatic urethra). Sekresi prostat merupakan komponen
utama dalam cairan seminal yang kaya akan acid phosphatase.5
Dasar dari prostat terletak pada leher kandung kemih dan bagian apeks
pada diafragma urogenital. Fascia Denonvillier merupakan suatu jaringan
Serabut-serabut otot skeletal dari diafragma urogenital meluas ke bagian
apeks prostat sampai bagian anterior midprostat.
Zona perifer terdiri dari seluruh jaringan kelenjar prostat pada bagian
apeks dan bagian posterior dekat kapsul. Pada zona ini lebih sering dijumpai
carcinoma, prostatitis kronik dan atropi postinflammatory. Zona sentral
merupakan suatu daerah yang berbentuk kerucut dengan bagian apeks
meliputi duktus ejakulasi dan uretra prostatik pada verumontanum. Zona
transisi terdiri dari dua bagian jaringan kelenjar pada bagian lateral uretra
dari bagian tengah kelenjar. Pada zona ini sering terjadi benign prostatic
hyperplasia (BPH). Stroma fibromuskular anterior membentuk kecembungan kelenjar ini pada bagian permukaan anterior. Bagian apeks
dari area ini kaya dengan otot lurik yang bercampur dengan kelenjar dan otot
dari diafragma pelvis. Menuju bagian basal, lebih dominan otot polos
bercampur dengan serabut-serabut dari leher kandung kemih. Bagian distal
dari stroma fibromuskular anterior penting untuk fungsi voluntary sphincter,
Gambar 2.1.Anatomi zona dari kelenjar prostat yang dideskripsi oleh
McNeal.4
Gambaran histologi dari kelenjar prostat terdiri dari duktus kelenjar yang
bercabang-cabang. Kelenjar dan duktus terdiri dari dua lapisan sel yaitu
lapisan sel kolumnar sekresi luminal dan lapisan sel basal. Pada lumen dari
kelenjar dan duktus prostat sering dijumpai massa eosinofilik yang
berlapis-lapis (corpora amylacea) yang lebih umum dijumpai pada laki-laki yang
lebih tua. Kapsul prostat terdiri dari jaringan fibrous yang mengelilingi
kelenjar dan merupakan suatu lapisan yang lebih fibrous dari otot yang
Gambar 2.2. Histologi kelenjar prostat dengan pewarnaan haematoksilin dan
eosin.6
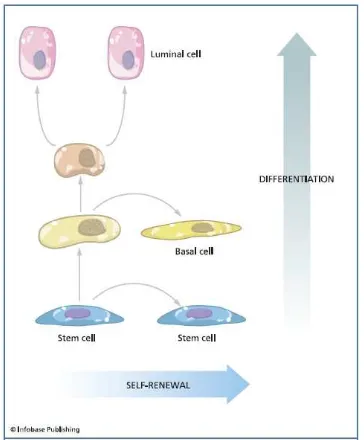
Selain sel-sel epitel luminal dan sel-sel basal, dapat juga dijumpai sel-sel
stem dan sel-sel neuroendokrin pada duktus prostat. Sel stem tersebut sama
dengan sel stem yang dijumpai pada semua jaringan di tubuh. Sel stem
berperan untuk regenerasi jaringan setelah injuri dan kematian sel. Sel stem
prostat terletak di dalam sel-sel basal dengan perbandingan 1:100 yang
berperan dalam regenerasi sel-sel epitel luminal dan sel-sel basal, mungkin
Gambar 2.3. Jenis-jenis sel pada prostat.7
Gambar 2.4. Diferensiasi sel-sel stem prostat.7
2.3. Persarafan Kelenjar Prostat
Prostat merupakan organ yang mendapat persarafan yang luar biasa. Dua
[image:31.595.233.415.397.617.2]pedikel superior dan inferior pada masing-masing sisi. Saraf-saraf ini penting
untuk pengaturan fisiologi, morfologi dan pematangan kelenjar. Prostat
mendapat inervasi saraf simpatetik dan parasimpatetik dari saraf hipogastrik
dan pelvis. Saraf ini penting untuk fungsi ereksi, sehingga mendapat
perhatian khusus pada operasi kanker prostat.4
2.4. Hiperplasia Prostat Jinak
Hiperplasia prostat jinak (hiperplasia nodular) merupakan penyakit yang
umum dijumpai pada laki-laki berumur 50 tahun ke atas. Ini ditandai dengan
hiperplasia dari sel-sel epitel dan stroma prostat yang menyebabkan
pembesaran prostat, nodul-nodul yang berbatas tegas di regio periuretra.
Karena pembesaran nodul ini sedemikian besar sehingga menyebabkan
obstruksi uretra sebagian atau total. Oleh karena itu penderita hiperplasia
prostat jinak biasanya memiliki keluhan sering miksi, nocturia, kesulitan
memulai dan mengakhiri miksi, dysuria dan retensi urin.
Telah banyak dipelajari tentang etiologi dari hiperplasia prostat jinak.
Hanya sedikit keraguan tentang hubungan hiperplasia prostat jinak dengan
aksi androgen. Sebagai contoh, kastrasi pada pria prepubertas mencegah
perkembangan hiperplasia prostat jinak. Dihidrotestosteron, metabolit dari
testosteron merupakan mediator pertumbuhan prostat. Dihidrotestosteron
disintesis di prostat dari testosteron sirkulasi oleh aksi enzim 5α-reduktase tipe 2. Enzim ini dijumpai pada sel-sel stroma, sehingga sel-sel tersebut
dihidrotestosteron dapat beraksi sebagai autokrin pada sel stroma dan
parakrin pada sel-sel epitel di sekitarnya. Pada kedua jenis sel tersebut,
dihidrotestoteron terikat pada reseptor androgen dan memberi signal ke
transcription of growth factors, yang mitogenik terhadap sel stroma dan
epitel.
Secara mikroskopik, karakteristik hiperplasia prostat jinak adalah
nodul-nodul yang disebabkan proliferasi kelenjar atau dilatasi dan proliferasi
stroma fibromuskular. Proporsi elemen-elemen ini bervariasi antara satu
nodul dengan nodul yang lain, mulai dari nodul proliferasi murni stroma
fibromuskular sampai dengan nodul fibroepitelial yang dominan kelenjar.
Proliferasi kelenjar membentuk kumpulan kelenjar-kelenjar kecil sampai
dengan kelenjar-kelenjar besar dan berdilatasi, dilapisi oleh dua lapisan sel
(bagian dalam oleh sel epitel kolumnar dan bagian luar oleh sel epitel kuboid
atau pipih) dengan membran basal yang utuh. Biasanya epitel tersebut
karakteristik membentuk tonjolan atau gambaran papillary ke arah lumen
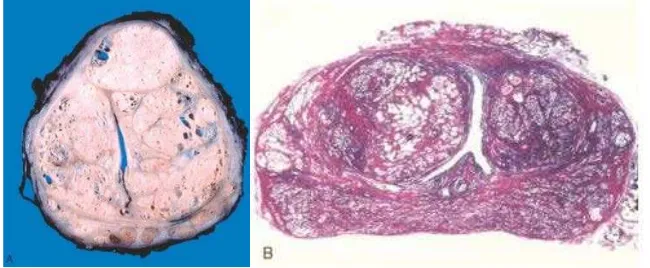
Gambar 2.5. A. Makroskopis hiperplasia prostat jinak; B. Mikroskopis
hiperplasia prostat jinak.8
2.5. Neoplasia Intraepitel Prostat
Neoplasia intraepitel prostat (PIN) merupakan proliferasi epitel yang
atipikal pada duktus dan asinar kelenjar prostat. PIN dibagi atas low grade
(LGPIN) dan high grade (HGPIN) berdasarkan derajat atipia selnya. Tidak
terbukti adanya hubungan antara LGPIN dengan adenokarsinoma prostat,
tetapi HGPIN memiliki hubungan erat dengan adenokarsinoma prostat dan
merupakan lesi prekursornya. Suatu kelenjar PIN memiliki arsitektur yang
jinak, tetapi dibatasi oleh sel-sel yang secara sitologi atipik.9 Lesi ini terdiri
dari kelenjar-kelenjar dengan proliferasi sel-sel yang menunjukkan anaplasia
inti. High grade PIN terdiri dari kelenjar-kelenjar yang terpisah lebih jauh,
kelenjar bercabang dengan struktur papillary. Ini berbeda jauh dengan
kanker yang invasif dimana karakteristiknya adalah kelenjar-kelenjar kecil,
tersusun rapat, tepi lumen yang datar (tidak bercabang). Pada PIN,
utuh.8,10 Secara histopatologi high grade PIN dapat berbentuk tufted,
papillary, cribriformis dan flat.10
Pada sekitar 80% kasus, jaringan prostat yang diambil karena karsinoma
mungkin menunjukkan lesi prekursor yang disebut dengan neoplasia
[image:35.595.173.476.278.378.2]intraepitel prostat (PIN) yang high grade.8,10
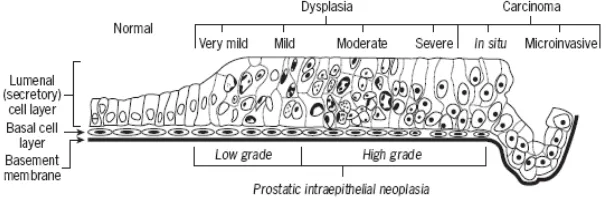
Gambar 2.6. Gambar perubahan atipia epitel pada PIN.10
Gambar 2.7. A. Kelenjar prostat yang normal (kiri) dan kelenjar prostat yang
mengalami PIN (kanan) ; B. Inti yang membesar dengan nukleoli yang
menonjol pada PIN.10
2.6. Adenokarsinoma Prostat
Adenokarsinoma prostat merupakan keganasan yang paling umum
dijumpai pada laki-laki yang berumur di atas 50 tahun dan penyebab kedua
[image:35.595.165.482.449.550.2]kematian karena keganasan. Perlu diketahui bahwa sering kali
adenokarsinoma prostat ini ditemukan secara insidentil, misalnya pada
pemeriksaan postmortem atau pada jaringan prostat hasil operasi dengan
indikasi hiperplasia prostat jinak.8
2.6.1. Etiologi
Perubahan gen pada kromosom 1, 17 dan kromosom X dijumpai pada
pasien-pasien dengan riwayat keluarga kanker prostat. Gen hereditary
prostate cancer 1 (HPC1) dan gen predisposing for cancer of the prostate
(PCAP) terdapat pada kromosom 1 sedang gen human prostate cancer pada
kromosom X. Sebagai tambahan, studi genetik menduga adanya suatu
predisposisi keluarga yang kuat pada 5-10% kasus kanker prostat. Laki-laki
dengan riwayat keluarga kanker prostat memiliki resiko yang lebih tinggi
untuk mendapat kanker prostat.11
Laki-laki Afrika Amerika memiliki prevalensi kanker prostat yang lebih
tinggi dan lebih agresif dibanding dengan laki-laki berkulit putih. Laki-laki
berkulit putih memiliki prevalensi kanker prostat yang lebih tinggi dibanding
dengan laki-laki Asia.2,5,11 Studi menemukan bahwa kadar hormon
testosteron pada laki-laki Afrika Amerika lebih tinggi 15% dibanding dengan
laki-laki berkulit putih. Selanjutnya terbukti juga 5α-reduktase mungkin lebih aktif pada suku Afrika Amerika dibanding dengan yang berkulit putih,
Diet tinggi lemak meningkatkan resiko terkena kanker prostat, sedangkan
diet tinggi kacang kedelai mungkin protektif. Observasi ini telah diutarakan
sebagai alasan rendahnya prevalensi kanker prostat di Asia. Studi kultur sel
menunjukkan asam lemak omega 6 positif dalam menstimulasi pertumbuhan
sel-sel kanker prostat, sedangkan omega 3 negatif. Lemak ini memiliki efek
pada perubahan hormon seks atau faktor pertumbuhan atau berefek pada 5α -reduktase. Kacang kedelai menurunkan pertumbuhan sel-sel kanker prostat
pada tikus percobaan, akan tetapi faktor epidemiologi menunjukkan tidak
terbukti efek yang bermakna pada manusia. Vitamin E memiliki efek
protektif karena merupakan antioksidan. Penurunan kadar vitamin A
mungkin suatu faktor resiko karena dapat memicu differensiasi sel dan sistim
imun. Defisiensi vitamin D diduga juga suatu faktor resiko dan studi
menunjukkan hubungan terbalik antara paparan ultraviolet dengan angka
kematian kanker prostat. Selenium mungkin memiliki efek protektif
berdasarkan studi epidemiologi dan dipercaya melalui efeknya sebagai
antioksidan.
Ablasi androgen menyebabkan regresi kanker prostat. Hsing dan
Comstock melakukan studi besar dengan membandingkan prevalensi kanker
prostat pada satu grup kontrol dengan satu grup yang diberikan inhibitor 5α
-reduktase. Inhibitor 5α-reduktase tersebut menunjukkan penurunan
prevalensi tumor. ASCO ( The American Society of Clinical Oncology )
merekomendasikan penggunaan inhibitor 5α-reduktase sebagai
2.6.2. Gejala Klinis
Penderita adenokarsinoma prostat selalu menunjukkan gejala lokal seperti
retensi urin (20-25%), nyeri pinggang dan tungkai (20-40%), hematuria
(10-15%), sering miksi (38%), penurunan aliran urin (23%). Akan tetapi 47%
pasien tidak menunjukkan gejala klinis, sehingga pasien mungkin didiagnosa
dengan adenokarsinoma prostat stadium lanjut tanpa adanya gejala.2,4,5,11
Selain gejala lokal, dapat dijumpai gejala-gejala metastasis, seperti
penurunan berat badan, kehilangan nafsu makan, nyeri pada tulang dengan
atau tanpa fraktur patologis, nyeri dan bengkak pada tungkai bawah, gejala
uremik dapat muncul akibat obstruksi uretra dan retroperitoneal
adenopathy.11
Oleh karena adenokarsinoma prostat muncul pada zona perifer, maka
keganasan ini sering bertahan dengan baik sebelum pasien mengeluh
kesulitan miksi akibat obstruksi uretra dan beberapa di antaranya tetap
tersembunyi bahkan sampai sudah metastasis jauh. Adenokarsinoma prostat
dapat dibagi atas tiga kategori berdasarkan sifatnya: 1. invasive prostatic
carcinoma (secara klinis telah dijumpai invasi lokal dan metastasis); 2. latent prostatic carcinoma (secara insidentil dijumpai pada kelenjar prostat dewasa
yang menetap untuk jangka waktu yang lama); 3. occult carcinoma (secara
2.6.3. Diteksi Dini
American Cancer Society menganjurkan agar semua pria berusia diatas 50
tahun mengikuti Program Deteksi Dini Kanker Prostat dengan melakukan
pemeriksaan prostate specific antigen total (PSA) dan perabaan prostat
melalui dubur yang disebut digital rectal examination (DRE). Pemeriksaan
DRE harus dilakukan oleh dokter, sedangkan pemeriksaan PSA dapat
dilakukan di laboratorium klinik. Bila ada riwayat kanker dalam keluarga,
program deteksi dini kanker prostat ini dianjurkan sejak usia 40 tahun.3
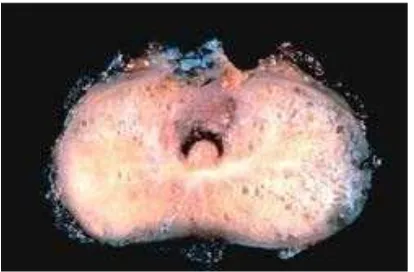
2.6.4. Gambaran Makroskopis
Identifikasi makroskopis adenokarsinoma prostat sampai saat ini sering
masih sulit atau tidak memungkinkan. Walaupun warna sebagian besar tumor
yang terlihat adalah putih kecoklatan, sebagian kecil berwarna kuning. Pada
prostatektomi, adenokarsinoma prostat cenderung multifokal, terutama
dijumpai pada zona perifer, diikuti pada zona transisional dan kemudian zona
sentral. Sebagian besar tumor teraba kenyal dan sebagian kecil teraba gembur
dan lunak. Sebagian besar tumor yang teraba dengan pemeriksaan colok
Gambar 2.8. Makroskopis adenokarsinoma prostat.8
2.6.5. Histopatologi
Adenokarsinoma prostat memiliki gambaran histopatologi mulai dari well
differentiated sampai dengan poorly differentiated. Gambaran umum semua
kanker prostat adalah hanya dijumpainya satu tipe sel tanpa adanya lapisan
sel basal. Berbeda dengan kelenjar prostat yang jinak dijumpai suatu lapisan
sel basal di bawah sel-sel sekresi. Pengenalan sel-sel basal dengan pewarnaan
hematoksilin dan eosin tidak mudah. Pada beberapa kasus yang jelas
karsinoma, mungkin terlihat sel-sel yang menyerupai sel-sel basal. Akan
tetapi apabila sel-sel tersebut diwarnai dengan antibodi yang spesifik untuk
sel basal maka hasilnya negatif dan sel tersebut hanya fibroblast yang
mengelilingi kelenjar yang ganas. Sebaliknya sel-sel basal mungkin tidak
dikenali pada kelenjar-kelenjar yang jinak tanpa pewarnaan khusus.5,13
Histopatologi kanker dibedakan dari kelenjar yang jinak dengan melihat
2.6.5.1. Gambaran arsitektur
Kelenjar prostat yang jinak cenderung tumbuh sebagai nodul-nodul yang
berbatas jelas dengan kelenjar yang hiperplasia, radial keluar dari uretra
dengan pola linier bahkan tersebar pada zona perifer. Berbeda dengan
kelenjar pada kanker prostat, dimana kelenjar-kelenjarnya lebih ramai,
tumbuh dengan pola yang tidak beraturan, batas kelenjar irreguler dipisahkan
oleh bundelan otot polos yang menandakan suatu proses infiltratif. Pola lain
yang menandakan telah adanya proses infiltratif adalah dijumpainya kelenjar
kecil yang atipikal di antara kelenjar-kelenjar besar yang jinak. Dengan
hilangnya diferensiasi kelenjar, pembentukan struktur cribriform, fusi
kelenjar-kelenjar dan kelenjar-kelenjar yang poorly differentiated,
memudahkan kita membedakannya dari kelenjar-kelenjar yang jinak.
Gambaran arsitektur merupakan komponen penting untuk grading
adenokarsinoma prostat.13
2.6.5.2. Gambaran inti
Inti sel pada adenokarsinoma prostat mulai dari yang tidak dapat
dibedakan dari epitel prostat yang jinak hingga yang jelas ganas. Biasanya
derajat atipia inti berkaitan dengan derajat arsitektur dari diferensiasi. Pada
sebagian besar adenokarsinoma prostat, perbedaan sitologi kelenjar yang
ganas ketika dibandingkan dengan kelenjar jinak sekelilingnya. Satu hal
yang sering dijumpai adalah inti sel yang membesar dengan nukleoli yang
Beberapa inti sel yang ganas tidak menunjukkan nukleoli yang menonjol,
tetapi menunjukkan pembesaran inti dan hiperkromatik. Pada inti sel
adenokarsinoma prostat, bahkan pada adenokarsinoma yang kehilangan
diferensiasi kelenjar menunjukkan variasi pada bentuk atau ukuran dari satu
inti dengan inti lainnya. Gambaran mitotik lebih sering terlihat pada
adenokarsinoma yang high grade dibandingkan dengan yang low grade.13,14
2.6.5.3. Gambaran sitoplasma
Sel-sel epitel kelenjar pada adenokarsinoma prostat memiliki sitoplasma
yang amphophilic, sedangkan pada kelenjar yang jinak lebih jernih dan
pucat. Akan tetapi pada adenokarsinoma prostat yang low grade,
sitoplasmanya sering juga jernih dan pucat sehingga sering tidak dapat
dibedakan. Sitoplasma sel adenokarsinoma prostat pada semua grade
biasanya kehilangan lipofuscin, sedangkan pada kelenjar prostat yang jinak
[image:42.595.221.427.552.677.2]dijumpai lipofuscin.13,14
Gambar 2.9. Adenokarsinoma prostat dengan sitoplasma yang amphophilic
2.6.5.4. Gambaran intraluminal
Suatu gambaran yang umum terlihat pada lumen kelenjar pada
adenokarsinoma prostat adalah kristaloid prostat, yaitu suatu struktur yang
menyerupai kristal berbentuk bujursangkar, segienam, segitiga atau batang.
Walaupun kristaloid tersebut bukan merupakan diagnosa karsinoma, tetapi
sangat sering dijumpai dijumpai pada kelenjar yang ganas dibanding dengan
yang jinak. Sebagai tambahan sering juga dijumpai sekresi aseluler padat
berwarna merah jambu atau sekresi musinous berwarna kebiruan pada
intraluminal kelenjar adenokarsinoma prostat, khususnya pada
adenokarsinoma yang low grade. Berbeda jelas dengan kelenjar yang jinak,
dimana sering dijumpai corpora amylacea yang terdiri dari struktur cincin
oval atau bulat yang berlapis-lapis.13,14
Gambar 2.10. Kristaloid intraluminal pada adenokarsinoma prostat yang low
grade.1
Adenokarsinoma prostat mempunyai beberapa varian histopatologi, yaitu
oncocytic, lymphoepithelioma-like, sarcomatoid (carcinosarcoma). 9,13
2.6.5.5. Varian Atrophic
Sebagian besar adenokarsinoma prostat memiliki sitoplasma yang banyak,
tetapi pada varian atrophic sitoplasmanya sedikit menyerupai atrofi kelenjar
yang jinak, akan tetapi ini dapat dibedakan. Untuk mendiagnosa
adenokarsinoma varian atrophic harus berdasarkan beberapa gambaran,
yaitu:
•Menunjukkan suatu proses infiltratif yang sebenarnya dengan kelenjar
atrofi ganas yang kecil berada diantara kelenjar-kelenjar besar yang jinak,
sedangkan kelenjar kecil yang jinak menunjukkan konfigurasi lobular dan
mengalami dilatasi sentral yang dikelilingi kelompokan kelenjar-kelenjar
yang lebih kecil (post atrophic hyperplasia).
•Tidak menunjukkan respon stroma yang desmoplastik, sedang kelenjar
jinak yang atrofi menunjukkan reaksi fibrosis.
•Menunjukkan sitologi yang atipik, dimana inti membesar, nukleoli
menonjol.9,13
2.6.5.6. Varian Pseudohyperplastic
Varian ini menyerupai kelenjar prostat yang jinak dengan kelenjar-kelenjar
ganas yang bercabang dan berstruktur papillary. Pengenalan varian ini
berdasarkan pola arsitektur dengan sejumlah kelompokan kelenjar yang rapat
dan intinya atipik serta sitoplasmanya banyak. Susunan kelenjarnya dengan
gambaran back to back.9,13
Gambar 2.12. Varian pseudohyperplastic.13
2.6.5.7. Varian Foamy gland
Varian ini ditandai dengan sitoplasma yang banyak dan foamy dengan
ratio inti terhadap sitoplasma sangat kecil. Walaupun sitoplasmanya
mempunyai gambaran xanthomatous tetapi tidak mengandung lipid. Pada
varian ini tidak terlihat pembesaran inti dan nukleoli tidak menonjol,
sehingga menyulitkan untuk mendiagnosa sebagai karsinoma. Inti selnya
bulat, kecil dan hiperkromatik padat. Ditandai sebagai karsinoma karena pola
terlihat sekresi padat aseluler yang berwarna merah jambu. Varian ini
sebaiknya diklasifikasikan sebagai karsinoma dengan intermediate grade.9,13
Gambar 2.13. Varian foamy gland.13
2.6.5.8. Varian Colloid dan Signet ring
Apabila dijumpai musin ekstraseluler minimal 25% dari tumor yang
direseksi maka dapat dibuat diagnosa adenokarsinoma musinosum prostat.
Varian ini merupakan varian morfologi adenokarsinoma prostat yang jarang.
Suatu pola cribriform cenderung utama dijumpai pada area musinous.
Varian ini terdiri dari genangan musin yang dibatasi oleh sel epitel kolumnar
dengan sel-sel goblet yang menunjukkan atipia inti dan sel-sel signet yang
mengandung musin. Varian ini memiliki sifat yang agresif dan kecendrungan
Gambar 2.14. Varian colloid.13
Gambar 2.15. Varian signet ring.13
2.6.5.9. Varian Oncocytic
Adenokarsinoma prostat jarang terdiri dari sel-sel besar (large cell) dengan
sitoplasma yang granular eosinofilik. Pada varian ini dijumpai sel-sel tumor
dengan inti sel yang bulat, oval, hiperkromatik dan positif kuat terhadap
PSA.9,13
2.6.5.10. Varian yang menyerupai Lymphoepithelioma
Varian ini merupakan karsinoma yang undifferentiated , dimana ditandai
dengan pola syncytial dari sel-sel ganas yang diinfiltrasi berat oleh limfosit.
Pada pemeriksaan hibridisasi insitu, varian ini negatif terhadap
2.6.5.11. Varian Sarcomatoid (Carsinosarcoma)
Sarcomatoid carcinoma prostat merupakan neoplasma yang jarang, terdiri
dari sel epitel dan sel spindle yang ganas dan atau elemen mesenkim.
Gambaran makroskopisnya menyerupai sarkoma. Secara mikroskopis
sarcomatoid carcinoma terdiri dari komponen kelenjar yang menunjukkan
Gleason score yang bervariasi. Komponen sarcomatoid sering terdiri dari
proliferasi sel-sel spindle ganas yang tidak spesifik.9,13
Gambar 2.16. Varian sarcomatoid (A) dengan formasi osteoid (B).13
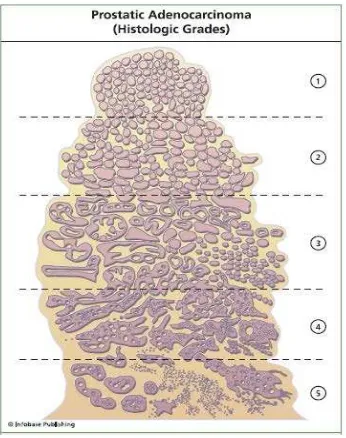
2.6.6. Gleason Grade
Tumor grading dari adenokarsinoma prostat merupakan penentu dasar dari
biologi penyakit dan prognosa. Prognosis ditentukan potensi agresif dari
tumor untuk menyebar ke organ lain. Gleason score merupakan metode
grading yang digunakan secara luas sampai saat ini yang merupakan suatu
faktor prognosis yang penting untuk adenokarsinoma prostat. Sehingga
sekali diagnosa adenokarsinoma prostat ditetapkan pada biopsi, penentuan
Gleason score merupakan penjumlahan dari primary grade (sebagian
besar yang terlihat pada tumor) dengan secondary grade (sebagian kecil yang
terlihat). Gleason score tertinggi menunjukkan tumor yang lebih agresif dan
prognosis yang lebih buruk. Primary Gleason grade menunjukkan lebih
besar dari 50% pola yang terlihat, sedangkan secondary Gleason grade
menunjukkan lebih kecil dari 50% pola yang terlihat, minimal 5%.
Kelemahan dari Gleason score adalah Gleason score dan grading sebagian
besar subjektif dan range dari Gleason score sempit, dimana sebagian besar
Gleason score yang dibuat 6,7 atau 8. Gleason score 2-4 sebaiknya tidak
dibuat pada biopsi prostat transrektal dan Gleason score 9,10 tidak umum.
Pengalaman dari masing-masing ahli patologi tidak sama dalam menilai
Gleason grade, khususnya pada sediaan biopsi yang kecil. Analisa kebenaran
dari Gleason score sebaiknya dikorelasikan antara perkiraaan Gleason score
dari sediaan biopsi dengan specimen operasi prostatektomi radikal. Gleason
score yang dibuat dari sediaan biopsi sering undergrading dibanding dengan
tumor yang sebenarnya. Proporsi grade 4 atau 5 memiliki nilai prognosis
yang bermakna, sehingga apabila dijumpai Gleason score 7 maka harus
ditentukan jumlah tampilan Gleason grade 4 atau 5.15
Digambarkan Gleason grade 1 apabila kelenjar-kelenjar tunggal, terpisah,
seragam, berukuran intermediate, closely packed dengan pinggir yang jelas,
tidak ada infiltrasi ke jaringan prostat sekitarnya, jumlahnya < 5% dari
seluruh serial. Adenokarsinoma grade 1 muncul pada zona tansisional,
atau reseksi transurethral. Gleason grade 1 hampir tidak pernah dijumpai
pada biopsi jarum.9,10,13,14,16,17
Gambar 2.17. Gleason grade 1.13
Gleason grade 2 terdiri dari sekitar 5% dari tumor dan muncul sebagai
suatu nodul yang terpisah, walaupun batas dengan jaringan prostate
sekitarnya samar-samar. Kelenjar-kelenjarnya tersusun lebih longgar, tidak
terlalu seragam dalam ukuran dan bentuk seperti pada grade 1. Mungkin juga
dijumpai invasi minimal oleh kelenjar yang ganas ke sekitar jaringan
prostate. Kelenjar-kelenjar berukuran intermediate dan lebih besar dari grade
3. Sebagian besar grade 2 muncul pada zona transisional dan juga tidak
biasanya sebagai pola pertama yang dijumpai pada biopsi jarum. Gleason
grade 2 biasanya merupakan pola kedua biopsi jarum dengan pola pertama
Gambar 2.18. Gleason grade 2.13
Gleason grade 3 umumnya merupakan pola yang sering dijumpai pada
biopsi jarum. Gambaran karakteristik grade 3 yang membedakannya dari
grade 1-2 adalah tidak ada batas tegas, adanya batas infiltratif dengan
kelenjar dan stroma yang jinak. Kelenjar-kelanjar pada grade 3 menunjukkan
variasi ukuran, bentuk dan jarak. Grade 3 meliputi arsitektur acinar dan
sering berbentuk angular. Kelenjar yang berukuran kecil biasanya yang
terlihat pada grade 3, tetapi dapat juga berukuran besar dan ireguler.
9,10,13,14,16,17
Gambar 2.19. Gleason grade 3.13
lengkap dipisahkan stroma. Bagian pinggir kelompokan kelenjar yang
berfusi adalah scalloped dan kadangkala dijumpai jaringan ikat yang tipis di
dalam kelompokan tersebut. 9,10,13,14,16,17
Gambar 2.20. Gleason grade 4.13
Pada Gleason grade 5 terlihat kehilangan lumen kelenjar, kehilangan
diferensiasi kelenjar dan nekrosis (comedonekrosis). Epitel kelenjar
membentuk lembaran padat atau sel-sel tunggal yang menginvasi
stroma.9,10,13,14,16,17
Gambar 2.22. Gleason grade pada adenokarsinoma prostate.17
2.6.7. Faktor Prognostik
Tiga kelompok faktor prognostik dapat dibedakan dalam kasus
adenokarsinoma prostat: 1. tahap perkembangan menurut TNM; 2.
diferensiasi tingkat keganasan berdasarkan klasifikasi Gleason dan Mostofi;
3. tingkat PSA (prostat spesifik antigen) dalam serum.
2.6.7.1. Klasifikasi TNM
T-tahap: tumor primer.
Tx-tumor primer tidak dapat dinilai.
T0-tidak ada bukti tumor primer.
T1-tumor tidak terlihat secara klinis, tidak teraba atau terlihat oleh
T1a-secara insidentil tumor yang ditemukan dalam tes histopatologi setelah
reseksi prostat transuretra atau setelah operasional adenectomy, ditemukan 5
% atau kurang pada jaringan yang direseksi.
T1b-seperti di atas; ditemukan lebih dari 5% pada jaringan yang direseksi.
T1c-tumor diidentifikasi secara histopatologi oleh biopsi jarum (karena
tingginya PSA).
T2-tumor terbatas dalam kelenjar prostat.
T2a-tumor melibatkan kurang dari setengah dari satu lobus.
T2b-tumor melibatkan lebih dari setengah dari satu lobus.
T2c-tumor melibatkan kedua lobus.
T3-tumor meluas melalui kapsul prostat.
T3a-ekstensi ekstrakapsular (unilateral atau bilateral).
T3b-tumor melibatkan vesikel seminalis.
T4-tumor melibatkan struktur yang berdekatan selain vesikel seminalis,
seperti leher kandung kemih, sfingter eksternal, rektum, otot levator atau
dinding pelvis.
N-tahap: kelenjar getah bening regional.
Nx-kelenjar getah bening regional tak dapat dinilai.
N0-tidak ada metastasis kelenjar getah bening regional.
M-tahap: metastasis jauh.
Mx-metastasis jauh tidak dapat dinilai.
M0-tidak ada metastasis jauh.
M1-ada metastasis jauh.
M1a-bukan kelenjar getah bening regional.
M1b-tulang.
M1c-tempat lain.11,13,18
Stadium klinis
Stadium I : T1a No Mo
Stadium II : T1a No Mo
T1b,c No Mo
T1,T2 No Mo
Stadium III : T3 No Mo
Stadium IV : T4 No Mo
Any T N1 Mo
Any T Any N M1 5,11,13,18
2.6.7.2. Tingkat diferensiasi kanker
Tingkat diferensiasi didefinisikan menurut klasifikasi dengan Mostofi dan
Gleason. Klasifikasi Mostofis menggunakan penilaian 3 kelas diferensiasi,
grade, makin rendah diferensiasi jaringan kanker, semakin besar atipik.
Klasifikasi Gleason telah dijelaskan di atas.18
Grade histopatologi:
GX : grade tidak dapat dinilai.
G1 : well differentiated ( Gleason score 2-4)
G2 : moderately differentiated (Gleason score 5-6)
G3 : poorly differentiated/undifferentiated (Gleason score 7-10).11,13
2.6.7.3. Tingkat PSA dalam serum
PSA adalah enzim yang bertanggung jawab atas proteolitik cairan sperma
untuk mencair. Hal ini terutama dihasilkan oleh kelenjar epitel, mungkin juga
diproduksi di organ-organ seperti kelenjar ludah, pankreas dan kelenjar
mammae dan karsinoma sel jernih. Nilai normal umum yang digunakan
adalah 0-4 ng / ml. Konsentrasi PSA seperti ini ditemukan di antara 97% dari
pria di atas 40. Tingkat lebih dari 12 ng / ml selalu berhubungan dengan
kelainan prostat. Kesulitan diagnosa ditemukan di antara para pasien yang
memiliki tingkat antara 5-10 ng / ml karena mungkin keduanya berasal dari
adenokarsinoma prostat atau pertumbuhan berlebihan dari prostat yang
ringan, yang menyebabkan perlunya metode diagnostik digunakan, seperti
TRUS. Tes ini memungkinkan untuk menentukan densitas PSA (PSA
density), dimana konsentrasi PSA dikonversikan ke satuan volume prostat.
dengan perkembangan adenokarsinoma prostat. Namun berguna sebagai
faktor prognostik setelah perawatan diterapkan dan dalam penentuan
prognosis. Namun, tingkat akhir yang tinggi menunjukkan tingkat
kelangsungan hidup yang rendah.8,18
2.6.8. Imunohistokimia
Pemeriksaan imunohistokimia terhadap adenokarsinoma prostat
bermacam-macam, seperti PSA (prostate specific antigen), PAP (prostatic
acid phosphatase), keratin 34βE12, p63, alpha methylacyl CoA racemase (P504S), androgen reseptor, p53.9,13,19
2.6.8.1. PSA (prostate specific antigen)
PSA merupakan suatu rantai tunggal glikoprotein, 34 kD, terdiri dari 237
asam amino, yang dihasilkan sel-sel epitel prostat. PSA merupakan suatu
protease serine, termasuk famili gen kallikrein. PSA menunjukkan aktifitas
yang menyerupai chymotrypsin, trypsin dan esterase. Pada serum, PSA
muncul sebagai suatu komplek dengan alpha-1-antichymotrypsin.
Pada prostat yang normal atau hiperplasia, PSA tampil pada bagian apikal
dari epitel kelenjar sel-sel sekresi. Intensitas pewarnaan menurun pada
Gambar 2.23. Imunohistokimia PSA pada epitel kelenjar prostat yang normal
(A) dan adenokarsinoma prostat yang poorly differentiated (B).19
2.6.8.2. PAP (prostatic acid phosphatase)
Pada kelenjar prostat normal dan hiperplasia prostat, PAP tampil pada
bagian apikal dari epitel kelenjar sel-sel sekresi. Ekspresi PAP lebih seragam
dan kuat pada epitel kelenjar well differentiated adenocarcinoma, tetapi
berkurang intensitasnya dan lebih bervariasi pada moderately dan poorly
differentiated adenocarcinoma.9,13,19,20
2.6.8.3. Keratin 34βE12
Pewarnaan keratin 34βE12 terekspresi pada seluruh sel-sel basal prostat
yang normal, tetapi tidak terwarnai pada sel-sel sekresi dan stroma. Keratin
34βE12 sensitif terhadap formalin dan membutuhkan pretreatment dengan
enzim atau panas jika fiksasi formalin yang digunakan.19
Hilangnya lapisan sel basal pada proliferasi prostat merupakan gambaran
basal mungkin membantu untuk membedakan adenokarsinoma prostat
invasif dengan lesi jinak yang menyerupai kanker seperti atrofi kelenjar,
hiperplasia post-atrofi, adenosis (atypical adenomatous hyperplasia),
adenosis sklerotik dan atipia yang diinduksi radiasi yang masih memiliki
[image:59.595.160.488.277.543.2]lapisan sel basal.9,13
Gambar 2.24.Imunohistokimia keratin 34βE12 pada epitel kelenjar prostat
yang normal (A); PIN (B); adenokarsinoma prostat (C).19
2.6.8.4. p63
p63 merupakan suatu protein inti yang dikode oleh gen pada kromosom
3q27-29 yang homolog dengan p53 (suatu tumor supressor gene), yang
dan traktus urogenital.12,21 Berbeda dengan p53, p63 mengkode minimal 6
isotipe utama. Tiga isotipe (TAp63α, TAp63β, TAp63γ) terdiri dari
transactivating domain (TA) dan mampu mengaktifkan p53 dan
menginduksi apoptosis. Berbeda dengan tiga isotipe lainnya (ΔNp63α,
ΔNp63β, ΔNp63γ) tidak mengandung TA domain dan mensupresi p53 dan
isotipe TAp63. p63 diekspresikan pada sel-sel basal sebagian besar organ
yang berepitel, demikian juga dengan prostat. p63 memiliki peranan dalam
perkembangan prostat dengan mempertahankan populasi sel stem prostat,
sehingga p63 juga tertampil pada sel stem prostat. Isotipe yang paling banyak
tertampil pada sel-sel basal prostat normal adalah ΔNp63α.21,22,23
Tampilan ΔNp63α menurun pada sel-sel yang telah berdifferensiasi secara
invitro dan invivo serta diduga ΔNp63α tertampil secara spesifik pada sel
stem yang menunjukkan kemampuan proliferatif yang tinggi. Tampilan
ΔNp63α diatur melalui jalur phosphoinositide 3-kinase.24
Tampilan berlebihan dari p63 menginduksi apoptosis, walaupun
masing-masing isotipe memiliki kemampuan yang berbeda. Mutasi p63 terjadi pada
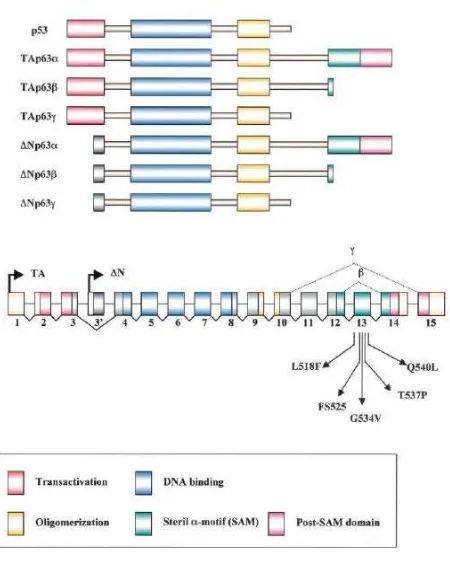
Gambar 2.25. Struktur p63.22
Perbedaan tampilan p63 berhubungan dengan progresi kanker atau suatu
prognosis yang jelek pada beberapa kanker, dimana tampilan berlebihan pada
ovarium dan karsinoma sel skuamous oral, penurunan tampilan pada saluran
kemih atas dan prostat serta tampilan aberant cytoplasmic pada
adenokarsinoma paru-paru.26
Pada prostat normal, sel-sel basal masih utuh sehingga akan menampilkan
p63, sedang pada adenokarsinoma prostat dimana tidak dijumpai lagi sel-sel
basal maka p63 mungkin tidak tertampil. Oleh karena itu dapat digunakan
Akan tetapi pada adenokarsinoma prostat dapat terlihat peningkatan
tampilan aberant p63 di sitoplasma yang berhubungan dengan mortalitas,
[image:62.595.171.488.223.460.2]proliferatif yang meningkat dan apoptosis yang menurun.26
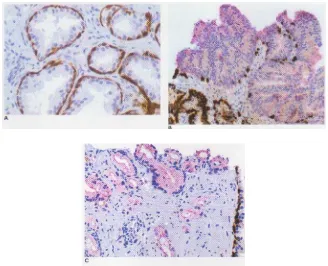
Gambar 2.26.A. Tampilan p63 pada sel basal kelenjar prostat normal; B.
Pewarnaan p63 negatif baik di sitoplasma maupun inti pada adenokarsinoma
prostat; C dan D. Pewarnaan p63 positif di sitoplasma pada adenokarsinoma
prostat.26
p63 memiliki kesamaan aplikasi dengan high molecular weight cytokeratin
dalam mendiagnosa adenokarsinoma prostat, tetapi memiliki keuntungan
seperti: 1. lebih sensitif dibanding 34βE12 dalam pewarnaan sel-sel basal
karena intensitas pewarnaan inti lebih kuat dan lemah pada
latarbelakangnya.19
2.6.8.5. Alpha methylacyl CoA racemase (AMACR)
AMACR merupakan suatu enzim yang terlibat dalam oksidasi β pada
rantai bercabang asam lemak. AMACR merupakan petanda tumor untuk
banyak kanker pada manusia termasuk adenokarsinoma prostat. Studi
pendahulu menunjukkan positif kuat pada 97%- 100% adenokarsinoma
prostat. Sebagai tambahan AMACR juga positif pada sebagian besar high
grade neoplasia intraepitel prostat, 10-15% pada atypical adenomatous
hyperplasia, kadang-kadang pada kelenjar yang jinak dan epitel vesikel
seminalis.13,19
Jadi AMACR tidak spesifik untuk adenokarsinoma prostat, akan tetapi
AMACR bermanfaat untuk konfirmasi adenokarsinoma prostat bersamaan
dengan morfologi H&E dan pewarnaan spesifik sel-sel basal.9,13
2.6.8.6. Reseptor androgen
Reseptor androgen berlokasi pada inti, terikat pada komplek protein yang
muncul pada sel epitel kelenjar prostat, sel basal dan sel stroma. Protein yang
teraktifasi merupakan suatu faktor transkripsi yang memperantarai fungsi sel
yang tergantung androgen seperti transkripsi PSA pada sel-sel sekresi dan
Sebagian besar adenokarsinoma prostat invasif imunoreaktif terhadap
reseptor androgen. Reseptor androgen tampil pada sel-sel yang respon dan
tidak respon terhadap androgen pada kanker prostat, sehingga dugaan
perkembangan sel-sel yang tidak tergantung terhadap androgen tidak seperti
konsekuensi terhadap kehilangan ekspresi reseptor androgen.19
2.6.8.7. p53
Inaktifasi tumor supressor p53 merupakan salah satu perubahan genetik
yang paling sering pada tumor ganas. Pada sebagian besar kasus, inaktifasi
p53 sebagian disebabkan suatu mutasi inaktifasi pada satu allele p53.
Sejumlah studi imunohistokimia menemukan peranan inaktifasi p53 pada
berbagai tipe kanker. Diduga adanya hubungan antara akumulasi p53 inti
dengan prognosis yang jelek.28
Sejumlah besar kanker menunjukkan akumulasi p53 inti setelah terapi
radiasi dan tampilan berlebihan p53 berhubungan dengan peningkatan
proliferasi sel-sel kanker. Akumulasi p53 inti juga berhubungan dengan efek
yang berlawanan dengan setelah terapi radiasi dan mungkin meningkatkan
kekambuhan adenokarsinoma prostat setelah terapi radiasi.
Prendergast et al. mempelajari 18 pasien dengan kekambuhan lokal
adenokarsinoma prostat setelah terapi dan menemukan 72% memiliki
imunoreaktif terhadap p53. Sekitar 5 pasien dengan biopsi sebelum terapi,
semuanya menunjukkan imunoreaktif terhadap p53. Pengamatan ini
mungkin dapat digunakan sebagai petanda preterapi untuk kekambuhan
kanker. Pasien dengan kecepatan proliferasi sel yang tinggi juga
menunjukkan tampilan berlebihan p53, sehingga diduga tumor tersebut aktif
secara biologi. 19
Gambar 2.27. Imunohistokimia p53 pada adenokarsinoma prostat yang
poorly differentiated.19
K.R.M.Leite et al. (1997) dalam mempelajari 51 pasien dengan radikal
prostatektomi karena kanker prostat menunjukkan bahwa ekspresi
imunohistokimia p53 berhubungan dengan proliferasi sel.29
Thorsten S et al. (2005) dalam mempelajari 3261 pasien dengan radikal
prostatektomi menunjukkan adanya hubungan antara ekspresi
imunohistokimia p53 dengan Gleason grade dan kanker prostat yang
hormone refractory.28
Petrescu A et al. (2006) dalam studinya menunjukkan deteksi
prostat, dimana tampilan berlebih p53 berhubungan dengan Gleason grade
yang tinggi dan menunjukkan prognosis yang jelek.30
Gambar 2.28. Pewarnaan imunohistokimia p53 yang kuat (a) dan sedang
(b).28
2.6.9. Pengobatan
Pengobatan terhadap adenokarsinoma prostat sangat efektif apabila belum
menyebar ke organ sekitarnya dan belum metastasis. Pengobatan terhadap
adenokarsinoma prostat yang masih terbatas pada organ prostat adalah
prostatektomi, radiasi dan brachyterapi. Apabila adenokarsinoma prostat
telah metastasis maka digunakan terapi hormon dengan cara ablasi hormonal
secara bedah (kastrasi), ablasi hormonal dengan obat-obatan (antagonis
reseptor androgen, inhibitor 5α-reduktase) atau gabungan keduanya
(combined androgen blockade).16,17,31,32
2.7. Kerangka Konsep
Neoplasia intraepitel prostat
Adenokarsinoma prostat
Tampilan p63 Kerusakan sel
basal yang sulit dikenali dengan pewarnaan HE
Inti sel basal
Sitoplasma sel luminal
+ _
Aberrant p63
BAB 3