ENKAPSULASI EKSTRAK TEMULAWAK MENGGUNAKAN
MATRIKS PATI TAPIOKA DAN SAGU NANOKRISTALIN
DAN MALTODEKSTRIN
FATIMAH JUMIATI PASARIBU
DEPARTEMEN TEKNOLOGI INDUSTRI PERTANIAN FAKULTAS TEKNOLOGI PERTANIAN
INSTITUT PERTANIAN BOGOR BOGOR
PERNYATAAN MENGENAI SKRIPSI DAN
SUMBER INFORMASI SERTA PELIMPAHAN HAK CIPTA*
Dengan ini saya menyatakan bahwa skripsi berjudul Enkapsulasi Ekstrak Temulawak Menggunakan Matriks Pati Tapioka dan Sagu Nanokristalin dan Maltodekstrin adalah benar karya saya dengan arahan dari komisi pembimbing dan belum diajukan dalam bentuk apa pun kepada perguruan tinggi mana pun. Sumber informasi yang berasal atau dikutip dari karya yang diterbitkan maupun tidak diterbitkan dari penulis lain telah disebutkan dalam teks dan dicantumkan dalam Daftar Pustaka di bagian akhir
Dengan ini saya melimpahkan hak cipta dari karya tulis saya kepada Institut Pertanian Bogor.
ABSTRAK
FATIMAH JUMIATI PASARIBU. Enkapsulasi Ekstrak Temulawak Menggunakan Matriks Pati Tapioka dan Sagu Nanokristalin dan Maltodekstrin. Dibimbing Oleh TITI CANDRA SUNARTI.
Ekstrak temulawak merupakan oleoresin rimpang temulawak yang mengandung bahan aktif kurkumin yang diketahui berkhasiat sebagai antioksidan. Akan tetapi pemanfaatannya terbatas karena sifatnya yang hidrofobik, bioavailabilitas rendah, serta sensitif terhadap pH, suhu, dan cahaya. Kelemahan tersebut dapat diatasi dengan enkapsulasi kurkumin menggunakan bahan penyalut pati nanokristalin. Kelebihan pati nanokristalin dibandingkan polimer lain sebagai matriks antara lain biodegradable, memiliki kekuatan pengikatan yang tinggi, dan ukuran yang kecil membuat penyerapannya lebih tinggi. Pati sagu dan tapioka nanokristalin merupakan pati potensial yang dapat dijadikan sebagai matriks karena kelarutan dan daya cernanya yang rendah. Penelitian ini bertujuan untuk mengetahui pengaruh persentase rasio pati nanokristalin dari tapioka dan sagu sebagai matriks dan maltodekstrin sebagai penstabil, serta konsentrasi ekstrak temulawak terhadap karakteristik nanokapsul yang dihasilkan, dan pengaruh enkapsulasi terhadap stabilitas aktivitas antioksidan ekstrak temulawak. Hasil penelitian menunjukkan bahwa rasio pati nanokristalin, maltodekstrin dan konsentrasi ekstrak temulawak berpengaruh nyata terhadap karakteristik nanokapsul. Perlakuan enkapsulasi terbaik pada matriks tapioka nanokristalin didapatkan pada rasio pati nanokristalin: maltodekstrin 25 : 75 (% b/b) dan konsentrasi ekstrak temulawak 10%, sedangkan pada matriks sagu nanokristalin adalah 75 : 25 (% b/b) dan konsentrasi ekstrak temulawak 10%. Aktivitas antioksidan ekstrak temulawak menurun setelah dilakukan enkapsulasi dibandingkan sebelum enkapsulasi. Penggunaan suhu tinggi saat spray drying mempengaruhi penurunan aktivitas antioksidan ekstrak temulawak.
Kata kunci : enkapsulasi, ekstrak temulawak, pati nanokristalin, tapioka, sagu
ABSTRACT
FATIMAH JUMIATI PASARIBU. Encapsulation of Temulawak Extract using Tapioca and Sago Nanocrystalline Starch Matrix and Maltodextrin. Supervised by TITI CANDRA SUNARTI.
percentage ratio of tapioca and sago nanocrystalline starch as matrix and maltodextrin as stabilizer; and the effect of concentration of temulawak extract on nanocapsule characteristics, as well as encapsulation effect on stability of antioxidant activity. The results showed that percentage ratio of nanocrystalline starch, maltodextrin and concentration of temulawak extract significantly affected to the nanocapsule characteristics. The best encapsulation condition obtained for tapioca nanocrystalline matrix with ratio of nanocrystalline starch : maltodextrin 25 : 75 (% w/w) and 10% concentration of temulawak extract, while for sago are 75: 25 (% w/w) and 10% concentration of temulawak extract. The use of high temperature on spray drying affected to the declining of antioxidant activity of encapsulated temulawak extract.
Skripsi
sebagai salah satu syarat untuk memperoleh gelar Sarjana Teknologi Pertanian
pada
Departemen Teknologi Industri Pertanian
ENKAPSULASI EKSTRAK TEMULAWAK MENGGUNAKAN
MATRIKS PATI TAPIOKA DAN SAGU NANOKRISTALIN
DAN MALTODEKSTRIN
FATIMAH JUMIATI PASARIBU
DEPARTEMEN TEKNOLOGI INDUSTRI PERTANIAN FAKULTAS TEKNOLOGI PERTANIAN
INSTITUT PERTANIAN BOGOR BOGOR
PRAKATA
Puji dan syukur penulis panjatkan kepada Allah subhanahu wa ta’ala atas segala limpahan rahmat dan karunia-Nya sehingga penyusunan skripsi dengan judul “Enkapsulasi Ekstrak Temulawak Menggunakan Matriks Pati Tapioka dan Sagu Nanokristalin dan Maltodekstrin” telah dapat diselesaikan. Penelitian ini dilaksanakan mulai bulan Juni 2014 sampai dengan Desember 2014 dan merupakan bagian dari penelitian KKP3N yang didanai oleh Badan Litbang Pertanian tahun 2014. Selama penyusunan skripsi ini penulis ingin mengucapkan terima kasih kepada :
1 Dr Ir Titi Candra Sunarti selaku pembimbing atas semua bimbingan, motivasi, saran selama penelitian hingga penyelesaian skripsi ini.
2 Ibu tercinta Nur Asimah Pohan, yang menjadi ayah sekaligus ibu bagi penulis, dan kakak Tini Safridar Pasaribu serta abang dan adik yang selalu mencurahkan doa dan dukungan kepada penulis.
3 Ibu Christina Winarti yang telah berbagi ilmu, saran, diskusi ilmiah dan banyak bantuan selama penyelesaian skripsi ini.
4 Teman seperjuangan di Laboratorium Bioindustri, Fithriani dan Ardhi Novrialdi Ginting, serta teman - teman TIN 47 lainnya.
5 Pihak - pihak lain yang tidak dapat disebutkan satu per satu atas segala bantuan dan dukungannya sehingga penulis dapat menyelesaikan penelitian dan penyusunan skripsi ini dengan baik.
semoga karya ilmiah ini bermanfaat bagi semua pihak yang membutuhkannya.
Bogor, Agustus 2015
DAFTAR ISI
DAFTAR TABEL x
DAFTAR GAMBAR x
DAFTAR LAMPIRAN x
PENDAHULUAN 1
Latar Belakang 1
Perumusan Masalah 2
Tujuan Penelitian 3
Manfaat Penelitian 3
Ruang Lingkup Penelitian 3
METODE 3
Bahan 3
Alat 4
Prosedur Penelitian 4
Rancangan Percobaan dan Analisis Data 6
HASIL DAN PEMBAHASAN 6
Karakteristik Pati Nanokristalin 6
Karakteristik Nanokapsul 9
SIMPULAN DAN SARAN 21
Simpulan 21
Saran 21
DAFTAR PUSTAKA 22
LAMPIRAN 25
DAFTAR TABEL
1 Komposisi penambahan maltodekstrin dan pati nanokristalin 4 2 Karakteristik fungsional pati tapioka dan pati sagu nanokristalin 8
DAFTAR GAMBAR
1 Diagram alir produksi pati nanokristalin 5
2 Ilustrasi perusakan daerah amorf pada proses lintnerisasi 7 3 Representasi skema struktur kompleks amilosa-bahan aktif dan
kemungkinan lokasi molekul yang terjerat 10
4 Struktur molekul maltodekstrin 11
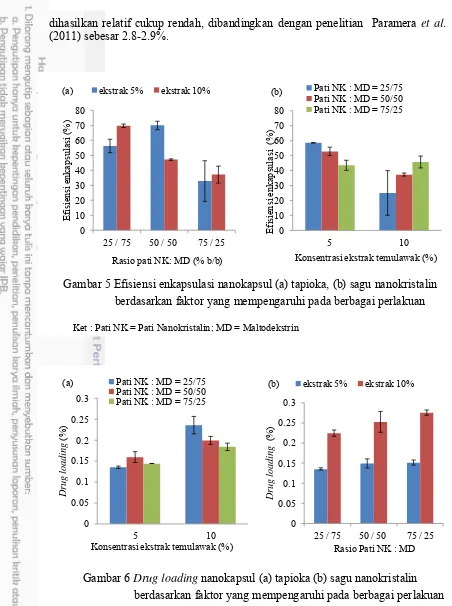
5 Efisiensi enkapsulasi nanokapsul (a) tapioka, (b) sagu nanokristalin berdasarkan faktor yang mempengaruhi pada berbagai perlakuan 14 6 Drug loading nanokapsul (a) tapioka (b) sagu nanokristalin
berdasarkan faktor yang mempengaruhi pada berbagai perlakuan 14 7 Struktur kimia radikal bebas (1) dan non radikal DPPH (2) 17 8 Aktivitas antioksidan nanokapsul (a) tapioka (b) sagu nanokristalin
sebelum enkapsulasi dan sesudah sesudah enkapsulasi berdasarkan faktor yang mempengaruhi pada berbagai perlakuan 18 9 Struktur kimia kurkumin dan demetoksikurkumin 20
DAFTAR LAMPIRAN
1 Karakterisasi pati nanokristalin 25
2 Penentuan kinerja nanokapsul 27
3 Hasil uji karakteristik nanokapsul 28
4 Hasil analisis keragaman faktor rasio pati tapioka nanopartikel : maltodekstrin, dan konsentrasi ekstrak temulawak terhadap
karakteristik nanokapsul 29
5 Hasil analisis keragaman faktor rasio pati sagu nanopartikel : maltodekstrin, dan konsentrasi ekstrak temulawak terhadap
karakteristik nanokapsul 31
PENDAHULUAN
Latar Belakang
Temulawak merupakan salah satu jenis tanaman khas Indonesia yang banyak dimanfaatkan sebagai obat atau jamu disebabkan mengandung senyawa aktif kurkumin yang berkhasiat sebagai antioksidan, mengatasi kurang nafsu makan, anti inflamasi, anti kanker, anti kolesterol, dan menyembuhkan berbagai penyakit lainnya. Penelitian dan studi klinis mengenai manfaat kurkumin ini telah banyak dilakukan (Dhillon et al. 2008; Gharcia et al. 2007; Sharma et al. 2001; Shoskes et al. 2005). Konsumsi temulawak saat ini umumnya secara komersil disajikan dalam bentuk ekstrak temulawak atau serbuk bahan dengan diseduh air panas. Penyerapan senyawa aktif kurkumin dalam tubuh dalam bentuk ekstrak temulawak tersebut kurang efektif karena sifat kurkumin yang memiliki bioavailabilitas yang rendah dan tidak dapat larut air. Selain itu kurkumin memiliki sensitivitas tinggi terhadap pH, suhu, dan cahaya. Oleh karena itu, salah satu cara untuk mengatasi kelemahan tersebut, yaitu untuk meningkatkan kelarutan dan bioavailabilitas kurkumin dalam ekstrak serta melindungi kurkumin adalah dengan menyalut kurkumin dengan bahan penyalut (matriks) yang sesuai.
Diantara berbagai bahan yang umum digunakan sebagai matriks, seperti lipid, protein, pati, atau polimer non biodegradagable seperti Eudragit, pati lebih banyak digunakan karena memiliki beberapa keunggulan, antara lain harganya yang relatif murah, tersedia dalam jumlah besar, bersifat biodegradable dan mudah dimodifikasi untuk perbaikan karakteristik fisiko-kimianya. Pati juga telah lama dimanfaatkan sebagai bahan tambahan pada sediaan obat di bidang farmasi, baik sebagai bahan pengisi, penstabil, atau penyalut obat. Oleh karena itu, pada penelitian ini digunakan pati sebagai bahan penyalut. Akan tetapi, penggunaan pati alami sebagai matriks memiliki kelemahan seperti tidak larut dalam air dingin, viskositas suspensi yang tidak stabil, dan daya cerna nya yang tinggi yang tidak sesuai dengan karakteristik matriks yang diinginkan. Oleh karena itu agar sesuai perlu dilakukan modifikasi terhadap pati. Modifikasi yang dapat dilakukan adalah dengan lintnerisasi, yaitu merusak bagian amorf pati dan amilosa pada titik percabangan rantai amilopektin untuk menjadi pati kristalin sehingga menurunkan daya cerna pati, dan mengubah ukuran pati menjadi nano (nanopartikel) melalui proses presipitasi.
2
dengan kristalinitas tinggi, dan berdasarkan penelitian Wulandari (2013), pati sagu dan tapioka nanopartikel memiliki nilai kelarutan, daya cerna pati yang rendah yang sesuai digunakan sebagai matriks pembawa. Oleh karena itu, enkapsulasi ekstrak temulawak pada penelitian ini menggunakan matriks dari pati sagu dan tapioka nanopartikel.
Menurut Barros dan Stringheta (2006), matriks enkapsulan ideal harus memiliki sifat pembentuk film, memiliki sifat pengemulsi, bersifat biodegradable, resisten terhadap saluran pencernaan, memiliki viskositas yang rendah pada konsentrasi tinggi, menunjukkan higroskopisitas rendah dan murah. Akan tetapi, tidak memungkinkan bahwa semua karakteristik tersebut dapat dipenuhi dengan menggunakan satu matriks saja. Oleh karena itu, pencampuran dari dua atau lebih komponen matriks lebih sering dilakukan (Barros dan Stringheta 2006).
Pada proses pengikatan senyawa aktif kurkumin yang tidak larut air, matriks pati nanopartikel memerlukan bantuan tambahan matriks lain yang berfungsi sebagai penstabil dan emulsifier. Bahan penstabil dibutuhkan untuk menghasilkan nanokapsul yang stabil. Umumnya, nanokapsul bahan aktif distabilkan menggunakan protein biokompatibel (misalnya serum albumin manusia) atau polimer (misalnya PVA) (Gupta 2006). Pada penelitian ini digunakan bahan penstabil berupa maltodekstrin. Maltodekstrin merupakan pati termodifikasi yang banyak diaplikasikan sebagai bahan penstabil dan emulsifier di industri pangan. Maltodekstrin memiliki sifat cepat terdispersi, dapat membentuk sifat higroskopis yang rendah, dan kemampuan membentuk film dan daya ikat yang kuat (Srihari et al. 2010). Karena daya ikatnya yang kuat, maltodekstrin juga digunakan sebagai co-matriks pada penelitian ini.
Aplikasi pati nanopartikel sebagai matriks enkapsulasi telah dilakukan oleh Winarti (2014) yang mengenkapsulasi kurkumin dengan pati garut. Pada penelitian ini enkapsulasi dilakukan menggunakan pati sagu dan pati tapioka nanopartikel sebagai matriks pembawa, dengan penambahan maltodekstrin yang berfungsi sebagai penstabil dan emulsifier, dan perlakuan perbedaan penambahan konsentrasi bahan aktif yang akan dienkapsulasi. Kedua faktor perlakuan tersebut dilakukan untuk melihat pengaruhnya terhadap karakteristik nanokapsul yang dihasilkan, dan pengaruh enkapsulasi terhadap stabilitas ekstrak temulawak dilihat dari aktivitas antioksidannya. Dari pengujian tersebut kemudian dipilih perlakuan terbaik dari tiap matriks yang digunakan dalam enkapsulasi ekstrak temulawak.
Perumusan Masalah
3 maltodekstrin sebagai matriks, dan penambahan ekstrak temulawak menjadi faktor pada penelitian ini.
Tujuan Penelitian
Tujuan umum dari penelitian ini adalah enkapsulasi ekstrak temulawak dalam matriks pati sagu dan tapioka nanokristalin. Tujuan khusus dari penelitian ini adalah untuk mengkaji pengaruh rasio pati nanokristalin dan maltodekstrin yang digunakan sebagai matriks serta konsentrasi ekstrak temulawak yang ditambahkan terhadap karakteristik nanokapsul ekstrak temulawak yang dihasilkan, dan pengaruh enkapsulasi terhadap stabilitas aktivitas antioksidan ekstrak temulawak.
Manfaat Penelitian
Hasil dari penelitian ini diharapkan dapat diaplikasikan sebagai formulasi enkapsulasi ekstrak temulawak dalam matriks nanocarrier. Aplikasi matriks ini sebagai bahan penyalut akan meningkatkan efektifitas senyawa aktif kurkumin dalam ekstrak temulawak dengan bioavalabilitas yang tinggi sehingga dapat dimanfaatkan khasiatnya secara maksimum.
Ruang Lingkup Penelitian
Ruang lingkup penelitian ini mempelajari pengaruh rasio penambahan pati tapioka dan pati sagu nanokristalin dengan maltodekstrin, dan perbedaan konsentrasi ekstrak temulawak yang ditambahkan terhadap karakteristik nanokapsul yang dihasilkan, meliputi rendemen, efisiensi enkapsulasi, drug loading, dan aktivitas antioksidan; mempelajari pengaruh enkapsulasi terhadap stabilitas ekstrak temulawak dilihat dari aktivitas antioksidan ekstrak temulawak sebelum dan sesudah dienkapsulasi, dan pemilihan perlakuan terbaik dari tiap matriks yang digunakan dalam enkapsulasi ekstrak temulawak.
METODE
Bahan
4
Alat
Peralatan yang digunakan pada penelitian ini yaitu waterbath, penangas, magnetic stirrer, oven pengering, neraca analitik, homogenizer Ultra Turrax T25 basic, spray dryer, kertas saring, sonikator (Branson 5510), inkubator, spektrofotometer UV-Vis (HP 8453), dan peralatan gelas untuk analisis.
Prosedur Penelitian
Penelitian ini dilaksanakan dalam tiga tahapan, yaitu preparasi dan karakterisasi pati nanokristalin, tahap enkapsulasi ekstrak temulawak dalam matriks, dan tahap pengujian nanokapsul.
Preparasi Pati Nanokristalin
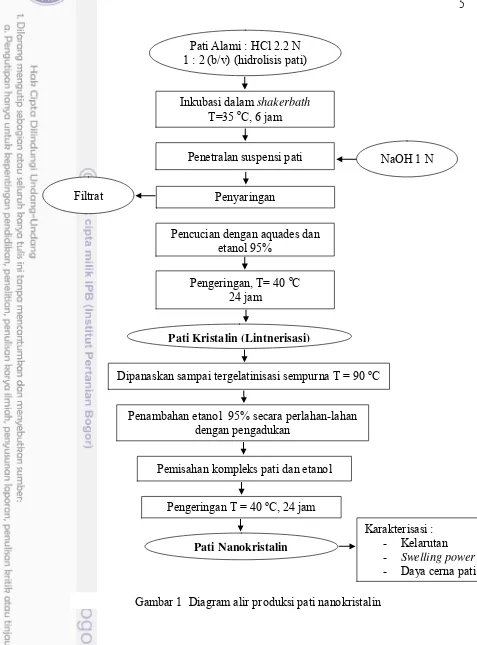
Pati tapioka dan sagu nanokristalin yang digunakan dihasilkan berdasarkan metode dari hasil penelitian Winarti (2014). Adapun proses pembuatan pati nanokristalin disajikan pada Gambar 1.
Karakterisasi Pati Nanokristalin
Karakterisasi pati sagu dan pati tapioka nanokristalin meliputi kelarutan, swelling power, dan daya cerna pati. Metode analisa karakterisasi pati disajikan pada Lampiran 1.
Proses Enkapsulasi Bahan Aktif (Modifikasi Winarti 2014)
Masing-masing matriks nanopatrikel pati sagu dan tapioka dicampurkan dengan maltodekstrin dengan perbandingan komposisi berbeda yang ditunjukkan pada Tabel 1, dengan berat total bahan 15 g (10% b/v). Dasar rasio tersebut digunakan untuk mengetahui pengaruh konsentrasi penyalut yang optimum dengan merepresentasikan nilai bahan penyalut dalam rendah, sama besar, dan tinggi. Kedua jenis campuran pati (pati sagu dan maltodekstrin; pati tapioka dan maltodekstrin) kemudian didispersi dengan akuades suhu 70 oC sambil diaduk dengan magnetic stirrer selama 15 menit, selanjutnya direhidrasi semalam. Ekstrak temulawak yang telah diencerkan dengan etanol hingga kadar padatan terlarut ≥ 20 oBrix dimasukkan ke dalam suspensi pati sebanyak 5% v/v dan 10% v/v, kemudian dihomogenisasi dengan Ultra Turrax selama 10 menit pada kecepatan 11000 rpm. Selanjutnya dilakukan atomisasi dan pengeringan dengan spray dryer dengan kondisi suhu inlet sekitar 80 oC dan suhu outlet 170 oC. Nanokapsul yang diperoleh ditimbang dan dihitung rendemennya.
Tabel 1 Komposisi penambahan maltodekstrin dan pati nanokristalin Basis Komposisi (%) Pati Sagu/Tapioka
Nanokristalin (g) Maltodekstrin (g)
15 g 25 : 75 3.75 11.25
50 : 50 7.50 7.50
5
Gambar 1 Diagram alir produksi pati nanokristalin Pati Alami : HCl 2.2 N
1 : 2 (b/v) (hidrolisis pati)
Inkubasi dalam shakerbath T=35 oC, 6 jam
Penetralan suspensi pati
Penyaringan
Pencucian dengan aquades dan etanol 95%
Pati Kristalin (Lintnerisasi) Filtrat
NaOH 1 N
Dipanaskan sampai tergelatinisasi sempurna T = 90 oC
Penambahan etanol 95% secara perlahan-lahan dengan pengadukan
Pemisahan kompleks pati dan etanol
Pati Nanokristalin Pengeringan, T= 40 oC
24 jam
Pengeringan T = 40 oC, 24 jam
6
Penentuan Karakteristik Nanokapsul
Penentuan karakteristik nanokapsul meliputi efisiensi enkapsulasi, drug loading, dan uji aktivitas antioksidan. Prosedur analisis selengkapnya disajikan pada Lampiran 2. Hasil uji aktivitas antioksidan nanokapsul nantinya akan dibandingkan dengan aktivitas antioksidan ekstrak temulawak sebelum dienkapsulasi untuk melihat stabilitas aktivitas antioksidan yang terjadi.
Rancangan Percobaan dan Analisis Data
Rancangan percobaan pada penelitian ini menggunakan rancangan acak lengkap faktorial (RALF), dengan dua faktor, yaitu faktor konsentrasi ekstrak temulawak (A) (5% dan 10%), dan faktor rasio pati nanokristalin : maltodekstrin (B) (25 : 75, 50 : 50, 75 : 25, ) terhadap karakteristik nanokapsul. Setiap perlakuan diulang sebanyak 3 kali. Data hasil penelitian dianalisis dengan analisis sidik ragam (α = 0.05) dan uji lanjut Duncan menggunakan perangkat lunak SAS 9.1. Model statistik yang digunakan adalah sebagai berikut :
ij = i j ( )ij ij
Keterangan :
Yij1 = nilai respon faktor A taraf ke-i, faktor B taraf ke-j dengan ulangan ke-1
= nilai rata - rata
Ai = pengaruh faktor konsentrasi ekstrak temulawak pada taraf ke-I (i = 5%
dan 10%)
Bj = pengaruh faktor rasio pati dan maltodekstrin pada taraf ke j (j = 25:75,
50:50, 75:25)
(AB)ij = pengaruh interaksi antara faktor A taraf ke-i dan faktor B taraf ke-j
ij = pengaruh galat atau error dari faktor A taraf ke-i, B taraf ke-j
HASIL DAN PEMBAHASAN
Karakteristik Pati Nanokristalin
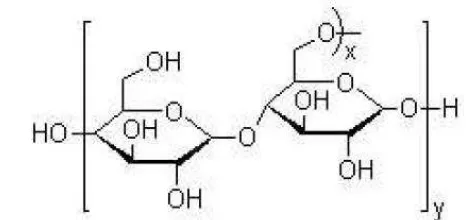
Pati merupakan polimer glukosa dengan ikatan α-glikosidik yang tersusun atas dua homopolimer yang memiliki struktur berbeda yaitu amilosa dan amilopektin. Komponen amilosa dan amilopektin merupakan salah satu faktor yang dapat mempengaruhi perbedaan karakteristik kimia dan fungsional pada pati. Pati tersusun atas granula pati, yang tersusun atas lapisan kristalin dan lapisan amorf. Bagian kristalin merupakan kumpulan molekul amilopektin dalam granula, sedangkan bagian amorf disusun oleh molekul amilosa yang tersebar pada cluster amilopektin.
7
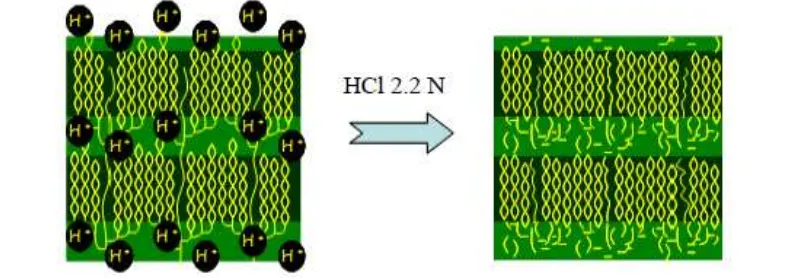
Gambar 2 Ilustrasi perusakan daerah amorf pada proses lintnerisasi (Srichuwong et al. 2005)
20-500 nm, tergantung asal botaninya. Satu bloklet granula tersusun oleh lapisan yang terdiri atas lamela kristal (5-6 nm) dan lamela amorf (2-5 nm) (Gallant et al. 1997). Pati nanopartikel memiliki sifat viskositas rendah walaupun pada konsentrasi tinggi dan memiliki daya mengikat yang tinggi, sehingga pati nanopartikel kerap dimanfaatkan di industri, seperti untuk bahan tambahan makanan, bahan pembawa dalam obat-obatan, coating binders, biodegradable composites, dan berbagai produk lainnya.
Pati nanokristalin dihasilkan melalui dua proses utama, yaitu lintnerisasi dan presipitasi pati. Lintnerisasi pati menghasilkan pati kristalin, yaitu pati termodifikasi yang telah dirusak fraksi amilosa rantai panjang dan titik percabangan α-1,6 inter klaster dari rantai amilopektin sehingga dihasilkan fraksi amilosa rantai pendek dengan bobot molekul yang lebih rendah dan membentuk struktur kristalin dengan dihidrolisis menggunakan asam kuat. Semakin banyak struktur yang diputus dengan asam kuat menjadi gula-gula sederhana, menghasilkan daya cerna pati yang semakin rendah. Lintnerisasi juga bertujuan untuk menurunkan viskositas pati dan meningkatkan kristalinitasnya. Adapun proses perusakan daerah amorf dan kristalin pada proses lintnerisasi diilustrasikan pada Gambar 2.
Lintnerisasi hanya memodifikasi struktur kimia pati, sehingga untuk pengecilan ukuran granula pati dilakukan proses lanjutan yaitu dengan presipitasi. Proses presipitasi dilakukan dengan penambahan pelarut organik secara perlahan dengan pengadukan yang cepat. Terbentuknya pati nanopartikel terjadi ketika pati mendapat perlakuan suhu tinggi saat proses gelatinisasi dan adanya energi mekanis yang mengakibatkan terjadinya perusakan ikatan kovalen dan hidrogen pada struktur double helix amilopektin dan pelelehan bagian kristalin, sehingga terbentuk partikel-partikel yang lebih kecil hingga sampai ukuran nano (Winarti 2014). Berdasarkan penelitian Winarti (2014), pati nanopartikel yang dihasilkan dengan proses presipitasi etanol berukuran antara 100-250 nm.
8
dengan meningkatnya suhu, serta kecepatan peningkatan kelarutan adalah khas untuk tiap pati (Pomeranz 1991). Berdasarkan penelitian Winarti (2014), nilai kelarutan pati nanokristalin lebih rendah dibandingkan pati kristalin (lintnerisasi). Peningkatan kelarutan pada lintnerisasi disebabkan proses hidrolisis telah merusak granula dan memecah rantai pati menjadi lebih pendek sehingga lebih mudah terlarut. Adapun kelarutan pati nanokristalin menurun disebabkan hilangnya molekul air akibat partikel presipitasi etanol. Etanol akan menggantikan molekul air di dalam bahan sehingga kelarutan cenderung rendah (Winarti 2014). Nilai kelarutan pati sagu (56.67%) lebih rendah dibandingkan dengan pati tapioka (72.78%). Hal ini sesuai dengan penelitian sebelumnya oleh Rizkiana (2015) dan Sauyana (2015). Faktor-faktor seperti rasio amilosa-amilopektin, kadar amilosa, dan kristalinitas pati mempengaruhi sifat swelling power dan kelarutan. Proses lintnerisasi cenderung menurunkan kadar amilosa pati dan meningkatkan derajat kristalinitasnya. Penurunan kadar amilosa meningkatkan kelarutan karena rantai panjang amilosa diputus menjadi amilosa rantai pendek sehingga lebih mudah terlarut. Amilosa rantai pendek memiliki bobot molekul rendah yang lebih mudah larut air sehingga meningkatkan kelarutannya. Hal ini sesuai dengan hasil penelitian sebelumnya oleh Rizkiana (2015) dan Sauyana (2015) yang kadar amilosa pati tapioka (19%) kristalin lebih rendah dibandingkan pati sagu kristalin (25%). Kadar amilosa pati pada sagu nanokristalin (23.89%) memang lebih rendah dibandingkan pati tapioka nanokristalin (34.66%) akan tetapi hal ini dapat terjadi karena proses presipitasi juga dapat menyebabkan kadar amilosa meningkat karena terjadi kompleksasi amilosa dengan pelarut organik yang digunakan sehingga mengendapkan kembali amilosa yang terlarut dalam air, serta amilosa merupakan fraksi pati yang larut air sehingga kemungkinan kelarutan pati tapioka nanokristalin lebih tinggi dibandingkan sagu nanokristalin karena lebih banyak amilosa yang terlarut. Sebagai matriks, nilai kelarutan pati diharapkan rendah, karena nilai kelarutan yang tinggi akan mempercepat matriks larut dalam air sehingga bahan aktif kurkumin yang disalut akan ikut luruh dan hilang sebelum sampai di jaringan pencernaan.
Swelling power didefinisikan sebagai pertambahan volume dan berat maksimum yang dialami pati dalam air (Buleon et al. 1998). Swelling power terjadi pada daerah amorf granula pati. Ikatan hidrogen yang lemah antar molekul pati pada daerah amorf akan terputus saat pemanasan, sehingga terjadi hidrasi air oleh granula pati. Granula pati akan terus mengembang, sehingga viskositas meningkat hingga volume hidrasi maksimum yang dapat dicapai oleh granula pati (Swinkels 1985).
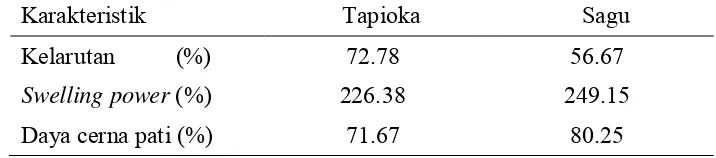
Tabel 2 Karakteristik fungsional Pati Tapioka dan Pati Sagu nanokristalin
Karakteristik Tapioka Sagu
Kelarutan (%) 72.78 56.67
Swelling power (%) 226.38 249.15
9 Swelling atau kapasitas menyerap air pada pati sangat penting dalam aplikasi biomedis atau farmasi, baik sebagai implan maupun sistem penghantaran obat. Hal itu disebabkan tingkat kesetimbangan swelling akan mempengaruhi- koefisien difusi pelarut melewati matriks, sifat permukaan dan mobilitas permukaan, termasuk sifat mekanisnya (Peppas et al. 1996). Proses lintnerisasi berpengaruh terhadap sifat swelling power karena selama proses hidrolisis, asam mendegradasi daerah amorf yang berperan sebagai pengembangan pati. Proses hidrolisis asam akan meningkatkan kelarutan namun menurunkan swelling power (Winarti 2014). Swelling power yang dihasilkan pada tapioka nanokristalin lebih rendah (226.38%) dibandingkan pati sagu nanokristalin (249.15%). Hasil ini bersesuaian dengan hasil kelarutan pati dimana kelarutan pati tapioka memang lebih tinggi dari pada kelarutan pati nano kristalin sehingga swelling power nya rendah. Proses hidrolisis merusak granula dan memecah rantai pati menjadi lebih pendek dan menurunkan bobot molekul pati. Meningkatnya rantai amilosa pendek pati meningkatkan sifat kristalinitas pati karena amilosa teretrogradasi membentuk struktur kristalin yang kokoh dan kompak sehingga air terhambat untuk masuk ke dalam granula pati yang mengakibatkan swelling power menurun (Winarti 2014). Sebagai matriks, diharapkan pati tidak terlalu mudah mengembang karena dengan pengembangan matriks maka struktur akan membuka dan bahan aktif akan cepat terlepas. Di lain pihak sebagai hidrogel, kemampuan membentuk jaringan gel yang akan melapisi permukaan nanokapsul juga diharapkan sehingga akan menghambat keluarnya bahan aktif.
Sifat daya cerna pati dipengaruhi oleh kristalinitas pati. Semakin kristalin maka daya cerna pati semakin menurun disebabkan daerah kristalin memiliki struktur yang rapat dan kompak sehingga akan sulit ditembus oleh enzim pankreatin amilase (Winarti 2014). Proses lintnerisasi dan presipitasi cenderung menurunkan daya cerna pati. Proses hidrolisis menyebabkan meningkatnya jumlah rantai polimer yang berbobot molekul rendah dan molekul amilosa rantai pendek. Bertambahnya jumlah fraksi amilosa rantai pendek akan memudahkan pati mengalami retrogradasi (Sajilata et al. 2006). Adapun pada proses presipitasi terjadi retrogradasi pati yang menyebabkan perubahan struktur amilosa dan amilopektin mengakibatkan terjadi perubahan kristanilitas pati yang berpengaruh terhadap perubahan sifat daya cerna pada pati yang dihasilkan. Daya cerna pati tapioka nanokristalin yang dihasilkan sebesar 71.67% dan lebih rendah dibandingkan daya cerna pati sagu nanokristalin (80.25%). Hasil ini bersesuaian dengan penelitian Wulandari (2013) yang derajat kristalinitas pati tapioka nanokristalin lebih tinggi (63.14%) dibandingkan pati sagu nanokristalin (51.14%). Berdasarkan data tersebut diketahui bahwa pati tapioka lebih tahan cerna dibandingkan pati sagu. Sebagai matriks, diharapkan daya cerna pati rendah terhadap enzim pencernaan. Hal ini diperlukan agar matriks tidak mudah diserang enzim dalam pencernaan sehingga matriks utuh sampai ke organ target yaitu usus kecil (Winarti 2014).
Karakteristik Nanokapsul
10
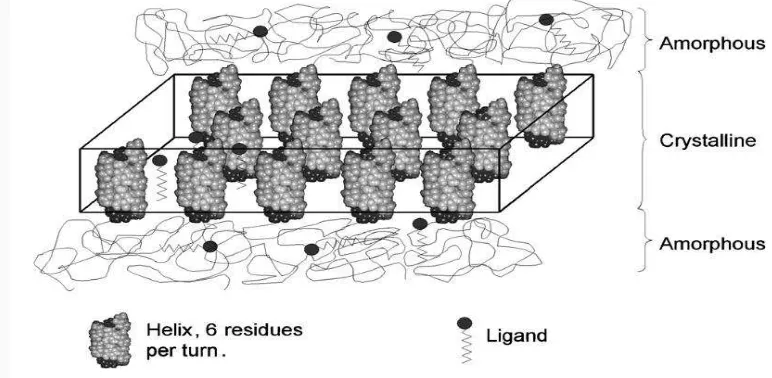
Gambar 3 Representasi skema struktur kompleks amilosa-bahan aktif dan kemungkinan lokasi molekul yang terjerat (Biais et al. 2006) pelindung tertentu yang dapat mengurangi kerusakan senyawa aktif tersebut. Enkapsulasi membantu memisahkan material inti dengan lingkungannya hingga material tersebut terlepas ke lingkungan. Material inti yang dilindungi disebut core dan struktur yang dibentuk oleh bahan pelindung yang menyelimuti inti disebut sebagai dinding membran, matriks, atau kapsul (Kailasapathy 2002). Berdasarkan ukuran partikelnya, produk enkapsulasi dapat dibagi menjadi makrokapsul (ukuran partikel > 5000 m), mikro enkapsulasi (ukuran partikel 1.0-5000 m) dan nano enkapsulasi (ukuran partikel < 1.0 m).
Pengikatan bahan aktif dalam kompleks dengan amilosa dideskripsikan oleh Biais et al. (2006) seperti pada Gambar 3. Digambarkan bahwa pengikatan kompleks asam lemak (aroma) seperti asam dekanoat, asam heksanoat, dan 1,5 dekanolakton dalam struktur kompleks amilosa dapat digunakan untuk menggambarkan pengikatan komponen tersebut dalam aplikasinya di pengolahan pangan. Dari gambar tersebut dapat disimpulkan bahwa bahan aktif akan terikat di dalam atau di luar heliks dalam daerah kristalin maupun daerah amorfous.
11
Emulsifier yang ditambahkan dalam fase air akan menstabilkan emulsi dan memainkan peran penting dalam pembentukan partikel. Karena bahan pengemulsi terdapat di lapisan batas antara fase air dan fase organik selama pembentukan partikel, emulsifier/stabilizer bisa dimasukkan ke dalam matriks polimer nanopartikel pada antar muka atau diserap karena interaksi ionik atau hidrofobik, sehingga memodifikasi sifat nanopartikel antara lain ukuran nanopartikel tersebut, zeta-potential, hidrofilisitas/hidropobisitas, muatan permukaan, adhesi, dll (Feng dan Huang 2001).
Secara umum, mekanisme emulsifikasi nanoenkapsulasi bahan aktif adalah proses mengemulsi bahan aktif yang terlarut dalam pelarut organik (etanol) dalam pelarut non organik (air) yang berisi pengemulsi untuk membentuk emulsi minyak pada air (o/w emulsion). Nanopartikel terbentuk setelah pelarut organik dari emulsi menguap. Bahan aktif bersifat lipofilik dapat dimasukkan ke dalam nanopartikel dengan melarutkannya dalam pelarut organik bersamaan dengan polimer sebelum emulsifikasi.
Berdasarkan penelitian Winarti (2014), nanokapsul ekstrak temulawak yang didapatkan telah berukuran nano yaitu sekitar 100 nm. Sistem nanopartikel disebut ideal bila menghasilkan rendemen yang tinggi, sehingga mengurangi jumlah matriks yang digunakan untuk formulasi. Hasil karakteristik nanokapsul ekstrak temulawak ditunjukkan pada Lampiran 3. Rendemen nanokapsul ekstrak temulawak dengan pati tapioka nanokristalin yang dihasilkan sebesar 32.75 - 37.64%, sedangkan nanokapsul matriks pati sagu nanokristalin yang dihasilkan sebesar 30.02 - 44.13%. Secara keseluruhan rendemen nanokapsul yang dihasilkan terbilang masih kecil. Menurut Hadi (2009), rendahnya rendemen kapsul yang dihasilkan dengan spray dryer disebabkan karena saat proses atomisasi terjadi pemisahan antara minyak dengan penyalut karena suhu yang tinggi. Hal tersebut mengakibatkan terjadi penumpukan cairan emulsi di tabung siklon. Selain itu, sedikitnya rendemen yang dihasilkan terjadi akibat beberapa kesalahan teknis saat penelitian yang seharusnya dapat dihindari. Oleh karena itu, untuk selanjutnya agar diperhatikan kesiapan dan performa alat sebelum dilakukan penelitian agar kesalahan yang tidak perlu tidak terjadi.
Efisiensi Enkapsulasi (EE)
Efisiensi enkapsulasi menunjukkan banyaknya bahan aktif yang terikat dalam matriks dilihat dari jumlah bahan aktif yang ditambahkan sebelum proses enkapsulasi. Tingginya nilai EE yang dihasilkan menunjukkan banyaknya bahan
12
aktif yang terikat dalam matriks, maka semakin tinggi nilai EE yang dihasilkan menunjukkan kemampuan matriks dalam mengenkapsulasi suatu bahan aktif semakin baik. Hasil penelitian menunjukkan EE nanokapsul matriks pati tapioka nanokristalin sebesar 32.89 - 69.95%, dan pada matriks sagu nanokristalin sebesar 33.19 - 58.54% (Gambar 5a). Hasil ini hampir sama dengan penelitian Paramera et al. (2011) yang melakukan enkapsulasi kurkumin dengan pati termodifikasi (OSA) dengan nilai EE 60.4% untuk perlakuan dengan penambahan emulsifier (Tween 80) dan 56.2% untuk perlakuan tanpa emulsifier. Penelitian lain seperti Winarti (2014) menghasilkan nanokapsul dengan EE sebesar 48.69-69.59% menggunakan pati garut nanopartikel. Perbedaan ini dapat disebabkan oleh perbedaan bahan penyalut dan emulsifier yang digunakan, dan perbedaan komposisi matriks dan emulsifier dalam formulasi nanokapsul sehingga mempengaruhi perbedaan dalam nilai EE tersebut. Selain itu, perbedaan nilai EE juga disebabkan perbedaan penggunaan bahan aktif. Pada penelitian ini, bahan aktif yang digunakan merupakan ekstrak temulawak kasar, sementara Paramera et al.. (2011) menggunakan kurkumin murni. Proses spray drying untuk pembentukan serbuk nanokapsul dimana bahan dikenakan suhu tinggi selama proses enkapsulasi juga mempengaruhi persentase EE.
Dari Gambar 5a ditunjukkan nilai EE matriks tapioka nanokristalin cenderung naik dengan meningkatnya konsentrasi maltodekstrin yang ditambahkan (penurunan konsentrasi pati nanokristalin dalam matriks). Nilai EE juga mengalami kenaikan dengan meningkatnya konsentrasi ekstrak temulawak yang ditambahkan, kecuali pada rasio pati : maltodekstrin 50:50 EE dengan konsentrasi ekstrak 5% lebih tinggi dibandingkan 10%. Pada nanokapsul matriks sagu nanokristalin, nilai EE pada konsentrasi ekstrak temulawak 5% terus meningkat dengan meningkatnya konsentrasi maltodekstrin yang ditambahkan, namun hal yang berbeda terjadi pada nilai EE pada konsentrasi ekstrak 10% yang cenderung menurun dengan meningkatnya konsentrasi maltodekstrin yang ditambahkan (Gambar 5b).
Hasil analisis keragaman (Lampiran 4) menunjukkan bahwa rasio pati tapioka nanokristalin dan maltodekstrin yang ditambahkan dan interaksi faktor rasio pati : maltodekstrin dan konsentrasi ekstrak temulawak berpengaruh nyata terhadap efisiensi enkapsulasi nanokapsul. Dari hasil uji lanjut Duncan ditunjukkan bahwa rasio terbaik dilihat dari rata-rata tertinggi adalah 25% pati nanokristalin dan 75% maltodekstrin. Pada Gambar 5a ditunjukkan nilai EE pada rasio 25 : 75 yang dihasilkan lebih tinggi dibandingkan dengan dua rasio polimer lainnya. Mirjazani et al. (2010) dan Rafati et al. (1997) menyatakan bahwa peningkatan konsentrasi stabiliser/ emulsifier dalam matriks meningkatkan nilai efisiensi enkapulasi dan drug loading capacity. Hal ini bersesuaian dengan hasil yang diperoleh dalam penelitian yang juga menunjukkan polimer dengan konsentrasi emulsifier tertinggi menghasilkan nilai EE yang lebih tinggi dibandingkan dua konsentrasi yang lain.
13 Zambaux et al. (1998) juga menyatakan hal yang sama dalam penelitiannya yang menunjukkan bahwa terjadi penurunan ukuran partikel dari 530 nm menjadi 380 nm dengan peningkatan konsentrasi PVA (emulsifier) dari 0.5% hingga 5% (b/v), dan penurunan polydispersity index sehingga menghasilkan ukuran partikel yang lebih seragam. Interaksi antara rasio pati : maltodekstrin dan konsentrasi ekstrak temulawak juga memberi pengaruh signifikan terhadap efisiensi nanokapsul tapioka. Berdasarkan hal tersebut dapat disimpulkan bahwa sebenarnya kedua faktor berpengaruh signifikan terhadap efisiensi nanokapsul ekstrak temulawak. Hasil uji Duncan menunjukkan nilai EE tertinggi dihasilkan oleh kombinasi rasio pati : maltodekstrin 25 : 75 (% b/b) dan konsentrasi ekstrak temulawak 10%. Pada formulasi tersebut, Nilai EE yang didapatkan sebesar 69.78 ± 1.13 %.
Gambar 5b menunjukkan bahwa efisiensi nanokapsul sagu nanokristalin dengan konsentrasi ekstrak temulawak 5% lebih tinggi dibandingkan dengan konsentrasi ekstrak 10%. Penurunan nilai EE yang cukup tinggi terjadi saat konsentrasi ekstrak temulawak yang dienkapsulasi dinaikkan menjadi 10%. Hasil ini dibuktikan dengan hasil analisis keragaman nanokapsul matriks sagu nanokristalin (Lampiran 5) yang menunjukkan bahwa faktor konsentrasi ekstrak temulawak yang ditambahkan berpengaruh nyata terhadap efisiensi enkapsulasi nanokapsul. Interaksi faktor rasio pati : maltodekstrin dengan konsentrasi ekstrak temulawak juga berpengaruh nyata terhadap efisiensi enkapsulasi nanokapsul pati sagu nanokristalin. Peningkatan konsentrasi ekstrak pada enkapsulasi selanjutnya akan memungkinkan terjadinya penurunan efisiensi enkapsulasi matriks. Penurunan nilai EE ini diduga disebabkan matriks hanya mampu mengikat bahan aktif ekstrak temulawak pada konsentrasi di bawah 10%. Lamprecht et al. (2000) menyatakan bahwa peningkatan jumlah bahan aktif (obat) membentuk sruktur polimer matriks yang lebih porous; di dalam inti polimer terdapat saluran besar dan lubang yang dapat diisi oleh obat dimana obat dapat dengan mudah keluar dari matriks. Selain itu, karena konsentrasi obat meningkat dalam nanopartikel, perbedaan tekanan osmotik antara fase luar dan dalam berubah, yang menyebabkan beberapa kerusakan sehingga terbentuk droplet kuasi-emulsi yang memudahkan obat keluar dari fase dalam matriks. Berdasarkan hasil uji lanjut Duncan, rata-rata efisiensi enkapsulasi nanokapsul tertinggi dihasilkan dari penambahan ekstrak temulawak 5%.
Interaksi antara rasio pati : maltodekstrin dan konsentrasi ekstrak temulawak juga memberi pengaruh signifikan terhadap efisiensi nanokapsul sagu nanokristalin. Berdasarkan hal tersebut dapat disimpulkan bahwa kedua faktor berpengaruh signifikan terhadap efisiensi nanokapsul ekstrak temulawak. Hasil uji Duncan menunjukkan nilai EE tertinggi dihasilkan oleh kombinasi konsentrasi ekstrak 5% dan rasio pati : maltodekstrin 25 : 75 (% b/b). Pada formulasi tersebut, Nilai EE yang didapatkan sebesar 58.54 ± 0.18 %.
Drug Loading (DL)
14
dihasilkan relatif cukup rendah, dibandingkan dengan penelitian Paramera et al. (2011) sebesar 2.8-2.9%.
Gambar 5 Efisiensi enkapsulasi nanokapsul (a) tapioka, (b) sagu nanokristalin berdasarkan faktor yang mempengaruhi pada berbagai perlakuan
Ket : Pati NK = Pati Nanokristalin; MD = Maltodekstrin
Gambar 6 Drug loading nanokapsul (a) tapioka (b) sagu nanokristalin berdasarkan faktor yang mempengaruhi pada berbagai perlakuan
Ket : Pati NK = Pati Nanokristalin; MD = Maltodekstrin
15 Gambar 6a menunjukkan bahwa nilai DL pada nanokapsul matriks tapioka nanokristalin meningkat ketika konsentrasi ekstrak juga dinaikkan dari 5% ke 10%. Selain itu, nilai DL cenderung turun pada tiap-tiap konsentrasi ekstrak temulawak ketika konsentrasi pati nanokristalin ditingkatkan, kecuali pada konsentrasi ekstrak 5%, DL pada rasio pati : maltodekstrin 50 : 50 (% b/b) lebih tinggi dibandingkan oleh dibandingkan 25 : 75 maupun 75 : 25 (% b/b). Hasil analisis keragaman (Lampiran 4) menunjukkan bahwa konsentrasi ekstrak temulawak, dan interaksi faktor rasio pati : maltodekstrin dan konsentrasi ekstrak temulawak berpengaruh signifikan terhadap drug loading nanokapsul. Hasil lanjut uji Duncan menunjukkan bahwa penambahan ekstrak temulawak 5% memberikan nilai drug loading yang lebih rendah dibandingkan dengan penambahan ekstrak temulawak 10%. Hasil ini mengikuti tren yang sama dengan penelitian Lin et al. (2009) yang menunjukkan semakin banyak kurkumin terenkapsulasi dengan meningkatnya konsentrasi kurkumin yang ditambahkan. Penambahan ekstrak temulawak 10% memberikan hasil drug loading yang terbaik.
Interaksi antara matriks yang digunakan dan konsentrasi ekstrak yang ditambahkan memberi pengaruh signifikan terhadap hasil drug loading pada matriks tapioka nanokristalin. Berdasarkan hal tersebut dapat disimpulkan bahwa kedua faktor berpengaruh signifikan terhadap drug loading ekstrak temulawak. Hasil pengelompokan dari uji lanjut Duncan menunjukkan bahwa kombinasi konsentrasi ekstrak temulawak 10% dan penambahan matriks dengan rasio pati nanokristalin : maltodekstrin 25 : 75 (% b/b) menghasilkan nilai rata-rata tertinggi. Hasil ini bersesuaian dengan data yang didapatkan karena nilai drug loading cenderung meningkat ketika persentase konsentrasi pati nanokristalin yang digunakan menurun (konsentrasi maltodekstrin meningkat). Pada formulasi tersebut, nilai DL yang didapatkan sebesar 0.24 ± 0.02%.
Hasil DL nanokapsul dengan matriks sagu nanokristalin ditunjukkan pada Gambar 6b. Pada grafik tersebut ditunjukkan bahwa nilai DL cenderung meningkat dengan meningkatnya konsentrasi ekstrak temulawak yang digunakan dari 5% ke 10% pada masing-masing persentase konsentrasi matriks yang digunakan. Nilai DL juga cenderung meningkat dengan meningkatnya konsentrasi pati sagu nanokristalin terhadap maltodekstrin yang digunakan sebagai matriks. Hasil tersebut sesuai, dibuktikan dengan hasil dari analisis keragaman (Lampiran 5) yang menunjukkan bahwa faktor konsentrasi ekstrak temulawak dan faktor rasio pati : maltodekstrin berpengaruh nyata terhadap drug loading nanokapsul. Hasil uji lanjut Duncan menunjukkan DL tertinggi dihasilkan pada konsentrasi ekstrak temulawak 10% dibandingkan pada konsentrasi 5%. Hasil ini mengikuti tren yang sama dengan penelitian Lin et al. (2009) yang menunjukkan semakin banyak kurkumin terenkapsulasi dengan meningkatnya konsentrasi kurkumin yang ditambahkan. Adapun pada konsentrasi rasio pati nanokristalin : maltodekstrin yang digunakan, berdasarkan hasil uji lanjut Duncan didapatkan bahwa matriks dengan rasio 75% pati sagu nanokristalin dan 25% maltodekstrin menghasilkan DL dengan nilai rata-rata tertinggi. Pada formulasi rasio pati sagu naokristalin : maltodekstrin 75 : 25 dan konsentrasi ekstrak temulawak 10% nilai DL yang didapatkan sebesar 0.28 ± 0.01%.
16
enkapsulasi dan 10% pada parameter drug loading. Hal ini mungkin terjadi disebabkan perbedaan pendekatan perhitungan masing-masing parameter. Pada efisiensi enkapsulasi, jumlah ekstrak temulawak terhitung merupakan ekstrak temulawak yang hanya terikat di bagian dalam matriks (ekstrak temulawak yang terikat pada bagian permukaan matriks tidak dihitung). Adapun pada drug loading, jumlah ekstrak temulawak terhitung merupakan ekstrak temulawak yang terdapat pada bagian dalam dan permukaan matriks (total bahan aktif yang teradsorbsi matriks). Selain itu, penghitungan drug loading didasarkan pada bobot nanokapsul, sedangkan pada efisiensi enkapsulasi bobot nanokapsul tidak mempengaruhi hasilnya. Oleh karena itu, semakin tinggi konsentrasi ekstrak yang digunakan maka akan semakin banyak bahan aktif yang dimuat pada matriks, akan tetapi belum tentu terikat seluruhnya dalam matriks.
Aktivitas Antioksidan
Antioksidan merupakan senyawa yang dapat menghambat reaksi oksidasi atau suatu zat yang dapat menetralkan radikal bebas, yang terbentuk sebagai hasil dari metabolisme oksidatif yaitu hasil dari reaksi-reaksi kimia dan proses metabolik yang terjadi dalam tubuh. Senyawa antioksidan dapat berfungsi sebagai penangkap radikal bebas, pembentuk kompleks dengan logam-logam prooksidan dan berfungsi sebagai senyawa pereduksi (Andlauer et al. 1998). Antioksidan dapat menangkap radikal bebas sehingga menghambat mekanisme oksidatif yang merupakan penyebab penyakit-penyakit degeneratif seperti penyakit jantung, kanker, penurunan fungsi otak dll.
Pengukuran aktivitas antioksidan umumnya dilakukan untuk mengevaluasi adanya aktivitas penghambatan proses oksidasi oleh senyawa antioksidan yang terdapat dalam bahan pangan atau ekstrak bahan alam. Pengukuran aktivitas antioksidan diperlukan untuk mengetahui kualitas antioksidan dan ketahanan produk selama proses pengolahan dan penyimpanan, serta implikasinya ke jaringan tubuh. Dari beberapa metode yang dapat digunakan untuk mengukur aktivitas antioksidan, pada penelitian ini digunakan metode uji DPPH untuk pengukuran aktivitas tersebut.
17
Gambar 7 Struktur kimia radikal bebas (1) dan non radikal DPPH (2) (Molyneux 2004)
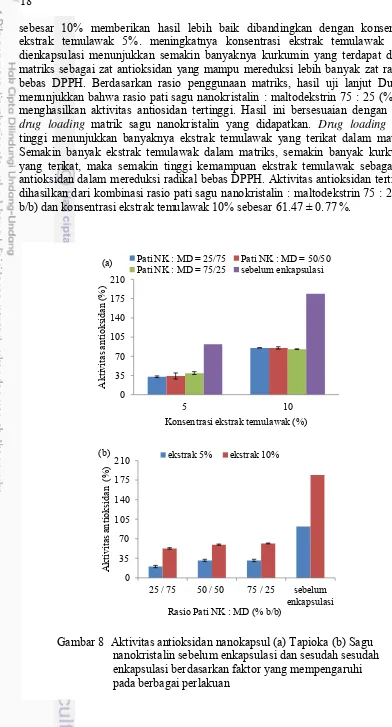
Aktivitas antioksidan yang direpresentasikan pada penelitian ini merupakan nilai persen inhibisi atau jumlah radikal bebas DPPH yang mampu diredam oleh ekstrak temulawak. Hasil penelitian (Gambar 8a) menunjukkan aktivitas antioksidan yang dihasilkan oleh nanokapsul matriks tapioka nanokristalin sebesar 32.76-85.25%. Hasil analisis keragaman (Lampiran 4) menunjukkan bahwa konsentrasi ekstrak temulawak dan faktor interaksi rasio pati nanokristalin : maltodekstrin dan konsentrasi ekstrak temulawak memberi pengaruh yang signifikan terhadap aktivitas antioksidan. Pada Gambar 8a ditunjukkan aktivitas antioksidan nanokapsul meningkat seiring dengan dinaikkannya konsentrasi ekstrak temulawak yang ditambahkan. Aktivitas antioksidan meningkat dari 32.76-32.96% hingga 85.25% saat konsentrasi ekstrak 5% dinaikkan menjadi 10%. Hasil uji lanjut Duncan membuktikan bahwa aktivitas antioksidan terbaik memang dihasilkan oleh nanokapsul dengan penambahan ekstrak temulawak 10%. Meningkatnya konsentrasi ekstrak temulawak yang ditambahkan menyebabkan semakin banyak bahan aktif kurkumin yang dapat terenkapsulasi, sehingga semakin banyak senyawa DPPH yang mampu direduksi. Hasil ini didukung oleh penelitian Lee et al. (2009) yang menyatakan bahwa semakin banyak kurkumin yang terenkapsulasi dengan semakin meningkatnya konsentrasi kurkumin yang ditambahkan. Interaksi antara rasio pati : maltodekstrin dan konsentrasi ekstrak temulawak juga memberi pengaruh signifikan terhadap efisiensi nanokapsul sagu nanokristalin. Berdasarkan hal tersebut dapat disimpulkan bahwa kedua faktor berpengaruh signifikan terhadap efisiensi nanokapsul ekstrak temulawak. Hasil uji Duncan menunjukkan nilai EE tertinggi dihasilkan oleh kombinasi konsentrasi ekstrak 10% dan rasio pati : maltodekstrin 25 : 75 (% b/b). Pada formulasi tersebut, aktivitas antioksidan yang didapatkan sebesar 85.25 ± 0.11 %.
18
Gambar 8 Aktivitas antioksidan nanokapsul (a) Tapioka (b) Sagu nanokristalin sebelum enkapsulasi dan sesudah sesudah enkapsulasi berdasarkan faktor yang mempengaruhi pada berbagai perlakuan
Ket. Pati NK : pati nanokristalin; MD : maltodekstrin
Pati NK : MD = 75/25 sebelum enkapsulasi (a)
19 Berdasarkan hasil yang didapatkan dari tiap karakteristik nanokapsul yang diujikan, dapat disimpulkan bahwa formulasi nanokapsul yang memberikan hasil terbaik pada matriks tapioka nanokristalin adalah rasio pati nanokristalin : maltodekstrin 25 : 75 (% b/b) dan konsentrasi ekstrak temulawak 10%, sedangkan pada matriks sagu nanokristalin adalah kombinasi rasio pati sagu nanokristalin : maltodekstrin 75 : 25 (% b/b) dan konsentrasi ekstrak temulawak 10%. Hasil tersebut menunjukkan bahwa pada matriks tapioka nanokristalin, maltodekstrin dengan konsentrasi yang lebih tinggi dari pati nanokristalin lebih berpengaruh terhadap karakteristik nanokapsul, sedangkan pada nanokapsul matriks sagu nanokristalin, konsentrasi tinggi pati sagu nanokristalin lebih berpengaruh terhadap karakteristik nanokapsul daripada maltodekstrin. Pada nanokapsul matriks tapioka nanokristalin, diduga karena penggunaan maltodekstrin yang tinggi dapat meningkatkan stabilitas emulsi. Hal ini karena maltodekstrin dapat meningkatkan viskositas emulsi. Semakin tinggi konsentrasi ekstrak maka semakin banyak maltodekstrin/emulsifier yang dibutuhkan untuk menjaga kestabilan emulsi (Nussinovitch 1997). Sebagai hidrokoloid, maltodekstrin akan meningkatkan viskositas fase air, sehingga menurunkan pergerakan droplet droplet minyak. Struktur morfologi pati juga akan mempengaruhi karakteristik kemampuannya dalam pengikatan bahan aktif. Morfologi partikel tapioka nanokristalin menunjukkan struktur yang lebih berpori (porous) dan longgar dibandingkan dengan morfologi pati sagu nanokristalin yang lebih rapat dan tidak berpori (Wulandari 2013). Morfologi tapioka nanokristalin yang lebih berpori dan longgar tersebut kemungkinan menyebabkan konsentrasi maltodekstrin yang dibutuhkan lebih tinggi untuk mengisi lubang-lubang kosong pada tapioka nanokristalin tersebut agar matriks yang dihasilkan lebih stabil dan kompak sehingga tidak mengakibatkan kebocoran yang membuat bahan aktif keluar dari matriks. Hal sebaliknya terjadi pada pati sagu nanokristalin. Morfologinya yang lebih rapat dan cenderung tidak berpori menyebabkan maltodekstrin sebagai bahan penstabil yang dibutuhkan hanya sedikit.
Menurut Waigh et al. (2000) nanokapsul dengan tingkat kristalinitas yang lebih tinggi akan menahan obat lebih lama dibandingkan polimer yang amorf. Hal ini disebabkan polimer yang amorf akan memudahkan air untuk masuk. Dari hasil penelitian diketahui efisiensi enkapsulasi dan aktivitas antioksidan nanokapsul matriks tapioka nanokristalin (Lampiran 3) yang memilki kristalinitas (63.14%) dan kadar amilosa lebih tinggi (34.66%) dibandingkan sagu nanokristalin (51.14% dan 23.89%) ternyata menghasilkan EE lebih tinggi dibandingkan nanokapsul matriks sagu nanokristalin. Hasil tersebut juga bersesuaian dengan hasil penelitian Winarti (2014), yang menyebutkan bahwa matriks dengan kadar amilosa tinggi kinerja matriks tersebut lebih baik terutama dalam kemampuan pengikatan (efisiensi enkapsulasi). Struktur linear dari amilosa memicu terbentuknya struktur rantai yang tersusun rapat (teretrogradasi) sehingga bahan aktif akan tertahan dalam matriks tinggi amilosa (Wing et al. 1988).
Stabilitas Aktivitas Antioksidan
20
Struktur kimia kurkumin dan demetoksikurkumin dapat dilihat pada Gambar 8. Menurut Rismunandar (1988), rimpang temulawak mengandung kurkumin 1.4-4 %.
Pemanfaatan kurkumin yang luas sebagai antioksidan terkendala sifatnya yang kelarutannya sangat rendah dalam air dan bioavailabilitasnya yang rendah dalam jaringan pencernaan, serta sensitivitasnya yang tinggi terhadap pH, suhu dan cahaya. Proses nanoenkapsulasi yang dilakukan akan melindungi kurkumin dari pengaruh faktor luar yang dapat merusak kurkumin sehingga kehilangan manfaatnya serta meningkatkan kelarutan dan bioavailabilitasnya dalam darah. Pengujian aktivitas antioksidan dilakukan untuk melihat stabilitas aktivitas antioksidan kurkumin dalam ekstrak temulawak sebelum dan sesudah dilakukan enkapsulasi.
Aktivitas antioksidan ekstrak temulawak pada kedua konsentrasi (5% dan 10%) sebelum dienkapsulasi menunjukkan angka yang tinggi diatas 50% (Gambar 8a dan 8b). Akan tetapi setelah proses enkapsulasi, terjadi penurunan aktivitas antioksidan yang cukup tinggi pada konsentrasi ekstrak temulawak 5% dan 10% pada masing-masing matriks pati nanokristalin yang digunakan. Aktivitas antioksidan dari konsentrasi ekstrak temulawak 5% sebelum enkapsulasi (91.85%) turun hingga sekitar 20%-39%, sedangkan pada konsentrasi ekstrak temulawak 10% (183.70%) turun hingga 52-85% pada matriks tapioka dan sagu nanokristalin setelah dienkapsulasi.
Hasil yang didapatkan sesuai dengan penelitian Wang et al. (2009). Pada penelitian Wang et al. (2009), kadar kurkumin yang didapatkan setelah enkapsulasi, penurunan kadar kurkumin yang terjadi sangat sedikit atau cenderung stabil walaupun diberikan perlakuan panas dengan suhu tinggi (80-100 oC) dan waktu pemanasan yang lama (10-50 menit). Proses enkapsulasi akan meningkatkan ketahanan bahan aktif terhadap panas (Paramera et al. 2011). Cairan atau bahan aktif yang dienkapsulasi akan terlindung dari pengaruh lingkungan yang merugikan seperti kerusakan-kerusakan akibat oksidasi, hidrolisis, penguapan atau degradasi panas, sehingga bahan aktif akan mempunyai masa simpan yang lebih panjang serta mempunyai kestabilan proses yang lebih baik. Selain itu, pelepasan bahan aktif dari dalam kapsul juga dapat dikendalikan sehingga efektifitasnya dapat dirancang sesuai dengan keinginan (Yuliani et al. 2007).
21 Penurunan aktivitas antioksidan yang terjadi setelah enkapsulasi diduga disebabkan oleh banyaknya ekstrak temulawak yang hilang akibat suhu tinggi yang dikenakan pada bahan saat proses pembentukan serbuk pada saat spray drying. Penggunaan suhu inlet yang tinggi menyebabkan viskositas dan ukuran partikel menurun akan tetapi dapat menyebabkan penguapan atau degradasi dari bahan aktif yang sensitif terhadap panas (Wang et al. 2009). Hasil analisis statistik (Lampiran 6) menunjukkan bahwa aktivitas antioksidan pada konsentrasi ekstrak 5% berbeda nyata dengan aktivitas antioksidan pada konsentrasi ekstrak 10%. Penambahan konsentrasi ekstrak temulawak 10% meningkatkan aktivitas antioksidan secara signifikan pada nanokapsul, baik pada matriks tapioka nanokristalin maupun matriks sagu nanokristalin. Hasil ini sesuai dengan penelitian Wang et al. (2009), yang melakukan mikroenkapsulasi kurkumin dengan proses spray drying sedikitnya menggunakan konsentrasi kurkumin 10% untuk menghasilkan efisiensi enkapsulasi diatas 50% pada rentang suhu inlet 180 - 200 oC.
SIMPULAN DAN SARAN
Simpulan
Konsentrasi ekstrak temulawak yang ditambahkan dan rasio pati nanokristalin dan maltodekstrin yang digunakan berpengaruh terhadap karakteristik nanokapsul. Kondisi proses terbaik pada matriks tapioka nanokristalin adalah penggunaan rasio pati tapioka nanokristalin : maltodekstrin 25 : 75 (% b/b) dan konsentrasi ekstrak temulawak 10%, sedangkan pada matriks sagu nanokristalin adalah konsentrasi pati sagu nanokristalin : maltodekstrin 75 : 25 (% b/b) dan konsentrasi ekstrak temulawak 10%. Aktivitas antioksidan ekstrak temulawak pada konsentrasi 5% dan 10% menurun setelah dilakukan enkapsulasi. Penurunan aktivitas antioksidan disebabkan penggunaan suhu inlet yang tinggi pada proses spray drying, mengakibatkan lebih banyak ekstrak temulawak yang menguap dibandingkan yang tertinggal dalam kapsul sehingga aktivitas antioksidan kapsul rendah setelah dilakukan enkapsulasi. Perlakuan spray drying dapat menurunkan aktivitas antioksidan ekstrak temulawak setelah dienkapsulasi dibandingkan sebelum enkapsulasi, akan tetapi setelah dienkapsulasi ketahanan bahan aktif akan meningkat terhadap panas dan akan terlindungi dari pengaruh faktor luar yang dapat merusak bahan aktif.
Saran
Berdasarkan penelitian yang dilakukan dapat disarankan beberapa hal antara lain:
22
2 Perlu dilakukan optimasi terhadap konsentrasi ekstrak temulawak untuk mengetahui konsentrasi ekstrak optimum yang dapat dienkapsulasi dalam matriks.
DAFTAR PUSTAKA
Anderson AK, Guraya HS, James C, Salvaggio L. 2002. Digestibility and pasting properties of rice starch heat-moisture treated at the melting temperature (tm). Starch. 54:401–409.
Andlauer W, Furst P. 1998. Antioxidative power of photochemicals with special reference to cereals. Cereal Foods World. 43(5):356-359.
Barros FARD, Stringheta PC. 2006. Microencapsulamento de antocianinas – uma alternativa para o aumento de sua aplicabilidade como ingrediente alimentício. Biotecnologia Ciência e Desenvolvimento. 36 :18-24.
Basalmah RS. 2006. Optimalisasi kondisi ekstraksi kurkuminoid temulawak: waktu, suhu, dan nisbah. [skripsi]. Bogor (ID): Institut Pertanian Bogor.
Biais B, Le Bail P, Robert P, Pontoire B, Buleon A. 2006. Stuructural and stoichiometric studies of complexes between aroma compounds and amylase. Polymorphic transitions and quantification in amorphous and crystalline areas. J Carbohydr Polym. 66:306-315 .doi:10.1016/j.carb.pol.2006.03.019.
Buleon A, Colonna P, Planchot V, Ball S. 1998. Starch granules: structure and biosynthesis. Int J Biol Macromol. 23:85-112.
Dhillon N, Anggarwal BB, Newman RA, Wolff RA, Kunnumakkara AB, Abbruzzese JL, Ng CS, Badmaev V, Kurzrock R. 2008. Phase II clinical trial of curcumin in patients with advanced pancreatic cancer. J Clinic Oncol. 24(18):141–151 .doi:10.1158/1078-0432.CCR-08-0024.
Djamil R, Anelia T. 2009. Penapisan fitokimia, uji BSLT, dan uji antioksidan ekstrak metanol beberapa spesies Papilionaceae. J Ilmu Kefarmasian Indonesia. 7(2): 65-71.
Feng S, Huang G. 2001. Effects of emulsifier on the controlled release of paclitaxel (Taxol) from nanospheres of biodegradable polymers. J Contr Release. 71:53-69.
Garcia AM, Borrelli LA, Rozkalne A, Hyman BT, Bacskai BJ. 2007. Curcumin labels amyloid pathology in vivo, disrupts existing plaques, and partially restores distorted neurites in an Alzheimer mouse model. J Neurochem. 102: 1095–1104 . doi: 10.1111/j.1471-4159.2007.04613.x.
Gallant D, Bouchet B, Baldwin P. 1997. Microscopy of starch: evidence of a new level of granule organization. J Carbohydr Polym. 60:379-389.
Griffin VK, Brooks JR. 1989. Production and size distribution of rice maltodextrin hydrolized from milled rice flour using heat stable alpha amylase. J Food Science. 54: 190-193.
23 Hadi S. 2009. Kajian optimasi produksi mikroenkapsulat minyak sawit merah.
[skripsi]. Bogor (ID): Institut Pertanian Bogor.
Herdini, Darusman LK, Sugita P. 2010. Disolusi mikroenkapsulasi kurkumin tersalut gel kitosan-alginat-glutaraldehida. J Makara Sains. 14(1):57-62.
Kailasapathy K. 2002. Microencapsulation of probic bacteria: technology and potential applications. Curr Issues Intest Microbiol. 3:39-48.
Lamprecht A, Ubrich N, Hombreiro PM, Lehr CM, Hoffman M, Maincent P. 2000. Influences of process parameters on nanoparticle preparation performed by a double emission pressure homogenization technique. Int J Pharm. lactide-co-glycolide) nanoparticles containing tamoxifen citrate. Iranian Polym J. 19(6):437-446.
Molyneux P. 2004. The use of the stable free radical diphenylpicrylhydrazyl (DPPH) for estimating antioxidant activity. Songklanakarin J Sci Technol. 26(2) : 211-219.
Nussinovitch A. 1997. Hydrocolloid applications : gum technology in the food and other industries. London (UK): Blackie Academic & Professional.
Paramera EI, Konteles SJ, Karathanos VT. 2011. Stability and release properties of curcumin encapsulated in Saccharomyces cerevisiae, ß-cyclodextrin, and
modified starch. J Food Chem. 125:913-922 .
Peppas NA, Vakkalanka S, Brazel CS, Luttrell AS, Mongia NK. 1996. Controlled release system using swellable random and block copolymers and terpolymers. Di alam Ogata N, Kim SW, Feijen J, Okano T. Editor. Advance Biomaterials in Biomedical Engineering and Drug Delivery System, Springer. hlm 3-6.
Perez LAB, Acevedo EA, Hernandez LS, Lopez OP. 1999. Isolation and partial characterization of banana starch. J Agric Food Chem 47:854-857.
Pomeranz Y. 1991. Functional Properties of Food Components. Second Edition. New York (US): Academic Pr.
Rafati H, Coombes AGA, Adler J, Holland J, Davis SS. 1997. Protein-loaded poly(dl-lactide-co-glycolide) microparticles for oral administration: formulation, structural and release characteristics. J Contr Release. 43:89-102. Rismunandar. 1988. Rempah-rempah komoditi ekspor Indonesia. Bandung: Sinar
Baru
Rizkiana W. 2015. Produksi pati tapioka nanokristalin terasetilasi. [skripsi]. Bogor (ID): Institut Pertanian Bogor.
Sajilata MG, Rekha SS, Puspha RK. 2006. Resistant starch –a review. J Compr Rev in Food Sci Food Safety. 5:1-17.
Sidik, Moelyono MW, Muhtadi A. 1995. Temulawak (Curcuma xanthorriza). Yayasan Pengembangan Obat Bahan Alam Phyto Medica. 200 hlm.
24
Shoskes D, Lapierre C, Cruz-Correa M, Muruve N, Rosario R, Fromkin B, Braun M, Copley J. 2005. Beneficial effects of the bioflavonoids curcumin and quercetin on early function incadaveric renal transplantation: a randomized placebo controlled trial. Transplantation. 80: 1556-1559.
Srichuwong S, Sunarti TC, Mishima T, Isono N, Hisamatsu M. 2005. Starches from different botanical sources I: contribution of amylopectin fine structure to thermal properties and enzyme digestibility. J Carbohydr Polym. 60:529-538. Srihari E, Lingganingrum FS, Hervita R, Wijaya H. 2010. Pengaruh penambahan
maltodekstrin pada pembuatan santan kelapa bubuk. Seminar Rekayasa Kimia dan Proses. ISSN : 1411- 4216. Universitas Diponegoro Semarang.
Swinkles JJM. 1985. Sources of starch, its chemistry and physics. Roels JA, Beynum GMAV, editor. New York (US): Marcel Dekker.
Wang Y, Lu Z, Lv F, Bie X. 2009. Study on microencapsulation of curcumin pigments by spray drying. Eur Food Res Technol. 229:391-396.
Waigh TA, Kato IS, Gidley MJ, Clarck CJ, Riekel C. 2000. Side chain liquid crystalline model for starch. Starch. 52:450-460.
Winarti C. 2014. Produksi pati garut nanopartikel sebagai matriks enkapsulasi bahan bioaktif herbal. [disertasi]. Bogor (ID) : Institut Pertanian Bogor.
Wing RE, Maiti S, Doane MW. 1988. Amylose content of starch controls the release of encapsulated bioactive agents. J Contr Release. 7:33-37.
Wulandari K. 2013. Penyiapan dan karakterisasi pati nanokristalin dari sagu dan tapioka. [skripsi]. Bogor (ID) : Institut Pertanian Bogor.
Yuliani S, Desmawarni, Harimurti N. 2007. Pengaruh laju alir umpan dan suhu inlet spray drying pada karakteristik mikrokapsul oleoresin jahe. J Pascapanen. 4(1):18-26.
25 Lampiran 1 Karakterisasi Pati Nanokristalin
1 Kelarutan dan Swelling Power ( Modifikasi metode Perez et al. 1999) Disiapkan suspensi pati yaitu 0.5 g sampel dilarutkan dengan 50 ml aquades dalam labu Erlenmeyer 100 ml. Sampel ditempatkan pada penangas air pada suhu 70 oC selama 2 jam dengan pengadukan secara kontinyu. Dari suspensi tersebut diambil 30 ml larutan yang jernih kemudian diletakkan pada cawan petri yang telah diketahui bobotnya. Cawan petri dikeringkan pada oven 100 oC hingga bobotnya tetap, kemudian ditimbang dan dihitung kenaikan bobotnya.
elarutan = 0.5 g 0 ml a 50ml 00
ll = o ot sampel ( 00(d c) kelarutan) 00
Keterangan :
a = bobot cawan petri awal (g) b = bobot cawan petri akhir (g) c = bobot erlenmeyer awal (g) d = bobot erlenmeyer akhir (g)
2 Daya Cerna Pati in Vitro (Modifikasi metode Anderson et al. 2002)
Daya cerna pati in vitro dianalisa dengan spektrofotometer yang mencakup tahapan pembuatan kurva standar maltosa dan analisa sampel sabagai berikut. - Pembuatan kurva standar larutan maltosa
Sebanyak 1 ml larutan maltosa standar yang mengandung 100, 150, 200, 250, 300, 350 dan 400 mg/L maltosa dimasukkan ke dalam tabung reaksi bertutup kemudian ditambahkan masing-masing 3 ml larutan dinitrosalisilat (DNS). Larutan dipanaskan dalam air mendidih selama 5 menit kemudian diukur absorbansinya dengan spektrofotometer UV-Vis pada panjang gelombang 550 nm. - Analisa sampel
26
dengan spektrofotometer UV-vis pada panjang gelombang 550 nm. Daya cerna pati dihitung sebagai berikut.
Da a cerna pati = a 00
Keterangan:
A = maltosa dalam sampel (mg) a = maltosa dalam blanko (mg) B = maltosa dalam pati murni (mg)
b = maltosa dalam blanko pati murni (mg)
y = 0.0038x - 0.4487 R² = 0.9939
0 0.2 0.4 0.6 0.8 1 1.2
0 100 200 300 400 500
ab
so
rb
an
si
konsentrasi (ppm)
27
Lampiran 2 Penentuan kinerja nanokapsul
1 Efisiensi Enkapsulasi dan Drug Loading (Modifikasi Herdini et al. 2010) Sebanyak 50 mg nanokapsul temulawak digerus, kemudian dilarutkan dalam 25 ml etanol p.a dan disonifikasi selama 15 menit. Hasil sonifikasi disaring, dan larutan filtrat dihitung absorbansinya untuk menentukan kadar kurkumin dalam nanokapsul dengan spektrofotometer UV-vis pada panjang gelombang 430 nm. Perhitungan efisiensi enkapsulasi (EE) dihitung berdasarkan selisih antara jumlah kurkumin awal dalam nanokapsul dengan jumlah kurkumin dalam filtrat terhadap jumlah kurkumin awal, sementara drug loading (DL), dihitung dengan membagi jumlah kurkumin total dalam nanokapsul terhadap berat nanokapsul. Adapun rumus EE dan DL adalah sebagai berikut :
= jumlah kurkumin total jumlah kurkumin dalam iltratjumlah kurkumin total 00
D = jumlah kurkumin total erat nanokapsul 00
2 Uji Aktivitas Antioksidan (Molyneux 2004; Djamil dan Anelia 2009) a Pembuatan larutan DPPH (1.1-diphenyl-2-pycryl hydrazil) ( 00 M)
Zat radikal bebas DPPH (BM 394.33 g/mol) ditimbang ± 3.94 mg, lalu dilarutkan dalam 100 ml etanol p.a
b Pembuatan larutan blangko
arutan DPPH ( 00 M) dipipet ml, kemudian dilarutkan hingga 5 ml dengan etanol p.a ke dalam tabung reaksi.
c Pembuatan larutan uji.
Nanokapsul temulawak ditimbang sebanyak 10 mg, lalu dilarutkan dalam 10 ml etanol (1000 ppm), dan disonfikasi selama 15 menit. Hasil sonifikasi disaring, larutan ekstrak hasil saringan diambil 1 ml, kemudian ditambahkan 1 ml larutan DPPH dan ditambahkan dengan etanol sampai 5 ml ke dalam tabung reaksi.
d Pengukuran serapan
Larutan uji diinkubasi pada suhu 37 oC selama 30 menit, kemudian diukur nilai absorbansinya pada panjang gelombang maksimum 518 nm menggunakan spektrofotometer UV-Vis. Aktivitas antioksidan dihitung sebagai persen inhibisi antioksidan terhadap zat radikal bebas, dengan rumus sebagai berikut:
28
Karakteristik
Konsentrasi ekstrak temulawak
(%)
Matriks
Tapioka nanokristalin : Maltodekstrin (% b/b) Sagu nanokristalin : Maltodekstrin (% b/b)
25 : 75 50 : 50 75 : 25 25 : 75 50 : 50 75 : 25
Rendemen (%)
5 32.75 34.64 35.52 31.46 30.02 37.52
10 37.73 37.64 36.95 43.62 44.13 33.19
Efisiensi enkapsulasi (%)
5 56.28 ± 4.45 69.95 ± 2.81 32.89 ± 13.54 58.54 ± 0.18 52.78 ± 2.82 43.52 ± 3.35 10 69.78 ± 1.13 47.15 ± 0.50 37.18 ± 5.63 25.03 ± 14.90 37.31 ± 1.02 45.71 ± 3.98 Drug
loading (%)
5 0.14 ± 0.00 0.16 ± 0.01 0.14 ± 0.00 0.14 ± 0.00 0.15 ± 0.01 0.15 ± 0.01 10 0.24 ± 0.02 0.20 ± 0.01 0.18 ± 0.01 0.22 ± 0.01 0.25 ± 0.03 0.28 ± 0.01 Aktivitas
antioksidan (%)
29 Lampiran 4 Hasil analisis keragaman faktor rasio pati tapioka nanopartikel :
maltodekstrin, dan konsentrasi ekstrak temulawak terhadap karakteristik nanokapsul
Keterangan :
X1 = konsentrasi ekstrak temulawak; X2 = rasio pati nanokristalin : maltodekstrin 1 Efisiensi Enkapsulasi
a Hasil analisis keragaman Sumber
Keragaman db Jumlah Kuadrat Kuadrat Rata -rata F Hitung Pr > F
X1 1 8.383408 8.383408 0.15 0.7149
X2 2 1808.561267 904.280633 15.83 0.0040*
X1*X2 2 712.246667 356.123333 6.23 0.0343*
* erpengaruh n ata pada α = 0.05 (p < 0.05)
b Hasil uji lanjut Duncan terhadap rasio penambahan pati
Grup Duncan Rata - rata N X2
A 63.028 4 25 : 75
A 58.553 4 50 : 50
B 35.038 4 75 : 25
*rata- rata yang diikuti huruf sama tidak berbeda nyata pada uji Duncan taraf 0.05
c Hasil uji lanjut Duncan terhadap pengaruh interaksi konsentrasi ekstrak dan rasio pati yang ditambahkan
Grup Duncan Rata - rata N X1X2
A 69.955 2 550 : 50
A 69.775 2 1025 : 75
B A 56.280 2 525 : 75
B C 47.150 2 1050 : 50
B C 37.185 2 1075 : 25
C 32.890 2 575 : 25
2 DrugLoading
a Hasil analisis keragaman Sumber
Keragaman db Jumlah Kuadrat Kuadrat Rata -rata F Hitung Pr > F
X1 1 0.01140833 0.01140833 72.05 0.0001*
X2 2 0.00111667 0.00055833 3.53 0.0971
X1*X2 2 0.00221667 0.00110833 7.00 0.0270*
30
b Hasil uji lanjut Duncan terhadap konsentrasi ekstrak temulawak
Grup Duncan Rata - rata N X1
A 0.206667 6 10
B 0.145000 6 5
rata- rata yang diikuti huruf sama tidak berbeda nyata pada uji Duncan taraf 0.05
c Hasil uji lanjut Duncan terhadap pengaruh interaksi konsentrasi ekstrak dan rasio pati yang ditambahkan
rata- rata yang diikuti huruf sama tidak berbeda nyata pada uji Duncan taraf 0.05
3 Aktivitas antioksidan
b Hasil uji lanjut Duncan terhadap pengaruh konsentrasi ekstrak temulawak Grup Duncan Rata - rata N X1
A 84.375 6 10 B 35.380 6 5
*rata- rata yang diikuti huruf sama tidak berbeda nyata pada uji Duncan taraf 0.05
c Hasil uji lanjut Duncan terhadap pengaruh interaksi konsentrasi ekstrak dan rasio pati yang ditambahkan