PENENTUAN KADAR ION BESI (Fe3+), KADMIUM (Cd2+), DAN SENG (Zn2+) PADA AIR MINUM DESA SUKATENDEL, DESA SURBAKTI,
DAN DESA NDOKUM SIROGA KABUPATEN KARO DENGAN METODE SPEKTROFOTOMETRI SERAPAN ATOM (SSA)
SKRIPSI
ANITA RIZKI ISNAINI HARAHAP 130822022
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM UNIVERSITAS SUMATERA UTARA
PENENTUAN KADAR ION BESI (Fe3+), KADMIUM (Cd2+), DAN SENG (Zn2+) PADA AIR MINUM DESA SUKATENDEL, DESA SURBAKTI,
DAN DESA NDOKUM SIROGA KABUPATEN KARO DENGAN METODE SPEKTROFOTOMETRI SERAPAN ATOM (SSA)
SKRIPSI
Diajukan untuk melengkapi tugas dan memenuhi syarat mencapai gelar Sarjana Sains
ANITA RIZKI ISNAINI HARAHAP 130822022
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM UNIVERSITAS SUMATERA UTARA
PERSETUJUAN
Judul : Penentuan Kadar Ion Besi (Fe3+), Kadmium (Cd2+), Dan Seng (Zn2+) Pada Air Minum Desa Sukatendel, Desa Surbaki, Dan Desa Ndokum Siroga Kabupaten Karo Dengan Metode Spektofotometri Serapan Atom (SSA)
Kategori : Skripsi
Nama : Anita Rizki Isnaini Harahap Nomor Induk Mahasiswa : 130822022
Program Studi : Sarjana (S1) Kimia Ekstensi
Departemen : Kimia
Fakultas : Matematika Dan Ilmu Pengetahuan Alam Universitas Sumatera Utara
Diluluskan di Medan, April 2015
Komisi Pembimbing
Dosen Pembimbing II Dosen Pembimbing I
Drs. Chairuddin M.Sc Drs. Ahmad Darwin Bangun M.Sc NIP. 195912311987011001 NIP.195211161980031001
Diketahui/Disetujui Oleh
Ketua Departemen Kimia FMIPA USU
PERNYATAAN
PENENTUAN KADAR ION BESI (Fe3+), KADMIUM (Cd2+), DAN SENG (Zn2+) PADA AIR MINUM DESA SUKATENDEL, DESA SURBAKTI,
DAN DESA NDOKUM SIROGA KABUPATEN KARO DENGAN METODE SPEKTROFOTOMETRI SERAPAN ATOM (SSA)
SKRIPSI
Saya mengakui bahwa tugas akhir ini adalah hasil kerja saya sendiri, kecuali beberapa kutipan dari ringkasan yang masing – masing disebut sumbernya.
Medan, April 2015
PENGHARGAAN
Bismillahirrahmanirrohim
Puji dan Syukur kehadirat Allah SWT atas berkah rahmat dan karunia-Nya saya dapat
menyelesaikan skripsi ini dengan tepat waktu sebagai salah satu syarat untuk meraih
gelar Sarjana Sains. Serta shalawat dan salam saya sampaikan kepada Rasulullah
Muhammad SAW semoga kelak mendapatkan syafaat dari Beliau. Amin.
Penghargaan yang tertinggi atas cinta kasih serta dukungan yang tiada terkira
kepada kedua orang tua saya, Ayahanda Maharib Tua Harahap dan Ibunda Halimah
atas segala doa, semangat, bimbingan, pengorbanan dan kasih sayang yang telah
diberikan kepada saya sehingga saya bisa menyelesaikan studi saya. Serta kepada
abang tersayang Sutan Nataris Oloan Harahap yang telah memberikan dukungan
kepada saya.
Dengan segala kerendahan hati, saya mengucapkan terima kasih kepada:
1. Bapak Drs. Ahmad Darwin Bangun, M.Sc selaku dosen pembimbing 1 dan Bapak
Drs. Chairuddin, M.Sc selaku dosen pembimbing 2 yang telah banyak
memberikan penghargaan, bimbingan, dan saran hingga terselesaikannya skripsi
saya ini.
2. Ibu Dr. Rumondang Bulan Nst, MS dan Bapak Drs. Albert Pasaribu, M.Sc selaku
ketua dan sekertaris Departemen Kimia FMIPA USU, serta seluruh staff pegawai
Departemen Kimia.
3. Bapak/Ibu dosen Kimia FMIPA USU yang telah memberikan ilmunya kepada
saya selama masa studi saya di FMIPA USU.
4. Teman – teman seperjuangan Kimia Ekstensi khususnya Stambuk 2013 yang
telah memberikan semangat, dukungan dan doa kepada saya.
5. Serta segala pihak yang telah membantu saya menyelesaikan skripsi ini.
Untuk semuanya semoga Allah membalasnya dengan kebaikan, kesehatan dan
Saya menyadari bahwa skripsi ini masih banyak kekurangan, karena
keterbatasan saya baik dalam literatur maupun pengetahuan. Oleh karena itu, saya
mengharapkan saran dan masukan demi kesempurnaan skripsi ini, dan semoga skripsi
ini bermanfaat bagi kita semua.
Penulis
Anita Rizki Isnaini Harahap
ABSTRAK
Telah dilakukan penelitian penentuan kadar ion besi (Fe3+), kadmium (Cd2+), dan seng (Zn2+) dalam sampel air minum. Sampel yang dianalisa adalah air minum dari desa Sukatendel, desa Surbakti, dan desa Ndokum Siroga Kabupaten Karo Sumatera Utara. Sampel dianalisa setiap minggu selama 5 minggu. Ke dalam sampel air ditambahkan HNO3(P) sebanyak 5 mL dan didesktruksi hingga sisa volume ± 15 mL,
dan dimasukkan ke dalam labu takar 100 mL melalui kertas saring. Kemudian ditentukan konsentrasi ion besi (Fe3+), kadmium (Cd2+), dan seng (Zn2+) dengan menggunakan Spektrofotometri Serapan Atom dengan λspesifik besi (Fe) =248,3 nm;
kadmium (Cd) = 228,8 nm; dan seng (Zn) = 213,9 nm. Hasil penelitian menunjukkan bahwa air minum dari desa Sukatendel mengandung ion besi (Fe3+) sebesar 0,2987 mg/L; kadmium (Cd2+) sebesar 0,0031 mg/L; seng (Zn2+) sebesar 0,3219 mg/L dan desa Surbakti mengandung ion besi (Fe3+) sebesar 0,2599 mg/L; kadmium (Cd2+) sebesar 0,0028 mg/L; seng (Zn2+) sebesar 0,2911 mg/L dan desa Ndokum Siroga mengandung ion besi (Fe3+) sebesar 0,1874 mg/L; kadmium (Cd2+) sebesar 0,0026 mg/L; seng (Zn2+) sebesar 0,1252 mg/L. Dari hasil tersebut dapat diketahui bahwa air minum tersebut masih memenuhi persyaratan air minum menurut PERMENKES RI nomor 492/MenKes/per/VI/2010.
DETERMINATION OF IRON IONS (Fe3+), CADMIUM (Cd2+), AND ZINC (Zn2+) OF DRINKING WATER’S DESA SUKATENDEL, DESA SURBAKTI, AND DESA NDOKUM SIROGA KABUPATEN KARO BY USING ATOMIC
ABSORPTION SPECTROPHOTOMETRIC METHOD (AAS)
ABSTRACT
Research on determination of iron ions (Fe3+), cadmium (Cd2+), and zinc (Zn2+) in drinking water samples has been carried out. Drinking water’s analyzed were drinking water’s from desa Sukatendel, desa Surbakti, and desa Ndokum Siroga Kabupaten Karo Sumatera Utara. Samples were analyzed every week during five weeks. Into samples water was added concentrated HNO3 as much as 5 mL and
destructed to remaining volume ± 15 mL and inserted into the flask through the filter paper. Then determination concentration of iron ions (Fe3+), cadmium (Cd2+), and zinc (Zn2+) by using Atomic Absorption Spectrophotometric with λspecific iron (Fe) =
DAFTAR ISI
Halaman
Persetujuan ii
Pernyataan iii
Penghargaan iv
Abstrak vi
Abstract vii
Daftar Isi viii
Daftar Tabel x
Daftar Gambar xii
Daftar Lampiran xiii
Bab 1 Pendahuluan 1
1.1 Latar Belakang 1
1.2 Permasalahan 3
1.3 Pembatasan Masalah 4
1.4 Tujuan Penelitian 4
1.5 Manfaat Penelitian 4
1.6 Lokasi Penelitian 4
1.7 Metode Penelitian 5
Bab 2 Tinjauan Pustaka 6
2.1 Tinjauan Umum Tentang Air 6
2.2 Penggolongan Air 8
2.3 Macam dan Sumber Air 8
2.4 Syarat Air Minum 10
2.5 Logam 10
2.6 Besi (Fe) 14
2.6.1 Efek Toksik Besi (Fe) 14
2.7 Kadmium (Cd) 15
2.7.1 Efek Toksik Kadmium (Cd) 15
2.8 Seng (Zn) 16
2.8.1 Efek Toksik Seng (Zn) 16
2.9 Spektrofotometri Serapan Atom (SSA) 17
2..9.1 Instrumentasi Spektrofotometri Serapan Atom (SSA) 18
2.9.1.1 Sumber Sinar 18
2.9.1.2 Tempat Sampel 19
2.9.1.3 Monokromator 19
2.9.1.4 Detektor 19
Bab 3 Metodologi Penelitian 20
3.1 Alat dan Bahan Penelitian 20
3.1.1 Alat – alat 20
3.1.2 Bahan – bahan 20
3.2 Prosedur Penelitian 21
3.2.1 Pengawetan dan Preparasi Sampel 21 3.2.2 Pembuatan Larutan Standar Ion Besi (Fe3+) 21
3.2.2.1 Pembuatan Larutan Standar Ion Besi (Fe3+)
100 mg/L 21
3.2.2.2 Pembuatan Larutan Standar Ion Besi (Fe3+)
10 mg/L 21
3.2.2.3 Pembuatan Larutan Standar Ion Besi (Fe3+)
1 mg/L 21
3.2.2.4 Pembuatan Larutan Seri Standar Ion Besi (Fe3+)
0,2; 0,4; 0,6; dan 0,8 mg/L 21
3.2.2.5 Pembuatan Kurva Kalibrasi Ion Besi (Fe3+) 22 3.2.3 Pembuatan Larutan Standar Ion Kadmium (Cd2+) 22
3.2.3.1 Pembuatan Larutan Standar Ion Kadmium (Cd2+)
100 mg/L 22
3.2.3.2 Pembuatan Larutan Standar Ion Kadmium (Cd2+)
10 mg/L 22
3.2.3.3 Pembuatan Larutan Standar Ion Kadmium (Cd2+)
1 mg/L 22
3.2.3.4 Pembuatan Larutan Seri Standar Ion Kadmium
(Cd2+) 0,001; 0,002; 0,003; 0,004 dan 0,005 mg/L 22 3.2.3.5 Pembuatan Kurva Kalibrasi Ion Kadmium (Cd2+) 22 3.2.4 Pembuatan Larutan Standar Ion Seng (Zn2+) 23
3.2.4.1 Pembuatan Larutan Standar Ion Seng (Zn2+)
100 mg/L 23
3.2.4.2 Pembuatan Larutan Standar Ion Seng (Zn2+)
10 mg/L 23
3.2.4.3 Pembuatan Larutan Standar Ion Seng (Zn2+)
1 mg/L 23
3.2.3.4 Pembuatan Larutan Seri Standar Ion Seng (Zn2+)
0,5; 1,5; 2,0 dan 2,5 mg/L 23
3.2.3.5 Pembuatan Kurva Kalibrasi Ion Seng (Zn2+) 23
3.3 Bagan Penelitian 24
3.3.1 Pembuatan Larutan Standar, Seri Standar dan Kurva
Kalibrasi Ion Besi (Fe3+) 24
3.3.2 Pembuatan Larutan Standar, Seri Standar dan Kurva
Kalibrasi Ion Kadmium (Cd2+) 25
3.3.3 Pembuatan Larutan Standar, Seri Standar dan Kurva
Kalibrasi Ion Seng (Zn2+) 26
3.3.4 Preparasi dan Penentuan Kadar Ion Besi (Fe3+) dalam
3.3.5 Preparasi dan Penentuan Kadar Ion Kadmium (Cd2+)
dalam Sampel 28
3.3.6 Preparasi dan Penentun Kadar Ion Seng (Zn2+) dalam
Sampel 29
Bab 4 Hasil dan Pembahasan 30
4.1 Hasil Penelitian 30
4.1.1 Besi (Fe) 30
4.1.2 Pengolahan Data Ion Besi (Fe3+) 31 4.1.2.1 Penurunan Persamaan Garis Regresi dengan
Metode Least Square 31
4.1.2.2 Koefisien Korelasi 34
4.1.2.3 Penentuan Konsentrasi 34
4.1.3 Kadmium (Cd) 38
4.1.4 Pengolahan Data Ion Kadmium (Cd2+) 38 4.1.4.1 Penurunan Persamaan Garis Regresi dengan
Metode Least Square 38
4.1.4.2 Koefisien Korelasi 41
4.1.4.3 Penentuan Konsentrasi 41
4.1.5 Seng (Zn) 46
4.1.6 Pengolahan Data Ion Seng (Zn2+) 47 4.1.6.1 Penurunan Persamaan Garis Regresi dengan
Metode Least Square 47
4.1.6.2 Koefisien Korelasi 49
4.1.6.3 Penentuan Konsentrasi 49
4.2 Pembahasan 54
Bab 5 Kesimpulan dan Saran 56
5.1 Kesimpulan 56
5.2 Saran 56
Daftar Pustaka 57
Lampiran 59
DAFTAR TABEL
Halaman
Tabel 2.1 Perbandingan antara embun, air hujan, salju, air permukaan 9 tanah dan air tanah dalam
Tabel 2.2 Logam – logam makro dan mikro yang ditemukan dalam 13
kerak bumi
Tabel 4.1 Kondisi alat Spektrofotometer Serapan Atom (SSA) Shimadzu 30 AA- 7000 pada pengukuran konsentrasi ion Besi (Fe3+) Tabel 4.2 Data Absorbansi Larutan Seri Standar Ion Besi (Fe3+) 32 Tabel 4.3 Penurunan persamaan garis regresi untuk penentuan konsentrasi 34
ion besi (Fe3+) berdasarkan pengukuran absorbansi larutan seri standar ion besi (Fe3+)
Tabel 4.4 Data absorbansi ion Besi (Fe3+) dalam samperl air minum dari 34 desa Sukatendel, desa Surbakti, dan desa Ndokum siroga
Tabel 4.5 A nalisis data statistik penentuan konsentrasi ion besi (Fe3+) pada 35 air minum dari desa Sukatendel
Tabel 4.6 A nalisis data statistik penentuan konsentrasi ion besi (Fe3+) pada 36 air minum dari desa Surbakti
Tabel 4.7 A nalisis data statistik penentuan konsentrasi ion besi (Fe3+) pada 37 air minum dari desa Ndokum Siroga
Tabel 4.8 Kondisi alat Spektrofotometer Serapan Atom (SSA) Shimadzu 38 AA- 7000 pada pengukuran konsentrasi ion Kadmium (Cd2+) Tabel 4.9 Data Absorbansi Larutan Seri Standar Ion Kadmium (Cd2+) 38 Tabel 4.10 Penurunan persamaan garis regresi untuk penentuan konsentrasi 38
ion Kadmium (Cd2+) berdasarkan pengukuran absorbansi larutan seri standar ion Kadmium (Cd2+)
Tabel 4.11 Data absorbansi ion Kadmium (Cd2+) dalam samperl air minum 42 dari desa Sukatendel, desa Surbakti, dan desa Ndokum siroga
Tabel 4.12 A nalisis data statistik penentuan konsentrasi ion Kadmium (Cd2+) 43 Pada air minum dari desa Sukatendel
Tabel 4.13 A nalisis data statistik penentuan konsentrasi ion Kadmium (Cd2+) 44 pada air minum dari desa Surbakti
Tabel 4.14 A nalisis data statistik penentuan konsentrasi ion Kadmium (Cd2+) 45 pada air minum dari desa Ndokum Siroga
Tabel 4.15 Kondisi alat Spektrofotometer Serapan Atom (SSA) Shimadzu 46 AA- 7000 pada pengukuran konsentrasi ion Seng (Zn2+)
Tabel 4.16 Data Absorbansi Larutan Seri Standar Ion Seng (Zn2+) 46 Tabel 4.17 Penurunan persamaan garis regresi untuk penentuan konsentrasi 47
standar ion Seng (Zn2+)
Tabel 4.18 Data absorbansi ion Seng (Zn2+) dalam samperl air minum dari 50 desa Sukatendel, desa Surbakti, dan desa Ndokum siroga
Tabel 4.19 A nalisis data statistik penentuan konsentrasi ion Seng (Zn2+) 51 Pada air minum dari desa Sukatendel
Tabel 4.20 A nalisis data statistik penentuan konsentrasi ion Seng (Zn2+) 52 pada air minum dari desa Surbakti
Tabel 4.21 A nalisis data statistik penentuan konsentrasi ion Seng (Zn2+) 53 pada air minum dari desa Ndokum Siroga
Tabel 4.22 Data hasil penelitian kadar ion besi (Fe3+), kadmium (Cd2+), 54 Seng (Zn2+) pada air minum desa Sukatendel, desa Surbakti,
DAFTAR GAMBAR
Halaman
DAFTAR LAMPIRAN
Halaman
Lampiran 1 Persyaratan Kualitas air Minum 59
Lampiran 2 Peta Lokasi Gunung Sinabung 63
ABSTRAK
Telah dilakukan penelitian penentuan kadar ion besi (Fe3+), kadmium (Cd2+), dan seng (Zn2+) dalam sampel air minum. Sampel yang dianalisa adalah air minum dari desa Sukatendel, desa Surbakti, dan desa Ndokum Siroga Kabupaten Karo Sumatera Utara. Sampel dianalisa setiap minggu selama 5 minggu. Ke dalam sampel air ditambahkan HNO3(P) sebanyak 5 mL dan didesktruksi hingga sisa volume ± 15 mL,
dan dimasukkan ke dalam labu takar 100 mL melalui kertas saring. Kemudian ditentukan konsentrasi ion besi (Fe3+), kadmium (Cd2+), dan seng (Zn2+) dengan menggunakan Spektrofotometri Serapan Atom dengan λspesifik besi (Fe) =248,3 nm;
kadmium (Cd) = 228,8 nm; dan seng (Zn) = 213,9 nm. Hasil penelitian menunjukkan bahwa air minum dari desa Sukatendel mengandung ion besi (Fe3+) sebesar 0,2987 mg/L; kadmium (Cd2+) sebesar 0,0031 mg/L; seng (Zn2+) sebesar 0,3219 mg/L dan desa Surbakti mengandung ion besi (Fe3+) sebesar 0,2599 mg/L; kadmium (Cd2+) sebesar 0,0028 mg/L; seng (Zn2+) sebesar 0,2911 mg/L dan desa Ndokum Siroga mengandung ion besi (Fe3+) sebesar 0,1874 mg/L; kadmium (Cd2+) sebesar 0,0026 mg/L; seng (Zn2+) sebesar 0,1252 mg/L. Dari hasil tersebut dapat diketahui bahwa air minum tersebut masih memenuhi persyaratan air minum menurut PERMENKES RI nomor 492/MenKes/per/VI/2010.
DETERMINATION OF IRON IONS (Fe3+), CADMIUM (Cd2+), AND ZINC (Zn2+) OF DRINKING WATER’S DESA SUKATENDEL, DESA SURBAKTI, AND DESA NDOKUM SIROGA KABUPATEN KARO BY USING ATOMIC
ABSORPTION SPECTROPHOTOMETRIC METHOD (AAS)
ABSTRACT
Research on determination of iron ions (Fe3+), cadmium (Cd2+), and zinc (Zn2+) in drinking water samples has been carried out. Drinking water’s analyzed were drinking water’s from desa Sukatendel, desa Surbakti, and desa Ndokum Siroga Kabupaten Karo Sumatera Utara. Samples were analyzed every week during five weeks. Into samples water was added concentrated HNO3 as much as 5 mL and
destructed to remaining volume ± 15 mL and inserted into the flask through the filter paper. Then determination concentration of iron ions (Fe3+), cadmium (Cd2+), and zinc (Zn2+) by using Atomic Absorption Spectrophotometric with λspecific iron (Fe) =
BAB 1
PENDAHULUAN
1.1Latar Belakang
Air merupakan zat yang paling penting dalam kehidupan setelah udara. Sekitar tiga
per empat bagian tubuh kita terdiri dari air dan tidak seorangpun dapat bertahan hidup
lebih dari 4 – 5 hari tanpa minum air. Selain itu, air juga dipergunakan untuk
memasak, mencuci, mandi, dan membersihkan kotoran yang ada disekitar rumah. Air
juga digunakan untuk keperluan industri, pertanian, pemadam kebakaran, tempat
rekreasi, transportasi, dan lain – lain. Penyakit – penyakit yang menyerang manusia
dapat juga ditularkan dan disebarkan melalui air. Kondisi tersebut tentunya dapat
menimbulkan wabah penyakit dimana – mana.
Volume air dalam tubuh manusia rata – rata 65% dari total berat badannya,
dan volume tersebut sangat bervariasi antara bagian – bagian tubuh seseorang.
Beberapa organ tubuh manusia yang mengandung banyak air, antara lain, otak 74,5%,
tulang 22%, ginjal 82,7%, otot 75,6%, dan darah 83%.
Ditinjau dari ilmu kesehatan masyarakat, penyediaan sumber air bersih harus
dapat memenuhi kebutuhan masyarakat karena persediaan air bersih yang terbatas
merupakan memudahkan timbulnya penyakit di masyarakat. Volume rata – rata
kebutuhan air setiap individu per hari berkisar antara 150 – 200 liter atau 35 – 40
galon. Kebutuhan air tersebut bervariasi bergantung pada keadaan iklim, standar
kehidupan, dan kebiasaan masyarakat (Chandra, 2005).
Demikianlah, dalam rangka mempertahankan kelangsungan hidup, manusia
yang digunakan tidak selalu sesuai dengan syarat kesehatan. Karena sering ditemui
air tersebut mengandung bibit penyakit ataupun zat – zat tertentu yang dapat
menimbulkan penyakit, yang justru membahayakan kelangsungan hidup manusia
(Azwar, 1996).
Seperti yang telah diuraikan, bahwa air sangat dibutuhkan oleh semua
makhluk di dunia, khususnya sebagai air minum. Namun air dapat juga menimbulkan
berbagai penyakit gangguan kesehatan terhadap si pemakai. Ini disebabkan karena
adanya kemampuan air untuk melarutkan bahan – bahan padat, mengabsorpsikan gas
– gas dan bahan cair lainnya, sehingga semua air yang mengandung mineral dan zat –
zat lain dalam larutan yang diperolehnya dari udara, tanah, dan bukit – bukit yang
dilaluinya. Kandungan bahan atau zat – zat ini dalam air dalam konsentrasi tertentu
dapat menimbulkan efek gangguan kesehatan pada si pemakai (Sutrisno, 2004).
Gunung Sinabung ini termasuk ke dalam gunung api bertipe strato vulkano.
Gunung Sinabung terletak di Kabupaten Karo, dengan ibu kota kabupaten adalah
Kabanjahe, provinsi Sumatera Utara dengan ibu kota provinsi adalah Medan. Letak
dan posisi geografisnya terletak pada 3°10 menit LU dan 98° 23,5 menit BT dengan
ketinggian 2.460 meter
(http://digilib.unimed.ac.id/public/UNIMED-undergraduate-25534-308321029%20Bab%201.pdf).
Gunung berapi atau gunung api secara umum adalah istilah yang
didefenisikan sebagai suatu saluran fluida panas (batuan dalam wujud cair atau lava)
yang memanjang dari kedalaman sekitar 10 km di bawah permukaan bumi sampai ke
permukaan bumi, termasuk endapan hasil akumulasi material yang dikeluarkan saat
dia meletus. Secara singkat, gunung berapi adalah gunung yang masih aktif dalam
mengeluarkan material didalamnya.
Apabila gunung berapi meletus, magma yang terdapat di bawah gunung
berbahaya dari gunung yang sedang meletus adalah aliran lumpur, abu, dan gas
beracun.
Hujan abu lebat terjadi ketika letusan gunung api sedang berlangsung.
Material berukuran halus (abu dan pasir halus) yang diterbangkan angin dan jatuh
sebagai hujan abu. Karena ukurannya yang sangat halus, material ini akan sangat
berbahaya bagi pernapasan, mata, pencemaran air tanah, dan pengrusakan tumbuh –
tumbuhan (Hartuti, 2009).
Berdasarkan hasil penelitian sebelumnya mengenai analisis logam berat dan
unsur hara debu vulkanik Gunung Sinabung Kabupaten Karo Sumatera Utara oleh
Sinuhaji, N. F, (2011), dan Penetapan kadar Mg, Fe, Pb, dan Cd dalam abu letusan
Gunung Sinabung secara Spektrofotometri Serapan Atom oleh Milala, I.V (2011),
dan juga Studi Perbandingan Kadar Logam Berat Fe, Mn, Zn, Pb, Cu, Al dan Na
Pada Debu Erupsi Gunung Sinabung dan Tanah Sebelum Erupsi oleh Tarigan, M
(2014) peneliti tertarik untuk melakukan penelitian dengan tujuan untuk mengetahui
kadar ion Besi (Fe3+), Kadmium (Cd2+), dan Seng (Zn2+) pada air minum dari desa
Sukatendel, Surbakti, dan desa Ndokum Siroga Kabupaten Karo Sumatera Utara.
1.2Permasalahan
Adapun permasalahan dalam penelitian ini adalah berapa kadar Ion Besi (Fe3+),
Kadmium (Cd2+), dan Seng (Zn2+) yang diperoleh dalam air minum dari desa
Sukatendel, Surbakti, dan desa Ndokum Siroga dan apakah air minum dari desa
Sukatendel, Surbakti, dan desa Ndokum Siroga memenuhi persyaratan kualitas air
1.3Pembatasan Masalah
Penelitian ini dibatasi pada penentuan kadar ion Besi (Fe3+), Kadmium (Cd2+), dan
Seng (Zn2+) pada air minum dari desa Sukatendel Kecamatan Tiganderket, desa
Surbakti Kecamatan Simpang Empat, dan desa Ndokum Siroga Kecamatan Simpang
Empat Kabupaten Karo dengan menggunakan metode Spektofotometri Serapan Atom
(SSA).
1.4Tujuan Penelitian
Penelitian ini bertujuan untuk mengetahui berapa kadar ion Besi (Fe3+), Kadmium
(Cd2+), dan Seng (Zn2+) pada air minum dari desa Sukatendel, Surbakti, dan desa
Ndokum Siroga dan apakah air minum dari desa Sukatendel, Surbakti, dan desa
Ndokum Siroga memenuhi persyaratan air kualitas minum menurut PERMENKES
RI nomor 492/MenKes/per/VI/2010.
1.5Manfaat Penelitian
Dari hasil penelitian ini diharapkan dapat memberikan informasi kepada masyarakat
mengenai kadar ion Besi (Fe3+), Kadmium (Cd2+), dan Seng (Zn2+) pada air minum
dan apakah air minum memenuhi persyaratan kualitas air minum menurut
PERMENKES RI nomor 492/MenKes/per/VI/2010.
1.6Lokasi Penelitian
Penelitian ini dilakukan di Laboratorium Kimia Dasar LIDA Universitas Sumatera
Utara dan Analisis Spektrofotometri Serapan Atom dilakukan di Balai Besar
1.7 Metodologi Penelitian
1. Penelitian ini merupakan penelitian laboratorium
2. Sampel yang dianalisis adalah air yang diambil dari air keran desa Sukatendel
Kecamatan Tiganderket (6 km), desa Surbakti Kecamatan Simpang Empat
(7 km), dan desa Ndokum Siroga Kecamatan Simpang Empat Kabupaten
Karo Sumatera Utara (8 km)
3. Pereaksi yang digunakan adalah asam nitrat pekat
4. Penentuan kadar ion Besi (Fe3+), Kadmium (Cd2+), dan Seng (Zn2+) dilakukan
dengan metode Spektrofotometri Serapan Atom (SSA) pada panjang
gelombang 248,3 nm untuk besi (Fe), kadmium (Cd) adalah 228,2 nm, dan
BAB 2
TINJAUAN PUSTAKA
2.1 Tinjauan Umum Tentang Air
Air merupakan sumber daya alam yang diperlukan untuk hajat hidup orang banyak,
bahkan oleh semua makhluk hidup. Oleh Karena itu, sumber daya air harus
dilindungi agar tetap dapat dimanfaatkan dengan baik oleh manusia serta makhluk
hidup yang lain (Effendi, 2003).
Hidrosfer adalah lingkungan air, sebagian besar dari permukaan bumi tertutup
oleh air yang begitu luasnya sehingga sangat berpengaruh pada iklim. Air yang
tersebar di alam tidak pernah terdapat dalam bentuk murni, tetapi bukan berarti semua
air sudah terpolusi. Sebagai contoh, meskipun di daerah pegunungan atau hutan yang
terpencil dengan udara yang bersih dan bebas dari polusi, air hujan selalu
mengandung bahan – bahan terlarut seperti CO2, O2, dan N2, serta bahan tersuspensi
seperti debu dan partikel – partikel lainnya yang terbawa dari atmosfer (Agusnar,
2007).
Makhluk hidup yang ada di bumi ini tidak dapat terlepas dari kebutuhan akan
air. Air merupakan kebutuhan utama bagi proses kehidupan di bumi ini. Tidak akan
ada kehidupan seandainya di bumi ini tidak ada air. Air yang relatif bersih
didambakan oleh manusia, baik untuk keperluan hidup sehari – hari, untuk keperluan
industri, untuk keperluan sanitasi kota, maupun untuk keperluan pertanian, dan lain
sebagainya.
Dewasa ini air menjadi masalah yang perlu mendapat perhatian yang seksama
menjadi barang yang mahal karena air sudah banyak tercemar oleh bermacam –
macam limbah dari hasil kegiatan manusia, baik limbah dari kegiatan rumah tangga,
limbah dari kegiatan industri dan kegiatan – kegiatan lainnya.
Untuk mendapatkan standar air yang bersih tidaklah mudah, karena
tergantung pada banyak faktor penentu. Faktor penentu tersebut adalah:
1) Kegunaan air:
a) Air untuk minum
b) Air untuk keperluan rumah tangga
c) Air untuk industri
d) Air untuk mengairi sawah
e) Air untuk kolam perikanan, dll.
2) Asal sumber air:
a) Air dari mata air di pegunungan
b) Air danau
c) Air sungai
d) Air hujan, dll.
Air yang ada di bumi ini tidak pernah terdapat dalam keadaan murni bersih,
tetapi selalu ada senyawa atau mineral (unsur) lain yang terlarut di dalamnya. Hal ini
tidak berarti bahwa semua air di bumi telah tercemar. Sebagai contoh, air yang di
ambil dari mata air di pegunungan dan air hujan. Keduanya dapat dianggap sebagai
yang bersih, namun senyawa atau mineral (unsur) yang terdapat didalamnya berlainan
(Wardhana, 2004).
Dari contoh – contoh tersebut di atas, jelas bahwa air yang tidak terpolusi
tidak selalu merupakan air murni, tetapi adalah air yang tidak mengandung bahan –
bahan asing tertentu dalam jumlah yang melebihi batas yang ditetapkan sehingga air
ledeng, air sumur), berenang/rekreasi (kolam renang, air laut di pantai), mandi (air
ledeng, air sumur), kehidupan hewan air (air sungai, danau), pengairan dan keperluan
industri. Adanya benda – benda asing yang mengakibatkan air tersebut tidak dapat
digunakan secara normal disebut polusi. Karena kebutuhan makhluk hidup akan air
sangat bervariasi, maka batasan polusi untuk berbagai jenis air juga berbeda. Sebagai
contoh air dari kali di pegunungan yang belum terpolusi tidak dapat dipergunakan
langsung sebagai air minum karena belum memenuhi persyaratan air minum
(Agusnar, 2007).
2.2 Penggolongan Air
Peraturan Pemerintah No. 20 tahun 1990 mengelompokkan kualitas air menjadi
beberapa golongan menurut peruntukannya. Adapun penggolongan air menurut
peruntukannya adalah sebagai berikut :
1) Golongan A, yaitu air yang dapat digunakan sebagai air minum secara
langsung, tanpa pengolahan terlebih dahulu
2) Golongan B, yaitu air yang dapat digunakan sebagai air baku air minum
3) Golongan C, yaitu air yang dapat digunakan untuk keperluan perikanan dan
peternakan
4) Golongan D, yaitu air yang dapat digunakan untuk keperluan pertanian, usaha
di perkotaan, industri, dan pembangkit listrik tenaga air (Effendi, 2003).
2.3 Macam dan Sumber Air
Jika membicarakan tentang macam air yang dikaitkan dengan sumber atau
asalnya, maka air dapat dibedakan atas :
1) Air hujan, embun ataupun salju, yakni air yang didapat dari angkasa, karena
terjadinya proses presipitasi dari awan, atmosfir yang mengandung uap air
2) Air permukaan tanah, dapat berupa air tergenang atau air yang mengalir,
seperti danau, sungai, laut. Air dari sumur yang dangkal, adalah juga air
3) Air dalam tanah, yakni air permukaan tanah yang meresap ke dalam tanah,
jadi telah mengalami penyaringan oleh tanah ataupun batu-batuan. Air dalam
tanah ini sekali waktu juga akan menjadi air permukaan, yakni dengan
mengalirnya air tersebut menuju ke laut.
Ditinjau dari segi kesehatan, ketiga macam air ini tidaklah selalu memenuhi
syarat kesehatan, karena ketiga-tiganya mempunyai kemungkinan untuk dicemari.
Embun, air hujan atau salju misalnya, yang berasal dari angkasa, ketika turun ke bumi
dapat menyerap abu, gas ataupun materi-materi berbahaya lainnya. Demikian pula air
permukaan, karena dapat terkontaminasi dengan berbagai zat-zat berbahaya untuk
kesehatan. Air dalam tanah demikian pula halnya, karena sekalipun telah terjadi
proses penyaringan, namun tetap saja ada kemungkinan terkontaminasi dengan
zat-zat mineral ataupun kimia yang mungkin membahayakan kesehatan. Adapun
perbandingan antara ketiga macam air tersebut sebagai berikut:
Tabel 2.1 Perbandingan antara embun, air hujan, dan salju, air permukaan tanah, dan
air tanah dalam
Embun, air hujan dan salju
Air permukaan tanah Air dalam tanah
Pada umumnya jika belum
terkontaminasi air bersifat
bersih, steril, murni, hanya
saja mudah merusak
logam (menimbulkan
karat ).
Pada umumnya telah
terkontaminasi jadi bersifat
kotor, mengandung bakteri
dan zat kimia, kaya akan
O2, CO2 serta mengandung
zat-zat lainnya yang
bersifat merusak.
Pada umumnya jika
mengalami penyaringan
sempurna maka bersifat
bersih, bebas dari bakteri.
Hanya saja kemungkinan
mengandung zat mineral
cukup besar, karena itu
sering berwarna, berbau
dan mempunyai rasa
yang tidak nyaman
Air yang diperuntukkan bagi konsumsi manusia harus berasal dari sumber
yang bersih dan aman. Batasan – batasan sumber air yang bersih dan aman tersebut,
antara lain :
1) Bebas dari kontaminasi kuman atau bibit penyakit
2) Bebas dari substansi kimia yang berbahaya dan beracun
3) Tidak berasa dan berbau
4) Dapat dipergunakan untuk mencakupi kebutuhan domestik dan rumah tangga
5) Memenuhi standar minimal yang ditentukan oleh WHO atau Departemen
Kesehatan RI.
Air dikatakan tercemar bila mengandung bibit penyakit, parasit, bahan – bahan kimia
yang berbahaya, dan sampah atau limbah industri (Chandra, 2005).
2.4 Syarat – Syarat Air Minum
Pada umumnya ditentukan beberapa standar (patokan) yang pada beberapa negara
berbeda – beda menurut :
1) Kondisi negara masing – masing
2) Perkembangan ilmu pengetahuan
3) Perkembangan teknologi
Dari segi kualitas air harus memenuhi :
a. Syarat Fisik :
1) Air tidak boleh berwarna
2) Air tidak boleh berasa
3) Air tidak boleh berbau
4) Suhu air hendaknya ± 25ºC
b. Syarat – Syarat Kimia
Air minum yang baik adalah air yang tidak tercemar secara berlebihan oleh zat – zat
kimia ataupun mineral – mineral, terutama oleh zat – zat ataupun mineral yang
berbahaya bagi kesehatan. Selanjutnya diharapkan pula zat ataupun bahan kimia yang
terdapat di dalam air minum, tidak sampai menimbulkan kerusakan pada tempat
penyimpanan air; sebaliknya zat ataupun bahan kimia dan atau mineral yang
dibutuhkan oleh tubuh, hendaknya harus terdapat dalam kadar yang sewajarnya
dalam sumber air minum tersebut (Azwar, 1996).
c. Syarat – syarat bakteriologik
Air minum tidak boleh mengandung bakteri – bakteri penyakit (patogen) sama sekali
dan tak boleh mengandung bakteri – bakteri golongan Coli melebihi batas – batas
yang telah ditentukannya yaitu 1 Coli/100ml air (Sutrisno, 2004).
2.5 Logam
Dalam kehidupan sehari – hari, kita tidak terpisah dari benda – benda yang bersifat
logam. Benda ini kita gunakan sebagai alat perlengkapan rumah tangga seperti
sendok, garpu, pisau dan lain – lain (logam biasa), sampai pada tingkat perhiasan
mewah yang tidak dapat dimiliki oleh semua orang seperti emas, perak, dan lain –
lain (logam mulia). Secara gamblang, dalam konotasi kesehatan kita beranggapan
bahwa logam diidentikkan dengan besi, padat, berat, keras dan sulit dibentuk.
Logam berat masih termasuk golongan logam dengan kriteria – kriteria yang
sama dengan logam – logam lain. Perbedaannya terletak dari pengaruh yang
dihasilkan bila logam berat ini berikatan dan atau masuk ke dalam tubuh organisme
hidup.
Sebagai contoh, bila unsur logam besi (Fe) masuk ke dalam tubuh, meski
dalam jumlah yang agak berlebihan, biasanya tidaklah menimbulkan pengaruh yang
mengikat oksigen. Sedangkan unsur logam berat beracun yang dipentingkan seperti
tenbaga (Cu), bila masuk kedalam tubuh dalam jumlah berlebihan akan menimbulkan
pengaruh - pengaruh buruk terhadap fungsi fisiologis tubuh. Jika yang masuk ke
dalam tubuh organisme hidup adalah unsur logam beracun seperti hidragyrum (Hg)
atau disebut juga air raksa, maka dapat dipastikan bahwa organisme tersebut akan
langsung keracunan.
Berbeda dengan logam biasa, logam berat biasanya menimbulkan efek – efek
khusus pada makhluk hidup. Dapat dikatakan bahwa semua logam berat dapat
menjadi bahan beracun yang akan meracuni makhluk hidup. Sebagai contoh adalah
logam air raksa (Hg), kadmium (Cd), timah hitam (Pb), dan khrom (Cr). Namun
demikian, meski logam berat dapat mengakibatkan keracunan atas makhluk hidup,
sebagian dari logam – logam berat tersebut tetap dibutuhkan oleh makhluk hidup.
Kebutuhan tersebut berada dalam jumlah yang sangat sedikit. Tetapi bila
kebutuhan dalam jumlah yanga sangat kecil itu tidak terpenuhi, maka dapat berakibat
fatal terhadap kelangsungan hidup dari setiap makhluk hidup. Karena tingkat
kebutuhan sangat dipentingkan maka logam – logam tersebut juga dinamakan sebagai
logam – logam atau mineral –mineral essensial tubuh.
Ternyata kemudian, bila jumlah dari logam – logam essesnsial ini masuk
kedalam tubuh dalam jumlah berlebihan, maka akan berubah fungsi menjadi zat
racun bagi tubuh. Contoh dari logam – logam berat essensial ini adalah tembaga (Cu),
seng (Zn), dan nikel (Ni) (Palar, 2004).
Berikut adalah Logam – logam makro dan mikro yang ditemukan dalam kerak
Tabel 2.2 Logam - logam makro dan mikro yang ditemukan dalam kerak bumi
Kelompok Logam Simbol Jumlah (mg/kg)
Makro Aluminium Al 81.300
Besi Fe 50.000
Kalsium* Ca 36.300
Natrium* Na 28.300
Kalium* K 25.900
Magnesium* Mg 20.900
Mangan Mn 1.000
Mikro Barium Ba 425
Nikel Ni 75
Seng Zn 70
Tembaga Cu 55
Plumbum Pb 12,5
Uranium U 2,7
Timah putih Sn 2
Kadmium Cd 0,2
Merkuri Hg 0,08
Perak Ag 0,07
Emas Au 0,004
*Logam ringan (Darmono, 1995).
Terdapat 80 jenis logam berat dari 109 unsur kimia di muka bumi ini. Logam
berat dibagi ke dalam dua jenis, yaitu:
1) Logam berat essensial; yakni logam dalam jumlah tertentu yang sangat
dibutuhkan oleh organisme. Dalam jumlah berlebihan, logam tersebut bisa
menimbulkan efek toksik. Contohnya adalah Zn, Cu, Fe, Co, Mn
2) Logam berat tidak essensial; yakni logam yang keberadaannya dalam tubuh
masih belum diketahui manfaatnya, bahkan bersifat toksik, seperti Hg, Cd,
Logam berat dapat menimbulkan efek gangguan terhadap kesehatan manusia,
tergantung pada bagian mana dari logam berat tersebut yang terikat dalam tubuh seta
besarnya dosis paparan. Efek toksik dari logam berat mampu menghalangi kerja
enzim sehingga mengganggu metabolisme tubuh, menyebabkan alergi, berifat
mutagen, atau karsinogen pada manusia atau hewan (Widowati, 2008).
2.6 Besi (Fe)
Besi (Fe) merupakan logam transisi dan memiliki nomor atom 26. Bilangan oksidasi
Fe adalah +3 dan +2. Fe memiliki berat atom 55,845 g/mol, titik leleh 1.580°C. Fe
menempati urutan sepuluh besar sebagai unsur di bumi. Fe menyusun 5 – 5,6% dari
kerak bumi dan menyusun 35% dari masa bumi. Fe menempati berbagai lapisan
bumi. Konsentrasi tertinggi terdapat pada lapisan dalam dari inti bumi dan sejumlah
kecil terdapat di lapisan kerak bumi. Besi (Fe) memiliki keistimewaan, antara lain:
1) Fe sangat kuat dibandingkan kayu ataupun kuprum (Cu)
2) Fe lebih mudah dibengkokkan dan dibentuk menjadi berbagai jenis perabot
dengan pemanasan
3) Fe bersifat tahan panas, tidak seperti kayu sehingga bisa digunakan sebagai
bahan pembuatan mesin (Widowati, 2008).
2.6.1 Efek Toksik Besi (Fe)
Sekalipun Fe itu diperlukan oleh tubuh, tetapi dalam dosis besar dapat merusak
dinding usus. Kematian seringkali disebabkan oleh rusaknya dinding usus. Debu Fe
juga dapat diakumulasi di dalam alveoli, dan menyebabkan berkurangnya fungsi paru
– paru (Slamet, 2009).
Konsumsi Fe dalam dosis tinggi pada anak – anak bisa mengakibatkan
2.7 Kadmium (Cd)
Kadmium (Cd) adalah logam berwarna putih perak, lunak, mengkilap, tidak larut
dalam basa. Cd memiliki nomor atom 40, berat atom 112,4 g/mol; titik leleh 321°C,
dan titik didih 767°C. Kadmium bersifat lentur, tahan terhadap tekanan. Keberadaan
kadmium (Cd) bisa mencemari lingkungan dan bisa berada di atmosfer, tanah, dan
perairan (Widowati, 2008).
Logam kadmium (Cd) sangat banyak digunakan dalam kehidupan sehari –
hari manusia. Logam ini telah digunakan semenjak tahun 1950 dan total produksi
dunia adalah sekitar 15.000 – 18.000 per tahun. Prinsip dasar atau prinsip utama
dalam penggunaan kadmium adalah sebagai bahan ‘stabilitasi’ sebagai bahan
pewarna dalam industri plastik dan pada elektroplating. Namun sebagian dari
substansi logam kadmium ini juga digunakan untuk solder dan alloy – alloynya
digunakan pula untuk baterai (Palar, 2004).
Kadmium (Cd) dalam konsentrasi rendah banyak digunakan dalam industri
pada proses pengolahan roti, pengolahan ikan, pengolahan minuman, serta industri
tekstil (Widowati, 2008).
2.7.1 Efek Toksik Kadmium (Cd)
Pada keracunan kronis yang disebabkan oleh Cd, umumnya berupa kerusakan –
kerusakan pada banyak sistem fisiologis tubuh. Sistem – sistem tubuh yang dapat
dirusak oleh keracunan kronis logam Cd ini adalah pada sistem urinaria (ginjal),
sistem respirasi (pernafasan/paru – paru), sistem sirkulasi (darah) dan jantung. Di
samping semua itu, keracunan kronis tersebut juga merusak kelenjar reproduksi,
sistem penciuman dan bahkan dapat mengakibatkan kerapuhan pada tulang (Palar,
2004).
2.8 Seng (Zn)
Seng (Zn) adalah komponen alam yang terdapat di kerak bumi. Zn adalah logam yang
memiliki karakteristik cukup reaktif, berwarna putih – kebiruan, pudar bila terkena
uap udara. Zn memiliki nomor atom 30 dan memiliki titik lebur 419,73°C (Widowati,
2008).
Logam Zn memiliki banyak keunggulan, antara lain memiliki daya energi
tinggi, bisa didaur ulang, ama, dan tidak menyisakan emisi (zero emition) sehingga
Zn bisa digunakan sebagai baterai habis pakai. Zn digunakan dalam berbagai jenis
industri elektronik seperti cat, produk karet, kosmetik, obat – obatan, pelapis lantai,
plastic, printing, tinta, baetari, tekstil, bahan kimia, solder. Kegunaan Zn pada berbagai jenis industri yaitu:
1) Melapisi besi atau baja guna mencegah korosi
2) Bahan tabung baterai
3) Bahan alloy seperti kuningan, nikel – perak, logam mesin ketik, dan
penyepuhan listrik
4) Sebagai bahan suplemen vitamin atau mineral yang memiliki aktivitas
antioksidan guna mencegah penuaan dini serta mempercepat proses
penyembuhan, dll (Widowati, 2008).
2.8.1 Efek Toksik Seng (Zn)
Seng (Zn) merupakan unsur esensial bagi tubuh, tetapi dalam dosis tinggi Zn dapat
berbahaya dan bersifat toksik. Toksisitas Zn bisa bisa bersifat kronis dan akut. Jika
Zn masuk ke dalam tubuh 150 – 450 mg/hari mengakibatkan pengurangan imunitas
tubuh, serta pengurangan kadar High Density Lipoprotein (HDL) kolesterol.
Konsumsi Zn sebesar 2 g atau lebih akan mengakibatkan mual, muntah, dan
demam. Orang yang mengkonsumsi lebih dari 12 g unsur Zn lebih dari 2 hari terbukti
2.9 Spektrofotometri Serapan Atom (SSA)
Peristiwa serapan atom pertama kali diamati oleh Fraunhofer, ketika menelaah garis –
garis hitam pada spektrum matahari. Sedangkan yang memanfaatkan prinsip serapan
atom pada bidang analisis adalah seorang Australia bernama Alan Walsh di tahun
1955. Sebelumnya ahli kimia banyak bergantung pada cara – cara spektrofotometrik
atau metode analisis spektrografik. Beberapa cara ini yang sulit dan memakan waktu,
kemudian segera digantikan dengan spektorskopi serapan atom atau Atomic
Absorption Spectroscopy (AAS) (Khopkar, 2008).
Spektofotometri serapan atom digunakan untuk analisis kuantitatif unsur –
unsur logam dalam jumlah sekelumit (trace) dan sangat kelumit (ultratrace). Cara
analasis ini memberikan kadar total unsur logam dalam suatu sampel dan tidak
tergantung pada bentuk molekul dari logam dalam sampel tersebut. Metode
Spektrofotometri Serapan Atom (SSA) mendasarkan pada prinsip absorpsi cahaya
oleh atom. Atom – atom akan menyerap cahaya pada panjang gelombang tertentu,
tergantung pada sifat unsurnya.
Cahaya pada panjang gelombang ini mempunyai cukup energi untuk
mengubah tingkat elektronik suatu atom yang mana transisi elektonik suatu atom
bersifat spesifik. Dengan menyerap suatu energi, maka atom akan memperoleh energi
sehingga suatu atom pada keadaan dasar dapat ditingkatkan energinya keringkat
2.9.1 Instrumentasi Spektrofotometri Serapan Atom (SSA)
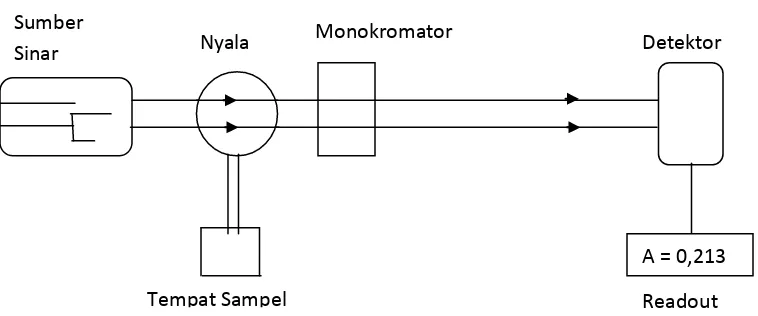
Sistem peralatan spektrofotometer serapan atom dapat dilihat pada gambar
berikut ini ;
[image:35.612.117.496.141.299.2]
Gambar 2.1 Sistem peralatan Spektrofotometer Serapan Atom (SSA) (Rohman,
2007).
2.9.1.1 Sumber Sinar
Sumber sinar yang lazim dipakai adalah lampu katoda berongga (hollow cathode
lamp). Lampu ini terdiri atas tabung kaca tertutup yang mengandung suatu katoda dan anoda. Katoda sendiri berbentuk silinder berongga yang terbuat dari logam atau
dilapisi dengan logam tertentu. Tabung logam ini diisi dengan gas mulia (neon atau
argon) dengan tekanan rendah (10 – 15 torr). Neon biasanya lebih disukai karena
memberikan intensitas pancaran lampu yang lebih rendah.
Salah satu kelemahan penggunaan lampu katoda berongga adalah satu lampu
digunakan untuk satu unsur, akan tetapi saat ini telah banyak dijumpai suatu lampu
katoda, berongga kombinasi; yakni satu lampu dilapisi dengan beberapa unsur
sehingga dapat digunakan untuk analisis beberapa unsur sekaligus (Rohman, 2007). A = 0,213
Sumber
Sinar Nyala
Monokromator
Detektor
2.9.1.2 Tempat Sampel
Dalam analisis spektrofotometri serapan atom, sampel yang akan dianalisis harus
diuraikan menjadi atom – atom netral yang masih dalam keadaan asas. Ada berbagai
macam alat yang dapat digunakan untuk mengubah suatu sampel menjadi uap atom –
atom yaitu dengan nyala (flame) dan dengan tanpa nyala (flameless) (Rohman, 2007).
2.9.1.3 Monokromator
Pada SSA, monokromator dimaksudkan untuk memisahkan dan memilih panjang
gelombang yang digunakan dalam analisis. Di samping sistem optik, dalam
monokromator juga terdapat suatu alat yang digunakan untuk memisahkan radiasi
resonansi dan kontinyu yang disebut chopper (Rohman, 2007).
2.9.1.4 Detektor
Detektor yang digunakan untuk mengukur intensitas cahaya yang melalui tempat
pengatoman. Biasanya digunakan tabung penggandaan foton (photomultiplier tube).
Ada dua cara yang dapat digunakan dalam sistem deteksi yaitu: (a) yang memberikan
respon terhadap radiasi resonansi dan radiasi kontinyu; dan (b) yang hanya
memberikan respon terhadap radiasi resonansi. Cara terbaik adalah dengan
menggunakan detektor yang hanya peka terhadap radiasi resonan yang termodulasi
(Rohman, 2007).
2.9.1.5 Readout
Readout merupakan suatu alat penunjuk atau dapat juga diartikan sebagai sistem pencatat hasil. Pencatat hasil dilakukan dengan suatu alat yang telah terkalibrasi
untuk pembacaan suatu transmisi atau absrobsi. Hasil pembacaan dapat berupa angka
atau berupa kurva dari suatu recorder yang menggambarkan absorbansi atau
BAB 3
METODE PENELITIAN
3.1 Alat dan Bahan Penelitian 3.1.1 Alat - alat
Adapun alat – alat yang digunakan dalam penelitian adalah sebagai berikut:
1) Gelas Beaker Pyrex 250 mL
2) Labu Takar Pyrex 100 mL
3) Pipet Tetes
4) Hot plate Cimaree
5) Kertas Saring Whatman No. 42
6) Spektrofotometri Serapan Atom Shimadzu AA-7000
7) Pipet Volume Pyrex 5 mL
8) Botol akuadest
9) Bola karet
10)Corong
3.1.2 Bahan - bahan
Bahan – bahan yang digunakan dalam penelitian adalah sebagai berikut:
1) Sampel air minum Desa Sukatendel
2) Sampel air minum Desa Surbakti
3) Sampel air minum Desa Ndokum Siroga
4) Larutan HNO3(P) p.a (E.Merck)
5) Larutan standar ion Fe3+ 1000 mg/L p.a (E.Merck)
6) Larutan standar ion Cd2+ 1000 mg/L p.a (E.Merck)
7) Larutan standar ion Zn2+ 1000 mg/L p.a (E.Merck)
3.2 Prosedur Penelitian
3.2.1 Pengawetan dan Preparasi Sampel
Sampel tidak dapat langsung di analisa, maka sampel diawetkan dengan ditambahkan
HNO3(p) sampai pH ± 2. Kemudian diambil sebanyak 100 mL sampel, dimasukkan ke
dalam beaker glass dan ditambahkan 5 mL HNO3(p). Dipanaskan sampai hampir
kering, kemudian ditambahkan 50 mL akuadest dan dimasukkan ke dalam labu takar
100 mL melalui kertas saring. Diencerkan dengan akuadest sampai garis tanda dan
diaduk sampai homogen.
3.2.2 Pembuatan Larutan Standar Ion Besi (Fe3+)
3.2.2.1 Pembuatan Larutan Standar Ion Besi (Fe3+) 100 mg/L
Sebanyak 5 mL larutan induk ion besi (Fe3+) 1000 mg/L dimasukkan ke dalam labu
takar 50 mL lalu diencerkan dengan akuadest sampai garis tanda dan dihomogenkan
3.2.2.2 Pembuatan Larutan Standar Ion Besi (Fe3+) 10 mg/L
Sebanyak 5 mL larutan standar ion besi (Fe3+) 100 mg/L dimasukkan ke dalam labu
takar 50 mL lalu diencerkan dengan akuadest sampai garis tanda dan dihomogenkan
3.2.2.3 Pembuatan Larutan Standar Ion Besi (Fe3+) 1 mg/L
Sebanyak 5 mL larutan standar ion besi (Fe3+) 10 mg/L dimasukkan ke dalam labu
takar 50 mL lalu diencerkan dengan akuadest sampai garis tanda dan dihomogenkan
3.2.2.4 Pembuatan Larutan Seri Standar Ion Besi (Fe3+) 0,2; 0,4; 0,6; 0,8 mg/L Sebanyak 10, 20, 30, dan 40 mL larutan standar ion besi (Fe3+) 1 mg/L dimasukkan
kedalam labu takar 50 mL lalu diencerkan dengan akuadest sampai garis tanda dan
dihomogenkan
3.2.2.5 Pembuatan Kurva Kalibrasi Ion Besi (Fe3+)
dilakukan sebanyak 3 kali. Dilakukan hal yang sama untuk banko (0,0) dan larutan
seri standar ion besi (Fe3+) 0,4; 0,6; 0,8; 1,0 mg/L.
3.2.3 Pembuatan Larutan Standar Ion Kadmium (Cd2+)
3.2.3.1 Pembuatan Larutan Standar Ion Kadmium (Cd2+) 100 mg/L
Sebanyak 5 mL larutan induk ion kadmium (Cd2+) 1000 mg/L dimasukkan ke dalam
labu takar 50 mL lalu diencerkan dengan akuadest sampai garis tanda dan
dihomogenkan.
3.2.3.2 Pembuatan Larutan Standar Ion Kadmium (Cd2+) 10 mg/L
Sebanyak 5 mL larutan standar ion kadmium (Cd2+) 100 mg/L dimasukkan ke dalam
labu takar 50 mL lalu diencerkan dengan akuadest sampai garis tanda dan
dihomogenkan.
3.2.3.3 Pembuatan Larutan Standar Ion Kadmium (Cd2+) 1 mg/L
Sebanyak 5 mL larutan standar ion kadmium (Cd2+) 10 mg/L dimasukkan ke dalam
labu takar 50 mL lalu diencerkan dengan akuadest sampai garis tanda dan
dihomogenkan.
3.2.3.4 Pembuatan Larutan Seri Standar Ion Kadmium (Cd2+) 0,001; 0,002; 0,003; 0,004; dan 0,005 mg/L
Sebanyak 0.05; 0,10; 0,15; 0,20; dan 0,25 mL larutan standar ion kadmium (Cd2+)
1 mg/L dimasukkan ke dalam labu takar 50 mL lalu diencerkan dengan akuadest
sampai garis tanda dan dihomogenkan.
3.2.3.5 Pembuatan Kurva Kalibrasi Ion Kadmium (Cd2+)
Larutan seri standar ion kadmium (Cd2+) 0,001 mg/L diukur absorbansinya dengan Spektrofotometri Serapan Atom pada λspesifik 228,8 nm. Perlakuan dilakukan
sebanyak 3 kali. Dilakukan hal yang sama untuk blanko (0,000) dan larutan seri
3.2.4 Pembuatan Larutan Standar Ion Seng (Zn2+)
3.2.4.1 Pembuatan Larutan Standar Ion Seng (Zn2+) 100 mg/L
Sebanyak 5 mL larutan induk ion seng (Zn2+) 1000 mg/L dimasukkan ke dalam labu
takar 50 mL lalu diencerkan dengan akuadest sampai garis tanda dan dihomogenkan.
3.2.4.2 Pembuatan Larutan Standar Ion Seng (Zn2+) 10 mg/L
Sebanyak 5 mL larutan standar ion seng (Zn2+) 100 mg/L dimasukkan ke dalam labu
takar 50 mL lalu diencerkan dengan akuadest sampai garis tanda dan dihomogenkan
3.2.4.3 Pembuatan Larutan Standar Ion Seng (Zn2+) 1 mg/L
Sebanyak 5 mL larutan standar ion seng (Zn2+) 10 mg/L dimasukkan ke dalam labu
takar 50 mL lalu diencerkan dengan akuadest sampai garis tanda dan dihomogenkan
3.2.4.4 Pembuatan Larutan Seri Standar Ion Seng (Zn2+) 0,5; 1,5; 2,0 dan 2,5 mg/L
Sebanyak 25 mL larutan standar ion seng (Zn2+) 1 mg/L dan sebanyak 7,5; 10 dan
12,5 mL larutan standar ion seng (Zn2+) 10 mg/L dimasukkan kedalam labu takar 50
mL lalu diencerkan dengan akuadest sampai garis tanda dan dihomogenkan
3.2.4.5 Pembuatan Kurva Kalibrasi Ion Seng (Zn2+)
Larutan seri standar ion seng (Zn2+) 0,5 mg/L di ukur absorbansinya dengan menggunakan Spektrofotometri Serapan Atom pada λspesifik 213,9 nm. Perlakuan
dilakukan sebanyak 3 kali. Dilakukan hal yang sama untuk blanko (0,0) dan larutan
3.3 Bagan Penelitian
3.3.1 Pembuatan Larutan Standar dan Seri Standar Ion Besi (Fe3+) 0,2; 0,4; 0,6; 0,8; dan 1,0 mg/L dan Pembuatan Kurva Kalibrasi
Dipipet sebanyak 5 mL larutan standar ion besi (Fe3+) dan dimasukkan kedalam labu takar 50 mL
Diencerkan dengan akuades sampai garis tanda
Diaduk hingga homogen
Dipipet sebanyak 5 mL larutan standar ion besi (Fe3+) dan dimasukkan kedalam labu takar 50 mL
Diencerkan dengan akuades sampai garis tanda
Diaduk hingga homogen
Dipipet sebanyak 5 mL larutan standar ion besi (Fe3+) dan dimasukkan kedalam labu takar 50 mL
Diencerkan dengan akuades sampai garis tanda
Diaduk hingga homogen
Dipipet sebanyak 10; 20; 30; dan 40 mL larutan standar ion besi (Fe3+) dan dimasukkan kedalam labu takar 50 mL
Diencerkan dengan akuades sampai garis tanda
Diaduk hingga homogen
Diukur absorbansinya sebanyak tiga kali dengan menggunakan Spektrofotometri Serapan Atom (SSA) dengan panjang gelombang spesifik 248,3 nm.
Larutan Standar Ion Besi (Fe3+) 1000 mg/L
Larutan Standar Ion Besi (Fe3+) 100 mg/L
Larutan Standar Ion Besi (Fe3+) 10 mg/L
Larutan Standar Ion Besi (Fe3+) 1 mg/L
Larutan Seri Standar Ion Besi (Fe3+) 0,0; 0,2; 0,4; 0,6 dan 0,8 mg/L
3.3.2 Pembuatan Larutan Standar dan Seri Standar Ion Kadmium (Cd2+) 0,001; 0,002; 0,003; 0,004; dan 0,005 mg/L dan Pembuatan Kurva Kalibrasi
Dipipet sebanyak 5 mL larutan standar ion kadmium (Cd2+) dan dimasukkan kedalam labu takar 50 mL
Diencerkan dengan akuades sampai garis tanda
Diaduk hingga homogen
Dipipet sebanyak 5 mL larutan standar ion kadmium (Cd2+) dan dimasukkan kedalam labu takar 50 mL
Diencerkan dengan akuades sampai garis tanda
Diaduk hingga homogen
Dipipet sebanyak 5 mL larutan standar ion kadmium (Cd2+) dan dimasukkan kedalam labu takar 50 mL
Diencerkan dengan akuades sampai garis tanda
Diaduk hingga homogen
Dipipet sebanyak 0,005; 0,10; 0,15; 0,20; dan 0,25 mL larutan standar ion kadmium (Cd2+) dan dimasukkan kedalam labu takar 50 mL
Diencerkan dengan akuades sampai garis tanda
Diaduk hingga homogen
Diukur absorbansinya sebanyak tiga kali dengan menggunakan Spektrofotometri Serapan Atom (SSA) dengan panjang gelombang spesifik 228,8 nm.
Larutan Standar Ion Kadmium (Cd2+) 1000 mg/L
Larutan Standar Ion Kadmium (Cd2+) 100 mg/L
Larutan Standar Ion Kadmium (Cd2+) 10 mg/L
Larutan Standar Ion Kadmium (Cd2+) 1 mg/L
Larutan Seri Standar Ion Kadmium (Cd2+) 0,000; 0,001; 0,002; 0,003; 0,004; dan 0,005 mg/L
3.3.3 Pembuatan Larutan Standar dan Seri Standar Ion Seng (Zn2+) 0,5; 1,0; 1,5; 2,0 dan 2,5 mg/L dan Pembuatan Kurva Kalibrasi
Dipipet sebanyak 5 mL larutan standar ion seng (Zn2+) dan dimasukkan kedalam labu takar 50 mL
Diencerkan dengan akuades sampai garis tanda
Diaduk hingga homogen
Dipipet sebanyak 5 mL larutan standar ion seng (Zn2+) dan dimasukkan kedalam labu takar 50 mL
Diencerkan dengan akuades sampai garis tanda
Diaduk hingga homogen
Dipipet sebanyak 5 mL larutan standar ion seng (Zn2+) dan dimasukkan kedalam labu takar 50 mL
Diencerkan dengan akuades sampai garis tanda
Diaduk hingga homogen
Dipipet sebanyak 25 mL larutan standar ion seng (Zn2+) dan dimasukkan kedalam labu takar 50 mL
Diencerkan dengan akuades sampai garis tanda
Diaduk hingga homogen
Dipipet sebanyak 7,5; 10 dan 12,5 mL larutan standar ion seng (Zn2+) 10mg/L dan dimasukkan kedalam labu takar 50 mL
Diencerkan dengan akuades sampai garis tanda
Diaduk hingga homogen
Diukur absorbansinya sebanyak tiga kali dengan menggunakan Spektrofotometri Serapan Atom (SSA) dengan panjang gelombang spesifik 213,9 nm.
Larutan Standar Ion Seng (Zn2+) 1000 mg/L
Larutan Standar Ion Seng (Zn2+) 100 mg/L
Larutan Standar Ion Seng (Zn2+) 10 mg/L
Larutan Standar Ion Seng (Zn2+) 1 mg/L
Larutan Seri Standar Ion Seng (Zn2+) 0,5 mg/L
Larutan seri standar Ion Seng (Zn2+) 0,0; 1,5; 2,0; dan 2,5 mg/l
3.4 Preparasi dan Penentuan Kadar Ion Besi (Fe3+) Pada Sampel
Ditambahkan HNO3(p) hingga pH ± 2
Dimasukkan kedalam beaker glass 100 mL
Ditambahkan 5 mL HNO3(p)
Dipanaskan perlahan diatas hotplate hingga sisa volume 15 mL
Ditambahkan 50 mL akuadest
Dimasukkan ke dalam labu takar 100 mL melalui kertas saring
Diencerkan dengan akuadest sampai garis tanda
Diaduk sampai homogen
Diukur absorbansinya dengan menggunakan Spektrofotometri Serapan Atom (SSA) pada λspesifik 248,3 nm
Catatan: dilakukan hal yang sama untuk sampel dari desa Ndokum Siroga dan Desa
Surbakti
Sampel Air Desa Sukatendel
Sampel Air 100 mL
3.5 Preparasi dan Penentuan Kadar Ion Kadmium (Cd2+) Pada Sampel
Ditambahkan HNO3(p) hingga pH ± 2
Dimasukkan kedalam beaker glass 100 mL
Ditambahkan 5 mL HNO3(p)
Dipanaskan perlahan diatas hotplate hingga sisa volume 15 mL
Ditambahkan 50 mL akuadest
Dimasukkan ke dalam labu takar 100 mL melalui kertas saring
Diencerkan dengan akuadest sampai garis tanda
Diaduk sampai homogen
Diukur absorbansinya dengan menggunakan Spektrofotometri Serapan Atom (SSA) pada λspesifik 228,8 nm
Catatan: dilakukan hal yang sama untuk sampel dari desa Ndokum Siroga dan Desa
Surbakti
Sampel Air Desa Sukatendel
Sampel Air 100 mL
3.6 Preparasi dan Penentuan Kadar Ion Seng (Zn2+) Pada Sampel
Ditambahkan HNO3(p) hingga pH ± 2
Dimasukkan kedalam beaker glass 100 mL
Ditambahkan 5 mL HNO3(p)
Dipanaskan perlahan diatas hotplate hingga sisa volume 15 mL
Ditambahkan 50 mL akuadest
Dimasukkan ke dalam labu takar 100 mL melalui kertas saring
Diencerkan dengan akuadest sampai garis tanda
Diaduk sampai homogen
Diukur absorbansinya dengan menggunakan Spektrofotometri Serapan Atom (SSA) pada λspesifik 213,9 nm
Catatan: dilakukan hal yang sama untuk sampel dari desa Ndokum Siroga dan Desa
Surbakti
Sampel Air Desa Sukatendel
Sampel Air 100 mL
BAB 4
HASIL DAN PEMBAHASAN
4.1 Hasil Penelitian 4.1.1 Besi (Fe)
Pembuatan kurva kalibrasi larutan standar Ion Besi (Fe3+) dilakukan dengan
menyiapkan larutan seri standar dengan berbagai konsentrasi yaitu pada pengukuran
0,0000; 0,2000; 0,4000; 0,6000; 0,8000 dan 1,0000 mg/L, kemudian diukur
[image:47.612.111.534.369.538.2]absorbansinya dengan menggunakan Spektrofotometri Serapan Atom (SSA).
Tabel 4.1 Kondisi Alat Spektrofotometri Serapan Atom (SSA) Shimadzu tipe AA-7000 Pada Pengukuran Konsentrasi Ion Besi (Fe3+)
No Parameter Ion Besi
1 Panjang Gelombang (nm) 248,3
2 Tipe Nyala Air-C2H2
3 Kecepatan Aliran Gas Pembakar (L/min) 2,2
4 Kecepatan Aliran Udara (L/min) 15,0
5 Ketinggian Tungku (mm) 9,0
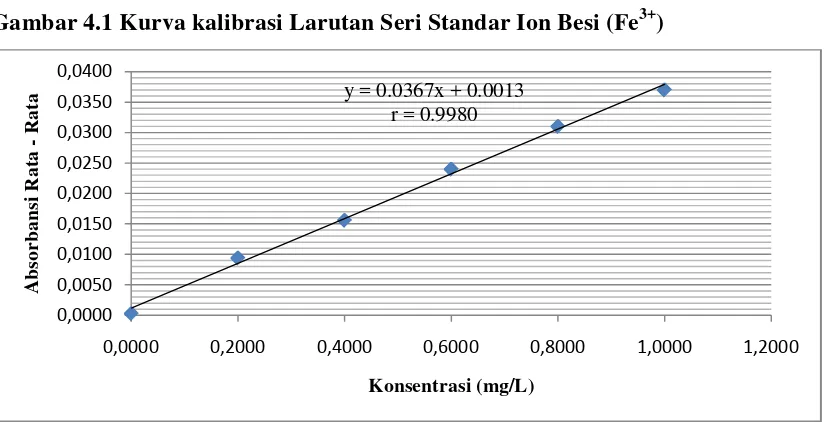
Tabel 4.2 Data Absorbansi Larutan Seri Standar Ion Besi (Fe3+) Konsentrasi (mg/L) Absorbansi Rata – rata
0,0000 0,0003
0,2000 0,0094
0,4000 0,0156
0,6000 0,0244
0,8000 0,0310
1,0000 0,0370
Gambar 4.1 Kurva kalibrasi Larutan Seri Standar Ion Besi (Fe3+)
4.1.2 Pengolahan Data
4.1.2.1 Penurunan Persamaan Garis Regresi dengan Metode Least Square
Hasil pengukuran absorbansi larutan seri standar Ion Besi (Fe3+) pada tabel 4.2 di
plotkan terhadap konsentrasi sehingga diperoleh kurva kalibrasi berupa garis linier.
Persamaan garis regresi untuk kurva kalibrasi ini dapat diturunkan dengan metode
least square dengan data pada table 4.3
y = 0.0367x + 0.0013 r = 0.9980
0,0000 0,0050 0,0100 0,0150 0,0200 0,0250 0,0300 0,0350 0,0400
0,0000 0,2000 0,4000 0,6000 0,8000 1,0000 1,2000
[image:48.612.118.531.316.527.2]Tabel 4.3 Penurunan Persamaan Garis Regresi Untuk Penentuan Konsentrasi Ion Besi (Fe3+) Berdasarkan Pengukuran Absorbansi Larutan Seri Standar Ion Besi (Fe3+)
No Xi Yi (Xi – X) (Yi – Y) (Xi – X)2 (Yi – Y)2 (Xi-X)(Yi-Y)
1 0,0000 0,0003 -0,5000 -0,0193 0,2500 3,7249x10-4 0,00965
2 0,2000 0,0094 -0,3000 -0,0102 0,0900 1,0404x10-4 0,00306
3 0,4000 0,0156 -0,1000 -0,0040 0,0100 1,6000x10-5 0,00040
4 0,6000 0,0244 0,1000 -0,0048 0,0100 2,3040x10-5 0,00048
5 0,8000 0,0310 0,3000 0,0114 0,0900 1,2996x10-4 0,00342
6 1,0000 0,0370 0,5000 0,0174 0,2500 3,0276x10-4 0,00870 Ƹ 3,0000 0,1177 0,0000 0,0095 0,7000 9,4829x10-4 0,02571
X =
Ƹ Xi n=
3,0000
6
=
0,5000Y =
Ƹ Yin
=
0,11776
=
0,0196Persamaan garis regresi untuk kurva kalibrasi dapat diturunkan dari persamaaan
garis:
Y = aX + b
dimana:
a = slope b = intersept
Selanjutnya harga slope dapat ditentukan dengan menggunakan metode least square
a = Ƹ (Xi−X ) (Yi−Y )
Ƹ (Xi−X )2
b = Y– aX
Dengan mensubstitusikan harga – harga yang tercantum pada tabel 4.2 pada
persamaan ini maka diperoleh :
� =0,2571
0,7000= 0,0367
b = 0,0196 – (0,0367) (0,5000)
= 0,0196 – 0,0183
= 0,0013
Maka persamaan garis yang diperoleh adalah :
Y = 0,0367 X + 0,0013
4.1.2.2 Koefisien Korelasi
Koefisien Korelasi dapat ditentukan dengan menggunakan persamaan sebagai
berikut:
r =
Ƹ (Xi−X)(Yi−Y) [Ƹ(Xi−X)2Ƹ(Yi−Y)2]1/2
=
0,02571[(0,7000 ) (9,4829�10−4)]1/2
=
0,025710,02576
4.1.2.3 Penentuan Konsentrasi
Untuk menghitung konsentrasi dari Ion Besi (Fe3+), maka diambil data hasil
pengukuran absorbansi Ion Besi (Fe3+) dalam sampel. Data selengkapnya ada pada
[image:51.612.113.533.230.584.2]Tabel 4.4.
Tabel 4.4 Data Absorbansi Ion Besi (Fe3+) dalam sampel air air minum dari Desa Sukatendel, Desa Surbakti, dan Desa Ndokum Siroga
Sampel Minggu Absorbansi Absorbansi
Rata – Rata (Ā)
A1 A2 A3
Desa
Sukatendel
I 0,0108 0,0105 0,0098 0,0103
II 0,0119 0,0117 0,0114 0,0116
III 0,0129 0,0121 0,0124 0,0124
IV 0,0137 0,0133 0,0128 0,0132
V 0,0142 0,0135 0,0131 0,0136
Desa
Surbakti
I 0,0098 0,0086 0,0083 0,0089
II 0,0102 0,0097 0,0095 0,0098
III 0,0116 0,0113 0,0099 0,0109
IV 0,0124 0,0116 0,0119 0,0119
V 0,0131 0,0128 0,0124 0,0127
Desa
Ndokum
siroga
I 0,0068 0,0055 0,0051 0,0058
II 0,0075 0,0069 0,0072 0,0072
III 0,0089 0,0078 0,0075 0,0080
IV 0,0097 0,0092 0,0087 0,0092
V 0,0113 0,0107 0,0104 0,0108
Konsentrasi Ion Besi (Fe3+) dalam sampel dapat diukur dengan mensubstitusikan nilai
Y (absorbansi) Ion Besi (Fe3+) ke persamaan:
Tabel 4.5 Analisis Data Statistik Penentuan Konsentrasi Ion Besi (Fe3+) Pada Air Minum dari Desa Sukatendel
No Xi (Xi – X)2
1 0,2453 28,5156x10-4
2 0,2866 1,4641x10-4
3 0,3024 1,3690x10-5
4 0,3242 6,5025x10-4
5 0,3351 13,2496x10-4
Ƹ 1,4936 49,8687x10-4
X = Ƹ Xi �
=
1,4936
5
=
0,2987SD =
�
Ƹ(��−�)2
�−1
=
�
49,8687�10−45−1
= 0,0353
Konsentrasi Ion Besi (Fe3+) yang diperoleh pada air minum dari desa Sukatendel
adalah = X ± SD
= 0,2987 ± 0,0353 mg/L.
Dengan cara yang sama dapat ditentukan konsentrasi Ion Besi (Fe3+) pada air minum
dari desa Surbakti dan juga desa Ndokum Siroga. Data selengkapnya dapat dilihat
Tabel 4.6 Analisis Data Statistik Penentuan Konsentrasi Ion Besi (Fe3+) Pada Air Minum dari Desa Surbakti
No Xi (Xi – X)2
1 0,2070 23,9121x10-4
2 0,2316 8,0089x10-4
3 0,2615 2,5600x10-6
4 0,2888 8,3521x10-4
5 0,3106 25,7049x10-4
Ƹ 1,2995 66,0036x10-4
X = Ƹ Xi �
=
1,2995
5
=
0,2599SD =
�
Ƹ(��−�)2
�−1
=
�
66,0036�10−45−1
= 0,0406
Konsentrasi Ion Besi (Fe3+) yang diperoleh pada air minum dari desa Surbakti adalah
= X ± SD
Tabel 4.7 Analisis Data Statistik Penentuan Konsentrasi Ion Besi (Fe3+) Pada Air Minum dari Desa Ndokum Siroga
No Xi (Xi – X)2
1 0,1226 41,9904x10-4
2 0,1607 7,1289x10-4
3 0,1825 2,4010x10-5
4 0,2152 6,3001x10-4
5 0,2588 54,9081x10-4
Ƹ 0,9371 110,5676x10-4
X = Ƹ Xi �
=
0,9371
5
=
0,1847SD =
�
Ƹ(��−�)2
�−1
=
�
110,5676�10−45−1
= 0,0525
Konsentrasi Ion Besi (Fe3+) yang diperoleh pada air minum dari desa Ndokum Siroga
adalah = X ± SD
4.1.3 Kadmium (Cd)
Pembuatan kurva kalibrasi larutan standar Ion Kadmium (Cd2+) dilakukan dengan
menyiapkan larutan seri standar dengan berbagai konsentrasi yaitu pada pengukuran
0,0000; 0,0001; 0,0002; 0,0003; 0,0004 dan 0,0005 mg/L, kemudian diukur
[image:55.612.115.533.259.425.2]absorbansinya dengan menggunakan Spektrofotometri Serapan Atom (SSA).
Tabel 4.8 Kondisi Alat Spektrofotometri Serapan Atom (SSA) Shimadzu tipe AA-7000 Pada Pengukuran Konsentrasi Ion Kadmium (Cd2+)
No Parameter Ion Kadmium
1 Panjang Gelombang (nm) 228,8
2 Tipe Nyala Air-C2H2
3 Kecepatan Aliran Gas Pembakar (L/min) 1,8
4 Kecepatan Aliran Udara (L/min) 15,0
5 Ketinggian Tungku (mm) 7,0
6 Burner Angle (degree) 0
Tabel 4.9 Data Absorbansi Larutan Seri Standar Ion Kadmium (Cd2+) Konsentrasi (mg/L) Absorbansi Rata – rata
0,0000 0,0003
0,0010 0,0015
0,0020 0,0031
0,0030 0,0045
0,0040 0,0059
[image:55.612.108.415.513.678.2]Gambar 4.2 Kurva kalibrasi Larutan Seri Standar Ion Kadmium (Cd2+)
4.1.4 Pengolahan Data
4.1.4.1 Penurunan Persamaan Garis Regresi dengan Metode Least Square
Hasil pengukuran absorbansi larutan seri standar Ion Kadmium (Cd2+) pada tabel 4.9
di plotkan terhadap konsentrasi sehingga diperoleh kurva kalibrasi berupa garis linier.
Persamaan garis regresi untuk kurva kalibrasi ini dapat diturunkan dengan metode
least square dengan data pada tabel 4.10
Tabel 4.10 Penurunan Persamaan Garis Regresi Untuk Penentuan Konsentrasi Ion Kadmium (Cd2+) Berdasarkan Pengukuran Absorbansi Larutan Seri Standar Ion Kadmium (Cd2+)
No Xi Yi (Xi – X) (Yi – Y) (Xi – X)2 (Yi – Y)2 (Xi-X)(Yi-Y)
1 0,0000 0,0003 -0,0025 -0,0034 6,2500x10-6 1,1560x10-5 8,5000x10-6
2 0,0010 0,0015 -0,0015 -0,0022 2,2500x10-6 4,8400x10-6 3,3000x10-6
3 0,0020 0,0031 -0,0005 -0,0006 2,5000x10-7 3,6000x10-7 3,0000x10-7
4 0,0030 0,0045 0,0005 0,0008 2,5000x10-7 6,4000x10-7 4,0000x10-7
5 0,0040 0,0059 0,0015 0,0022 2,2500x10-6 4,8400x10-6 3,3000x10-6
6 0,0050 0,0071 0,0025 0,0034 6,2500x10-6 1,1560x10-5 8,5000x10-6 Ƹ 0,0150 0,0224 0,0000 0,0002 1,7500x10-5 3,3800x10-5 2,4300x10-5
y = 1.3885x + 0.0003 r = 0.9991
0,0000 0,0010 0,0020 0,0030 0,0040 0,0050 0,0060 0,0070 0,0080
0,0000 0,0010 0,0020 0,0030 0,0040 0,0050 0,0060
[image:56.612.108.565.512.686.2]X =
Ƹ Xi n=
0,0150
6
=
0,0025Y =
Ƹ Yin
=
0,02246
=
0,0037Persamaan garis regresi untuk kurva kalibrasi dapat diturunkan dari persamaaan
garis:
Y = aX + b
dimana:
a = slope b = intersept
Selanjutnya harga slope dapat ditentukan dengan menggunakan metode least square
sebagai berikut:
a = Ƹ (Xi−X ) (Yi−Y )
Ƹ (Xi−X )2
b = Y– aX
Dengan mensubstitusikan harga – harga yang tercantum pada tabel 4.7 pada
persamaan ini maka diperoleh :
� =2,4300�10
−5
1,7500�10−5 = 1,3885
b = 0,0037 – (1,3885) (0,0025)
= 0,0037 – 0,0034
Maka persamaan garis yang diperoleh adalah :
Y = 1,3885 X + 0,0003
4.1.4.2 Koefisien Korelasi
Koefisien Korelasi dapat ditentukan dengan menggunakan persamaan sebagai
berikut:
r =
Ƹ (Xi−X)(Yi−Y) [Ƹ(Xi−X)2Ƹ(Yi−Y)2]1/2
=
2,4300�10−5
[(1,7500�10−5) (3,3800�10−5)]1/2
=
2,4300 x10−5
2,4300 x10−5
= 0,9991
4.1.4.3 Penentuan Konsentrasi
Untuk menghitung konsentrasi dari Ion Kadmium (Cd2+), maka diambil data hasil
pengukuran absorbansi Ion Kadmium (Cd2+) dalam sampel. Data selengkapnya ada
Tabel 4.11 Data Absorbansi Ion Kadmium (Cd2+) dalam sampel air air minum dari Desa Sukatendel, Desa Surbakti, dan Desa Ndokum Siroga
Sampel Minggu Absorbansi Absorbansi
Rata – Rata (Ā)
A1 A2 A3
Desa
Sukatendel
I 0,0037 0,0035 0,0030 0,0034
II 0,0049 0,0046 0,0042 0,0045
III 0,0053 0,0047 0,0050 0,0050
IV 0,0057 0,0049 0,0055 0,0053
V 0,0061 0,0056 0,0053 0,0056
Desa
Surbakti
I 0,0034 0,0031 0,0027 0,0030
II 0,0046 0,0043 0,0040 0,0043
III 0,0049 0,0044 0,0047 0,0046
IV 0,0051 0,0049 0,0043 0,0047
V 0,0057 0,0053 0,0051 0,0053
Desa
Ndokum
siroga
I 0,0032 0,0028 0,0025 0,0028
II 0,0038 0,0030 0,0033 0,0033
III 0,0046 0,0041 0,0037 0,0041
IV 0,0052 0,0048 0,0041 0,0047
V 0,0059 0,0056 0,0047 0,0054
Konsentrasi Ion Kadmium (Cd2+) dalam sampel dapat diukur dengan
mensubstitusikan nilai Y (absorbansi) Ion Kadmium (Cd2+) ke persamaan:
Tabel 4.12 Analisis Data Statistik Penentuan Konsentrasi Ion Kadmium (Cd2+) Pada Air Minum dari Desa Sukatendel
No Xi (Xi – X)2
1 0,0022 8,1000x10-7
2 0,0030 1,0000x10-8
3 0,0033 4,0000x10-8
4 0,0036 2,5000x10-7
5 0,0038 4,9000x10-7
Ƹ 0,0159 1,6000x10-6
X = Ƹ Xi �
=
0,0159
5
=
0,0031SD =
�
Ƹ(��−�)2
�−1
=
�
1,6000�10−45−1
= 0,0006
Konsentrasi Ion Kadmium (Cd2+