PENGARUH SALINITAS TERHADAP PREVALENSI EKTOPARASIT PADA IKAN KERAPU MACAN (Epinephelus fuscoguttatus)
SKRIPSI
RESTI FAUZIAH 070805047
DEPARTEMEN BIOLOGI
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM UNIVERSITAS SUMETERA UTARA
PENGARUH SALINITAS TERHADAP PREVALENSI EKTOPARASIT PADA IKAN KERAPU MACAN (Epinephelus fuscoguttatus)
SKRIPSI
Diajukan untuk melengkapi dan memenuhi syarat mencapai gelar Sarjana Sains
RESTI FAUZIAH 070805047
DEPARTEMEN BIOLOGI
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM UNIVERSITAS SUMETERA UTARA
PERSETUJUAN
Diluluskan di
Medan, November 2011
Komisi Pembimbing :
Pembimbing 2 Pembimbing 1
Dedy Arief Hendriyanto S.St,Pi. M.Si Prof. Dr. Dwi Suryanto M.Sc NIP. 19780524200003 1 002 NIP. 19640409199403 1 003
Diketahui/Disetujui oleh
Departemen Biologi FMIPA USU
Ketua
Dr. Nursahara Pasaribu, M.Sc
NIP. 19630123 199003 2 001
Judul : PENGARUH SALINITAS TERHADAP
PREVALENSI EKTOPARASIT PADA IKAN KERAPU MACAN (Epinephelus fuscoguttatus)
Kategori : SKRIPSI
Nama : RESTI FAUZIAH
Nomor Induk Mahasiswa : 070805047
Program Sudi : SARJANA (S1)
Departemen : BIOLOGI
Fakultas : MATEMATIKA DAN ILMU PENGETAHUAN
PERNYATAAN
PENGARUH SALINITAS TERHADAP PREVALENSI EKTOPARASIT PADA
IKAN KERAPU MACAN (Epinephelus fuscoguttatus)
SKRIPSI
Saya mengakui bahwa skripsi ini adalah hasil kerja saya sendiri, kecuali beberapa
kutipan dan ringkasan yang masing-masing disebutkan sumbernya.
Medan, November 2011
RESTI FAUZIAH
PENGHARGAAN
Puji dan syukur penulis sampaikan ke hadirat Allah SWT Yang Maha Pengasih lagi Maha Penyayang atas rahmat dan karunia-Nya, penulis dapat menyelesaikan skripsi yang berjudul “PENGARUH SALINITAS TERHADAP PREVALENSI EKTO PARASIT PADA IKAN KERAPU MACAN (Epinephelus fuscoguttatus) “ sebagai salah satu syarat untuk meraih gelar sarjana Biologi, Fakultas Matematika dan Ilmu Pengetahuan Alam Universitas Sumatera Utara Medan. Serta shalawat beriring salam penulis hanturkan kepada Nabi Muhammad SAW yang telah membawa manusia dari zaman kebodohan menuju zaman berilmu saat ini.
Dalam kesempatan ini penulis ingin mengucapkan terimakasih yang sebesar-besarnya kepada: Prof. Dr. Dwi Suryanto M.Sc sebagai Dosen Pembimbing 1, dan Bapak Dedy Arief Hendriyanto S.St,Pi. M.Siselaku Dosen Pembimbing 2. Kepada Dra. Nunuk Priyani, M.Sc dan Bapak Prof. Syafruddin Ilyas M.Biomed selaku Dosen Penguji yang telah memberikan banyak saran dan arahan dalam penulisan skripsi ini juga kepada Bapak Riyanto Sinaga, S.Si selaku Dosen Penasehat Akademik. Ketua Departemen Biologi, Ibu Dr. Nursahara Pasaribu, M.Sc serta seluruh staff pengajar dan pegawai di Departemen Biologi.
Penulis juga mengucapkan terima kasih kepada Ibu Nurhasni Muluk selaku aboran di aboratorium Mikrobiologi FMIPA USU serta kepada Ibu Roslina Ginting dan Bang Endra Raswin selaku Pegawai Administrasi Program Studi Biologi FMIPA USU. Terima kasih atas keluangan waktu dan keikhlasan dalam membantu penulis selama ini.
Secara khusus penulis ucapkan terima kasih kepada Bapak Ir. Viktor Immanuel selaku Kepala Balai Karantina Ikan Kelas I Polonia Medan, Ibu Barita Aritonang, Pak Ramon Nasution, Bang Sahala Sianturi, Ibu Marlina Dolok, Kak Retna, Kak Atika, Pak Oscar, Pak Su, Pak Akum, Bg Joko, Bg Randy, Bg Wisran, Kak Puji dan Kak Yuni yang banyak memberikan masukan dan arahan kepada penulis selama melakukan penelitian. Kepada adik-adik dari SMKN 1 Kisaran: Nico, Dedi, Eva, Kesy dan Adik-adik dari SMKN 2 Tanjung Balai: Sinta, Dera, Fitri, terima kasih buat kerjasama dan bantuannya. Serta rekan seperjuangan Helmi Kristina Simamora dan Laura Aprilini terima kasih atas kerjasama dan kebersamaannya selama ini.
selalu melimpahkan kebaikan dan rahmat kepada keluarga kita. Amin. serta keponakanku Azura dan Azmi atas setiap canda tawa pelipur lara penulis.
Terima kasih penulis ucapkan kepada saudariku Rysa, Dwi, Riwil dan Anti atas suka duka dan tawa yang telah kita lewati bersama, semoga ikatan persaudaraan di hati kita tidak akan pernah lekang oleh waktu. Teman-teman Like D’Ants Crew 2007: Maika, Putri, Aini, Nila, Irma, Desy, Maria, Helmi, Laura, Yanti, Abel, Misel, Adeka, Risma, Umi, Nia, Tika, Nisa, Sari, Else, Hotda, Siti, Natal, Ibeth, Katrina, Marie, Astri, Yeni, Erlinda, Fatma, Dina, Affan, Asril, Mirza, Ncay, Jayana, Jupe, Reymond, Farid, Alex, terimakasih atas pertemanan yang indah sejak awal perkuliahan.
Kepada kakak-kakak di MSC (Microbiology Study Club) Bang Yopi, Bang Kabul, Bang Fendi, Kak Utien, Kak Imus, Kak Sarah, Kak Netti untuk segala ilmu yang telah diberikan. Kepada BFS (Bengkel Fotografi Sains) Crew Bang Ayul, Bang Panji, Bang Koto, Bang Ferdi, Mas Edi, Bang Andi, Bang Juned, Bang Zulfan, Kak Diah, Kak Atika, Kak Ummi, Eka, Dewi, Nopi, Sirma dan Andini atas kebersamaan dan momen yang indah. Kepada rekan-rekan di laboratorium mikrobiologi Asril, Mirza, Affan, Yanti, Nila, Ria, Nina, Ayu dan Frans terimakasih atas segala bantuan yang diberikan selama ini, jangan pernah berhenti berjuang.
Kepada kakak stambuk 2006 Kak Ami, Kak Nikmah, Kak Ika, Kak Yayan, Kak Nana, Kak Siti, Kak Sari, Kak Lia, Kak Reni, Kak Vita, Bg Kasbi terima kasih atas arahan dan masukannya selama ini, kepada Ibu-ibu S2: Kak Wiwin, Kak Yuni, Bu Siti, Bu Rita, Bu Yunilas dan Bang Rizki kehadiran kalian telah memberi warna tersendiri di hati penulis. Untuk MO Community Yekti, Nina, Bowo, Rio, Ial, Dedi, Dwi, Rudi terima kasih atas semua yang telah kita lewati bersama.
Penulis juga mengucapkan terimakasih kepada saudaraku di UKMI AL- FALAK FMIPA USU: Ukhti Sri. Heni, Kiki. Lia, Arni, Rini, Ayu, Nova, Minah, Evie, Titin, Dilla, Kak Nana, Kak Yossi, Kak Shinta, Kak Halimah, Kak Tika, Kak Muti serta Akh Agus, Emir, Yudha, Heru, Subhan, Adam, Zubeir dan Ganda atas silaturrahmi yang selama ini terjalin.
Terima kasih penulis ucapkan kepada guru penulis semenjak SD, SMP sampai SMA atas segala ilmu yang telah diberikan secara ikhlas tanpa pamrih. Tanpa kalian mungkin penulis tidak akan menjadi seperti sekarang. Kalianlah pahlawan tanpa tanda jasa di hati penulis. Semoga skripsi ini bermanfaat untuk semua pihak, dan mohon maaf atas segala kekurangan selama ini. Amin ya Rabbal Alamin.
Medan, November 2011
PENGARUH SALINITAS TERHADAP PREVALENSI EKTOPARASIT PADA BENIH KERAPU MACAN (Epinephelus fuscoguttatus)
ABSTRAK
Tujuan penelitian ini adalah untuk mengetahui jenis serangan ektoparasit serta untuk mengetahui pengaruh salinitas terhadap prevalensi ektoparasit pada ikan kerapu macan. Penelitian ini dilaksanakan di Laboratorium Parasitologi, Balai Karantina Ikan Kelas I Polonia, Medan dari bulan Januari sampai Juni 2011. Pemeriksaan ektoparasit menggunakan metode kerokan kulit dan metode mount insang, dan analisis data menggunakan uji chi square dengan 6 perlakuan yaitu 20, 25, 30, 35, 40 dan 45 ppt, masing-masing dengan 4 kali ulangan. Wadah yang digunakan pada penelitian ini adalah akuarium yang diisi air dengan volume 20 liter dan tiap wadah diisi dengan 10 ekor ikan. Ikan yang digunakan berukuran ± 10 cm. Pengamatan terhadap perkembangan parasit dilakukan setiap 2 minggu sekali. Dari total ikan yang diperiksa diperoleh prevalensi tertinggi pada Oodonium sp. 14,48 %, Trichodina sp. 14,21 %, Diplectanum sp. 12,69 dan prevalensi terendah pada Benedenia sp. 12,49 %. Pada salinitas 30-35 ppt terjadi penurunan tingkat infeksi ektoparasit terhadap kerapu macan yang baik untuk penurunan prevalensi ektoparasit.
INFLUENCE OF SALINITY IN PREVALENCE ECTOPARASITES AT THE SEED OF TIGER GROUPER (Epinephelus fuscoguttatus)
ABSTRACT
This study was conducted to know ectoparasites infecting tiger grouper, and the influence of salinity in ectoparasites prevalency in the tiger gouper. The study was conducted at Parasitology Laboratorium, Fish Quarantine, First Class in Polonia-Medan from January to June 2011. Double layer slide glass method and gill mount methods were used to examine ectoparasite prevalency. Chi-square analysis was utilized to compare all treatment of salinity (20, 25, 30, 35, 40 and 45 ppt). Ten fish of ±10 cm was used. Observation was done every two weeks during six weeks of study. The result showed that salinity affected the ectoparasites prevalency. Ectoparasites were found in two of the body, in the surface and gills. Oodonium sp., Trichodina sp. and Diplectanum sp. showed relatively high prvelency by 14,48 %, 14,21 % and 12,69 %, respectively Benedenia sp. showed low prevalency by 12,49 %. Salinity at 35 ppt showed relatively lower prevalency compared to other salinity.
DAFTAR ISI
Halaman
PERSETUJUAN ii
PERNYATAAN iii PENGHARGAAN iv ABSTRAK vi ABSTRACT vii
DAFTAR ISI vii
DAFTAR TABEL x DAFTAR GAMBAR xi
DAFTAR LAMPIRAN xii
BAB 1 PENDAHULUAN 1 1.1Latar Belakang 1
1.2Permasalahan 2
1.3Tujuan Penelitian 3 1.4Hipotesis 3 1.5Manfaat Penelitian 3
BAB 2 TINJAUAN PUSTAKA 4 2.1 Ikan Kerapu Macan (Epinephelus fuscoguttatus) 4 2.2 Salinitas Air 6
2.3 Penyakit Akibat Infeksi Parasit 7
2.4 Hubungan antara Inang dan Parasit 8
2.5 Ektoparasit pada Kerapu Macan 9
BAB 3 BAHAN DAN METODE 11
3.1 Waktu dan Tempat 11
3.2 Alat dan Bahan 11
3.2.1 Alat 11
3.3.2 Bahan 11
3.3 Metode Penelitian 11
3.3.1 Pemeriksaan Sampel 12
3.3.2 Pemeriksaan Ektoparasit 12
3.3.2.1 Metode Kerokan Kulit (Double Layer Slide Glass Method) 12
3.3.2.2 Meode Mount Insang 13
3.4 Gejala Klinis 13
3.5 Pengukuran Nilai Prevalensi 13
3.6 Analisis Data 13 BAB 4 HASIL DAN PEMBAHASAN 15
4.1 Identifikasi dan Deskripsi Jenis Ektoparasit 15
4.1.1 Jenis Ektoparasit Insang 15
4.1.2 Jenis Ektoparasit Kulit 17
4.2 Prevalensi Ektoparasit terhadap Salinitas 20
BAB 5 KESIMPULAN DAN SARAN 26
5.1 Kesimpulan 26
5.2 Saran 26
DAFTAR PUSTAKA 27
LAMPIRAN 32
DAFTAR TABEL
Halaman
Tabel 1. Prevalensi Trichodina sp. 20
Tabel 2. Prevalensi Oodonium sp. 20
Tabel 3. Prevalensi Diplectanum sp. 21
Tabel 4. Prevalensi Benedenia sp. 21
DAFTAR GAMBAR
Halaman
Gambar 1. Pola hubungan interaksi antara patogen penyakit, inang dan lingkungan
2
Gambar 2 Jenis-jenis ektoparasit pada kerapu macan 9
Gambar 3. Infeksi Diplectanum sp. 16
Gambar 4. Infeksi Oodonium sp. 17
Gambar 5. Trichodina sp. 18
Gambar 6. Infeksi Trichodina sp. 18
Gambar 7. Infeksi Benedenia sp. 19
Gambar 8. Histogram kerapu macan yang terinfeksi ektoparasit berdasarkan kadar salinitas
DAFTAR LAMPIRAN
Halaman
Lampiran A. Kaidah pengambilan sampel 32
Lampiran B. Alur kerja kerokan kulit dan mount insang 33
Lampiran C. Data pengamatan mingguan ektoparasit 35
Lampiran D. Tabel chi square 36
Lampiran E. Dokumentasi Penelitian 37
38
PENGARUH SALINITAS TERHADAP PREVALENSI EKTOPARASIT PADA BENIH KERAPU MACAN (Epinephelus fuscoguttatus)
ABSTRAK
Tujuan penelitian ini adalah untuk mengetahui jenis serangan ektoparasit serta untuk mengetahui pengaruh salinitas terhadap prevalensi ektoparasit pada ikan kerapu macan. Penelitian ini dilaksanakan di Laboratorium Parasitologi, Balai Karantina Ikan Kelas I Polonia, Medan dari bulan Januari sampai Juni 2011. Pemeriksaan ektoparasit menggunakan metode kerokan kulit dan metode mount insang, dan analisis data menggunakan uji chi square dengan 6 perlakuan yaitu 20, 25, 30, 35, 40 dan 45 ppt, masing-masing dengan 4 kali ulangan. Wadah yang digunakan pada penelitian ini adalah akuarium yang diisi air dengan volume 20 liter dan tiap wadah diisi dengan 10 ekor ikan. Ikan yang digunakan berukuran ± 10 cm. Pengamatan terhadap perkembangan parasit dilakukan setiap 2 minggu sekali. Dari total ikan yang diperiksa diperoleh prevalensi tertinggi pada Oodonium sp. 14,48 %, Trichodina sp. 14,21 %, Diplectanum sp. 12,69 dan prevalensi terendah pada Benedenia sp. 12,49 %. Pada salinitas 30-35 ppt terjadi penurunan tingkat infeksi ektoparasit terhadap kerapu macan yang baik untuk penurunan prevalensi ektoparasit.
INFLUENCE OF SALINITY IN PREVALENCE ECTOPARASITES AT THE SEED OF TIGER GROUPER (Epinephelus fuscoguttatus)
ABSTRACT
This study was conducted to know ectoparasites infecting tiger grouper, and the influence of salinity in ectoparasites prevalency in the tiger gouper. The study was conducted at Parasitology Laboratorium, Fish Quarantine, First Class in Polonia-Medan from January to June 2011. Double layer slide glass method and gill mount methods were used to examine ectoparasite prevalency. Chi-square analysis was utilized to compare all treatment of salinity (20, 25, 30, 35, 40 and 45 ppt). Ten fish of ±10 cm was used. Observation was done every two weeks during six weeks of study. The result showed that salinity affected the ectoparasites prevalency. Ectoparasites were found in two of the body, in the surface and gills. Oodonium sp., Trichodina sp. and Diplectanum sp. showed relatively high prvelency by 14,48 %, 14,21 % and 12,69 %, respectively Benedenia sp. showed low prevalency by 12,49 %. Salinity at 35 ppt showed relatively lower prevalency compared to other salinity.
BAB 1
PENDAHULUAN
1.1 Latar Belakang
Ikan kerapu macan (Ephinephelus fuscoguttatus) merupakan salah satu jenis ikan laut
yang mempunyai nilai ekonomi tinggi, karena sangat disukai didalam maupun di luar
negeri seperti negara-negara Asean, Hongkong, Cina, dan Jepang. Budidaya ikan ini
sangat potensial akan tetapi masih terkendala dengan rentannya penyakit terutama
oleh bakteri dan pertumbuhannya relatif agak lambat (Feliatra, 2002).
Penyakit ikan merupakan salah satu masalah serius yang harus dihadapi dalam
pengembangan usaha budidaya ikan. Kerugian yang diakibatkan oleh penyakit ikan
selain dapat mematikan ikan juga dapat menurunkan mutu dari ikan itu sendiri.
Kematian yang ditimbulkan oleh penyakit ikan sangat tergantung pada jenis penyakit
ikan yang menyerang, kondisi ikan dan kondisi lingkungan. Apabila kondisi
lingkungan menurun maka kematian yang diakibatkan oleh wabah penyakit sangat
tinggi, tapi sebaliknya apabila kondisi lingkungan baik maka kematian akibat infeksi
suatu penyakit lebih rendah. Tinggi rendahnya kematian akibat infeksi suatu penyakit
juga tergantung pada kondisi immunitas ikan. Wabah penyakit yang terjadi pada
kondisi ikan sedang sehat tidak akan mengakibatkan kematian yang tinggi, dan
sebaliknya akan mengakibatkan kematian yang tinggi apabila kondisi ikan kurang
sehat (Supriyadi, 2007). Penyakit akibat infestasi parasit merupakan penyakit yang
sering dijumpai pada kegiatan budidaya ikan laut (Koesharyani et al., 2001).
Menurut penyebabnya, penyakit ikan dibedakan atas penyakit infeksi dan non
infeksi. Penyakit infeksi disebabkan oleh jasad parasitik, bakteri, jamur dan virus.
Penyakit parasiter yaitu penyakit akibat infeksi jasad parasitik seperti golongan
parasitik meliputi sporozoa, ciliata dan flagellate, sedangkan metazoa meliputi
crustacea dan isopoda. Jasad parasiter tersebut dapat menginfeksi ikan air tawar
maupun ikan laut (Taukhid, 2006).
Jika terjadi tekanan lingkungan (akibat perubahan mendadak dan pemakaian
antibiotik pada budidaya di pertambakan) dan perairan tidak dalam keadaan seimbang
dinamis (Stady state), maka ikan akan mengalami perubahan fisiologis. Kerentanan
ikan sebagai hospes atau inang juga sangat ditentukan oleh kualitas air sebagai media
hidupnya (Adji, 2008). Organisme yang hidup di laut atau perairan payau (Estuarine)
hanya dapat bertahan pada perubahan-perubahan salinitas yang relatif kecil, hal
tersebut sangat berhubungan dengan tekanan osmotik sel (Hutabarat, 1984).
1.2Permasalahan
Diketahui bahwa adanya parasit mampu muncul pada kondisi yang kurang baik di
lingkungan. Hal ini menjadi salah satu pemicu akan penyakit ikan baik dari segi
budidaya maupun nilai ekonomis. Munculnya suatu penyakit pada organisme
disebabkan oleh adanya interaksi tiga unsur yang bekerja secara bersamaan, yaitu
unsur lingkungan, patogen dan inang (organisme budidaya). Hubungan tersebut dapat
digambarkan pada gambar 1.
Gambar 1. Pola hubungan interaksi antara patogen penyakit, inang dan lingkungan (Lio-Po et al., 2001)
Host Patogen
Environment
Munculnya penyakit parasiter merupakan hasil interaksi antara kondisi
lingkungan budidaya yang tidak mendukung kehidupan di dalamnya, ikan (inang)
yang rentan dan adanya parasit (patogen). Pada kondisi lingkungan yang jelek ikan
menjadi stress sehingga daya tahan tubuhnya lemah dan memudahkan patogen
menyerang inang (Sindermann, 1990).
Kualitas lingkungan perairan merupakan suatu kelayakan lingkungan perairan
untuk menunjang kehidupan dan pertumbuhan organisme air yang nilainya
dinyatakan dalam suatu kisaran tertentu. Sementara itu, perairan ideal adalah perairan
yang dapat mendukung kehidupan organisme dalam menyelesaikan daur hidupnya
(Boyd, 1979). Kondisi lingkungan atau kualitas air yang buruk termasuk fluktuasi
suhu yang terlalu tinggi dan salinitas juga merupakan penyebab ikan stress (Kordi,
2004).
1.3Tujuan
Adapun tujuan dalam penelitian ini adalah :
Untuk mengetahui jenis ektoparasit pada kerapu macan serta mengetahui ada
tidaknya pengaruh salinitas terhadap prevalensi ektoparasit pada kerapu macan.
1.4 Hipotesis
Ada pengaruh salinitas terhadap prevalensi dari ikan kerapu macan terhadap
ektoparasit yang beragam.
1.5 Manfaat
Adapun manfaat dari penelitian ini adalah:
1. Sebagai indikator bahwa lingkungan perairan sekitar budidaya telah menurun
ditandai dengan adanya ektoparasit pada prevalensi dan intensitas tertinggi.
2. Sebagai bahan informasi bagi stake holder / pembudidaya terkait penyakit parasit
BAB 2
TINJAUAN PUSTAKA
2.1 Kerapu Macan
Perairan Indonesia terletak di antara dua Samudera, Samudera Indonesia dan
Samudera Pasifik dengan panjang garis pantai lebih dari 80.000 km yang banyak
terdiri dari perairan karang sehingga dapat dijumpai berbagai jenis ikan karang,
termasuk ikan kerapu (Serranidae). Ikan tersebut bersifat karnivora, rakus dan dapat
memangsa berbagai jenis ikan, cephalopoda, crustacea, dan lain-lain (Munro, 1967).
Ikan kerapu macan mempunyai ukuran tubuh yang relatif lebih besar dan
pertumbuhan lebih cepat dibandingkan dengan jenis ikan lain (Sunaryat & Minjoyo,
2004). Ikan kerapu merupakan salah satu komoditas yang potensial untuk
dikembangkan budidayanya karena harganya cukup mahal. Kebutuhan ikan kerapu
hidup semakin meningkat baik untuk konsumsi lokal maupun ekspor (Nurjana, 2007
dalam Bunga, 2008).
Ikan kerapu di Indonesia umumnya mempunyai daerah penyebaran di perairan
karang-karang di seluruh perairan Indonesia diantaranya di Teluk Banten, Ujung
Kulon, Kepulauan Riau, Kepulauan Karimun Jawa, NTB (Manyunar et al., 1991).
Dan di seluruh perairan Indo-Pasifik lainnya seperti Teluk Benggala, Teluk Siam,
sepanjang Laut Cina, selat dan bagian perairan utara Australia (Djamali et al., 1998).
Menurut Dennis et al., (2006), ciri-ciri morfologis ikan kerapu macan adalah
bentuknya agak bulat memanjang dan mempunyai ukuran badan lebih tinggi, sirip
dada berwarna kemerahan dan sirip lainnya mempunyai tepi kecoklatan.
Ikan kerapu termasuk ikan pemakan aktif dan sensitif terhadap perubahan
kualitas air yang fluktuatif, perlu cahaya tetapi tidak langsung dari matahari, hidup di
rata-rata maksimal 90 cm. Tubuh kerapu macan dipenuhi sisik yang berukuran
kecil yang berbentuk sikloid. Nama kerapu diberikan biasanya untuk empat genus
Serranidae yaitu Epinephelus, Variola, Plectropampus dan Cromileptes. Di Indonesia
Epinephelus sendiri mempunyai 38 spesies. Sebagian besar famili Serranidae hidup di
perairan dangkal dengan dasar pasir berkarang, walaupun beberapa jenis dapat
ditemukan di perairan dalam (Burgess et al., 1990). Menurut Heemstra & Randall
(1999), ikan kerapu berjumlah 110 jenis dari 11 genus seperti Aethaloperca,
Anyperodon, Cephalopolis, Cromileptes, Dermatolepis, Ephinephelus, Gracila,
Plectropomus, Saloptia, Triso, dan Variola.
Kerapu macan memiliki sirip dorsal (punggung), sirip anal (perut), sirip
pektoral (dada), sirip garis lateral (gurat sisi) dan sirip caudal (ekor). Sirip dorsal
memanjang hampir sepanjang bagian punggung, bagian jari-jari kerasnya memiliki
jumlah yang sama dengan jari-jari lunaknya, jumlah jari-jari adalah 13-15 buah. Sirip
anal terdiri dari 3 buah jari-jari. Sedangkan jumlah jari-jari di sirip ekor adalah 15-17
buah dan bercabang dengan jumlah 13-15 buah. Sisik yang menutupi seluruh
permukaan tubuh berbentuk kecil, mengkilat dengan bentuk sikloid. Warna dasar
kerapu macan adalah cokelat, dengan perut berwarna putih serta bercak hitam dan
putih disekujur tubuh yang tidak beraturan. Bentuk badan kerapu macan memanjang
dan cenderung gepeng (compressed) atau agak membulat. Ketebalan tubuh 2,6 – 2,9
cm dari panjang standar, dengan skala garis lateral adalah 53-58 cm. Panjang total
tubuh kerapu macan dapat mencapai 80 cm. Mulut berukuran lebar dengan posisi
serong keatas dan bibir bawah menonjol keatas. Lubang hidung besar berada diatas
mulut berbentuk bulan sabit (Abduh, 2007).
Laju pertumbuhan ikan kerapu yang dibudidaya sangat lambat, seperti yang
dilaporkan oleh Soni (2002), ikan kerapu macan laju pertumbuhannya 0,45 g/hari dan
sebesar 0,60 g/hari, sedangkan kerapu lumpur sebesar 0,61 g/hari. Laju pertumbuhan
tersebut dapat menyebabkan biaya operasional menjadi tinggi sehingga kurang
menguntungkan secara ekonomis. Namun demikian sebagian pertumbuhan ikan
kerapu akhir-akhir ini sudah menunjukkan peningkatan. Akbar & Sudaryanto (2001)
melaporkan bahwa ikan kerapu macan laju pertumbuhannya 2,30 g/hari, sedangkan
2.2 Salinitas Air
Salinitas adalah komposisi ion-ion dalam perairan (Wetzel, 1983). Ion-ion yang
terdapat dalam perairan laut terdiri dari enam elemen, yaitu klorin, sodium,
magnesium, sulfur, kalsium dan potassium. Menurut Dawes (1993), salinitas
merupakan faktor kimia yang mempengaruhi sifat fisik air, diantaranya adalah tekanan
osmotik dan densitas air. Salinitas perairan laut yang normal berkisar antara 33 ppt
hingga 37 ppt. Salinitas berpengaruh terhadap proses fisiologis seluruh organisme
yang hidup dalam perairan tersebut. Andrews et al., (2003) salinitas atau kadar garam
merupakan jumlah total material terlarut dalam air.
Menurut Subyakto & Cahyaningsih (2003), salinitas ideal untuk pemeliharaan
kerapu adalah 28 – 33 ppt. Salinitas pada penelitian sedikit diatas salinitas optimun
untuk kerapu, tetapi benih kerapu masih bisa beradaptasi terhadap salinitas tersebut.
Sedangkan kondisi lingkungan perairan pada lokasi penangkapan ikan kerapu di alam,
seperti suhu berkisar antara 27-29,62 oC, dengan salinitas berkisar antara 34,259 – 34,351 ‰, oksigen terlarut berkisar antara 3,95 - 4,28 ml/L, nitrat berkisar antara 1-6 μg.at/L dan posfat berkisar antara 0,80 - 1,40 μg.at/L (Langkosono & Wenno, 2003). Menurut Chua & Teng (1978), kualitas perairan yang optimal untuk pertumbuhan ikan
kerapu, seperti suhu berkisar antara 24-31o C, salinitas antara 30-33 ppt, oksigen terlarut > 3,5 ppm dan pH berkisar antara 7,8-8,0. Sementara itu Suprakto & Fahlivi
(2007) melaporkan kualitas air pada lokasi budidaya yaitu kecepatan arus 15-30 cm/s,
suhu 27-29º C, salinitas 30-33 ppt, pH 8,0 - 8,2; oksigen >5 ppm dan kedalaman >
5m.
Menurut Nontji (1993), di samudera salinitas berkisar antara 34 – 35 ppt.
Variasi salinitas di permukaan air sangat mirip dengan keseimbangan evaporasi dan
presipitasi. Salinitas merupakan faktor pembatas bagi organisme perairan terutama
yang berada pada range yang sempit. Densitas air laut naik sejalan dengan kenaikan
salinitas dan tekanan serta penurunan temperatur. Satu bagian per 1000 garam
2.3 Penyakit Akibat Infeksi Parasit
Pertumbuhan ikan dipengaruhi oleh dua faktor, yaitu faktor internal yang meliputi
genetik dan kondisi fisiologis ikan serta faktor eksternal yang berhubungan dengan
lingkungan. Faktor eksternal tersebut yaitu komposisi kualitas kimia dan fisika air,
bahan buangan metabolik, ketersediaan pakan, dan penyakit (Hepper & Prugnin,
1984).
Parasit merupakan suatu organisme yang mengambil bahan untuk kebutuhan
metabolismenya (makanan) dari tubuh inangnya dan merugikan bagi inang tersebut.,
sehingga parasit tidak dapat hidup lama di luar tubuh inangnya (Alifuddin, 2004).
Kisaran batas toleransi temperatur yang sesuai untuk ikan adalah sekitar 20 – 32 oC, sedangkan untuk daerah tropis sebaiknya 27 oC dengan fluktuasi 30 oC (Riani, 2004).
Menurut Supriyadi (2004), berdasarkan sifat hidupnya parasit dapat dibedakan
menjadi dua golongan, yaitu obligat dan fakultatif. Parasit obligat yaitu parasit yang
hanya bisa hidup jika berada pada inang. Parasit fakultatif yaitu parasit yang mampu
hidup di lingkungan air jika tidak ada inang disekitarnya. Ekosistem perairan tambak
merupakan ekosistem binaan yang bertujuan untuk produksi udang maupun ikan.
Menurut Afrianto & Liviawaty (1992), penyakit adalah suatu gangguan pada
organisme yang disebabkan oleh parasit, kekurangan gizi atau faktor fisik dan
lingkungan serta menyebabkan daya tahan tubuh ikan melemah.
Penyakit dalam budidaya ikan dapat menyebabkan kerugian secara ekonomi
yang besar (Sudjiharno, 2003). Menurut Reantoso et al., (2004), mengemukakan
bahwa permasalahan penyakit pada budidaya ikan laut di Asia Timur dan Asia
Tenggara telah diidentifikasi dengan beberapa faktor dalam budidaya yaitu melalui
perbaikan lingkungan (polusi dan racun dari akibat kelimpahan plankton) dan
perbaikan manajemen (aklimatisasi, penanganan mortalitas dan tranportasi mortalitas)
pada juvenil. Program manajemen kesehatan harus memenuhi beberapa persyaratan
dan dapat mencakup semua aktifititas budidaya. Pada tingkat produksi, syarat yang
harus dipenuhi adalah pemilihan benih, nutrisi, penanganan limbah, optimalisasi
2.4 Hubungan antara Inang dan Parasit
Pengertian inang menurut Kusumah (1976), adalah organisme hidup yang
dipendeki (ditempati) oleh parasit. Antara inang dan parasit terdapat hubungan
simbiosis parasitisme yaitu bentuk kehidupan bersama antara dua spesies organisme
yang berbeda atau lebih dan organisme yang ditumpanginya akan mendapat kerugian
karenanya.
Parasit ada di lingkungan perairan seperti juga ikan hidup di lingkungan air.
Jika kualitasnya air jelek mengakibatkan ikan stress, tetapi kondisi ini justru
merupakan media yang baik bagi parasit sehingga mereka berkembang biak dan
populasinya cukup untuk menginfeksi ikan hingga sakit (Taukhid, 2006). Parasit
adalah organisme yang hidupnya dapat menyesuaikan diri dengan inangnya, dan
merugikan organisme yang ditempatinya (inangnya). Dimana inang spesifik sebagai
inang yang dapat menyediakan kebutuhan parasit yang bersangkutan dan parasit
tersebut mempunyai kesempatan untuk masuk ke dalam inang tanpa adanya
hambatan-hambatan (Noble & Noble, 1989).
Salah satu parasit pada ikan kerapu macan adalah dari kelompok protozoa.
Protozoa dicirikan dengan ukurannya yang mikroskopik bersel satu dan termasuk
eukariotik. Ukuran protozoa berkisar dari 1-50 μm atau lebih. Bersifat holozoik atau
sporozoik, tetapi sedikit yang holopitik. Reproduksi organisme ini dapat berlangsung
secara seksual dan aseksual tergantung kepada kelompoknya. Beberapa spesies
protozoa hidup bebas atau bersifat parasit. Kemampuannya yang tinggi untuk
memperbanyak diri pada inang telah menyebabkan parasit protozoa sangat berbahaya
pada ikan (Dana et al., 1994).
Populasi gabungan organisme yang hidup bersama di dalam suatu jaringan
organ insang dikenal sebagai campuran parasit. Selanjutnya dikatakan bahwa, parasit
di dalam inangnya dipengaruhi oleh adanya parasit spesies lain. Infeksi bersama
antara spesies yang berbeda dapat bersifat antagonistik, dimana keberadaan suatu
spesies akan menghambat perkembangan atau dapat bersifat sinergistik atau saling
Menurut Kabata (1985), parasit dapat ditinjau dari tempat hidupnya yaitu
parasit ekto dan endo. Jika ditinjau dari segi siklus hidupnya, Kusumah (1976)
mengatakan ada tiga penggolongan parasit yaitu intermitter parasit yaitu siklus
hidupnya secara periodik dalam waktu tertentu berada di dalam inang, tetapi di waktu
lain meningggalkan inang yang ditumpanginya. Siklus hidup yang lain adalah
fakultatif parasit dimana dapat hidup tanpa organisme lain. Kemudian obligateri
parasit yang mana siklus hidupnya membutuhkan organisme lain dan hidup
selamanya.
2.5 Ektoparasit pada Kerapu Macan
Menurut Widyastuti (2002), bahwa parasit dapat dibedakan menjadi dua yaitu
ektoparasit dan endoparasit. Ektoparasit adalah parasit yang hidup pada permukaan
luar tubuh inang atau di dalam liang-liang kulit yang mempunyai hubungan dengan
dunia luar. Endoparasit yaitu parasit yang hidup pada organ dalam tubuh ikan seperti
hati, limfa, otak dan dalam sistem pencernaan, sirkulasi darah, pencernaan, sirkulasi
darah, pernafasan, dalam rongga perut, otot, daging, dan jaringan tubuh lain.
Ektoparasit merupakan parasit yang menyerang tubuh ikan bagian luar
(Bhagawati et al., 1991). Ektoparasit dapat menyebabkan mortalitas tinggi yang
bersifat akut. Infeksi ektoparasit juga menimbulkan kerugian non letal yaitu
pertumbuhan yang lambat, penurunan efisiensi pencernaan dan faktor predisposisi
bagi infeksi jamur, bakteri dan virus (Sommerville, 1998 dalam Mulia, 2005).
Gambar 2. Jenis-jenis ektoparasit pada kerapu macan 10 x 40 (A. Diplectanum; B. Trichodina sp.)
Monogenea merupakan cacing pipih dengan ukuran panjang 0,15-20 mm
bentuk tubuhnya fusiform, haptor di bagian posterior dan siklus kait sentral sepasang
dan sejumlah kait marginal. Salah satu contoh kelas monogenea yaitu Dactylogyridae
yang mempunyai alat bantu organ tambahan pada tubuhnya yang biasa disebut
squamodis yang berfungsi sebagai perekat, selanjutnya dikatakan bahwa ada sekitar
1500 spesies monogenea yang ditemukan pada ikan (Gusrina, 2008). Menurut Kabata
(1985), bahwa Monogenea umumnya ektoparasit dan jarang bersifat endoparasit.
Monogenea salah satu parasit yang sebagian besar menyerang bagian luar tubuh ikan
(ektoparasit) jarang menyerang bagian dalam tubuh ikan (endoparasit) biasanya
menyerang kulit dan insang. Menurut Noga (1996), monogenea merupakan parasit
yang umum ditemukan di insang dan kulit ikan air tawar maupun laut.
Menurut Prayitno, (1998), parasit monogenea menyebabkan rusaknya insang
ditambah dengan produksi lendir yang berlebihan ini akan mengganggu pertukaran
gas oksigen. Akibatnya sel-sel mati dan tidak berfungsi sehingga ikan akan mati
karena tidak bernafas dengan baik. Ciri ikan yang terserang monogenea adalah
produksi lendir pada bagian epidermis akan meningkat, kulit terlihat lebih pucat dari
normalnya, frekuensi pernapasan terus meningkat karena insang tidak dapat berfungsi
secara sempurna, kehilangan berat badan (kurus) melompat-lompat ke permukaan air
dan terjadi kerusakan berat pada insang.
BAB 3
BAHAN DAN METODE
3.1 Waktu dan Tempat
Penelitian ini dilaksanakan pada bulan Januari 2011 sampai Juni 2011 di
Laboratorium Parasitologi milik Balai Karantina Ikan Kelas I Polonia, Medan.
3.2 Alat dan Bahan 3.2.1 Alat
Adapun alat yang dipakai adalah akuarium (60x 40x 40) cm3, aerator/ filter air, refraktometer, pH meter, termometer, disecting set, scalpel, objek glass, cover glass,
sarung tangan, masker, kamera digital, serokan ikan tanggok, pipet tetes dan
mikroskop Olympus CCTV stereo.
3.2.2 Bahan
Adapun bahan yang dipakai adalah kerapu macan (Epinephelus fuscoguttatus)
sebanyak 240 ekor dengan ukuran panjang ± 10 cm, alkohol 70 %, tissue, kapas,
akuades dan reagen NaCl fisiologis.
3.3 Metode Penelitian
Metode yang digunakan dalam penelitian ini adalah deskriptif komparatif yaitu suatu
metode dalam meneliti status kelompok, suatu objek dengan tujuan untuk membuat
deskripsi atau gambaran secara sistematis dan akurat mengenai fakta maupun sifat
3.3.1 Pengambilan Sampel
Pengambilan sampel dilakukan di Keramba Jaring Apung wilayah Pesisir Timur,
Belawan sebanyak 240 ekor benih kerapu macan dengan ukuran ±10 cm secara acak.
Sebanyak 10 ekor digunakan untuk masing-masing perlakuan salinitasnya, dalam 4
ulangan yang dilakukan setiap 2 minggu sekali. Sampel dimasukkan ke dalam kantong
plastik diberikan oksigen lalu dibawa ke Laboratorium Parasitologi Balai Karantina
Ikan Kelas I Polonia, Medan. Kemudian ditampung dalam akuarium berukuran
(60x40x40) cm3 sebanyak 24 buah. Sebelum digunakan akuarium di desinfeksi dengan KMnO4 5 ppm lalu dibilas dengan air bersih dan dikeringkan. Setelah wadah
disiapkan benih kerapu macan diaklimatisasi untuk penyesuaian salinitas sesuai
perlakuan. Selama proses aklimatisasi kondisi kesehatan ikan dievaluasi.
3.3.2 Pemeriksaan Ektoparasit
Pemeriksaan ektoparasit ini bertujuan mencari dan menentukan ektoparasit pada
bagian tubuh eksternal ikan kerapu macan yaitu sirip, lendir, kulit dan insang yang
menimbulkan gangguan pada kesehatan ikan kerapu macan. Metode yang digunakan
sesuai metode Kabata (1985) dan Purnowati et al., (2002) yang dimodifikasi yaitu
metode kerokan kulit (double layer slide glass method) dan metode mount insang.
Pengamatan dilakukan menggunakan mikroskop dengan pembesaran 10x100.
Identifikasi parasit dilakukan dengan berdasarkan Kabata (1985) dan Dana et al.,
(1984).
3.3.2.1 Metode Kerokan Kulit (Double Layer Slide Glass Method)
Bagian kulit dari kepala sampai ekor dikerok dengan menggunakan scalpel yang
bersih, sehingga diperoleh cairan mucus (lendir), sel epitel serta parasit pada kulit
(kerokan kulit dilakukan dari sisi lateral tubuh, sirip belakang dan pangkal sirip).
Kemudian kerokan diusapkan pada objek glass dan ditetesi dengan NaCl fisiologis
atau akuades sebanyak 2-3 tetes di bagian permukaan usapan dengan menggunakan
pipet tetes hingga merata, kemudian ditutup dengan cover glass. Pengamatan
3.3.2.2 Metode Mount Insang
Sebagian insang dari ikan kerapu macan diambil dengan mengggunakan forcep dan
gunting, kemudian kartilago filament dipotong dengan scalpel dan ditempatkan di
objek glass lalu ditutup dengan cover glass agar filament insang tidak bergerak.
Selanjutnya, teteskan NaCl fisiologis atau akuades sebanyak 2-3 tetes di bawah
usapan sampai merata dengan menggunakan pipet tetes. Pengamatan di lakukan di
bawah mikroskop.
3.4 Gejala Klinis
Pengamatan gejala abnormal ikan kerapu macan setelah terserang ektoparasit
dievaluasi setiap 2 minggu sekali, selama dua bulan. Berdasarkan gejala klinis khas
ektoparasit pada setiap perlakuan secara visual dicatat di tabel pengamatan. Ikan
abnormal yang menunjukkan gejala klinis khas ektoparasit berupa adanya produksi
lendir yang berlebihan, terjadinya luka, dan perubahan warna pada kulit ikan yang
berubah menjadi lebih pucat.
3.5 Pengukuran Nilai Prevalensi
Parameter utama yang diamati dalam penelitian ini meliputi jenis ektoparasit yang
menyerang ikan kerapu macan dan tingkat infeksinya. Menurut Saleh (1996),
prevalensi pada ikan dapat dihitung dengan menggunakan rumus sebagai berikut:
3.6 Analisis Data
Data yang didapat dari setiap pengamatan dicatat dan disusun ke dalam bentuk tabel.
Data dilihat perbandingannya dengan menggunakan Uji Chi Square (non parametrik) Jumlah ikan yang terserang parasit
X 100 % Prevalensi =
untuk pengujian hipotesis melalui adanya perbandingan antara frekuensi observasi
yang benar-benar terjadi / aktual dengan frekuensi harapan/ekspektasi. Adapun pada
prevalensi ektoparasit berdasarkan kadar salinitas yang dikaitkan dengan frekuensi
ekspektasi dengan nilai/perbandingan dalam Ho. Derajat bebas (Db) = k-1. Ho
(P<0,05) menyatakan nilai setimbang, pernyataan diterima. Sedangkan H1 (P>0,05)
BAB 4
HASIL DAN PEMBAHASAN
4.1 Identifikasi dan Deskripsi Jenis Ektoparasit
Berdasarkan hasil pengamatan secara mikroskopis terhadap ikan kerapu macan yang
diteliti, diketahui bahwa jenis parasit yang sering menginfeksi insang ikan tersebut
adalah Diplectanum sp. yang merupakan parasit monogenea, Oodonium sp. yang
termasuk ke dalam parasit protozoa filum Sarcomastigophora, dan jenis parasit yang
menyerang permukaan tubuh yaitu Trichodina sp. dari famili Trichodinidae, dan
Benedenia sp. dari famili Capsylidae berdasarkan buku identifikasi Kabata (1985) dan
Dana et al., (1984).
4.1.1 Jenis Ektoparasit Insang
Pengamatan mikroskopik menunjukkan ektoparasit lain yang menyerang kerapu
macan dengan ciri-ciri memiliki alat penempel dengan bentuk tubuh seperti cacing
monogenea dan biasanya menyerang bagian insang. Gejala klinis yang diperoleh
selama penelitian berupa kerusakan pada bagian insang akibat ditumpangi oleh parasit
tersebut. Menurut Rakovac et al, (2002) parasit yang memiliki alat pengait yang
melebar (untuk mengaitkan diri pada inang) yang disebut anchor dan dilengkapi
dengan organ penempel tambahan yang dinamakan lamelle atau squamodisc
merupakan Diplectanum sp. (Gambar 3). Agen infeksi dan kondisi patologis antara
ikan budidaya dan ikan alam mempunyai insidensi berbeda. Diplectanum sp. adalah
parasit monogenea yang menyebabkan reaksi proliferatif sel-sel epitel insang yang
Gambar 3. Diplectanum sp. (10x40)
Parasit monogenea termasuk Diplectanum sp. mempunyai siklus hidup yang
langsung, sederhana, tidak melibatkan inang perantara dan hanya melibatkan satu
inang saja sehingga bila kondisi perkembangannya baik, maka parasit ini akan
berkembang lebih cepat tanpa memerlukan inang perantara (Anshary et al., 2001).
Siklus hidup parasit ini dimulai dari telur parasit yang menetas dalam waktu 5-8 hari
yang berkembang menjadi parasit muda (Oncomiracidia) yang dilengkapi dengan cilia
berfungsi sebagai alat gerak untuk menemukan inang baru, di inang biasanya tumbuh
dan berkembang di bagian insang (Koesharyani, 2001).
Jenis ektoparasit lainnya yang menyerang kerapu macan mempunyai bentuk
bulat dan tidak memiliki flagella. Gejala klinis yang menunjukkan bahwa parasit ini
menyebabkan luka pada bagian tubuh dari ikan kerapu macan. Menurut Kabata (1985)
parasit yang dapat menyebabkan kerusakan pada kulit inang-inangnya adalah rizoid
Oodonium sp. (Gambar 4). Penyakit ini lebih dikenal dengan nama velvet yang
merupakan ektoparasit yang menginfeksi kulit dan insang. Akibat yang ditimbulkan
oleh penyakit ini ikan mengalami anoreksia dan terjadi pendarahan pada insang.
Gejala ikan yang terinfeksi Oodonium dengan kondisi yang sudah parah pada kulitnya
Gambar 4. A. Oodonium sp. (10x10); B. Permukaan tubuh yang luka akibat terinfeksi Oodonium sp.
Dana et al., (1994) mengatakan bahwa Oodonium sp. termasuk ke dalam parasit
protozoa, filum Sarcomastigophora, subfilum Mastigophora, famili Blantoniidae, genus
Oodinium dan spesies Oodinioum sp. Adapun filum Sarcomastigophora ini dibedakan
atas tiga kelompok subfilum yakni Mastigophora, Sarcodina dan Opalinata. Dimana
stadia parasit atau disebut trofont berbentuk bulat. Ukurannya terggantung pada jenis
dan stadia siklus hidupnya berukuran lebar 15-70 μm dan mencapai panjang 150-670 μm. Trofont tidak berflagella sehingga tidak dapat berenang bebas. Trofont biasanya diseliputi oleh suatu membran tipis transparan yang memperlihatkan struktur
sitoplasmik, terdapat bentuk seperti akar (rizoid) yang digunakan untuk melekatkan diri
pada substrat.
4.1.2 Jenis Ektoparasit Kulit
Dari pengamatan ditemukan ektoparasit berbentuk seperti lonceng dan memiliki cilia
pada sisi tubuhnya. Cilia yang digunakan sebagai alat gerak. Pada saat parasit ini
bergerak parasit ini akan melebarkan dan memendekkan tubuhnya. Menurut
Hidayaturrohman (1990), bahwa parasit yang berbentuk seperti lonceng terbalik ini
merupakan Trichodina sp.(Gambar 5). Sisi dorsalnya cembung, dapat dikontraksikan
serta memiliki dua mahkota bercilia. Sisi bagian ventral sedikit cekung dan berfungsi
sebagai alat penghisap. Mulut terdapat di tengah alat penghisapnya dan dikelilingi
oleh cincin yang menempel padanya, terdiri dari 20-30 tanduk-tanduk kecil. Bila
parasit ini memanjangkan atau memendekkan tubuhnya, mulutnya akan melebar atau
menyempit. Parasit ini tidak tahan hidup lama tanpa adanya inang.
[image:32.595.109.517.85.210.2]
Gambar 5. Trichodina sp. (10x10)
Menurut Irianto, (2005) Trichodina sp. merupakan jenis Protozoa dari
kelompok Ciliata yang memiliki bulu getar, memiliki bentuk badan seperti cawan, berdiameter 5μm, dengan bulu getar terangkai pada kedua sisi sel. Trichodina sp. merupakan parasit yang mudah memisahkan diri menjadi dua bagian yang lebih kecil
dan kemudian masing-masing bagian akan kembali memperbanyak diri. Menurut
Kabata (1985), Trichodina sp. termasuk dalam famili Trichodinidae, sub ordo
Mobilina, ordo Petrichida dan kelas Ciliophora.
Secara visual selama penelitian jenis ektoparasit ini menyerang ikan kerapu
macan dengan menampakkan gejala klinis seperti adanya warna pada permukaan
tubuh yang memucat jika dibandingkan dengan ikan yang normal (Gambar 6) dan
gejala lainnya seperti adanya bagian tubuh ikan yang rusak atau mengalami luka
akibat sering menggosok-gosokkan tubuh pada permukaan akuarium. Dari
pemeriksaansecara mikroskopik Trichodina sp. banyak ditemukan pada bagian kulit
serta insangdari ikan kerapu macan yang diserang.
Gambar 6. A. Infeksi Trichodina sp. warna tubuh ikan menjadi pucat, B. Warna tubuh ikan kerapu macan normal
Menurut Afrianto & Liviawaty (1992), Trichodina sp. menyebabkan penyakit
gatal (Trichodinasis) pada ikan dan pada bagian tubuh ikan yang diserangnya terutama
kulit, sirip dan insang. Kabata (1985), menyatakan bahwa ikan yang terkena infeksi
Trichodina sp. menyebabkan sirip ikan menjadi rusak, demikian pula pada insangnya.
Bila sudah demikian, kehadiran bakteri dan jamur sebagai agen penyakit sekunder
sangat besar kemungkinan menyerang kulit dan menyerang ikan dalam skala
pembenihan.
Klinger & Floyd (1998) mengatakan bahwa Trichodina sp. merupakan salah
satu parasit yang sering menyerang ikan budidaya, terutama bagian kulit dan insang.
Infeksi dalam jumlah yang sedikit tidak akan mengakibatkan kerugian pada budidaya
ikan. Namun, jika ikan mengalami stress atau kualitas air menurun, maka parasit ini
akan berkembang biak dengan cepat dan mengakibatkan kerugian yang besar. Lebih
lanjut dinyatakan bahwa infeksi dalam jumlah yang besar akan mengakibatkan ikan
tampak pucat, nafsu makan turun dan sensitif terhadap infeksi bakteri.
Dari hasil pengamatan secara mikroskopik ditemukan jenis ektoparasit lainnya
yang menyerang kerapu macan dengan bentuk bentuk pipih seperti cacing yang
memiliki alat pengait pada bagian posterior tubuhnya dengan gejala infeksi pada ikan
kerapu macan yang terserang seperti pernafasan ikan meningkat dan produksi lendir
yang berlebihan pada permukaan tubuh inang yaitu Benedenia yang banyak
menyerang bagian insang dan permukaan tubuh ikan. Ciri-cirinya memiliki panjang
1,4-2,7 mm, bentuk pipih agak oval, bagian anterior terdapat sepasang alat penempel,
sedangkan pada bagian posterior terdapat haptor yang dilengkapi dengan sepasang alat
pengait (Zafran, 1998) pada Gambar 7.
Dibandingkan dengan parasit insang, parasit kulit yang ditemukan pada ikan
budidaya jenisnya sangat sedikit, dan umumnya jenis yang banyak ditemukan adalah
Bendenia sp. yang merupakan skin monogenetic trematodes atau disebut juga parasit
kulit, karena banyak ditemukan pada lendir tubuh ikan atau bagian kulit tubuh ikan.
Menurut Kabata, (1985) bahwa ektoparasit Benedenia termasuk ke dalam ordo
Dactylogridae, famili Capsylidae, genus Benedenia dan spesies Benedenia sp.
Menurut Gusrina (2008), bahwa Benedenia sp. sering menyerang ikan kerapu macan
terutama di bagian kulit dan insang dan menyerang kulit bahkan beberapa ikan yang
terserang parasit ini menunjukkan gejala klinis abnormal pada mata yaitu terjadi
kebutaan. Insang merupakan organ penting yang sangat dibutuhkan oleh organisme
perairan sebab insang merupakan organ primer untuk pertukaran gas-gas juga
berperan dalam proses osmoregulasi.
4.2Prevalensi ektoparasit terhadap salinitas
Dari pengamatan diperoleh bahwa terjadi prevalensi ektoparasit terhadap salinitas
pada parasit Trichodina (Tabel 1) Oodonium (Tabel 2) Diplectanum (Tabel 3) dan
[image:35.595.103.531.502.612.2]Benedenia (Tabel 4).
Tabel 1. Prevalensi parasit Trichodina sp.
Salinitas (ppt)
oi Ei (oi-ei) (oi-ei)2 (oi-ei)2/ei
20 0.125 0.03 0.095 9.02x10-3 0.30
25 0.20 0.03 0.17 0.028 0.96
30 0.275 0.03 0.245 0.06 2
35 0.30 0.03 0.27 0.073 2.43
40 0.375 0.03 0.345 0.12 3.96
45 0.40 0.03 0.37 0.137 4.56
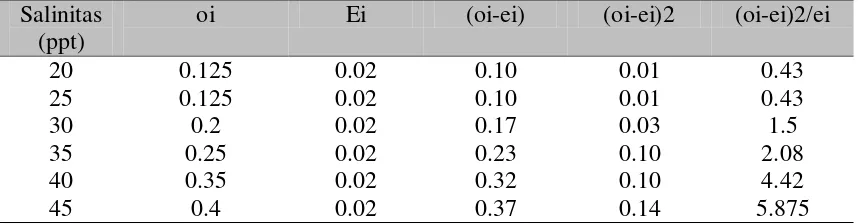
Tabel 2. Prevalensi parasit Odonium sp.
Salinitas (ppt)
oi Ei (oi-ei) (oi-ei)2 (oi-ei)2/ei
20 0.125 0.02 0.10 0.01 0.43
25 0.125 0.02 0.10 0.01 0.43
30 0.2 0.02 0.17 0.03 1.5
35 0.25 0.02 0.23 0.10 2.08
40 0.35 0.02 0.32 0.10 4.42
[image:35.595.103.532.654.766.2]Tabel 3. Prevalensi parasit Diplectanum
Salinitas (ppt)
oi Ei (oi-ei) (oi-ei)2 (oi-ei)2/ei
20 0.125 0.02 0.105 0.01 0.5
25 0.175 0.02 0.155 0.02 1.2
30 0.2 0.02 0.18 0.03 1.5
35 0.25 0.02 0.22 0.053 2.65
40 0.3 0.02 0.28 0.078 3.92
45 0.3 0.02 0.28 0.078 3.92
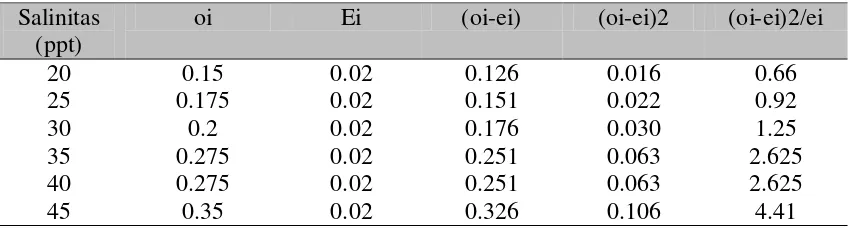
Tabel 4. Prevalensi parasit Benedenia
Salinitas (ppt)
oi Ei (oi-ei) (oi-ei)2 (oi-ei)2/ei
20 0.15 0.02 0.126 0.016 0.66
25 0.175 0.02 0.151 0.022 0.92
30 0.2 0.02 0.176 0.030 1.25
35 0.275 0.02 0.251 0.063 2.625
40 0.275 0.02 0.251 0.063 2.625
45 0.35 0.02 0.326 0.106 4.41
Dari tabel di atas dapat diketahui bahwa adanya perbedaan nilai antara
masing-masing parasit. Pada Trichodina nilai prevalensi tertinggi pada salinitas 45 ppt yaitu
sebesar 4,56 dan terendah pada salinitas 20 ppt yaitu 0,3; sedangkan pada Oodonium
nilai prevalensi terendah pada salinitas 20-25 ppt yaitu 0,43 dan tertinggi pada
salinitas 45 ppt yaitu 5,875. Diplectanum memiliki nilai prevalensi terendah pada
salinitas 20 ppt yaitu 0,5 dan tertinggi pada salinitas 40-45 ppt sama yaitu 3,92. Hal ini
juga terjadi pada Benedenia yang memiliki nilai prevalensi terendah pada salinitas 20
ppt yaitu 0,66 dan tertinggi pada salinitas 45 ppt yaitu 4,41.
Hasil uji chi square menunjukkan perbedaan prevalensi ektoparasit pada
tingkat salinitas berbeda (p<0,05). Salinitas merupakan salah satu faktor lingkungan
yang berpengaruh pada kehidupan organisme akuatik. Menurut Buchmann (1988
dalam Bunga, 2008) bahwa parasit mempunyai tingkat infeksi yang berbeda
berdasarkan umur, panjang dan berat ikan. Dari pengamatan selama penelitian
diperoleh 235 ekor kerapu macan terinfeksi ektoparasit, sedangkan 5 ekor dari benih
kerapu macan tidak ditemukan parasitnya. Namun ditemukan kista yang belum dapat
diidentifikasi yang dapat dijumpai pada salinitas 20 ppt di minggu awal pengamatan
[image:36.595.106.530.259.373.2]jumlah ikan yang terinfeksi sedikit dan pada salinitas 40-45 ppt terdapat tingkat infeki
ektoparasit yang tinggi dari setiap minggunya. Keseimbangan air pada ikan tergantung
pada kadar garam air tersebut. Ikan di laut seringkali menghadapi masalah yang
berlawanan dengan menahan air tubuh mereka dengan adanya air laut yang tingi kadar
garamnya. Semakin jauh perbedaan tekanan osmotik antara tubuh dan lingkungan,
semakin banyak energi metabolisme yang dibutuhkan untuk melakukan osmoregulasi
sebagai upaya adaptasi, namun tetap ada batas toleransi. Karena itu, sangat penting
dalam mengelola kualitas air, terutama salinitas (Fujaya, 2004). Djokosetyanto (2006),
mengatakan bahwa salinitas merupakan faktor penting untuk kelangsungan hidup dan
metabolisme ikan. Salah satu aspek fisiologis ikan yang dipengaruhi salinitas adalah
tekanan dan konsentrasi osmotik serta konsentrasi ion tubuh.
Dari 240 ekor sampel kerapu macan yang diperiksa yaitu 60 ekor (10 ekor
setiap 2 minggu) dari masing-masing salinitas ditemukan 4 (empat) spesies ektoparasit
yaitu pada insang 2 spesies yaitu Diplectanum sp., dan Oodonium sp., sedangkan di
kulit (lendir) ditemukan 2 spesies yaitu Trichodina sp. dan Benedenia sp. Hal ini
sesuai dengan observasi yang pernah dilakukan olehKoesharyani et al., (2001) bahwa
Trichodina sp. menyerang kulit kerapu dengan tingkat patogenitas tinggi, sedangkan
Diplectanum sp. menyerang insang kerapu dengan tingkat patogenitas sedang, akan
tetapi Benedenia sp. menyerang kulit dengan tingkat patogenitas rendah dan frekuensi
sedang. Dengan nilai parasit Trichodina sp. prevalensi parasit sebesar 14,21 %.
Diplectanum sp. 12,69 % dan Benedenia sp.dengan prevalensi12,49 %.
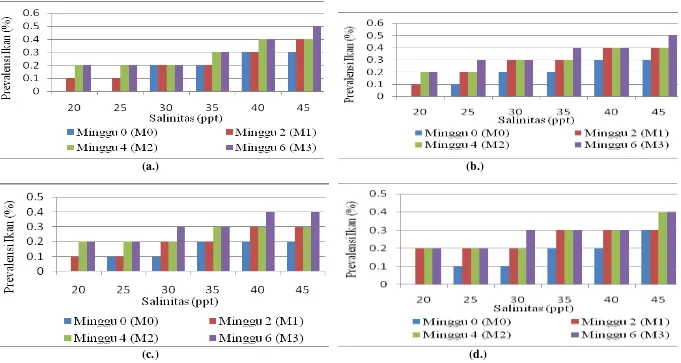
Tingkat infeksi ikan kerapu macan yang terserang penyakit parasit semakin
meningkat dari setiap minggunya (Gambar 8.) Pada salinitas 40-45 ppt prevalensi ikan
yang terinfeksi parasit jauh lebih banyak di minggu ke-6 dibandingkan pada minggu
ke-0. Hal ini dapat disebabkan karena siklus hidup dari parasit itu sendiri yang
(a.) (b.)
(c.) (d.)
Hal ini sesuai dengan pernyataan Akbar & Sudaryanto (2001), bahwa salinitas
yang terlalu rendah dapat mempengaruhi pertumbuhan dan tingkat infeksi ektoparasit
pada tubuh ikan. Menurut Bhagawati et al., (1991) bahwa jenis parasit tersebut
diduga terdapat dalam tubuh ikan kerapu macan karena menyebar secara horizontal
melalui telur, kista atau spora dalam air yang berkembang dalam kualitas air yang
ekstrim. Selain melalui air, parasit dapat masuk melalui carrier (pembawa) dan vector
(perantara) yang menyatakan bahwa benih ektoparasit dapat masuk ke dalam perairan
kolam karena terbawa oleh air, tumbuhan dan dapat pula karena adanya benda-benda
atau binatang yang masuk ke dalam kolam, juga terbawa oleh binatang renik.
Jenis ektoparasit dari monogenea umumnya menyerang dalam jumlah yang
cukup banyak dibandingkan dengan ektoparasit lainnya. Noga (1996) menyebutkan
infestasi monogenea biasanya merupakan indikator bahwa sanitasi (kebersihan) dan
pengawasan kualitas air buruk seperti tingginya ammonia atau nitrit dan rendahnya
oksigen terlarut.
4.3 Kualitas Air
Air merupakan media kehidupan ikan. Selain jumlah, kualitasnya juga harus
memenuhi syarat yang diperlukan agar budidaya ikan yang dilakukan berhasil.
Pengelolaan kualitas air merupakan tindakan preventif dalam menanggulangi serangan
penyakit parasit. Adapun parameter kualitas air meliputi salinitas, pH dan suhu.
[image:39.595.177.467.618.664.2]Parameter kualitas air selama penelitian disajikan dalam Tabel 3.
Tabel 5. Hasil pengamatan kualitas air selama penelitian
Parameter Hasil
Ph 7,5-8,0
Suhu (ºC) 28-31 ºC
Menurut Wardoyo (1981), kualitas air merupakan salah satu faktor yang perlu
diketahui dalam mengelola sumberdaya perikanan. Diantaranya suhu merupakan
pertumbuhan organisme. Hasil pengamatan terhadap derajat keasaman (pH air tercatat
7,5-8,0) masih dalam batas yang layak, terhadap kisaran tersebut masih pada batas
yang cukup untuk menunjang pertumbuhan dan kelangsungan hidup ikan. Kisaran pH
air yang ideal bagi perikanan 6,5-8,5 (Wardoyo 1981).
Pengukuran suhu air selama penelitian ini adalah 28 – 31 ºC, kondisi suhu ini
masih memungkinkan ikan hidup optimal. Kisaran suhu yang baik bagi kepentingan
budidaya ikan adalah 25-32 ºC (Daelami, 2001). Menurut Nurhudah (2006) perubahan
suhu air berlangsung secara lambat sehingga air memiliki sifat sebagai penyimpan
panas yang sangat baik. Sifat ini dapat menghindarkan terjadinya perubahan suhu
yang mendadak dapat menyebabkan organisme perairan stress. Kenaikan maupun
penurunan suhu yang mendadak akan mengakibatkan ikan mengalami stress dengan
gejala ikan berenang melonjak, mengapung di permukaan dan penurunan nafsu
makan, daya tahan menurun sehingga pada kondisi ini ikan akan rentan terhadap
BAB 5
KESIMPULAN DAN SARAN
5.1 Kesimpulan
Berdasarkan hasil penelitian dapat disimpulkan sebagai berikut:
1. Jumlah parasit dengan prevalensi tertinggi yaitu Oodonium sp. dengan prevalensi
14,48%, Trichodina sp. yang berasal dari kelas Ciliata sebesar 14,21%,
Diplectanum sp. 12,69%, dan prevalensi terendah pada parasit Benedenia sp.
12,49%.
2. Salinitas mempengaruhi prevalensi ektoparasit.
3. Salinitas 30-35 ppt menunjukkan prevalensi ektoparasit yang paling kecil.
5.2 Saran
Diharapkan adanya penelitian lanjutan tentang kajian parameter kualitas air yang lebih
berkaitan dengan hubungannya terhadap prevalensi ektoparasit pada benih kerapu
DAFTAR PUSTAKA
Abduh, M. 2007. Pembesaran Kerapu Macan Di Karamba Jaring Apung. Batam: Balai Budidaya Laut Batam.
Adji, K. 2008. Evaluasi Kontaminasi Bakteri Patogen pada Ikan Segar di Paerairan Teluk Semarang. Tesis. Semarang. Universitas Diponegoro.
Afrianto, E. & Liviawaty. 1992. Pengendalian Hama dan Penyakit Ikan. Yogyakarta: Penerbit Kanisius. hlm. 11, 22-77.
Akbar, S & Sudaryanto. 2001. Pembenihan dan Pembesaran Kerapu Bebek. Jakarta: Penebar Swadaya.
Alifuddin, M. 2004. Diagnostik Pewarnaan Sediaan Parasit. Dalam: Pelatihan Dasar Karantina Ikan Tingkat Ahli dan Terampil. Pusat Karantina Ikan. Bogor: hlm. 15.
Andrews, C. Adrian, E & Neville, C. 2003. Manual of Fish Health. A Firefly Publisher. Canada. Fisrt Printing. hlm. 207.
Anshary, H., & Ogawa. K. 2001. Microhabitats and Made of Attachment of Neoheterobothrium hirame, a Monogenean Parasite of Japanese Flounder. Fish Pathology. 36 (1): 21-26.
Aryati, Y. 2003. Prevalensi dan Derajat Infeksi Ichtyophthirius sp. pada Benih Gurami (Osphronemus gouramy L.) di Kabupaten Sleman. Skripsi. Fakultas Perikanan Universitas Gadjah Mada. Yogyakarta. hlm. 30.
Bhagawati, D., Petrus, H.T., & Ramawati,S. 1991. Mengenal Ektoparasit Penyebab Penyakit pada Kolam Rakyat di Desa Beji Purwokwerto. Karya Ilmiah. Fakultas Biologi UNSOED. Purwokerto.
Boyd, C. E. 1979. Water Quality in Warm Water Fiah Ponds. Department of Fisheries and Allied Aquacultures. Agricultural Experiment Station. Auburn University Alabama. USA.
Bunga, M. 2008. Prevalensi dan Intensitas Serangan Parasit Diplectanum sp. pada Insang Ikan Kerapu Macan (Epinephelus fuscoguttatus Forsskal) di Keramba Jaring Apung. Jurnal Ilmu Kelautan dan Perikanan. Universitas Hasanudin. 18 (3): 204-210.
Chua, T. E. & Teng, S. K. 1978. Effects of Feeding Frequency on The growth of Young Estuary Grouper, Epinephelus tauvina Forskal, Culture in Floating Net Cage. Aquaculture.14: 31 – 47.
Dana, D. Sarono, A,. Alifudin, M., Sukenda & Widodo. 1994. Petunjuk Teknis Determinasi Parasit Ikan. Buku 3. Kerjasama Pusat Karantina Pertanian-Fakultas Perikanan. Bogor. hlm. 24-25.
Daelami, D.A.S. 2001. Agar Ikan Sehat. Jakarta. Penebar Swadaya. hlm. 2, 11-79.
Dawes, C.J. 1993. Marine Botany. A Wiley Interscience Publication. New York: John Wiley and Sons.
Dennis, K. G., Dong, J. L., Gun, W. B., Hee, J. Y., Nam, S. S., Hwa, Y. Y., Cheol, Y. H., Jun, H. P., & Se, C. P. 2006. Detection of Betanodaviruses in Apparently Healthy Aaquarium Fishes and Invertebrates. Zoonotic Disease Priority Research Institute, and College of Veterinary Medicine. Korea: Seoul National University. hlm.151-742.
Djamali, A. Sutomo, A., Fatuchri, M & Mubarak, H. 1998. Sumber Daya Benih Komersial. Dalam Potensi dan Penyebaran Sumber Daya Ikan Laut di Perairan Indonesia. Komisi Nasional Pengkajian Stock Sumber Daya Ikan Laut Lembaga Ilmu Pengetahuan Indonesia. hlm. 169-183.
Djokosetyanto, D. 2006. Pengelolaan Parameter Fisika dan Kimia Air. Makalah Perawatan dan Pemeliharaan Ikan. Pusat Karantina Ikan. Jakarta.
Feliatra. 2002. Implementasi dan Pengembangan Bioteknologi Kelautan dalam Upaya Optimalisasi Pemanfaatan Laut Indonesia. Makalah dalam Pengukuhan Guru Besar. Fakultas Perikanan dan Ilmu Kelautan Universitas Riau, Pekanbaru.
Fujaya, Y. 1999. Fisiologi Ikan. Jurusan Perikanan. Fakultas Ilmu Kelautan dan Perikanan. Makassar: Universitas Hasanuddin. hlm. 88-101.
Gusrina. 2008. Budidaya Ikan. Jilid 3. Diakses Dari
Hamzah, M. S. 2003. Studi Variasi Musiman Beberapa Parameter Oseanografi terhadap Pertumbuhan dan Kelangsungan Hidup Kerang Mutiara (Pinctada maxima) di Perairan Teluk Kombal, Lombok Barat. Seminar Nasional ISOI, Jakarta. 30 – 31 Juli 2003. hlm. 12.
Heemstra, P.C. & Randall, J.E. 1999. Seranidae; Gruopers and Sea Bass (also Soap Fishes,Anthiines, In The Living Marine Recources of The Western Central Pacific. KE Carpenter and VH Niem (Mugilidae to Carangidae). Fish. Biol.
Hidayaturrohman. 1990. Penyakit Penting Ikan Budidaya di Indonesia. Bogor: ITB Press. hlm. 19.
Hutabarat. 1984. Pengantar Oseanografi. Cetakan Ketiga. Jakarta: Penerbit UI-Press.
Irianto, A. 2005. Patologi Ikan Telestotei. Yogyakarta: UGM Press.
Jobling, M. 1981. The Influences of Feeding on The Metabolic Rate of Fishes. Fish. Biol. 18: 385-400.
Kabata, Z. 1985. Parasites and Diseases of Fish Cultured in The Tropics. United Kingdom: International Development Reasearch Council. hlm. 135, 163, 317-318.
Klinger, R.E. & Floyd, R.F. 1998. Introduction to Freshwater Fish Paraites. Coorporative Extension Service Instintute of Food and Agricultural Sciences University of Florida. hlm 17.
Koesharyani, I., Mahardika, K., Johnny, F., Zafran, D.R. & Yuasa, K. 2001. Manual for Fish Disease Diagnostic-II. Marine Fish and Crustacean Disease in Indonesia. Gondol. Research Institute for Marine Culture and Japan International Cooperation Agency (JICA). hlm. 57.
Kordi, M. G. H. 2004. Penanggulangan Hama dan Penyakit Ikan. Jakarta: Rineka Cipta.
Kusumah, H. 1976. Penyakit dan Hama Ikan. Departemen Pertanian, Badan Diklat dan Penyuluhan Pertanian. Sekolah Usaha Perikanan Menengah. Bogor.
Langkosono & Wenno, L. F. 2003. Distribusi Ikan Kerapu (Serranidae) dan Kondisi Lingkungan Perairan Kecamatan Tanimbar Utara, Maluku Tenggara. Prosiding Lokakarya Nasional dan Pameran Pengembangan Agribisnis Kerapu II. Jakarta, 8–9 Oktober 2002. “Menggalang Sinergi unrtuk Pengembangan Agribisnis Kerapu”. Pusat Pengkajian dan Penerapan Teknologi Budidaya Pertanian BPPT. Jakarta: hlm. 203-212.
Lightner, D.V. 1996. A Handbook of Shrimp Pathology and Diagnostic Procedures for Diseases of Cultured Penaeid Shrimp. World Aquaculture Society, Baton Rouge, Louisiana, USA. hlm. 304.
Lio-Po, G. D., Lavilla, C. R., Cruz-Lacierda, E. R. 2001. Health Management in Aquaculture. Aquaculture Department Southeast Asian Fisheries Development Centre. Philipines: Tigbauan Hoilo. hlm. 187.
Meadows, P.S & Campbell, J.I. 1998. An Introduction to Marine Science. New York: John Wiley and Sons.
Mudjiman, A. 2004. Makanan Ikan. Edisi Revisi. Jakarta: Penebar Swadaya.
Munro, I. S. R. 1967. The fishes of New Guinea, Departement of Agriculture Stock and Fisheries Port Mores. hlm. 651.
Mulia, D.S. 2005. Tingkat Infeksi Ektoparasit Protozoa pada Benih Ikan Nila (Oreochromis niloticus) di Balai Benih Ikan (BBI) Pandak dan Sidabowa, Kabupaten Banyumas. Jurnal Sains Akuatik. 10 (1): 1-11.
Noble, E.R & Noble G.A. 1989. Parasitologi Biologi Parasit Hewan. Edisi Kelima. Yogyakarta: UGM Press.
Noga, E.J. 1996. Fish Disease. Diagnosis and Treatment. Department of Companion Animal & Special Species Medicine. North Caroline State University. hlm. 23-25.
Nontji, A. 1993. Laut Nusantara. Jakarta: Penerbit Djambatan.
Nurhudah, M. 2006. Pengelolaan Kualitas Air. Makalah Pendidikan dan Pelatihan Dasar Pengendali Hama Penyakit Ikan Tingkat Ahli. Pusat Karantina Ikan. Jakarta.
Prayitno, S. B. 1998. Prinsip-Prinsip Diagnosa Penyakit Ikan. Semarang: Penerbit UNDIP. hlm. 19.
Rakovac, R.C, Perovic, I.S, Popovic, N.T. Hacmanjek, M. Simpraga, B. & Teskeredzik, E. 2002. Health Status of Wild and Cultured Sea Bass in The Northern Adriatic Sea. Center for Marine and Environmental Research. LIRA, Bijenicka 54, 10000. Zagreb, Croatia.
Reantoso, M.G.B, Shomkiat, K & Chinabut, S. 2004. Review of Grouper Diseases and Health Management. Regional Workshop on Sea Farming Grouper Culture. Departement of Fisheries Compound. Thailand.
Riani, E. 2004. Manajemen Kualitas Air. Dalam: Pelatihan Dasar Karantina Ikan Tingkat Ahli dan Terampil. Bogor: Pusat Karantina Ikan. hlm. 12.
Rokhmani. 2002. Beberapa Penyakit Parasiter pada Budidaya Gurami (Osphronemus gouramy Lac.) di Kabupaten Banyumas. Sains Akuatik. 5 (1): 21-26.
Saleh, S. 1996. Statistik Non Parametrik. Edisi kedua. BPFE. Yogyakarta. hlm. 39-58.
Sommerville, C. 1998. Parasites of Farmed Fish. In: K.D. Black & A.D. Pickering (eds). Biology of farmed fish. Sheffield Academic Press. hlm. 146-179.
Soni, A. F. M. 2002. Penggunaan Beberapa Shelter pada Pendederan Ikan Kerapu Macan di Tambak. Dalam: Budidaya Air Payau. Departemen Kelautan dan Perikanan, Dirjen Perikanan Budidaya Balai Besar Pengembangan Budidaya Air Payau Jepara. hlm. 9.
Subyakto, S & Cahyaningsih. S 2003. Pembenihan Kerapu Skala Rumah Tangga. Jakarta: Agromedia Pustaka. hlm. 65.
Sudjiharno. 2003. Pengembangan Usaha Budidaya Kerapu di Keramba Jaring Apung di Wilayah Perairan Lampung. Buletin Budidaya Laut No. 16. Balai Budidaya Laut. hlm. 53-60.
Sunaryat. H. & Minjoyo, 2004. Perbedaan Frekuensi Pemberian Pakan pada Kerapu Macan (Epinephelus fuscoguttatus) di Keramba Jaring Apung. Budidaya Laut.
17: 27-33.
Suprakto, B. & Fahlivi, M. R. 2007. Studi Tentang Kesesuaian Lokasi Budidaya Ikan di KJA di perairan Kecamatan Sapeken Kabupaten Sumenep. Pembangunan Kelautan Berbasis IPTEK. Dalam Rangka Peningkatan Kesejahteraan Masyarakat Pesisir. Prosiding SeminarKelautan III. 24: 58 – 65.
Supriyadi, H. 2007. Pemeriksaan dan Identifikasi Hama dan Penyakit Ikan / Hama dan Penyakit Ikan Karantina. Dalam: Pelatihan Dasar Karantina Ikan Tingkat Ahli dan Terampil. Pusat Karantina Ikan. Jakarta. hlm 6.
Suryabrata, S. 2003. Metodologi Penelitian. Universitas Gadjah Mada. Rajawali Pers. Jakarta: PT. Rajawali Grafindo Persada.
Sutisna, H.D & Sutarmanto, R. 1995. Pembenihan Ikan Air Tawar. Yogyakarta: Penerbit Kanisius.
Taukhid. 2006. Manajemen Kesehatan Ikan dan Lingkungan. Laboratorium Riset Kesehatan ikan. Bogor.
Wardoyo, S.T.H. 1981. Kriteria Kualitas Air untuk Keperluan Pertanian dan Perikanan. Training Analisa Dampak Lingkungan Hasil Kerjasama UNDP-PS IPB. Bogor. hlm. 41.
Wetzel, R.G. 1983. Limnology. 2nd Edition. Toronto: Saunders College Publishing.
Lampiran A. Kaidah pengambilan sampel ikan
Amos (1985) dalam Lightner (1996)
Populasi ikan
Jumlah Sampel ikan yang diperlukan pada Asumsi Prevalensi
2% 5% 10% 20% 30% 40% 50%
50 50 35 20 10 7 5 2
100 75 45 23 11 9 7 6
250 110 50 25 10 9 8 7
500 130 55 26 10 9 8 7
1000 140 55 27 10 9 9 8
1500 140 55 27 10 9 9 8
2000 145 60 27 10 9 9 8
4000 145 60 27 10 9 9 8
10000 145 60 27 10 9 9 8
Lampiran B. Alur kerja kerokan kulit (Double Layer Slide Glass Method) dan mount insang (Kabata, 1985)
Alur kerja kerokan kulit (Double Layer Slide Glass Method)
v Bagian kulit dari kepala sampai ekor
Diperoleh cairan lendir (mucus)
Hasil
Diusapkan pada objek glass
Ditetesi dengan NaCl atau akuadest sebanyak 2-3 tetes
Ditutup dengan cover glass
Alur kerja mount insang
Sebagian dari insang
Hasil
Hasil
Diambil dengan menggunakan forcep atau gunting
Dipotong kartilago filament dengan scalpel
Ditempatkan di atas objek glass
Ditutup dengan cover glass agar filament insang tidak bergerak
Ditetesi dengan NaCl atau akuadest sebanyak 2-3 tetes di bawah usapan sampai merata
Lampiran C. Data pengamatan mingguan ektoparasit
b. Parasit Diplectanum Salinitas Minggu 0
(M0) Minggu 2 (M1) Minggu 4 (M2) Minggu 6 (M3) Total
20 ppt 0 1 2 2 5
25 ppt 1 2 2 2 7
30 ppt 1 2 2 3 8
35 ppt 2 2 3 3 10
40 ppt 2 3 3 4 12
45 ppt 2 3 3 4 12
Total 8 13 15 18 54
c. Parasit Trichodina Salinitas Minggu 0
(M0) Minggu 2 (M1) Minggu 4 (M2) Minggu 6 (M3) Total
20 ppt 0 1 2 2 5
25 ppt 1 2 2 3 8
30 ppt 2 3 3 3 11
35 ppt 2 3 3 4 12
40 ppt 3 4 4 4 15
45 ppt 3 4 4 5 16
Total 11 17 18 21 67
a. Parasit Oodonium Salinitas Minggu 0
(M0) Minggu 2 (M1) Minggu 4 (M2) Minggu 6 (M3) Total
20 ppt 0 1 2 2 5
25 ppt 0 1 2 2 5
30 ppt 2 2 2 2 8
35 ppt 2 2 3 3 10
40 ppt 3 3 4 4 14
45 ppt 3 4 4 5 16
d. Parasit Benedenia Salinitas Minggu 0
(M0) Minggu 2 (M1) Minggu 4 (M2) Minggu 6 (M3) Total
20 ppt 0 2 2 2 6
25 ppt <