KONSENTRASI KADMIUM (Cd) DAN TEMBAGA (Cu)
DALAM AIR, SESTON, KERANG DAN FRAKSINASINYA
DALAM SEDIMEN DI PERAIRAN DELTA BERAU,
KALIMANTAN TIMUR
Oleh: Ardi Afriansyah
C64104063
PROGRAM STUDI ILMU DAN TEKNOLOGI KELAUTAN FAKULTAS PERIKANAN DAN ILMU KELAUTAN
PERNYATAAN MENGENAI SKRIPSI DAN SUMBER INFORMASI
Dengan ini saya menyatakan bahwa Skripsi yang berjudul:
KONSENTRASI KADMIUM (Cd) DAN TEMBAGA (Cu)
DALAM AIR, SESTON, KERANG DAN FRAKSINASINYA
DALAM SEDIMEN DI PERAIRAN DELTA BERAU,
KALIMANTAN TIMUR
adalah benar merupakan hasil karya sendiri dan belum diajukan dalam bentuk apa pun kepada perguruan tinggi mana pun. Semua sumber data dan informasi yang berasal atau dikutip dari karya yang diterbitkan maupun tidak diterbitkan dari penulis lain telah disebutkan dalam teks dan dicantumkan dalam Daftar Pustaka dibagian akhir Skripsi ini.
Bogor, Juni 2009
RINGKASAN
ARDI AFRIANSYAH. Konsentrasi Kadmium (Cd) dan Tembaga (Cu) dalam Air, Seston, Kerang dan Fraksinasinya dalam Sedimen di Perairan Delta Berau, Kalimantan Timur. Dibimbing oleh TRI PRARTONO dan ZAINAL ARIFIN.
Penelitian dengan topik geokimia logam berat dalam sedimen dan
ketersediaannya pada biota bentik ini bertujuan untuk menentukan konsentrasi Cd dan Cu dalam sedimen, air, seston, dan kerang, serta mengkuantifikasi
karakteristik geokimia Cd, dan Cu dalam sedimen di perairan Delta Berau, Kalimantan Timur.
Pengambilan contoh sedimen, air, dan biota dilakukan pada 25 - 30 April 2008 di perairan Delta Berau, Kalimantan Timur dan dianalisis di Laboratorium
Pencemaran dan Laboratorium Geologi P2O-LIPI pada Mei 2008-Januari 2009. Contoh sedimen dikumpulkan dari 21 stasiun dimulai dari sungai, muara, hingga laut, sedangkan sampel air hanya dikumpulkan dari 6 stasiun di daerah muara dan laut.
Metode yang digunakan untuk analisis logam berat total dan fraksinasi logam berat Cd, dan Cu sedimen yaitu prosedur ekstraksi secara simultan. Sedimen diukur konsentrasi logam beratnya pada fraksi-fraksi sedimen berupa easily
reducuble (logam-logam yang berasosiasi dengan Mn oksida), easily
reducible+reducible (logam-logam yang berasosiasi dengan Mn+Fe oksida),
organik, dan residual.
Nilai kualitas perairan Delta Berau yaitu suhu perairan: 26,3 0C – 29,7 0C, salinitas: 0 - 30, pH: 6,46 – 8,02, DO: 4,34 mg/l – 6,4 mg/l. Konsentrasi logam Cu terlarut berkisar antara ttd – 0,001 mg/l, sedangkan untuk Cd berkisar antara 0,0005 mg/l – 0,001 mg/l. Konsentrasi logam Cu dalam seston berkisar 18,667 –
104,388 µg/g dan Cd berkisar <0,002 µg/g – 23,048 µg/g. Konsentrasi total Cu dalam sedimen berkisar antara 1,575 µg/g – 34,112 µg/g BK, total Cd berkisar antara 0,022 µg/g - 0, 125 µg/g BK, sedangkan TOM berkisar 0,9-19,8%. Tipe sedimen umumnya lebih didominasi oleh fraksi lumpur, kemudian diikuti pasir, dan sedikit dijumpai adanya kerikil. Konsentrasi logam berat Cd umumnya banyak dijumpai dalam fraksi organik dan easy reducible, hanya sebagian kecil
terdapat dalam fraksi reducible dan residual, Sedangkan konsentrasi logam Cu
banyak dijumpai dalam fraksi residual, dan hanya sedikit dijumpai pada fraksi organik, reducible maupun easy reducible.
KONSENTRASI KADMIUM (Cd) DAN TEMBAGA (Cu)
DALAM AIR, SESTON, KERANG DAN FRAKSINASINYA
DALAM SEDIMEN DI PERAIRAN DELTA BERAU,
KALIMANTAN TIMUR
Skripsi
Sebagai salah satu syarat untuk memperoleh gelar Sarjana Perikanan pada Fakultas Perikanan dan Ilmu Kelautan
Institut Pertanian Bogor
Oleh: Ardi Afriansyah
C64104063
PROGRAM STUDI ILMU DAN TEKNOLOGI KELAUTAN FAKULTAS PERIKANAN DAN ILMU KELAUTAN
© Hak cipta milik Ardi Afriansyah, tahun 2009
Hak cipta dilindungi
Judul : KONSENTRASI KADMIUM (Cd) DAN TEMBAGA (Cu) DALAM AIR, SESTON, KERANG DAN FRAKSINASINYA DALAM SEDIMEN DI PERAIRAN DELTA BERAU, KALIMANTAN TIMUR
Nama : Ardi Afriansyah NRP : C64104063
Disetujui,
Pembimbing I
Dr. Ir. Tri Prartono, M.Sc NIP. 19600727 198603 1 005
Pembimbing II
Dr. Ir. Zainal Arifin, M.Sc NIP. 19590914 198503 1 002
Mengetahui,
Dekan Fakultas Perikanan dan Ilmu Kelautan
Prof. Dr. Ir. Indra Jaya, M.Sc NIP. 19610410 198601 1 002
KATA PENGANTAR
Puji dan syukur kehadirat Allah S.W.T atas berkat dan karunia-Nya sehingga
skripsi dengan judul “Konsentrasi Kadmium (Cd) dan Tembaga (Cu) dalam Air,
Seston, kerang dan Fraksinasinya dalam Sedimen di Perairan Delta Berau,
Kalimantan Timur” dapat terselesaikan. Skripsi ini merupakan bagian kegiatan
riset kompetitif LIPI Nasib Kontaminan Logam di Delta Berau tahun 2008.
Pengukuran logam berat total dalam sedimen belum dapat menerangkan
pengaruh logam berat tersebut terhadap biota bentik. Dengan mengetahui
kandungan logam berat dalam fraksi - fraksi sedimen, dapat memberikan indikasi
apakah keberadaan logam berat dalam sedimen tersebut berbahaya terhadap
kehidupan biota akuatik. Skripsi ini memberikan pengetahuan sampai sejauh
mana keberadaan bahan pencemar logam berat dalam komponen ekosistem di
perairan Delta Berau.
Penulis menyadari bahwa skripsi ini tidaklah sempurna, namun demikian hasil
penelitian dapat memberikan informasi tentang karakteristik logam dalam
sedimen dan peran yang terlibat.
Bogor, Juni 2009
UCAPAN TERIMA KASIH
Atas terselesaikannya skripsi ini penulis mengucapkan terima kasih kepada:
1. Allah S.W.T atas rahmat dan Kasih-Nya, sehingga penulis dapat
menghadapi segala permasalahan yang dihadapi.
2. Ayah dan Ibu beserta Kakak dan Adik penulis atas kasih sayang,
dukungan, dan doanya.
3. Dosen pembimbing skripsi, Dr. Ir. Tri Prartono, M.Sc. atas segala bantuan
dan bimbingan sehingga skripsi ini dapat terselesaikan.
4. Dosen pembimbing skripsi, Dr. Ir. Zainal Arifin, M.Sc. atas perhatian,
bimbingan, saran, dan kritik mengenai penelitian ini.
5. Peneliti di Laboratorium Pencemaran P2O-LIPI: Abdul Rozak, A.Md,
Dra. Endang Rochyatun (alm.), Lestari, S.Si, Taufik Kaisupy, dan Triyoni
Purbonegoro, S.Si atas bimbingan dan bantuan yang diberikan kepada
penulis.
6. Prof. Dr. Ir. Harpasis S. Sanusi, M.Sc. sebagai dosen penguji dan Dr. Ir.
Henry M. Manik, M.T. sebagai Koordinator Program Pendidikan ITK,
FPIK IPB
7. Adimulyo Nugroho atas kerjasamanya selama analisis dan proses
pengolahan data, serta seluruh teman-teman di Departemen Ilmu dan
DAFTAR ISI
2.5 Fraksinasi logam berat dalam sedimen ... 16
3 METODE PENELITIAN ... 22
4.1 Kualitas perairan Delta Berau ... 31
4.2 Konsentrasi Cd dan Cu terlarut ... 39
4.3 Konsentrasi Cd dan Cu dalam seston ... 41
4.5 Kandungan bahan organik total (Total Organic Matter / TOM)
dalam sedimen ... 44
4.6 Konsentrasi Cd dan Cu dalam sedimen ... 45
4.7 Konsentrasi Cd dan Cu dalam fraksi sedimen ... 47
4.7.1 Konsentrasi Cd dalam fraksi sedimen ... 47
4.7.2 Konsentrasi Cu dalam fraksi sedimen ... 50
4.8 Hubungan bahan organik total (Total Organic Matter / TOM) dengan konsentrasi Cd dan Cu dalam sedimen ... 54
4.9 Hubungan antara persentase lumpur (mud) dengan konsentrasi Cd dan Cu dalam sedimen ... 57
4.10 Konsentrasi Cd dan Cu dalam Anadara granosa ... 58
5 KESIMPULAN DAN SARAN ... 61
5.1 Kesimpulan ... 61
5.2 Saran ... 62
DAFTAR PUSTAKA ... 63
LAMPIRAN ... 67
DAFTAR TABEL
Halaman
1. Konsentrasi Cd dan Cu (ppm) pada beberapa perairan di Indonesia ... 9
2. Konsentrasi Cd dan Cu (ppm) pada sedimen di beberapa Perairan di
Indonesia ... 12
3. Kandungan beberapa logam berat pada biota bentik (ppm) di Perairan
Semarang dan Kuala Tungkal ... 15
4. Hubungan antara ukuran butiran sedimen (µm) dan konsentrasi Cd dan Cu (µg/g) ... 19
5. Kandungan Mn- Fe dan beberapa logam pada fraksi-fraksi laut dalam,
satuan µg/g ... 20
6. Alat dan bahan penelitian yang digunakan di lapangan dan di
laboratorium... 23
7. Perbedaan klasifikasi fraksi resistan dan non resistan antara yang digunakan dalam skripsi dengan Thomas dan Bendell-Young (1998) ... 30
8 Persentase pembagian logam berat dalam fraksi sedimen easily reducible
(ER), reducible (RED), organic (ORG), residual (RES), resistan (RES),
dan non-resistan (ER+RED+ORG). Nilai diperoleh dari rata-rata semua
DAFTAR GAMBAR
Halaman
1. Skema pembagian logam di lingkungan perairan ··· 16
2. Peta lokasi penelitian dan penentuan stasiun perairan Delta Berau,
Kalimantan Timur April 2008··· 23
3. Skema analisis fraksinasi logam berat dalam sedimen ··· 30
4. Nilai suhu perairan (0C) pada stasiun pengamatan menurut zonasi di perairan Delta Berau, April 2008 ··· 32
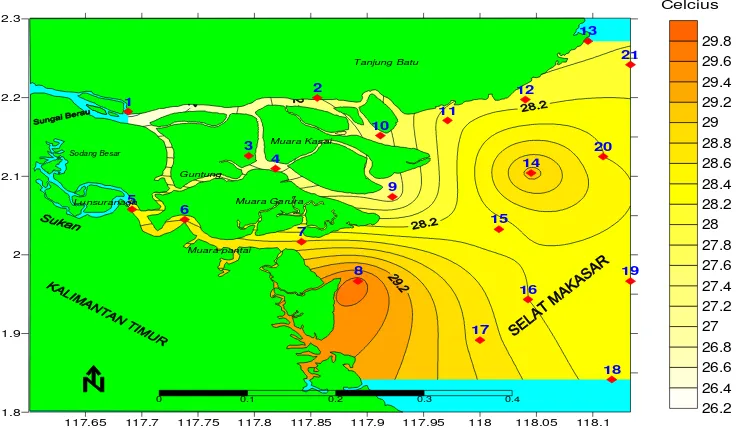
5. Sebaran spasial suhu (0C) di perairan Delta Berau, April 2008 ··· 32
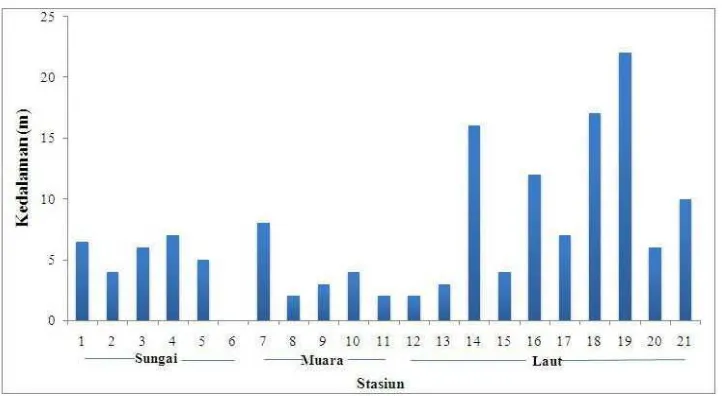
6. Kedalaman perairan (m) pada stasiun pengamatan menurut zonasi di
perairan Delta Berau, April 2008 ··· 33
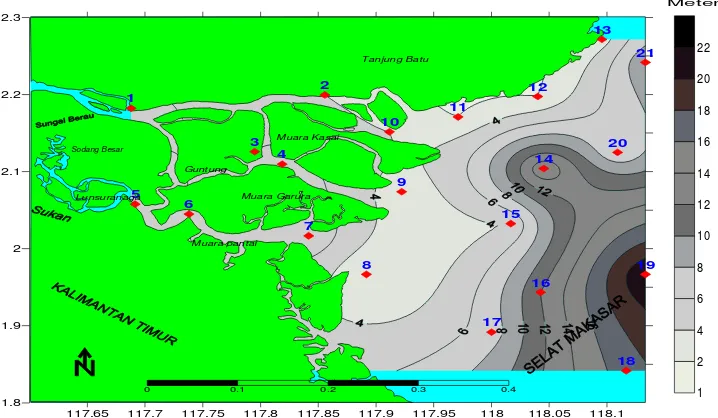
7. Sebaran spasial kedalaman (m) perairan Delta Berau, April 2008 ··· 34
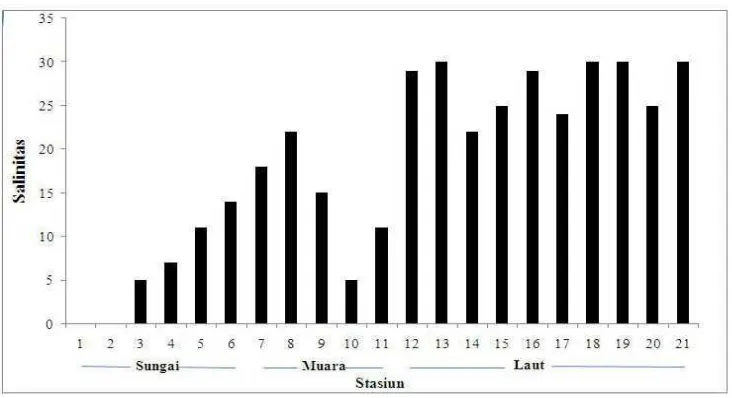
8. Nilai salinitas pada stasiun pengamatan menurut zonasi di perairan Delta Berau, April 2008 ··· 35
9. Sebaran spasial salinitas di perairan Delta Berau, April 2008 ··· 35
10.Nilai pH pada stasiun pengamatan menurut zonasinya di perairan Delta Berau, April 2008 ··· 36
11.Sebaran spasial pH di perairan Delta Berau, April 2008 ··· 36
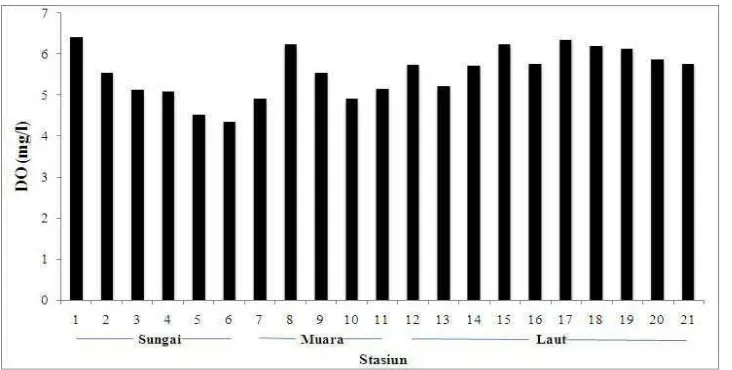
12.Kadar oksigen terlarut (mg/l) pada stasiun pengamatan menurut zonasi di perairan Delta Berau, April 2008 ··· 37
13.Sebaran spasial oksigen terlarut (mg/l) di Perairan Delta Berau, April 2008 ··· 38
14.Nilai padatan tersuspensi total (TSS) pada stasiun pengamatan
berdasarkan zonasi di Perairan Delta Berau, April 2008 ··· 39
15.Sebaran spasial TSS (mg/l) di perairan Delta Berau, April 2008 ··· 39
16.Konsentrasi Cd dan Cu terlarut (mg/l) pada stasiun pengamatan
menurut zonasi di perairan Delta Berau, April 2008 ··· 41
17.Konsentrasi Cd dan Cu (µg/g) dalam seston pada stasiun pengamatan
18.Tipe sedimen pada stasiun pengamatan Perairan Delta Berau, April
2008 ··· 43
19.Persentase kandungan bahan organik total dalam sedimen pada stasiun pengamatan menurut zonasi di perairan Delta Berau, April 2008 ··· 45
20.Konsentrasi Cd total (µg/g) dalam sedimen pada stasiun pengamatan
berdasarkan zonasinya di perairan Delta Berau, April 2008 ··· 47
21.Konsentrasi Cu total (µg/g) dalam sedimen pada stasiun pengamatan
berdasarkan zonasinya di perairan Delta Berau, April 2008 ··· 47
22.Konsentrasi Cd (µg/g) dalam fraksi sedimen pada stasiun pengamatan
berdasarkan zonasi di perairan Delta Berau, April 2008 ··· 49
23.Persentase Cd pada fraksi sedimen (%) pada stasiun pengamatan
berdasarkan zonasi di perairan Delta Berau, April 2008 ··· 50
24.Konsentrasi Cu (µg/g) dalam fraksi sedimen pada stasiun pengamatan
berdasarkan zonasi di perairan Delta Berau, April 2008 ··· 51
25.Persentase Cu pada fraksi sedimen (%) pada stasiun pengamatan
berdasarkan zonasi di perairan Delta Berau, April 2008 ··· 52
26.Hubungan keberadaan kandungan bahan organik dengan Cd (µg/g) dalam fraksi non-resistan (a) dan total sedimen (b) ··· 56
27.Hubungan keberadaan kandungan bahan organik dengan Cu (µg/g) dalam fraksi non-resistan (a) dan total sedimen (b) ··· 56
28.Hubungan antara persentase lumpur (mud) dengan konsentrasi Cd (µg/g)
dalam sedimen ··· 58
29.Hubungan antara persentase lumpur (mud) dengan konsentrasi Cu (µg/g)
dalam sedimen ··· 58
DAFTAR LAMPIRAN
5. Prosedur analisis ukuran butiran sedimen (Rahayuningsih, 2007) ··· 72
6. Prosedur analisis kandungan bahan organik total (TOM) dalam sedimen (APHA, 1992) ··· 73
7. Prosedur analisis fraksinasi logam Cd dan Cu dalam sedimen (Young
et al., 1992 in Thomas dan Young, 1998 ) ··· 74
8. Nilai beberapa parameter kualitas air, kedalaman menurut posisi stasiun pengamatan di Delta Berau, Kalimantan Timur, April 2008 ··· 76
9. Konsentrasi Cd dan Cu terlarut pada perairan Delta Berau, April 2008 ·· 76
10.Konsentrasi Cd dan Cu dalam seston di Perairan Delta Berau, April 2008 ··· 77
11.Hasil analisis butiran (grain size analisis) sedimen Perairan Delta Berau
Kalimantan Timur, April 2008 ··· 78
12.Nilai persentase tekstur sedimen dan tipe sedimen pada Perairan Delta Berau, April 2008 ··· 80
13.Bahan organik total (TOM) dalam sedimen perairan Delta Berau April 2008, yang ditunjukkan dengan persentase bahan organik yang hilang dalam pembakaran 500 oC selama 4 jam ··· 81
14.Konsentrasi Cd dan Cu (µg/g) dalam Total sedimen Perairan Delta Berau, April 2008 ··· 82
15.Konsentrasi Cd dan Cu (µg/g) dalam fraksi sedimen ··· 83
16.Nilai konsentrasi Cu dan Cd dalam Anadara granosa (µg/g) di perairan
17.Rangkuman data hasil penelitian di Delta Berau ··· 85
1. PENDAHULUAN
1.1Latar Belakang
Ekosistem perairan pesisir merupakan daerah yang memiliki potensi
sumberdaya yang sangat besar, sehingga wilayah itu cepat berkembang menjadi
pusat perekonomian. Perairan Delta Berau merupakan salah satu contoh wilayah
pesisir yang telah menjadi daerah pusat perekonomian diantaranya mencakup
industri tambang batu bara, kegiatan hutan (logging), industri pulp (Julianery,
2001).
Namun demikian, di sisi lain berbagai kegiatan yang ada khususnya bidang
industri telah memberikan dampak yang negatif seperti penurunan kualitas air
khususnya logam berat. Berdasarkan hasil penelitian terakhir yang dilakukan di
perairan Delta Berau menunjukkan bahwa kegiatan industri telah membawa
dampak terhadap peningkatan jumlah kadar logam berat di perairan tersebut
dimana kandungan logam berat umumnya lebih tinggi terdapat pada sedimen
(Arifin et al., 2006).
Disamping kegiatan industri, perairan Delta Berau memiliki potensi sumber
daya perairan seperti ikan, kerang, udang maupun jenis biota lain yang banyak
dimanfaatkan oleh masyarakat setempat. Menurut Julianery (2001) budidaya laut
di Perairan Delta Berau diperkirakan mempunyai potensi sebesar 2.500 hektar
dengan potensi penangkapan sebesar 35.000 ton per tahun. Selain itu, daerah
perairan Delta Berau merupakan tempat bagi penyu hijau (Chelonia mydas) untuk
bertelur. Produksi telur penyu yang dihasilkan dari daerah ini 94,9 ton dengan
Keberadaan sumberdaya perikanan yang berada di perairan terkontaminasi
logam berat dapat menurunkan nilai penting sumberdaya tersebut karena
memiliki peluang terkontaminasi. Beberapa penelitian telah menunjukkan bahwa
organisme perairan dapat mengakumulasi logam berat. Menurut Suprijanto
(1998) Pb dan Hg terdeteksi pada jaringan lunak Anadara granosa di perairan
Semarang dengan konsentrasi masing-masing berkisar antara 10,3492 – 40,2414
mg/kg dan 0,01748 – 0,31898 mg/kg yang hidup pada perairan yang
mengandung logam berat dengan konsentrasi Hg dan Pb masing-masing 0,0002
- 0,0004 mg/l dan 0,0086-0,0091 mg/l.
Akumulasi logam berat dalam perairan ke dalam tubuh organisme telah
banyak diungkapkan dalam berbagai pustaka dan peneliti. Namun proses
akumulasi kadar logam berat belum begitu jelas karena berbagai macam faktor
yang mempengaruhinya seperti rute logam berat ke dalam tubuh organisme dapat
melalui absorpsi makanan, adsorpsi air melalui insang, keberadaan partikel,
mobilitas logam antara partikel di udara dan air. Disamping itu, beberapa faktor
penting lain adalah spesiasi logam dalam air yang juga berperan penting dalam
mekanisme “sink dan source” logam dalam air.
Penelitian ini mencoba mengidentifikasi konsentrasi logam pada masing-masing
komponen abiotik seperti air, seston dan sedimen di Delta Berau serta konsentrasi
Cd dan Cu pada tiap fraksi sedimen (organik, mangan oksida dan besi oksida)
yang dapat menduga ketersediaan logam bagi biota (bioavailability).
1.2Tujuan
Penelitian ini bertujuan untuk:
1.Mengukur konsentrasi Cd dan Cu pada air, sedimen dan kerang di perairan
Delta Berau, Kalimantan Timur.
2.Mengkaji karakteristik geokimia Cd dan Cu dalam sedimen perairan Delta
2. TINJAUAN PUSTAKA
2.1 Karakteristik Logam Berat
Logam merupakan unsur alam yang diperoleh dari laut, erosi batuan,
vulkanisme dan sebagainya (Clark, 1986). Golongan logam umumnya memiliki
daya hantar dan daya panas yang tinggi. Berdasarkan densitasnya, golongan
logam dibagi atas dua golongan, yaitu golongan logam ringan (light metal) yang
mempunyai densitas < 5 g/cm3, sedangkan logam berat (heavy metal) mempunyai
densitas > 5 g/cm3 (Hutagalung et al., 1997).
Menurut Darmono (1995) sifat logam berat sangat unik, tidak dapat
dihancurkan secara alami dan cenderung terakumulasi dalam rantai makanan
melalui proses biomagnifikasi. Pencemaran logam berat ini menimbulkan
berbagai permasalahan diantaranya: 1) berhubungan dengan estetika (perubahan
bau, warna dan rasa air); 2) berbahaya bagi kehidupan tanaman dan binatang; 3)
berbahaya bagi kesehatan manusia; 4) menyebabkan kerusakan pada ekosistem.
Karakteristik logam berat menurut Palar (2004) adalah sebagai berikut:
1. Memiliki spesifikasi gravitasi yang sangat besar (4 gr/cm3)
2. Mempunyai nomor atom 23-34 dan 40-50 serta unsur lantanida dan
aktanida.
3. Mempunyai respon biokimia (spesifik) pada organism hidup.
2.1.1 Kadmium (Cd)
Kadmium (Cd) adalah salah satu logam berat dengan penyebaran yang
sangat luas di alam, logam ini bernomor atom 48, berat atom 112,40 dengan titik
sebagai greennocckite (CdS) yang ditemui bersamaan dengan senyawa spalerite
(ZnS). Kadmium merupakan logam lunak (ductile) berwarna putih perak dan
mudah teroksidasi oleh udara bebas dan gas amonia (NH3) (Palar, 2004)..
Kadmium bervalensi dua (Cd2+) adalah bentuk terlarut stabil dalam
lingkungan perairan laut pada pH dibawah 8,0. Kadar Cd di perairan alami
berkisar antara 0,29-0,55 ppb dengan rata-rata 0,42 ppb. Dalam lingkungan alami
yang bersifat basa, kadmium mengalami hidrolisis, teradsorpsi oleh padatan
tersuspensi dan membentuk ikatan kompleks dengan bahan organik. Di perairan
alami, Cd membentuk ikatan kompleks dengan ligan baik organik maupun
anorganik, yaitu Cd2+, Cd(OH)+, CdCl+, CdSO4, CdCO3 dan Cd organik (Sanusi,
2006).
2.1.2 Tembaga (Cu)
Tembaga atau copper (Cu) umumnya berbentuk kristal dan memiliki warna
kemerahan. Dalam tabel periodik unsur kimia, tembaga memiliki nomor atom
(NA) 29 dan memiliki bobot atau berat atom (BA) 63,546 (Palar, 2004).
Keberadaan unsur tembaga di alam dapat ditemukan dalam bentuk logam
bebas, akan tetapi lebih banyak ditemukan dalam bentuk persenyawaan atau
sebagai senyawa padat dalam bentuk mineral (Palar, 2004). Tembaga (Cu) di
perairan alami terdapat dalam bentuk partikulat, koloid dan terlarut. Fase terlarut
merupakan Cu2+ bebas dan ikatan kompleks, baik dengan ligan inorganik,
terutama (CuOH+, Cu2(OH)22+) maupun organik. Ikatan Cu kompleks dengan
ligan organik, terutama adalah oleh material humus. Ikatan kompleks Cu yang
dalam kolom air laut stabilitasnya paling rendah (Moore dan Ramamoorthy, 1984
in Sanusi, 2006).
2.2 Logam Berat dalam Air
Logam dalam perairan biasanya terikat oleh senyawa lain sehingga berbentuk
molekul dan jarang dijumpai dalam bentuk berbentuk ion tersendiri. Ikatan ini
dapat berupa garam organik, seperti senyawa metil, etil, fenil maupun garam
anorganik berupa oksida, klorida, sulfida, karbonat, hidroksida dan sebagainya.
Bentuk ion dari garam tersebut biasanya banyak ditemukan dalam air dan
kemudian bersenyawa atau diserap dan selanjutnya tertimbun dalam tanaman dan
hewan air (Darmono, 1995).
Dalam perairan, logam berat dapat ditemukan dalam bentuk terlarut dan tidak
terlarut. Logam berat terlarut adalah logam yang membentuk komplek dengan
senyawa organik dan anorganik, sedangkan logam berat yang tidak terlarut
merupakan partikel-partikel yang berbentuk koloid dan senyawa kelompok metal
yang teradsorbsi pada partikel-partikel yang tersuspensi (Razak, 1980 in Erlangga
2007). Logam berat yang dilimpahkan ke perairan, baik di sungai ataupun laut
akan dipindahkan dari badan airnya melalui beberapa proses yaitu : pengendapan,
adsorbsi dan absorbsi oleh organisme perairan. Logam berat mempunyai sifat
yang mudah mengikat bahan organik dan mengendap di dasar perairan dan
bersatu dengan sedimen sehingga kadar logam berat dalam sedimen lebih tinggi
dibandingkan dalam air (Harahap, 1991).
Menurut Bryan (1976) dan Connel dan Miller (1995) secara umum sumber –
1. Logam berat yang masuk ke perairan laut secara alami, berasal dari tiga
sumber yaitu:
a) Masukkan dari daerah pantai (coastal supply) yang berasal dari
sungai-sungai dan hasil abrasi pantai oleh aktivitas gelombang.
b) Masukkan dari laut dalam (deep sea supply) meliputi logam –
logam yang dibebaskan oleh aktivitas gunung berapi di laut dan
logam-logam yang dibebaskan dari partikel/sedimen-sedimen dari
proses kimiawi.
c) Masukkan dari lingkungan dekat daerah pantai, termasuk logam –
logam dari atmosfer sebagai partikel – partikel debu.
2. Sumber buatan manusia (man – made) adalah:
a) Limbah dan buangan industri.
b) Limbah cair perkotaan.
c) Aktivitas perkapalan (pelayaran).
d) Aktivitas pertanian.
e) Cairan limbah rumah tangga.
f) Aktivitas pertambangan.
g) Perikanan budi daya.
Kelarutan logam dalam air pada prinsipnya di atur oleh 1) pH; 2) Jenis dan
kepekatan ligan dan zat-zat pengkhelat; 3) Keadaan oksidasi komponen mineral
dan lingkungan redoks sistem tersebut (Leckie dan James, 1974 in Connel dan
Miller, 1995). Pada umumnya partikel yang mengendap mempunyai ukuran 100
µm, partikel yang yang larut adalah yang berukuran kurang dari 1 µm (Tinsley,
logam dan spesies lainnya dalam larutan air (Leckie dan James, 1974; Stumm dan
Morgan, 1970 in Connel dan Miller, 1995) dapat dijelaskan sebagai berikut ;
1. Reaksi hidrolisis ion-ion logam; sebagian besar ion-ion logam yang paling
mudah berpindah (seperti Th4+, Fe3+, dan Cr3+) merupakan yang paling mudah
dihidrolisis dalam larutan air.
2. Pengompleksan ion-ion logam. Ion-ion logam juga bereaksi dengan zat-zat
pengompleks organik dan anorganik yang ada dalam air baik dari sumber alamiah
maupun sumber pencemaran. Ligan pengompleks anorganik yang dominan
meliputi meliputi Cl-, SO
4-2, HCO3-, F-, sulfida dan spesies fosfat. Reaksi ini
mirip dengan reaksi hidrolisis ion-ion logam dalam hal terbentuknya ion
kompleks yang larut dan tidak larut, bergantung pada kepekatan logam dan ligan
serta pH.
Logam dalam perairan juga dapat berikatan dengan zat-zat organik alamiah
atau buatan dengan jalan :1) Atom karbon yang menghasilkan zat organologam;
2) Gugus karboksil yang membentuk garam dari asam organik; 3) Atom donor
elektron seperti O, N, S, P dan sebagainya yang membentuk kompleks koordinasi.
Kandungan logam berat dalam perairan dipengaruhi oleh parameter fisika
seperti arus, suhu, salinitas dan kimiawi yaitu, padatan tersuspensi dan derajat
keasaman (pH). Pada umumnya faktor oseanografi yang paling berperan dalam
penyebaran bahan pencemar adalah arus, pasang surut, gelombang dan keadaan
bathimetri perairan (Uktolseya, 1991 in Suryanto, 2003).
Dalam air laut, kadar logam berat berkisar antara 10-5-10-2 ppm. Kadar
tersebut akan meningkat bila limbah perkotaan, pertambangan, pertanian dan
unsur logam berat terutama yang bersifat esensial seperti Cu dan Zn dibutuhkan
oleh biota perairan untuk pertumbuhan dan perkembangan hidupnya, tetapi bila
jumlahnya berlebihan maka akan bersifat racun (Phillips, 1980 in Suryanto,
2003). Konsentrasi logam berat Cd dan Cu pada beberapa perairan di Indonesia
dapat dilihat pada Tabel 1.
Tabel 1. Konsentrasi Cd dan Cu (ppm) pada beberapa perairan di Indonesia
Lokasi Konsentrasi Logam penelitian Tahun Sumber Cd (ppm) Cu (ppm)
Perairan Batu Ampar, P. Batam
0,0283-0,0305
(0,0293±0,0010) (0,0287±0,0076) 0,0167-0,0367
1983,
September (1990) Razak 0,0009-0,0038
(0,0026±0,0016) (0,0027±0,0026) 0,0005-0,0070 0,0009-0,0052
(0,0035±0,0019) (0,0016±0,0012) ttd-0,0028
Perairan Sekupang, P.
Batam
0,0246-0,0269
(0,0260±0,0010) (0,0467±0,0049) 0,0417-0,0516
1983,
<0,001 <0,001-0,002 2005, Juni
Anindita
(0,001) 2004, Januari Sianingsih (2005)
Perairan Laut Banda
0,0006-0,0032 0,0018-0,0105 2006, Juli
Hamzah (2006)
Delta Berau
2.3 Logam Berat dalam Sedimen
Logam berat yang masuk ke dalam lingkungan perairan akan mengalami
pengendapan, pengenceran dan dispersi, kemudian diserap oleh organisme yang
hidup di perairan tersebut. Logam berat mempunyai sifat yang mudah mengikat
bahan organik dan mengendap di dasar perairan dan bersatu dengan sedimen
sehingga kadar logam berat dalam sedimen lebih tinggi dibanding dalam air
(Hutagalung, 1991)
Mengendapnya logam berat bersama-sama dengan padatan tersuspensi
akan mempengaruhi kualitas sedimen di dasar perairan dan juga perairan
sekitarnya. Kekuatan ionik yang terdapat di air laut disebabkan adanya berbagai
kandungan anion dan kation pada air laut, sehingga memungkinkan terjadinya
proses koagulasi (penggumpalan) senyawa logam berat yang ada dan
memungkinkan terjadinya proses sedimentasi (pengendapan). Jika kapasitas
angkut sedimen cukup besar, maka sedimen di dasar perairan akan terangkat dan
terpindahkan. Sesuai teori gravitasi, apabila partikulat memiliki massa jenis lebih
besar dari massa jenis air laut maka partikulat akan mengendap di dasar laut atau
terjadi proses sedimentasi (Erlangga, 2007).
Menurut Greaney (2005), ada 3 kemungkinan mekanisme logam masuk dan
diikat oleh sedimen serta bahan tersuspensi :
1. Proses adsorpsi fisika- kimia dari kolom perairan.
2. Proses uptake oleh bahan organik atau organisme
Akumulasi fisik dari bahan partikulat yang banyak mengandung logam oleh
Adsorpsi fisika-kimia secara langsung dari kolom perairan terjadi melalui
berbagai cara. Adsorpsi secara fisik biasanya terjadi ketika bahan partikulat
secara langsung mengabsorpsi logam berat dari kolom perairan. Adsorpsi secara
biologi dan kimia lebik kompleks prosesnya dari pada adsorpsi secara fisik karena
dikontrol oleh banyak faktor seperti pH dan oksidasi.
Kelarutan logam dalam air dikontrol oleh pH air. Kenaikan pH menurunkan
kelarutan logam dalam air, karena kenaikan pH mengubah kestabilan dari bentuk
karbonat menjadi hidroksida yang membentuk ikatan dengan partikel pada badan
air, sehingga akan mengendap membentuk lumpur (Palar, 2004). Selain itu,
kenaikan suhu air laut dan penurunan pH akan mengurangi adsorpsi senyawa
logam berat pada partikulat. Suhu air laut yang lebih dingin akan meningkatkan
adsorpsi logam berat ke partikulat untuk mengendap di dasar laut. Pada saat suhu
air laut naik, senyawa logam berat akan melarut di air laut karena penurunan laju
adsorpsi ke dalam partikulat. Logam yang memiliki kelarutan yang kecil akan
ditemukan di permukaan air laut selanjutnya dengan perpindahan dan waktu
tertentu akan mengendap hingga ke dasar laut, artinya logam tersebut hanya akan
berada di dekat permukaan air laut dalam waktu yang sesaat saja untuk kemudian
mengendap lagi. Hal ini ditentukan antara lain oleh massa jenis air laut, viskositas
(kekentalan) air laut, temperatur air laut, arus serta faktor-faktor lainnya
(Erlangga, 2007).
Daya larut logam berat dapat menjadi lebih tinggi atau lebih rendah
tergantung pada kondisi lingkungan perairan. Pada daerah yang kekurangan
oksigen, misalnya akibat kontaminasi bahan-bahan organik, daya larut logam
Zn,Cu, Cd, Pb, Hg dan Ag akan sulit terlarut dalam kondisi perairan yang anoksik
(Ramlal, 1987 in Erlangga 2007). Logam berat yang terlarut dalam air akan
berpindah ke dalam sedimen jika berikatan dengan materi organik bebas atau
materi organik yang melapisi permukaan sedimen, dan penyerapan langsung oleh
permukaan partikel sedimen (Wilson, 1988 in Erlangga 2007).
Logam berat mempunyai sifat yang mudah terikat oleh bahan organik dan
selanjutnya mengendap di dasar perairan dan bersatu dengan sedimen, maka kadar
logam berat dalam sedimen umumnya lebih tinggi dibandingkan dengan di kolom
perairan (Harahap, 1991). Kandungan logam berat pada sedimen umumnya
rendah pada musim kemarau dan tinggi pada musim penghujan. Penyebab
tingginya kadar logam berat dalam sedimen pada musim penghujan kemungkinan
disebabkan oleh tingginya laju erosi pada permukaan tanah yang terbawa ke
dalam badan sungai, sehingga sedimen dalam sungai yang diduga mengandung
logam berat akan terbawa oleh arus sungai menuju muara dan pada akhirnya
terjadi proses sedimentasi (Bryan, 1976). Tabel di bawah ini menunujukkan
konsentrasi logam Cd dan Cu dalam sedimen di beberapa Perairan di Indonesia.
Tabel 2. Konsentrasi Cd dan Cu (ppm) pada sedimen di beberapa Perairan di Indonesia
Lokasi Konsentrasi logam Tahun Sumber Cd (ppm) Cu (ppm)
Perairan Teluk Jakarta
0,90-2,66
(1,75±0,62) (27,6±13,5) 7,6-52,6
1990, Juni Hutagalung (1994)
ttd-0,011 1,884-5,983 September 1998, Nanty (1998) 1,625-6,073 1998, Juli Nanty (1998) Perairan Teluk
Jakarta 0,007-0,277 (0,109)
4,792-2.3 Logam Berat pada Biota Bentik
Logam yang ada pada perairan suatu saat akan turun dan mengendap pada
dasar perairan, membentuk sedimentasi, hal ini akan menyebabkan organisme
yang mencari makan di dasar perairan (udang, rajungan, dan kerang) akan
memiliki peluang yang besar untuk terpapar logam berat yang telah terikat di
dasar perairan dan membentuk sedimen (Rahman, 2006). Akumulasi logam berat
dalam sedimen dalam jumlah banyak dapat berperan sebagai sumber kontaminan
logam untuk kolom air diatasnya ketika tidak ada lagi input ke dalam ekosistem
(Fadhlina, 2008).
Bahan pencemar (racun) masuk ke tubuh organisme melalui
proses absorpsi. Absorpsi merupakan proses perpindahan racun dari tempat
pemejanan atau tempat absorpsinya ke dalam sirkulasi darah. Absorpsi, distribusi
dan ekskresi bahan pencemar tidak dapat terjadi tanpa transpor melintasi
membran. Proses transportasi dapat berlangsung dengan 2 cara : transpor pasif
(yaitu melalui proses difusi) dan transpor aktif (yaitu dengan sistem transport
khusus, dalam hal ini zat lazimnya terikat pada molekul pengemban) (Hutagalung,
1997).
Menurut Simkiss dan Mason (1983) bahwa logam-logam ringan seperti Na, K,
Ca dan Mg merupakan logam dalam kelompok kelas A yang keterlibatan ion
logamnya dalam makhluk hidup menyangkut proses fisiologis. Logam berat yang
dimasukkan dalam kelas B merupakan logam-logam yang terlibat dalam
proses-proses enzimatik dan menimbukan polusi misalnya Zn, Cd, Hg dan Pb. Aktivitas
dari logam kelas A masuk ke dalam tubuh hewan biasanya dengan cara difusi
Faktor lingkungan yang mempengaruhi absorbsi logam berat yaitu konsentrasi
logam berat, salinitas, suhu bentuk fisika kimia logam tersebut (Bayne, 1976 in
Ningtyas, 2002). Sementara faktor yang mempengaruhi laju absorbsi logam berat
pada biota yaitu, konsentrasi logam berat dalam tubuh, ukuran organisme,
pertumbuhan, kondisi fisiologi, seks dll. Logam berat masuk ke dalam jaringan
tubuh biota menurut Simkiss dan Mason (1983) secara umum melalui tiga cara:
1. Endositas
Endositas adalah pengambilan partikel dari permukaan sel dengan membentuk
wahana perpindahan oleh membran plasma. Proses endositas sepertinya
berperan dalam pengambilan logam berat dalam bentuk tidak terlarut.
2. Diserap dari air
Kandungan logam berat dalam jaringan tubuh biota 90% berasal dari
penyerapan oleh sel epitel insang. Insang diduga sebagai organ yang
menyerap logam berat dalam air.
3. Diserap dari makanan dan sedimen
Penyerapan logam dari makanan dan sedimen oleh biota tergantung pada
strategi makanan dan life histories dari biota yang diamati. Pada jenis filter
feeder penyerapan tersebut bukan dari larutan seperti yang dijelaskan di atas,
tetapi makanan dan partikel yang tersarng.
Logam berat merupakan logam yang berperan dalam proses enzimatik. Jenis
logam ini masuk ke dalam jaringan melalui ikatan dengan protein (ligand
binding). Pasangan ion logam dalam air laut akan berbentuk (LCl)0, (LCO3)0,
(LSO4)0, (LCl2)0, dan (LCl3)- yang ikatan ionnya bergantung pada pH air.
menyebabkan membran menjadi ligan protein dalam sel agar logam dapat
berikatan. Logam berat lebih reaktif terhadap ikatan ligan dibandingkan dengan
logam lainnya sehingga dalam sistem metaloenzim akan mengganggu proses
metabolisme sel (Darmono, 1995).
Menurut Darmono (1995) sebagian dari logam berat bersifat essensial bagi
organisme air untuk pertumbuhan dan perkembangan hidupnya, antara lain dalam
pembentukan haemosianin dalam sistem darah dan enzimatik pada biota. Akan
tetapi bila jumlah dari logam berat masuk ke dalam tubuh dengan jumlah berlebih,
maka akan berubah fungsi menjadi racun bagi tubuh (Palar, 2004). Berikut ini
adalah konsentrasi logam berat pada tubuh biota Anadara granosa pada beberapa
Perairan di Indonesia
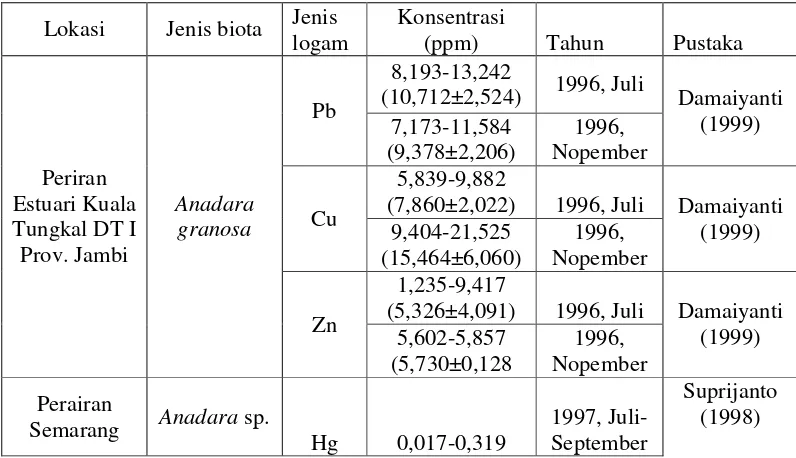
Tabel 3. Kandungan beberapa logam berat pada biota bentik di Perairan Semarang dan Kuala Tungkal
Lokasi Jenis biota Jenis logam Konsentrasi (ppm) Tahun Pustaka
(10,712±2,524) 1996, Juli Damaiyanti (1999)
(7,860±2,022) 1996, Juli Damaiyanti (1999)
(5,326±4,091) 1996, Juli Damaiyanti (1999) 5,602-5,857
(5,730±0,128 Nopember 1996, Perairan
Semarang Anadara sp. Hg 0,017-0,319 1997, Juli-September
2.3 Fraksinasi Logam Berat dalam Sedimen
Logam dalam lingkungan perairan akan berasosiasi dengan berbagai ligan
organik dan anorganik terlarut sebaliknya fraksi yang lain akan berasosiasi dengan
bahan partikulat melalui proses adsorpsi, presipitasi, copresipitasi atau oleh proses
uptake oleh organisme plankton. Proses kimia, fisika dan biologi yang kompleks
menyebabkan fraksi utama dari logam akan masuk dan berasosiasi ke dalam
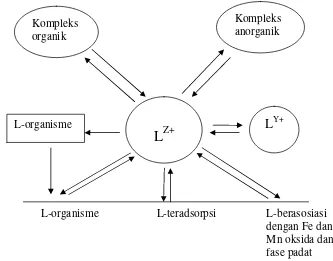
sedimen perairan hal ini dapat dilihat pada gambar 1 (Tessier dan Campbell,
1987).
L-organisme L-teradsorpsi L-berasosiasi dengan Fe dan Mn oksida dan fase padat lainnya L: Logam
Sumber: Tessier dan Campbell, 1987
Gambar 1. Skema pembagian logam di lingkungan perairan
Sedimen merupakan campuran kompleks hasil dari pelapukan dan erosi
seperti alumosilikat dan besi, alumunium oksihidroksida dan sulfida, dan
substansi yang dihasilkan oleh aktivitas biologi baik organik (mikroorganisme, Kompleks
organik
Kompleks anorganik
L
Z+L
Y+
detritus dan substansi humus) maupun inorganik (karbonat, fosfat, dan silikat)
(Tessier, 1992 in Škvarla, 1998). Ketersediaan logam berat dalam sedimen
dipengaruhi oleh hubungan logam - logam berat dengan satu atau lebih dari
komponen penyusun sedimen, karenanya konsentrasi logam berat dalam fraksi
sedimen memberikan gambaran tentang ketersediaan logam berat bagi biota.
Penentuan ketersediaan logam dalam fraksi sedimen telah banyak dikaji.
Tessier et al (1979) membagi fraksi-fraksi di dalam sedimen yang menyebabkan
berikatannya logam, diantaranya ;
1. Fraksi exchangeable ; Komponen utama pada fraksi ini muliputi lempung
(clay), Oksigen hidrat dari besi dan mangan, dan asam humus. Fraksi ini
memiliki mobilitas yang tinggi. Perubahan dari komposisi kation dapat
menyebabkan terlepasnya logam (seperti di lingkungan estuari).
2. Fraksi yang berikatan dengan karbonat ; Logam dapat berasosiasi dengan
karbonat. Fraksi ini mudah berubah dengan perubahan pH.
3. Fraksi berikatan dengan besi dan mangan oksida ; Terdiri dari logam yang
diadsorpsi atau dilapisi oleh Fe-Mn oksida. Fraksi ini memiliki mobilitas
yang relatif tinggi, tergantung pada perubahan kondisi redoks. Perubahan
ini menyebabkan terlepasnya logam tetapi sebagian lagi mengendap jika
terdapat mineral mineral sulfide. Bongkahan atau nodul mangan (Mn) dan
besi (Fe) yang terbentuk di dasar laut adalah bentuk dari sedimen
hydrogeneous yang dihasilkan melalui reaksi kimia dalam air laut.
4. Fraksi yang berikatan dengan bahan organik ; Logam dapat berikatan
dengan berbagai bentuk bahan organik seperti organisme hidup, detritus,
dalam perairan alami, bahan organik dapat terdegradasi dan terjadi
pelepasan logam terlarut.
5. Fraksi residual ; Fase residual terdiri dari mineral utama atau kedua
(primary and secondary minerals) dimana logam berada pada struktur
kristal. Logam tidak akan berubah ke dalam bentuk terlarut pada jangka
waktu tertentu di bawah kondisi normal.
Ketersediaan logam berat dalam sedimen sangat berkaitan erat dengan
sifat-sifat dan ukuran sedimen. Sedimen yang mengandung jumlah mineral lempung
(clay) dan bahan organik akan cenderung mengakumulasi logam lebih tinggi,
karena senyawa-senyawa tersebut memiliki sifat mengikat logam (Tack et. al.,
1997 in Arifin, 2006). Menurut Thomas dan Bendell –Young (1998 ) komponen
hasil oksida besi dan magnesium dan bahan organik merupakan komponen
geokimia yang paling penting dalam mengontrol pengikatan logam - logam berat
dari sedimen estuari. Oleh karena itu, pengetahuan tentang pembagian
logam-logam utama diantara tiga komponen sedimen ini (hasil oksida besi dan
magnesium dan bahan organik) sangat penting untuk mengestimasi ketersediaan
logam-logam berat dalam sedimen.
Ukuran partikel sedimen (grain size) merupakan salah satu faktor yang
mempengaruhi konsentrasi dan proses adsorpsi logam berat dalam sedimen.
Afinitas logam berat umumnya lebih besar pada sedimen yang berukuran lebih
halus (Penny, 1984 dan Gaw, 1997 in Parera 2004) sehingga konsentrasi logam
berat lebih besar pada permukaan sedimen yang memiliki ukuran partikel lebih
kecil (Penny, 1984; Gaw, 1997; Burden, 2002 in Parera 2004). Menurut Bernhard
yang berupa lumpur, tanah liat, pasir berlumpur dan campuran dari ketiganya
dibandingkan dengan yang berupa pasir murni. Tabel 4 menunjukkan hubungan
konsentrasi logam berat Cu, Pb dan Zn terhadap ukuran butiran sedimen.
Tabel 4. Hubungan antara ukuran butiran sedimen (µm) dan konsentrasi logam Cu, Pb dan Zn (µg/g)
Ukuran butiran sedimen (µm)
Faktor lain yang mempengaruhi kandungan logam berat adalah kandungan
bahan organik. Gaw (1997 in Parera 2004) menemukan hubungan yang positif
antara kandungan materi organik dengan konsentrasi logam berat dalam sedimen
walaupun bahan organik bukan merupakan faktor utama yang mengatur
konsentrasi logam berat dalam sedimen khususnya di daerah estuari. Keberadaan
bahan organik mampu mengikat 5-20 % atau lebih dari kandungan logam dalam
sedimen (Campbell et al., 1988).
Mangan oksida dan besi oksida dalam sedimen mempengaruhi kandungan dan
asosiasi logam berat dalam sedimen. Besi oksida yang hidrous, mangan dan
alumunium terutama Fe dan Mn oksida pada keadaan dapat mengoksidasi, dapat
menyerap atau mengkopresipitasi kation dan anion dari larutan dan dapat
menyerap logam-logam dalam air terutama logam runutan. Dalam keadaan
reduksi logam yang terserap dapat diremobilisasi kembali ke larutan dan bertindak
sedimen akan mengalami diagenesis melibatkan peningkatan bobot molekul dan
hilangnya gugus fungsi. Terbentuknya cadangan logam berat dalam sedimen
perairan umumnya relatif stabil dan kurang reaktif, namun demikian mobilisasi
dapat terjadi melalui proses mikrobial (Connel dan Miller, 1995). Menurut
Campbell et al. (1988) keberadaan mangan dan besi oksida dalam sedimen
mampu mengikat logam 10-50 % bahkan lebih dari total logam dalam sedimen
walaupun fraksi Mangan dan besi oksida tersebut jarang sekali ditemukan banyak
sebagai material penyusun sedimen terrigenous. Kandungan logam pada beberapa
fraksi sedimen laut dalam dapat dilihat pada Tabel 5.
Tabel 5. Kandungan Mn- Fe dan beberapa logam pada fraksi-fraksi laut dalam, satuan µg/g
Logam laut dalam Karbonat Lempung (c
lay)
Pembagian logam berat logam dalam sedimen bergantung pada banyak faktor
diantaranya; lingkungan dan konsentrasi ligan di perairan, konsentrasi padatan
subsrat, Eh, pH. Perbedaan faktor lingkungan seperti pengadukan sedimen
anoksik atau proses acidifikasi di kolom perairan dapat merubah pembagian
logam di sedimen (Tessier dan Campbell, 1987). Pembagian logam berat dalam
air dan sedimen juga sangat dipengaruhi kondisi redoks selain keberadaan bahan
pH merupakan salah satu faktor yang sangat penting dalam proses spesiasi logam
berat, kelarutan dari mineral, transport dan kemampuan logam berat dapat diserap
oleh organisme. pH berpengaruh terhadap kemampuan daya larut logam berat
dan proses adsorpsi-desorpsi. Kebanyakan logam berat (mineral hydroxide)
memiliki kelarutan yang sangat rendah di bawah kondisi pH perairan alami,
karena aktivitas ion hydroxide secara langsung berhubungan dengan pH,
kelarutan mineral logam hydroxide akan bertambah seiring dengan penurunan pH,
dan kemudian logam berat yang terlarut sangat potensial dapat dimanfaatkan
dalam proses biologi saat kondisi pH turun (Salomon, 1995 in John dan
Leventhal, 1995).
Faktor lain yang mempengaruhi proses spesiasi logam berat adalah
temperatur. Pada lingkungan perairan, reaksi kimia sangat sensitif terhadap
perubahan temperatur. Temperatur juga dapat mempengaruhi kuantitas logam
berat yang diserap organisme, karena rata-rata proses biologi akan meningkat dua
kali pada tiap kenaikan temperatur 100C. Kenaikan temperatur mempengaruhi
tingkat pemasukan dan pengeluaran logam berat, bioakumulasi mungkin
3. BAHAN DAN METODE
3.1 Lokasi dan waktu penelitian
Penelitian ini merupakan kegiatan program penelitian tentang fate kontaminan
logam di Delta Berau yang dilakukan oleh bagian Dinamika Laut, Pusat Penelitian
Oseanografi Lembaga Ilmu Pengetahuan Indonesia (P2O-LIPI). Penelitian
meliputi pengambilan contoh dan pengukuran data di lapangan dan analisis di
Laboratorium. Pengambilan contoh air, sedimen dan biota dilakukan di Perairan
Delta Berau, Kabupaten Berau, Kalimantan Timur pada tanggal 25-30 April 2008
oleh tim peneliti P2O-LIPI. Analisis laboratorium yang meliputi pengukuran
konsentrasi logam dalam air, kerang, sedimen dan seston dilakukan pada bulan
Mei 2008 hingga Januari 2009 di Laboratorium Pencemaran P2O-LIPI, Jakarta
Utara.
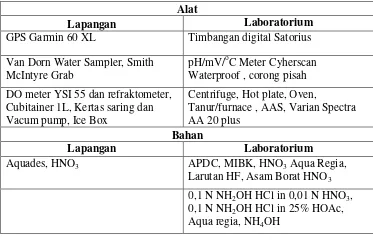
3.2 Alat dan bahan
Penelitian ini menggunakan alat dan bahan yang digunakan di lapangan dan di
laboratorium yang secara rinci disajikan pada Tabel 6
3.3 Teknik pengambilan data 3.3.1 Penentuan stasiun pengamatan
Stasiun pengambilan contoh ditentukan berdasarkan sumber polutan, yaitu
daerah hulu dan mulut-mulut muaranya dan mewakili seluruh perairan delta.
Penentuan geografis stasiun pengambilan contoh menggunakan Global
Positioning System (GPS) yang kemudian diplotkan ke dalam peta (Gambar 2).
Contoh sedimen yang diambil sebanyak 21 stasiun meliputi daerah yang mewakili
Tabel 6. Alat dan bahan penelitian yang digunakan di lapangan dan di laboratorium
Alat
Lapangan Laboratorium
GPS Garmin 60 XL Timbangan digital Satorius
Van Dorn Water Sampler, Smith McIntyre Grab
pH/mV/oC Meter Cyherscan
Waterproof , corong pisah DO meter YSI 55 dan refraktometer,
Cubitainer 1L, Kertas saring dan Vacum pump, Ice Box
Centrifuge, Hot plate, Oven,
Tanur/furnace , AAS, Varian Spectra AA 20 plus
Bahan
Lapangan Laboratorium
Aquades, HNO3 APDC, MIBK, HNO3 Aqua Regia,
Larutan HF, Asam Borat HNO3
0,1 N NH2OH HCl in 0,01 N HNO3,
0,1 N NH2OH HCl in 25% HOAc,
Aqua regia, NH4OH
3.3.2 Pengambilan data di lapangan
Pengambilan data dilakukan melalui pengukuran secara langsung di Perairan
Delta Berau. Pengukuran data di lapangan meliputi suhu air laut (oC), salinitas,
oksigen terlarut (DO, mg/L), dan derajat keasaman perairan (pH) dengan
menggunakan DO meter digital dan refraktometer. Pengambilan sampel air
dilakukan pada kedalaman 1 meter sebanyak 3 kali ulangan.
3.3.3 Pengambilan contoh air
Pengambilan contoh air laut untuk pengukuran Total Suspended Solid (TSS)
dan logam berat dilakukan dengan menggunakan Van Dorn Water Sampler yang
terbuat dari bahan organik PolyVinyl Clorida (PVC) dan memiliki kapasitas 2 liter
sebanyak 1 liter yang diambil dari kedalaman 1 meter dari permukaan air. Contoh
air untuk analisa logam berat disaring dengan nucleopore dengan ukuran pori 0,45
µm yang sebelumnya telah direndam dalam HCl 6 N selama seminggu, dibilas
dengan akuades dan ditimbang berat kosongnya. Contoh seston diambil dari
kertas saring nucleopore yang dipakai untuk menyaring contoh air laut sebanyak 1
liter. Kertas saring nucleopore yang telah digunakan dimasukkan dalam plastik
bersegel dan diberi label. Air yang telah disaring kemudian dimasukkan ke dalam
botol cubitainer 1 liter dan diawetkan dengan menambahkan HNO3 65% (pH < 2)
sebanyak 1 ml . Contoh air dan seston kemudian dimasukkan ke dalam ice box
dengan suhu < 4ºC untuk dianalisis lebih lanjut di laboratorium, kemudian
disimpan dalam ice box untuk dianalisis kandungan logam berat lebih lanjut di
3.3.4 Pengambilan contoh sedimen
Contoh sedimen diambil dengan menggunakan Smith Mcintyre Grab yang
terbuat dari stainless steel pada lapisan permukaan sedimen dengan kedalaman
0-5 cm. Contoh sedimen diambil sebanyak tiga kali ulangan pada setiap stasiun
yang kemudian dikumpulkan (dikomposit) menjadi satu. Contoh kemudian
dimasukkan ke dalam wadah yang terbuat dari polietilen yang terlebih dahulu
dibersihkan dengan perendaman dalam 6 N HNO3 dan dibilas tiga kali dengan air
suling bebas ion kemudian disimpan dalam ice box.
3.3.5 Pengambilan contoh biota Anadara granosa
Pengambilan contoh biota Anadara granosa dilakukan dengan menggunakan
cawuk Smith McIntyre yang memiliki bukaan mulut 0,05 m2. Contoh sedimen
yang didapatkan kemudian ditempatkan ke dalam ayakan bermata saringan 500
m dan dibilas in situ dengan air laut hingga relatif bersih dari lumpur. Residu
sedimen tersebut kemudian dimasukkan kedalam kantung plastik yang telah diberi
label dan difiksasi dengan campuran formalin 10%. Biota Anadara granosa
kemudian dibekukan sampai analisis berikutnya.
3.4 Analisis contoh
3.4.1 Pengukuran logam dalam air laut
Analisis logam berat terlarut dalam air laut menggunakan prosedur APHA,
1992 in Hutagalung et al., 1997. Sebanyak 250 ml contoh air yang telah diambil
ditambahkan HNO3 (1N) dan NaOH (1N) hingga pH sampel air menjadi 3,5 – 4
kemudian dimasukkan ke dalam corong pisah polietilen. Dalam suasana asam,
kandungan logam berat (kecuali Hg) yang terkandung dalam air laut bereaksi jika
kompleks organik yang tidak larut dalam fase air. Dengan penambahan pelarut
organik (MIBK), senyawa kompleks logam berat-APDC larut dalam metil iso
butil keton (MIBK). Kompleks logam berat-APDC dipecah dengan HNO3 pekat,
sehingga terbentuk ion dan larut kembali ke dalam fase air. Fase air ditampung
kemudian diukur konsentrasi logam beratnya. Analisis konsentrasi logam berat
dalam air laut dapat dilihat pada Lampiran 1.
3.4.2 Pengukuran logam dalam seston
Analisis logam berat dalam seston menggunakan prosedur APHA, 1992 in
Hutagalung et al., 1997. Kertas saring yang telah digunakan untuk menyaring 1L
air laut dikeringkan dalam oven selama 24 jam, kemudian digunakan untuk
menghitung zat padat tersuspensi/TSS dan logam berat dalam seston. Destruksi
contoh TSS dengan menggunakan aquaregia (campuran HCl dan HNO3 pekat 3 :
1) dan penambahan 1 ml HF pekat dan kemudian dipanaskan pada suhu 90 –
1000C selama 4 jam. Setelah larutan contoh dingin pada suhu kamar, larutan
contoh dimasukkan ke dalam labu ukur polyethylene yang telah berisi campuran 5
ml asam borat dan dibilas dengan aquades teflon bombnya hingga volume
penepatan 25 ml. Larutan contoh dikocok-kocok dan dibiarkan selama 24 jam,
kemudian larutan contoh didekantasi menggunakan kertas saring nucleopore
ukuran ukuran pori 0,45 m. Larutan contoh yang telah didekantasi kemudian
diukur dengan AAS menggunakan nyala udara asetilen. Analisis pengukuran
3.4.3 Pengukuran logam dalam sedimen
Analisis logam berat total dalam sedimen menggunakan prosedur
Bendell-Young et al. (1992) in Thomas dan Bendell-Young (1998), dimana nilai
konsentrasi hasil destruksi menggunakan aqua regia sebagai nilai yang mendekati
konsentrasi logam berat total dalam sedimen. Contoh sedimen (± 5 gram Berat
basah) didestruksi menggunakan campuran HCl pekat dengan HNO3 pekat (3:1)
kemudian dipanaskan 850C dalam penangas selama 8 jam. Sampel sedimen
kemudian ditepatkan 25 ml dengan akuades dan disentrifuge pada 250 RPM dan
diambil fase supernatannya untuk kemudian dihitung konsentrasinya dengan AAS
(Lampiran 3).
3.4.4 Pengukuran logam berat dalam Anadara granosa
Analisis logam berat dalam tubuh Anadara granosa menggunakan metode
Parsons (1999). Namun sebelumnya, Anadara granosa dikelompokkan terlebih
dahulu ke dalam 3 ukuran panjang yaitu; ukuran kecil (< 2,5 cm), sedang (2,5 –
3cm) dan besar (3 – 5 cm) sebelum dilakukan analisis. Analisis hanya dilakukan
pada jaringan (tissue) tubuhya. Sampel jaringan kerang yang di analisis
ditimbang dengan bobot ± 10 gram berat basah, kemudian sampel didestruksi
dengan larutan 10 ml HNO3 pekat di dalam teflon bomb, kemudian ditentukan
konsentrasi logam dengan AAS. Analisis logam berat pada tubuh Anadara
granosa dapat dilihat pada Lampiran 4.
3.4.5 Ukuran butiran sedimen
Ukuran butiran sedimen ditentukan menggunakan alat ayakan mekanik.
0,15 mm, dan 0,063 mm. Pengayakan dilakukan dengan metode pengayakan
basah. Butiran sedimen diklasifikasi berdasarkan klasifikasi Wenworth, 1922 in
Wibisono, 2005. Klasifikasi ini memisahkan sedimen ke dalam fraksi ukuran
butiran yang berbeda yaitu kerakal 8-16 mm, kerikil 2-8 mm, pasir (sand) 0,063-2
mm, lanau (silt) 0,004-0,063 mm, lumpur (mud) <0,063 dan lempung (clay)
<0,004 mm. Pada penelitian ini data grain size sedimen hanya didapatkan pada
fraksi kerikil, pasir dan lumpur (Lampiran 5).
Analisis ukuran butiran sedimen dikerjakan pada gabungan sampel dari 3 kali
ulangan tiap masing-masing stasiun yang dilakukan di Laboratorium Geologi,
P2O- LIPI. Hasil analisis butiran sedimen dapat dilihat pada Lampiran 11.
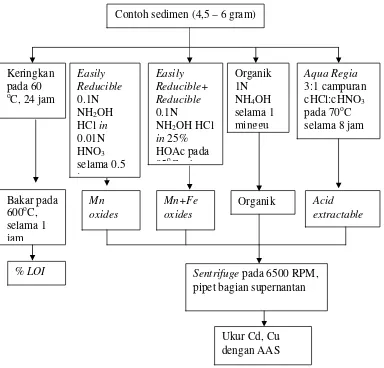
3.4.6 Analisis fraksinasi logam berat dalam sedimen
Analisis pengukuran logam berat dalam fraksi sedimen menggunakan metode
ekstraksi secara simultan yang dikembangkan Bendell-Young et al. (1992) in
Thomas dan Bendell-Young (1998) seperti pada Gambar 9 dan Lampiran 7.
Prosedur ekstraksi secara simultan menghitung konsentrasi logam berat yang
secara operasional dibagi kedalam komponen-komponen geokimia sedimen:
easily reducible (berasosiasi dengan fase sedimen mangan oksida); easily
reducible+reducible (berasosiasi dengan fase sedimen mangan oksida dan besi
oksida); organik (fraksi sedimen yang berikatan dengan bahan organik); dan aqua
regia (mendekati konsentrasi logam berat total dalam sedimen).
Sebanyak 4,5 – 6 gram berat basah contoh sedimen diambil untuk mengukur
konsentrasi logam berat pada setiap fraksi sedimen tersebut. Ekstraksi logam
pada fraksi easily reducible menggunakan 10 ml 0,1N NH2OH HCl in 0.01N
0.1N NH2OH HCl in 25% HOAc dengan pemanasan pada suhu 950C selama 6
jam, sedangkan ekstraksi logam pada fraksi organik dengan menggunakan 20 ml
1N NH4OH ke dalam contoh sedimen kemudian dibiarkan selama seminggu
(Gambar 3).
Pada penelitian ini, dilakukan beberapa modifikasi terhadap metode
Bendell-Young et al., 1992 in Thomas and Bendell-young, 1998, analisis bahan organik
total (TOM) pada sedimen yang dinyatakan dengan persentase lost on ignition
(%LOI) dianalisis menurut APHA (1992) yaitu dengan pembakaran sampel
sedimen pada suhu 500oC selama 4 jam, dapat dilihat pada Lampiran 5.
Selain itu, terdapat perbedaan terhadap penentuan klasifikasi logam berat
dalam fraksi resistan dan non-resistan berdasarkan metode yang digunakan
Thomas dan Bendell-young (1998). Pada metode Thomas dan Bendell-young,
fraksi reducible dan easy reducible termasuk ke dalam fraksi non-resistan (dapat
diserap oleh biota), sedangkan fraksi organik dan residual termasuk ke dalam
resistan (tidak dapat diserap oleh biota). Pada penelitian ini fraksi organik
termasuk ke dalam fraksi non-resistan, dengan alasan tahapan destruksi pada
fraksi organik tidak menggunakan asam kuat (HNO3/HCl) seperti pada prosedur
menurut Bendell-Young dan Harvey (1992). Perbedaan klasifikasi fraksi resistan
Sumber : Bendell-Young et al., 1992 in Thomas dan Bendell-Young, 1998
Gambar 3. Skema analisis fraksinasi geokimia logam berat pada sedimen
Tabel 7. Perbedaan klasifikasi fraksi resistan dan non resistan antara yang digunakan dalam skripsi dengan Thomas dan Bendell-Young (1998)
Fraksi sedimen Thomas dan Bendell-
Young (1998) Skripsi
Sentrifuge pada 6500 RPM,
4. HASIL DAN PEMBAHASAN
4.1 Kualitas Perairan Delta Berau
Kondisi perairan Delta Berau berdasarkan hasil pengamatan dipengaruhi oleh
masukan 2 aliran sungai utama yaitu aliran Sungai Kelay dan dan Sungai Segah.
Rincian data parameter kualitas air yang diamati disajikan pada Lampiran 8.
Suhu stasiun pengamatan perairan Delta Berau, April 2008 memiliki kisaran
antara 26,3 0C – 29,7 0C, dengan suhu terendah berada pada stasiun 1 dan suhu
tertinggi pada stasiun 8 (Gambar 4). Pada wilayah sungai suhu perairan berkisar
antara 26,3oC – 28,6oC dengan rata-rata 27,4oC, untuk wilayah muara suhu
perairan berkisar 27,5 oC – 29,7 oC dengan rata-rata 28,4 oC, sedangkan untuk
wilayah laut suhunya berkisar antara 28,1 oC – 29,1 oC dengan rata-rata 28,4 oC.
Menurut Nontji (1987), suhu air permukaan di perairan Indonesia berkisar antara
28 oC – 31oC dan dalam setahun terdapat dua suhu maksimum yaitu pada musim
pancaroba awal tahun (April – Mei) dan pancaroba akhir tahun (November),
sedangkan pada penelitian sebelumnya kisaran suhu untuk perairan Delta Berau
berkisar antara 29,4 oC – 32,1 oC. Suhu di perairan Delta Berau pada saat
pengamatan dan penelitian sebelumnya tidak jauh berbeda sehingga dapat
dikatakan suhu Perairan Delta Berau masih dalam kondisi normal.
Temperatur memiliki pengaruh penting dalam spesiasi logam, karena
kebanyakan tingkat reaksi kimia sangat sensitif terhadap perubahan temperatur.
Temperatur juga dapat mempengaruhi kuantitas logam berat yang diserap
organisme, karena rata-rata proses biologi akan meningkat dua kali lipat pada tiap
influx (pemasukan) dan efflux (pengeluaran) logam berat, bioakumulasi total
mungkin meningkat atau tidak (Luoma, 1983 in John dan Leventhal, 1995)
Gambar 4. Nilai suhu perairan (0C) pada stasiun pengamatan menurut zonasi di perairan Delta Berau, April 2008
117.65 117.7 117.75 117.8 117.85 117.9 117.95 118 118.05 118.1
1.8
Perairan pada stasiun pengamatan Delta Berau memiliki kedalaman yang berbeda.
Stasiun pengamatan yang memiliki kedalaman paling besar pada Stasiun 19,
sedangkan stasiun yang memiliki kedalaman terendah berada pada Stasiun 11 dan
12. Gambar 6 menunjukkan kedalaman perairan Delta Berau pada stasiun
pengamatan. Kedalaman Perairan Delta Berau pada stasiun pengamatan
tergolong dangkal dengan kisaran kedalaman antara 2 – 22 meter. Stasiun daerah
sungai dan muara umumnya lebih dangkal daripada stasiun di daerah laut,
sehingga sebaran kedalaman secara spasial menunjukkan bahwa nilai kedalaman
pada daerah laut lebih tinggi dari daerah sungai maupun muara (Gambar 7). Pada
stasiun 6 tidak ada nilai kedalamannya.
117.65 117.7 117.75 117.8 117.85 117.9 117.95 118 118.05 118.1
Gambar 7. Sebaran spasial kedalaman (m) secara horizontal perairan Delta Berau, April 2008
Salinitas perairan Delta Berau dari sungai hingga ke laut memiliki kisaran
antara 0 -30 dengan rata-rata 18,2. Kisaran nilai salinitas untuk daerah sungai 0 -
14 dengan rata-rata 6,2, daerah muara memiliki kisaran salinitas 18 - 22 dengan
rata-rata 14,2, sedangkan pada stasiun di laut memiliki kisaran salinitas 22 - 30
dengan rata-rata 27,4. Pada Stasiun 1 dan Stasiun 2 salinitas bernilai 0 artinya
daerah sungai tersebut tidak dipengaruhi pencampuran air laut ketika pasang.
Nilai salinitas tertinggi ada pada Stasiun 13, 18, 19 dan 21 dengan nilai salinitas
30, sehingga secara umum nilai salinitas meningkat menuju kearah laut. Hasil
pengamatan nilai salinitas disajikan pada Gambar 8, sedangkan sebaran spasial
salinitas Perairan Delta Berau dapat dilihat pada Gambar 9. Kisaran salinitas
stasiun pengamatan Delta Berau dapat dikatakan masih berada dalam kisaran
alami di alam, kisaran alami salinitas untuk perairan estuari di Indonesia menurut
Gambar 8 . Nilai salinitas pada stasiun pengamatan menurut zonasinya di perairan Delta Berau, April 2008
117.65 117.7 117.75 117.8 117.85 117.9 117.95 118 118.05 118.1 1.8
Gambar 9. Sebaran spasial salinitas di perairan Delta Berau, April 2008
Derajat keasaman (pH) pada stasiun pengamatan perairan Delta Berau, April
2008 berkisar antara 6,46 – 8,02 dengan pH terendah berada pada Stasiun 1 dan
pH tertinggi pada Stasiun 21 (Gambar 10). Nilai rata-rata pH untuk stasiun di
daerah sungai bernilai 6,86, nilai rata-rata pH untuk stasiun di daerah muara 7,37
sungai umumnya kecil kemudian bertambah besar berdasarkan zonasinya menuju
daerah laut (Gambar 11). Kisaran pH pada stasiun pengamatan dapat dikatakan
berada pada kisaran nilai pH alami di alam. Menurut Romimohtarto (2007) pH
perairan pesisir permukaan di Indonesia berada pada kisaran 6,00 - 8,50.
Gambar 10. Nilai pH pada stasiun pengamatan menurut zonasinya di perairan Delta Berau, April 2008
117.65 117.7 117.75 117.8 117.85 117.9 117.95 118 118.05 118.1 1.8
Kadar oksigen terlarut (DO) pada stasiun pengamatan perairan Delta Berau, April
2008 memiliki kisaran antara 4,34 mg/l – 6,40 mg/l. Kadar terendah berada pada
Stasiun 6 dan kadar tertinggi pada Stasiun 1. Kadar oksigen terlarut pada stasiun
pengamatan semakin bertambah besar nilainya berdasarkan zonasi ke arah laut
dengan rata-rata kadar oksigen terlarut di derah sungai, muara dan laut 5,16 mg/l,
5,33 mg/l, dan 5,88 mg/l (Gambar 8). Secara keseluruhan perairan Delta Berau
dapat dikatakan masih layak untuk kehidupan biota. Kadar DO minimum
peruntukan kehidupan organisme akuatik 4,0 mg/l (Monoarfa, 2002)
Oksigen terlarut di dalam sedimen (interstitial water) juga mempengaruhi
keberadaan mangan. Mn2+ terlarut pada lapisan oksidasi sedimen akan dioksidasi
menjadi (MnO2)S, dan pada lapisan dibawahnya (lapisan reduksi sedimen) Mn
oksida akan direduksi kembali menjadi (Mn2+)AQ. Dengan demikian, jumlah
Mn2+ terlarut meningkat dengan bertambahnya kedalaman sedimen, sedangkan
Mn fase solid akan menurun (Chester, 1990).
Muara Garura
Gambar 13. Sebaran spasial oksigen terlarut (mg/l) di Perairan Delta Berau, April 2008
Total padatan tersuspensi (Total Suspended Solid/ TSS) adalah bahan-bahan
tersuspensi (diameter >1 m) yang tertahan pada saringan millipore dengan
diameter pori 0,45 m. TSS terdiri atas lumpur dan pasir halus serta jasad-jasad
renik terutama yang disebabkan oleh kikisan tanah atau erosi yang terbawa ke
dalam badan air. TSS pada Perairan Delta Berau berkisar antara 5,50 mg/l –
41,80 mg/l. TSS terendah pada stasiun 13 dan tertinggi pada stasiun 1. TSS di
wilayah sungai berkisar antara 10,9 mg/l – 41,8 mg/l dengan rata-rata 23,71 mg/l,
di wilayah muara berkisar antara 8,60 mg/l – 24,10 mg/l dengan rata-rata 16,39
mg/l, di wilayah laut TSS berkisar antara 5,50 mg/l – 16,75 mg/l dengan nilai
rata-rata 8,94 mg/l (Gambar 14). Sebaran TSS secara spasial menunjukkan bahwa
semakin ke arah laut nilai TSS semakin kecil, nilai TSS terbesar terdapat pada
padatan tesuspensi sebagai akibat dari pelapukan batuan, kikisan tanah atau erosi
yang terjadi di daratan dan terbawa dalam aliran air sungai.
Gambar 14. Nilai padatan tersuspensi total (TSS) (mg/l) pada stasiun pengamatan berdasarkan zonasi di Perairan Delta Berau, April 2008
117.65 117.7 117.75 117.8 117.85 117.9 117.95 118 118.05 118.1
1.8
4.2 Konsentrasi Cd dan Cu terlarut
Konsentrasi Cu dan Cd terlarut di perairan Delta Berau, Kalimantan Timur
pada bulan April 2008 disajikan pada Gambar 10 dan Lampiran 9. Pengambilan
data logam berat terlarut pada perairan Delta Berau hanya dilakukan pada 6
stasiun, 4 stasiun untuk daerah muara sungai dan 2 stasiun untuk daerah laut.
Konsentrasi Cu pada perairan Delta Berau berada pada kisaran ttd – 0,001 mg/l
dengan konsentrasi terendah pada Stasiun 8 dan tertinggi pada Stasiun 7 dan 18.
Konsentrasi Cd pada perairan Delta Berau berkisar antara 0,0005 mg/l – 0,001
mg/l dengan konsentrasi terendah berada di Stasiun 9, 10, 13 dan konsentrasi Cd
terbesar pada Stasiun 7, 8, 9, 18.
Keberadaan Cd dan Cu terlarut di Perairan Delta Berau sangat dipengaruhi
oleh aktivitas manusia di daerah aliran sungai, aktivitas manusia di kawasan Delta
Berau seperti pertambangan, pelabuhan atau aktivitas kapal, pembuangan limbah
pabrik, penebangan hutan, pengawetan kayu juga diduga dapat menghasilkan
bahan pencemar senyawa yang mengandung Cd dan Cu di perairan Delta Berau
sehingga konsentrasinya bertambah (Situmorang, 2008). Konsentrasi Cd dan Cu
terlarut pada stasiun pengamatan Delta Berau masih tergolong sesuai dengan
kadar alami dalam air laut. Konsentrasi Cd alami dalam air laut sebesar 0,11 ppb
(Whaldichuck, 1974 in Rohyatun et al., 2003) dan konsentrasi Cu alami dalam air
laut berkisar antara 0,002 – 0,005 ppm (Palar, 1994) atau 0,002 ppm
(Whaldichuck, 1974 in Rohyatun et al., 2003). Konsentrasi Cd dan Cu dalam
perairan pada beberapa penelitian di Perairan Indonesia dapat dilihat pada Tabel
Gambar 10. Konsentrasi Cd dan Cu (mg/l) terlarut pada stasiun pengamatan menurut zonasi di perairan Delta Berau, April 2008
4.3 Konsentrasi Cd dan Cu dalam seston
Konsentrasi logam berat dalam seston menunjukkan besarnya kandungan
logam dalam padatan tersuspensi dalam kolom perairan. Gambar 11
menunjukkan konsentrasi Cd dan Cu dalam seston di wilayah Delta Berau,
Kalimantan Timur pada bulan April 2008. Konsentrasi Cu dalam seston berkisar
antara 18,667 µg/g – 104,388 µg/g dengan konsentrasi terbesar pada Stasiun 4 dan
konsentrasi terendah pada Stasiun 12. Konsentrasi Cd dalam seston di perairan
Delta Berau berkisar antara <0,001 µg/g – 23,048 µg/g dengan konsentrasi
terbesar pada Stasiun 18 dan konsentrasi terendah pada Stasiun 2, 5 dan 15.
Konsentrasi Cu dalam seston jauh lebih besar dari pada Cd, bahkan pada beberapa
Gambar 11. Konsentrasi Cd dan Cu (µg/g) dalam seston pada stasiun
pengamatan menurut zonasi di perairan Delta Berau, April 2008
4.4 Ukuran butiran sedimen (grain size)
Sedimen perairan terdiri dari berbagai tipe substrat dengan ukuran yang
berbeda, umumnya sedimen terdiri dari campuran dari bermacam-macam tipe
sedimen yang berbeda. Penentuan jenis dan komposisi sedimen pada penelitian
ini didasarkan pada tiga tipe fraksi utama yakni pasir, kerikil dan lumpur.
Komposisi fraksi sedimen periran Delta Berau pada stasiun pengamatan dapat
Gambar 12. Tipe sedimen pada stasiun pengamatan Perairan Delta Berau, April 2008
Tipe sedimen perairan Delta Berau pada stasiun pengamatan didominasi oleh
lumpur (mud) dengan persentasi antara 6,26% – 97,99% dengan persentasi
terbesar berada pada Stasiun 18 dan persentasi terkecil pada Stasiun 1. Fraksi
pasir mendominasi pada Stasiun 1, 5 , 12, 13 dan 21. Kisaran persentasi fraksi
pasir pada stasiun pengamatan adalah 2,01% – 92,09%, sedangkan hanya sedikit
fraksi kerikil yang ditemukan pada stasiun pengamatan. Pada stasiun di daerah
aliran sungai dan di daerah muara didominasi oleh fraksi lumpur demikian juga
dengan stasiun pada zonasi di daerah laut lebih didominasi oleh fraksi lumpur,
hasil analisis butiran sedimen secara lengkap dapat dilihat pada Lampiran 11 dan
12. Tipe sedimen akan mempengaruhi kandungan logam berat dan spesiasinya
dalam sedimen, sedimen yang banyak mengandung fraksi yang lebih halus
memiliki kemampuan mengikat logam berat lebih tinggi bila dibandingkan fraksi