PENGUJIAN TERHADAP PENGIKATAN DAN PELEPASAN
SEFALEKSIN PADA ERITROSIT SECARA IN VITRO
Matheus Timbul Simanjuntak
Jurusan Farmasi FMIPA Universitas Sumatera Utara
Jl. Bioteknologi No. 1 Kampus USU Medan 20155
Abstrak
Telah dilakukan penelitian mengenai pengujian terhadap pengikatan dan pelepasan sefaleksin pada eritrosit manusia secara in vitro. Pengikatan dan pelepasan sefaleksin terhadap eritrosit manusia dilakukan pada temperatur kamar, pHin = pHout = 7,4. Hasil percobaan pengikatan sefaleksin terhadap eritrosit
manusia menunjukkan adanya kenaikan konsentrasi obat terikat dengan menaiknya konsentrasi sefaleksin dan pada konsentrasi di atas 1 mM terjadi peningkatan yang lebih tajam dan pelepasan sefaleksin dari ikatan sefaleksin terhadap eritrosit manusia berlangsung dengan cepat.
Kata Kunci: Sefaleksin, eritrosit, ikatan protein, in vitro
PENDAHULUAN
Eritrosit dapat berfungsi sebagai pembawa obat karena mempunyai sifat biodegradasi, nonimunogenik dan dapat ditargetkan secara selektif pada hati atau limpa tergantung pada karakteristik membran, sehingga dapat diaplikasikan untuk penyampaian secara target terbatas terutama untuk pengobatan penyakit yang terjadi pada lisosom dan toksisitas logam. (Gennaro, 2000)
Sefaleksin merupakan suatu antimikroba turunan amino sefalosporin yang bersifat lipofilik dan sukar diabsorbsi pada usus halus dari kelinci percobaan (Kimura T. dkk, 1985) dengan pKa 1 = 2,5, pKa2 = 5,2, dan pKa3 = 7,3 dan luas digunakan untuk pengobatan (Moffat, 1986).
Berbagai penelitian tentang ikatan protein terhadap obat pada eritosit manusia telah dilakukan antara lain untuk; golongan sulfonamid (Matsumoto, et al., 1989), zonisamid dengan metode sentrifugasi dan ultrafiltrasi menyatakan bahwa sel utuh dan karbonik anhidrase mempunyai afinitas yang tinggi untuk berikatan (Matsumoto, et al.,1989), sulfadimetoksin dan metabolit utamanya (Otagiri, et al., 1989), pentosifilin
dengan metode spektroskopi spin resonansi yang menyatakan bahwa fluiditas pada daerah posfolipid dalam eritrosit meningkat dengan peningkatan konsentrasi obat dan adanya interaksi liposom dengan eritrosit menyebabkan perubahan dalam molekul membran sel di sekitar Band 3 yang menghasilkan pelepasan protein dari membran eritrosit (Sato, et al., 1990), terhadap metabolit hidroklotiazid ditemukan adanya dua ikatan dan salah satu adalah pada karbonik anhidrase (Yamazaki, et al., 1990), modifikasi liposom dengan glisirrhizin (Tsuji, et al., 1991), karprofen (Kohita, et al., 1994), glisirrhizin (Ishida, et al., 2001) dan KE – 298 (Endo, et al., 2001). Namun bagaimana hubungan antara sefaleksin dengan eritrosit belum banyak diteliti sampai saat ini.
BAHAN DAN METODA
Bahan
Sefaleksin (Sigma, St.Louis, M.O), darah manusia (PMI), Natrium Klorida (Widatra Bhakti, Pandaan), membran selulosa (Cellophan Tubing Seamless).
Pembuatan Kurva Serapan Sefaleksin
Ditimbang seksama 50 mg sefaleksin dan dimasukkan ke dalam labu tentukur 100 ml, dilarutkan dengan larutan natrium klorida fisiologis dan dicukupkan volume sampai garis tanda. Larutan ini dipipet 3,4 ml dan dimasukkan ke dalam labu tentukur 100 ml kemudian dicukupkan volume dengan penambahan larutan natrium klorida fisiologis sampai garis tanda, konsentrasi sefaleksin = 17 mcg/ml. Ukur serapan larutan dengan spektrofotometer pada panjang gelombang 220-320 nm.
Pembuatan Larutan Induk Baku
Ditimbang seksama 35 mg sefaleksin, dimasukkan dalam labu tentukur 100 ml dilarutkan dalam larutan natrium klorida fisiologis dan dicukupkan volumenya hingga garis tanda.
Pembuatan Kurva Kalibrasi
Dari larutan induk baku dibuat larutan sefaleksin dengan berbagai konsentrasi yaitu: 0,002; 0,006; 0,01; 0,02; 0,03; 0,04; 0,05; 0,06; 0,07; 0,08; 0,09; 0,1 mM dengan cara memipet larutan induk baku 0; 0,1; 0,3; 0,5; 1; 1,5; 2; 2,5; 3; 3,5; 4; 4,5; 5 ml ke dalam labu tentukur 50 ml, kemudian ditambahkan larutan natrium klorida fisiologis sampai garis tanda. Ukur serapan pada panjang gelombang 263 nm.
Pencucian Membran Selulosa
Membran selulosa dengan panjang 12 cm dimasukkan dalam wadah yang telah berisi aquadest, kemudian dipanaskan selama 3 jam sampai transparan.
Penyediaan Media Eritrosit
Ke dalam 5 ml eritrosit yang bercampur dengan antikoagulansia ditambahkan 5 ml larutan natrium klorida
fisiologis dingin, campur sampai homogen dengan bantuan pencampur sentuh (touch-mixer). Disentrifuge dengan kecepatan 3000 rpm selama 5 menit. Pisahkan supernatan dari endapan. Endapan (eritrosit) ditambah kembali dengan 5 ml larutan natrium klorida fisiologis dingin campur sampai homogen dengan bantuan touch-mixer. Kemudian disentrifuge pada 3000 rpm selama 5 menit dan kembali dilakukan pemisahan supernatan dari endapan. Percobaan diulangi sampai diperoleh supernatan yang jernih. Eritrosit yang telah bersih disimpan pada temperatur dingin.
Percobaan Pengikatan Sefaleksin Terhadap Eritrosit
1. Untuk Blanko 1
Masukkan 10 ml larutan natrium klorida fisiologis ke dalam membran selulosa dengan panjang 12 cm, ikat ke 2 ujung membran dengan benang bedah dan dilakukan uji kebocoran, kemudian masukkan ke dalam beakerglass 250 ml yang telah berisi medium berupa 50 ml larutan natrium klorida fisiologis. Setiap 15 menit aduk perlahan-lahan, dan lakukan percobaan selama 1 jam. Ukur absorbansi dari larutan medium pada λ = 263 nm.
2. Untuk Blanko 2
2 ml darah yang telah dicuci dicampur dengan 8 ml larutan natrium klorida fisiologis didalam membran selulosa dengan panjang 12 cm, ikat ke 2 ujung membran dengan benang bedah dan dilakukan uji kebocoran, kemudian masukkan ke dalam beaker glass 250 ml yang telah berisi medium 50 ml larutan natrium klorida fisiologis. Setiap 15 menit aduk perlahan-lahan, dan lakukan percobaan selama 1 jam. Ukur absorbansi dari larutan medium pada λ = 263 nm.
Masukkan 10 ml larutan natrium klorida fisiologis ke dalam membran selulosa dengan panjang 12 cm, ikat ke 2 ujung membran dengan benang bedah dan dilakukan uji kebocoran, kemudian masukkan ke dalam beakerglass 250 ml yang berisi medium 50 ml larutan sefaleksin dalam larutan natrium klorida fisiologis dengan konsentrasi 0,02 mM. Setiap 15 menit aduk perlahan-lahan, dan lakukan percobaan selama 1 jam. Ukur absorbansi dari larutan medium pada λ = 263 nm.
4. Untuk Sampel
2 ml darah yang telah dicuci dicampur dengan 8 ml larutan natrium klorida fisiologis didalam membran selulosa dengan panjang 12 cm, ikat ke 2 ujung membran dengan benang bedah dan dilakukan uji kebocoran, kemudian masukkan ke dalam beaker glass 250 ml yang berisi medium 50 ml larutan sefaleksin dalam larutan natrium klorida fisiologis dengan konsentrasi 0,02 mM. Setiap 15 menit aduk perlahan-lahan, dan lakukan percobaan selama 1 jam. Ukur absorbansi dari larutan medium pada λ = 263 nm. Lakukan percobaan sama seperti prosedur di atas dengan variasi konsentrassi 0,02 mM – 1,5 mM.
Percobaan Pelepasan Sefaleksin dari pengikatan dengan eritrosit
1) Untuk sampel 1
2 ml darah yang telah dicuci dicampur dengan 8 ml larutan natrium klorida fisiologis didalam membran selulosa dengan panjang 12 cm, ikat ke 2 ujung membran dengan benang bedah dan dilakukan uji kebocoran, kemudian masukkan ke dalam beakerglass 250 ml yang berisi larutan sefaleksin 0,5 mM didiamkan selama 1 jam. Dilakukan uji pelepasan terhadap hasil pengikatan di atas dengan menggunakan medium 200 ml larutan natrium klorida fisiologis. Dilakukan variasi waktu sampling sampai dengan setengah jam. Volume 10 ml medium yang digunakan segera diganti dengan
10 ml larutan natrium klorida fisiologis. Larutan medium yang diperoleh diukur dengan menggunakan spektrofotometer ultraviolet pada λ = 263 nm
HASIL DAN PEMBAHASAN
Kurva serapan sefaleksin dalam larutan natrium klorida fisiologis
Serapan maksimum larutan sefaleksin dengan konsentrasi 17 mcg/ml dalam larutan natrium klorida fisiologis dengan metode spektrofotometer ultraviolet diperoleh pada panjang gelombang 263 nm. Hasil ini hampir sesuai dengan Farmakope Indonesia Edisi IV yang menyatakan bahwa λ maks sefaleksin adalah 262 nm.
Kurva kalibrasi sefaleksin dalam larutan natrium klorida fisiologis
Kurva kalibrasi dari larutan sefaleksin dibuat dengan mengukur absorbansi pada panjang gelombang 263 nm dengan metode spektrofotometri dari suatu seri larutan sefaleksin dalam larutan natrium klorida fisiologis dengan interval konsentrasi pengukuran yaitu 0,002 mM; 0,006 mM; 0,01 mM; 0,02 mM; 0,03 mM; 0,04 mM; 0,05 mM; 0,06 mM; 0,07 mM; 0,08 mM; 0,09 mM; 0,1 mM. Dari grafik absorbansi vs konsentrasi diperoleh harga persamaan garis regresi Y = 9,2408X + 0,0062 dengan koefisien korelasi (r) = 0,9989 yang memperlihatkan adanya korelasi liner antara peningkatan konsentrasi dengan absorbsi dalam inerval 0,002 mM – 0,1 mM.
Pengikatan sefaleksin terhadap eritrosit
Percobaan ini dilakukan untuk menge-tahui kemampuan dari sefaleksin untuk berikatan dengan eritrosit manusia.
Rancangan urutan percobaan pengi-katan sefaleksin terhadap eritrosit seperti yang tercantum pada metodologi dilakukan dengan maksud :
2. Prosedur b: untuk mengetahui pengaruh eritrosit terhadap membran selulosa.
3. Prosedur c: untuk mengetahui pengaruh membran selulosa terhadap obat.
4. Prosedur d: untuk mengetahui pengaruh eritrosit terhadap obat.
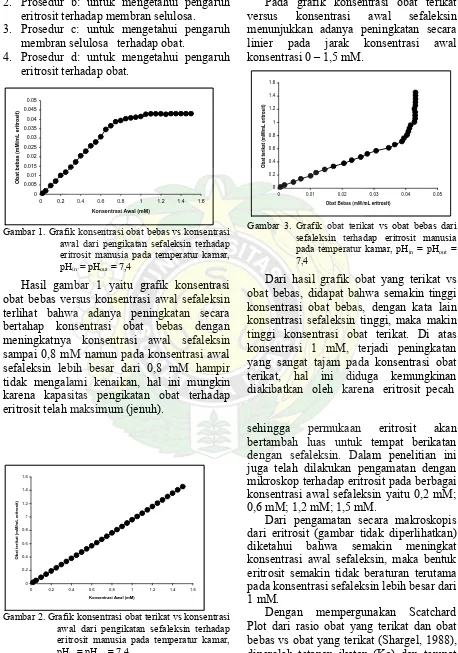
Gambar 1. Grafik konsentrasi obat bebas vs konsentrasi awal dari pengikatan sefaleksin terhadap eritrosit manusia pada temperatur kamar, pHin = pHout = 7,4
Hasil gambar 1 yaitu grafik konsentrasi obat bebas versus konsentrasi awal sefaleksin terlihat bahwa adanya peningkatan secara bertahap konsentrasi obat bebas dengan meningkatnya konsentrasi awal sefaleksin sampai 0,8 mM namun pada konsentrasi awal sefaleksin lebih besar dari 0,8 mM hampir tidak mengalami kenaikan, hal ini mungkin karena kapasitas pengikatan obat terhadap eritrosit telah maksimum (jenuh).
Gambar 2. Grafik konsentrasi obat terikat vs konsentrasi awal dari pengikatan sefaleksin terhadap eritrosit manusia pada temperatur kamar, pHin = pHout = 7,4
Pada grafik konsentrasi obat terikat versus konsentrasi awal sefaleksin menunjukkan adanya peningkatan secara linier pada jarak konsentrasi awal konsentrasi 0 – 1,5 mM.
Obat Bebas (mM/mL eritrosit)
Obat ter
ikat (mM/mL er
itr
Konsentrasi Awal (mM)
O
b
at bebas (mM/
mL eri
trosi
t)
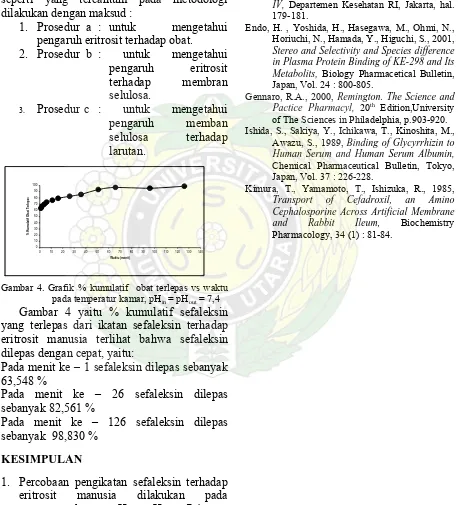
Gambar 3. Grafik obat terikat vs obat bebas dari sefaleksin terhadap eritrosit manusia pada temperatur kamar, pHin = pHout =
7,4
Dari hasil grafik obat yang terikat vs obat bebas, didapat bahwa semakin tinggi konsentrasi obat bebas, dengan kata lain konsentrasi sefaleksin tinggi, maka makin tinggi konsentrasi obat terikat. Di atas konsentrasi 1 mM, terjadi peningkatan yang sangat tajam pada konsentrasi obat terikat, hal ini diduga kemungkinan diakibatkan oleh karena eritrosit pecah
sehingga permukaan eritrosit akan bertambah luas untuk tempat berikatan dengan sefaleksin. Dalam penelitian ini juga telah dilakukan pengamatan dengan mikroskop terhadap eritrosit pada berbagai konsentrasi awal sefaleksin yaitu 0,2 mM; 0,6 mM; 1,2 mM; 1,5 mM.
Konsentrasi Awal (mM)
O
Dari pengamatan secara makroskopis dari eritrosit (gambar tidak diperlihatkan) diketahui bahwa semakin meningkat konsentrasi awal sefaleksin, maka bentuk eritrosit semakin tidak beraturan terutama pada konsentrasi sefaleksin lebih besar dari 1 mM.
berikatan (n) dari sefaleksin terhadap eritrosit. (grafik tidak diperlihatkan)
2. Pelepasan sefaleksin dari ikatan sefaleksin terhadap eritrosit manusia berlangsung dengan cepat.
Pelepasan sefaleksin dari eritrosit manusia
DAFTAR PUSTAKA
Urutan percobaan pelepasan sefaleksin dari ikatan sefaleksin terhadap eritrosit manusia seperti yang tercantum pada metodologi dilakukan dengan maksud :
DitJen POM, 1995, Farmakope Indonesia. Edisi Ke IV, Departemen Kesehatan RI, Jakarta, hal. 179-181.
1. Prosedur a : untuk mengetahui pengaruh eritrosit terhadap obat.
2. Prosedur b : untuk mengetahui pengaruh eritrosit terhadap membran selulosa.
Endo, H. , Yoshida, H., Hasegawa, M., Ohmi, N., Horiuchi, N., Hamada, Y., Higuchi, S., 2001,
Stereo and Selectivity and Species difference in Plasma Protein Binding of KE-298 and Its
Metabolits, Biology Pharmacetical Bulletin,
Japan, Vol. 24 : 800-805.
3. Prosedur c : untuk mengetahui pengaruh memban selulosa terhadap larutan.
Gennaro, R.A., 2000, Remington. The Science and
Pactice Pharmacyl, 20th Edition,University
of The Sciences in Philadelphia, p.903-920. Ishida, S., Sakiya, Y., Ichikawa, T., Kinoshita, M.,
Awazu, S., 1989, Binding of Glycyrrhizin to Human Serum and Human Serum Albumin,
Chemical Pharmaceutical Bulletin, Tokyo, Japan, Vol. 37 : 226-228.
0 10 20 30 40 50 60 70 80 90 100
0 10 20 30 40 50 60 70 80 90 100 110 120 130 140
Waktu (menit)
% K
u
mu
la
ti
f O
b
a
t T
e
rl
e
p
a
s
Kimura, T., Yamamoto, T., Ishizuka, R., 1985,
Transport of Cefadroxil, an Amino Cephalosporine Across Artificial Membrane
and Rabbit Ileum, Biochemistry
Pharmacology, 34 (1) : 81-84.
Gambar 4. Grafik % kumulatif obat terlepas vs waktu pada temperatur kamar, pHin = pHout = 7,4
Gambar 4 yaitu % kumulatif sefaleksin yang terlepas dari ikatan sefaleksin terhadap eritrosit manusia terlihat bahwa sefaleksin dilepas dengan cepat, yaitu:
Pada menit ke – 1 sefaleksin dilepas sebanyak 63,548 %
Pada menit ke – 26 sefaleksin dilepas sebanyak 82,561 %
Pada menit ke – 126 sefaleksin dilepas sebanyak 98,830 %
KESIMPULAN