LAPORAN PENELITIAN KOLEKTIF
REKAYASA MATERIAL ABSORBER GELOMBANG
MIKRO BERBASIS LANTANUM MANGANAT
PENELITI
Ketua
SITTI AHMIATRI SAPTARI
19770416 200501 2 008
Anggota
PRIYAMBODO
19800507 200910 1 002
Pusat Penelitian dan Penerbitan
Lembaga Penelitian dan Pengabdian kepada Masyarakat (LP2M)
DAFTAR ISI
DAFTAR GAMBAR
Gambar 2.1. Struktur perovskite ideal 5
Gambar 2.2. Diagram fase La1-x CaxMnO3 8
Gambar 2.3. Diagram fase La1-xBaxMnO3 9
Gambar 2.4. Diagram fase La1-xSrxMnO3 10
Gambar 2.5. Hubungan refletation loss dengan frekuensi gelombang mikro pada La0,6Sr0,4MnO3 11
Gambar 2.18. Skema Teori Double Exchange (DE) 37
Gambar 2.19. Mekanisme interaksi superexchange 39
Gambar 2.20. Perubahan energi elektronik selama proses pembentukan kompleks 40
Gambar 2.21. Splitting octahedral pada level d5 41
Gambar 2.22. Spin state pada weak field dan strong field ligand untuk d4 sistem 43
DAFTAR TABEL
Tabel 2.1. Tujuh sistem kristal 17
Tabel 2.2. Energi ionisasi beberapa atom ringan 20
Tabel 2.3. Pembagian daerah jangkauan gelombang mikro 53
BAB 1
PENDAHULUAN
1.1. Latar Belakang
Beberapa tahun terakhir ini, polusi interferensi gelombang elektromagnet
cukup serius muncul akibat perkembangan yang pesat dari bisnis alat komunikasi,
seperti telepon selular dan sistem radar [1]. Hal ini dapat menyebabkan
terganggunya sistem peralatan berbasis elektronik dan sistem keamanan yang
sangat vital. Diyakini pula bahwa radiasi gelombang mikro yang berasal dari
sinyal telepon selular dapat memicu terjadinya sel kanker [2]. Fenomena tersebut
menarik minat banyak peneliti untuk mengembangkan material yang mampu
menyerap gelombang elektromagnet. Material absorber ini dapat mengubah
energi gelombang elektromagnet menjadi energi panas sehingga material ini
sangat bermanfaat untuk melindungi suatu objek dari gelombang elektromagnet
yang tidak diinginkan [3].
Material absorber secara umum dibagi menjadi dua tipe yaitu material
dielektrik dan material magnetik. Magnet lunak seperti ferit tipe spinel dan
campuran feromagnet adalah material yang biasa digunakan sebagai absorber [4].
Namun pada umumnya saat daerah frekuensi 1-5 GHz, absorber seperti ferit tipe
spinel tidak dapat berfungsi dengan baik karena permeabilitasnya menurun
dengan drastis seperti yang ditentukan oleh Snoek (Snoek’s limit) [5]. Oleh
karena itu banyak peneliti melakukan riset untuk merekayasa atau pun mencari
material baru yang memiliki permeabilitas tetap besar ketika daerah frekuensi
Material lantanum manganat La1-xAxMnO3 (A : Sr, Ba, Ca) telah beberapa
dekade ini menjadi topik riset yang menarik bagi para peneliti. Hal ini disebabkan
karena sifat magnetik dan transport yang tidak biasa, serta adanya fenomena
magnetoresistansi yakni perubahan resistansi listrik ketika ada medan magnet
eksternal [6,7]. Sifat magnetoresistensi ini diaplikasikan untuk sensor magnetik
dan juga penyimpanan data (data storage) [8]. Selain itu, ditemukan pula bahwa
lantanum manganat dapat menjadi kandidat yang potensial sebagai material
penyerap gelombang mikro pada frekuensi tinggi.
Pada tahun 2002 Li dkk [9] mensintesis La1-xSrxMnO3 dengan metode
solid state reaction kemudian absorbsi gelombang mikronya dikarakterisasi pada rentang frekuensi 8-14 GHz. Selanjutnya terdapat penelitian yang mendoping
material La1-xSrxMnO3 dengan ion Fe sehingga menjadi La1-xSrxMn1-yFeyO3
[10-12]. Penelitian tersebut menggunakan metode sol-gel dan sifat absorbsi
gelombang mikronya dipelajari dengan rentang frekuensi 2-18 GHz. Dari hasil
pendopingan tersebut diperoleh bandwidth dan intensitas gelombang mikro yang
lebih baik. Zhou dkk [13] melaporkan bahwa nanopartikel La0,8Ba0,2MnO3
memiliki sifat absorbsi gelombang mikro pada frekuensi 2-18 GHz, dengan
puncak 13 dB pada frekuensi 6,7 GHz, dan bandwidth absorbing diatas 10 dB
pada frekuensi 1,8 GHz.
Penelitian tentang material absorber gelombang mikro terus mengalami
perkembangan dengan ditemukannya berbagai material baru atau pun rekayasa
material. Berdasarkan deskripsi yang telah dipaparkan kami tertarik untuk
1.2. Rumusan Masalah
Kriteria sebuah material untuk dapat dijadikan material absorber
gelombang elektromagnet salah satunya adalah bahan tersebut memililki nilai
permeabilitas dan permitivitas setinggi mungkin dan saturasi magnet yang tinggi.
Material lanthanum manganat diketahui memiliki criteria yang sesuai untuk
keperluan sebagai bahan absorber gelombang elektromagnet terutama setelah
adanya substitusi ion divalent terhadap La. Namun material ini masih memiliki
permeabilitas yang rendah. Oleh karena itu masih diperlukan rekayasa material
lanthanum manganat agar dapat menjadi material absorber gelombang
electromagnet yang unggul.
1.3. Tujuan Penelitian
Penelitian ini bertujuan
a. Untuk menganalisis proses pembentukan sampel La0,67Ba0,33Mn1-xNixO3.
b. Untuk menganalisis struktur kristal sampel La0,67Ba0,33Mn1-xNixO3.
c. Untuk menganalisis karakteristik magnetik sampel La0,67Ba0,33Mn1-xNixO3.
d. Untuk menganalisis pengaruh dopan Ni pada sampel La0,67Ba0,33Mn
1-xNixO3 terhadap kinerja sampel sebagai material absorber gelombang
mikro.
1.4. Batasan Penelitian
Kajian penelitian hanya dibatasi pada pembuatan sampel dengan variasi
TGA (Thermogravimetry Analyser), XRD (X Ray Diffraction), SEM (Scanning
Electron Microscope), Permagraf, dan VNA (Vector Network Analyser).
1.5. Manfaat Penelitian
Penelitian ini di lakukan dengan harapan mendapatkan material berbasis
lantanum manganat yakni La0.67Ba0.33Mn1-xNixO3 yang dapat diaplikasikan
BAB 2
TINJAUAN PUSTAKA
2.1. Lantanum Manganat
Lantanum manganat, La1-xAxMnO3, dapat dianggap sebagai sistem biner
yang terdiri dari larutan padat LaMnO3 dan AMnO3, untuk x = 0 dan x = 1. G.H
Jonker dan J.H Van Saten [14] adalah pelopor penelitian bahan perovskite pada
tahun 1950, dengan menerbitkan kilasan dari sistem biner bahan perovskite
seperti LaMnO3– CaMnO3, LaMnO3– SrMnO3, dan LaMnO3– BaMnO3.
2.1.1. Struktur Kristal Lantanum Manganat
Struktur kristal lantanum manganat merupakan turunan dari struktur
perovskite, yang memiliki formula umum ABO3. Gambar 2.1 menunjukkan
struktur perovskite kubik yang ideal. Dalam lantanum manganat kedudukan A
diisi oleh ion La3+ dan jika x>0 maka disubstitusi kation Ca2+, Sr2+, Ba2+, dan
lain-lain. Sedangkan kedudukan B diisi oleh ion Mn.
Kestabilan struktur perovskite tergantung pada ukuran ion kedudukan A
dan B. Jika ada ketidakcocokan antara ukuran ion kedudukan A dan B dalam kisi
dimana mereka berada maka stuktur perovskite akan mengalami distorsi.
Goldschmidt [16] mendefinisikan faktor toleransi sebagai berikut
(2.1)
Dengan rA dan rB adalah jari-jari ion kedudukan A dan kedudukan B, secara
bertuturut-turut., dan rO adalah jari-jari ion oksigen. Struktur perovskite kubik
yang ideal didapatkan jika harga t*=1.
.Norby dkk [17] melaporkan bahwa material dasar dari lantanum
manganat, LaMnO3, memiliki struktur ortorombik pada suhu ruang. Berbeda
halnya dengan lanthanum manganat yang telah didoping oleh ion lain,
strukturnya tergantung dari ion dopingnya, variasi konsentrasi ion doping,
temperatur, dan lain-lain. Untuk La1-xSrxMnO3 ketika harga x sekitar 0,1 memiki
struktur ortorombik namun saat x=0,175 memiliki struktur rombohedral [18]. Ju
dkk [19] memperoleh struktur La0,62Ba0,38MnO3 adalah kubik dengan parameter
kisinya 3,906 Å. Pada penelitian lain yang dilakukan oleh Sergei [20] La
1-xBaxMnO3, saat 0≤x≤0,05 memiliki struktur ortorombik, saat 0,1≤x≤0,β5
strukturnya rombohedral sedangkan saat 0,β7≤x≤0,5 strukturnya kubik.
Transformasi fasa struktur ini biasanya disertai dengan perubahan fasa magnetik
2.1.2. Sifat Magnetik Lantanum Manganat
Karakteristik mendasar dari manganat dengan valensi campuran adalah
hubungan yang dekat antara transport elektronik dan kemagnetan. Ciri utamanya
adalah transisi simultan dari antiferomagnetik dengan sifat isolator ke
feromagnetik dengan sifat konduktor akibat adanya substitusi pada kedudukan A.
Teori dasar dari fenomena ini telah dikemukan oleh Zener tahun 1951 [21] , yang
memperkenalkan konsep double exchange, yaitu terjadi karena transfer elektron
yang bergantung pada spin dari ion Mn3+ ke Mn4+ pada tetangga terdekat melalui
ion O2-. Teori ini selanjutnya diperbarui oleh Anderson dan Hasegawa tahun 1953
[22] dan de Gennes tahun 1960 [23] yang melibatkan distorsi Jahn-Taller.
Schiffer dan Ramirez [24] pada tahun 1995 melakukan penelitian tentang
diagram fase magnetik dari La1-x CaxMnO3 dengan variasi konsentrasi 0≤x≤1
(Gambar 2.2). Ketika x=0 dan x=0,1 bahan bersifat feromagneti isolator pada
temperature rendah dengan temperature Currie sekitar 160K. Diantara x=0,2 dan
x=0,45 bahan bersifat feromagnetik logam dan menunjukkan fenomena colossal
magnetoresistance (CMR). Untuk x lebih besar dari 0,45 bahan bersifat antiferomanetik isolator.
Gambar 2.2. Diagram fase La1-x CaxMnO3 [24]
Penelitian diagram fase magnetik La1-xBaxMnO3 (Gambar 2.3) dilakukan
oleh Ju dkk [19]. Sampel keramik padatan La1-xBaxMnO3 (x=0; 0,06; 0,13; 0,19;
0,25; 0,31; 0,38; 0,44; 0,5; 0,63; 0,75; 0,88; 1,0) dibuat dengan metode solid state
reaction. Bahan La2O3, BaCO3, dan MnCO3 dicampur selanjutnya dipanaskan
pada suhu 1100oC-1300oC kemudian dikalsinasi pada suhu 1400oC-1550oC. Sifat
magnetic dikarakterisasi dengan menggunakan SQUID (superconducting quantum
interference device). Ditemukan bahwa bahan bersifat feromagnetik untuk seluruh
harga x, namun terdapat tiga fase. Untuk wilayah konsentrasi doping yang rendah
bahan bersifat feromagnetik isolator, wilayah 0,β≤x≤0,5 bahan bersifat
feromagnetik logam, sedangkan untuk konsentrasi doping yang tinggi bahan
Gambar 2.3. Diagram fase La1-xBaxMnO3 [19]
Urushibara dkk [18] pada tahun 1995 melakukan pendopingan Sr
terhadap LaMnO3, ketika doping Sr kecil bahan bersifat isolator. Saat x mencapai
titik kritis yakni sekitar 0,17 bahan bersifat metalik diserta dengan munculnya
Gambar 2.4. Diagram fase La1-xSrxMnO3 [18]
2.1.3. Sifat Absorbsi Gelombang Elektromagnet Lantanum Manganat
Penelitian yang dilakukan oleh Cheng dkk [25] menemukan bahwa
nanopartikel La0,6Sr0,4MnO3 yang dibuat dengan metode sol gel mampu
menyerap gelombang mikro. Daerah frekuensi yang diamati dari 1 GHz sampai
12 GHz. Reflection loss (RL) optimal -41,1 dB pada frekuensi 8,2 GHz dengan
ketebalan 2,2 mm, bandwidth dengan haga RLkurang dari -10 dB dicapai pada
daerah frekuensi 5,5-11,3 GHz (Gambar 2.5). Dalam laporannya Cheng juga
mengungkapkan bahwa semakin kecil ukuran partikel maka sifat absorbsinya
Gambar 2.5. Hubungan refletation loss dengan frekuensi gelombang
mikro pada La0,6Sr0,4MnO3 [25]
Zhou dkk pada tahun 2007 [13] melaporkan bahwa nanopartikel
La0,8Ba0,2MnO3 memiliki sifat absorbsi gelombang mikro pada frekuensi 2-18
GHz, dengan puncak 13 dB pada frekuensi 6,7 GHz, dan bandwidth absorbing
diatas 10 dB pada frekuensi 1,8 GHz. Nanopartikel La0,8Ba0,2MnO3 dibuat dengan
metode sol-gel dari bahan dasar La2O3, Mn(C2H4O2)2, dan Ba(OH)2 dengan berat
fraksi mol 2:5:1. Bahan dasar tersebut dicampur bersama pada suhu 70oC selama
6 jam dan selanjutnya dikalsinasi pada suhu 800oC selama 2 jam. Kurva
Gambar 2.6. Hubungan antara reflektansi dan frekuensi gelombang mikro
pada La0,8Ba0,2MnO3 [13]
2.2. Struktur Kristal
Zat padat yang terdapat di alam ini bila ditinjau secara mikrostruktur dapat
dikelompokkan ke dalam dua kategori, yaitu zat padat yang memiliki susunan
atom tidak teratur ( non kristal ) dan zat padat yang memiliki susunan atom yang
teratur (kristal) [26].
Kristal didefinisikan sebagai material padat yang letak atom-atomnya
membentuk barisan yang teratur rapih secara periodik dalam pola tiga dimensi,
sehingga memiliki sifat fisika maupun kimia serba sama di seluruh bagiannya,
adapun yang termasuk bahan-bahan kristal seperti: semua logam, sebagian besar
2.2.1. Kisi kristal
Cara paling sederhana untuk memahami kisi kristal adalah dengan
membayangkan atom-atom dalam kristal berupa titik-titik. Setiap titik-titik
mempunyai lingkungan yang serba sama, sehingga satu sama lain tidak dapat
dibedakan walaupun dipandang dari segala arah. Bila tiap-tiap titik tersebut
dihubungkan maka akan diperoleh kisi-kisi yang teratur dan periodik memenuhi
ruang. Gambar 2.1 adalah ilustrasi yang menunjukan kisi sebuah suatu sistem
kristal [27].
2.2.2. Parameter Kisi
Panjang tiap-tiap ruang sel yang searah dengan sumbu kristalografi disebut
dengan tetapan kisi (lattice constant), dan dinamakan dengan parameter kisi
sumbu a, b, dan c. Sudut yang dibentuk oleh garis bc, ac, dan ab berturut-turut
disebut dengan α, , . Gambar β.8 adalah ilustrasi dari parameter kisi.
2.2.3. Sistem kristal
Terdapat tujuh sistem kristal yang dikembangkan menjadi empat belas kisi
bravais dalam pengelompokan struktur kristal. Pengelompokan ini berdasarkan
pada karakteristik unit selnya, antara lain sifat-sifat vektor basis, sudut antar
vektor basis dan karakteristik elemen simetrinya. Pada karakteristik unit sel
terdapat sifat-sifat geometri kristal antara lain ; indeks Miller, bidang kristal (hkl)
dan konstanta kisi. Pada gambar 2.9 ditunjukkan tujuh system krsital berikut
2.2.4. Indeks Miller
Misalkan x adalah fraksi perkalian dari vektor basis a, y adalah fraksi
perkalian dari vektor b dan z adalah perkalian dari vektor basis c, maka invers dari
ketiga fraksi dapat dikalikan dengan suatu bilangan sedemikian rupa sehingga
ketiga fraksi (triplet) menghasilkan bilangan bulat terkecil. Triplet atau set
bilangan bulat ini disebut indeks miller, diberi simbol (hkl). Hubungan ketiga
indeks miller ini akan membentuk bidang yang disebut dengan bidang Bragg.
2.2.5. Jarak Bidang Kristal ( d )
Untuk mengetahui jarak antara bidang di dalam kristal adalah harus
mengetahui indeks miller dari bidang-bidang tersebut. Misalkan jarak antar
bilangan diberi symbol dhkl , maka secara matematis hubungan antara dhkl dengan
indeks miller basis kostanta kisi untuk sistem orthorombik, dapat ditulis sebagai
berikut:
(2.2)
dimana : h k l itu merupakan bidang kristalografi atau indeks miller.
2.3. Teori Dasar Sinar-X
Sinar-X adalah salah satu bentuk dari radiasi gelombang elektromagnetik
yang memiliki panjang gelombang antara 0,01 – 100 Ǻ. Karena berbentuk
mengionisasi elektron terdalam dari beberapa unsur ringan seperti pada Tabel 2.2
Tabel 2.2 Energi ionisasi beberapa atom ringan
Atom Energi Ionisasi (eV)
Sinar-x ditemukan dengan tidak sengaja oleh seorang professor Fisika
Wilhelm K. Rontgen 8 November 1895 ketika sedang melakukan percobaan
dalam laboratorium yang berada di lantai dua apartemennya di Würzburg, Bavaria
(sekarang bagian dari German). Dia melakukan percobaan dengan menggunakan
tabung sinar katoda dengan sumber tegangan DC sebesar 20 Volt dan dengan
menggunakan koil dia dapat menaikan tegangan sampai 35000 Volt dengan cara
memutus secara periodik aliran arus ke rangkaian sebanyak 8 kali per detik. Dia
menyimpulkan bahwa radiasi dengan kemampuan tembus yang besar dapat
ditimbulkan jika elektron dengan energi kinetik yang besar menumbuk materi.
Radiasi ini dapat menembus bahan dengan mudah, menyebabkan bahan
belum diketahui maka pada saat itu dinamakan sinar-X. Daya tembus sinar-X
akan bertambah dangan bertambahnya energi kinetik elektronnya, juga intensitas
yang makin besar dengan bertambahnya jumlah elektron.
Pada Gambar 2.11 diperlihatkan skema dari produksi sinar-X didalam
sebuah tabung katoda. Beda potensial Ua akan mempercepat gerakan elektron dari
katoda ke target anoda, sedangkan Uh menentukan banyaknya elektron yang
terlepas dari katoda. Elektron yang terlepas akan menumbuk target anoda
sehingga akan kehilangan sebagian besar atau seluruh energi kinetiknya ketika
mengalami tumbukan dengan dengan atom target; energi inilah yang berubah
menjadi sinar-X.
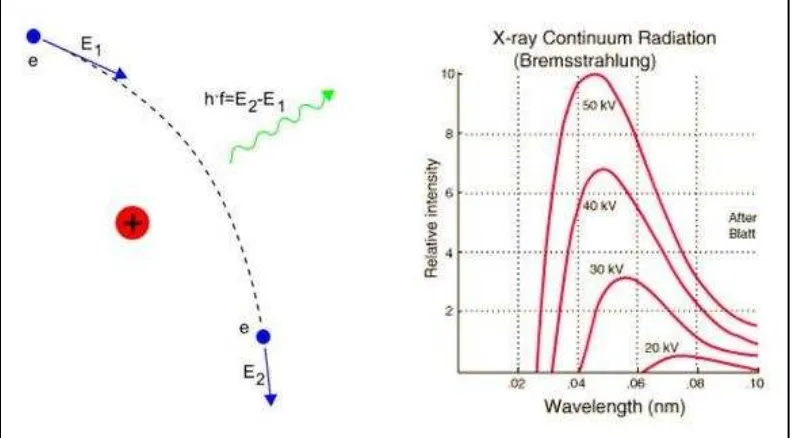
2.3.1. Brehmsstrahlung
Elektron yang bergerak cepat dari katoda akan mengenai target anoda dan
mengalami penghentian mendadak. Berdasarkan teori elektromagnetik, muatan
listrik yang mengalami percepatan akan meradiasikan gelombang elektromagnetik
dan elektron yang bergerak cepat yang tiba-tiba dihentikan jelas mengalami
percepatan. Sinar-X brehmsstrahlung atau “breaking radiation” merupakan
produksi sinar-x yang dihasilkan dari penghentian elektron yang bergerak dengan
kecepatan yang tinggi oleh inti atom target. Kekuatan sinar-x yang dihasilkan
merupakan selisih energi kinetik elektron mula-mula dan energi elektron setelah
mengalami penghentian. Gambar 2.9 menjelaskan bagaimana proses terjadinya
sinar-X bremsstarhlung dan spektrum sinar-X tungsten pada berbagai potensial
pemercepat [29].
2.3.2 Sinar-X Karakteristik
Pada gambar 2.13 terlihat dua puncak dengan intensitas yang tajam pada
panjang gelombang tertentu dari target unsur molybdenum. Puncak-puncak ini
timbul pada berbagai panjang gelombang tertentu untuk masing-masing bahan
target dan asalnya adalah penataan kembali struktur elektron atom target setelah
diganggu oleh tembakan elektron energi tinggi.
Gambar 2.13 Sinar-X karakteristik
Elektron dari katoda yang bergerak dengan percepatan yang cukup tinggi,
dapat mengenai elektron dari atom target (anoda) sehingga menyebabkan elektron
tereksitasi dari atom, selanjutnya elektron lain yang berada pada sub kulit yang
dengan memancarkan sinar-X yang memiliki energi sebanding dengan selisih
level energi elektronnya.
Mekanisme munculnya K dan K adalah ketika kekosongan terjadi pada
kulit kulit-K (n=1), elektron dari kulit di atasnya (L, M, N dst) akan turun mengisi
kekosongan tersebut sambil memancarkan foton dengan energi yang merupakan
selisih energi dari kulit elektron asal (L,M,N dst) dan kulit-K . Sinar-X yang
dihasilkan oleh elektron dari L ke K dinamakan sinar-X Kα dan sinar-X K untuk
dari M ke K. Sedangkan pada kulit-L akan menghasilkan sinar-X Lα untuk
transisi M ke L dan L untuk transisi N ke L dan seterusnya. Sedangkan
kekosongan pada kulit yang ditinggalkan elektron untuk mengisi level energi
dibawahnya akan diisi oleh elektron dengan level energi yang ada diatasnya dan
seterusnya sehingga dihasilkan sinar-X dengan berbagai panjang gelombang.
2.3.3. X-Ray Diffractometer (XRD)
Pada tahun 1912, Max Von Laue menyatakan bahwa panjang gelombang
sinar-X ternyata bersesuaian dengan jarak antar atom-atom dalam kristal. Dengan
alasan itu dia mengusulkan untuk menggunakan kristal untuk mendifraksikan
sinar-X dengan kisi kristal berlaku sebagai kisi tiga dimensi.
Sebuah kristal terdiri dari deretan atom yang teratur letaknya,
masing-masing atom dapat menghamburkan gelombang elektromagnetik yang
mengenainya. Berkas sinar-X monokromatik yang jatuh pada sebuah kristal akan
tertentu gelombang hambur itu akan berineraksi konstruktif sedangkan yang lain
berinteraksi destruktif. Atom-atom dalam kristal membentuk keluarga bidang
datar dengan masing-masing keluarga mempunyai jarak tertentu untuk tiap
komponen bidangnya. Analisis ini diusulkan oleh W. L. Bragg pada tahun 1913,
yang kemudian bidang-bidang tersebut dinamai bidang Bragg.
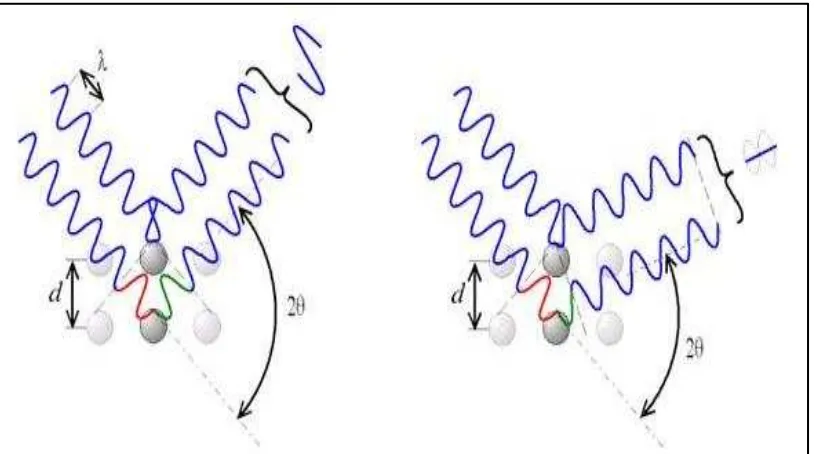
Ketika suatu bidang kristal disinari, maka akan terjadi dua kemungkinan
interferensi akibat difraksi atom-atom penyusun kristalnya; pertama interferensi
konstruktif: berkas sinar yang didifraksikan saling menguatkan karena
mempunyai fasa yang sama dan kedua intrferensi destruktif: berkas sinar yang
didifraksikan saling melemahkan. Kedua jenis interferensi tersebut dapat dilihat
pada Gambar 2.14
Gambar 2.15 Hamburan sinar-X pada kristal
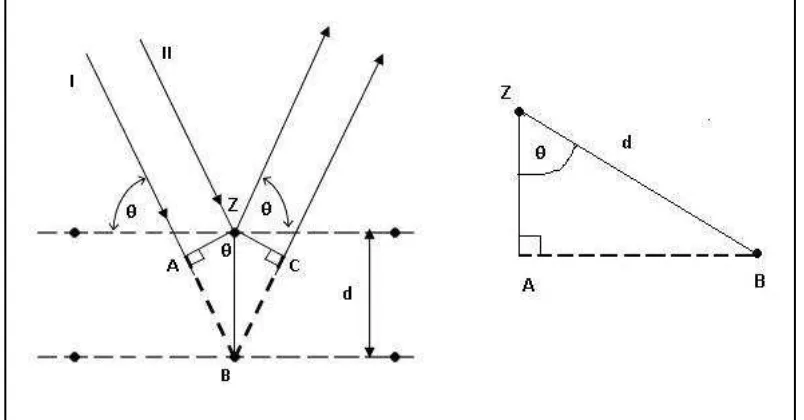
Syarat yang diperlukan agar sinar-x membentuk interaksi konstruktifdapat
dilihat pada Gambar 2.15 diatas. Suatu berkas sinar-x dengan panjang gelombang
λ jatuh pada kristal dengan sudut θ terhadap permukaan bidang Bragg yang jarak
diantaranya d. Berkas sinar mengenai atom Z pada bidang pertama dan atom B
pada bidang berikutnya, dan masing-masing atom akan menghamburkan sebagian
berkas tersebut pada arah rambang. Interferensi konstruktif hanya terjadi antara
sinar yang terhambur sejajar dengan beda jarak jalannya tepat λ, β λ, γ λ dan
seterusnya. Jadi beda jarak jalan harus nλ, dengan n sebagai bilangan bulat.
Maka syarat Bragg untuk berkas hamburan konstruktif adalah
- Sudut jatuh dan sudut hambur kedua berkas harus sama
- 2d sin θ = n λ ; n = 1, 2, 3, ... dst
bilangan bulat n menyatakan orde berkas sinar yang dihamburkan.
Gambar 2.16 Skema XRD
2.4. Metode Analisis Rietveld
Metode tradisional untuk melakukan analisis kualitatif dan kuantitatif pada
teknik Difraksi sinar-X biasanya melibatkan pengukuran intensitas dari puncak
yang terpilih dan membandingkannya dengan data standar seperti International
Committee Difraction Data (ICDD). Bagaimanapun, metoda ini sangat membosankan, disamping memerlukan data standar yang sangat bervariasi pada
saat muncul keganjilan intensitas yang disebabkan oleh penyimpangan sudut.
Disamping itu pula metode ini tak dapat lagi memberikan hasil yang akurat jika
terdapat banyak puncak-puncak yang saling tumpang tindih (overlap) sehingga
akan menyebabkan hilangnya rincian informasi yang terkandung di dalam profil
puncak difraksi tersebut. Dengan demikian diperkenalkan metode baru untuk
menganalisis profil multifasa dari pola difraksi serbuk.
Dasar untuk analisis profil multifasa dari pola difraksi serbuk secara
lengkap pertama kali diperkenalkan oleh Rietveld tahun 1969. Rietveld
menunjukkan bahwa kemungkinan mereplika hasil sebuah pengukuran pola
difraksi dengan pola hitungan/kalkulasi. Kelebihannya adalah di kala terjadi
kesalahan yang disebabkan oleh penyimpangan intensitas dari preparasi cuplikan
atau ketidaksempurnaan model struktur cenderung akan meninggalkan sisa
intensitas baik negative maupun positif selama factor-faktor dari kalkulasi
tersebut tidak diubah oleh Taylor tahun 1991. Kemudian para peneliti lain seperti
Hewat tahun 1973, Wiles & Young tahun 1981, Will, Huang dan Parrish tahun
1983, Hill dan Howard tahun 1986, dan Taylor tahun 1991 melengkapi hasil
refinement program Rietveld ini dengan memberikan sebuah parameter kualitas.
Setiap titik pada pola difraksi dipandang sebagai satu pengamatan tunggal
yang kemungkinan mengandung kontribusi dari sejumlah refleksi Bragg yang
berbeda. Pada setiap posisi sudut atau setiap titik pada profil pola difraksi, jumlah
kontribusi intensitas akibat overlap dapat dihitung berdasarkan nilai
parameter-parameter yang didapat dengan asas perhitungan Siroquant. Siroquant adalah
suatu program analisis multi fasa jenis Rietveld yang dapat mereplika pola
difraksi hasil pengukuran/observasi dengan memanfaatkan least-square fitting
terbaik mendekati pola difraksi yang terukur. Sehingga perbedaan yang dihasilkan
dari pola difraksi observasi dan kalkulasi ditandai dengan derajat tingkat
replikasinya. Derajat tingkat replika (degree of fit) dilambangkan dengan sebuah
parameter statistik χ2 (
chi-squared). Idealnya nilai dari chi-squaredχ2 = 1. Namun nilai ini sangat sulit dicapai, umumnya kurang dari 3. Namun program Rietveld
versi Izumi (1994) memberikan parameter lain, dimana goodness of fit yang
dilambangkan dengan parameter S terbaik kurang dari 1,3 [30].
2.4.1. Prinsip Dasar
Prinsip dasar analisis Rietveld adalah mencocokkan (fitting) profil puncak
perhitungan terhadap profil puncak pengamatan. Pencocokan profil tersebut
dilakukan dengan menerapkan prosedur perhitungan kuadrat terkecil non linear
yang diberi syarat batas. Jadi analisis Rietveld tidak lain adalah problem optimasi
fungsi non linear dengan pembatas (constraints). Sehingga minimumkan fungsi
obyektif dapat dinyatakan sebagai berikut :
22.4.2. Persamaan Profile Pola Difraksi
Fungsi intensitas secara fisis yang dinyatakan :
2
( )k k( ) ( )k
I s F hkl ML (2.5)
dengan s, Fk(hkl), M, dan L berturut-turut adalah factor skala, factor struktur,
multiplisitas, dan faktor Lorentz-polarization. Persamaan tersebut menyatakan
bahwa banyaknya elektron akan didifraksikan hanya jika sudut hamburan ()
sama dengan sudut Bragg (k). Jadi fungsi intensitas tidak lain adalah persamaan
intensitas garis. Namun pada kenyataannya bahwa pengukuran intensitas difraksi
tersebut tidak terbentuk garis tetapi berupa puncak-puncak Bragg yang melebar.
Berdasarkan hasil pengembangan program analisis Rietveld ini bahwa
fungsi bentuk puncak merupakan fungsi pseudo-voigt yang telah dimodifikasi,
yakni kombinasi linear dari fungsi Gauss dan fungsi Lorentz dengan tinggi
puncak dan lebar penuh setengah tinggi puncak maksimum (FWHM) tidak sama.
Fungsi pseudo-Voigt yang telah dimodifikasi dituliskan sebagai berikut :
1
bentuk puncak asimetris. Faktor koreksi bentuk asimetris perlu diberikan karena
pada sudut hamburan yang sangat rendah dan sangat tinggi, puncak-puncak
difraksi menjadi tidak simetris akibat terbatasnya divergensi vertikal berkas. A =
parameter asimetris dan t = konstanta yang diberi nilai +1, 0 atau -1 tergantung
pada apakah selisih (22 )k berturut-turut positif, nol atau negatif.
Persamaan (2.8) menyatakan ketergantungan H Gk( ) pada k, U V dan W
disebut parameter FWHM. Bila korelasi antara parameter-parameter FWHM
sangat tinggi, maka Cs sebaiknya diberi nilai 0,6. Dalam persamaan (2.6)
terdapat lima buah parameter variabel yakni : U, V, W, dan . Fungsi bentuk
puncak dapat diubah-ubah tergantung pada berapa nilai parameter . Jika = 1
bentuk puncak memenuhi fungsi Gauss dan bentuk puncak memenuhi fungsi
Untuk pola difraksi neutron, profile puncak difraksinya tepat memenuhi fungsi
Gauss ( = 1).
Dengan demikian nilai intensitas profile pola difraksi pada posisi 2i
dapat dihitung dengan mengalikan persamaan (2.4) dengan persamaan (2.6),
setelah dikoreksi dengan fungsi latar belakang yib( )c dan fungsi orientasi
melambangkan penjumlahan jika terdapat puncak-puncak Bragg yang saling
tumpang tindih. Penjumlahan dilakukan terhadap semua refleksi yang dianggap
masih dapat menyumbangkan intensitasnya pada y ci( ) [28].
2.5. Magnetisasi Material
Ketika suatu material ditempatkan pada medan magnet, maka material
tersebut akan mengalami magnetisasi. Momen magnet persatuan volume yang
terbentuk dalam material disebut magnetisasi M. Pada suatu material dengan n
magnetic dipole atomic elementer persatuan volume dengan masing-masing m
momen magnet, maka saat momen-momen ini tersusun secara paralel akan
memiliki magnetisasi yang disebut magnetisasi saturasi M [31]. Parameter yang
penting adalah suseptibilitas magnetic , yang menyatakan kualitas dari suatu
(2.11)
dimana H adalah kuat medan magnet eksternal.
Medan magnet dapat di deskripsikan sebagai dua vektor, yaitu induksi
magnet B dan medan magnet H yang memiliki hubungan seperti pada persamaan
dalam kondisi vakum berikut ini
(2.12)
Dimana adalah permeabilitas pada ruang vakum (4 x 10-7 Hz/m)
Ketika sebuah material diletakkan pada medan magnet, maka material tersebut
akan mengalami magnetisasi. Magnetisasi ini dinyatakan dengan vektor M, yang
menyatakan besaran momen magnet persatuan volume. Induksi magnetik didalam
material dinyatakan dengan
(2.13)
Jika magnetisasi diinduksi oleh medan magnet H, maka magnetisasi yang ada
akan berbanding lurus dengan medan magnet, yaitu :
(2.14)
Dimana koefisien disebut suseptibilitas magnetic material. Jadi persamaan B
(2.15)
Pada bahan ferromagnetic, nilai dan tidak memiliki nilai yang konstan.
Permeabilitas dan suseptibilitas sangat dipengaruhi oleh medan magnet luar.
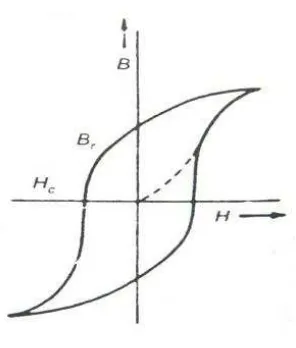
Kurva magnetisasi mempresentasikan densitas fluks induksi magnet B terhadap
kekuatan medan magnet luar untuk bahan ferromagnetic dapat dilihat pada
Gambar 2.17.
Gambar 2.17. Kurva Histerisis
Kurva magnetisasi untuk bahan yang belum termagnetisasi disebut dengan
initial curve magnetization. Kurva diawali dengan permeabilitas awal, dengan
bertambahnya medan magnet H, induksi magnetic B dengan cepat naik (disebut
dengan easy magnetization) dan selanjutnya menjadi menjadi lebih rendah hingga
tercapai nilai maksimum tertentu atau disebut dengan saturasi magnetik. Jika
medan magnet H diturunkan kembali, maka fluks induksi magnet B juga ikut
turun, tetapi lebih pelan dari medan magnet H nya. Dengan kata lain, menurunnya
kurva magnetisasi tidak mengikuti kurva ketika medan magnet dinaikkan pertama
ketika medan magnet telah mencapai nol. Untuk mengembalikan B kembali ke
nol, diperlukan medan magnet negative yang disebut dengan coercive force. Jika
medan magnet negative terus dinaikkan, maka material akan termagnetisasi
dengan arah polaritas kearah negative. Ketika medan magnet dinaikkan hingga
nol, maka juga akan didapati residu induksi medan magnet –B yang
membutuhkan medan magnet positif untuk membuat induksi medan magnet
menjadi nol kembali. Kurva seperti ini yang disebut dengan kurva loop histerisis
[31].
Berdasarkan koersivitasnya, bahan magnetik dapat dibedakan menjadi soft
magnetic dan hard magnetic. Untuk bahan yang memiliki koersivitas yang besar
(di atas 10 kA/m) disebut hard magnetic, sedangkan untuk bahan yang memiliki
koersivitas kecil (dibawah 1 kA/m) disebut soft magnetic [32].
2.6. Teori Double Exchange (DE)
Mekanisme Double Exchange (DE) merupakan tipe magnetik exchange
yang muncul diantara ion yang berdekatan dengan keadaan oksidasi yang berbeda
[33]. Teori ini pertama kali diajukan oleh Zener (1951) dan mempunyai implikasi
yang penting dari sifat magnetik dari suatu material. Energi sistem berada pada
nilai terendah jika spin inti yang bertetangga saling sejajar atau parallel. Demikian
juga dengan keadaan spin elektron, energi akan menjadi lebih rendah ketika spin
elektron parallel dengan spin inti ion Mn [34]. Teori ini sesuai dengan aturan
Hund untuk membuat energi sistem menjadi seminimal mungkin. Aturan pertama
Hund menyatakan bahwa energi akan minimum bila susunan spin-spin elektron
Teori Double Exchange (DE) merupakan salah satu dari sekian banyak
teori pertukaran yang ada dalam material. Mekanisme Double Exchange (DE)
pada material perovskite manganites terjadi perpindahan spin elektron yang
parallel pada tetangga terdekat dengan melakukan dua kali hopping secara
bersamaan dari Mn3+ ke Mn4+ melalui O2-. Pada sistem sampel LaSrMnO3, yang
berperan sebagai ion ialah atom Mn karena atom Mn telah menjadi ion Mn3+ dan
Mn4+ akibat adanya doping unsur Sr pada site La.
Zener (1951) telah mendapatkan persamaan yang menggambarkan
korelasi antara konduktivitas listrik terhadap sifat magnetiknya, yang dikaitkan
terhadap temperatur Curie (Tc) ferromagnetik pada sistem sampel La1-xAxMnO3
(A = Ca atau Sr), tetapi hanya berlaku untuk variasi doping
Berikut persamaan yang menyatakan hubungan tersebut
(2.16)
Dimana x adalah konsentrasi doping A (untuk ),
, h = konstanta Planck, e = muatan elektron, T adalah
temperature, dan Tc adalah temperature Curie. Berdasarkan persamaan (2.16)
dapat diketahui bahwa untuk sistem sampel La1-xAxMnO3 dimana
membuka hubungan linier antara magnetoresistansi terhadap magnetisasi dari
sampel, sehingga dapat disimpulkan konduktivitas listrik dan sifat magnetik
Gambar 2.18. Skema Teori Double Exchange (DE) [35]
Gambar 2.18 mengilustrasikan mekanisme Double Exchange (DE) yang
terjadi pada Mn3+-O-Mn4+. Elektron dari orbital eg pada ion Mn3+ melompat ke
orbital O2- dan secara bersamaan elektron pada orbital 2p O2- melompat ke orbital
eg ion Mn4+ yang kosong. Kedua elektron yang terlibat dalam pertukaran harus
memiliki spin yang sama (sesuai prinsip larangan pauli). Hal ini menyebabkan
terjadinya sifat feromagnetik dari elektron eg [35].
Teori lebih lanjut telah dilakukan oleh Anderson & Hasegawa yang
menyatakan bahwa sudut antara spin inti ion Mn tetangga terdekat turut
mempengaruhi pada proses Double Exchange (DE) [22]. Hal ini diperkuat oleh
de Gennes [23] membahas tentang batas besarnya coupling Hund (JH), spin
elektron pada eg terikat pada inti spin t2g yang mengubah parameter hopping (t),
yang dipenuhi oleh persamaan berikut :
Dimana θij adalah sudut antara spin inti pada t2g yang berdekatan dengan ion
manganese, dan tijhanya bergantung pada orientasi relatif pada dua spin. Energi
kinetik pada elektron eg adalah sebanding terhadap t. Dengan demikian, jika spin
tersusun secara feromagnetik (spin parallel) maka nilai t akan maksimum
sehingga resistivitas sampel bernilai minimum [22].
2.7. Teori Interaksi Superexchange
Superexchange merupakan coupling kuat antara interaksi spin antiferomagnetik terhadap tetangga terdekat kation melalui anion non magnetik
[36]. Gagasan bahwa pertukaran dapat dimediasi oleh sebuah atom non magnetik
telah diajukan pada tahun 1934, dan secara resmi dikembangkan oleh Anderson
pada tahun 1950.
Pada superexchange, interaksi magnetik antara ion yang berdekatan di
mediasi oleh ion non-magnetik dengan spin elektron yang berpasangan. Hal ini
merupakan interaksi yang lazim terjadi pada oksida manganiat terisolasi, dimana
ion penghubungnya adalah O2-. Pada kasus manganat, orbital yang telibat adalah
orbital eg yang kosong dari ion Mn dan orbital 2p pada O2- yang terisi. Jadi
elektron pada orbital 2p pada O2- terbagi diantara dua ion Mn yang berdekatan
yang mengisi orbital eg yang kosong. Ini merupakan transfer elektron secara tidak
langsung yang menjadi ciri khas dari mekanisme interaksi superexchange [36].
Gambar 2.19. Mekanisme interaksi superexchange (a) sesama ion Mn3+
dan (b) sesama ion Mn4+[36].
2.8. Ligand Field Theory (LFT)
Ligand Field Theory (LFT) merupakan salah satu teori yang digunakan untuk menjelaskan struktur elektronik kompleks [37]. Awalnya teori ini adalah
aplikasi dari Crystal Field Theory (CFT). Menurut LFT, interaksi antara metal
transisi dan ligand muncul karena adanya gaya tarik antara muatan positif pada
metal sebagai kation bebas dengan muatan negatif pada elektron yang tidak
berikatan pada ligand. Ketika ligand tertarik mendekati ion metal,
elektron-elektron pada ligand juga akan semakin mendekati elektron-elektron-elektron-elektron yang ada
pada orbital d, sehingga menghasilkan gaya tolak diantara kedua muatan yang
sama tersebut. Elektron-elektron pada orbital d yang mempunyai jarak paling
yang lain, sehingga akan terjadi perbedaan energi. Perbedaan energi ini disebut
d-orbital splitting energy.
Oktahedral kompleks merupakan bentuk paling umum yang membentuk
ikatan dengan metal-metal transisi. Lima orbital d dalam kation logam transisi
terdegenerasi dan memiliki energi yang sama, dimana probabilities density
elektron berbanding lurus dengan satuan level energi yang akan ditempati elektron
pada orbital d tersebut, dan adanya ligand akan menimbulkan pemisahan level
energi pada beberapa sub orbitalnya.
Gambar 2.20. Perubahan energi elektronik selama proses pembentukan
kompleks [37]
Gambar 2.20 di atas menyatakan bahwa medan listrik negatif sferik di
sekitar kation logam akan menghasilkan tingkat energi total yang lebih rendah
dari tingkat energi kation bebas yang disebabkan karena adanya interaksi
elektrostatis. Interaksi repulsif antara elektron dalam orbital logam dan medan
Sekarang ion tidak berada dalam medan negatif yang seragam, tetapi dalam
logam yang dihasilkan oleh enam ligand yang terkoordinasi secara octahedral
pada atom logam. Medan negatif dari ligand disebut medan ligand. Level energi
yang lebih rendah diberi simbol t2g (triply degenerate orbital) dan level energi
yang lebih tinggi diberi simbol eg (exited degenerate orbital).
Bila ligand ditempatkan di sumbu, reaksi repulsifnya lebih besar untuk
orbital eg dari pada untuk t2g , dan orbital eg di
stabilkan dan orbital t2g distabilkan dengan penstabilan yang sama. Perbedaan
energi antara orbital t2g dan eg sangat penting dan energi rata-rata orbital-obital ini
dianggap sebagai skala nol. Bila perbedaan energi dua orbital eg dan tiga orbital
t2gdianggap Δo, tingkat energi eg adalah dan energi total t2g adalah .
Gambar 2.21. Splitting octahedral pada level d5 [37]
Ion logam transisi memiliki 0 sampai 10 elektron d dan bila orbital d yang
terbelah diisi dari tingkat energi rendah, konfigurasi elektron yang
ditentukan sebagai tingkat energi rata-rata, energi konfigurasi elektron relatif
terhadap energi nol adalah
(2.18)
Nilai ini disebut energi penstabilan medan ligand (Ligand Field Stabilization
Energy LFSE). Konfigurasi elektron dengan nilai LFSE lebih kecil (dengan memperhitungkan tanda minusnya). LFSE merupakan parameter penting untuk
menjelaskan kompleks medan transisi.
Syarat lain selain tingkat energi yang diperlukan untuk menjelaskan
pengisian elektron dalam orbital t2g dan eg adalah energi pemasangan (pairing
energy Pe), yaitu energi yang diperlukan untuk memasangkan dua elektron dalam level energi yang sama namun dengan syarat spin berlawanan. Ada dua
kemungkinan yang muncul bila ada 4 jumlah elektron di orbital d. orbital yang
energinya lebih rendah t2g lebih disukai, tetapi pengisian orbital ini akan
memerlukan energi pemasangan (Pe). Energi totalnya menjadi
(2.19)
Bila elektron mengisi orbital yang energinya lebih tinggi eg, maka energi totalnya
menjadi
Dengan demikian, jelas bahwa untuk ion Mn yang terdapat pada material
perovskite manganites lebih menyukai konfigurasi medan lemah (weak field)
karena akan lebih stabil. Parameter pemisahan medan ligand ∆O ditentukan oleh
ligand dan logam, sedangkan energi pemasangan (Pe) hampir konstan dan
menunjukkan sedikit ketergantungan pada identitas logam [37].
Pada keadaan high-spin state ∆O > Pe, konfigurasi t2g4 lebih disukai dan
konfigurasinya disebut medan kuat (strong field) karena gaya tolakan yang terjadi
lebih besar dibandingkan pada kasus low-spin state. Sedangkan pada keadaan
low-spin state ∆O < Pe yaitu konfigurasi t2g3 eg1 lebih disukai dan disebut
konfigurasi medan lemah (weak field) atau konfigurasi elektron spin tinggi.
Gambar 2.22. Spin state pada weak field dan strong field ligand untuk
d4 sistem [37]
Dengan demikian, jelas bahwa untuk ion Mn yang terdapat pada material
perovskite manganites lebih menyukai konfigurasi medan lemah (weak field)
ligand dan logam, sedangkan energi pemasangan (Pe) hampir konstan dan
menunjukkan sedikit ketergantungan pada identitas logam [37].
Pada sifat elektrik dari lantanum manganat La1-xSrxMnO3 sangat terkait
dengan adanya ion manganese dengan valensi yang berbeda. Untuk x = 0 dan 1
ion manganese hanya memiliki satu jenis valensi dan biasanya bersifat
antiferromagnetic-insulator (AF-I). Untuk konsentrasi doping intermediate, ion manganese muncul dengan valensi yang berbeda, dan mengubah sifatnya menjadi
ferromagnetic- metallic (F-M). Orbital yang aktif secara elektronik adalah orbital
d manganese, dimana konfigurasi keadaan dasar dari trivalent dan quadrivalent
Mn adalah 3d4 dan 3d3.
Kelima orbital d masing-masing dapat mengakomodasi elektron dengan
satu spin up dan satu spin down akan terpecah (splitting) akibat adanya medan
kristal octahedral yang berasal dari 6 atom oksigen yang berada disekeliling ion
Mn. Pemisahan energi ini membagi orbital d menjadi tiga orbital pada energi
rendah t2g dan dua orbital pada level energi yang lebih tinggi eg
. Terjadinya pemisahan orbital ini berada pada orde 1,5 eV,
sehingga elektron mengisi pada keadaan orbital dengan spin maksimum sesuai
dengan aturan Hund. Oleh karena itu, konfigurasi elektronik pada Mn3+ adalah
, dan Mn4+ adalah
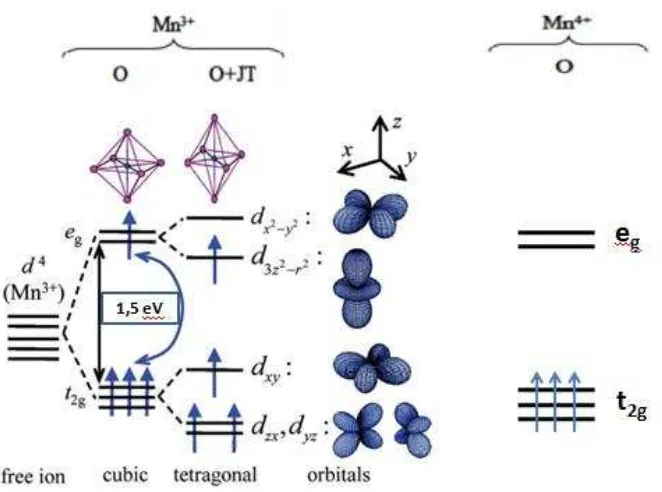
Gambar 2.23. Struktur elektronik dari Mn3+ dan Mn4+ sebelum dan
setelah adanya distorsi Jahn-Teller [15]
Gambar 2.23 mengilustrasikan splitting Jahn-Teller, energi dari Mn3+
menjadi lebih rendah sekitar 0,6 eV, sedangkan Mn4+ tidak mengalami apapun
akibat distorsi octahedron oksigen [37].
2.9. Mechanical Alloying
Proses mechanical alloying dengan mekanisme mechanical milling atau
pun dengan menggunakan high energy ball milling (HEBM) pada prinsipnya
adalah pengurangan ukuran butir atau partikel dan proses substitusi yang
diakibatkan oleh tumbukan yang terus menerus antar bola logam (ball mill) dan
sampel di dalam alat milling, seperti pada Gambar 2.24. Aplikasi metode
Gambar 2.25. Aplikasi metode mechanical alloying [38]
Parameter yang harus diperhatikan di dalam proses mechanical milling,
yang akan mempengaruhi kualitas produk akhir dari serbuk yang dicampur adalah
Gambar 2.26. Parameter-parameter di dalam proses mechanical milling [40]
Ball mill adalah alat yang baik untuk grinding banyak material menjadi
bubuk halus. Ball Mill digunakan untuk menggiling berbagai jenis tambang dan
bahan lainnya. Ada dua jenis proses grinding yaitu proses kering dan proses
basah. Setelah bahan mengalami proses grinding maka bahan padat akan berubah:
ukuran, bentuk partikelnya, dan lain-lainnya.
2.10. Mekanisme Absorpsi Gelombang Elektromagnet
Pada dasarnya suatu material jika dikenai gelombang electromagnet
maka akan mengalami interaksi antara material dengan gelombang electromagnet.
Misalkan suatu bahan memiliki ketebalan x dikenai gelombang electromagnet
dengan intensitas maka gelombang electromagnet akan mengalami attenuasi
(2.21)
dengan µ adalah konstanta. Dari persamaan (2.21) terlihat semakin tebal bahan
maka energi gelombang electromagnet semakin banyak yang diserap.
x
Gambar 2.27. Skema absorpsi gelombang electromagnet
Namun seiring dengan perkembangan zaman, material absorber yang
dibutuhkan adalah bahan yang tipis tapi memiliki kemampuan absorpsi yang
maksimal. Selain karena ketebalan suatu bahan, absorpsi gelombang elektomagnet
juga terjadi akibat interaksi gelombang dengan material yang menghasilkan efek
rugi-rugi energy yang umumnya didisipasikan dalam bentuk panas. Dalam hal ini
material absorber dibagi menjadi dua yakni material dielektrik dan magnetic. Pada
bahan dielektrik energy gelombang electromagnet diserap sehingga terjadi
polarisasi yang mengikuti arah medan listrik. Ketika gelombang electromagnet
berubah-ubah terhadap waktu maka arah polarisasi juga berubah-ubah sehingga
Gambar 2.28. Pengaruh medan listrik pada bahan dielektrik (telah diolah
kembali)
Hal yang analog juga terjadi pada bahan ferromagnetik. Ketika medan
magnet mengenai bahan ferromagnet maka energy gelombang electromagnet akan
digunakan untuk menyearahkan momen magnet. Untuk material absorber yang
baik dibutuhkan bahan magnetic yang memiliki koersifitas yang rendah.
Karakteristik dielektrik dan magnetik suatu bahan direpresentasikan oleh
permitifitas kompleks dan permeabilitas kompleks [41]
(2.22)
(2.23)
Dimana , tanda ‘ dan ‘’ bagian real dan imaginer. Impedansi yang tiba
pada material ditunjukkan
(2.24)
(2.25)
f adalah frekuensi dan c adalah kecepatan gelombang elektomagnet dalam ruang
vakum.
Reflektifitas radiasi electromagnet, Γ, dalam gelombang normal yang tiba
pada permukaan material ditunjukkan
(2.26)
Dan reflection loss- nya, R (dB), didefinisikan sebagai
= (2.27)
Dimana adalah bilangan kompleks dan adalah modulus dari . Sedangkan
adalah impedansi pada ruang hampa.
(2.28)
Nilai H/m dan F/m, sehingga diperoleh
. Kondisi impedansi yang cocok saat menunjukkan bahwa
terjadi penyerapan yang sempurna.
Secara umum criteria material absorber yang baik haruslah memiliki
permeabilitas dan permitifitas yang tinggi. Selain itu diperlukan resistifitas yang
2.11. Gelombang Mikro
Gelombang electromagnet ketika sampai pada material maka sebagian
gelombang tersebut akan direfleksikan dan sebagian lagi diabsorpsi. Karakter ini
bisa kita manfaatkan untuk mengurangi pantulan radiasi. Beberapa material
memantulkan banyak radiasi namun ada juga yang hampir tidak memantulkan
sama sekali. Sebagai contoh air, yang hampir tidak memantulkan radiasi sama
sekali oleh karena itu air termasuk absorber yang bagus. Material magnetic
misalnya ferit juga dapat menyerap gelombang electromagnet. Hal ini
dikarenakan adanya perubahan arah momen magnetic ketika dikenai medan
electromagnet [42].
Gelombang mikro adalah bagian dari gelombang electromagnet yang
memiliki daerah frekuensi sekitar 0,3-300 GHz atau panjang gelombang
1m-1mm. Gelombang mikro digunakan pertama kali untuk teknologi RADAR pada
awal perang dunia kedua. Saat ini gelombang mikro umum digunakan sebagai
oven microwave atau pun perangkat-perangkat komunikasi dan teknologi
informasi. Gelombang mikro dibagi dalam beberapa daerah jangkauan yang telah
Tabel 2.3. Pembagian daerah jangkauan gelombang mikro [43].
Simbol Daerah Frekuensi (GHz)
L 1.22 - 1.70
2.12. Scanning Electron Microscope (SEM)
Scanning Electron Microscope (SEM) adalah suatu alat yang digunakan untuk mengamati dan menganalisis karakteristik strukturmikro dari material baik
yang konduktif maupun non konduktif. Dibandingkan dengan MO, SEM
mempunyai daya pisah (resolusi) yang lebih tinggi yaitu 5nm, sehingga SEM
dapat menghasilkan perbesaran hingga 500.000 kali. Perbedaan daya pisah ini
pada SEM mempunyai panjang gelombang yang jauh lebih pendek dari pada sinar
foton pada MO.
Berkas elektron primer yang datang mengenai permukaan benda uji akan
berinteraksi dan menghasilkan berbagai macam sinyal secara serentak,
sinyal-sinyal tersebut diantaranya adalah elektron, sinar-X dan foton. Secara skematik
ditunjukan pada Gambar 2.29. Interaksi elektron primer dengan benda uji
tersebut mengakibatkan hamburan elektron (elastic scattering) dan hamburan
nonelastik (inelastic scattering).
Hamburan elastik ditimbulkan akibat adanya tumbukan berkas elektron
terjadinya hamburan elastik, arah komponen kecepatan elektron, v, akan berubah,
tetapi besarnya |v| relatif konstan, sehingga energi kinetik E = 1/2 mev2, dengan me adalah massa elektron, tidak berubah. Dalam hal ini energi sebesar <1eV
dipindahkan dari elektron [primer ke benda uji, perpindahan energi ini relatif kecil
bila dibandingkan dengan energi elektron primer sebesar 10 keV, karenanya
perpindahan enrgi tersebut dapat diabaikan. Hamburan elektron dari permukaan
benda uji setelah berkas elektron primer masuk ke dalam benda uji dan melintasi
jarak beberapa nm dengan distribusi energi 0≤E≤Eo, dimana Eo adalah energi
elektron p[rimer, disebut sebagai backscattered electron (elektron terhambur balik
– BSE).
Hamburan nonelastik (inelastic scattering) diakibatkan adanya tumbukan
elektron primer dengan elektron benda uji. Dalam proses tumbukan ini terjadi
perpindahan energi dari elektron primer ke atom dan elektron benda uji, sehingga
terjadi penurunan energi kinetik dari berkas elektron. Energi yang berada dalam
benda uji tersebut akan didistribusikan dan menghasilkan sinyal-sinyal yang
digunakan untuk analisis mikro. Sinyal-sinyal tersebut adalah secondary electron
(elektron sekunder – SE), Auger electron, continuum X-ray atau bremsstrahlung,
characteristic X-ray dan secondary fluorescence emission.
Secondary electron (elektron sekunder) adalah elektron yang dipancarkan dari benda uji akibat dari interaksi antara berkas elektron primer dengan
elektron-elektron pada pita penghantar benda uji. Interaksi ini hanya menghasilkan
perpindahan energi yang relatif rendah (3-5 eV) ke elektron pita penghantar.
Karena elektron sekunder ini mempunyai energi rendah, maka elektron-elektron
dengan kata lain elektron sekunder dari suatu area tertentu akan memberikan
informasi benda uji pada area tersebut dalam bentuk image (citra) .
Mekanisme terbentuknya citra pada SEM meliputi beberapa hal penting
diantaranya; sistem scanning untukpembentukan citra, mekanisme kontras sebagai
hasil interaksi elektron dan benda uji, karakteristik detektor dan pengaruhnya
terhadap kualitas citra, kualitas sinyal dan pengaruhnya terhadap kualitas citra dan
proses pen-sinyal-an untuk tampilan pada layar monitor. Ilustrasi proses
pembentukan citra pada SEM diilustrasikan pada Gambar 2.30.
BAB 3
METODE PENELITIAN
3.1. Waktu dan Tempat penelitian
Penelitian ini dilakukan dari bulan Juni sampai November 2013. Untuk
tahap preparasi/pembuatan sampel dilakukan di laboratorium Departemen Fisika
FMIPA UI. Sedangkan tahap karakterisasi sampel dilaksanakan di PLT UIN
Jakarta, Departemen Fisika FMIPA UI, dan LIPI Bandung.
3.2. Alat dan Bahan
Alat yang digunakan sebagai berikut:
a. Timbangan digital, digunakan untuk menimbang bahan dasar
b. Spatula, beaker glass
c. Dies (cetakan specimen/sampel) berbentuk silindris.
d. Planetary Ball Milling untuk mencampur serbuk bahan dasar
e. Bola baja (ball mill) digunakan untuk menumbuk campuran di dalam vial
Planetary Ball Milling.
f. Furnace (dapur pemanas) untuk men-sintering sampel
g. Universal testing machine atau pressing mechine digunakan untuk
membuat/mengkompaksi sampel (green body).
h. Cawan kramik digunakan untuk tempat sampel ketika disintering
i. Thermogravimetric Analyser (TGA) digunakan untuk mengetahui suhu
j. X Ray Diffraction (XRD) digunakan untuk melihat struktur kristal
sampel
k. Permagraph Magnet-Physic Dr. Steingroever GmbH digunakan untuk
pengujian sifat magnetik sampel
l. Vector Network Analyzer (VNA) digunakan untuk pengujian sifat
absorber sampel.
Bahan habis pakai yang digunakan sebagai berikut
a. Serbuk bahan dasar La2O3, MnCO3, BaCO3, dan NiO selengkapnya
dapat dilihat pada Tabel 3.1
b. Tissue, aquabidest
c. Serbuk karbon diunakan untuk membersihkan vial planetary ball mill
d. PVAc, digunakan sebagai perekat pada saat mencetak spesimen dengan
kompaksi.
e. Sabun cream diunakan untuk membersihkan vial dan ball mill
Tabel 3.1 Bahan Dasar Penelitian
3.3.1. Thermogravimetric analysis (TGA)
Dasar dari TGA adalah mengamati perubahan massa sampel terhadap kenaikan temperatur. Kurva kontinu perubahan massa terhadap temperatur diperoleh ketika sampel dipanaskan dengan kecepatan yang seragam. Kurva thermogravimetric (TG) umumnya merupakan plot antara penurunan massa pada sumbu y (ordinat) dan kenaikan temperatur pada sumbu x (absis).
Karakterisasi sampel dengan TGA dilakukan di Pusat Laboratorium
Terpadu UIN Jakarta. TGA (TA Instrument) tersebut menggunakan gas oksigen
Gambar 3.1. TGA
3.3.2. Difraksi Sinar-X (XRD)
Analisa kuantitas dan kualitas fasa-fasa yang ada dalam sampel
menggunakan XRD merek Shimadzu. Berkas sinar-x dihasilkan dari tube anode
Cu, dengan panjang gelombang 1,5405Å, mode: continous-scan, step size: 0,2 dan
timer per step 0,5 detik, dilakukan di Pusat Laboratorium Terpadu UIN Jakarta.
Pola difraksi sinar X yang diperoleh selanjutnya di olah dengan program
High Score Plus (HSP). Dari hasil pengolahan tersebut maka diperoleh informasi struktur kristal, parameter kisi, fasa yang terkandung pada sampel dan juga
Gambar 3.2. Alat Difraksi sinar-X (XRD) Shimadzu-7000
3.3.3. SEM
Karakterisasi dengan Scanning Electron Microscope (SEM) dilakukan
untuk mengetahui morfologi dari sampel. Karakterisasi SEM dilakukan di PTBIN
BATAN, Serpong. Dengan spesifikasi alat Jeol JED-2300.
3.3.4. Permagraf
Karakterisasi dengan permagraf dilakukan dengan tujuan mengetahui sifat
magnetik dari sampel, seperti saturasi dan koersifitas magnet. Karakterisasi
permagraf dilakukan di laboratorium UI Depok.
Gambar 3.2. Permagraf
3.3.5. VNA (Vector Network Analyser)
Karakterisasi sampel dengan VNA betujuan untuk mengukur nilai absorbsi
material dan juga nilai reflection loss. Pengukuran ini dilakukan di LIPI Bandung.
3.4. Diagram Alir Penelitian
Preparasi Material
Bahan-bahan dasar
Pencampuran (Mixing)
Proses mechanical milling,
Kalsinasi
Kompaksi
Sintering
Karakterisasi
Pengolahan data dan Analisis
Material
3.5. Jadwal Penelitian
Penelitian dilakukan selama enam bulan dari bulan Juni – November 2013
Uraian Penelitian Juni Juli Ags Sept Okt Nov
Studi literature
Penyediaan bahan-bahan dan
persiapan instrument
Proses sintesis material absorber
Karakterisasi material
BAB 4
HASIL DAN PEMBAHASAN
4.1. Karakterisasi TGA(Thermogravimetric Analysis)
Sampel La0.67Ba0.33Mn1-xNixO3 disintesa dari beberapa bahan dasar yaitu
La2O3, BaCO3, MnCO3, dan NiO yang memiliki tingkat kemurnian rata-rata
diatas 99%. Seluruh bahan dasar tersebut dimilling dengan Planetary Ball Mill
selama 25 jam. Hasil milling tersebut selanjutnya dikarakterisasi dengan alat
TGA (Thermogravimetric Analysis) yang memliki kemampuan mengkarakterisasi
sampel dari 0oC sampai 1000oC. Hasil TGA campuran bahan dasar yang selesai
dimilling dapat dilihat dalam Gambar 4.1
Dari kurva TGA tersebut tampak adanya penurunan berat sampel ketika
terjadi kenaikan suhu sekitar 50oC – 800oC. Penurunan berat sampel
dimungkinkan karena ada ion karbon yang berasal dari bahan dasar BaCO3 mau
pun MnCO3 terbuang ketika terjadi pemanasan. Atas dasar inilah tahapan
selanjutnya dilakukan kalsinasi pada suhu 800oC selama 10 jam untuk
Gambar 4.1. Kurva TGA campuran bahan dasar setelah milling
4.2. Karakterisasi SEM
Untuk mengetahui morfologi dari sampel, maka sampel La0,67Ba0,33Mn
1-xNixO3 yang telah disintesa dikarakterisasi dengan SEM. Hasil SEM dapat di lihat
Gambar 4.2. SEM sampel La0,67Ba0,33MnO3
Gambar 4.4. SEM sampel La0,67Ba0,33Mn0,96Ni0,04O3
4.3. Difraksi Sinar X
Untuk mengetahui struktur kristal, parameter kisi, dan fasa yang
terkandung dari sampel, maka sampel yang telah disintesa dikarakterisasi dengan
alat difraksi sinar X (XRD). Berkas sinar-X dihasilkan dari tube anode Cu,
dengan panjang gelombang 1,5405Å, mode continous-scan, step size 0,2 dan time
per step 0,5 detik. Data diambil dari sudut dua theta 10 derajat sampai 80 derajat.
Karakterisasi ini dilakukan di Pusat Laboratorium Terpadu UIN Jakarta.
4.3.1. XRD Sampel La0,67Ba0,33MnO3
Pola difraksi sinar X untuk sampel La0,67Ba0,33MnO3 dapat dilihat pada
Gambar 4.6. Untuk mengetahui lebih lanjut struktur kristal atau pun analisa
kuantitatif lainnya dari sampel yang telah disintesa, maka pola difraksi sinar X
yang telah diperoleh di olah dengan menggunakan software High score Plus
Gambar 4.7. Refinement sampel La0,67Ba0,33MnO3
Dari hasil pengolahan data dengan program High Score Plus diperoleh
informasi bahwa fasa yang terkandung dalam sampel adalah 100%
La0,67Ba0,33MnO3. Parameter kisi ; ; dan
dengan sudut . Struktur kristal monoklinik , ukuran kristal 74,35 nm,
4.3.2. XRD Sampel La0,67Ba0,33Mn0,98Ni0,02O3
Pola difraksi sinar X untuk sampel La0,67Ba0,33Mn0,98Ni0,02O3 dapat
dilihat pada Gambar 4.8. Untuk mengetahui lebih lanjut struktur kristal atau pun
analisa kuantitatif lainnya dari sampel yang telah disintesa, maka pola difraksi
sinar X yang telah diperoleh di olah dengan menggunakan software High score
Plus (HSP). Hasil refinement sampel La0.67Ba0.33Mn0,98Ni0,02O3 dapat dilihat pada
Gambar 4.9. Refinement sampel La0,67Ba0,33Mn0,98Ni0,02O3
Pola difraksi sinar X sampel La0,67Ba0,33Mn0,98Ni0,02O3 (Gambar 4.8)
menunjukkan adanya perbedaan dengan pola difraksi sinar X sampel
La0,67Ba0,33MnO3 (Gambar 4.6) , ditandai dengan adanya penambahan beberapa
puncak di sudut dua theta. Dari hasil pengolahan data dengan program High
Score Plus diperoleh informasi bahwa fasa yang terkandung dalam sampel ada
dua yakni fasa La0,67Ba0,33Mn0,98Ni0,02O3 dan fasa BaMnO3. Fraksi berat
masing-masing fasa dalam sampel adalah 93,7% untuk fasa La0,67Ba0,33Mn0,98Ni0,02O3 dan
Fasa La0,67Ba0,33Mn0,98Ni0,02O3 memiliki parameter kisi ;
; dan dengan sudut . Struktur kristal
monoklinik , ukuran kristal 26,25 nm, densitas 6,72 g/cm3, volume 238,40 Å3.
Sedangkan untuk fasa keduanya, fasa BaMnO3 memiliki parameter kisi
; ; dan dengan sudut dan
Struktur kristal heksagonal , ukuran kristal 2791,3 nm, densitas 5,73
g/cm3, volume 626,53 Å3.
4.3.3. XRD Sampel La0,67Ba0,33Mn0,96Ni0,04O3
Pola difraksi sinar X untuk sampel La0,67Ba0,33Mn0,96Ni0,04O3 dapat
dilihat pada Gambar 4.10. Untuk mengetahui lebih lanjut struktur kristal atau pun
analisa kuantitatif lainnya dari sampel yang telah disintesa, maka pola difraksi
sinar X yang telah diperoleh di olah dengan menggunakan software High score
Plus (HSP). Hasil refinement sampel La0,67Ba0,33Mn0,96Ni0,04O3 dapat dilihat pada
Gambar 4.11.
Sama halnya dengan sampel La0,67Ba0,33Mn0,98Ni0,02O3, pola difraksi sinar
X sampel La0,67Ba0,33Mn0,96Ni0,04O3 (Gambar 4.10) menunjukkan adanya
perbedaan dengan pola difraksi sinar X sampel La0,67Ba0,33MnO3 (Gambar 4.6) ,
ditandai dengan adanya penambahan beberapa puncak di sudut dua theta. Dari
hasil pengolahan data dengan program High Score Plus diperoleh informasi
bahwa fasa yang terkandung dalam sampel ada dua yakni fasa
dalam sampel adalah 92,6% untuk fasa La0,67Ba0,33Mn0,96Ni0,04O3 dan 7,4% untuk
fasa BaMnO3.
Fasa La0,67Ba0,33Mn0,96Ni0,04O3 memiliki parameter kisi ;
; dan dengan sudut . Struktur kristal
monoklinik , ukuran kristal 40,72 nm, densitas 6,74 g/cm3, volume 238,06 Å3.
Sedangkan untuk fasa keduanya, fasa BaMnO3 memiliki parameter kisi
; ; dan dengan sudut dan


![Gambar 2.24. Prinsip dan tahapan dari mechanical alloying [39]](https://thumb-ap.123doks.com/thumbv2/123dok/728110.455969/54.595.139.491.101.599/gambar-prinsip-dan-tahapan-dari-mechanical-alloying.webp)
![Gambar 2.25. Aplikasi metode mechanical alloying [38]](https://thumb-ap.123doks.com/thumbv2/123dok/728110.455969/55.595.165.460.85.334/gambar-aplikasi-metode-mechanical-alloying.webp)
![Gambar 2.26. Parameter-parameter di dalam proses mechanical milling [40]](https://thumb-ap.123doks.com/thumbv2/123dok/728110.455969/56.595.205.461.88.320/gambar-parameter-parameter-di-dalam-proses-mechanical-milling.webp)