PROSES PEMBUATAN BIODIESEL MINYAK JARAK PAGAR (Jatropha curcas L.) DENGAN TRANSESTERIFIKASI
SATU DAN DUA TAHAP
Oleh
ARIZA BUDI TUNJUNG SARI F34103041
2007
DEPARTEMEN TEKNOLOGI INDUSTRI PERTANIAN
FAKULTAS TEKNOLOGI PERTANIAN
INSTITUT PERTANIAN BOGOR
PROSES PEMBUATAN BIODIESEL MINYAK JARAK PAGAR (Jatropha curcas L.) DENGAN TRANSESTERIFIKASI
SATU DAN DUA TAHAP
SKRIPSI
Sebagai salah satu syarat untuk memperolah gelar
SARJANA TEKNOLOGI PERTANIAN
Pada Departemen Teknologi Industri Pertanian
Fakultas Teknologi Pertanian
Institut Pertanian Bogor
Oleh
ARIZA BUDI TUNJUNG SARI F34103041
2007
FAKULTAS TEKNOLOGI PERTANIAN
INSTITUT PERTANIAN BOGOR
FAKULTAS TEKNOLOGI PERTANIAN INSTITUT PERTANIAN BOGOR
PROSES PEMBUATAN BIODIESEL MINYAK JARAK PAGAR (Jatropha curcas L.) DENGAN TRANSESTERIFIKASI
SATU DAN DUA TAHAP
SKRIPSI
Sebagai salah satu syarat untuk memperolah gelar
SARJANA TEKNOLOGI PERTANIAN
Pada Departemen Teknologi Industri Pertanian
Fakultas Teknologi Pertanian
Institut Pertanian Bogor
Oleh
ARIZA BUDI TUNJUNG SARI F34103041
Dilahirkan pada tanggal 14 Januari 1985 Di Surabaya
Tanggal lulus :
Menyetujui, Bogor, 2007
Ariza Budi Tunjung Sari. F34103041. Proses Pembuatan Biodiesel Minyak Jarak Pagar (Jatropha curcas L.) dengan Transesterifikasi Satu dan Dua Tahap. Di bawah bimbingan : M. Zein Nasution dan Tatang Hidayat.2007
RINGKASAN
Kebutuhan akan bahan bakar alternatif semakin meningkat. Salah satu pengganti bahan bakar konvensional dari minyak bumi adalah minyak nabati. Minyak jarak pagar merupakan salah satu minyak nabati yang potensial. Tanaman Jarak pagar (Jatropha curcas L.) sudah banyak diteliti dan dikembangkan, terutama berkaitan dengan sifatnya yang non-edible serta kemampuannya untuk tumbuh dan berkembang di lahan kering.
Minyak nabati memiliki nilai kalor yang hampir sama dengan bahan bakar konvensional, namun viskositasnya jauh lebih tinggi dari minyak diesel. Hal ini menghambat proses injeksi dan mengakibatkan pembakaran yang tidak sempurna serta meninggalkan residu karbon pada injektor.
Upaya untuk mengurangi viskositas minyak antara lain dengan pengenceran minyak dengan pelarut, emulsifikasi, pirolisis, dan transesterifikasi. Transesterifikasi adalah cara yang paling banyak dilakukan karena tidak membutuhkan energi dan suhu yang tinggi. Reaksi ini akan menghasilkan metil atau etil ester, tergantung dengan jenis alkohol yang direaksikan. Metil atau etil ester ini memiliki viskositas rendah dan nilai kalor yang mendekati bahan bakar konvensional.
Proses transesterifikasi dengan katalis basa dapat dilakukan satu tahap atau dua tahap, pada berbagai rentang suhu dan beragam konsentrasi metanol. Metil ester dengan viskositas kinematik terkecil dihasilkan dari reaksi pada suhu rendah 30 °C dengan nisbah mol metanol lima kali mol minyak. Pada kondisi tersebut, viskositas dan densitas metil ester hasil proses dua tahap lebih kecil dari proses satu tahap namun memiliki bilangan asam yang lebih besar bahkan melebihi batas yang ditetapkan standar ASTM D664.
Oleh karena itu disimpulkan perlakuan terbaik adalah proses transesterifikasi satu tahap pada suhu 30 °C dengan molar rasio metanol: minyak sebesar 5:1. Metil ester yang dihasilkan memiliki viskositas kinematik 3.89 cSt, densitas 0.88g/cm3 dan bilangan asam 0.48 mg KOH/g sampel.
KATA PENGANTAR
Puji syukur kehadirat Allah SWT karena atas rahmat dan karuniaNya,
penulis dapat menyelesaikan skripsi ini dengan baik. Skripsi ini disusun
berdasarkan hasil penelitian di Laboratorium Penelitian Balai Besar Penelitian dan
Pengembangan Pasca Panen Pertanian berlokasi di Bogor, Jawa Barat. Selain itu,
penulis pun mengumpulkan data-data dari berbagai publikasi ilmiah.
Dalam menyelesaikan penyusunan skripsi ini penulis tidak akan berhasil
tanpa adanya bantuan dan dukungan dari berbagai pihak. Oleh karena itu, pada
kesempatan ini penulis ingin mengucapkan terima kasih kepada:
1. Ir. M Zein Nasution, MAppSc., selaku dosen pembimbing yang telah banyak
memberikan arahan dalam penyelesaian skripsi ini.
2. Ir. Tatang Hidayat, MSi., selaku dosen pembimbing yang telah membimbing
penulis dalam melakukan penelitian dan penyusunan skripsi.
3. Orang Tua, keluarga dan rekan-rekan yang selalu memberikan dukungan dan
perhatian kepada penulis..
Penulis menyadari bahwa skripsi ini masih jauh dari sempurna sehingga kritik
dan saran dari seluruh pihak sangat penulis harapkan. Semoga skripsi ini dapat
memberikan informasi yang bermanfaat.
Bogor, September 2007
DAFTAR ISI
Halaman
KATA PENGANTAR ... iii
DAFTAR ISI ... iv
DAFTAR TABEL ... vi
DAFTAR GAMBAR ... vii
DAFTAR LAMPIRAN... viii
I. PENDAHULUAN... 1
II. TINJAUAN PUSTAKA ... 3
A. JARAK PAGAR ... 3
B. BIODIESEL ... 4
C. TRANSESTERIFIKASI... 7
III. METODOLOGI ... 10
A. BAHAN DAN ALAT ... 10
B. METODE ... 10
IV. HASIL DAN PEMBAHASAN ... 17
A. BAHAN BAKU ... 17
B. METIL ESTER ... 18
1.Karakteristik Fisik Metil Ester... 18
2.Viskositas Kinematik ... 18
3.Densitas... 21
4.Bilangan Asam... 22
5.Perbandingan Proses Transesterifikasi Satu Tahap Dan Dua Tahap... 24
7. KESIMPULAN DAN SARAN ... 32
A. KESIMPULAN ... 29
B. SARAN ... 29
DAFTAR PUSTAKA ... 31
DAFTAR GAMBAR
Halaman
Gambar 1. Tanaman Jarak Pagar... 3
Gambar 2. Buah jarak pagar dan biji jarak pagar... 4
Gambar 3. Reaksi pembentukan metil ester... 5
Gambar 4. Reaksi pembentukan etil ester... 5
Gambar 5. Minyak jarak pagar sebelum dan sesudah dinetralisasi... 18
Gambar 6. Reaksi transesterifikasi menghasilkan metil ester... 20
Gambar 7. Reaksi oksidasi membentuk peroksida dan asam lemak rantai pendek... 22
Gambar 8. Prinsip reaksi reversibel... 25
Gambar 8. Prinsip reaksi transesterifikasi... 26
DAFTAR TABEL
Halaman
Tabel 1. Kandungan asam lemak pada minyak jarak pagar... 4
Tabel 2: Sifat fisikokimia minyak jarak pagar... 4
Tabel 3. Ciri biodiesel secara umum... 6
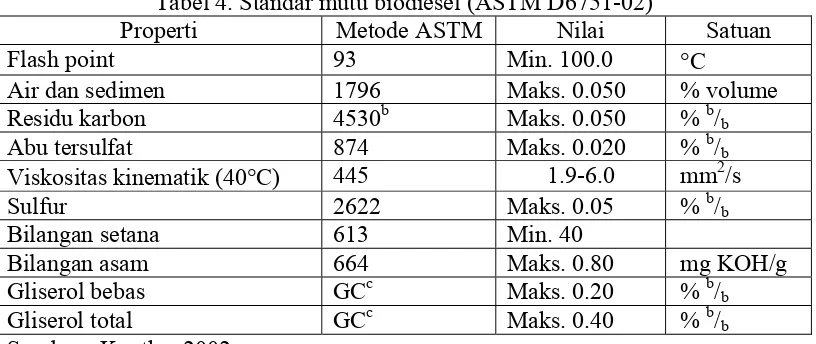
Tabel 4. Standar mutu biodiesel (ASTM D6751-02)... 6
Tabel 5. Karakteristik minyak jarak pagar sebelum dan sesudah dinetralisasi... 17
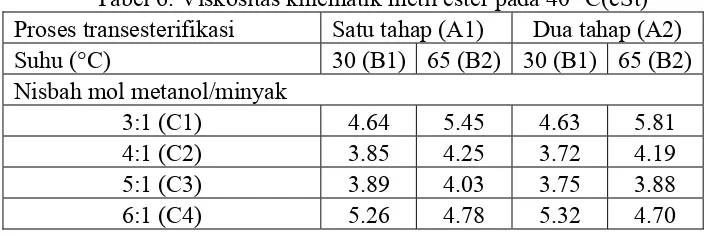
Tabel 6. Viskositas kinematik metil ester pada 40 °C... 19
Tabel 7. Densitas metil ester pada suhu 25 °C... 21
DAFTAR LAMPIRAN
Halaman
Lampiran 1. Diagram alir pembuatan larutan metanolik-KOH
dan proses transesterifikasi... 33
Lampiran 2. Hasil analisis sidik ragam viskositas kinematik metil ester... 35
Lampiran 3. Hasil analisis sidik ragam bilangan asam metil ester... 36
Lampiran 4. Hasil analisis sidik ragam densitas metil ester... 38
Lampiran 5. Analisa biaya biodiesel... 39
PROSES PEMBUATAN BIODIESEL MINYAK JARAK PAGAR (Jatropha curcas L.) DENGAN TRANSESTERIFIKASI
SATU DAN DUA TAHAP
Oleh
ARIZA BUDI TUNJUNG SARI F34103041
2007
DEPARTEMEN TEKNOLOGI INDUSTRI PERTANIAN
FAKULTAS TEKNOLOGI PERTANIAN
INSTITUT PERTANIAN BOGOR
PROSES PEMBUATAN BIODIESEL MINYAK JARAK PAGAR (Jatropha curcas L.) DENGAN TRANSESTERIFIKASI
SATU DAN DUA TAHAP
SKRIPSI
Sebagai salah satu syarat untuk memperolah gelar
SARJANA TEKNOLOGI PERTANIAN
Pada Departemen Teknologi Industri Pertanian
Fakultas Teknologi Pertanian
Institut Pertanian Bogor
Oleh
ARIZA BUDI TUNJUNG SARI F34103041
2007
FAKULTAS TEKNOLOGI PERTANIAN
INSTITUT PERTANIAN BOGOR
FAKULTAS TEKNOLOGI PERTANIAN INSTITUT PERTANIAN BOGOR
PROSES PEMBUATAN BIODIESEL MINYAK JARAK PAGAR (Jatropha curcas L.) DENGAN TRANSESTERIFIKASI
SATU DAN DUA TAHAP
SKRIPSI
Sebagai salah satu syarat untuk memperolah gelar
SARJANA TEKNOLOGI PERTANIAN
Pada Departemen Teknologi Industri Pertanian
Fakultas Teknologi Pertanian
Institut Pertanian Bogor
Oleh
ARIZA BUDI TUNJUNG SARI F34103041
Dilahirkan pada tanggal 14 Januari 1985 Di Surabaya
Tanggal lulus :
Menyetujui, Bogor, 2007
Ariza Budi Tunjung Sari. F34103041. Proses Pembuatan Biodiesel Minyak Jarak Pagar (Jatropha curcas L.) dengan Transesterifikasi Satu dan Dua Tahap. Di bawah bimbingan : M. Zein Nasution dan Tatang Hidayat.2007
RINGKASAN
Kebutuhan akan bahan bakar alternatif semakin meningkat. Salah satu pengganti bahan bakar konvensional dari minyak bumi adalah minyak nabati. Minyak jarak pagar merupakan salah satu minyak nabati yang potensial. Tanaman Jarak pagar (Jatropha curcas L.) sudah banyak diteliti dan dikembangkan, terutama berkaitan dengan sifatnya yang non-edible serta kemampuannya untuk tumbuh dan berkembang di lahan kering.
Minyak nabati memiliki nilai kalor yang hampir sama dengan bahan bakar konvensional, namun viskositasnya jauh lebih tinggi dari minyak diesel. Hal ini menghambat proses injeksi dan mengakibatkan pembakaran yang tidak sempurna serta meninggalkan residu karbon pada injektor.
Upaya untuk mengurangi viskositas minyak antara lain dengan pengenceran minyak dengan pelarut, emulsifikasi, pirolisis, dan transesterifikasi. Transesterifikasi adalah cara yang paling banyak dilakukan karena tidak membutuhkan energi dan suhu yang tinggi. Reaksi ini akan menghasilkan metil atau etil ester, tergantung dengan jenis alkohol yang direaksikan. Metil atau etil ester ini memiliki viskositas rendah dan nilai kalor yang mendekati bahan bakar konvensional.
Proses transesterifikasi dengan katalis basa dapat dilakukan satu tahap atau dua tahap, pada berbagai rentang suhu dan beragam konsentrasi metanol. Metil ester dengan viskositas kinematik terkecil dihasilkan dari reaksi pada suhu rendah 30 °C dengan nisbah mol metanol lima kali mol minyak. Pada kondisi tersebut, viskositas dan densitas metil ester hasil proses dua tahap lebih kecil dari proses satu tahap namun memiliki bilangan asam yang lebih besar bahkan melebihi batas yang ditetapkan standar ASTM D664.
Oleh karena itu disimpulkan perlakuan terbaik adalah proses transesterifikasi satu tahap pada suhu 30 °C dengan molar rasio metanol: minyak sebesar 5:1. Metil ester yang dihasilkan memiliki viskositas kinematik 3.89 cSt, densitas 0.88g/cm3 dan bilangan asam 0.48 mg KOH/g sampel.
KATA PENGANTAR
Puji syukur kehadirat Allah SWT karena atas rahmat dan karuniaNya,
penulis dapat menyelesaikan skripsi ini dengan baik. Skripsi ini disusun
berdasarkan hasil penelitian di Laboratorium Penelitian Balai Besar Penelitian dan
Pengembangan Pasca Panen Pertanian berlokasi di Bogor, Jawa Barat. Selain itu,
penulis pun mengumpulkan data-data dari berbagai publikasi ilmiah.
Dalam menyelesaikan penyusunan skripsi ini penulis tidak akan berhasil
tanpa adanya bantuan dan dukungan dari berbagai pihak. Oleh karena itu, pada
kesempatan ini penulis ingin mengucapkan terima kasih kepada:
1. Ir. M Zein Nasution, MAppSc., selaku dosen pembimbing yang telah banyak
memberikan arahan dalam penyelesaian skripsi ini.
2. Ir. Tatang Hidayat, MSi., selaku dosen pembimbing yang telah membimbing
penulis dalam melakukan penelitian dan penyusunan skripsi.
3. Orang Tua, keluarga dan rekan-rekan yang selalu memberikan dukungan dan
perhatian kepada penulis..
Penulis menyadari bahwa skripsi ini masih jauh dari sempurna sehingga kritik
dan saran dari seluruh pihak sangat penulis harapkan. Semoga skripsi ini dapat
memberikan informasi yang bermanfaat.
Bogor, September 2007
DAFTAR ISI
Halaman
KATA PENGANTAR ... iii
DAFTAR ISI ... iv
DAFTAR TABEL ... vi
DAFTAR GAMBAR ... vii
DAFTAR LAMPIRAN... viii
I. PENDAHULUAN... 1
II. TINJAUAN PUSTAKA ... 3
A. JARAK PAGAR ... 3
B. BIODIESEL ... 4
C. TRANSESTERIFIKASI... 7
III. METODOLOGI ... 10
A. BAHAN DAN ALAT ... 10
B. METODE ... 10
IV. HASIL DAN PEMBAHASAN ... 17
A. BAHAN BAKU ... 17
B. METIL ESTER ... 18
1.Karakteristik Fisik Metil Ester... 18
2.Viskositas Kinematik ... 18
3.Densitas... 21
4.Bilangan Asam... 22
5.Perbandingan Proses Transesterifikasi Satu Tahap Dan Dua Tahap... 24
7. KESIMPULAN DAN SARAN ... 32
A. KESIMPULAN ... 29
B. SARAN ... 29
DAFTAR PUSTAKA ... 31
DAFTAR GAMBAR
Halaman
Gambar 1. Tanaman Jarak Pagar... 3
Gambar 2. Buah jarak pagar dan biji jarak pagar... 4
Gambar 3. Reaksi pembentukan metil ester... 5
Gambar 4. Reaksi pembentukan etil ester... 5
Gambar 5. Minyak jarak pagar sebelum dan sesudah dinetralisasi... 18
Gambar 6. Reaksi transesterifikasi menghasilkan metil ester... 20
Gambar 7. Reaksi oksidasi membentuk peroksida dan asam lemak rantai pendek... 22
Gambar 8. Prinsip reaksi reversibel... 25
Gambar 8. Prinsip reaksi transesterifikasi... 26
DAFTAR TABEL
Halaman
Tabel 1. Kandungan asam lemak pada minyak jarak pagar... 4
Tabel 2: Sifat fisikokimia minyak jarak pagar... 4
Tabel 3. Ciri biodiesel secara umum... 6
Tabel 4. Standar mutu biodiesel (ASTM D6751-02)... 6
Tabel 5. Karakteristik minyak jarak pagar sebelum dan sesudah dinetralisasi... 17
Tabel 6. Viskositas kinematik metil ester pada 40 °C... 19
Tabel 7. Densitas metil ester pada suhu 25 °C... 21
DAFTAR LAMPIRAN
Halaman
Lampiran 1. Diagram alir pembuatan larutan metanolik-KOH
dan proses transesterifikasi... 33
Lampiran 2. Hasil analisis sidik ragam viskositas kinematik metil ester... 35
Lampiran 3. Hasil analisis sidik ragam bilangan asam metil ester... 36
Lampiran 4. Hasil analisis sidik ragam densitas metil ester... 38
Lampiran 5. Analisa biaya biodiesel... 39
I. PENDAHULUAN
A. LATAR BELAKANG
Permintaan terhadap bahan bakar semakin meningkat dan harga bahan
bakar minyak semakin tinggi. Keadaan tersebut menimbulkan kebutuhan akan
adanya bahan bakar alternatif. Bahan bakar alternatif yang dikehendaki adalah
yang bahan bakunya tersedia secara lokal, mudah didapat dan terpulihkan
(renewable).
Salah satu pengganti bahan bakar konvensional dari minyak bumi
adalah minyak nabati. Minyak nabati tersedia dalam jenis dan jumlah yang
besar di Indonesia, misalnya minyak kelapa, minyak kelapa sawit, kemiri,
kacang tanah, jarak dan jarak pagar. Minyak Jarak pagar merupakan salah
satu minyak nabati yang potensial. Tanaman Jarak pagar (Jatropha curcas L.)
sudah banyak diteliti dan dikembangkan, terutama berkaitan dengan
kemampuannya untuk tumbuh dan berkembang di lahan kering. Selain itu
minyak jarak pagar bersifat non-edible sehingga penggunaanya sebagai bahan
bakar tidak bersaing dengan minyak pangan.
Minyak nabati memiliki nilai kalor yang hampir sama dengan bahan
bakar konvensional, namun penggunaan secara langsung sebagai bahan bakar
masih menemui kendala. Minyak nabati memiliki viskositas jauh lebih besar
dari minyak diesel, hal ini menghambat proses injeksi dan mengakibatkan
pembakaran yang tidak sempurna. Penggunaan minyak nabati sebagai bahan
bakar juga meninggalkan residu karbon pada injektor.
Upaya untuk mengurangi viskositas minyak nabati antara lain dengan
pengenceran minyak dengan pelarut, emulsifikasi, pirolisis, dan
transesterifikasi. Transesterifikasi adalah cara yang paling banyak dilakukan
karena tidak membutuhkan energi dan suhu yang tinggi. Reaksi ini akan
menghasilkan metil atau etil ester, tergantung dengan jenis alkohol yang
direaksikan. Jika direaksikan dengan metanol, akan terbentuk metil ester,
sedangkan jika direaksikan dengan etanol akan terbentuk etil ester. Metil atau
etil ester ini memiliki viskositas rendah dan nilai kalor yang mendekati bahan
Proses transesterifikasi yang dilakukan dewasa ini melalui satu tahap
atau dua tahap. Pada proses satu tahap minyak direaksikan dengan metanol
dan KOH sekaligus, sedangkan pada proses dua tahap minyak direaksikan
dengan sebagian larutan metanolik-KOH, kemudian metil ester yang terbentuk
dipisahkan dari gliserol dan direaksikan kembali dengan sisa larutan
metanolik-KOH. Metanol yang digunakan dalam proses transesterifikasi
biasanya dalam jumlah yang berlebih untuk memicu berlangsungnya reaksi
transesterifikasi. Reaksi transesterifikasi dua tahap diharapkan mampu
mempengaruhi kesetimbangan reaksi kimia dan memacu reaksi yang lebih
sempurna.
Parameter keberhasilan reaksi adalah viskositas kinematik dan densitas
metil ester. Semakin rendah nilai keduanya, diduga tingkat konversi esternya
semakin tinggi.Untuk itu diperlukan penelitian yang mengkaji pengaruh
aplikasi transesterifikasi satu tahap dan dua tahap terhadap mutu biodiesel
yang dihasilkan.
B. TUJUAN
1. Mendapatkan data perbandingan antara proses transesterifikasi satu tahap
dan dua tahap pada pembuatan biodiesel dari minyak jarak pagar
(Jatropha curcas L.).
2. Mendapatkan molar rasio metanol/minyak dan suhu reaksi yang dapat
II. TINJAUAN PUSTAKA
A. JARAK PAGAR
Tanaman jarak pagar termasuk famili Euphorbiaceae, satu famili
dengan karet dan ubikayu. Pohonnya berupa perdu dengan tinggi tanaman
antara 1–7 m, bercabang tidak teratur (Gambar 1). Batangnya berkayu,
silindris, bila terluka mengeluarkan getah. Daunnya berupa daun tunggal,
berlekuk, bersudut 3 atau 5, tulang daun menjari dengan 5 – 7 tulang utama,
warna daun hijau (permukaan bagian bawah lebih pucat dibanding bagian
atas). Panjang tangkai daun antara 4 – 15 cm (www.ristek.go.id, 2005).
Gambar 1. Tanaman Jarak Pagar
Bunga tanaman jarak berwarna kuning kehijauan, berupa bunga
majemuk berbentuk malai, berumah satu. Bunga jantan dan bunga betina
tersusun dalam rangkaian berbentuk cawan, muncul di ujung batang atau
ketiak daun. Buah berupa buah kotak berbentuk bulat telur, diameter 2 – 4
cm, berwarna hijau ketika masih muda dan kuning jika masak. Buah jarak
terbagi 3 ruang yang masing – masing ruang diisi 3 biji. Biji berbentuk bulat
lonjong, warna coklat kehitaman. Biji inilah yang banyak mengandung
minyak dengan rendemen sekitar 30 – 40 % (www.ristek.go.id, 2005). Buah
dan biji jarak pagar dapat dilihat pada Gambar 2.
Minyak jarak pagar diperoleh dari biji dengan metode pengempaan
panas atau dengan ekstraksi pelarut. Minyak jarak pagar tidak dapat
senyawa ester forbol (Syah, 2006). Komponen asam lemak terbanyak dalam
minyak adalah oleat. Kandungan asam lemak pada minyak jarak pagar dapat
dilihat pada Tabel 1, sedangkan sifat fisikokimia minyak jarak pagar terdapat
pada Tabel 2.
Gambar 2. Buah jarak pagar dan biji jarak pagar
Tabel 1. Kandungan asam lemak pada minyak jarak pagar
Jenis asam lemak Komposisi (%)
Asam miristat
Tabel 2. Sifat fisikokimia minyak jarak pagar
Sifat minyak Nilai
Biodiesel adalah bahan bakar diesel alternatif yang terbuat dari sumber
daya hayati terbarukan seperti minyak nabati atau lemak hewani (Ma dan
yang terbarukan, sekaligus sebagai alternatif bahan bakar minyak yang
berbasis petroleum (petrodiesel). Karakteristik minyak nabati tidak
memungkinkan penggunaannya secara langsung sebagai bahan bakar.
Berbagai produk turunan minyak nabati telah banyak diteliti untuk
memperbaiki sifat minyak nabati, termasuk diantaranya ester alkohol dari
minyak nabati (Korus, 2000).
Sumber alkohol yang digunakan dapat bermacam-macam. Apabila
direaksikan dengan metanol, maka akan didapat metil ester, apabila
direaksikan dengan etanol akan didapat etil ester. Metanol lebih banyak
digunakan sebagai sumber alkohol karena rantainya lebih pendek, lebih polar
dan harganya lebih murah dari alkohol lainnya (Ma dan Hanna, 2001).
Gambar 3 menunjukkan reaksi pembentukan metil ester, sementara Gambar 4
menunjukkan reaksi pembentukan etil ester.
Metil ester yang diproduksi sebagai pengganti bahan bakar konvensional
minyak bumi, harus memenuhi standar biodiesel. Legowo et al. (2001),
CH2OCOR''' CH2OH R'''COOC2H5
Gambar 4. Reaksi pembentukan etil ester
CH2OCOR''' CH2OH R'''COOCH3
menyebutkan ciri biodiesel secara umum meliputi densitas, viskositas
kinematik, bilangan setana, kalor pembakaran, titik tuang, titik pijar, dan titik
awan. Ciri biodiesel secara umum dapat dilihat pada Tabel 3.
Mutu biodiesel di Amerika Serikat mengikuti standar yang terdapat
dalam ASTM D6751-02, yaitu spesifikasi standar untuk bahan bakar biodiesel
B100 (Van Gerpen, 2004a). Standar mutu biodiesel dapat dilihat pada Tabel 4.
Tabel 3. Ciri biodiesel secara umum
Parameter Nilai
Densitas (g/cm3)
Viskositas kinematik (40 oC) Bilangan setana
Bilangan asam adalah berat KOH (dalam mg) yang dibutuhkan untuk
menetralkan asam lemak bebas dari satu gram minyak atau lemak. (Lang et
al., 2001). Van Gerpen et al. (1996) menyatakan, asam lemak bebas pada
biodiesel dapat bereaksi dengan sisa katalis dan membentuk sabun, hal ini
dapat menyebabkan terbentuknya abu saat pembakaran biodiesel. Bilangan
asam yang diperbolehkan dalam ASTM D664 tidak lebih dari 0,8 mg KOH/g.
Tabel 4. Standar mutu biodiesel (ASTM D6751-02)
Properti Metode ASTM Nilai Satuan
Densitas atau bobot jenis adalah perbandingan berat contoh pada suhu
25 °C dengan berat air pada volume dan suhu yang sama. Densitas biodiesel
pada suhu 15 °C tidak boleh melebihi 0.900 kg/m3. Jika densitasnya lebih dari
0.900 kg/m3 pada suhu 60 F, kemungkinan reaksi transesterifikasi tidak
berjalan sempurna dan masih terdapat banyak trigliserida (Syah, 2006).
Viskositas (kekentalan) diartikan sebagai ukuran ketahanan bahan bakar
untuk mengalir. Kisaran viskositas kinematis yang ditetapkan dalam ASTM
D445 antara 1.9-6.0 mm/s pada suhu 40 °C. Sistem pembakaran
membutuhkan bahan bakar yang dapat membentuk partikulat halus ketika
diinjeksi. Jika viskositas bahan bakar terlalu rendah, akan menyebabkan
kebocoran yang mengurangi daya pembakaran, jika viskositas terlalu tinggi,
bahan bakar akan sulit disuplai ke ruang pembakaran, hal ini juga
menyebabkan berkurangnya daya pembakaran (Van Gerpen, 2004b)
C. TRANSESTERIFIKASI
Transesterifikasi adalah reaksi ester untuk menghasilkan ester baru yang
mengalami penukaran posisi asam lemak (Swern, 1982). Transesterifikasi
dapat menghasilkan biodiesel yang lebih baik dari proses mikroemulsifikasi,
pencampuran dengan petrodiesel atau pirolisis (Ma dan Hanna, 2001).
Reaksi transesterifikasi untuk memproduksi biodiesel tidak lain adalah
reaksi alkoholisis, reaksi ini hampir sama dengan reaksi hidrolisis tetapi
menggunakan alkohol. Reaksi ini bersifat reversible dan menghasilkan alkil
ester dan gliserol. Alkohol berlebih digunakan untuk memicu reaksi
pembentukan produk (Khan, 2002).
Menurut Swern (1982), jumlah alkohol yang dianjurkan sekitar 1,6 kali
jumlah yang dibutuhkan secara teoritis. Jumlah alkohol yang lebih dari 1,75
kali jumlah teoritis tidak mempercepat reaksi bahkan mempersulit pemisahan
gliserol selanjutnya. Freedman (1984) menyebutkan bahwa untuk
transesterifikasi menggunakan katalis basa, nisbah mol metanol:minyak
sebesar 6:1 adalah optimal.
Katalis yang banyak digunakan adalah katalis basa, namun katalis asam
bebasnya tinggi. Katalis basa dinilai lebih baik dari katalis asam karena
dengan katalis basa reaksi dapat berjalan pada suhu lebih rendah, bahkan pada
suhu kamar. Adapun reaksi dengan katalis asam membutuhkan suhu yang
lebih tinggi (Dmytryshyn et al., 2004).
Katalis basa yang umum digunakan adalah NaOH, KOH, karbonat dan
alkoksida dari Natrium dan Kalium seperti Natrium metoksida, etoksida,
propoksida dan butoksida (Khan,2002). Menurut Knothe (2002) produksi
biodiesel saat ini lebih sering menggunakan KOH, dengan reaksi yang
dilakukan pada suhu ruang, tingkat konversi 80-90 % dapat dicapai dalam
waktu 5 menit. Tingkat konversi metil ester bahkan bisa mencapai 99 % pada
proses transesterifikasi dua tahap.
Pemakaian katalis KOH pada reaksi transesterifikasi telah berhasil pada
berbagai jenis minyak, antara lain minyak biji canola (Dmytryshyn et al.,
2004), minyak biji rami (linseed), minyak rapeseed (Lang et al., 2001),
minyak kelapa sawit (Darnoko dan Cheryan, 2000), minyak zaitun dan
minyak kelapa sawit bekas (Dorado et al.,2002) dan minyak jarak pagar (Foidl
et al., 1996). Katalis KOH juga dipilih karena harganya lebih murah dari
NaOH.
Pada reaksi dengan menggunakan katalis basa minyak yang digunakan
harus netral. Kadar asam lemak bebas yang lebih dari 0.5 % dapat
menurunkan rendemen trasesterifikasi minyak (Freedman et al., 1984). Goff et
al. (2004) menyatakan bahwa minyak dengan kadar air kurang dari 0.1 %
dapat menghasilkan metil ester lebih dari 90 %.
Menurut Darnoko dan Cheryan (2000), transesterifikasi minyak kelapa
sawit menggunakan katalis KOH kurang dari 1,0 % bobot minyak
menunjukkan gejala terjadinya jeda reaksi selama 6 menit, sebelum
terbentuknya metil ester. Vicente et al. (1998) dalam Darnoko dan Cheryan
(2000) merekomendasikan penggunaan katalis dengan konsentrasi yang lebih
tinggi dari 1 %.
Beberapa penelitian melaporkan reaksi transesterifikasi yang
dilangsungkan pada beberapa suhu. Semakin tinggi suhu reaksi, konstanta laju
produk lebih besar dari konstanta laju reaksi balik. (Noureddini, 1997). Suhu
maksimum untuk reaksi transesterifikasi adalah 65 °C, di bawah titik didih
metanol 68 °C. Metilasi minyak kelapa sawit mencapai kondisi stasioner
setelah 60 menit reaksi pada 50 oC (Darnoko dan Cheryan, 2000). Adapun
Foidl et al. (1996) melaporkan reaksi transesterifikasi minyak jarak pagar
(Jatropha curcas L.) dapat dilakukan pada suhu 30 °C dan menghasilkan
biodiesel dengan kadar metil ester 99.6 %.
Pengadukan diperlukan untuk homogenisasi campuran. Ketika metanol
dan katalis dicampurkan dengan minyak, akan terbentuk dua fase, yaitu fase
metanol di bagian atas dan fase minyak di bagian bawah. Adanya pemisahan
fase ini menghambat laju reaksi, karena rendahnya peluang kontak antara
minyak, metanol dan katalis (Boocock, 1998). Korus (2000) menyebutkan
diperlukan pengadukan yang sangat cepat untuk membantu homogenisasi
campuran.
Menurut Noureddini (1997) sebelum reaksi transesterifikasi benar-benar
berlangsung, reaksi didahului proses transfer massa yang mengakibatkan
terjadinya semacam penundaan sebelum reaksi benar-benar berlangsung. Pada
transesterifikasi minyak kacang kedelai (soybean oil) dengan suhu 70 °C dan
pengadukan 600 rpm, kondisi penundaan ini hampir tidak ada.
Reaksi transesterifikasi dengan menggunakan katalis basa dapat
dilakukan dalam satu tahap atau dua tahap. Reaksi tiga tahap bahkan dapat
mengurangi pemakaian alkohol hingga 1,2 kali jumlah teoritis (Swern, 1982).
Pada proses satu tahap minyak direaksikan dengan metanol dan KOH
sekaligus, sedangkan pada proses dua tahap minyak direaksikan dengan
sebagian larutan metanolik-KOH, kemudian metil ester yang terbentuk
dipisahkan dari gliserol dan direaksikan kembali dengan sisa larutan
III. METODOLOGI
A. BAHAN DAN ALAT
Bahan utama yang dibutuhkan dalam penelitian ini adalah minyak jarak
pagar hasil pengepresan biji jarak pagar yang berasal Lampung. Bahan lainnya
untuk reaksi transesterifikasi adalah metanol dan KOH. Selain itu digunakan
bahan-bahan untuk netralisasi minyak yaitu NaOH, dan untuk analisa meliputi
etanol 95% dan indikator phenolphthalein.
Alat yang digunakan untuk reaksi transesterifikasi adalah labu kaca
leher tiga kapasitas 1 liter, pengaduk, pemanas, kondensor, temperature
controller dan labu pemisah. Alat untuk analisa adalah piknometer,
viskometer ostwald, dan alat gelas lainnya.
B. METODOLOGI
1. Penyiapan bahan baku
Bahan baku minyak yang digunakan pada proses transesterifikasi
terlebih dahulu mengalami tahapan pemurnian meliputi degumming dan
netralisasi. Degumming bertujuan menghilangkan getah atau lendir yang
terdapat pada minyak, sedangkan netralisasi bertujuan menghilangkan
asam lemak bebas sehingga minyak memenuhi syarat untuk reaksi
transesterifikasi.
a. Degumming
Minyak jarak dipanaskan sampai suhu 80 °C kemudian
ditambahkan air panas bersuhu 60 °C dan diaduk. Air dipisahkan dari
minyak menggunakan labu pemisah. Setelah itu ke dalam minyak
ditambahkan air lagi dan dikocok. Tahap ini diulang sampai air cucian
b. Netralisasi
Minyak jarak dipanaskan hingga suhu 60oC, kemudian
ditambahkan NaOH 20°Be sebanyak jumlah yang telah
diperhitungkan. Kebutuhan larutan basa untuk netralisasi ditentukan
melalui perhitungan sebagai berikut ( JICA, 1984):
Dengan :
AV = Bilangan asam ( mg KOH/g minyak)
Larutan diaduk selama 2 menit kemudian dipindahkan ke labu
pemisah. Pada labu pemisah dituangkan air panas bersuhu 70 oC
sebanyak 5-10 % volume minyak awal. Campuran dibiarkan sementara
waktu hingga minyak dan air dapat dipisahkan. Prosedur pencucian
diulang beberapa kali hingga pH minyak sama dengan pH air. Terakhir
ditambahkan gel silika untuk menyerap sisa air.
ml NaOH = AV x 40 x ml minyak x 1.3 x densitas minyak x 10
56 x 1000 x 16.7
2. Transesterifikasi
Transesterifikasi dilakukan pada labu bulat berleher tiga
dengan kapasitas 1 liter dilengkapi temperature controller, kondensor
dan pengaduk yang ditempatkan pada lempeng pemanas listrik.
Sebanyak 100 g minyak dipanaskan dalam labu reaksi setelah suhu
minyak mencapai suhu tertentu (30 oC, 65 oC).
Katalis KOH sebanyak 1.5 % bobot minyak dilarutkan dalam
metanol ( jumlah mol metanol sebanyak 4 ; 5; 6; 7 kali mol minyak)
disertai pengadukan selama 15 menit hingga terbentuk larutan
metanolik KOH. Larutan metanolik-KOH ini dicampurkan ke dalam
minyak jarak dan waktu reaksi mulai dihitung.
Selama reaksi dilakukan pengadukan dengan kecepatan 400
controller. Reaksi dihentikan setelah tercapai waktu reaksi yang
diinginkan (60 menit). Campuran reaktan diendapkan selama semalam
(± 12 jam) hingga terpisah membentuk lapisan-lapisan. Metil ester
yang berada pada lapisan atas dipisahkan dari gliserol yang berwarna
gelap.
Metil ester dimasukkan ke dalam corong pisah, kemudian
ditambahkan aquadest yang bersuhu 50 °C sebanyak metil ester yang
ditambahkan ke dalam corong pisah. Campuran dikocok dengan kuat
dan didiamkan beberapa saat sampai terbentuk dua lapisan. Lapisan air
di bagian bawah dibuang dan pencucian diulang beberapa kali
menggunakan akuades sampai metil ester netral.
Pada transesterifikasi dua tahap, larutan metanolik-KOH
digunakan sebagian (50%). Reaksi transesterifikasi dilangsungkan
selama 30 menit. Kemudian campuran reaktan diendapkan selama dua
jam hingga terpisah menjadi lapisan-lapisan. Lapisan metil ester yang
berada di bagian atas dipisahkan dan direaksikan kembali dengan sisa
larutan metanolik-KOH. Reaksi dilanjutkan seperti reaksi
transesterifikasi sebelumnya selama 30 menit. Tahapan selanjutnya
dari reaksi dua tahap ini sama seperti reaksi satu tahap. Diagram alir
reaksi transesterifikasi dapat dilihat pada Lampiran 1.
3. Prosedur analisis
Pengamatan terhadap metil ester yang dihasilkan meliputi
viskositas kinematik, bilangan asam, dan densitas.
a. Penentuan bilangan asam (AOAC,1995))
Sebanyak 5 gram minyak ditimbang (ketelitian 0.005 g) dalam
labu erlenmeyer. Kemudian ditambahkan 50 ml 95 % (v/v) etanol yang
telah dinetralkan. Setelah ditambahkan sebanyak 5 tetes indikator
fenolftalin, larutan dititrasi dengan larutan KOH 0.1 N yang telah
10 detik. Analisis diulang sebanyak 3 kali. Bilangan asam dihitung
N = Normalitas KOH setelah distandarisasi (N)
V = Volume KOH yang digunakan untuk titrasi (ml)
M = Bobot sampel minyak (g)
b. Penentuan kadar air (AOAC,1995)
Sebanyak 10 g minyak dimasukkan ke dalam oven 104-106oC
selama 30 menit. Minyak diangkat dari oven dan didinginkan dalam
desikator sampai mencapai suhu kamar, setelah itu ditimbang.
Prosedur diulang sampai bobotnya stabil (tidak berbeda lebih dari
0.005 %). Kadar air dan zat yang mudah menguap dihitung sebagai :
Dengan :
Mo = Bobot sebelum pemanasan (g)
M1 = Bobot sesudah pemanasan (g)
Kadar Air (%) = M1 – Mo x 100 Mo
c. Viskositas Metode Otswald (ASTM D445)
Viskometer otswald dibersihkan dengan cairan pembersih,
kemudian dibilas hati-hati dengan air suling dan dikeringkan dengan
aseton di udara terbuka. Alat dicelupkan ke dalam termostat air yang
bertemperatur 25 oC agar tercapai equilibrium. Gelas yang berisi air
diletakkan di dalam termostat tersebut. Air suling yang telah
H = Bt, ρ
Densitas air juga diukur pada alat tersebut pada kondisi yang sama
dengan pengukuran viskositas air. Untuk fluida nonkompresibel,
digunakan persaman poiseuille untuk menghitung viskositas, yaitu :
Dengan:
(P1 – P2) = beda tekanan pada kedua ujung tabung kapiler
Oleh karena (P1 – P2) sebanding dengan densitas ρ ditunjukkan
bahwa untuk total volume cairan ,
dengan t adalah waktu yang dibutuhkan fluida untuk melewati
batas atas sampai batas bawah pada viskometer Otswald, dan
B adalah konstanta alat yang ditentukan melewati kalibrasi
dengan cairan yang telah diketahui viskositasnya.
Bila viskositas air suling dapat diketahui, maka viskositas
fluida dapat dihitung melalui persamaan :
s
Dengan µ adalah viskositas dinamis (cp),θ waktu yang
dibutuhkan fluida untuk batas atas sampai batas bawah pada
viskometer Otswald,, ρ adalah densitas dan s mentunjukkan
standard yaitu air pada 298 °K. Untuk mendapatkan viskositas
kinematis, nilai µ dibagi dengan densitas sampel. dV = π r4 (P1 – P2 )
dt 8 ηL
d. Densitas (AOAC,1995)
Piknometer 50 ml ditimbang bobot kosongnya. Piknometer
lalu ditimbang. Pengukuran diulang tiga kali, hasil analisis dinyatakan
dalam rataan hitungnya. Densitas dihitung sebagai:
Dengan :
ρt = densitas pada suhu (g/ml)
m1 = bobot piknometer yang berisi minyak (g)
m1 = bobot piknometer kosong (g)
Vt = volume piknometer pada suhu t (ml)
ρt = m1 – mo Vt
C. RANCANGAN PERCOBAAN
Penelitian ini menggunakan rancangan acak lengkap faktorial dengan
tiga variabel perlakuan. Variabel perlakuan yang digunakan adalah tahap
transesterifikasi (A), suhu reaksi (B), dan molar ratio metanol-minyak (C).
Tahap transesterifikasi meliputi proses satu tahap (A1) dan dua tahap
(A2). Suhu dinyatakan dalam 2 taraf yaitu 30 °C (B1), 65 °C (B2). Molar ratio
dinyatakan dalam 4 taraf, yaitu 3:1 (C1), 4:1 (C2), 5:1 (C3), 6:1 (C4). Setiap
kombinasi perlakuan dilakukan ulangan sebanyak dua kali. Model linier aditif
untuk setiap metode dapat dilihat di persamaan berikut:
Yijk = µ + Bi + Cj + (BC)ij + ℮ijk
Dengan :
Yijk : pengamatan (viskositas kinematik, densitas, bilangan asam)
µ : nilai tengah umum
Bi : pengaruh molar ratio metanol ke-i
Cj : pengaruh konsentrasi katalis ke-j
(AB)ij : pengaruh interaksi faktor Ai dengan Bj
Data yang diperoleh diolah dengan ANOVA untuk melihat pengaruh
perlakuan yang telah diberikan. Hasil analisis sidik ragam dilanjutkan dengan
Uji Duncan untuk mengetahui kombinasi perlakuan yang menyebabkan
perbedaan nyata dari densitas, bilangan asam dan viskositas dari metil ester
IV. HASIL DAN PEMBAHASAN
A. BAHAN BAKU
Minyak jarak pagar memiliki kadar asam lemak bebas sebesar 3.07 %.
Menurut Freedman et al. (1984) minyak yang digunakan dalam reaksi
transesterifikasi dengan katalis basa, harus memiliki kadar asam lemak bebas
kurang dari 0.5 %. Asam lemak bebas akan bereaksi dengan katalis basa
membentuk sabun, hal ini mengurangi efektifitas katalis dan menurunkan laju
reaksi pembentukan metil ester. Oleh karena itu harus dilakukan proses
netralisasi untuk menurunkan kadar asam lemak bebas dalam minyak.
Proses netralisasi didahului penghilangan gum (degumming) untuk
menghilangkan getah atau lendir yang terdapat pada minyak. Setelah
dinetralisasi, kadar asam lemak bebas turun menjadi 0.22 % dan warnanya
menjadi lebih cerah. Viskositas kinematik minyak jarak pagar menurun karena
gum dan lendirnya telah hilang. Kadar air minyak yang telah dinetralisasi
sebesar 0.06 % telah memenuhi syarat untuk transesterifikasi. Karakteristik
minyak jarak pagar sebelum dan sesudah dinetralisasi dapat dilihat pada Tabel
5. Penampilan minyak jarak pagar sebelum dan sesudah dinetralisasi dapat
dilihat pada Gambar 5.
Tabel 5. Karakteristik minyak jarak pagar sebelum dan sesudah dinetralisasi
Parameter Minyak jarak pagar Minyak yang telah
dinetralisasi
Bilangan asam (mg KOH/g) 6.11 0.43
FFA (%) 3.07 0.22
Kadar Air (%b/b) 0.47 0.06
Viskositas kinematik (30°C) (cSt) 50.76 48.26
Densitas (25°C) (g/cm3) 0.92 0.91
Dapat dilihat pada tabel di atas, minyak yang digunakan memiliki
viskositas kinematik yang tinggi sebesar 48.26-50.76 cSt dan densitas lebih dari
0.90 g/cm3. Kedua nilai inilah yang akan menjadi parameter keberhasilan reaksi
hingga ke tingkat yang ditetapkan dalam standar, maka reaksi transesterifikasi
yang dilakukan dianggap berhasil.
Gambar 5. Minyak jarak pagar sebelum dan sesudah dinetralisasi
B. METIL ESTER
1. Karakteristik Fisik Metil Ester
Metil ester yang dihasilkan berwarna kuning pucat, transparan, encer
dan masih ada bau minyak jarak pagar. Secara visual tidak terdapat
perbedaan antara metil ester dari berbagai perlakuan. Pada saat proses
pemisahan, metil ester berada di lapisan atas, sedangkan gliserol berada di
lapisan bawah. Gliserol yang terbentuk selama proses transesterifikasi
berwarna coklat tua dan kental.
Semakin rendah nisbah mol metanol:minyak, gliserol semakin kental
bahkan memadat. Metanol yang tersisa setelah reaksi transesterifikasi
berakhir akan bercampur bersama metil ester dan gliserol. Jika nisbah mol
metanol rendah, maka sisa metanol ini hanya sedikit, dan akibatnya gliserol
semakin kental.
2.Viskositas Kinematik
Viskositas kinematik menjadi parameter utama dalam penentuan mutu
metil ester, karena memiliki pengaruh besar terhadap efektifitas metil ester
sebagai bahan bakar. Minyak nabati memiliki viskositas jauh di atas
viskositas bahan bakar diesel, inilah yang menjadi kendala penggunaan
transesterifikasi adalah menurunkan viskositas minyak nabati sehingga
memenuhi standar bahan bakar diesel.
Viskositas kinematik metil ester yang dihasilkan pada penelitian ini
berkisar antara 3.72-5.81 cSt. Standar mutu biodiesel ASTM D445
menetapkan viskositas kinematik biodiesel pada suhu 40°C berkisar 1.9-6.0
cSt. Hasil analisis sidik ragam menunjukkan nisbah mol metanol dan suhu
reaksi merupakan faktor yang berpengaruh signifikan terhadap perubahan
viskositas kinematik. Viskositas kinematik metil ester dapat dilihat pada
Tabel 6, sedangkan hasil analisis sidik ragam dan uji lanjutannya dapat
dilihat pada Lampiran 2.
Tabel 6. Viskositas kinematik metil ester pada 40 °C(cSt)
Proses transesterifikasi Satu tahap (A1) Dua tahap (A2)
Suhu (°C) 30 (B1) 65 (B2) 30 (B1) 65 (B2)
Uji lanjut Duncan menunjukkan perlakuan pada suhu 65 °C
memberikan respon viskositas kinematik yang lebih tinggi daripada pada
suhu 30 °C. Pada perlakuan suhu tinggi, terdapat indikasi terjadi reaksi
oksidasi termal, yaitu dekomposisi susunan kimiawi akibat pengaruh panas.
Reaksi oksidasi ini dapat terjadi selama proses pemanasan minyak sebelum
metanol ditambahkan. Reaksi ini juga dapat terjadi pada metil ester saat
reaksi transesterifikasi berlangsung.
Peristiwa oksidasi ini menyebabkan terbentuknya molekul
hidroperoksida, aldehida, keton dan asam yang dapat mengubah sifat bahan
bakar. Senyawa hidroperoksida memicu terjadinya polimerisasi dan
mengakibatkan terbentuknya endapan yang tak larut. Hal ini menyebabkan
peningkatan viskositas pada biodiesel yang diberi perlakuan suhu 60 °C,
80°C dan 90 °C selama 12 jam.
Suhu reaksi yang tinggi dapat memacu laju reaksi transesterifikasi
seiring dengan meningkatnya konstanta laju reaksi, namun perlakuan ini
sekaligus memperbesar resiko terjadinya reaksi oksidasi yang dapat
meningkatkan viskositas kinematik biodiesel. Oleh karena itu perlakuan
suhu yang dipilih adalah suhu rendah yaitu 30°C ( B1).
Uji lanjut Duncan juga diterapkan pada variabel perlakuan nisbah mol
metanol. Respon viskositas kinematik paling tinggi diperoleh dari nisbah
mol 3:1 (C1) sementara respon paling rendah diperoleh dari nisbah mol 5:1
(C3).
Tingginya viskositas kinematik pada perlakuan nisbah mol 3:1
menandakan reaksi pembentukan metil ester tidak berjalan dengan tuntas.
Jika reaksi tidak berjalan dengan tuntas, akan terdapat banyak trigliserida
yang tidak diubah menjadi metil ester. Keadaan ini berdampak pada
tingginya nilai viskositas kinematik, karena trigliserida lebih kental dari
metil ester. Oleh karena itu viskositas kinematik sekaligus mengindikasikan
kesempurnaan reaksi transesterifikasi.
Banyak penelitian yang menganjurkan penggunaan metanol berlebih
untuk memicu jalannya reaksi pembentukan metil ester. Dapat dilihat pada
Gambar 6, secara stoikiometri jumlah mol metanol yang dibutuhkan adalah
tiga kali jumlah mol minyak, inilah yang disebut nisbah mol metanol 3:1.
Jumlah metanol ditingkatkan untuk mempengaruhi kesetimbangan sehingga
reaksi bergeser ke arah pembentukan produk. Untuk menjamin keberhasilan
reaksi, maka jumlah metanol biasanya ditingkatkan sampai nisbah mol 6:1.
Trigliserida + 3ROH 3R’CO2-R + Gliserol
Gambar 6. Reaksi transesterifikasi menghasilkan metil ester
Perlakuan nisbah mol metanol 5:1 menghasilkan respon viskositas
kinematik paling rendah. Perlakuan ini tidak berbeda nyata dengan nisbah
Perlakuan terbaik yang dipilih adalah transesterifikasi dengan nisbah
mol metanol 5:1 pada suhu 30°C (B1C3). Pada kombinasi B1C3 ini, proses
transesterifikasi satu tahap memiliki viskositas kinematik 3.89 cSt,
sementara proses dua tahap memiliki viskositas kinematik sebesar 3.75 cSt.
3. Densitas
Selain viskositas, densitas juga dapat menjadi parameter keberhasilan
reaksi transesterifikasi. Biodiesel dengan densitas lebih dari 0.900 g/cm3
pada 60 °F, kemungkinan merupakan hasil dari reaksi yang tidak sempurna.
Densitas biodiesel seharusnya berkisar 0.860-0.900 g/cm3 (Syah, 2006).
Metil ester minyak jarak pagar dengan kadar ester 99.6 % memiliki densitas
sebesar 0.879 pada suhu 15 °C (Foidl et al., 1996).
Densitas metil ester yang dihasilkan berkisar 0.848-0.884 g/cm3,
selengkapnya dapat dilihat pada Tabel 7. Hasil analisis uji sidik ragam
menunjukkan tidak ada faktor yang berpengaruh secara signifikan terhadap
perubahan densitas. Densitas paling kecil adalah pada perlakuan A2B1C1,
sedangkan yang paling besar pada perlakuan A1B2C2. Hasil analisis sidik
ragam densitas metil ester dapat dilihat pada Lampiran 4.
Tabel 7. Densitas metil ester pada suhu 25 °C (g/cm3)
Proses transesterifikasi Satu tahap (A1) Dua tahap (A2)
Suhu (°C) 30 (B1) 65 (C1) 30 (B1) 65 (C1)
Perlakuan terbaik yang disimpulkan pada parameter viskositas
kinematik yaitu B1C3 (suhu 30°C, nisbah mol metanol 5:1) memiliki densitas rata-rata 0.875 g/cm3. Pada suhu dan nisbah mol tersebut, densitas
metil ester proses satu tahap adalah 0.877 g/cm3, sedangkan hasil proses dua
4. Bilangan Asam
Asam lemak bebas dapat mengakibatkan terbentuknya abu pada saat
pembakaran biodiesel. Nilai bilangan asam juga menjadi indikator
kerusakan yang terjadi pada metil ester. Hal ini disebabkan peningkatan
bilangan asam seperti halnya peningkatan viskositas dan bilangan peroksida
adalah hasil aktifitas oksidasi pada metil ester (Canacki, 1999). Oleh karena
itu, jika bilangan asam metil ester tinggi, berarti telah terjadi kerusakan
akibat oksidasi.
Bilangan asam sekaligus meramalkan tingkat kerusakan metil ester
selama penyimpanan beberapa waktu ke depan. Tingkat oksidasi tinggi juga
menandakan metil ester tidak tahan lama disimpan, sebab senyawa
peroksida yang menjadi produk intermediet pada reaksi oksidasi dapat
menyerang asam lemak lainnya yang masih utuh, sehingga akan terbentuk
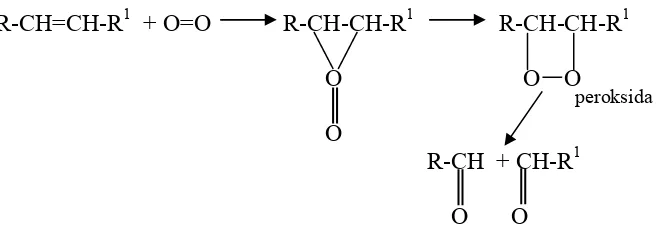
asam lemak bebas rantai pendek yang lebih banyak. Mekanisme reaksi
oksidasi yang membentuk senyawa peroksida dan asam lemak bebas dapat
dilihat pada Gambar 7.
Bilangan asam metil ester yang dihasilkan berkisar antara 0.40-0.83
mg KOH/g sampel. Standar mutu biodiesel ASTM D664 mensyaratkan
bilangan asam biodiesel tidak lebih dari 0,80 mg KOH/g sampel. Bilangan
asam metil ester dapat dilihat pada Tabel 8.
R-CH=CH-R1 + O=O R-CH-CH-R1 R-CH-CH-R1
O O O
O
R-CH + CH-R1
O O
Gambar 7. Reaksi oksidasi membentuk peroksida dan asam lemak rantai pendek
Analisis sidik ragam menunjukkan bahwa nisbah mol metanol,
interaksi perlakuan tahap transesterifikasi dan nisbah mol metanol (A*C),
interaksi tahap transesterifikasi dan suhu (A*B) dan interaksi suhu dan
nisbah mol metanol (B*C) berpengaruh nyata terhadap bilangan asam metil
ester. Adapun perlakuan tahap transesterifikasi (A), suhu (B) dan interaksi
perlakuan tahap transesterifikasi, suhu dan nisbah mol metanol (A*B*C)
tidak berpengaruh nyata terhadap nilai bilangan asam.
Tabel 8. Bilangan asam metil ester (mg KOH/ g sampel)
Proses transesterifikasi Satu tahap (A1) Dua tahap (A2)
suhu (°C) 30 (B1) 65 (C1) 30 (B1) 65 (C1)
Uji lanjut Duncan diterapkan untuk menganalisa interaksi perlakuan
tahap transesterifikasi dan suhu (A*B), interaksi perlakuan tahap
transesterifikasi dan nisbah mol metanol (A*C) dan interaksi perlakuan suhu
dan nisbah mol metanol (B*C). Keterangan di atas dirangkum dalam
Lampiran 3.
Pada proses transesterifikasi satu tahap, peningkatan nisbah mol
metanol tidak menimbulkan perbedaan yang nyata terhadap perubahan
bilangan asam, kecuali pada taraf terbesar yaitu 6:1, respon bilangan asam
pada taraf ini merupakan yang terbesar. Adapun pada proses
transesterifikasi dua tahap, peningkatan nisbah mol metanol dari 3:1 ke 4:1
menimbulkan perbedaan yang nyata, yaitu dengan adanya peningkatan
bilangan asam secara signifikan.
Peningkatan suhu menimbulkan perbedaan yang nyata pada bilangan
asam metil ester yang dihasilkan. Pada suhu yang lebih rendah proses
transesterifikasi satu tahap menghasilkan respon bilangan asam lebih
rendah, sedangkan proses dua tahap menghasilkan respon yang lebih tinggi.
yang nyata setelah nisbah mol 5:1, dengan munculnya respon tertinggi.
Adapun pada suhu 65 °C, perbedaan bilangan asam yang nyata muncul pada
nisbah mol 4:1, yang juga memberikan respon tertinggi.
Perlakuan yang menghasilkan respon bilangan asam paling rendah
adalah kombinasi proses dua tahap dengan nisbah mol metanol 3:1 (A2C1).
Sementara perlakuan yang menghasilkan respon bilangan asam paling tinggi
adalah kombinasi proses dua tahap dengan nisbah mol 4:1 (A2C2).
Pada perlakuan B1C3, nilai bilangan asam rata-rata adalah sebesar
0.66 mg KOH/g sampel. Proses transesterifikasi satu tahap dengan
kombinasi B1C3 memiliki bilangan asam 0.48 mg KOH/g sampel,
sedangkan proses dua tahap dengan kombinasi tersebut memiliki bilangan
asam 0.83 mg KOH/g sampel.
5.Perbandingan Proses Transesterifikasi Satu Tahap dan Dua Tahap
Hasil analisis sidik ragam viskositas kinematik, densitas maupun
bilangan asam menunjukkan tidak terdapat pengaruh signifikan yang
ditimbulkan oleh perlakuan transesterifikasi satu tahap maupun dua tahap.
Oleh karena itu untuk membandingkan kinerja proses satu tahap dan dua
tahap digunakan nilai viskositas kinematik dan densitas.
Pada suhu dan nisbah mol metanol yang sama, proses dua tahap
menghasilkan metil ester dengan viskositas kinematik dan densitas yang
lebih rendah dari proses satu tahap. Nilai viskositas kinematik dan densitas
ini menjadi parameter tingkat konversi trigliserida menjadi metil ester.
Semakin rendah nilai keduanya, diduga semakin tinggi kadar metil esternya,
dengan kata lain tingkat konversinya juga tinggi.
Hasil penelitian Dorado et al.(2002) melaporkan, transesterifikasi dua
tahap pada minyak sayur memiliki tingkat konversi yang lebih tinggi
daripada transesterifikasi satu tahap. Konversi metil ester pada proses satu
tahap berkisar 83-91%, sementara pada proses dua tahap mencapai 87-95%.
Keberhasilan konversi metil ester pada reaksi transesterifikasi dua
yang bersifat reversibel, kesetimbangan dicapai saat laju reaksi ke kiri sama
dengan laju reaksi ke kanan (Gambar 8).
Tetapan kesetimbangan ditentukan dari perbandingan konsentrasi
produk dan pereaksi dalam keadaan setimbang.
[ ] [ ]
Untuk menduga arah reaksi, setiap saat selama reaksi berlangsung dapat
dibuat nisbah konsentrasi (Q) yang rumusnya sama dengan rumus tetapan
kesetimbangan (K). Jika nilai Q = K, maka reaksi dalam keadaan setimbang,
jika nilai Q < K, maka reaksi berlangsung ke kanan untuk memperbesar
nilai [C] dan [D], sementara jika nilai Q > K, maka reaksi berlangsung ke
kiri untuk memperbesar nilai [A] dan [B].
Adakalanya kesetimbangan telah terjadi sebelum seluruh reaktan
bereaksi, yaitu nilai Q = K, padahal A dan B belum habis bereaksi. Keadaan
seperti ini mengakibatkan pembentukan produk tidak maksimal. Oleh
karena itu dilakukan upaya agar reaksi berlangsung ke arah pembentukan
produk.
Kesetimbangan dapat bergeser apabila terdapat gangguan dari luar
sistem. Gangguan tersebut dapat berupa perubahan volume, tekanan,
konsentrasi dan suhu. Berdasarkan prinsip Le Chatelier, setiap gangguan
akan mengakibatkan pergeseran kesetimbangan ke arah yang melawan
gangguan tersebut. Penambahan konsentrasi pereaksi pada sisi kiri akan
menggeser reaksi pembentukan produk ke arah kanan. Pengurangan
konsentrasi produk di sisi kanan akan menggeser reaksi ke arah kanan juga,
untuk membentuk kesetimbangan baru.
aA + bB cC + dD Pereaksi (sisi kiri) Produk (sisi kanan)
Pembentukan metil ester pada reaksi transesterifikasi, disebabkan
pergeseran kesetimbangan akibat adanya gangguan ini. Transesterifikasi
merupakan reaksi sebagai berikut (Gambar 8).
Rumus tetapan kesetimbangan (K) untuk reaksi transesterifikasi
adalah sebagai berikut.
Nilai Q untuk menduga arah reaksi juga ditentukan dengan rumus yang
sama seperti di atas.
Pada reaksi transesterifikasi yang biasa dilakukan dengan proses satu
tahap, jenis gangguan yang dilakukan adalah dengan meningkatkan
konsentrasi pereaksi. Dengan menambah metanol, nilai [M] semakin besar,
sehingga Q < K, dan reaksi akan berlangsung ke arah kanan.
Pada reaksi dua tahap, gangguan yang terjadi adalah pengurangan
konsentrasi gliserol. Pemisahan gliserol yang dilakukan di tengah reaksi
menurunkan nilai [GL] dan nilai Q menjadi lebih kecil. Ketika terjadi
penambahan sisa larutan metanolik-KOH, nilai [M] naik dan Q akan
semakin kecil. Reaksi akan berlangsung ke arah kanan karena Q < K.
Melalui mekanisme seperti ini pembentukan produk dapat dipicu tanpa
meningkatkan konsumsi pereaksi. Dengan jumlah metanol yang sama,
proses dua tahap mampu mencapai konversi ester yang lebih tinggi dari
proses satu tahap.
Metil ester hasil proses transesterifikasi dua tahap memiliki bilangan
asam yang lebih tinggi. Hal ini disebabkan proses dua tahap membutuhkan TG + 3M GL + 3ME
Trigliserida metanol gliserol metil ester
waktu yang lebih lama daripada proses satu tahap. Pada proses dua tahap,
metil ester mengalami 14 jam pengendapan, dua jam lebih lama daripada
proses satu tahap. Pengendapan yang bertujuan memisahkan gliserol ini,
membutuhkan waktu dua jam di tengah proses dan 12 jam setelah reaksi
selesai.
Canacki (1999) melaporkan adanya kenaikan bilangan asam terhadap
metil ester seiring bertambahnya waktu penyimpanan. Dengan waktu
pengendapan yang lebih lama, diduga tingkat oksidasi pada proses dua
tahap lebih tinggi dari proses satu tahap. Hal ini mengakibatkan bilangan
asam yang lebih tinggi.
Proses dua tahap dapat meningkatkan pembentukan metil ester namun
memiliki resiko oksidasi yang lebih besar. Proses satu tahap menghasilkan
respon viskositas dan densitas sedikit lebih tinggi namun bilangan asamnya
rendah. Proses satu tahap dipilih sebagai perlakuan terbaik dikombinasikan
dengan suhu 30°C dan nisbah mol metanol 5:1 (A2B1C3). Metil ester dan gliserol hasil kombinasi perlakuan tersebut dapat dilihat pada Gambar 9.
Gambar 9. Metil ester dan gliserol perlakuan terbaik
6.Biaya produksi biodiesel
Komponen penyusun biaya produksi biodiesel meliputi biaya tetap
dan biaya tidak tetap. Biaya tetap meliputi gaji tenaga kerja tak langsung,
biaya pemeliharaan alat dan mesin, asuransi, biaya overhead serta pajak
bumi dan bangunan. Biaya tidak tetap antara lain biaya bahan baku
biodiesel, gaji tenaga kerja langsung, biaya bahan bakar dan listrik,
Biaya bahan baku pembuatan biodiesel masih lebih tinggi dari harga
jual solar yang beredar saat ini sebesar Rp 4 300/liter. Jika metanol dan
KOH yang digunakan adalah analitycal grade, biaya bahan baku biodiesel
sebesar Rp 36 130.57,-/kg. Jika bahan yang digunakan bersifat teknis, maka
biaya ini dapat ditekan hingga Rp 8 061.38,-/kg (Lampiran 5). Perhitungan
biaya ini berdasarkan asumsi harga biji jarak pagar kering Rp 1000/kg dan
rendemen minyak jarak pagar sebanyak 25 % bobot kering biji.
Hasil samping produksi biodiesel dapat dijual untuk memperoleh
pendapatan tambahan. Sudrajat (2007) menyebutkan, hasil sampingan
tersebut antara lain bungkil biji jarak, tempurung biji dan gliserol. Gliserol
yang telah dimurnikan dapat dijual seharga Rp 25000/liter, bungkil biji jarak
V. KESIMPULAN DAN SARAN
A. KESIMPULAN
Minyak jarak pagar memiliki kadar asam lemak melebihi batas yang
ditentukan untuk reaksi transesterifikasi berkatalis basa, karena itu sebelum
digunakan untuk proses transesterifikasi minyak harus dinetralisasi dahulu.
Netralisasi minyak didahului proses degumming untuk menghilangkan gum
dan getah yang terdapat pada minyak. Proses netralisasi dapat menurunkan
kadar asam lemak bebas pada minyak dari 3.07 % menjadi sebesar 0.22%.
Perlakuan optimal yang dipilih pada penelitian ini adalah yang
memberikan respon viskositas kinematik terkecil yang sesuai dengan standar.
Kemudian dilihat nilai densitas dan bilangan asamnya apakah sesuai dengan
standar. Metil ester yang dihasilkan dari proses transesterifikasi dua tahap
memiliki viskositas kinematik dan densitas yang lebih kecil dari metil ester
hasil proses satu tahap. Kendati demikian nilai bilangan asamnya lebih tinggi,
bahkan melampaui batas yang ditetapkan standar ASTM D664.
Proses transesterifikasi satu tahap menghasilkan viskositas kinematik
dan densitas yang sedikit lebih besar, namun bilangan asam metil esternya
kecil. Oleh karena itu proses satu tahap ditetapkan sebagai perlakuan optimal
dikombinasikan dengan suhu rendah (30°C) dan nisbah mol metanol 5:1.
Metil ester yang dihasilkan dari kombinasi perlakuan tersebut memiliki
viskositas kinematik 3.89 cSt, densitas 0.88 g/cm3 dan bilangan asam 0.48 mg
KOH/g sampel.
Biaya bahan baku biodiesel masih lebih tinggi dari harga solar yang
beredar saat ini. Biaya produksi biodiesel yang menggunakan bahan kimia
analitycal grade mencapai Rp 36 130.57,-/liter. Jika bahan yang digunakan
bersifat teknis, maka biaya ini dapat ditekan hingga Rp 8 061.38,-/liter.
B. SARAN
Proses netralisasi minyak tidak perlu dilakukan jika kadar asam lemak
minyak rendah. Minyak dengan kadar asam lemak yang rendah diperoleh dari
harus diperoleh dari biji yang baik, sehingga proses pembuatan biodiesel
dapat lebih efisien karena tidak perlu melakukan netralisasi dahulu.
Perlu adanya pengukuran karakteristik metil ester yang lain seperti
indeks setana, titik tuang, titik awan dan sebagainya. Karakteristik inilah yang
menentukan efektifitas metil ester ketika digunakan sebagai bahan bakar.
Untuk produksi biodiesel dengan skala yang lebih besar, dapat digunakan
bahan kimia yang bersifat teknis, sehingga biaya produksi biodiesel dapat
DAFTAR PUSTAKA
Canacki, M., A. Monyem, J. Van Gerpen. 1999. Accelerated Oxidation Processes in Biodiesel. Transaction of the American Society of Agricultural Engineers. 001-2351/99/4206-1656. 42(6) : 1565-1572.
Darnoko, D., Cheryan M., 2000. Kinetics of Palm Oil Transesterification in Batch Reactor. J. Am. Oil Chem. Soc. 77:1263-1237
Dmytryshyn, S.L., A.K.Dalai, S.T. Chaudari, H.K. Mishra, M.J. Reaney. 2004. Synthesis and Characterization of Vegetable Oil Derived Esters: Evaluation of Their Diesel Additive Properties. Bioresource Tech. 92:55-64.
Dorado., M.P., E. Ballesteros, J.A. De Almeida, C. Schellert, H.P. Lohrlein, R. Krause. 2002. An Alkali-Catalyzed Transesterification Process for High Free Fatty Acid Waste Oils. Transaction of American Society of Agricultural Engineers. ISSN 0001-2351. 45(3): 525-529
Foidl, N., G. Foidl, M. Sanchez, M. Mittelbach, S. Hackle.1996. Jatropha Curcas for Biodiesel Production in Nicaragua. Bioresouce Tech. 58(1): 77-82.
Freedman, B., Pryde Eh, Mounts Tl. 1984. Variables Affecting the Yields of Fatty Esters from Transesterified Vegetable Oils. J. Am. Oil Chem. Soc. 61:1638-1643.
Goff, M.J., Bauer N.S., Sutterlin W.R., Suppes G.J. 2004. Acid-Catalized Alcoholysis of Soybean Oil. J. Am. Oil Chem. Soc. 81 : 415-420.
Van Gerpen, Jon, Earl G. Hammond, Lawrence A. Johnson, Stephen J. Marley, Liangping Yu, Inmok Lee, Abdul Monyem. 1996. Determining the Influence of Contaminants on Biodiesel Properties. Iowa State University.
Van Gerpen, Jon. 2004 a. Biodiesel Production and Quality. Department of Biological and Agricultural Engineering. University of Idaho, Moscow.
Van Gerpen, Jon. 2004 b. Basics of Diesel Engines and Diesel Fuels. Department of Biological and Agricultural Engineering. University of Idaho. Moscow.
Khan, Adam Karl. 2002. Research Into Biodiesel Kinetics and Development. The University of Queensland, Queensland.
Korus, Roger A.,Dwight S. Hoffman, Narendra Bam, Charles L. Peterson, David C. Drown. 2000. Transesterification Process to Manufacture Ethyl Ester of Rape Oil. Department of Chemical Engineering. University of Idaho, Moscow.
Jaya, Indra. 2005. Optimasi Sintesis Biodiesel dari Minyak Jarak Pagar (Jatropha Curcas L.) Melalui Proses Esterifikasi-Transesterifikasi. Skripsi. Departemen Kimia. Fakultas Matematika dan Ilmu Pengetahuan Alam. IPB, Bogor.
Lang, X., A.K. Dalai, N.N. Bakhshi, M.J. Reaney, P.B. Hertz. 2001. Preparation and Characterization of Bio-Diesels from Various Bio-Oils. Bioresouce Tech. 80: 77-82.
Legowo E.H., Gafar Q., Sijabat O., Pupung Pl., Arifin Z. 2001. Experience in Palm Oil Biodiesel Application for Transportation. Di dalam. Jaya, Indra. 2005. Optimasi Sintesis Biodiesel dari Minyak Jarak Pagar (Jatropha Curcas L.) Melalui Proses Esterifikasi-Transesterifikasi. Skripsi. Departemen Kimia. Fakultas Matematika dan Ilmu Pengetahuan Alam. IPB, Bogor.
Ma, Fangrui dan Hanna, Milford A. 1999. Biodiesel Production : A Review. Bioresouce Tech. 70: 77-82.
Manurung, Robert.2003. Jatropha, A Promising Plant: Community Development. Bio-Technology Research Center. Institut Teknologi Bandung. Bandung
Noureddini, H., Zhu D. 1997. Kinetics of Transesterification of Soybean Oil. J. Am. Oil Chem. Soc.74:1457-1463.
Rohmawati, Euis. 2007. Studi Kelayakan Pendirian Industri Biodiesel Terpadu dari Jarak Pagar (Jatropha curcas L.) di Kawasan Pabrik Gula Jatitujuh, Majalengka, Jawa Barat. Skripsi. Fakultas Teknologi Pertanian. Institut Pertanian Bogor, Bogor.
Sudrajat, H.R., Dadang S., Yetiw., Rani A., Sahirman. 2007. Permasalahan dalam Teknologi Pengolahan Biodiesel dari Minyak Jarak Pagar (Jatropha Curcas L.). Prosiding Lokakarya II. Status Teknologi Tanaman Jarak Pagar (Jatropha Curcas L.). Badan Penelitian dan Pengembangan Pertanian. Pusat Penelitian dan Pengembangan Perkebunan. Bogor.
Swern, D. Editor. 1982. Bailey’s Industrial Oil and Fat Products. Ed Ke-4. Volume Ke-2. John Wiley and Sons. New York.
Lampiran 1. Diagram alir pembuatan larutan metanolik-KOH
Metanol
(14.6; 18.4; 21.8; 25.6 g)
KOH 1.5 g
Pengadukan 15 menit
Larutan metanolik-KOH
Diagram alir transesterifikasi satu tahap :
Pengadukan 400 rpm, pada 30 atau 65 oC,60 menit Minyak jarak 100 gram
Larutan metanolik-KOH
Pengendapan 12 jam
Pemisahan metil ester
Pencucian dengan air panas 50 °C
Penambahan silica gel
Filtrasi metil ester
Diagram alir transesterifikasi dua tahap
Minyak jarak 100 gram
Pengadukan 400 rpm, 30/65 oC, 30 menit Larutan
metanolik-KOH (50 %)
Pengendapan 2 jam
Pemisahan metil ester
Pengadukan 400 rpm, pada 30 atau 65 oC, 90 menit Larutan
metanolik-KOH (50 %)
Pengendapan 12 jam
Pencucian dengan air panas 50 °C
Penambahan silica gel
Filtrasi metil ester
Lampiran 2. Hasil analisis sidik ragam viskositas kinematik metil ester
Proses transesterifikasi Satu tahap Dua tahap
Suhu (°C) 30 65 30 65
Analysis of Variance untuk viskositas kinematik,
Sumber DF Seq SS Adj SS Adj MS F P
Uji lanjut untuk suhu reaksi
Grup duncan Mean N Suhu reaksi
A 4.6900 16 65
B 4.3288 16 30
Uji lanjut untuk nisbah mol metanol
Grup duncan Mean N Nisbah mol metanol
A 5.8963 8 3
B 4.3500 8 4
C 3.9088 8 6
Lampiran 3. Hasil analisis sidik ragam bilangan asam metil ester
Proses transesterifikasi Satu tahap Dua tahap
Suhu (°C) 30 65 30 65
General Linear Model: 1/x2 versus tahap transesterikasi; suhu; nisbah mol metanol
Faktor Tipe Taraf Nilai Tahap transesterifikasi fixed 2 1; 2 Suhu fixed 2 30; 65 Nisbah mol metanol fixed 4 3; 4; 5; 6
Analysis of Variance for 1/x2, using Adjusted SS for Tests
Sumber DF Seq SS Adj SS Adj MS F P
Uji lanjut interaksi tahap transesterifikasi dan suhu reaksi Grup duncan Mean perlakuan
Uji lanjut interaksi tahap transesterifikasi dan nisbah mol metanol
Grup duncan Mean Perlakuan
A 0,62107 A2C2
Uji lanjut interaksi suhu dan nisbah mol metanol Grup duncan Mean Perlakuan
Lampiran 4. Hasil analisis sidik ragam densitas metil ester
Proses transesterifikasi Satu tahap Dua tahap
Suhu (°C) 30 65 Suhu (°C) 30
Analysis of Variance for densitas, using Adjusted SS for Tests
Source DF Seq SS Adj SS Adj MS F P tahap tr 1 0.0001810 0.0001810 0.0001810 0.99 0.335 suhu rea 1 0.0002086 0.0002086 0.0002086 1.14 0.302 nisbah mol metanol 3 0.0001207 0.0001207 0.0000402 0.22 0.881 tahap transesterifikasi*suhu reaksi 1 0.0000942 0.0000942 0.0000942 0.51 0.484 tahap transesterifikasi*nisbah mol metanol 3 0.0005170 0.0005170 0.0001723 0.94 0.444 suhu reaksi*nisbah mol metanol 3 0.0003829 0.0003829 0.0001276 0.70 0.568 tahap transesterifikasi*suhu reaksi*
nisbah mol metanol 3 0.0002627 0.0002627 0.0000876 0.48 0.702
Lampiran 5. Analisa biaya biodiesel
Daftar harga bahan baku
Kebutuhan Bahan Baku Unit Harga per unit (Rp/kg)
Biji jarak pagar kg 1,000.00
metanol p.a kg 113,924.05
metanol teknis kg 12,658.23
KOH p.a kg 199,000.00
KOH teknis kg 12,500.00
NaOH p.a kg 365,000.00
NaOH teknis kg 6,000.00
(Hasil survei di Toko Alat dan Bahan Kimia ”Setia Guna”, Bogor,15 September 2007)
Kebutuhan bahan baku untuk setiap 1 kg biodiesel Kebutuhan Bahan Baku Kebutuhan (Kg)
Biji jarak pagar 5.13
Metanol 0.21
KOH 0.02
NaOH 0.01
Biaya bahan baku untuk setiap 1 kg biodiesel
Lampiran 6. Neraca massa pembuatan biodiesel
Proses transesterifikasi satu tahap
Keterangan gram Yield (b/b MJK) Loss
Minyak jarak kasar (MJK) 1060.00
Minyak jarak didegumming 960.00 90.57%
Minyak jarak netral 935.00 88.21%
Metanol 171.80
KOH 16.29
Metil ester 826.74 77.99%
Gliserol 199.30 18.80% 3.20 %
Proses transesterifikasi dua tahap
Keterangan gram Yield (b/b MJK) Loss
Minyak jarak kasar (MJK) 1060.00
Minyak jarak didegumming 960.00 90.57%
Minyak jarak netral (MJN) 935.00 88.21%
Metanol 171.80
KOH 16.29
Metil ester 750.46 70.80%