INSTITUT PERTANIAN BOGOR
BOGOR
Jati belanda, jambu biji, dan temulawak merupakan tumbuhan obat
tradisional yang telah digunakan sebagai antioksidan. Penggunaan tumbuhan
tersebut sebagai antioksidan masih terbatas pada masing1masing tumbuhan saja,
sedangkan potensi antioksidasi ketiga tumbuhan tersebut dalam bentuk ramuan
belum dilakukan. Penelitian ini bertujuan untuk mendapatkan informasi potensi
antioksidasi dari ramuan daun jati belanda, serta menetukan konsentrasi lipid
peroksida hati tikus hiperlipidemia yang diberi ramuan ekstrak daun jati belanda
yang mengandung daun jambu biji dan rimpang temulawak.
Ramuan daun jati belanda yang terdiri dari daun jambu biji dan rimpang
temulawak diekstraksi dengan pelarut etanol 70% secara maserasi. Hasil ekstraksi
digunakan untuk menentukan konsentrasi lipid peroksida hati dari tikus yang
hiperlipidemia. Konsentrasi lipid peroksida hati diukur menggunakan uji TBA.
Jati belanda, guavas, and temulawak are traditional herbs that has been
widely used as antioxidant. The use of those as antioxidant were limited to the
single plants one each, while potency of those plants in potions had not been
known. This research aims to provide informations related to the antioxidant
potency of jati belanda leaf potions, also to determine lipid peroxidation
concentration of hyperlipidemic rat liver which were given by potion containing
jati belanda leaves, guava leaves, and temulawak extracts.
Potions of jati belanda leaves, guava, and temulawak rhizome, were
extracted with ethanol 70% by maceration. Filtrate were used to measure lipid
peroxide concentration in hyperlipidemic rat liver. The concentration was
measured by TBA test.
NIM
: G44102028
Disetujui
Komisi Pembimbing
Dr.Anna P. Roswiem, MS.
drh. Sulistiyani, M.Sc.,PhD
Ketua
Anggota
Diketahui
Dekan Fakultas Matematika dan Ilmu Pengetahuan Alam
Institut Pertanian Bogor
Prof. Dr. Ir. Yonny Koesmaryono, M.S.
NIP 131 473 999
pada Program Studi biokimia Fakultas Matematika dan Ilmu Pengetahuan Alam.
Penelitian dilaksanakan selama bulan Juli1November 2006 dengan judul Khasiat
Ramuan Ekstrak
Daun Jati Belanda terhadap Peroksidasi Lipid Hati
Hiperlipidemia.
Ucapan terima kasih penulis tujukan kepada semua pihak. Terima kasih
penulis ucapakan kepada para pembimbing penulis Dr. Anna P. Roswiem, MS,
dan drh. Sulistiyani, M.Sc.,PhD atas bimbingan dan dorongannya selama ini.
Tidak lupa juga penulis ucapkan terima kasih kepada teman seperjuangan Yayu,
Icha, Meta, Indri, Liga, Aan, Fitri, khususnya Mba Itin atas bantuannya selama
penelitian, Chandra, Emi, Dinar dan Feni. Ucapan terima kasih juga disampaikan
kepada bapak, dan ibu tercinta, serta seluruh keluarga, atas segala doa dan kasih
sayangnya.
Semoga karya ilmiah ini dapat bermanfaat.
Tahun 2002, penulis lulus dari SMU Negeri 52 Jakarta dan pada tahun yang
sama lulus masuk Institut Pertanian Bogor (IPB) di Departemen Biokimia
Fakultas Matematika dan Ilmu Pengetahuan Alam melalui jalur Undangan Seleksi
Masuk IPB (USMI).
Selama mengikuti perkuliahan, penulis menjadi asisten praktikum mata
kuliah Biokimia Fisik S1 Biokimia tahun ajaran 2005/2006, Biokimia Umum S1
Kimia 2005/2006, Biokimia Umum D3 Perikanan 2005/2006 dan 2006/2007,
Biokimia Umum S1 Biologi 2006/2007, dan Biokimia Akademi Perawat
2006/2007. Pada tahun 2005 penulis melaksanakan praktik lapangan di
Laboratorium Treub, Bidang Botani Pusat Penelitian Biologi LIPI Bogor selama
bulan Juli1Agustus dengan tema Penapisan Fitokimia dan Penentuan Nilai
PENDAHULUAN ...
1
TINJAUAN PUSTAKA
Peroksidasi Lipid ...
2
Hiperlipidemia dan Lipid Peroksida ...
3
Bahan1bahan Alami Antioksidan ...
4
BAHAN DAN METODE
Bahan dan Alat ...
7
Metode Penelitian ...
7
Analisis Data ...
8
HASIL DAN PEMBAHASAN
Keadaan Awal dan Bobot Badan Hewan Coba ...
9
Perbandingan Konsentrasi Lipid Peroksida Hati Tikus Normal dengan
Tikus Hiperlipidemia ... 10
Pengaruh Ekstrak Ramuan Daun Jati Belanda Terhadap Konsentrasi
Lipid Peroksida Hati ... 11
Korelasi antara Lipid Peroksida Hati dan Kolesterol Hati serta TPC ... 12
SIMPULAN DAN SARAN ... 13
DAFTAR PUSTAKA ... 14
2 Reaksi antara TBA dan MDA ...
3
3 Tumbuhan jati belanda (
Lamk.) ...
5
4 Tumbuhan jambu biji (
Linn.) ...
6
5 Tanaman temulawak (
Roxb.) ... 7
6 Perubahan bobot badan tikus selama perlakuan ...
9
7 Kenaikan konsentrasi kolesterol selama induksi kolesterol ... 10
8 Perbandingan konsentrasi lipid peroksida hati kelompok normal dengan
kelompok hiperlipidemia ... 10
9 Konsentrasi Lipid peroksidasi lipid hati ... 12
10 Korelasi antara konsentrasi kolesterol hati dan konsentrasi lipid peroksida
hati ... 13
dan PTU ... 18
3 Hasil kurva standar TMP ... 19
4 Perubahan rata1rata bobot badan tikus selama percobaan ... 20
5 Data konsentrasi lipid peroksida hati saat peningkatan kolesterol pada
minggu ke19 ... 20
6 Data konsentrasi lipid peroksida hati diakhir perlakuan pada
minggu ke114 ... 20
7 Data konsentrasi kolesterol hati ... 21
10 Analisis statistik rancangan acak lengkap ... 22
11 Hasil analisis korelasi antara lipid peroksida hati dan kolesterol hati
Indonesia merupakan negara kepulauan yang kaya akan sumber daya alamnya. Negara ini dikenal sebagai negara
terbesar nomor dua di dunia setelah Brasil.
Kekayaan hayati Indonesia yang sudah
dimanfaatkan nenek moyang sejak dahulu kala, sampai saat ini masih berpotensi untuk dikembangkan. Diperkirakan sumber daya hayati yang dimiliki Indonesia berkisar antara 30 000140 000 spesies tumbuhan. Berdasarkan jumlah tersebut terdapat sebesar 1 100 spesies tumbuhan yang dapat digunakan sebagai obat tradisional. Tumbuhan yang dapat digunakan sebagai obat tradisional antara lain adalah jati belanda, jambu biji, dan temulawak (Heyne 1987).
Masyarakat tradisional biasanya
menggunakan tumbuhan daun jati belanda sebagai obat pelangsing, obat diare, batuk dan nyeri perut (Heyne 1987). Daun Jambu biji sebagai antibakteri, antidiabetes, dan maag,
sedangkan rimpang temulawak sebagai
antiradang, antibakteri, dan memperlancar pengeluaran ASI (Dalimartha 2002). Selain itu berdasarkan penelitian sebelumnya daun jati belanda, daun jambu biji, dan rimpang
temulawak memiliki aktivitas sebagai
antioksidan. Hasil penelitian Tombilangi (2004) menginformasikan bahwa pemberian ekstrak etanol daun jati belanda mampu menurunkan konsentrasi lipid peroksida
dalam darah secara nyata dibandingkan
dengan kelompok hiperlipidemia. Indriani (2006) melaporkan bahwa ekstrak etanol daun jambu biji putih dapat menghambat oksidasi
lipid sebesar 94.19%. Adji (2004)
menyebutkan bahwa ekstrak etanol rimpang temulawak mampu mencegah peningkatan konsentrasi lipid peroksida dalam darah sebesar 64.30% terhadap kondisi awal.
Dewasa ini, perkembangan zaman dan arus globalisasi dapat mempengaruhi gaya hidup dan pola makan masyarakat Indonesia
yang cenderung mengkonsumsi makanan
cepat saji. Hal ini dapat menyebabkan
timbulnya penyakit degeneratif. Penyakit
degeneratif ini dapat disebabkan oleh
meningkatnya proses peroksidasi lipid akibat molekul radikal bebas di dalam tubuh.
Salah satu penyakit degeneratif yang disebabkan oleh radikal bebas adalah penyakit
jantung koroner (PJK). Penyakit ini
disebabkan oleh penyempitan, penyumbatan, atau kelainan pembuluh nadi koroner yang dikenal sebagai aterosklerosis. Aterosklerosis ini disebabkan oleh tingginya kolesterol LDL
( ) di dalam pembuluh
darah arteri akibat kurangnya reseptor LDL
dalam mengambil lipoprotein yang
mengandung kolesterol. Semakin
meningkatnya konsentrasi kolesterol LDL di dalam jaringan maka semakin besar pula jumlah kolesterol LDL yang akan dioksidasi.
Untuk mengurangi lipid peroksida di dalam tubuh diperlukan suatu senyawa yang dapat mencegah proses peroksidasi lipid.
Senyawa yang mampu menghambat
kerusakan lipid akibat radikal bebas adalah antioksidan. Di dalam tubuh manusia sendiri
mampu mensintesis senyawa antioksidan
seperti superoksida dismutase (SOD),
glutathion peroksidase, dan katalase. Namun dengan bertambahnya usia, terjadi penurunan enzim1enzim tersebut, sehingga radikal bebas baik dari dalam maupun luar tubuh tidak sepenuhnya dapat ditangani. Oleh sebab itu, tubuh perlu senyawa antioksidan yang berasal dari luar (eksogen).
Saat ini, semakin mahalnya harga obat1 obatan sintetik di pasaran menyebabkan
masyarakat Indonesia cenderung
memanfaatkan bahan1bahan alami terutama yang berasal dari tumbuh1tumbuhan. Selain memiliki harga yang lebih murah, obat1obatan tradisional juga memiliki efek samping lebih
kecil dibandingkan dengan obat1obatan
sintetik, serta mudah didapat. Jati belanda,
jambu biji, dan temulawak merupakan
tumbuhan obat tradisional yang telah
digunakan sebagai antioksidan. Namun
penggunaan ketiga tumbuhan tersebut sebagai antioksidan masih terbatas pada masing1 masing tumbuhan saja, sedangkan potensi antioksidasi ketiga tumbuhan tersebut dalam
bentuk ramuan belum dibuktikan secara
ilmiah. Penelitian ini adalah bagian dari penelitian yang bekerjasama dengan industri fitofarmaka yang akan mengkaji formulasi
ramuan ketiga tumbuhan tersebut dalam
kaitannya sebagai antioksidan.
Penelitian bertujuan untuk mendapatkan informasi potensi antioksidasi dari ramuan
daun jati belanda, serta menentukan
ramuan daun jati belanda dengan daun jambu
biji dan rimpang temulawak sebagai
antioksidan.
!"#$%& $% %'%&
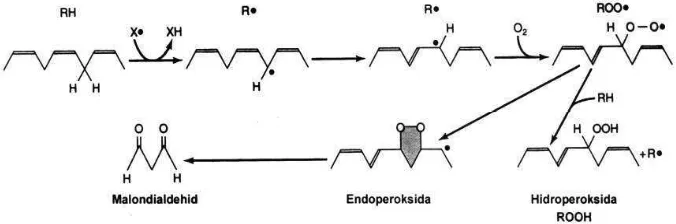
Lipid merupakan salah satu molekul yang paling sensitif terhadap serangan radikal bebas, sehingga terbentuk lipid peroksida. Peroksidasi lipid adalah reaksi yang terjadi akibat serangan radikal bebas terhadap asam lemak tak jenuh majemuk (Polyunsaturated fatty Acid, PUFA) (Halliwel & Gutteridge 1999). Radikal bebas ini sangat labil dan bersifat reaktif sehingga cenderung bereaksi seketika dengan setiap zat disekitarnya.
Peroksidasi lipid merupakan suatu rantai reaksi yang berlangsung terus menerus, sebab reaksi ini menghasilkan radikal lipid bebas
(R*) yang lain, sehingga peroksidasi
berlangsung lebih lanjut. Pada umumnya, peroksidasi lipid dapat dibagi menjadi tiga tahap reaksi yaitu tahap inisiasi, propagasi, dan terminasi (Murray 2001).
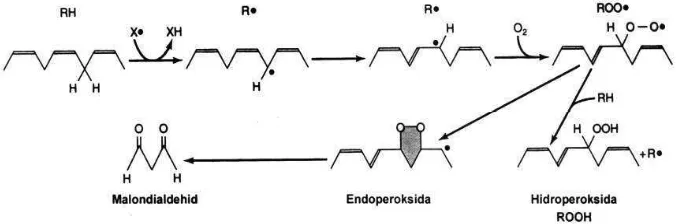
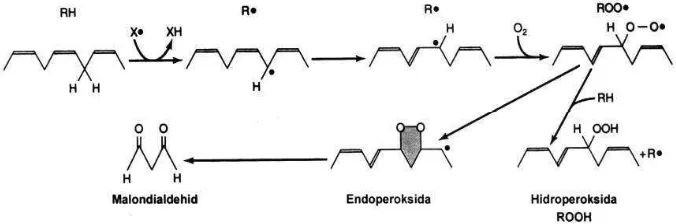
Reaksi peroksidasi lipid diawali melalui pengambilan sebuah atom hidrogen dari gugus metilena (1CH21) pada PUFA oleh radikal
bebas. Pada tahap ini, terjadi pembentukan radikal bebas karbon (1FCH1) yang disebabkan oleh penghilangan satu atom H pada CH2. Hal
ini disebabkan adanya ikatan rangkap pada asam lemak yang dapat melemahkan ikatan antara atom C dan H yang berdekatan dengan ikatan rangkap, sehingga atom H mudah diambil oleh radikal bebas.
Tahap selanjutnya yaitu penstabilan radikal bebas karbon melalui penataan ulang ikatan rangkap, sehingga terbentuk diena
terkonjugasi. Apabila diena terkonjugasi bereaksi dengan O2, maka akan terbentuk
radikal lipid peroksida (ROO*). Hadirnya radikal peroksida ini dapat memudahkan pengambilan atom hidrogen dari molekul lipid lain, sehingga tahap ini disebut sebagai tahap propagasi. Radikal peroksida selanjutnya dapat bergabung dengan atom H yang lain membentuk lipid hidroperoksida dan radikal bebas yang baru. Jalur lain yang ditempuh
oleh radikal peroksida yaitu dengan
membentuk peroksida siklik yang disebut
dengan endoperoksida. Tahap terminasi
terjadi jika radikal lipid peroksida bereaksi dengan radikal bebas yang lain seperti senyawa antioksidan atau senyawa biologi seperti protein. Proses peroksidasi asam lemak tak jenuh dapat dilihat pada Gambar 1.
Lipid peroksida atau lipid hidroperoksida merupakan suatu molekul yang stabil pada suhu fisiologis atau suhu tubuh. Namun, ion1 ion logam transisi yang terdapat di dalam tubuh seperti besi (Fe) dan tembaga (Cu)
dapat mengkatalisis penguraian lipid
hidroperoksida hingga membentuk produk yang berbahaya seperti epoksida, keton, asam, dan aldehid. Dua diantara sejumlah aldehid yang dihasilkan dari peruraian peroksida
adalah malondialdehida (MDA) dan 41
hidroksinonenal. Kedua produk aldehid
tersebut dapat menyerang protein terutama pada gugus tiol (1SH) dan gugus amin (1NH2),
sehingga enzim1enzim yang membutuhkan
senyawa1senyawa tersebut untuk akivitasnya akan terhambat bila peroksidasi lipid sedang berlangsung (Sulistyo 1998). Peroksidasi lipid yang disebabkan oleh radikal bebas ini dapat menyebabkan membran kehilangan fluiditas, dan gangguan transport (O’Brien 1981, diacu dalam Widyarti 1995).
Gambar 1 Reaksi pembentukan MDA dari peroksidasi rantai hidrokarbon berikatan ganda.
Organ hati merupakan pusat dari metabolisme dalam sebagian besar hewan. Organ ini berfungsi dalam proses detoksifikasi senyawa1senyawa toksik, sekresi produk akhir metabolisme seperti bilirubin, amonia, dan urea, hematologik, sistem imun tubuh, serta
berperan dalam proses metabolisme
biomolekul (protein, karbohidrat, hormon, dan bilirubin) (Kaplan & Pesce 1989). Membran1
membran mikrosom hati sangat rentan
terhadap peroksidasi lipid, sebab membran ini banyak sekali mengandung asam lemak tak jenuh. Proses peroksidasi lipid pada mikrosom hati dapat berlangsung secara enzimatis dan
nonenzimatis. Secara enzimatis yaitu
peroksidasi lipid yang bergantung oleh
NADPH, sedangkan secara nonenzimatis
yaitu peroksidasi lipid yang bergantung oleh
ion Fe3+, ion ini berfungsi sebagai
pengkompleks ADP, pirofosfat, dan EDTA (Halliwel & Gutteridge 1999).
Tingginya konsentrasi lipid peroksida dapat menjadi indikasi awal rusaknya sel hati. Peningkatan konsentrasi lipid peroksida lebih jauh dapat menyebabkan terjadinya nekrosis hati. Yagi (1994) menyatakan bahwa apabila konsentrasi lipid peroksida di hati meningkat, maka lipid peroksida ini dapat merusak sel hati sehingga peroksida akan keluar dari hati menuju pembuluh darah dan dapat merusak organ atau jaringan lain. Konsentrasi lipid
peroksida yang berlebih pada jaringan
maupun organ dapat mengakibatkan berbagai
penyakit degeneratif. Di dalam tubuh
manusia, kadar lipid peroksida dapat
meningkat seiring dengan bertambahnya usia, namun jumlahnya tidak boleh melebihi kadar normalnya yaitu 4 nmol/mL (Yagi 1994).
Berdasarkan penelitian Sayogya (2002)
menunjukkan konsentrasi lipid peroksida hati
normal tikus galur sebesar
100.46 nmol/g, sedangkan lipid peroksida normal dalam serum darah galur
sebesar 0.46±0.05 ng/mL (Adji 2004). Berdasarkan kedua hasil penelitian tersebut
dapat dilihat bahwa konsentrasi lipid
peroksida hati lebih besar dari pada
konsentrasi lipid peroksida di dalam serum darah.
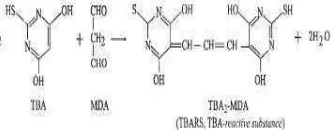
Uji TBA (asam 21tiobarbiturat) dapat digunakan untuk mengukur konsentrasi dari lipid peroksida yang terakumulasi secara
di dalam organ dan partikel subseluler (Tappel & Zalkin 1960). Uji TBA didasarkan pada reaksi asam 21tiobarbiturat dengan produk oksidasi lipid (MDA). TBA akan bereaksi dengan gugus karbonil dari MDA yaitu satu molekul MDA akan berikatan
dengan dua molekul TBA, sehingga
membentuk senyawa kompleks berwarna
merah (Halliwel & Gutteridge 1999). Warna merah yang diukur dengan spektofotometer
pada panjang gelombang 532 nm ini
menunjukkan tingkat oksidasi lipid. Reaksi penggabungan antara TBA dan MDA dapat
dilihat pada Gambar 2. Uji TBA ini
merupakan uji yang spesifik untuk hasil oksidasi asam lemak tak jenuh dan baik diterapkan untuk uji terhadap lemak pangan yang mengandung asam lemak tak jenuh (Ketaren 1986).
Gambar 2 Reaksi antara TBA dan MDA. Sumber: Halliwel & Gutteridge (1999)
%' ! %'%& % & %'%& !"#$%&
Hiperlipidemia merupakan suatu keadaan tingginya konsentrasi lipid yang ditandai dengan meningkatnya konsentrasi trigliserida, LDL, dan kolesterol (lipid netral) darah melebihi batas normal (pada manusia > 200 mg/dL) (Ganong 2001). Faktor1faktor yang dapat menyebabkan hiperlipidemia adalah bobot badan, usia, kurang olahraga, stres, gangguan metabolisme, gangguan genetik dan pola konsumsi makanan sehari1hari yang dapat meningkatkan konsentrasi lipid atau
kolesterol. Menurut Grundy (1991),
mengkonsumsi makanan yang kaya kolesterol
dan asam lemak jenuh dapat menekan
pembentukan reseptor LDL, sehingga
meningkatkan kolesterol di dalam darah.
Keadaan hiperlipidemia dapat
menyebabkan aterosklerosis yaitu
penyumbatan pembuluh darah arteri akibat penumpukan lipid pada dinding arteri. Jika aterosklerosis terjadi pada pembuluh darah arteri yang mensuplai O2 ke jantung, maka
dapat menyebabkan penyakit jantung koroner
(PJK). Salah satu faktor utama dalam
patogenesis aterosklerosis adalah
hiperkolesterolemia yang disebabkan oleh peningkatan konsentrasi lipoprotein densitas
rendah (LDL) (Schwartz 1993 diacu
dalam Taher 2003).
darah, VLDL mulai kehilangan kandungan trigliseridanya karena dihidrolisis oleh enzim lipoprotein lipase (LPL) menjadi asam lemak dan gliserol. Setelah trigliseridanya sebagian
besar dihidrolisis oleh LPL, VLDL ini
berubah menjadi lipoprotein densitas
menengah (IDL) dan akhirnya menjadi LDL. Selanjutnya LDL akan diendositosis oleh sel1 sel jaringan perifer dan hepatosit setelah terlebih dahulu diikat oleh reseptor LDL (Voet & Voet 1995).
Aterosklerosis biasanya lebih banyak diderita oleh pria daripada wanita yang masih
aktif haid. Hal ini disebabkan hormon
esterogen yang memiliki aktivitas antioksidan yang dapat menghambat terjadinya oksidasi LDL (Rifici & Khachadurian 1992 diacu
dalam Taher 2003). Selain itu hormon
esterogen juga diketahui dapat menghambat perkembangan awal aterosklerosis dengan mengurangi pembentukkan sel busa makrofag,
yaitu dengan mengurangi penangkapan
lipoprotein melalui lintas reseptor pembersih (Sulistyani 1997 diacu dalam Taher 2003).
Tingginya konsentrasi lipid peroksida di dalam tubuh dapat disebabkan oleh kondisi hiperkolesterolemia. Pada kondisi ini, jumlah LDL meningkat sehingga dapat memperbesar kemungkinan terjadinya oksidasi, sebab ketersediaan substrat yang dapat dioksidasi lebih banyak. Hal ini didukung oleh penelitian Tombilangi (2004) yang menyatakan bahwa pemberian kolesterol sebesar 0.25% dapat meningkatkan konsentrasi lipid peroksida
darah kelinci. Uphadya (2002) juga
melaporkan bahwa mencit yang diberi
kolesterol sebanyak 1.16% selama tujuh minggu mampu meningkatkan konsentrasi lipid peroksida lebih tinggi dibandingkan dengan mencit yang hanya diberi pakan standar. Menurut Iritani (1986), tikus yang diberi diet minyak jagung 10% nilai peroksidasi lipid dalam serum, hati dan jaringan adiposa lebih tinggi dari pada tikus dengan diet minyak jagung 5%.
Salah satu dari fungsi kolesterol adalah sebagai prekusor pembentukan asam empedu yang disintesis di dalam hati. Tahap pertama dalam biosintesis asam empedu adalah reaksi 7α1hidroksilasi terhadap kolesterol yang dikatalisis oleh enzim mikrosomal yaitu 7α1 hidroksilase. Proses reaksi ini memerlukan
oksigen, NADPH dan sitokrom P1450
oksidase. Semakin meningkatnya konsentrasi
kolesterol plasma dalam tubuh
hiperkolesterolemia, maka semakin banyak
asam empedu yang disintesis, sehingga
semakin meningkat pula oksigen dan NADPH
yang dibutuhkan serta peningkatan aktivitas sitokrom P1450 oksidase (Murray 2001).
Sitokrom P1450 oksidase merupakan
enzim yang berperan dalam memperantarai metabolisme retikulum endoplasmik yang menghasilkan radikal superoksida (O21)
(Dhaunsi 1992 diacu dalam Wresdiyati
2005). Oleh sebab itu semakin meningkatnya aktivitas sitokrom P1450 oksidase, maka
radikal bebas yang dihasilkan semakin
meningkat pula. Jika produksi radikal bebas
terjadi secara berlebihan maka enzim
antioksidan di dalam tubuh khususnya di organ hati seperti superoksida dismutase (SOD) tidak mampu mengatasinya. Hal ini dapat menimbulkan kondisi stres oksidatif yaitu suatu kondisi yang dapat menyebabkan tejadinya beberapa kerusakan atau kelainan baik proses biokimia maupun fisiologi di dalam sel akibat dari proses peroksidasi lipid.
Kondisi hiperlipidemia dapat dibuat pada beberapa spesies hewan percobaan yaitu dengan menambahkan lemak dan kolesterol pada makanan yang disebut induksi eksogen (Amstrong & Heistad 1990). Menurut panduan dari KKI Phyto Medica (1993) induksi hiperlipidemia pada tikus dapat dilakukan dengan pemberian pakan tinggi kolesterol (1%) dan propil tiourasil (PTU) (0.01%)selama dua minggu. PTU merupakan zat antitiroid yang dapat merusak kelenjar tiroid. Kerusakan kelenjar tiroid ini dapat
menyebabkan meningkatnya konsentrasi
kolesterol akibat pembentukan reseptor LDL di hati berkurang (Ganong 2001).
( )* ( % +%"#$%&
Dewasa ini, masyarakat Indonesia
cenderung menggunakan bahan1bahan alami terutama tumbuhan obat tradisional dalam
memelihara kesehatannya. Dengan
mengkonsumsi bahan alami dan gizi
seimbang, diharapkan dapat mencegah atau
mengurangi radikal bebas yang dapat
menyebabkan penyakit degeneratif seperti
PJK dan ! . Bahan1bahan alami yang
biasa digunakan sebagai antioksidan dapat berasal dari buah1buahan seperti apel, anggur, jeruk sayur1sayuran seperti brokoli, wortel ataupun yang berasal dari tumbuh1tumbuhan seperti teh hijau. Pada penelitian ini bahan
alami yang akan digunakan sebagai
+% & , #-.
Jati Belanda merupakan tumbuhan yang berasal dari negara Amerika beriklim tropis. Tumbuhan ini juga tumbuh secara liar di wilayah tropis lainnya seperti di pulau Jawa dan Madura. Jati belanda atau jati londo (Jawa Tengah) tumbuh baik pada daerah dengan ketinggian 11800 m di atas permukaan laut. Klasifikasi dari tumbuhan jati belanda yaitu
divisi Spermatophyta, subdivisi
Angiospermae, kelas Dicotyledonae, bangsa
Malvales, suku Steruliaceae, marga ,
dan jenis Lamk.
Tumbuhan jati belanda berupa pohon peneduh di tepi jalan dengan tinggi 10120 meter. Memiliki batang berbentuk bulat, keras, permukaannya kasar, banyak alur, bercabang, dan berwarna hijau keputih1 putihan. Daun berbentuk bundar bulat sampai lanset, ujung daun lancip, serta permukaan daun bagian atas berbulu. Berbunga banyak, bentuk bunga agak ramping, serta memiliki mahkota bunga yang berwana kuning. Bijinya kecil, keras, diameter ± 2 mm, berwarna coklat muda, serta memiliki akar tunggang (Sugati 1991). Bentuk daun jati belanda dapat dilihat pada Gambar 3.
Daun dan kulit batang jati belanda
mengandung alkaloid, serta flavonoid, selain itu daunnya mengandung saponin dan tanin. Menurut Soesilo (1989) daun jati belanda
mengandung senyawa flavonoid, asam
fenolat, tanin, steroid atau triterpenoid, dan karotenoid. Hal ini didukung dari hasil
penelitian Tombilangi (2004) yang
menunjukkan bahwa ekstrak etanol daun jati belanda mengandung flavonoid.
Daun jati belanda berkhasiat sebagai obat
pelangsing tubuh, sehingga simplisia
tumbuhan ini banyak digunakan di dalam ramuan galian singset. Hal ini didukung oleh penelitian Lestari dan Muhtadi (1997) yang menunjukkan bahwa pemberian ekstrak etanol daun jati belanda sebanyak 1g/Kg bobot
badan tikus yang hiperlipidemia mampu
menurunkan kadar kolesterol. Namun, hasil penelitian yang dilakukan Rachmadani (2001) menunjukkan bahwa tikus yang diberi ekstrak air daun jati belanda sebanyak 1 g/Kg bobot badan tidak menunjukan penurunan kadar kolesterol.
Pemakaian rebusan daun jati belanda secara berlebihan dapat mengakibatkan iritasi usus, sedangkan pemakaian biji tumbuhan jati
belanda secara berlebihan dapat
mengakibatkan diare atau radang usus
(Sastroamidjojo 1988). Rebusan biji
tumbuhan jati belanda yang dibakar dapat
digunakan sebagai obat sembelit, sedangkan jika dicampur dengan minyak adas dapat digunakan untuk penyakit perut kembung dan sesak nafas. Biasanya rebusan biji tumbuhan ini digunakan oleh masyarakat dengan cara meminumnya seperti meminum kopi (Heyne 1987).
Gambar 3 Tumbuhan jati belanda
( Lamk.).
*/ %0% , %
-Jambu biji adalah salah satu tumbuhan buah perdu yang dalam bahasa Inggris disebut
" . Tanaman ini berasal dari
Brazilia Amerika Tengah, menyebar ke
Thailand kemudian ke negara Asia lainnya seperti Indonesia. Nama lain dari jambu biji yaitu Petokal, Tokal (Jawa), Sotong (Bali), dan Glima breuh (Aceh). Klasifikasi dari
tumbuhan jambu biji yaitu divisi
Spermatophyta, subdivisi Angiospermae, kelas Dicotyledonae, bangsa Myrtales, suku
Myrtaceae, marga , dan jenis
L
Tumbuhan jambu biji dapat tumbuh di daerah tropis maupun di daerah subtropik dengan intensitas curah hujan yang diperlukan berkisar 100012000 mm/tahun dan merata
disepanjang tahun. Tumbuhan ini dapat
tumbuh di daerah tropis pada ketinggian antara 511200 meter di atas permukaan laut. Jambu biji termasuk tumbuhan semak atau pohon yang memiliki ketinggian 3110 meter. Tumbuhan ini memiliki banyak cabang dan ranting, batang pohonnya keras, permukaan kulit luar berwarna coklat dan licin. Daunnya berbentuk bulat telur, bertulang menyirip, serta berwarna hijau kekuningan. Bunganya kecil1kecil berwarna putih dan memiliki akar tunggang, seperti terlihat pada Gambar 4. (Soesilo 1989).
Senyawa kimia yang terkandung di dalam jambu biji antara lain polifenol dan tanin.
Daun dan kulit batangnya mengandung
saponin, tanin dan minyak atsiri. Selain itu daunnya mengandung asam ursolat, asam psidiolat, asam katogolat, asam oleanolat, asam gujaverin dan vitamin C. Vitamin C pada buah jambu biji sebesar 316 kali lebih
besar dibandingkan buah jeruk. Adanya
dalam melawan bakteri (Triarsari 2006). Hal ini didukung oleh penelitian Khan
(1980) Soesilo (1989) yang
menunjukkan bahwa daun jambu biji
berkhasiat sebagai antibakteri terhadap .
Selain itu, Indariani (2006) menyatakan bahwa jambu biji juga memiliki aktivitas antioksidan yang erat khasiatnya dalam
mengobati berbagai penyakit. Hasil
penelitiannya menunjukkan bahwa ekstrak daun jambu biji putih lokal memiliki faktor protektif mendekati vitamin E (α1tokoferol) sebesar 1.0, sedangkan α1tokoferol sendiri memiliki faktor protektif sebesar 1.16. Ekstrak etanol daun jambu biji putih lokal juga dapat menghambat oksidasi lipid sebesar 94.19%.
Hasil penelitian Lestariana (2005)
melaporkan bahwa pemberian ekstrak kering daun jambu biji sebanyak 2 mg dalam 0.2 mL air yang diberikan 1 kali, 2 kali, dan 3 kali sehari selama 90 hari dapat memberikan
penurunan yang bermakna terhadap
konsentrasi glukosa darah tikus. Namun, menunjukkan perbedaan yang tidak bermakna
terhadap konsentrasi kolesterol dan
trigliserida serum darah tikus.
Selain sebagai antibakteri dan antioksidan, jambu biji juga berkhasiat sebagai antidiare, antiinflamasi, antimutagenik, analgesik, penyakit diabetes melitus, serta maag (Soesilo 1989). Pada umumnya, dosis penggunaan daun jambu biji yang sering dipakai oleh masyarakat adalah sebesar 15130 g. Untuk pengobatan, biasanya daun jambu biji ini direbus selama 15 menit, kemudian air hasil
rebusan dari tumbuhan ini diminum
(Wijayakusumah 1993).
Gambar 4 Tumbuhan jambu biji
( Linn.
/ 1 # , "2*-.
Temulawak merupakan tanaman asli
Indonesia yang memiliki khasiat obat.
Tanaman ini dapat tumbuh baik di dataran rendah pada ketinggian 1500 meter di atas permukaan laut (Syukur & Hernani 2002). Tanaman temulawak banyak ditemukan di
hutan1hutan daerah tropis serta tersebar luas di daerah Jawa, Maluku, dan Kalimantan. Selain di Indonesia tanaman ini juga ditemukan di India (Harida/Haldi), Bengali (halud), Arab (kurkum), Persia (zardehobach), dan Cina (ilang1hoang). Sejak dulu oleh masyarakat Indonesia, tanaman ini digunakan untuk meningkatkan nafsu makan, sembelit, sakit kepala, sakit perut bahkan dipercaya sebagai
jamu yang dapat memperlambat proses
penuaan, menghilangkan bintik1bintik hitam di wajah serta kelenturan tubuh.
Temulawak tergolong dalam famili
Zingiberaceae. Ciri khas dari tanaman ini yaitu memiliki rimpang yang berbau aromatik
tajam dan rasanya pahit agak pedas
(Dalimartha 2002). Nama lain dari tanaman ini yaitu temu putih (Indonesia), koneng gede
(Sunda), serta temu labak (Madura).
Klasifikasi dari temulawak yaitu divisi Spermatophyta, subdivisi Angiospermae, kelas Monocotyledonae, bangsa Zingiberales,
suku Zingiberaceae, marga , dan
genus Roxb.
Tanaman ini termasuk jenis tumbuhan herba yang batang pohonnya berbentuk batang semu serta tingginya mencapai 2 meter bahkan lebih. Daun tanaman ini berbentuk lanset, warnanya hijau tua dengan jari1jari coklat dibagian tulang daunnya. Pada bagian
tengah daun berwarna ungu. Bunga
temulawak bersifat lateral. Tangkai bunga ramping dan berbulu dengan panjang 4137 cm. Rimpangnya berukuran besar, bercabang1 cabang, berwarna kuning tua atau kecoklatan,
beraroma tajam, dan rasanya pahit
(Dalimartha 2002). Tanaman ini dapat dilihat pada Gambar 5.
Rimpang temulawak terdiri atas fraksi pati, kurkuminoid, dan minyak atsiri. Fraksi
kurkuminoid merupakan komponen yang
dapat memberi warna kuning pada rimpang
temulawak. Zat warna kuning yang
terkandung di dalam rimpang temulawak ini sebesar 112% yang terdiri atas kurkumin dan
monodesmetoksi1kurkumin. Senyawa
kurkumin yang terkandung di dalam rimpang
temulawak mempunyai khasiat sebagai
antibakteri dan merangsang dinding kantong empedu untuk mengeluarkan cairan empedu ke usus, antiradang, peluruh kencing serta mempelancar pengeluaran ASI (Dalimartha 2002). Selain itu, temulawak juga digunakan sebagai pengobatan gangguan hati, batu empedu, sembelit, obat luka, dan kulit
(Darwis 1991). Budhidjaya (1988)
tween 80 dan air dapat menurunkan kadar kolesterol total dan trigliserida darah, sedangkan pada dosis 20 mg dapat menaikkan HDL1kolesterol kelinci yang hiperlipidemia.
Masyarakat Indonesia pada umumnya
menggunakan tumbuhan ini dengan cara memarut 20 g rimpang temulawak segar, lalu
menyeduhnya, dan air hasil seduhannya
diminum (Dalimartha 2002).
Senyawa aktif kurkumin memiliki
aktivitas sebagai antioksidan dan
imunomodulator. Namun, jika temulawak
diminum bersamaan dengan obat elektrofilik seperti parasetamol dapat beresiko tinggi bagi
organ tubuh, sebab selain sebagai
imunomodulator senyawa ini juga dapat
menghambat aktivitas enzim glutation1s1 transferase (GST) di dalam tubuh. Hal ini
dapat menyebabkan terganggunya proses
didetoksifikasi parasetamol di dalam tubuh (Martono 2006). Berdasarkan penelitian Adji (2004) menunjukan bahwa ekstrak etanol 75% temulawak dengan dosis 100 mg/Kg BB mampu mencegah peningkatan konsentrasi lipid peroksida serum darah secara nyata dibandingkan dengan kontrol positif.
Gambar 5 Tanaman temulawak ( Roxb.).
( & +
Hewan uji yang digunakan adalah tikus
putih dewasa galur , berjenis
kelamin jantan, sehat, berumur 2 bulan dan memiliki berat badan sekitar 200 g. Tikus ini diperoleh dari PT Indo Anilab dan Fakultas Peternakan Institut Pertanian Bogor. Bahan1 bahan yang digunakan dalam penelitian ini adalah hati tikus, ekstrak ramuan daun jati belanda yang mengandung daun jambu biji, dan rimpang temulawak yang diperoleh dari Pusat Studi Biofarmaka (PSB) LPPM IPPB. Bahan untuk uji TBA antara lain NaCl dingin 0.9%, KCl dingin 1.15%, sodium dodesil sulfat (SDS) 8.1%, NaOH 1M, asam asetat 20%, asam tiobarbiturat (TBA) 1.0% dalam
pelarut asam asetat 50%, akuades, n1
butanol:piridin (15:1 v/v), serta 1,1,3,31
tetrametoksi propana (TMP) sebagai larutan standar. Bahan1bahan lainnya seperti pakan standar, pakan kolesterol (kuning telur, lemak kambing, minyak goreng curah, dan pakan standar), dan propil tiourasil (PTU) 0.01%.
Alat1alat yang digunakan antara lain mikropipet, neraca analitik, sentrifus (Hettich Universal), pengaduk magnetik, vorteks,
penangas air, oven, pH1meter,
spektofotometer UV1VIS, sonde, siring,
gunting, pinset, .
+"& %+%
*/ + #$+! # / / +% &
Daun jati belanda, daun jambu biji, dan rimpang temulawak yang telah dicuci bersih
dikeringkan dalam oven pada suhu 60 .
Selanjutnya, daun jati belanda, daun jambu biji, dan rimpang temulawak yang telah kering diekstraksi dengan pelarut etanol 70% secara maserasi. Lalu hasil maserasi diuapkan
dengan . Campuran ekstrak
etanol daun jati belanda, daun jambu biji, dan rimpang temulawak dibuat sesuai dengan formulasi yang ditetapkan oleh PSB.
"$%$ ( % 3 4 %4/ #
Dosis ekstrak ramuan daun jati belanda yang mengandung daun jambu biji dan rimpang temulawak yang akan diberikan pada
kelompok perlakuan I merupakan dosis
campuran dengan perbandingan (1x:1y:1z). Nilai koefisien satu adalah satu kali dosis efektif daun jati belanda, daun jambu biji, dan rimpang temulawak. Penggunaan dosis efektif
daun jati belanda adalah 1g/Kg BB
(Rachmadani 2001), sedangkan dosis efektif daun jambu biji dan rimpang temulawak adalah dosis yang telah ditentukan oleh mitra industri dan tidak bisa dilaporkan berkenaan
dengan rahasia perusahaan. Kelompok
perlakuan yang lain mendapatkan dosis yang merupakan variasi kelipatan dari masing1 masing dosis efektif.
1 "* & 5 4 !5"*
Sebelum mendapatkan perlakuan, tikus
diadaptasikan selama 2 minggu untuk
menyeragamkan cara hidup dan makannya. Tikus yang digunakan sebanyak 40 ekor yang dibagi menjadi 6 kelompok, masing1masing kelompok terdiri atas 10 ekor untuk kelompok
normal dan hiperlipidemia, sedangkan
kelompok perlakuan masing1masing 5 ekor
tikus. Untuk memperoleh kondisi
dengan memberikan pakan kolesterol dan larutan (0.01%) PTU dengan dosis 0.5 mg/Kg BB.
Kelompok I merupakan kelompok normal yaitu kelompok yang hanya diberi pakan standar selama percobaan dan dicekok dengan akuades untuk memperoleh kondisi stres yang
sama. Kelompok II yaitu kelompok
hiperlipidemia, sedangkan kelompok III, IV, V, dan VI merupakan kelompok perlakuan.
Kelompok hiperlipidemia dan kelompok
perlakuan merupakan kelompok yang
menerima pakan kolesterol dan dicekok
larutan (0.01%) PTU dengan dosis 0.5 mg/Kg BB selama delapan minggu percobaan. Pada satu minggu diakhir induksi hingga akhir penelitian kelompok hiperlipidemia dan perlakuan diberi pakan kolesterol yang mengandung lemak kambing 10% dan minyak goreng curah 1%, serta peningkatan dosis (0.01%) PTU menjadi dua kalinya. Selain mendapatkan pakan kolesterol, kelompok perlakuan juga dicekok campuran ekstrak etanol daun jati belanda, daun jambu biji dan rimpang temulawak dengan dosis campuran berturut1turut (1x:1y:1z), (2x:1y:1z), (1x:0y:1z), dan (1x:0y:0z) g/Kg BB selama
lima minggu setelah sembilan minggu
diinduksi kolesterol. Penimbangan bobot badan hewan coba dilakukan setiap satu
minggu selama perlakuan. Selanjutnya
analisis kolesterol total plasma darah dilakukan selama dua minggu sekali sampai minggu keempat induksi, dan selanjutnya dilakukan setiap satu minggu sekali selama perlakuan.
Analisis konsentrasi lipid peroksida hati awal dilakukan setelah sembilan minggu peningkatan kolesterol terhadap kelompok normal dan hiperlipidemia masing1masing sebanyak 5 ekor. Analisis konsentrasi lipid peroksida hati akhir dilakukan pada tiap1tiap kelompok setelah 5 minggu perlakuan.
*/ + '/ 4 / % 4 /!
Tepung kolesterol dibuat dari kuning telur ayam. Kuning telur yang telah dipisahkan dari putihnya, dikukus dengan air mendidih selama 30 menit. Lalu dalam keadaan masih panas
kuning telur digerus kasar, kemudian
dikeringkan dalam oven pada suhu 60170 ºC hingga kering (± 24 jam), sambil sekali1kali digerus hingga halus (Momuat 2001).
*/ + # " $+ !"
Pakan kolesterol dibuat dari 1.5%
kolesterol dari kuning telur ayam, 5% lemak kambing, 6% minyak goreng curah, dan pakan
standar sehingga mencapai 100%. Semua bahan1bahan tersebut dicampur hingga rata, dan dibuat dalam bentuk pelet. Jumlah pakan harian baik pakan kolesterol maupun pakan standar yang diberikan adalah 20g/ekor/hari dan air minum yang diberikan secara
"
4/#/! " $ +! $% %'%& !"#$%& , 4% 6778.
*/ + /!9 + & !- Kurva standar dibuat dengan menggunakan larutan stok pereaksi 1,1,3,31tetrametoksi propana (TMP) 6M yang diencerkan dengan akuades menjadi 0.1, 0.3, 0.5, 0.8, 1.0, 2.0, 3.0, 6.0, 9.0. 12, dan 14 NM. Larutan masing1masing konsentrasi dipipet sebanyak 4 mL ke dalam tabung reaksi. Lalu masing1masing tabung ditambah 1 mL TBA 1.0% dalam pelarut asam asetat 50%, dipanaskan di penangas air mendidih pada suhu 95 ºC selama 60 menit, kemudian didinginkan pada suhu kamar.
Selanjutnya pada masing1masing tabung
ditambahkan 1.0 mL akuades dan 5 mL n1 butanol:piridin (15:1 v/v), diaduk dengan vorteks, lalu disentrifugasi pada kecepatan 3000 rpm selama 15 menit. Lapisan atas yang
terbentuk pada larutan diambil, lalu
serapannya diukur pada panjang gelombang 532 nm dengan spektrofotometer.
%$%$ %'%& !"#$%&
+%-Pengukuran kadar lipid peroksida hati
dilakukan pada akhir perlakuan. Sebanyak 112 g hati disimpan dalam larutan NaCl dingin 0.9%. Dari hati segar tersebut dibuat 10% b/v homogenat hati dalam larutan KCl dingin
1.15%. Lalu diambil sebanyak 0.1 mL
homogenat ke dalam tabung reaksi.
Selanjutnya ke dalam tiap tabung
ditambahkan 0.2 mL SDS 8.1% dan 1.5 mL asam asetat 20%, serta diatur pHnya dari 2.5 menjadi pH 3.5 oleh NaOH 1 M dengan
menggunakan pH meter. Selanjutnya
ditambahkan 0.7 mL akuades dan 1.5 mL TBA 1.0% dalam pelarut asam asetat 50%, kemudian dipanaskan ke dalam penangas air mendidih pada suhu 95 ºC selama 60 menit, didinginkan pada suhu ruang. Lalu tiap tabung ditambahkan 1 mL akuades dan 5 mL n1 butanol:piridin (15:1 v/v), diaduk dengan vorteks, disentrifus pada kecepatan 4000 rpm selama 10 menit, diambil lapisan atasnya, diukur serapannya dengan spektrofotometer pada panjang gelombang 532 nm.
%$%$ +
Rancangan yang digunakan pada
(RAL). Analisis data dilakukan dengan
metode ANOVA ( ). Jika
terdapat perbedaan dalam perlakuan, maka dilakukan dengan uji Duncan. Model RAL
adalah sebagai berikut (Mattjik &
Sumertajaya 2000): Yij= N + τi+ εij
i = 1,2,…,t dan j = 1,2,…., r
Yij= Pengamatan pada pelakuan ke1i dan
ulangan ke1j
N = Rataan umum (overall mean)
τi =Pengaruh perlakuan ke1i, i = 1,2,3,4,5,6.
εij = Pengaruh galat acak pada perlakuan ke1i,
dan ulangan ke1j, j = 1,2,
Konsentrasi lipid peroksida hati pada tiap kelompok dikorelasikan dengan konsentrasi kolesterol hati dan kolesterol total (TPC)
menggunakan korelasi Pearson dengan
α=0.05.
& 1 & "*"+ & 1 "*
Hewan percobaan mula1mula
diadaptasikan selama dua minggu. Masa adaptasi tikus terhadap lingkungan ini
dilakukan untuk menghindari resiko
timbulnya gangguan stres dan untuk
mengamati kondisi tikus apakah masih dapat
terus dipergunakan selama percobaan.
Penimbangan hewan coba setiap satu minggu dilakukan untuk mengetahui kesehatan hewan coba selama berlangsungnya penelitian.
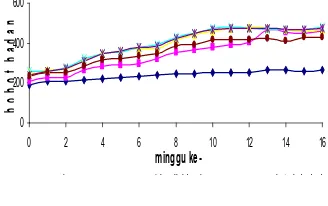
Perubahan bobot badan tikus selama
perlakuan terbagi menjadi dua yaitu masa adaptasi dan masa perlakuan. Selama masa penelitian bobot badan tikus cenderung meningkat seiring dengan bertambahnya usia tikus pada umur dua bulan (Gambar 6). Pemberian pakan kolesterol pada tikus selama penelitian, mampu meningkatkan bobot badan yang lebih besar dengan rata1rata konsumsi pakan perhari sebesar 17.90 g selama induksi dibandingkan dengan tikus yang diberi pakan standar dengan rata1rata konsumsi sebesar 15.01 g pada jumlah gram yang diberikan sebesar 20 g/ekor/hari. Setelah satu minggu peningkatan kolesterol, tikus yang diberi pakan kolesterol tinggi bobot badannya
meningkat sebesar 25% secara nyata
dibandingkan keadaan awal (kondisi hari ke1 nol yaitu bobot badan tikus pada saat pertama kali), sedangkan peningkatan bobot badan
kelompok tanpa pakan kolesterol hanya
meningkat sebesar 13% secara tidak nyata dibandingkan dengan keadaan awal. Hal ini
sesuai dengan pernyataan Ide (1978)
Kristiani (2003) bahwa pertumbuhan tikus dengan pakan mengandung lemak lebih besar dari pada tikus dengan diet bebas lemak. Lemak kambing dan minyak goreng curah yang terkandung di dalam pakan kolesterol kaya akan asam lemak jenuh. Asam lemak
jenuh merupakan prekusor dalam
pembentukan trigliserida. Trigliserida
merupakan simpanan lipid utama dalam
jaringan adiposa (Murray 2001).
Semakin banyak lemak yang dikonsumsi oleh tikus, maka semakin besar pula lipid yang tersimpan dalam jaringan adiposa sehingga bobot badan tikus menjadi lebih besar.
Selama pemberian ramuan ekstrak daun jati belanda yang terdiri atas daun jati belanda, daun jambu biji, dan rimpang temulawak terjadi penurunan bobot badan pada kelompok hewan coba yang diberi perlakuan ramuan ekstrak daun jati belanda (1x:1y:1z), ramuan ekstrak daun jati belanda yang mengandung daun jati belanda lebih banyak (2x:1y:1z), ramuan ekstrak daun jati belanda tanpa daun jambu biji (1x:0y:1z) masing1masing sekitar
0.67%, 1.2%, dan 0,67%, sedangkan
kelompok hewan coba yang diberi perlakuan ramuan ekstrak daun jati belanda tunggal (1x:0y:0z) mengalami kenaikan sekitar 1.54%
dibandingkan bobot badan satu minggu
sebelum diberi ekstrak. Meskipun demikian,
secara statistik bobot badan kelompok
perlakuan hingga akhir percobaan tidak berbeda nyata dibandingkan dengan kelompok hiperlipidemia (p>0.05) selama perlakuan.
Bila ditinjau dari jumlah pakan yang dikonsumsi, konsumsi pakan tikus kelompok hewan coba yang diberi ramuan ekstrak daun
Gambar 6 Perubahan bobot badan tikus selama perlakuan. Normal
( ), Hiperlipidemia ( ),
jati belanda, ramuan ekstrak daun jati belanda dengan daun jati belanda lebih banyak, ramuan ekstrak daun jati belanda tanpa daun jambu biji, dan ramuan ekstrak daun jati belanda tunggal selama pencekokan masing1 masing mengalami penurunan sekitar 29.25%, 27.28%, 24.92%, dan 28.37% dibandingkan dengan jumlah rata1rata konsumsi pakan selama peningkatan kolesterol. Meskipun demikian penurunan konsumsi pakan tidak mempengaruhi penurunan bobot badan tikus.
!* &% 4 " $ +! $% %'%& !"#$%& +% %#/$ "! & 4 %#/$
%' ! %'%& %
Banyak perlakuan yang dapat digunakan untuk menstimulasi terjadinya lipid peroksida seperti defisiensi vitamin E dan kondisi hiperglikemia. Dalam penelitian ini, untuk menstimulasi terjadinya lipid peroksida dipilih
diet lemak tinggi atau kondisi
hiperkolesterolemia. Analisis konsentrasi lipid peroksida hati pada tahap awal dilakukan setelah konsentrasi kolesterol tikus pada
kelompok hiperlipidemia dan kelompok
perlakuan sudah meningkat.
Pada penelitian ini, pengukuran
konsentrasi kolesterol total darah pada tikus tidak dilakukan sendiri melainkan data
sekunder. Pada awalnya, masa induksi
kolesterol tikus pada kelompok hiperlipidemia dan kelompok perlakuan dilakukan hingga
empat minggu peningkatan kolesterol.
Meskipun demikian kenaikan kolesterol pada
minggu keempat peningkatan tidak
menunjukan kenaikan secara signifikan.
Konsentrasi kolesterol total darah
meningkat secara signifikan terjadi saat pengambilan darah keempat atau pada minggu
kesembilan peningkatan kolesterol.
Peningkatan kolesterol total darah terjadi saat dosis PTU ditingkatkan menjadi dua kali dosis semula dan perubahan beberapa komposisi pakan kolesterol yaitu dari 5% lemak kambing dan 6% minyak goreng curah menjadi 10% lemak kambing dan 1% minyak goreng curah
pada minggu kedelapan peningkatan
kolesterol. Konsentrasi kolesterol pada
kelompok hiperlipidemia dan kelompok
perlakuan setelah sembilan minggu diinduksi kolesterol hanya meningkat sekitar 66.64%
dibandingkan dengan kelompok normal
(Gambar 7).
Konsentrasi lipid peroksida hati tikus yang berusia lima bulan pada kelompok normal
yang dinekropsi (dibedah) pada minggu
keduabelas adalah sebesar 87.10 nmol/g. Nilai ini sedikit berbeda dari hasil penelitian
Gambar 7 Kenaikan konsentrasi kolesterol selama induksi kolesterol. Konsentrasi kolesterol awal ( ), Minggu kedua peningkatan (■), Minggu keenam (■), dan Minggu kesembilan ( ).
Sayogya (2002) yaitu nilai lipid peroksida hati kelompok normal yang dinekropsi setelah 19 minggu pada usia 8.5 bulan adalah sebesar 100.46 nmol/g. Hal ini mungkin disebabkan karena perbedaan usia tikus itu sendiri.
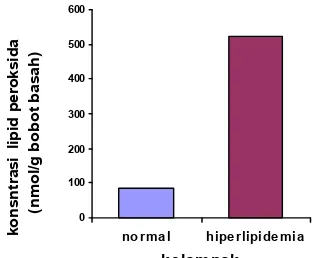
Konsentrasi lipid peroksida hati pada kelompok hiperlipidemia yang dinekropsi
pada minggu keduabelas adalah sebesar
523.55 nmol/g. Bila dibandingkan dengan kelompok normal, konsentrasi lipid peroksida hati kelompok hiperlipidemia yang diberi pakan kolesterol sebesar 1.25% lebih besar lima kalinya secara bermakna dari pada kelompok normal (Gambar 8). Hasil ini sesuai
dengan laporan Uphadya (2002) bahwa
mencit yang diberi kolesterol sebanyak 1.16% selama tujuh minggu mampu meningkatkan konsentrasi lipid peroksida dalam eritrosit dan aorta lebih tinggi dibandingkan dengan mencit yang hanya diberi pakan standar.
Gambar 8 Perbandingan konsentrasi lipid peroksida hati kelompok normal dengan kelompok
Begitu pula dengan hasil penelitian Tombilangi (2004) yaitu pemberian kolesterol
sebesar 0.25% dapat meningkatkan
konsentrasi lipid peroksida darah kelinci
sembilan kalinya dibandingkan dengan
kelompok normal. Hasil penelitian Widyarti (1995) yaitu pemberian pakan diet protein normal dan lemak tinggi pada tikus jantan selama delapan minggu
mampu meningkatkan konsentrasi lipid
peroksida hati sekitar 81.78% dibandingkan dengan tikus yang diberi pakan diet protein dan lemak normal.
Selain dipengaruhi oleh pakan kolesterol, tingginya konsentrasi lipid peroksida juga dapat disebabkan oleh PTU. PTU merupakan salah satu benda asing bagi tubuh yang
apabila masuk ke dalam tubuh akan
mengalami biotransformasi di dalam hati. Proses biotransformasi ini melibatkan suatu sistem sitokrom P1450 yaitu suatu enzim yang terdapat di dalam retikulum endoplasma. Sitokrom P1450 ini akan segera melakukan biotransformasi oksidatif, sehingga dapat merubah PTU menjadi senyawa yang toksik dan reaktif atau senyawa radikal (Koolman 1995).
Senyawa lipid peroksida lebih banyak di dalam jaringan dibandingkan dengan di dalam darah. Berdasarkan penelitian Adji (2004) yaitu konsentrasi lipid peroksida darah dalam keadaan normal sekitar 0.46 ng/mL. Bila dibandingkan dengan lipid peroksida hati, nilai konsentrasi lipid peroksida dalam darah jauh lebih kecil. Hal ini disebabkan oleh radikal bebas seperti radikal hidroperoksil (HO2
.
), radikal superoksida (O2), dan hidroksil
radikal (OH.) dibentuk dalam sel sebagai
senyawa intermediet dari transfer elektron di mitokondria sehingga lebih mudah menyerang jaringan. Hasil penelitian ini juga sesuai
dengan pernyataan Mete (2001) yaitu
konsentrasi malonaldehida hati jauh lebih
besar dibandingkan dengan konsentrasi
malonaldehid dalam plasma darah.
4 !/( #$+! # / / +% & !( & ' " $ +! $% %'%&
!"#$%& +%
Sebelum mendapatkan perlakuan, hewan coba dikelompokan berdasarkan kenaikan kolesterol secara acak. Pengaruh pemberian
ekstrak ramuan daun jati belanda yang
dicekok selama lima minggu terhadap
konsentrasi lipid peroksida hati dapat dilihat pada Gambar 9. Berdasarkan gambar tersebut
dapat dilihat bahwa pemberian ramuan
ekstrak daun jati belanda pada hewan coba
belum dapat menurunkan konsentrasi lipid peroksida hati. Bila dibandingkan dengan kelompok hiperlipidemia, konsentrasi lipid peroksida hati pada kelompok hewan coba yang diberi ramuan ekstrak daun jati belanda
sebesar 1.19%. Namun secara statistik
peningkatan ini tidak berbeda makna. Hal ini
mungkin disebabkan oleh efek
ketidaksinergisan senyawa1senyawa bioaktif yang terkandung di dalam ramuan tersebut.
Pada kelompok hewan coba yang diberi ramuan ekstrak daun jati belanda tunggal
mampu menurunkan konsentrasi lipid
peroksida hati sebesar 7.24%, sedangkan kelompok yang diberi ramuan ekstrak daun jati belanda dengan daun jati belanda lebih banyak sebesar 13.25%. Meskipun demikian penurunan konsentrasi lipid peroksida hati yang diberi ramuan ekstrak daun jati belanda dan ramuan ekstrak daun jati belanda dengan daun jati belanda lebih banyak tidak berbeda
nyata dengan kelompok hiperlipidemia.
Penurunan konsentrasi lipid peroksida hati terbesar terjadi pada kelompok hewan coba yang diberi ramuan ekstrak daun jati belanda tanpa daun jambu biji yaitu sebesar 26.31% secara nyata dibandingkan dengan kelompok hiperlipidemia (p<0.1). Berdasarkan nilai tersebut dapat dilihat penurunan konsentrasi lipid peroksida hati terlihat secara nyata saat daun jambu biji dihilangkan dari kamposisi ramuan daun jati belanda.
Lain halnya dengan pengaruh ramuan
daun jati belanda terhadap penurunan
kolesterol total dalam darah. Setelah lima minggu dicekok ramuan, kelompok hewan coba yang diberi ramuan ekstrak daun jati
belanda mampu menurunkan kolesterol
sebesar 27.56% secara nyata dibandingkan
kelompok hiperlipidemia., sedangkan
kelompok yang diberi ramuan ekstrak daun jati belanda tanpa daun jambu biji hanya mampu menurunkan kolesterol total dalam darah sebesar 13.34% secara tidak nyata
dibandingkan dengan kelompok
hiperlipidemia (p>0.1).
Gambar 9 Konsentrasi Lipid peroksidasi hati Kelompok normal ( ), kelompok hiperlipidemia (■), kelompok perlakuan ekstrak 1x:1y:1z (■), kelompok perlakuan ekstrak 2x:1y:1z ( ), kelompok perlakuan ekstrak 1x:0y:1z (■), kelompok perlakuan ekstrak 1x:0y:0z (■).
Ramuan ekstrak daun jati belanda tediri atas daun jati belanda, daun jambu biji dan temulawak. Berdasarkan hasil penelitian sebelumnya daun jati belanda, daun jambu
biji, dan temulawak dapat menurunkan
konsentrasi lipid peroksida. Hasil penelitian
Tombilangi (2004) melaporkan bahwa
pemberian ekstrak etanol daun jati belanda dengan dosis 1g/Kg BB mampu menurunkan konsentrasi lipid peroksida dalam darah secara
nyata pada minggu kedua perlakuan
dibandingkan dengan kelompok
hiperlipidemia. Indriani (2006) melaporkan bahwa ekstrak etanol daun jambu biji putih dapat menghambat oksidasi lipid sebesar
94.19%. Hasil penelitian Adji (2004)
menyebutkan bahwa ekstrak etanol 75% rimpang temulawak dengan dosis 100 mg/Kg
BB mampu mencegah peningkatan
konsentrasi lipid peroksida dalam darah sebesar 64.30% terhadap kondisi awal.
Senyawa bioaktif yang bersifat sebagai antioksidan yang terkandung di dalam ketiga tumbuhan obat tersebut antaralain flavonoid, tanin, vitamin C, dan kurkumin. Kemampuan flavonoid dalam menghambat peroksidasi lipid tergantung dari nilai RSA (#
). Jenis flavonoid seperti apigenin, flavon, flavonon, dan hesperidin, memiliki nilai RSA yang kecil (<50%), sedangkan morin, kuersetin, mirisetin, dan 31 hidroksiflavon memiliki nilai RSA yang besar
(>50%) (Amic 2003). Vitamin C
merupakan suatu senyawa bioaktif bersifat terhadap radikal bebas terutama superoksida (O2-) dan singlet oksigen (1O2).
Pada konsentrasi rendah vitamin C dapat
bereaksi langsung dengan radikal peroksil LOO-(Hishino . 2000).
"! $% + ! %'%& !"#$%& +% & 4 " $+ !" +% &
Pengaruh kolesterol terhadap peroksidasi lipid dapat dilihat dari korelasi antara konsentrasi kolesterol hati dengan lipid peroksida hati dan konsentrasi kolesterol total plasma (TPC) selama 16 minggu perlakuan.
Korelasi digunakan untuk mengetahui
hubungan antara lipid peroksida dan
konsentrasi kolesterol hati dan TPC. Pada penelitian ini diharapkan adanya korelasi
positif antara lipid peroksida dengan
kolesterol hati dan TPC yaitu semakin besar konsentrasi kolesterol hati dan TPC maka semakin besar pula konsentrasi lpid peroksida hati. Analisis statistik yang digunakan untuk melihat korealasi antara lipid peroksida dengan kolsterol hati dan TPC digunakan korelasi Pearson pada α= 0.05.
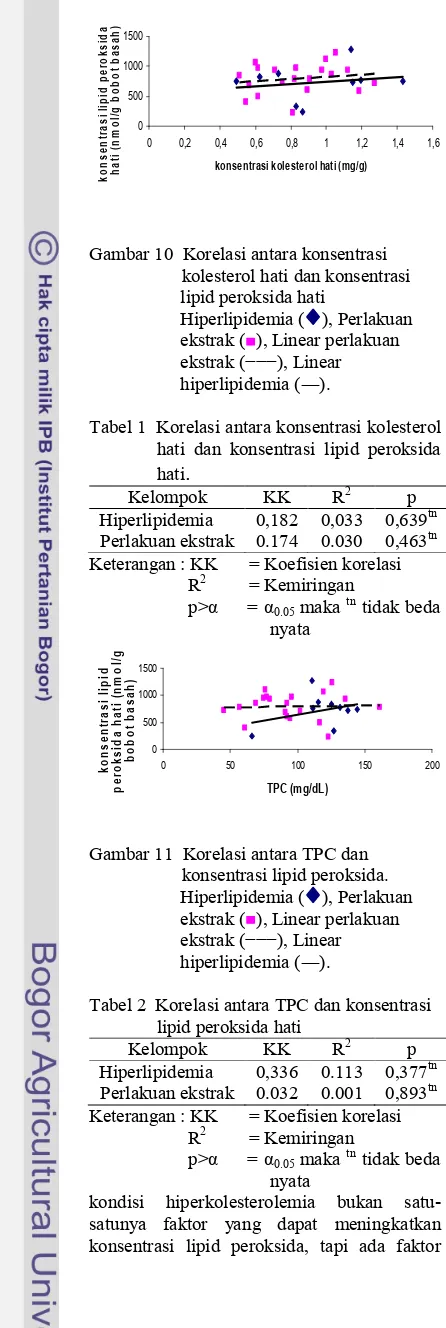
Berdasarkan Gambar 10 terlihat bahwa adanya korelasi positif antara kolesterol hati dan konsentrasi lipid peroksida hati baik pada
kelompok hiperlipidemia dan kelompok
perlakuan yang diberi ekstrak dengan
komposisi yang bervariasi. Hal ini terlihat dari koefisien keragaman (R2) baik pada kelompok
hiperlipidemia dan kelompok perlakuan
ekstrak sebesar 3%. Meskipun demikian, secara statistik korelasi tersebut tidak berbeda nyata (p>0.05).
Korelasi antara TPC dan konsentrasi lipid peroksida hati (Gambar 11) menunjukan
adanya korelasi positif pada kelompok
hiperlipidemia sebesar 11.3%. Meskipun demikian secara statistik korelasi tersebut tidak berbeda nyata (p>0.05), sedangkan pada kelompok yang diberi perlakuan ekstrak dengan komposisi yang bervariasi tidak
menunjukan korelasi antara TPC dan
konsentrasi lipid peroksida hati. Hal ini dapat dilihat dari kemiringan kurva yang mendekati nol.
Hasil ini sesuai dengan hasil yang
dilaporkan Sayogya (2002) yang menyatakan
bahwa tidak ada korelasi antara lipid
peroksida hati dengan kolesterol pada ekor
monyet panjang ($ ) yang
diberi pengobatan dengan %
# $ (BRMTm). Begitupula
Gambar 10 Korelasi antara konsentrasi kolesterol hati dan konsentrasi lipid peroksida hati
Hiperlipidemia ( ), Perlakuan ekstrak ( ), Linear perlakuan ekstrak (−−−), Linear hiperlipidemia (―).
Tabel 1 Korelasi antara konsentrasi kolesterol hati dan konsentrasi lipid peroksida hati
.
Kelompok KK R2 p
Hiperlipidemia 0,182 0,033 0,639tn
Perlakuan ekstrak 0.174 0.030 0,463tn Keterangan : KK = Koefisien korelasi
R2 = Kemiringan
p>α = α0.05maka tn
tidak beda nyata
!"#
Gambar 11 Korelasi antara TPC dan konsentrasi lipid peroksida. Hiperlipidemia ( ), Perlakuan ekstrak ( ), Linear perlakuan ekstrak (−−−), Linear hiperlipidemia (―).
Tabel 2 Korelasi antara TPC dan konsentrasi lipid peroksida hati
Kelompok KK R2 p
Hiperlipidemia 0,336 0.113 0,377tn
Perlakuan ekstrak 0.032 0.001 0,893tn Keterangan : KK = Koefisien korelasi
R2 = Kemiringan
p>α = α0.05maka tn
tidak beda nyata
kondisi hiperkolesterolemia bukan satu1 satunya faktor yang dapat meningkatkan konsentrasi lipid peroksida, tapi ada faktor
lain yang ikut berperan terhadap peroksidasi lipid seperti faktor usia dan kondisi stres.
Tidak adanya korelasi antara lipid
peroksida hati dengan kolesterol dapat juga disebabkan oleh perbedaan antara proses biosintesis kolesterol dan peroksidasi lipid.
Kolesterol merupakan komponen penting
membran sel, prekusor asam empedu, dan hormon steroid. Biosintesis kolesterol meliputi empat tahapan yaitu perubahan asetil1koA menjadi mevalonat, perubahan
mevalonat menjadi skualena, pelipatan
struktur skualena membentuk lanosterol, dan perubahan lanosterol menjadi kolesterol
(Lehninger 1994). Lain halnya dengan
peroksidasi lipid. Lipid peroksida terbentuk akibat serangan radikal bebas terhadap membran sel. Jadi biosintesis kolesterol berbeda dengan peroksidasi lipid.
Peroksidasi lipid merupakan salah satu proses yang dapat menimbulkan penyakit yang banyak terjadi dimasyarakat. Degradasi peroksidatif terhadap PUFA dan komponen
fosfolipid membran dapat menyebabkan
kerusakan struktural, fungsional organ dan jaringan (Popova & Popov 2002). Kerusakan membran biologis menyebabkan perubahan fluiditas serta perubahan aktivitas dari enzim1 enzim yang terikat pada membran.
Peroksidasi lipid yang terjadi di dalam hati
dapat mengakibatkan gangguan pada
membran sel mikrosom hati, sehingga fungsi
membran sel mikrosom dapat dirusak.
Aktivitas enzimatik yang ada di dalam
retikulum endoplasmik hati diantaranya enzim untuk biosintesis trigliserida, katabolisme
asam lemak, katabolisme kolesterol,
biosintesis kolesterol, serta aktivitas glukosa 61fosfatase (Gibson & Skeet 1991). Jadi, apabila membran sel mikrosom hati dirusak oleh peroksidasi lipid maka aktivitas enzim1 enzim tersebut dapat terganggu.
% '/
Ramuan ekstrak daun jati belanda tanpa daun jambu biji bersifat sebagai antioksidan
dengan menurunkan konsentrasi lipid
peroksida hati tikus hiperlipidemia sebesar 26.31%. Ramuan ekstrak daun jati belanda bersifat sebagai prooksidan, dan tidak adanya korelasi antara lipid peroksida hati dengan kolesterol hati dan TPC.
!
belanda terhadap lipid peroksida dalam darah, dan menambahkan kelompok hewan coba yang diberi vitamin E sebagai kelompok pembanding. Selain itu, perlu penambahan waktu percobaan sehingga diharapkan dengan semakin lamanya waktu pemberian ekstrak pengaruhnya bisa semakin terlihat.
Amic D, Davidovic1Amic D, Beslo D. 2003. Structure1radical scavenging activity relationships of flavonoids.
76(1):55161.
Budhidjaja P. 1988. Pengaruh kurkuminoid dari temulawak (
Roxb) terhadap kolesterol total, trigliserida, dan HDL1kolesterol darah kelinci dalam keadaan hiperlipidemia. [laporan penelitian]. Bandung: Jurusan Farmasi FMIPA UNPAD.
Dalimartha S. 2002. # & " '"
( ! $ ! ! . Jakarta:
Penebar Swadaya.
Darwis SN, Hiyah S, Madjo I.1991.
& " '" ) * " .
Bogor: Pusat Pengembangan Tanaman Industri.
Ganong WF. 2001. % ! )
+ ! . Ed1ke20. Djauhari
Widjajakusumah, penerjemah. Jakarta:
EGC. Terjemahan dari: #
$ .
Gibson G, Skett. 1991.
$ " '" . Aisyah,
penerjemah. Jakarta: UI Press.
Grundy SM. 1991. Multifantorial etiology of hypercholesterolemia: Implication for prevention of coronary heart disease.
" 11:
161911635.
Halliwel B, Gutteridge JMC. 1999. )
# % $ .
1999. Ed ke13. New York: Oxford University.
Heyne K. 1987. & " %
, . Jakarta: Yayasan Sarana
Wana Jaya.
Hishino H. 2000. Cancer prevention by carotenoids and curcumin. Di dalam:
Bidlack WR . Editor,
Phytochemicals as Bioactive Agent. Lancaster Technomic Publishing . 1611 165.
Indariani S. 2006. Jambu biji berkhasiat
sebagai antioksidan.
http://www.ipb.ac.id/pariwara/pilihan.p hp3?klp=1&.html [7 Maret 2006]. Iritani N, Nagashima K, Fukuda H, Katsurada
A, Tanaka T. 1986. Effects of dietary on lipogenic enzymes in rat liver. -. . 116: 1901197
Kaplan LA, Pesce AJ. 1989.
/ . New York:
Mosby Tear Book .
[KKI] Kelompok Kerja Ilmiah Phyto Medica. 1993.
" ) ! . Jakarta:
Yayasan Pengembangan Obat Bahan Alam Phyto Medica.
Ketaren S. 1986.$ ! 0 ! .
Jakarta: Universitas Indonesia. Kleiner IS, Dotti LB. 1958. 0 "
, % . Ed. ke15.
St.Louis: Mosby.
Koolman J, Rohm KH. 2001. Atlas berwarna
&Teks Biokimia. Wanandi S,
penerjemah. Jakarta: Hipokrates. Terjemahan dari:
% .
Kristiani EBE. 2003. Ekstrak daun jati
belanda ( Lamk.)
sebagai obat alternatif untuk
hiperlipidemia: kajian dan
. [tesis]. Bogor: Program Pasca Sarjana, Institut Pertanian Bogor. Lautan J. 1997. Radikal bebas pada eritrosit
dan leukosit.
+ ! . 116: 49152.
Lehninger AL. 1994. Dasar1dasar Biokimia. Jilid II. Thenawidjaya, penerjemah. Jakarta: Erlangga.
Lestari K, Muhtadi A. 1997. Uji aktivitas antihiperlipidemia daun jati belanda
( Lamk.) pada tikus.
[laporan penelitian]. Bandung:
Universitas Padjajaran.
Lestariana W, Mulyono H, Ratnaningsih T,
Nugroho LN, dan Suyito. 2005.
Pengaruh pemberian ekstrak air daun
jambu biji ( Linn)
secara kronis terhadap kadar glukosa darah, kadar trigliserida, dan kolesterol
serum tikus (# ). % !
+ 1 %$,. Pekan Baru 30 Nov11 Des 2005.
Martono S. 2006. Jangan minum parasetamol
dengan kunyit dan temulawak.
http://www.republika.co.id/koran1 detail.asp?id=230394&kat.html.[8 Maret 2006].
Matjik AA, Sumertajaya M. 2000.
"
! $ " - ,.
Bogor: IPB Press.
Mete N, Isik B, Erdinc L, Gurkan F. 1999. The effect of fish oil on liver and plasma MDA and antioxidant status of
rats.& - $ 29: 11
6
Momuat LI, Sulistiyani, Khomsan A, Sajuhti D. 2001. Minyak sawit mempercepat regresi aterosklerosis aorta pada kelinci hiperkolesterolemia ringan, tetapi tidak pada yang hiperkolesterolemia berat.
$ 3 + 1122: 26134.
Murray RK, Granner DK, Mayes PA, Rodwell
VW. 2001.% ! 4 . Ed ke125.
Hartanto A, penerjemah. Jakarta: EGC.
Terjemahan dari: 4 5
% .
Popova, Popov CS. 2001. Damage to
suvcellular structures evoked by lipid
peroxidation.* . 57c: 3611
365
Rachmadani. 2001. Ekstrak air daun jati
belanda ( Lamk)
berpotensi menurunkan kadar lipid
darah tikus Wistar. [skripsi].
Bogor: Jurusan Kimia FMIPA IPB.
Sastroamidjojo AS.1988.'" , .
Jakarta: Dian Rakyat.
Soesilo S. 1989. 2 ! % '"
. Jakarta: Direktorat Jendral Pengawasan Obat dan Makanan. Sugati S, Syamsuhidayat, Hutapea JR. 1991.
, & '" ,
678. Jakarta: Balai Penelitian dan Pengembangan Kesehatan RI.
Sulistyo BI.1998. Radikal bebas, peroksidasi
lipida dan antioksidan. !
! . 1: 55161.
Syukur C, Hernani. 2002.% &
'" + . Jakarta: Penebar
Swadaya.
Taher A. 2003. Peran fitoestrogen kedelai
sebagai antioksidan dalam
penanggulangan aterosklerosis. [tesis]. Bogor: Program Pasca Sarjana, Institut Pertanian Bogor.
Tappel AL, Zalkin H. 1960. Inhibition of lipid peroxidation in microsomes by vitamin E.. . 185: 35.
Tombilangi AK. 2004. Khasiat ekstrak daun
jati belanda ( Lamk)
terhadap kadar lipid peroksida darah kelinci yang hiperlipidemia. [skripsi]. Bogor: Jurusan Kimia FMIPA IPB Triarsari D. 2006. Betulkah jambu biji
mengatasi demam berdarah ?.
http://wwwdepkes.go.id/index.php?opti on=viewarticle&artid=73.html [7Maret 2006].
Upadhya S . 2002. Lipid peroxidation in different tissues: effect of high cholesterol and fish oil in the diet.
, - . 46(4):
4751481.
Voet D, Voet JG. 1995. % . New
York: J Wiley.
Widyarti S. 1995. Pengaruh pemberian
ekstrak teh hijau terhadap kadar peroksida lipid tikus yang diberi diet protein rendah dan lemak tinggi [tesis]. Bogor: Program Pasca Sarjana, Institut Pertanian Bogor.
Wijayakusuma H. 1993.& % !
'" , - + 9:. Jakarta:
Pustaka Kartini.
Wresdiyati T, Astawan M. 2005. Deteksi secara imunohistokimia antioksidan superoksida dismutase (SOD) pada jaringan tikus hiperkolesterolemia yang diberi pakan rumput laut. [laporan
penelitian]. Bogor: Fakultas
Kedokteran Hewan, Institut Pertanian Bogor.
Yagi K. 1994. Lipid peroxides in hepatic, gastrointestional, and pancreatic diseases, hlm. 1651169. Di dalam:)
# , $ .
Normal n=10
Hiperlipidemia n=10
Perlakuan I n=5
Perlakuan II n=5
Perlakuan IV n=5 Perlakuan III
n=5
Adaptasi 2 minggu
Induksi kolesterol 9 minggu Pembedahan awal
@ 5ekor
Analisis Lipid peroksida hati
Pembuatan pakan kolesterol
Analisis kolesterol Pencekokan ekstrak
selama 5 minggu
Pembedahan akhir @ 5ekor
Analisis statistik
1
Lampiran 2 Perhitungan dosis jumlah kolesterol kuning telur, lemak kambing dan
PTU.
1. kolesterol kuning telur
Jika diketahui kolesterol kuning telur 60 mg, jumlah pakan kolesterol yang
diinginkan sebesar 30 Kg dengan persentase kolesterol kuning telur sebesar
1.5%, maka kuning telur yang dibutuhkan adalah:
1.5 g x 30.000 g pakan = 450 g kolesterol
100 g
450 g x 1 g kuning telur = 750 g kuning telur
0.060 g
2. Lemak kambing (5% b/b)
5 g
x 30.000 g pakan
= 1500 g lemak kambing
100 g
3. PTU 0.01% b/V (0.5 mg/Kg BB)
Diketahui konsentrasi PTU 0,01%, PTU 100 mg dengan bobot tablet PTU 236
mg, maka jumlah PTU yang ditimbang:
0.01% = 0.01 g/100 mL air
= 10 mg/100 mL
= 0.1 mg/1mL
PTU 100 mg ∞ 236 mg
1 mg
∞ 2.36 mg
10 mg/100 mL PTU, maka 0.0236 g/100 mL air
Jika dosis yang ingin dicekokan 0.5 mg/Kg BB pada tikus dengan bobot 200 g,
maka volume yang dicekokan:
0.5 mg x 0.2 Kg = 0.1 mg
1 Kg
Dosis PTU yang diinginkan: 0.1 mg = 0.1 mg
1 mL
x mL
Lampiran 3 Hasil kurva standar TMP.
! "#
$
" % & # # ' (
) )
)*
* *
) *
) +
+ *
* +
* )
) +
$ !%"
, * ( ) ' , ** +
(
&
Contoh perhitungan:
Dari persamaan garis pada kurva standar: y= 0.0915x – 0.0063, r = 99.47%
Misal absorbansi sampel 0.070, maka: 0.070= 0.0915x – 0.0063
x= 0.8338 NM
Volume total homogenat hati = 10.281 mL
Volume total homogenat hati yang digunakan= 0.1 mL
Bobot hati pada 10% b/v = 1.0281g yang berasal dari 1.0281g/10.281 mL
Konsentrasi lipid peroksida dalam nmol/g:
=
C (NM) x volume total homogenat hati (mL)/ volume homogenat hati yang direaksikan (mL) bobot hati pada 10% b/v homogenat (g)= 0.8338 NM x 10.281 mL/0.1 mL
1.0281 g
Lampiran 4 Perubahan rata1rata bobot badan tikus selama percobaan.
' ( - - - ".
../ (
* )
* +) + +
) ) + ) ) +
) + ) ) * )
+ * ) + ) ) )
) * )+) ) ) ))+
+ ) ) ) )+ ) * ) ) *
) * * )
* ) + + )*
) * + * +
)* +) + +
) + + +
) + + + +
+
) )
+ * * +* + +
Lampiran 5 Data konsentrasi lipid peroksida hati saat peningkatan kolesterol pada
minggu ke19.
#
$
" %.
# $
" %.
+ ) ) * ))
) ) + ) ++ *
) +) ) )+
+ +) + + )
+ ( +) )
( +) + !0 +) +
!0 )
Lampiran 6 Data konsentrasi lipid peroksida hati diakhir perlakuan pada minggu
ke114.
#
$
" %.
#
$
" %.
* ) + ) )))
* ) +*
) + * + ) + +
+ +) )
' ( +* *) *+ +* + )
!0 ) ' ( *) +*
Lampiran 6 (Lanjutan)
$ / $ /
#
$
" %.
#
$
" %.
) ** * )
++ * +
) + ) *
* * )
) + *
' ( * * * ' ( + ) ++ *
!0 ) + ) + !0 ) ))+ +
$ / $ /
#
$
" %.
#
$
" %.
+ * * + + +
++ )++ ++ + +
) + + ++* ) ) + * +
+ * * *) ))
+ ) + *+
' ( * ' ( + *
! 0 + ** ! 0 )
Lampiran 7 Data konsentrasi kolesterol hati.
$
" .%.
-$
" .%.
-+ +
*+
) ) +
* )
+ *)
)*
+ ) +
)
* * * +
( + ( *
!0 !0 )
$ / $ /
$
" .%.
-$
" .%.
-+ +
) ** )
)
+
( ( +
Lampiran 7 (Lanjutan)
$ / $ /
$
" .%.
-$
" .%. * +
*
) * )
+ *+
+ *
( * + )
!0
( !0
Keterangan : data kolesterol hati adalah data sekunder.
Lampiran 8 Analisis statistik rancangan acak lengkap.
Analisis ragam konsentrasi lipid peroksida hati minggu ke116
1/ /
0 2
-$/
. 3
4 / + *
5 *+ ) ) )* )
6 ) )
Analisis ragam konsentrasi kolesterol selama lima minggu perlakuan
1//
0 2
-$/
. 3
4 / + * * ) +)
5 ** * ) * )
6
Uji Duncan konsentrasi lipid peroksida hati minggu ke116
!/- 7 ,
4 /
)
*) *
+
++ * ++ *
* ) * )
*) +* *) +*
) )
! . )
Uji Duncan konsentrasi kolesterol selama lima minggu perlakuan
!/- 7 ,
8#'
)
* * * *
*+ + *+ +
) * ) *
Lampiran 8 (Lanjutan)
Uji Duncan bobot badan hewan coba pada minggu kelima perlakuan
!/- 7 ,
8#'
+
+ *
) *
+ +* ! .
Uji Duncan bobot badan hewan coba setelah satu minggu induksi pada kelompok
normal
!/- 7 ,
8#' )
*
) *
! .
Uji Duncan bobot badan hewan coba setelah satu minggu induksi pada kelompok
perlakuan
!/- 7 ,
8#'
)
)
) )
* * ! .
Lampiran 9 Hasil analisis korelasi antara lipid peroksida hati dan kolesterol
hati serta TPC.
Korelasi antara lipid peroksida hati dan kolesterol hati serta TPC kelompok
hiperlipidemia.
& $ 649
& 94 ))
! . " ( )* )++
* * *
$ 4
9 )
! . " ( )* +
* * *
649 4
9 )) )
! . " ( )++ +
Lampiran 9 (Lanjutan)
Korelasi antara lipid peroksida hati dan kolesterol hati serta TPC kelompok
perlakuan ekstrak 1x:1y:1z.
& $
649
& 4
9 +) +
! . " ( *
$ 4
9 +) ) +
! . " ( *
649 4
9 + ) +
! . " (
Korelasi antara lipid peroksida hati dan kolesterol hati serta TPC kelompok
perlakuan ekstrak 2x:1y:1z.
& $
649
& 4
9 ( ) ( ++
! . " ( +
$ 4
9 ( ) (
! . " (
649 4
9 ( ++ (
! . " ( +
Korelasi antara lipid peroksida hati dan kolesterol hati serta TPC kelompok
perlakuan ekstrak 1x:0y:1z.
& $
649
& 4
9 + *
! . " ( + *
$ 4
9 + (
! . " ( + *
649 4
9 * (
Lampiran 9 (Lanjutan)
Korelasi antara lipid peroksida hati dan kolesterol hati serta TPC kelompok
perlakuan ekstrak 1x:0y:0z.
& $
649
& 4
9 ( ) *
! . " (
$ 4
9 ( (
! . " (
* +
649 4
9 ) * (
! . " (
* +
Korelasi antara lipid peroksida hati dan kolesterol hati pada seluruh kelompok
perlakuan ekstrak.
#
+ )
+ )
4 9
! . " (
4 9
! . " ( &
$
& $
Korelasi antara lipid peroksida hati dan TPC pada seluruh kelompok peerlakuan
ekstrak.
#
) *)
) *)
4 9
! . " (
4 9
! . " ( &
649
&
Jati belanda, jambu biji, dan temulawak merupakan tumbuhan obat
tradisional yang telah digunakan sebagai antioksidan. Penggunaan tumbuhan
tersebut sebagai antioksidan masih terbatas pada masing1masing tumbuhan saja,
sedangkan potensi antioksidasi ketiga tumbuhan tersebut dalam bentuk ramuan
belum dilakukan. Penelitian ini bertujuan untuk mendapatkan informasi potensi
antioksidasi dari ramuan daun jati belanda, serta menetukan konsentrasi lipid
peroksida hati tikus hiperlipidemia yang diberi ramuan ekstrak daun jati belanda
yang mengandung daun jambu biji dan rimpang temulawak.
Ramuan daun jati belanda yang terdiri dari daun jambu biji dan rimpang
temulawak diekstraksi dengan pelarut etanol 70% s