PEMANFAATAN PATI KELAPA SAWIT SEBAGAI
BAHAN BAKU DEKSTRIN
RIDWANSYAH
SEKOLAH PASCA SARJANA
INSTITUT PERTANIAN BOGOR
RIDWANSYAH. F325010011. Pemanfaatan Pati Kelapa Sawit Sebagai Bahan Baku Dekstrin. Di bawah bimbingan M. Zein Nasution, Titi Candra Sunarti dan Anas M. Fauzi.
ABSTRAK
Batang kelapa sawit merupakan limbah dari peremajaan perkebunan kelapa sawit. Ekstraksi batang kelapa sawit menghasilkan ± 4,7% pati. Pati yang dihasilkan dikarakterisasi sifat fisik dan kimianya dibandingkan dengan pati komersil yaitu sagu dan tapioka. Pati tersebut dimodifikasi menjadi dekstrin dengan hidrolisis enzimatis dan asam dan dikarakterisasi mutu dekstrin yang dihasilkan.
Pati kelapa sawit memiliki kadar lemak (0,37%), abu (0,68%), serat (1,78%) lebih tinggi dari pati sagu dan tapioka, tetapi memiliki kandungan amilosa (28,76%) yang lebih rendah. Suhu gelatinisasi pati kelapa sawit (770C) sama dengan sagu tetapi lebih besar dari tapioka, sedangkan derajat putih pati (83,02%) dan kejernihan pasta (15,4%T) lebih kecil dari sagu dan tapioka.
Penerimaan pati kelapa sawit terhadap α-amilase lebih rendah dibandingkan dengan sagu dan tapioka sedangkan penerimaan pati kelapa sawit terhadap asam adalah hampir sama dengan sagu dan tapioka. Mutu dekstrin pati kelapa sawit baik hidrolisis secara enzimatis dan asam lebih rendah dari tapioka tetapi hampir sama dengan sagu berdasarkan kadar abu, viskositas dan kelarutan dalam air dingin dari dekstrin yang dihasilkan.
RIDWANSYAH. F325010011. Utilization of Oil Palm Starch for Dextrin Production. Supervised by M. Zein Nasution, Titi Candra Sunarti dan Anas M. Fauzi.
ABSTRACT
The oil palm trunks become waste from the rejuvenation of the oil palm plantation. The extraction of the oil palm trunk yielded 4,7% of starch. The starch was extracted and characterized its physical and chemical properties and compared it to the commercial starches (sago and tapioca). The extracted starch was modified to be dextrin by enzymatic and acid hydrolysis.
The oil palm starch contained lipid (0,37%), ash (0,68%), fiber (1,78%) which were higher than that of sago and tapioca. However, the amylosa content (28,67%) of the oil palm starch was lower. The gelatinization temperature of oil palm starch (770C) was similar with that of sago, but was higher than of tapioca. The whiteness degree of starch (83,02%) and the paste clarity (15,4%T) of the oil palm starch were lower than sago and tapioca.
The α-amilase susceptibility of oil palm starch was lower than that tapioca and sago; however, the susceptibility of the oil palm starch on acid was almost similar with sago and tapioca. The dextrin quality of the oil palm starch, either from enzymatic or acid hydrolysis was lower than the tapioca; however, it was almost similar with the sago based on ash content, viscosity an solubility in cold water.
@ Hak cipta milik Fransiskus Anggawen, tahun 2006 Hak cipta dilindungi
PERNYATAAN MENGENAI TESIS DAN SUMBER INFORMASI
Dengan ini saya menyatakan bahwa tesis Pemanfaatan Pati Kelapa Sawit
Sebagai Bahan Baku Dekstrin adalah karya saya sendiri dengan arahan dari
komisi pebimbing dan belum diajukan dalam bentuk apaun kepada perguruan
tinggi manapun. Sumber informasi yang berasal atau dikutip dari karya yang
diterbitkan maupun tidak diterbitkan dari penulis lain telah disebutkan dalam teks
dan dicantumkan dalam Daftar Pustaka di bagian akhir tesis ini.
Bogor, Agustus 2006
Ridwansyah
PEMANFAATAN PATI KELAPA SAWIT SEBAGAI
BAHAN BAKU DEKSTRIN
RIDWANSYAH
Tesis
Sebagai salah satu syarat untuk memperoleh gelar Magister Sains pada
Program Studi Teknologi Industri Pertanian
SEKOLAH PASCA SARJANA
INSTITUT PERTANIAN BOGOR
PRAKATA
Puji dan syukur penulis panjatkan kehadirat Allah SWT yang telah melimpahkan Rahmat dan Karunia-Nya sehingga tesis ini dapat diselesaikan. Adapun judul dari tesis ini adalah Pemanfaatan Pati Kelapa Sawit Sebagai Bahan Baku Dekstrin.
Terima kasih penulis sampaikan kepada Bapak M. Zein Nasution, Ibu Titi Candra Sunarti dan Bapak Anas M. Fauzi sebagai pembimbing yang telah mengarahkan dan membimbing penulis hingga dapat menyelesaikan tesis ini. Disamping itu penghargaan penulis sampaikan kepada staff laboran dan rekan-rekan TIP atas kerjasamanya. Ungkapan terima kasih penulis sampaikan kepada bapak, ibu dan adik-adik serta keluarga atas kasih sayang, doa dan segala pengorbanan yang telah diberikan kepada penulis hingga dapat menyelesaikan studinya.
Semoga tesis ini dapat bermanfaat bagi kita semua.
Bogor, Agustus 2006
RIWAYAT HIDUP
Penulis dilahirkan di Medan, Sumatera Utara, pada tanggal 13 Desember
1972 dari Bapak M. Hasan dan Ibu Hanifah. Penulis merupakan putra kedua dari
lima bersaudara.
Penulis menyelesaikan pendidikan tingkat dasar pada SD Negeri 060908
Medan pada tahun 1985, Sekolah Menengah Pertama di SMP Negeri 4 Medan
pada tahun 1988, Sekolah Menengah Atas di SMA Negeri 13 Medan pada tahun
1991. Pada tahun 1991 penulis diterima menjadi mahasiswa Fakultas Pertanian
Jurusan Teknologi Hasil Pertanian Universitas Sumatera Utara dan lulus pada
tahun 1996.
Penulis diterima menjadi staff Pengajar Fakultas Pertanian USU tahun
1999, pada tahun 2001 melanjutkan pendidikan Magister (S2) di Program Studi
DAFTAR ISI TINJAUAN PUSTAKA ... Potensi Batang Kelapa Sawit ...
BAHAN DAN METODELOGI PENILITIAN ... Tempat Dan Waktu Penelitian...
HASIL DAN PEMBAHASAN ... Ekstraksi Pati Kelapa Sawit... Karakterisasi Pati ... Produksi Dekstrin ... Karakterisasi Mutu Dekstrin ... Potensi Pemanfaatan Limbah Batang Kelapa Sawit ...
DAFTAR TABEL
Halaman 1 Volume impor dekstrin Indonesia ... 2 Potensi batang kelapa sawit dari kegiatan peremajaan ... 3 Kandungan amilosa dan amilopektin dari beberapa sumber pati... 4 Komposisi pati kelapa sawit, tapioka dan sagu ... 5 Karakteristik dan sifat pirodekstrin ... 6 Komposisi kimia kandungan jaringan vaskular dan parenkim batang
kelapa sawit ... 7 Komposisi pati kelapa sawit, sagu dan tapioka ... 8 Sifat-sifat fisik pati kelapa sawit, sagu dan tapioka ... 9 Sifat amilografi kelapa sawit, sagu dan tapioka... 10 pH suspensi pati sebelum dan sesudah penambahan HCl... 11 Hasil analisa mutu dekstrin hidrolisis enzimatis dan asam... 12 Hubungan panjang rantai degan warna dalam lugol ... 13 Asumsi dasar produksi pati kelapa sawit... 14 Biaya tetap produksi pati kelapa sawit ... 15 Biaya tidak tetap produksi pati kelapa sawit... 16 Biaya pengolahan kayu sawit terkompregnasi ...
3 4 7 9 17
PEMANFAATAN PATI KELAPA SAWIT SEBAGAI
BAHAN BAKU DEKSTRIN
RIDWANSYAH
SEKOLAH PASCA SARJANA
INSTITUT PERTANIAN BOGOR
RIDWANSYAH. F325010011. Pemanfaatan Pati Kelapa Sawit Sebagai Bahan
Baku Dekstrin. Di bawah bimbingan M. Zein Nasution, Titi Candra Sunarti dan Anas M. Fauzi.
ABSTRAK
Batang kelapa sawit merupakan limbah dari peremajaan perkebunan kelapa sawit. Ekstraksi batang kelapa sawit menghasilkan ± 4,7% pati. Pati yang dihasilkan dikarakterisasi sifat fisik dan kimianya dibandingkan dengan pati komersil yaitu sagu dan tapioka. Pati tersebut dimodifikasi menjadi dekstrin dengan hidrolisis enzimatis dan asam dan dikarakterisasi mutu dekstrin yang dihasilkan.
Pati kelapa sawit memiliki kadar lemak (0,37%), abu (0,68%), serat (1,78%) lebih tinggi dari pati sagu dan tapioka, tetapi memiliki kandungan amilosa (28,76%) yang lebih rendah. Suhu gelatinisasi pati kelapa sawit (770C) sama dengan sagu tetapi lebih besar dari tapioka, sedangkan derajat putih pati (83,02%) dan kejernihan pasta (15,4%T) lebih kecil dari sagu dan tapioka.
Penerimaan pati kelapa sawit terhadap α-amilase lebih rendah dibandingkan dengan sagu dan tapioka sedangkan penerimaan pati kelapa sawit terhadap asam adalah hampir sama dengan sagu dan tapioka. Mutu dekstrin pati kelapa sawit baik hidrolisis secara enzimatis dan asam lebih rendah dari tapioka tetapi hampir sama dengan sagu berdasarkan kadar abu, viskositas dan kelarutan dalam air dingin dari dekstrin yang dihasilkan.
RIDWANSYAH. F325010011. Utilization of Oil Palm Starch for Dextrin Production. Supervised by M. Zein Nasution, Titi Candra Sunarti dan Anas M. Fauzi.
ABSTRACT
The oil palm trunks become waste from the rejuvenation of the oil palm plantation. The extraction of the oil palm trunk yielded 4,7% of starch. The starch was extracted and characterized its physical and chemical properties and compared it to the commercial starches (sago and tapioca). The extracted starch was modified to be dextrin by enzymatic and acid hydrolysis.
The oil palm starch contained lipid (0,37%), ash (0,68%), fiber (1,78%) which were higher than that of sago and tapioca. However, the amylosa content (28,67%) of the oil palm starch was lower. The gelatinization temperature of oil palm starch (770C) was similar with that of sago, but was higher than of tapioca. The whiteness degree of starch (83,02%) and the paste clarity (15,4%T) of the oil palm starch were lower than sago and tapioca.
The α-amilase susceptibility of oil palm starch was lower than that tapioca and sago; however, the susceptibility of the oil palm starch on acid was almost similar with sago and tapioca. The dextrin quality of the oil palm starch, either from enzymatic or acid hydrolysis was lower than the tapioca; however, it was almost similar with the sago based on ash content, viscosity an solubility in cold water.
@ Hak cipta milik Fransiskus Anggawen, tahun 2006 Hak cipta dilindungi
PERNYATAAN MENGENAI TESIS DAN SUMBER INFORMASI
Dengan ini saya menyatakan bahwa tesis Pemanfaatan Pati Kelapa Sawit
Sebagai Bahan Baku Dekstrin adalah karya saya sendiri dengan arahan dari
komisi pebimbing dan belum diajukan dalam bentuk apaun kepada perguruan
tinggi manapun. Sumber informasi yang berasal atau dikutip dari karya yang
diterbitkan maupun tidak diterbitkan dari penulis lain telah disebutkan dalam teks
dan dicantumkan dalam Daftar Pustaka di bagian akhir tesis ini.
Bogor, Agustus 2006
Ridwansyah
PEMANFAATAN PATI KELAPA SAWIT SEBAGAI
BAHAN BAKU DEKSTRIN
RIDWANSYAH
Tesis
Sebagai salah satu syarat untuk memperoleh gelar Magister Sains pada
Program Studi Teknologi Industri Pertanian
SEKOLAH PASCA SARJANA
INSTITUT PERTANIAN BOGOR
PRAKATA
Puji dan syukur penulis panjatkan kehadirat Allah SWT yang telah
melimpahkan Rahmat dan Karunia-Nya sehingga tesis ini dapat diselesaikan.
Adapun judul dari tesis ini adalah Pemanfaatan Pati Kelapa Sawit Sebagai
Bahan Baku Dekstrin.
Terima kasih penulis sampaikan kepada Bapak M. Zein Nasution, Ibu Titi
Candra Sunarti dan Bapak Anas M. Fauzi sebagai pembimbing yang telah
mengarahkan dan membimbing penulis hingga dapat menyelesaikan tesis ini.
Disamping itu penghargaan penulis sampaikan kepada staff laboran dan
rekan-rekan TIP atas kerjasamanya. Ungkapan terima kasih penulis sampaikan kepada
bapak, ibu dan adik-adik serta keluarga atas kasih sayang, doa dan segala
pengorbanan yang telah diberikan kepada penulis hingga dapat menyelesaikan
studinya.
Semoga tesis ini dapat bermanfaat bagi kita semua.
Bogor, Agustus 2006
RIWAYAT HIDUP
Penulis dilahirkan di Medan, Sumatera Utara, pada tanggal 13 Desember 1972 dari Bapak M. Hasan dan Ibu Hanifah. Penulis merupakan putra kedua dari lima bersaudara.
Penulis menyelesaikan pendidikan tingkat dasar pada SD Negeri 060908 Medan pada tahun 1985, Sekolah Menengah Pertama di SMP Negeri 4 Medan pada tahun 1988, Sekolah Menengah Atas di SMA Negeri 13 Medan pada tahun 1991. Pada tahun 1991 penulis diterima menjadi mahasiswa Fakultas Pertanian Jurusan Teknologi Hasil Pertanian Universitas Sumatera Utara dan lulus pada tahun 1996.
DAFTAR ISI
TINJAUAN PUSTAKA ... Potensi Batang Kelapa Sawit ...
BAHAN DAN METODELOGI PENILITIAN ... Tempat Dan Waktu Penelitian...
HASIL DAN PEMBAHASAN ... Ekstraksi Pati Kelapa Sawit... Karakterisasi Pati ... Produksi Dekstrin ... Karakterisasi Mutu Dekstrin ... Potensi Pemanfaatan Limbah Batang Kelapa Sawit ...
DAFTAR TABEL
Halaman 1 Volume impor dekstrin Indonesia ...
2 Potensi batang kelapa sawit dari kegiatan peremajaan ...
3 Kandungan amilosa dan amilopektin dari beberapa sumber pati...
4 Komposisi pati kelapa sawit, tapioka dan sagu ...
5 Karakteristik dan sifat pirodekstrin ...
6 Komposisi kimia kandungan jaringan vaskular dan parenkim batang
kelapa sawit ...
7 Komposisi pati kelapa sawit, sagu dan tapioka ...
8 Sifat-sifat fisik pati kelapa sawit, sagu dan tapioka ...
9 Sifat amilografi kelapa sawit, sagu dan tapioka...
10 pH suspensi pati sebelum dan sesudah penambahan HCl...
11 Hasil analisa mutu dekstrin hidrolisis enzimatis dan asam...
12 Hubungan panjang rantai degan warna dalam lugol ...
13 Asumsi dasar produksi pati kelapa sawit...
14 Biaya tetap produksi pati kelapa sawit ...
15 Biaya tidak tetap produksi pati kelapa sawit...
16 Biaya pengolahan kayu sawit terkompregnasi ... 3
4
7
9
17
30
34
35
38
42
45
46
64
65
65
DAFTAR GAMBAR
Halaman 1 Struktur rantai linier dari molekul amilosa... 2 Struktur molekul amilopektin ... 3 Pengaruh dari aktivitas enzim amilase pada amilopektin... 4 Proses dekstrinisasi pati dengan enzim α-amilase ... 5 Mekanisme reaksi transglukosidasi... 6 Mekanisme reaksi hidrolisis dan repolimerisasi ... 7 Tahapan proses ekstraksi pati kelapa sawit... 8 Proses dekstrinisasi secara enzimatis... 9 Proses dekstrinisasi secara hidrolisis asam ... 10 Proses peremajaan tanaman kelapa sawit PTPN 2 Langkat ... 11 Bagian batang yang akan diekstraksi... 12 Serbuk kayu hasil penyerutan dari batang kelapa sawit ... 13 Neraca masa pembuatan pati kelapa sawit... 14 Bentuk granula pati tapioka, sagu dan kelapa sawit tanpa polarisasi
cahaya... 15 Bentuk granula pati tapioka, sagu dan kelapa sawit dengan polarisasi
cahaya... 16 Pati tapioka, sagu dan kelapa sawit ... 17 Pola amilografi pati tapioka, sagu dan kelapa sawit... 18 Bagian yang tidak dapat diserang α-amilase ... 19 Hidrolisis enzimatis pati tapioka, sagu dan kelapa sawit... 20 Hidrolisis asam terhadap pati tapioka, sagu dan kelapa sawit ... 21 Warna dekstrin yang ditetesin larutan lugol... 22 Kadar abu dekstrin tapioka, sagu dan kelapa sawit hidrolisis enzimatis . 23 Kadar abu dekstrin tapioka, sagu dan kelapa sawit hidrolisis asam ... 24 Kadar serat dekstrin tapioka, sagu dan kelapa sawit hidrolisis enzimatis 25 Kadar serat dekstrin tapioka, sagu dan kelapa sawit hidrolisis asam ... 26 Kelarutan air dingin dekstrin tapioka, sagu dan kelapa sawit hidrolisis
enzimatis ... 27 Kelarutan air dingin dekstrin tapioka, sagu dan kelapa sawit hidrolisis
asam ... 28 Viskositas dekstrin tapioka, sagu dan kelapa sawit hidrolisis enzimatis ..
29 Viskositas dekstrin tapioka, sagu dan kelapa sawit hidrolisis asam... 30 Derajat putih dekstrin tapioka, sagu dan kelapa sawit hidrolisis
enzimatis ... 31 Dekstrin komersial, tapioka, sagu dan kelapa sawit hidrolisis enzimatis. 32 Derajat putih dekstrin tapioka, sagu dan kelapa sawit hidrolisis asam... 33 Dekstrin komersial, tapioka, sagu dan kelapa sawit hidrolisis asam ... 34 Kejernihan pasta dekstrin tapioka, sagu dan kelapa sawit hidrolisis
enzimatis ... 35 Kejernihan pasta dekstrin tapioka, sagu dan kelapa sawit hidrolisis asam... 36 Derajat asam dekstrin tapioka, sagu dan kelapa sawit hidrolisis asam.... 37 Pemanfaatan limbah batang kelapa sawit... 38 Diagram alir peralatan ekstraksi pati kelapa sawit ...
55
56 56 57 58
59
DAFTAR LAMPIRAN
Halaman 1 Analisa sifat fisik-kimia pati...
2 Karakterisiasi dekstrin ...
3 Hasil pengamatan nilai DE dan DP terhadap hidrolisis enzimatis pati
kelapa sawit, sagu dan tapioka ...
4 Hasil pengamatan nilai DE dan DP terhadap hidrolisis asam pati kelapa
sawit, sagu dan tapioka ...
5 Hasil analisa mutu dekstrin hidrolisis enzimatis ...
6 Hasil analisa mutu dekstrin hidrolisis asam ...
7 Sidik ragam mutu dekstrin hidrolisis enzimatis...
8 Sidik ragam mutu dekstrin hidrolisis asam ... 74
79
82
83
84
85
86
PENDAHULUAN
Latar Belakang
Pati merupakan zat yang penting dalam dunia perdagangan dan industri
terutama pada negara berkembang di seluruh dunia. Pati tersebut dimanfaatkan
dalam industri tekstil, pengolahan pangan, produk-produk farmasi, kertas, dan
industri polimer sintetik (Lawal dan Adebowale 2005). Pati dapat diperoleh
dengan cara mengekstrak dari bagian beberapa tanaman seperti akar dan umbi,
batang dan biji-bijian.
Indonesia merupakan daerah yang cukup potensial sebagai penghasil
pati seperti ubi kayu, sagu, jagung, ubi jalar dan lain sebagainya karena tanaman
tersebut tersebar di seluruh wilayah Indonesia. Disamping itu ada upaya baru
untuk menghasilkan pati dari batang kelapa sawit.
Areal perkebunan kelapa sawit Indonesia tumbuh dengan laju sekitar
11% per tahun, dari 1 126 juta ha pada tahun 1991 mencapai sekitar 3 584 juta
ha pada tahun 2001(Susila 2003). Kelapa sawit yang pertama kali ditanam dalam
skala besar di Indonesia pada tahun 1978, akan segera mengakhiri masa
produktifnya (Guritno dan Darnoko 2003).
Rata-rata luas areal peremajaan selama kurun waktu tahun 2001 – 2005
diperkirakan mencapai 32 155 ha/tahun. Limbah padat berupa batang atau kayu
sawit dan pelepah kelapa sawit akan dihasilkan masing-masing sebesar 2 257
281 ton dan 514 480 ton per tahun, sedangkan pada kurun waktu tahun 2006 –
2010 ada kenaikan di dalam areal tanaman kelapa sawit yang diremajakan yaitu
rata-rata setiap tahunnya seluas 89 965 ha. Pada kurun waktu tersebut batang
dan pelepah hasil peremajaan akan mencapai berturut-turut 6 315 543 ton dan 1
439 440 ton per tahun. Sebagai limbah lignoselulosa, pemanfaatan kedua limbah
padat tersebut perlu mendapatkan perhatian. Hal ini mengingat bahwa cara-cara
yang telah dilakukan sekarang ini yaitu dengan cara bakar akan mencemari
udara dan juga adanya pelarangan sesuai dengan aturan yang tertuang di dalam
Rencana Undang-Undang Perkebunan. Membiarkan batang dan pelepah hasil
peremajaan dapat menimbulkan masalah bagi tanaman kelapa sawit baru yaitu
dijadikan sebagai sarang serangga dan tikus. Hasil evaluasi sifat fisik dan kimia
batang dan pelepah kelapa sawit menunjukkan bahwa kedua limbah tersebut
pulp dan kertas, industri pati, serta industri perkayuan. Pemanfaatan
limbah-limbah padat ini tentunya akan memberikan keuntungan tambahan bagi
perkebunan kelapa sawit (Guritno dan Darnoko 2003).
Sampai saat ini pemanfaatan batang kelapa sawit untuk keperluan
industri masih terbatas. Ginting (1995) memanfaatkan batang kelapa sawit
menjadi pati dengan cara mengekstrak 2 meter dari pucuk batang kelapa sawit
dengan rendemen pati dari batang kelapa sawit adalah 7,15%. Selanjutnya pati
tersebut dapat dijadikan bahan pangan maupun bahan baku untuk fermentasi
alkohol (Tomimura 1992). Dari hasil penelitian pendahuluan Azemi et al. (1999)
menyatakan pati kelapa sawit memiliki potensi untuk menggantikan pati
komersial baik dalam bidang pangan dan non pangan.
Untuk beberapa keperluan industri, pati yang digunakan merupakan pati
hasil modifikasi atau turunannya. Modifikasi pati bertujuan untuk memperbaiki
atau menambah sifat-sifat fungsional tertentu, yang tidak terdapat pada pati asli
sehingga aplikasinya dalam industri menjadi lebih luas. Sifat-sifat fungsional
tersebut antara lain memperbaiki kelarutan dalam air dingin dan sifat-sifat
gelatinisasi, pembentukan gel, pembentukan film dan sebagainya. Salah satu
produk pati termodifikasi diantaranya adalah dekstrin.
Dekstrin adalah suatu produk hidrolisat parsial dari pati, berbentuk tepung
halus, bewarna putih sampai agak kekuningan. Dalam pembuatan dekstrin rantai
panjang pati dipotong oleh enzim atau katalis asam menjadi molekul rantai
pendek dengan jumlah unit glukosa antara 6 sampai 10 unit. Proses ini
mengakibatkan terjadinya perubahan sifat-sifat diantaranya menjadi larut pada
air dingin, kurang menyerap air, tekstur menjadi lembut dan daya rekat
meningkat (Soekarto et al. 1991).
Dekstrin sangat dibutuhkan dalam industri, baik industri pangan dan
industri non pangan. Kebutuhan dekstrin dan pati termodifikasi dari tahun ke
tahun terus meningkat, dan kebutuhan tersebut masih diimpor dari luar negeri.
Volume impor dekstrin dan pati termodifikasi Indonesia disajikan pada Tabel 1.
Bahan baku untuk pembuatan dekstrin umumnya dibuat dari pati
komersial seperti tapioka, jagung, sagu dan lain sebagainya. Dalam penelitian ini
akan dimanfaatkan batang kelapa sawit yang merupakan limbah dari perkebunan
menjadi pati dan dikonversi menjadi dekstrin. Hal ini dimaksudkan sebagai salah
satu upaya untuk mengurangi impor dekstrin Indonesia. Selain itu juga untuk
pembanding dalam penelitian ini juga dibuat dekstrin dari jenis pati komersial
yaitu pati sagu dan tapioka.
Tabel 1 Volume impor dekstrin dan pati termodifikasi Indonesia
Tahun Berat bersih (kg) Nilai (US $)
2001 87 927 717 50 184 576
2002 80 319 465 41 875 152
2003 78 752 720 34 064 818
2004 77 720 843 35 328 984
2005 93 070 990 44 020 497
Sumber : BPS (2001 - 2005)
Tujuan Penelitian
1. Mempelajari proses ekstraksi pati kelapa sawit dan mengkarakterisasi
pati kelapa sawit yang dihasilkan, dibandingkan dengan sagu dan
tapioka.
2. Mempelajari proses dekstrinisasi dari pati kelapa sawit, sagu dan tapioka
secara enzimatis dan asam
3. Membandingkan mutu dekstrin dari pati kelapa sawit, sagu dan tapioka.
Ruang Lingkup Penelitian
1. Kelapa sawit yang digunakan berasal dari limbah batang peremajaan
PTPN 2, Gohor Lama, Kabupaten Langkat, Sumatera Utara, berumur 25
tahun dan varietas Tenera.
2. Pati komersial sebagai pembanding sagu dan tapioka berasal dari industri
kecil di Bogor daerah Kedung Halang dan Pabrik Budi yang selanjutnya
dikeringkan dan disaring dengan saringan 80 mesh.
3. Proses dekstrinisasi secara enzimatis menggunakan α-amilase thermofil
TINJAUAN PUSTAKA
Potensi Batang Kelapa Sawit
Kegiatan replanting atau peremajaan tanaman kelapa sawit di Indonesia mulai berjalan secara besar-besaran pada awal tahun 1990-an karena pada
umumnya penanaman kelapa sawit secara komersial dilakukan pada awal tahun
1960. Diperkirakan rata-rata luas areal peremajaan pada kurun waktu tahun
2001-2005 mencapai 32 155 ha/tahun. Dari luas areal tersebut akan dihasilkan
batang hasil peremajaan 2 257 281 ton. Pada kurun waktu tahun 2006 – 2010,
rata-rata luas areal yang akan diremajakan seluas 89 965 ha. Dengan perkataan
lain, ada kenaikan lebih kurang sebesar 2,5 kali luas areal yang diremajakan
pada kurun waktu tahun 2001 – 2005. Pada kurun waktu tersebut batang hasil
peremajaan akan mencapai 6 315 543 ton. Data tersebut dapat dilihat pada
Tabel 2. Limbah kelapa sawit berupa batang hasil kegiatan peremajaan akan
bertambah pada kurun waktu berikut, karena penanaman kelapa sawit meningkat
pesat pada tahun 1990 (Guritno dan Darnoko 2003).
Tabel 2 Potensi batang kelapa sawit dari kegiatan peremajaan
Tahun Total luas areal
peremajaan (ha)1
Dihitung berdasarkan penambahan luas areal pada 25 tahun yang lalu 2
Dihitung berdasarkan 70,2 ton/ ha dari luas areal yang diremajakan
Pohon kelapa sawit yang diremajakan umurnya sudah lebih dari 25 tahun,
mempunyai tinggi 10-15 m dengan diameter batang berkisar antara 45 – 65 cm
yang diukur dari ketinggian 1,5 meter dari tanah. Bagian kulitnya mempunyai
ketebalan 3 – 3,5 cm (Susila 2003 ; Guritno dan Darnoko 2003).
Pati
Pati adalah cadangan karbohidrat dari tanaman, pati ini disimpan dalam
butiran granula yang ukuran diameter selnya berkisar 1 – 100 µm (Wurzburg,
1989). Pati secara alami terdapat dalam senyawa–senyawa organik yang
tersebar luas seperti di dalam biji-bijian, akar, batang dari tanaman yang berdaun
hijau yang disimpan sebagai energi selama dormansi dan perkecambahan
(Smith 1982).
Secara histologis, pati disimpan dalam bentuk plastid yang dinamakan
amiloplast atau kloroplast di dalam sel, Pati terdapat dalam bentuk ikatan dengan
air, lemak, silikat, serta senyawa-senyawa lainnya terutama fosfat. Dilihat dari
susunan kimianya, pati adalah polimer dari glukosa atau maltosa. Unit terkecil di
dalam rantai pati adalah glukosa yang merupakan hasil proses fotosintesa di
dalam bagian tubuh tumbuh-tumbuhan yang mengandung klorofil. Pembentukan
polimer yang lebih panjang dilakukan dengan bantuan D-enzim untuk amilosa
dan Q-enzim untuk amilopektin (Tjokroadikoesoemo 1986).
Pati adalah polimer yang seluruhnya terdiri dari unit D-glukosa, dengan
ikatan α-glikosidik. Berbagai macam pati tidak sama sifatnya, tergantung dari
panjang rantai C-nya, serta apakah lurus atau bercabang rantai molekulnya
(Wilbraham dan Matta 1992; Winarno 1997).
Pati terdiri dari dua fraksi yang dapat dipisahkan dengan air panas.
Fraksi terlarut disebut amilosa dan fraksi tidak larut disebut amilopektin. Amilosa
mempunyai struktur lurus dengan ikatan α-(1,4)-D-glikosidik, sedangkan
amilopektin mempunyai cabang dengan ikatan α-(1,6)-D-glikosidik sebanyak 4 –
5% dari berat total (Winarno 1997).
Amilosa merupakan homopolimer berantai lurus dengan ikatan α
(1,4)-glikosidik. Panjang rantainya bervariasi tergantung dengan jenis tanaman, secara
umum panjang rantai amilosa 500-2000 unit glukosa. Sedangkan amilopektin
terdiri dari molekul D-glukosa yang berikatan α-(1,4) dan juga mengandung
ikatan silang α-(1,6). Ikatan ini menyebabkan penampilan molekul amilopektin
O
berada di titik percabangan amilopektin. Setiap percabangan terdiri atas 25
sampai 30 unit D-glukosa. Rumus bangun dari amilosa dan amilopektin disajikan
pada Gambar 2 dan 3 berikut ini (Wilbraham dan Matta 1992; Smith 1982).
Gambar 1 Struktur rantai linier dari molekul amilosa
Gambar 2 Struktur molekul amilopektin.
Perbandingan antara amilosa dan amilopektin di dalam pati sangat
bervariasi, tergantung jenis tanaman asalnya. Pati yang kecil kandungan
amilosanya semakin lengket pati tersebut sedangkan pati yang kandungan
amilosanya tinggi berperan dalam pembentukan gel dan menghasilkan film yang
O
baik (Winarno 1997; Smith 1982). Perbandingan kandungan antara amilosa dan
amilopektin dari beberapa sumber pati disajikan pada Tabel 3 berikut ini.
Tabel 3 Kandungan amilosa dan amilopektin dari beberapa sumber pati
Sumber pati Amilosa (%, bb) Amilopektin (%, bb)
Jagung 28 72
Kentang 21 79
Gandum 28 72
Tapioka 17 83
Jagung waxy 0 100
Sorgum 28 72
Beras 17 83
Sagu 27 73
Garut 20 80
Amilomaize 50-80 20-50
Pati batang kelapa sawit mempunyai bentuk butiran (granula) agak bulat
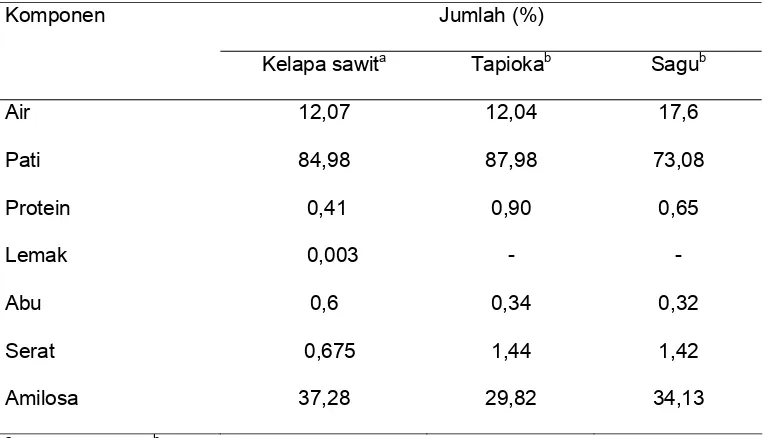
dan bersifat memadat ( truncated ). Ukurannya hampir sama dengan pati jagung dan waxymaize, tetapi bentuknya seperti pati tapioka. Komposisi pati kelapa sawit, tapioka dan sagu disajikan pada Tabel 4 berikut ini.
Tabel 4 Komposisi pati kelapa sawit, tapioka dan sagu
Jumlah (%) Komponen
Kelapa sawita Tapiokab Sagub
Air 12,07 12,04 17,6
Pati 84,98 87,98 73,08
Protein 0,41 0,90 0,65
Lemak 0,003 - -
Abu 0,6 0,34 0,32
Serat 0,675 1,44 1,42
Amilosa 37,28 29,82 34,13
Ukuran granula pati sangat bervariasi (2 – 100 µm) tergantung dari
sumber patinya. Sifat yang penting dari pengaruh ukuran granula pati adalah
perbedaan derajat gelatinisasi. Bila pati mentah dimasukan ke dalam air dingin,
granula patinya akan menyerap air dan membengkak. Namun demikian jumlah
air yang terserap dan pembengkakannya terbatas. Peningkatan volume granula
pati yang terjadi didalam air pada suhu 55 - 650C merupakan pembengkakan
yang sesungguhnya dan bersifat dapat kembali kebentuk pati semula. Granula
pati dapat dibuat membengkak luar biasa dan tidak dapat kembali lagi pada
kondisi semula. Perubahan tersebut disebut gelatinisasi (Winarno 1997).
Pada dasarnya mekanisme gelatinisasi terjadi melalui tiga tahapan yaitu :
(1) Penyerapan air oleh granula pati sampai batas yang akan mengembang
secara lambat dimana air secara perlahan-lahan dan bolak-balik berimbibisi ke
dalam granula, sehingga terjadi pemutusan ikatan hidrogen antara
molekul-molekul granula,(2) Pengembangan granula secara lambat karena menyerap air
secara cepat sampai kehilangan sifat birefringence, dan (3) Jika suhu terus naik molekul amilosa keluar dari granula (Swinkels 1985).
Bila suspensi pati dalam air dipanaskan, beberapa perubahan selama
terjadi gelatinisasi dapat diamati. Mula-mula suspensi pati yang keruh seperti
susu tiba-tiba mulai menjadi jernih pada suhu tertentu, tergantung jenis pati yang
digunakan. Terjadinya translusi larutan pati tersebut biasanya diikuti
pembengkakan granula. Bila energi kinetik molekul-molekul air menjadi lebih kuat
daripada daya tarik menarik antarmolekul pati di dalam granula, air dapat masuk
ke dalam butir-butir pati.
Suhu gelatinisasi tergantung juga pada konsentrasi pati. Makin kental
larutan, suhu tersebut makin lambat tercapai. Suhu gelatinisasi berbeda-beda
bagi tiap jenis pati dan merupakan suatu kisaran. Dengan viskosimeter suhu
gelatinisasi dapat ditentukan, misalnya jagung 62 – 720C, beras 68 – 780C,
gandum 54,5 - 640C dan tapioka 52 – 640C. Granula pati mempunyai sifat
merefleksikan cahaya terpolarisasi sehingga di bawah mikroskop terlihat kristal
hitam-putih. Sifat ini disebut birefregence. Pada waktu granula pati mulai pecah,
sifat birefregence ini akan menghilang (Winarno 1997).
Suhu gelatinisasi dapat ditentukan dengan Brabender Visco-amylograph,
dengan mikroskop elektron maupun mikroskop terpolarisasi yang didasari oleh
hilangnya sifat birefregence.
Alfa Amilase
Amilase merupakan enzim yang mempunyai aktivitas memecah molekul
pati, glikogen dan turunan polisakarida. Amilase menghidrolisis ikatan α-(1,4) dan
atau α-(1,6) glikosidik. Amilase yang dapat memecah ikatan α-(1,4) dibagi dua
yaitu (1) endo-enzim yang memecah ikatan α-(1,4) yang berada ditengah rantai
polimer, dan (2) ekso-enzim yang memecah ikatan α-(1,4)dari ujung polimer
(Judoamidjodjo 1989 ; Whitaker 1994).
Alfa amilase adalah endo-enzim yang bekerja memutuskan ikatan α-(1,4)
secara acak di bagian dalam molekul baik pada amilosa dan amilopektin. Karena
pengaruh aktivitasnya, pati terputus-putus menjadi dekstrin dengan rantai
sepanjang 6 – 10 unit glukosa. Jika waktu reaksi diperpanjang, dekstrin tersebut
dapat dipotong-potong menjadi campuran antara glukosa, maltosa, maltotriosa,
dan ikatan lain yang lebih panjang.
Secara umum α-amilase stabil pada pH 5,5 – 8,0; aktivitas optimum α
-amilase secara normal berada pada pH 4,8 – 6,5; tetapi bentuk kurva aktivitas
pH berbeda untuk enzim yang dihasilkan dari sumber berbeda. Amilase dari
Bacillus subtilis mempunyai aktivitas optimum pada kisaran pH 5 – 7, sedangkan amilase dari Bacillus stearothermophilus pada pH 3. Aktivitas α-amilase menurun secara cepat pada suhu diatas 500C, tetapi dengan adanya ion Ca2+ penurunan
aktivitas α-amilase pada suhu tersebut dapat diperlambat
Baciilus licheniformis menunjukkan spektrum pH yang luas diantara pH 5 dan 9. Enzim ini dapat dikatakan tidak bergantung kepada kalsium. Stabilitasnya
yang tinggi menyebabkan enzim ini dapat dimanfaatkan pada suhu sampai
1050C.
Alfa amilase mempunyai rantai peptida tunggal pada gugusan proteinnya
dan setiap molekul mengandung satu g atom Ca. Adanya kalsium yang berikatan
dengan molekul protein enzim, membuat enzim α-amilase bersifat relatif tahan
terhadap suhu, pH, dan senyawa seperti urea atau enzim-enzim protease.
Karena peranannya didalam industri, α-amilase dari berbagai sumber telah
Bacillus amyloliquefaciens dan Baciilus licheniformis dikenal menghasilkan enzim yang bersifat termostabil (Suhartono 1989).
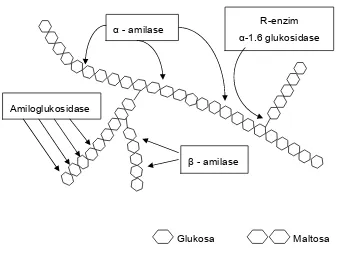
Aktivitas kerja enzim amilase terhadap ikatan yang terdapat pada
amilopektin disajikan pada Gambar 3 berikut (Pomeranz 1991).
Gambar 3 Pengaruh dari aktivitas enzim amilase pada amilopektin.
Hidrolisis amilopektin oleh α-amilase menghasilkan glukosa, maltosa dan
berbagai jenis α-limit dekstrin, yaitu oligisakarida yang teridiri dari empat atau
lebih residu glukosa yang mengandung ikatan α-1,6-glikosidik. Hidrolisis amilosa
oleh α-amilase terjadi melalui dua tahap. Tahap pertama adalah degradasi
menjadi maltosa dan maltotriosa yang terjadi secara acak. Degeredasi ini terjadi
sangat cepat diikuti pula dengan penurunan viskositas dengan cepat. Tahapan
kedua relatif lambat dengan pembentukan glukosa dan maltosa sebagai hasil
akhir.
β - amilase Amiloglukosidase
R-enzim
α-1.6 glukosidase
α - amilase
Likuifikasi Pati
Likuifikasi adalah proses dispersi granula pati yang tidak larut di dalam air
dan diikuti dengan hidrolisis parsial dengan menggunakan amilase termostabil.
Selain enzim dapat juga digunakan asam sebagai katalis. Likuifikasi merupakan
proses yang penting dan mendasar dalam menghidrolisis pati. Jika proses ini
tidak berlangsung dengan baik maka berbagai masalah akan muncul sepeti
sulitnya proses filtrasi larutan yang diproses. Proses likuifikasi yang baik penting
untuk keberhasilan proses sakarifikasi dan isomerisasi (Fogarty 1983; Taji 1988;
Olsen 1995).
Likuifikasi Pati dengan α-Amilase
Likuifikasi adalah tahap awal dari proses hidrolisis pati, misalnya pada
pembuatan dekstrin, glukosa dan sirup fruktosa. Dalam proses likuifikasi dengan
α- amilase akan terjadi pemutusan ikatan α-1,4 glikosidik. Kesempurnaan dan lama proses likuifikasi akan menentukan komposisi akhir produk likuifikasi
(Dziedzic dan Kearsley 1984).
Menurut Bigelis (1993) proses likuifikasi yang diawali dengan proses
gelatinisasi, dimana larutan pati yang sudah digelatinisasi mengandung 30 – 40
% bahan padatan ditambahkan α-amilase termostabil yang dihasilkan Bacillus licheniformis dapat bekerja pada pH 6,5 dan suhu 103 – 1070C selama 5 – 10 menit. Setelah itu suhu diturunkan menjadi 950C selama satu sampai dua jam
yang memungkinkan hidrolisis pati ini menjadi sirup dengan DE 0,5 – 1,5.
Hidrolisis dibiarkan terus berlangsung sampai mencapai DE 10 – 15. Proses
likuifikasi baik pada suhu lebih tinggi maupun lebih rendah tergantung pada
efisensi kerja dari heat-stable bacterial α- amilase.
Likuifikasi merupakan proses yang penting dan mendasar dalam proses
pengolahan pati dan bilamana proses ini tidak berlangsung dengan baik,
berbagai masalah seperti sulitnya filtrasi, turbilitas larutan yang diproses dan
lain-lain terjadi. Faktor yang paling penting untuk likuifikasi pati yang ideal yaitu
larutan pati yang mengandung α-amilase dipanaskan pada suhu 105 – 1070C
secepat mungkin (Taji 1988). Menurut Pomeranz (1991) pada proses likuifikasi
dengan α-amilase pati harus terlebih dahulu digelatinisasi, hal ini disebabkan α
-amilase mempunyai aktivitas yang rendah terhadap pati yang belum
Likuifikasi dengan α-amilase menyebabkan komponen amilosa
terhidrolisis menjadi produk glukosa, maltosa, maltotriosa, maltopentaosa dan
maltoheksosa. Pemecahan maltoheptosa menghasilkan maltoheksosa dan
glukosa, sedangkan maltooktaosa menjadi maltoheksosa dan maltosa. Likuifikasi
dengan α-amilase tidak dapat memutuskan ikatan α-1,4-glikosidik yang
berdekatan dengan ikatan α-1,6-glikosidik pada pati dan glikogen (Yamamoto
1988). Hidrolisis amilopektin akan menghasilkan glukosa, maltosa dan α- limit
dekstrin. Produk α- limit dekstrin dengan minimal empat residu glukosa masih
mempunyai ikatan glikosidik α-1,6 (Pomeranz 1991).
Likuifikasi Pati dengan Asam Klorida
Hidrolisis asam adalah suatu metode yang digunakan untuk
menghasilkan thin boiling starch. Perlakuan dengan asam lemah dari granula pati cenderung memotong ikatan α-D-glikosidik dari fraksi amilosa pati jagung,
menurunkan ukuran molekul dan viskositas pasta panas. Asam yang digunakan
biasanya HCl dan H2SO4 di dalam kondisi terkontrol. Sifat-sifat birefregence tidak terpengaruh, hal ini mengindikasikan bahwa proses hidrolisis cenderung
berlangsung di dalam daerah amorf daripada daerah kristalin dari granula.
Perlakuan hidrolisis asam memungkinkan pati untuk dimasak didalam sistem
padatan gula yang tinggi, karena retrogradible amylose ada dalam konsentrasi yang tinggi sehingga dapat diperoleh gel yang kuat (Smith 1982). Modifikasi
asam lebih lanjut akan menghasilkan dekstrin yang memiliki viskositas yang
rendah (Fleche 1985).
Pada likuifikasi ini, asam akan menghidrolisis ikatan glikosidik,
memendekkan rantai. Ikatan α-1,4 lebih mudah terhidrolisis daripada ikatan α
-1,6. Hidrolisis asam lebih mudah menyerang daerah amorf dibandingkan dengan
daerah kristalin. Pada daerah kristalin, struktur linier dengan ikatan α-1,4 lebih
tahan terhadap asam. Hal ini disebabkan bahwa daerah tersebut tersusun sangat
rapat sehingga sukar dimasuki air atau asam. Bagian daerah amorf walaupun
tersusun dari ikatan α-1,6 tetapi merupakan daerah yang kurang padat, sehingga
dapat ditembus oleh air dan selanjutnya memudahkan penetrasi asam untuk
menghidrolis pati (Wurzburg 1986).
Dalam proses likuifikasi asam, akan terjadi pemutusan ikatan –C-O-C-
dengan menghasilkan gula dan beberapa polimernya. Bila diteruskan proses
polimer-polimer tersebut dihidrolisa menjadi glukosa. Asam memecah pati secara
acak dan gula yang terbentuk sebagian besar merupakan gula pereduksi
(Wurzburg 1986).
Penggunaan asam pekat pada proses hidrolisis membutuhkan biaya yang
lebih mahal dan peralatan yang tahan korosi dibanding dengan penggunaan
asam encer. Di samping itu hidrolisis dengan asam pekat dapat mempercepat
proses hidrolisis akan tetapi menurunkan hasil hidrolisis karena glukosa lebih
mudah diuraikan oleh asam pekat. Penggunaan asam encer memperlambat
proses hidrolisis karena adanya daya tahan dari kristal pati, akan tetapi
mengurangi proses penguraian glukosa oleh asam encer. Dari beberapa
penelitian menyatakan bahwa penggunaan HCl dengan konsentrasi 0,1 % dalam
proses likuifikasi menunjukkan hasil yang optimal (Ega 2002).
Hidrolisis asam mempunyai kelemahan antara lain yaitu diperlukan
peralatan yang tahan korosi, menghasilkan sakarida dengan spektra-spektra
tertentu saja karena katalis asam menghidrolisis secara acak. Kelemahan lain,
jika nilai dekstrosa ekuivalen ditingkatkan, disamping terjadi degradasi
karbohidrat juga terjadi rekombinasi produk degradasi yang yang dapat
mempengaruhi warna, rasa, bahkan menimbulkan masalah teknis (Judoamidjojo
1989).
Dekstrin
Pengertian dan Klasifikasi Dekstrin
Dekstrin adalah suatu produk yang merupakan hasil modifikasi pati
melalui proses hidrolisa asam, enzimatis dan pemanasan kering (Wurzburg
1986). Menurut Somaatmadja (1984) dekstrin adalah oligosakarida (beberapa
monosakarida) yang dapat diperoleh dengan menghidrolisis pati (polisakarida).
Dekstrin murni berupa serbuk (bubuk), bewarna putih atau hampir putih, tidak
mempunyai rasa, tidak berbau dan dapat larut dalam air dingin. Berdasarkan
Standar Nasional Indonesia (1992) dekstrin didefinisikan sebagai salah satu
produk hidrolisis pati, berbentuk serbuk amorf, bewarna putih sampai
kekuning-kuningan.
Pengertian dekstrin sangat luas mencakup setiap produk degradasi pati
yang diperoleh secara kimia maupun enzimatis, tetapi secara praktis kata
pirokonversi pati. Pirokonversi adalah proses pemanasan kering pati, produknya
terdiri dari tiga kelompok yaitu dekstrin putih, dekstrin kuning dan British gum (Fleche, 1985).
Berdasarkan tahapan pembentukan dalam proses hidrolisis pati, dikenal
tiga jenis dekstrin yaitu amilodekstrin, eritrodekstrin dan akrodekstrin. Pada tahap
awal konversi akan dihasilkan amilodekstrin yang memiliki sifat larut dalam air.
Amilodekstrin akan memberikan warna biru apabila direaksikan dengan larutan
iodium. Konversi berikutnya dihasilkan jenis dekstrin yang kedua yaitu
eritrodekstrin yang akan memberikan warna merah kecoklatan bila direaksikan
dengan larutan iodium. Tahap terakhir dari konversi dihasilkan adalah
eritrodekstrin yang apabila ditetesi dengan iodium tidak akan memberikan warna
(Garard 1977).
Proses Dekstrinisasi
Proses dekstrinisasi pati dapat dilakukan dengan tiga cara yaitu (a)
hidrolisis dengan α-amilase, (b) hidrolisis dengan asam klorida, (c) pemanasan
kering (Satterwaite dan Iwinski 1973 ; Fleche 1985 ; Wurzburg 1986).
1. Hidrolisis dengan α-amilase
Secara umum produksi dekstrin dilakukan proses likuifikasi dengan α
-amilase dari bakteri, kemudian inkubasi dengan suhu 95 – 970C. Lamanya
inkubasi tergantung dari jenis produk yang diinginkan, selanjutnya diikuti dengan
proses penjernihan larutan pati terlikuifikasi, dan dikeringkan dengan spray drying. Proses Dekstrinisasi pati secara hidrolisis dengan α-amilase disajikan pada Gambar 5.
Produksi dekstrin dengan hidrolisis α-amilase berlangsung dalam dua
tahap, pemanasan bubur pati pada suhu 1000C atau lebih tinggi untuk
mengembangkan dan menggelatinisasi pati diikuti dengan hidrolisis enzimatis
pada suhu 80–950C. Waktu yang dibutuhkan untuk menghasilkan dekstrin antara
2 – 4 jam (Pithcer 1980).
Alfa amilase komersial yang berasal dari Bacillus licheniformis tahan terhadap suhu tinggi. Enzim ini aktif dan stabil pada proses likuifikasi larutan pati
sampai suhu 1100C, dikenal dengan nama dagang Termamyl (Novo Enzyme)
(Judoammidjojo 1989). Reaksi hidrolisis α-amilase termostabil tersebut disajikan
α-amilase
Pati + n (H2O) G1 + G2 + G3 + G4 + G5 + …..
Termostabil + Oligosakarida bercabang
Tahapan hidrolisis α-amilase termostabil yang berasal dari Bacillus licheniformis terhadap pati adalah sebagai berikut ; pada tahap pertama amilosa dihidrolisis menjadi G5 – G9 dalam jumlah yang lebih banyak dari pada G2 dan
G3. pada tahap berikutnya terbentuk G1 dan G5 dalam jumlah yang meningkat,
sementara pembentukan G6 dan G9 menurun. Cara hidrolisis α-amilase pada
amilopektin hampir sama dengan amilosa (Endo 1988).
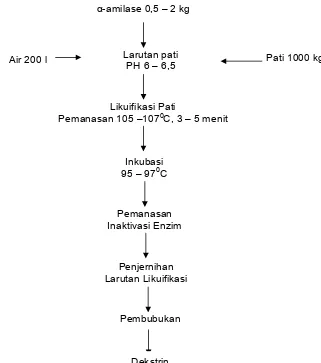
Gambar 4 Proses dekstrinisasi pati dengan α-amilase (Taji, 1988).
Turunan pati yang diperoleh melalui proses likuifikasi mempunyai nilai
komersial sebagai bahan pangan. Produk mempunyai nilai DE sekitar 10 dan
dijual sebagai maltodekstrin, yang akan membentuk karbohidrat dengan Larutan pati
PH 6 – 6,5 Pati 1000 kg
α-amilase 0,5 – 2 kg
Pembubukan Pemanasan Inaktivasi Enzim
Inkubasi 95 – 970C
Penjernihan Larutan Likuifikasi
Likuifikasi Pati
Pemanasan 105 –1070C, 3 – 5 menit Air 200 l
komposisi 3 % maltosa, 4 % maltotriosa dan 93 % tetraosa atau polisakarida
berukuran besar (Bigelis 1993).
Maltodekstrin dapat dihasilkan dengan hidrolisis dispersi pati secara
enzimatis maupun asam, biasanya dijelaskan dengan nila dekstrosa ekuivalen
(DE). Nilai DE ini terkait dengan derajat polimerisasi (DP) dengan formula DE =
100/DP. Maltodekstrin didefinisikan sebagai produk dengan nilai DE kurang dari
20, maltodekstrin dengan nilai DE terendah bersifat tidak higroskopis sedangkan
dengan nilai DE tertinggi cenderung menyerap air. Maltodekstrin bersifat lunak
dan tidak berasa manis dan sangat baik sumbangannya terhadap sistem pangan
(BeMiller dan Whistler 1996).
2. Hidrolisis dengan Asam Klorida
Pembuatan dekstrin dengan hidrolisis asam dilakukan dengan
memanaskan bubur pati didalam larutan asam secara perlahan-lahan sampai
pada derajat konversi yang diinginkan. Selanjutnya larutan dinetralisasi kemudian
didinginkan dan selanjutnya dikeringkan pada roll panas atau spray dryer (Satterwaite dan Iwinski 1973). Somaatmadja (1984) membuat dekstrinisasi
basah dengan katalis asam yaitu dengan merendam pati dalam larutan asam
klorida encer (10%) selama 24 jam. Dan setelah asam dipisahkan, pati
dikeringkan sampai sisa-sisa asam menguap dan selanjutnya digiling.
Proses dekstrinisasi pati dengan hidrolisis katalis HCl, terlebih dahulu
dilakukan proses likuifikasi. Proses likuifikasi asam dilakukan dengan sistem
curah, pada pH 1,8 sampai 2,0 dengan HCl. Pati yang telah diasamkan
dipanaskan pada suhu 900C selama 30 menit kemudian dimasak pada pressure cooker pada suhu 120 – 1400C sampai pemecahan pati menjadi sempurna. Tingkat degradasi pati dapat diukur dari nilai DE dari Produk yang dilikuifikasi,
dikontrol dengan mengatur waktu di pressure cooking. Nilai DE diatas 3 diperoleh dengan mengontrol laju alir didalam alat pengkonpersi. Tujuannya untuk
mendapat produk dengan nilai DE sedang, nilai DE yang rendah akan
menghasilkan produk yang akan mengalami retrogradasi. Nilai DE yang tinggi
akan menurunkan produk akhir glukosa (Fullbrook 1984).
Katalis asam yang sering digunakan dalam proses pembuatan dekstrin
adalah asam klorida. Hal ini disebabkan karena aktivitas HCl yang tinggi,
biayanya murah, bersifat volatil. Pada saat proses dekstrinisasi berlangsung
(Kennedy dan Fischer 1984). Konsentrasi HCl yang digunakan tergantung pada
derajat konversi yang diinginkan, untuk praktisnya dapat digunakan 0,1 – 1%
(Fleche 1985).
3. Pemanasan Kering
Dekstrin yang dihasilkan dengan cara hidrolisis asam atau pemanasan
kering (roasting) disebut pirodekstrin (Satterwaite dan Iwinski 1973). Prosesnya disebut dengan pirodekstrin, yaitu perlakuan pati yang diasamkan kering dengan
menggunakan panas (Fleche 1985). Prosesnya dilakukan dengan pemanasan
pati kering sambil diaduk, kemudian disemprot dengan asam klorida dan sulfat.
Derajat hidrolisisnya tergantung dari waktu, suhu, dan pH dari proses konversi
(Smith 1982).
Secara umum berdasarkan sifat dan kondisi pembuatannya pirodekstrin
dapat diklasifikasikan menjadi tiga jenis yaitu dekstrin putih, dekstrin kuning dan
British gum. Kondisi dan sifat dekstrin disajikan pada Tabel 5 berikut ini.
Tabel 5. Karakteristik dan sifat pirodekstrin
Karakteristik Dekstrin Putih Dekstrin Kuning Britihs Gum
Suhu Pemanasan
Jumlah Katalis Tinggi Medium Rendah
Kelarutan Rendah – tinggi Tinggi Rendah-tinggi
Viskositas Rendah – tinggi Rendah Rendah-tinggi
Warna Putih – krem
Kekuning-kuningan-gelap
Terang – gelap
Sumber : Ruterlberg dan Solarek (1984)
Jenis pirodekstrin ini berbeda dalam cara perlakuan pati sebelum
dipanaskan, cara dan tingkat pemanasan, dan sifaf-sifat produk yang dihasilkan.
Secara umum dekstrin putih dibuat dengan konversi pada suhu rendah dan pH
yang tergantung kecepatan proses konversi tanpa pembentukan warna yang
berlebihan. Dekstrin kuning merupakan produk yang terkonversi lebih tinggi yang
lain dikonversi pada pH yang tinggi dan suhu yang tinggi untuk konversinya,
sehingga warna British gum lebih gelap daripada dekstrin putih (Wurzburg 1986). Prinsip pembuatan dekstrin adalah menghidrolisis molekul-molekul pati
yang besar menjadi fraksi-fraksi yang lebih kecil. Pemanasan dan penggunaan
asam akan menggunting ikatan-ikatan α-D-glikosidic pada pati sehingga
didapatkan monomer-monomer glukosa (Smith, 1982). Proses pirokonversi,
pengunaan panas selain untuk pemotongan ikatan α-D-glikosidik juga untuk
mengurangi kadar air pati. Pengurangan air ini akan mencegah proses konversi
dekstrin lebih lanjut, dekstrin yang dihasilkan harus segera dikeringkan.
Proses pembuatan dekstrin dengan pemanasan kering dilakukan empat
tahap meliputi persiapan bahan, pemanasan pendahuluan, pirokonversi atau
pemanasan lanjut, dan pendinginan.
Persiapan bahan
Pada tahap persiapan, pati diberi katalis asam. Jumlah asam yang
diberikan tergantung dari sifat pirodekstrin yang diinginkan, kandungan air pati,
jenis pati dan peralatan yang digunakan untuk pengeringan awal dan
pemanasan. Biasanya larutan asam disemprotkan ke pati dengan pengadukan
secara horizontal dan vertikal. Pengadukan ini bertujuan untuk mendistribusikan
asam ke seluruh bagian pati hingga homogen (Wurzburg 1986; Somaatmadja
1970).
Pemanasan pendahuluan
Pemanasan pendahuluan dapat dilakukan atau tidak, tergantung dari
jenis pirodekstrin yang akan dihasilkan atau peralatan yang digunakan. Tujuan
dari pemanasan pendahuluan untuk mengurangi kandungan air yang terdapat di
dalam pati sehingga proses reaksi hidrolisis berkurang. Hal ini penting untuk
pembuatan dekstrin kuning. Berbeda halnya dalam pembuatan dekstrin putih dan
British gum, reaksi hidrolisis diperlukan untuk menentukan sifat-sifat produk yang diinginkan. Pemanasan pendahuluan dapat digabungkan dengan proses
pirokonversi yang dilakukan dengan pemanasan pati asam dilakukan secara
lambat, pengadukan yang kuat dan dialirkan udara yang maximum untuk
menghilangkan air. Pemanasan pendahuluan juga dapat dilakukan terpisah dari
proses pirokonversi.
Pirokonversi
Pirokonversi dilakukan dengan alat pemasakan yang dapat bergerak
pengaduk. Panas yang digunakan berupa pemanasan langsung (direct heat) maupun dengan sistem jacket pemanas.
Suhu dan waktu konversi bervariasi tergantung kepada jenis pirodekstrin
yang dihasilkan dan bentuk alat yang digunakan. Suhu pemanasan bervariasi
dari 100 sampai lebih dari 2000C, waktu pemanasan bervariasi dari beberapa
menit sampai beberapa jam. Secara umum dekstrin putih cenderung dibuat pada
suhu rendah dan waktu yang singkat sedangkan dekstrin kuning dan British gum memerlukan waktu reaksi yang lama dan suhu yang tinggi. Kadar air dekstrin dari
proses konversi dapat dicapai 0 – 5 % (Wurzburg 1986).
Pendinginan
Dekstrin yang dihasilkan dari proses pirokonversi harus segera
didinginkan dengan cara memasukkan dekstrin panas kedalam mixer pendingin
atau konveyor yang dilengkapi dengan jaket pendingin. Tujuan proses
pendinginan adalah untuk mencegah konversi lebih lanjut dari dekstrin.
Apabila pH konversi sangat rendah maka dilakukan penetralan asam
untuk mencegah konversi lebih lanjut. Netralisasi dilakukan dengan
pencampuran kering yang menggunakan reagen alakali amonium karbonat dan
garam fosfat. Kelembaban dekstrin pada akhir konversi berkisar 0,5 sampai 2 –3
%. Dekstrin dilembabkan dengan membiarkannya di udara terbuka sampai
tingkat kelembaban 5 – 12 % sebelum pengemasan (Fleche 1985; Wurzburg
1986).
Kimia Konversi
Perubahan - perubahan kimia yang terjadi pada pati selama proses
dekstrinisasi adalah kompleks dan belum sepenuhnya dipahami. Terdapat tiga
reaksi kimia yang terjadi yaitu hidrolisis, transglukosidasi dan repolimerisasi
(Wurzburg 1986).
Reaksi hidrolisis akan mengakibatkan pemotongan ikatan α-D-(1,4) dan
α-D-(1,6) dalam pati selama tahap pemanasan pendahuluan dan tahap awal proses dekstrinisasi. Dalam reaksi ini akan terjadi penurunan berat molekul pati,
viskositas dan peningkatan gugus reduksi yang disebakan oleh hidrolisis ikatan
glikosidik. Mekanisme hidrolisis pati oleh enzim telah dijelaskan dalam proses
likuifikasi dengan α-amilase. Mekanisme hidrolisis dengan asam disajikan pada
O
Transglukosidasi adalah reaksi yang mengakibatkan hilangnya ikatan
glukosida α-D- (1,4) dari proses hidrolisis yang diikuti dengan penggabungan
fragmen-fragmen yang dekat dengan gugus bebas yang menghasilkan struktur
bercabang (Wurzburg 1986).
Transglukosidasi merupakan reaksi yang penting dalam pirodekstrinisasi.
Hal ini mungkin karena reaksi tersebut merupakan reaksi perubahan intermolekul
pada beberapa ikatan α-D-(1,4)-glikosidik pati asli yang diubah ke ikatan α
-D-(1,6). Mekanisme reaksinya disajikan pada Gambar 6 berikut ini.
Gambar 5 Mekanisme reaksi transglukosidasi (Satterwaite dan Iwinski 1973).
Glukosa dapat mengalami proses polimerisasi pada suhu tinggi dengan
adanya katalis asam. Pembuatan dekstrin kuning membuktikan terjadinya
repolimerisasi glukosa. Hal ini diduga dari penurunan kadar gula pereduksi,
kecilnya peningkatan viskositas serta penurunan jumlah dekstrin yang larut
dalam campuran 90% etanol dan 10% air. Walaupun proses repolimerisasi ini
belum sepenuhnya diyakini, namun proses ini terjadi dalam pembuatan dekstrin
kuning (Wurzburg 1986).
Dekstrin kuning dihasilkan dengan pemanasan pati kering yang
diasamkan sampai mencapai suhu yang lebih tinggi dari suhu dekstrin putih. Bila
kandungan air turun dibawah 3 %, proses hidrolisis tidak lagi berlangsung.
sebaliknya molekul-molekul yang terfragmentasi oleh reaksi hidrolisis kembali
membentuk struktur yang bercabang. Pengabungan kembali fragment tersebut
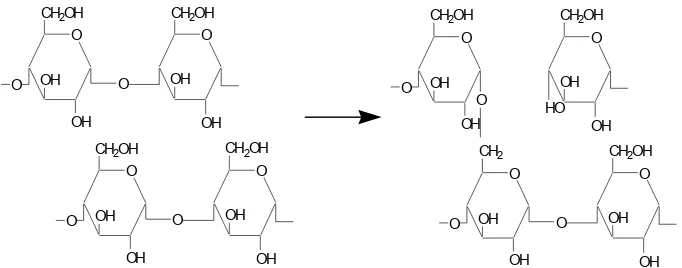
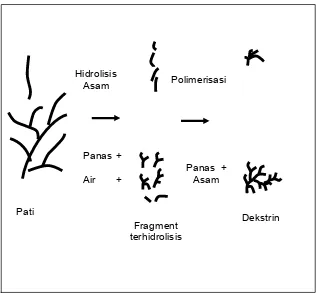
bersifat acak. Mekanisme reaksi hidrolisis asam dan repolimerisasi disajikan
pada Gambar 7.
Beberapa bukti memperlihatkan bahwa produk dekstrin kuning memiliki
berat molekul yang lebih tinggi dari pati asalnya, tetapi sebagian molekulnya kecil
Hidrolisis
Asam Polimerisasi
Panas +
Air +
Panas + Asam
Dekstrin Fragment
terhidrolisis Pati
Karena panjang cabang sangat pendek, dekstrin kuning memperlihatkan tidak
adanya sifat retrogradasi dalam larutan yang konsentrasinya tinggi (Pomeranz
1991). Pada pembuatan British gum, reaksi yang terjadi adalah reaksi hidrolisis pada tahap awal dekstrinisasi. Hidrolisis disebabkan oleh adannya residu air
yang terdapat didalam pati dan sejumlah asam yang terbentuk selama
pemanasan, sebagian besar proses transglukosidasi (Satterwaite dan Iwinski
1973).
Gambar 6 Mekanisme reaksi hidrolisis asam dan repolimerisasi. (Pomeranz 1991)
Penggunaan Dekstrin
Dekstrin dapat digunakan dalam industri pangan dan non pangan. Dalam
bidang pangan dekstrin digunakan sebagai pembentuk film dan edible adhesive untuk menggantikan gum arab pada produk-produk tertentu seperti pelapis
kacang dan candy. Dekstrin juga digunakan sebagai bahan pengisi dan pembawa aroma yang disemprot kering (Smith 1982). Dekstrin dapat juga
Maltodeksrin dalam industri pangan dimanfaatkan untuk meningkatkan
penerimaan konsumen terhadap produk pangan cair, sebagai bahan pembantu
dalam proses pengeringan dengan pengeringan semprot, dan maltodekstrin DE
rendah dapat digunakan sebagai bahan pengisi dan aditif dalam proses
pengeringan bahan makananan yang besifat higroskopis (Bigelis 1993).
Penggunaan dekstrin dalam bidang non pangan meliputi industri bahan
perekat, industri kertas dan tekstil dan farmasi (Satterwaite dan Iwinski 1973;
Somaatmadja 1984).
Dekstrin mempunyai daya rekat yang sangat baik sehingga banyak
digunakan dalam pembuatan berbagai perekat seperti glokul, glotun dan
sebagainya. Perekat (lem) yang dihasilkan dari dekstrin dapat dicampurkan
dengan berbagai resin sintetik pada pH netral utnuk menghasikan perekat karton
yang dilapisi berbagai bahan seperti alumminium foil. Dekstrin ini juga dapat digunakan untuk perekat rokok (BAT) dan Faroka (Somaatmadja 1984). Selain
itu dekstrin kuning dapat dijadikan sebagai perekat yang lembab pada prangko,
label dan amplop (Pomeranz 1991). Dalam industri kertas desktrin digunakan
sebagai bahan pelapis dan membentuk permukaan yang halus.
Dalam industri farmasi, dekstrin digunakan sebagai carrier atau pembawa. Hal ini disebabkan karena dekstrin mudah larut dalam air dingin,
sehingga tablet yang menggunakan dekstrin mudah larut dalam air ludah bila
tablet tersebut dimakan (Somaatmadja 1984).
Dalam industri tekstil, dekstrin digunakan dalam finishing kain mori (kain putih) dimana apabila hendak dicetak harus dihilangkan kanjinya terlebih dahulu.
Penghilangan dekstrin dalam kain putih lebih mudah dilakukan dibandingkan
dengan penggunaan pati (polisakarida). Dekstrin dapat dihilangkan dengan air
dingin, sedangkan pati dihilangkan dengan air panas dan sedikit asam klorida
BAHAN DAN METODOLOGI PENELITIAN
Tempat dan Waktu Penelitian
Penelitian dilaksanakan di Laboratorium Kimia, Fakultas Pertanian
Universitas Sumatera Utara, Laboratorium Teknik Kimia, Bioindustri, LDIT
Departemen Teknologi Industri Pertanian dan Pusat Antar Universitas Pangan
dan Gizi Institut Pertanian Bogor. Penelitian ini dilaksanakan 24 bulan sejak
Februari 2004.
Bahan dan Alat
Bahan baku yang digunakan dalam penelitian ini adalah batang kelapa
sawit yang berasal dari peremajaan PTPN 2 Gohor Lama Kabupaten Langkat
Universitas Sumatera Utara, berumur 25 tahun dan varitas Tenera. Selain itu
digunakan juga pati sagu industri kecil (Kedung Halang) Bogor dan tapioka
komersial (Pabrik Budi Bogor) sebagai pembanding. Enzim yang digunakan
adalah α-amilase dengan merek dagang Termamyl (Novo) dan HCl (katalis
proses hidrolisis).
Bahan kimia analisa yang digunakan untuk penelitian ini adalah H2SO4, H2BO3, NaOH, Pereaksi KI (Kadar amilosa), pereaksi Somoygi (kadar pati), larutan lugol, larutan iod, larutan kanji, DNS, kertas saring Whatman No. 41,
alkohol dan akuades.
Peralatan dan instrumentasi yang digunakan adalah pemarut, ember, kain
saring dan plastik, blender (alat ekstraksi). Peralatan proses desktrinisasi adalah
water bath shaker, ruang asam, pengaduk kaca dan sarung tangan. Peralatan analisa yang digunakan antara lain labu Kjeldahl, Soxhlet, Oven, Biuret,
desikator, spektrofotometer UV 200 S, penangas air, pH meter, mixer,
mikropipet, pengaduk magnetik, saringan 80 mesh, timbangan kasar, timbangan
analitis, Brookfield viscometer, tanur, pinggan datar, Kett whitenessmeter,
Metode Penelitian
Penelitian ini terdiri lima tahap, yaitu ekstraksi pati kelapa sawit,
karakterisasi pati kelapa sawit, sagu dan tapioka. Selanjutnya dekstrinisasi pati
kelapa sawit, sagu dan tapioka dilakukan melalui hidrolisis enzimatis dan asam.
Pada proses dekstrinisasi dilakukan pengamatan waktu dekstrinisasi. Waktu
proses tersebut digunakan dalam pembuatan dekstrin dan selanjutnya
karakterisasi produk dekstrin.
Ekstraksi Pati Kelapa Sawit.
Pembuatan pati kelapa sawit dilakukan dengan membelah batang kelapa
sawit kemudian memisahkan kulit keras dan empelurnya. Empelur tersebut
diserut hingga jadi serbuk kayu. Serbuk kayu ditambah air, selanjutnya diperas
kemudian disaring dengan kain saring. Ampasnya dibuang sedangkan air yang
mengandung pati diendapkan selama 3 jam, kemudian dihasilkan pati basah.
Pati basah tersebut dicuci dengan menambahkan air dan diendapkan selama 3
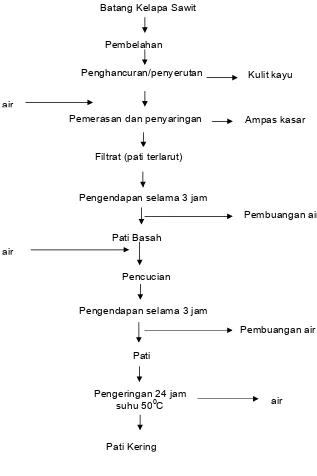
jam kemudian pati basah tersebut dikeringkan dengan oven pada suhu 500C sampai kadar air pati menjadi ±10 %. Proses pembuatan pati kelapa sawit dapat
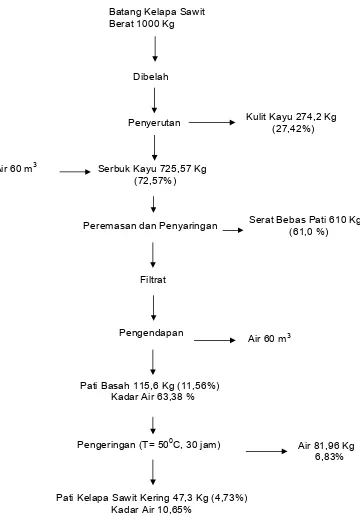
dilihat pada Gambar 7. Pohon kelapa sawit yang dipotong serbuk gergajiannya
diuji dulu kandungan patinya yaitu dengan penambahan air dan diremas dan
disaring selanjutnya diendapkan pada erlenmeyer 250 ml. Jika mengandung pati
proses ekstraksi dilanjutkan.
Karakterisasi Pati
Pati kelapa sawit yang diperoleh dari ekstraksi batang kelapa sawit,
dikarakterisasi meliputi komposisi kimia (kadar air, kadar abu, kadar serat, kadar
protein, kadar lemak, kadar amilosa dan kadar pati), sifat fisik (derajat putih,
bentuk dan ukuran granula pati dan sifat amilografi) demikian juga dilakukan
terhadap pati sagu dan tapioka. Tata cara analisa dapat dilihat pada Lampiran 1.
Pengaruh waktu Proses Terhadap Laju Dekstrinisasi
Penentuan waktu proses dekstrinisasi hidrolisis pati secara enzimatis dan
asam disajikan pada Gambar 8 dan 9. Untuk masing-masing proses dekstrinisasi
pengamatan waktunya dilakukan setiap 15 menit sekali selama tiga jam
nilai DE dan DP. Pengamatan ini dilakukan pada saat kondisi substrat dalam
bentuk hidrolisat pati.
Inaktivasi untuk desktrin enzimatis dilakukan dengan penambahan NaOH
0,1 N kemudian dinetralkan dengan penambahan HCl 0,1 N, sedangkan dalam
proses hidrolisis asam, penghentian proses hidrolisis dilakukan dengan
penambahan NaOH 0,1N sampai pH hampir mendekati netral.
Gambar 7 Tahapan proses ekstraksi pati kelapa sawit ( Modifikasi Ginting 1995)
Penghancuran/penyerutan Batang Kelapa Sawit
Pembelahan
air
Pemerasan dan penyaringan Ampas kasar
Filtrat (pati terlarut)
Pengendapan selama 3 jam
Pati Basah
Pencucian
Pengendapan selama 3 jam
Pati
Pengeringan 24 jam suhu 500C
Pati Kering air
Kulit kayu
air
Pembuangan air
Proses Pembuatan Dekstrin
Pada penelitian ini akan dikaji pengaruh proses dekstrinisasi pati kelapa
sawit (hidrolisis enzim dan asam) terhadap produk dekstrin yang dihasilkan,
sebagai pembanding digunakan pati sagu dan tapioka.
1. Dekstrinisasi dengan Hidrolisis enzimatis
Pada proses ini masing-masing pati (substrat) dibuat dengan konsentrasi 30 % (b/b) substrat kering, sedangkan untuk dosis α-amilase yang digunakan 0,7 U/g dari pati kering. Enzim yang digunakan pada penelitian ini optimal pada suhu
950C, pH 5,2 dan memiliki aktivitas 1478,12 U/ml enzim (Gunawan 2004). Proses pembuatan dekstrin, dilakukan dengan mensuspensikan jenis pati sesuai dengan
perlakuan diatas, lalu diaduk sampai merata. Keasaman suspensi diatur pada
kisaran pH 5,2 dengan penambahan NaOH 0,1 N melalui bantuan pH meter.
Kemudian ditambahkan α-amilase, suspensi dilikuifikasi pada suhu 950C sambil terus diaduk dan waktunya sesuai dengan proses dekstrinisasi. Pengadukan
dilakukan secara manual, setelah lewat gelatinisasi water bathnya ditutup dan
lamanya sesuai dengan proses likuifikasi. Proses likuifikasi dihitung menit ke nol
pada saat suspensi pati dihidrolisis dalam water bath shaker yang sudah mencapai suhu 950C. Proses ini merupakan modifikasi dari penelitian Griffin dan Brooks (1989).
Proses inaktivasi enzim dilakukan dengan pendinginan pada suhu -40C selama 60 menit. Dekstrin cair yang diperoleh dituang setebal lima mm kedalam
loyang aluminum yang sudah dilapisi dengan plastik, kemudian dikeringkan
dalam oven pada suhu 500C selama dua hari. Setelah kering dekstrin tersebut dihaluskan dengan blender kemudian saring dengan ayakan 80 mesh. Proses
pembuatan dekstrin hidrolisis secara enzimatis dapat dilihat pada Gambar 8.
2. Dekstrinisasi dengan Hidrolisis HCl
Proses dekstrinisasi ini dilakukan dengan pembuatan suspensi pati
dengan konsentrasi 30% (b/b) substrat kering, konsentrasi HCl yang digunakan
0,5 % dari pati kering. Suspensi pati kemudian dilikuifikasi pada 950C dengan pengadukan manual dan lamanya sesuai dengan waktu dari pengamatan
pendahuluan. Setelah proses likufikasi pHnya dinetralkan, dekstrin cair yang
diperoleh dituang setebal 5 mm kedalam loyang aluminum yang sudah dilapisi
hari. Setelah kering dekstrin tersebut dihaluskan dengan blender kemudian
disaring dengan ayakan 80 mesh. Proses dekstrinisasi secara hidrolisis dengan
katalis asam klorida dapat dilihat pada Gambar 9.
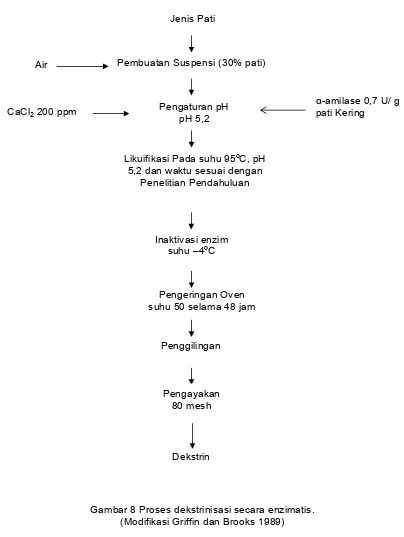
Gambar 8 Proses dekstrinisasi secara enzimatis. (Modifikasi Griffin dan Brooks 1989)
α-amilase 0,7 U/ g pati Kering
Inaktivasi enzim suhu –4oC
Likuifikasi Pada suhu 95oC, pH 5,2 dan waktu sesuai dengan
Penelitian Pendahuluan Air
Penggilingan Pengeringan Oven suhu 50 selama 48 jam
Pengaturan pH pH 5,2
Pembuatan Suspensi (30% pati)
Dekstrin Pengayakan
80 mesh Jenis Pati
Gambar 9 Proses dekstrinisasi secara hidrolisis asam. (Modifikasi Ega 2002).
Dalam proses hidrolisis asam dilakukan penambahan HCl dengan cara
mencoba berbagai konsentrasi HCl 0,25-0,75 % dengan konsentrasi suspensi
pati 30% (b/b) berat kering pati. Kemudian ditetapkan konsentrasi HCl 0,5 % pati
kering kemudian dilakukan hidrolisis terhadap ketiga jenis pati. Penambahan HCl
ini dilakukan pada saat sebelum proses likuifikasi. Proses likuifikasi dihitung Penambahan NaOH 0,1 N Untuk
Penghentian Hidrolisis Likuifikasi pada suhu 95oC Waktu sesuai dengan Penelitian
Pendahuluan Air
Penggilingan Pengeringan Oven suhu
50oC selama 48 jam Penambahan HCl 0,5%
dari berat Pati Kering Pembuatan Suspensi (30% pati)
Dekstrin Pengayakan
menit ke-nol pada saat suspensi pati dihidrolisis dalam water bath shaker yang sudah mencapai suhu 950C. Proses ini merupakan modifikasi dari penelitian Ega (2002).
Rancangan penelitian yang digunakan adalah rancangan acak lengkap
faktor tunggal. Faktor yang diamati yaitu jenis pati meliputi pati kelapa sawit,
sagu dan tapioka. Penelitian dilakukan pada pembuatan dekstrin enzimatis dan
asam yang dilakukan secara terpisah dan dibandingkan sesuai dengan nilai DE
dan DP yang terbentuk. Ulangan dilakukan sebanyak tiga kali, model rancangan
percobaan adalah sebagai berikut.
Y(ijk) = µ + i + εij
Dengan : i=1, 2, 3…,t dan j = 1,2…,r
Y(ijk) = Respon hasil pengaruh dari jenis pati ke-i dan ulangan ke-j. µ = Rataan umum.
i = Pengaruh jenis pati taraf ke-i.
εij = Galat percobaan dari jenis pati ke-ipada ulangan ke-j. (Montgomery 1991).
Karakterisasi Dekstrin.
Dekstrin yang dihasilkan dikarakterisasi dan dibandingkan dengan SNI
dekstrin untuk industri pangan (SNI 01-2593-1992) dan non pangan (SNI
06-1451-1989). Sifat-sifat dekstrin yang dianalisa meliputi : warna dalam larutan
lugol, kadar air, kadar abu, serat kasar, bagian yang larut dalam air dingin,
kekentalan, derajat putih dan derajat asam dan kejernihan pasta. Tata cara
HASIL DAN PEMBAHASAN
Ekstraksi Pati Kelapa Sawit
Kelapa sawit adalah tanaman monokotil dan batangnya mengandung
jaringan vaskular dan parenkim. Batang kelapa sawit memiliki karakter yang
spesial. Kandungan airnya tinggi 1,5 sampai 2,5 kali dari bobot keringnya, serta
memiliki kandungan selulosa dan lignin yang rendah dan kandungan yang larut
dalam air dan NaOH yang tinggi dibanding kayu karet dan ampas tebu (Husin et
al. 1985 diacu dalam Tomimura 1992). Batang kelapa sawit ini mengandung
jaringan vaskular sekitar 71-76 % dan jaringan parenkim 24-26 %. Tabel 6
berikut ini menyajikan hasil analisa kimia jaringan vaskular dan parenkim
(Tomimura, 1992).
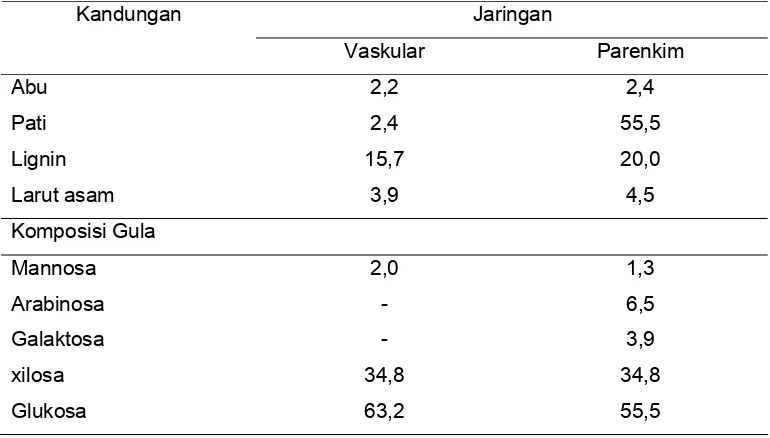
Tabel 6 Komposisi kimia kandungan jaringan vaskular dan parenkim batang kelapa sawit (%).
Jaringan Kandungan
Vaskular Parenkim
Abu 2,2 2,4
Pati 2,4 55,5
Lignin 15,7 20,0
Larut asam 3,9 4,5
Komposisi Gula
Mannosa 2,0 1,3
Arabinosa - 6,5
Galaktosa - 3,9
xilosa 34,8 34,8
Glukosa 63,2 55,5
(Tomimura 1992)
Batang kelapa sawit yang diekstraksi berasal dari PTPN 2 kebun Gohor
Lama Kabupaten Langkat, Propinsi Sumatera Utara hasil peremajan kebun.
Proses penebangan di kebun PTPN 2 ini dapat dilihat pada Gambar 10. Proses
ekstraksi pati dilakukan dengan cara memotong 2 m batang kelapa sawit dari
pucuk batang. Hal ini disebabkan batang sawit bagian atas mempunyai struktur