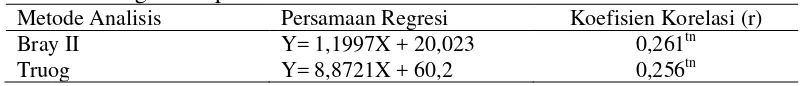PENILAIAN METODE BRAY II DAN TRUOG PADA TANAH SULFAT MASAM POTENSIAL UNTUK TANAMAN PADI
SKRIPSI
OLEH:
ACHMAD HAMBALI NST 090301053/ AGROEKOTEKNOLOGI
PROGRAM STUDI AGROEKOTEKNOLOGI FAKULTAS PERTANIAN
PENILAIAN METODE BRAY II DAN TRUOG PADA TANAH SULFAT MASAM POTENSIAL UNTUK TANAMAN PADI
SKRIPSI
OLEH:
ACHMAD HAMBALI NST 090301053/ AGROEKOTEKNOLOGI
Skripsi Sebagai Salah Satu Syarat untuk Memperoleh Gelar Sarjana di Fakultas Pertanian
Universitas Sumatera Utara
PROGRAM STUDI AGROEKOTEKNOLOGI FAKULTAS PERTANIAN
Judul Skripsi : Penilaian Metode Bray II dan Truog Pada TanahSulfat Masam
Potensial Untuk Tanaman Padi
Nama : Achmad Hambali Nst
NIM : 090301053
Program Studi : Agroekoteknologi
Minat : Ilmu Tanah
Disetujui Oleh : Komisi Pembimbing
Ketua Pembimbing Anggota Pembimbing
(Ir. Fauzi, MP.) (Prof. Ir. Lahuddin Musa, MS.)
NIP. 195711101986011003 NIP. 1305174454
Diketahui Oleh:
(Ir. T. Sabrina, M. Agr. Sc., Ph.D.) Ketua Program Studi Agroekoteknologi
NIP. 1964 0620 1998 0320 01
ABSTRACT
ACHMAD HAMBALI NST, The Testing of Bray II and Truog Method for Sulfate Acid Soil to The Paddy. Supervised by Fauzi and Lahuddin.
The research was conducted to get the right analysis method for sulfate acid soil Karanganyar village region of Secanggang by examining twoP-available of soil analysis method. The research held in Seed Technology Laboratory (seeding), green house and also in Research and Technology Laboratory Agriculture Faculty University of Sumatera Utara. The research used non factorial Randomized Block Design with 3 repetition, which as main factor is the giving of Natural Phosphate with 9 kind of dosages, that is: 0, 50, 100, 150, 200, 250, 300, 350, and 400 ppm. The giving of Natural Phosphate was significant to the phosphorus sorption and pH with the best dosage is P7 (350 ppm). The examining of analysis method was Bray II and Truog. The right analysis method was chosen by correlating the analysis result of P-available with P-sorption. The method which had the highest coefficient of correlation would be chosen as the right method, and Bray II has chosen as the right method with r value was 0,261. P critical limit of Paddy for Bray II was 24,1 ppm and for Truog was 12,13 ppm.
ABSTRAK
ACHMAD HAMBALI NST, Penilaian Metode Bray II dan Truog Pada TanahSulfat Masam Untuk Tanaman Padi. Dibimbing oleh Fauzi dan Lahuddin.
Penelitian ini dilaksanakan guna untuk menetapkan metode analisis yang tepat untuk tanah sulfat masam potensial desa Karanganyar kecamatan Secanggang dengan menguji dua metode analisis P-tersedia tanah yang telah direkomendasikan. Penelitian ini dilaksanakan di Laboratorium Teknologi Benih (penyemaian benih), Rumah Kasa dan Laboratorium Riset dan Teknologi Fakultas Pertanian Universitas Sumatera Utara. Penelitian ini menggunakan Rancangan Acak Kelompok non faktorial dengan 3 ulangan, dimana yang menjadi faktor perlakuan adalah pemberian pupuk fosfat alam dengan dengan 9 taraf dosis yaitu: 0, 50, 100, 150, 200, 250, 300, 350, dan 400 ppm. Pemberian fosfat alam berpengaruh nyata terhadap Serapan P tanaman dan pH tanah dengan perlakuan terbaik adalah P7 (350 ppm). Metode analisis yang diuji adalah Bray II dan Truog. Metode analisis yang tepat ditetapkan dengan cara mengkorelasikan hasil analisis P tersedia dengan serapan P tanaman. Metode yang memiliki nilai koefisien korelasi tertinggi terpilih sebagai metode yang tepat, dalam hal ini Bray II adalah metode yang tepat dengan nilai r sebesar 0,261. Batas kritis P tanaman untuk Bray II sebesar 24,1 ppm dan Truog sebesar 12,13 ppm.
RIWAYAT HIDUP
Penulis dilahirkan di Belawan, 6 Maret 1991 dari Ayah Abdul Karim
Nasution dan Ibunda Chairani Rangkuti. Penulis merupakan anak terakhir dari 6
bersaudara.
Tahun 2009 penulis lulus dari SMA Dharmawangsa Medan dan pada
tahun yang sama penulis lulus seleksi masuk Universitas Sumatera Utara melalui
jalur UMB (Ujian Masuk Bersama) pada pilihan kedua yaitu Agroekoteknologi.
Selama di bangku perkuliahan, penulis aktif di berbagai organisasi internal
maupun eksternal USU, yaitu BKM (Badan Kenaziran Mushalla) Al Mukhlisin
FP USU, BKM-research, SGC (Smart Generation Community), Sahiva Drama
Musikal, Trust Danone USU Club, TIM Mentoring Agama Islam, XL Future
Leader Medan, dan Ikatan Mahasiswa Medan Utara (IMAMU). Penulis juga
pernah menjadi asisten Laboratorium Morfologi dan Taksonomi Tumbuhan dan
Laboratorium Botani.
Prestasi yang pernah diraih penulis selama menjadi mahasiswa USU
adalah peraih beasiswa PPA, peraih dana wirausaha SEC USU 2011 dengan usaha
TobayaQ, Juara Cipta Puisi FP USU, Finalist Trust International Business game
di Jakarta, Mahasiswa Berprestasi FP USU 2012, Runner up 1 Mahasiswa
Berprestasi USU 2012, 10 tim Debat Bahasa Inggris terbaik seIndonesia, 5 tim
terbaik dalam lomba KTI UGM Yogyakarta, 15 besar nominasi Astra Youth
Award Indonesia, Delegasi Sumatera Utara di XL Future Leader Indonesia Season
1, peraih medali Perunggu kategori International Best Presenter IMT GT 2012 di
Malaysia, Semifinalist DYSE International Entrepreneurship di Jakarta,
MITI, serta menjadi pembicara dalam Workshop pelatihan KTI oleh Gamadiksi
USU dan Inkubs USU.
Penulis melaksanakan Praktek Kerja Lapangan (PKL) di PTPN 2 Kebun
KATA PENGANTAR
Puji dan syukur penulis panjatkan kehadiratAllah Yang Maha Esa karena
atas berkat dan rahmat Nya penulis dapat menyelesaikan skripsi ini yang berjudul
“Penilaian Metode Bray II dan Truog Pada TanahSulfat Masam Untuk Tanaman
Padi”, yang merupakan salah satusyarat untuk dapat memperoleh gelar Sarjana di
Program studi Agroekoteknologi Minat Ilmu Tanah Fakultas Pertanian,
Universitas Sumatera Utara, Medan.
Ungkapan terima kasih terkhusus penulis sampaikan kepada Ibunda
tercinta Chairani Rangkuti dan Ayahanda tercintaAbdul Karim Nasution atas
segala kasih sayang, perhatian, nasehat, motivasi dan doanya.Serta kakanda dan
abangda yang selalu memberi semangat untuk maju.
Pada kesempatan ini penulis mengucapkan terima kasih kepada Bapak Ir.
Fauzi, MP sebagai ketua komisi pembimbing dan kepada Bapak Prof. Ir.
Lahuddin, MP sebagai anggota komisi pembimbing yang telah banyak
membimbing dan memberi saran kepada penulis dalam menyusun dan
menyelesaikan skripsi ini.
Serta ucapan terima kasih kepada bapak Ir. Mukhlis, MSi selaku dosen
Kesuburan tanah yang telah banyak memberikan motivasi dan ajarannya, ibu
Dr. Ir. Hamidah Hanum, MP. Selaku dosen Perancangan Percobaan yang selalu
bersedia menjawab pertanyaan penulis, abangda Rudi dan ibu Murni selaku orang
penting di Laboratorium Riset dan Teknologi yang selalu mengajari penulis, dan
terima kasih atas kesetiaannya untuk teman-teman tercinta Yasir, Nikko, Andrian,
Nisa, Iman, Sisko, Fadli, Ryan, Dedes, Egit, Fadma, Dina, Evi, Richard, Alvi dan
Penulis menyadari skripsi ini jauh dari sempurna. Oleh sebab itu penulis
sangat mengharapkan masukan dan saran yang bersifat membangun demi
kesempurnaan penulisan ini.
Akhir kata penulis berharap semoga skripsi ini dapat bermanfaat bagi kita
Semua, khususnya untuk khasanah keilmuan di Indonesia.
Medan, Januari 2014
DAFTAR ISI
ABSTRACT ... i
ABSTRAK ... ii
RIWAYAT HIDUP ... iii
KATA PENGANTAR ... v
DAFTAR ISI ... vii
DAFTAR TABEL ... ix
DAFTAR GAMBAR ... x
DAFTAR LAMPIRAN ... xi
PENDAHULUAN Latar Belakang ... 1
Tujuan Penelitian ... 2
Hipotesis Penelitian ... 3
Kegunaan Penulisan ... 3
TINJAUAN PUSTAKA Tanah Sulfat Masam ... 4
Padi Sawah ... 7
Unsur Hara P ... 8
Pupuk Fosfat Alam ... 11
Metode Analisis P ... 13
Batas Kritis Hara P ... 16
BAHAN DAN METODE Tempat dan Waktu Penelitian ... 18
Bahan dan Alat ... 18
Metode Penelitian ... 18
Pelaksanaan Percobaan Pengambilan sampel tanah ... 19
Persiapan media tanam ... 20
Penyemaian benih ... 20
Inkubasi tanah ... 20
Penanaman dan penjarangan ... 21
Pemanenan ... 21
Parameter Amatan Tanah ... 21
Tanaman ... 21
Uji Statistik ... 22
Tinggi Tanaman, Jumlah Anakan, Berat Kering Tajuk dan Akar, dan Serapan P Tanaman ... 24 Penilaian Metode Analisis... 27 Penetapan Batas Kritis P ... 30
KESIMPULAN DAN SARAN
Kesimpulan ... 32 Saran ... 32
DAFTAR PUSTAKA
DAFTAR TABEL
No. Hal.
1. Hubungan antara analisis tanah dengan respon terhadap Pupuk P ... 13
2. Perlakuan dosis pupuk P ... 19
3. Metode analisis P tersedia dan ekstraktan yang digunakan ... 20
4. Kadar P-tersedia tanah sulfat masam potensial dan P-tanaman ... 23
5. Tinggi tanaman, jumlah anakan dan pH tanah ... 25
DAFTAR GAMBAR
No. Hal.
1. Korelasi P tersedia metode Bray II terhadap serapan P tanaman ... 28
2. Korelasi P tersedia metode Truog terhadap serapan P tanaman ... 29
3. Batas kritis P tersedia untuk metode Bray II ... 30
DAFTAR LAMPIRAN
No. Hal.
1. Bagan Penelitian di Rumah Kasa FP USU ... 38
2. Prosedur Metode Bray II ... 39
3. Prosedur Metode Truog ... 42
4. Prosedur Penetapan P-daun ... 45
5. Ciherang ... 47
6. Perhitungan Berat Tanah/ember dan Perhitungan Pupuk Fosfat Alam Ciamis ... 48
7. Data Serapan P Tanaman ... 51
8. Data Hasil Analisis Tanah Metode Bray II ... 52
9. Data Hasil Analisis Sidik Ragam Bray II ... 52
10.Data Hasil Analisis Tanah Metode Truog ... 53
11.Data Hasil Analisis Sidik Ragam Truog ... 53
12.Data Hasil Analisis Serapan P Tanaman ... 54
13.Data Hasil Analisis Sidik Ragam Serapan P Tanaman ... 54
14.Data Hasil Uji Duncan Untuk Serapan P Tanaman ... 55
15.Data Hasil Tinggi Tanaman Padi ... 56
16.Data Analisis Sidik Ragam Tinggi Tanaman ... 56
17.Data Hasil Jumlah Anakan Padi ... 57
18.Data Hasil Analisis Sidik Ragam Jumlah anakan ... 57
19.Data Hasil Berat Kering Tajuk Padi... 58
20.Data Hasil Analisis Sidik Ragam Berat Kering Tajuk Padi ... 58
21.Data Hasil Berat Kering Akar Padi ... 59
22.Data Hasil Analisis Sidik Ragam Berat Kering Akar Padi ... 59
23.DataPersentase Serapan P tanaman ... 60
ABSTRACT
ACHMAD HAMBALI NST, The Testing of Bray II and Truog Method for Sulfate Acid Soil to The Paddy. Supervised by Fauzi and Lahuddin.
The research was conducted to get the right analysis method for sulfate acid soil Karanganyar village region of Secanggang by examining twoP-available of soil analysis method. The research held in Seed Technology Laboratory (seeding), green house and also in Research and Technology Laboratory Agriculture Faculty University of Sumatera Utara. The research used non factorial Randomized Block Design with 3 repetition, which as main factor is the giving of Natural Phosphate with 9 kind of dosages, that is: 0, 50, 100, 150, 200, 250, 300, 350, and 400 ppm. The giving of Natural Phosphate was significant to the phosphorus sorption and pH with the best dosage is P7 (350 ppm). The examining of analysis method was Bray II and Truog. The right analysis method was chosen by correlating the analysis result of P-available with P-sorption. The method which had the highest coefficient of correlation would be chosen as the right method, and Bray II has chosen as the right method with r value was 0,261. P critical limit of Paddy for Bray II was 24,1 ppm and for Truog was 12,13 ppm.
ABSTRAK
ACHMAD HAMBALI NST, Penilaian Metode Bray II dan Truog Pada TanahSulfat Masam Untuk Tanaman Padi. Dibimbing oleh Fauzi dan Lahuddin.
Penelitian ini dilaksanakan guna untuk menetapkan metode analisis yang tepat untuk tanah sulfat masam potensial desa Karanganyar kecamatan Secanggang dengan menguji dua metode analisis P-tersedia tanah yang telah direkomendasikan. Penelitian ini dilaksanakan di Laboratorium Teknologi Benih (penyemaian benih), Rumah Kasa dan Laboratorium Riset dan Teknologi Fakultas Pertanian Universitas Sumatera Utara. Penelitian ini menggunakan Rancangan Acak Kelompok non faktorial dengan 3 ulangan, dimana yang menjadi faktor perlakuan adalah pemberian pupuk fosfat alam dengan dengan 9 taraf dosis yaitu: 0, 50, 100, 150, 200, 250, 300, 350, dan 400 ppm. Pemberian fosfat alam berpengaruh nyata terhadap Serapan P tanaman dan pH tanah dengan perlakuan terbaik adalah P7 (350 ppm). Metode analisis yang diuji adalah Bray II dan Truog. Metode analisis yang tepat ditetapkan dengan cara mengkorelasikan hasil analisis P tersedia dengan serapan P tanaman. Metode yang memiliki nilai koefisien korelasi tertinggi terpilih sebagai metode yang tepat, dalam hal ini Bray II adalah metode yang tepat dengan nilai r sebesar 0,261. Batas kritis P tanaman untuk Bray II sebesar 24,1 ppm dan Truog sebesar 12,13 ppm.
PENDAHULUAN Latar Belakang
Kebutuhan lahan yang terus meningkat menjadi penyebab
dimanfaatkannya lahan-lahan marginal seperti lahan rawa pasang surut sulfat
masam. Dari 20.11 juta ha lahan pasang surut yang ada di Indonesia, 6.7 juta ha
adalah lahan sulfat masam. Kalau digabungkan dengan lahan potensial (yang juga
berpotensi sulfat masam) 2.07 juta ha lahan, maka jumlahnya mencapai 8.77 juta
ha. Lahan sulfat masam merupakan ekosistem yang potensial untuk
dikembangkan sebagai lahan pertanian, karena arealnya yang cukup luas sehingga
mempunyai peran yang strategis dalam mendukung peningkatan produksi beras
nasional (Subiksa dan Diah, 2009)
Tanah sulfat masam potensial dicirikan oleh adanya material sulfidik.
Material sulfidik adalah tanah mineral yang mengandung komponen sulfur yang
dapat teroksidasi dan mempunyai pH >3.5 pada kondisi alamiah atau setelah
teraerasi (Maas, 1989).
Menurut Subiksa dan Diah (2009) Bahan sulfidik adalah sumber
kemasaman tanah, bila bahan ini teroksidasi akan menghasilkan kondisi sangat
masam. Kemasaman tanah yang tinggi memicu larutnya unsur beracun dan kahat
hara sehingga tanah menjadi tidak produktif. Diperlukan upaya ekstra untuk
mengelola lahan ini menjadi produktif. Masalah hara yang paling banyak
dilaporkan pada lahan sulfat masam adalah ketersediaan hara P yang rendah dan
fiksasi P yang tinggi oleh Al dan Fe. Hara P merupakan salah satu unsur hara
akar, transfer energi dalam proses fotosintesis dan respirasi, perkembangan buah
dan biji, kekuatan batang dan ketahanan terhadap penyakit.
Perilaku P- tanah dapat mempengaruhi status ketersediaan P dalam tanah
sehingga dapat ditentukan jumlah pupuk P yang diperlukan tanaman untuk
mencapai hasil yang optimum. Untuk menentukan konsentrasi unsur hara P dalam
tanah harus menggunakan metode analisis yang sesuai untuk tanah dan tanaman
yang diusahakan.
Analisis P-tersedia dalam tanah dapat diukur dengan menggunakan
berbagai bahan pengekstrak. Ada beberapa metode pengekstrak yang sering
digunakan yaitu metode Bray I, Bray II, Truog, Olsen dan North Carolina. Namun
dari beberapa hasil penelitian dilaporkan bahwa tidak semua metode sesuai
dengan semua jenis tanah, tanaman maupun kondisi lingkungan.
Dari hasil penelitian yang pernah dilakukan oleh Ali dan Rahman (2010)
diketahui bahwa Batas kritis untuk padi tercatat 14.5 mg/kg untuk metode
ekstraksi Hunter, Olsen dan Bray kecuali Nelson di mana nilainya adalah 34.5
mg/kg. Mengingat prinsipnya, semakin tinggi nilai r2 adalah semakin cocok.
Prosedur Nelson dan Bray lebih cocok untuk memprediksi respon P untuk
tanaman padi.
Berdasarkan uraian diatas maka peneliti tertarik untuk menggunakan dua
metode analisis P tersedia terhadap tanah sulfat masam pada pertanaman padi
untuk mengetahui batas kitis P tersedia.
Tujuan Penelitian
- Untuk menetapkan metode analisis P tersedia tanah sulfat masam potensial
- Untuk menetapkan batas kritis hara P tersedia pada tanah sulfat masam
potensial.
Hipotesis Penelitian
- Kadar P tersedia tanah sulfat masam potensial sesuai ditetapkan dengan salah
satu metode analisis P tersedia.
- Adanya pengaruh batas kritis hara P tersedia terhadap pemupukan fosfat alam
pada tanah sulfat masam potensial dan terhadap pertumbuhan padi.
Kegunaan Penulisan
Sebagai bahan informasi dalam penetapan metode analisis P tersedia pada
TINJAUAN PUSTAKA Tanah Sulfat Masam
Endapan marine yang membentuk tanah sulfat masam, kaya akan pirit dan
miskin kalium. Oleh karena itu sifat dan ciri tanah sulfat masam sangat ditentukan
oleh keadaan pembentukan serta oksidasi daripada pirit. Daerah estuari adalah
daerah yang mengalami interaksi antara air sungai dengan air laut, merupakan
daerah pertanian yang potensial, tapi sayangnya daerah ini merupakan tempat
pembentukan sulfida-sulfida. Faktor vegetasi, fisiografi, iklim dan fauna turut
mempengaruhi pembentukan pirit. Vegetasi mempunyai peranan penting dalam
pembentukan pirit. Untuk mereduksi sulfat diperlukan bahan organik sebagai
elektron donor (Noor, 2004).
Bahan organik merupakan substrat bagi mikroorganisme anaerob dan
akibatnya terjadi deplesi oksigen sehingga menyebabkan penurunan redoks
potensial dan peningkatan pH (Hanum, 2004).
Tanah sulfat masam dicirikan oleh tingginya kandungan sulphur (0.4-3%
S) dan rendahnya pH ketika dalam kondisi kering. pH tanah ini juga bisa tetap
pada tingkat yang rendah dalam jangka waktu perendaman tertentu. Dalam
percobaan reklamasi tanah sulfat masam tergenang dengan atau tanpa
penambahan bahan organik akan terjadi perubahan pada pH2S, pH dan konsentrasi
Fe+3. Konsentrasi H2S meningkat pesat setelah satu hari perendaman, terutama
ketika bahan organik ditambahkan. Konsentrasi mencapai nilai puncak pada hari
ketiga dan kemudian menurun lagi. Nilai puncak konsentrasi H2S untuk perlakuan
Penurunan konsentrasi H2S setelah nilai puncak paralel dengan peningkatan pH
tetapi tidak dengan penurunan Fe+2 konsentrasi (Tian-ren, 1985).
Bila tanah digenangi, persediaan oksigen menurun sampai mencapai nol
dalam waktu kurang dari sehari. Laju difusi oksigen udara melalui lapisan air atau
pori yang berisi air, 10.000 kali lebih lambat daripada melalui udara atau pori
yang berisi udara. Jasad renik aerob dengan cepat menghabiskan udara yang
tersisa dan menjadi tak aktif lagi atau mati. Bakteri anaerob atau anaerob fakultatif
berkembangbiak dengan cepat dan mengambil alih proses perebutan bahan
organik tanpa menggunakan oksigen, dan sebagai gantinya menggunakan
komponen tanah yang teroksidasi sebagai penangkap elektron. Hasil ini direduksi
menurut tuntunan termodinamika sebagai berikut: nitrat, senyawa mangan,
senyawa feri, senyawa antara dari pereputan bahan organik, sulfat, dan sulfit
(Sanchez, 1993).
Iklim mungkin berperanan dalam pembentukan pirit dalam hubungannya
dengan produksi bahan organik. Tanah-tanah sulfat masam didaerah tropis
biasanya terdapat di daerah iklim musiman, dengan demikian dapat tercipta
keadaan aerobik dan menghasilkan tanah-tanah yang kaya sulfat masam dengan
pH rendah (Noor, 2004).
Senyawa-senyawa belerang yang banyak dijumpai di daerah pasang surut
berasal dari laut. Kandungan unsur ini di dalam air laut sangat tinggi, berkisar
antara 885 ppm, kurang lebih 4 kali kadarnya di dalam kerak bumi, granit, basalt
ataupun shale. Proses pembentukan sulfida dimulai dari akumulasi sulfat yang
timbul oleh proses-proses reduksi menjadi sulfida-sulfida dan S elementer. Proses
suasana reduksi pada pH 7.0 – 8.5 dan kehadiran bahan organik.
Tanaman-tanaman daerah tropik seperti Rizopora recemora, Nipa fructicans, dan Avicenia
sp. merupakan sumber-sumber bahan organik yang diperlukan oleh bakteri-bakteri
tersebut (Noor, 2004).
Taraf selanjutnya pirit terbentuk dari reaksi antara FeS dan H2S yang
berlangsung disekitar daerah kontak antara sedimen dan genangan air diatasnya.
Reaksinya sebagai berikut:
Pembentukan pirit:
FeS + S FeS2
2FeS + 2H2S + O2 FeS2 + 2H2O
Reaksi senyawa pirit, FeS2, merupakan contoh klasik dalam
menggambarkan reaksi redoks pembentukan senyawa ini adalah reaksi/kombinasi
antara unsur Fe yang berikatan dengan S dan keduanya dalam kondisi tereduksi.
Di alam pirit dijumpai dalam bentuk deposit mineral, dibawah lapisan permukaan
tanah yang terus menerus tergenang dan tergantung pada kekayaan unsur besi dan
sulfur. Tanah yang mengandung pirit umumnya ditemukan di wilayah pantai,
pada pertemuan antara limpasan air yang mengandung sulfur dan air laut yang
kaya besi (Lahuddin, 2011).
Tanah yang kaya pirit disebut tanah potensial sulfat masam. Bahan pirit
bila terekspos udara akan terjadi oksidasi pirit yang dibantu oleh bakteri sebagai
katalisator, reaksinya sebagai berikut:
Pada reaksi diatas kelihatan bahwa Fe+2 teroksidasi menjadi Fe+3 dan S-2 menjadi
S+6, dan kelihatan pula terbebasnya H+ yang berpotensi mengasamkan tanah
(Lahuddin, 2011).
Pada kondisi anaerob atau tergenang, pirit dalam keadaan stabil.
Sebaliknya dalam keadaan aerob, pirit mudah mengalami oksidasi, terbentuk asam
sulfat. Bila karena drainase alami atau buatan, muka air tanah sampai ke lapisan
pirit, maka tanah sulfat masam potensial berubah menjadi tanah sulfat masam
aktual (Putu dan Adhi, 1990).
Padi Sawah
Dari bukti-bukti arkeologi, berdasarkan sejarah padi di masa purbakala
ditemukan dari Ampur Non Nok Tha di provinsi Korn Kaen, padi ditanam
sebelum 5.500 tahun yang lalu (sekitar 2960 SM). Hal ini bahkan lebih awal dari
Cina (sekitar 2737 SM) dan di India (sekitar 1957 SM). Selanjutnya,
gambar-gambar orang kuno di Pha Taem di provinsi Ubon Rajathanee bahwa pada 6.000
tahun lalu menunjukkan adanya tanaman padi (Gomez, 2001).
Produktivitas padi di lahan pasang surut adalah berkisar dari 4-5
ton/Ha yang lebih rendah dari hasil di sawah irigasi yaitu 8 ton/Ha. Rendahnya
produktivitas padi di lahan pasang surut disebabkan oleh rendahnya kesuburan
tanah, yang dicirikan oleh kahat hara terutama fosfat, kemasaman yang tinggi,
keracunan alumunium, besi dan pirit. Varietas Indra giri, Punggur, Marta pura,
Mendawan, Mergasari, Siak raya, dan Tenggulang merupakan varietas padi yang
toleran di lahan masam (Suwandi, dkk. 2012).
Budidaya padi menggunakan sejumlah besar air biasanya dalam kondisi
melalui irigasi, meliputi setengah dari sekitar areal sawah di seluruh dunia, dan
menghasilkan tiga-empat dari total produksi beras dunia (Nakano, 2004).
Padi merupakan tanaman pangan berupa rumput berumpun. Tanaman
pertanian kuno berasal dari dua benua yaitu Asia dan Afrika Barat tropis dan
subtropis. Bukti sejarah memperlihatkan bahwa penanaman padi di Zhejiang
(Cina) sudah dimulai pada 3.000 tahun SM. Fosil butir padi dan gabah ditemukan
di Hastinapur Utara Pradesh India sekitar 100-800 SM. Selain Cina dan India,
beberapa wilayah asal padi adalah, Bangladesh Utara, Burma, Thailand, Laos,
Vietnam (Prihatman, 2000).
Indonesia merupakan produsen padi terbesar ketiga di dunia setelah
Negara Cina dan India. Menurut data BPS pada tahun 2009, produksi padi
Indonesia mencapai 64.398.890 ton dan mengalami peningkatan produksi pada
tahun 2010 menjadi 66.411.469 ton. Seiring dengan semakin bertambahnya
jumlah penduduk dan berkurangnya jumlah lahan produktif membuat kebutuhan
padi semakin meningkat. Oleh karena itu, diperlukan usaha untuk meningkatkan
produktivitas pertanian (Rusd, 2011).
Unsur Hara P
Unsur hara fosfor adalah unsur hara makro, dibutuhkan tanaman dalam
jumlah yang banyak dan essensial bagi pertumbuhan tanaman. Sumber fosfor di
dalam tanah terdiri dari bentuk organik dan anorganik. Anion-anion fosfat yang
dapat larut menjadi bentuk yang tidak tersedia Karena terikat dengan
logam-logam seperti Al, Fe dan Mn, sehingga tidak tersedia bagi tanaman. Sebagai
akibat dari sifat kimia fosfat, konsentrasi fosfat di dalam larutan tanah adalah
Ketersediaan fosfat meningkat setelah penggenangan, terutama karena
reduksi feri (Fe3+) fosfat menjadi fero (Fe2+) fosfat, meskipun terjadi
perubahan-perubahan yang lain, seperti hidrolisis dari aluminium fosfat dan larutan kalsium
fosfat. Mekanisme perubahan yang dimaksud adalah sebagai berikut:
1. Reduksi feri (Fe3+) fosfat menjadi fero (Fe2+) fosfat melepaskan P, walaupun
sejumlah P yang dilepaskan akan diserap kembali
2. Pelepasan occluded P akibat feri oksida yang menyeliputi P menjadi fero
oksida yang lebih larut selama penggenangan. Penyelimutan P oleh feri oksida
berada dalam liat dan zarah liat membentuk occluded P
3. Peningkatan pH tanah masam akibat penggenangan meningkatkan kelarutan
strengit dan variscit, selanjutnya terjadi peningkatan ketersediaan P
4. Dekomposisi bahan organik pada kondisi tanah anaerob meningkatkan
kelarutan dari senyawa Ca-P maupun Fe-P dan Al-P melalui proses khelasi.
Pengeringan tanah setelah penggenangan umumnya menurunkan kelarutan fosfor
yang berasal dari tanah maupun pupuk dan meningkatkan fiksasi fosfor sehingga
menurunkan kelarutan fosfor. Diantara berbagai fraksi fosfat, fosfat yang
diselimuti oksida besi yang berkadar air (occluded phosfat) adalah sangat
menarik karena tidak tersedia pada tanah yang tidak tergenang
(Setyorini dan Abdulrachman, 2009).
Bentuk P di dalam tanah selain dibedakan berdasarkan ketersediaannya,
beberapa ahli juga membedakan P berdasarkan P-labil dan P-non labil. Seperti
telah dijelaskan diatas bawa P-larut didalam tanah apabila hilang (diserap
tanaman) akan segera cepat diganti oleh bentuk labil (sebagian bentuk
dengan P-larut membutuhkan waktu sekitar 24 hingga 48 jam. Sedangkan apabila
waktu yang dibutuhkan lebih lama maka P tersebut berasal dari bentuk P-non labil
(Winarso, 2005).
Tanaman menyerap sebagian besar unsur hara P dalam bentuk ion
ortofosfat primer (H2PO4-). Sejumlah kecil diserap dalam bentuk ion ortofosfat
sekunder (HPO4-2). Kemasaman tanah sangat besar pengaruhnya terhadap
perbandingan serapan ion-ion tersebut, yaitu makin masam kadar H2PO4- makin
besar sehingga makin banyak yang diserap tanaman dibandingkan dengan HPO4-2.
Pada pH tanah sekitar 7,22 konsentrasi H2PO4- dan HPO4-2 setimbang. Oleh
karena sebagian besar tanah mempunyai pH dibawah 7, maka sebagian besar
tanah mempunyai konsetrasi H2PO4- lebih besar atau dominan dibandingkan
dengan HPO4-2. Hal inilah salah satu faktor yang menyebabkan tanaman lebih
banyak menyerap bentuk ion ortofosfat primer dibandingkan dengan bentuk ion
ortofosfat sekunder (Winarso, 2005).
Serapan hara P saat fase vegetative yaitu mulai perkecambahan hingga
akan berbunga (umur 51 hari) total serapan tidak lebih dari 10%. Sehingga 90%
unsur hara P selama pertumbuhannya diserap saat fase generative. Sedangkan
apabila dihitung berdasarkan kecepatan serapan P setiap harinya menunjukkan
bahwa kecepatan serapan P per hari pada fase generative bisa mencapai hamper
16 kali apabila dibandingkan dengan fase vegetative. Kadar P pada bagian
generative tanaman (khususnya biji) lebih tinggi dibandingkan dengan
bagian-bagian lainnya. Pada jerami padi kadar P adalah 0.09% dan pada biji padi kadar P
Fiksasi fosfor berlangsung cepat pada tanah tergenang yang bereaksi
masam atau netral. Fiksasi tersebut jauh lebih lemah pada tanah bereaksi agak
alkali. Tanah yang mengandung oksida besi dan aluminium, halosit, dan alofan
memfiksasi fosfor dalam keadaan tergenang maupun tanah kering
(Setyorini dan Abdulrachman, 2009).
Tanaman menyerap fosfor dalam bentuk ion H2PO4- atau ion HPO-24.
Spesies ion yang merajai tergantung pada pH sistem tanah-pupuk tanaman, yang
mempunyai ketersediaan tinggi pada pH 5.5-7.0. Kepekatan H2PO4-yang tinggi
dalam larutan memungkinkan tanaman mengangkutnya dalam takaran besar,
karena perakaran tanaman diperkirakan mempunyai 10 kali loka penyerapan
untuk H2PO4- dibandingkan untuk HPO-24 (Mas’ud, 1992).
Serapan hara P yang cukup akan menjamin tanaman tumbuh dengan baik.
Oleh karenanya pemupukan P pada lahan sulfat masam adalah komponen
teknologi yang harus mendapat prioritas. Pengapuran untuk mengurangi
kemasaman tanah dan unsur beracun dan pemupukan P untuk mengurangi kahat P
diharapkan dapat meningkatkan produktivitas lahan sulfat masam. Dalam kaitan
dengan pemanfaatan fosfat alam, lahan sulfat masam memiliki nilai tambah
karena dengan tingkat kemasaman yang tinggi maka kelarutan fosfat alam akan
lebih cepat. Karena sebagian kandungan fosfat alam adalah CaCO3, maka
pemanfaatan fosfat alam akan mampu mengurangi tingkat kemasaman tanah
sehingga membantu memperbaiki pertumbuhan tanaman (Subiksa dan Diah,
Pupuk Fosfat Alam
Fosfat alam adalah mineral apatit yang umumnya memiliki kelarutan yang
rendah, sehingga ketersediaannya untuk tanaman sangat rendah. Untuk
meningkatkan kelarutannya, dalam proses pembuatan pupuk P komersial seperti
SSP, TSP, SP-36 dan pupuk fosfat mudah larut lainnya, fosfat alam diasamkan
dengan menambahkan asam kuat seperti asam sulfat atau asam fosfat
(Subiksa dan Diah, 2009).
Reaksi yang terjadi dapat digambarkan sebagai berikut:
Ca10(PO4)6CO3 + 7 H2SO4 + 3H2O 3Ca(H2PO4)2H2O + 7 CaSO4 + H2CO3
Penambahan asam dimaksudkan untuk menghancurkan mineral apatit agar fosfat
membentuk ikatan yang lebih lemah sehingga mudah larut dan pada akhirnya
lebih tersedia bagi tanaman. Lahan sulfat masam dalam proses pembentukannya
menghasilkan asam sulfat sehingga membentuk reaksi sangat masam dalam
lingkungan tanah. Oleh karenanya fosfat alam yang diberikan pada tanah sulfat
masam akan mengalami peningkatan kelarutan yang sangat signifikan, sehingga
dapat dikatakan lahan sulfat masam adalah “pabrik pupuk alami”
(Subiksa dan Diah, 2009).
Fosfat alam merupakan salah satu pupuk fosfat alami karena berasal dari
bahan tambang, sehingga kandungan P sangat bervariasi. Efektivitas fosfat alam
pada lahan sulfat masam dipengaruhi oleh kualitas fosfat alam dan tingkat
kehalusan butir. Fosfat alam yang bagus mengandung fosfat alam (P2O5) lebih
dari 25% (Subiksa dan Diah, 2009).
Kelemahan dari perubahan bentuk pupuk tunggal menjadi pupuk majemuk
menggunakan pupuk secara spesifik lokasi, karena kalau jerami atau sisa tanaman
dikembalikan ke dalam tanah maka tanah tidak lagi memerlukan pupuk P dan K
dengan takaran tinggi (Zaini, 2013).
Metode Analisis P
Analisis tanah merupakan cara yang cepat dan ekonomis untuk
menentukan status fosfor suatu tanah. ada sejumlah faktor yang mempengaruhi
ketersediaan fosfor, beberapa di antaranya dapat diubah atau dikendalikan oleh
petani. faktor-faktor yang mendukung ketersediaan fosfor yang lebih tinggi yaitu
(a) pH 6.5-7.5, (b) tingkat fosfor tinggi dalam tanah, (c) pasokan bahan organik
terurai dalam tanah, (d) tingkat kelembaban tinggi tanah, dan (e) kandungan
seskuioksida bebas yang rendah di fraksi liat (Thompson, 1957).
Analisis tanah sangat mempengaruhi respon tanah terhadap pupuk P.
Hubungan keduanya bersifat berbanding terbalik, artinya disaat analisis tanah
menunjukkan tingkat yang rendah maka respon tanah terhadap pupuk akan tinggi.
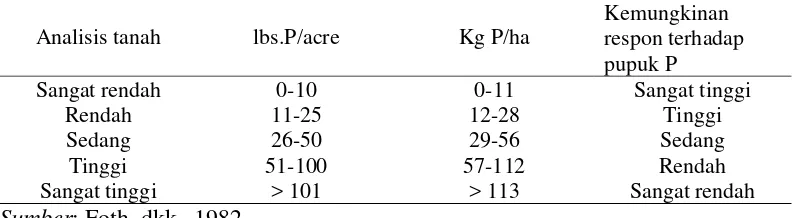
Begitu juga sebaliknya. Hal ini terlihat pada Tabel 1.
Tabel 1. Hubungan antara analisis tanah dengan respon terhadap Pupuk P
Analisis tanah lbs.P/acre Kg P/ha
Kemungkinan respon terhadap pupuk P
Sangat rendah 0-10 0-11 Sangat tinggi
Rendah 11-25 12-28 Tinggi
Sedang 26-50 29-56 Sedang
Tinggi 51-100 57-112 Rendah
Sangat tinggi > 101 > 113 Sangat rendah
Sumber: Foth, dkk., 1982.
Ekstraksi Fosfat dengan metode Bray telah menunjukkan korelasi yang
baik dengan hasil tanaman pada tanah-tanah masam dan netral di beberapa daerah.
Untuk tanah masam, fluoride di ekstraktan bray dapat meningkatkan pelepasan P
pembentukan berbagai kompleks Al-F. Fluoride juga efektif menekan readsorpsi
dari dilarutkannya P oleh koloid tanah. Sifat asam ekstraktan tersebut (pH 2,6)
juga berkontribusi terhadap pelepasan P tersedia dari Al, Ca, Fe dan bentuk-terikat
di sebagian besar tanah. Metode Bray tidak cocok untuk tanah liat dengan tingkat
kejenuhan basa yang cukup tinggi, lempung liat berlumpur atau tanah bertekstur
lebih halus yang berkapur atau memiliki nilai pH yang tinggi (pH> 6,8) atau
memiliki tingkat kejenuhan basa tinggi, tanah dengan karbonat kalsium setara>
7% dari kejenuhan basa, atau tanah dengan jumlah kapur yang tinggi (> 2%
CaCO3) (Sims, 2000).
Prinsip kerja dari analisis P tersedia metode Bray II yaitu P tersedia tanah
diekstrak oleh NH4F dan HCl, P yang bebas direaksikan dengan molibdat asam
akan menjadi berwarna biru dengan adanya asam askorbat. Perkembangan warna
biru diukur sebagai kadar P secara spektrometri (Mukhlis, 2007).
Prinsip kerja dari analisis P tersedia metode Truog yaitu dimana P tersedia
tanah diekstrak oleh NH4SO4, P yang bebas direaksikan dengan molibdat asam
akan menjadi berwarna biru dengan adanya asam askorbat. Perkembangan warna
biru diukur sebagai kadar P secara spektrometri (Mukhlis, 2007).
Analisis tanaman didasarkan pada anggapan bahwa jumlah elemen tertentu
dalam tanaman merupakan indikasi pasokan nutrisi yang tertentu dan dengan
demikian secara langsung berkaitan dengan kuantitas nya di dalam tanah. Karena
kekurangan elemen akan membatasi pertumbuhan, elemen lain mungkin
terakumulasi dalam sel getah dan menunjukkan tes "tinggi" tanpa pasokan.
ini ada indikasi, bahwa jika nitrogen yang memadai diterapkan pada jagung
pasokan fosfor akan cukup (Tisdale dan Nelson, 1961).
Untuk kemudahan dalam analisis tanaman sering dipilih organ tanaman
berupa daun, sehingga dikenal sebagai foliar analysis. Daun yang dianggap cocok
untuk dianalisis yang memenuhi persyaratan a). Pertumbuhan organ tersebut telah
cukup, b). Tidak terlalu muda (pucuk) atau terlalu tua, dan c). Sebaiknya sebelum
fase generatif. Daun yang dianggap baik sebagai contoh untuk dianalisis disebut
daun indikator (Rosmarkam dan Yuwono, 2002).
Kegunaan analisis (baik analisis tanah maupun analisis tanaman) adalah
sebagai berikut:
- untuk mengetahui status hara dalam tanah dan dalam tanaman
- untuk kelestarian kesuburan tanah dan produktivitas lahan; dengan
mengetahui kadar hara dalam tanah dan produksi tanaman, maka kehilangan
hara dari tanah karena panen dapat dihitung
- menduga produksi tanaman dan menghitung keuntungan apabila dilakukan
pemupukan
- untuk mengetahui hara yang menjadi faktor pembatas yang harus diperbaiki
dan membuat rekomendasi pemupukan
- untuk menilai lahan secara ekonomis, misalnya harga tanah, pajak dan
sebagainya.
(Rosmarkam dan Yuwono, 2002).
Besarnya nilai kebutuhan fosfat standar (KFS) adalah jumlah fosfat yang
harus ke sistem koloid larutan agar konsentrasi P larutan setimbang. Penentuan
kebutuhan P anorganik yang dibutuhkan oleh tanaman didalam tanah sehingga
Batas Kritis Hara P
Setiap nutrisi esensial memiliki fungsi spesifik untuk menjalani perannya
dalam tubuh tumbuhan dan kehadiran mereka diatas batas kritis adalah suatu
keharusan agar tanaman dapat melengkapi siklus hidupnya. Batas kritis / level
yang cukup sering digunakan untuk berbagai macam tanah dan tanaman,
meskipun batas kritis mungkin berbeda tidak hanya untuk spesies tanaman, tanah,
tetapi juga untuk varietas yang berbeda dari tanaman (Subbarayappa .dkk, 2009).
Batas kritis P tersedia tanah ditentukan oleh Bray Persen Hasil diplot
terhadap P tersedia tanah masing-masing. Demikian pula batas kritis P pada daun
yang ditentukan dengan memplot bahan kering daun terhadap P tersedia daun
masing-masing dengan menggunakan diagram pencar dan statistik seperti yang
dijelaskan oleh Cate dan Nelson (1971) (Subbarayappa .dkk, 2009).
Analisa korelasi sederhana meneliti hubungan dan bagaimana eratnya
hubungan itu, tanpa melihat bentuk hubungan. Dalam analisa korelasi sederhana
variabel yang digunakan semua random dan kedua-duanya “bivariate normal”.
Jika kenaikan di dalam satu variabel diikuti dengan kenaikan didalam variabel
yang lain, maka dapat dikatakan bahwa kedua variabel tersebut mempunyai
korelasi yang positif. Tetapi jika kenaikan di dalam satu variabel diikuti oleh
penurunan didalam variabel yang lain maka dapat dikatakan bahwa kedua variabel
tersebut mempunyai korelasi negative. Dan jika tidak ada perubahan pada satu
variabel walaupun variabel lainnya berubah, maka dikatakan bahwa kedua
BAHAN DAN METODE Tempat Dan Waktu Penelitian
Penelitian dilakukan di Laboratorium Teknologi Benih, Rumah Kasa dan
Laboratorium Riset dan Teknologi Fakultas Pertanian Universitas Sumatera Utara,
Medan dengan ketinggian tempat 25-26 meter diatas permukaan laut dimulai dari
bulan Mei sampai November 2013.
Bahan Dan Alat
Bahan yang digunakan dalam penelitian adalah tanah sulfat masam yang
diambil secara komposit yang berasal dari desa Karang Anyar kecamatan
Secanggang, benih padi varietas Ciherang sebagai tanaman indikator, fosfat alam
Ciamis (FA Ciamis) (30.30% P2O5) sebagai sumber hara fosfat, pupuk dasar yaitu
Urea (46% N) 200 ppm N dan KCl (60% K2O) 150 ppm K dan bahan-bahan
kimia untuk keperluan analisis di laboratorium.
Alat yang digunakan dalam penelitian adalah cangkul untuk pengambilan
contoh tanah, ember plastik sebagai wadah tanah, meteran untuk mengukur tinggi
tanaman, timbangan untuk menimbang berat kering tajuk serta akar tanaman,
oven sebagai alat untuk mengeringkan tanaman dan alat-alat laboratorium yang
dibutuhkan dalam analisis penelitian.
Metode Penelitian
Penelitian ini menggunakan rancangan acak kelompok (RAK) non
faktorial dengan 1 faktor perlakuan yaitu dosis fosfat alam dan 3 ulangan,
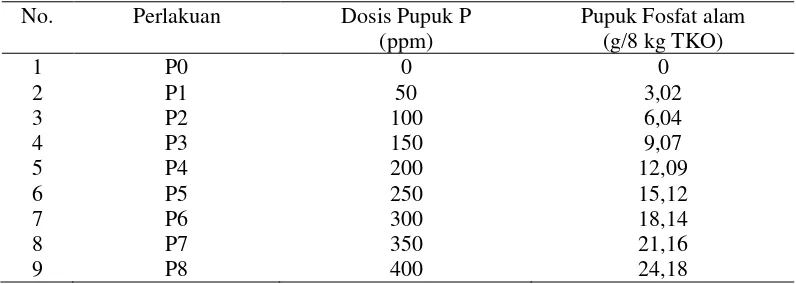
Tabel 2. Perlakuan dosis pupuk P
No. Perlakuan Dosis Pupuk P
(ppm)
Pupuk Fosfat alam (g/8 kg TKO)
1 P0 0 0
2 P1 50 3,02
3 P2 100 6,04
4 P3 150 9,07
5 P4 200 12,09
6 P5 250 15,12
7 8 9 P6 P7 P8 300 350 400 18,14 21,16 24,18
Data hasil penelitian akan dianalisis dengan menggunakan uji sidik ragam
berdasarkan model linier sebagai berikut:
Yij = µ + τi + βj + Ԑij
i = 1,2,3,…..,8 j = 1,2,3
Yij : Respon atau nilai pengamatan dari perlakuan fosfat alam pada taraf ke-i
dan ulangan ke-j
µ : Nilai tengah umum
τi : Pengaruh perlakuan fosfat alam pada taraf ke-i
βj : Pengaruh ulangan ke-j
Ԑij : Pengaruh galat percobaan dari perlakuan fosfat alam pada taraf ke-i dan
ulangan ke-j
Pelaksanaan Percobaan Pengambilan sampel tanah
Sampel tanah sulfat masam diambil secara komposit dari desa
Karang Anyar dengan kedalaman 0-20 cm. selanjutnya dilakukan analisis awal
meliputi pH H2O dan pH KCl dengan metode Elektrometri, P tersedia dengan
Walkey and Black, N total dengan metode Kjedhal, serta Al-dd dengan metode
ekstraksi KCl.
Persiapan media tanam
Contoh tanah dimasukkan kedalam ember yang setara dengan 10 kg tanah
kering oven. Pada masing-masing ember tanah digenangi dengan aquadest selama
2 minggu untuk mengembalikan tanah pada kondisi sawah (tereduksi).
Penyemaian benih
Benih padi varietas Ciherang direndam dalam air selama 24 jam.
Penyemaian dilakukan dengan menggunakan bak kecambah, kemudian di
masukkan kedalam tissue basah sampai muncul akar dan dilakukan
penyemprotan, yang dilakukan antara 15-20 hari.
Inkubasi tanah
Pada masing-masing ember tanah diberikan perlakuan fosfat alam sesuai
dengan taraf perlakuan lalu diinkubasikan selama 10 hari. Setelah itu sampel
tanah diambil untuk dilakukan analisis kadar P tersedia tanah dengan berbagai
[image:36.595.108.505.553.651.2]metode seperti tertera pada Tabel 3.
Tabel 3. Metode analisis P tersedia dan ekstraktan yang digunakan
Metode Analisis Berat tanah (g) Larutan ekstraktan Volume ekstrak (mL) Lama goncangan (menit) Bray II Truog 2 2
NH4F 1N + HCl 5N
(NH4)2SO4 + H2O + H2SO4 0,002N
20
20
30
Penanaman dan penjarangan
Sebelum penanaman contoh tanah diberikan pupuk dasar Urea 200 ppm
dan KCl 150 ppm lalu tanah sulfat masam tersebut kembali disawahkan.
Kemudian dilakukan penanaman sebanyak 3 bibit tiap ember.
Pemanenan
Sebelum dilakukan pemanenan terlebih dahulu diukur tinggi tanaman.
Penelitian dilakukan sampai akhir masa vegetatif atau tanaman mulai muncul
malai bunga 75%. Tanaman padi dipotong hingga batas permukaan tanah dan
dipisahkan dari akar tanaman kemudian dikeringanginkan dan dimasukkan ke
dalam kertas amplop untuk diovenkan pada suhu 700C selama 24 jam atau sampai
beratnya konstan.
Parameter Amatan Tanah
- P tersedia tanah dengan menggunakan metode Bray II dan Truog
Tanaman
- Tinggi tanaman (cm)
Tinggi tanaman diukur pada akhir fase vegetatif .
- Jumlah anakan maksimum
Jumlah anakan maksimum dihitung pada akhir fase vegetatif.
- Berat kering akar (g)
Berat kering akar dihitung setelah akhir fase vegetatif dan dioven dengan suhu
- Berat kering tajuk (g)
Berat kering tajuk dihitung setelah akhir fase vegetatif dan dioven dengan
suhu 70oC selama 24 jam.
- Serapan P tanaman (mg/tan)
Serapan P tanaman dihitung setelah akhir fase vegetatif, setelah diperoleh
kandungan P tanaman dengan metode Destruksi basah.
Uji Statistik
Data yang diperoleh melalui analisis pengukuran dengan beberapa metode
pengekstrak, diuji menggunakan uji korelasi. Nilai kadar P tersedia tanah dari
setiap metode di tetapkan sebagai variabel x, sedangkan hasil pengukuran
parameter tanaman (serapan P tanaman) sebagai variabel y, sehingga diperoleh
nilai koefisien korelasinya yaitu nilai r.
Nilai r diperoleh dari rumus :
r = ∑ �� �.���.���
Dimana
r = nilai koefisien relasi
∑XY = jumlah variabel x dikalikan dengan variabel y
n = jumlah perlakuan
SDx = standar deviasi variabel x
SDy = standar deviasi variabel y
Nilai koefisien korelasi dari r masing-masing metode yang tertinggi
HASIL DAN PEMBAHASAN P-tersedia Tanah
Hasil analisis sidik ragam untuk parameter P-tersedia tanah sulfat masam
potensial dengan metode Bray II menunjukkan bahwa perlakuan dosis tidak
berpengaruh nyata, akan tetapi pengaruh blok berpengaruh nyata. Sedangkan
untuk parameter P-tersedia tanah sulfat masam potensial dengan metode Truog
menunjukkan bahwa perlakuan dosis dan Blok tidak berpengaruh nyata. Hal ini
dapat dilihat pada Lampiran 10-13. Rataan P-tersedia tanah sulfat masam
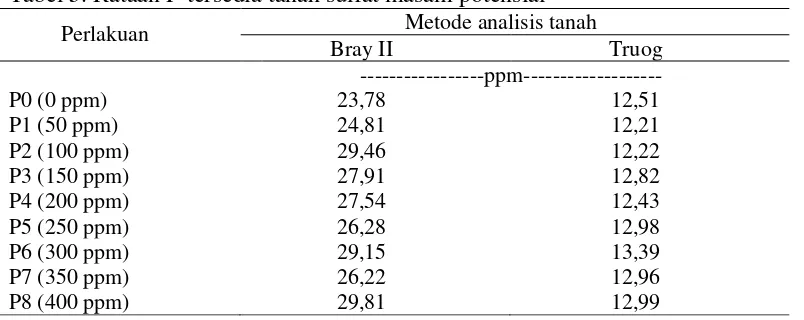
[image:39.595.109.511.343.503.2]potensial dengan dua metode analisis P-tersedia disajikan pada Tabel 5.
Tabel 5. Rataan P-tersedia tanah sulfat masam potensial
Perlakuan Metode analisis tanah
Bray II Truog
---ppm---
P0 (0 ppm) 23,78 12,51
P1 (50 ppm) 24,81 12,21
P2 (100 ppm) 29,46 12,22
P3 (150 ppm) 27,91 12,82
P4 (200 ppm) 27,54 12,43
P5 (250 ppm) 26,28 12,98
P6 (300 ppm) 29,15 13,39
P7 (350 ppm) 26,22 12,96
P8 (400 ppm) 29,81 12,99
Dari Tabel 5 dapat kita lihat bahwa rataan nilai P tersedia pada metode
Bray II yang tertinggi adalah perlakuan P8 yaitu 29,81 ppm, sedangkan P-tersedia
yang terendah pada perlakuan P0 yaitu 23,78 ppm.
Hasil analisis pada metode Truog menunjukkan bahwa nilai rataan
P-tersedia tertinggi pada perlakuan P8 yaitu 12,99 ppm dan P-P-tersedia yang terendah
pada perlakuan P1 yaitu 12,21 ppm.
Kemampuan ekstraktan Bray II dalam mengekstrak P dari dalam tanah
sulfat masam jauh lebih tinggi dari ekstraktan Truog. Perbedaan ekstraktan dari
berbeda dengan uji Truog. Dilihat dari metode Bray II menggunakan ekstraktan
NH4F dan HCl, bila tanah diekstrak dengan larutan NH4F maka ion-ion yang
mengikat P seperti Al3+, Fe3+ dan Ca-fosfat dalam larutan asam akan diikat oleh
ion F-. sehingga ion fosfat yang terikat dapat dibebaskan. Adapun reaksi yang
diduga adalah :
3NH4F + 3HCl + AlPO4 PO43- + NH4+ + Al3+ + Cl- + F-
3NH4F + 3HCl + FePO4 PO43- + NH4+ + Fe3+ + Cl- + F
-Selanjutnya
PO43- + 12 MoO4= + 27H+ H7[P(Mo2O7)6] + 10H2O
H7[P(Mo2O7)6] + vit.C Biru Molibden
Sedangkan prinsip dari metode Truog yaitu dimana P tersedia tanah
diekstrak oleh NH4SO4, P yang bebas direaksikan dengan molibdat asam akan
menjadi berwarna biru dengan adanya asam askorbat. Adapun reaksi yang diduga
adalah:
3NH4SO4 + AlPO4 PO43- + NH4+ + SO4-2
3NH4SO4 + FePO4 PO43- + NH4+ + SO4-2
Selanjutnya
PO43- + 12 MoO4= + 27H+ H7[P(Mo2O7)6] + 10H2O
H7[P(Mo2O7)6] + vit.C Biru Molibden
Tinggi Tanaman, Jumlah Anakan, Berat Kering Tajuk dan Akar, dan Serapan P Tanaman
Dari hasil analisis sidik ragam yang terdapat pada Lampiran 14-24.
Parameter amatan setelah panen meliputi Tinggi, Jumlah anakan, berat kering
tajuk, berat kering akar, dan serapan P tanaman. Nilai rataan tinggi tanaman,
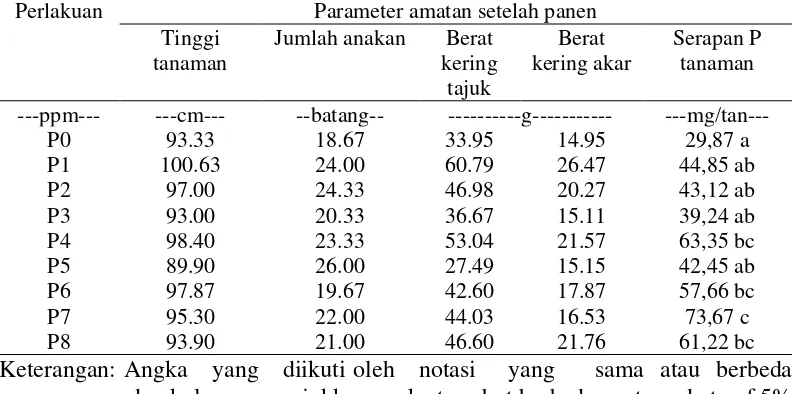
Tabel 6. Tinggi tanaman, jumlah anakan, berat kering tajuk, berat kering akar dan serapan P tanaman.
Perlakuan Parameter amatan setelah panen
Tinggi tanaman
Jumlah anakan Berat kering tajuk Berat kering akar Serapan P tanaman
---ppm--- ---cm--- --batang-- ---g--- ---mg/tan---
P0 93.33 18.67 33.95 14.95 29,87 a
P1 100.63 24.00 60.79 26.47 44,85 ab
P2 97.00 24.33 46.98 20.27 43,12 ab
P3 93.00 20.33 36.67 15.11 39,24 ab
P4 98.40 23.33 53.04 21.57 63,35 bc
P5 89.90 26.00 27.49 15.15 42,45 ab
P6 97.87 19.67 42.60 17.87 57,66 bc
P7 95.30 22.00 44.03 16.53 73,67 c
P8 93.90 21.00 46.60 21.76 61,22 bc
Keterangan: Angka yang diikuti oleh notasi yang sama atau berbeda pada kolom menunjukkan angka tersebut berbeda nyata pada taraf 5% menurut uji DMRT
Dari Tabel 6 dapat kita lihat bahwa parameter tinggi tanaman dengan nilai
tertinggi terdapat pada P1 yaitu 100,63 cm dan yang terendah yaitu P5 yaitu 89,90
cm. Dari hasil ini dapat dilihat bahwa pada parameter ini berbeda tidak nyata.
Dari Tabel 6 dapat kita lihat juga jumlah anakan paling tinggi terdapat
pada perlakuan P5 yaitu 26,00 batang dan yang terendah terdapat pada perlakuan
P0 yaitu 18,67 batang. Dari hasil ini dapat dilihat bahwa parameter jumlah anakan
tidak menunjukkan pengaruh yang nyata akibat pemberian pupuk fosfat alam.
Dari Tabel 6 dapat dilihat pada parameter berat kering tajuk yang tertinggi
terdapat pada P1 yaitu sebesar 60,79 g dan yang terendah terdapat pada perlakuan
P5 yaitu 27,49 g. Dari hasil ini dapat kita ketahui bahwa pengaruh pemberian
fosfat alam tidak berpengaruh nyata terhadap parameter berat kering tajuk.
Dari Tabel 6 dapat dilihat pada parameter berat kering akar padi yang
tertinggi yaitu P1 sebesar 26,47 g dan yang terendah yaitu P0 sebesar 14,95 g.
Dari hasil tersebut dapat kita ketahui bahwa pengaruh pemberian pupuk fosfat
Dari parameter amatan setelah panen yang telah diperoleh dapat diketahui
bahwa pemberian pupuk fosfat alamtidak menunjukkan respon yang nyata. Hal ini
menunjukkan bahwa tanaman padi varietas Ciherang memiliki respon yang
kurang baik terhadap pupuk fosfat alam ciamis di tanah sulfat masam potensial
desa Karanganyar.
Dari pengamatan yang dilakukan dilapang diperoleh informasi bahwa pada
tanah sulfat masam potensial yang diambil dari desa Karanganyar kecamatan
Secanggang ditemukan banyaknya sisah bahan organik yang belum melapuk
dengan sempurna, seperti jerami padi, dan akar-akar tanaman. Hal ini bisa
menjadi salah satu penyebab kenapa pupuk fosfat alam tidak memberikan
pengaruh yang nyata terhadap tinggi tanaman, jumlah anakan, berat kering
tajukdan akar padi. Pernyataan ini didukung oleh Zaini (2013) yang menyatakan
bahwa petani lebih sulit menggunakan pupuk secara spesifik lokasi, karena kalau
jerami atau sisa tanaman dikembalikan ke dalam tanah maka tanah tidak lagi
memerlukan pupuk P dan K dengan takaran tinggi.
Pada dasarnya pupuk fosfat alam merupakan deposit guano dengan
kandungan seskuioksida yang rendah serta slow release P yang dapat
menyebabkan lambat tersedianya P untuk tanaman. Dilirik dari fungsi unsur P
terhadap tanaman salah satunya yaitu merangsang perkembangan akar. Hal ini
menjadi alasan mengapa pemberian pupuk fosfat alam tidak berpengaruh secara
nyata terhadap tinggi tanaman, jumlah anakan, berat kering tajuk dan akar padi.
Ditambah oleh Subiksa dan Diah (2009) yang menyatakan bahwa Fosfat alam
adalah mineral apatit yang umumnya memiliki kelarutan yang rendah, sehingga
Dari Tabel 6 dapat dilihat bahwa Serapan P tanaman berbeda nyata akibat
pemberian perlakuan pupuk fosfat alam dengan berbagai dosis. Perlakuan terbaik
adalah dengan dosis fosfat alam 350 ppm (P7) dimana tanaman mampu menyerap
secara optimal. Hal ini dapat dilihat dari rataannya yang tertinggi diantara
perlakuan dosis lainnya.
Berdasarkan Tabel 6 dapat dilihat bahwa perlakuan dengan serapan P
tanaman tertinggi menunjukkan nilai P tersedia yang rendah di tanahnya. Hal ini
didukung oleh pernyataan Foth, dkk (1982) yang menyatakan bahwa hasil analisis
tanah yang rendah kemungkinan serapan P tanamannya akan tinggi, begitu
sebaliknya.
Penilaian Metode Analisis
Dari hasil analisis P tersedia tanah dengan dua metode P tersedia dan
serapan P tanaman dilakukan uji korelasi antara keduanya guna untuk menentukan
metode analisis P tersedia yang sesuai pada tanah sulfat masam potensial desa
Karanganyar kecamatan Secanggang. Adapun hasil uji korelasi tersebut dapat
[image:43.595.105.506.552.595.2]dilihat pada Tabel 7.
Tabel 7. Persamaan regresi dan koefisien korelasi antara kadar P tersedia tanah dengan serapan P tanaman
Metode Analisis Persamaan Regresi Koefisien Korelasi (r)
Bray II Y= 1,1997X + 20,023 0,261tn
Truog Y= 8,8721X + 60,2 0,256tn
Dari Tabel 7 dapat dilihat bahwa dari persamaan regresi dan koefisien
korelasi dari kedua Metode yang diuji-cobakan berpengaruh tidak nyata setelah
diuji dengan uji T α 5%.
Pemilihan metode analisis P tersedia tanah sulfat masam potensial yang
y = 1.1997x + 20.023 r = 0.261
0 20 40 60 80 100 120
20 21 22 23 24 25 26 27 28 29 30 31 32 33 34 35 36
S er ap an P T an am an ( % )
P-tersedia (ppm) Bray II
dengan bentuk P yang diserap oleh tanaman. Sehingga untuk menentukan metode
analisis P tersedia yang tepat adalah dengan mengambil metode analisis yang
memiliki koefisien korelasi (r) yang tertinggi. Dalam hal ini, Bray II merupakan
metode analisis yang terbaik untuk tanah sulfat masam potensial desa
Karanganyar kecamatan Secanggang dengan koefisien korelasi sebesar 0,261.
Hasil uji korelasi kadar P tersedia pada analisis metode Bray II terhadap
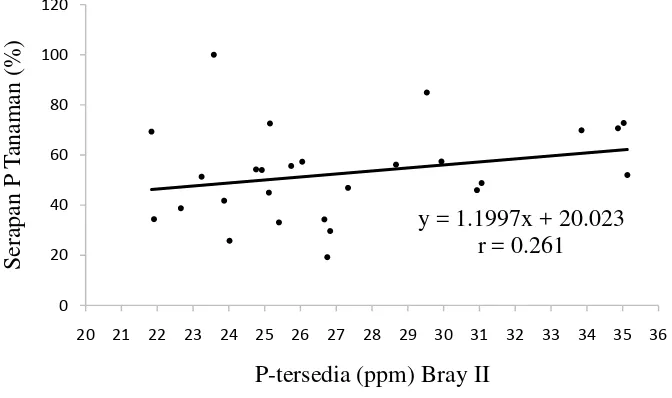
[image:44.595.146.482.293.492.2]serapan P tanaman dapat dilihat pada Gambar 1 berikut ini.
Gambar 1. Korelasi P tersedia metode Bray II terhadap serapan P tanaman
Dari Gambar 1, dapat dilihat bahwa koefisien korelasi kadar P tersedia
hasil analisis metode Bray II terhadap serapan P tanaman bernilai 0,261 dengan
persamaan regresi Y= 1,1997x + 20,023. Dari persamaan tersebut dapat kita
ketahui bahwa sifat dari hubungan antara P tersedia hasil analisis metode Bray II
terhadap serapan P tanaman berkorelasi positif, dimana koefisien X bernilai
positif.
Hasil uji korelasi kadar P tersedia pada analisis metode Truog terhadap
y = 8.8721x - 60.2 r = 0.256
0 20 40 60 80 100 120
11,5 12 12,5 13 13,5 14
S er ap an P T an am an ( % )
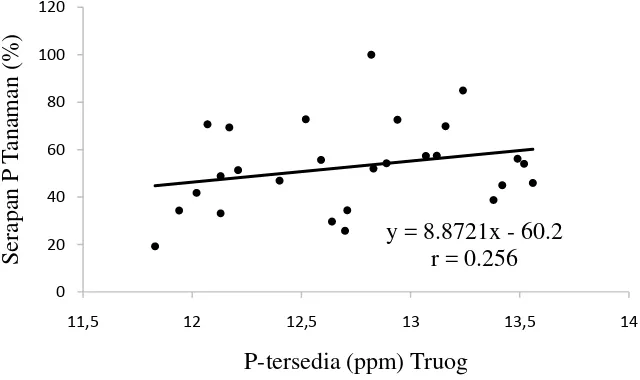
[image:45.595.154.474.93.283.2]P-tersedia (ppm) Truog
Gambar 2. Korelasi P tersedia metode Truog terhadap serapan P tanaman
Dari Gambar 2, dapat dilihat bahwa koefisien korelasi kadar P tersedia
hasil analisis metode Truog terhadap serapan P tanaman bernilai 0,256 dengan
persamaan regresi Y= 8,8721x + 60,2. Dari persamaan tersebut dapat kita ketahui
bahwa sifat dari hubungan antara P tersedia hasil analisis metode Truog terhadap
serapan P tanaman berkorelasi positif dimana koefisien X bernilai positif.
Koefisien korelasi (r) dari kedua uji tersebut tidak berbeda jauh, dimana r
untuk Bray II bernilai 0,261 dan r untuk Truog bernilai 0,256. Tetapi dalam
menentukan metode yang tepat untuk tanah sulfat masam potensial desa
Karanganyar kecamatan Secanggang ini yaitu dengan mengambil uji tanah yang
memiliki r2 tertinggi. Hal ini di dukung oleh pernyataan Ali dan Rahman (2010)
yang menyatakan bahwa Mengingat prinsipnya, semakin tinggi nilai r2 adalah
semakin cocok. Prosedur Nelson dan Bray lebih cocok untuk memprediksi respon
P untuk tanaman padi. Ditambah oleh Sims (2000) yang menyatakan bahwa
Ekstraksi Fosfat dengan metode Bray telah menunjukkan korelasi yang baik
dengan hasil tanaman pada tanah-tanah masam dan netral di beberapa daerah.
0 20 40 60 80 100 120
20 21 22 23 24 25 26 27 28 29 30 31 32 33 34 35 36
S er ap an P T an am an ( % )
P-tersedia (ppm) Bray II
dari fosfat aluminium dengan mengurangi aktivitas Al dalam larutan melalui
pembentukan berbagai kompleks Al-F. Fluoride juga efektif menekan readsorpsi
dari dilarutkannya P oleh koloid tanah.
Penetapan Batas Kritis P
Batas kritis hara P tersedia ditetapkan dengan metode Cate and Nelson
(1965) dengan cara menghubungkan antara kadar P tersedia tanah dari metode
yang terpilih yaitu metode Bray II dan Truog terhadap persentase hasil (serapan P
tanaman). Hubungan antara Serapan P tanaman (%) terhadap P tersedia metode
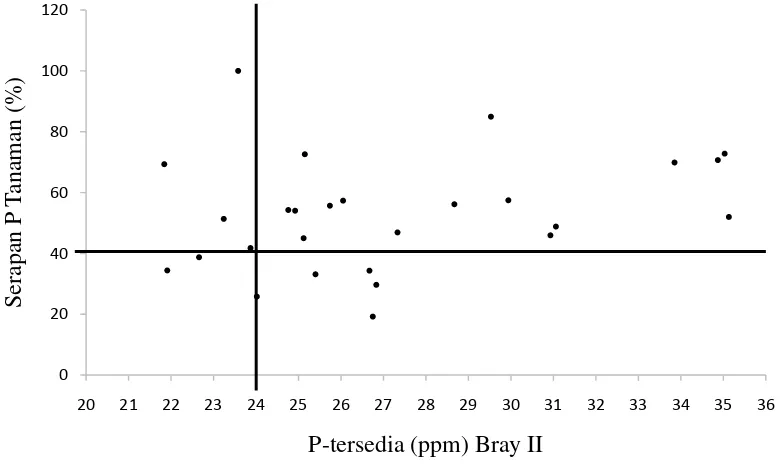
[image:46.595.111.503.332.570.2]Bray II dan Truog dapat dilihat dari Gambar 3 dan 4 dibawah ini.
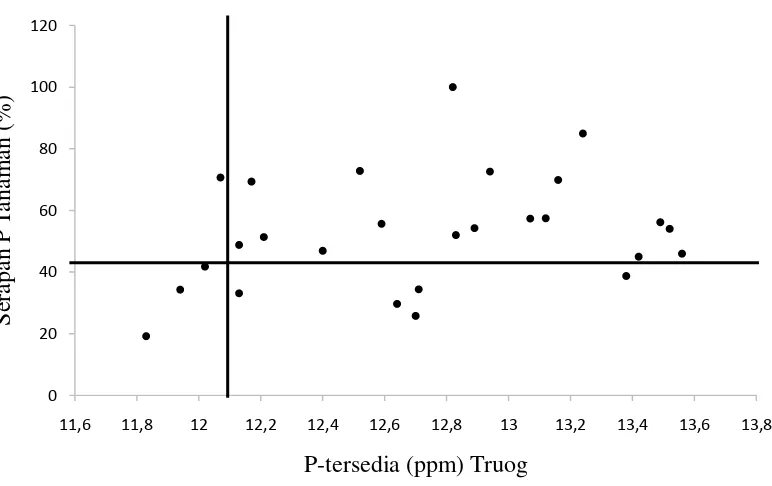
Gambar 3. Batas kritis P tersedia untuk metode Bray II
Dari Gambar 3 dapat dilihat bahwa sebaran titik terbanyak berada di
kuadran positif. Hal ini menunjukkan bahwa bentuk korelasi yang terjadi antara
serapan P tanaman (%) terhadap P tersedia tanah untuk kedua metode tersebut
0 20 40 60 80 100 120
11,6 11,8 12 12,2 12,4 12,6 12,8 13 13,2 13,4 13,6 13,8
S er ap an P T an am an ( % )
[image:47.595.129.515.83.326.2]P-tersedia (ppm) Truog
Gambar 4. Batas kritis P tersedia untuk metode Truog.
Dari Gambar 4 dapat dilihat bahwa sebaran titik terbanyak berada di
kuadran positif. Hal ini menunjukkan bahwa bentuk korelasi yang terjadi antara
serapan P tanaman (%) terhadap P tersedia tanah untuk metode tersebut yaitu
Korelasi Positif. Ditambah dari pernyataan Iswardono (2003) bahwa jika kenaikan
didalam satu variabel diikuti dengan kenaikan didalam variabel yang lain, maka
dapat dikatakan bahwa kedua variabel tersebut mempunyai korelasi yang positif.
Penentuan batas kritis hara P tersedia dengan metode Cate and Nelson
(1965) yaitu dengan cara menghubungkan antara kadar P tersedia tanah dari
metode Bray II dan Truog terhadap persentase hasil (serapan P tanaman). Adapun
nilai batas kritis tanah sulfat masam potensial desa Karanganyar kecamatan
Secanggang dengan serapan P tanaman untuk metode Bray II sebesar 24,1 ppm
KESIMPULAN DAN SARAN Kesimpulan
1. Metode analisis P tersedia tanah yang sesuai untuk tanah sulfat masam
potensial desa Karanganyar kecamatan Secanggang yaitu Bray II dengan nilai
r sebesar 0,261.
2. Batas kritis hara P tersedia tanah dari Bray II yaitu sebesar 24,1 ppm dan
Truog sebesar 12,13 ppm.
3. Pemberian fosfat alam berpengaruh nyata terhadap Serapan P tanaman dengan
perlakuan terbaik yaitu P7 (350 ppm).
Saran
Perlu dilakukan penelitian lanjutan terhadap penggunaan berbagai metode
DAFTAR PUSTAKA
Ali, M.I. dan G.K.M.M. Rahman. 2010. Phosphorus extractability in Bangladesh soils and its Critical limit for rice and wheat. Bangladesh Institute of Nuclear Agriculture. Scientific registration 954. Poster.
Damanik, M.M.B., B.E. Hasibuan., Fauzi, Sarifuddin, dan H. Hanum. 2011. Kesuburan tanah dan pemupukan. USU press, Medan.
Foth, H.D., L.V. Withee, H.S. Jacobs, dan S.J. Thien. 1982. Laboratory manual for introductory Soil science sixth edition. Wm.C.Brown company publishers, Iowa.
Gomez, K.A. 2001. Rice, the grain of culture. Board Member and Secretary of the Thai Rice Foundation. the Siam Society Lecture Series, Thailand.
Hanum, H. 2004. Peningkatan produktivitas tanah mineral masam yang baru disawahkan berkaitan dengan P tersedia melalui pemberian bahan organik, fosfat alam dan pencucian besi. Disertasi. IPB, Bogor.
Hutagalung, I. 2012. Tingkat ketersediaan logam berat kadmium akibat pemberian beberapa sumber fosfat dan waktu inkubasi pada bahan tanah andisol. Skripsi. Ilmu Tanah. Universitas Sumatera utara, Medan.
Iswardono. 2003. Sekelumit analisa regresi dan korelasi. Fakultas ekonomi UGM, Yogyakarta.
Lahuddin. 2011. Reaksi-reaksi kimia dalam tanah (chemical reactions in soils). USU Press, Medan.
Maas, A. 1989. Identifikasi tanah sulfat masam aktual dan potensial. Prosiding. Kongres nasional V Himpunan ilmu tanah Indonesia (Medan,7-10 desember) : Pp.1084-1090.
Mas’ud, P. 1992. Telaah kesuburan tanah. Penerbit Angkasa, Bandung.
Mukhlis. 2007. Analisis Tanah Tanaman. USU Press, Medan.
Nakano, Y. 2004. Water saving practices in rice paddy cultivation. ICID journal for irrigation system. Japan. http://www.icid.org/paddy_japan.pdf .
Noor, M. 2004. Lahan rawa, sifat dan pengelolaan tanah bermasalah sulfat masam. Penerbit PT Raja Grafindo persada, Jakarta.
Nurhayati, H., Y. Nyak, A.M. Lubis, S. Gani, R. Saul, A. Diha dan H.H. Baley. 1986. Dasar-dasar ilmu tanah. Penerbit UNILA, Lampung.
Putu, I. G. dan W. Adhi. 1990. Pengendalian keracunan besi pada lahan sulfat masam. Prosiding seminar pengelolaan sawah bukaan baru, prospek dan masalah. Fakultas pertanian universitas ekasakti dan balai penelitian tanaman pangan sukarami, Padang. hal. 199-215.
Rosmarkam, A. dan N.W. Yuwono. 2002. Ilmu kesuburan tanah. Penerbit Kanisius, Yogyakarta.
Rusd, A.M.I. 2011. Pengujian toleransi padi (Oryza sativa L.) terhadap salinitas pada fase perkecambahan. Skripsi. IPB, Bogor.
Sanchez, P.A. 1993. Sifat dan pengelolaan tanah tropika jilid 2. Penerbit ITB, Bandung.
Setyorini, D. dan S, Abdulrachman. 2009. Pengelolaan hara mineral tanaman padi, Badan Litbang Pertanian, Departemen Pertanian.
Sims, J.T. 2000. Soil test phosphorus: Bray and Kurtz P-1, Methods of phosphorus analysis for soils, sediments, residuals, and waters. Southern Cooperative series Bulletin No. 396, Manhattan.
Subbarayappa, C.T., U.D. Bongale dan N, Srinivasa. 2009. Determination of critical limits of phosphorus and zinc in soils and mulberry leaf. Karnataka J. Agric. Sci. 22(1): Pp. 95-98.
Subiksa, I.G.M. dan Diah S. 2009. Pemanfaatan fosfat alam untuk lahan sulfat masam, Buku Fosfat Alam: Pemanfaatan Pupuk Fosfat Alam sebagai Sumber Pupuk P, Balai Penelitian Tanah, Balai Besar Litbang Sumberdaya Lahan Pertanian. Badan Litbang Pertanian, Departemen Pertanian.
Suwandi, Amar M., dan Irsan C. 2012. Pendekatan terpadu berbasis aplikasi pupuk hayati majemuk untuk perbaikan kesuburan tanah, efisiensi pemupukan, toleransi terhadap hama-penyakit dan produksi padi pasang surut di kabupaten banyuasin. Prosiding. Insinas (Palembang, 29-30 November 2012): Pp. 92-97.
Swami, S. dan M. Singh. 2008. Critical limits of phosphorus for durum wheat in normal and heavy metal polluted soils. Indian J.Agric. Res. 42(4): Pp. 252-259.
Thompson, L.M. 1957. Soils and soil fertility. McGraw-Hill book company Inc., New York.
Tian-ren, Y. 1985. Physical chemistry of paddy soils. Science press, Beijing.
Winarso, S. 2005. Kesuburan tanah dasar kesehatan dan kualitas tanah. Penerbit Gava media, Yogyakarta.
Lampiran 1. Bagan Penelitian di Rumah Kasa FP USU
P7
P4
P8
P2 P6 P3 P1 P5
P0
P3
P0
P5
P8
P6
P7
P1
P2
P4
P5
P0 P1 P7 P6 P8 P4 P3 P2
U1 U2 U3
Lampiran 2. Prosedur Metode Bray II
Prinsip : P tersedia tanah diekstrak oleh NH4F dan HCl, P yang bebas direaksikan
dengan molibdat asam akan menjadi berwarna biru dengan adanya asam askorbat.
Perkembangan warna biru diukur sebagai kadar P secara spektrometri.
Alat-alat :
1. Shaker machine
2. Pipet skala dan volumetric
3. Corong
4. Spektronik
5. Tabung reaksi
6. Gelas Erlenmeyer
Bahan-bahan :
1. Larutan ammonium fluoride 1N
Larutkan 3.7 g NH4F dengan H2O menjadi 100 mL
2. Larutkan HCl 5N
Larutkan 20.2 mL HCl pekat dengan H2O menjadi 500 mL.
3. Larutkan Bray II
Larutkan 30 mL larutan NH4F 1N dengan 20 mL HCl 5N dan jadikan larutan
menjadi 1L dengan menambahkan H2O.
4. Asam sulfat 5N
Larutkan 140 H2SO4 pekat BD 1.84 kg/L dengan H2O hingga volume larutan
menjadi 1000 mL
5. Amonium molibdat
6. Kalium antimonite tartarat
Larutkan 0.298 g KSbOC4H4O6 dalam 100 mL H2O
7. Asam ascorbat
8. Pereaksi fosfat A
Campurkan bahan no. 4, 5, dan 6 jadikan 2 L dengan menambahkan H2O.
9. Pereaksi fosfat B
Campurkan 1 g Asam ascorbat ke dalam 200 mL pereaksi campuran A
10.Larutan standar P 50 ppm
Larutkan 0.275 g K2HPO4.3H2O dengan H2O hingga 1 L
11.Larutan standar 0-0.5-1.0-2.0-3.0-4.0-5.0 ppm P
Pipet larutan standar 50 ppm P masing-masing sebanyak 0-1-2-4-6-8 dan 10
mL ke dalam labu ukur 100 mL dan penuhkan dengan H2O.
Cara kerja :
1. Timbang 2 g contoh tanah dan tempatkan pada gelas Erlenmeyer 250 cc
2. Tambahkan larutan Bray II sebanyak 20 mL, dan goncang pada shaker selama
30 menit
3. Saring dengan kertas saring whatman no.42
4. Pipet filtrat sebanyak 5 mL dan tempatkan pada tabung reaksi
5. Tambahkan pereaksi fosfat B sebanyak 10 mL. biarkan selama 5 menit
6. Ukur transmitan pada spectronic dengan panjang gelombang 660 nm
7. Pada saat yang bersamaan pipet juga masing-masing 5 mL larutan standar
larutan standar P 0-0.5-1.0-2.0-3.0-4.0 dan 5.0 ppm P ke tabung reaksi,
8. Ukur juga transmitan standar pada spectronik dengan panjang gelombang
yang sama yaitu 660 nm
Perhitungan
Nilai Absorben = -log transmita/100
Buat kurva standar P (0-5 ppm P) sebagai sumbu X dan nilai absorben sebagai
sumbu Y. konsentrasi P larutan ditetapkan dengan menginterpolasikan nilai
absorben dari sampel ke kurva standar. (kurva standar dan interpolasi dapat
dilakukan secara mudah dengan menggunakan kalkulator pakai program LR).
Pavl (ppm) = Plrt X 20/2 X factor pengencer (bila ada)
Reaksi
3NH4F + 3HCl + AlPO4 PO43- + NH4+ + Al3+ + Cl- + F-
3NH4F + 3HCl + FePO4 PO43- + NH4+ + Fe3+ + Cl- + F
-Selanjutnya
PO43- + 12 MoO4= + 27H+ H7[P(Mo2O7)6] + 10H2O
Lampiran 3. Prosedur Metode Truog
Prinsip : P tersedia tanah diekstrak oleh NH4SO4, P yang bebas direaksikan
dengan molibdat asam akan menjadi berwarna biru dengan adanya asam askorbat.
Perkembangan warna biru diukur sebagai kadar P secara spektrometri
Alat-alat :
1. Shaker machine
2. Pipet skala dan volumetric
3. Corong
4. Spektronik
5. Tabung reaksi
6. Gelas Erlenmeyer
Bahan-bahan :
1. Larutan Asam Sulfat 0,002 N
Larutkan 0,055 mL H2SO4 96% dengan H2O menjadi 100 mL.
2. Larutan Truog
Larutkan 3 g (NH4)2SO4 dengan H2O menjadi 1 L dan tambahkan H2SO4
0,002 N set pH menjadi 3,0.
3. Asam sulfat 5N
Larutkan 140 H2SO4 pekat BD 1.84 kg/L dengan H2O hingga volume larutan
menjadi 1000 mL
4. Amonium molibdat
Larutkan 12 g (NH4)6Mo7O24.4H2O dengan H2O hingga 250 mL
5. Kalium antimonite tartarat
6. Asam ascorbat
7. Pereaksi fosfat A
Campurkan bahan no. 2, 3, dan 5 jadikan 2 L dengan menambahkan H2O.
8. Pereaksi fosfat B
Campurkan 1 g Asam ascorbat ke dalam 200 mL pereaksi campuran A
9. Larutan standar P 50 ppm
Larutkan 0.275 g K2HPO4.3H2O dengan H2O hingga 1 L
10.Larutan standar 0-0.5-1.0-2.0-3.0-4.0-5.0 ppm P
Pipet larutan standar 50 ppm P masing-masing sebanyak 0-1-2-4-6-8 dan 10
mL ke dalam labu ukur 100 mL dan penuhkan dengan H2O.
Cara kerja :
1. Timbang 2 g contoh tanah dan tempatkan pada gelas Erlenmeyer 250 cc
2. Tambahkan larutan Truogsebanyak 100 mL, dan goncang pada shaker
selama 30 menit
3. Saring dengan kertas saring whatman no.42
4. Pipet filtrat sebanyak 5 mL dan tempatkan pada tabung reaksi
5. Tambahkan pereaksi fosfat B sebanyak 10 mL. biarkan selama 5 menit
6. Ukur transmitan pada spectronic dengan panjang gelombang 660 nm
7. Pada saat yang bersamaan pipet juga masing-masing 5 mL larutan standar
larutan standar P 0-0.5-1.0-2.0-3.0-4.0 dan 5.0 ppm P ke tabung reaksi,
kemudian tambahkan 10 mL pereaksi fosfat B
8. Ukur juga transmitan standar pada spectronik dengan panjang gelombang
Perhitungan
Nilai Absorben = -log transmitan/100
Buat kurva standar P (0-5 ppm P) sebagai sumbu X dan nilai absorben sebagai
sumbu Y. konsentrasi P larutan ditetapkan dengan menginterpolasikan nilai
absorben dari sampel ke kurva standar. (kurva standar dan interpolasi dapat
dilakukan secara mudah dengan menggunakan kalkulator pakai program LR).
Pavl (ppm) = Plrt X 20/2 X factor pengencer (bila ada)
Reaksi
3NH4SO4 + AlPO4 PO43- + NH4+ + SO4-2
3NH4SO4 + FePO4 PO43- + NH4+ + SO4-2
Selanjutnya
PO43- + 12 MoO4= + 27H+ H7[P(Mo2O7)6] + 10H2O
Lampiran 4. Prosedur Penetapan P daun Alat-alat
1. Tabung reaksi
2. Spectrophotometer
Bahan-bahan
1. Asam Sulfat 5 N
Larutkan 140 mL H2SO4 pekat BD 1.84 dengan H2O hingga volume larutan
menjadi 1000
2. Amonium Molibdat
Larutkan 12 g (NH4)6Mo7O24.4H2O dengan H2O hingga 250 mL
3. Kalium antimonit tartarat
Larutkan 0.298 g KSbOC4H4O6 dalam 100 mL H2O
4. Asam ascorbat
5. Pereaksi fosfat A
Campurkan bahan no. 4, 5 dan 6 jadikan 2 L dengan menambahkan H2O
6. Pereaksi fosfat B
Campurkan 1 g Asam ascorbat ke dalam 200 mL pereaksi campuran A
7. Larutan standar P 50 ppm
Larutkan 0.275 g K2HPO4.3H2O dengan H2O hingga 1 L
8. Larutan standar 0-2,0-4,0-6,0-8,0-10,0 ppm P
Pipet larutan standar 50 ppm P masing-masing sebanyak 0-4-8-12-16-20 mL
Cara Kerja
1. Pipet 5 mL cairan destruksi encer tempatkan pada tabung reaksi
2. Tambahkan 10 mL Reagen fosfat B biarkan ± 10 menit. Kemudian ukur
transmitan (absorben) pada spectronic dengan λ 660 nm
3. Pada saat yang sama dilakukan pula pada larutan standar 0-2-4-6-8 dan 10
ppm P, dengan cara memipet masing-masing 5 mL dan ditambahkan 10 mL
Reagen fosfat B dan diukur pada spectronic
Perhitungan
P daun (%) = Plrt X 50/0,25 X 50/5 X 10-4
= Plarutan X 0,2
Lampiran 5
CIHERANG
Nomor seleksi : S3383-1D-PN-41-3-1
Asal persilangan : IR18349-53-1-3-1-3/3*IR19661-131-3-1-3//4*IR64
Golongan : Cere
Umur tanaman : 116-125 hari
Bentuk tanaman : Tegak
Tinggi tanaman : 107-115 cm
Anakan produktif : 14-17 batang