ESTERIFIKASI GLISEROL DENGAN ASAM LEMAK SAWIT
MENGGUNAKAN KATALIS
METHYL ESTER SULFONIC ACID
(MESA)
SRI WAHYUNI
SEKOLAH PASCASARJANA INSTITUT PERTANIAN BOGOR
PERNYATAAN MENGENAI TESIS DAN
SUMBER INFORMASI SERTA PELIMPAHAN HAK CIPTA
Dengan ini saya menyatakan bahwa tesis berjudul Esterifikasi Gliserol dengan Asam Lemak Sawit Menggunakan Katalis Methyl Ester Sulfonic Acid(MESA) adalah benar karya saya dengan arahan dari komisi pembimbing dan belum diajukan dalam bentuk apa pun kepada perguruan tinggi mana pun. Sumber informasi yang berasal atau dikutip dari karya yang diterbitkan maupun tidak diterbitkan dari penulis lain telah disebutkan dalam teks dan dicantumkan dalam Daftar Pustaka di bagian akhir tesis ini.
Dengan ini saya melimpahkan hak cipta dari karya tulis saya kepada Institut Pertanian Bogor.
Bogor, Oktober 2015
Sri Wahyuni
RINGKASAN
SRI WAHYUNI. Esterifikasi Gliserol dengan Asam Lemak Sawit Menggunakan Katalis Methyl Ester Sulfonic Acid (MESA) Dibimbing oleh ERLIZA HAMBALI
dan BONAR TUA HALOMOAN MARBUN.
Esterifikasi gliserol merupakan salah satu metode yang banyak digunakan untuk mengkonversi gliserol menjadi produk turunan yang bernilai tambah lebih tinggi. Produk yang dihasilkan bersifat terbarukan dan ramah lingkungan sehingga sangat berpotensi dimanfaatkan pada berbagai industri. Penelitian ini bertujuan untuk mengetahui pengaruh jenis asam lemak (asam oleat, asam stearat, asam palmitat, asam miristat) dan lama proses esterifikasi gliserol terhadap sifat fisiko-kimia gliserol ester yang dihasilkan. Penelitian ini terdiri atas dua tahap. Tahap pertama adalah persiapan sampel yang meliputi pemurnian gliserol hasil samping produksi biodiesel olein sawit dan analisis sifat fisiko-kimia sampel gliserol dan katalis MESA. Tahap selanjutnya dilakukan sintesis gliserol ester dengan mereaksikan gliserol 94 % dengan asam oleat, asam stearat, asam palmitat dan asam miristat menggunakan katalis MESA 0,5 % dalam reaktor yang dialiri gas nitrogen 100 cc/menit. Proses esterifikasi dilakukan pada suhu 180°C, dengan kecepatan pengadukan 400 rpm selama 90 menit, 120 menit dan 150 menit. Selanjutnya dilakukan analisis sifat fisiko-kimia gliserol ester yang meliputi rendemen, bilangan asam, densitas, viskositas kinematis, titik nyala, titik tuang dan pencirian spektrum dengan mengunakan FTIR.
Sifat-sifat gliserol ester ditentukan oleh karakteristik struktural asam lemak dan gliserol reaktannya. Penggunaan jenis asam lemak yang berbeda dan gliserol 94% pada proses sintesis gliserol ester memberikan pengaruh terhadap sifat fisiko-kimia gliserol ester yang dihasilkan. Rendemen yang dihasilkan semakin besar dengan meningkatnya lama proses esterifikasi dengan nilai tertinggi dihasilkan pada kondisi lama proses 150 menit. Gliserol ester oleat memiliki rendemen 93,1-98,1 % dengan sifat fisiko-kimia sebagai berikut bilangan asam 18,6-24,7 mg KOH/g sampel, densitas 0,910-0,913 g/cm3, viskositas kinematis (100 oC) 7,3-8,8 cSt, titik nyala 202-213 oC, dan titik tuang 0 oC. Gliserol ester stearat memiliki rendemen 94,5-96,1 % dengan sifat fisiko-kimia sebagai berikut bilangan asam 22,7-24,8 mg KOH/g sampel, densitas 0,899-0,903 g/cm3, viskositas kinematis (100 oC) 10,6-11,3 cSt, titik nyala 203-207 oC, dan titik tuang 54-55,5 oC. Gliserol ester palmitat memiliki rendemen 93,8-96 % dengan sifat fisiko kimia sebagai berikut bilangan asam 21,4-24,2 mg KOH/g sampel, densitas 0,907-0,909 g/cm3, viskositas kinematis (100 oC) 10,2-11,2 cSt, titik nyala 197-204 oC, dan titik tuang 54 oC. Gliserol ester miristat memiliki rendemen 92,3-96,0 % dengan sifat fisiko kimia sebagai berikut bilangan asam 20,9-24,1 mg KOH/g sampel, densitas 0,812-0,813 g/cm3, viskositas kinematis (100 oC) 4,2-4,3 cSt, titik nyala 173-179 oC, dan titik tuang 57 oC.
SUMMARY
SRI WAHYUNI. Esterification of Glycerol with Palm Fatty Acids Using The Methyl Ester Sulfonic Acid (MESA) Catalyst Supervised by ERLIZA HAMBALI
and BONAR TUA HALOMOAN MARBUN.
Glycerol esterification is one method widely used to convert glycerol into derivative products with more added values. The products are renewable and environmentally friendly so it potentially to applied in industries. This research aims to study the effect of fatty acids (oleic acid, stearic acid, palmitic acid and myristic acid) and time period process of glycerol esterification on physico-chemical properties glycerol ester. This studies have two stages. The first stage is the preparation of samples that include purification of glycerol using 5% (v/v) phosphoric acid 85 % and followed by refinery and vacuum distillation to producing glycerol with ± 94 % glycerol content and physico-chemical properties analysis of samples glycerol and MESA catalyst. The next stage is synthesis of glycerol ester by it reacted glycerol 94 % with oleic acid, stearic acid, palmitic acid and myristic acid), using the catalyst in a reactor MESA 0,5% nitrogen gas flowed 100 cc/min. Esterification process is conducted on temperature of 180 °C, with a stirring speed 400 rpm for 90 minutes, 120 minutes and 150 minutes. Next analysis of the physico-chemical properties of glycerol esters include extraction, acid number, density, kinematic viscosity, flash point, pour point and characterizing spectrum using FTIR.
The properties are determined by fatty acids characteristics structure of glycerol esters and reactant glycerol. The different types of fatty acids and glycerol 94% in synthesis glycerol ester significantly affected on physico-chemical properties of the resulted glycerol ester. The bigger yield is generated by increasing the long process of esterification with the highest value generated on the condition of 150 minutes. Oleic glycerol esters have 93.1-98.1 % of the yield with physico-chemical properties as follows acid number from 18.6-24.7 mg KOH/g sample, density of 0.910-0.913 g/cm3, kinematic viscosity (100 oC) 7.3-8.8 cSt, flash point 202-213 °C, and pour point 0 °C. Stearic glycerol esters have 94,5-96,1 % of the yield with physico-chemical properties as follows acid value 22.7-24.8 mg KOH/g sample, density 0.890-0.903 g/cm3, kinematic viscosity (100
oC) 10.6-11.3 cSt, flash point 203-207 °C, and pour point 54-55.5 °C. Palmitic
glycerol esters have 93.8-96 % of the yield with physico chemical properties as follows acid number from 21.4-24.2 mg KOH/g sample, the density 0.907-0.909 g/cm3, kinematic viscosity 10.2-11.2 cSt (100 °C), flash point 197-204 °C, and pour point 54 oC. Myristic glycerol esters have 92.3-96.0 % of the yield with physical and chemical properties as follows acid number 20.9-24.1 mg KOH/g sample, density 0.812-0.813 g/cm3, kinematic viscosity (100 °C) 4.2-4.3 cSt, flash point 173 -179 ° C, and pour point 57 oC .
© Hak Cipta Milik IPB, Tahun 2015
Hak Cipta Dilindungi Undang-Undang
Dilarang mengutip sebagian atau seluruh karya tulis ini tanpa mencantumkan atau menyebutkan sumbernya. Pengutipan hanya untuk kepentingan pendidikan, penelitian, penulisan karya ilmiah, penyusunan laporan, penulisan kritik, atau tinjauan suatu masalah; dan pengutipan tersebut tidak merugikan kepentingan IPB
Tesis
sebagai salah satu syarat untuk memperoleh gelar Magister Sains
pada
Program Studi Teknologi Industri Pertanian
ESTERIFIKASI GLISEROL DENGAN ASAM LEMAK SAWIT
MENGGUNAKAN KATALIS
METHYL ESTER SULFONIC ACID
(MESA)
SEKOLAH PASCASARJANA INSTITUT PERTANIAN BOGOR
BOGOR 2015
PRAKATA
Alhamdulillaahirobbil’alamiin, segala puji dan syukur penulis panjatkan kepada Allah SWT atas segala rahmat dan karunia-Nya, sehingga tesis dengan judul “Esterifikasi Gliserol dengan Asam Lemak Sawit Menggunakan Katalis
Methyl Ester Sulfonic Acid (MESA)” berhasil diselesaikan.
Terima kasih penulis ucapkan kepada Prof. Dr. Erliza Hambali dan Dr- Ing. Bonar Tua Halomoan Marbun selaku pembimbing yang telah memberikan arahan, bimbingan, dorongan semangat serta ilmu kepada penulis selama penelitian dan penyusunan karya ilmiah ini. Secara khusus, ungkapan terima kasih tak terhingga disampaikan kepada suami dan ananda tersayang yang selalu mendampingi atas cinta kasih, dorongan semangat, kesabaran dan doa. Begitu pula kepada orang tua (apa dan almh ama’) dan seluruh keluarga yang selalu mengirimkan doa, semangat dan kasih sayangnya kepada penulis. Penulis juga menyampaikan penghargaan yang setinggi-tingginya kepada staf manajemen dan peneliti di SBRC LPPM – IPB. Khususnya sahabat peneliti seperjuangan Fina, Kak Vonny, Wica terimakasih atas segala dukungan dan kebersamaan selama menyelesaikan penelitian.
Terimakasih kepada seluruh rekan mahasiswa pascasarjana S2 TIP IPB angkatan 2012 atas segala dukungan dan kebersamaan selama menempuh kuliah dan menyelesaikan studi. Ungkapan terimakasih juga disampaikan kepada Ibu Nur dan Pak Candra sebagai staff di Departemen S2 TIP yang tidak pernah bosan membantu.
Semoga karya ilmiah ini dapat memberikan manfaat kepada kita semua.
Bogor, Oktober 2015
v
DAFTAR ISI
DAFTAR ISI v
DAFTAR TABEL vi
DAFTAR GAMBAR vi
DAFTAR LAMPIRAN vii
1 PENDAHULUAN
Latar Belakang 1
Perumusan Masalah 2
Tujuan Penelitian 2
Manfaat Penelitian 2
Ruang Lingkup Penelitian 2
2 TINJAUAN PUSTAKA
Asam Lemak Sawit 3
Gliserol 3
Gliserol Ester 4
Katalis MESA 5
Penelitian Sebelumnya 6
3 METODE
Alat dan Bahan 9
Metode Penelitian 9
Waktu dan Tempat Penelitian 11
4 HASIL DAN PEMBAHASAN
Sifat Fisiko-Kimia Sampel Gliserol 12
Sifat Fisiko-Kimia Katalis MESA (Methyl Ester Sulfonic Acid) 15
Sifat Fisiko-Kimia Gliserol Ester 15
Rendemen 18
Bilangan Asam 19
Densitas 21
Viskositas kinematis 22
Titik Nyala 24
Titik Tuang 25
Hasil Analisis Spektrum FTIR 27
5 SIMPULAN DAN SARAN
Simpulan 30
Saran 30
DAFTAR PUSTAKA 31
LAMPIRAN 35
vi
DAFTAR TABEL
2.1 Komposisi asam lemak minyak sawit (CPO) 3
2.2 Perkembangan studi kondisi proses gliserol ester hasil penelitian sebelumnya 6 4.1 Sifat fisikokimia gliserol kasar dan gliserol hasil pemurnian 13
4.2 Sifat fisikokimia katalis MESA 15
DAFTAR GAMBAR
2.1 Visualisasi molekul dan rumus struktur kimia gliserol 3 2.2 Reaksi pembentukan gliserol dengan metode transesterifikasi 4 2.3 Reaksi esterifikasi antara gliserol dengan asam lemak 4
3.1 Diagram alir penelitian 9
4.1 Tiga lapisan yang terbentuk setelah penambahan asam fosfat 12 4.2 (A) Reaksi pembentukan garam K3PO4; (B) Reaksi pembentukan FFA 13
4.3 (A) Gliserol kasar 45 %; (B) Gliserol hasil pemurnian 94 % 14
4.4 Reaksi pembentukan asam lemak bebas 15
4.5 Reaksi pembentukan: (A) Gliserol monoester; (B) Gliserol diester dan (C)
Gliserol trimester 16
4.6 Dua lapisan hasil esterifikasi (pada suhu ruang) 17
4.7 Jenis asam lemak dan hasil esterifikasi: (A) Asam lemak oleat, stearat, palmitat, miristat; (B) Gliserol ester oleat, stearat, palmitat, miristat 17
4.8 Rendemen produk gliserol ester 18
4.9 Pengaruh jenis asam lemak dan lama proses esterifikasi terhadap bilangan
asam gliserol ester 19
4.10 Pengaruh jenis asam lemak dan lama proses esterifikasi terhadap densitas
gliserol ester 21
4.11 Pengaruh jenis asam lemak dan lama proses esterifikasi terhadap viskositas
kinematis gliserol ester 23
4.12 Pengaruh jenis asam lemak dan lama proses esterifikasi terhadap titik nyala
gliserol ester 24
4.13 Pengaruh jenis asam lemak dan lama proses esterifikasi terhadap titik tuang
gliserol ester 26
4.14 Profil FTIR (A) asam oleat; (B) Gliserol; (C) Sisa gliserol dan (D) Gliserol
vii
DAFTAR LAMPIRAN
1 Prosedur analisis 35
2 Tabel data, analisis varian (α=η%), dan uji Duncan parameter rendemen 40 3 Tabel data, analisis varian (α=η%), dan uji Duncan parameter bilangan
asam 41
4 Tabel data, analisis varian (α=η%), dan uji Duncan parameter densitas 43 5 Tabel data, analisis varian (α=η%), dan uji Duncan parameter viskositas
kinematis
1
1
PENDAHULUAN
Latar Belakang
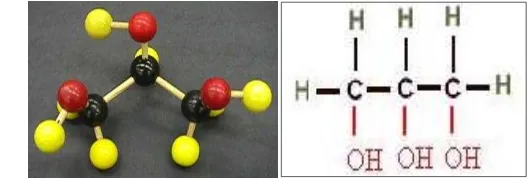
Gliserol (C3H8O3) merupakan senyawa golongan alkohol polihidrat dengan
tiga buah gugus hidroksil dalam satu molekul, bersifat polar kental (viscous) dan
mempunyai banyak kegunaan di berbagai industri. Gliserol dapat diperoleh melalui proses transesterifikasi pada industri biodiesel, proses saponifikasi pada industri sabun dan proses hidrolisis pada industri fatty acid.
Konsumsi bioenergi dalam negeri akan terus meningkat karena didukung dengan adanya kebijakan mandatori biodiesel melalui Permen ESDM No. 20 Tahun 2014. Peraturan tersebut menetapkan kewajiban pemanfaatan minimal biodiesel sebagai campuran BBM secara bertahap sampai tahun 2025 sehingga menjadi pemicu meningkatnya kegiatan produksi biodiesel yang tentunya juga diiringi dengan peningkatan produksi gliserol. Hal ini karena gliserol merupakan senyawa hasil samping utama pada industri biodiesel.
Pada industri biodiesel akan dihasilkan gliserol sebanyak 12,5 % dari kapasitas produksinya dengan tingkat kemurnian yang masih rendah karena mengandung komponen air dan bahan pengotor lainnya. Realisasi produksi industri biodiesel nasional saat ini telah mencapai 3,2 juta kL untuk tahun 2014 (KESDM 2014), yang berarti dihasilkan pula gliserol kasar sekitar 400 ribu kL. Peningkatan kapasitas produksi industri biodiesel akan menyebabkan meningkatnya produksi gliserol kasar, sehingga harus diiringi dengan perluasan pasar dan peningkatan nilai tambah agar gliserol tetap bernilai jual.
Peningkatan nilai tambah gliserol hasil samping industri biodiesel ini harus dilakukan agar dapat memenuhi kebutuhan berbagai industri dan stakeholder terkait. Kegiatan yang dapat dilakukan untuk mencapai tujuan tersebut adalah melalui penelitian pengembangan pemanfaatan gliserol. Banyak penelitian yang telah dilakukan untuk menghasilkan produk turunan gliserol. Salah satu metode yang dapat digunakan adalah proses esterifikasi gliserol dengan asam lemak sawit menjadi gliserol ester. Gliserol ester adalah emulsifier yang banyak dibutuhkan oleh industri pangan dan industri kimia.
Pada beberapa negara penghasil kedelai, saat ini gliserol hasil samping biodiesel minyak kedelai sedang dikembangkan menjadi base fluid dalam drilling fluid untuk kebutuhan pemboran sumur minyak. Derivatif gliserol berupa ester,
terutama ester parsial (mono- dan di-gliserida) telah menjadi komponen yang sangat khusus untuk produk emulsi. Sifat emulsi dan pelumas dari derivated gliserol ini dimanfaatkan untuk meningkatkan kualitas lumpur pemboran minyak dengan menjadikannya sebagai bahan formulasi pembuat oil based mud (OBM).
Selama ini OBM tidak banyak digunakan karena mahal dan kurang ramah lingkungan (Soares et al. 2011). Untuk itu diperlukan derivated gliserol sebagai
alternatif lain dalam penggunaan bahan dasar lumpur dari bahan terbarukan dan ramah lingkungan sehingga kadar aromatik dan sifat toksiknya berkurang.
2
biodiesel olein sawit dengan asam lemak miristat, asam lemak palmitat asam lemak stearat dan asam lemak oleat.
Hasil penelitian ini diharapkan dapat memberikan informasi lama proses terbaik esterifikasi gliserol 94 % dengan asam lemak miristat, asam lemak palmitat, asam lemak stearat dan asam lemak oleat yang menggunakan katalis
Methyl Ester Sulfonic Acid (MESA) dan mendapatkan hasil sifat fisiko-kimia
gliserol ester tersebut.
Perumusan Masalah
Proses esterifikasi gliserol sebagai salah satu alternatif untuk mengatasi jatuhnya harga gliserol. Melalui proses esterifikasi gliserol, akan dapat ditingkatkan nilai tambah gliserol sehingga tetap bernilai jual. Oleh karena itu diperlukan suatu pengembangan pemanfaatan gliserol dengan melakukan proses esterifikasi gliserol dengan beberapa asam lemak sawit sehingga dapat memperluas fungsi dan kegunaan dari gliserol. Kondisi proses yang optimum dengan lama proses esterifikasi yang tepat diharapkan akan meningkatkan efektifitas dan efisiensi pembentukan gliserol ester. Hal tersebut merupakan sebuah tantangan untuk memperoleh sifat fisiko-kimia gliserol ester yang baik dan karakteristiknya sesuai dengan kebutuhan berbagai industri.
Tujuan Penelitian
Penelitian ini bertujuan untuk mengetahui pengaruh jenis asam lemak miristat, asam lemak palmitat asam lemak stearat dan asam lemak oleat dan lama proses esterifikasi gliserol 94 % menggunakan katalis MESA 0,5 % dengan rasio mol gliserol dan asam lemak 0,94:1 terhadap sifat fisiko-kimia gliserol ester yang dihasilkan.
Manfaat Penelitian
Hasil penelitian ini diharapkan dapat menghasilkan informasi sifat fisiko-kimia gliserol ester berdasarkan jenis asam lemak dan lama proses esterifikasi sehingga dapat menjadi acuan untuk proses esterifikasi gliserol dengan asam lemak lainnya. Selain itu juga diharapkan dihasilkan ester-ester asam lemak dengan fungsi dan kegunaan yang lebih baik sehingga dapat memperluas pemanfaatannya di berbagai industri.
Ruang Lingkup Penelitian
Penelitian ini dibatasi pada ruang lingkup berikut ini.
1. Gliserol yang digunakan adalah gliserol hasil transesterifikasi olein sawit. 2. Pemurnian gliserol menggunakan asam fosfat teknis 85 % sebanyak 5 %
(v/v).
3. Katalis yang digunakan adalah Methyl Ester Sulfonic Acid (MESA)
sebanyak 0,5 % (w/w).
3
2
TINJAUAN PUSTAKA
Asam Lemak Sawit
Minyak kelapa sawit mentah (CPO) merupakan minyak yang berasal dari sabut (mesokarp) yang dapat diolah menjadi metil ester, asam lemak (fatty acid),
dan gliserol (glycerine) (Ketaren 2008). Minyak kelapa sawit kasar (Crude Palm Oil) tersusun atas 50 % asam lemak jenuh seperti asam kaprat (1-3 %), asam
laurat (0-1 %), asam miristat (0,9-1,5 %), asam pamitat (39,2-45,8 %), asam stearat (3,7-5,1 %) dan 50 % asam lemak tidak jenuh seperti asam oleat (37,44-44,1 %), asam linoleat (8,7-12,5 %) dan asam linolenat (0,0-0,6 %) (Basiron 2005). Komposisi asam lemak CPO disajikan pada Tabel 2.1.
Tabel 2.1. Komposisi asam lemak minyak sawit (CPO)
Jenis Asam Lemak
Kadar (%) Titik Cair (°C)
CPO* CPO** Olein** Stearin** Asam Lemak Jenuh
Asam kaprat (C10:0) 1-3 - - - 31,5
Asam laurat (C12:0) 0-1 0,1-0,4 0,2-0,4 0,1-0,3 44 Asam miristat (C14:0) 0,9-1,5 1,0-1,4 0,9-1,2 1,1-1,7 58
Asam palmitat (C16:0) 39,2-45,8
40,9-47,5
36,8-43,2
49,8-68,1 64 Asam stearat (C18:0) 3,7-5,1 3,8-4,8 3,7-4,8 3,9-5,6 70
Asam Lemak Tidak Jenuh
Asam oleat (C18:1) 37,4-44,1 36,4-4,2 39,8-44,6 20,4-34,4 14 Asam linoleat (C18:2) 8,7-12,5 9,2-11,6 10,4-12,9 5,0-8,9 -11 Asam linolenat (C18:3) 0,0-0,6 0,05-0,6 0,1-0,6 0,0-0,5 -9
Sumber : *Basiron (2005), **Gee (2007)
Gliserol
Gliserol (C3H5(OH)3) dengan nama kimia 1,2,3-propanetriol merupakan
cairan kental yang memiliki rasa manis, tidak berwarna, tidak berbau, mudah larut air, meningkatkan viskositas larutan, mengikat air dan menurunkan aktivitas air (aw). Gliserol juga larut sempurna dalam alkohol, eter dan etil asetat, namun tidak larut dalam hidrokarbon. Gliserol memiliki berat molekul sebesar 923 g/mol, densitas 1,26 g/ml, viskositas 1,5 Pa.s, titik leleh 17,8°C dan titik nyala 290°C (Pagliaro dan Rossi 2008). Visualisasi molekul dan rumus struktur gliserol dapat dilihat pada Gambar 2.1.
4
Produksi gliserol dari asam lemak dapat dilakukan melalui tiga metode, yaitu metode transesterifikasi, saponifikasi dan hidrolisis (Tovbin et al. 1976).
Akhir dari proses tersebut menghasilkan senyawa gliserol mentah yang masih banyak mengandung partikel-partikel pengotor diantaranya sisa metanol, sisa katalis dan asam lemak bebas sehingga perlu dimurnikan agar dapat dimanfaatkan. Reaksi pembentukan gliserol dari transesterifikasi trigliserida dengan metanol dalam produksi biodiesel dapat dilihat pada Gambar 2.2.
Trigliserida Metanol Gliserol Metil Ester Gambar 2.2. Reaksi pembentukan gliserol dengan metode transesterifikasi
Pemurnian gliserol kasar dapat dilakukan dengan banyak metode diantaranya menggunakan asam sulfat, aqua demineralisasi (aqua DM), vakum
distilasi, kombinasi perlakuan fisikokimia dan distilasi. Proses peningkatan kemurnian gliserol yang lebih sederhana dan relatif lebih murah dilakukan oleh Farobie (2009) dengan cara mereaksikan gliserol kasar dengan asam fosfat teknis sebanyak 5 % (v/v). Proses ini berhasil meningkatkan kemurnian gliserol dari 50 % menjadi 82,15 % dan menghasilkan produk samping berupa garam kalium fosfat yang dapat digunakan sebagai pupuk dan asam lemak.
Gliserol Ester
Gliserol ester merupakan senyawa turunan dari asam karboksilat yang dihasilkan dari proses esterifikasi gliserol dengan asam lemak. Dalam proses esterifikasi terjadi penggantian satu (atau lebih) atom hidrogen pada gugus
hidroksil dengan suatu gugus organik (biasa dilambangkan dengan R’). Reaksi esterifikasi gliserol dengan asam lemak dapat dilihat pada Gambar 2.3.
C3H5(OH)3 + RCOOH C3H5(OH)2OCR + H2O
Gliserol As. Karboksilat Gliserol Ester Air
Gambar 2.3. Reaksi esterifikasi gliserol dengan asam lemak
5 alkohol, menghasilkan senyawa kompleks teraktivasi. Selanjutnya terjadi protonasi terhadap salah satu gugus hidroksil yang diikuti dengan pelepasan molekul air dan menghasilkan ester (Fessenden & Fessenden 1982).
Reaksi esterifikasi merupakan reaksi endotermal yang bersifat reversible sehingga konversi sempurna tidak mungkin tercapai. Kirk dan Othmer (1994) menjelaskan bahwa apabila salah satu reaktan dibuat berlebih, maka reaksi kesetimbangan akan bergeser ke arah kanan (pembentukan ester) dan tumbukan antar molekul semakin besar yang mengakibatkan konversi menjadi produk semakin besar pula. Laju reaksi esterifikasi sangat dipengaruhi oleh struktur molekul reaktan dan radikal yang terbentuk dalam senyawa antara.
Secara umum laju reaksi esterifikasi mempunyai sifat sebagai berikut : a. Alkohol primer bereaksi paling cepat, disusul alkohol sekunder, dan paling
lambat alkohol tersier.
b. Ikatan rangkap memperlambat reaksi.
c. Makin panjang rantai alkohol, cenderung mempercepat reaksi atau tidak terlalu berpengaruh terhadap laju reaksi.
Faktor-faktor yang mempengaruhi reaksi esterifikasi yaitu :
a. Lama reaksi; semakin lama proses reaksi maka kontak antar zat semakin besar, sehingga akan menghasilkan biodiesel dengan konversi yang besar. Jika kesetimbangan reaksi sudah tercapai, maka dengan bertambahnya waktu reaksi tidak akan menguntungkan karena tidak akan menaikkan konversi. b. Pengadukan; pengadukan akan menambah bilangan gelombang tumbukan
antara molekul zat pereaksi dengan zat yang bereaksi, sehingga mempercepat reaksi. Semakin besar tumbukan, maka semakin besar pula nilai konstanta kecepatan reaksi (k).
c. Katalisator; katalisator berfungsi untuk mengurangi tenaga aktivasi pada suatu reaksi sehingga pada suhu tertentu nilai konstanta kecepatan reaksi semakin besar.
d. Suhu reaksi; semakin tinggi suhu yang dioperasikan maka semakin tinggi konversi yang dihasilkan, hal ini sesuai dengan persamaan Arrhenius. Bila suhu naik, maka nilai konstanta kecepatan reaksi (k) makin besar, sehingga reaksi berjalan cepat dan konversi ester makin tinggi.
Produk kasar yang diperoleh dari proses esterifikasi gliserol merupakan campuran dari asam-asam lemak dan gliserol yang tidak bereaksi, monogliserida, digliserida (1,2- dan 1,3-) dan trigliserida dengan komposisi yang berbeda (Susi 2010). Komposisi produk tersebut tergantung dari rasio gliserol terhadap asam lemak, jenis asam lemak, jenis dan konsentrasi katalis serta kondisi reaksi yang digunakan dalam proses.
Katalis MESA
Katalis merupakan salah satu faktor yang memberikan pengaruh penting pada proses esterifikasi. Katalis ikut serta dalam suatu tahap reaksi, akan tetapi pada akhir reaksi katalis akan terbentuk kembali. Tujuan penggunaan katalis untuk menghindari kebutuhan temperatur yang tinggi, waktu reaksi yang lebih lama serta produk yang berwarna gelap (Hui 1996).
6
terhadap aktivitas katalitiknya. Katalis homogen asam sebagai donor proton dalam pelarut organik yang banyak digunakan pada awalnya adalah H2SO4, HF, H3PO4,
RSO3H dan PTSA. Hanya saja katalis-katalis tersebut bersifat korosif dan beracun
(Juan et al. 2007).
Pada beberapa penelitian sebelumnya katalis p-toluena sulfonic acid
(PTSA) banyak digunakan karena merupakan katalis organik dari jenis asam kuat yang bersifat non-oksidator meskipun dapat menyebabkan iritasi pada kulit. Katalis PTSA lebih aktif daripada asam sulfat karena sifat hidrofobilitasnya yang tinggi sehingga mudah menyerang molekul trigliserida, sebaliknya asam sulfat selain sifatnya dapat mengoksidasi, kemampuannya bercampur dengan minyak (hidrofobilitasnya) juga rendah (Guan 2009). Namun katalis tersebut bersifat korosif dan berasal dari minyak bumi yang merupakan sumber daya alam tak terbarukan sehingga kurang ramah lingkungan sehingga diperlukan katalis baru untuk menjawab permasalahan tersebut. Oleh karena itu diperlukan katalis dari sumber daya alam terbarukan dan harganya ekonomis seperti Methyl Ester Sulfonic Acid.
Katalis Methyl Ester Sulfonic Acid (MESA) merupakan produk antara
dalam produksi MES, berwarna gelap dan bersifat asam, dihasilkan dari minyak kelapa sawit melalui reaksi sulfonasi metil ester dengan SO3. Utami (2013)
melaporkan bahwa MESA memberikan pengaruh signifikan terhadap sifat fisiko-kimia gliserol ester oleat yang dihasilkan yaitu mendekati gliserol ester komersial, Sarapar dan Saraline. Penelitian terbaru dilakukan oleh Andriani (2014) dan Kurniati (2014) menggunakan katalis MESA untuk menghasilkan mono-diasilgliserol (MAG dan DAG) dan memperoleh rendemen 30,2 %. Putri (2014) juga menggunakan katalis MESA untuk menghasilkan gliserol ester oleat dan memperoleh rendemen 79,55 %.
Penelitian Sebelumnya
Tabel 2.2. Perkembangan studi kondisi proses gliserol ester hasil penelitian sebelumnya
Kondisi proses Performa Rujukan
Esterifikasi gliserol dengan asam oleat, rasio mol (1:1,32; 2:1; 3:1; 4:1;4.68 :1) atau % berat KOH terhadap asam oleat (0,009; 0,03; 0,06; 0,09; 0,11)%, temperatur rasio molar gliserol terhadap asam oleat 3:1, katalis KOH 0,16% (terhadap berat asam oleat), temperatur 180 oC, waktu reaksi 77,5 menit dan kecepatan putaran pengaduk 600 rpm
Pardi (2005)
Reaksi tanpa katalis; temperatur 170 oC, vakum (P-40 kPa), rasio
Konversi gliserol dan perolehan MCT yang terbaik dicapai pada reaksi esterifikasi tanpa katalis dalam kondisi vakum dan waktu reaksi 8 jam, yaitu berturut-turut sebesar 100% dan 97,80%
7 Tabel 2.2. Perkembangan studi kondisi proses gliserol ester hasil penelitian
sebelumnya (lanjutan)
Kondisi proses Performa Rujukan
Esterifikasi asam oleat dan gliserol menggunakan katalis laju penurunan bilangan asam terbesar dan menghasilkan yield FAME sebesar 93.75 % dengan waktu 90 menit, rasio katalis dan reaktan 1:100, rentang berat
8
Tabel 2.2. Perkembangan studi kondisi proses gliserol ester hasil penelitian sebelumnya (lanjutan)
Kondisi proses Performa Rujukan
Proses esterifikasi gliserol dan asam oleat dengan katalis MESA gliserol ester oleat dengan bilangan asam terendah yakni 48,07 mg KOH/g sampel, densitas 0,9124 g/cm3, viskositas 68,32 Cp (25°C), viskositas kinematis 36 cSt (40°C), titik nyala 230°C dan titik tuang -15°C
Utami (2013)
Esterifikasi gliserol dan asam lemak PFAD dengan katalis 30,20%, persentase fraksi MAG 16,21%, DAG 31,00%
Andriani (2014)
Esterifikasi gliserol dengan asam
lemak bebas PFAD. terbaik adalah pada suhu 160 °C dengan rasio volume 1:3 dan
Proses esterifikasi gliserol dan asam oleat dengan katalis MESA
Rasio molar dan konsentrasi katalis MESA terbaik ialah rasio molar 0,8:1 (gliserol : asam oleat), katalis MESA sebanyak 0,5% menghasilkan gliseril ester dengan rendemen 79,55%, densitas 0,940 g/cm3, bilangan asam 44 mg KOH/g sampel, viskositas 90 cP (30 oC), viskositas kinematis 49,04 cSt (40 oC), titik nyala 206 oC, titik tuang -1,5 oC, titik didih 105 oC.
9
3
METODE
Alat dan Bahan
Bahan yang digunakan adalah gliserol hasil samping industri biodiesel dari SBRC (Surfactant and Bioenergy Research Center) IPB, asam oleat dari PT
Brataco Chemical, asam stearat dan asam palmitat diperoleh dari PT Wilmar serta asam miristat dari PT Ecogreen Oleochemical, katalis MESA dari SBRC IPB, asam fosfat teknis 85% dari Toko kimia Setiaguna Bogor dan gas nitrogen dari PT Rahayu Mulya Gas Bogor. Bahan untuk analisis meliputi asam sulfat, larutan NaOH dan NaIO4, etilen glikol, alkohol netral, larutan Wijs, larutan KI, indikator bromtimol biru dan indikator PP dari Toko kimia Frisconina Bogor.
Peralatan yang digunakan terdiri atas alat-alat proses seperti reaktor pemurnian gliserol berkapasitas 20 liter dan reaktor esterifikasi berupa labu leher tiga, hot plate, termometer, neraca analitik dan kondensor. Untuk analisis
digunakan density meter DMA 4500M Anton Paar, viscometer Brookfield DV-III
ultra, viscometer Otswald dan pH meter, Pensky-Martens closed cup tester, jar test, aniline point apparatus dan FTIR spektrofotometer.
Metode Penelitian
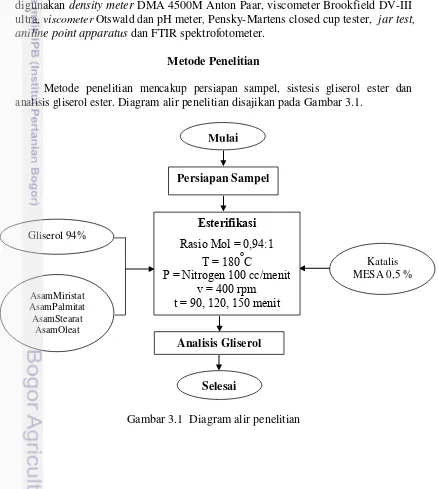
Metode penelitian mencakup persiapan sampel, sistesis gliserol ester dan analisis gliserol ester. Diagram alir penelitian disajikan pada Gambar 3.1.
Gambar 3.1 Diagram alir penelitian Mulai
Katalis MESA 0,5 %
Selesai Esterifikasi
Rasio Mol = 0,94:1 T = 180oC
P = Nitrogen 100 cc/menit v = 400 rpm
t = 90, 120, 1η0 menit
AnalisisGliserol Ester
AsamMiristat AsamPalmitat AsamStearat
AsamOleat As.
Gliserol 94%
10
Persiapan Sampel
Tahap persiapan sampel meliputi pemurnian gliserol, analisis gliserol sampel dan katalis MESA.
Pemurnian Gliserol
Pemurnian gliserol dilakukan dengan menggunakan reaktor pemurnian yang meliputi proses pengasaman (asidifikasi) dengan menggunakan asam fosfat teknis
85 % sebanyak 0,5 % (v/v) kemudian dilanjutkan dengan proses vakum filter dan vakum distilasi.
Proses pemurnian yang dilakukan adalah sebagai berikut: gliserol kasar dipanaskan mencapai suhu 50 oC kemudian ditambahkan asam fosfat teknis sebanyak 5 % (v/v). Selanjutnya reaksi dilakukan pada suhu 75-80 oC dan diaduk selama 4 jam. Produk yang terbentuk didiamkan selama 1 jam sehingga terbentuk tiga lapisan. Lapisan paling bawah berbentuk padatan merupakan garam kalium fosfat, lapisan tengah adalah gliserol dan lapisan atas adalah sisa asam lemak. Lapisan tengah dan atas dipisahkan dari lapisan paling bawah. Filtrat yang dihasilkan kemudian dipisahkan dengan vakum filter. Pemurnian dilanjutkan dengan destilasi vakum untuk menguapkan air dan sedikit metanol yang masih terkandung dalam gliserol. Distilasi vakum dilakukan dua tahap yaitu pada temperatur 95 oC dan 150 oC selama 3 jam dan dihasilkan gliserol murni dengan kadar 94 %.
Analisis Sifat Fisiko-kimia Sampel Gliserol dan Katalis MESA
Analisis sifat fisikokimia gliserol yang dilakukan mencakup kadar abu (SNI 06-1564-1995), kadar gliserol (SNI 06-1564-1995), densitas dengan menggunakan densitymeter DMA 4500M Anton Paar, viskositas dengan
menggunakan viscometer Brookfield DV-III ultra, warna (visual), pH dengan
menggunakan pH meter, bilangan asam (SNI 01-3555-1998), titik nyala (ASTM D 92 2005a), titik tuang (ASTM D 97 2009) dan kadar air (SNI 06-1564-1995).
Analisis sifat fisikokimia katalis MESA mencakup densitas dengan menggunakan density meter DMA 4500M Anton Paar, viskositas dengan
menggunakan viscometer Brookfield DV-III ultra, pH dengan menggunakan pH
meter, warna (visual), dan bilangan asam (SNI 01-3555-1998). A. Sintesis Gliserol Ester
11 Rancangan percobaan yang digunakan pada tahap sintesis gliserol ester adalah Rancangan Acak Lengkap (RAL) faktorial. Model yang digunakan tersusun atas 2 faktor perlakuan, yaitu faktor pertama adalah jenis asam lemak sawit yang terdiri dari empat taraf yaitu A1 = asam lemak oleat, A2 = asam lemak stearat, A3 = asam lemak palmitat dan A4 = asam lemak miristat. Faktor kedua adalah perlakuan waktu dengan tiga taraf, yaitu B1 = 90 menit, B2 = 120 menit dan B3 = 150 menit. Setiap kombinasi faktor perlakuan diulang dua kali. Model matematis dari rancangan percobaan adalah sebagai berikut.
Yijk = μ + Ai + Bj + (AB)ij + εijk
Keterangan:
Yijk = nilai pengamatan akibat pengaruh faktor A taraf ke-i dan faktor B taraf ke-j pada ulangan ke-k
= nilai rata- rata
Ai = pengaruh jenis asam lemak taraf ke-i (i = 1, 2,3,4) Bj = pengaruh faktor perlakuan waktu taraf ke-j (j = 1, 2,3) (AB)ij = pengaruh interaksi faktor A taraf ke-i, faktor B taraf ke-j
εijk = galat satuan percobaan taraf ke-i faktor A, taraf ke-j faktor B, pada ulangan ke-k (k = 1, 2)
Analisis Gliserol Ester
Adapun analisis sifat fisikokimia gliserol ester mencakup bilangan asam (SNI 01-3555-1998), densitas dengan menggunakan density meter DMA 4500M
Anton Paar, viskositas kinematis dengan menggunakan vikometer Otswald (ASTM D 445 2009), titik nyala dengan menggunakan Pensky-Martens closed cup tester (ASTM 92 2005a), titik tuang dengan menggunakan jar test (ASTM D
97 2009), titik anilin dengan aniline point apparatus (ASTM D 611–04) dan
pencirian spektrum dengan spektrofotometer Fourier-Transformed Infra Red
(FTIR).
Waktu dan Tempat Penelitian
Penelitian ini dilaksanakan selama tujuh bulan dimulai pada bulan Juni 2014 sampai dengan Januari 2015 di laboratorium Surfactant and Bioenergy Research Center Lembaga Penelitian dan Pengabdian kepada Masyarakat Institut
12
4
HASIL DAN PEMBAHASAN
Sifat Fisiko-Kimia Sampel Gliserol
Gliserol kasar hasil samping industri biodiesel memiliki kualitas rendah akibat adanya zat impuirities seperti sisa metanol, sisa katalis, sabun, biodiesel, air
dan bahan-bahan pengotor lainnya yang berasal dari bahan baku, sehingga harus dimurnikan agar dapat dimanfaatkan pada beragam industri. Pemurnian gliserol kasar dilakukan dengan cara mereaksikan gliserol kasar dengan asam fosfat teknis sebanyak 5 % (v/v). Asam fosfat digunakan karena sifatnya yang sangat higroskopis, sehingga sangat mudah berikatan dengan bahan yang bersifat polar. Pada penelitian ini setelah penambahan asam fosfat ke dalam gliserol kasar menyebabkan terbentuknya tiga lapisan yaitu asam lemak, gliserol, dan endapan garam (Gambar 4.1).
Persentase distribusi massa masing-masing lapisan yang terbentuk adalah sebagai berikut :
a. Lapisan atas yaitu asam lemak sebanyak 20-25 %, berwujud padat di bawah suhu kamar
b. Lapisan tengah yaitu gliserol sebanyak 50-60 %, berwujud cair
c. Lapisan bawah yaitu endapan garam K3PO4 sebanyak 20-30 %, berwujud padat
Gambar 4.1. Tiga lapisan yang terbentuk setelah penambahan asam fosfat
Penambahan asam fosfat tersebut bertujuan untuk menetralkan sisa katalis KOH dan sabun kalium. Sabun kalium merupakan garam yang terbentuk dari asam lemak dengan basa kalium pada proses produksi biodiesel. Setelah penambahan asam fosfat ke dalam gliserol kasar, ion kalium dari basa dan sabun akan berikatan dengan ion fosfat sehingga membentuk garam. Reaksi antara asam fosfat dengan KOH akan membentuk garam berupa kalium fosfat (K3PO4)
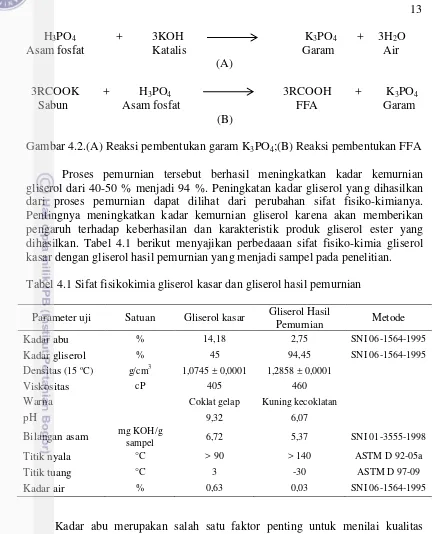
(Gambar 4.2a), berwujud padat yang dapat digunakan sebagai pupuk sedangkan reaksi antara sabun kalium dengan asam fosfat akan membentuk asam lemak bebas dan garam (Gambar 4.2b). Garam yang terbentuk akan mengendap karena kelarutannya rendah dan dimurnikan melalui filtrasi vakum. Adapun sisa metanol, air dan bahan pengotor lainnya terpisah melalui distilasi vakum.
Asam lemak bebas
Gliserol
13 H3PO4 + 3KOH K3PO4 + 3H2O
Asam fosfat Katalis Garam Air (A)
3RCOOK + H3PO4 3RCOOH + K3PO4
Sabun Asam fosfat FFA Garam (B)
Gambar 4.2.(A) Reaksi pembentukan garam K3PO4;(B) Reaksi pembentukan FFA
Proses pemurnian tersebut berhasil meningkatkan kadar kemurnian gliserol dari 40-50 % menjadi 94 %. Peningkatan kadar gliserol yang dihasilkan dari proses pemurnian dapat dilihat dari perubahan sifat fisiko-kimianya. Pentingnya meningkatkan kadar kemurnian gliserol karena akan memberikan pengaruh terhadap keberhasilan dan karakteristik produk gliserol ester yang dihasilkan. Tabel 4.1 berikut menyajikan perbedaaan sifat fisiko-kimia gliserol kasar dengan gliserol hasil pemurnian yang menjadi sampel pada penelitian. Tabel 4.1 Sifat fisikokimia gliserol kasar dan gliserol hasil pemurnian
Parameter uji Satuan Gliserol kasar Gliserol Hasil
Pemurnian Metode
Kadar abu % 14,18 2,75 SNI 06-1564-1995
Kadar gliserol % 45 94,45 SNI 06-1564-1995
Densitas (15 oC) g/cm3 1,0745 ± 0,0001 1,2858 ± 0,0001
Viskositas cP 405 460
Warna Coklat gelap Kuning kecoklatan
pH 9,32 6,07
Bilangan asam mg KOH/g sampel 6,72 5,37 SNI 01-3555-1998
Titik nyala °C > 90 > 140 ASTM D 92-05a
Titik tuang °C 3 -30 ASTM D 97-09
Kadar air % 0,63 0,03 SNI 06-1564-1995
Kadar abu merupakan salah satu faktor penting untuk menilai kualitas gliserol. Adanya abu di dalam gliserol membuat kualitas gliserol menjadi turun. Kadar abu menggambarkan jumlah senyawa anorganik yang terdapat di dalam gliserol. Kadar abu gliserol kasar sebesar 14,18 % yang berasal dari sabun, asam lemak, dan katalis KOH dari reaksi transesterifikasi. Hal ini disebabkan gliserol merupakan bahan organik yang terdiri atas atom C, H, dan O yang akan berubah menjadi gas CO2 dan uap H2O ketika diabukan. Oleh karena itu, salah satu tujuan
pemurnian gliserol adalah menurunkan kadar abu gliserol. Kadar abu gliserol setelah proses pemurnian sebesar 2,75 %, nilai tersebut lebih rendah dibandingkan gliserol sebelum proses pemurnian.
14
dihilangkan melalui proses pemurnian dengan menggunakan asam fospat, filtrasi vakum dan distilasi vakum.
Nilai densitas dan viskositas gliserol semakin meningkat dengan dilakukannya proses pemurnian. Densitas gliserol kasar sebesar 1,0745 g/cm3, setelah pemurnian meningkat menjadi 1,2858 g/cm3. Setelah pemurnian gliserol menjadi lebih kental sehingga nilai viskositasnya meningkat menjadi 460 cP.
Gliserol yang telah dimurnikan mengalami perubahan warna dari coklat gelap menjadi kuning kecoklatan (Gambar 4.3). Warna gliserol dipengaruhi oleh warna CPO (Crude Palm Oil) sebagai bahan baku biodiesel. CPO mengandung
zat warna alami berupa α dan β-karoten, xantofil, klorofil, dan antosianin yang menyebabkan minyak berwarna kuning, kuning kecoklatan, kehijau-hijauan dan kemerah-merahan. Pigmen berwarna merah jingga atau kuning disebabkan oleh karotenoid yang bersifat larut dalam minyak. Warna gelap pada gliserol kasar merupakan hasil degradasi zat warna alami dan suhu pemanasan yang tinggi sehingga minyak mengalami reaksi oksidasi (Ketaren 2008).
Gambar 4.3. (A) Gliserol kasar 45 %; (B) Gliserol hasil pemurnian 94 %
Uji pH menunjukkan bahwa gliserol hasil samping industri biodiesel mempunyai pH 9,32. Tingkat derajat keasaman (pH) gliserol kasar tersebut menunjukkan sifatnya yang basa. Hal ini disebabkan adanya kandungan KOH dan sabun kalium. Setelah diberi penambahan asam fosfat pada gliserol, nilai pH gliserol menjadi turun. Uji pH gliserol murni menunjukkan bahwa nilai pH sebesar 6,07. Reaksi asam fosfat di dalam gliserol akan menurunkan pH. Hal ini terjadi karena ion OH- yang menyebabkan tingginya pH telah berikatan dengan H+ dari asam mineral menghasilkan air.
15
Gambar 4.4 Reaksi pembentukan asam lemak bebas Sifat Fisiko-Kimia Katalis MESA (Methyl Ester Sulfonic Acid)
Reaksi esterifikasi berlangsung sangat lama, dapat berlangsung selama berjam-jam. Maka untuk mempercepat reaksi ditambahkan katalis MESA pekat. Menurut Hui (1996) tujuan penggunaan katalis adalah untuk menghindari kebutuhan temperatur yang tinggi, waktu reaksi yang lebih lama serta produk yang berwarna gelap. MESA merupakan senyawa aktif yang bersifat renewable
dan biodegradable sehingga ramah lingkungan. Katalis MESA adalah jenis
surfaktan anionik, berwarna gelap dan bersifat sangat asam karena tidak dilakukan netralisasi. Keasaman MESA dibuktikan dengan nilai pH yang sangat rendah yaitu 2,18. MESA sebagaimana katalis asam lainnya, diduga dapat menciptakan protonisasi dari hidroksil asam lemak pada proses pembentukan ester. Sifat fisiko-kimia katalis MESA yang digunakan dapat dilihat pada Tabel 4.2.
Tabel 4.2 Sifat fisikokimia katalis MESA
Parameter Satuan Nilai
pH (28 oC) 2,18
Densitas (25 oC) g/cm3 0,9173 ± 0,0001
Viskositas cP 1380
Bilangan Asam mg KOH/g sampel 47,4
Warna Hitam
Sifat Fisiko-Kimia Gliserol Ester
16
tetap berjalan ke arah kanan. Untuk memperoleh produk yang maksimum, kesetimbangan reaksi harus digeser ke arah reaksi pembentukan produk dengan beberapa cara, yakni pemasokan energi ke dalam reaksi, pengumpanan reaktan dalam jumlah berlebih serta pengambilan produk reaksi secara kesinambungan selama reaksi (Kirk dan Othmer 1994; Fessenden & Fessenden 1982).
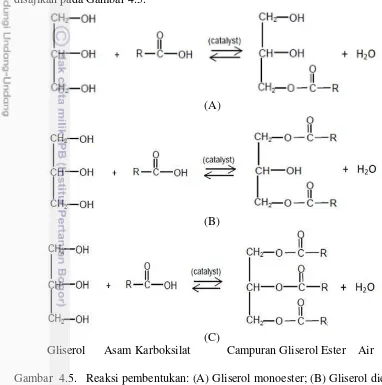
Produk gliserol ester yang dihasilkan dari keempat jenis asam lemak tersebut merupakan campuran antara gliserol monoester, diester, triester, sisa katalis, sisa gliserol, air dan asam lemak bebas. Reaksi pembentukan gliserol ester disajikan pada Gambar 4.5.
(A)
(B)
(C)
Gliserol Asam Karboksilat Campuran Gliserol Ester Air Gambar 4.5. Reaksi pembentukan: (A) Gliserol monoester; (B) Gliserol diester
dan (C) Gliserol triester
17
Gambar 4.6. Dua lapisan hasil esterifikasi
Secara umum karakteristik sifat fisiko-kimia keempat jenis gliserol ester yang dihasilkan berbeda tergantung dari jenis asam lemak yang digunakan sebagai reaktan. Sifat fisiko-kimia gliserol ester yang dihasilkan dipengaruhi oleh konfigurasi struktural asam lemak seperti panjang rantai, tingkat kejenuhan dan cabang rantai. Gliserol ester yang berasal dari asam lemak tak jenuh (asam oleat) berwujud cair pada suhu kamar, sedangkan gliserol ester yang berasal dari asam lemak jenuh (asam stearat, palmitat dan miristat) berwujud padat pada suhu kamar. Semakin panjang rantai asam karboksilat lemak jenuh maka ester yang dihasilkan berwujud padat dengan tekstur yang semakin keras. Jenis asam lemak dan hasil esterifikasi ditunjukkan pada Gambar 4.7.
Gambar 4.6. Jenis asam lemak dan hasil esterifikasi: (A) Asam lemak oleat, stearat, palmitat, miristat; (B) Gliserol ester oleat, stearat, palmitat, miristat
Setelah dilakukan esterifikasi gliserol hasil pemurnian, selanjutnya dilakukan perhitungan rendemen dan pengujian terhadap parameter bilangan asam,
Gliserol Ester
18
densitas, viskositas kinematis, titik nyala, titik tuang, dan titik anilin untuk mengetahui sifat fisiko-kimia produk gliserol ester.
Rendemen
Rendemen merujuk pada jumlah produk reaksi yang dihasilkan pada suatu reaksi kimia atau persentase produk yang dihasilkan dibanding dengan bahan baku yang terolah sehingga dapat menunjukkan efektivitas dari prosedur. Pada proses esterifikasi rendemen tidak mungkin dapat mencapai 100 % karena reaksi esterifikasi bersifat reversibel sehingga konversi sempurna tidak mungkin tercapai. Uap air yang terbentuk merupakan salah satu faktor yang dapat mengurangi rendemen produk gliserol ester apabila tidak dipisahkan dari dalam reaktor karena dapat menghidrolisis gliserol ester menjadi gliserol dan asam karboksilat kembali. Persentase rendemen produk gliserol ester yang dihasilkan disajikan pada Gambar 4.8.
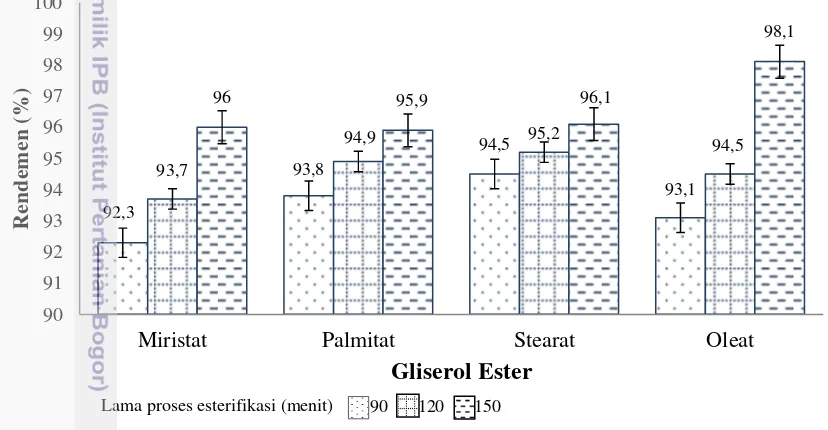
Gambar 4.8. Rendemen produk gliserol ester
Gambar 4.8 menunjukkan bahwa peningkatan nilai rendemen terjadi pada seluruh gliserol ester yang dihasilkan dan peningkatannya berbanding lurus dengan lama proses esterifikasi. Berdasarkan hasil perhitungan, rendemen tertinggi diperoleh pada lama reaksi 150 menit dengan nilai rendemen hampir maksimal yaitu mencapai 98 %. Ini terjadi karena dengan adanya penambahan lama proses maka waktu untuk berlangsungnya reaksi esterifikasi menjadi lebih lama sehingga kesetimbangan dapat tercapai dan konversi reaktan menjadi gliserol ester semakin tinggi. Rendemen tertinggi dihasilkan dari gliserol ester oleat sebesar 98,1 %, sedangkan rendemen terendah dihasilkan dari gliserol ester miristat sebesar 96,0 %.
Tingginya nilai rendemen yang diperoleh dari penelitian ini selain dipengaruhi oleh lama proses yang optimal juga dipengaruhi oleh kadar kemurnian gliserol yang digunakan. Apabila dibandingkan dengan penelitian Putri (2014) yang menggunakan gliserol 84%, nilai rendemen yang diperoleh hanya
19 mencapai 79,55 %. Semakin tinggi kemurnian gliserol maka semakin banyak terbentuk ikatan ester antara gliserol dengan asam lemak sehingga semakin meningkat pula nilai rendemen produk gliserol ester yang dihasilkan. Rendemen produk gliserol ester yang terbaik diperoleh pada lama proses 150 menit dengan nilai berturut-turut yaitu 96 % (miristat dan palmitat); 96,1 % (stearat) dan 98,1 % (oleat). Data nilai rendemen selengkapnya disajikan pada Lampiran 3a.
Hasil analisis varian terhadap nilai rendemen (Lampiran 3b) menunjukkan bahwa penggunaan jenis asam lemak yang berbeda dan peningkatan lama proses esterifikasi dari 90 menit hingga 150 menit menunjukkan adanya peningkatan nilai rendemen yang signifikan pada α = 0,0η, akan tetapi tidak terdapat interaksi antara kedua faktor tersebut.
Hasil uji Duncan menunjukkan bahwa nilai rendemen gliserol ester dari asam lemak palmitat (94,9 %) tidak berbeda nyata dengan nilai rendemen gliserol
ester asam lemak oleat (95,2 %) dan gliserol ester asam lemak stearat (95,3 %). Namun gliserol ester dari ketiga jenis asam lemak tersebut berbeda nyata dengan gliserol ester dari asam lemak miristat (93,5 %). Adapun lama proses 90 menit (93,4 %) tidak berbeda nyata dengan lama proses 120 menit (94,5 %), namun keduanya berbeda nyata dengan lama proses 150 menit (96,2 %). Uji Duncan terhadap nilai rendemen akibat perlakuan penggunaan jenis asam lemak yang berbeda dan lama proses dapat dilihat pada Lampiran 3c dan 3d.
Bilangan asam
Analisis bilangan asam dilakukan untuk mengetahui sisa asam lemak bebas yang terkandung dalam produk. Sisa asam lemak tersebut mempunyai korelasi dengan kandungan gliserol ester yang terbentuk selama reaksi. Selain itu juga memberikan informasi tingkat korosifitas produk. Hasil percobaan terhadap bilangan asam tersaji pada Gambar 4.9.
20
Secara umum pada Gambar 4.9 memperlihatkan adanya penurunan bilangan asam. Semakin lama proses esterifikasi maka bilangan asam yang dihasilkan semakin rendah. Penurunan bilangan asam ini menunjukkan adanya konversi asam lemak menjadi ester sehingga semakin sedikit kandungan asam lemaknya. Hal ini disebabkan dengan semakin meningkatnya lama proses esterifikasi maka semakin banyak asam lemak yang terkonversi menjadi gliserol ester. Selain itu semakin lama reaksi menyebabkan tumbukan antar molekul reaktan semakin sering terjadi sehingga konversi menjadi produk semakin besar.
Peningkatan lama proses menunjukkan adanya perbedaan yang signifikan terhadap penurunan bilangan asam, semakin lama proses esterifikasi terlihat semakin kecil nilai bilangan asam gliserol ester. Konversi tertinggi terjadi pada lama proses 150 menit dengan rata-rata nilai penurunan bilangan asam keempat gliserol ester tersebut > 87 %. Sebagai perbandingan asam miristat memiliki nilai bilangan asam 244-248 mg KOH/g sampel, setelah esterifikasi pada produk campuran dihasilkan nilai bilangan asam sebesar 20,9-24,1 mg KOH/g sampel. Asam palmitat memiliki nilai bilangan asam 217-220 mg KOH/g sampel, setelah esterifikasi pada produk campuran dihasilkan nilai bilangan asam sebesar 21,4-24,2 mg KOH/g sampel. Asam stearat memiliki nilai bilangan asam 198-203 mg KOH/g sampel, setelah esterifikasi pada produk campuran dihasilkan nilai bilangan asam sebesar 22,7-24,8 mg KOH/g sampel. Asam oleat memiliki nilai bilangan asam 194-204 mg KOH/g sampel, setelah esterifikasi pada produk campuran dihasilkan nilai bilangan asam sebesar 18,6-24,7 mg KOH/g sampel. Kondisi terbaik reaksi esterifikasi pada penelitian ini dapat dilihat dari konversi tertinggi berdasarkan nilai bilangan asam terendah dari masing-masing produk gliserol ester. Konversi tertinggi produk gliserol ester terjadi pada lama proses 150 menit dengan nilai bilangan asam berturut-turut yaitu 20,9 mg KOH/g sampel (miristat); 21,4 mg KOH/g sampel (palmitat); 22,7 mg KOH/g sampel (stearat) dan 18,6 mg KOH/g sampel (oleat). Data analisa bilangan asam selengkapnya disajikan pada Lampiran 4a.
Secara umum produk gliserol ester yang dihasilkan memiliki bilangan asam yang rendah. Hal tersebut menunjukkan bahwa gliserol ester tidak mudah mengkorosi logam-logam yang dilaluinya. Ini penting mengingat korosi yang terjadi pada saat penyimpanan dan penggunaan berhubungan dengan banyak hal terutama keselamatan (safety).
Berdasarkan hasil analisis varian (Lampiran 4b) menunjukkan bahwa perlakuan jenis asam lemak dan lama proses esterifiksi memberikan pengaruh sangat nyata terhadap bilangan asam gliserol ester, sedangkan interaksi antara
kedua perlakuan tersebut tidak berpengaruh nyata (α = 0,0η). Hasil analisis varian
perlakuan jenis asam lemak dan lama proses terhadap bilangan asam gliserol ester dapat dilihat pada Lampiran 4b.
Hasil uji Duncan menunjukkan bahwa bilangan asam gliserol ester dari asam lemak oleat (21,5 mg KOH/g sampel) tidak berbeda nyata dengan bilangan asam
21 perlakuan lama proses terhadap bilangan asam menunjukkan bahwa tiap taraf perlakuan memberikan hasil yang saling berbeda nyata. Bilangan asam dengan lama proses 90 menit (20,9 mg KOH/g sampel) berbeda nyata dengan lama proses 120 menit (22,2 mg KOH/g sampel) dan lama proses 150 menit (24,5 mg KOH/g sampel). Uji Duncan terhadap nilai rendemen akibat perlakuan penggunaan jenis asam lemak yang berbeda dan lama proses dapat dilihat pada Lampiran 4c dan 4d. Densitas
Pengujian densitas dilakukan untuk mengetahui berat jenis atau kerapatan antar molekul dalam gliserol ester yang dihasilkan. Hasil pengujian densitas gliserol ester disajikan pada Gambar 4.10. Pada Gambar 4.10 menunjukkan bahwa jenis asam lemak memberikan pengaruh signifikan terhadap nilai densitas sedangkan lama proses esterifikasi tidak berpengaruh secara signifikan. Nilai densitas meningkat secara perlahan sejalan lama proses esterifikasi namun perubahannya sangat kecil.
Gambar 4.10. Pengaruh jenis asam lemak dan lama proses esterifikasi terhadap densitas gliserol ester
Secara umum dapat dilihat nilai densitas gliserol ester yang dihasilkan berkisar antara 0,8-0,9 g/cm3. Densitas tetinggi diperoleh dari gliserol ester oleat yaitu 0,913 g/cm3, sedangkan densitas gliserol ester terendah diperoleh dari gliserol ester miristat yaitu 0,812 g/cm3. Hal ini diduga karena perbedaan bobot molekul jenis asam lemak yang digunakan. Phillps dan Mattamal (1978) menjelaskan bahwa nilai densitas ester dari asam lemak karboksilat dipengaruhi oleh bobot molekul. Menurut Ramirez et al. (2012) densitas akan berkurang
dengan meningkatnya bobot molekul dan densitas meningkat seiring meningkatnya ketidakjenuhan asam lemak. Data densitas gliserol ester disajikan pada Lampiran 5a.
Pada grafik terlihat nilai densitas terendah bukan diperoleh dari gliserol ester stearat yang memiliki bobot molekul terbesar melainkan gliserol ester
22
miristat. Hal ini diduga karena tingkat kemurnian asam miristat lebih rendah dari asam lemak yang lain dan dapat juga disebabkan oleh jenis dari gliserol ester miristat yang terbentuk didominasi campuran diester atau triester yang memiliki bobot molekul yang paling besar. Ferrari et al. 2011 menjelaskan bahwa densitas
tergantung pada kemurnian dan komposisi asam lemaknya. Densitas meningkat dengan penurunan panjang rantai dan meningkat sejalan dengan adanya ikatan ganda, atau dapat dikurangi dengan adanya kontaminan densitas rendah seperti metanol. Selain itu dapat juga dipengaruhi oleh senyawa aromatik yang terkandung di dalam asam lemak. Densitas meningkat seiring meningkatnya kadar aromatik (Nynas Naphthenics 1997).
Nilai densitas terbaik pada penelitian ini berdasarkan nilai terendah dari masing-masing produk gliserol ester, umumnya diperoleh pada lama proses 90 menit meskipun perbedaan nilai dengan lama proses 120 dan 150 menit tidak signifikan. Nilai densitas terbaik produk gliserol ester berturut-turut yaitu 0,812 g/cm3 (miristat) pada lama proses 150 menit; 0,907 g/cm3 (palmitat) pada lama proses 90 menit; 0,899 g/cm3 (stearat) pada lama proses 90 menit dan 0,910 g/cm3 (oleat) pada lama proses 90 menit.
Berdasarkan hasil analisis varian pada Lampiran 5b menunjukkan bahwa perlakuan jenis asam lemak memberikan pengaruh nyata terhadap densitas gliserol ester, sedangkan lama proses dan interaksi antara kedua perlakuan tidak berpengaruh nyata (α = 0,0η). Hasil uji Duncan terhadap perlakuan jenis asam lemak (Lampiran 5c) menunjukkan bahwa tiap taraf perlakuan memberikan hasil yang saling berbeda nyata. Densitas gliserol ester oleat (0,912 g/cm3), stearat (0,909 g/cm3), palmitat (0,901 g/cm3), dan miristat (0,813 g/cm3) saling berbeda nyata.
Viskositas kinematis
Pengujian viskositas kinematis digunakan untuk mengetahui besarnya hambatan gliserol ester untuk dialirkan. Semakin tinggi nilai viskositas kinematis, maka akan semakin sulit untuk mengalir sehingga hal tersebut dihindari pada penggunaan gliserol ester sebagai pelumas. Pengaruh jenis asam lemak dan lama proses esterifikasi terhadap viskositas kinematis gliserol ester dapat dilihat pada Gambar 4.11. Gambar 4.11 menunjukkan bahwa penggunaan jenis asam lemak mempengaruhi nilai viskositas kinematis gliserol ester yang dihasilkan dan secara umum terlihat terjadi peningkatan viskositas kinematis seiring meningkatnya lama proses esterifikasi namun tidak signifikan.
23 Knothe 2008; Razon 2009; Knothe dan Steidley 2011; Ramirez et al. 2011). Data
viskositas kinematis gliserol ester disajikan pada Lampiran 6a.
Gambar 4.11. Pengaruh jenis asam lemak dan lama proses esterifikasi terhadap viskositas kinematis gliserol ester
Nilai viskositas kinematis terbaik pada penelitian ini berdasarkan nilai viskositas kinematis terendah dari produk gliserol ester yang diperoleh pada lama proses 90 menit dengan nilai berturut-turut yaitu 4,2 cSt (miristat); 10,2 cSt (palmitat); 10,6 cSt (stearat) dan 7,3 cSt (oleat). Gliserol ester oleat merupakan produk ester terbaik dibandingkan 3 ester yang lainnya karena memiliki nilai viskosimatis kinematis terendah dan berwujud cair pada suhu ruang.
Hasil analisis varian (Lampiran 6b) menunjukkan bahwa perlakuan jenis asam lemak dan lama proses memberikan pengaruh nyata terhadap viskositas kinematis gliserol ester, sedangkan interaksi kedua perlakuan tidak memberikan pengaruh pada α = 0,0η. Hasil uji Duncan terhadap jenis asam lemak (Lampiran 6c) menunjukkan bahwa viskositas kinematis gliserol ester asam lemak stearat (11,0 cSt) dan palmitat (10,9 cSt) tidak berbeda nyata satu sama lain, namun kedua taraf tersebut berbeda nyata dengan viskositas kinematis gliserol ester asam lemak oleat (8,0 cSt) dan miristat (4,3 cSt). Sedangkan antara gliserol ester asam lemak oleat dengan asam lemak miristat saling berbeda nyata. Adapun uji Duncan terhadap lama proses (Lampiran 6d) menunjukkan bahwa lama proses 90 menit (8,1 cSt) berbeda nyata dengan lama proses 120 menit (8,7 cSt) dan 150 menit (8,9 cSt), sedangkan antara lama proses 120 menit dan 150 menit tidak berbeda. Titik nyala
Titik nyala mengindikasikan tinggi rendahnya volatilitas dan menunjukkan temperatur terendah bahan tersebut dapat terbakar dengan sendirinya ketika bereaksi dengan udara. Semakin rendah titik nyala suatu bahan maka akan semakin mudah bahan tersebut untuk terbakar sehingga membutuhkan
24
penanganan khusus dalam penyimpanan. Hasil pengujian titik nyala dapat dilihat pada Gambar 4.12.
Gambar 4.12. Pengaruh jenis asam lemak dan lama proses esterifikasi terhadap titik nyala gliserol ester
Secara umum gliserol ester yang dihasilkan pada penelitian ini memiliki nilai titik nyala yang tinggi. Gliserol kasar dan gliserol hasil pemurnian sebelum esterifikasi memiliki titik nyala yang lebih rendah dibandingkan dengan gliserol ester. Hal ini membuktikan bahwa proses esterifikasi mampu meningkatkan titik nyala dari produk ester.
Titik nyala dapat menunjukkan adanya kemungkinan unsur yang sangat mudah menguap dan mudah terbakar. Titik nyala yang lebih tinggi setelah esterifikasi menunjukkan bahwa telah terjadi penurunan kandungan fraksi ringan pada gliserol ester. Pada proses esterifikasi, komponen gliserol yang lebih mudah terbakar akan mengalami pelepasan proton dari gugus hidroksil sehingga menghasilkan senyawa kompleks teraktivasi. Pelepasan air dan protonasi kemudian menghasilkan gugus ester yang memiliki titik nyala lebih tinggi. Menurut Mittelbach dan Remschmidt (2004) titik nyala dipengaruhi oleh kandungan fraksi ringan (residu alkohol). Kandungan fraksi ringan yang semakin tinggi, maka semakin rendah temperatur yang dibutuhkan ester untuk menyala.
Berdasarkan Gambar 4.12, titik nyala gliserol ester dari asam lemak jenuh (stearat, palmitat dan miristat) menunjukkan nilai yang lebih rendah dibandingkan gliserol ester dari asam lemak tak jenuh (oleat). Setyawardhani et al. 2010
menjelaskan bahwa produk ester dari asam lemak jenuh memiliki kelemahan yaitu memiliki titik nyala yang rendah karena produk ester tersebut mudah larut dalam senyawa yang mengandung fraksi alkohol sehingga menurunkan titik nyala bahan tersebut. Titik nyala terendah dihasilkan oleh gliserol ester miristat sebesar 173 oC, sedangkan titik nyala tertinggi dihasilkan oleh gliserol ester oleat sebesar 213
oC pada lama proses esterifikasi 150 menit. Titik nyala gliserol ester dengan nilai di
25 atas 200°C merupakan nilai tambah yang sangat baik untuk dapat diaplikasikan pada berbagai proses lanjutan.
Nilai titik nyala terbaik pada penelitian ini, berdasarkan nilai titik nyala tertinggi dari produk gliserol ester yang diperoleh pada lama proses 150 menit meskipun perbedaan nilai dengan lama proses 90 dan 120 menit tidak signifikan. Semakin tinggi nilai titik nyala suatu bahan, maka akan semakin baik dan semakin mudah dalam transportasi, penanganan dan penyimpanan. Nilai titik nyala terbaik produk gliserol ester berturut-turut yaitu 179 oC (miristat) pada lama proses 90 menit; 204 oC (palmitat) pada lama proses 150 menit; 207 oC (stearat) pada lama proses 150 menit dan 213 oC (oleat) pada lama proses 150 menit. Data titik nyala gliserol ester disajikan pada Lampiran 7a.
Hasil analisis varian pengujian titik nyala (Lampiran 7b) menunjukkan bahwa jenis asam lemak berpengaruh nyata terhadap titik nyala, sedangkan lama
proses dan interaksi kedua perlakuan tidak berpengaruh nyata pada α = 0,0η. Hasil uji Duncan terhadap titik nyala gliserol ester pada Lampiran 7c menunjukkan bahwa titik nyala gliserol ester asam lemak miristat (175 OC) berbeda nyata dengan titik nyala gliserol ester asam lemak oleat (207 OC), asam lemak stearat (204 OC) dan asam lemak palmitat (200 OC), sedangkan antara gliserol ester asam lemak oleat, asam lemak stearat dan asam lemak palmitat tidak berbeda.
Titik tuang
Titik tuang dapat menunjukkan derajat temperatur terendah gliserol ester masih dapat mengalir dan dipompa. Apabila minyak tersebut berada pada temperatur terendahnya maka minyak akan membeku dan tidak dapat mengalir lagi. Semakin rendah titik tuang suatu bahan, maka bahan tersebut mampu mengalir pada suhu yang rendah.
26
Gambar 4.13. Pengaruh jenis asam lemak dan lama proses esterifikasi terhadap titik tuang gliserol ester
Nilai titik tuang gliserol ester stearat, gliserol ester palmitat dan gliserol ester miristat cenderung stabil dan tidak dipengaruhi oleh lama proses. Gliserol ester stearat dan palmitat memiliki nilai titik tuang yang hampir sama yaitu 54 °C sedangkan gliserol ester miristat memiliki titik tuang tertinggi yaitu 57 °C. Ketiga gliserol ester yang dihasilkan berwujud padat pada suhu ruang. Panjang rantai dan ketidakjenuhan suatu molekul mempengaruhi nilai titik tuangnya. Rantai molekul yang semakin panjang akan meningkatkan nilai titik tuang, sedangkan adanya ikatan rangkap yang menandakan ketidakjenuhan akan menurunkan nilai titik tuang (Knothe 2005; Soriano et al. 2006; Ramos et al. 2009; Knothe 2009; Edith et al. 2012). Meskipun miristat memiliki berat molekul dan panjang rantai paling
kecil dari stearat dan palmitat namun nilai titik tuangnya terbesar. Hal ini diduga karena gugus alkil asam lemak miristat yang digunakan berantai lurus, sedangkan stearat dan palmitat rantai gugus alkilnya bercabang. Sebagian besar asam lemak jenuh berantai lurus namun ada juga yang bercabang (Rustan et al. 2005).
Menurut Dunn (2009) rantai gugus alkil yang bercabang dapat mengurangi titik tuang dibandingkan gugus alkil yang berantai lurus. Data titik tuang disajikan pada Lampiran 8a.
Nilai titik tuang terbaik pada penelitian ini, berdasarkan nilai titik tuang terendah dari produk gliserol ester yang diperoleh dari gliserol ester oleat yaitu 0
oC. Oleh karena ester yang dihasilkan dari asam lemak tak jenuh ini memiliki nilai
titik tuang yang rendah maka menyebabkan gliserol ester oleat lebih baik dan mudah dalam aplikasi. Namun, ester dari asam lemak jenuh memiliki stabilitas oksidasi dan pelumasan yang lebih tinggi (Edith 2012) sehingga dapat digunakan sebagai bahan aditif peningkatan kualitas pengapian pada biodiesel. Nilai titik tuang dari gliserol ester yang dihasilkan disajikan pada Gambar 4.13.
27 titik tuang gliserol ester asam lemak oleat (0 OC) berbeda nyata dengan titik tuang gliserol ester asam lemak stearat (54,5 OC), palmitat (54 OC) dan miristat (57 OC). Adapun titik tuang gliserol ester asam lemak miristat berbeda nyata dengan titik tuang gliserol ester asam lemak palmitat dan asam lemak stearat, sedangkan antara gliserol ester asam lemak palmitat dan asam lemak stearat tidak berbeda.
Hasil Analisis Spektrum FTIR
Pada penelitian ini dilakukan identifikasi senyawa dengan metode spektrofotometri infra merah (FTIR) untuk menentukan keberhasilan reaksi esterifikasi yang dilakukan. Dalam penentuan keberhasilan proses esterifikasi dibuat perbandingan antara spektrum FTIR gliserol ester dengan spektrum FTIR reaktan (gliserol dan asam lemak). Pengujian dengan FTIR tersebut menggunakan sampel cair (asam oleat) untuk memudahkan proses analisis FTIR-nya dibandingkan dengan sampel padatan atau gas. Pada sampel cair, sampel cukup diteteskan pada plat NaCl yang terdapat dalam instrumen tanpa harus merubah bentuknya apabila menggunakan sampel padatan.
Hasil analisis struktur menggunakan metode spektroskopi infra merah (FTIR) terhadap gliserol ester ini menunjukkan adanya kesesuaian dengan yang diharapkan. Melalui metode ini dapat dilihat adanya perubahan gugus-gugus fungsi pada senyawa kimia reaktan dan gliserol ester. Pada spektrum analisis FTIR reaktan asam oleat (Gambar 4.14A) terdapat puncak yang tajam pada bilangan gelombang 1709,33 cm-1 dan 3003,89 cm-1 yang berarti bahwa sampel mengandung gugus karbonil yaitu asam karboksilat. Pada spektrum analisis FTIR reaktan gliserol (Gambar 4.14B) gugus alkohol ditunjukkan pada bilangan gelombang 3340,50 cm-1 dan 2938,49 cm-1.
Berdasarkan spektrum analisis FTIR produk gliserol ester pada Gambar 4.14D menunjukkan adanya perubahan gugus fungsi sebagai hasil dari proses reaksi esterifikasi. Pada spektrum tersebut ditemukan beberapa gugus fungsi dan yang terpenting adalah ditemukannya gugus ester yang membuktikan keberhasilan dari proses esterifikasi. Ester-ester asam karboksilat biasanya memberikan dua puncak serapan infra merah yang kuat, yaitu puncak serapan vibrasi regang C=O dan puncak serapan vibrasi regang C – O. Puncak-puncak vibrasi regang kedua ikatan ini berintensitas tinggi disebabkan kedua ikatan itu bersifat polar, bahkan jauh lebih polar dari pada ikatan-ikatan lain di dalam molekul ester asam karboksilat.
28
baik C=C, C=O, C=N, maupun N=O. Gliserol ester tidak mengandung C=N maupun N=O, sehingga puncak pada daerah bilangan gelombang tersebut hanya mungkin berasal dari vibrasi C=O dan C=C. Asam karboksilat juga memiliki serapan C=O yang khas dan juga pita O-H yang sangat terbedakan dan miring ke dalam pita absorpsi CH. Puncak yang khas tersebut pada bilangan gelombang 3008,89 cm-1 dan 1650,87 cm-1 menunjukkan adanya gugus fungsi asam karboksilat. Sedangkan serapan O-H pada bilangan gelombang 3401,87 cm-1 dan diperkuat dengan adanya C-O pada bilangan gelombang 1300-1000 cm-1 menunjukkan gugus alkohol. Berdasarkan grafik spektrum tersebut maka dapat diketahui bahwa sampel produk gliserol ester mengandung gugus ester, asam karboksilat dan alkohol.
Gambar 4.14. Profil FTIR (A) Asam oleat; (B) Gliserol; (C) Sisa gliserol dan (D) Gliserol ester
(A)
(D) (C)
(B)
O-H C-H
C=O C-O C-C
CH bending
OH bending
29
Hasil spektrum FTIR di atas di dukung oleh data yang dihasilkan dari beberapa parameter uji seperti nilai bilangan asam, densitas, viskositas kinematis, titik nyala dan titik tuang produk gliserol ester. Berdasarkan data hasil uji terlihat penurunan nilai bilangan asam secara signifikan, hal ini menunjukkan telah terjadi konversi asam lemak menjadi ester sehingga kandungan asam lemaknya berkurang. Nilai bilangan asam gliserol ester berturut-turut yaitu 20,9-24,1 mg KOH/g sampel (miristat); 21,4-24,2 mg KOH/g sampel (palmitat); 22,7-24,8 mg KOH/g sampel (stearat) dan 18,6-24,7 mg KOH/g sampel (oleat). Nilai bilangan asam reaktan adalah 5,37 mg KOH/g sampel (gliserol) dan 244-248 mg KOH/g sampel (miristat); 217-220 mg KOH/g sampel (palmitat); 198-203 mg KOH/g sampel (stearat) dan 194-204 mg KOH/g sampel (oleat).