KARAKTERISASI SIMPLISIA, SKRINING FITOKIMIA,
ISOLASI DAN IDENTIFIKASI SENYAWA FLAVONOIDA DARI
HERBA TUMBUHAN PATIKAN KEBO
(Euphorbia hirta L.)
SKRIPSI
Oleh: YULIA NANDA
071524087
PROGRAM EKSTENSI SARJANA FARMASI
FAKULTAS FARMASI
KARAKTERISASI SIMPLISIA, SKRINING FITOKIMIA,
ISOLASI DAN IDENTIFIKASI SENYAWA FLAVONOIDA DARI
HERBA TUMBUHAN PATIKAN KEBO
(Euphorbia hirta L.)
SKRIPSI
Diajukan untuk Melengkapi Salah Satu Syarat untuk Mencapai Gelar Sarjana Farmasi pada Fakultas Farmasi
Universitas Sumatera Utara
Oleh: YULIA NANDA
071524087
PROGRAM EKSTENSI SARJANA FARMASI
FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA
MEDAN
Pengesahan Skripsi
KARAKTERISASI SIMPLISIA, SKRINING FITOKIMIA, ISOLASI DAN IDENTIFIKASI SENYAWA FLAVONOIDA DARI HERBA
TUMBUHAN PATIKAN KEBO (Euphorbiae hirtae Herba)
Oleh: YULIA NANDA
NIM 071524087
Dipertahankan di Hadapan Panitia Penguji Fakultas Farmasi
Universitas Sumatera Utara
Dra. Aswita Hafni Lubis, M.Si., Apt. NIP 195304031983032001
Panitia Penguji,
Dra. Herawati Ginting, M.Si., Apt. NIP 195103261978022001
Dra. Misra Gafar, MS., Apt. NIP 195609051986012001
Drs. Syafruddin, MS., Apt. NIP
Drs. Suryadi Achmad, M.Sc., Apt. NIP
Dekan Fakultas Farmasi
KATA PENGANTAR
Puji dan syukur kehadirat Allah SWT atas segala nikmat yang tak terhingga sehingga penulis bisa menyelesaikan penelitian dan penulisan skripsi sebagai salah satu syarat untuk mencapai gelar Sarjana Farmasi pada Fakultsa Farmasi. Shalawat dan salam kepada Rasulullah SAW.
Terima kasih yang sebenar-benarnya penulis sampaikan kepada ayahanda Almarhum H. Zakaria Ali dan Ibunda Zubaidah Ismail atas dukungan yang begitu luar biasa yang telah diberikan kepada ananda, serta kepada kakak dan abang, Azhari Fahrizal, ST dan Ainul Riza Nova, SP.
Penulis juga mengucapkan terima kasih yang sebesar-besarnya kepada:
1. Ibu Dra. Misra Gaffar M.S., Apt., dan Ibu Dra. Aswita Hafni Lubis MSi, Apt., selaku dosen pembimbing yang telah membimbing penulis dengan penuh kesabaran dan keikhlasan selama penelitian hingga selesainya penulisan skripsi ini. 2. Bapak Prof. Dr. Sumadio Hadisahputra, Apt., selaku Dekan Fakultas Farmasi
Universitas Sumatera Utara yang telah mensahkan dan memberikan pengarahan dalam penyusunan skripsi ini.
3. Bapak Drs. Suryadi Achmad, M.Sc, Apt., selaku dosen wali yang selama ini telah banyak membina dan membimbing penulis selama masa pendidikan.
4. Ibu Herawaty Ginting, M.Si., Apt., Bapak Drs. Syafruddin, MS., Apt., dan Bapak Drs. Suryadi Achmad, M.Sc., Apt selaku dosen penguji yang telah memberikan masukan dan saran kepada penulis hingga selesainya penulisan skripsi ini
5. Bapak Drs. Panal Sitorus, Apt., selaku kepala Lab.Farmakognosi dan Ibu Dra. Marline Nainggolan, M.Si., Apt selaku kepala Lab. Fitokimia.
6. Bapak/Ibu dosen Fakultas Farmasi USU yang telah memberikan didikan dan bimbingan selama penulis menuntut ilmu di Fakultas Farmasi USU
7. kepada teman-teman farmasi ekstensi 07 yang langsung maupun tidak langsung membantu dalam penyeleseaian skripsi ini.
Serta buat semua pihak yang tidak dapat penulis sebutkan satu persatu yang telah banyak membantu dalam penyelesaian skripsi ini. Kiranya Allah SWT memberikan balasan yang berlipat ganda atas segala kebaikan dan bantuan yang telah diberikan kepada penulis.
Penulis menyadari bahwa skripsi ini masih jauh dari kesempurnaan, sehingga penulis mengharapkan kritik dan saran yang bersifat membangun. Akhir kata semoga tulisan ini dapat menjadi sumbangan yang berarti bagi ilmu pengetahuan khususnya bidang Farmasi.
Medan, April 2010 Penulis
KARAKTERISASI SIMPLISIA, SKRINING FITOKIMIA ISOLASI
DAN IDENTIFIKASI SENYAWA FLAVONOIDA DARI HERBA
PATIKAN KEBO (Euphorbiae hirtae Herba)
ABSTRAK
Pemanfaatan sebagian besar tumbuhan telah dilakukan sejak dahulu untuk mengobati berbagai penyakit. Tumbuhan patikan kebo merupakan tumbuhan terna yang banyak digunakan untuk pengobatan mata, asma, batuk dan sakit tengorokan. Tujuan penelitian ini adalah untuk mengetahui karakterisasi simplisia dan isolasi senyawa flavonoida secara spektrofotometri ultraviolet dengan menggunakan pereaksi geser (Shift reagen). Ekstraksi dilakukan secara perkolasi dengan menggunakan pelarut etanol, kemudian pemisahan senyawa flavonoida dilakukan secara ekstraksi cair-cair dengan menggunakan pelarut n-heksana, kloroform dan etil asetat. Fraksi etil asetat kemudian dikromatografi kertas dengan berbagai fase gerak dan perbandingan untuk mencari pengembang yang terbaik. Selanjutnya fraksi etil asetat dipisahkan dengan kromatografi kertas preparatif dengan menggunakan pengembang asam asetat 50%, dari hasil preparatif didapat dua isolat F1 dan F2. Selanjutnya isolat ini dikromatografi dua arah, dari hasil diketahui bahwa isolat F1 sudah murni sedangkan isolat F2 belum murni. Salah satu isolat yang diperoleh dianalisis secara spektrofotometri ultraviolet dengan penambahan pereaksi geser. Hasil pemeriksaan karakterisasi simplisia diperoleh kadar air 6,654%, kadar sari yang larut dalam air 22,06%, kadar sari yang larut dalam etanol 18,36%, kadar abu total 1,074% dan kadar abu yang tidak larut dalam asam 0,12%. Hasil skrining fitokimia menunjukkan adanya senyawa golongan alkaloid, flavonoida, tanin, glikosida, glikosida antrakuinon, steroida, saponin. Hasil analisis spektrofotometri ultraviolet dengan spektrofotometer, absorbsi maksimum terdapat pada panjang gelombang 381 nm yang menunjukkan bahwa isolat tersebut golongan flavonoida. Penafsiran spektrum ultraviolet dengan penambahan pereaksi geser menunjukkan adanya gugus hidroksil pada posisi 3,5. Hasil karakterisasi isolat setelah dianalisis secara spektrofotometri ultraviolet dapat disimpulkan sebagai flavonol.
Kata kunci: patikan kebo, flavonoida, spektrofotometri ultraviolet
CHARACTERIZATION SIMPLEX, PHYTOCHEMICAL
SCREENING ISOLATION AND IDENTIFICATION COMPOUND
FLAVONOIDA FROM PATIKAN KEBO HERB (Euphorbiae
hirtae Herba)
ABSTRACT
Utilization a large part of floras had been conducted since former to cure various of diseases. Flora patikan kebo is flora terna that most used for asthma medication, cough and red lane pain. This Research main to know characterization of simplex and compound isolation flavonoida by spektrofotometri ultraviolet by using shift reagent. Extraction are conducted in percolation by using ethanol solvent, then compound dissociation flavonoida is conducted in liquid-liquid extraction by using n-heksana solvent, chloroform and acetate ethyl. Fraction of acetate ethyl then paper chromatography with various of motion phase and comparisons to look for the best developer. Furthermore fraction of acetate ethyl is dissociated with preparatif paper chromatography by using developer of acetate acid 50%, from result preparatif is got two isolat F1s and F2. Furthermore this isolat was chromatography two directions, from result known that isolat F1 has been pure whereas isolat F2 not pure. One of isolat that got analysed in spektrofotometri ultraviolet with addition shifts reagent. The Result characterization of simplex gave the water conten value 6,654%, the water soluble extract value 22,06%, the etanol soluble extract value 18,36%, the total ash value 1,074% and the acid insoluble ash value 0,12%. The result phytochemical screening shows there is alkaloid compound, flavonoida, tanin, glikosida, glikosida antrakuinon, steroida, saponin. Analysis Result spektrofotometri ultraviolet with spektrofotometer, maximum absorption exist on wavelength 381 nm that indicate that isolat are flavonoida group. Interpretation of ultraviolet spectrum with addition shifts reagent show existence of hydroxyl bunch on course 3,5. Result characterization of isolat after analysed with spektrofotometri ultraviolet can be concluded as flavonol.
2.3 Ekstraksi ... 11
3.5 Pemeriksaan Karakterisasi Simplisia ... 22
3.5.1 Pemeriksaan Makroskopik ... 23
3.5.2 Pemeriksaan Mikroskopik ... 23
3.5.4 Penetapan Kadar Abu Total ... 24
3.9 Analisis Senyawa Flavonoida dari Ekstrak Hasil Fraksinasi Dengan Cara Kromatografi Kertas ... 29
3.10 Pemisahan Senyawa Flavonoida dari Fraksi Etil Asetat Dengan Cara Kromatografi Kertas Preparatif ... 30
3.11 Uji Kemurnian terhadap Senyawa Flavonoida Hasil Kromatografi Kertas Preparatif ... 31
3.12 Karakterisasi Hasil Isolasi ... 32
3.12 Krakterisasi Isolat dengan Spektrofotometri Ultraviolet Dengan Penambahan Pereaksi Geser (Shift reagen) ... 32
BAB IV HASIL DAN PEMBAHASAN ... 33
BAB V KESIMPULAN DAN SARAN ... 37
5.1 Kesimpulan ... 37
5.2 Saran .. ... 37
DAFTAR PUSTAKA ... 38
DAFTAR LAMPIRAN
5. Gambar Pemeriksaan Mikroskopik Sayatan Melintang Daun Tumbuhan Patikan Kebo ... 43
6. Gambar Pemeriksaan Mikroskopik Sayatan Membujur Atas Daun Tumbuhan Patikan Kebo ... 44
7. Gambar Pemeriksaan Mikroskopik Sayatan Membujur Bawah Daun Tumbuhan Patikan Kebo ... 45
8. Gambar Pemeriksaan Mikroskopik Serbuk Simplisia Herba Patikan Kebo ... 46
9. Perhitungan Hasil Karakterisasi Pemeriksaan Simplisia Herba Patikan Kebo (Euphorbiae hirtae herba) ... 47
10. Hasil Karakterisasi Serbuk Simplisia Herba Patikan Kebo (Euphorbiae hirtae herba) ... 52
11. Hasil Penapisan Fitokimia Serbuk Simplisia Herba Patikan Kebo (Euphorbiae hirtae herba) ... 52
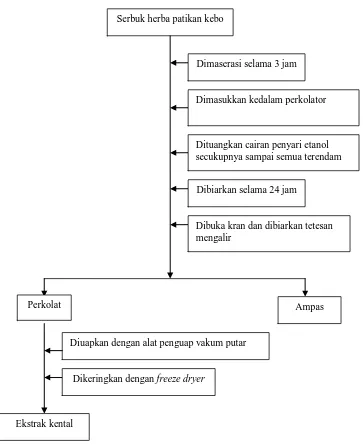
12. Bagan Pembuatan Ekstrak Serbuk Simplisia Herba Patikan Kebo Secara Perkolasi ... 53
13. Bagan Ektraksi Cair-Cair Senyawa Flavonoida dari Ekstrak Etanol ... 54
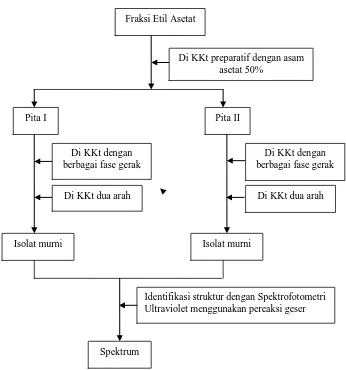
14. Bagan Isolasi Senyawa Flavonoida dari Fraksi Etil Asetat ... 55
15. Kromatogram Hasil Fraksinasi Herba Patikan Kebo (Euphorbiae hirtae herba) dengan KKt dengan Fase Gerak BAA ... 56
16. Kromatogram Hasil Fraksinasi Herba Patikan Kebo (Euphorbiae hirtae herba) dengan KKt dengan Fase Gerak Forestal... 57
17. Kromatogram Hasil Fraksinasi Herba Patikan Kebo (Euphorbiae hirtae herba) dengan KKt dengan Fase Gerak Asam Asetat 50% . . 58
18. Kromatogram Hasil Fraksinasi Herba Patikan Kebo (Euphorbiae hirtae herba) dengan KKt dengan Fase Gerak Asam Asetat 15% . . 59
19. Kromatogram Hasil Fraksinasi Herba Patikan Kebo (Euphorbiae
hirtae herba) dengan KKt dengan Fase Gerak HCl 1% ... 60
20. Kromatogram Hasil KKt Ekstrak Etanol Herba Patikan Kebo
(Euphorbiae hirtae herba) ... 61
21. Kromatogram Hasil KKt Fraksi n-heksana Herba Patikan Kebo
(Euphorbiae hirtae herba) ... 62
22. Kromatogram Hasil KKt Fraksi Kloroform Herba Patikan Kebo
(Euphorbiae hirtae herba) ... . 63
23. Kromatogram Hasil KKt Fraksi Etil Asetat Herba Patikan Kebo
(Euphorbiae hirtae herba) ... . 64
24. Kromatogram Hasil KKt Fraksi Air Herba Patikan Kebo
(Euphorbiae hirtae herba) ... 65
25. Penggambaran Kromatogram dari KKt Preparatif Fraksi Etil
Asetat Herba Patikan Kebo (Euphorbiae hirtae herba) ... 66
26. Kromatogram F1 dengan KKt Herba Patikan Kebo
(Euphorbiae hirtae herba) ... 67
27. Kromatogram F1 dengan KKt Herba Patikan Kebo
(Euphorbiae hirtae herba) ... 68
28. Kromatogram F1 dengan KKt Herba Patikan Kebo
(Euphorbiae hirtae herba) ... 69
29. Kromatogram F1 dengan KKt Herba Patikan Kebo
(Euphorbiae hirtae herba) ... 70
30. Kromatogram F1 dengan KKt Herba Patikan Kebo
(Euphorbiae hirtae herba) ... 71
31. Kromatogram F2 dengan KKt Herba Patikan Kebo
(Euphorbiae hirtae herba) ... 72
32. Kromatogram F2 dengan KKt Herba Patikan Kebo
(Euphorbiae hirtae herba) ... 73
33. Kromatogram F2 dengan KKt Herba Patikan Kebo
(Euphorbiae hirtae herba) ... 74
34. Kromatogram F2 dengan KKt Herba Patikan Kebo
(Euphorbiae hirtae herba) ... 75
35. Kromatogram F2 dengan KKt Herba Patikan Kebo
(Euphorbiae hirtae herba) ... 76
36. Kromatogram Hasil Uji Kemurnian Isolat F1 dengan KKt
37. Spektrum Ultraviolet dari Isolat F1 dalam Metanol ... 78
38. Spektrum Ultraviolet Larutan Isolat F1 dalam Metanol dan
Setelah Penambahan NaOH... 79
39. Spektrum Ultraviolet Larutan Isolat F1 dalam Metanol dengan
Penambahan NaOH dan Penambahan NaOH setelah 5 menit ... . 80
40. Spektrum Ultraviolet Larutan Isolat F1 dalam Metanol setelah
Penambahan AlCl3/HCl ... 81
41. Spektrum Ultraviolet Larutan Isolat F1 dalam Metanol setelah Penambahan AlCl3/HCl dan Spektrum Larutan Isolat dengan
Penambahan AlCl3 ... 82
42. Spektrum Ultraviolet Larutan Isolat F1 dalam Metanol setelah
Penambahan Natrium Asetat ... 83
43. Spektrum Ultraviolet Larutan Isolat F1 dalam Metanol setelah Penambahan Natrium Asetat dan setelah Penambahan
Natrium Asetat/ Asam Borat ... 84
DAFTAR GAMBAR
Halaman
Gambar
1. Kerangka Flavonoida ... 7
2. Struktur Dasar Flavonida... 7
3. Struktur Flavanon... 8
4. Struktur Flavanonol... 8
5. Struktur Flavon ... 9
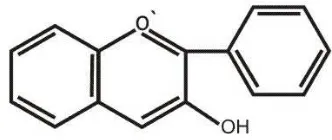
6. Struktur Flavonol ... 9
7. Struktur Isoflavon ... 10
8. Struktur Antosianin ... 10
9. Struktur Auron ... 11
10. Struktur Kalkon... 11
11. 3, 5 dihirdoksil flavonol ... 36
12. Tumbuhan Patikan Kebo (Euphorbia hirta L.) ... 41
13. Simplisia Herba Patikan Kebo (Euphorbiae hirtae herba) ... 41
14. Bagan Penelitian... 42
15. Pemeriksaan Mikroskopik Sayatan Melintang Daun Tumbuhan Patikan Kebo ... 43
16. Pemeriksaan Mikroskopik Sayatan Membujur Atas Daun Tumbuhan Patikan Kebo ... 44
17. Pemeriksaan Mikroskopik Sayatan Membujur Bawah Daun Tumbuhan Patikan Kebo ... 45
20. Bagan Ekstraksi Cair-Cair Senyawa Flavonoida dari Ekstrak
Etanol ... 54 21. Bagan Isolasi Senyawa dari Fraksi Etil Asetat ... 55 22. Kromatogram Hasil Fraksinasi Herba Patikan Kebo (Euphorbiae
hirtae herba) dengan KKt dengan Fase Gerak BAA ... 56
23. Kromatogram Hasil Fraksinasi Herba Patikan Kebo (Euphorbiae
hirtae herba) dengan KKt dengan Fase Gerak Forestal... 57
24. Kromatogram Hasil Fraksinasi Herba Patikan Kebo (Euphorbiae
hirtae herba) dengan KKt dengan Fase Gerak Asam Asetat 50% .. 58
25. Kromatogram Hasil Fraksinasi Herba Patikan Kebo (Euphorbiae
hirtae herba) dengan KKt dengan Fase Gerak Asam Asetat 15% .. 59
26. Kromatogram Hasil Fraksinasi Herba Patikan Kebo (Euphorbiae
hirtae herba) dengan KKt dengan Fase Gerak HCl 1% ... 60
27. Kromatogram Hasil KKt Ekstrak Etanol Herba Patikan Kebo
(Euphorbiae hirtae herba) ... 61
28. Kromatogram Hasil KKt Fraksi n-heksana Herba Patikan Kebo
(Euphorbiae hirtae herba) ... 62
29. Kromatogram Hasil KKt Fraksi Kloroform Herba Patikan Kebo
(Euphorbiae hirtae herba) ... . 63
30. Kromatogram Hasil KKt Fraksi Etil Asetat Herba Patikan Kebo
(Euphorbiae hirtae herba) ... . 64
31. Kromatogram Hasil KKt Fraksi Air Herba Patikan Kebo
(Euphorbiae hirtae herba) ... 65
32. Penggambaran Kromatogram dari KKt Preparatif Fraksi Etil
Asetat Herba Patikan Kebo (Euphorbiae hirtae herba) ... 66
33. Kromatogram F1 dengan KKt Herba Patikan Kebo
(Euphorbiae hirtae herba) ... 67
34. Kromatogram F1 dengan KKt Herba Patikan Kebo
(Euphorbiae hirtae herba) ... 68
35. Kromatogram F1 dengan KKt Herba Patikan Kebo
(Euphorbiae hirtae herba) ... 69
36. Kromatogram F1 dengan KKt Herba Patikan Kebo
(Euphorbiae hirtae herba) ... 70
37. Kromatogram F1 dengan KKt Herba Patikan Kebo
(Euphorbiae hirtae herba) ... 71
38. Kromatogram F2 dengan KKt Herba Patikan Kebo
(Euphorbiae hirtae herba) ... 72
39. Kromatogram F2 dengan KKt Herba Patikan Kebo
(Euphorbiae hirtae herba) ... 73
40. Kromatogram F2 dengan KKt Herba Patikan Kebo
(Euphorbiae hirtae herba) ... 74
41. Kromatogram F2 dengan KKt Herba Patikan Kebo
(Euphorbiae hirtae herba) ... 75
42. Kromatogram F2 dengan KKt Herba Patikan Kebo
(Euphorbiae hirtae herba) ... 76
43. Kromatogram Hasil Uji Kemurnian Isolat F1 dengan KKt
Dua Arah ... 77
44. Spektrum Ultraviolet dari Isolat F1 dalam Metanol ... 78
45. Spektrum Ultraviolet Larutan Isolat F1 dalam Metanol dan Setelah Penambahan NaOH ... 79
46. Spektrum Ultraviolet Larutan Isolat F1 dalam Metanol dengan
Penambahan NaOH dan Penambahan NaOH setelah 5 menit ... 80
47. Spektrum Ultraviolet Larutan Isolat F1 dalam Metanol setelah
Penambahan AlCl3/HCl ... 81
48. Spektrum Ultraviolet Larutan Isolat F1 dalam Metanol setelah Penambahan AlCl3/HCl dan Spektrum Larutan Isolat dengan
Penambahan AlCl3 ... 82
49. Spektrum Ultraviolet Larutan Isolat F1 dalam Metanol setelah
Penambahan Natrium Asetat ... 83
50. Spektrum Ultraviolet Larutan Isolat F1 dalam Metanol setelah Penambahan Natrium Asetat dan setelah Penambahan
DAFTAR TABEL
Halaman
Tabel
1. Hasil Pemeriksaan Karakteristik Serbuk Simplisia Herba
Patikan Kebo (Euphorbiae hirtae herba) ... 52
2 Hasil Penapisan Fitokimia Serbuk Simplisia Herba Patikan Kebo
(Euphorbiae hirtae herba) ... 52
KARAKTERISASI SIMPLISIA, SKRINING FITOKIMIA ISOLASI
DAN IDENTIFIKASI SENYAWA FLAVONOIDA DARI HERBA
PATIKAN KEBO (Euphorbiae hirtae Herba)
ABSTRAK
Pemanfaatan sebagian besar tumbuhan telah dilakukan sejak dahulu untuk mengobati berbagai penyakit. Tumbuhan patikan kebo merupakan tumbuhan terna yang banyak digunakan untuk pengobatan mata, asma, batuk dan sakit tengorokan. Tujuan penelitian ini adalah untuk mengetahui karakterisasi simplisia dan isolasi senyawa flavonoida secara spektrofotometri ultraviolet dengan menggunakan pereaksi geser (Shift reagen). Ekstraksi dilakukan secara perkolasi dengan menggunakan pelarut etanol, kemudian pemisahan senyawa flavonoida dilakukan secara ekstraksi cair-cair dengan menggunakan pelarut n-heksana, kloroform dan etil asetat. Fraksi etil asetat kemudian dikromatografi kertas dengan berbagai fase gerak dan perbandingan untuk mencari pengembang yang terbaik. Selanjutnya fraksi etil asetat dipisahkan dengan kromatografi kertas preparatif dengan menggunakan pengembang asam asetat 50%, dari hasil preparatif didapat dua isolat F1 dan F2. Selanjutnya isolat ini dikromatografi dua arah, dari hasil diketahui bahwa isolat F1 sudah murni sedangkan isolat F2 belum murni. Salah satu isolat yang diperoleh dianalisis secara spektrofotometri ultraviolet dengan penambahan pereaksi geser. Hasil pemeriksaan karakterisasi simplisia diperoleh kadar air 6,654%, kadar sari yang larut dalam air 22,06%, kadar sari yang larut dalam etanol 18,36%, kadar abu total 1,074% dan kadar abu yang tidak larut dalam asam 0,12%. Hasil skrining fitokimia menunjukkan adanya senyawa golongan alkaloid, flavonoida, tanin, glikosida, glikosida antrakuinon, steroida, saponin. Hasil analisis spektrofotometri ultraviolet dengan spektrofotometer, absorbsi maksimum terdapat pada panjang gelombang 381 nm yang menunjukkan bahwa isolat tersebut golongan flavonoida. Penafsiran spektrum ultraviolet dengan penambahan pereaksi geser menunjukkan adanya gugus hidroksil pada posisi 3,5. Hasil karakterisasi isolat setelah dianalisis secara spektrofotometri ultraviolet dapat disimpulkan sebagai flavonol.
CHARACTERIZATION SIMPLEX, PHYTOCHEMICAL
SCREENING ISOLATION AND IDENTIFICATION COMPOUND
FLAVONOIDA FROM PATIKAN KEBO HERB (Euphorbiae
hirtae Herba)
ABSTRACT
Utilization a large part of floras had been conducted since former to cure various of diseases. Flora patikan kebo is flora terna that most used for asthma medication, cough and red lane pain. This Research main to know characterization of simplex and compound isolation flavonoida by spektrofotometri ultraviolet by using shift reagent. Extraction are conducted in percolation by using ethanol solvent, then compound dissociation flavonoida is conducted in liquid-liquid extraction by using n-heksana solvent, chloroform and acetate ethyl. Fraction of acetate ethyl then paper chromatography with various of motion phase and comparisons to look for the best developer. Furthermore fraction of acetate ethyl is dissociated with preparatif paper chromatography by using developer of acetate acid 50%, from result preparatif is got two isolat F1s and F2. Furthermore this isolat was chromatography two directions, from result known that isolat F1 has been pure whereas isolat F2 not pure. One of isolat that got analysed in spektrofotometri ultraviolet with addition shifts reagent. The Result characterization of simplex gave the water conten value 6,654%, the water soluble extract value 22,06%, the etanol soluble extract value 18,36%, the total ash value 1,074% and the acid insoluble ash value 0,12%. The result phytochemical screening shows there is alkaloid compound, flavonoida, tanin, glikosida, glikosida antrakuinon, steroida, saponin. Analysis Result spektrofotometri ultraviolet with spektrofotometer, maximum absorption exist on wavelength 381 nm that indicate that isolat are flavonoida group. Interpretation of ultraviolet spectrum with addition shifts reagent show existence of hydroxyl bunch on course 3,5. Result characterization of isolat after analysed with spektrofotometri ultraviolet can be concluded as flavonol.
Keyword: patikan kebo, flavonoida, ultraviolet spectrophotometric
BAB I
PENDAHULUAN
1.1 Latar Belakang
Indonesia merupakan salah satu negara penghasil tanaman obat yang potensial
dengan keanekaragaman hayati yang dimilikinya. Tumbuhan merupakan gudang
berbagai jenis senyawa kimia, mulai dari struktur dan sifat yang sederhana sampai
yang rumit dan unik. Upaya pencarian tumbuhan berkhasiat obat telah lama dilakukan,
baik untuk mencari senyawa baru ataupun menambah keanekaragaman senyawa yang
telah ada, dan hasil pencarian dan penelitian tersebut kemudian dilanjutkan dengan
upaya pengisolasian senyawa murni. Beragam jenis dan senyawa kimia yang
terkandung dalam tumbuhan akan berkorelasi positif dengan khasiat dan manfaat yang
dimilikinya. Prospek pengembangan produksi tanaman obat semakin pesat saja
mengingat perkembangan industri obat modern dan obat tradisional terus meningkat
(Djauhauriya, 2004).
Pemanfaatan sebagian besar tumbuhan telah dilakukan sejak dahulu untuk
mengobati berbagai penyakit. Tumbuhan-tumbuhan tersebut dalam penggunaannya
dikenal sebagai obat tradisional. Popularitas dan perkembangan obat tradisional
semakin meningkat seiring dengan slogan ’’kembali ke alam’’ yang kian menggema
sehingga banyak yang tertarik untuk meneliti khasanah tumbuhan yang ada di
Indonesia. Diantara tumbuhan yang digunakan dan diteliti adalah herba patikan kebo
(Euphorbiae hirtae herba).
Tumbuhan patikan kebo merupakan tumbuhan terna, tegak dengan tinggi lebih
kurang 60 cm, bagian yang digunakan dari tumbuhan ini yakni seluruh bagian dari
tumbuhan yang berada diatas tanah. Tumbuhan patikan kebo ini banyak digunakan
untuk pengobatan asma, batuk, sakit tenggorokan, gatal (obat luar) (Anonim, 2009).
Pada beberapa daerah seperti Aceh, Jawa, Sunda tumbuhan ini telah digunakan secara
khitanan, serta untuk obat gatal, dengan adanya khasiat dari patikan kebo yang dapat
mengobati beberapa penyakit maka dilakukan isolasi terhadap senyawa yang
berkhasiat dalam pengobatan tersebut seperti flavonoida.
Senyawa flavonoida merupakan salah satu kandungan metabolit sekunder yang
terdapat pada herba tumbuhan patikan kebo, yaitu golongan fenol alam yang
jumlahnya tersebar dan banyak digunakan dalam pengobatan tradisional. Senyawa
flavonoida terdapat pada semua tumbuhan hijau, dan banyak digunakan dalam
pengobatan tradisional untuk menghambat pendarahan, antioksidan, antihipertensi,
antivirus, mengobati gangguan fungsi hati, antiinflamasi, inhibitor kuat pernapasan,
dan sebagai obat sariawan . Seiring dengan efek flavonoid terhadap macam-macam
organisme sangat banyak maka alasan ini yang menjelaskan mengapa tumbuhan yang
mengandung flavonoida banyak digunakan sebagai bahan obat tradisioanal dalam
pengobatan (Robinson, 1995).
Terdapat sejumlah besar jenis dan cara kromatografi untuk pemisahan dan
pemurnian kandungan tumbuhan diantaranya kromatografi kertas (KKt), kromatigrafi
lapis tipis (KLT), kromatografi gas cair (KGC), kromatografi cair kinerja tinggi
(KCKT). Untuk memisahkan senyawa flavonoida dari herba patikan kebo (Euphorbiae
hirtae herba) digunakan kromatografi kertas (KKt). Kromatografi kertas (Kkt)
merupakan cara kromatografi yang paling umum dan berguna yang dilakukan oleh
kimiawan pada saat ini (Markham, 1988). Cara ini ditemukan jauh sebelum KLT dan
telah dipakai secara efektif selama bertahun-tahun untuk pemisahan molekul biologi
yang polar seperti asam amino, gula, dan nukleotida (Gritter, 1991).
Berdasarkan uraian diatas maka peneliti melakukan uji terhadap flavonoida
dan mengisolasi flavonoida dari herba patikan kebo (Euphorbiae hirtae herba) dengan
alasan karena adanya kandungan flavonoida serta keanekaragaman aktivitas biologis
yang dimiliki oleh flavonoida. Serta juga melakukan identifikasi terhadap senyawa
flavonoida hasil isolasi secara spektrofotometri ultraviolet (UV) menggunakan
pereaksi geser (shift reagent).
1.2 Perumusan Masalah
1. Apakah karakteristik simplisia herba patikan kebo yang diteliti sesuai dengan
parameter Materia Medika Indonesia?
2. Apakah senyawa flavonoida yang terdapat pada ekstrak herba patikan kebo dapat
dipisahkan dan dimurnikan dengan kromatografi kertas?
3. Apakah senyawa flavonoida dari herba patikan kebo hasil isolasi dapat
diidentifikasikan secara spektrofotometri (UV) dengan menggunakan pereaksi
geser (shift reagen)?
1.3 Hipotesa
1. Diduga herba patikan kebo memenuhi persyaratan karakterisasi simplisa yang
tertera pada MMI.
2. Diduga senyawa flavonoida yang terdapat dalam ekstrak herba patikan kebo dapat
dipisahkan dan dimurnikan dengan kromatografi kertas.
3. Diduga senyawa flavonoida dari herba patikan kebo hasil isolasi dapat
diidentifikasikan secara spektrofotometri (UV) dengan menggunakan pereaksi
geser (shift reagen).
1.4 Tujuan Penelitian
1. Untuk mengetahui karakterisasi simplisia herba patikan kebo (Euphorbiae hirtae
herba) yang diteliti
2. Untuk mengetahui cara mengisolasi senyawa flavonoida yang terdapat dalam
herba patikan kebo (Euphorbiae hirtae herba).
3. Untuk mengidentifikasi senyawa flavonoida hasil isolasi yang terdapat dalam
herba patikan kebo (Euphorbiae hirtae herba) secara spektrofotometri (UV)
1.5 Manfaat Penelitian
1. Diperoleh informasi mengenai karakterisasi simplisia herba patikan kebo
(Euphorbiae hirtae herba) yang diteliti.
2. Diperoleh informasi mengenai cara mengisolasi senyawa flavonoida dari herba
patikan kebo dengan kromatografi kertas.
3. Diperoleh informasi golongan senyawa flavonoida dari herba patikan kebo
(Euphorbiae hirtae herba).
BAB II
TINJAUAN PUSTAKA
2.1 Uraian Tumbuhan
Uraian tumbuhan meliputi habitat dan daerah tumbuh, sistematika tumbuhan,
nama asing, nama daerah, morfologi tumbuhan, kandungan senyawa kimia, serta
penggunaan tumbuhan.
2.1.1Habitat (Daerah Tumbuh)
Tumbuhan patikan kebo merupakan tumbuhan yang berasal dari Amerika.
Tumbuhan ini juga terdapat di India, Cina, Malaysia dan Australia. Di Indonesia
banyak dijumpai pada padang rumput ditepi sungai atau dikebun, pada ketinggian
tempat antara 1 m sampai 1.400 m di atas permukaan laut (Depkes RI, 1978).
Tumbuhan patikan kebo merupakan tumbuhan yang tidak lama hidupnya, tumbuhan
ini tumbuh tegak dan merupakan suatu kosmopolit dari daerah tropis dan banyak
terdapat didataran rendah serta pada tanah yang tidak terlalu lembab dan biasanya
berumput (Heyne, 1987).
2.1.2Sistematika Tumbuhan
Sistematika tumbuhan patikan kebo adalah sebagai berikut (Depkes RI, 2001) :
Divisi : Spermatophyta
Subdivisi : Angiospermae
Kelas : Dicotyledoneae
2.1.4Nama Daerah
Nama daerah dari patikan kebo adalah daun biji kacang (Sumatera), nanangkaan
(Sunda), gendong anak (Jakarta), patikan kebo (Jawa), kaksekakan (Madura),
sosonanga (Maluku), isu maibi (Ternate) (Depkes RI, 2001).
2.1.5Morfologi Tumbuhan
Patikan kebo merupakan tumbuhan gulma, terna, tegak dengan tinggi 6 cm
sampai 60 cm, batang berambut, percabangan selalu keluar dari dekat pangkal batang
dan tumbuh lurus ke atas, akar tunggang dan jarang yang tumbuh mendatar dengan
permukaan tanah (Ditjen POM, 1978). Patikan kebo berbatang lunak dan bergetah
putih. Warna batangnya adalah hijau kecoklatan. Daunnya berbentuk jorong
meruncing sampai tumpul, tepinya bergerigi dan berbulu dipermukaan atas dan
bawah. Panjang helaian daun mencapai 50 mm dan lebarnya 25 mm, pertulangan
menyirip, letak daun yang satu dengan yang lain berhadap-hadapan .Daunnya
berwarna hijau atau hijau keunguan. Tumbuhan patikan kebo mampu bertahan hidup
selama 1 tahun dan berkembang biak melalui biji (Anonim a, 2009).
2.1.6Kandungan Kimia
Patiakan kebo mengandung beberapa unsur kimia, antara lain : alkaloida, tanin,
saponin, senyawa polifenol (seperti asam gallat), flavonoid, dan senyawa
triterpenoida/steroida (Anonim a, 2009).
2.1.7Penggunaan Tumbuhan
Seluruh bagian tumbuhan patikan kebo segar atau kering dapat digunakan untuk
mengobati penyakit antara lain : asma, disentri, melancarkan kencing, abses paru dan
bronkhitis kronis (Hariana, 2007).
2.2 Senyawa Flavonoida
Senyawa flavonoida merupakan senyawa polifenol yang mengandung 15 atom
karbon dalam inti dasarnya, yang tersusun dalam konfigurasi C6 – C3 – C6, yaitu dua
cincin aromatik yang dihubungkan oleh satuan tiga karbon yang dapat atau tidak dapat
membentuk cincin ketiga (Markham, 1988).
Gambar 1. Kerangka Flavonoida
Flavonoida sering terdapat sebagai glikosida. Golongan terbesar flavonoid berciri
mempunyai cincin piran yang menghubungkan rantai tiga karbon dengan salah satu
dari cincin benzena. Sistem penomoran untuk turunan flavonoid adalah :
Gambar 2. Struktur Dasar Flavonoid
Flavonoida mencakup banyak pigmen dan terdapat pada tumbuhan mulai dari fungus
sampai angiospermae. Pada tumbuhan tinggi, flavonoida terdapat baik dalam bagian
vegetatif maupaun bunga. Sebagai pigmen bunga, flavonoida berperan dalam menarik
burung, dan serangga penyerbuk bunga. Beberapa flavonoida tidak berwarna tetapi
menyerap sinar ultraviolet. Beberapa kemungkinan fungsi flavonoida untuk tumbuhan
yang mengandungnya ialah pengatur tumbuh, pengatur fotosintesis, kerja antimikroba,
antivirus, dan kerja terhadap serangga (Robinson, 1995).
Flavonoida sering terdapat dalam tumbuhan sebagai campuran dari flavonoida
yang berbeda golongan dan jarang sekali dijumpai hanya flavonoida tunggal dalan
struktur molekul dengan beberapa bentuk kombinasi glikosida. Oleh karena itu dalam
menganalisis flavonoid lebih baik memeriksa aglikon yang telah terhidrolisis
dibanding dalam bentuk glikosida dengan strukturnya yang rumit dan kompleks
(Harborne, 1987).
Menurut Robinson (1995), senyawa flavonoid dapat diklasifikasikan sebagai
berikut :
1. Flavanon dan Flavanonol
Senyawa ini terdapat hanya sedikit sekali jika dibandingkan dengan flavonoid
lain. Flavanon dan flavononol tidak berwarna atau hanya kuning sedikit. Flavanon
(dihidroflavon) sering terjadi sebagai aglikon, tetapi beberapa glikosidanya dikenal
sebagai, misalnya hesperidin dan naringin. Flavononol (dihidroflavonol) merupakan
flavonoid yang kurang dikenal, dan tidak diketahui apakah senyawa ini terdapat
sebagai glikosoda (Robinson, 1995).
Gambar 3. Struktur flavanon Gambar 4. Struktur Flavanonol
2. Flavon dan flavonol
Flavon dan flavonol barangkali merupakan senyawa yang paling tersebar luas
dari semua pigmen tumbuhan kuning. Flavon berbeda dengan flavonol karena pada
flavon tak terdapat gugus 3- hidroksi. Hal ini mempengaruhi serapan UV-nya, gerakan
kromatografinya, serta reaksi warnanya, dan karena itu flavon dapat dibedakan dari
flavonol berdasarkan ketiga sifat tersebut. Hanya ada dua flavon yang umum, yaitu
apigenin dan luteolin. Jenis yang paling umum adalah 7- glikosida. Dalam tumbuhan
falvonol sering terdapat sebagai glikosiida, biasanya 3-glikosida. Aglikon flavonol
yang umumnya dijumpai yaitu kemferol, kuersetin, dan mirisetin (Harborne, 1987).
Gambar 5. Struktur Flavon Gambar 6. Struktur Flavonol
3. Isoflavon
Isoflavon sukar dicirikan karena reaksinya tidak khas dengan pereaksi warna
apapun. Beberapa isoflavon memberikan warna biru cemerlang dengan sinar UV bila
diuapi amonia, tetapi kebanyakan yang lain tampak sebagai bercak lembayung pudar
yang dengan amoniaberubah menjadi coklat pudar. Isoflavon merupakan golongan
flavonoid yang penyebarannya terbatas dan jumlahnya sedikt (Harborne, 1987).
Gambar 7. Struktur Isoflavon
4. Antosianin
Antosianin merupakan pewarna yang paling penting dan paling tersebar luas
dalam tumbuhan, merupakan pembentuk dasar pigmen warna merah, ungu dan biru
pada tanaman, terutama sebagai bahan pewarna bunga dan buah-buahan. Sebagian
besar antosianin adalah glikosida, dan aglikonnya disebut antosianidin, yang terbentuk
bila antosianin dihidrolisis dengan asam.Antosianin yang paling umum adalah sianidin
yang berwarna merah lembayung (Harborne, 1987; Robinson, 1995; Sastrohamidjojo,
Gambar 8. Struktur Antosianidin
5. Auron dan kalkon
Auron berupa bercak kuning, dengan sinar UV mereka tampak berbeda, warna
auron kuning murup kuat dan berubah menjadi merah jingga bila diuapi amonia.
Kalkon adalah pigmen fenol kuning yang berwarna coklat dengan sinar UV
(Harborne, 1987).
Gambar 9. Struktur Auron Gambar 10. Struktur Kalkon
2.3 Ekstraksi
Ekstraksi adalah kegiatan penarikan kandungan kimia yang dapat larut
sehingga terpisah dari bahan yang tidak dapat larut dengan menggunakan pelarut cair.
Senyawa aktif yang terdapat dalam berbagai simplisia dapat digolongkan ke dalam
golongan minyak atsiri, alkaloida, flavonoid, dan lain-lain. Dengan diketahuinya
senyawa aktif yang dikandung simplisia akan mempermudah pemilihan pelarut dan
cara ekstraksi yang tepat. Cara ekstraksi yang tepat tergantung pada tumbuhan yang
diekstraksi dan jenis senyawa yang diisolasi (Ditjen POM, 2000: Gritter, 1991).
Ekstraksi dapat dilakukan dengan berbagai cara (Ditjen POM, 2000), yaitu:
1. Maserasi
Maserasi adalah proses ekstraksi simplisia dengan menggunakan pelarut dengan
beberapa kali pengocokan atau pengadukan pada temperatur ruangan. Maserasi
kinetik berarti dilakukan pengadukan yang kontinu (terus-menerus).
Remaserasi berarti dilakukan pengulangan penambahn pelarut setelah dilakukan
penyaringan maserat pertama, dan seharusnya.
2. Perkolasi
Perkolasi adalah ekstraksi dengan pelarut yang selalu baru sampai sempurna yang
umunya dilakukan pada temperatur ruangan. Proses ini terdiri dari tahapan
pengembangan bahan, tahap maserasi antara, tahap perkolasi sebenarnya
(penetesan/penampungan ekstrak), terus-menerus sampai ekstrak yang diinginkan
habis tersari. Tahap pengembangan bahan dan maserasi antara dilakukan dengan
maserasi serbuk menggunakan cairan penyari sekurang-kurangnya 3 jam, hal ini
penting terutama untuk serbuk yang keras dan bahan yang mudah mengembang.
3. Refluks
Refluks adalah ekstraksi dengan pelarut pada temperatur titik didihnya selama
waktu tertentu dan jumlah pelarut terbatas yang relatif konstan dengan adanya
pendingin balik.
4. Sokletasi
Sokletasi adalah ekstraksi menggunakan pelarut yang selalu baru, umumnya
dilakukan dengan alat khusus sehingga terjadi ekstraksi kontinu dengan jumlah
pelarut relatif konstan dengan adanya pendingin balik.
5. Digesti
Digesti adalah maserasi kinetik (dengan pengadukan kontinu) pada temperatur
yang lebih tinggi dari temperatur ruangan, yaitu pada temperatur 40-50°C.
Infus adalah ekstraksi dengan pelarut air pada temperatur penangas air (bejana
infus tercelup dalam penangas air mendidih, temperatur 96-98°C) selama waktu
tertentu (15-20 menit).
7. Dekok
Dekok adalah infus pada waktu yang lebih lama dan temperatur sampai titik didih
air.
2.4 Kromatografi
Kromatografi adalah suatu metode pemisahan berdasarkan perbedaan
perpindahan dari komponen-komponen senyawa diantara dua fase yaitu fase diam
(dapat berupa zat cair atau zat padat) dan fase gerak (dapat berupa gas atau zat cair)
(Depkes RI, 1995). Jika fase tetatp berupa zat padat maka cara tersebut dikenal
sebagai kromatografi serapan, jika zat cair dikenal sebagai kromatografi partisi.
Karena fase bergerak dapat berupa zat cair dan gas maka ada empat macam sistem
kromatografi (Sastrohamidjojo, 1985):
1. Fase bergerak zat cair - fase tetap padat:
- Kromatografi lapis tipis
- Kromatografi penukar ion
2. Fase bergerak gas – fase tetap padat
- Kromatografi gas padat
3. Fase bergerak zat cair – fase tetap zat cair
Dikenal sebagai kromatografi partisi
- Kromatografi kertas
4. Fase bergerak gas – fase tetap zat cair
- Kromatografi gas cair
- Kromatografi kolom kapiler
2.4.1 Kromatografi Kertas
Salah satu keuntungan utama KKt ialah kemudahan dan kesederhanaan pada
pelaksanaan pemisahan, yaitu hanya pada lembaran kertas saring yang berlaku sebagai
medium pemisahan. Pada KKt, senyawa biasanya dideteksi sebagai bercak berwarna
atau bercak berfluoresensi ultraviolet setelah direaksikan dengan penampak bercak.
Pada kromatografi kertas sebagai fase diam digunakan sehelai kertas dengan
susunan serabut dan tebal yang sesuai. Pemisahan dapat dilakukan menggunakan
pelarut tunggal dengan proses yang analog dengan kromatografi penyerapan atau
menggunakan dua pelarut yang tidak dapat bercampur dengan proses yang analog
dengan kromatografi pembagian, fase gerak merambat perlahan-lahan melalui fase
diam yang membungkus serabut kertas.
Menurut Gritter (1991), kromatogram dapat dikembangkan dengan cara
menaik atau dengan cara menurun. Untuk cara menaik, kertas digantungkan pada
penggantung berbentuk kail yang dipasang pada penutup bejana kromatografi, dan
pelarut berada di bawah bejana. Untuk cara menurun lazimnya dipakai bejana yang
lebih besar. Bejana dilengkapi dengan sejenis wadah pelarut yang dipasang pada
penopang, dan kertas kromatografi dicelupkan kedalam pelarut didalam wadah itu dan
berarti batang kaca supaya tetap pada tempatnya.
Fase gerak biasanya merupakan campuran yang terdiri atas satu komponen
organik yang utama air dan berbagai tambahan seperti asam-asam, basa dengan tujuan
untuk memperbesar kelarutan dari beberapa senyawa atau untuk mengurangi kelarutan
(Sastrohamidjojo, 1985).
Gerakan noda suatu senyawa dalam pengembang tertentu disebut bilangan Rf
senyawa itu dalam pengembang tersebut. Bilangan Rf didefinisikan sebagai jarak yang
ditempuh oleh senyawa dibagi dengan jarak yang ditempuh oleh garis depan fase
gerak (diukur dari garis awal). Karena itu bilangn Rf selalu lebih kecil dari 1,0.
sejenis merupakan cara yang berguna untuk membandingkan flavonoida yang sedang
diientifikasi dengan flavonoida yang tidak ada dilaboratorium (Markham, 1988).
Menurut Sastrohamidjojo (1985), faktor-faktor yang mempengaruhi harga Rf
adalah struktur kimia dari senyawa yang dipisahkan, sifat dari penyerap, tebal dan
kerataan lapisan penyerap, pelarut, kertas, sifat dari campuran, derajat kejenuhan dari
bejana pengembangan, tehnik percobaan, jumlah cuplikan yang digunakan, suhu dan
kesetimbangan.
2.5 Spektrofotometri Ultraviolet
Spektrofotometri ultraviolet merupakan suatu cara analisis berdasarkan atas
pengukuran serapan suatu larutan yang dilalui radiasi cahaya elektromagnetis.
Spektrum ultraviolet digambarkan sebagai hubungan antara panjang gelombang
dengan intensitas serapan (transmitansi atau absorbansi) (Sastrohamidjojo, 1985).
Spektrofotometri ultraviolet pada umumnya digunakan untuk menentukan jenis
kromofor, ikatan rangkap yang terkonyugasi, menjelaskan informasi dari struktur
berdasarkan panjang gelombang maksimum suatu senyawa. Ketika suatu molekul
menyerap cahaya maka energi tersebut akan menyebabkan tereksitasinya elektron
pada kulit terluar ke tingkat energi yang lebih tinggi. Sinar ultraviolet akan
menyebabkan elektron tereksitasi ke orbital yang lebih tinggi (Dachriyanus, 2004).
Beberapa istilah yang digunakan dalam spektrofotometri ultraviolet meliputi
(Dahcriyanus, 2004):
1. Kromofor: merupakan gugus tidak jenuh yang menyerap radiasi di daerah
ultraviolet dengan hampir semua kromofor mempunyai ikatan tidak jenuh.
Contohnya : C=C, C=O, NO2.
2. Auksokrom: merupakan suatu gugus fungsi dengan adanya elektron bebas(tidak
terikat), dimana jika gugus ini bergabung dengan kromofor, akan mengubah
panjang gelombang dan intensitas dari serapan maksimum. Contohnya : OH,
-NH2, -Cl.
3. Pergeseran batokromik: merupakan pergeseran absorban ke daerah panjang
gelombang yang lebih panjang karena adanya substitusi pada kromofor (oleh
auksokrom) atau efek pelarut.
4. Pergeseran hipsokromik: merupakan pergeseran ke daerah panjang gelombang
yang lebih pendek karena adanya substitusi atau efek pelarut.
5. Efek hiperkromik: merupakan peningkatan intensitas absorban.
6. Efek hipokromik: merupakan penurunan intensitas absorban.
Spektroskopi serapan ultraviolet adalah cara yang berguna untuk menganalisis
struktur flavonoida. Cara tersebut digunakan untuk mengidentifikasi jenis flavonoida
dan menetukan pola oksigenasi. Disamping itu, kedudukan gugus hidroksil fenol
bebas pada inti flavonoid dapat ditentukan dengan menambahkan pereaksi geser ke
dalam larutan cuplikan dan mengamati pergeseran puncak serapan yang terjadi.
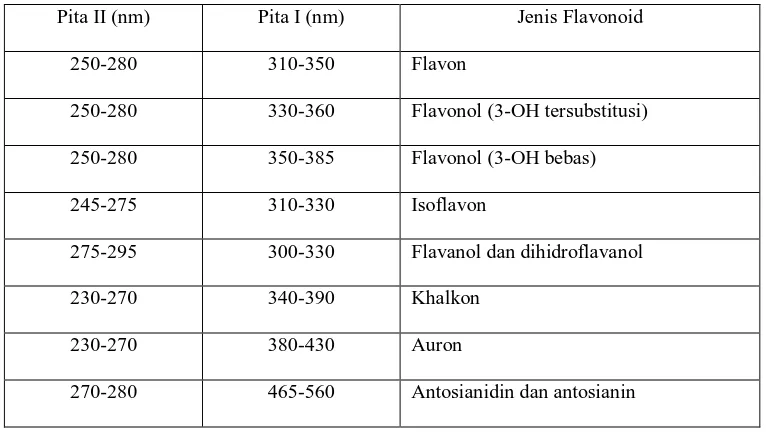
Spektrum flavonoid biasanya ditentukan dalam larutan dengan pelarut metanol atau
etanol. Spektrum khas terdiri dari 2 pita absorbsi maksimum, yaitu pada rentang
240-285 nm (pita II) dan 300-550 nm (pita I) (Markham, 1988).
Langkah pertama yang dilakukan untuk menafsirkan spektrum yaitu,
menentukan jenis flavonoid dengan memperhatikan:
1. Bentuk umum spektrum dalam metanol
2. Panjang gelombang pita serapan
3. Data kromatografi kertas.
Langkah kedua adalah mempertimbangkan arti perubahan spektrum yang
disebabkan oleh berbagai pereaksi geser (Markham, 1988).
Spektrum natrium metoksida
Natrium metoksida merupakan basa kuat yang dapat mengionisasi hampir
semua gugus hidroksi pada inti flavonoid. Penambahan natrium metoksida ke dalam
pengurangan kekuatan spektrum setelah waktu tertentu merupakan petunjuk baik akan
adanya gugus yang peka terhadap basa. Pereaksi pengganti antrium metoksida yang
cocok adalah natrium hidroksida 2M dalam air (Markham, 1988).
Spektrum AlCl3 dan AlCl3/HCl
Aluminium klorida membentuk kompleks tahan asam dengan gugus hidroksi
(pada C3 dan C5) dan keton, juga membentuk kompleks tak tahan asam dengan gugus
orto-hidroksi, sehingga dapat digunakan untuk mendeteksi kedua gugus tersebut.
Spektrum AlCl3/HCl hanya berguna untuk mendeteksi gugus hidroksi yang
bertetangga dengan gugus keton, karena gugus tersebut dengan AlCl3 akan
membentuk senyawa kompleks yang tahan asam (Markham, 1988).
Spektrum natrium asetat
Natrium asetat digunakan terutama untuk mendeteksi adanya gugus 7-hidroksi
bebas. Pengurangan kekuatan intensitas natrium asetat dari flavonol merupakan
petunjuk adanya gugus yang peka terhadap basa (Markham, 1988).
Spektrum natrium asetat/asam borat
Menjembatani kedua gugus hidroksil pada gugus orto-dihidroksi dan
digunakan untuk mendeteksinya (Markham, 1988).
BAB III
METODOLOGI PENELITIAN
Metode yang diterapkan adalah metode deskriptif meliputi pengumpulan bahan
tanaman, identifikasi tanaman, pengolahan tanaman, karakterisasi simplisia, skrining
fitokimia, pembuatan ekstrak, analisis kromatografi kertas (KKt), uji kemurnian isolat,
dan identifikasi senyawa hasil isolasi (isolat) secara spektrofotometri (UV) dengan
penambahan pereaksi geser (shift reagen).
Alat-alat yang digunakan
Alat-alat yang digunakan dalam penelitian ini adalah alat-alat gelas, blender
(National), neraca kasar (Ohaus), neraca listrik (Sartorius), alat perkolasi, eksikator,
penangas air (Yenaco), freeze dryer, penguap vakum putar (Buchi 461), chamber,
seperangkat alat penetapan kadar air, mikroskop (Olympus), lampu spiritus, kaca
objek, kaca penutup dan spektrofotometer (UV) (Shimadzu UV-1240).
Bahan-bahan yang digunakan
Bahan tumbuhan yang digunakan pada penelitian ini adalah herba patikan kebo
(Euphorbiae hirtae herba). Bahan kimia yang digunakan kecuali dinyatakan lain
berkualitas pro analisis yaitu n-heksan, etil asetat, etanol, metanol, isopropanol,
benzen, toluen, asam asetat glasial, asam klorida pekat, asam sulfat pekat, amil
alkohol, kloroform, n-butanol, asam nitrat pekat, natrium hidroksida timbal (II) asetat,
besi (III) klorida, iodium, raksa (II) klorida, aluminium (III) klorida, kalium iodida,
asam asetat anhidrat, asam borat, serbuk magnesium, alpa naftol, kloralhidrat,
floroglusinol, air suling, kertas Whatman No.1 dan No. 3.
Pengumpulan dan Pengolahan Bahan Tumbuhan
Pengambilan Bahan Tumbuhan
Bahan tumbuhan yang digunakan adalah herba patikan kebo (Euphorbiae
hirtae herba) yang telah lengkap dengan bunga, buah dan biji, yang diperoleh dari
Identifikasi Tumbuhan
Identifikasi tumbuhan telah dilakukan di Pusat Penelitian dan Pengembangan
Biologi, LIPI, Bogor. Hasil identifikasi tumbuhan dapat dilihat pada lampiran 1
halaman 40. Gambar tumbuhan dan simplisia dapat dilihat pada lampiran 2 halaman
41.
Pengolahan Bahan Tumbuhan
Herba patikan kebo yang telah dikumpulkan, disortasi basah yaitu memisahkan
tumbuhan lain yang terikut dan kotoran-kotoran, kemudian dicuci untuk
menghilangkan tanah dan pengotoran lainnya dilakukan dengan air yang bersih,
ditiriskan lalu disebarkan diatas koran polos dan kemudian ditimbang, lalu dilakukan
mikroskopik terhadap bahan tumbuhan yang segar, kemudian dipotong-potong dan
dipisahkan antara daun dan batang lalu dikeringkan dalam lemari pengering pada
temperatur ± 40°C hingga kering atau sampai mudah dipatahkan lalu ditimbang,
diperoleh simplisia kering, dapat dilihat pada lampiran 2 halaman 27. Simplisia kering
diserbuk menggunakan blender dan ditimbang sebagai berat serbuk simplisia.
Selanjutnya serbuk disimpan dalam kantung plastik dan dimasukkan kedalam lemari
pengering untuk mencegah pengaruh lembab dan pengotoran lainnya. Pengolahan
bahan tumbuhan dapat dilihat pada lampiran 3 halaman 42.
3.4 Pembuatan Larutan Pereaksi.
3.4.1 Pereaksi Natrium Hidroksida 2 N
Sebanyak 8,002 g natrium hidroksida dilarutkan dalam air suling bebas
karbondioksida hingga 100 ml (Depkes RI, 1979).
Pereaksi Asam Klorida 6 N
Sebanyak 50 ml asam klorida pekat diencerkan dalam air suling hingga 150
ml(Markham, 1988).
Pereaksi Aluminium Klorida 5% b/v
Sebanyak 5,0 g aluminium klorida ditimbang kemudian dilarutkan dalam
etanol hingga 100 ml (Markham, 1988).
Pereaksi Dragendorff
Sebanyak 8,0 g bismut (III) nitrat dilarutkan dalam 20 ml asam nitrat dan
dilarutkan 27,2 g, kalium iodida dalam 50 ml air suling. Campur kedua larutan dan
diamkan sampai memisah sempurna. Diambil larutan jernih dan diencerkan dalam air
secukupnya hingga 100 ml (Depkes RI, 1995).
Pereaksi Bouchardat
Sebanyak 4,0 g kalium iodida dilarutkan dalam air suling secukupnya sampai
KI larut dengan sempurna, lalu ditambahkan 2 g iodium sedikit demi sedikit dan
dicukupkan dengan air suling hingga volume 100 ml (Depkes RI,1979).
Pereaksi Mayer
Sebanyak 1,36 g raksa (II) klorida dilarutkan dalam air suling hingga 60 ml.
Pada wadah lain, 5 g kalium iodida dilarutkan dalam 10 ml air suling. Kemudian 60
ml larutan I dicampurkan dengan 10 ml larutan II dan ditambahkan air suling hingga
100 ml (Depkes RI, 1995).
Pereaksi Molish
Sebanyak 3,0 g α- naftol dilarutkan dalam asam nitrat 0,5 N hingga diperoleh
100 ml larutan (Depkes RI, 1995).
Pereaksi Timbal (II) Asetat 0,4 M
Sebanyak 15,17 g Timbal (II) Asetat dilarutkan dalam air suling bebas
karbondioksida hingga 100 ml (Depkes RI, 1995).
Pereaksi Kloralhidrat jenuh
Sebanyak 50 g kloralhidrat dilarutkan didalam 20 ml air suling (Depkes RI,
3.4.10 Pereaksi Asam Klorida 2N
Sebanyak 17 ml asam klorida pekat diencerkan dengan air suling hingga 100
ml (Depkes RI, 1979).
3.4.11 Pereaksi Floroglusinol HCl
1,0 g floroglusinol ditambah beberapa tetes HCl pekat sampai memerahkan
lignin (Depkes RI, 1995).
3.4.12 Pereaksi Besi (III) klorida 1%
Sebanyak 1,0 g besi (III) klorida dilarutkan dalam air suling hinnga 100 ml
(Depkes RI, 1995).
Pemeriksaan Karakterisasi Simplisia
Pemeriksaan karakterisasi simplisia meliputi pemeriksaan makroskopik dan
mikroskopik, penetapan kadar air, penetapan kadar abu total, penetapan kadar abu
tidak larut asam, penetapan kadar sari larut dalam air, dan penetapan kadar sari larut
dalam etanol (Depkes RI, 1995; WHO, 1992).
3.5.1 Pemeriksaan Makroskopik
Pemeriksaan makroskopik dilakukan dengan mengamati bentuk, bau dan
warna dari simplisia herba patikan kebo (Euphorbiae hirtae herba).
3.5.2 Pemeriksaan Mikroskopik
Sebelum dilakukan pemeriksaan mikroskopik dari serbuk simplisia maka
dilakukan pemeriksaan mikroskopik pada tanaman segar.
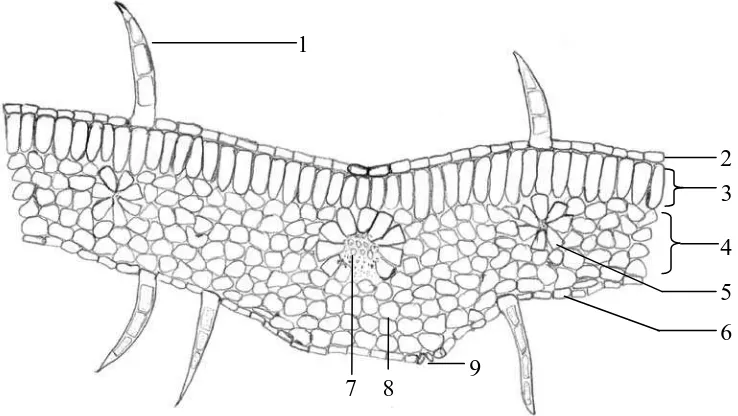
- Sayatan melintang daun tumbuhan patikan kebo
Cara kerja: Pada kaca objek ditetesi kloralhidrat, diletakkan sayatan melintang daun
tumbuhan patikan kebo, dipanaskan diatas lampu spiritus, tidak sampai kering, dicuci
dengan beberapa tetes akuades, kemudian ditetesi beberapa tetes floroglusinol HCl,
didiamkan selama 10 menit, ditutup dengan kaca penutup, kemudian diamati dibawah
mikroskop.
- Sayatan membujur (atas dan bawah) daun tumbuhan patikan kebo
Cara kerja: Pada kaca objek ditetesi kloralhidrat, diletakkan sayatan membujur daun
tumbuhan patikan kebo, dipanaskan diatas lampu spiritus, tidak sampai kering, dicuci
dengan beberapa tetes akuades, ditambah kloralhidrat, ditutup dengan kaca penutup,
kemudian diamati dibawah mikroskop. Hasil mikroskopik sayatan melintang dan
membujur daun tumbuhan patikan kebo dapat dilihat padalampiran 4 halaman 43-45.
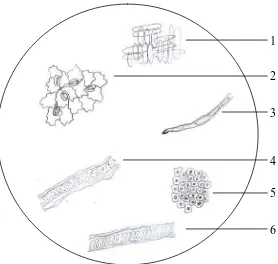
- Pemeriksaan serbuk simplisia
Pemeriksaan mikroskopik dilakukan terhadap serbuk simplisia herba patikan
kebo. Serbuk simplisia ditaburkan diatas kaca objek yang telah ditetesi larutan kloral
hidrat kemudian ditutup dengan kaca penutup, kemudian diamati pada mikroskop.
Hasil mikroskopik serbuk simplisia herba patikan kebo dapat dilihat pada lampiran 4
halaman 46.
3.5.3 Penetapan Kadar Air
Penetapan kadar air dilakukan dengan metode Azeotropi (Destilasi Toluen).
Alat-alat terdiri dari labu alas bulat 500 ml, pendingin, tabung penyambung, tabung
penerima.
Cara kerja : kedalam labu alas bulat dimasukkan 200 ml toluen dan 2 ml air suling,
didestilasi selama 2 jam, toluen didinginkan selama 30 menit dan volume air dalam
tabung penerima dibaca. Kemudian kedalam labu dimasukkan 5 g serbuk simplisia
yang telah ditimbang seksama, lalu dipanaskan hati-hati selama 15 menit, setelah
toluen mendidih, kecepatan tetesan diatur 2 tetes tiap detik sampai sebagian air
terdestilasi, kemudian kecepatan destilasi dinaikkan sampai 4 tetes tiap detik. Setelah
semua air terdestilasi, bagian dalam pendingin dibilas dengan toluen, destilasi
dilanjutkan selama 5 menit, kemudian tabung penerima dibiarkan mendingin pada
suhu kamar. Setelah air dan toluen memisah sempurna, dibaca volume air dengan
3.5.4 Penetapan Kadar Abu Total
Sebanyak 2 g serbuk yang telah digerus dan ditimbang seksama dimasukkan
dalam krus porselin yang telah dipijar dan ditara, kemudian ditarakan. Krus dipijar
perlahan-lahan sampai arang habis, pemijaran dilakukan pada suhu 600° C selama 2
jam kemudian didinginkan dan ditimbang sampai diperoleh bobot tetap. Kadar abu
dihitung terhadap bahan yang telah dikeringkan di udara (Depkes RI, 1995).
3.5.5 Penetapan Kadar Abu yang Tidak Larut dalam Asam
Abu yang telah diperoleh dalam penetapan kadar abu dididihkan dalam 25 ml
asam klorida encer selama 5 menit, bagian yang tidak larut dalam asam dikumpulkan,
disaring melalui kertas saring dipijarkan sampai bobot tetap, kemudian didinginkan
dan ditimbang. Kadar abu yang tidak larut dalam asam dihitung terhadap bahan yang
dikeringkan diudara (Depkes RI, 1995).
3.5.6 Penetapan Kadar Sari yang Larut dalam Air
Sebanyak 5 g serbuk dimaserasi selama 24 jam dalam 100 ml air-kloroform (2,5
ml kloroform dalam air sampai 1 liter) dalam labu bersumbat sambil dikocok selama 6
jam pertama, kemudian dibiarkan selama 18 jam. Saring, sejumlah 20 ml filtrat
diuapkan hingga kering dalam cawan dangkal berdasar rata yang telah ditara, dan sisa
dipanaskan pada suhu 105° C hingga bobot tetap. Persen kadar sari yang larut dalam
air, dihitung terhadap bahan dikeringkan di udara (Depkes RI, 1995).
3.5.7 Penetapan Kadar Sari yang Larut dalan Etanol
Sebanyak 5 g serbuk dimaserasi selama 24 jam dalam 100 ml etanol 96% dalam
labu tersumbat sambil dikocok sesekali selama 6 jam pertama, kemudian dibiarkan
selama 18 jam. Saring cepat untuk menghindari penguapan etanol, uapkan 20 ml filtrat
hingga kering dalam cawan dangkal berdasar rata yang telah ditara dan panaskan sisa
pada suhu 105°C hingga bobot tetap. Dihitung kadar sari yang larut dalam etanol
terhadap bahan yang telah dikeringkan di udara (Depkes RI, 1995).
3.6 Skrining Fitokimia
Skrining fitokimia dari serbuk simplisia meliputi pemeriksaan senyawa
golongan alkaloida, steroida/ triterpenoida, tanin, saponin, flavonoida, glikosida dan
glikosida antrakuinon
.
3.6.1Pemeriksaan Alkaloida
Sebanyak 0,5 g serbuk simplisia, kemudian ditambah 1 ml asamklorida 2 N dan
9 ml air suling, dipanaskan diatas penangas air selama 2 menit. Dinginkan dan
disaring. Filtrat digunakan untuk percobaan berikut :
a. Filtrat sebanyak 3 tetes ditambah dengan 2 tetes larutan pereaksi Mayer, akan
terbentuk endapan menggumpal berwarna putih atau kuning.
b. Filtrat sebanyak 3 tetes ditambah pereaksi Bouchardat, akan terbentuk
endapan berwarna coklat sampai hitam.
c. Filtrat sebanyak 3 tetes ditambah dengan 2 tetes pereaksi Dragendorff, akan
terbentuk warna merah atau jingga.
Alkaloida positif jika terjadi endapan atau kekeruhan paling sedikit dua dari
ketiga percobaan diatas (Depkes RI, 1995).
3.6.2 Pemeriksaan Flavonoida
Sebanyak 10 g serbuk simplisia ditambahkan air panas, dididihkan selama 5
menit dan disaring dalam keadaan panas, ke dalam 5 ml filtrat ditambahkan 0,1 g
serbuk magnesium dan 1 ml asam klorida pekat dan 2 ml amil alkohol, dikocok dan
dibiarkan memisah. Flavonoida positif jika warna merah, kuning, jingga pada lapisan
amil alkohol (Farnsworth, 1996).
3.6.3 Pemeriksaan Saponin
Sebanyak 0,5 g serbuk simplisia, dimasukkan kedalam tabung reaksi.
dan tidak hilang dengan penambahan asam klorida 2 N menunjukkan adanya saponin
(Depkes RI, 1995).
3.6.4 Pemeriksaan Glikosida
Sebanyak 3 g serbuk simplisia disari dengan 30 ml campuran etanol 96 %
dengan air (7:3), dan 10 ml asam sulfat 2 N. Direfluks selama 1 jam, didinginkan dan
disaring. Pada 20 ml filtrat ditambahkan 25 ml Timbal (II) asetat 0,4 M, dikocok dan
didiamkan selama 5 menit, disaring. Disari filtrat 3 kali, tiap kali dengan 20 ml
campuran kloroform-isopropanol (3:2). Pada kumpulan sari di tambahkan Natrium
sulfat anhidrat, disaring dan diuapkan pada suhu tidak lebih dari 50oC. Dilarutkan sisa
dengan 2 ml etanol. Larutan sisa dimasukkan dalam tabung reaksi selanjutnya
diuapkan diatas penangas air, pada sisa ditambahkan 2 ml air dan 5 tetes Molisch.
Tambahkan hati-hati 2 ml asam sulfat pekat melalui dinding tabung, terbentuknya
cincin ungu pada batas kedua cairan menunujukkan adanya gula, dengan demikian
menunjukkan adanya glikosida (Depkes RI, 1995).
3.6.5 Pemeriksaan Tanin
Sebanyak 0,5 g serbuk simplisia, disari dengan 10 ml air suling lalu
dipanaskan, disaring. Filtratnya diencerkan dengan air sampai tidak berwarna. Larutan
diambil sebanyak 2 ml dan ditambahkan 1-2 tetes pereaksi besi (III) klorida 1 %. Jika
terjadi warna biru atau hijau kehitaman, menunjukkan adanya tannin (Depkes RI,
1995).
3.6.6 Pemeriksaan Steroida dan triterpenoida
Sebanyak 1 g serbuk dimaserasi dengan 20 ml n-heksana selama 2 jam,
disaring, filtrat diuapkan di cawan penguap. Sisanya ditambahkan 20 tetes asam asetat
anhidrat dan 1 tetes asam sulfat pekat (pereaksi Liebermann-Bourchard). Apabila
terbentuk warna ungu atau merah yang berubah menjadi biru ungu atau biru hijau
menunjukkan adanya steroida/triterpenoida (Harborne, 1987).
3.6.7 Pemeriksaan Glikosida Antrakuinon
Sebanyak 0,2 g serbuk simplisia ditambah dengan 5 ml asam sulfat 2 N,
dipanaskan sebentar, setelah dingin ditambahkan 10 ml benzena, dikocok dan
didiamkan. Lapisan benzena dipisahkan dan disaring. Kocok lapisan benzena dengan
2 ml NaOH 2 N, didiamkan. Lapisan ini berwarna merah dan lapisan benzena tidak
berwarna menunjukkan adanya antrakuinon (Depkes RI, 1995). Hasil skrining
fitokimia serbuk simplisia dapat dilihat pada lampiran 6 halaman 52.
3.7 Pembuatan Ekstrak
Pembuatan ekstrak dilakukan dengan cara perkolasi menggunakan pelarut
etanol.
Cara kerja :
Sebanyak 300 g serbuk simplisia dibasahi dengan cairan penyari dan dibiarkan selama
3 jam, kemudian dimasukkan ke dalam alat perkolator. Lalu dituang cairan penyari
secukupnya sampai semua terendam dan terdapat selapis cairan penyari diatasnya,
mulut tabung perkolator ditutup dengan aluminium foil dan dibiarkan selama 24 jam,
kemudian kran dibuka dan dibiarkan tetesan ekstrak mengalir. Perkolasi dihentikan
setelah tetesan perkolat terakhir tidak bereaksi lagi dengan pereaksi untuk uji senyawa
golongan flavonoida. Selanjutnya ekstrak diuapkan dengan penguap vakum putar pada
temperatur tidak lebih dari 50°C sampai diperoleh ekstrak kental. Kemudian
dikeringkan dengan freeze dryer selama lebih kurang 24 jam Bagan ekstraksi serbuk
simplisia dapat dilihat pada lampiran 7 halaman 53.
3.8 Ekstraksi Cair-Cair Senyawa Flavonoida
Ekstraksi cair-cair senyawa flavonoida dari ekstrak etanol dilakukan
berturut-turut dengan pelarut n-heksana, kloroform dan etil asetat. Caranya : ekstrak etanol
ditambah 10 ml etanol, kemudian dilarutkan dalam air panas sebanyak 100 ml,
selanjutnya dihidrolisis dengan asam (ditambah asam klorida 2N), di refluks selama 5
sebanyak 100 ml, diperoleh fraksi n-heksana dan fraksi air. Fraksi n-heksana
dipisahkan, fraksi air kemudian difraksinasi lagi dengan kloroform sebanyak 100 ml,
diperoleh fraksi kloroform dan fraksi air, kemudian fraksi kloroform dipisahkan fraksi
air difraksinasi lagi dengan 100 ml etil asetat, diperoleh fraksi etil asetat dan fraksi air.
Ekstrak hasil fraksinasi dipekatkan dengan diuapkan diatas penangas air (Markham,
1988). Bagan ekstraksi cair-cair dari ekstrak etanol dapat dilihat pada lampiran 8
halaman 54.
3.9 Analisis Senyawa Flavonoida dari Ekstrak Hasil Fraksinasi Dengan Cara Kromatografi Kertas
Terhadap ekstrak hasil fraksinasi dilakukan kromatografi kertas (KKt) dengan
fase gerak asam asetat 50 % , BAA (n-butanol - asam asetat - air = 4:1:5) dan forestal
(asam asetat - air - asam klorida), asam asetat 15%, HCl 1% Fase diam adalah kertas
whatman No.1 yang berukuran 3x25 cm.
Cara kerja :
Ekstrak etanol, fraksi n-heksana, fraksi kloroform, fraksi etil asetat dan fraksi air
masing-masing ditotolkan pada kertas whatman dari tepi bawah, kemudian kertas
tersebut dimasukkan kedalam chamber yang berisi fase gerak yang telah dijenuhkan,
lalu dielusi dengan jarak rambat 20 cm. Kertas diangkat dan dikeringkan. Hasil
disemprot dengan pereaksi AlCl3 5% dalam etanol dan diamati dibawah lampu
ultraviolet. Hasil kromatogram dengan KKt dari ekstrak etanol, fraksi n-heksana,
fraksi kloroform, fraksi etil asetat,fraksi air dapat dilihat pada lampiran 10 halaman
56-65.
3.10Pemisahan Senyawa Flavonoida Dari Fraksi Etil Asetat Dengan Cara Kromatografi Kertas Preparatif
Terhadap fraksi etil asetat dilakukan pemisahan secara kromatografi kertas
preparatif (KKt preparatif) dengan fase gerak asam asetat 50 % dan fase diam kertas
whatman No.3 dengan ukuran 15 x 15 cm.
Cara kerja :
Fraksi etil asetat yang telah diencerkan ditotolkan pada kertas berupa pita, kemudian
dimasukkan kedalam chamber berisi fase gerak yang telah dijenuhkan. Lalu dielusi
dengan jarak 20 cm, kertas diangkat, dan dikeringkan, diamati diabawah sinar
ultraviolet. Bercak diberi tanda dan digunting menjadi potongan kecil-kecil, direndam
dalam metanol selama 24 jam dan sekali-kali dikocok lalu disaring. Selanjutnya filtrat
dikumpulkan dan dipekatkan hingga diperoleh isolat kental. Isoalat kental yang
diperoleh dari hasil KKt preparatif dilakukan KKt kualitatif. Hasil kromatogram
dengan KKt preparatif dari fraksi etil asetat dapat dilihat pada lampiran 10 halaman
66.
3.11Uji Kermunian terhadap Senyawa Flavonoida Hasil Kromatografi Kertas Preparatif
Uji kemurnian terhadap isolat hasil isolasi dilakukan dengan cara:
1. Kromatografi kertas menggunakan berbagai fase gerak, yaitu: asam asetat
50%, BAW (n-butanol - asam asetat - air = 4 : 1 : 5), asam asetat 15 %, HCl
1% dengan penampak bercak aluminium klorida 5% b/v.
Cara kerja:
Isolat ditotolkan pada kertas Whatman No. 1 berukuran 3x25 cm,
kemudian dimasukkan ke dalam bejana kromatografi yang telah jenuh
dengan uap fase gerak dan dielusi dengan jarak rambat 20 cm. Selanjutnya
kertas dikeluarkan dan dikeringkan. Hasilnya dilihat di bawahsinar lampu
UV 366 nm dan dideteksi dengan penampak bercak aluminium klorida 5%
b/v, dan dilihat kembali dibawah sinar UV 366 nm.
2. Kromatografi kertas dua arah dengan memakai dua sistem fase gerak, fase
gerak I adalah BAW (n-butanol - asam asetat - air = 4 : 1 : 5) dan fase gerak
II adalah asam asetat 50% v/v.
Isolat ditotolkan pada kertas Whatman No. 3, kemudian dimasukkan
kedalam bejana kromatografi yang telah jenuh dengan uap fase gerak
pertama, lalu dielusi dengan jarak rambat 15 cm. Kertas dikeluarkan dan
dikeringkan selanjutnya dielusi kembali dengan fase gerak kedua, kemudian
kertas dikeluarkan dan dikeringkan. Hasilnya dilihat di bawah sinar lampu
UV 366 nm dan dideteksi dengan penampak bercak aluminium klorida 5%
dan dilihat kembali di bawah sinar lampu UV 366 nm. Hasil kromatogram
dengan KKt kualitatif isolat serta hasil kromatogram dengan KKt dua arah
dapat dilihat pada lampiran 10 halaman 67-77.
3.12Karakterisasi Hasil Isolasi
Karakterisasi senyawa hasil isolasi dilakukan dengan spektrofotometri
ultraviolet.
3.12.1 Karakterisasi Isolat dengan Spektrofotometri Ultraviolet dengan Penambahan Pereaksi Geser (Shift reagent)
1. Isolat dilarutkan dalam metanol, dimasukkan ke dalam kuvet dan
kemudian diukur absobansinya pada panjang gelombang 210-500 nm.
Setelah diukur spektrumnya dalam metanol, ditambahkan tiga tetes larutan
NaOH 2 N ke dalam kuvet dan direkam spektrumnya, kemudian direkam
kembali setelah 5 menit.
2. Larutan isolat ditambahkan enam tetes pereaksi AlCl3, dikocok dan diukur
spektrumnya, selanjutnya ditambahkan tiga tetes HCl dan diukur
spektrumnya.
3. Larutan isolat ditambahkan serbuk natrium asetat hingga kira-kira 2 mm
lapisan natrium asetat pada dasar kuvet dikocok dan diukur
spektrumnya.Spektrum natrium asetat diukur kembali setelah 5 menit. Ke
dalam kuvet ditambahkan serbuk asam borat anhidrat kira-kira setengah
dari serbuk natrium asetat dan dicampur, lalu diukur spektrum natrium
asetat/asam borat.
Spektrum dari isolat hasil isolasi dengan spektrofotometri UV
menggunakan pereaksi geser (shift reagen) dapat dilihat pada lampiran 11 halaman
BAB IV
HASIL DAN PEMBAHASAN
Hasil identifikasi tumbuhan yang dipakai sebagai penelitian di Lembaga Ilmu
Pengetahuan Indonesia, Pusat Penelitian Biologi, Bogor, menunjukkan identitas
sampel tumbuhan adalah Euphorbia hirta L. suku Euphorbiaceae.
Hasil pemeriksaan makroskopik simplisia herba patikan kebo menunjukkan
bahwa batang kecil panjang dan bulat, daun berhadapan dengan warna hijau tua
sampai hijau kelabu bentuk jorong meruncing sampai tumpul, bunga kecil, biji
berwarna coklat kemerahan, herba patikan kebo berbau lemah dan rasa agak pahit.
Hasil pemeriksaan mikroskopik serbuk simplisia herba patikan kebo menunjukkan
bahwa adanya rambut penutup, stomata tipe anomositik, saluran getah, fragmen kulit
buah, fragmen kulit biji dan berkas pembuluh.
Hasil karakteristik serbuk simplisia diperoleh kadar air 6,654%, kadar sari larut
dalam air 22,06%, kadar sari larut dalam etanol 18,36%, kadar abu total 1,074%, kadar
abu tidak larut dalam asam 0,12%. Hasil penapisan fitokimia serbuk simplisia
menunjukkan adanya golongan senyawa alkaloida, flavonida, saponin, tanin, glikosida
dan steroida/ triterpenoida dan glikosida antrakuinon. Hasil karakteristik serbuk
simplisia yang diteliti sesuai dengan persyaratan Materia Medika Indonesia (Ditjen
POM, 1978).
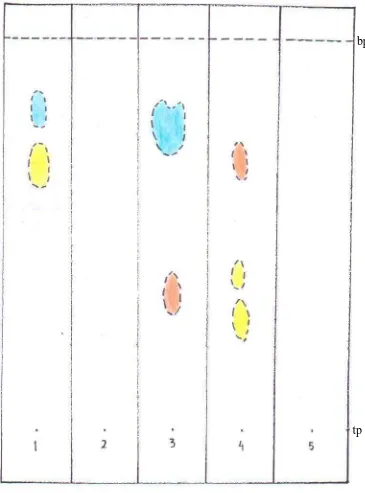
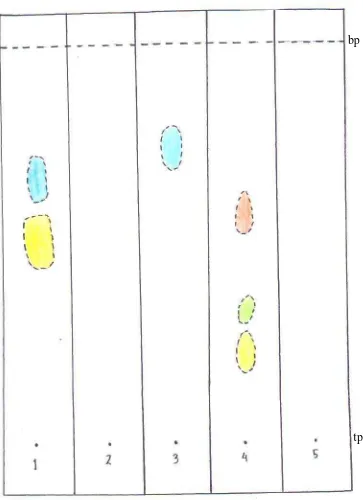
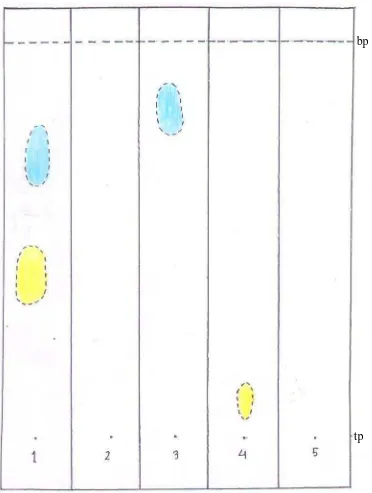
Hasil analisis kromatografi kertas (KKt) maka fraksi etil asetat ternyata
memberikan pemisahan yang terbaik. Dari lima fase gerak yaitu BAA, forestal, asam
asetat 50%, asam asetat 15%, HCl 1% dan sebagai fase diam kertas whatman no. 1
dengan penampak bercak digunakan sinar lampu ultravioelt (UV) dan AlCl3 5%
diperoleh pemisahan yang baik dengan fase gerak asam asetat 50%. Pada fraksi etil
asetat diperoleh tiga bercak dengan AlCl3/UV 366nm, yaitu warna kuning (Rf1 =
0,32) kuning hijau (Rf = 0,43) dan jingga (Rf = 0,71).