PENENTUAN PROFIL FARMAKOKINETIKA
DEKSAMETASON PADA KELINCI
(Oryctolagus cuniculus)
SKRIPSI
OLEH: MIRNAWATY NIM 091524071
PROGRAM EKSTENSI SARJANA FARMASI
FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA
MEDAN
PENENTUAN PROFIL FARMAKOKINETIKA
DEKSAMETASON PADA KELINCI
(Oryctolagus cuniculus)
SKRIPSI
Diajukan Untuk Melengkapi Salah Satu Syarat Untuk Memperoleh Gelar Sarjana Farmasi Pada Fakultas Farmasi
Universitas Sumatera Utara
OLEH: MIRNAWATY NIM 091524071
PROGRAM EKSTENSI SARJANA FARMASI
FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA
MEDAN
PENGESAHAN SKRIPSI
PENENTUAN PROFIL FARMAKOKINETIKA
DEKSAMETASON PADA KELINCI
(Oryctolagus cuniculus)
OLEH: MIRNAWATY NIM 091524071
Dipertahankan di Hadapan Panitia Penguji Fakultas Farmasi
Universitas Sumatera Utara Pada Tanggal: Agustus 2011
Disetujui Oleh:
Pembimbing I, Panitia Penguji
Dr. Edy Suwarso, S.U., Apt. Prof. Dr. Karsono, Apt. NIP 130935857 NIP 195409091982011001
Dr. Edy Suwarso, S.U., Apt. Pembimbing II, NIP 130935857
Prof. Dr. rer. nat. Effendy D. P, SU., Apt. Prof. Dr. M. T. Simanjuntak, Msc., Apt NIP 195306191983031001 NIP 195212041980021001
Dr. Kasmirul Ramlan Sinaga, M.S., Apt NIP 195504241983031003
Disahkan oleh:
Dekan Fakultas Farmasi,
KATA PENGANTAR
Segala Puji dan syukur penulis ucapkan kehadirat Tuhan yang Maha Kuasa yang telah melimpahkan kasih-Nya, sehingga penulis dapat melaksanakan penelitian dan menyelesaikan penulisan skripsi ini dengan baik. Skripsi ini yang merupakan salah satu syarat untuk memperoleh gelar sarjana farmasi pada Fakultas Farmasi Universitas Sumatera Utara.
Ucapan terima kasih dan penghargaan yang sebesar-besarnya kepada :
1. Ayahanda tercinta P. Situmorang dan Ibunda D. Sitinjak karena telah memberikan kasih sayangnya yang melimpah kepada penulis dan memberikan dukungan sehinggga penulis dapat menyelesaikan pendidikan Sarjana Farmasi.
2. Bapak Dr. Edy Suwarso, S.U., Apt dan bapak Prof. Dr. rer. nat. Effendy De Lux Putra, S.U., Apt, selaku pembimbing yang telah memberikan waktu, bimbingan, kesabaran dan petunjuk kepada penulis sehingga dapat menyelesaikan penyusunan skripsi ini.
3. Bapak Prof. Dr. Sumadio Hadisahputra, Apt., yang telah memberikan izin fasilitas sehingga penulis dapat menyelesaikan pendidikan.
4. Bapak Prof. Dr. Karsono, Apt., Prof. Dr. M. Timbul Simanjuntak Msc, Apt., dan Dr. Kasmirul Ramlan Sinaga M.S., Apt., selaku dosen penguji yang telah memberikan kritik saran dan arahan sehingga penulis dapat menyelesaikan skripsi ini.
semangat dan keceriaan sehinggga penulis dapat menyelesaikan penelitian dan penulisan skripsi ini.
6. Rekan-rekan lain yang tidak dapat saya sebutkan satu persatu yang memberikan dukungan, semangat, kritik dan saran kepada penulis selama penelitian dan penulisan skripsi ini.
Penulis menyadari sepenuhnya bahwa penulisan skripsi ini masih belum sempurna. Untuk itu dengan segala kerendahan hati penulis mengharapkan saran dan kritik yang bersifat membangun demi kesempurnaan skripsi ini. Akhir kata penulis berharap semoga skripsi ini dapat menjadi kontribusi yang bermanfaat bagi ilmu pengetahuan khususnya dibidang farmasi.
Medan, Agustus 2011 Penulis
ABSTRAK
Fase farmakokinetik berkaitan dengan masuknya zat aktif ke dalam tubuh. Pemasukan in vivo tersebut secara keseluruhan merupakan fenomena fisiko-kimia yang terpadu di dalam organ penerima obat. Penelitian ini bertujuan untuk mengetahui bagaimana profil farmakokinetika dari deksametason.
Untuk mendapatkan keadaan yang optimal, penelitian ini dilakukan dengan cara memberikan suspensi Deksametason baku kepada 6 ekor hewan kelinci jantan yang beratnya sekitar 1,5-2,0 kg dengan pemberian secara oral. Dan untuk mendapatkan kadar obat dalam darah pada masing-masing kelinci jantan maka darah diambil dengan selang waktu 0; 0,5; 0,75; 1,25; 1,75; 2,25; 3,25; 4,25; 5,25; 7,25; dan 9,25 jam. Lalu divortex dengan menggunakan Acetonitril dan disentrifuge. Pengukuran kadar obat Deksametason dalam plasma kelinci jantan dilakukan dengan menggunakan KCKT (Kromatografi Cair Kinerja Tinggi). Fase gerak yang digunakan untuk mengukur kadar Deksametason dalam plasma kelinci
jantan adalah asetonitril : air dengan perbandingan (45:55) dan laju alir 2 ml/menit.
Dari hasil penentuan parameter farmakokinetik Deksametason diketahui nilai rata-rata ± SD dari Ka 0,802 ± 0,054 jam-1 ; t1/2abs 0,867 ± 0,0556 jam ; AUC 0-∞ 105,152 ± 2,059 mcg/ml.jam ; AUMC0-∞ 555,98 ± 24,493 mcg/ml.jam2 ; MRT 5,285 ± 0,138 jam ; Cmaks 33,937 ± 2,103 mcg/ml ; Tmaks 1,848 ± 0,0694 jam ; Vd 17,2175 ± 0,8946 ml ; Kel 0,346 ± 0,016 jam-1 ; t1/2el 2,007 ± 0,096 jam ; klirens 5,947 ± 0,259 ml/jam.
ABSTRACT
Pharmacokinetic phase refers to the entrance substance to the body. The in vivo influx, overall, is a harmonious physico-chemical phenomenon in the drug receiving organ. This research objective is to know and assess the pharmacokinetic form of dexamethasone.
To obtain optimal condition, this research was done by giving standard dexamethasone suspense to six male rabbits, weight about 1.5-2.0 kg orally. And to get the value of drug blood level in each rabbit, then the blood was extracted in fixed time range 0; 0.5; 0.75; 1.25; 1.75; 2.25; 3.25; 4.25; 5.25; 7.25, and 9.25 hour. Then put in a vortex by using acetonitrile and centrifuged. The determination of the dexamethasone in male rabbit’s plasma was done using HPLC. The mobile phase used in measuring the level of dexamethasone in male rabbit plasma was acetonitrile : water ratio (45:55) and flow rate 2 ml/minute.
From the result of the determination of the pharmacokinetic parameter of dexamethasone mean is known ± deviation standard (SD) from Ka 0.802 ± 0.054 hour-1 ; t1/2abs 0.867 ± 0.0556 hour ; AUC 0-∞ 105.152 ± 2.059 mcg/ml.hour ; AUMC0-∞ 555.98 ± 24.493 mcg/ml.hour2 ; MRT 5.285 ± 0.138 hour ; Cmaks 33.937 ± 2.103 mcg/ml ; Tmaks 1.848 ± 0.0694 hour ; Vd 17.2175 ± 0.8946 ml ; Kel 0.346 ± 0.016 hour-1 ; t1/2el 2.007 ± 0.096 hour ; klirens 5.947 ± 0.259 ml/hour. Keywords : Dexamethasone, HPLC, The Pharmacokinetic Profile, Male Rabbit,
DAFTAR ISI
Halaman
JUDUL ... i
LEMBAR PENGESAHAN ... iii
KATA PENGANTAR ... iv
ABSTRAK ... vi
ABSTRACT ... vii
DAFTAR ISI ... viii
DAFTAR TABEL ... ix
DAFTAR GAMBAR ... x
DAFTAR LAMPIRAN ... xi
BAB I PENDAHULUAN ... 1
1.1 Latar Belakang ... 1
1.2 Perumusan Masalah ... 4
1.3 Hipotesis ... 4
1.4 Tujuan Penelitian ... 4
1.5 Manfaat Penelitian... 4
BAB II TINJAUAN PUSTAKA ... 5
2.1 Deksametason ... 5
2.1.1 Rumus Bangun ... 5
2.2 Nasib Obat Dalam Badan ... 8
2.3 Farmakokinetika ... 9
2.4 Kromatografi Cair Kinerja Tinggi (KCKT) ... 17
BAB III METODE PENELITIAN ... 19
3.1 Alat ... 19
3.2 Bahan-bahan ... 19
3.3 Pengambilan sampel ... 20
3.4 Rancangan Penelitian ... 20
3.4.1 Penyiapan Bahan ... 20
3.4.1.1 Pembuatan Fase Gerak ... 20
3.4.1.2 Pembuatan Pelarut ... 20
3.4.1.3 Pembuatan LIB deksametason (250 mcg/ml)... 20
3.4.1.4 Pembuatan Suspensi Deksametason ... 21
3.4.1.5 Analisis Kualitatif ... 21
3.4.1.6 Pengambilan sampel darah untuk kurva baku ... 21
3.4.1.7 Penetapan kadar deksametason dalam plasma kelinci ... 22
BAB IV HASIL DAN PEMBAHASAN ... 24
BAB V KESIMPULAN DAN SARAN ... 31
5.1 Kesimpulan ... 31
5.2 Saran ... 31
DAFTAR PUSTAKA ... 33
DAFTAR TABEL
Halaman
Tabel 4.1 Hasil penyuntikan kurva baku deksametason dalam plasma ……… 25 Tabel 4.2 Konsentrasi rata-rata ± SD deksametason dalam plasma kelinci
terhadap waktu……….….. 27 Tabel 4.3 Nilai parameter farmakokinetik deksametason ± SD dalam plasma
DAFTAR GAMBAR
Halaman
Gambar 4.1 Kromatogram deksametason BPFI dengan konsentrasi 250 mcg/ml, dengan fase gerak asetonitril-air (45:55) dan laju
alir 2 ml/menit ... .. 24 Gambar 4.2 Kromatogram deksametason BPFI dalam plasma dengan
konsentrasi 100 mcg/ml, dengan fase gerak asetonitril-air
(45:55) dan laju alir 2 ml/menit ... .. 25 Gambar 4.3 Kurva kalibrasi deksametason dengan konsentrasi vs luas
area puncak deksametason ... .. 26 Gambar 4.4 Konsentrasi rata-rata (log c) vs waktu (t=jam) deksametason
DAFTAR LAMPIRAN
Halaman
Lampiran 1. Hasil orientasi gambar dengan menggunakan alat KCKT... 36
Lampiran 2. Kromatogram Deksametason dalam plasma... 37
Lampiran 3. Sertifikat pengujian Deksametason BPFI... 40
Lampiran 4. Perhitungan persamaan regresi dan kurva kalibrasi deksametason yang diperoleh secara KCKT pada λ 241nm... 41
Lampiran 5. Konversi perhitungan dosis antar jenis hewan dan perhitungan dosis yang diberikan kepada masing-masing hewan percobaan... 43
Lampiran 6. Kadar deksametason dalam plasma pada sampling time... 44
Lampiran 7. Grafik konsentrasi (log c) vs waktu (t=jam) deksametason dalam plasma... 45
Lampiran 8. Parameter farmakokinetik deksametason ± SD... 46
Lampiran 9. Contoh perhitungan parameter farmakokinetik secara manual... 47
ABSTRAK
Fase farmakokinetik berkaitan dengan masuknya zat aktif ke dalam tubuh. Pemasukan in vivo tersebut secara keseluruhan merupakan fenomena fisiko-kimia yang terpadu di dalam organ penerima obat. Penelitian ini bertujuan untuk mengetahui bagaimana profil farmakokinetika dari deksametason.
Untuk mendapatkan keadaan yang optimal, penelitian ini dilakukan dengan cara memberikan suspensi Deksametason baku kepada 6 ekor hewan kelinci jantan yang beratnya sekitar 1,5-2,0 kg dengan pemberian secara oral. Dan untuk mendapatkan kadar obat dalam darah pada masing-masing kelinci jantan maka darah diambil dengan selang waktu 0; 0,5; 0,75; 1,25; 1,75; 2,25; 3,25; 4,25; 5,25; 7,25; dan 9,25 jam. Lalu divortex dengan menggunakan Acetonitril dan disentrifuge. Pengukuran kadar obat Deksametason dalam plasma kelinci jantan dilakukan dengan menggunakan KCKT (Kromatografi Cair Kinerja Tinggi). Fase gerak yang digunakan untuk mengukur kadar Deksametason dalam plasma kelinci
jantan adalah asetonitril : air dengan perbandingan (45:55) dan laju alir 2 ml/menit.
Dari hasil penentuan parameter farmakokinetik Deksametason diketahui nilai rata-rata ± SD dari Ka 0,802 ± 0,054 jam-1 ; t1/2abs 0,867 ± 0,0556 jam ; AUC 0-∞ 105,152 ± 2,059 mcg/ml.jam ; AUMC0-∞ 555,98 ± 24,493 mcg/ml.jam2 ; MRT 5,285 ± 0,138 jam ; Cmaks 33,937 ± 2,103 mcg/ml ; Tmaks 1,848 ± 0,0694 jam ; Vd 17,2175 ± 0,8946 ml ; Kel 0,346 ± 0,016 jam-1 ; t1/2el 2,007 ± 0,096 jam ; klirens 5,947 ± 0,259 ml/jam.
ABSTRACT
Pharmacokinetic phase refers to the entrance substance to the body. The in vivo influx, overall, is a harmonious physico-chemical phenomenon in the drug receiving organ. This research objective is to know and assess the pharmacokinetic form of dexamethasone.
To obtain optimal condition, this research was done by giving standard dexamethasone suspense to six male rabbits, weight about 1.5-2.0 kg orally. And to get the value of drug blood level in each rabbit, then the blood was extracted in fixed time range 0; 0.5; 0.75; 1.25; 1.75; 2.25; 3.25; 4.25; 5.25; 7.25, and 9.25 hour. Then put in a vortex by using acetonitrile and centrifuged. The determination of the dexamethasone in male rabbit’s plasma was done using HPLC. The mobile phase used in measuring the level of dexamethasone in male rabbit plasma was acetonitrile : water ratio (45:55) and flow rate 2 ml/minute.
From the result of the determination of the pharmacokinetic parameter of dexamethasone mean is known ± deviation standard (SD) from Ka 0.802 ± 0.054 hour-1 ; t1/2abs 0.867 ± 0.0556 hour ; AUC 0-∞ 105.152 ± 2.059 mcg/ml.hour ; AUMC0-∞ 555.98 ± 24.493 mcg/ml.hour2 ; MRT 5.285 ± 0.138 hour ; Cmaks 33.937 ± 2.103 mcg/ml ; Tmaks 1.848 ± 0.0694 hour ; Vd 17.2175 ± 0.8946 ml ; Kel 0.346 ± 0.016 hour-1 ; t1/2el 2.007 ± 0.096 hour ; klirens 5.947 ± 0.259 ml/hour. Keywords : Dexamethasone, HPLC, The Pharmacokinetic Profile, Male Rabbit,
BAB I PENDAHULUAN
1.1Latar Belakang
Fase farmakokinetik berkaitan dengan masuknya zat aktif ke dalam tubuh. Pemasukan in vivo tersebut secara keseluruhan merupakan fenomena fisikokimia yang terpadu di dalam organ penerima obat. Fase farmakokinetik ini merupakan salah satu unsur penting yang menentukan profil keberadaan zat aktif pada tingkat biofase dan selanjutnya menentukan aktivitas terapeutik obat (Aiache, 1993).
Aktivitas serta toksisitas suatu obat tergantung pada lama keberadaan dan perubahan zat aktif didalam tubuh (Aiache, 1993). Menurut Shargel (1988), bahwa intensitas efek farmakologik atau efek toksik suatu obat seringkali dikaitkan dengan konsentrasi obat pada reseptor, yang biasanya terdapat dalam sel-sel jaringan. Oleh karena sebagian besar sel-sel jaringan diperfusi oleh cairan jaringan atau plasma, maka pemeriksaan kadar obat dalam plasma merupakan suatu metode yang sesuai untuk pemantauan pengobatan.
Pemantauan konsentrasi obat dalam darah atau plasma meyakinkan bahwa dosis yang telah diperhitungkan benar-benar telah melepaskan obat dalam plasma dalam kadar yang diperlukan untuk efek terapetik. Dengan demikian pemantauan konsentrasi obat dalam plasma memungkinkan untuk penyesuaian dosis obat secara individual dan juga untuk mengoptimasi terapi (Shargel, 1988).
farmakokinetik yang kemudian diuji kebenarannya, dan selanjutnya diperoleh parameter-parameter farmakokinetiknya (Shargel, 1988).
Model farmakokinetik sendiri dapat memberikan penafsiran yang lebih teliti tentang hubungan kadar obat dalam plasma dan respons farmakologik. Model kompartemen satu terbuka menganggap bahwa berbagai perubahan kadar obat dalam plasma mencerminkan perubahan yang sebanding dengan kadar obat dalam jaringan. Tetapi model ini tidak menganggap bahwa konsentrasi obat dalam tiap jaringan tersebut adalah sama dengan berbagai waktu. Disamping itu, obat didalam tubuh juga tidak ditentukan secara langsung, tetapi dapat ditentukan konsentrasi obatnya dengan menggunakan cuplikan cairan tubuh (Shargel, 1988). Saat ini telah tersedia data farmakokinetik obat, yang meliputi berbagai parameter farmakokinetik, yaitu bioavailabilitas oral, volume distribusi, waktu paruh dan bersihan (clearance) dalam keadaan fisiologik maupun patologik. Dimana kondisi fisiologik dan kondisi patologik ini dapat menimbulkan perubahan pada parameter farmakokinetik obat (Setiawati, 2007).
Data farmakokinetik ini sangat penting untuk semua jenis obat terutama untuk obat yang lazim dikonsumsi masyarakat. Karena kemungkinan besar konsumsi obat yang terlalu sering akan menimbulkan toksisitas serta efek samping yang beresiko terhadap kelanjutan penyakit. Menurut Setiawati (2007), prinsip dan data farmakokinetik sangatlah penting diketahui oleh seorang dokter agar dapat menetapkan regimen dosis yang optimal bagi masing-masing pasien dengan berpedoman pada kadar obat dalam plasma atau serum.
oleh Widodo, dkk (1993), dengan perolehan data farmakokinetik sebagai berikut ; Vd = 0,8 L/kg, ketersediaan biologik = 80%, waktu paruh = 3 jam, eliminasi sekitar 3% terjadi direnal tanpa diubah, sisanya dimetabolisme didalam hati.
Menurut hasil penelitian Robert and William (1987), diperoleh data farmakokinetik deksametason sebagai berikut ; availabilitas oral (%) 78 ± 14, ekskresi urin (%) 2,6 ± 0,6, ikatan protein plasma (%) 68 ± 3, klirens (ml.min-1.kg-1) 3,7 ± 0,9, t1/2 (jam) 3,0 ± 0,8.
Dari data hasil penelitian sebelumnya telah diketahui data farmakokinetik deksametason. Namun penelitian tersebut hanya menggunakan produk jadi deksametason yang beredar dipasaran baik dalam bentuk tablet, injeksi maupun sediaan tetes mata. Dan belum pernah ada penelitian serta data yang menggunakan baku murni deksametason untuk ditetapkan profil farnakokinetiknya.
1.2Perumusan Masalah
Berdasarkan latar belakang diatas, maka yang menjadi perumusan masalah dalam penelitian ini adalah apakah bentuk dan model kompartemen yang berkaitan dengan profil farmakokinetika Deksametason ?
1.3Hipotesis
Berdasarkan perumusan masalah diatas, maka yang menjadi hipotesis dalam penelitian ini adalah profil farmakokinetika Deksametason mengikuti salah satu model kompartemen yang terdapat pada farmakokinetika.
1.4Tujuan Penelitian
Berdasarkan hipotesis di atas, maka yang menjadi tujuan penelitian ini adalah untuk mengetahui bentuk dan model kompartemen serta profil farmakokinetika dari Deksametason.
1.5Manfaat Penelitian
BAB II
TINJAUAN PUSTAKA
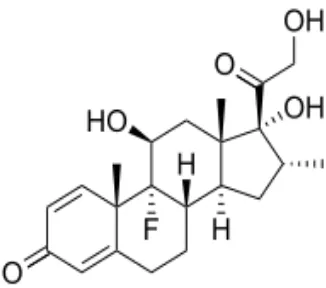
2.1 Deksametason 2.1.1 Rumus Bangun
[image:19.595.209.372.223.367.2]
Gambar 1. Struktur kimia Deksametason 2.1.2 Sifat Fisikokimia
Rumus molekul : C22H29FO5 Berat molekul : 392,47
Nama kimia : 9-Fluoro-11β,17,21-trihidroksi-16α -metilpregna-1,4-diena-3,20-dion
Pemerian : Serbuk hablur, putih sampai praktis putih, tidak berbau, stabil diudara. Melebur pada suhu lebih kurang 250º disertai peruraian Kelarutan : Praktis tidak larut dalam air, agak sukar larut
Deksametason, seperti kortikosteroid lainnya memiliki efek anti inflamasi dan anti alergi dengan pencegahan pelepasan histamine (Anonim1,2009). Deksametason merupakan salah satu kortikosteroid sintetis terampuh. Kemampuannya dalam menaggulangi peradangan dan alergi kurang lebih sepuluh kali lebih hebat dari pada yang dimiliki prednisone (Katzung, 1998). Penggunaan deksametason di masyarakat sering kali kita jumpai, antara lain: pada terapi arthritis rheumatoid, systemik lupus erithematosus, rhinitis alergika, asma, leukemia, lymphoma, anemia hemolitik atau auto immune, selain itu deksametason dapat digunakan untuk menegakkan diagnosis sindroma cushing. Efek samping pemberian deksametason antara lain terjadinya insomnia, osteoporosis, retensi cairan tubuh, glaukoma dan lain-lain ( Suherman, 2007).
Kegunaan kortikosteroid pada gangguan fungsi adrenal merupakan suatu fungsi kemampuan mereka untuk menekan respons inflamasi dan imun. Pada kasus dengan respons inflamasi atau imun, penting dalam mengontrol proses patologis, terapi dengan kortikosteroid dapat berbahaya, tetapi dipertimbangkan untuk mencegah kerusakan yang tidak dapat diperbaiki dari suatu respons inflamasi jika digunakan dalam hubungannya dengan terapi khusus untuk proses penyakit tersebut (Katzung, 2002).
Kortikosteroid seperti deksametason bekerja dengan cara mempengaruhi kecepatan sintesis protein. Molekul hormon memasuki sel jaringan melalui membran plasma secara difusi pasif di jaringan target, kemudian bereaksi dengan reseptor protein yang spesifik dalam sitoplasma sel jaringan dan membentuk kompleks reseptor steroid. Kompleks ini mengalami perubahan konformasi, lalu bergerak menuju nukleus dan berikatan dengan kromatin. Ikatan ini menstimulasi transkripsi RNA dan sintesis protein spesifik. Induksi sintesis protein ini merupakan perantara efek fisiologik steroid ( Suherman, 2007).
Kortisol dan analog sintetiknya pada pemberian oral diabsorpsi cukup baik. Glukokortikoid dapat diabsorpsi melalui kulit, sakus konjungtiva dan ruang sinovial. Metabolitnya merupakan senyawa inaktif atau berpotensi rendah. Setelah penyuntikan IV, sebagian besar dalam waktu 72 jam diekskresi dalam urin, sedangkan di feses dan empedu hampir tidak ada. Diperkirakan paling sedikit
70% kortisol yang diekskresi mengalami metabolisme di hepar ( Suherman, 2007).
Efek terapeutik glukokortikoid seperti deksametason yang paling penting adalah kemampuannya untuk mengurangi respons peradangan secara dramatis dan untuk menekan imunitas. Telah diketahui bahwa penurunan dan penghambatan limfosit dan makrofag perifer memegang peranan. Juga penghambatan fosfolipase A2 secara tidak langsung yang menghambat pelepasan asam arakidonat, prekursor prostaglandin dan leukotrien, dari fosfolipid yang terikat pada membran (Mycek, 2001).
beradang (Daniel dan Tino, 2002). Deksametason (dexamethasone) merupakan glukokortikoid sintetis yang memiliki efek antiinflamasi, antialergi, antirematik, dan antishock yang sangat kuat (Anonim2, 2010). Menurut Suherman (2007), penggunaan klinik kortikosteroid sebagai antiinflamasi merupakan terapi paliatif, dalam hal ini penyebab penyakit tetap ada hanya gejalanya yang dihambat. Hal inilah yang menyebabkan obat ini banyak digunakan untuk berbagai penyakit, bahkan disebut sering disebut life saving drugs, tetapi juga mungkin menimbulkan reaksi yang tidak diinginkan.
2.2 Nasib Obat Dalam Badan
2.3 Farmakokinetika
Farmakokinetika dapat didefinisikan sebagai setiap proses yang dilakukan tubuh terhadap obat, yaitu absorpsi, distribusi, metabolisme, dan ekskresi. Dalam arti sempit farmakokinetika khususnya mempelajari perubahan-perubahan konsentrasi dari obat dan metabolitnya di dalam darah dan jaringan sebagai fungsi dari waktu (Tjay dan Rahardja, 2002).
Profil keberadaan bahan obat dalam darah sebagai fungsi dari waktu menggambarkan interaksi antara fase ketersediaan zat aktif dan fase disposisinya. Selain itu profil tersebut juga mengungkapkan nasib obat di dalam tubuh. Oleh karena fenomena penyerapan zat aktif dari darah menuju jaringan dapat terjadi secara bolak-balik (reversible), maka selalu terjadi hubungan dinamik antara konsentrasi zat aktif dalam jaringan dan konsentrasi zat aktif dalam darah (Aiache, 1993).
Absorpsi sistemik suatu obat dari saluran cerna atau tempat ekstravaskular yang lain bergantung pada bentuk sediaan, anatomi dan fisiologi tempat absorpsi. Faktor-faktor seperti luas permukaan dinding usus, kecepatan pengosongan lambung, pergerakan saluran cerna dan aliran darah ke tempat absorpsi, semuanya mempengaruhi laju dan jumlah absorpsi obat (Shargel, 2005).
membran dan pentingnya kelarutan atau keterlarutan zat aktif padat (Aiache, 1993).
Absorpsi obat ini melalui saluran cerna berlangsung cepat, dan mengalami metabolisme dihati menjadi bentuk inaktif (Anonim2, 2010). Menurut Widodo (1993), ikatan protein plasma deksametason yaitu 70% (pada dosis yang lebih tinggi lebih kecil), terikat pada transcortin (afinitas tinggi, kapasitas kecil) dan pada albumin (afinitas rendah, kapasitas besar).
Informasi tentang kecepatan dan tingkat absorpsi obat jarang mempunyai kepentingan klinis. Namun, absorpsi biasanya terjadi selama dua jam pertama setelah dosis obat dan bervariasi menurut asupan makanan, posisi tubuh dan aktivitas. Oleh karena itu tidak boleh mengambil darah sebelum absorpsi lengkap (kira-kira 2 jam setelah dosis oral) (Holford, 1998).
Proses-proses absorpsi, distribusi dan eliminasi (metabolisme dan ekskresi) yang dialami oleh hampir semua obat pada dosis terapi mengikuti kinetika orde pertama (first order), artinya kecepatan proses-proses tersebut sebanmding dengan jumlah obat yang ada (yang tinggal). Jadi jumlah obat yang diabsorpsi, distribusi dan dieliminasi persatuan waktu makin lama makin sedikit, sebanding dengan jumlah obat yang masih belum mengalami proses tersebut (Setiawati, 2005).
Obat harus dapat melewati berbagai membran sel (misalnya sel usus halus, pembuluh darah, dan sel saraf ) (Shargel, 2005).
Penyebaran zat aktif tergantung pada berbagai parameter, terutama sifat fisiko-kimia molekul obat. Dengan demikian proses penyerapan zat aktif terjadi apabila sebelumnya sudah dibebaskan dari sediaan dan sudah melarut dalam cairan biologi setempat. Tahap pelepasan dan pelarutan zat aktif merupakan tahap penentu pada proses penyerapan zat aktif, baik dalam jumlah yang diserap maupun laju penyerapannya (Aiache, 1993).
Pada distribusinya khususnya melalui peredaran darah, obat yang telah melalui hati bersamaan dengan metabolitnya disebarkan secara merata ke seluruh jaringan tubuh. Melalui kapiler dan cairan ekstrasel (yang mengelilingi jaringan) obat diangkut ke tempat kerjanya didalam sel (cairan intrasel), yaitu organ atau otot yang sakit. Tempat kerja ini hendaknya memiliki penyaluran darah yang baik karena obat hanya dapat melakukan aktivitasnya bila konsentrasi setempatnya cukup tinggi selama waktu yang cukup lama ( Tjay dan Rahardja, 2002).
Pada tahap distribusi ini penyebarannya sangat peka terhadap berbagai pengaruh yang terkait dengan tahap penyerapan dan tahap yang terjadi sesudahnya yaitu peniadaan, serta terkait pula dengan komposisi biokimia serta keadaaan fisiopatologi subyeknya, disamping itu perlu diingat kemungkinan adanya interaksi dengan molekul lainnya. Pada tahap ini merupakan fenomena dinamik yang selalu terdiri dari fase peningkatan dan penurunan kadar zat aktif (Aiache, 1993).
paru-paru, dan jaringan lainnnya). Di dalam lever terdapat enzim khusus yaitu sitokrom P-450 yang akan mengubah obat menjadi bentuk metabolitnya. Metabolit umumnya menjadi lebih larut dalam air (polar) dan akan dengan cepat diekskresi ke luar tubuh melalui urin, feses, keringat, dan lain-lain. Hal ini akan secara dramatik mempengaruhi kadar obat dalam plasma dimana obat yang mengalami first pass metabolism akan kurang bioavailabilitasnya sehingga efek yang dihasilkan juga berkurang (Hinz, 2005).
Efektivitas suatu senyawa obat pada pemakaian klinik berhubungan dengan farmakokinetikanya. Efek obat terhadap tubuh dasarnya merupakan akibat interaksi obat dengan reseptornya, maka secara teoretis intensitas efek obat baik efek terapi maupun efek toksik tergantung dari kadar obat di tempat reseptor atau tempat kerjanya. Oleh karena kadar obat di tempat kerja belum dapat diukur, maka sebagai gantinya diambil kadar obat dalam plasma/serum yang umum dalam keseimbangan dengan kadarnya di tempat kerja (Setiawati, 2005).
Pada umumnya zat aktif suatu obat akan menunjukkan efek farmakologik pada titik tangkap jaringan bila bahan tersebut telah mencapai tempat tersebut dengan perantaraan darah. Peredaran darah bagaikan ”lempeng berputar” dari perjalanan obat. Fenomena penyerapan sebagai tahap awal farmakokinetika, ditentukan oleh penembusan zat aktif ke dalam darah yang selanjutnya oleh darah dihantarkan menuju sasaran kerja farmakologik, mengalami perubahan hayati dan selanjutnya ditiadakan (Aiache, 1993).
Tipe metabolisme dibedakan menjadi dua bagian yaitu Nonsynthetic Reactions (Reaksi Fase I) dan Synthetic Reactions (Reaksi Fase II). Reaksi fase I
lebih aktif dari senyawa asalnya. Umumnya tidak dieliminasi dari tubuh kecuali dengan adanya metabolisme lebih lanjut. Reaksi fase II berupa konjugasi (glukoronidasi dan sulfatasi) yaitu penggabungan suatu obat dengan suatu molekul lain. Metabolit umumnya lebih larut dalam air dan mudah diekskresikan (Hinz, 2005).
Faktor yang mempengaruhi metabolisme obat yaitu induksi enzim yang dapat meningkatkan kecepatan biotransformasi dirinya sendiri, atau obat lain yang dimetabolisme oleh enzim yang sama yang dapat menyebabkan toleransi. Selain itu, inhibisi enzim yang merupakan kebalikan dari induksi enzim, biotransformasi obat diperlambat, menyebabkan bioavailabilitasnya meningkat, menimbulkan efek menjadi lebih besar dan lebih lama. Kompetisi (interaksi obat) juga berpengaruh terhadap metabolisme dimana terjadi oleh obat yang dimetabolisir oleh sistem enzim yang sama. Perbedaan individu juga berpengaruh terhadap metabolisme karena adanya genetic polymorphism, dimana seseorang mungkin memiliki kecepatan metabolisme berbeda untuk obat yang sama (Hinz, 2005).
Pengeluaran obat atau metabolitnya dari tubuh, terutama dilakukan oleh ginjal melalui air seni disebut ekskresi. Lazimnya tiap obat di ekskresi berupa metabolitnya dan hanya sebagian kecil dalam keadaan asli yang utuh. Tapi adapula beberapa cara lain, yaitu melalui kulit bersama keringat, paru-paru melalui pernapasan, melalui hati dengan empedu (Tjay dan Rahardja, 2002).
efek obat tergantung pada konsentrasinya di target site dan ini berhubungan erat dengan konsentrasi plasma (Waldon, 2008).
Turunnya kadar plasma obat dan lama efeknya tergantung pada kecepatan metabolisme dan ekskresi. Kedua faktor ini menentukan kecepatan eliminasi obat yang dinyatakan dengan pengertian plasma half life eliminasi (waktu paruh = t1/2) yaitu rentang waktu dimana kadar obat dalam plasma pada fase eliminasi menurun sampai separuihnya. Kecepatan eliminasi obat dan plasma t1/2-nya tergantung dari kecepatan biotransformasi dan ekskresi. Obat dengan metabolisme cepat half life-nya juga pendek. Sebaliknya zat yang tidak mengalami boitransformasi atau yang diresorpsi kembali oleh tubuli ginjal, dengan sendirinya t1/2-nya panjang (Waldon, 2008).
Dasar-Dasar Perhitungan Farmakokinetika
Hal-hal yang penting dalam rangka penelitian farmakokinetika untuk parameter-parameter tertentu adalah :
a. Bioavailability (BA, Ketersediaan Hayati)
b. Volume distribusi (Vd)
Volume distribusi (Vd) menunjukkan volume penyebaran obat dalam tubuh dengan kadar plasma atau serum. Vd tidak perlu menunjukkan volume penyebaran obat yang sesungguhnya ataupun volume secara anatomik, tetapi hanya volume imajinasi dimana tubuh dianggap sebagai 1 kompartemen yang terdiri dari plasma atau serum, dan Vd menghubungkan jumlah obat dalam tubuh dengan kadarnya dalam plasma atau serum (Setiawati, 2005).
Vd = jumlah obat didalam tubuh C
Volume distribusi yang diperoleh mencerminkan suatu keseimbangan antara ikatan pada jaringan, yang mengurangi konsentrasi plasma dan membuat nilai distribusi lebih besar, dengan ikatan pada protein plasma, yang meningkatkan konsentrasi plasma dan membuat volume distribusi menjadi lebih kecil. Perubahan-perubahan dalam ikatan dengan jaringan ataupun dengan plasma dapat mengubah volume distribusi yang ditentukan dari pengukuran-pengukuran konsentrasi plasma (Holford, 1998).
c. Tetapan laju eliminasi dan waktu paruh dalam plasma
Waktu paruh dalam plasma adalah waktu dimana konsentrasi obat dalam darah (plasma) menurun hingga separuh nilai seharusnya. Pengukuran t½ memungkinkan perhitungan konstanta laju eliminasi dengan rumus :
Kel = 0,693 t½
plasma. Waktu paruh merupakan besaran farmakkokinetika yang sangat penting. Waktu paruh memberi dasar untuk perhitungan dosis pada pemakaian ulang bahan obat, pada setiap terapi jangka panjang (Mutschler, 1991).
d. Konsentrasi maksimum (Cmaks)
Konsentrasi plasma puncak menunjukkan konsentrasi obat maksimum dalam plasma setelah pemberian secara oral. Untuk beberapa obat diperoleh suatu hubungan antara efek farmakologi suatu obat dan konsentrasi obat dalam plasma. Konsentrasi plasma puncak memberi suatu petunjuk bahwa obat cukup diabsorpsi secara sistemik untuk memberi suatu respons terapetik. Selain itu konsentrasi plasma puncak juga memberi petunjuk dari kemungkinan adanya kadar toksik obat (Shargel, 2005).
e. Area Under Curve (AUC)
Area Under Curve (AUC) adalah permukaan di bawah kurva (grafik) yang menggambarkan naik turunnya kadar plasma sebagai fungsi dari waktu. AUC dapat dihitung secara matematis dan merupakan ukuran untuk bioavailabilitas suatu obat. AUC dapat digunakan untuk membandingkan kadar masing-masing plasma obat bila penentuan kecepatan eliminasinya tidak mengalami perubahan. Selain itu antara kadar plasma puncak dan bioavailabilitas terdapat hubungan langsung (Tjay dan Rahardja, 2002).
f. Waktu konsentrasi plasma puncak (tmaks)
yang lebih lambat. Harga tmaks menjadi lebih kecil (berarti sedikit waktu yang diperlukan untuk mencapai konsentrasi plasma puncak) bila laju absorpsi obat menjadi lebih cepat (Shargel, 2005).
g. Klirens
Klirens suatu obat adalah suatu ukuran eliminasi obat dari tubuh tanpa mempermasalahkan mekanisme prosesnya. Umumnya jaringan tubuh atau organ dianggap sebagai suatu kompartemen cairan dengan volume terbatas (volume distribusi) dimana obat terlarut didalamnya (Shargel, 2005).
2.4 Kromatografi Cair Kinerja Tinggi (KCKT)
Kromatografi didefenisikan sebagai prosedur pemisahan zat terlarut oleh suatu proses migrasi diferensial dinamis dalam sistem yang terdiri dari dua fase atau lebih, salah satu diantaranya bergerak secara berkesinambungan dalam arah tertentu dan didalamnya zat–zat itu menunjukkan perbedaan mobilitas disebabkan adanya perbedaan dalam adsorbsi, partisi, kelarutan, tekanan uap, ukuran molekul atau kerapatan muatan ion. Teknik kromatografi umum membutuhkan zat terlarut terdistribusi diantara dua fase, satu diantaranya diam (fase diam), yang lainnya bergerak (fase gerak). Fase gerak membawa zat terlarut melalui media, sehingga zat tersebut terpisah dari zat terlarut lain, yang terelusi lebih awal atau lebih akhir. Umumnya zat terlarut dibawa melewati media pemisah oleh aliran suatu pelarut berbentuk cairan atau gas yang disebut eluen (Depkes RI, 1995).
operasional seperti jenis kolom, fase gerak, panjang dan diameter kolom, kecepatan alir fase gerak, suhu kolom, dan ukuran sampel (Rohman, 2007).
Metode KCKT merupakan metode yang sangat populer untuk menetapkan kadar senyawa obat baik dalam beuntuk sediaan atau dalam sampel hayati. Hal ini disebabkan KCKT merupakan metode yang memberikan sensitifitas dan spesifitas yang tinggi (Rohman, 2007).
BAB III
METODE PENELITIAN
Penelitian ini merupakan penelitian deskriptif dan pengukuran dilakukan dengan menggunakan alat Kromatografi Cair Kinerja Tinggi (KCKT). Penelitian ini dilakukan di Laboratorium Farmakologi dan di Laboratorium Penelitian Fakultas Farmasi USU.
3.1 Alat
Alat-alat yang digunakan pada penelitian ini adalah timbangan, beaker gelas, neraca analitis (Baeco), pipet tetes, tabung sentrifugasi, rak tabung, gelas ukur, alat vortex (Baeco Germany), alat sentrifugasi (Health HC 1120T), termos es, spuit 1 ml, spuit 3 ml, politube, labu tentukur, batang pengaduk, vial 10 ml, satu unit alat KCKT Agilent 1120 Compact LC, kolom ODS, wadah solven, injektor, syringe 50 µ l, pompa vakum (Gast DOA-PG04-BN), sonifikator (Branson 1510), kertas membran filter whatman cellulosa nitrate 0,45 µm, kertas membran filter PTFE 0,5 µm, penyaring PTFE 0,2 µm.
3.2 Bahan
3.3 Pengambilan Sampel
Hewan uji yang digunakan dalam penelitian ini adalah kelinci jantan dengan berat 1,5-2,0 kg, yang telah dikondisikan selama 1 minggu dan diberi makanan kangkung selama penelitian berlangsung. Kelinci yang diambil darahnya adalah kelinci yang telah diberi suspensi deksametason secara oral. Waktu pengambilan darah adalah 0,5 jam setelah pemberian obat. Data hasil pengukuran plasma dapat dilihat pada lampiran.
3.4 Rancangan Penelitian 3.4.1 Penyiapan Bahan
3.4.1.1 Pembuatan Fase Gerak
Fase gerak terdiri dari campuran air dan asetonitril dengan perbandingan 55:45. Fase gerak dibuat sebanyak 500 ml dengan mencampurkan asetonitril sebanyak 225 ml dan air sebanyak 275 ml. Sebelum digunakan fase gerak disaring melalui penyaring PTFE. Kemudian diawaudarakan selama ± 20 menit menggunakan sonifikator (Hemanth, 2004).
3.4.1.2 Pembuatan Pelarut
Pelarut dibuat secara kuantitatif dari metanol dan aquabidest dengan perbandingan 1:1. Pelarut lalu disaring dengan milipore 0,45 μm, kemudian
diawaudarakan selama ± 20 menit menggunakan sonifikator.
fase gerak sampai garis tanda sehingga diperoleh larutan dengan konsentrasi 250 mcg/ml, disaring dan filtratnya digunakan sebagai larutan induk.
3.4.1.4 Pembuatan Suspensi Deksametason
Ditimbang 500 mg CMC Na, kemudian taburkan diatas lumpang yang telah berisi 20 ml air panas. Diamkan selama 15 menit hingga CMC Na mengembang. Setelah mengembang gerus CMC Na, lalu masukkan deksametason sebanyak 50 mg, gerus hingga homogen. Kemudian tambahkan aquadest sedikit demi sedikit sampai massa tercampur rata. Lalu cukupkan volumenya hingga 100 ml.
3.4.1.5 Analisis Kualitatif
Analisis kualitatif Deksametason dapat dilakukan dengan membandingkan waktu tambat yang sama dari kromatogram pada penyuntikan sampel dengan kromatogram pada penyuntikan larutan baku pembanding Deksametason.
3.4.1.6 Pengambilan Sampel Darah Untuk Kurva Baku
Ambil darah kelinci jantan lebih kurang 15 ml dari vena marginal telinga kelinci, dimasukkan kedalam tabung yang sudah berisi 2 tetes heparin. Siapkan 5 buah tabung dan masing-masing tabung dimasukkan Larutan Induk Baku Deksametason dengan konsentrasi :
1. Tabung pertama dimasukkan LIBD dengan konsentrasi 10 mcg/ml (0,1 ml) kemudian dicukupkan dengan darah ad 2,5 ml.
2. Tabung kedua dimasukkan LIBD dengan konsentrasi 25 mcg/ml (0,25 ml) kemudian dicukupkan dengan darah ad 2,5 ml.
4. Tabung keempat dimasukkan LIBD dengan konsentrasi 75 mcg/ml (0,75 ml) kemudian dicukupkan dengan darah ad 2,5 ml.
5. Tabung kelima dimasukkan LIBD dengan konsentrasi 100 mcg/ml (1 ml) kemudian dicukupkan dengan darah ad 2,5 ml.
Disentrifugasi dengan kecepatan 4000 putaran per menit selama 5 menit. Dipisahkan supernatan dari endapan. Dipipet supernatan dari tiap tabung sebanyak 1 ml kemudian tambahkan Asetonitril sebanyak 1 ml lalu di vorteks dan disentrifugasi selama 5 menit dengan kecepatan 4000 putaran per menit. Dipisahkan supernatan dari endapan. Supernatan yang diperoleh diambil dengan menggunakan spuit kemudian disaring dengan penyaring PTFE diameter 0,2 µ m, lalu diinjeksikan ke dalam sistem KCKT dengan volume penyuntikan 20 µ l dengan laju aliran (flow rate) 2 ml/menit, deteksi pada panjang gelombang 241 nm.
3.4.1.7 Penetapan Kadar Deksametason Dalam Plasma Darah Kelinci
Ambil darah enam hewan uji masing-masing 1 ml dari vena marginal telinga kelinci dan dimasukkan kedalam tabung yang sudah berisi 2 tetes heparin. Disentrifugasi selama 5 menit dengan kecepatan 4000 putaran per menit. Dipisahkan supernatan dari endapan. Dipipet 0,5 ml plasma, dimasukkan ke dalam politube dan ditambahkan 0,5 ml acetonitril untuk mengendapkan protein lalu divortex. Disentrifugasi dengan kecepatan 4000 rpm selama 5 menit. Dipisahkan supernatan dari endapan dan digunakan sebagai blanko.
BAB IV
HASIL DAN PEMBAHASAN
[image:38.595.120.542.505.623.2]Penentuan perbandingan fase gerak Asetonitril dengan aquabidest dilakukan terlebih dahulu sebelum dilakukan penetapan kadar Deksametason dalam plasma pada panjang gelombang 241 nm. Setelah perbandingan fase gerak di dapatkan kemudian ditentukan laju alir, waktu tambat dan tekanan kolom yang optimal. Setelah hal di atas dilakukan kemudian dilakukan penyuntikan larutan Deksametason dengan konsentrasi 250 mcg/ml sebanyal 20µ l kedalam sistem KCKT dengan perbandingan fase gerak Asetonitril : Air (45:55) dan laju alir yang tetap yaitu 2 ml/menit diperoleh waktu tambat sekitar 2.907 menit, seperti yang tertera pada Gambar 4.1 di bawah ini :
Gambar 4.2 Kromatogram Deksametason BPFI dalam plasma dengan konsentrasi 100 mcg/ml, dengan fase gerak Asetonitril–air (45:55) dan laju alir 2 ml/menit, volume penyuntikan 20 µl dan deteksi pada panjang gelombang 241 nm.
Dari Gambar 4.2 di atas digunakan sebagai dasar dalam penentuan kurva baku Deksametason dalam plasma.
Penentuan linieritas kurva baku dari Deksametason ditentukan berdasarkan luas puncak pada konsentrasi 10, 25, 50, 75 dan 100 mcg/ml, diperoleh hubungan yang linier dengan koefisien korelasi (r) = 0,9964 dan persamaan regresi: Y = 15728,0795 X - 11787,4634 dengan data hasil penyuntikan larutan baku Deksametason pada Tabel 4.1 di bawah ini :
Tabel 4.1 Hasil penyuntikan kurva baku deksametason dalam plasma Konsentrasi (mcg/ml) Luas Area
10 182829
25 381585
50 768859
75 1270733
[image:39.595.166.411.537.672.2]Kurva baku dapat dilihat pada Gambar 4.3 di bawah ini:
Gambar 4.3 Kurva baku Deksametason dengan konsentrasi versus luas area puncak Deksametason
Menurut Johnson & Stevenson (1991), penentuan kadar dapat dilakukan dengan mengukur luas puncak atau tinggi puncak. Baik tinggi puncak maupun luasnya dapat dihubungkan dengan konsentrasi. Tinggi puncak mudah diukur, akan tetapi sangat dipengaruhi perubahan waktu retensi yang disebabkan oleh variasi suhu dan komposisi pelarut. Oleh karena itu, luas puncak dianggap merupakan parameter yang lebih akurat untuk pengukuran kuantitatif (Ditjen POM, 1995). Kadar sampel dapat dihitung menggunakan persamaan regresi Y = 15728,0795 X - 11787,4634 yaitu dengan mensubsitusikan Y dengan harga rasio luas puncak. Hasil perhitungan diketahui harga X (kadar sampel) dapat dilihat pada lampiran 4.
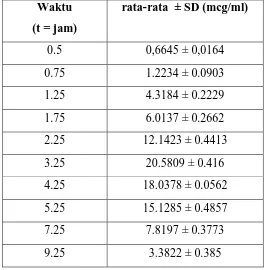
Dari data yang diperoleh pada lampiran 4, maka dapat diketahui konsentrasi rata-rata ± SD (standart deviasi) dari 6 ekor kelinci jantan seperti yang terlihat pada Tabel 4.2 di bawah ini :
Tabel 4.2 Konsentrasi rata-rata ± SD Deksametason dalam plasma kelinci terhadap waktu (n=6)
Waktu (t = jam)
rata-rata ± SD (mcg/ml)
0.5 0,6645 ± 0,0164
0.75 1.2234 ± 0.0903
1.25 4.3184 ± 0.2229
1.75 6.0137 ± 0.2662
2.25 12.1423 ± 0.4413
3.25 20.5809 ± 0.416
4.25 18.0378 ± 0.0562
5.25 15.1285 ± 0.4857
7.25 7.8197 ± 0.3773
9.25 3.3822 ± 0.385
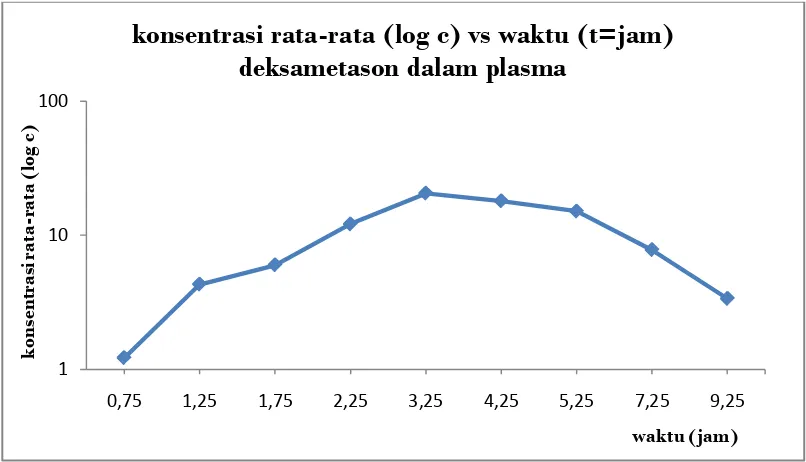
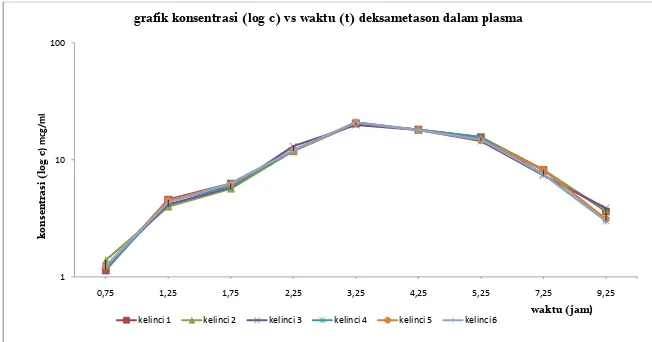
[image:41.595.168.433.209.479.2]Gambar 4.4 konsentrasi rata-rata (log c) VS waktu (t = jam) deksametason dalam plasma
Dari Gambar 4.4 selanjutnya digunakan untuk menentukan nilai parameter farmakokinetika deksametason dalam plasma dengan perhitungan secara manual dimana hasilnya tersaji dalam tabel 4.3.
Tabel 4.3 Nilai parameter farmakokinetik Deksametason ± SD dalam plasma kelinci (n = 6)
Parameter
Farmakokinetik Nilai Satuan
ka 0.802 ± 0.054 jam -1
Tmaks 1.848 ± 0.0694 jam
Cmaks 33.937 ± 2.103 mcg/ml
T1/2abs 0.8673 ± 0.0556 jam
AUC0-∞ 105.152 ± 2.059 mcg/ml . Jam
AUMC0-∞ 555.98 ± 24.493 mcg/ml . Jam2
MRT 5.285 ± 0.138 jam
Vd 17.2175 ± 0.8946 ml
kel 0.346 ± 0.016 jam -1
T1/2 el 2.007 ± 0.096 jam
CL 5.947 ± 0.259 ml/jam
1 10 100
0,75 1,25 1,75 2,25 3,25 4,25 5,25 7,25 9,25
ko nse nt ra si ra ta -r at a (l og c ) waktu (jam)
[image:42.595.169.527.491.694.2]Dari data diatas diperoleh nilai ka 0.802 ± 0.054 jam -1 yang cukup besar dan nilai Tmaks yang diperoleh 1.848 ± 0.0694 jam cukup cepat dalam mencapai nilai Cmaks yaitu 33.937 ± 2.103 mcg/ml. Hal ini menggambarkan bahwa ke enam ekor hewan percobaan (kelinci) yang diberikan Deksametason secara peroral melewati sistem jalur metabolisme lintas pertama yaitu ELP (Efek Lintas Pertama) dimana obat akan mengalami metabolisme pada membran usus sebelum mencapai sirkulasi sistemik.
Menurut Shargel (1988), untuk beberapa obat rute pemakaian mempengaruhi kecepatan metabolismenya. Obat-obat yang diberikan secara oral diabsorpsi secara normal dalam duodenal dari usus halus dan ditransport melalui pembuluh mesenterika menuju vena porta hepatik dan kemudian ke hati sebelum ke sirkulasi sistemik. Metabolisme secara cepat dari obat-obat yang diberikan secara oral sebelum mencapai sirkulasi umum disebut ”first pass effects” (FPE) atau eliminasi presistemik. Terjadinya ”first pass effects” (FPE) dapat diduga apabila terdapat berkurangnya jumlah senyawa induk atau obat utuh dalam sirkulasi sistemik sesudah pemberian oral.
Dari hasil penelitian diperoleh nilai AUC0-∞ sebesar 105.152 ± 2.059 mcg/ml.jam, jumlah ini menggambarkan keberadaan Deksametason dalam
Nilai Vd (volume distribusi) yang diperoleh 17.2175 ± 0.8946 ml, nilai ini menggambarkan jumlah volume cairan tubuh yang mengandung Deksametason yang tersebar ke seluruh tubuh sangatlah kecil. Hal ini disebabkan karena dosis obat yang diberikan sangat kecil dan nilai kel serta nilai AUC yang besar sehingga berpengaruh terhadap penyebaran volume distribusi.
BAB V
KESIMPULAN DAN SARAN
5.1 Kesimpulan
Profil farmakokinetika Deksametason pada kelinci jantan mengikuti model satu kompartemen, dimana proses distribusinya sangat cepat sehingga seolah-olah fase distribusi dilewati dan langsung masuk ke fase eliminasi. Pada fase absorpsi penyerapan obat berlangsung cepat dengan perolehan nilai ka 0.802 ± 0.054 jam-1 dan T1/2abs 0.8673 ± 0.0556 jam. Selain itu diperoleh nilai AUC0-∞ 105.152 ± 2.059 mcg/ml.jam dan AUMC0-∞ 555.98 ± 24.493 mcg/ml.jam2 serta nilai MRT 5.285 ± 0.138 jam. Pada fase distribusi obat akan didistribusikan dengan laju reaksi yan sama kedalam berbagai kelompok jaringan yang berbeda dengan nilai Vd yang diperoleh sebesar 17.2175 ± 0.8946 ml. Kadar obat dalam jaringan akhirnya akan mencapai puncak dengan Tmaks 1.848 ± 0.0694 jam dengan perolehan Cmaks 33.937 ± 2.103 mcg/ml dan kemudian mulai menurun dengan perolehan nilai kel 0.346 ± 0.016 jam-1 dan T1/2 el yang besar yaitu 2.007 ± 0.096 jam yang mempengaruhi klirens (CL) menjadi lebih cepat dengan nilai CL 5.947 ± 0.259 ml/jam.
5.2 Saran
1. Disarankan kepada peneliti lain untuk melanjutkan penelitian dengan rute pemberian obat yang berbeda.
DAFTAR PUSTAKA
Aiache, J.M. (1993). Farmasetika 2 Biofarmasi. Edisi ke-2. Penerjemah: Dr. Widji Soeratri. Surabaya: Penerbit Airlangga University Press. Hal. 7.
Anonim1, 2009. Pemakaian steroid posttonsillectomia.
Anonim2, 2010. Program ” one day-one drug”.
http://www.glitter-graphics.co.id
Daniel E.Furst, MD., dan Tino Munster, MD. (2002). Obat-obat Antiinflamasi Nonsteroid, Obat-obat Antireumatik Pemodifikasi Penyakit, Analgesik Nonopioid dan Obat-obat Untuk Pirai. Dalam Farmakologi Dasar dan Klinik. Edisi kedelapan. Penerjemah: Bagian Farmakologi FKUA. Jakarta: Penerbit Salemba Medika. Hal. 450.
De Lux Putra, E. (2007). Dasar-Dasar Kromatografi Cair Kinerja Tinggi. Fakultas Farmasi USU-Medan. Hal. 51.
Ditjen POM. (1995). Farmakope Indonesia. Edisi IV. Jakarta: Departemen Kesehatan RI. Hal. 286-287, 1011.
Donatus, I. A. (1996). Petunjuk Praktikum Toksikologi. Edisi ke-8. Yogyakarta : Laboratorium Farmakologi dan Toksikologi Fakultas Farmasi Universitas Gadjah Mada.
Johnson, E. L., dan Stevenson, R. (1991). Dasar Kromatografi Cair. Penerjemah: Dr. Kosasih Padmawinata. Bandung: Penerbit ITB. Hal. 236.
Katzung, B.G. (1998). Farmakologi Dasar dan Klinik. Edisi keempat. Penerjemah: Bagian Farmakologi FKUA. Jakarta: Penerbit Salemba Medika. Hal. 36.
Katzung, B.G. (2002). Farmakologi Dasar dan Klinik. Edisi kedelapan. Penerjemah: Bagian Farmakologi FKUA. Jakarta: Penerbit Salemba Medika. Hal. 589.
Hemanth K., Chandra I., Geetha R., Chelvi K.S., Lalitha V., Prema G. (2004). A validated high-performance liquid chromatography method for the determination of rifampicin and desacetyl rifampicin in plasma and urine. Indian J Pharmacol Vol 36. Chennai. India : Hal 231-233.
Holford, N.H. (1998). Farmakokinetik dan Farmakodinamik: Pemilihan Dosis yang Rasional dan Waktu Kerja Obat. Dalam Farmakologi Dasar dan Klinik. Edisi IV. Penerjemah: Bagian Farmakologi FKUA. Jakarta: Penerbit Salemba Medika. Hal. 24.
Mahesh N. Samtani., William J. Jusko. (2005). Stability of Dexamethasone Sodium Phosphate in Rat Plasma. Internasional Journal of Pharmaceutics 301. Elsevier. Hal. 1.
Mutschler, E. (1991). Dinamika Obat. Edisi kelima. Penerjemah: Mathilda B Widianto. Bandung: Penerbit ITB. Hal. 5, 51, 358.
Mycek, M.J., Harvey, R.A., Champe, P.C. (2001). Farmakologi Ulasan Bergambar. Edisi II. Editor: Huriawati Hartanto. Jakarta: Widya Medika. Hal. 277.
Robert H., William O. Robertson. (1987). Handbook Of Poisoning. Twelfth edition. Appleton and Lange/California. Hal. 57,59.
Rohman, A. (2007). Kimia Farmasi Analisis. Cetakan ke-I. Yogyakarta: Penerbit Pustaka Pelajar. Hal. 379, 406.
Rosyd M.R. (2010). Pengaruh Pemberian Deksametason Dosis Bertingkat Peroral 30 hari Terhadap Kerusakan Tubulus Ginjal Tikus Wistar. Artikel Karya Tulis Ilmiah. Fakultas Kedokteran Universitas Diponegoro. Hal: 1.
Setiawati, A. (2007). Farmakokinetik Klinik. Dalam Farmakologi dan Terapi. Edisi IV. Jakarta: Penerbit Bagian farmakologi Fakultas Kedokteraan UI. Hal. 876-877.
Shargel, L. (1988). Biofarmasetika dan Farmakokinetika Terapan. Penerjemah: Fasich dan Sjamsiah. Edisi II. Surabaya: Airlangga University Press. Hal. 297-298.
Suherman, K.S. (2007). Adrenokortikotropin, Adrenokortikosteroid, Analog-Sintetik dan Antagonisnya. Dalam Farmakologi dan Terapi. Edisi kelima. Jakarta: Penerbit Bagian farmakologi FKUI. Hal. 486-487, 492-493. Tjay, T.H., dan Rahardja, K. (2002). Obat-Obat Penting. Edisi kelima. Cetakan
ke-2. Jakarta: Penerbit PT. Elex Media Komputindo. Hal. 13, 20, 27-28, 807-808.
Waldon, D.J. (2008). Pharmacokinetic and Drug Metabolism. Cambridge: Amgen, Inc., One Kendall Square, Building 1000, USA.
Lampiran 1
Hasil Orientasi Dengan Menggunakan Alat KCKT
2.1 Kromatogram hasil penyuntikan larutan baku deksametason BPFI dengan konsentrasi 100 mcg/ml, fase gerak asetonitril : air (35:65) dengan laju alir 1 ml/menit, dan waktu tambat 10,040 menit
2.2 Kromatogram hasil penyuntikan larutan baku deksametason BPFI dengan konsentrasi 100 mcg/ml, fase gerak asetonitril : air (45:55) dengan laju alir 1 ml/menit, dan waktu tambat 5,9 menit
2.3 Kromatogram hasil penyuntikan larutan baku deksametason BPFI dengan konsentrasi 100 mcg/ml, fase gerak asetonitril : air (45:45) dengan laju alir 2 ml/menit, dan waktu tambat 2,9 menit
Lampiran 2
Deksametason Dalam Plasma
3.1 Deksametason dalam plasma 0.75 jam
3.2 Deksametason dalam plasma 1.25 jam
3.4 Deksametason dalam plasma 2.25 jam
3.5 Deksametason dalam plasma 3.25 jam
3.7 Deksametason dalam plasma 5.25 jam
3.8 Deksametason dalam plasma 7.25 jam
Lampiran 4. Perhitungan Persamaan Regresi dan Kurva Kalibrasi Deksametason yang Diperoleh Secara KCKT pada λ 241 nm
Data Kalibrasi Deksametason Konsentrasi (x) terhadap Rasio Luas Area Puncak (y)
No. Konsentrasi (mcg/ml) (x) Rasio Luas Area Puncak (y)
x.y x2 y2
1. 10 182829 1828290 100 3,3426443 x 1010
2. 25 381585 9539625 625 1,4560711 x 1011
3. 50 768859 38442950 2500 5,9114416 x 1011
4. 75 1270733 95304975 5625 1,6147623 x 1012
5. 100 1544232 154423200 10000 2,3846524 x 1012
Σ 260 4148238 299539040 18850 4,7695924 x 1012
Rata-rata 52 829647,6 59907808 3770 9,5391848 x 10
11
a
=( )( )
( )
x /n x n / y x xy 2 2∑
∑
∑
∑
∑
− − = 5 / ) 260 ( 18850 5 / ) 4148238 )( 260 ( 299539040 2 − − = 13520 -18850 215708376 299539040− = 5330 83830664a
= 15728,07955Y = aX + b b = Y – aX
= 829647,6 – 817860,1366 b = 11787,4634
Sehingga, diperoleh persamaan regresi Y = 15728,07955 X - 11787,4634
Untuk mencari hubungan kadar (X) dengan perbandingan luas area (Y) digunakan pengujian koefisien kolerasi (r).
r =
( )( )
( )
(
)
(
( )
)
[
n n]
n
∑
∑
∑
−∑
∑
∑
∑
− − 2 2 2 2 y y x x y x xy r =(
)(
)
[
2 12 2]
) 4148238 ( 10 x 4,7695924 x 5 ) 260 ( 18850 x 5 4148238) ).( 260 ( ) 299539040 ( 5 − − − r =
(
)
(
)
[
13 13]
10 x 1,7207878 x10 2,3847962 67600 94250 1078541880 1497695200 − − − r =
(
)
(
)
[
12]
10 x 6,640084 26650 419153320 r = 8 420664044, 419153320
Lampiran 5
Konversi Perhitungan Dosis Antar Jenis Hewan Dan Perhitungan Dosis yang Diberikan Kepada masing-masing Hewan Percobaan
Konversi Perhitungan Dosis Antar Jenis Hewan (Donatus, 1996)
Perlakuan Mencit 20g
Tikus 200g
Marmot 400g
Kelinci 1,5kg
Kera 4kg
Anjing 12kg
Manusia 70kg
Mencit 20g 1,0 7,0 12,25 27,8 64,1 124,2 387,9
Tikus 200g 0,14 1,0 1,74 3,9 9,2 17,8 56,0
Marmot 400g 0,08 0,57 1,0 2,25 5,2 10,2 31,5
Kelinci 1,5kg 0,04 0,25 0,44 1,0 2,4 4,5 14,2
Kera 4kg 0,016 0,11 0,19 0,42 1,0 1,9 6,1
Anjing 12kg 0,008 0,06 0,10 0,22 0,52 1,0 3,1
Manusia 70kg 0,0026 0,018 0,031 0,07 0,16 0,32 1,0
Perhitungan Dosis yang Diberikan Kepada masing-masing Hewan Percobaan
KELINCI I
dosis lazim = 7.5 mg
berat hewan = 1.9 kg
konversi dosis pada kelinci = 0.07
dosis konversi = 7.5 mg x 0.07 = 0.525 mg
dosis perkiraan per kg BB = 1000g x 0.525 mg = 0.35 mg/kg BB 1500g
= 350 mcg/kg BB
Dosis = 1900g x 350 mcg = 665 mcg
1000g
LAMPIRAN 6. KADAR DEKSAMETASON DALAM PLASMA PADA SAMPLING TIME
Waktu (t=jam)
KELINCI I KELINCI II KELINCI III KELINCI IV KELINCI V KELINCI VI Rata-Rata Kadar
± SD (mcg/ml)
Area Kadar Area kadar Area Kadar Area Kadar Area Kadar Area Kadar
0.5 22448 0,6778 22348 0,6714 21948 0,6460 22388 0,674 22428 0,6765 21874 0,6413 0,6645 ± 0,0164
0.75 29577 1,1310 33589 1,3861 30945 1,2180 29855 1,1487 30988 1,2207 31228 1,2360 1,2234 ± 0,0903
1.25 83409 4,5537 74253 3,9716 76772 4,1317 81253 4,4166 82352 4,4865 79865 4,3284 4,3148 ± 0,2229
1.75 110125 6,2523 100849 5,6625 102652 5,7772 104874 5,9184 108753 6,1651 110985 6,3070 6,0137 ± 0,2662
2.25 198644 11,8804 198641 11,8802 216683 13,0273 199754 11,9510 200875 12,0222 201987 12,0929 12,1423 ± 0,4413
3.25 332901 20,4165 335220 20,5640 323902 19,8444 341678 20,9746 338984 20,8033 340233 20,8827 20,5809 ± 0,416
4.25 296690 18,1142 295634 18,0471 294635 17,9836 294928 18,0022 296357 18,0931 294681 17,9865 18,0378 ± 0,0562
5.25 256766 15,5758 255965 15,5249 239286 14,4645 256471 15,5571 243681 14,7439 246215 14,9050 15,1285 ± 0,4857
7.25 140744 8,1991 138954 8,0853 127659 7,3672 130788 7,5661 140549 8,1867 129967 7,5139 7,8197 ± 0,3773
Lampiran 7
Grafik Konsentrasi (log c) vs Waktu (t) Deksametason Dalam Plasma
1 10 100
0,75 1,25 1,75 2,25 3,25 4,25 5,25 7,25 9,25
ko
n
se
n
tr
as
i (
lo
g
c
)
m
cg
/m
l
[image:58.842.93.745.135.477.2]waktu (jam)
grafik konsentrasi (log c) vs waktu (t) deksametason dalam plasma
Lampiran 8. Parameter Farmakokinetika deksametason ± SD
Kelinci BB
(kg)
Dosis (mcg)
Ka
(Jam-1)
T1/2 abs
(jam)
Cmaks
(mcg/ml)
Tmaks
(jam)
AUC0-∞
(mcg/ml.jam)
AUMC0-∞
(mcg/ml.jam2)
MRT
(jam)
Vd
(ml)
Kel
(jam-1)
T1/2el
(jam)
CL (ml/jam)
I 1,9 665 0,7777 0,891 32,5882 1,921 107,926 582,7584 5,3996 18,7912 0,3279 2,1134 6,1616
II 1,8 630 0,7404 0,9359 34,921 1,9415 107,1033 577,2695 5,3898 17,250 0,341 2,0322 5,8822
III 1,65 577,5 0,9034 0,7671 30,3769 1,7625 105,3371 572,5603 5,4355 16,7453 0,3274 2,1167 5,4824
IV 1,8 630 0,7903 0,8769 36,1317 1,82 103,5217 532,2413 5,1414 16,6731 0,3650 1,8986 6,0857
V 1,84 644 0,7954 0,8712 34,3898 1,841 104,4138 544,2797 5,2127 17,567 0,3511 1,974 6,1677
VI 1,73 605,5 0,8039 0,862 35,214 1,8407 102,612 526,7603 5,1335 16,2783 0,3625 1,9117 5,900
Rata2 0,802 0,8673 33,937 1,848 105,152 555,98 5,285 17,2175 0,346 2,007 5,9466
Lampiran 9
Contoh Perhitungan Parameter Farmakokinetika Secara Manual a. Hewan I
Waktu (t) Konsentrasi (C) A.eKelt Residual
(jam) (mcg / ml)
0,5 0,6678 68,4189 /-67,7412/
0,75 1,1310 63,0339 /-61,9029/ Ln R = LnB-Ka.t
1,25 4,5537 53,5022 /-48,9485/ =4,7935 – 0,7777.t
1,75 6,2523 45,4118 /-39,1595/ R = B.e-Ka.t
2,25 11,8804 38,5449 /-26,6645/ = 120,7232.e-0,7777. t 3,25 20,4165 27,7691 /-7,3526/ r = -0,9649
Ln CE = Ln A-Kel.t
4,25 18,1142 = 4,3896-0,3279. t
5,25 15,5758 CE = A.e-Kel.t
7,25 8,1991 = 80,6081.e-0,3279.t 9,25 3,6155 r = -0,9908
Kel = 0,3279 jam-1 T1/2 el =
3279 , 0 693 , 0
= 2,1134 jam
Ka = 0,7777 jam-1 T1/2 ab =
7777 , 0 693 , 0
= 0,891 jam
b. AUC (Area Under the Curve)
AUC0-t = { 2 1 1xt C } + { 2 ) ( )
(C2 +C1 x t2 −t1 } + {
2
) (
)
(Cn +Cn−1 x tn −tn−1 } ={ 2 5 , 0 6778 , 0 x }+{ 2 ) 25 , 0 )( 1310 , 1 6778 , 0 ( + }+{ 2 ) 5 , 0 )( 5537 , 4 1310 , 1 ( + } +{ 2 ) 5 , 0 )( 2523 , 6 5537 , 4 ( + }+{ 2 ) 5 , 0 )( 8804 , 11 2523 , 6 ( + }+{ 2 ) 1 )( 4165 , 20 8804 , 11 ( + } +{ 2 ) 1 )( 1142 , 18 4165 , 20 ( + }+{ 2 ) 1 )( 5758 , 15 1142 , 18 ( + }+{ 2 ) 2 )( 1991 , 8 5758 , 15 ( + } +{ 2 ) 2 )( 6155 , 3 1991 , 8 ( + }
AUC9,25-∞ = Kel Ctn = 3279 , 0 6155 , 3
= 11,0262 mcg/ml.jam
AUC0-∞= AUC0-t + AUC9,25-∞
= 96,8998 + 11,0262
= 107,926 mcg/ml.jam
c. AUMC
t 0,5 0,75 1,25 1,75 2,25 3,25 4,25 5,25 7,25 9,25
C.t 0,3389 0,8483 5,6921 10,9415 26,7309 66,3536 76,9854 81,773 59,4434 33,4434
AUMC0-t ={ 2
) (C1t1xt1
}+{
2
) )( (C2t2 +C1t1 t2 −t1
}+{
2
) )(
(Cntn +Cn−1tn−1 tn −tn−1 }
AUMC0-t ={
2 ) 5 , 0 3389 , 0 ( x }+{ 2 ) 25 , 0 )( 8483 , 0 3389 , 0 ( + }+{ 2 ) 5 , 0 )( 6921 , 5 8483 , 0 ( + } +{ 2 ) 5 , 0 )( 9415 , 10 6921 , 5 ( + }+{ 2 ) 5 , 0 )( 7309 , 26 9415 , 10 ( + } +{ 2 ) 1 )( 3536 , 66 7309 , 26 ( + }+{ 2 ) 1 )( 9854 , 76 3536 , 66 ( + } +{ 2 ) 1 )( 773 , 81 9854 , 76 ( + }+ { 2 ) 2 )( 4434 , 59 773 , 81 ( + }+{ 2 ) 2 )( 4434 , 33 4434 , 59 ( + }
= 447,1389 mcg/ml.jam2
AUMC9,25-∞ = Kel Cttn
+ 2
) (Kel Ctn = 3279 , 0 4434 , 33
+ 2
) 3279 , 0 ( 6155 , 3
= 135,6195 mcg/ml.jam2
AUMC0-∞ = AUMC0-t + AUMC9,25-∞
= 447,1389 + 135,6195
MRT = ∞ − ∞ − 0 0 AUC AUMC = jam ml mcg jam ml mcg . / 926 , 107 . / 7584 , 582 2
= 5,3996 jam
Vd =
ke AUC Dosis × ∞ − 0 = ml mcg mcg / 3279 , 0 926 , 107 665 ×
= 18,7912 ml
Tmaks =
Ke Ka ke Ka log 303 , 2 − = 3279 , 0 7777 , 0 log 3279 , 0 7777 , 0 303 , 2 −
= 1,921 jam
Cmaks =
max . ) (
. ket
e ke ka Vd Dosis ka − −
= . 0,3279 1,921
) 3279 , 0 7777 , 0 ( 7912 , 18 665 7777 , 0 x e x − −
= 32,5882 mcg / ml
Kliren (CL) =
∞ − 0 AUC Dosis = jam ml mcg mcg . / 926 , 107 665
Lampiran 10
Gambar Alat
[image:63.595.108.539.568.689.2]Gambar 10.1 Alat KCKT (Shimadzu)
Gambar 10.3 Sonifikator (Branson 1510)
Gambar 10.5 Degasser (DGU 20 AS)
[image:65.595.216.443.460.688.2]
Gambar 10.7 Alat Sentrifuge Gambar 10.8 Alat Vorteks
Gambar 10.9 Erlenmeyer Gambar 10.10 Beaker Glass
Gambar 10.13 Kelinci
[image:67.595.139.503.487.709.2]Gambar 10.14 Proses Pengambilan Darah