STUDI PENURUNAN KADAR LOGAM MANGAN (Mn) DAN
NIKEL (Ni) DALAM AIR MINUM ISI ULANG YANG DIOLAH
DENGAN SISTEM
REVERSE OSMOSIS
SKRIPSI
RAHMANI KARTIKA AYU
090802054
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
UNIVERSITAS SUMATERA UTARA
STUDI PENURUNAN KADAR LOGAM MANGAN (Mn) DAN
NIKEL (Ni) DALAM AIR MINUM ISI ULANG YANG DIOLAH
DENGAN SISTEM
REVERSE OSMOSIS
SKRIPSI
Diajukan untuk melengkapi tugas dan memenuhi syarat mencapai gelar Sarjana Sains
RAHMANI KARTIKA AYU 090802054
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM UNIVERSITAS SUMATERA UTARA
PERSETUJUAN
Judul : STUDI PENURUNAN KADAR LOGAM
MANGAN (Mn) DAN NIKEL (Ni) DALAM AIR MINUM ISI ULANG YANG DIOLAH DENGAN SISTEM REVERSE OSMOSIS
Kategori : SKRIPSI
Nama : RAHMANI KARTIKA AYU
Nomor Induk Mahasiswa : 090802054
Program Studi : SARJANA (S1) KIMIA
Departemen : KIMIA
Fakultas : MATEMATIKA DAN ILMU PENGETAHUAN
ALAM (FMIPA) UNIVERSITAS SUMATERA UTARA
Disetujui di
Medan, Februari 2013
Komisi Pembimbing :
Pembimbing 2 Pembimbing 1
Dr. Tini Sembiring Drs. Chairuddin, M.Sc.
NIP. 194805131971072001 NIP. 195912311987011001
Diketahui/Disetujui oleh :
Departemen Kimia FMIPA USU Ketua,
DR. Rumondang Bulan Nst.,MS. NIP. 195408301985032001
PERNYATAAN
ANALISIS KADAR LOGAM MANGAN (Mn) DAN NIKEL (Ni) DALAM AIR MINUM ISI ULANG SISTEM REVERSE OSMOSIS DENGAN METODE
SPEKTROFOTOMETRI SERAPAN ATOM (SSA)
SKRIPSI
Saya mengakui bahwa skripsi ini adalah hasil kerja saya sendiri, kecuali beberapa kutipan dan ringkasan yang masing-masing disebutkan sumbernya.
Medan, Februari 2013
PENGHARGAAN
Bismillahirrahmanirrahim
Puji dan syukur kehadirat Allah SWT atas berkah dan karunia-Nya saya dapat menyelesaikan skripsi ini sebagai salah satu syarat untuk meraih gelar Sarjana Sains. Shalawat Berangkai salam saya sampaikan pada junjungan Nabi besar Muhammad SAW, insya Allah saya mendapatkan syafaatnya di hari akhir kelak. Amin Yaa Rabbal Alamin.
Penghargaan yang tinggi atas cinta kasih dan dukungan tiada terkira kepada ibunda saya Dra. Sumarni yang telah memberikan pelajaran hidup dan kasih sayang yang tak terkira kepada saya dan untuk ayahanda Yuzuarman yang telah memberikan kesabaran hidup yang sangat berarti. Dan untuk adik-adik saya Fani, Mitha, Indah dan Shinta yang selalu memberikan keceriaan dan semangat setiap harinya. Serta kepada seluruh keluarga dan terkhusus kepada nenek tersayang yang telah memberikan doa dan dorongan semangat saya ucapkan terimakasih.
Dengan segala kerendahan hati saya dan setulus-tulusnya saya mengucapkan banyak terima kasih kepada Bapak Drs. Chairuddin, M.Sc selaku dosen pembimbing 1 dan Ibu Dr. Tini Sembiring selaku dosen pembimbing 2 yang telah sangat banyak membantu dan memberikan pengarahan serta bimbingannya hingga terselesaikannya skripsi saya ini. Tidak lupa juga Ibu Dr. Rumondang Bulan Nst. Ms dan Bapak Drs. Albert Pasaribu, M.Sc selaku ketua dan sekretaris Departemen Kimia FMIPA USU. Kepada Bapak Prof. Dr. Zul Alfian, M.Sc selaku dosen wali saya yang telah membantu saya dalam menjalani perkuliahan, terima kasih atas motivasi yang bapak berikan kepada saya. Dan kepada seluruh dosen di jurusan Kimia FMIPA USU, terima kasih saya ucapkan atas ilmu-ilmu yang bapak/ibu berikan selama saya menjalani perkuliahan.
Untuk seluruh asisten laboratorium kimia dasar, kakak dan abang stambuk 2008, Ilman, Irwan, Icha, Dwi, Indah, Rina serta adik-adik stambuk 2010 dan 2011 terimakasih atas dukungan dan doanya yang telah membantu saya dalam penelitian. Dan terima kasih kepada kak Ayu selaku laboran laboratorium Kimia Dasar atas fasilitas yang diberikan kepada saya. Untuk rekan-rekan seperjuangan di HMI Komisariat FMIPA USU, Menwa Yon A USU dan PEMA FMIPA USU periode 2011/2012 terima kasih untuk perjuangan yang telah dilalui bersama yang memberikan banyak pelajaran hidup buat saya. Kepada seluruh teman-teman Kimia stambuk 2009 dan terkhusus buat Abangda Hadi Kurniawan Tambunan yang telah dengan sabar membimbing saya hingga saat ini terima kasih buat semua dukungannya .
Penulis
ABSTRAK
STUDY OF DECREASED THE CONTENTS OF MANGANESE AND NICKEL IN DRINKING WATER REVERSE OSMOSIS SYSTEM
ABSTRACT
DAFTAR ISI
2.9. Spektrofotometri Serapan Atom 14
Bab 3 Metode Penelitian 18 3.3.3. Pembuatan Larutan Standar Mangan (Mn) 0,00;
3.3.6. Pembuatan Larutan Standar Nikel (Ni) 10 mg/L 20 3.3.7. Pembuatan Larutan Standar Nikel (Ni) 1 mg/L 20 3.3.8. Pembuatan Larutan Standar Nikel (Ni) 0,0; 0,03; 0,05;
0,07; 0,10; dan 0,13 mg/L 20
3.3.9. Pembuatan Kurva Standar Logam Nikel (Ni) 20 3.3.10 Pengawetan dan Tahap Destruksi Sampel 20
3.4.Bagan Penelitian 22
3.4.1. Pembuatan Larutan Seri Standar dan Kurva Kalibrasi
Logam Mangan (Mn) 22
3.4.2. Pembuatan Larutan Seri Standar dan Kurva Kalibrasi
Logam Nikel (Ni) 23
3.4.3. Preparasi dan Penentuan Mangan (Mn) dalam Sampel
Air Baku 24
3.4.4. Preparasi dan Penentuan Nikel (Ni) dalam Sampel Air
Baku 25
Bab 4 Hasil dan Pembahasan 26
4.1.Hasil Penelitian 26
4.1.1. Logam Mangan (Mn) 26
4.1.2. Pengolahan Data Logam Mangan (Mn) 27 4.1.2.1. Penurunan Persamaan Garis Regresi dengan
Metode Least Square 27
4.1.2.2. Koefisien Korelasi 28
4.1.2.3. Penentuan Konsentrasi 29 4.1.2.4. Persentase (%) penurunan konsentrasi logam
Mangan (Mn) 30
4.1.3. Logam Nikel (Ni) 32
4.1.4. Pengolahan Data Logam Nikel (Ni) 32 4.1.4.1. Penurunan Persamaan Garis Regresi dengan
Metode Least Square 32
4.1.4.2. Koefisien Korelasi 34
4.1.4.3. Penentuan Konsentrasi 35 4.1.4.4. Persentase (%) penurunan konsentrasi logam
DAFTAR TABEL
Halaman
Tabel 4.1. Data absorbansi larutan standar Mangan (Mn) 26 Tabel 4.2. Penurunan persamaan garis regresi untuk penentuan konsentrasi
logam mangan (Mn) berdasarkan pengukuran absorbansi larutan
standar mangan (Mn) 27
Tabel 4.3. Data absorbansi logam mangan (Mn) dalam sampel yang diukur
Sebanyak7 kali 29
Tabel 4.4. Analisis data statistik penentuan konsentrasi logam mangan (Mn)
pada Air Baku 30
Tabel 4.5. Hasil penentuan konsentrasi logam mangan (Mn) dalam Sampel 31 Tabel 4.6. Persentase (%) hasil penurunan kadar logam mangan (Mn)
dalam sampel 32
Tabel 4.7. Data absorbansi larutan standar nikel (Ni) 33 Tabel 4.8. Penurunan persamaan garis regresi untuk penentuan konsentrasi
logam nikel (Ni) berdasarkan pengukuran absorbansi larutan
standar nikel (Ni) 34
Tabel 4.9. Data absorbansi logam nikel (Ni) dalam sampel yang diukur
sebanyak 7 kali 36
Tabel 4.10. Analisis data statistik penentuan konsentrasi logam
nikel (Ni) pada Air Baku 37
Tabel 4.11.Hasil penentuan konsentrasi logam nikel (Ni) dalam sampel 38 Tabel 4.12. Persentase (%) hasil penurunan kadar logam nikel (Ni) dalam
DAFTAR GAMBAR
Halaman
Gambar 2.1.: Membran Reverse Osmosis 13
DAFTAR LAMPIRAN
Halaman
Lampiran 1. Persyaratan Kualitas Air Minum 43
Lampiran 2. Kondisi alat SSA Merek Shimadzu tipe AA-6300 pada
pengukuran konsentrasi logam Besi (Fe) 47 Lampiran 3. Kondisi alat SSA Merek Shimadzu tipe AA-6300 pada
pengukuran konsentrasi logam Tembaga (Cu) 47 Lampiran 4. Kondisi alat SSA Merek Shimadzu tipe AA-6300 pada
pengukuran konsentrasi logam Zinkum (Zn) 47
Lampiran 5. Gambar Alat SSA 48
ABSTRAK
STUDY OF DECREASED THE CONTENTS OF MANGANESE AND NICKEL IN DRINKING WATER REVERSE OSMOSIS SYSTEM
ABSTRACT
BAB 1
PENDAHULUAN
1.1Latar Belakang
Air dibutuhkan untuk bermacam-macam keperluan. Kualitas air untuk keperluan minuman berbeda dengan untuk keperluan industri. Air untuk minum rumah tangga dan keperluan lainnya termasuk air golongan II. (Agusnar, 2008). Air untuk minum dan juga untuk penyiapan makanan harus bebas dari mikroorganisme yang dapat menyebabkan penyakit dan juga harus bebas dari mineral-mineral dan senyawa organik yang dapat menimbulkan gangguan fisiologis. (Borchardt, 1971)
Saat ini masalah utama yang dihadapi oleh sumber daya air meliputi kualitas air yang sudah tidak mampu memenuhi kebutuhan yang terus meningkat dan kualitas air untuk keperluan domestik yang semakin menurun. Kegiatan industri, domestik, dan kegiatan lain berdampak negatif terhadap sumber daya air, antara lain menyebabkan penurunan kualitas air. Kondisi ini dapat menimbulkan gangguan, kerusakan, dan bahaya bagi semua makhluk hidup yang bergantung pada sumber daya air. Oleh karena itu, diperlukan pengelolaan dan perlindungan sumber daya air secara seksama. (Effendi, H.2003)
Dimana jika konsentrasi nikel pada air tanah itu tinggi maka fungsi air pun menjadi menurun.(Darmono, 1995)
Pemurnian dan pelunakan air dapat dilakukan dengan berbagai cara, bergantung pada rencana penggunaan air itu sendiri. Untuk penyediaan air minum dari air bersih di perkotaan biasanya diperlukan pengolahan air. (Austin, 1996). Filtrasi sering digunakan untuk pemisahan partikel-partikel dalam proses pengolahan air. Dimana hanya partikel dengan ukuran yang kecil yang dapat lewat melalui filter. (Connor, 2009).
Air minum dapat diproses dalam beberapa tahap baik menggunakan proses pemurnian air (Reverse Osmosis / Tanpa Mineral) maupun proses biasa Water treatment processing (Mineral), dimana sumber air yang digunakan untuk Air kemasan mineral berasal dari mata air pengunungan, untuk Air kemasan Non mineral biasanya dapat juga digunakan dengan sumber mata air tanah / mata air pengunungan. (http://www.divaropro.com/2011/10/divaro-reverse-osmosis-normal-0-false.html)
Dalam proses reverse osmosis ada tahapan-tahapan yang harus diperhatikan antara lain sumber air bahan baku, proses pengolahan air, jenis mesin reverse osmosis dan kapasitas produk yang diharapkan. (Goosen, F.A, 2004)
Berdasarkan hasil penelitian sebelumnya oleh Siahaan (2012) tentang efisiensi pemakaian reverse osmosis pada depot air minum terhadap penurunan kadar ion besi (Fe3+), tembaga (Cu2+) dan zinkum (Zn2+)” dimana diperoleh metode reverse osmosis efektif untuk mengurangi kadar logam tersebut. Oleh sebab itu, maka penulis tertarik untuk melakukan penelitian untuk menganalisis kadar logam mangan (Mn) dan nikel (Ni) pada air minum isi ulang sebelum dan sesudah proses reverse osmosis menggunakan spektrofotometer serapan atom.
1.2Permasalahan
1. Berapakah kandungan logam mangan (Mn) dan nikel (Ni) sebelum dan sesudah diproses dengan sistem reverse osmosis (RO).
2. Apakah kadar logam mangan (Mn) dan nikel (Ni) pada air minum isi ulang telah memenuhi persyaratan kualitas air minum.
1.3Pembatasan Masalah
Pembatasan masalah pada penelitian ini adalah :
1. Sampel air adalah air sumur bor sebelum dan sesudah sistem reverse osmosis (RO) dari depot air minum yang menggunakan sistem membran reverse osmosis di daerah Kota Binjai Kecamatan Binjai Timur.
2. Jenis Mesin reverse Osmosis (RO) yang digunakan adalah RO merk Kemflo F5633/C
1.4Tujuan Penelitian
Adapun tujuan dari penelitian ini adalah :
1. Untuk mengetahui kandungan logam mangan (Mn) dan nikel (Ni) sebelum dan sesudah diproses dengan sistem reverse osmosis (RO).
2. Untuk mengetahui apakah kandungan logam mangan (Mn) dan nikel (Ni) pada air minum isi ulang telah memenuhi persyaratan kualitas air minum.
1.5Manfaat Penelitian
1.6Lokasi Penelitian
Penelitian ini dilakukan di Laboratorium Kimia dasar LIDA Universitas Sumatera Utara dan Analisis Spektrofotometri Serapan Atom dilakukan di Laboratorium Kimia Analitik Fakultas Matematika dan Ilmu Pengetahuan Alam (FMIPA) Universitas Sumatera Utara.
1.7 Metodologi Penelitian
1. Penelitian ini merupakan penelitian laboratorium..
2. Sampel yang dianalisis adalah air sebelum dan sesudah diproses dengan sistem reverse osmosis dari depot air minum isi ulang dengan sistem reverse osmosis (RO) yang sumber airnya berasal dari sumur bor.
3. Sampel diambil sebanyak 7 kali setiap hari selama 1 minggu setelah penggantian membran reverse osmosis
4. Sampel terlebih dahulu didestruksi dengan asam nitrat pekat.
BAB 2
TINJAUAN PUSTAKA
2.1 Air
Air di permukaan bumi ini terdiri atas 97% air asin di lautan, 2% masih berupa es, 0,0009% berupa danau, 0,00009% merupakan air tawar di sungai dan sisanya merupakan air permukaan yang dapat dimanfaatkan untuk kebutuhan hidup mahasiswa, tumbuhan dan hewan yang hidup di daratan. Oleh sebab itu, air merupakan barang yang paling dominan dibutuhkan di permukaan bumi ini. (Nugroho, A. 2006).
Air merupakan senyawa yang paling melimpah di permukaan bumi. Sifat-sifat dari air memiliki pengaruh yang berarti untuk penyediaan air, kualitas air dan teknik
pengolahan air. (Montgomery, J.M. 1985).
Walaupun air merupakan sumber daya alam yang dapat diperbarui, tetapi air akan dapat dengan mudah terkontaminasi oleh aktivitas manusia. Air banyak digunakan oleh manusia untuk tujuan yang bermacam-macam sehingga dengan mudah dapat tercemar. Air tanah dapat terkontaminasi dari beberapa sumber pencemar, baik lokal maupun regional. (Darmono, 2001)
Air alamiah dan bahan-bahan partikulat yang berhubungan merupakan sistem elektrolit heterogen yang rumit dan mengandung sejumlah besar spesies organik dan anorganik tersebar di antara fase cair dan padat. (Connel, D.W. 1995)
2.2. Standar Baku Kualitas Air Minum
Standar baku kualitas air minum merupakan parameter yang digunakan untuk menentukan kualitas air minum. Dengan standar tersebut, dapat diketahui kualitas air minum layak atau tidak untuk diminum. Standar baku kualitas air minum harus memenuhi kualitas secara fisika, kimia dan biologi. Standar fisika menetapkan batasan tentang sifat fisik air. Standar kimia menetapkan tentang batasan kandungan sifat dan bahan kimia yang terkandung didalam air minum yang masih diperbolehkan dan tidak berbahaya untuk dikonsumsi. Standar biologi menetapkan ada atau tidaknya mikroorganisme patogen dan nonpatogen yang terkandung atau hidup didalam air minum.
Kehadiran besi dan mangan dalam air yang mengendap mengubah penampilan dari air, mengubahnya menjadi keruh kuning-coklat hingga hitam. Selain itu, pengendapan presipitat ini akan menyebabkan pewarnaan perlengkapan pipa dan
binatu. Kondisi lain yang telah dikaitkan dengan kehadiran besi dan mangan dalam persediaan air adalah pertumbuhan mikroorganisme dalam sistem distribusi. Akumulasi pertumbuhan mikroba dapat menyebabkan penurunan daya dukung pipa dan penyumbatan meter dan katup. Peluruhan dari akumulasi sering menyebabkan kerugian konsumen termasuk keluhan pada listrik sering terjadi oleh laju aliran yang meningkat menyebabkan kekeruhan tinggi.
Standar mutu air minum atau air untuk kebutuhan rumah tangga ditetapkan berdasarkan peraturan menteri kesehatan Republik Indonesia No. 492/MENKES/PER/VII/2010 tentang syarat-syarat dan pengawasan kualitas air minum tersebut disesuaikan dengan Standar Internasional yang dikeluarkan oleh WHO. Ada banyak logam yang terkandung dalam air, namun dalam penelitian ini hanya dibatasi pada logam mangan dan nikel dimana untuk logam mangan kadar maksimum yang diperbolehkan adalah 0,4 mg/L dan untuk nikel 0,07 mg/L.
Dengan adanya standarisasi tersebut, dapat dinilai kelayakan pendistribusian sumber air untuk keperluan rumah tangga (Kusnaedi, 2010).
2.3. Depot Air Minum
Depot air minum merupakan usaha industri yang melakukan proses pengolahan air baku menjadi air minum dan menjual langsung kepada konsumen. Adapun air minum yang dimaksud adalah air baku yang telah di proses dan aman untuk diminum. Sementara air baku adalah air yang belum diproses atau sudah diproses menjadi air bersih yang memenuhi persyaratan mutu sesuai peraturan menteri kesehatan untuk diolah menjadi produk air minum.
Setiap depot air minum menurut keputusan Menperindag No 651 Tahun 2004 harus berpedoman pada cara produksi air minum yang baik pada seluruh mata rantrai produksi air minum, mulai dari pengadaan bahan sampai penjualan ke konsumen,
seperti dalam bagian-bagian berikut:
a. Desain dan konstruksi depot
b. Bahan baku, mesin, dan peralatan produksi c. Proses produksi
d. Produk air minum
e. Pemilihan sarana produksi dan program sanitasi f. Karyawan
g. Penyimpanan air baku dan penjualan (Kacaribu,K.2008).
Istilah “logam” secara khas memberikan suatu unsur yang merupakan konduktor listrik yang baik dan mempunyai konduktivitas panas, rapatan, kemudahan ditempa, kekerasan, dan keelektropositifan yang tinggi. Istilah “logam berat” digunakan secara luas dalam literatur ilmiah untuk memberikan terhadap logam beracun. Defenisi “logam berat” terutama berdasarkan (1) gaya berat spesifik logam (lebih besar dari 4 atau 5), (2) tempatnya pada Tabel Periodik, sebagai contoh, unsur-unsur dengan jumlah atom 22-34 dan 40-52, serta lantanida dan aktinida, dan (3) tanggapan spesifik biokimiawi di dalam hewan dan tumbuhan (Connel, D.W. 1995)
.
Logam juga dapat menyebabkan timbulnya suatu bahaya pada makhluk hidup. Hal ini terjadi jika sejumlah logam mencemari lingkungan. Logam – logam tertentu sangat berbahaya jika ditemukan dalam konsentrasi tinggi dalam lingkungan, karena logam tersebut mempunyai sifat merusak tubuh makhluk hidup. Disamping hal tersebut, beberapa logam sangat diperlukan dalam proses kehidupan makhluk hidup. Dalam hal ini logam dapat dibagi menjadi dua bagian, yaitu logam esensial dan nonesensial. Logam esensial adalah logam yang sangat menbantu di dalam proses
fisiologis makhluk hidup dengan jalan membantu kerja enzim atau pembentukan organ dari makhluk yang bersangkutan. Sedangkan logam nonesensial adalah logam yang peranannya dalam tubuh makhluk hidup belum diketahui, kandungannya dalam jaringan hewan sangat kecil dan apabila kandungannya tinggi akan merusak organ – organ tubuh makhluk yang bersangkutan (Vogel, A.I. 1994).
Logam berat (heavy metal) atau logam toksik (toxic metals) adalah bentuk umum yang digunakan untuk menjelaskan sekelompok elemen-elemen logam yang kebanyakan tergolong berbahaya bila masuk ke dalam tubuh makhluk hidup. Logam berat yang terdapat baik di lingkungan maupun di dalam tubuh manusia dalam konsentrasi yang sangat rendah disebut juga sebagai trace metals. Trace metals seperti Cadmium (Cd), Timbal (Pb) dan Merkuri (Hg) mempunyai berat jenis sedikitnya 5 kali lebih besar daripada air.
mengumpul di dalam tubuh suatu organism dan tetap tinggal dalam jangka waktu lama sebagai racun yang terakumulasi. (Nugroho, A. 2006).
Di dalam air biasanya logam berikatan dalam senyawa kimia atau dalam bentuk logam ion, bergantung pada kompartemen tempat logam tersebut berada. Tingkat kandungan logam pada setiap kompartemen sangat bervariasi, bergantung pada lokasi , jenis kopartemen dan tingkat pencemarannya. Telah banyak dilaporkan mengenai konsentrasi logam dalam air dan biota yang hidup di dalamnya.
Tujuan utama untuk mengetahui konsentrasi logam dalam lingkungan perairan ialah ;
a. Mengetahui konsentrasi logam yang tinggi dalam hewan air, baik ikan air laut maupun air tawar, yang dapat digunakan sebagai pedoman untuk mencegah terjadinya toksisitas kronis maupun akut pada orang yang memakannya.
b. Mengetahui konsentrasi logam yang tinggi dalam air dan sedimen, yang dapat digunakan sebagai pedoman untuk memonitor kualitas air yang mungkin
digunakan sebagai irigasi ataupun air minum, yang akhirnya berakibat buruk bagi orang yang mengonsumsinya.
Karena itu suatu pencemaran logam berat dalam lingkungan perairan perlu diperhatikan secara serius, mengingat akan timbulnya akibat buruk bagi keseimbangan makhluk hidup. (Darmono, 2001)
2.5. Sumber Pencemaran
Kegiatan manusia juga merupakan suatu sumber utama pemasukan logam ke dalam lingkungan perairan. Pemasukan logam berasal dari buangan langsung berbagai jenis limbah yang mengganggu, gangguan pada cekungan-cekungan pengairan, presipitasi dan yang berasal dari atmosfer. Sumber-sumber utamanya sebagai berikut :
3. Limbah Dan Buangan Industri
4. Aliran Pertanian (Connel, D.W. 1995).
2.6. Mangan (Mn)
Mangan (Mn) adalah logam berwarna abu-abu keputihan, merupakan logam keras, mudah retak, serta mudah teroksidasi. Senyawa Mn secara alami berbentuk padat di lingkungan dan hanya sebagian kecil yang berada di air dan di udara sebagai debu.
Mangan (Mn) merupakan mikronutrien essensial bagi semua makhluk hidup. Mn bersifat essensial bagi komponen lebih dari 36 jenis enzim untuk metabolism karbohidrat, protein dan lipid, sebagai kofaktor beberapa kelompok enzim oksidoreduktase, transferase, hidrolase, liase, isomerase, ligase, lektin, dan integrin.
Mangan dalam dosis tinggi bersifat toksik. Paparan dosis tinggi dalam waktu
singkat menunjukkan gejala berupa kegemukan, glukosa intoleransi, penggumpalan darah gangguan kulit, gangguan skeleton, menurunnya kadar kolesterol, mengakibatkan cacat lahir, perubahan warna rambut, gangguan sistem syaraf, gangguan hati, jantung, dan pembuluh vaskuler, menurunnya tekanan darah, mengakibatkan cacat pada fetus, kerusakan otak, serta iritasi alat pencernaan. (Widowati, W. 2008).
Besi dan mangan yang teroksida dalam air berwarna kecoklatan dan tidak larut, menyebabkan penggunaan air menjadi terbatas. Air tidak dapat dipergunakan untuk keperluan rumah tangga dan industri. Kedua macam bahan ini berasal dari larutan batu-batuan yang mengandung senyawa Fe atau Mn seperti pyrite, kematit, mangan dan lain-lain. (Agusnar, H. 2008).
dilakukan adalah dengan penukar ion, dan metode ketiga adalah menstabilisasi besi dan mangan dalam suspensi. (Connor, J.T. 1971).
2.7. Nikel (Ni)
Nikel adalah logam putih perak yang keras. Nikel bersifat liat, dapat ditempah dan sangat kukuh. Logam ini melebur pada 1445oC dan bersifat sedikit magnetis (Vogel,A.I. 1994).
Nikel terbentuk secara alami pada kerak bumi dan tersebar di lingkungan. Kontaminasi Ni dalam makanan pada umumnya berasal dari polusi industri, peralatan dan bahan yang digunakan selama pengolahan bahan makanan.
Nikel merupakan zat gizi esensial yang berfungsi menstabilisasi struktur asam nukleat dan protein serta sebagai kofaktor berbagai enzim. Nikel juga berperan
mengatur kadar lipid dalam jaringan dan dalam sintesis fosfolipid. Nikel juga merupakan nonspesifik aktifator enzim.
Logam nikel dan senyawa nikel mrtupakan bahan karsinogenik. Inhalasi debu mengandung Ni-sulfida, Ni-subsulfida dapat mengakibatkan kanker paru-paru, kanker rongga hidung, dan kanker pita suara, bahkan dapat mengakibatkan kematian.
Untuk mengetahui adanya paparan Ni, bisa dilakukan analisis terhadap kadar Ni dalam darah, urin, feses dan rambut. Konsumsi makanan mengandung Ni 600 µg/hari sudah menunjukkan toksisitas pada manusia. (Widowati, W. 2008).
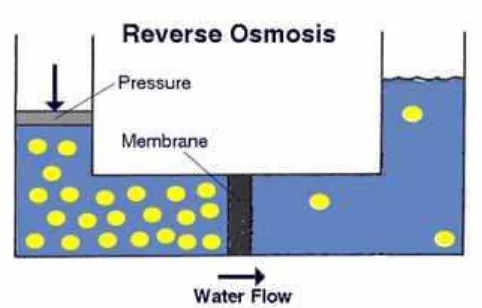
Reverse osmosis adalah proses membran dalam pemurnian air dengan menggunakan tekanan hidrostatik untuk membawa air melalui membran semipermeabel dimana sejumlah besar zat kontaminan akan dihilangkan.
Proses reverse osmosis menggunakan tekanan tinggi agar air bisa melewati membran, di mana kerapatan membran reverse osmosis ini adalah 0,0001 mikron. Jika air mampu melewati membran reverse osmosis, maka air inilah yang akan kita pakai, tapi jika air tidak bisa melewati membran semipermeable maka akan terbuang pada saluran khusus.
.
Proses Reverse osmosis untuk pemurnian air tidak membutuhkan energi termal. Aliran air dengan sistem Reverse osmosis dapat diatur dengan pompa tekanan tinggi. Pemurnian air tergantung pada berbagai faktor termasuk ukuran membran, ukuran pori membran, suhu, tekanan operasi dan luas permukaan membran.
Proses reverse osmosis terjadi ketika tekanan osmosis membawa molekul air melalui membran permeable pada keadaan kesetimbangan. Keadaan seperti ini dapat kembali dengan memberikan tekanan hidrostatik pada larutan air garam yang lebih tinggi daripada tekanan osmosisnya. (Fair, G.M. 1968).
Gambar 2.1 Skematis proses reverse osmosis
2.8.2 Tipe Membran
Secara praktek membran reverse osmosis untuk pengaplikasiannya pada air harus memiliki beberapa karakteristik. Pertama dan paling utama adalah dapat ditembus air yang mengandung senyawa-senyawa lainnya dalam larutan. Kedua, rata-rata air yang menembus permukaan membran per unit (fluks air) harus tinggi untuk memperoleh produk yang baik agar proses analisisnya ekonomis. Ketiga, membran harus tahan lama, secara kimia, fisika, dan biologi sera memiliki daya pakai yang lama. (Belfort, G. 1984).
Membran yang digunakan untuk reverse osmosis memiliki lapisan yang padat dalam matriks polimer - baik kulit membran asimetrik atau lapisan interfasial dipolimerisasi dalam membran tipis-film-komposit di mana pemisahan terjadi. Dalam kebanyakan kasus, membran ini dirancang untuk memungkinkan air hanya melewati lapisan padat, sementara mencegah bagian dari zat terlarut (seperti ion garam).
digunakan sebagai membran bisa berupa selulosa asetat (lebih cocok untuk air payau) atau poliamida (cocok untuk air laut). (Austin, G.T. 1985)
2.8.2 Kelebihan dan Kekurangan Reverse Osmosis
Sistem pengolahan reverse osmosis jika dibandingkan dengan pengolahan air minum lain seperti sistem ultra violet, perebusan, sedimentasi, ozonisasi dan pengolahan air minum lainnya, teknologi pengolahan air sistem reverse osmosis (RO) adalah sistem pengolahan air minum terbaik untuk menghasilkan air minum bersih, steril, sehat. Kelebihan air hasil dari sistem reverse osmosis adalah bebas dari semua bahan pencemar air seperti virus, bakteri, bahan kimia dan logam berat. Dengan kualitas air yang baik maka pencemaran air sekarang ini, sekaligus mampu memenuhi kebutuhan akan air bersih dan sehat.
Berikut adalah perbandingan sistem reverse osmosis dengan pemurnian air lainnya.
Tabel 2.1. Perbandingan Metode-metode Pemurnian Air
No Metode Pemurni Air Kekurangan dan Kelebihan
1. Air Murni Reverse
Osmosis
a. Air murni dengan kandungan oksigen yang tinggi
dapat menguatkan sel-sel dan organ-organ tubuh, meningkatkan daya tahan dan daya penyembuhan tubuh.
b. Bebas dari segala jenis logam berat, kotoran dan
kuman. Mengandung zat mineral tanpa ion.
c. Dapat diminum langsung, nikmat rasanya, air
minum yang ideal untuk olahragawan.
2. Air Penukaran Ion a. Biaya operasi tinggi dan memerlukan penyelengaraan yang profesional
b. Hanya membuang logam berat tetapi masih
mengandung banyak natrium yang dapat mengakibatkan hipertensi, pengapuran pembuluh darah dan masalah jantung.
c. Bahan-bahan organik, bakteri dan virus tidak
3. Air Penyulingan a. Biaya tinggi, penggunaan secara terus menerus akan memboroskan listrik dan harus selalu membersihkan endapan yang tertinggal secara rutin.
b. Hasilnya dianggap sebagai air mati karena
kekurangan oksigen dan berbau
c. Gagal untuk membuang bahan organik seperti
triklorometana.
4. Air dari Penyaringan
Karbon Teraktif
a. Mutu berbeda dan terdapat perbedaan besar
dalam hasil.
b. Tidak dapat membuang virus, logam berat,
asbestos, nitrat dan bahan lain-lain.
c. Mudah menjadi tempat pembiakan kuman dan
bakteri
5. Pengendapan a. Kualitas tidak stabil, perbedaannya besar
b. Tidak dapat membuang bakteri, logam berat,
asbestos, nitrat, garam, dsb
c. Tempat pembiakan bakteri.
6. Air Mendidih a. Berfungsi untuk membunuh bakteri, tapi sisanya tetap tertinggal dalam air.
b. Mempercepat reaksi antara bahan organik untuk
bergabung dengan klorin yang membentuk triklorometana.
c. Pada saat mendidih terjadi uap air (penguapan).
Hal ini menyebabkan bertambahnya kepekatan bahan pencemaran air dan sisa kalsium.
7. Sterilisasi Ozon a. Hanya dapat membunuh bakteri, hasilnya lebih buruk dibandingkan dengan metode pendidihan.
b. Biaya tinggi, harus menukar tabung lampu setiap
3-6 bulan
c. Tidak dapat menyaring keluar bahan pencemar.
8. Air Hasil Cahaya Ultra
Violet
a. Dapat membunuh bakteri, tetapi kurang efektif
dibandingkan dengan air mendidih.
b. Biaya tinggi, memerlukan penukaran tabung
lampu setiap 3-6 bulan
c. Selain membunuh bakteri, ia tidak dapat
menghapus kotoran lain.
9. Air Mineral a. 45% dari air mineral di pasaran mengandung bahan fosforus
b. Mutu berubah dan kebersihan tidak terjamin.
c. Mahal.
dengan metode pemurnian yang lain lain).
Kekurangan Reverse Osmosis antara lain adalah :
• Investasi dan biaya operasional tinggi
• Kapasitas air terbuang besar
• Diperlukan pretreatment yang baik
• Resiko pemampatan pada membran
• Toleransi terhadap kenaikan debit air
• Daya listrik lebih besar
Resiko pemampatan membran reverse osmosis adalah terjadinya fouling dan scalling. Fouling dapat didefinisikan sebagai proses terbentuknya lapisan oleh material yang tidak diinginkan pada permukaan membran. Secara teknis, scaling didefinisikan sebagai akumulasi kerak (scale) akibat adanya peningkatan konsentrasi dari materi anorganik yang melewati hasil kali kelarutannya pada permukaan membran dan menyebabkan penurunan kinerja membran sehingga definisi fouling sudah termasuk scaling. Dalam penggunaannya, istilah fouling lebih banyak pada materi biologis dan koloid, sedangkan istilah scaling digunakan untuk pengendapan garam atau mineral anorganik. (Tzotzi, C, 2007)
2.9. Spektrofotometri Serapan Atom
unsur bersifat spesifik. Dengan absorpsi energi, berarti memperoleh lebih banyak energi, suatu atom pada keadaan dasar dinaikkan tingkat energinya ke tingkat eksitasi.
Umumnya bahan bakar yang digunakan adalah propana, butana, hidrogen dan asetilen, sedangkan oksidatornya adalah udara, oksigen, N2O dan asetilen. Logam- logam yang mudah diuapkan seperti Cu, Pb, Zn, Cd, umumnya ditentukan pada suhu rendah sedangkan untuk unsur-unsur yang tak mudah diatomisasi diperlukan suhu tinggi. Suhu tinggi dapat dicapai dengan menggunakan suatu oksidator bersama dengan gas pembakar, contohnya atomisasi unsur seperti Al, Ti, Be perlu menggunakan nyala oksida asetilena atau nyala nitrogen oksida asetilena sedangkan untuk atomisasi unsur alkali yang membentuk refraktori harus menggunakan campuran asetilena udara. (Khopkar, S.M. 2007)
Perbedaan prinsip dengan spektrofotometri emisi atom menyangkut metode dan instrumentasi. Pada Spektrofotometri serapan atom terjadi penyerapan sumber radiasi (di luar nyala) oleh atom-atom netral dalam keadaan gas yang berada dalam
nyala. Radiasi yang diserap oleh atom-atom netral dalam keadaan gas tadi biasanya radiasi sinar tampak atau ultraviolet. Spektrofotometri serapan atom kegunaannya lebih ditentukan untuk analisis kuantitatif logam-logam alkali dan alkali tanah. (Mulja, M. 1995).
Untuk keperluan analisis kuantitatif dengan spektrofotometer serapan atom, maka sampel harus dalam bentuk larutan. Untuk menyiapkan larutan, sampel harus diperlakukan sedemikian rupa yang pelaksanaannya tergantung dari macam dan jenis sampel. Yang penting untuk diingat adalah bahwa larutan yang akan dianalisis haruslah sangat encer.
Ada beberapa cara untuk melarutkan sampel, yaitu :
• Langsung dilarutkan dengan pelarut yang sesuai
• Sampel dilarutkan di dalam suatu asam
• Sampel dilarutkan dalam suatu basa atau dilebur dahulu dengan basa kemudian
Metode pelarutan apapun yang akan dipilih untuk dilakukan analisis dengan spektrofotometer serapan atom, yang terpenting adalah bahwa larutan yang dihasilkan harus jernih, stabil dan tidak mengganggu zat-zat yang akan dianalisis. (Rohman, A. 2007).
Komponen penting yang membentuk spektrofotometer serapan atom diperlihatkan pada gambar di bawah ini.
Gambar 2.2. Komponen-komponen spektrofotometer serapan atom (Day, R.A.Jr.,Underwood A.L. 1988).
1. Sumber sinar
Sumber sinar yang lazim dipakai adalah lampu katoda berongga. Lampu ini terdiri atas tabung kaca tertutup yang mengandung suatu katoda dan anoda. Katoda sendiri berbentuk silinder berongga yang terbuat dari logam atau dilapisi dengan logam tertentu. Tabung logam ini diisi dengan gas mulia (neon atau argon) dengan tekanan rendah. Neon biasanya lebih disukai karena memberikan intensitas pancaran lampu yang lebih rendah.
2. Tempat Sampel
Dalam analisis dengan spektrofotometri serapan atom, sampel yang akan dianalisis harus diuraikan menjadi atom-atom netral yang masih dalam keadaan asas. Ada berbagai macam alat yang dapat digunakan untuk mengubah suatu sampel menjadi uap atom-atom yaitu dengan nyala dan tanpa nyala.
a. Nyala (flame)
Nyala digunakan untuk mengubah sampel yang berupa padatan atau cairan menjadi bentuk uap atomnya, dan juga berfungsi untuk atomisasi.
Tabung katoda cekung
Pemotong
berputar Nyala M onokrom ator D etektor
Penguat arus
searah Pencatat
Sum ber tenaga
B ahan
b. Tanpa nyala (flameless)
Teknik atomisasi dengan nyala dinilai kurang peka karena atom gagal mencapai nyala, tetesan sampel yang masuk kedalam nyala terlalu besar, dan proses atomisasi kurang sempurna. Oleh karena itu muncullah suatu teknik atomisasi yang baru yakni atomisasi tanpa nyala. Pengatoman dapat dilakukan dalam tungku dari grafit. Sampel diletakkan dalam tabung grafit, kemudian tabung tersebut dipanaskan dengan system elektris dengan cara melewatkan arus listrik grafit. Akibat pemanasan ini, maka zat yang akan dianalisis berubah menjadi atom-atom netral (Rohman, A. 2007).
3. Monokromator
Monokromator memisahkan, mengisolasi dan mengontrol intensitas dari radiasi energi yang mencapai detektor. Pada hakekatnya mungkin saja dapat dianggap sebagai suatu saringan yang dapat disesuaikan dengan suatu daerah yang spesifik, yang mana spectrum transmisi yang tidak sesuai akan ditolak. Idealnya monokromator harus mampu memisahkan garis resonansi. Karena ada beberapa unsur yang mudah dan ada beberapa unsur yang sulit (Haswell, 1991).
4. Detektor
Detektor dapat diatur sedemikian rupa pada nilai frekuensi tertentu, sehingga tidak memberikan respon terhadap nilai emisi yang berasal dari eksitasi termal.
5. Readout
BAB 3
3.1Alat
- Spektofotometer Serapan Atom Shimadzu AA-6300
- Labu Takar Pyrex
- Gelas Ukur Pyrex
- Pipet Volumetri Pyrex
- Gelas Beaker Pyrex
- Termometer -
- Bola Karet -
- Hot Plate Cimarec
- Pipet Skala Pyrex
- Kertas saring Whatman
- pH meter WalkLAB
- Mesin Reverse Osmosis Kemflo F5633/C
- Botol Sampel -
- Sampel cup -
- Kaca arloji -
- Pipet tetes -
- Botol Aquadest -
3.2Bahan
- Sampel Air baku
- Sampel Air hasil olahan
- Larutan induk Mn 1000 mg/L p.a.E.Merck - Larutan induk Ni 1000 mg/L p.a.E.Merck
- HNO3(p) p.a.E.Merck
- Akuades -
3.3.1 Pembuatan Larutan Standar Mangan 100 mg/L
Sebanyak 5 mL larutan induk mangan 1000 mg/L dimasukkan ke dalam labu takar 50 mL lalu diencerkan dengan akuades hingga garis tanda dan dihomogenkan.
3.3.2 Pembuatan Larutan Standar Mangan 10 mg/L
Sebanyak 5 mL larutan standar mangan 100 mg/L dimasukkan ke dalam labu takar 50 ml lalu diencerkan dengan akuades hingga garis tanda dan dihomogenkan.
3.3.3 Pembuatan Larutan Seri Standar Mangan 0,00; 0,20; 0,40; 0,60; 0,80 dan
1,00 mg/L
Sebanyak 0,00; 1,00; 2,00; 3,00 ; 4,00 dan 5,00 mL larutan standar mangan 10 mg/L dimasukkan ke dalam labu takar 50 mL lalu diencerkan dengan akuades hingga garis tanda dan di homogenkan.
3.3.4 Pembuatan Kurva Standar Logam Mangan (Mn)
Larutan seri standar logam Mangan 0,00 mg/L diukur absorbansinya dengan menggunakan Spektrofotometri Serapan Atom pada λspesifik 279,5 nm. Perlakuan dilakukan sebanyak 3 kali. Dilakukan hal yang sama untuk larutan seri standar mangan 0,20; 0,40; 0,60; 0,80 dan 1,00 mg/L. (SNI 6989.5:2009)
3.3.5 Pembuatan Larutan Standar Nikel 100 mg/L
Sebanyak 5 mL larutan induk nikel 1000 mg/L dimasukkan ke dalam labu takar 50 mL lalu diencerkan dengan akuades hingga garis tanda dan dihomogenkan.
Sebanyak 5 mL larutan standar nikel 100 mg/L dimasukkan ke dalam labu takar 50 mL lalu diencerkan dengan akuades hingga garis tanda dan di homogenkan.
3.3.7 Pembuatan Larutan Standar Nikel 1 mg/L
Sebanyak 5 mL larutan standar nikel 10 mg/L dimasukkan ke dalam labu takar 50 mL lalu diencerkan dengan akuades hingga garis tanda dan dihomogenkan.
3.3.8 Pembuatan Larutan Seri Standar Nikel 0,00; 0,03; 0,05; 0,07 ,0,10 dan 0,13
mg/L
Sebanyak 0,00; 1,50; 2,50; 3,50; 5,00 dan 6,50 mL larutan standar nikel 1 mg/L dimasukkan ke dalam labu takar 50 mL lalu diencerkan dengan akuades hingga garis tanda dan dihomogenkan.
3.3.9 Pembuatan Kurva Standar Logam Nikel (Ni)
Larutan seri standar logam nikel 0,00 mg/L diukur absorbansinya dengan menggunakan Spektrofotometri Serapan Atom pada λspesifik 232,0 nm. Perlakuan dilakukan sebanyak 3 kali. Dilakukan hal yang sama untuk larutan seri standard nikel 0,03; 0,05; 0,07; 0,10 dan 0,13 mg/L. (SNI 6989.18:2009)
3.3.10 Pengawetan dan Tahap Destruksi Sampel (SNI 6989.18:2009)
pada λspesifik 279,5 nm dan kadar unsur Ni pada λspesifik 232,0 nm dengan menggunakan Spektrofotometer Serapan Atom (SSA).
3.4Bagan Penelitian
3.4.1. Pembuatan Larutan Seri Standar dan Pembuatan Kurva Kalibrasi
Mangan (Mn) (SNI 6989.5:2009)
Dipip
Dipipet sebanyak 5 mL larutan standar mangan dan dimasukkan ke dalam labu takar 50 mL
Diencerkan dengan akuades hingga garis tanda Diaduk hingga homogen
Dipipet sebanyak 5 mL larutan standar mangan dan dimasukkan ke dalam labu takar 50 mL
Diencerkan dengan akuades hingga garis tanda Diaduk hingga homogen
Dipipet sebanyak 0,0; 1,00; 2,00; 3,00; 4,00; 5,00 larutan standar mangan dan dimasukkan ke dalam labu takar 50 mL
Diencerkan dengan akuades sampai garis tanda Diaduk hingga homogen
4
5
Diukur absorbansinya dengan Spektrofotometer Serapan Atom pada
�spesifik 279,5 nm
3.4.2. Pembuatan Larutan Seri Standar dan Pembuatan Kurva Kalibrasi Nikel (Ni) (SNI 6989.18:2009)
Dipipet sebanyak 5 mL larutan standar nikel dan dimasukkan ke dalam labu takar 50 mL
Larutan Standar Mangan (Mn) 100 mg/L
Larutan Standar Mangan (Mn) 10 mg/L
Larutan Seri Standar Mangan (Mn) 0,00; 0,20; 0,40; 0,60; 0,80 dan 1,00 mg/L
Hasil
Diaduk hingga homogen
Dipipet sebanyak 5 mL larutan standar nikel dan dimasukkan ke dalam labu takar 50 mL
Diencerkan dengan akuades hingga garis tanda Diaduk hingga homogen
Dipipet sebanyak 5 mL larutan standar nikel dan dimasukkan ke dalam labu takar 50 mL
Diencerkan dengan akuades hingga garis tanda Diaduk hingga homogen
6
Dipipet sebanyak 0,0;5;10;15;20; dan 25 mL larutan standar nikel dan dimasukkan ke dalam labu takar 50 mL
Diencerkan dengan akuades hingga garis tanda Diaduk hingga homogen
Diukur absorbansinya dengan Spektrofotometer Serapan Atom pada
�spesifik 232.0 nm
7
3.4.3 Preparasi dan Penentuan Mangan (Mn) dalam Sampel Air Baku (SNI
6989.5:2009)
Ditambahkan HNO3(p) hingga pH ≤ 2 Sampel Air Baku
Larutan Standar Nikel (Ni) 100 mg/L
Larutan Standar Nikel (Ni) 10 mg/L
Larutan Standar Nikel (Ni) 1 mg/L
Larutan Seri Standar Nikel (Ni) 0,0; 0,03; 0,05; 0,07: 0,10 dan 0,13 mg/L
Dimasukkan ke dalam gelas beaker Ditambahkan 5 mL HNO3(p)
Ditutup dengan kaca arloji
Dipanaskan hingga sisa volume 15-20 mL Didinginkan
Dimasukkan ke dalam labu takar 50 mL melalui kertas saring
Diencerkan dengan akuades hingga garis tanda Diukur absorbansi dengan SSA pada �spesifik
279,5 nm
Catatan : Perlakuan yang sama dilakukan pada sampel air hasil olahan
3.4.4 Preparasi dan Penentuan Nikel (Ni) dalam Sampel Air Baku (SNI
6989.18:2009)
≤ 2 Hasil
Dimasukkan ke dalam gelas beaker Ditambahkan 5 mL HNO3(p)
Ditutup dengan kaca arloji
Dipanaskan hingga sisa volume 15-20 mL Didinginkan
Dimasukkan ke dalam labu takar 50 mL melalui kertas saring
Diencerkan dengan akuades hingga garis tanda Diukur absorbansi dengan SSA pada �spesifik
232,0 nm
Catatan : Perlakuan yang sama dilakukan pada sampel air hasil olahan
BAB 4
HASIL DAN PEMBAHASAN
Hasil
4.1. Hasil Penelitian
4.1.1. Logam Mangan (Mn)
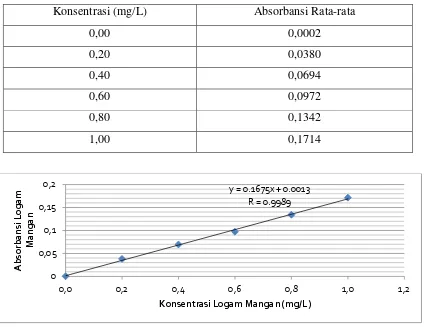
Pembuatan kurva kalibrasi larutan standar logam Mangan (Mn) dilakukan dengan membuat larutan standar dengan berbagai konsentrasi yaitu pada pengukuran 0,00; 0,20; 0,40; 0,60; 0,80; dan 1,00 mg/L, kemudian diukur absorbansinya dengan alat SSA (kondisi alat pada lampiran 2). Data absorbansi untuk larutan standar Mangan (Mn) dapat dilihat pada tabel 4.1 di bawah ini.
Tabel 4.1. Data absorbansi larutan standar Mangan (Mn)
Konsentrasi (mg/L) Absorbansi Rata-rata
0,00 0,0002
Gambar 4.1. Kurva kalibrasi larutan standar Mangan (Mn)
4.1.2. Pengolahan Data Logam Mangan (Mn)
y = 0.1675x + 0.0013
4.1.2.1. Penurunan Persamaan Garis Regresi dengan Metode Least Square
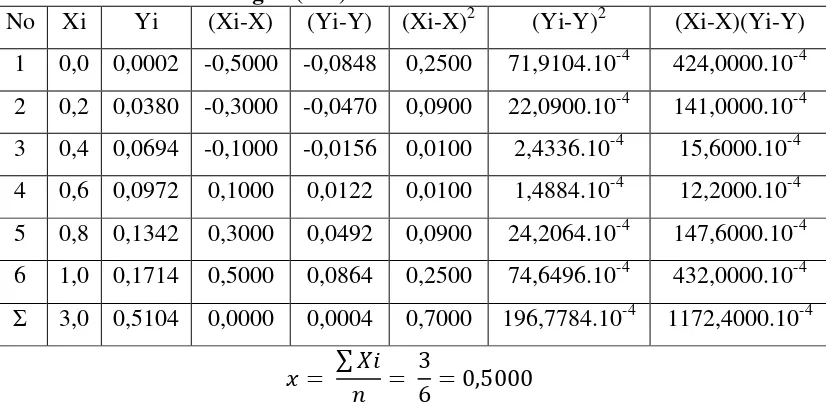
Hasil pengukuran absorbansi larutan seri standar logam Mangan (Mn) pada tabel 4.1. diplotkan terhadap konsentrasi sehingga diperoleh kurva kalibrasi berupa garis linier. Persamaan garis regresi untuk kurva kalibrasi ini dapat diturunkan dengan metode least square dengan data pada tabel 4.2.
Tabel 4.2. Penurunan persamaan garis regresi untuk penentuan konsentrasi logam Mangan (Mn) berdasarkan pengukuran absorbansi larutan standar Mangan (Mn)
No Xi Yi (Xi-X) (Yi-Y) (Xi-X)2 (Yi-Y)2 (Xi-X)(Yi-Y)
Persamaan garis regresi untuk kurva kalibrasi dapat diturunkan dari persamaan garis :
dimana :
Dengan mensubstitusikan harga-harga yang tercantum pada tabel 4.2. pada persamaan ini maka diperoleh :
1675
Maka pesamaan garis yang diperoleh adalah : 0013
4.1.2.2. Koefisien Korelasi
Koefisien korelasi dapat ditentukan dengan menggunakan persamaan sebagai berikut :
Koefisien korelasi untuk logam Mangan (Mn) adalah:
2
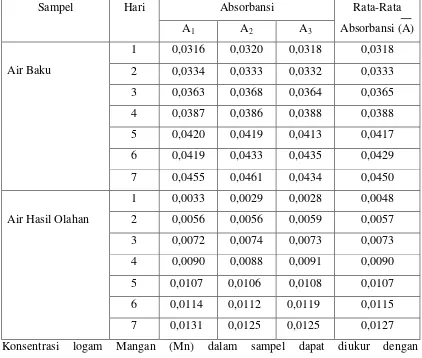
Untuk menghitung konsenrasi dari logam Mangan (Mn), maka diambil data hasil pengukuran absorbansi logam Mangan (Mn) dalam sampel. Data selengkapnya pada Tabel 4.3.
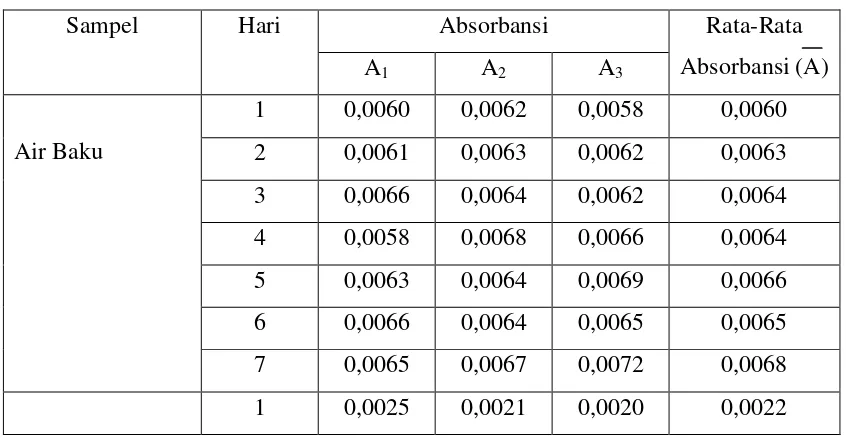
Tabel 4.3. Data absorbansi logam Mangan (Mn) dalam sampel yang diukur sebanyak 7 kali
Sampel Hari Absorbansi Rata-Rata
Absorbansi (A)
Air Hasil Olahan
1 0,0033 0,0029 0,0028 0,0048
Konsentrasi logam Mangan (Mn) dalam sampel dapat diukur dengan mensubstitusikan nilai Y (absorbansi) logam Mangan (Mn) ke persamaan :
0013
Dengan cara yang sama dapat ditentukan konsentrasi logam Mangan (Mn) hari ke 2, 3, 4, 5, 6 dan 7 serta dalam air hasil olahan . Data selengkapnya pada tabel 4.4.
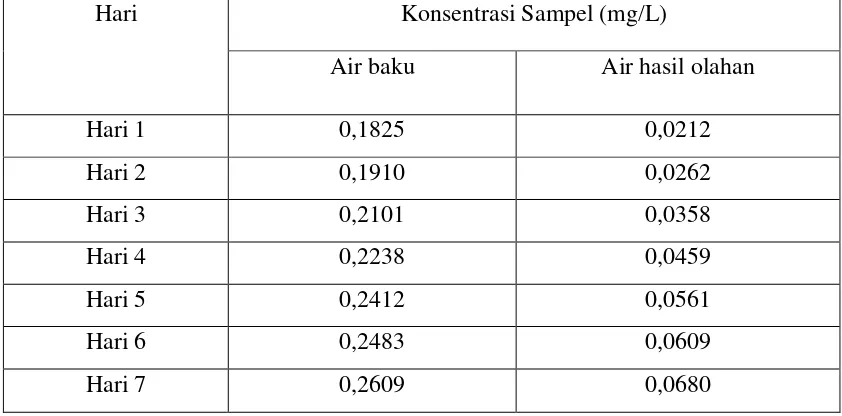
Tabel 4.4. Hasil penentuan konsentrasi logam Mangan (Mn) dalam Sampel
Hari Konsentrasi Sampel (mg/L)
Air baku Air hasil olahan
Hari 1 0,1825 0,0212
4.1.2.4. Persentase (%) penurunan konsentrasi logam Mangan (Mn)
Dari data di atas dapat ditentukan persentase (%) penurunan konsentrasi logam Mangan (Mn) dengan menggunakan rumus :
[
] [
]
Dimana : Air baku merupakan air sebelum penyaringan Air hasil olahan merupakan air setelah penyaringan
Maka persentasi (%) penurunan konsentrasi logam Mangan (Mn) dari air baku menjadi air hasil olahan yang telah diolah melalui membran reverse osmosis pada hari ke 1 adalah :
Tabel 4.5. Persentase (%) hasil penurunan kadar logam Mangan (Mn) pada
sampel
Hari Konsentrasi Mn dalam sampel (mg/L) Persentase penurunan Mn dalam sampel Air baku Air hasil olahan
Hari 1 0,1825 0,0212 88,38 %
Hari 2 0,1910 0,0262 86,28 %
Hari 3 0,2101 0,0358 82,96 %
Hari 4 0,2238 0,0459 79,49 %
Hari 5 0,2412 0,0561 76,74 %
Hari 6 0,2483 0,0609 75,47 %
Hari 7 0,2609 0,0680 73,93 %
4.1.3. Logam Nikel (Ni)
Pembuatan kurva kalibrasi larutan standar logam nikel (Ni) dilakukan dengan membuat larutan standar dengan berbagai konsentrasi yaitu pada pengukuran 0,00; 0,03; 0,05; 0,07; 0,10; 0,13 mg/L, kemudian diukur absorbansinya dengan alat SSA (kondisi alat pada lampiran 3). Data absorbansi untuk larutan standar nikel (Ni) dapat dilihat pada tabel 4.6 di bawah ini
Tabel 4.6. Data absorbansi larutan standar Nikel (Ni)
Konsentrasi (mg/L) Absorbansi Rata-rata
0,00 0,0014
0,03 0,0039
0,05 0.0062
0,07 0,0083
0,10 0,0111
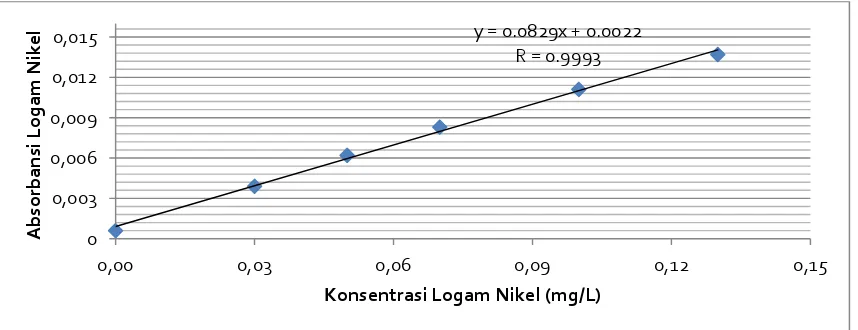
Gambar 4.2. Kurva kalibrasi larutan standar Nikel (Ni)
4.1.4. Pengolahan Data Logam Nikel (Ni)
4.1.4.1. Penurunan Persamaan Garis Regresi dengan Metode Least Square
Hasil pengukuran absorbansi larutan seri standar logam Nikel (Ni) pada tabel 4.6. diplotkan terhadap konsentrasi sehingga diperoleh kurva kalibrasi berupa garis linier. Persamaan garis regresi untuk kurva kalibrasi ini dapat diturunkan dengan metode
least square dengan data pada tabel 4.7.
Tabel 4.7. Penurunan persamaan garis regresi untuk penentuan konsentrasi
logam Nikel (Ni) berdasarkan pengukuran absorbansi larutan
standar Nikel (Ni)
No Xi Yi (Xi-X) (Yi-Y) (Xi-X)2 (Yi-Y)2 (Xi-X)(Yi-Y)
6 0,13 0,0137 0,0697 0,0063 0,4858.10-2 0,0397.10-3 4,3911.10-4
Persamaan garis regresi untuk kurva kalibrasi dapat diturunkan dari persamaan garis :
dimana :
Selanjutnya harga slope dapat ditentukan dengan mengunakan metode least square sebagai berikut :
Dengan mensubstitusikan harga-harga yang tercantum pada tabel 4.10. pada persamaan ini maka diperoleh :
0829
Maka pesamaan garis yang diperoleh adalah : 0022
Koefisien korelasi dapat ditentukan dengan menggunakan persamaan sebagai berikut :
Koefisien korelasi untuk logam Nikel (Ni) adalah:
(
)(
)
4.1.4.3Penentuan konsentrasi
Untuk menghitung konsentrasi dari logam Nikel (Ni), maka diambil data hasil pengukuran absorbansi logam Nikel (Ni) dalam air baku dan air hasil olahan. Data selengkapnya pada Tabel 4.8.
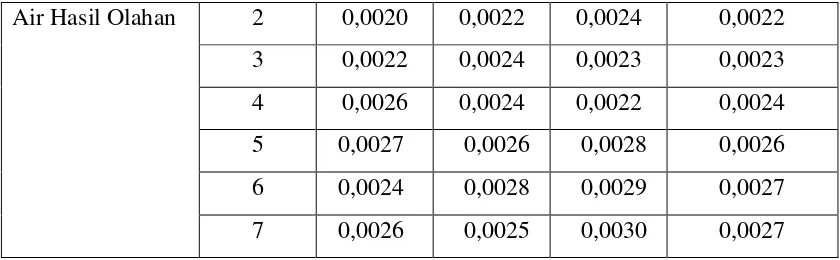
Tabel 4.8. Data absorbansi logam Nikel (Ni) dalam sampel yang diukur sebanyak
7 kali
Sampel Hari Absorbansi Rata-Rata
Air Hasil Olahan 2 0,0020 0,0022 0,0024 0,0022
Konsentrasi logam Nikel (Ni) dalam sampel dapat diukur dengan mensubstitusikan nilai Y (absorbansi) logam Nikel (Ni) ke persamaan :
0022
Untuk hari ke 1 konsentrasi logam Nikel (Ni) di dalam air baku adalah sebagai berikut 0022
Dengan cara yang sama dapat ditentukan konsentrasi logam Nikel (Ni) dalam air baku pada hari ke 2, 3, 4, 5, 6 dan 7 serta pada air hasil olahan . Data selengkapnya pada tabel 4.9.
Tabel 4.9. Hasil penentuan konsentrasi logam Nikel (Ni) dalam Sampel
Hari Konsentrasi Sampel (mg/L)
Air baku Air hasil olahan
Hari 1 0,0458 Tidak Terdeteksi
Hari 2 0,0494 Tidak Terdeteksi
Hari 3 0,0526 0,0012
Hari 4 0,0527 0,0024
Hari 6 0,0518 0,0060
Hari 7 0,0554 0,0060
Keterangan : Tidak terdeteksi : Konsentrasi di bawah batas deteksi alat
4.1.4.4. Persentase (%) penurunan konsentrasi logam Nikel (Ni)
Dari data di atas dapat ditentukan persentase (%) penurunan konsentrasi logam Nikel (Ni) dengan menggunakan rumus :
[
] [
]
Dimana : Air baku merupakan air sebelum penyaringan Air hasil olahan merupakan air setelah penyaringan
Maka persentase (%) penurunan konsentrasi logam nikel (Ni) dari air baku menjadi air hasil olahan yang telah diolah melalui membran reverse osmosis pada hari ke 1 adalah:
Dengan cara yang sama dapat ditentukan persentase (%) penurunan konsentrasi logam Mangan (Ni) pada hari ke 2, 3, 4, 5, 6 dan 7. Data selengkapnya pada tabel 4.10.
Tabel 4.10. Persentase (%) hasil penurunan kadar logam Nikel (Ni) pada sampel
Hari Konsentrasi Ni dalam sampel (mg/L) Persentase penurunan Ni dalam sampel Air baku Air hasil olahan
4.2. Pembahasan
Penelitian ini dilakukan dengan mengukur kadar logam mangan (Mn) dan nikel (Ni) dalam air baku dan air hasil olahan pada depot air minum yang menggunakan reverse osmosis.
Sampel dianalisis setiap hari selama seminggu sesuai dengan masa waktu pencucian membran reverse osmosis yang dilakukan 7 hari selama seminggu setelah penggantian filter dengan mendestruksi sampel air terlebih dahulu. Kemudian diukur nilai absorbansi dan konsentrasi dari sampel menggunakan alat Spektrofotometer Serapan Atom pada panjang gelombang tertentu. Konsentrasi sampel air baku yang didapat dibandingkan dengan konsentrasi sampel air hasil olahan. Kemudian
ditentukan persentasi (%) penurunan konsentrasinya.
Gambar 4.3. Grafik Persentase Penurunan Konsentrasi Mangan (Mn)
Sedangkan pada logam nikel (Ni) tidak terjadi penurunan pada persentase penurunan konsentrasi pada hari ke 2 namun hari selanjutnya mengalami penurunan sebesar 97,62%, 95,26%, 90,94%, 88,85% dan 82,88% dimana konsentrasi logam nikel (Ni) pada air baku berkisar antara 0,0458 mg/L hingga 0,0554 mg/L dan pada air hasil olahan sekitar 0,0000 mg/L sampai 0,0060 mg/L yang dapat dilihat pada gambar 4.4 di bawah ini.
Gambar 4.4. Grafik Persentase Penurunan Konsentrasi Nikel (Ni)
Pada grafik di atas dapat dilihat bahwa efisiensi membran reverse osmosis
semakin lama semakin menurun tergantung dari lamanya waktu pemakaian membran reverse osmosis. Hal ini disebabkan karena semakin lama waktu pemakaian, akan menimbulkan scalling dan fouling pada membran reverse osmosis yang dapat
digunakan mengandung kontaminan yang tinggi maka akan mengakibatkan efisiensi dari membran reverse osmosis tersebut pun menjadi menurun dan lama pemakaian membran pun semakin singkat.
Kandungan logam tertinggi pada air hasil olahan pada depot air minum sebesar 0,0680 mg/L untuk logam mangan dan 0,0060 mg/L untuk nikel yang masih memenuhi standar air minum untuk kandungan logam tersebut menurut peraturan menteri kesehatan nomor 492/MENKES/PER/VII/2010.
BAB 5
KESIMPULAN DAN SARAN
5.1. Kesimpulan
menteri kesehatan nomor 492/MENKES/PER/VII/2010 yaitu sebesar 0,0680 mg/L untuk logam mangan dan 0,0060 mg/L untuk nikel.
5.2. Saran
Perlu dilakukan penelitian lebih lanjut untuk melihat efisiensi pemakaian reverse osmosis terhadap penurunan kadar mineral dan membandingkannya dengan beberapa depot dengan sumber air baku yang lain.
DAFTAR PUSTAKA
Agusnar, H. 2008.Analisa Pencemaran dan Pengendalian Lingkungan. Medan: USU Press.
Austin, G.T. 1996. Industri Proses Kimia. Jilid 1. Edisi 5. Jakarta: Erlangga.
Belfort, G. 1984. Synthetic Membran Processes Fundamentals and Water Applications. New York : Academic Press, Inc.
Borchardt, J.A. 1971. Water Quality and Treatment. Third Edition. New York: Mc-Graw Hill Company.
Connel, D.W. 1995. Kimia Dan Ekotoksikologi Pencemaran. Jakarta : UI-Press Connor, J.T. 2009. Water Treatment. New Jersey: John Willey & Sons, Inc. Darmono. 1995. Logam dalam Sistem Biologi Makhluk Hidup. Jakarta: UI Press.
Darmono. 2001. Lingkungan Hidup dan Pencemaran. Jakarta: UI Press.
Effendi,H.2003. Telaah Kualitas Air Bagi Pengelolaan Sumber Daya Dan Lingkungan Perairan. Yogyakarta: Kansius
Fair, G.M. 1968. Water and Wastewater Engineering. Volume 2. New York: john Willey and Sons, Inc.
Frei, R.W and Brinkman, U.A.Th. 1983. Analysis and Chemistry of Water Pollutants. New York: Gordon and Breach Science Publishers.
Goosen, M.A. 2004. Fouling of Reverse Osmosis and Ultrafiltration membranes. Separation and Technology Membranes Journal. Imperial College.
Haswell,S.J.1991.Atomic Absorption Spectrometry Theory, Design and Application. Amsterdam: Elsevier
reverse-osmosis-dengan-sistem-penyaringan-yang-lain
Kacaribu,K.2008.Kandungan Kadar Seng (Zn) dan Besi (Fe) Dalam Air Minum Dari Depot Air Minum Isi Ulang Air Pegunungan Sibolangit di Kota Medan.USU e-Repository.
Khopkar, S.M.2007. Konsep Dasar Kimia Analitik. Jakarta: UI-Press.
Kusnaedi, 2010.Mengolah Air Kotor Untuk Air Minum.Bekasi: Penebar Swadaya
Montgomery, J. M. 1985. Water Treatment Principles and Design. New York: John Willey and Sons, Inc.
Mulja, M. 1995. Analisis Instrumental. Surabaya: Airlangga University Press. Nugroho, A. 2006. Bioindikator Kualitas Air. Jakarta: Penerbit Universitas Trisakti. Rohman A. 2007. Kimia FarmasiAnalisis. Yogyakarta: Pustaka Pelajar.
Sari, N. 2012. Penurunan Kadar Mangan (Mn) pada Air Sumur Dengan Menggunakan Arang Tempurung Kelapa Pada Konsentrasi 10% b/v dengan Variasi Lama Perendaman.
Siahaan, M.A. Efisiensi Pemakaian Reverse Osmosis Pada Depot Air Minum Terhadap Penurunan Kadar Ion Besi (Fe3+), Tembaga (Cu2+) dan Zinkum (Zn2+). Skripsi. Universitas Sumatera Utara.
SNI 6989.5:2009. Cara Uji Mangan (Mn) secara Spektrofotometri Serapan Atom (SSA)-nyala.
SNI 6989.18:2009. Cara Uji Nikel (Ni) secara Spektrofotometri Serapan Atom (SSA)-nyala.
Tzotzi, C..2007. A Study of CaCO3 Scale Formation and Inhibition in RO and NF Membrane Processes. Desalination journal. Volume 296.
Vogel, A.I. 1994. Buku Teks Anorganik Kualitatif Makro dan Semimikro. Edisi Kelima. Jakarta: PT.Kalman Media Pustaka.
Lampiran 1. Persyaratan Kualitas Air Minum
Peraturan Menteri Kesehatan RI Nomor: 492/MENKES/PER/VII/2010
1. PARAMETER WAJIB
No Jenis Parameter Satuan
Kadar maksimum yang
diperbolehkan 1. Parameter yang berhubungan
langsung dengan kesehatan
a. Parameter Mikrobiologi
1). E. Coli Jumlah per 100
mL sampel
0
2). Total bakteri Koliform Jumlah per 100 mL sampel
0
b. Kimia Anorganik
2). Fluorida mg/L 1,5
2. Parameter yang tidak langsung berhubungan dengan kesehatan
a. Parameter Fisik
1). Bau Tidak berbau
b. Parameter Kimiawi
1). Aluminium mg/L 0,2
II. PARAMETER TAMBAHAN
No Jenis Parameter Satuan
Kadar maksimum yang
diperbolehkan 1. KIMIAWI
a. Bahan Anorganik
b. Bahan Organik
Ethylendiaminetetraacetic acid (EDTA)
Aldrin dan dieldrin mg/L 0,00003
Atrarine mg/L 0,002
Carbofuran mg/L 0,007
Chlordane mg/L 0,0002
Chlorotoluron mg/L 0,03
DDT mg/L 0,001
1,2-Dibromo-3-chloropropane (DBCP) mg/L 0,001 2,4-Dichlorophenoxyacetic acid (2,4-D) mg/L 0,03
1,2-dichloropropane mg/L 0,04
Isoproturon mg/L 0,009
Lindane mg/L 0,002
MCPA mg/L 0,002
Methoxychlor mg/L 0,02
Metolachor mg/L 0,01
Pendimethaline mg/L 0,02
Pentachlorophenol (PCP) mg/L 0,009
Permethrin mg/L 0,3
Simarine mg/L 0,002
Trifluralin mg/L 0,02
Chlorophenoxy herbicides selain 2,4-D dan MCPA
2,4-DB mg/L 0,090
Dicholoroprop mg/L 0,10
Fenoprop mg/L 0,009
Mecoprop mg/L 0,001
2,4,5-Trichlorophenoxyacetic acid mg/L 0,009
d. Desinfektan dan Hasil Sampingnya
Desinfektan
2,4,6-Trichlorofenols (2,4,6-TCP) mg/L 0,2
Bromoform mg/L 0,1
Dibromochloromethane (DBCM) mg/L 0,1 Bromodicholoromethane (BDCM) mg/L 0,06
Chloroform mg/L 0,3
Chlorinated acetic acids
Dichloroacetic acid mg/L 0,05
Cyanogen chloride (Sebagai CN) mg/L 0,07
2. RADIOAKTIFITAS
Gross alpha activity Bq/L 0,1
Gross beta activity Bq/L 1
Menteri Kesehatan RI Ttd.
Lampiran 2. Kondisi alat SSA Merek Shimadzu tipe AA-6300 pada pengukuran konsentrasi logam mangan (Mn)
No Parameter Logam Mangan (Mn)
1 2 3 4 5 6
Panjang gelombang (nm) Tipe nyala
Kecepatan aliran gas pembakar (L/min) Kecepatan aliran Udara (L/min)
Lebar Celah (nm) Ketinggian tungku (mm)
279,5 nm Udara-C2H2
2,0 15,0
Lampiran 3. Kondisi alat SSA Merek Shimadzu tipe AA-6300 pada pengukuran konsentrasi logam Nikel (Ni)
No Parameter Logam Nikel (Ni)
1 2 3
4 5 6
Panjang gelombang (nm) Tipe nyala
Kecepatan aliran gas pembakar (L/min)
Kecepatan aliran Udara (L/min) Lebar Celah (nm)
Ketinggian tungku (mm)
232,0 nm Udara-C2H2
1,6
15,0 0,2
7
Lampiran 4. Alat SSA tipe nyala merek Shimadzu seri AA-6300
Lampiran 5. Alat Reverse Osmosis Merk Kemflo F5633/C